珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、この材料を用いたリチウムイオン二次電池、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法
【課題】高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるとともに、空気や水と反応して発火することがなく取り扱いが容易であって工業的実用性が高い、リチウムイオン二次電池用負極材料及びその製造方法を提供すること。
【解決手段】リチウムを含有する珪素酸化物粉末を、Cu−kα線源でのX線回折(XRD)において、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、0.01<B/A<5.0、C/A<1.0、D/A<1.0を満たすものとする。
【解決手段】リチウムを含有する珪素酸化物粉末を、Cu−kα線源でのX線回折(XRD)において、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、0.01<B/A<5.0、C/A<1.0、D/A<1.0を満たすものとする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるとともに、取り扱いが容易であって工業的な実用性が高い、珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、この材料を用いたリチウムイオン二次電池、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法に関する。
【背景技術】
【0002】
リチウムイオン二次電池は、ニッケルカドミウム電池、ニッケル水素電池等の二次電池と比較して高容量、長寿命、軽量であるという優れた特性を有している。そのため、近年、移動体通信機器、携帯用電子機器、電動自転車等の主電源としての利用が拡大している。
【0003】
リチウムイオン二次電池の負極材料(負極活物質)には、一般的に黒鉛質負極材料が使用されている。しかし、黒鉛質負極材料を用いたリチウムイオン二次電池は、充放電容量が小さいという問題があった。
これに対して、SiO等の珪素酸化物を負極材料として用いた場合、黒鉛質負極材料に比べて高い充放電容量を有するリチウムイオン二次電池が得られることが知られている。(例えば、下記特許文献1参照)
【0004】
珪素酸化物からなる負極材料は、初期充電時に、可逆的にリチウムを吸蔵放出できる物質及びリチウムを吸蔵放出できない物質(不可逆物質)へと合金化反応する。そのため、設計当初正極にあったリチウムイオンが減少してしまうという問題がある。
【0005】
一方、電池を組む前の負極材料に対して、一定のリチウムイオンを予め充填することにより不可逆容量を補償するプリドープ(予備吸蔵)と呼ばれる方法が知られている。(例えば、下記特許文献2参照)
従来、プリドープ法としては、例えば、活物質を含有する電極に金属リチウムの薄膜を貼り付ける方法や、リチウムを蒸着する方法などが知られている。
しかし、金属リチウムやLi−Si合金は、空気や水との接触によって容易に発火するため、前者の方法は製造工程における金属リチウム薄膜の取り扱い性に問題がある。また、後者の方法は、工業化(量産化)が困難であるという問題があり、いずれの方法も工業的な実用性という点では好ましい方法とは言えない。
【0006】
一方、下記特許文献3には、リチウムイオン二次電池の負極材料として用いられるリチウム含有珪素粉末及びその製造方法が開示されている。
具体的には、一般式SiLixOyで表されるリチウム含有酸化珪素粉末であって、x、yの範囲が0<x<1.0,0<y<1.5であり、リチウムが融合化しかつその5〜50%が結晶化しているリチウム含有酸化珪素粉末が開示されている。
このリチウム含有酸化珪素粉末は、SiOガスを発生する原料粉末として比表面積が1〜100m2/gのSiOz粉末(1.0≦z<1.6)と金属リチウム又はリチウム化合物との、珪素原子に対するリチウム原子のモル比(Li/Si)が0.05≦Li/Si≦0.6となる混合物を不活性ガス雰囲気又は減圧下、900〜1,300℃の温度で加熱して反応させるという製造方法により得られる。
【0007】
しかしながら、特許文献3に開示されたリチウム含有酸化珪素粉末の具体的な製造方法について実施例を参照すると、出発原料としてLiOHやLi2Oを使用している。そのため、製造過程において出発原料を還元処理しなければならないという問題がある。
更に、900〜1,300℃の温度で加熱して反応させることにより製造されるため、SiOはSiとSiO2に不均化してしまい、負極材料としての機能を果たさなくなるという重大な問題がある。尚、この点について、特許文献3(段落[0026]参照)には、1300℃以上で不均化すると記載されている。しかし、本願発明者は、SiOは900℃以上で加熱すると不均化することを実験により確認している。
また、実施例1を参照すると、製造過程においてボールミルを使用することが記載されているが、このボールミルによる処理は、900℃で熱処理した後のものを僅か1rpmという回転速度で解砕するものであるから、この処理によってSiOにリチウムがプリドープされた珪素酸化物粉末を得ることはできない。
【0008】
以上より、特許文献3に記載された製造方法により得られるリチウム含有珪素粉末は、LiOHの分解物等とSi,SiO2との単なる混合物であって、後述する本発明に係る珪素酸化物粉末とは物質が全く異なり、高い充放電容量を有するリチウムイオン二次電池の負極材料とはなり得ない。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特許第4634515号公報
【特許文献2】特開2007−299698号公報
【特許文献3】特許第4702410号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、上記したような従来技術が有する課題を解決するためになされたものであって、高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるとともに、空気や水と反応して発火することがなく取り扱いが容易であって工業的実用性が高い、珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、この材料を用いたリチウムイオン二次電池、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法を提供するものである。
【課題を解決するための手段】
【0011】
本発明は、上記課題を解決するために以下の手段を提供する。
請求項1に係る発明では、
リチウムを含有する珪素酸化物粉末であって、
Cu−kα線源でのX線回折(XRD)において、
2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、
0.01<B/A<5.0
C/A<1.0
D/A<1.0
を満たすことを特徴とする珪素酸化物粉末とする。
【0012】
これにより、高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるととともに、空気や水と反応して発火することがなく取り扱いが容易であって工業的実用性が高いリチウムイオン二次電池の負極材料としての珪素酸化物粉末が提供される。
本発明に係る珪素酸化物粉末、即ちCu−kα線源でのXRDにおいて、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、0.01<B/A<5.0、C/A<1.0、D/A<1.0を満たす珪素酸化物粉末を負極材料(負極活物質)として使用したリチウムイオン二次電池は、これらを満たさない珪素酸化物粉末を負極材料として使用したリチウムイオン二次電池と比較して高い充放電容量を有している。
【0013】
請求項2に係る発明では、
請求項1に係る発明において、2θ=18.7°±0.2°におけるピークの面積強度をEとしたとき、0.2≦E/B<1を満たすことを特徴とする珪素酸化物粉末とする。
【0014】
これにより、Si及びLi4SiO3がナノレベルで高分散した珪素酸化物粉末となる。
【0015】
請求項3に係る発明では、
請求項1又は2に係る発明において、粒度の積算分布曲線における累積頻度50%の粒径D50が0.5μm≦D50≦50μmであり、且つBET比表面積50m2/g以下であることを特徴とする珪素酸化物粉末とする。
【0016】
これにより、珪素酸化物粉末の単位質量当たりの表面積が少なくなり、珪素酸化物表面に形成されるSiO膜の含有量を低減することができる。そのため、リチウムイオン二次電池の負極材料として用いた場合に、SiO膜によるリチウムイオン二次電池の初期効率及びサイクル特性の低下を防ぐことができる。
【0017】
請求項4に係る発明では、
請求項1乃至3いずれかに記載の珪素酸化物粉末を含有することを特徴とするリチウムイオン二次電池用負極材料とする。
【0018】
この負極材料を使用してリチウムイオン二次電池を製造することにより、高い充放電容量を有するリチウムイオン二次電池を提供することができる。
【0019】
請求項5に係る発明では、
請求項4に記載の負極材料を用いた負極を備えることを特徴とするリチウムイオン二次電池とする。
【0020】
このリチウムイオン二次電池は、上記珪素酸化物粉末を含有する負極材料を用いているため、高い充放電容量を有するリチウムイオン二次電池となる。
【0021】
請求項6に係る発明では、
リチウムイオン二次電池の負極材に用いられる珪素酸化物粉末の製造方法であって、
SiOからなる第一の原料と、金属リチウムからなる第二の原料を使用し、
不活性雰囲気下において、前記第一の原料と前記第二の原料の混合物を遠心加速度30G以上でメカニカルミリング処理することによって、SiOにリチウムがプリドープされた珪素酸化物粉末を得ることを特徴とする珪素酸化物粉末の製造方法とする。
【0022】
これにより、活物質を含有する電極に金属リチウムの薄膜を貼り付ける方法やリチウムを蒸着する方法などの従来のプリドープ方法に比べて、工業的な実用性が高く、高い充放電容量を有するリチウムイオン二次電池を得ることが可能である、珪素酸化物粉末が提供される。
また、前記第一の原料と前記第二の原料の混合物を遠心加速度30G以上でメカニカルミリング処理することによって、SiOにリチウムがプリドープされた珪素酸化物粉末を確実に得ることができる。
更に、出発物質の一つである第二の原料として金属リチウムを使用しているため、LiOHやLiO2を使用した場合のように還元処理を行う必要がない。
【0023】
請求項7に係る発明では、
前記メカニカルミリング処理後の珪素酸化物粉末を、不活性雰囲気下において、648℃以上850℃以下の温度で加熱処理することを特徴とする請求項6記載の珪素酸化物粉末の製造方法とする。
【0024】
これにより、SiOにリチウムをプリドープした時に、リチウムが不可逆容量分に比べて過剰に入った場合や、過剰に入っていなくともSiOとリチウムの混合が不均一でリチウム濃度が高い部分がある場合に生成されるLi12Si7を、加熱処理により分解除去することができる。また、リチウム濃度が全体に均一化し、SiとLi4SiO4の結晶化が促進されることで安定化する。これにより、発火の危険性が少なく安全で安定したリチウムイオン二次電池負極材用の珪素酸化物粉末を提供することが可能となる。
また、加熱処理の温度を650℃〜850℃に設定することにより、SiOが存在してもSiとSiO2に不均化することが防がれ、SiやLi4SiO4等がナノレベルで高分散した珪素酸化物粉末を得ることができる。
【発明の効果】
【0025】
本発明によれば、高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるとともに、空気や水と反応して発火することがなく取り扱いが容易であって工業的実用性が高い、リチウムイオン二次電池用の負極材料及びその製造方法と、高い充放電容量を有するリチウムイオン二次電池が提供される。
【図面の簡単な説明】
【0026】
【図1】実施例サンプルについてのXRDチャートである。
【図2】比較例1サンプルについてのXRDチャートである。
【図3】比較例2サンプルについてのXRDチャートである。
【図4】比較例3サンプルについてのXRDチャートである。
【図5】比較例4サンプルについてのXRDチャートである。
【図6】実施例サンプルについてのCV測定結果である。
【図7】比較例1サンプルについてのCV測定結果である。
【図8】比較例2サンプルについてのCV測定結果である。
【図9】比較例3サンプルについてのCV測定結果である。
【図10】比較例4サンプルについてのCV測定結果である。
【図11】(a)は実施例サンプルについての充放電曲線図であり、(b)は(a)の1次微分曲線である。
【図12】(a)は比較例1サンプルについての充放電曲線図であり、(b)は(a)の1次微分曲線である。
【図13】(a)は比較例2サンプルについての充放電曲線図であり、(b)は(a)の1次微分曲線である。
【図14】(a)は比較例3サンプルについての充放電曲線図であり、(b)は(a)の1次微分曲線である。
【図15】Li−Si二元系状態図である。(出典:T.B.Massalski, H. Okamoto, P. R. Subramanian, and L. Kacprzak, eds., Binary Alloy Phase Diagrams, 2nd ed. (ASM International, Metals Park, Ohio, 1990)
【図16】Li2O−SiO2疑二元系状態図である。(出典:A. Skokan, H. Wedemeyer, D. Vollath and E. Gunther:Proc. 14th Symp. On Fusion Technology, Avignon, Sept. 8-12, 1986, p.1255)
【発明を実施するための形態】
【0027】
以下、本発明に係る珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、この材料を用いたリチウムイオン二次電池、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法の好適な実施形態について説明する。
【0028】
<珪素酸化物粉末について>
本発明に係る珪素酸化物粉末は、リチウムを含有する珪素酸化物粉末であって、Cu−kα線源でのX線回折(XRD)において、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、0.01<B/A<5.0、C/A<1.0、D/A<1.0を満たすものである。
また、2θ=18.7°±0.2°におけるピークの面積強度をEとしたとき、0.2≦E/B<1を満たすことが好ましい。
【0029】
後述する実施例及び比較例に示す如く、上記条件を満たす珪素酸化物粉末を負極材料(負極活物質)として使用したリチウムイオン二次電池は、これらを満たさない珪素酸化物粉末を負極材料として使用したリチウムイオン二次電池と比較して、高い充放電容量を有する。
【0030】
また、本発明に係る珪素酸化物粉末は、粒度の積算分布曲線における累積頻度50%の粒径D50が0.5μm≦D50≦50μmであり、且つBET比表面積50m2/g以下である。
【0031】
D50が0.5μm未満であると、電極スラリー製造時にスラリー中の粒子が凝集し易くなり、均一なスラリーが得難いという問題があるため、好ましくない。また、粒子が細かいと、表面積が大きくなり、試料の保存中に表面が酸化し易くなってしまうため、好ましくない。一方、D50が50μmを超えると、大きい粒径の珪素酸化物を多数含有することとなり、リチウムイオン二次電池の負極材として使用すると、リチウムイオンが珪素酸化物の内部まで入り込めず、酸化珪素が性能を充分に発揮できずに初期効率が低下するため、好ましくない。なお上記した電極スラリーとは、電極製造時に集電体へ塗工するペースト状のものであり、活物質、導電助剤、バインダー(結着材)、粘度調整用の溶媒、などを混練して得られるもののことをいう。
BET比表面積50m2/gを超えると、珪素酸化物粉末の単位質量当たりの表面積が多くなり、珪素酸化物表面に形成されるSiO膜の含有量が増加する。そのため、リチウムイオン二次電池の負極材料として用いた場合に、SiO膜によるリチウムイオン二次電池の初期効率及びサイクル特性の低下が生じる虞があり、好ましくない。
【0032】
粒度の積算分布曲線における累積頻度50%の粒径D50(μm)は、レーザー回折散乱法による粒度分布の測定結果に基づいて算出することができる。測定機としては、例えばMastersizer2000(Malvern社製)等を使用することができる。
BET比表面積は、窒素ガス吸着式によるBET一点法により測定される値であり、測定機としては、例えばMacsorb HM model(マウンテック社製)等を使用することができる。
【0033】
<珪素酸化物粉末の製造方法について>
本発明に係る珪素酸化物粉末の製造方法では、SiOからなる第一の原料と、金属リチウムからなる第二の原料を使用し、不活性雰囲気下において、前記第一の原料と前記第二の原料の混合物を乾式にてメカニカルミリング処理することにより、SiOにリチウムがプリドープされた珪素酸化物粉末を得る。
【0034】
メカニカルミリング処理とは、衝撃・引張り・摩擦・圧縮・せん断等の外力を原料に与える方法であって、転動ミル、振動ミル、遊星ミル、揺動ミル、水平ミル、アトライターミル、ジェットミル、擂潰機、ホモジナイザー、フルイダイザー、ペイントシェイカー、ミキサー等などを用いる方法が挙げられる。
例えば、遊星ミルを用いる方法では、原料粉末とボールとを共に容器に入れ、自転と公転をさせることによって生じる力学的エネルギーにより、原料を粉砕・混合又は固相反応させることができる。
【0035】
第一の原料としては、SiO粉末が好適に使用される。SiO粉末としては、粒径1μm〜20μmのもの、より好ましくは粒径1μm〜10μmのものが好適に使用される。粒径が1μm未満であると電極スラリー製造時にスラリー中の粒子が凝集し易くなり、均一なスラリーが得難いという問題があるため、好ましくない。また、粒子が細かいと、表面積が大きくなり、試料の保存中に表面が酸化し易くなってしまうため、好ましくない。また、粒径が20μmを超えると塗工する電極が厚くなってしまい、充放電時に電極が劣化しやすく、充放電サイクル寿命が低下する原因となり、いずれの場合も好ましくない。
第二の原料としては、例えば金属リチウムの薄膜が使用される。薄膜としては、例えば金属リチウム金属薄膜(厚さ500μm、幅50mm)を所定のサイズ(例えば2〜10mm角程度)に切断したものが使用される。
これら第一の原料と第二の原料を、不活性雰囲気下(例えばアルゴン等の不活性ガス雰囲気下)において、メディア(例えばボール)と共に容器(例えばポット)内に入れて容器を高速で回転させる(メカニカルミリング処理する)ことにより、SiOにリチウムが不可逆容量分プリドープされた珪素酸化物粉末を得る。
第一の原料と第二の原料の配合比(重量比)は、第一の原料1に対して第二の原料が0.12〜0.17となるように設定することが好ましい。この配合比より第二の原料が少ないとプリドープされるリチウムが不可逆容量分に満たない虞があり、逆に多いとリチウムが不可逆容量分に比べて過剰となる虞があり、いずれの場合も好ましくない。
【0036】
容器の内面の材質は、例えばジルコニア、ステンレス、窒化珪素、炭化珪素等が好適であるが、このうちリチウムと反応しないステンレスが最も好適である。
メディアとしては、直径2mm〜4mm程度のボールが好適に使用される。メディアの材質は、ジルコニア、ステンレス、窒化珪素、炭化珪素等が好適であるが、このうちリチウムと反応しないステンレスが最も好適である。
ミリング条件は、遠心加速度30G以上に設定する。遠心加速度が30G未満の場合、SiOにリチウムが不可逆容量分プリドープされた珪素酸化物粉末が得られない虞があり好ましくない。好適には、30〜150G×10分〜10時間の範囲に設定することができ、例えば100G×3時間に設定される。
【0037】
本発明においては、上記メカニカルミリング処理により得られた珪素酸化物粉末(SiOにリチウムがプリドープされた珪素酸化物粉末)を、不活性雰囲気下(例えばアルゴン等の不活性ガス雰囲気下)において加熱処理することが好ましい。
加熱処理の温度は648℃以上1255℃以下、好ましくは650℃〜850℃に設定される。加熱時間は、加熱温度が650℃〜850℃の場合、例えば30分〜10時間に設定される。
この加熱処理を行う理由は、以下の通りである。
【0038】
上記メカニカルミリング処理により得られた珪素酸化物粉末は、SiOにリチウムが不可逆容量分プリドープされており、理想的には、ナノサイズレベルの微小なSiと、微小なLi4SiO4とが高分散した状態となっているものと考えられる。
しかし、もし不可逆容量分に比べて過剰にリチウムが入った場合や、又は過剰でなくても混合が不均一でリチウム濃度が高い部分がある場合には、SiとLi4SiO4以外にLi12Si7が生成すると考えられる。
このLi12Si7合金は、水分に接触すると発火の危険性がある物質である。そのため、最終的に得られるリチウムイオン二次電池負極材用の珪素酸化物粉末中に存在することは好ましくない。
【0039】
Siの融点は約1410℃であるため、それ以下の温度域では安定に存在する。
Li4SiO4は、図16のLi2O−SiO2疑二元系状態図より、1255℃(=1528K−273)までは安定に存在できる。
一方、リチウムプリドープ時に余分に生成し得るLi12Si7は、図15のLi−Si二元系状態図より648℃以上では安定に存在できない。
【0040】
これらのSi、Li4SiO4、Li12Si7の各物質の安定温度域の関係から、上記メカニカルミリング処理により得られた珪素酸化物粉末を、不活性雰囲気下において648℃以上1255℃以下の温度で加熱処理すると、余分なLi12Si7は分解され、不可逆容量分を超えた過剰なリチウムを除去することができる。また、リチウム濃度が全体に均一化し、SiとLi4SiO4の結晶化が促進されることで安定化する。
また、加熱処理の温度を650℃〜850℃に設定すると、SiOが存在しても不均化しなくなる温度域となるため、より一層好ましい。上述した通り、本願発明者は、SiOは900℃以上で加熱すると不均化することを実験により確認している。
【0041】
<リチウムイオン二次電池について>
上記した本発明に係る珪素酸化物粉末をリチウムイオン二次電池用負極材料として使用してリチウムイオン二次電池を製造することができる。
リチウムイオン二次電池の製造においては、公知のリチウムイオン二次電池の電池要素(正極、セパレーター、電解液等)を用い、常法に従って、角型、円筒型、コイン型等の電池に組み立てればよい。
【0042】
負極材料は、本発明に係る珪素酸化物粉末(活物質)と、導電助剤と、バインダーとから構成することができる。必要であれば、その他の活物質を添加してもよい。
負極材料は、本発明に係る珪素酸化物粉末を50〜95%含有することが好ましい。
50%未満であると珪素酸化物の容量向上効果が充分に得られず、95%を超えるとバインダーが少なくなり、電極が充放電に伴う体積変化に耐えられず、電極が劣化して機能しなくなるため、いずれの場合も好ましくない。配合比(重量比)の一例を挙げると、本発明に係る珪素酸化物粉末:導電助剤:バインダー=85:5:10である。
【0043】
導電助剤としては、通常用いられているもの、例えばアセチレンブラック(AB)、ケッチェンブラック(KB)、黒鉛、カーボンファイバー、カーボンチューブ、非晶質炭素等の炭素材料を、一種単独で、或いは二種以上を組み合わせて使用することができる。
【0044】
バインダーも通常用いられているもの、例えば、ポリフッ化ビニリデン(PVdF)、ポリテトラフルオロエチレン(PTFE)、ポリイミド(PI)、ポリアミド、ポリアミドイミド、ポリアクリル、スチレンブタジエンゴム(SBR)、スチレン−エチレン−ブチレン−スチレン共重合体(SEBS)、カルボキシメチルセルロース(CMC)等の材料を一種単独で、或いは二種以上を組み合わせて使用することができる。
【0045】
集電体は、電子伝導性を有し、保持した負極材料に通電し得る材料であれば特に限定されない。例えば、C、Ti、Cr、Ni、Cu、Au、ステンレス鋼等が好ましく使用される。
【0046】
正極としては、例えば、コバルト酸リチウム(LiCoO2)、ニッケル酸リチウム(LiNiO2)、マンガン酸リチウム(LiMn2O4)、リン酸鉄リチウム(LiFePO4)、コバルトマンガンニッケル酸リチウム(LiCo0.33Ni0.33Mn0.33O2)等の公知のものが用いられる。
【0047】
セパレータとしては、公知のリチウムイオン二次電池に用いられるものが使用できる。
例えば、ポリエチレン(PE)、ポリプロピレン(PP)、ポリエステル、セルロース、アラミド、ポリアミドイミド(PAI)、ポリアミド(PA)、ポリイミド(PI)等の樹脂からなる多孔質シート、ガラスフィルター、不織布等を用いることができるが、これらに限定はされない。
【0048】
電解質は、リチウムイオン二次電池で用いられるものであれば特に限定されないが、その電解質塩としては、リチウム塩が好適である。このリチウム塩としては、具体的には、ヘキサフルオロリン酸リチウム、過塩素酸リチウム、テトラフルオロホウ酸リチウム、トリフルオロメタンスルホン酸リチウム及びトリフルオロメタンスルホン酸イミドリチウムよりなる群から選択される少なくとも一種を用いることができる。
【0049】
上記電解質の溶媒としては、プロピレンカーボネート(PC)、エチレンカーボネート(EC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、γ−ブチロラクトン、2−メチルテトラヒドロフラン、1,3−ジオキソラン、4−メチル−1,3−ジオキソラン、1,2−ジメトキシエタン、1,2−ジエトキシエタン、ジエチルエーテル、スルホラン、メチルスルホラン、ニトロメタン、N,N−ジメチルホルムアミド、ジメチルスルホキシドよりなる群から選択される少なくとも一種を用いることができる。但し、溶媒を用いずにポリマー電解質や固体電解質としてもよい。
【実施例】
【0050】
以下、本発明の実施例及び比較例を示すことにより本発明の効果を明確にする。但し、本発明は以下の実施例に何ら限定されるものではない。
【0051】
<1.サンプルの作製>
(1)実施例サンプル
SiO粉末10.0245g(大阪チタニウムテクノロジーズ社製)と金属リチウムのテープ(厚さ500μm、幅50mm)(本庄金属社製)を2mm×2mmに切断したもの(1.574g)とをジルコニア製のポットに入れ、グローボックス不活性雰囲気(アルゴン雰囲気)にて、φ2mmのジルコニア製ボールをメディア(粉砕媒体)として使用し、100G×3時間の運転条件にて、ボールミルにてメカニカルミニング処理することにより、SiOにリチウムが不可逆容量分ドープされた珪素酸化物粉末を得、これを実施例サンプルとした。
【0052】
(2)比較例1サンプル
実施例サンプルで使用したものと同じSiO粉末そのものを比較例1サンプルとした。
【0053】
(3)比較例2サンプル
実施例サンプルで使用したものと同じSiO粉末を、アルゴン雰囲気で1200℃×3時間の条件で焼成し、SiO粉末の一部を不均化反応(2SiO→Si+SiO2)させたものを比較例2サンプルとした。
【0054】
(4)比較例3サンプル
比較例2サンプル(不均化SiO)を、実施例サンプルの作製時と同条件でメカニカルミニング処理することにより、比較例2サンプル(不均化SiO)にリチウムが不可逆容量分ドープされた珪素酸化物粉末を得、これを比較例3サンプルとした。
【0055】
(5)比較例4サンプル
通常の塗工SiO電極を対極とし、金属リチウムで電池(半電池)を組んで、充放電させることにより、SiOにリチウムを不可逆容量分ドープさせ、これを比較例4サンプルとした。
【0056】
<2.XRD分析>
実施例及び比較例1〜4のサンプルについて、下記条件によりXRD分析を行った。
・X線回折装置:ブルカーAXS社製、型番:M06XCE
・線源:CuKα(波長λ=0.15418nm)
・出力:40kV,100mA
・サンプリング幅:0.02°
・走査範囲:2θ=10〜70°
・分析ソフト:Windows(登録商標)版 JADE(6.0)、理学電機社製
【0057】
分析結果を図1〜図5、表1〜表3に示す。
なお、XRDピークの2θ角度、高さ、面積及び半値幅の分析値は、上記分析ソフトによる多重ピーク分離処置により求められた値を用いた。
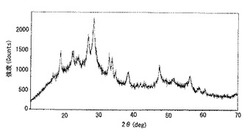
図1は実施例サンプルについてのXRDチャートであり、表1は図1のXRDチャートの分析結果である。
【0058】
【表1】

【0059】
実施例サンプルは、図1に示すように、アモルファスの傾向が見られるものの、Li−Si−O酸化物(Li2SiO3及びLi4SiO4)のピークが確認できる。Li−Si−O酸化物は不可逆成分であり、空気や水と反応して発火することがない。
実施例サンプルは、表1に示すように、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、A=13064、B=18423、C=0、D=5016であるから、0.01<B/A<5.0、C/A<1.0、D/A<1.0を満たしている。
また、2θ=18.7°±0.2°におけるピークの面積強度をEとしたとき、E=
10362であるから、0.2≦E/B<1を満たしている。
【0060】
図2は比較例1サンプルについてのXRDチャートである。
比較例1サンプルは、図2に示すように、アモルファス状態であり、ピークが確認できない。
【0061】
図3は比較例2サンプルについてのXRDチャートであり、表2は図3のXRDチャートの分析結果である。
【0062】
【表2】

【0063】
比較例2サンプルは、図3に示すように、SiOから不均化されたSiとSiO2のピークが確認できるが、不可逆成分であるLi−Si−O酸化物(Li2SiO3及びLi4SiO4)のピークは確認できない。
また、表2に示すように、2θ=28.4°±0.2°のピーク(Siのピーク)が検出されたが、2θ=18.7°±0.2°のピーク(Li2SiO3のピーク)、22.1°±0.2°のピーク(Li4SiO4のピーク)、40.5°±0.2°のピーク(Li13Si14のピーク)、56.2°±0.2°のピーク(Li2Oのピーク)がいずれも検出されていない。
表2では、Siの回折ピークが低角側へシフトしており、28.041°に現れている。これは、1200℃の熱処理によりSiOからSiが生成する不均化反応の際に、温度が低くこの反応が不完全であるため、純Si結晶と同じ結晶格子のサイズにはならず、28.4°±0.2°からシフトしたものと考えられる。1400℃以上まで熱処理温度を上げると、結晶Siと結晶SiO2に不均化することが知られている。
【0064】
図4は比較例3サンプルについてのXRDチャートであり、表3は図4のXRDチャートの分析結果である。
【0065】
【表3】

【0066】
比較例3サンプルは、図4に示すように、SiOから不均化されたSiとSiO2のピークに加えて、不可逆成分であるLi−Si−O酸化物(Li4SiO4)のピークが確認できる。これは、焼成時に残っていたSiOがプリドープされたためであると考えられる。
また、表3に示すように、2θ=22.1°±0.2°のピーク(Li4SiO4のピーク)と28.4°±0.2°(Siのピーク)は存在しているが、18.7°±0.2°のピーク(Li2SiO3のピーク)、40.5°±0.2°のピーク(Li13Si14のピーク)、56.2°±0.2°のピーク(Li2Oのピーク)がいずれも存在していない。
表3では、Siの回折ピークが低角側へシフトしており、28.082°に現れている。これは、1200℃の熱処理によりSiOからSiが生成する不均化反応の際に、温度が低くこの反応が不完全であるため、純Si結晶と同じ結晶格子のサイズにはならず、28.4°±0.2°からシフトしたものと考えられる。1400℃以上まで熱処理温度を上げると、結晶Siと結晶SiO2に不均化することが知られている。
【0067】
図5は比較例4サンプルについてのXRDチャートである。
比較例4サンプルは、図5に示すように、不可逆成分であるLi−Si−O酸化物(Li2SiO3及びLi4SiO4)のピークが確認できない。
また、2θ=22.1°±0.2°のピーク(Li4SiO4のピーク)だけでなく、18.7°±0.2°のピーク(Li2SiO3のピーク)、28.4°±0.2°のピーク(Siのピーク)、40.5°±0.2°のピーク(Li13Si14のピーク)、56.2°±0.2°のピーク(Li2Oのピーク)も確認できない。
【0068】
<2.CV測定>
実施例及び比較例1〜4のサンプルについて、下記条件によりCV(サイクリックボルタンメトリ)測定を行った。
・電気化学測定装置:ソーラトロン社製、型番:1280B
・走引速度:0.2mV/sec
・電圧範囲:0〜3V
・雰囲気温度:30℃
【0069】
測定は、作用極ペレット法(実施例及び比較例1〜3)、作用極スラリー塗工法(比較例4)により行った。
実施例及び比較例1〜3の作用極ペレット法では、ドライルーム又はグローボックス内で各材料(各サンプルと他の材料)を乳鉢で混合し、混合物を加圧成形(プレス圧:20kN)して円板状のペレット(φ10mm、厚さ1〜2mm)を作製することにより、負極ペレットを構成し、これを作用極として用いた。尚、このペレットは後述する充放電試験でも使用した。
【0070】
実施例サンプルについては、これを負極活物質として用い、Cuとこの活物質を97.9wt%:2.1wt%(0.2643g:0.0057g)の割合で混合して上記方法により負極ペレットを構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
比較例1サンプルについては、これを負極活物質として用い、Cuとこの活物質を97.6wt%:2.4wt%(0.0715g:0.0018g)の割合で混合して上記方法により負極ペレットを構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
比較例2サンプルについては、これを負極活物質として用い、Cuとこの活物質を98.0wt%:2.0wt%(0.9807g:0.0201g)の割合で混合して上記方法により負極ペレットを構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
比較例3サンプルについては、これを負極活物質として用い、Cuとこの活物質を97.5wt%:2.5wt%(0.9829g:0.0251g)の割合で混合して上記方法により負極ペレットを構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
比較例4サンプルについては、SiOとKB(ケッチェンブラック)とPI(ポリイミド)の比率が80wt%:5wt%:15wt%(活物質量:0.002g)となる電極(負極)を構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
【0071】
測定結果を図6〜図10に示す。
図6は実施例サンプルについてのCV測定結果(0〜2V)である。
図7〜10は比較例1〜4サンプルについてのCV測定結果(0〜2V)である。
【0072】
実施例サンプル(図6)では、比較例1サンプル(図7)に比べて初期電圧値が低くなり(3.0V→1.4V)、1サイクル目と2サイクル目の軌道がほぼ一致した。このことから、ほぼ理論通りにSiOに対してリチウムが不可逆プリドープされた(不可逆容量分のみプリドープされた)ことが確認できる。
比較例2サンプル(図8)では、実施例サンプルに比べて充放電反応が鈍いことが確認できる。これは、不均化処理により粒子表面にSiO2膜が生成されたためであると考えられる。
比較例3サンプル(図9)では、比較例2サンプルに比べると充放電反応が良好となったことが確認できる。これは、メカニカルミリング処理によりSiO2膜が粉砕されたことにより、比較例2サンプルと比べて充放電し易くなったと考えられる。しかし、SiO不可逆プリドープができる設計量のリチウムを加えたが、初期電圧値は2.4Vまでしか低下しなかった。
比較例4サンプル(図10)では、初期電圧値の低下は見られない。
尚、OCV(Opened Circuit Voltage)は、実施例サンプル:3.4V、比較例1サンプル:1.4V、比較例2サンプル:3.1V、比較例3サンプル:2.4Vであり、実施例サンプルが最も高かった。
【0073】
<3.充放電試験>
実施例及び比較例1〜3のサンプルについて、上記CV測定において作製したペレットを使用してコインセルを作製し、下記条件により充放電試験を行った。
・電圧範囲:0〜1V vs Li+/Li
・電流値:0.1C
【0074】
コインセルは以下の方法により作製した。
実施例及び比較例1〜3のサンプルを用いて作製したペレット電極と、対極の金属リチウムとを、電解液を含ませたセパレータを挟んで直接接触させないように配置し、2032型コインセル部材(宝泉株式会社製)を用いて密封し、コインセルを作製した。
セパレータにはポリプロピレン製微多孔膜Celgard2400(Celgard社製)とガラスファイバーフィルターGA100(ADVANTEC社製)を1枚ずつ重ねたものを使用し、電解液には1 M LiPF6/(エチレンカーボネート(EC:ジエチルカーボネート(DEC), 1:1 体積比)、対極には金属リチウム箔(直径13mm、0.5mm厚、本城金属社製)をそれぞれ用いた。
【0075】
試験結果を図11〜図14の(a)に示し、(a)の1次微分曲線を(b)に示す。
図11は実施例サンプルについての試験結果である。
図12〜14は比較例1〜3サンプルについての試験結果である。
表5は、実施例及び比較例1〜3サンプルについての可逆理論容量と1サイクル目及び2サイクル目の容量を示す。表中の数値の単位は「mAh/g」である。
【0076】
【表4】

【0077】
実施例サンプル(図11)では、比較例1サンプル(図12)において0.41V付近にあった不可逆容量が殆ど見られなくなった。((b)図参照)これは、リチウムがプリドープされたことにより初期不可逆容量成分の生成反応が無くなった為と考えられる。また不可逆容量は、比較例1サンプルが2911−1839=1072mAh/gであったのに対して、実施例サンプルでは1688−1355=333mAh/gと低くなった。
比較例2サンプル(図13)でも、比較例1サンプルにおいて0.41V付近にあったピークが見られない。これは、不均化処理によりSiとSiO2に分離して不可逆容量が消えたと考えられる。
比較例3サンプル(図14)でも、比較例1サンプルにおいて0.41V付近にあったピークが見られない。不可逆容量は1453−1122=331mAh/gと小さかったが、容量は実施例サンプル(図11)よりも低かった。
【0078】
<4.注水試験>
実施例サンプル及び比較例3サンプルについて、洗瓶を用いて、サンプルに直接水滴をかけるという方法により注水試験を行った。その結果、実施例サンプル及び比較例3サンプル共に、ガスが発生したものの発火しなかった。
【0079】
<5.D50の測定>
実施例サンプル及び比較例1〜4サンプルについて、粒度の積算分布曲線における累積頻度50%の粒径D50をレーザー回折式粒度分布測定装置としてMastersizer2000(Malvern)を使用して測定した。結果を表6に示す。
【0080】
【表5】

【0081】
<6.BET比表面積の測定>
実施例サンプル及び比較例1〜4サンプルについて、BET比表面積を窒素ガス吸着式によるBET一点法により、測定機としてMacsorb HM model(マウンテック社製)を使用して測定した。結果を表7に示す。
【0082】
【表6】

【0083】
表6及び表7に示すように、実施例サンプルは0.5μm≦D50≦50μm、BET比表面積50m2/g以下を満たしたが、比較例サンプルはいずれも満たさなかった。尚、比較例サンプルについては、原料のSiO粉末のBET比表面積が実施例サンプルよりも大きいものを使用した。
【0084】
<まとめ>
実施例サンプル(本発明に係る珪素酸化物粉末)は、Cu−kα線源でのXRDにおいて、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°、18.7°±0.2°におけるピークの面積強度を夫々A,B,C,D,Eとしたとき、0.01<B/A<5.0、C/A<1.0、D/A<1.0、0.2≦E/B<1を満たすが、比較例1〜4サンプルは満たさないことが確認された。
実施例サンプルは0.5μm≦D50≦50μm、BET比表面積50m2/g以下を満たすが、比較例サンプルはいずれも満たさないことが確認された。
実施例サンプルは、Li−Si−O酸化物(Li2SiO3及びLi4SiO4)から構成されており、リチウム不可逆プリドープが行われていることが確認された。また、発火し易い単体リチウムやLi−Si合金は存在していないため、発火の危険性が無く、取り扱いが容易であると言える。このことは注水試験によっても確認された。
一方、比較例1〜4サンプルでは、比較例1,2,4サンプルではLi−Si−O酸化物(Li2SiO3及びLi4SiO4)の存在が確認されなかった。比較例3サンプルは、Li−Si−O酸化物の存在が確認されたが、SiO2の存在も確認され、不可逆成分の生成が不十分であった。また、充放電容量において実施例サンプルに劣っていた。
【産業上の利用可能性】
【0085】
本発明に係る珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法は、高い充放電容量を有するリチウムイオン二次電池を得ることができ、取り扱いが容易であって工業的な実用性にも優れているため、リチウムイオン二次電池の製造において極めて有用である。また本発明に係るリチウムイオン二次電池は、高い充放電容量を有することから、電気自動車や移動体通信端末等の様々な利用分野における電源として極めて有用である。
【技術分野】
【0001】
本発明は、高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるとともに、取り扱いが容易であって工業的な実用性が高い、珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、この材料を用いたリチウムイオン二次電池、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法に関する。
【背景技術】
【0002】
リチウムイオン二次電池は、ニッケルカドミウム電池、ニッケル水素電池等の二次電池と比較して高容量、長寿命、軽量であるという優れた特性を有している。そのため、近年、移動体通信機器、携帯用電子機器、電動自転車等の主電源としての利用が拡大している。
【0003】
リチウムイオン二次電池の負極材料(負極活物質)には、一般的に黒鉛質負極材料が使用されている。しかし、黒鉛質負極材料を用いたリチウムイオン二次電池は、充放電容量が小さいという問題があった。
これに対して、SiO等の珪素酸化物を負極材料として用いた場合、黒鉛質負極材料に比べて高い充放電容量を有するリチウムイオン二次電池が得られることが知られている。(例えば、下記特許文献1参照)
【0004】
珪素酸化物からなる負極材料は、初期充電時に、可逆的にリチウムを吸蔵放出できる物質及びリチウムを吸蔵放出できない物質(不可逆物質)へと合金化反応する。そのため、設計当初正極にあったリチウムイオンが減少してしまうという問題がある。
【0005】
一方、電池を組む前の負極材料に対して、一定のリチウムイオンを予め充填することにより不可逆容量を補償するプリドープ(予備吸蔵)と呼ばれる方法が知られている。(例えば、下記特許文献2参照)
従来、プリドープ法としては、例えば、活物質を含有する電極に金属リチウムの薄膜を貼り付ける方法や、リチウムを蒸着する方法などが知られている。
しかし、金属リチウムやLi−Si合金は、空気や水との接触によって容易に発火するため、前者の方法は製造工程における金属リチウム薄膜の取り扱い性に問題がある。また、後者の方法は、工業化(量産化)が困難であるという問題があり、いずれの方法も工業的な実用性という点では好ましい方法とは言えない。
【0006】
一方、下記特許文献3には、リチウムイオン二次電池の負極材料として用いられるリチウム含有珪素粉末及びその製造方法が開示されている。
具体的には、一般式SiLixOyで表されるリチウム含有酸化珪素粉末であって、x、yの範囲が0<x<1.0,0<y<1.5であり、リチウムが融合化しかつその5〜50%が結晶化しているリチウム含有酸化珪素粉末が開示されている。
このリチウム含有酸化珪素粉末は、SiOガスを発生する原料粉末として比表面積が1〜100m2/gのSiOz粉末(1.0≦z<1.6)と金属リチウム又はリチウム化合物との、珪素原子に対するリチウム原子のモル比(Li/Si)が0.05≦Li/Si≦0.6となる混合物を不活性ガス雰囲気又は減圧下、900〜1,300℃の温度で加熱して反応させるという製造方法により得られる。
【0007】
しかしながら、特許文献3に開示されたリチウム含有酸化珪素粉末の具体的な製造方法について実施例を参照すると、出発原料としてLiOHやLi2Oを使用している。そのため、製造過程において出発原料を還元処理しなければならないという問題がある。
更に、900〜1,300℃の温度で加熱して反応させることにより製造されるため、SiOはSiとSiO2に不均化してしまい、負極材料としての機能を果たさなくなるという重大な問題がある。尚、この点について、特許文献3(段落[0026]参照)には、1300℃以上で不均化すると記載されている。しかし、本願発明者は、SiOは900℃以上で加熱すると不均化することを実験により確認している。
また、実施例1を参照すると、製造過程においてボールミルを使用することが記載されているが、このボールミルによる処理は、900℃で熱処理した後のものを僅か1rpmという回転速度で解砕するものであるから、この処理によってSiOにリチウムがプリドープされた珪素酸化物粉末を得ることはできない。
【0008】
以上より、特許文献3に記載された製造方法により得られるリチウム含有珪素粉末は、LiOHの分解物等とSi,SiO2との単なる混合物であって、後述する本発明に係る珪素酸化物粉末とは物質が全く異なり、高い充放電容量を有するリチウムイオン二次電池の負極材料とはなり得ない。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特許第4634515号公報
【特許文献2】特開2007−299698号公報
【特許文献3】特許第4702410号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、上記したような従来技術が有する課題を解決するためになされたものであって、高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるとともに、空気や水と反応して発火することがなく取り扱いが容易であって工業的実用性が高い、珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、この材料を用いたリチウムイオン二次電池、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法を提供するものである。
【課題を解決するための手段】
【0011】
本発明は、上記課題を解決するために以下の手段を提供する。
請求項1に係る発明では、
リチウムを含有する珪素酸化物粉末であって、
Cu−kα線源でのX線回折(XRD)において、
2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、
0.01<B/A<5.0
C/A<1.0
D/A<1.0
を満たすことを特徴とする珪素酸化物粉末とする。
【0012】
これにより、高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるととともに、空気や水と反応して発火することがなく取り扱いが容易であって工業的実用性が高いリチウムイオン二次電池の負極材料としての珪素酸化物粉末が提供される。
本発明に係る珪素酸化物粉末、即ちCu−kα線源でのXRDにおいて、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、0.01<B/A<5.0、C/A<1.0、D/A<1.0を満たす珪素酸化物粉末を負極材料(負極活物質)として使用したリチウムイオン二次電池は、これらを満たさない珪素酸化物粉末を負極材料として使用したリチウムイオン二次電池と比較して高い充放電容量を有している。
【0013】
請求項2に係る発明では、
請求項1に係る発明において、2θ=18.7°±0.2°におけるピークの面積強度をEとしたとき、0.2≦E/B<1を満たすことを特徴とする珪素酸化物粉末とする。
【0014】
これにより、Si及びLi4SiO3がナノレベルで高分散した珪素酸化物粉末となる。
【0015】
請求項3に係る発明では、
請求項1又は2に係る発明において、粒度の積算分布曲線における累積頻度50%の粒径D50が0.5μm≦D50≦50μmであり、且つBET比表面積50m2/g以下であることを特徴とする珪素酸化物粉末とする。
【0016】
これにより、珪素酸化物粉末の単位質量当たりの表面積が少なくなり、珪素酸化物表面に形成されるSiO膜の含有量を低減することができる。そのため、リチウムイオン二次電池の負極材料として用いた場合に、SiO膜によるリチウムイオン二次電池の初期効率及びサイクル特性の低下を防ぐことができる。
【0017】
請求項4に係る発明では、
請求項1乃至3いずれかに記載の珪素酸化物粉末を含有することを特徴とするリチウムイオン二次電池用負極材料とする。
【0018】
この負極材料を使用してリチウムイオン二次電池を製造することにより、高い充放電容量を有するリチウムイオン二次電池を提供することができる。
【0019】
請求項5に係る発明では、
請求項4に記載の負極材料を用いた負極を備えることを特徴とするリチウムイオン二次電池とする。
【0020】
このリチウムイオン二次電池は、上記珪素酸化物粉末を含有する負極材料を用いているため、高い充放電容量を有するリチウムイオン二次電池となる。
【0021】
請求項6に係る発明では、
リチウムイオン二次電池の負極材に用いられる珪素酸化物粉末の製造方法であって、
SiOからなる第一の原料と、金属リチウムからなる第二の原料を使用し、
不活性雰囲気下において、前記第一の原料と前記第二の原料の混合物を遠心加速度30G以上でメカニカルミリング処理することによって、SiOにリチウムがプリドープされた珪素酸化物粉末を得ることを特徴とする珪素酸化物粉末の製造方法とする。
【0022】
これにより、活物質を含有する電極に金属リチウムの薄膜を貼り付ける方法やリチウムを蒸着する方法などの従来のプリドープ方法に比べて、工業的な実用性が高く、高い充放電容量を有するリチウムイオン二次電池を得ることが可能である、珪素酸化物粉末が提供される。
また、前記第一の原料と前記第二の原料の混合物を遠心加速度30G以上でメカニカルミリング処理することによって、SiOにリチウムがプリドープされた珪素酸化物粉末を確実に得ることができる。
更に、出発物質の一つである第二の原料として金属リチウムを使用しているため、LiOHやLiO2を使用した場合のように還元処理を行う必要がない。
【0023】
請求項7に係る発明では、
前記メカニカルミリング処理後の珪素酸化物粉末を、不活性雰囲気下において、648℃以上850℃以下の温度で加熱処理することを特徴とする請求項6記載の珪素酸化物粉末の製造方法とする。
【0024】
これにより、SiOにリチウムをプリドープした時に、リチウムが不可逆容量分に比べて過剰に入った場合や、過剰に入っていなくともSiOとリチウムの混合が不均一でリチウム濃度が高い部分がある場合に生成されるLi12Si7を、加熱処理により分解除去することができる。また、リチウム濃度が全体に均一化し、SiとLi4SiO4の結晶化が促進されることで安定化する。これにより、発火の危険性が少なく安全で安定したリチウムイオン二次電池負極材用の珪素酸化物粉末を提供することが可能となる。
また、加熱処理の温度を650℃〜850℃に設定することにより、SiOが存在してもSiとSiO2に不均化することが防がれ、SiやLi4SiO4等がナノレベルで高分散した珪素酸化物粉末を得ることができる。
【発明の効果】
【0025】
本発明によれば、高い充放電容量を有するリチウムイオン二次電池を得ることが可能であるとともに、空気や水と反応して発火することがなく取り扱いが容易であって工業的実用性が高い、リチウムイオン二次電池用の負極材料及びその製造方法と、高い充放電容量を有するリチウムイオン二次電池が提供される。
【図面の簡単な説明】
【0026】
【図1】実施例サンプルについてのXRDチャートである。
【図2】比較例1サンプルについてのXRDチャートである。
【図3】比較例2サンプルについてのXRDチャートである。
【図4】比較例3サンプルについてのXRDチャートである。
【図5】比較例4サンプルについてのXRDチャートである。
【図6】実施例サンプルについてのCV測定結果である。
【図7】比較例1サンプルについてのCV測定結果である。
【図8】比較例2サンプルについてのCV測定結果である。
【図9】比較例3サンプルについてのCV測定結果である。
【図10】比較例4サンプルについてのCV測定結果である。
【図11】(a)は実施例サンプルについての充放電曲線図であり、(b)は(a)の1次微分曲線である。
【図12】(a)は比較例1サンプルについての充放電曲線図であり、(b)は(a)の1次微分曲線である。
【図13】(a)は比較例2サンプルについての充放電曲線図であり、(b)は(a)の1次微分曲線である。
【図14】(a)は比較例3サンプルについての充放電曲線図であり、(b)は(a)の1次微分曲線である。
【図15】Li−Si二元系状態図である。(出典:T.B.Massalski, H. Okamoto, P. R. Subramanian, and L. Kacprzak, eds., Binary Alloy Phase Diagrams, 2nd ed. (ASM International, Metals Park, Ohio, 1990)
【図16】Li2O−SiO2疑二元系状態図である。(出典:A. Skokan, H. Wedemeyer, D. Vollath and E. Gunther:Proc. 14th Symp. On Fusion Technology, Avignon, Sept. 8-12, 1986, p.1255)
【発明を実施するための形態】
【0027】
以下、本発明に係る珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、この材料を用いたリチウムイオン二次電池、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法の好適な実施形態について説明する。
【0028】
<珪素酸化物粉末について>
本発明に係る珪素酸化物粉末は、リチウムを含有する珪素酸化物粉末であって、Cu−kα線源でのX線回折(XRD)において、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、0.01<B/A<5.0、C/A<1.0、D/A<1.0を満たすものである。
また、2θ=18.7°±0.2°におけるピークの面積強度をEとしたとき、0.2≦E/B<1を満たすことが好ましい。
【0029】
後述する実施例及び比較例に示す如く、上記条件を満たす珪素酸化物粉末を負極材料(負極活物質)として使用したリチウムイオン二次電池は、これらを満たさない珪素酸化物粉末を負極材料として使用したリチウムイオン二次電池と比較して、高い充放電容量を有する。
【0030】
また、本発明に係る珪素酸化物粉末は、粒度の積算分布曲線における累積頻度50%の粒径D50が0.5μm≦D50≦50μmであり、且つBET比表面積50m2/g以下である。
【0031】
D50が0.5μm未満であると、電極スラリー製造時にスラリー中の粒子が凝集し易くなり、均一なスラリーが得難いという問題があるため、好ましくない。また、粒子が細かいと、表面積が大きくなり、試料の保存中に表面が酸化し易くなってしまうため、好ましくない。一方、D50が50μmを超えると、大きい粒径の珪素酸化物を多数含有することとなり、リチウムイオン二次電池の負極材として使用すると、リチウムイオンが珪素酸化物の内部まで入り込めず、酸化珪素が性能を充分に発揮できずに初期効率が低下するため、好ましくない。なお上記した電極スラリーとは、電極製造時に集電体へ塗工するペースト状のものであり、活物質、導電助剤、バインダー(結着材)、粘度調整用の溶媒、などを混練して得られるもののことをいう。
BET比表面積50m2/gを超えると、珪素酸化物粉末の単位質量当たりの表面積が多くなり、珪素酸化物表面に形成されるSiO膜の含有量が増加する。そのため、リチウムイオン二次電池の負極材料として用いた場合に、SiO膜によるリチウムイオン二次電池の初期効率及びサイクル特性の低下が生じる虞があり、好ましくない。
【0032】
粒度の積算分布曲線における累積頻度50%の粒径D50(μm)は、レーザー回折散乱法による粒度分布の測定結果に基づいて算出することができる。測定機としては、例えばMastersizer2000(Malvern社製)等を使用することができる。
BET比表面積は、窒素ガス吸着式によるBET一点法により測定される値であり、測定機としては、例えばMacsorb HM model(マウンテック社製)等を使用することができる。
【0033】
<珪素酸化物粉末の製造方法について>
本発明に係る珪素酸化物粉末の製造方法では、SiOからなる第一の原料と、金属リチウムからなる第二の原料を使用し、不活性雰囲気下において、前記第一の原料と前記第二の原料の混合物を乾式にてメカニカルミリング処理することにより、SiOにリチウムがプリドープされた珪素酸化物粉末を得る。
【0034】
メカニカルミリング処理とは、衝撃・引張り・摩擦・圧縮・せん断等の外力を原料に与える方法であって、転動ミル、振動ミル、遊星ミル、揺動ミル、水平ミル、アトライターミル、ジェットミル、擂潰機、ホモジナイザー、フルイダイザー、ペイントシェイカー、ミキサー等などを用いる方法が挙げられる。
例えば、遊星ミルを用いる方法では、原料粉末とボールとを共に容器に入れ、自転と公転をさせることによって生じる力学的エネルギーにより、原料を粉砕・混合又は固相反応させることができる。
【0035】
第一の原料としては、SiO粉末が好適に使用される。SiO粉末としては、粒径1μm〜20μmのもの、より好ましくは粒径1μm〜10μmのものが好適に使用される。粒径が1μm未満であると電極スラリー製造時にスラリー中の粒子が凝集し易くなり、均一なスラリーが得難いという問題があるため、好ましくない。また、粒子が細かいと、表面積が大きくなり、試料の保存中に表面が酸化し易くなってしまうため、好ましくない。また、粒径が20μmを超えると塗工する電極が厚くなってしまい、充放電時に電極が劣化しやすく、充放電サイクル寿命が低下する原因となり、いずれの場合も好ましくない。
第二の原料としては、例えば金属リチウムの薄膜が使用される。薄膜としては、例えば金属リチウム金属薄膜(厚さ500μm、幅50mm)を所定のサイズ(例えば2〜10mm角程度)に切断したものが使用される。
これら第一の原料と第二の原料を、不活性雰囲気下(例えばアルゴン等の不活性ガス雰囲気下)において、メディア(例えばボール)と共に容器(例えばポット)内に入れて容器を高速で回転させる(メカニカルミリング処理する)ことにより、SiOにリチウムが不可逆容量分プリドープされた珪素酸化物粉末を得る。
第一の原料と第二の原料の配合比(重量比)は、第一の原料1に対して第二の原料が0.12〜0.17となるように設定することが好ましい。この配合比より第二の原料が少ないとプリドープされるリチウムが不可逆容量分に満たない虞があり、逆に多いとリチウムが不可逆容量分に比べて過剰となる虞があり、いずれの場合も好ましくない。
【0036】
容器の内面の材質は、例えばジルコニア、ステンレス、窒化珪素、炭化珪素等が好適であるが、このうちリチウムと反応しないステンレスが最も好適である。
メディアとしては、直径2mm〜4mm程度のボールが好適に使用される。メディアの材質は、ジルコニア、ステンレス、窒化珪素、炭化珪素等が好適であるが、このうちリチウムと反応しないステンレスが最も好適である。
ミリング条件は、遠心加速度30G以上に設定する。遠心加速度が30G未満の場合、SiOにリチウムが不可逆容量分プリドープされた珪素酸化物粉末が得られない虞があり好ましくない。好適には、30〜150G×10分〜10時間の範囲に設定することができ、例えば100G×3時間に設定される。
【0037】
本発明においては、上記メカニカルミリング処理により得られた珪素酸化物粉末(SiOにリチウムがプリドープされた珪素酸化物粉末)を、不活性雰囲気下(例えばアルゴン等の不活性ガス雰囲気下)において加熱処理することが好ましい。
加熱処理の温度は648℃以上1255℃以下、好ましくは650℃〜850℃に設定される。加熱時間は、加熱温度が650℃〜850℃の場合、例えば30分〜10時間に設定される。
この加熱処理を行う理由は、以下の通りである。
【0038】
上記メカニカルミリング処理により得られた珪素酸化物粉末は、SiOにリチウムが不可逆容量分プリドープされており、理想的には、ナノサイズレベルの微小なSiと、微小なLi4SiO4とが高分散した状態となっているものと考えられる。
しかし、もし不可逆容量分に比べて過剰にリチウムが入った場合や、又は過剰でなくても混合が不均一でリチウム濃度が高い部分がある場合には、SiとLi4SiO4以外にLi12Si7が生成すると考えられる。
このLi12Si7合金は、水分に接触すると発火の危険性がある物質である。そのため、最終的に得られるリチウムイオン二次電池負極材用の珪素酸化物粉末中に存在することは好ましくない。
【0039】
Siの融点は約1410℃であるため、それ以下の温度域では安定に存在する。
Li4SiO4は、図16のLi2O−SiO2疑二元系状態図より、1255℃(=1528K−273)までは安定に存在できる。
一方、リチウムプリドープ時に余分に生成し得るLi12Si7は、図15のLi−Si二元系状態図より648℃以上では安定に存在できない。
【0040】
これらのSi、Li4SiO4、Li12Si7の各物質の安定温度域の関係から、上記メカニカルミリング処理により得られた珪素酸化物粉末を、不活性雰囲気下において648℃以上1255℃以下の温度で加熱処理すると、余分なLi12Si7は分解され、不可逆容量分を超えた過剰なリチウムを除去することができる。また、リチウム濃度が全体に均一化し、SiとLi4SiO4の結晶化が促進されることで安定化する。
また、加熱処理の温度を650℃〜850℃に設定すると、SiOが存在しても不均化しなくなる温度域となるため、より一層好ましい。上述した通り、本願発明者は、SiOは900℃以上で加熱すると不均化することを実験により確認している。
【0041】
<リチウムイオン二次電池について>
上記した本発明に係る珪素酸化物粉末をリチウムイオン二次電池用負極材料として使用してリチウムイオン二次電池を製造することができる。
リチウムイオン二次電池の製造においては、公知のリチウムイオン二次電池の電池要素(正極、セパレーター、電解液等)を用い、常法に従って、角型、円筒型、コイン型等の電池に組み立てればよい。
【0042】
負極材料は、本発明に係る珪素酸化物粉末(活物質)と、導電助剤と、バインダーとから構成することができる。必要であれば、その他の活物質を添加してもよい。
負極材料は、本発明に係る珪素酸化物粉末を50〜95%含有することが好ましい。
50%未満であると珪素酸化物の容量向上効果が充分に得られず、95%を超えるとバインダーが少なくなり、電極が充放電に伴う体積変化に耐えられず、電極が劣化して機能しなくなるため、いずれの場合も好ましくない。配合比(重量比)の一例を挙げると、本発明に係る珪素酸化物粉末:導電助剤:バインダー=85:5:10である。
【0043】
導電助剤としては、通常用いられているもの、例えばアセチレンブラック(AB)、ケッチェンブラック(KB)、黒鉛、カーボンファイバー、カーボンチューブ、非晶質炭素等の炭素材料を、一種単独で、或いは二種以上を組み合わせて使用することができる。
【0044】
バインダーも通常用いられているもの、例えば、ポリフッ化ビニリデン(PVdF)、ポリテトラフルオロエチレン(PTFE)、ポリイミド(PI)、ポリアミド、ポリアミドイミド、ポリアクリル、スチレンブタジエンゴム(SBR)、スチレン−エチレン−ブチレン−スチレン共重合体(SEBS)、カルボキシメチルセルロース(CMC)等の材料を一種単独で、或いは二種以上を組み合わせて使用することができる。
【0045】
集電体は、電子伝導性を有し、保持した負極材料に通電し得る材料であれば特に限定されない。例えば、C、Ti、Cr、Ni、Cu、Au、ステンレス鋼等が好ましく使用される。
【0046】
正極としては、例えば、コバルト酸リチウム(LiCoO2)、ニッケル酸リチウム(LiNiO2)、マンガン酸リチウム(LiMn2O4)、リン酸鉄リチウム(LiFePO4)、コバルトマンガンニッケル酸リチウム(LiCo0.33Ni0.33Mn0.33O2)等の公知のものが用いられる。
【0047】
セパレータとしては、公知のリチウムイオン二次電池に用いられるものが使用できる。
例えば、ポリエチレン(PE)、ポリプロピレン(PP)、ポリエステル、セルロース、アラミド、ポリアミドイミド(PAI)、ポリアミド(PA)、ポリイミド(PI)等の樹脂からなる多孔質シート、ガラスフィルター、不織布等を用いることができるが、これらに限定はされない。
【0048】
電解質は、リチウムイオン二次電池で用いられるものであれば特に限定されないが、その電解質塩としては、リチウム塩が好適である。このリチウム塩としては、具体的には、ヘキサフルオロリン酸リチウム、過塩素酸リチウム、テトラフルオロホウ酸リチウム、トリフルオロメタンスルホン酸リチウム及びトリフルオロメタンスルホン酸イミドリチウムよりなる群から選択される少なくとも一種を用いることができる。
【0049】
上記電解質の溶媒としては、プロピレンカーボネート(PC)、エチレンカーボネート(EC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、γ−ブチロラクトン、2−メチルテトラヒドロフラン、1,3−ジオキソラン、4−メチル−1,3−ジオキソラン、1,2−ジメトキシエタン、1,2−ジエトキシエタン、ジエチルエーテル、スルホラン、メチルスルホラン、ニトロメタン、N,N−ジメチルホルムアミド、ジメチルスルホキシドよりなる群から選択される少なくとも一種を用いることができる。但し、溶媒を用いずにポリマー電解質や固体電解質としてもよい。
【実施例】
【0050】
以下、本発明の実施例及び比較例を示すことにより本発明の効果を明確にする。但し、本発明は以下の実施例に何ら限定されるものではない。
【0051】
<1.サンプルの作製>
(1)実施例サンプル
SiO粉末10.0245g(大阪チタニウムテクノロジーズ社製)と金属リチウムのテープ(厚さ500μm、幅50mm)(本庄金属社製)を2mm×2mmに切断したもの(1.574g)とをジルコニア製のポットに入れ、グローボックス不活性雰囲気(アルゴン雰囲気)にて、φ2mmのジルコニア製ボールをメディア(粉砕媒体)として使用し、100G×3時間の運転条件にて、ボールミルにてメカニカルミニング処理することにより、SiOにリチウムが不可逆容量分ドープされた珪素酸化物粉末を得、これを実施例サンプルとした。
【0052】
(2)比較例1サンプル
実施例サンプルで使用したものと同じSiO粉末そのものを比較例1サンプルとした。
【0053】
(3)比較例2サンプル
実施例サンプルで使用したものと同じSiO粉末を、アルゴン雰囲気で1200℃×3時間の条件で焼成し、SiO粉末の一部を不均化反応(2SiO→Si+SiO2)させたものを比較例2サンプルとした。
【0054】
(4)比較例3サンプル
比較例2サンプル(不均化SiO)を、実施例サンプルの作製時と同条件でメカニカルミニング処理することにより、比較例2サンプル(不均化SiO)にリチウムが不可逆容量分ドープされた珪素酸化物粉末を得、これを比較例3サンプルとした。
【0055】
(5)比較例4サンプル
通常の塗工SiO電極を対極とし、金属リチウムで電池(半電池)を組んで、充放電させることにより、SiOにリチウムを不可逆容量分ドープさせ、これを比較例4サンプルとした。
【0056】
<2.XRD分析>
実施例及び比較例1〜4のサンプルについて、下記条件によりXRD分析を行った。
・X線回折装置:ブルカーAXS社製、型番:M06XCE
・線源:CuKα(波長λ=0.15418nm)
・出力:40kV,100mA
・サンプリング幅:0.02°
・走査範囲:2θ=10〜70°
・分析ソフト:Windows(登録商標)版 JADE(6.0)、理学電機社製
【0057】
分析結果を図1〜図5、表1〜表3に示す。
なお、XRDピークの2θ角度、高さ、面積及び半値幅の分析値は、上記分析ソフトによる多重ピーク分離処置により求められた値を用いた。
図1は実施例サンプルについてのXRDチャートであり、表1は図1のXRDチャートの分析結果である。
【0058】
【表1】

【0059】
実施例サンプルは、図1に示すように、アモルファスの傾向が見られるものの、Li−Si−O酸化物(Li2SiO3及びLi4SiO4)のピークが確認できる。Li−Si−O酸化物は不可逆成分であり、空気や水と反応して発火することがない。
実施例サンプルは、表1に示すように、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、A=13064、B=18423、C=0、D=5016であるから、0.01<B/A<5.0、C/A<1.0、D/A<1.0を満たしている。
また、2θ=18.7°±0.2°におけるピークの面積強度をEとしたとき、E=
10362であるから、0.2≦E/B<1を満たしている。
【0060】
図2は比較例1サンプルについてのXRDチャートである。
比較例1サンプルは、図2に示すように、アモルファス状態であり、ピークが確認できない。
【0061】
図3は比較例2サンプルについてのXRDチャートであり、表2は図3のXRDチャートの分析結果である。
【0062】
【表2】

【0063】
比較例2サンプルは、図3に示すように、SiOから不均化されたSiとSiO2のピークが確認できるが、不可逆成分であるLi−Si−O酸化物(Li2SiO3及びLi4SiO4)のピークは確認できない。
また、表2に示すように、2θ=28.4°±0.2°のピーク(Siのピーク)が検出されたが、2θ=18.7°±0.2°のピーク(Li2SiO3のピーク)、22.1°±0.2°のピーク(Li4SiO4のピーク)、40.5°±0.2°のピーク(Li13Si14のピーク)、56.2°±0.2°のピーク(Li2Oのピーク)がいずれも検出されていない。
表2では、Siの回折ピークが低角側へシフトしており、28.041°に現れている。これは、1200℃の熱処理によりSiOからSiが生成する不均化反応の際に、温度が低くこの反応が不完全であるため、純Si結晶と同じ結晶格子のサイズにはならず、28.4°±0.2°からシフトしたものと考えられる。1400℃以上まで熱処理温度を上げると、結晶Siと結晶SiO2に不均化することが知られている。
【0064】
図4は比較例3サンプルについてのXRDチャートであり、表3は図4のXRDチャートの分析結果である。
【0065】
【表3】

【0066】
比較例3サンプルは、図4に示すように、SiOから不均化されたSiとSiO2のピークに加えて、不可逆成分であるLi−Si−O酸化物(Li4SiO4)のピークが確認できる。これは、焼成時に残っていたSiOがプリドープされたためであると考えられる。
また、表3に示すように、2θ=22.1°±0.2°のピーク(Li4SiO4のピーク)と28.4°±0.2°(Siのピーク)は存在しているが、18.7°±0.2°のピーク(Li2SiO3のピーク)、40.5°±0.2°のピーク(Li13Si14のピーク)、56.2°±0.2°のピーク(Li2Oのピーク)がいずれも存在していない。
表3では、Siの回折ピークが低角側へシフトしており、28.082°に現れている。これは、1200℃の熱処理によりSiOからSiが生成する不均化反応の際に、温度が低くこの反応が不完全であるため、純Si結晶と同じ結晶格子のサイズにはならず、28.4°±0.2°からシフトしたものと考えられる。1400℃以上まで熱処理温度を上げると、結晶Siと結晶SiO2に不均化することが知られている。
【0067】
図5は比較例4サンプルについてのXRDチャートである。
比較例4サンプルは、図5に示すように、不可逆成分であるLi−Si−O酸化物(Li2SiO3及びLi4SiO4)のピークが確認できない。
また、2θ=22.1°±0.2°のピーク(Li4SiO4のピーク)だけでなく、18.7°±0.2°のピーク(Li2SiO3のピーク)、28.4°±0.2°のピーク(Siのピーク)、40.5°±0.2°のピーク(Li13Si14のピーク)、56.2°±0.2°のピーク(Li2Oのピーク)も確認できない。
【0068】
<2.CV測定>
実施例及び比較例1〜4のサンプルについて、下記条件によりCV(サイクリックボルタンメトリ)測定を行った。
・電気化学測定装置:ソーラトロン社製、型番:1280B
・走引速度:0.2mV/sec
・電圧範囲:0〜3V
・雰囲気温度:30℃
【0069】
測定は、作用極ペレット法(実施例及び比較例1〜3)、作用極スラリー塗工法(比較例4)により行った。
実施例及び比較例1〜3の作用極ペレット法では、ドライルーム又はグローボックス内で各材料(各サンプルと他の材料)を乳鉢で混合し、混合物を加圧成形(プレス圧:20kN)して円板状のペレット(φ10mm、厚さ1〜2mm)を作製することにより、負極ペレットを構成し、これを作用極として用いた。尚、このペレットは後述する充放電試験でも使用した。
【0070】
実施例サンプルについては、これを負極活物質として用い、Cuとこの活物質を97.9wt%:2.1wt%(0.2643g:0.0057g)の割合で混合して上記方法により負極ペレットを構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
比較例1サンプルについては、これを負極活物質として用い、Cuとこの活物質を97.6wt%:2.4wt%(0.0715g:0.0018g)の割合で混合して上記方法により負極ペレットを構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
比較例2サンプルについては、これを負極活物質として用い、Cuとこの活物質を98.0wt%:2.0wt%(0.9807g:0.0201g)の割合で混合して上記方法により負極ペレットを構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
比較例3サンプルについては、これを負極活物質として用い、Cuとこの活物質を97.5wt%:2.5wt%(0.9829g:0.0251g)の割合で混合して上記方法により負極ペレットを構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
比較例4サンプルについては、SiOとKB(ケッチェンブラック)とPI(ポリイミド)の比率が80wt%:5wt%:15wt%(活物質量:0.002g)となる電極(負極)を構成し、これを作用極として用い、対極及び参照極として金属リチウムを用いた。
【0071】
測定結果を図6〜図10に示す。
図6は実施例サンプルについてのCV測定結果(0〜2V)である。
図7〜10は比較例1〜4サンプルについてのCV測定結果(0〜2V)である。
【0072】
実施例サンプル(図6)では、比較例1サンプル(図7)に比べて初期電圧値が低くなり(3.0V→1.4V)、1サイクル目と2サイクル目の軌道がほぼ一致した。このことから、ほぼ理論通りにSiOに対してリチウムが不可逆プリドープされた(不可逆容量分のみプリドープされた)ことが確認できる。
比較例2サンプル(図8)では、実施例サンプルに比べて充放電反応が鈍いことが確認できる。これは、不均化処理により粒子表面にSiO2膜が生成されたためであると考えられる。
比較例3サンプル(図9)では、比較例2サンプルに比べると充放電反応が良好となったことが確認できる。これは、メカニカルミリング処理によりSiO2膜が粉砕されたことにより、比較例2サンプルと比べて充放電し易くなったと考えられる。しかし、SiO不可逆プリドープができる設計量のリチウムを加えたが、初期電圧値は2.4Vまでしか低下しなかった。
比較例4サンプル(図10)では、初期電圧値の低下は見られない。
尚、OCV(Opened Circuit Voltage)は、実施例サンプル:3.4V、比較例1サンプル:1.4V、比較例2サンプル:3.1V、比較例3サンプル:2.4Vであり、実施例サンプルが最も高かった。
【0073】
<3.充放電試験>
実施例及び比較例1〜3のサンプルについて、上記CV測定において作製したペレットを使用してコインセルを作製し、下記条件により充放電試験を行った。
・電圧範囲:0〜1V vs Li+/Li
・電流値:0.1C
【0074】
コインセルは以下の方法により作製した。
実施例及び比較例1〜3のサンプルを用いて作製したペレット電極と、対極の金属リチウムとを、電解液を含ませたセパレータを挟んで直接接触させないように配置し、2032型コインセル部材(宝泉株式会社製)を用いて密封し、コインセルを作製した。
セパレータにはポリプロピレン製微多孔膜Celgard2400(Celgard社製)とガラスファイバーフィルターGA100(ADVANTEC社製)を1枚ずつ重ねたものを使用し、電解液には1 M LiPF6/(エチレンカーボネート(EC:ジエチルカーボネート(DEC), 1:1 体積比)、対極には金属リチウム箔(直径13mm、0.5mm厚、本城金属社製)をそれぞれ用いた。
【0075】
試験結果を図11〜図14の(a)に示し、(a)の1次微分曲線を(b)に示す。
図11は実施例サンプルについての試験結果である。
図12〜14は比較例1〜3サンプルについての試験結果である。
表5は、実施例及び比較例1〜3サンプルについての可逆理論容量と1サイクル目及び2サイクル目の容量を示す。表中の数値の単位は「mAh/g」である。
【0076】
【表4】

【0077】
実施例サンプル(図11)では、比較例1サンプル(図12)において0.41V付近にあった不可逆容量が殆ど見られなくなった。((b)図参照)これは、リチウムがプリドープされたことにより初期不可逆容量成分の生成反応が無くなった為と考えられる。また不可逆容量は、比較例1サンプルが2911−1839=1072mAh/gであったのに対して、実施例サンプルでは1688−1355=333mAh/gと低くなった。
比較例2サンプル(図13)でも、比較例1サンプルにおいて0.41V付近にあったピークが見られない。これは、不均化処理によりSiとSiO2に分離して不可逆容量が消えたと考えられる。
比較例3サンプル(図14)でも、比較例1サンプルにおいて0.41V付近にあったピークが見られない。不可逆容量は1453−1122=331mAh/gと小さかったが、容量は実施例サンプル(図11)よりも低かった。
【0078】
<4.注水試験>
実施例サンプル及び比較例3サンプルについて、洗瓶を用いて、サンプルに直接水滴をかけるという方法により注水試験を行った。その結果、実施例サンプル及び比較例3サンプル共に、ガスが発生したものの発火しなかった。
【0079】
<5.D50の測定>
実施例サンプル及び比較例1〜4サンプルについて、粒度の積算分布曲線における累積頻度50%の粒径D50をレーザー回折式粒度分布測定装置としてMastersizer2000(Malvern)を使用して測定した。結果を表6に示す。
【0080】
【表5】

【0081】
<6.BET比表面積の測定>
実施例サンプル及び比較例1〜4サンプルについて、BET比表面積を窒素ガス吸着式によるBET一点法により、測定機としてMacsorb HM model(マウンテック社製)を使用して測定した。結果を表7に示す。
【0082】
【表6】

【0083】
表6及び表7に示すように、実施例サンプルは0.5μm≦D50≦50μm、BET比表面積50m2/g以下を満たしたが、比較例サンプルはいずれも満たさなかった。尚、比較例サンプルについては、原料のSiO粉末のBET比表面積が実施例サンプルよりも大きいものを使用した。
【0084】
<まとめ>
実施例サンプル(本発明に係る珪素酸化物粉末)は、Cu−kα線源でのXRDにおいて、2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°、18.7°±0.2°におけるピークの面積強度を夫々A,B,C,D,Eとしたとき、0.01<B/A<5.0、C/A<1.0、D/A<1.0、0.2≦E/B<1を満たすが、比較例1〜4サンプルは満たさないことが確認された。
実施例サンプルは0.5μm≦D50≦50μm、BET比表面積50m2/g以下を満たすが、比較例サンプルはいずれも満たさないことが確認された。
実施例サンプルは、Li−Si−O酸化物(Li2SiO3及びLi4SiO4)から構成されており、リチウム不可逆プリドープが行われていることが確認された。また、発火し易い単体リチウムやLi−Si合金は存在していないため、発火の危険性が無く、取り扱いが容易であると言える。このことは注水試験によっても確認された。
一方、比較例1〜4サンプルでは、比較例1,2,4サンプルではLi−Si−O酸化物(Li2SiO3及びLi4SiO4)の存在が確認されなかった。比較例3サンプルは、Li−Si−O酸化物の存在が確認されたが、SiO2の存在も確認され、不可逆成分の生成が不十分であった。また、充放電容量において実施例サンプルに劣っていた。
【産業上の利用可能性】
【0085】
本発明に係る珪素酸化物粉末及びこれを用いたリチウムイオン二次電池用負極材料、並びにリチウムイオン二次電池負極材用の珪素酸化物粉末の製造方法は、高い充放電容量を有するリチウムイオン二次電池を得ることができ、取り扱いが容易であって工業的な実用性にも優れているため、リチウムイオン二次電池の製造において極めて有用である。また本発明に係るリチウムイオン二次電池は、高い充放電容量を有することから、電気自動車や移動体通信端末等の様々な利用分野における電源として極めて有用である。
【特許請求の範囲】
【請求項1】
リチウムを含有する珪素酸化物粉末であって、
Cu−kα線源でのX線回折(XRD)において、
2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、
0.01<B/A<5.0
C/A<1.0
D/A<1.0
を満たすことを特徴とする珪素酸化物粉末。
【請求項2】
2θ=18.7°±0.2°におけるピークの面積強度をEとしたとき、
0.2≦E/B<1
を満たすことを特徴とする請求項1記載の珪素酸化物粉末。
【請求項3】
粒度の積算分布曲線における累積頻度50%の粒径D50が0.5μm≦D50≦50μmであり、且つBET比表面積50m2/g以下であることを特徴とする請求項1又は2記載の珪素酸化物粉末。
【請求項4】
請求項1乃至3いずれかに記載の珪素酸化物粉末を含有することを特徴とするリチウムイオン二次電池用負極材料。
【請求項5】
請求項4に記載の負極材料を用いた負極を備えることを特徴とするリチウムイオン二次電池。
【請求項6】
リチウムイオン二次電池の負極材に用いられる珪素酸化物粉末の製造方法であって、
SiOからなる第一の原料と、金属リチウムからなる前記第二の原料を使用し、
不活性雰囲気下において、前記第一の原料と前記第二の原料の混合物を遠心加速度30G以上でメカニカルミリング処理することにより、SiOにリチウムがプリドープされた珪素酸化物粉末を得ることを特徴とする珪素酸化物粉末の製造方法。
【請求項7】
前記メカニカルミリング処理後の珪素酸化物粉末を、不活性雰囲気下において、648℃以上850℃以下の温度で加熱処理することを特徴とする請求項6記載の珪素酸化物粉末の製造方法。
【請求項1】
リチウムを含有する珪素酸化物粉末であって、
Cu−kα線源でのX線回折(XRD)において、
2θ=22.1°±0.2°、28.4°±0.2°、40.5°±0.2°、56.2°±0.2°におけるピークの面積強度を夫々A,B,C,Dとしたとき、
0.01<B/A<5.0
C/A<1.0
D/A<1.0
を満たすことを特徴とする珪素酸化物粉末。
【請求項2】
2θ=18.7°±0.2°におけるピークの面積強度をEとしたとき、
0.2≦E/B<1
を満たすことを特徴とする請求項1記載の珪素酸化物粉末。
【請求項3】
粒度の積算分布曲線における累積頻度50%の粒径D50が0.5μm≦D50≦50μmであり、且つBET比表面積50m2/g以下であることを特徴とする請求項1又は2記載の珪素酸化物粉末。
【請求項4】
請求項1乃至3いずれかに記載の珪素酸化物粉末を含有することを特徴とするリチウムイオン二次電池用負極材料。
【請求項5】
請求項4に記載の負極材料を用いた負極を備えることを特徴とするリチウムイオン二次電池。
【請求項6】
リチウムイオン二次電池の負極材に用いられる珪素酸化物粉末の製造方法であって、
SiOからなる第一の原料と、金属リチウムからなる前記第二の原料を使用し、
不活性雰囲気下において、前記第一の原料と前記第二の原料の混合物を遠心加速度30G以上でメカニカルミリング処理することにより、SiOにリチウムがプリドープされた珪素酸化物粉末を得ることを特徴とする珪素酸化物粉末の製造方法。
【請求項7】
前記メカニカルミリング処理後の珪素酸化物粉末を、不活性雰囲気下において、648℃以上850℃以下の温度で加熱処理することを特徴とする請求項6記載の珪素酸化物粉末の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【公開番号】特開2013−114820(P2013−114820A)
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願番号】特願2011−258303(P2011−258303)
【出願日】平成23年11月25日(2011.11.25)
【出願人】(301021533)独立行政法人産業技術総合研究所 (6,529)
【出願人】(397064944)株式会社大阪チタニウムテクノロジーズ (133)
【Fターム(参考)】
【公開日】平成25年6月10日(2013.6.10)
【国際特許分類】
【出願日】平成23年11月25日(2011.11.25)
【出願人】(301021533)独立行政法人産業技術総合研究所 (6,529)
【出願人】(397064944)株式会社大阪チタニウムテクノロジーズ (133)
【Fターム(参考)】
[ Back to top ]

