生体吸収性医療材料
【課題】創傷部に密着し、止血、癒着防止などの効果を有する生体吸収性医療材料を提供する。
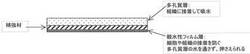
【解決手段】生体組織に接する面を生体吸収性の多孔質層とし、その反対面を生体吸収性の親水性フィルム層で構成することによって、生体組織の創傷部において止血、空気漏れ防止のみならず、周囲組織との癒着を防止できる生体吸収性医療材料とした。さらに多孔質層と親水性フィルム層の間に補強材料を配置することによって、湿潤状態でも取り扱い性を向上させたシート状の生体吸収性医療材料である。
【解決手段】生体組織に接する面を生体吸収性の多孔質層とし、その反対面を生体吸収性の親水性フィルム層で構成することによって、生体組織の創傷部において止血、空気漏れ防止のみならず、周囲組織との癒着を防止できる生体吸収性医療材料とした。さらに多孔質層と親水性フィルム層の間に補強材料を配置することによって、湿潤状態でも取り扱い性を向上させたシート状の生体吸収性医療材料である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、生体内の組織に密着して創傷部における止血、被覆、閉鎖の効果の役目を果たすとともに、創傷部と周囲組織との癒着を防止する効果を有する、フィルム層と多孔質層からなる生体吸収性医療材料に関する。
【背景技術】
【0002】
生体組織に創傷ができると生体組織から出血する。一時的に止血しても、不完全なままに放置されているとさらなる出血を引き起こすこととなり好ましくない。また、創傷部の生体組織から体液などが漏れるため、創傷部を何らかの手段で閉鎖することが必要になる。さらに、創傷部が大きい場合にはシート状材料などで創傷部を被覆しなければ、周囲から細胞や生体組織が侵入して創傷部と周囲の正常組織との間に癒着が発生し、創傷部の治癒を阻害するだけでなく種々の合併症が発生する危険性がある。
【0003】
このような理由から、外科手術においては創傷部の止血材、被覆材、閉鎖材、癒着防止材など種々のシート状の医療材料が使用されている。よく知られた例としては、コラーゲンフリースの片面にフィブリノーゲンとトロンビンを付着したシート状の止血材料(商品名タココンブ)がある。癒着防止を目的とした材料としては、ヒアルロン酸とカルボキシメチルセルロースからなるフィルム状材料(商品名セプラフィルム)、酸化再生セルロースからなる布状材料(商品名インターシード)、ゼラチンフィルムからなる材料(特許文献1、2)などがある。また、創傷部の被覆を目的とした医療材料としては、ポリグリコリドの不織布(商品名ネオベール)などがある。これらの材料はいずれも生体吸収性であり、かつ、平面状材料である。
【0004】
これらの材料は創傷部に密着し、容易に移動しないことが必要である。例えば、コラーゲンフリースの片面にフィブリノーゲンとトロンビンを付着したシート状材料は、フィブリノーゲンとトロンビンの接着効果によって生体組織に密着する。ヒアルロン酸とカルボキシメチルセルロースからなるフィルム状材料にはこのような接着効果はないが、生体組織に接触させると物理的に密着する。ポリグリコール酸製不織布にはこのような接着効果や密着性がないために、フィブリン糊などの接着剤を用いて生体組織に密着、固定させる必要がある。
【0005】
これらの吸収性医療材料は外科手術の成績向上に大いに貢献しているが、一方で欠点も指摘されている。例えば、ヒアルロン酸とカルボキシメチルセルロースからなるフィルム状材料の生体組織への密着効果は十分でなく、しばしば、創傷部から材料が移動してしまい、その結果として癒着を起こしてしまうことがあった。さらに、水分で濡れると材料が破れやすく、そのために材料の位置を修正するための移動ができないという欠点があった。コラーゲンフリースの片面にフィブリノーゲンとトロンビンを付着したシート状材料は、材料の伸展度が低いために生体組織に密着しにくく、そのために止血効果が不十分となる場合がある。ポリグリコリド製不織布は、接着剤を使用しなければ生体組織表面に密着、固定させることができないという問題があった(特許文献3、4)。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2004−209228号公報
【特許文献2】特開2007−44080号公報
【特許文献3】特開2009−183649号公報
【特許文献4】WO2009/128474号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
生体組織の創傷部に密着することが可能であり、かつ取り扱い性に優れ、止血、被覆、閉鎖、癒着防止の効果を有するとともに創傷部の治癒を促進させることができる生体吸収性医療材料を提供することである。
【課題を解決するための手段】
【0008】
本願発明者らは、これらの問題を解決するために鋭意研究を重ねた結果、生体吸収性医療材料が生体組織表面上に存在する少量の水分と接触したときにヒドロゲル状になることによって、良好な密着性を生じることを見出した。すなわち、生体吸収性医療材料の生体組織と接触する面に少量の水分によってヒドロゲル状になる多孔質層が存在するような材料を設計した。一方で、反対面には親水面のフィルム層を配し、周囲組織との癒着を防止する効果を有するように材料設計を行った。このように、多孔質層とフィルム層からなる二層構造を有する生体吸収性医療材料を用いることによって、創傷部に密着して止血、被覆、閉鎖する効果を発揮し、創傷部の治癒を促進し、さらには創傷部と周囲組織との癒着を防止することができるという、これまでの医療材料にはない優れた効果が得られることを見いだした。また、多孔質層とフィルム層からなる二層構造であるだけでなく、薄いシート状(二層シート)とすることによって、材料に柔軟性を与えることができ組織への密着性が高まり、一方では材料の強度が向上することによって壊れにくいという取り扱いに優れた材料となることを見いだした。また、補強材料を複合化させた三層シート構造とすることによって、さらに壊れにくく取り扱い性に優れた材料とすることに成功した。
【発明の効果】
【0009】
本発明の生体吸収性医療材料は生体吸収性高分子からなり、創傷部が治癒した後には生体内で分解吸収され、異物が生体内に残存するようなことはない。また、吸水面は生体組織に密着しやすいことから縫合糸や接着剤を用いなくとも材料を創傷部に密着、固定することができるのみならず、創傷部の止血、閉鎖の効果が得られるものであるが、接着剤などとの併用によってさらに効果を高めることも可能である。また、創傷部に密着する面と反対側の面は親水性であることから、周囲組織との癒着を防止する効果が得られる。すなわち、本発明に係る材料を生体組織の創傷部に押しつけるだけで密着、固定することができ、さらに創傷部への癒着を防止できるという、これまでにない画期的な効果が得られるものである。
また、補強材料と複合化させることによって従来のフィルム状の材料と比較して材料の強度が向上し、一旦組織に密着させた材料を再度移動させることが可能になるばかりでなく、内視鏡手術のように狭い視野で操作を行う場合にも壊れにくいという、これまでにない医療現場で取り扱い性に優れた材料が得られるものである。
【図面の簡単な説明】
【0010】
【図1】本発明に係る三層シート構造を有する医療材料の断面を示す図である。
【図2】図2は、湿潤状態における二層シートおよび三層シートの引張強度を表すグラフである。
【図3】図3は、シートの吸水量の時間変化を表すグラフである。
【図4】図4は、架橋時間の異なる材料をラット皮下に埋入した時のの重量残存率を表すグラフである。
【図5】図5は、ラットの体内における二層シートの癒着評価を表すグラフである。
【図6】図6は、二層シートをイヌの腸管に貼付したときの3週間後の腸管顕微鏡写真である。
【図7】図7は、対照区の材料をイヌの腸管に貼付したときの3週間後の組織切片像である。
【発明を実施するための形態】
【0011】
本発明に係る生体吸収性医療材料を構成する高分子は、生体内で分解吸収されるものであれば特に限定されるものではないが、親水性高分子、特に天然高分子であることが望ましい。このような天然高分子としては、コラーゲン、ゼラチン、ヒアルロン酸、アルギン酸、キチン、キトサンなどを例示することができる。このなかでも、水に溶解させることができ、加工性に優れるゼラチンを用いることが好ましい。
【0012】
これらの天然高分子は生体内ですぐに溶解してしまうことから、何らかの架橋処理がされている必要がある。架橋は加熱処理や紫外線照射、放射線照射などの物理的方法と、グルタルアルデヒドやカルボジイミドなどの架橋剤を用いる化学的方法がある。このうち、材料に架橋剤が残らない加熱処理や紫外線照射などの物理的方法による架橋を行うことが好ましい。
【0013】
生体吸収性医療材料が生体内で長期間残存すると、周囲の組織を傷つけ、かえって癒着を引き起こすことになってしまう。一方で、あまりに短期間で分解、吸収されてしまうと、止血や創傷治癒、癒着防止の効果が十分に得られない。本発明の生体吸収性医療材料は、生体内に埋入後12時間は存在していることが必要であり、一方で埋入後90日以内にすみやかに分解、吸収されることが望ましい。
【0014】
生体吸収性医療材料を生体組織の創傷部に密着させるためには、生体組織に接着する側の材料表面が、生体組織の少量の水分を吸水し、ヒドロゲル状になる層が存在する必要がある。このような層としては、親水性材料からなる多孔質層があげられる。すなわち、材料表面に吸水を容易にする微少な孔などが多数存在しているような構造であればよい。このような構造としては、編物、織物、不織布のような繊維構造であってもよいし、スポンジのような多孔質構造であってもよい。この中でも、水溶性高分子を用いる場合に作製が容易なスポンジ状の多孔質体からなることが好ましい。このようなスポンジ状の多孔質体からなる多孔質層の存在により、フィブリン糊や縫合糸などを用いなくても、必要な期間、生体組織に生体吸収性医療材料を密着、固定させることができるものである。
【0015】
このようなスポンジ状の多孔質体の製造方法としては、生体吸収性高分子を水などの溶媒に溶解した後に、この溶液を凍結乾燥する方法がある。あるいは、生体吸収性高分子水溶液を発泡しておいてから、その多孔構造を維持しながら凍結乾燥、風乾、あるいは生体吸収性高分子水溶液に非溶媒を加えて相分離させるなどの方法を例示することができる。
【0016】
スポンジ状の多孔質体の孔径は、1μm〜1,000μmであり、好ましくは5μm〜800μm
の範囲である。孔径が1μmより小さいと生体組織の水が材料に吸い込まないために密着性が悪くなり、材料が創傷部に密着できなくなるためである。一方、1,000μmを超えると孔径が大きすぎるために多孔質体の強度が下がりすぎて破れやすくなってしまうためである。
【0017】
スポンジ状の多孔質体の厚みは20μm〜15,000μmであり、好ましくは50μm〜10,000μmの範囲である。20μm未満であると材料が壊れやすく、一方で15000μm以上であると材料が硬くなり創傷部に密着しなくなってしまうためである。
【0018】
生体吸収性医療材料が創傷部と周囲組織との癒着を防止するためには、材料が生体組織と接触して密着する面とは反対面の材料表面が親水性のフィルム状であって、かつ、材料表面に細胞や組織が接着しないことが必要である。このような材料としては、親水性で表面が平滑なフィルム状の材料であれば特に限定されるものではない。このフィルム状の材料は、厚ければ柔軟性と操作性に欠けるため、できるだけ薄くすることが必要である。フィルム状の材料の厚さは1μm〜200μmであり、好ましくは2μm〜100μmの範囲である。厚さが1μm未満であると材料が壊れやすいために扱いにくく、一方で200μm以上であると材料が硬く創傷部に密着しなくなってしまうためである。
【0019】
フィルム状の材料の作製方法は特に限定されないが、生体吸収性高分子を溶媒に溶解したのちに、この溶液を型枠に流し込んで溶媒を除去するキャスト法や、溶液を平板上に流延して溶媒を除去する流延法などが例示できる。
【0020】
本発明に係る生体吸収性医療材料は、前述のごとく創傷部と密着する層を構成する多孔質層と、創傷部と周囲組織との癒着を防止するためのフィルム層を構成する材料からなる二層構造であることを特徴とする二層シートである。二層構造とするためには、各層を別個に作製しておいてから複合化させてもよいし、一つの層を作製してからさらにもう一つの層を作製させてもよい。さらには、二つの層を同時に作製させる方法であってもよい。
【0021】
本願発明に係る生体吸収性医療材料は、二層シートとすることによって操作性がきわめて良好になるものである。材料が水分で膨潤すると柔軟さが生じ、シート状を保った状態で肺のように常に形状の変化する組織に対しても密着し続けることができる。
【0022】
本願発明に係る生体吸収性医療材料は、内視鏡手術で用いることが想定される。内視鏡手術では手術器械を用いて狭い視野で手術を行うこととなり、創傷部に材料を密着させる場合に何度も位置を直すことありうる。このような場合、水分を吸収した材料は柔らかくて壊れやすく、さらなる補強が求められる。
【0023】
補強材料としては、生体吸収性繊維からなる薄い織物、編物、不織布などがあげられる。生体吸収性繊維の材料としては、吸収性高分子であれば特に限定されるものではないが、吸水時に容易に膨潤しない合成の吸収性高分子であることが好ましい。このうち、吸収速度が速いポリグリコリド、グリコリド−ラクチド共重合体、あるいはグリコリド−ε―カプロラクトン共重合体であることがより好ましい。
【0024】
本願発明に係る生体吸収性医療材料は、組織への密着性を高めるためには柔軟であることが必要である。そのためには、補強材はできる限り薄く柔軟性があることが必要である。補強材の厚さは5μm〜500μmであり、好ましくは10μm〜400μmの範囲である。5μm未満であると補強材自体の取り扱いが難しく成型が困難になってしまい、一方で500μm以上であると材料が硬く創傷部に密着しなくなってしまうためである。本願発明に係る医療材料は、多孔質層、フィルム層、さらに補強材料の三層構造からなる三層シートであってもよい。
【0025】
このように、本願発明の生体吸収性医療材料は、創傷部に材料を押し付けることによって密着させることができ、さらには創傷部の止血、閉鎖、組織再生、癒着防止などの種々の組織修復に必要な効果を発揮する。
【実施例】
【0026】
以下、実施例を挙げて本発明を説明するが、本発明はこれらの実施例に限定されるものではない。
【0027】
(実施例1)凍結乾燥法による二層シートの作製その1
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。トレー上に作製した前記ゼラチンフィルムの上から1.0%ゼラチン水溶液を5mL流し込み、25℃にて10分間静置した。その後、トレーを‐80℃の冷凍庫に30分間入れてゼラチン水溶液を凍結させた後、凍結乾燥機中で24時間処理することによりゼラチン多孔質層−フィルム層複合体(二層シート)を作製した。このときのシート全体の厚みは2mmであった。その後、二層シートを真空乾燥機に入れ、真空下、140℃で3時間、熱処理を行うことにより加熱架橋した。得られた二層材料をステンレス板で挟み、上から荷重を5分間かけることによってプレスした。得られた材料のフィルム層は平滑であり、スポンジ層は凸凹のある不透明体であった。材料の厚みは、1.3±0.1mmであった。スポンジ体の孔径は92μmであった。
【0028】
(実施例2)凍結乾燥法による二層シートの作製その2
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。トレー上に作製した前記ゼラチンフィルムの上から1.0%ゼラチン水溶液を10mL流し込み、25℃にて10分間静置した。その後、トレーを‐80℃の冷凍庫に30分間入れてゼラチン水溶液を凍結させた後、凍結乾燥機中で24時間処理することによりゼラチン多孔質層−フィルム層複合体(二層シート)を作製した。このときのシート全体の厚みは4mmであった。その後、二層シートを真空乾燥機に入れ、真空下、140℃で3時間、熱処理を行うことにより加熱架橋した。得られた二層材料をステンレス板で挟み、上から荷重を5分間かけることによってプレスした。得られた材料のフィルム層は平滑であり、スポンジ層は凸凹のある不透明体であった。材料の厚みは、2.5±0.1mmであった。スポンジ体の孔径は98μmであった。
【0029】
(実施例3)凍結乾燥法による二層シートの作製その3
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。トレー上に作製した前記ゼラチンフィルムの上から0.3%コラーゲン水溶液コラーゲンIP(新田ゼラチン社製)を5mL流し込み、25℃にて10分間静置した。その後、トレーを‐80℃の冷凍庫に30分間入れてゼラチン水溶液を凍結させた後、凍結乾燥機中で24時間処理することによりコラーゲン多孔質層−ゼラチンフィルム層複合体(二層シート)を作製した。このときのシート全体の厚みは1mmであった。その後、二層シートを真空乾燥機に入れ、真空下、140℃で3時間、熱処理を行うことにより加熱架橋した。得られた二層材料をステンレス板で挟み、上から荷重を5分間かけることによってプレスした。得られた材料のフィルム層は平滑であり、スポンジ層は凸凹のある不透明体であった。材料の厚みは、1.3±0.1mmであった。
【0030】
(実施例4)発泡法による二層シートの作製その1
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。続いて、2%ゼラチン水溶液を十分攪拌して起泡させ、起泡させたゼラチン水溶液6gをトレー上に作製した前記ゼラチンフィルムの上から流し込み、ゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは1mmであった。
これらの二層シートを真空乾燥機に入れ、真空下、140℃にて3時間、熱処理を行って加熱架橋した。このとき得られたシートのトレー側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は223μmであった。
【0031】
(実施例5)発泡法による二層シートの作製その2
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm2)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。続いて、4.5%ゼラチン水溶液を十分攪拌して起泡させ、起泡させたゼラチン水溶液3gをトレー上に作製した前記ゼラチンフィルムの上から流し込み、−20℃でゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは48μmであった。
これらの二層シートを真空乾燥機に入れ、真空下、140℃にて3時間、熱処理を行って加熱架橋した。このとき得られたシートのトレー側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は147μmであった。
【0032】
(実施例6)発泡法による二層シートの作製その3
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延した。続いて、2%ゼラチン水溶液を十分攪拌して起泡させ、起泡させたゼラチン水溶液6gトレー上に作製した前記ゼラチンフィルムの上から流し込み、ゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは1mmであった。
これらの二層シートを真空乾燥機に入れ、真空下、140℃にて1、3、5、8時間、熱処理を行って加熱架橋した。このとき得られたシートのトレー側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は223μmであった。
【0033】
(実施例7)発泡法による二層シートの作製その3
ゼラチン粉末(ニッピ社製)を注射用水に溶解して2%のゼラチン水溶液を調製し、十分攪拌して起泡させ、起泡させたゼラチン水溶液6gをガラストレー(8.5×5.5cm)に流し込み、ゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは5mmであった。このシートを真空乾燥機に入れ、真空下、140℃にて3時間、熱処理を行って加熱架橋した。このとき得られたシートのガラス板側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は223μmであった。
【0034】
(実施例4)相分離法による二層シートの作製
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流し込み、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。続いて、2%ゼラチン水溶液をトレー上に作製した前記ゼラチンフィルムの上から流し込み、その上に冷却したエタノール(10ml)をさらに流し込み、ゼラチンを沈殿させた。エタノールを用いて洗浄後、25℃で風乾した。得られた二層シートの表面には白濁したゼラチン沈殿物が固着しており、凸凹であった。
【0035】
(実施例9)補強材入り三層シートの作製
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流し込み、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した
トレー上に作製した前記ゼラチンフィルムの上に、補強材となるポリグリコリド繊維からなる経編布(12g/cm2)を置いた。続いて、2%ゼラチン水溶液を十分攪拌して起泡させ、起泡させたゼラチン水溶液6gをトレー上に作製した前記ゼラチンフィルムとポリグリコリド繊維からなる経編布の上から流し込み、ゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは1mmであった。これらの二層シートを真空乾燥機に入れ、真空下、140℃にて3時間、熱処理を行って加熱架橋した。このとき得られたシートのトレー側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は223μmであった。
補強材としては、前記経編布以外に、ポリグリコリド不織布(ニードルパンチ)、ポリグリコリド不織布(メルトブロー)を用いた。
【0036】
(比較例1)一層フィルムの作製
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、このゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃にて24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。得られたゼラチンフィルムを真空乾燥機中、140℃で3時間熱処理を行うことにより熱架橋した。得られたフィルムは両面とも平滑な透明体であり、60℃の温水に不溶であった。
【0037】
(比較例2)一層スポンジ状シートの作製
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1%のゼラチン水溶液を調製し、この1%ゼラチン水溶液1mLをプラスチックトレー(8.5×5.5cm)に流し込み、−80℃の冷凍庫で凍結した。その後、凍結乾燥器に24時間入れてスポンジを作製した。得られた多孔質層の厚みは〜1mmであった。得られたスポンジシートは実施例1〜7において得られた二層シート、あるいは実施例8において得られた三層シートとは異なり、手で引張るだけで容易に引き裂かれ、脆弱であるために本発明の目的を達しなかった。
【0038】
(引張強度の評価)
実施例4で作製した二層シートおよび実施例8で作製した三層シートを湿潤状態で測定したときの引張り強度を図2に示す。湿潤状態下での強度は、シート全体を湿潤させてしまうと試験機のチャックにはさむことができなかったため、乾燥シートをチャックにはさんでからシート中央の長さ1cm部分のみを水で潤潤させて測定した。
図2にみられるように、PGA布の種類によって湿潤強度に若干の差は認められたが、いずれも、補強なしシートの湿潤強度よりは明らかに高値であった。
【0039】
(吸水性の評価)
実施例4で作製した二層シートおよび実施例8で作製した三層シートの吸水性を次の方法によって評価した。対照として、比較例1で作製したゼラチンフィルムを用いた。まず、リン酸緩衝生理食塩水を30mg/cm2となるように水平な台上に滴下し、その上に1cm2の乾燥した二層シートあるいは三層シートを静置した。シートを水平な台に置いてからのシートの吸水量の時間変化を図3に示した。比較のために、比較例1で作製したゼラチン一層シートについても測定した。図2に示されるように二層シートおよび三層シートはすみやかに水分を吸収しているのに対して、比較例のゼラチン一層シートは水分を吸水するのに時間がかかった。
【0040】
(分解性評価)
実施例4で作製した二層シート(1×1cm2)について、in vivoでの分解性を下記の方法で評価した。麻酔下でラットの皮下に、重量を測定した滅菌シートを埋入し、1、3、5、7、10日後にシートを取り出した。洗浄後、乾燥させ、分解吸収後の残量を測定した。結果を図4に示す。
【0041】
(生体組織への密着性評価)
実施例1で作製した二層シート(厚み1.3mm)、実施例2で作製した二層シート(厚み2.5mm)、比較例1で作製したゼラチン一層フィルム、および市販のヒアルロン酸とカルボキシメチルセルロースからなるフィルム(商品名セプラフィルム)の生体組織への密着性を、下記の方法により評価した。実施例1で作製した二層シートあるいはセプラフィルム(1cm×1cm)の片面にテープを貼り、その真ん中に糸を通した。犠牲死させたラットの盲腸に二層シートあるいはセプラフィルムを貼り、30秒間指で押さえて密着させた。糸に強力測定器を取り付け、垂直にゆっくりと引張り、剥がれるときの強度を測定した。試験を2回行ったときの引張強度は、実施例1で作製した二層シートは117.5±10.6gf/cm2であったのに対して、セプラフィルムは70.0±42.4gf/cm2で、組織への密着性は二層シートの方が優れていた。
また、ブタの肝臓に対する密着性評価のために、実施例1で作製した二層シート(厚み1.3mm)、実施例2で作製した二層シート(厚み2.5mm)、および比較例1で作製したゼラチンフィルムの生体組織への密着性を、下記の方法により評価した。まず、二層シートあるいはゼラチンフィルム(2×4cm2) の片面にテープを貼り、その真ん中に糸を通した。犠牲死させたブタの肝臓にフィルムあるいはシートを貼り、30秒間指で押さえて密着させた。糸に強力測定器を取り付け、垂直にゆっくりと引張り、剥がれるときの強度を測定した。試験を5回行ったときの引張強度は実施例1の二層シートは14.0±3.7gf/cm2(二層シート、厚み1.3mm)、29.0±11.3gf/cm2(二層シート、厚み2.5mm)であったのに対して、比較例1のゼラチンフィルムは9.9±3.7gf/cm2(フィルム)で、組織への密着性は二層シートの方が優れていた。
【0042】
(止血性評価)
実施例1および2で作製した二層シートの止血効果を下記の方法により評価した。麻酔下でラットの腹部を切開して胃を露出させ、前壁に0.5×0.5cm2の上皮剥離創を作製して組織から出血させた。ガーゼを30秒間創部に押し付けても止血できないことを確認してから、創部に1×2cm2の二層シートを置き、30秒間、ピンセットで押し付けた。その結果、いずれの二層シートも創部に密着し、5分後においても止血効果が認められた。
【0043】
(圧迫による止血性評価)
実施例4で作製した二層シートと実施例8で作製した三層シートの圧迫による止血効果を下記の方法により評価した。麻酔下でイヌの腹部を切開して脾臓を露出させ、前壁に1.0×1.0cm2の上皮剥離創を作製し、出血させて出血量の多いモデルを作製した。ガーゼで30秒間、押しても止血できないことを確認してから、創部に2×2cm2の二層シートあるいは三層シートを置き、さらにシートの上にガーゼを置いた。ガーゼの上から5分間強く押し付けた。その結果、出血量の多い場合では、二層シートは形がくずれてガーゼに接着して組織から剥がれてしまったが、三層シートは患部に密着し、止血効果が認められた。
【0044】
(癒着防止効果の評価)
実施例4で作製した二層シートについて、癒着防止効果を下記の方法により評価した。創傷部位に
麻酔下でラットの腹部を切開し、盲腸前壁と腹膜に癒着を起こすように15mm径の漿膜をゆるく傷つけた。その上に2×2cm2の大きさの二層シートを置き、30秒間押し付けた。ゼラチン製の医療用接着剤を塗布してから、二層シートを置き、同様の操作を行った。対照例として市販のヒアルロン酸とカルボキシメチルセルロースからなるフィルム(商品名セプラフィルム)を用いた。また、創傷部位に何も置かず腹部を縫合した例を作製した(Sham Ope)。2週間後に開腹して癒着の有無を観察し、癒着スコア(0=癒着無し、1=mild、2=moderate、3=severe、4=very severe)を用いて、癒着防止効果を各6匹のラットモデルで評価した。評価結果を図5に示す。いかなる材料も用いずに組織面を傷つけたままに放置しておいた場合には6匹すべてに強い癒着が生じ、セプラフィルムを組織面に密着させた場合は6匹中2匹癒着していたのに対し、二層シートを組織面に密着させた場合には、6匹中1匹しか癒着が認められなかった。また、二層シートを接着剤と併用した場合では3匹すべてに癒着が認められなかった。
【0045】
(空気漏れ防止効果)
実施例1、4および5で作製した二層シートの空気漏れ(Air leak)防止効果を下記の方法で評価した。犠牲死させたイヌの肺に空気を入れ、圧を5cm/H2Oに保ちながら18G針で穿刺して孔を作製した。空気漏れを確認した後、実施例1で得られた1.5×1.5cm2の大きさの二層シートを、孔が真ん中にくるように置き、30秒間、圧迫してから圧をゆっくりと高めていった。いずれの二層シートを用いた場合でも、空気漏れの生じた圧は56cm/H2Oであった。
二層シートの周辺部に、さらにゼラチン製の医療用接着剤を塗布した場合、空気漏れの生じた圧は80 cm/H2Oであった。同様の実験をフィブリン糊(商品名ベリプラスト)を用いて行ったときの結果は38 cm/H2Oであり、二層シート、あるいはシートと接着剤の併用材料のほうが高い値であった。ヒトが咳をした時に必要な耐圧は50 cm/H2Oであるため、これらの材料の空気漏れ防止効果は十分に認められた。
【0046】
(組織再生能)
実施例1で作製した二層シート、市販のヒアルロン酸とカルボキシメチルセルロースからなるフィルム(商品名セプラフィルム)、および材料を何も用いなかった場合についての、創傷部の組織再生効果を下記の方法で評価した。まず、麻酔下でイヌの腹部を切開し、回盲部から口側10cmの漿膜を4×3cm2だけ紙やすりでゆるく削りとり創傷部を作製した。止血後、創傷部に5×4.5cm2の大きさの二層シートあるいは、ヒアルロン酸フィルムを置き、30秒間押し付けた。対比として、材料を何も置かずに腹部を縫合した。3週間後に開腹して癒着の有無を観察してから患部を切り取り、ホルマリン固定した後に組織切片を作製して、腹膜中皮を酵素抗体法によりHBME1抗体にて染色した。二層シートを用いた場合の組織切片像を図6に、ヒアルロン酸とカルボキシメチルセルロースからなるフィルムを用いた場合の組織切片像を図7に示す。その結果、いずれの二層シートでも中皮の再生が確認できたが、ヒアルロン酸フィルム中皮の再生は確認できなかった。
【0047】
(水漏れ防止効果の評価)
実施例4で作製した二層シート、実施例7で作製した三層シートについて、水漏れ防止効果を下記の方法で評価した。トリ胸肉に穴を開けて内径1mmのチューブを挿入し、チューブ末端をトリ胸肉表面の開口部に固定した。チューブ内に水が一定量流れるようポンプを配置し、トリ胸肉表面の開口部から水が流れる水漏れ評価モデルを作製した。流量0.5mL/minの水漏れ評価モデルにおいて、2×2cm2の大きさの二層シートあるいは三層シートを開口部に貼付し、ゼラチン製の医療用接着剤をシート周囲に塗付した。対比として、二層シートあるいは三層シートを用いずにゼラチン製の医療用接着剤のみを開口部に塗付した。その結果、二層シートあるいは三層シートを用いた場合は、シートがトリ胸肉から外れることなく吸水して開口部からの水漏れを防止できたが、二層シートあるいは三層シートを用いなかった場合は、ゼラチン製の医療用接着剤がトリ胸肉から外れて開口部からの水漏れを防止できなかった。
【産業上の利用可能性】
【0048】
本発明の生体吸収性医療材料は、外科手術において、生体組織の創傷部において、止血、空気漏れ防止、組織再生能、癒着防止効果を発揮するものである。
【技術分野】
【0001】
本発明は、生体内の組織に密着して創傷部における止血、被覆、閉鎖の効果の役目を果たすとともに、創傷部と周囲組織との癒着を防止する効果を有する、フィルム層と多孔質層からなる生体吸収性医療材料に関する。
【背景技術】
【0002】
生体組織に創傷ができると生体組織から出血する。一時的に止血しても、不完全なままに放置されているとさらなる出血を引き起こすこととなり好ましくない。また、創傷部の生体組織から体液などが漏れるため、創傷部を何らかの手段で閉鎖することが必要になる。さらに、創傷部が大きい場合にはシート状材料などで創傷部を被覆しなければ、周囲から細胞や生体組織が侵入して創傷部と周囲の正常組織との間に癒着が発生し、創傷部の治癒を阻害するだけでなく種々の合併症が発生する危険性がある。
【0003】
このような理由から、外科手術においては創傷部の止血材、被覆材、閉鎖材、癒着防止材など種々のシート状の医療材料が使用されている。よく知られた例としては、コラーゲンフリースの片面にフィブリノーゲンとトロンビンを付着したシート状の止血材料(商品名タココンブ)がある。癒着防止を目的とした材料としては、ヒアルロン酸とカルボキシメチルセルロースからなるフィルム状材料(商品名セプラフィルム)、酸化再生セルロースからなる布状材料(商品名インターシード)、ゼラチンフィルムからなる材料(特許文献1、2)などがある。また、創傷部の被覆を目的とした医療材料としては、ポリグリコリドの不織布(商品名ネオベール)などがある。これらの材料はいずれも生体吸収性であり、かつ、平面状材料である。
【0004】
これらの材料は創傷部に密着し、容易に移動しないことが必要である。例えば、コラーゲンフリースの片面にフィブリノーゲンとトロンビンを付着したシート状材料は、フィブリノーゲンとトロンビンの接着効果によって生体組織に密着する。ヒアルロン酸とカルボキシメチルセルロースからなるフィルム状材料にはこのような接着効果はないが、生体組織に接触させると物理的に密着する。ポリグリコール酸製不織布にはこのような接着効果や密着性がないために、フィブリン糊などの接着剤を用いて生体組織に密着、固定させる必要がある。
【0005】
これらの吸収性医療材料は外科手術の成績向上に大いに貢献しているが、一方で欠点も指摘されている。例えば、ヒアルロン酸とカルボキシメチルセルロースからなるフィルム状材料の生体組織への密着効果は十分でなく、しばしば、創傷部から材料が移動してしまい、その結果として癒着を起こしてしまうことがあった。さらに、水分で濡れると材料が破れやすく、そのために材料の位置を修正するための移動ができないという欠点があった。コラーゲンフリースの片面にフィブリノーゲンとトロンビンを付着したシート状材料は、材料の伸展度が低いために生体組織に密着しにくく、そのために止血効果が不十分となる場合がある。ポリグリコリド製不織布は、接着剤を使用しなければ生体組織表面に密着、固定させることができないという問題があった(特許文献3、4)。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2004−209228号公報
【特許文献2】特開2007−44080号公報
【特許文献3】特開2009−183649号公報
【特許文献4】WO2009/128474号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
生体組織の創傷部に密着することが可能であり、かつ取り扱い性に優れ、止血、被覆、閉鎖、癒着防止の効果を有するとともに創傷部の治癒を促進させることができる生体吸収性医療材料を提供することである。
【課題を解決するための手段】
【0008】
本願発明者らは、これらの問題を解決するために鋭意研究を重ねた結果、生体吸収性医療材料が生体組織表面上に存在する少量の水分と接触したときにヒドロゲル状になることによって、良好な密着性を生じることを見出した。すなわち、生体吸収性医療材料の生体組織と接触する面に少量の水分によってヒドロゲル状になる多孔質層が存在するような材料を設計した。一方で、反対面には親水面のフィルム層を配し、周囲組織との癒着を防止する効果を有するように材料設計を行った。このように、多孔質層とフィルム層からなる二層構造を有する生体吸収性医療材料を用いることによって、創傷部に密着して止血、被覆、閉鎖する効果を発揮し、創傷部の治癒を促進し、さらには創傷部と周囲組織との癒着を防止することができるという、これまでの医療材料にはない優れた効果が得られることを見いだした。また、多孔質層とフィルム層からなる二層構造であるだけでなく、薄いシート状(二層シート)とすることによって、材料に柔軟性を与えることができ組織への密着性が高まり、一方では材料の強度が向上することによって壊れにくいという取り扱いに優れた材料となることを見いだした。また、補強材料を複合化させた三層シート構造とすることによって、さらに壊れにくく取り扱い性に優れた材料とすることに成功した。
【発明の効果】
【0009】
本発明の生体吸収性医療材料は生体吸収性高分子からなり、創傷部が治癒した後には生体内で分解吸収され、異物が生体内に残存するようなことはない。また、吸水面は生体組織に密着しやすいことから縫合糸や接着剤を用いなくとも材料を創傷部に密着、固定することができるのみならず、創傷部の止血、閉鎖の効果が得られるものであるが、接着剤などとの併用によってさらに効果を高めることも可能である。また、創傷部に密着する面と反対側の面は親水性であることから、周囲組織との癒着を防止する効果が得られる。すなわち、本発明に係る材料を生体組織の創傷部に押しつけるだけで密着、固定することができ、さらに創傷部への癒着を防止できるという、これまでにない画期的な効果が得られるものである。
また、補強材料と複合化させることによって従来のフィルム状の材料と比較して材料の強度が向上し、一旦組織に密着させた材料を再度移動させることが可能になるばかりでなく、内視鏡手術のように狭い視野で操作を行う場合にも壊れにくいという、これまでにない医療現場で取り扱い性に優れた材料が得られるものである。
【図面の簡単な説明】
【0010】
【図1】本発明に係る三層シート構造を有する医療材料の断面を示す図である。
【図2】図2は、湿潤状態における二層シートおよび三層シートの引張強度を表すグラフである。
【図3】図3は、シートの吸水量の時間変化を表すグラフである。
【図4】図4は、架橋時間の異なる材料をラット皮下に埋入した時のの重量残存率を表すグラフである。
【図5】図5は、ラットの体内における二層シートの癒着評価を表すグラフである。
【図6】図6は、二層シートをイヌの腸管に貼付したときの3週間後の腸管顕微鏡写真である。
【図7】図7は、対照区の材料をイヌの腸管に貼付したときの3週間後の組織切片像である。
【発明を実施するための形態】
【0011】
本発明に係る生体吸収性医療材料を構成する高分子は、生体内で分解吸収されるものであれば特に限定されるものではないが、親水性高分子、特に天然高分子であることが望ましい。このような天然高分子としては、コラーゲン、ゼラチン、ヒアルロン酸、アルギン酸、キチン、キトサンなどを例示することができる。このなかでも、水に溶解させることができ、加工性に優れるゼラチンを用いることが好ましい。
【0012】
これらの天然高分子は生体内ですぐに溶解してしまうことから、何らかの架橋処理がされている必要がある。架橋は加熱処理や紫外線照射、放射線照射などの物理的方法と、グルタルアルデヒドやカルボジイミドなどの架橋剤を用いる化学的方法がある。このうち、材料に架橋剤が残らない加熱処理や紫外線照射などの物理的方法による架橋を行うことが好ましい。
【0013】
生体吸収性医療材料が生体内で長期間残存すると、周囲の組織を傷つけ、かえって癒着を引き起こすことになってしまう。一方で、あまりに短期間で分解、吸収されてしまうと、止血や創傷治癒、癒着防止の効果が十分に得られない。本発明の生体吸収性医療材料は、生体内に埋入後12時間は存在していることが必要であり、一方で埋入後90日以内にすみやかに分解、吸収されることが望ましい。
【0014】
生体吸収性医療材料を生体組織の創傷部に密着させるためには、生体組織に接着する側の材料表面が、生体組織の少量の水分を吸水し、ヒドロゲル状になる層が存在する必要がある。このような層としては、親水性材料からなる多孔質層があげられる。すなわち、材料表面に吸水を容易にする微少な孔などが多数存在しているような構造であればよい。このような構造としては、編物、織物、不織布のような繊維構造であってもよいし、スポンジのような多孔質構造であってもよい。この中でも、水溶性高分子を用いる場合に作製が容易なスポンジ状の多孔質体からなることが好ましい。このようなスポンジ状の多孔質体からなる多孔質層の存在により、フィブリン糊や縫合糸などを用いなくても、必要な期間、生体組織に生体吸収性医療材料を密着、固定させることができるものである。
【0015】
このようなスポンジ状の多孔質体の製造方法としては、生体吸収性高分子を水などの溶媒に溶解した後に、この溶液を凍結乾燥する方法がある。あるいは、生体吸収性高分子水溶液を発泡しておいてから、その多孔構造を維持しながら凍結乾燥、風乾、あるいは生体吸収性高分子水溶液に非溶媒を加えて相分離させるなどの方法を例示することができる。
【0016】
スポンジ状の多孔質体の孔径は、1μm〜1,000μmであり、好ましくは5μm〜800μm
の範囲である。孔径が1μmより小さいと生体組織の水が材料に吸い込まないために密着性が悪くなり、材料が創傷部に密着できなくなるためである。一方、1,000μmを超えると孔径が大きすぎるために多孔質体の強度が下がりすぎて破れやすくなってしまうためである。
【0017】
スポンジ状の多孔質体の厚みは20μm〜15,000μmであり、好ましくは50μm〜10,000μmの範囲である。20μm未満であると材料が壊れやすく、一方で15000μm以上であると材料が硬くなり創傷部に密着しなくなってしまうためである。
【0018】
生体吸収性医療材料が創傷部と周囲組織との癒着を防止するためには、材料が生体組織と接触して密着する面とは反対面の材料表面が親水性のフィルム状であって、かつ、材料表面に細胞や組織が接着しないことが必要である。このような材料としては、親水性で表面が平滑なフィルム状の材料であれば特に限定されるものではない。このフィルム状の材料は、厚ければ柔軟性と操作性に欠けるため、できるだけ薄くすることが必要である。フィルム状の材料の厚さは1μm〜200μmであり、好ましくは2μm〜100μmの範囲である。厚さが1μm未満であると材料が壊れやすいために扱いにくく、一方で200μm以上であると材料が硬く創傷部に密着しなくなってしまうためである。
【0019】
フィルム状の材料の作製方法は特に限定されないが、生体吸収性高分子を溶媒に溶解したのちに、この溶液を型枠に流し込んで溶媒を除去するキャスト法や、溶液を平板上に流延して溶媒を除去する流延法などが例示できる。
【0020】
本発明に係る生体吸収性医療材料は、前述のごとく創傷部と密着する層を構成する多孔質層と、創傷部と周囲組織との癒着を防止するためのフィルム層を構成する材料からなる二層構造であることを特徴とする二層シートである。二層構造とするためには、各層を別個に作製しておいてから複合化させてもよいし、一つの層を作製してからさらにもう一つの層を作製させてもよい。さらには、二つの層を同時に作製させる方法であってもよい。
【0021】
本願発明に係る生体吸収性医療材料は、二層シートとすることによって操作性がきわめて良好になるものである。材料が水分で膨潤すると柔軟さが生じ、シート状を保った状態で肺のように常に形状の変化する組織に対しても密着し続けることができる。
【0022】
本願発明に係る生体吸収性医療材料は、内視鏡手術で用いることが想定される。内視鏡手術では手術器械を用いて狭い視野で手術を行うこととなり、創傷部に材料を密着させる場合に何度も位置を直すことありうる。このような場合、水分を吸収した材料は柔らかくて壊れやすく、さらなる補強が求められる。
【0023】
補強材料としては、生体吸収性繊維からなる薄い織物、編物、不織布などがあげられる。生体吸収性繊維の材料としては、吸収性高分子であれば特に限定されるものではないが、吸水時に容易に膨潤しない合成の吸収性高分子であることが好ましい。このうち、吸収速度が速いポリグリコリド、グリコリド−ラクチド共重合体、あるいはグリコリド−ε―カプロラクトン共重合体であることがより好ましい。
【0024】
本願発明に係る生体吸収性医療材料は、組織への密着性を高めるためには柔軟であることが必要である。そのためには、補強材はできる限り薄く柔軟性があることが必要である。補強材の厚さは5μm〜500μmであり、好ましくは10μm〜400μmの範囲である。5μm未満であると補強材自体の取り扱いが難しく成型が困難になってしまい、一方で500μm以上であると材料が硬く創傷部に密着しなくなってしまうためである。本願発明に係る医療材料は、多孔質層、フィルム層、さらに補強材料の三層構造からなる三層シートであってもよい。
【0025】
このように、本願発明の生体吸収性医療材料は、創傷部に材料を押し付けることによって密着させることができ、さらには創傷部の止血、閉鎖、組織再生、癒着防止などの種々の組織修復に必要な効果を発揮する。
【実施例】
【0026】
以下、実施例を挙げて本発明を説明するが、本発明はこれらの実施例に限定されるものではない。
【0027】
(実施例1)凍結乾燥法による二層シートの作製その1
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。トレー上に作製した前記ゼラチンフィルムの上から1.0%ゼラチン水溶液を5mL流し込み、25℃にて10分間静置した。その後、トレーを‐80℃の冷凍庫に30分間入れてゼラチン水溶液を凍結させた後、凍結乾燥機中で24時間処理することによりゼラチン多孔質層−フィルム層複合体(二層シート)を作製した。このときのシート全体の厚みは2mmであった。その後、二層シートを真空乾燥機に入れ、真空下、140℃で3時間、熱処理を行うことにより加熱架橋した。得られた二層材料をステンレス板で挟み、上から荷重を5分間かけることによってプレスした。得られた材料のフィルム層は平滑であり、スポンジ層は凸凹のある不透明体であった。材料の厚みは、1.3±0.1mmであった。スポンジ体の孔径は92μmであった。
【0028】
(実施例2)凍結乾燥法による二層シートの作製その2
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。トレー上に作製した前記ゼラチンフィルムの上から1.0%ゼラチン水溶液を10mL流し込み、25℃にて10分間静置した。その後、トレーを‐80℃の冷凍庫に30分間入れてゼラチン水溶液を凍結させた後、凍結乾燥機中で24時間処理することによりゼラチン多孔質層−フィルム層複合体(二層シート)を作製した。このときのシート全体の厚みは4mmであった。その後、二層シートを真空乾燥機に入れ、真空下、140℃で3時間、熱処理を行うことにより加熱架橋した。得られた二層材料をステンレス板で挟み、上から荷重を5分間かけることによってプレスした。得られた材料のフィルム層は平滑であり、スポンジ層は凸凹のある不透明体であった。材料の厚みは、2.5±0.1mmであった。スポンジ体の孔径は98μmであった。
【0029】
(実施例3)凍結乾燥法による二層シートの作製その3
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。トレー上に作製した前記ゼラチンフィルムの上から0.3%コラーゲン水溶液コラーゲンIP(新田ゼラチン社製)を5mL流し込み、25℃にて10分間静置した。その後、トレーを‐80℃の冷凍庫に30分間入れてゼラチン水溶液を凍結させた後、凍結乾燥機中で24時間処理することによりコラーゲン多孔質層−ゼラチンフィルム層複合体(二層シート)を作製した。このときのシート全体の厚みは1mmであった。その後、二層シートを真空乾燥機に入れ、真空下、140℃で3時間、熱処理を行うことにより加熱架橋した。得られた二層材料をステンレス板で挟み、上から荷重を5分間かけることによってプレスした。得られた材料のフィルム層は平滑であり、スポンジ層は凸凹のある不透明体であった。材料の厚みは、1.3±0.1mmであった。
【0030】
(実施例4)発泡法による二層シートの作製その1
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。続いて、2%ゼラチン水溶液を十分攪拌して起泡させ、起泡させたゼラチン水溶液6gをトレー上に作製した前記ゼラチンフィルムの上から流し込み、ゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは1mmであった。
これらの二層シートを真空乾燥機に入れ、真空下、140℃にて3時間、熱処理を行って加熱架橋した。このとき得られたシートのトレー側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は223μmであった。
【0031】
(実施例5)発泡法による二層シートの作製その2
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm2)に流延、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。続いて、4.5%ゼラチン水溶液を十分攪拌して起泡させ、起泡させたゼラチン水溶液3gをトレー上に作製した前記ゼラチンフィルムの上から流し込み、−20℃でゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは48μmであった。
これらの二層シートを真空乾燥機に入れ、真空下、140℃にて3時間、熱処理を行って加熱架橋した。このとき得られたシートのトレー側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は147μmであった。
【0032】
(実施例6)発泡法による二層シートの作製その3
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延した。続いて、2%ゼラチン水溶液を十分攪拌して起泡させ、起泡させたゼラチン水溶液6gトレー上に作製した前記ゼラチンフィルムの上から流し込み、ゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは1mmであった。
これらの二層シートを真空乾燥機に入れ、真空下、140℃にて1、3、5、8時間、熱処理を行って加熱架橋した。このとき得られたシートのトレー側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は223μmであった。
【0033】
(実施例7)発泡法による二層シートの作製その3
ゼラチン粉末(ニッピ社製)を注射用水に溶解して2%のゼラチン水溶液を調製し、十分攪拌して起泡させ、起泡させたゼラチン水溶液6gをガラストレー(8.5×5.5cm)に流し込み、ゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは5mmであった。このシートを真空乾燥機に入れ、真空下、140℃にて3時間、熱処理を行って加熱架橋した。このとき得られたシートのガラス板側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は223μmであった。
【0034】
(実施例4)相分離法による二層シートの作製
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流し込み、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。続いて、2%ゼラチン水溶液をトレー上に作製した前記ゼラチンフィルムの上から流し込み、その上に冷却したエタノール(10ml)をさらに流し込み、ゼラチンを沈殿させた。エタノールを用いて洗浄後、25℃で風乾した。得られた二層シートの表面には白濁したゼラチン沈殿物が固着しており、凸凹であった。
【0035】
(実施例9)補強材入り三層シートの作製
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、この1.4%ゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流し込み、25℃、24時間、風乾して厚さ10μmのゼラチンフィルムを作製した
トレー上に作製した前記ゼラチンフィルムの上に、補強材となるポリグリコリド繊維からなる経編布(12g/cm2)を置いた。続いて、2%ゼラチン水溶液を十分攪拌して起泡させ、起泡させたゼラチン水溶液6gをトレー上に作製した前記ゼラチンフィルムとポリグリコリド繊維からなる経編布の上から流し込み、ゲル化させた後に25℃で風乾した。このとき得られたシート全体の厚みは1mmであった。これらの二層シートを真空乾燥機に入れ、真空下、140℃にて3時間、熱処理を行って加熱架橋した。このとき得られたシートのトレー側は平滑なフィルム状であり、空気面は凸凹のあるスポンジ体であった。スポンジ体の孔径は223μmであった。
補強材としては、前記経編布以外に、ポリグリコリド不織布(ニードルパンチ)、ポリグリコリド不織布(メルトブロー)を用いた。
【0036】
(比較例1)一層フィルムの作製
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1.4%のゼラチン水溶液を調製し、このゼラチン水溶液4mLをプラスチックトレー(8.5×5.5cm)に流延、25℃にて24時間、風乾して厚さ10μmのゼラチンフィルムを作製した。得られたゼラチンフィルムを真空乾燥機中、140℃で3時間熱処理を行うことにより熱架橋した。得られたフィルムは両面とも平滑な透明体であり、60℃の温水に不溶であった。
【0037】
(比較例2)一層スポンジ状シートの作製
ゼラチン粉末(ニッピ社製)を注射用水に溶解して1%のゼラチン水溶液を調製し、この1%ゼラチン水溶液1mLをプラスチックトレー(8.5×5.5cm)に流し込み、−80℃の冷凍庫で凍結した。その後、凍結乾燥器に24時間入れてスポンジを作製した。得られた多孔質層の厚みは〜1mmであった。得られたスポンジシートは実施例1〜7において得られた二層シート、あるいは実施例8において得られた三層シートとは異なり、手で引張るだけで容易に引き裂かれ、脆弱であるために本発明の目的を達しなかった。
【0038】
(引張強度の評価)
実施例4で作製した二層シートおよび実施例8で作製した三層シートを湿潤状態で測定したときの引張り強度を図2に示す。湿潤状態下での強度は、シート全体を湿潤させてしまうと試験機のチャックにはさむことができなかったため、乾燥シートをチャックにはさんでからシート中央の長さ1cm部分のみを水で潤潤させて測定した。
図2にみられるように、PGA布の種類によって湿潤強度に若干の差は認められたが、いずれも、補強なしシートの湿潤強度よりは明らかに高値であった。
【0039】
(吸水性の評価)
実施例4で作製した二層シートおよび実施例8で作製した三層シートの吸水性を次の方法によって評価した。対照として、比較例1で作製したゼラチンフィルムを用いた。まず、リン酸緩衝生理食塩水を30mg/cm2となるように水平な台上に滴下し、その上に1cm2の乾燥した二層シートあるいは三層シートを静置した。シートを水平な台に置いてからのシートの吸水量の時間変化を図3に示した。比較のために、比較例1で作製したゼラチン一層シートについても測定した。図2に示されるように二層シートおよび三層シートはすみやかに水分を吸収しているのに対して、比較例のゼラチン一層シートは水分を吸水するのに時間がかかった。
【0040】
(分解性評価)
実施例4で作製した二層シート(1×1cm2)について、in vivoでの分解性を下記の方法で評価した。麻酔下でラットの皮下に、重量を測定した滅菌シートを埋入し、1、3、5、7、10日後にシートを取り出した。洗浄後、乾燥させ、分解吸収後の残量を測定した。結果を図4に示す。
【0041】
(生体組織への密着性評価)
実施例1で作製した二層シート(厚み1.3mm)、実施例2で作製した二層シート(厚み2.5mm)、比較例1で作製したゼラチン一層フィルム、および市販のヒアルロン酸とカルボキシメチルセルロースからなるフィルム(商品名セプラフィルム)の生体組織への密着性を、下記の方法により評価した。実施例1で作製した二層シートあるいはセプラフィルム(1cm×1cm)の片面にテープを貼り、その真ん中に糸を通した。犠牲死させたラットの盲腸に二層シートあるいはセプラフィルムを貼り、30秒間指で押さえて密着させた。糸に強力測定器を取り付け、垂直にゆっくりと引張り、剥がれるときの強度を測定した。試験を2回行ったときの引張強度は、実施例1で作製した二層シートは117.5±10.6gf/cm2であったのに対して、セプラフィルムは70.0±42.4gf/cm2で、組織への密着性は二層シートの方が優れていた。
また、ブタの肝臓に対する密着性評価のために、実施例1で作製した二層シート(厚み1.3mm)、実施例2で作製した二層シート(厚み2.5mm)、および比較例1で作製したゼラチンフィルムの生体組織への密着性を、下記の方法により評価した。まず、二層シートあるいはゼラチンフィルム(2×4cm2) の片面にテープを貼り、その真ん中に糸を通した。犠牲死させたブタの肝臓にフィルムあるいはシートを貼り、30秒間指で押さえて密着させた。糸に強力測定器を取り付け、垂直にゆっくりと引張り、剥がれるときの強度を測定した。試験を5回行ったときの引張強度は実施例1の二層シートは14.0±3.7gf/cm2(二層シート、厚み1.3mm)、29.0±11.3gf/cm2(二層シート、厚み2.5mm)であったのに対して、比較例1のゼラチンフィルムは9.9±3.7gf/cm2(フィルム)で、組織への密着性は二層シートの方が優れていた。
【0042】
(止血性評価)
実施例1および2で作製した二層シートの止血効果を下記の方法により評価した。麻酔下でラットの腹部を切開して胃を露出させ、前壁に0.5×0.5cm2の上皮剥離創を作製して組織から出血させた。ガーゼを30秒間創部に押し付けても止血できないことを確認してから、創部に1×2cm2の二層シートを置き、30秒間、ピンセットで押し付けた。その結果、いずれの二層シートも創部に密着し、5分後においても止血効果が認められた。
【0043】
(圧迫による止血性評価)
実施例4で作製した二層シートと実施例8で作製した三層シートの圧迫による止血効果を下記の方法により評価した。麻酔下でイヌの腹部を切開して脾臓を露出させ、前壁に1.0×1.0cm2の上皮剥離創を作製し、出血させて出血量の多いモデルを作製した。ガーゼで30秒間、押しても止血できないことを確認してから、創部に2×2cm2の二層シートあるいは三層シートを置き、さらにシートの上にガーゼを置いた。ガーゼの上から5分間強く押し付けた。その結果、出血量の多い場合では、二層シートは形がくずれてガーゼに接着して組織から剥がれてしまったが、三層シートは患部に密着し、止血効果が認められた。
【0044】
(癒着防止効果の評価)
実施例4で作製した二層シートについて、癒着防止効果を下記の方法により評価した。創傷部位に
麻酔下でラットの腹部を切開し、盲腸前壁と腹膜に癒着を起こすように15mm径の漿膜をゆるく傷つけた。その上に2×2cm2の大きさの二層シートを置き、30秒間押し付けた。ゼラチン製の医療用接着剤を塗布してから、二層シートを置き、同様の操作を行った。対照例として市販のヒアルロン酸とカルボキシメチルセルロースからなるフィルム(商品名セプラフィルム)を用いた。また、創傷部位に何も置かず腹部を縫合した例を作製した(Sham Ope)。2週間後に開腹して癒着の有無を観察し、癒着スコア(0=癒着無し、1=mild、2=moderate、3=severe、4=very severe)を用いて、癒着防止効果を各6匹のラットモデルで評価した。評価結果を図5に示す。いかなる材料も用いずに組織面を傷つけたままに放置しておいた場合には6匹すべてに強い癒着が生じ、セプラフィルムを組織面に密着させた場合は6匹中2匹癒着していたのに対し、二層シートを組織面に密着させた場合には、6匹中1匹しか癒着が認められなかった。また、二層シートを接着剤と併用した場合では3匹すべてに癒着が認められなかった。
【0045】
(空気漏れ防止効果)
実施例1、4および5で作製した二層シートの空気漏れ(Air leak)防止効果を下記の方法で評価した。犠牲死させたイヌの肺に空気を入れ、圧を5cm/H2Oに保ちながら18G針で穿刺して孔を作製した。空気漏れを確認した後、実施例1で得られた1.5×1.5cm2の大きさの二層シートを、孔が真ん中にくるように置き、30秒間、圧迫してから圧をゆっくりと高めていった。いずれの二層シートを用いた場合でも、空気漏れの生じた圧は56cm/H2Oであった。
二層シートの周辺部に、さらにゼラチン製の医療用接着剤を塗布した場合、空気漏れの生じた圧は80 cm/H2Oであった。同様の実験をフィブリン糊(商品名ベリプラスト)を用いて行ったときの結果は38 cm/H2Oであり、二層シート、あるいはシートと接着剤の併用材料のほうが高い値であった。ヒトが咳をした時に必要な耐圧は50 cm/H2Oであるため、これらの材料の空気漏れ防止効果は十分に認められた。
【0046】
(組織再生能)
実施例1で作製した二層シート、市販のヒアルロン酸とカルボキシメチルセルロースからなるフィルム(商品名セプラフィルム)、および材料を何も用いなかった場合についての、創傷部の組織再生効果を下記の方法で評価した。まず、麻酔下でイヌの腹部を切開し、回盲部から口側10cmの漿膜を4×3cm2だけ紙やすりでゆるく削りとり創傷部を作製した。止血後、創傷部に5×4.5cm2の大きさの二層シートあるいは、ヒアルロン酸フィルムを置き、30秒間押し付けた。対比として、材料を何も置かずに腹部を縫合した。3週間後に開腹して癒着の有無を観察してから患部を切り取り、ホルマリン固定した後に組織切片を作製して、腹膜中皮を酵素抗体法によりHBME1抗体にて染色した。二層シートを用いた場合の組織切片像を図6に、ヒアルロン酸とカルボキシメチルセルロースからなるフィルムを用いた場合の組織切片像を図7に示す。その結果、いずれの二層シートでも中皮の再生が確認できたが、ヒアルロン酸フィルム中皮の再生は確認できなかった。
【0047】
(水漏れ防止効果の評価)
実施例4で作製した二層シート、実施例7で作製した三層シートについて、水漏れ防止効果を下記の方法で評価した。トリ胸肉に穴を開けて内径1mmのチューブを挿入し、チューブ末端をトリ胸肉表面の開口部に固定した。チューブ内に水が一定量流れるようポンプを配置し、トリ胸肉表面の開口部から水が流れる水漏れ評価モデルを作製した。流量0.5mL/minの水漏れ評価モデルにおいて、2×2cm2の大きさの二層シートあるいは三層シートを開口部に貼付し、ゼラチン製の医療用接着剤をシート周囲に塗付した。対比として、二層シートあるいは三層シートを用いずにゼラチン製の医療用接着剤のみを開口部に塗付した。その結果、二層シートあるいは三層シートを用いた場合は、シートがトリ胸肉から外れることなく吸水して開口部からの水漏れを防止できたが、二層シートあるいは三層シートを用いなかった場合は、ゼラチン製の医療用接着剤がトリ胸肉から外れて開口部からの水漏れを防止できなかった。
【産業上の利用可能性】
【0048】
本発明の生体吸収性医療材料は、外科手術において、生体組織の創傷部において、止血、空気漏れ防止、組織再生能、癒着防止効果を発揮するものである。
【特許請求の範囲】
【請求項1】
片面が生体吸収性フィルム層からなり、反対面が生体吸収性多孔質層からなる、二層シート構造からなる生体吸収性医療材料。
【請求項2】
片面が生体吸収性フィルム層からなり、反対面が生体吸収性多孔質層からなり、その間に生体吸収性補強材料を有する三層シート構造からなる生体吸収性医療材料。
【請求項3】
生体吸収性フィルム層と生体吸収性多孔質層が天然高分子である請求項1または2に記載の生体吸収性医療材料。
【請求項4】
天然高分子がコラーゲンまたはゼラチンである請求項3に記載の生体吸収性医療材料。
【請求項5】
コラーゲンまたはゼラチンが架橋されている請求項4に記載の生体吸収性医療材料。
【請求項6】
架橋が熱架橋である請求項5に記載の生体吸収性医療材料。
【請求項7】
補強材料が合成高分子である請求項2に記載の生体吸収性医療材料。
【請求項8】
合成高分子がグリコリド、ラクチド、カプロラクトン、トリメチレンカーボネート、ジオキサノンのホモポリマー、もしくはこれらの共重合体である請求項7に記載の生体吸収性医療材料。
【請求項1】
片面が生体吸収性フィルム層からなり、反対面が生体吸収性多孔質層からなる、二層シート構造からなる生体吸収性医療材料。
【請求項2】
片面が生体吸収性フィルム層からなり、反対面が生体吸収性多孔質層からなり、その間に生体吸収性補強材料を有する三層シート構造からなる生体吸収性医療材料。
【請求項3】
生体吸収性フィルム層と生体吸収性多孔質層が天然高分子である請求項1または2に記載の生体吸収性医療材料。
【請求項4】
天然高分子がコラーゲンまたはゼラチンである請求項3に記載の生体吸収性医療材料。
【請求項5】
コラーゲンまたはゼラチンが架橋されている請求項4に記載の生体吸収性医療材料。
【請求項6】
架橋が熱架橋である請求項5に記載の生体吸収性医療材料。
【請求項7】
補強材料が合成高分子である請求項2に記載の生体吸収性医療材料。
【請求項8】
合成高分子がグリコリド、ラクチド、カプロラクトン、トリメチレンカーボネート、ジオキサノンのホモポリマー、もしくはこれらの共重合体である請求項7に記載の生体吸収性医療材料。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2012−95731(P2012−95731A)
【公開日】平成24年5月24日(2012.5.24)
【国際特許分類】
【出願番号】特願2010−244193(P2010−244193)
【出願日】平成22年10月29日(2010.10.29)
【出願人】(000001339)グンゼ株式会社 (919)
【Fターム(参考)】
【公開日】平成24年5月24日(2012.5.24)
【国際特許分類】
【出願日】平成22年10月29日(2010.10.29)
【出願人】(000001339)グンゼ株式会社 (919)
【Fターム(参考)】
[ Back to top ]

