生体成分分析方法及び生体成分分析装置
【課題】被験者が発汗した場合でも正確に測定対象成分を分析することができる生体成分分析方法を提供する。
【解決手段】被験者の皮膚から抽出された組織液に含まれる成分を分析する生体成分分析方法。組織液の抽出を促進する処理を被験者の皮膚の一部に施す工程と、促進処理が施された皮膚から測定対象成分を収集する工程と、促進処理が施された皮膚から第1補助成分を収集する工程と、促進処理が施されていない皮膚から汗に含まれる第2補助成分を収集する工程と、収集された測定対象成分、第1補助成分及び第2補助成分に基づいて、測定対象成分を分析する工程とを含んでいる。
【解決手段】被験者の皮膚から抽出された組織液に含まれる成分を分析する生体成分分析方法。組織液の抽出を促進する処理を被験者の皮膚の一部に施す工程と、促進処理が施された皮膚から測定対象成分を収集する工程と、促進処理が施された皮膚から第1補助成分を収集する工程と、促進処理が施されていない皮膚から汗に含まれる第2補助成分を収集する工程と、収集された測定対象成分、第1補助成分及び第2補助成分に基づいて、測定対象成分を分析する工程とを含んでいる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は生体成分分析方法及び生体成分分析装置に関する。さらに詳しくは、組織液の抽出を促進する処理が施された被験者の皮膚から抽出された組織液に含まれる測定対象成分を分析する方法及び装置に関する。
【背景技術】
【0002】
従来、被験者の皮膚から抽出された組織液に含まれる測定対象成分を測定する方法が知られている(例えば、特許文献1参照)。
特許文献1には、被験者の皮膚から抽出された組織液を用いて当該被験者の血糖―時間曲線下面積を算出(推定)する方法が開示されている。この方法は、被験者の皮膚に穿刺具を用いて微細孔を形成し、微細孔が形成された皮膚にゲルからなる収集体を有する組織液収集シートを所定時間(例えば、60分以上の時間)貼り付けることにより、当該皮膚から滲み出る組織液を収集する。ついで、収集体に収集された組織液に含まれるグルコース量及びナトリウムイオン量を測定し、得られるグルコース量及びナトリウムイオン量に基づいて、被験者の血糖―時間曲線下面積を推定する。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】国際公開第2010/013808号パンフレット
【発明の概要】
【発明が解決しようとする課題】
【0004】
特許文献1記載の方法において、被験者が発汗しないことを前提としている。しかしながら、実際には、組織液の収集中に発汗する被験者も存在する。
【0005】
本発明は、このような事情に鑑みてなされたものであり、発汗した被験者における測定対象成分を正確に分析することが可能な生体成分分析方法及び生体成分分析装置を提供することを目的としている。
【課題を解決するための手段】
【0006】
本発明の生体成分分析方法は、被験者の皮膚から抽出された組織液に含まれる成分を分析する生体成分分析方法であって、
組織液の抽出を促進する処理を被験者の皮膚の一部に施す工程と、
促進処理が施された皮膚から測定対象成分を収集する工程と、
促進処理が施された皮膚から第1補助成分を収集する工程と、
促進処理が施されていない皮膚から汗に含まれる第2補助成分を収集する工程と、
収集された測定対象成分、第1補助成分及び第2補助成分に基づいて、測定対象成分を分析する工程と
を含むことを特徴としている。
【0007】
本発明の生体成分分析方法において、促進処理が施された皮膚の表面からは組織液と汗に由来する第1補助成分が収集される。一方、促進処理が施されていない皮膚の表面では、組織液がほとんど湧き出ないため、汗にのみ由来する第2補助成分が収集される。したがって、このような第1補助成分と第2補助成分を収集し、両者を比較することで、第1補助成分にどの程度の汗由来の補助成分が混在しているのかを把握することができる。これにより、仮に被験者が発汗した場合であっても、本発明の生体成分分析方法によれば、収集された測定対象成分、第1補助成分及び第2補助成分に基づいて、正確な測定対象成分の解析結果を生成することができる。
【0008】
前記第1補助成分と第2補助成分は、同じ期間に収集されることが好ましい。
前記第1補助成分と第2補助成分は、同じ腕において収集されることが好ましい。
【0009】
前記分析工程は、
収集された第2補助成分を測定して第1測定値を取得する第1測定工程と、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値より小さい場合に、収集された測定対象成分を測定して第2測定値を取得する第2測定工程と、
第1測定値が所定の閾値より小さい場合に、収集された第1補助成分を測定して第3測定値を取得する第3測定工程と、
第2及び第3測定値に基づいて、測定対象成分の量に関する値を含む解析結果を生成する工程を含むものとすることができる。
【0010】
前記分析工程は、
収集された第2補助成分を測定して第1測定値を取得する第1測定工程と、
収集された測定対象成分を測定して第2測定値を取得する第2測定工程と、
収集された第1補助成分を測定して第3測定値を取得する第3測定工程と、
第1乃至第3測定値に基づいて、測定対象成分の解析結果を生成する工程と、
を含むものとすることができる。
【0011】
前記解析結果を生成する工程は、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値以上である場合に、第2及び第3の測定値に基づく測定対象成分の量に関する値と、この値の信頼性が低いことを示す情報とを含む解析結果を生成する工程を含むものとすることができる。
【0012】
前記解析結果を生成する工程は、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程を含むものとすることができる。
【0013】
前記解析結果を生成する工程は、
第1測定値と、第1の閾値及び第1の閾値より大きい第2の閾値とを比較する工程と、
第1測定値が第1の閾値以上であり且つ第2の閾値より小さい場合に、第2及び第3の測定値に基づく測定対象成分の量に関する値と、この値の信頼性が低いことを示す情報とを含む解析結果を生成する工程と、
第1測定値が第2の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程と、
を含むものとすることができる。
【0014】
第1測定値を、第2補助成分の量に関する値とし、
第2測定値を、測定対象成分の量に関する値とし、且つ
第3測定値を、第1補助成分の量に関する値とすることができる。
【0015】
分析工程は、第1測定値及び第3測定値に基づいて得られる補正値で第2測定値を補正することにより測定対象成分の解析結果を生成するものとすることができる。
【0016】
補正値は、第3測定値から第1測定値を減ずることにより得られた値とすることができる。
量に関する値は、単位時間あたりの補助成分の抽出量とすることができる。
前記解析結果を生成する工程は、
第1測定値と、第1の閾値及び第1の閾値より大きい第2の閾値とを比較する工程と、
第1測定値が第1の閾値以上であり且つ第2の閾値より小さい場合に、第1及び第3の測定値に基づく補正値で第2測定値を補正することにより測定対象成分の解析結果を生成する工程と、
第1測定値が第2の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程と、
を含むことができる。
【0017】
前記測定対象成分をグルコースとすることができる。
前記第1補助成分及び第2補助成分を無機イオンとすることができる。
前記第1補助成分と第2補助成分を同一種類の成分とすることができる。
前記無機イオンをナトリウムイオンとすることができる。
【0018】
前記測定対象成分及び第1補助成分を、被験者の皮膚に貼付可能な貼付面を有する保持シートの当該貼付面に配置された収集体に収集することができる。
前記収集体がゲルからなることが好ましい。
【0019】
本発明の生体成分分析装置は、被験者の皮膚から抽出される組織液に含まれる成分を分析する生体成分分析装置であって、
前記成分の抽出を促進する処理が施された被験者の皮膚の一部に所定時間配置された収集部材から測定対象成分及び第1補助成分に関する情報を取得する取得部と、
この取得部において取得された測定対象成分及び第1補助成分に関する情報と、促進処理が施されていない皮膚からの汗に含まれる第2補助成分に関する情報とに基づいて、測定対象成分を分析する解析部と
を備えたことを特徴としている。
【0020】
前記第2補助成分に関する情報を取得する第2取得部を更に備えていることが好ましい。
前記第2補助成分に関する情報を受け付ける情報受付部を更に備えていることが好ましい。
【発明の効果】
【0021】
本発明の生体成分分析方法及び生体成分分析装置によれば、発汗した被験者の測定対象成分を正確に分析することができる。
【図面の簡単な説明】
【0022】
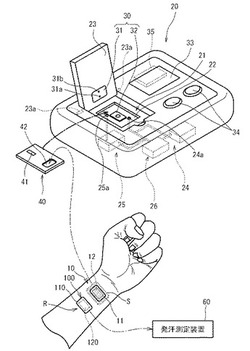
【図1】本発明の生体成分分析装置の一実施の形態の外観を示す斜視説明図である。
【図2】図1に示される生体成分分析装置のブロック図である。
【図3】本測定用カートリッジの構成を示す概略断面図である。
【図4】被験者の皮膚に微細孔を形成する微細孔形成装置の一例の斜視説明図である。
【図5】図4に示される微細孔形成装置に装着される微細針チップの斜視図である。
【図6】微細孔形成装置によって微細孔が形成された皮膚の断面説明図である。
【図7】本測定用収集部材の一例の斜視説明図である。
【図8】図7のA−A線断面図である。
【図9】発汗チェック用収集部材の一例の斜視説明図である。
【図10】第2補助成分を含むゲルの導電率を測定する原理を説明する図である。
【図11】第2補助成分を含むゲル中のナトリウムイオン濃度を測定する原理を説明する図である。
【図12】第1の実施形態の生体成分分析方法のフローチャートである。
【図13】グルコース透過率とナトリウムイオン抽出速度との相関を示すグラフである。
【図14】測定値乖離率とナトリウムイオン抽出速度JNa2との関係を示すグラフである。
【図15】測定値乖離率とNa相対値との関係を示すグラフである。
【図16】エラー症例を除外する前のグルコース透過率とナトリウムイオン抽出速度の相関を示すグラフである。
【図17】エラー症例を除外する前の推定血糖AUC値と採血血糖AUC値の相関を示すグラフである。
【図18】エラー症例を除外する前の測定値乖離率と非穿刺部位ナトリウムイオン抽出速度の関係を示すグラフである。
【図19】エラー症例を除外した後のグルコース透過率とナトリウムイオン抽出速度の相関を示すグラフである。
【図20】エラー症例を除外した後の推定血糖AUC値と採血血糖AUC値の相関を示すグラフである。
【図21】第2の実施形態の生体成分分析方法のフローチャートである。
【図22】第2の実施形態における制御部の処理を示すフローチャートである。
【図23】第3の実施形態における制御部の処理を示すフローチャートである。
【図24】共通収集部材の斜視説明図である。
【図25】第4の実施形態における生体成分分析方法のフローチャートである。
【図26】第4の実施形態における制御部の処理を示すフローチャートである。
【図27】発汗補正を行わなかったときのグルコース透過率とナトリウムイオン抽出速度との相関を示すグラフである。
【図28】非穿刺部位におけるナトリウムイオン抽出速度と測定値乖離率との関係を示すグラフである。
【図29】発汗補正を行ったときのグルコース透過率とナトリウムイオン抽出速度との相関を示すグラフである。
【図30】発汗補正前と発汗補正後の測定値乖離率を示すグラフである。
【発明を実施するための形態】
【0023】
以下、添付図面を参照しつつ、本発明の生体成分分析方法及び生体成分分析装置の実施の形態を詳細に説明する。
【0024】
(第1の実施形態)
図1は、本発明の一実施の形態に係る生体成分分析装置20の外観を示す斜視説明図であり、図2は、図1に示される生体成分分析装置のブロック図である。まず図1を参照して、生体成分分析方法の概略を説明する。
【0025】
本実施形態の生体成分分析方法は、後述するように、被験者の皮膚に微細孔を形成し、微細孔を介して組織液を抽出し、抽出された組織液に含まれるグルコース及びナトリウムイオンを収集し、収集されたグルコース及びナトリウムイオンの濃度に基づいて、被験者における血中グルコース(血糖)を分析する方法である。より具体的には、血糖―時間曲線下面積(血糖AUC)を算出する方法である。
【0026】
被験者が発汗すると、組織液に由来するナトリウムイオンに重畳するようにして汗由来のナトリウムイオンが収集され、ナトリウムイオン濃度が高くなる。本実施形態の生体成分分析方法では、グルコースとともに収集されたナトリウムイオンに基づいて被験者の血糖―時間曲線下面積を推定するため、汗由来のナトリウムイオンが過剰に収集されると、算出される血糖AUCの信頼性が低下することがある。
【0027】
そこで、本実施形態の方法では、微細孔が形成された皮膚Sに本測定用収集部材10を貼り付けるとともに、微細孔が形成されていない皮膚Rに発汗チェック用収集部材100を貼り付ける。この状態で、本測定用収集部材10に、組織液に含まれるグルコース及びナトリウムイオンを収集する。同時に、発汗チェック用収集部材100に、微細孔が形成されていない皮膚からの汗に含まれるナトリウムイオンを収集する。そして、発汗チェック用収集部材100に収集されたナトリウムイオンを測定(以下、発汗測定ともいう)し、ナトリウムイオン濃度が閾値よりも高いときには、本測定用収集部材10に収集されたグルコース濃度及びナトリウムイオンの濃度の測定(以下、本測定ともいう)、並びにこれらに基づく血糖AUCの解析を行わないように促すエラーメッセージを表示することとしている。これにより、信頼性の低い血糖AUCの解析結果が出力されることが回避される。
【0028】
〔生体成分分析装置〕
この生体成分分析装置20は、後述する本測定用収集部材10の収集体12に収集された組織液に含まれるグルコース及びナトリウムイオンを測定(以下、本測定と呼称することがある)して、グルコース濃度(CGlu)及びナトリウムイオン濃度(CNa1)を取得し、取得したCGlu及びCNa1に基づいて、被験者の血糖―時間曲線下面積(以下、血糖AUCともいう)を算出し、血糖AUCを含む解析結果を生成して表示する装置である。生体成分分析装置20は、検出部30と、解析部を含む制御部35と、解析結果やエラーメッセージなどを表示する表示部33と、測定開始の指示などを行うための操作部としての操作ボタン34とを備えている。
【0029】
生体成分分析装置20は、厚みのある直方体形状の筐体を備えており、筐体上面の天板には凹部21が形成されている。凹部21には、当該凹部21よりもさらに深く形成された凹部からなるカートリッジ配置部22が設けられている。さらに凹部21には、当該凹部21の側壁の高さとほぼ同じ厚みを有する可動天板23が連結されている。可動天板23は、支軸23aを中心に折り畳むことによって、図1に示される状態から凹部21内に収納し、又は凹部21に収納された状態から図1に示されるように起立させることができる。カートリッジ配置部22は、後述する本測定用カートリッジ40を収納することができる大きさを有している。
【0030】
可動天板23は、凹部21に収納される方向に付勢されるように、支軸23aに支持されている。したがって、カートリッジ配置部22に配置された本測定用カートリッジ40は、可動天板23によって上方から押さえつけられる。
【0031】
検出部30は、本測定用収集部材10の収集体12に収集された組織液に含まれる成分の情報を取得するものであり、測定対象成分であるグルコースの濃度CGluを検出するグルコース検出部31と、第1補助成分であるナトリウムイオンの濃度CNa1を検出するナトリウムイオン検出部32とを備えている。
【0032】
グルコース検出部31は、可動天板23の裏面、すなわち可動天板23が凹部21に収納されたときにカートリッジ配置部22と対向する側の面に設けられている。グルコース検出部31は、光を照射するための光源31aと、この光源31aによって照射された光の反射光を受光するための受光部31bとを備えている。これにより、グルコース検出部31は、カートリッジ配置部22に配置された本測定用カートリッジ40に対して光を照射するとともに、照射された本測定用カートリッジ40からの反射光を受光できるように構成されている。
【0033】
ナトリウムイオン検出部32は、カートリッジ位置部22の底面に設けられている。ナトリウムイオン検出部32は、カートリッジ配置部22の底面に設けられた長方形状を有する板状の部材を備え、この板状部材の略中央には一対のナトリウムイオン濃度測定用電極が設けられている。ナトリウムイオン濃度測定用電極は、ナトリウムイオン選択膜を備えた銀/塩化銀からなるナトリウムイオン選択性電極と、対電極である銀/塩化銀電極を含んでいる。
【0034】
制御部35は、生体成分分析装置20の内部に設けられており、解析部であるCPUや、記憶部であるROM、RAMなどを含んでいる。CPUは、ROMに記憶されたプログラムを読み出して実行することにより、各部の動作を制御する。RAMは、ROMに記憶されたプログラムが実行される際のプログラムの展開領域として利用される。
【0035】
生体成分分析装置20は、その内部にポンプからなる供給部24、本測定用収集部材10の収集体12に収集された組織液を回収するための純水からなる回収液を収容するタンク26、及び廃液を収容する廃液タンク25を備えている。供給部24は、タンク26に空気を送り込むことにより、ニップル24aを介して、カートリッジ配置部22に配置された本測定用カートリッジ40にタンク26内に収容されている回収液を注入する。
【0036】
廃液タンク25は、供給部24によって本測定用カートリッジ40に送液された純水が排出される機構であり、ニップル25aを介して、排出された液体を収容する。
【0037】
図3は、カートリッジ配置部22に本測定用カートリッジ40が配置された状態を示す概略断面図である。まず図3を参照して本測定用カートリッジ40の構成について説明する。
【0038】
本測定用カートリッジ40は、主な構成として、ゲル収容部42と、グルコース反応体41と、光導波部材44とを備えている。ゲル収容部42は、本測定用カートリッジ40の表面に形成された凹部からなる。ゲル収容部42の底部には、カートリッジ配置部22に設けられたニップル24aと連通する注入孔42aが設けられている。本測定用カートリッジ40の下面にはゲル収容部42と連通する溝が形成されている。この溝とカートリッジ配置部22の底部に設けられたナトリウムイオン検出部32とによって流路43aが形成される。この流路43aの一部は、ナトリウムイオン検出部32によりナトリウムイオン濃度が検出される第1貯留部43とされている。流路43aの下流は、第2貯留部45に連通している。第2貯留部45は本測定用カートリッジ40の表面に設けられた凹部からなり、その開口が光導波路を有する光導波部材44によって閉塞されている。この光導波部材44の下面に、グルコースと反応して変色するグルコース反応体41が設けられている。第2貯留部の底部には、カートリッジ配置部22に設けられたニップル25aと連通する排出孔45aが設けられている。
【0039】
生体成分分析装置20は、次のようにして本測定用収集部材10に収集された組織液に含まれるグルコースの濃度CGlu及びナトリウムイオンの濃度CNa1を測定する。まず、図1において、一点鎖線で示されるように、被験者の皮膚Sに所定時間貼り付けられた本測定用収集部材10が皮膚から取り外され、本測定用カートリッジ40のゲル収容部42に貼り付けられる。この本測定用カートリッジ40が生体成分分析装置20のカートリッジ配置部22に配置され、可動天板23が閉じられる。
【0040】
操作ボタン34によって測定開始が指示されると、供給部34からタンク26に向けて空気が供給され、タンク26からニップル24aに向けて回収液が送られる。回収液は注入孔42aからゲル収容部42に注入され、ゲル収容部42が回収液で満たされる。この状態で所定時間が経過すると、収集体12に収集された組織液が回収液に拡散する。所定時間が経過したら、供給部24はバイパス路24aを介してゲル収容部42に空気を送り込む。これにより、ゲル収容部42内の液体が流路43aを通じて第1貯留部43および第2貯留部45に送液される。
【0041】
ナトリウムイオン検出部32は、ナトリウムイオン濃度測定用電極によって第1貯留部43に貯留された液体に一定電圧を印加して電流値を取得する。このときの電流値は、液体に含まれるナトリウムイオン濃度に比例する。ナトリウムイオン検出部32は、得られた電流値を検出信号として制御部35に出力する。制御部35は、検出信号に含まれる電流値と予め制御部35の記憶部に記憶されている検量線とに基づいて、ナトリウムイオン濃度CNa1を取得する。
【0042】
第2貯留部では、回収液中のグルコースとグルコース反応体41とが反応し、グルコース反応体41が変色する。グルコース検出部31は、光源31aから光導波部材44に向かって光を照射し、光導波部材44から出射した光を受光部31bによって受光する。光源31aから光が照射されると、光は、変色したグルコース反応体41により吸光されながら、光導波部材44の内部で反射を繰り返して受光部31bに入射する。受光部31bにおける受光量はグルコース反応体41の変色度合いに比例し、この変色度合いが回収液中のグルコース量に比例する。グルコース検出部31は、得られた受光量を検出信号として制御部35に出力する。制御部35は、検出信号に含まれる受光量と予め制御部35の記憶部に記憶されている検量線とに基づいてグルコース濃度CGluを取得する。
【0043】
ナトリウムイオン濃度CNa1およびグルコース濃度CGluが取得されると、供給部24から本測定用カートリッジ40にさらに空気が送り込まれる。これにより回収液が排出孔45aおよびニップル25aを介して廃液タンク25に送られ、一連の測定が終了する。
【0044】
〔微細孔形成装置〕
つぎに被験者の皮膚に微細孔を形成する微細孔形成装置の一例について説明する。微細孔形成装置は、被験者の皮膚の一部に多数の微細な孔を形成して当該被験者の皮膚からの組織液の抽出を促進する装置である。本実施形態では、組織液抽出促進のための微細孔が形成された被験者の皮膚S(図1参照)からグルコース及びナトリウムイオンが収集されるとともに、後述するように、微細孔が形成されていない被験者の皮膚Rからの汗に含まれるナトリウムイオンが収集される。
【0045】
図4は、本発明の生体成分分析方法において被験者の皮膚に組織液抽出促進用の微細孔を形成するのに用いられる微細孔形成装置の一例に係る穿刺具100の斜視説明図であり、図5は、図4に示される穿刺具100に装着される微細針チップ200の斜視図であり、図6は、穿刺具100によって微細孔が形成された皮膚Sの断面説明図である。
【0046】
図4〜6に示されるように、穿刺具100は、滅菌処理された微細針チップ200を装着して、当該微細針チップ200の微細針201を生体の表皮(被験者の皮膚300)に当接させることによって、被験者の皮膚300に組織液の抽出孔(微細孔301)を形成する装置である。微細針チップ200の微細針201は、穿刺具100により微細孔301を形成した場合に、当該微細孔301が皮膚300の表皮内にとどまり真皮までは到達しないような大きさを有する。
【0047】
図4に示されるように、穿刺具100は、筐体101と、この筐体101の表面に設けられたリリースボタン102と、筐体101の内部に設けられたアレイチャック103及びバネ部材104とを備えている。筐体101の下部101aの下端面(皮膚に当接する面)には、前記微細針チップ200が通過可能な開口(図示せず)が形成されている。バネ部材104はアレイチャック103を穿刺方向に付勢する機能を有する。アレイチャック103は下端に微細針チップ200を装着することができる。微細針チップ200の下面には、複数の微細針201が形成されている。微細針チップ200の下面は、10mm(長辺)×5mm(短辺)の大きさからなる。また、穿刺具100は、アレイチャック103をバネ部材104の付勢力に逆らって上方(反穿刺方向)に押し上げた状態で固定する固定機構(図示せず)を有しており、使用者(被験者)がリリースボタン102を押下することにより、当該固定機構によるアレイチャック103の固定が解除され、バネ部材104の付勢力によって当該アレイチャック103が穿刺方向に移動し、前記開口から突出した微細針チップ200の微細針201が皮膚を穿刺するように構成されている。なお、図4において、105は筐体101の下部101aに形成された鍔部であり、穿刺具100の使用時には前記鍔部105の裏面が被験者の皮膚の所定箇所に当接される。
【0048】
〔本測定用収集部材〕
つぎに被験者の皮膚から組織液を収集する本測定用収集部材10について説明する。本測定用収集部材10は被験者の皮膚から組織液を収集するために当該被験者の皮膚に貼付され、所定時間経過後に皮膚から剥がされるものである。
【0049】
図7は、保持シート11と、この保持シート11に保持された収集体12とを備えた本測定用収集部材10の斜視説明図であり、図8は、図7のA−A線断面図である。
【0050】
収集体12は、被験者の皮膚から抽出した組織液を保持可能な保水性を有するゲルからなっており、抽出媒体としての純水を含有している。このゲルは、組織液を収集することが可能であれば特に限定されないが、ポリビニルアルコールやポリビニルピロリドンからなる群より選ばれる少なくとも一種の親水性ポリマーから形成されたゲルが好ましい。ゲルを形成する親水性ポリマーは、ポリビニルアルコール単独又はポリビニルピロリドン単独であってもよく、また両者の混合物であってもよいが、ポリビニルアルコール単独又はポリビニルアルコールとポリビニルピロリドンとの混合物であることがより好ましい。
【0051】
ゲルは、親水性ポリマーを水溶液中で架橋する方法により形成することができる。ゲルは、親水性ポリマーの水溶液を基材上に塗工して塗膜を形成し、該塗膜中に含まれる親水性ポリマーを架橋する方法により形成することができる。親水性ポリマーの架橋法としては、化学架橋法や放射線架橋法などがあるが、ゲル中に各種化学物質が不純物として混入し難い点より、放射線架橋法を採用することが望ましい。
【0052】
収集体12は、図7〜8に示される例では直方体形状を呈しており、皮膚と当接する面のサイズは7mm×12mmである。ただし、収集体12の形状及びサイズは、これに限定されるものではない。
【0053】
保持シート11は、小判形状のシート本体11aと、このシート本体11aの片面に形成された粘着剤層11bとで構成されており、前記粘着剤層11bが形成された側の面が粘着面とされている。収集体12は、同じく小判形状の、台紙としても機能する剥離シート13のほぼ中央に配設されており、この収集体12を覆うように前記保持シート11が剥離シート13に貼付されている。収集体12は、保持シート11の粘着面の一部によって当該保持シート11に保持されている。保持シート11の面積は、組織液収集時における収集体12の乾燥を防ぐために、収集体12を覆うことが可能な大きさを有している。すなわち、保持シート11によって収集体12を覆うことにより、組織液収集時に皮膚と保持シート11との間を気密に保つことができ、組織液収集時に収集体12に含まれる水分が蒸発するのを抑制することができる。
【0054】
保持シート11のシート本体11aは、無色透明又は有色透明であり、当該シート本体11aの表面側(粘着剤層11bと反対側の面)から、保持シート11に保持されている収集体12を目視にて容易に確認することができる。シート本体11aは、組織液の蒸発や収集体の乾燥を防ぐため透湿性が低いものが好ましい。シート本体11aの材質としては、例えばポリエチレンフィルム、ポリプロピレンフィルム、ポリエステルフィルム、ポリウレタンフィルムなどが挙げられ、その中でもポリエチレンフィルム、ポリエステルフィルムが好ましい。シート本体11aの厚さは、特に限定されないが、概ね0.025〜0.5mm程度である。
【0055】
本測定用収集部材10は、収集体12が被験者の微細孔形成領域R(組織液の抽出を促進させるために穿刺具100によって被験者の皮膚300に複数の微細孔301が形成された領域)に配置されるように、保持シート11の粘着面によって当該被験者の皮膚300に貼付される。そして、収集体12を微細孔形成領域に配置した状態で所定時間、例えば60分以上、好ましくは180分以上放置することにより、微細孔を介して抽出される組織液に含まれる成分を当該収集体12に収集する。
【0056】
〔発汗チェック用収集部材〕
つぎに被験者の皮膚から汗を収集する発汗チェック用収集部材100について説明する。図9は、本実施形態における発汗チェック用収集部材100の構成を示す斜視図である。発汗チェック用収集部材100は、上述の本測定用収集部材10と同じ構成を備えており、保持シート110と、この保持シート110に保持された収集体120と剥離シート130とを備えている。発汗チェック用収集部材100の各部の構成については、図7および図8に示した本測定用収集部材10と同様であるため、詳細な説明は省略する。
【0057】
〔発汗測定装置〕
図10は、本実施形態の生体成分分析方法に用いられる発汗測定装置の概略説明図である。発汗測定装置60は、発汗チェック用収集部材100の収集体120が載せられる基台60a、基台60aの上面に設けられた対向電極61a及び61b、交流電源62a、対向電極61a及び61b間の電圧を計測する電圧計62b、解析部60b及び表示部60cを備えている。基台60a上に収集体120が載置されると、対向電極61a及び61bが収集体120に差し込まれ、対向電極61aと61bとが収集体120を通じて短絡する。この状態で交流電源62aによって電圧が印加されると、対向電極61a及び61b間の電圧が電圧計62bによって計測される。解析部60bは、計測された電圧値と検量線とに基づいて、発汗チェック用収集部材100の収集体12に収集されたナトリウムイオンの濃度CNa2を解析し、表示部に60cにナトリウムイオン濃度CNa2を表示させる。
【0058】
また、発汗測定装置として、図11に示されるように、ナトリウムイオン選択膜を備えた銀/塩化銀からなるナトリウムイオン選択性電極63と、対電極である銀/塩化銀電極64とからなる一対のナトリウムイオン濃度測定用電極を備えていてもよい。
【0059】
〔生体成分分析方法〕
つぎに本発明の第1実施形態の生体成分分析方法の一実施の形態について説明する。
図12は、第1の実施の形態に係る生体成分分析方法のフローチャートである。
【0060】
まずステップS1において、図4に示される穿刺具を用いて被験者の皮膚に微細孔が形成される。具体的には、被験者の皮膚300をアルコールなどを用いて清拭し、測定結果の外乱要因となる物質(塵など)を除去する。その後、当該被験者の皮膚に、前述した微細針チップ200を装着した穿刺具100の鍔部105を配置し、ついでリリースボタン102を押圧して微細針チップ200の微細針201を被験者の皮膚300に接触させることで、当該皮膚300に微細孔301を形成する。かかる微細孔を形成することで、皮膚300からの組織液の抽出を促進させることができる。
【0061】
ついで、ステップS2において、穿刺具100を被験者の皮膚300から離し、その後微細孔301が形成された領域S(微細孔形成領域)に収集体12が配置されるように、本測定用収集部材10の保持シート11を被験者の皮膚300に貼付する(図1参照)。
【0062】
ついで、ステップS3において、発汗チェック用収集部材100を非穿刺部位R、例えば被験者の微細孔形成領域近傍の皮膚に貼付する。微細孔は、通常、被験者の腕に形成される。本測定用収集部材10と、発汗チェック用収集部材100とを別々の腕に貼付することも可能であるが、できるだけ測定条件を同じにするという観点からは、本測定用収集部材10と、発汗チェック用収集部材100とを、同じ腕に貼付することが好ましい。同じ腕に貼付することで、右腕と左腕とで発汗量が異なる場合であっても、本測定用収集部材10と発汗チェック用収集部材100とで、収集される汗由来のナトリウムイオンの量の差を小さくすることができる。
【0063】
ついで、ステップS4において、本測定用収集部材10中に被験者の皮膚からの組織液が抽出され、組織液に含まれるグルコース及びナトリウムイオンが本測定用収集部材10の収集体12に収集され、蓄積される。このとき、被験者が発汗した場合には、組織液とともに被験者の皮膚から、汗に含まれるナトリウムイオンも本測定用収集部材10中に収集される。同時に、発汗チェック用収集部材100によって、汗に含まれるナトリウムイオンが収集される。収集時間は、例えば60分〜180分程度である。
【0064】
ついで、ステップS5において、本測定用収集部材10及び発汗チェック用収集部材100を被験者の皮膚から取り外す。
【0065】
ステップS6〜S11は、ステップS4において収集された各成分を分析する工程である。
まず、ステップS6において、被験者の皮膚から取り外された発汗チェック用収集部材100が発汗測定装置60にセットされる。発汗測定装置60の対向電極61a及び61bが、発汗チェック用収集部材100の収集体120に埋設されるように、発汗チェック用収集部材100が発汗測定装置60にセットされる。
【0066】
ついで、ステップS7において、発汗チェック用収集部材100の収集体120の導電率を測定することで、収集体120に含まれるナトリウムイオン濃度CNa2を測定する。ゲルの導電率から推定したナトリウムイオン量は、イオンクロマトグラムを用いて別途測定をしたナトリウムイオン量と高い相関関係を有することが確認されている。したがって、ゲルの導電率を測定するという比較的簡便な方法で、ゲル中のナトリウムイオン量を推定することができる。発汗測定装置60によって測定されたナトリウムイオン濃度CNa2は、表示部60cに表示される。
【0067】
ついで、ステップS8において、ステップS7において測定されたナトリウムイオン濃度CNa2が操作ボタン34によって生体成分分析装置20に入力される。ついで、ステップS8において、制御部35は、入力されたナトリウムイオン濃度CNa2が所定の閾値よりも高いか否かの判断をする。制御部35は、ナトリウムイオン濃度CNa2が閾値よりも高いと判断すると、表示部33にエラーメッセージ(発汗量が多いので、本測定を行っても精度が保証できない旨)を表示する。本測定(グルコース濃度CGlu及びナトリウムイオン濃度CNa1の測定、並びに血糖AUC推定値の算出)は、上述の本測定用カートリッジ40を用いて行われる。本測定用カートリッジ40は、グルコース反応体41を含む使い捨てのカートリッジであるので、発汗量のチェックを行って精度の低い分析の中止を促すことで、本測定用カートリッジ40の無駄な消費を抑えることができる。閾値は、後述する血糖AUC推定値、採血による血糖AUC及び発汗量についての実験データなどから、例えば、以下に述べるようにして予め求めることができる。
【0068】
〔閾値の設定〕
発汗の多い症例と発汗の少ない症例とを分類するための指標としては、(1)非穿刺部位におけるナトリウムイオン抽出速度(単位時間あたりに発汗チェック用収集部材100に収集されたナトリウムイオンの総量)に対する閾値、及び(2)本測定用収集部材10に収集されたナトリウムイオンの濃度CNa1から得られるナトリウムイオン抽出速度に対する非穿刺部位のナトリウムイオン抽出速度(単位時間あたりに発汗チェック用収集部材100に収集されたナトリウムイオンの総量)の相対値(以下、「Na相対値」という)のいずれかを用いることができる。これらの指標に対して閾値を設定し、被験者から得られた指標と閾値とを比較することにより、グルコース濃度CGlu及びナトリウムイオン濃度CNa1に基づいて信頼性の高い血糖AUCが得られるか否かを判断することができる。かかる閾値は、実験により予め求めることができる。以下、実験的に設定される閾値の例を説明する。
【0069】
図13は、複数の症例に関するグルコース透過率(縦軸)と、ナトリウムイオン抽出速度(横軸)との関係を示すグラフである。図14は、図13のデータを、ナトリウムイオン抽出速度JNa2に対する閾値に基づいて区分したグラフである。図15は、図13のデータを、相対Na値に対する閾値に基づいて区分したグラフである。
図13〜15のデータを得るにあたっては、本実施形態における組織液および汗に含まれる成分の収集と並行して、所定時間毎に複数回採血を行った。組織液に含まれるグルコース及びナトリウムイオン並びに後述の式(1)に基づいて血糖AUCを算出した(推定血糖AUCという)。また、複数回の採血によって得られた複数時点における血糖値から周知の台形近似法によって血糖AUCを算出した(採血血糖AUCという)。
【0070】
図13の縦軸に示したグルコース透過率とは、本測定用収集部材10に収集されたグルコース量を採血血糖AUCで除した値である。つまり、グルコース透過率は、体内の血糖AUCに対して体外で抽出されるグルコース量の比率を示している。一方、ナトリウムイオン抽出速度とは、単位時間あたりに本測定用収集体10に収集されたナトリウムイオンの量のことである。
【0071】
図13に示した症例の中から、発汗が多い例(記号◆)と、発汗が少ない例(記号▲)とを抽出した。それぞれの測定結果を、以下の表1に示す。
【0072】
【表1】

【0073】
なお、Na相対値は、次の式に基づいて求めた。
Na相対値={(JNa2)−(定数γ)}÷(JNa1)
ここで、定数γ=0.047として計算した。ナトリウムイオンは全く発汗しない場合でも皮膚からわずかな量だけ検出されるが、定数γは、このような場合に検出されるNa値の誤差を除去することができる値が用いられる。
【0074】
<ナトリウムイオン抽出速度JNa2に対する閾値>
ナトリウムイオン抽出速度JNa2に対する閾値の一例として、0.04(μmol/h)なる値を用いた。つまり、発汗チェック用収集体に収集された単位時間あたりのナトリウムイオン量が0.04(umol/h)を超える症例が除外される。この閾値を用いて図13に示される症例を区分した。結果を図14に示す。
【0075】
図14において、縦軸は測定値乖離率、横軸は非穿刺部位におけるナトリウムイオン抽出速度JNa2である。測定値乖離率は、各症例について測定した推定血糖AUCと採血血糖AUCとの比であり、これが1に近いほど推定血糖AUCの信頼性が高いことを示す。図14に示されるように、ナトリウムイオン抽出速度JNa2に対する閾値を0.04とすることにより、測定値乖離率が0.8を下回るような信頼性の低い測定結果を多数排除することができる。
【0076】
<Na相対値に対する閾値>
Na相対値に対する閾値の一例として、0.045なる値を用いた。この閾値を用いて図13に示される症例を区分した。結果を図15に示す。図15において、縦軸は測定値乖離率、横軸はNa相対値である。
図15に示されるように、Na相対値に対する閾値を0.045とすることにより、測定値乖離率が0.8を下回るような信頼性の低い測定結果を多数排除することができる。
【0077】
ナトリウムイオン抽出速度JNa2に対する閾値を用いる場合には、発汗量の多い症例を、ナトリウムイオン抽出速度JNa1を測定することなく除外することができる。したがって、信頼性の低い解析結果となることが予見されるような症例について、無駄な本測定を回避できる利点がある。
【0078】
Na相対値に対する閾値を用いる場合には、ナトリウムイオン抽出速度JNa1に対してナトリウムイオン抽出速度JNa2の影響が相対的に大きい症例のみを排除することができる。したがって、ナトリウムイオン抽出速度JNa2の絶対値は比較的大きいものの、本測定への影響が小さいと考えられる症例については、本測定の結果を棄却することなく、本測定の結果を有効に活用することができる。
なお、第1実施形態においては、ナトリウムイオン抽出速度JNa2に対する閾値を用いて、発汗量の多い症例を除外する形態を説明する。
【0079】
図12に戻って、ナトリウムイオン抽出速度JNa2が閾値以下である場合(ステップS8において「No」)、ステップS10において、本測定用収集部材10が本測定用カートリッジ40の所定箇所に貼付され、当該本測定用カートリッジ40が生体成分分析装置20のカートリッジ配置部22にセットされる。
【0080】
ついで、ステップS11において、生体成分分析装置20によって上述した測定処理が実行されることにより、グルコース濃度CGlu及びナトリウムイオン濃度CNa1が測定される。ついで、制御部35は、グルコース濃度CGlu及びナトリウムイオン濃度CNa1と下記式(1)とに基づいて血糖AUCを算出する。
AUC=CGlu×V/{α×(CNa1×V/t)+β} ・・・(1)
式(1)において、Vは本測定用収集部材10の収集体12の体積である。α及びβは実験により求められる定数である。式(1)に基づいて血糖AUCが算出される原理については、国際公開公報第2010/013808号に詳細に説明されている。国際公開公報第2010/013808号は本明細書において参照として組み込まれる。
ついで、ステップS12において、算出された結果が制御部35によって表示部33に出力される。
【0081】
本実施の形態では、微細孔形成処理が施されていない皮膚Rからの汗に含まれるナトリウムイオンを収集し、収集されたナトリウムイオン濃度が閾値よりも高い場合に本測定(CGlu及びCNa1の測定並びに血糖AUCの解析)を行わないようにすることで、信頼性の低い血糖AUC解析を回避することができる。
【0082】
〔効果の検証〕
以下、第1実施形態による生体成分分析方法による測定精度の向上例について説明する。 図16は、乖離症例を除外する前のグルコース透過率とナトリウムイオン抽出速度の相関を示すグラフである。図17は、推定血糖AUC値と採血血糖AUC値(測定血糖AUC値)の相関を示すグラフである。図18は、測定値乖離率と非穿刺部位におけるナトリウムイオン抽出速度の関係を示すグラフである。図19は、図16に対応するグラフであり、乖離症例を除外したグルコース透過率とナトリウムイオン抽出速度の相関を示すグラフである。図20は、図17に対応するグラフであり、乖離症例を除外した推定血糖AUCと採血血糖AUCの相関を示すグラフである。
【0083】
図16〜18において、「●」は糖尿病患者の症例であり、「×」は健常人の症例である。また、○で囲んだものが乖離症例(発汗量が多く、測定値乖離率が1から大きく離れている症例)である。乖離症例は、すべて糖尿病患者に認められた。
図16〜20のデータを得るにあたっては、本実施形態における組織液および汗に含まれる成分の収集と並行して、所定時間毎に複数回採血を行った。組織液に含まれるグルコース及びナトリウムイオン並びに上述の式(1)に基づいて血糖AUCを算出した(推定血糖AUCという)。また、複数回の採血によって得られた複数時点における血糖値から周知の台形近似法によって血糖AUCを算出した(採血血糖AUCという)。
【0084】
図16は、グルコース透過率を縦軸とし、ナトリウムイオン抽出速度を横軸としたグラフである。グルコース透過率とは、本測定用収集部材10に収集されたグルコース量を採血血糖AUCで除した値である。つまり、グルコース透過率は、体内の血糖AUCに対して体外で抽出されるグルコース量の比率を示している。ナトリウムイオン抽出速度とは、単位時間あたりに本測定用収集部材100に収集されたナトリウムイオンの量である。国際公開公報2010/013808号に詳細に記載されているように、ナトリウムイオン抽出速度とグルコース透過率とは相関関係にある。図16に示すように、ナトリウムイオン抽出速度とグルコース透過率をプロットすると、一定の傾きからなる回帰直線の周辺にプロットが収束する。
【0085】
被験者が発汗すると、汗に由来するナトリウムイオンが本測定用収集部材10に余分に収集される。その結果、図16に丸印で示したように、ナトリウムイオン抽出速度のみが増大し、回帰直線に対してプロットが右側にシフトする。図16に示したプロット全てを対象として相関係数を求めたところ、相関係数は0.81であった。
【0086】
図16に示したデータについて、推定血糖AUC値と採血血糖AUC値の相関を調べた。結果を図17に示す。
図17は、推定血糖AUCを縦軸とし、横軸を採血血糖AUCを横軸としたグラフである。図17に丸印で示したように、発汗の多い症例はナトリウムイオン濃度の増大に起因して、推定血糖AUCと血糖AUCとの乖離が大きい。図17に示した全症例について相関係数を求めたところ、相関係数は0.68であった。
【0087】
図18は、測定値乖離率を縦軸とし、非穿刺部位におけるナトリウムイオン抽出速度を横軸としたグラフである。図18に示した測定値乖離率とは、図17に示した推定血糖AUCを採血血糖AUCで除した値である。測定値乖離率が1に近いほど、推定血糖AUCの信頼性が高いことを意味する。図18に示すように、測定値乖離率は、非穿刺部位におけるナトリウムイオン抽出速度が増大するにしたがって、低下している。そこで、本例では、非穿刺部位におけるナトリウムイオン抽出速度が0.06(μmol/h)を超える5症例10部位のデータを解析対象から除外し、再度解析を行った。その結果を図19及び図20に示す。
【0088】
5症例10部位の乖離症例を解析対象から除外すると、図19に示されるように、グルコース透過率とナトリウムイオン抽出速度との相関係数が0.81から0.90に向上した。さらに、図20に示されるように、推定血糖AUC値と血糖AUC値との相関係数が0.68から0.82に向上した。このことから、発汗チェック用収集部材100に収集されたナトリウムイオン量に基づいて、発汗の多い症例についての本測定を回避することにより、信頼性の低い血糖AUC推定値の解析がユーザに提供されることが防止されることが実証された。
【0089】
(第2の実施形態)
つぎに本発明の第2実施形態の生体成分分析方法について説明する。図21は、第2の実施形態に係る生体成分分析方法のフローチャートである。
第1の実施形態では、発汗測定の結果(JNa2)に基づいて、本測定(CGlu及びCNa1の測定)及び血糖AUCの算出を実行するか否かを決定する形態を例示した。第2の実施形態では、発汗測定及び本測定を実行したうえで、血糖AUCの信頼性に関する情報を血糖AUCの解析結果とともに出力する。
【0090】
図21のフローチャートにおいて、ステップS101〜105の工程は、図12に示した第1実施形態におけるステップS1〜5と同じであるから、ステップS101〜S105については詳細な説明を省略し、ステップS106〜S111の分析工程について詳細に説明する。ステップS106〜S111は、ステップS104において収集された成分を分析する工程である。
【0091】
まず、ステップS106において、発汗チェック用収集部材100が発汗測定装置60にセットされ、ステップS107において、収集体120に収集されたナトリウムイオンの濃度CNa2が測定される。ついで、ステップS108において、本測定用収集部材10が本測定用カートリッジ40の所定箇所に貼付され、本測定用カートリッジ40が生体成分分析装置20のカートリッジ配置部22にセットされる。ステップS109において、収集体12に収集されたグルコース濃度CGlu及びナトリウムイオン濃度CNa1が測定され、グルコース濃度CGlu及びナトリウムイオン濃度CNa1に基づいて血糖AUC推定値が算出される。
【0092】
ついでステップS110において、ユーザによって、ステップS107において得られたナトリウムイオン抽出速度JNa2が生体成分分析装置20に入力される。ステップS111において、制御部35によって解析結果が生成され、ステップS112において、生成された解析結果が表示部33に出力される。
【0093】
図22は、ステップS111において制御部35により実行される処理のフローチャートである。
まず、制御部35は、ステップS121において、入力されたナトリウムイオン抽出速度JNa2と閾値とを比較し、ナトリウムイオン抽出速度JNa2が閾値以上であるか否かを判断する。閾値以上であると判断した場合(ステップS121においてYES)、制御部35は、ステップS122に処理を進める。ステップS122において、制御部35は、ステップS109で算出された血糖AUCと、この血糖AUCの信頼性が低いことを示すフラグ情報とを含む解析結果を生成する。一方、ナトリウムイオン抽出速度JNa2が閾値未満であると判断した場合(ステップS122においてNO)、制御部35は、ステップS123に処理を進める。ステップS123において、制御部35は、ステップS109で算出された血糖AUCのみを含む解析結果を生成する。ナトリウムイオン抽出速度JNa2が閾値未満である場合には、血糖AUCの信頼性は高いため、解析結果にフラグ情報は含まれない。
第2実施形態によれば、被験者が血糖AUCの算出結果に影響を及ぼす程発汗した場合に、血糖AUCの信頼性が低下したことをユーザに知らせることができる。ユーザは、このフラグ情報を、出力された血糖AUCを利用するか否かの決定に役立てることができる。
なお、第2の実施形態では、JNa2を閾値と比較する形態を示したが、JNa1及びJNa2に基づいてNa相対値を求め、Na相対値と閾値とを比較する形態であってもよい。
【0094】
(第3の実施形態)
前述した第1及び第2実施形態では、1つの閾値を設定し、ナトリウムイオン抽出速度JNa2が閾値よりも高いか否かの判断をしているが、複数の段階的な閾値を設定することもできる。例えば2つの閾値(第1の閾値と、これよりも大きい第2の閾値)を設定し、ナトリウムイオン抽出速度JNa2に応じて異なる解析結果を生成するように構成してもよい。
【0095】
図23は、第3の実施形態に係る生体成分分析方法における制御部の処理を示すフローチャートである。第3の実施形態は、制御部35による処理を除いて図21のステップS101〜S112と同じであるので、ここでは説明を省略する。
【0096】
まず、ステップS131において、制御部35は、ナトリウムイオン抽出速度JNa2が第1の閾値以上であるか否かを判断する。ここで、第1の閾値としては、血糖AUCの解析結果を棄却するほどではないが、血糖AUCの解析に影響を及ぼす値が設定される。制御部35は、ナトリウムイオン抽出速度JNa2が第1の閾値以上であると判断した場合(ステップS131においてYES)、ステップS132に処理を進め、ナトリウムイオン濃度CNa2が第1の閾値未満であると判断した場合(ステップS131においてNO)、ステップS136に処理を進める。
【0097】
ステップS136において、制御部35は、ステップS109で算出された血糖AUCのみを含む解析結果を生成する。
ステップS132において、制御部35は、ナトリウムイオン抽出速度JNa2が、第2の閾値以上であるか否かを判断する。ここで、第2の閾値としては、第1の閾値よりも大きい値であって、血糖AUCの解析結果を棄却する必要が生じる値が設定される。制御部35は、ナトリウムイオン抽出速度JNa2が第2の閾値以上であると判断した場合(ステップS132においてYES)、ステップS133に処理を進め、ナトリウムイオン抽出速度JNa2が第2の閾値未満であると判断した場合(ステップS132においてNO)、ステップS134に処理を進める。
【0098】
ステップS134において、制御部35は、ステップS109で算出された血糖AUCと、この血糖AUCの信頼性が低い旨のフラグ情報を含む解析結果を生成する。
ステップS133において、制御部35は、「解析結果の信頼性を保証できないため血糖AUCの解析結果を表示できません。再測定を行ってください」といった内容のメッセージを含む解析結果を生成する。この場合、ステップS109で算出された血糖AUCは解析結果に含まれない。
【0099】
第3実施形態によれば、被験者の発汗量に応じて異なる解析結果を出力することができる。さらに、血糖AUCの解析結果を棄却する必要が生じる程被験者が発汗したときには、血糖AUCの解析結果を出力しない旨のメッセージを出力することにより、発汗量を抑えて再度測定を行うことを促すことができる。
なお、第3の実施形態では、JNa2を閾値と比較する形態を示したが、JNa1及びJNa2に基づいてNa相対値を求め、Na相対値と閾値とを比較する形態であってもよい。
【0100】
(第4の実施形態)
前述した実施の形態では、JNa2を本測定に進むか否かの判断材料として用いるか(第1の実施形態)、又は、JNa2の測定に続いて本測定を行い、JNa2の値によっては血糖AUCの解析結果の信頼性が低い旨の表示をしている(第2又は第3の実施形態)が、第1補助成分の量に関する値から、第2補助成分の量に関する値を減じるなどの補正処理を行うことで、測定対象成分の解析の精度を向上させることも可能である。
【0101】
本実施形態では、かかる補正処理を行うことで測定対象成分の解析の精度を向上させている。図25は、第4の実施形態における生体成分分析方法のフローチャートである。
ステップT1(微細孔形成処理)からステップT5(本測定用収集部材及び発汗用収集部材の取り外し)までの処理内容は、図12に示される第1の実施形態におけるステップS1からステップS5までのものと同様であるので、簡単のため、それらについての説明は省略する。
【0102】
ステップT6〜ステップT10は、ステップT4において収集された各成分を分析する工程である。本実施の形態では、分析時間を短縮するために、発汗チェック用収集部材で収集された成分と、本測定用収集部材で収集された成分とを並行して分析している。
まず、ステップT6において、被験者の皮膚から取り外された発汗チェック用収集部材100が発汗測定装置60にセットされる。発汗測定装置60の対向電極61a及び61bが、発汗チェック用収集部材100の収集体120に埋設されるように、発汗チェック用収集部材100が発汗測定装置60にセットされる。
【0103】
ついで、ステップT7において、発汗チェック用収集部材100の収集体120の導電率を測定することで、収集体120に含まれるナトリウムイオン濃度CNa2を測定する。発汗測定装置60によって測定されたナトリウムイオン濃度CNa2は、表示部60cに表示される。そして、測定されたナトリウムイオン濃度CNa2が操作ボタン34によって生体成分分析装置20に入力されると、制御部35は、入力されたナトリウムイオン濃度CNa2に基づいて以下の式に従い、非穿刺部位のナトリウムイオン抽出速度JNa2を算出する。
JNa2=CNa2×V2/t
ここで、V2は発汗チェック用収集部材100の収集体120の体積であり、tは抽出時間である。
【0104】
一方、ステップT6と並行して、ステップT8において、本測定用収集部材10が本測定用カートリッジ40の所定箇所に貼付され、当該本測定用カートリッジ40が生体成分分析装置20のカートリッジ配置部22にセットされる。
【0105】
ついで、ステップT9において、生体成分分析装置20によって上述した測定処理が実行されることにより、グルコース濃度CGlu及びナトリウムイオン濃度CNa1が測定される。ついで、制御部35は、グルコース濃度CGlu及びナトリウムイオン濃度CNa1と下記式とに基づいて、抽出グルコース量MGlu及び穿刺部位のナトリウムイオン抽出速度JNa1を算出する。
MGlu=CGlu×V1
JNa1=CNa1×V1/t
ここで、V1は本測定用収集部材10の収集体12の体積であり、tは抽出時間である。
【0106】
ついで、ステップT10において、制御部35は、ステップT7において算出されたJNa2及びステップT9において算出されたMGlu及びJNa1を用いて下記式(2)に従い補正された血糖AUC推定値を算出する。
【0107】
【数1】

【0108】
ここで、α及びβは実験により求められる定数である。
ついで、ステップT11において、制御部35によって解析結果が生成され、ステップT12において、生成された解析結果が表示部33に出力される。
【0109】
図26は、第4の実施形態に係る生体成分分析方法における制御部の処理を示すフローチャートである。
【0110】
まず、ステップT131において、制御部35は、ナトリウムイオン抽出速度JNa2が第1の閾値以上であるか否かを判断する。ここで、第1の閾値としては、血糖AUCの解析結果を棄却するほどではないが、血糖AUCの解析に影響を及ぼす値が設定される。制御部35は、ナトリウムイオン抽出速度JNa2が第1の閾値以上であると判断した場合(ステップT131においてYes)、ステップT132に処理を進め、ナトリウムイオン抽出速度JNa2が第1の閾値未満であると判断した場合(ステップT131においてNo)、ステップT136に処理を進める。
【0111】
ステップT136において、制御部35は、ステップT9で算出された血糖AUCを含む解析結果を生成する。
ステップT132において、制御部35は、ナトリウムイオン抽出速度JNa2が、第2の閾値以上であるか否かを判断する。ここで、第2の閾値としては、第1の閾値よりも大きい値であって、血糖AUCの解析結果を棄却する必要が生じる値が設定される。制御部35は、ナトリウムイオン抽出速度JNa2が第2の閾値以上であると判断した場合(ステップT132においてYes)、ステップT133に処理を進め、ナトリウムイオン抽出速度JNa2が第2の閾値未満であると判断した場合(ステップT132においてNo)、ステップT134に処理を進める。
【0112】
ステップT134において、制御部35は、ステップT10で算出された、補正された血糖AUC推定値を含む解析結果を生成する。
ステップT133において、制御部35は、「解析結果の信頼性を保証できないため血糖AUCの解析結果を表示できません。再測定を行ってください」といった内容のメッセージを含む解析結果を生成する。この場合、ステップT9及びT10で算出された血糖AUCは解析結果に含まれない。
【0113】
第4実施形態によれば、被験者の発汗量に応じて異なる解析結果を出力することができる。このような構成にすることにより、汗の影響が補正できる程度の発汗であれば、補正値を用いて血糖AUC推定値を出力することができる。さらに、血糖AUCの解析結果を棄却する必要が生じる程被験者が発汗したときには、血糖AUCの解析結果を出力しない旨のメッセージを出力することにより、発汗量を抑えて再度測定を行うことを促すことができる。
【0114】
〔効果の検証〕
以下、第4実施形態に係る生体成分分析方法による測定精度の向上例について説明する。図27は、前述した発汗補正を行わなかったときの複数の被験者におけるグルコース透過率(PGlu)とナトリウムイオン抽出速度(JNa1)の相関を示すグラフであり、図28は、非穿刺部位におけるナトリウムイオン抽出速度(JNa2)と測定値乖離率との関係を示すグラフであり、図29は、上記式(2)による発汗補正を行ったときのグルコース透過率(PGlu)とナトリウムイオン抽出速度(JNa1−JNa2)の相関を示すグラフである。図27〜29及び後出する図30において、「□」は室温24℃の条件下における実験例であり、「+」は室温31℃の条件下における実験例である。
【0115】
図27は、グルコース透過率を縦軸とし、ナトリウムイオン抽出速度を横軸としたグラフである。グルコース透過率とは、本測定用収集部材10に収集されたグルコース量を採血血糖AUCで除した値である。つまり、グルコース透過率は、体内の血糖AUCに対して体外で抽出されるグルコース量の比率を示している。ナトリウムイオン抽出速度とは、単位時間あたりに本測定用収集部材100に収集されたナトリウムイオンの量である。国際公開公報2010/013808号に詳細に記載されているように、ナトリウムイオン抽出速度とグルコース透過率とは相関関係にある。図27に示すように、ナトリウムイオン抽出速度とグルコース透過率をプロットすると、一定の傾きからなる回帰直線の周辺にプロットが収束する。
【0116】
ところが、被験者が発汗すると、汗に由来するナトリウムイオンが本測定用収集部材10に余分に収集される。この傾向は、室温が高くなるほど増大する。31℃での測定においては、発汗由来のナトリウムイオン量がより多く上乗せされるため、発汗の少ない24℃での測定データに対して右方向に偏った分布となる。図27に示したプロット全てを対象として相関係数を求めたところ、相関係数は0.95であった。また、測定誤差(測定値乖離率の標準偏差)は10.8%であった。さらに、31℃における測定を行った10症例中3症例が発汗により、測定値乖離率0.8以下という低い値を示した。
図28より、31℃の場合は24℃の場合に比べ、発汗由来のナトリウムイオンの抽出速度が大幅に増大していること、及び、測定値乖離率が0.8以下の例が増加することが分かる。
【0117】
これに対し、穿刺部位のナトリウムイオン抽出速度JNa1から非穿刺部位のナトリウムイオン抽出速度JNa2を減じるという発汗補正を行うと、図29に示されるように、24℃と31℃の測定データの分布の偏りは解消し、測定精度が向上した。図29に示したプロット全てを対象として相関係数を求めたところ、相関係数は0.96であった。また、測定誤差は8.6%に減少した。さらに、測定乖離率が0.8を下回る症例がゼロとなった。
【0118】
図30は補正前と補正後のそれぞれの測定値乖離率を示すグラフである。発汗の少ない24℃では大きな変化が見られなかったが、発汗の多い31℃では、補正前の測定値乖離率の平均値は約0.87であったが、補正後の平均値は約1.0であり、測定精度が改善されたことが確認された。
【0119】
〔他の変形例〕
なお、本発明は、前述した実施の形態に限定されるものではなく、種々の変更が可能である。
【0120】
上記実施形態では、測定対象成分としてグルコースを測定した例を示したが、本発明はこれに限らず、組織液中に含まれるグルコース以外の物質の量を測定してもよい。本発明により測定される物質としては、たとえば、生化学成分や被験者に投与された薬剤などが挙げられる。生化学成分としては、生化学成分の一種であるたんぱく質の、アルブミン、グロブリンおよび酵素などが挙げられる。また、たんぱく質以外の生化学成分として、クレアチニン、クレアチン、尿酸、アミノ酸、フルクトース、ガラクトース、ペントース、グリコーゲン、乳酸、ピルビン酸およびケトン体などが挙げられる。また、薬剤としては、ジギタリス製剤、テオフィリン、不整脈用剤、抗てんかん剤、アミノ酸糖体抗生物質、グリコペプチド系抗生物質、抗血栓剤および免疫抑制剤などが挙げられる。
【0121】
また、上述した実施形態では、第1補助成分及び第2補助成分としてナトリウムイオンを用いる例を示したが、本発明はこれに限られない。
例えば、第1補助成分と第2補助成分は、異なる成分であってもよい。
第1補助成分としては、体内に一定の濃度で含まれている成分であって、微細孔の形成状態を反映する成分であればよく、ナトリウムイオンの他に、カリウムイオン、カルシウムイオン、マグネシウムイオンなどの無機イオンを用いることができる。
第2補助成分としては、汗に含まれる成分であればよく、ナトリウムイオンの他に、カリウムイオン、カルシウムイオン、マグネシウムイオンなどの無機イオン、または水分であってもよい。
【0122】
また、前述した実施の形態では、発汗測定装置60と、本測定を行う生体成分分析装置20とは別体であるが、両装置を一体化させることもできる。この場合、本測定用の収集部材10を貼付した本測定用カートリッジ40とは別に、発汗チェック用の収集部材100を貼付するための発汗チェック用カートリッジを設け、これを生体成分分析装置20の配置部22に配置することにより、生体成分分析装置20において、発汗測定及び本測定を行うようにしてもよい。さらなる変形例として、本測定用収集部材10と発汗チェック用収集部材100とを貼付可能な共通のカートリッジを設け、このカートリッジを受け入れ可能な分析装置を設けてもよい。これにより、二つの収集部材に収集された成分を同時に分析することができる。
【0123】
また、前述した実施の形態では、本測定用収集部材10と発汗チェック用収集部材100とを別体とした例を示したが、図24に示すように、これらを一体としてもよい。図24は、共通収集部材300の構成を示す斜視図である。この共通収集部材300は、本測定用の第1収集部310と発汗チェック用の第2収集部320とを備えている。第1収集部310は、前述の本測定用収集部材10と同じ構成からなり、本測定用の収集体312を備えている。第2収集部320は、前述の発汗チェック用収集部材100と同じ構成からなり、発汗チェック用の収集体322を備えている。収集体312及び収集体322は、共通保持シート330に保持されている。共通保持シート330は、前述の保持シートと同じ構成からなっている。共通保持シート330には、第1収集部310と第2収集部320とを分断するためのミシン目340が設けられている。
【0124】
この共通収集部材300は、次のようにして使用される。本測定用の収集体312が微細孔形成領域Sに位置し、発汗チェック用の収集体322が非穿刺部位Rに位置するように、共通保持シート330を被験者の皮膚に貼付する。成分の収集が終了したのち、共通収集部材300は皮膚から取り外され、ミシン目340に沿って第1収集部310と第2収集部320とに分断される。第1収集部310は生体成分分析装置20によって本測定が行われ、第2収集部320は発汗測定装置60によって発汗測定が行われる。
このように、収集部材を一体とすることにより、組織液が抽出される部位(穿刺部位S)に近い位置で汗を収集することができ、第1収集部310と第2収集部320とで、収集される汗の量の差を小さくすることができる。
【0125】
また、前述した実施の形態では、発汗測定装置によって測定されたナトリウムイオン抽出速度JNa2を、ユーザが生体成分分析装置に入力する形態を例示したが、このような形態に限られない。例えば、発汗測定装置と生体成分分析装置とを通信可能に接続し、発汗測定装置で得られた結果(データ)を生体成分分析装置の制御部に送信するように構成することもできる。
【符号の説明】
【0126】
10 収集部材
11 保持シート
12 収集体
20 生体成分分析装置
22 カートリッジ配置部
23 可動天板
24 送液部
25 廃液部
26 タンク
30 検出部
31 グルコース検出部
32 ナトリウムイオン検出部
33 表示部
34 操作ボタン
35 制御部
40 本測定用カートリッジ
100 穿刺具(微細孔形成装置)
200 微細針チップ
201 微細針
300 皮膚
301 微細孔
【技術分野】
【0001】
本発明は生体成分分析方法及び生体成分分析装置に関する。さらに詳しくは、組織液の抽出を促進する処理が施された被験者の皮膚から抽出された組織液に含まれる測定対象成分を分析する方法及び装置に関する。
【背景技術】
【0002】
従来、被験者の皮膚から抽出された組織液に含まれる測定対象成分を測定する方法が知られている(例えば、特許文献1参照)。
特許文献1には、被験者の皮膚から抽出された組織液を用いて当該被験者の血糖―時間曲線下面積を算出(推定)する方法が開示されている。この方法は、被験者の皮膚に穿刺具を用いて微細孔を形成し、微細孔が形成された皮膚にゲルからなる収集体を有する組織液収集シートを所定時間(例えば、60分以上の時間)貼り付けることにより、当該皮膚から滲み出る組織液を収集する。ついで、収集体に収集された組織液に含まれるグルコース量及びナトリウムイオン量を測定し、得られるグルコース量及びナトリウムイオン量に基づいて、被験者の血糖―時間曲線下面積を推定する。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】国際公開第2010/013808号パンフレット
【発明の概要】
【発明が解決しようとする課題】
【0004】
特許文献1記載の方法において、被験者が発汗しないことを前提としている。しかしながら、実際には、組織液の収集中に発汗する被験者も存在する。
【0005】
本発明は、このような事情に鑑みてなされたものであり、発汗した被験者における測定対象成分を正確に分析することが可能な生体成分分析方法及び生体成分分析装置を提供することを目的としている。
【課題を解決するための手段】
【0006】
本発明の生体成分分析方法は、被験者の皮膚から抽出された組織液に含まれる成分を分析する生体成分分析方法であって、
組織液の抽出を促進する処理を被験者の皮膚の一部に施す工程と、
促進処理が施された皮膚から測定対象成分を収集する工程と、
促進処理が施された皮膚から第1補助成分を収集する工程と、
促進処理が施されていない皮膚から汗に含まれる第2補助成分を収集する工程と、
収集された測定対象成分、第1補助成分及び第2補助成分に基づいて、測定対象成分を分析する工程と
を含むことを特徴としている。
【0007】
本発明の生体成分分析方法において、促進処理が施された皮膚の表面からは組織液と汗に由来する第1補助成分が収集される。一方、促進処理が施されていない皮膚の表面では、組織液がほとんど湧き出ないため、汗にのみ由来する第2補助成分が収集される。したがって、このような第1補助成分と第2補助成分を収集し、両者を比較することで、第1補助成分にどの程度の汗由来の補助成分が混在しているのかを把握することができる。これにより、仮に被験者が発汗した場合であっても、本発明の生体成分分析方法によれば、収集された測定対象成分、第1補助成分及び第2補助成分に基づいて、正確な測定対象成分の解析結果を生成することができる。
【0008】
前記第1補助成分と第2補助成分は、同じ期間に収集されることが好ましい。
前記第1補助成分と第2補助成分は、同じ腕において収集されることが好ましい。
【0009】
前記分析工程は、
収集された第2補助成分を測定して第1測定値を取得する第1測定工程と、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値より小さい場合に、収集された測定対象成分を測定して第2測定値を取得する第2測定工程と、
第1測定値が所定の閾値より小さい場合に、収集された第1補助成分を測定して第3測定値を取得する第3測定工程と、
第2及び第3測定値に基づいて、測定対象成分の量に関する値を含む解析結果を生成する工程を含むものとすることができる。
【0010】
前記分析工程は、
収集された第2補助成分を測定して第1測定値を取得する第1測定工程と、
収集された測定対象成分を測定して第2測定値を取得する第2測定工程と、
収集された第1補助成分を測定して第3測定値を取得する第3測定工程と、
第1乃至第3測定値に基づいて、測定対象成分の解析結果を生成する工程と、
を含むものとすることができる。
【0011】
前記解析結果を生成する工程は、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値以上である場合に、第2及び第3の測定値に基づく測定対象成分の量に関する値と、この値の信頼性が低いことを示す情報とを含む解析結果を生成する工程を含むものとすることができる。
【0012】
前記解析結果を生成する工程は、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程を含むものとすることができる。
【0013】
前記解析結果を生成する工程は、
第1測定値と、第1の閾値及び第1の閾値より大きい第2の閾値とを比較する工程と、
第1測定値が第1の閾値以上であり且つ第2の閾値より小さい場合に、第2及び第3の測定値に基づく測定対象成分の量に関する値と、この値の信頼性が低いことを示す情報とを含む解析結果を生成する工程と、
第1測定値が第2の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程と、
を含むものとすることができる。
【0014】
第1測定値を、第2補助成分の量に関する値とし、
第2測定値を、測定対象成分の量に関する値とし、且つ
第3測定値を、第1補助成分の量に関する値とすることができる。
【0015】
分析工程は、第1測定値及び第3測定値に基づいて得られる補正値で第2測定値を補正することにより測定対象成分の解析結果を生成するものとすることができる。
【0016】
補正値は、第3測定値から第1測定値を減ずることにより得られた値とすることができる。
量に関する値は、単位時間あたりの補助成分の抽出量とすることができる。
前記解析結果を生成する工程は、
第1測定値と、第1の閾値及び第1の閾値より大きい第2の閾値とを比較する工程と、
第1測定値が第1の閾値以上であり且つ第2の閾値より小さい場合に、第1及び第3の測定値に基づく補正値で第2測定値を補正することにより測定対象成分の解析結果を生成する工程と、
第1測定値が第2の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程と、
を含むことができる。
【0017】
前記測定対象成分をグルコースとすることができる。
前記第1補助成分及び第2補助成分を無機イオンとすることができる。
前記第1補助成分と第2補助成分を同一種類の成分とすることができる。
前記無機イオンをナトリウムイオンとすることができる。
【0018】
前記測定対象成分及び第1補助成分を、被験者の皮膚に貼付可能な貼付面を有する保持シートの当該貼付面に配置された収集体に収集することができる。
前記収集体がゲルからなることが好ましい。
【0019】
本発明の生体成分分析装置は、被験者の皮膚から抽出される組織液に含まれる成分を分析する生体成分分析装置であって、
前記成分の抽出を促進する処理が施された被験者の皮膚の一部に所定時間配置された収集部材から測定対象成分及び第1補助成分に関する情報を取得する取得部と、
この取得部において取得された測定対象成分及び第1補助成分に関する情報と、促進処理が施されていない皮膚からの汗に含まれる第2補助成分に関する情報とに基づいて、測定対象成分を分析する解析部と
を備えたことを特徴としている。
【0020】
前記第2補助成分に関する情報を取得する第2取得部を更に備えていることが好ましい。
前記第2補助成分に関する情報を受け付ける情報受付部を更に備えていることが好ましい。
【発明の効果】
【0021】
本発明の生体成分分析方法及び生体成分分析装置によれば、発汗した被験者の測定対象成分を正確に分析することができる。
【図面の簡単な説明】
【0022】
【図1】本発明の生体成分分析装置の一実施の形態の外観を示す斜視説明図である。
【図2】図1に示される生体成分分析装置のブロック図である。
【図3】本測定用カートリッジの構成を示す概略断面図である。
【図4】被験者の皮膚に微細孔を形成する微細孔形成装置の一例の斜視説明図である。
【図5】図4に示される微細孔形成装置に装着される微細針チップの斜視図である。
【図6】微細孔形成装置によって微細孔が形成された皮膚の断面説明図である。
【図7】本測定用収集部材の一例の斜視説明図である。
【図8】図7のA−A線断面図である。
【図9】発汗チェック用収集部材の一例の斜視説明図である。
【図10】第2補助成分を含むゲルの導電率を測定する原理を説明する図である。
【図11】第2補助成分を含むゲル中のナトリウムイオン濃度を測定する原理を説明する図である。
【図12】第1の実施形態の生体成分分析方法のフローチャートである。
【図13】グルコース透過率とナトリウムイオン抽出速度との相関を示すグラフである。
【図14】測定値乖離率とナトリウムイオン抽出速度JNa2との関係を示すグラフである。
【図15】測定値乖離率とNa相対値との関係を示すグラフである。
【図16】エラー症例を除外する前のグルコース透過率とナトリウムイオン抽出速度の相関を示すグラフである。
【図17】エラー症例を除外する前の推定血糖AUC値と採血血糖AUC値の相関を示すグラフである。
【図18】エラー症例を除外する前の測定値乖離率と非穿刺部位ナトリウムイオン抽出速度の関係を示すグラフである。
【図19】エラー症例を除外した後のグルコース透過率とナトリウムイオン抽出速度の相関を示すグラフである。
【図20】エラー症例を除外した後の推定血糖AUC値と採血血糖AUC値の相関を示すグラフである。
【図21】第2の実施形態の生体成分分析方法のフローチャートである。
【図22】第2の実施形態における制御部の処理を示すフローチャートである。
【図23】第3の実施形態における制御部の処理を示すフローチャートである。
【図24】共通収集部材の斜視説明図である。
【図25】第4の実施形態における生体成分分析方法のフローチャートである。
【図26】第4の実施形態における制御部の処理を示すフローチャートである。
【図27】発汗補正を行わなかったときのグルコース透過率とナトリウムイオン抽出速度との相関を示すグラフである。
【図28】非穿刺部位におけるナトリウムイオン抽出速度と測定値乖離率との関係を示すグラフである。
【図29】発汗補正を行ったときのグルコース透過率とナトリウムイオン抽出速度との相関を示すグラフである。
【図30】発汗補正前と発汗補正後の測定値乖離率を示すグラフである。
【発明を実施するための形態】
【0023】
以下、添付図面を参照しつつ、本発明の生体成分分析方法及び生体成分分析装置の実施の形態を詳細に説明する。
【0024】
(第1の実施形態)
図1は、本発明の一実施の形態に係る生体成分分析装置20の外観を示す斜視説明図であり、図2は、図1に示される生体成分分析装置のブロック図である。まず図1を参照して、生体成分分析方法の概略を説明する。
【0025】
本実施形態の生体成分分析方法は、後述するように、被験者の皮膚に微細孔を形成し、微細孔を介して組織液を抽出し、抽出された組織液に含まれるグルコース及びナトリウムイオンを収集し、収集されたグルコース及びナトリウムイオンの濃度に基づいて、被験者における血中グルコース(血糖)を分析する方法である。より具体的には、血糖―時間曲線下面積(血糖AUC)を算出する方法である。
【0026】
被験者が発汗すると、組織液に由来するナトリウムイオンに重畳するようにして汗由来のナトリウムイオンが収集され、ナトリウムイオン濃度が高くなる。本実施形態の生体成分分析方法では、グルコースとともに収集されたナトリウムイオンに基づいて被験者の血糖―時間曲線下面積を推定するため、汗由来のナトリウムイオンが過剰に収集されると、算出される血糖AUCの信頼性が低下することがある。
【0027】
そこで、本実施形態の方法では、微細孔が形成された皮膚Sに本測定用収集部材10を貼り付けるとともに、微細孔が形成されていない皮膚Rに発汗チェック用収集部材100を貼り付ける。この状態で、本測定用収集部材10に、組織液に含まれるグルコース及びナトリウムイオンを収集する。同時に、発汗チェック用収集部材100に、微細孔が形成されていない皮膚からの汗に含まれるナトリウムイオンを収集する。そして、発汗チェック用収集部材100に収集されたナトリウムイオンを測定(以下、発汗測定ともいう)し、ナトリウムイオン濃度が閾値よりも高いときには、本測定用収集部材10に収集されたグルコース濃度及びナトリウムイオンの濃度の測定(以下、本測定ともいう)、並びにこれらに基づく血糖AUCの解析を行わないように促すエラーメッセージを表示することとしている。これにより、信頼性の低い血糖AUCの解析結果が出力されることが回避される。
【0028】
〔生体成分分析装置〕
この生体成分分析装置20は、後述する本測定用収集部材10の収集体12に収集された組織液に含まれるグルコース及びナトリウムイオンを測定(以下、本測定と呼称することがある)して、グルコース濃度(CGlu)及びナトリウムイオン濃度(CNa1)を取得し、取得したCGlu及びCNa1に基づいて、被験者の血糖―時間曲線下面積(以下、血糖AUCともいう)を算出し、血糖AUCを含む解析結果を生成して表示する装置である。生体成分分析装置20は、検出部30と、解析部を含む制御部35と、解析結果やエラーメッセージなどを表示する表示部33と、測定開始の指示などを行うための操作部としての操作ボタン34とを備えている。
【0029】
生体成分分析装置20は、厚みのある直方体形状の筐体を備えており、筐体上面の天板には凹部21が形成されている。凹部21には、当該凹部21よりもさらに深く形成された凹部からなるカートリッジ配置部22が設けられている。さらに凹部21には、当該凹部21の側壁の高さとほぼ同じ厚みを有する可動天板23が連結されている。可動天板23は、支軸23aを中心に折り畳むことによって、図1に示される状態から凹部21内に収納し、又は凹部21に収納された状態から図1に示されるように起立させることができる。カートリッジ配置部22は、後述する本測定用カートリッジ40を収納することができる大きさを有している。
【0030】
可動天板23は、凹部21に収納される方向に付勢されるように、支軸23aに支持されている。したがって、カートリッジ配置部22に配置された本測定用カートリッジ40は、可動天板23によって上方から押さえつけられる。
【0031】
検出部30は、本測定用収集部材10の収集体12に収集された組織液に含まれる成分の情報を取得するものであり、測定対象成分であるグルコースの濃度CGluを検出するグルコース検出部31と、第1補助成分であるナトリウムイオンの濃度CNa1を検出するナトリウムイオン検出部32とを備えている。
【0032】
グルコース検出部31は、可動天板23の裏面、すなわち可動天板23が凹部21に収納されたときにカートリッジ配置部22と対向する側の面に設けられている。グルコース検出部31は、光を照射するための光源31aと、この光源31aによって照射された光の反射光を受光するための受光部31bとを備えている。これにより、グルコース検出部31は、カートリッジ配置部22に配置された本測定用カートリッジ40に対して光を照射するとともに、照射された本測定用カートリッジ40からの反射光を受光できるように構成されている。
【0033】
ナトリウムイオン検出部32は、カートリッジ位置部22の底面に設けられている。ナトリウムイオン検出部32は、カートリッジ配置部22の底面に設けられた長方形状を有する板状の部材を備え、この板状部材の略中央には一対のナトリウムイオン濃度測定用電極が設けられている。ナトリウムイオン濃度測定用電極は、ナトリウムイオン選択膜を備えた銀/塩化銀からなるナトリウムイオン選択性電極と、対電極である銀/塩化銀電極を含んでいる。
【0034】
制御部35は、生体成分分析装置20の内部に設けられており、解析部であるCPUや、記憶部であるROM、RAMなどを含んでいる。CPUは、ROMに記憶されたプログラムを読み出して実行することにより、各部の動作を制御する。RAMは、ROMに記憶されたプログラムが実行される際のプログラムの展開領域として利用される。
【0035】
生体成分分析装置20は、その内部にポンプからなる供給部24、本測定用収集部材10の収集体12に収集された組織液を回収するための純水からなる回収液を収容するタンク26、及び廃液を収容する廃液タンク25を備えている。供給部24は、タンク26に空気を送り込むことにより、ニップル24aを介して、カートリッジ配置部22に配置された本測定用カートリッジ40にタンク26内に収容されている回収液を注入する。
【0036】
廃液タンク25は、供給部24によって本測定用カートリッジ40に送液された純水が排出される機構であり、ニップル25aを介して、排出された液体を収容する。
【0037】
図3は、カートリッジ配置部22に本測定用カートリッジ40が配置された状態を示す概略断面図である。まず図3を参照して本測定用カートリッジ40の構成について説明する。
【0038】
本測定用カートリッジ40は、主な構成として、ゲル収容部42と、グルコース反応体41と、光導波部材44とを備えている。ゲル収容部42は、本測定用カートリッジ40の表面に形成された凹部からなる。ゲル収容部42の底部には、カートリッジ配置部22に設けられたニップル24aと連通する注入孔42aが設けられている。本測定用カートリッジ40の下面にはゲル収容部42と連通する溝が形成されている。この溝とカートリッジ配置部22の底部に設けられたナトリウムイオン検出部32とによって流路43aが形成される。この流路43aの一部は、ナトリウムイオン検出部32によりナトリウムイオン濃度が検出される第1貯留部43とされている。流路43aの下流は、第2貯留部45に連通している。第2貯留部45は本測定用カートリッジ40の表面に設けられた凹部からなり、その開口が光導波路を有する光導波部材44によって閉塞されている。この光導波部材44の下面に、グルコースと反応して変色するグルコース反応体41が設けられている。第2貯留部の底部には、カートリッジ配置部22に設けられたニップル25aと連通する排出孔45aが設けられている。
【0039】
生体成分分析装置20は、次のようにして本測定用収集部材10に収集された組織液に含まれるグルコースの濃度CGlu及びナトリウムイオンの濃度CNa1を測定する。まず、図1において、一点鎖線で示されるように、被験者の皮膚Sに所定時間貼り付けられた本測定用収集部材10が皮膚から取り外され、本測定用カートリッジ40のゲル収容部42に貼り付けられる。この本測定用カートリッジ40が生体成分分析装置20のカートリッジ配置部22に配置され、可動天板23が閉じられる。
【0040】
操作ボタン34によって測定開始が指示されると、供給部34からタンク26に向けて空気が供給され、タンク26からニップル24aに向けて回収液が送られる。回収液は注入孔42aからゲル収容部42に注入され、ゲル収容部42が回収液で満たされる。この状態で所定時間が経過すると、収集体12に収集された組織液が回収液に拡散する。所定時間が経過したら、供給部24はバイパス路24aを介してゲル収容部42に空気を送り込む。これにより、ゲル収容部42内の液体が流路43aを通じて第1貯留部43および第2貯留部45に送液される。
【0041】
ナトリウムイオン検出部32は、ナトリウムイオン濃度測定用電極によって第1貯留部43に貯留された液体に一定電圧を印加して電流値を取得する。このときの電流値は、液体に含まれるナトリウムイオン濃度に比例する。ナトリウムイオン検出部32は、得られた電流値を検出信号として制御部35に出力する。制御部35は、検出信号に含まれる電流値と予め制御部35の記憶部に記憶されている検量線とに基づいて、ナトリウムイオン濃度CNa1を取得する。
【0042】
第2貯留部では、回収液中のグルコースとグルコース反応体41とが反応し、グルコース反応体41が変色する。グルコース検出部31は、光源31aから光導波部材44に向かって光を照射し、光導波部材44から出射した光を受光部31bによって受光する。光源31aから光が照射されると、光は、変色したグルコース反応体41により吸光されながら、光導波部材44の内部で反射を繰り返して受光部31bに入射する。受光部31bにおける受光量はグルコース反応体41の変色度合いに比例し、この変色度合いが回収液中のグルコース量に比例する。グルコース検出部31は、得られた受光量を検出信号として制御部35に出力する。制御部35は、検出信号に含まれる受光量と予め制御部35の記憶部に記憶されている検量線とに基づいてグルコース濃度CGluを取得する。
【0043】
ナトリウムイオン濃度CNa1およびグルコース濃度CGluが取得されると、供給部24から本測定用カートリッジ40にさらに空気が送り込まれる。これにより回収液が排出孔45aおよびニップル25aを介して廃液タンク25に送られ、一連の測定が終了する。
【0044】
〔微細孔形成装置〕
つぎに被験者の皮膚に微細孔を形成する微細孔形成装置の一例について説明する。微細孔形成装置は、被験者の皮膚の一部に多数の微細な孔を形成して当該被験者の皮膚からの組織液の抽出を促進する装置である。本実施形態では、組織液抽出促進のための微細孔が形成された被験者の皮膚S(図1参照)からグルコース及びナトリウムイオンが収集されるとともに、後述するように、微細孔が形成されていない被験者の皮膚Rからの汗に含まれるナトリウムイオンが収集される。
【0045】
図4は、本発明の生体成分分析方法において被験者の皮膚に組織液抽出促進用の微細孔を形成するのに用いられる微細孔形成装置の一例に係る穿刺具100の斜視説明図であり、図5は、図4に示される穿刺具100に装着される微細針チップ200の斜視図であり、図6は、穿刺具100によって微細孔が形成された皮膚Sの断面説明図である。
【0046】
図4〜6に示されるように、穿刺具100は、滅菌処理された微細針チップ200を装着して、当該微細針チップ200の微細針201を生体の表皮(被験者の皮膚300)に当接させることによって、被験者の皮膚300に組織液の抽出孔(微細孔301)を形成する装置である。微細針チップ200の微細針201は、穿刺具100により微細孔301を形成した場合に、当該微細孔301が皮膚300の表皮内にとどまり真皮までは到達しないような大きさを有する。
【0047】
図4に示されるように、穿刺具100は、筐体101と、この筐体101の表面に設けられたリリースボタン102と、筐体101の内部に設けられたアレイチャック103及びバネ部材104とを備えている。筐体101の下部101aの下端面(皮膚に当接する面)には、前記微細針チップ200が通過可能な開口(図示せず)が形成されている。バネ部材104はアレイチャック103を穿刺方向に付勢する機能を有する。アレイチャック103は下端に微細針チップ200を装着することができる。微細針チップ200の下面には、複数の微細針201が形成されている。微細針チップ200の下面は、10mm(長辺)×5mm(短辺)の大きさからなる。また、穿刺具100は、アレイチャック103をバネ部材104の付勢力に逆らって上方(反穿刺方向)に押し上げた状態で固定する固定機構(図示せず)を有しており、使用者(被験者)がリリースボタン102を押下することにより、当該固定機構によるアレイチャック103の固定が解除され、バネ部材104の付勢力によって当該アレイチャック103が穿刺方向に移動し、前記開口から突出した微細針チップ200の微細針201が皮膚を穿刺するように構成されている。なお、図4において、105は筐体101の下部101aに形成された鍔部であり、穿刺具100の使用時には前記鍔部105の裏面が被験者の皮膚の所定箇所に当接される。
【0048】
〔本測定用収集部材〕
つぎに被験者の皮膚から組織液を収集する本測定用収集部材10について説明する。本測定用収集部材10は被験者の皮膚から組織液を収集するために当該被験者の皮膚に貼付され、所定時間経過後に皮膚から剥がされるものである。
【0049】
図7は、保持シート11と、この保持シート11に保持された収集体12とを備えた本測定用収集部材10の斜視説明図であり、図8は、図7のA−A線断面図である。
【0050】
収集体12は、被験者の皮膚から抽出した組織液を保持可能な保水性を有するゲルからなっており、抽出媒体としての純水を含有している。このゲルは、組織液を収集することが可能であれば特に限定されないが、ポリビニルアルコールやポリビニルピロリドンからなる群より選ばれる少なくとも一種の親水性ポリマーから形成されたゲルが好ましい。ゲルを形成する親水性ポリマーは、ポリビニルアルコール単独又はポリビニルピロリドン単独であってもよく、また両者の混合物であってもよいが、ポリビニルアルコール単独又はポリビニルアルコールとポリビニルピロリドンとの混合物であることがより好ましい。
【0051】
ゲルは、親水性ポリマーを水溶液中で架橋する方法により形成することができる。ゲルは、親水性ポリマーの水溶液を基材上に塗工して塗膜を形成し、該塗膜中に含まれる親水性ポリマーを架橋する方法により形成することができる。親水性ポリマーの架橋法としては、化学架橋法や放射線架橋法などがあるが、ゲル中に各種化学物質が不純物として混入し難い点より、放射線架橋法を採用することが望ましい。
【0052】
収集体12は、図7〜8に示される例では直方体形状を呈しており、皮膚と当接する面のサイズは7mm×12mmである。ただし、収集体12の形状及びサイズは、これに限定されるものではない。
【0053】
保持シート11は、小判形状のシート本体11aと、このシート本体11aの片面に形成された粘着剤層11bとで構成されており、前記粘着剤層11bが形成された側の面が粘着面とされている。収集体12は、同じく小判形状の、台紙としても機能する剥離シート13のほぼ中央に配設されており、この収集体12を覆うように前記保持シート11が剥離シート13に貼付されている。収集体12は、保持シート11の粘着面の一部によって当該保持シート11に保持されている。保持シート11の面積は、組織液収集時における収集体12の乾燥を防ぐために、収集体12を覆うことが可能な大きさを有している。すなわち、保持シート11によって収集体12を覆うことにより、組織液収集時に皮膚と保持シート11との間を気密に保つことができ、組織液収集時に収集体12に含まれる水分が蒸発するのを抑制することができる。
【0054】
保持シート11のシート本体11aは、無色透明又は有色透明であり、当該シート本体11aの表面側(粘着剤層11bと反対側の面)から、保持シート11に保持されている収集体12を目視にて容易に確認することができる。シート本体11aは、組織液の蒸発や収集体の乾燥を防ぐため透湿性が低いものが好ましい。シート本体11aの材質としては、例えばポリエチレンフィルム、ポリプロピレンフィルム、ポリエステルフィルム、ポリウレタンフィルムなどが挙げられ、その中でもポリエチレンフィルム、ポリエステルフィルムが好ましい。シート本体11aの厚さは、特に限定されないが、概ね0.025〜0.5mm程度である。
【0055】
本測定用収集部材10は、収集体12が被験者の微細孔形成領域R(組織液の抽出を促進させるために穿刺具100によって被験者の皮膚300に複数の微細孔301が形成された領域)に配置されるように、保持シート11の粘着面によって当該被験者の皮膚300に貼付される。そして、収集体12を微細孔形成領域に配置した状態で所定時間、例えば60分以上、好ましくは180分以上放置することにより、微細孔を介して抽出される組織液に含まれる成分を当該収集体12に収集する。
【0056】
〔発汗チェック用収集部材〕
つぎに被験者の皮膚から汗を収集する発汗チェック用収集部材100について説明する。図9は、本実施形態における発汗チェック用収集部材100の構成を示す斜視図である。発汗チェック用収集部材100は、上述の本測定用収集部材10と同じ構成を備えており、保持シート110と、この保持シート110に保持された収集体120と剥離シート130とを備えている。発汗チェック用収集部材100の各部の構成については、図7および図8に示した本測定用収集部材10と同様であるため、詳細な説明は省略する。
【0057】
〔発汗測定装置〕
図10は、本実施形態の生体成分分析方法に用いられる発汗測定装置の概略説明図である。発汗測定装置60は、発汗チェック用収集部材100の収集体120が載せられる基台60a、基台60aの上面に設けられた対向電極61a及び61b、交流電源62a、対向電極61a及び61b間の電圧を計測する電圧計62b、解析部60b及び表示部60cを備えている。基台60a上に収集体120が載置されると、対向電極61a及び61bが収集体120に差し込まれ、対向電極61aと61bとが収集体120を通じて短絡する。この状態で交流電源62aによって電圧が印加されると、対向電極61a及び61b間の電圧が電圧計62bによって計測される。解析部60bは、計測された電圧値と検量線とに基づいて、発汗チェック用収集部材100の収集体12に収集されたナトリウムイオンの濃度CNa2を解析し、表示部に60cにナトリウムイオン濃度CNa2を表示させる。
【0058】
また、発汗測定装置として、図11に示されるように、ナトリウムイオン選択膜を備えた銀/塩化銀からなるナトリウムイオン選択性電極63と、対電極である銀/塩化銀電極64とからなる一対のナトリウムイオン濃度測定用電極を備えていてもよい。
【0059】
〔生体成分分析方法〕
つぎに本発明の第1実施形態の生体成分分析方法の一実施の形態について説明する。
図12は、第1の実施の形態に係る生体成分分析方法のフローチャートである。
【0060】
まずステップS1において、図4に示される穿刺具を用いて被験者の皮膚に微細孔が形成される。具体的には、被験者の皮膚300をアルコールなどを用いて清拭し、測定結果の外乱要因となる物質(塵など)を除去する。その後、当該被験者の皮膚に、前述した微細針チップ200を装着した穿刺具100の鍔部105を配置し、ついでリリースボタン102を押圧して微細針チップ200の微細針201を被験者の皮膚300に接触させることで、当該皮膚300に微細孔301を形成する。かかる微細孔を形成することで、皮膚300からの組織液の抽出を促進させることができる。
【0061】
ついで、ステップS2において、穿刺具100を被験者の皮膚300から離し、その後微細孔301が形成された領域S(微細孔形成領域)に収集体12が配置されるように、本測定用収集部材10の保持シート11を被験者の皮膚300に貼付する(図1参照)。
【0062】
ついで、ステップS3において、発汗チェック用収集部材100を非穿刺部位R、例えば被験者の微細孔形成領域近傍の皮膚に貼付する。微細孔は、通常、被験者の腕に形成される。本測定用収集部材10と、発汗チェック用収集部材100とを別々の腕に貼付することも可能であるが、できるだけ測定条件を同じにするという観点からは、本測定用収集部材10と、発汗チェック用収集部材100とを、同じ腕に貼付することが好ましい。同じ腕に貼付することで、右腕と左腕とで発汗量が異なる場合であっても、本測定用収集部材10と発汗チェック用収集部材100とで、収集される汗由来のナトリウムイオンの量の差を小さくすることができる。
【0063】
ついで、ステップS4において、本測定用収集部材10中に被験者の皮膚からの組織液が抽出され、組織液に含まれるグルコース及びナトリウムイオンが本測定用収集部材10の収集体12に収集され、蓄積される。このとき、被験者が発汗した場合には、組織液とともに被験者の皮膚から、汗に含まれるナトリウムイオンも本測定用収集部材10中に収集される。同時に、発汗チェック用収集部材100によって、汗に含まれるナトリウムイオンが収集される。収集時間は、例えば60分〜180分程度である。
【0064】
ついで、ステップS5において、本測定用収集部材10及び発汗チェック用収集部材100を被験者の皮膚から取り外す。
【0065】
ステップS6〜S11は、ステップS4において収集された各成分を分析する工程である。
まず、ステップS6において、被験者の皮膚から取り外された発汗チェック用収集部材100が発汗測定装置60にセットされる。発汗測定装置60の対向電極61a及び61bが、発汗チェック用収集部材100の収集体120に埋設されるように、発汗チェック用収集部材100が発汗測定装置60にセットされる。
【0066】
ついで、ステップS7において、発汗チェック用収集部材100の収集体120の導電率を測定することで、収集体120に含まれるナトリウムイオン濃度CNa2を測定する。ゲルの導電率から推定したナトリウムイオン量は、イオンクロマトグラムを用いて別途測定をしたナトリウムイオン量と高い相関関係を有することが確認されている。したがって、ゲルの導電率を測定するという比較的簡便な方法で、ゲル中のナトリウムイオン量を推定することができる。発汗測定装置60によって測定されたナトリウムイオン濃度CNa2は、表示部60cに表示される。
【0067】
ついで、ステップS8において、ステップS7において測定されたナトリウムイオン濃度CNa2が操作ボタン34によって生体成分分析装置20に入力される。ついで、ステップS8において、制御部35は、入力されたナトリウムイオン濃度CNa2が所定の閾値よりも高いか否かの判断をする。制御部35は、ナトリウムイオン濃度CNa2が閾値よりも高いと判断すると、表示部33にエラーメッセージ(発汗量が多いので、本測定を行っても精度が保証できない旨)を表示する。本測定(グルコース濃度CGlu及びナトリウムイオン濃度CNa1の測定、並びに血糖AUC推定値の算出)は、上述の本測定用カートリッジ40を用いて行われる。本測定用カートリッジ40は、グルコース反応体41を含む使い捨てのカートリッジであるので、発汗量のチェックを行って精度の低い分析の中止を促すことで、本測定用カートリッジ40の無駄な消費を抑えることができる。閾値は、後述する血糖AUC推定値、採血による血糖AUC及び発汗量についての実験データなどから、例えば、以下に述べるようにして予め求めることができる。
【0068】
〔閾値の設定〕
発汗の多い症例と発汗の少ない症例とを分類するための指標としては、(1)非穿刺部位におけるナトリウムイオン抽出速度(単位時間あたりに発汗チェック用収集部材100に収集されたナトリウムイオンの総量)に対する閾値、及び(2)本測定用収集部材10に収集されたナトリウムイオンの濃度CNa1から得られるナトリウムイオン抽出速度に対する非穿刺部位のナトリウムイオン抽出速度(単位時間あたりに発汗チェック用収集部材100に収集されたナトリウムイオンの総量)の相対値(以下、「Na相対値」という)のいずれかを用いることができる。これらの指標に対して閾値を設定し、被験者から得られた指標と閾値とを比較することにより、グルコース濃度CGlu及びナトリウムイオン濃度CNa1に基づいて信頼性の高い血糖AUCが得られるか否かを判断することができる。かかる閾値は、実験により予め求めることができる。以下、実験的に設定される閾値の例を説明する。
【0069】
図13は、複数の症例に関するグルコース透過率(縦軸)と、ナトリウムイオン抽出速度(横軸)との関係を示すグラフである。図14は、図13のデータを、ナトリウムイオン抽出速度JNa2に対する閾値に基づいて区分したグラフである。図15は、図13のデータを、相対Na値に対する閾値に基づいて区分したグラフである。
図13〜15のデータを得るにあたっては、本実施形態における組織液および汗に含まれる成分の収集と並行して、所定時間毎に複数回採血を行った。組織液に含まれるグルコース及びナトリウムイオン並びに後述の式(1)に基づいて血糖AUCを算出した(推定血糖AUCという)。また、複数回の採血によって得られた複数時点における血糖値から周知の台形近似法によって血糖AUCを算出した(採血血糖AUCという)。
【0070】
図13の縦軸に示したグルコース透過率とは、本測定用収集部材10に収集されたグルコース量を採血血糖AUCで除した値である。つまり、グルコース透過率は、体内の血糖AUCに対して体外で抽出されるグルコース量の比率を示している。一方、ナトリウムイオン抽出速度とは、単位時間あたりに本測定用収集体10に収集されたナトリウムイオンの量のことである。
【0071】
図13に示した症例の中から、発汗が多い例(記号◆)と、発汗が少ない例(記号▲)とを抽出した。それぞれの測定結果を、以下の表1に示す。
【0072】
【表1】

【0073】
なお、Na相対値は、次の式に基づいて求めた。
Na相対値={(JNa2)−(定数γ)}÷(JNa1)
ここで、定数γ=0.047として計算した。ナトリウムイオンは全く発汗しない場合でも皮膚からわずかな量だけ検出されるが、定数γは、このような場合に検出されるNa値の誤差を除去することができる値が用いられる。
【0074】
<ナトリウムイオン抽出速度JNa2に対する閾値>
ナトリウムイオン抽出速度JNa2に対する閾値の一例として、0.04(μmol/h)なる値を用いた。つまり、発汗チェック用収集体に収集された単位時間あたりのナトリウムイオン量が0.04(umol/h)を超える症例が除外される。この閾値を用いて図13に示される症例を区分した。結果を図14に示す。
【0075】
図14において、縦軸は測定値乖離率、横軸は非穿刺部位におけるナトリウムイオン抽出速度JNa2である。測定値乖離率は、各症例について測定した推定血糖AUCと採血血糖AUCとの比であり、これが1に近いほど推定血糖AUCの信頼性が高いことを示す。図14に示されるように、ナトリウムイオン抽出速度JNa2に対する閾値を0.04とすることにより、測定値乖離率が0.8を下回るような信頼性の低い測定結果を多数排除することができる。
【0076】
<Na相対値に対する閾値>
Na相対値に対する閾値の一例として、0.045なる値を用いた。この閾値を用いて図13に示される症例を区分した。結果を図15に示す。図15において、縦軸は測定値乖離率、横軸はNa相対値である。
図15に示されるように、Na相対値に対する閾値を0.045とすることにより、測定値乖離率が0.8を下回るような信頼性の低い測定結果を多数排除することができる。
【0077】
ナトリウムイオン抽出速度JNa2に対する閾値を用いる場合には、発汗量の多い症例を、ナトリウムイオン抽出速度JNa1を測定することなく除外することができる。したがって、信頼性の低い解析結果となることが予見されるような症例について、無駄な本測定を回避できる利点がある。
【0078】
Na相対値に対する閾値を用いる場合には、ナトリウムイオン抽出速度JNa1に対してナトリウムイオン抽出速度JNa2の影響が相対的に大きい症例のみを排除することができる。したがって、ナトリウムイオン抽出速度JNa2の絶対値は比較的大きいものの、本測定への影響が小さいと考えられる症例については、本測定の結果を棄却することなく、本測定の結果を有効に活用することができる。
なお、第1実施形態においては、ナトリウムイオン抽出速度JNa2に対する閾値を用いて、発汗量の多い症例を除外する形態を説明する。
【0079】
図12に戻って、ナトリウムイオン抽出速度JNa2が閾値以下である場合(ステップS8において「No」)、ステップS10において、本測定用収集部材10が本測定用カートリッジ40の所定箇所に貼付され、当該本測定用カートリッジ40が生体成分分析装置20のカートリッジ配置部22にセットされる。
【0080】
ついで、ステップS11において、生体成分分析装置20によって上述した測定処理が実行されることにより、グルコース濃度CGlu及びナトリウムイオン濃度CNa1が測定される。ついで、制御部35は、グルコース濃度CGlu及びナトリウムイオン濃度CNa1と下記式(1)とに基づいて血糖AUCを算出する。
AUC=CGlu×V/{α×(CNa1×V/t)+β} ・・・(1)
式(1)において、Vは本測定用収集部材10の収集体12の体積である。α及びβは実験により求められる定数である。式(1)に基づいて血糖AUCが算出される原理については、国際公開公報第2010/013808号に詳細に説明されている。国際公開公報第2010/013808号は本明細書において参照として組み込まれる。
ついで、ステップS12において、算出された結果が制御部35によって表示部33に出力される。
【0081】
本実施の形態では、微細孔形成処理が施されていない皮膚Rからの汗に含まれるナトリウムイオンを収集し、収集されたナトリウムイオン濃度が閾値よりも高い場合に本測定(CGlu及びCNa1の測定並びに血糖AUCの解析)を行わないようにすることで、信頼性の低い血糖AUC解析を回避することができる。
【0082】
〔効果の検証〕
以下、第1実施形態による生体成分分析方法による測定精度の向上例について説明する。 図16は、乖離症例を除外する前のグルコース透過率とナトリウムイオン抽出速度の相関を示すグラフである。図17は、推定血糖AUC値と採血血糖AUC値(測定血糖AUC値)の相関を示すグラフである。図18は、測定値乖離率と非穿刺部位におけるナトリウムイオン抽出速度の関係を示すグラフである。図19は、図16に対応するグラフであり、乖離症例を除外したグルコース透過率とナトリウムイオン抽出速度の相関を示すグラフである。図20は、図17に対応するグラフであり、乖離症例を除外した推定血糖AUCと採血血糖AUCの相関を示すグラフである。
【0083】
図16〜18において、「●」は糖尿病患者の症例であり、「×」は健常人の症例である。また、○で囲んだものが乖離症例(発汗量が多く、測定値乖離率が1から大きく離れている症例)である。乖離症例は、すべて糖尿病患者に認められた。
図16〜20のデータを得るにあたっては、本実施形態における組織液および汗に含まれる成分の収集と並行して、所定時間毎に複数回採血を行った。組織液に含まれるグルコース及びナトリウムイオン並びに上述の式(1)に基づいて血糖AUCを算出した(推定血糖AUCという)。また、複数回の採血によって得られた複数時点における血糖値から周知の台形近似法によって血糖AUCを算出した(採血血糖AUCという)。
【0084】
図16は、グルコース透過率を縦軸とし、ナトリウムイオン抽出速度を横軸としたグラフである。グルコース透過率とは、本測定用収集部材10に収集されたグルコース量を採血血糖AUCで除した値である。つまり、グルコース透過率は、体内の血糖AUCに対して体外で抽出されるグルコース量の比率を示している。ナトリウムイオン抽出速度とは、単位時間あたりに本測定用収集部材100に収集されたナトリウムイオンの量である。国際公開公報2010/013808号に詳細に記載されているように、ナトリウムイオン抽出速度とグルコース透過率とは相関関係にある。図16に示すように、ナトリウムイオン抽出速度とグルコース透過率をプロットすると、一定の傾きからなる回帰直線の周辺にプロットが収束する。
【0085】
被験者が発汗すると、汗に由来するナトリウムイオンが本測定用収集部材10に余分に収集される。その結果、図16に丸印で示したように、ナトリウムイオン抽出速度のみが増大し、回帰直線に対してプロットが右側にシフトする。図16に示したプロット全てを対象として相関係数を求めたところ、相関係数は0.81であった。
【0086】
図16に示したデータについて、推定血糖AUC値と採血血糖AUC値の相関を調べた。結果を図17に示す。
図17は、推定血糖AUCを縦軸とし、横軸を採血血糖AUCを横軸としたグラフである。図17に丸印で示したように、発汗の多い症例はナトリウムイオン濃度の増大に起因して、推定血糖AUCと血糖AUCとの乖離が大きい。図17に示した全症例について相関係数を求めたところ、相関係数は0.68であった。
【0087】
図18は、測定値乖離率を縦軸とし、非穿刺部位におけるナトリウムイオン抽出速度を横軸としたグラフである。図18に示した測定値乖離率とは、図17に示した推定血糖AUCを採血血糖AUCで除した値である。測定値乖離率が1に近いほど、推定血糖AUCの信頼性が高いことを意味する。図18に示すように、測定値乖離率は、非穿刺部位におけるナトリウムイオン抽出速度が増大するにしたがって、低下している。そこで、本例では、非穿刺部位におけるナトリウムイオン抽出速度が0.06(μmol/h)を超える5症例10部位のデータを解析対象から除外し、再度解析を行った。その結果を図19及び図20に示す。
【0088】
5症例10部位の乖離症例を解析対象から除外すると、図19に示されるように、グルコース透過率とナトリウムイオン抽出速度との相関係数が0.81から0.90に向上した。さらに、図20に示されるように、推定血糖AUC値と血糖AUC値との相関係数が0.68から0.82に向上した。このことから、発汗チェック用収集部材100に収集されたナトリウムイオン量に基づいて、発汗の多い症例についての本測定を回避することにより、信頼性の低い血糖AUC推定値の解析がユーザに提供されることが防止されることが実証された。
【0089】
(第2の実施形態)
つぎに本発明の第2実施形態の生体成分分析方法について説明する。図21は、第2の実施形態に係る生体成分分析方法のフローチャートである。
第1の実施形態では、発汗測定の結果(JNa2)に基づいて、本測定(CGlu及びCNa1の測定)及び血糖AUCの算出を実行するか否かを決定する形態を例示した。第2の実施形態では、発汗測定及び本測定を実行したうえで、血糖AUCの信頼性に関する情報を血糖AUCの解析結果とともに出力する。
【0090】
図21のフローチャートにおいて、ステップS101〜105の工程は、図12に示した第1実施形態におけるステップS1〜5と同じであるから、ステップS101〜S105については詳細な説明を省略し、ステップS106〜S111の分析工程について詳細に説明する。ステップS106〜S111は、ステップS104において収集された成分を分析する工程である。
【0091】
まず、ステップS106において、発汗チェック用収集部材100が発汗測定装置60にセットされ、ステップS107において、収集体120に収集されたナトリウムイオンの濃度CNa2が測定される。ついで、ステップS108において、本測定用収集部材10が本測定用カートリッジ40の所定箇所に貼付され、本測定用カートリッジ40が生体成分分析装置20のカートリッジ配置部22にセットされる。ステップS109において、収集体12に収集されたグルコース濃度CGlu及びナトリウムイオン濃度CNa1が測定され、グルコース濃度CGlu及びナトリウムイオン濃度CNa1に基づいて血糖AUC推定値が算出される。
【0092】
ついでステップS110において、ユーザによって、ステップS107において得られたナトリウムイオン抽出速度JNa2が生体成分分析装置20に入力される。ステップS111において、制御部35によって解析結果が生成され、ステップS112において、生成された解析結果が表示部33に出力される。
【0093】
図22は、ステップS111において制御部35により実行される処理のフローチャートである。
まず、制御部35は、ステップS121において、入力されたナトリウムイオン抽出速度JNa2と閾値とを比較し、ナトリウムイオン抽出速度JNa2が閾値以上であるか否かを判断する。閾値以上であると判断した場合(ステップS121においてYES)、制御部35は、ステップS122に処理を進める。ステップS122において、制御部35は、ステップS109で算出された血糖AUCと、この血糖AUCの信頼性が低いことを示すフラグ情報とを含む解析結果を生成する。一方、ナトリウムイオン抽出速度JNa2が閾値未満であると判断した場合(ステップS122においてNO)、制御部35は、ステップS123に処理を進める。ステップS123において、制御部35は、ステップS109で算出された血糖AUCのみを含む解析結果を生成する。ナトリウムイオン抽出速度JNa2が閾値未満である場合には、血糖AUCの信頼性は高いため、解析結果にフラグ情報は含まれない。
第2実施形態によれば、被験者が血糖AUCの算出結果に影響を及ぼす程発汗した場合に、血糖AUCの信頼性が低下したことをユーザに知らせることができる。ユーザは、このフラグ情報を、出力された血糖AUCを利用するか否かの決定に役立てることができる。
なお、第2の実施形態では、JNa2を閾値と比較する形態を示したが、JNa1及びJNa2に基づいてNa相対値を求め、Na相対値と閾値とを比較する形態であってもよい。
【0094】
(第3の実施形態)
前述した第1及び第2実施形態では、1つの閾値を設定し、ナトリウムイオン抽出速度JNa2が閾値よりも高いか否かの判断をしているが、複数の段階的な閾値を設定することもできる。例えば2つの閾値(第1の閾値と、これよりも大きい第2の閾値)を設定し、ナトリウムイオン抽出速度JNa2に応じて異なる解析結果を生成するように構成してもよい。
【0095】
図23は、第3の実施形態に係る生体成分分析方法における制御部の処理を示すフローチャートである。第3の実施形態は、制御部35による処理を除いて図21のステップS101〜S112と同じであるので、ここでは説明を省略する。
【0096】
まず、ステップS131において、制御部35は、ナトリウムイオン抽出速度JNa2が第1の閾値以上であるか否かを判断する。ここで、第1の閾値としては、血糖AUCの解析結果を棄却するほどではないが、血糖AUCの解析に影響を及ぼす値が設定される。制御部35は、ナトリウムイオン抽出速度JNa2が第1の閾値以上であると判断した場合(ステップS131においてYES)、ステップS132に処理を進め、ナトリウムイオン濃度CNa2が第1の閾値未満であると判断した場合(ステップS131においてNO)、ステップS136に処理を進める。
【0097】
ステップS136において、制御部35は、ステップS109で算出された血糖AUCのみを含む解析結果を生成する。
ステップS132において、制御部35は、ナトリウムイオン抽出速度JNa2が、第2の閾値以上であるか否かを判断する。ここで、第2の閾値としては、第1の閾値よりも大きい値であって、血糖AUCの解析結果を棄却する必要が生じる値が設定される。制御部35は、ナトリウムイオン抽出速度JNa2が第2の閾値以上であると判断した場合(ステップS132においてYES)、ステップS133に処理を進め、ナトリウムイオン抽出速度JNa2が第2の閾値未満であると判断した場合(ステップS132においてNO)、ステップS134に処理を進める。
【0098】
ステップS134において、制御部35は、ステップS109で算出された血糖AUCと、この血糖AUCの信頼性が低い旨のフラグ情報を含む解析結果を生成する。
ステップS133において、制御部35は、「解析結果の信頼性を保証できないため血糖AUCの解析結果を表示できません。再測定を行ってください」といった内容のメッセージを含む解析結果を生成する。この場合、ステップS109で算出された血糖AUCは解析結果に含まれない。
【0099】
第3実施形態によれば、被験者の発汗量に応じて異なる解析結果を出力することができる。さらに、血糖AUCの解析結果を棄却する必要が生じる程被験者が発汗したときには、血糖AUCの解析結果を出力しない旨のメッセージを出力することにより、発汗量を抑えて再度測定を行うことを促すことができる。
なお、第3の実施形態では、JNa2を閾値と比較する形態を示したが、JNa1及びJNa2に基づいてNa相対値を求め、Na相対値と閾値とを比較する形態であってもよい。
【0100】
(第4の実施形態)
前述した実施の形態では、JNa2を本測定に進むか否かの判断材料として用いるか(第1の実施形態)、又は、JNa2の測定に続いて本測定を行い、JNa2の値によっては血糖AUCの解析結果の信頼性が低い旨の表示をしている(第2又は第3の実施形態)が、第1補助成分の量に関する値から、第2補助成分の量に関する値を減じるなどの補正処理を行うことで、測定対象成分の解析の精度を向上させることも可能である。
【0101】
本実施形態では、かかる補正処理を行うことで測定対象成分の解析の精度を向上させている。図25は、第4の実施形態における生体成分分析方法のフローチャートである。
ステップT1(微細孔形成処理)からステップT5(本測定用収集部材及び発汗用収集部材の取り外し)までの処理内容は、図12に示される第1の実施形態におけるステップS1からステップS5までのものと同様であるので、簡単のため、それらについての説明は省略する。
【0102】
ステップT6〜ステップT10は、ステップT4において収集された各成分を分析する工程である。本実施の形態では、分析時間を短縮するために、発汗チェック用収集部材で収集された成分と、本測定用収集部材で収集された成分とを並行して分析している。
まず、ステップT6において、被験者の皮膚から取り外された発汗チェック用収集部材100が発汗測定装置60にセットされる。発汗測定装置60の対向電極61a及び61bが、発汗チェック用収集部材100の収集体120に埋設されるように、発汗チェック用収集部材100が発汗測定装置60にセットされる。
【0103】
ついで、ステップT7において、発汗チェック用収集部材100の収集体120の導電率を測定することで、収集体120に含まれるナトリウムイオン濃度CNa2を測定する。発汗測定装置60によって測定されたナトリウムイオン濃度CNa2は、表示部60cに表示される。そして、測定されたナトリウムイオン濃度CNa2が操作ボタン34によって生体成分分析装置20に入力されると、制御部35は、入力されたナトリウムイオン濃度CNa2に基づいて以下の式に従い、非穿刺部位のナトリウムイオン抽出速度JNa2を算出する。
JNa2=CNa2×V2/t
ここで、V2は発汗チェック用収集部材100の収集体120の体積であり、tは抽出時間である。
【0104】
一方、ステップT6と並行して、ステップT8において、本測定用収集部材10が本測定用カートリッジ40の所定箇所に貼付され、当該本測定用カートリッジ40が生体成分分析装置20のカートリッジ配置部22にセットされる。
【0105】
ついで、ステップT9において、生体成分分析装置20によって上述した測定処理が実行されることにより、グルコース濃度CGlu及びナトリウムイオン濃度CNa1が測定される。ついで、制御部35は、グルコース濃度CGlu及びナトリウムイオン濃度CNa1と下記式とに基づいて、抽出グルコース量MGlu及び穿刺部位のナトリウムイオン抽出速度JNa1を算出する。
MGlu=CGlu×V1
JNa1=CNa1×V1/t
ここで、V1は本測定用収集部材10の収集体12の体積であり、tは抽出時間である。
【0106】
ついで、ステップT10において、制御部35は、ステップT7において算出されたJNa2及びステップT9において算出されたMGlu及びJNa1を用いて下記式(2)に従い補正された血糖AUC推定値を算出する。
【0107】
【数1】

【0108】
ここで、α及びβは実験により求められる定数である。
ついで、ステップT11において、制御部35によって解析結果が生成され、ステップT12において、生成された解析結果が表示部33に出力される。
【0109】
図26は、第4の実施形態に係る生体成分分析方法における制御部の処理を示すフローチャートである。
【0110】
まず、ステップT131において、制御部35は、ナトリウムイオン抽出速度JNa2が第1の閾値以上であるか否かを判断する。ここで、第1の閾値としては、血糖AUCの解析結果を棄却するほどではないが、血糖AUCの解析に影響を及ぼす値が設定される。制御部35は、ナトリウムイオン抽出速度JNa2が第1の閾値以上であると判断した場合(ステップT131においてYes)、ステップT132に処理を進め、ナトリウムイオン抽出速度JNa2が第1の閾値未満であると判断した場合(ステップT131においてNo)、ステップT136に処理を進める。
【0111】
ステップT136において、制御部35は、ステップT9で算出された血糖AUCを含む解析結果を生成する。
ステップT132において、制御部35は、ナトリウムイオン抽出速度JNa2が、第2の閾値以上であるか否かを判断する。ここで、第2の閾値としては、第1の閾値よりも大きい値であって、血糖AUCの解析結果を棄却する必要が生じる値が設定される。制御部35は、ナトリウムイオン抽出速度JNa2が第2の閾値以上であると判断した場合(ステップT132においてYes)、ステップT133に処理を進め、ナトリウムイオン抽出速度JNa2が第2の閾値未満であると判断した場合(ステップT132においてNo)、ステップT134に処理を進める。
【0112】
ステップT134において、制御部35は、ステップT10で算出された、補正された血糖AUC推定値を含む解析結果を生成する。
ステップT133において、制御部35は、「解析結果の信頼性を保証できないため血糖AUCの解析結果を表示できません。再測定を行ってください」といった内容のメッセージを含む解析結果を生成する。この場合、ステップT9及びT10で算出された血糖AUCは解析結果に含まれない。
【0113】
第4実施形態によれば、被験者の発汗量に応じて異なる解析結果を出力することができる。このような構成にすることにより、汗の影響が補正できる程度の発汗であれば、補正値を用いて血糖AUC推定値を出力することができる。さらに、血糖AUCの解析結果を棄却する必要が生じる程被験者が発汗したときには、血糖AUCの解析結果を出力しない旨のメッセージを出力することにより、発汗量を抑えて再度測定を行うことを促すことができる。
【0114】
〔効果の検証〕
以下、第4実施形態に係る生体成分分析方法による測定精度の向上例について説明する。図27は、前述した発汗補正を行わなかったときの複数の被験者におけるグルコース透過率(PGlu)とナトリウムイオン抽出速度(JNa1)の相関を示すグラフであり、図28は、非穿刺部位におけるナトリウムイオン抽出速度(JNa2)と測定値乖離率との関係を示すグラフであり、図29は、上記式(2)による発汗補正を行ったときのグルコース透過率(PGlu)とナトリウムイオン抽出速度(JNa1−JNa2)の相関を示すグラフである。図27〜29及び後出する図30において、「□」は室温24℃の条件下における実験例であり、「+」は室温31℃の条件下における実験例である。
【0115】
図27は、グルコース透過率を縦軸とし、ナトリウムイオン抽出速度を横軸としたグラフである。グルコース透過率とは、本測定用収集部材10に収集されたグルコース量を採血血糖AUCで除した値である。つまり、グルコース透過率は、体内の血糖AUCに対して体外で抽出されるグルコース量の比率を示している。ナトリウムイオン抽出速度とは、単位時間あたりに本測定用収集部材100に収集されたナトリウムイオンの量である。国際公開公報2010/013808号に詳細に記載されているように、ナトリウムイオン抽出速度とグルコース透過率とは相関関係にある。図27に示すように、ナトリウムイオン抽出速度とグルコース透過率をプロットすると、一定の傾きからなる回帰直線の周辺にプロットが収束する。
【0116】
ところが、被験者が発汗すると、汗に由来するナトリウムイオンが本測定用収集部材10に余分に収集される。この傾向は、室温が高くなるほど増大する。31℃での測定においては、発汗由来のナトリウムイオン量がより多く上乗せされるため、発汗の少ない24℃での測定データに対して右方向に偏った分布となる。図27に示したプロット全てを対象として相関係数を求めたところ、相関係数は0.95であった。また、測定誤差(測定値乖離率の標準偏差)は10.8%であった。さらに、31℃における測定を行った10症例中3症例が発汗により、測定値乖離率0.8以下という低い値を示した。
図28より、31℃の場合は24℃の場合に比べ、発汗由来のナトリウムイオンの抽出速度が大幅に増大していること、及び、測定値乖離率が0.8以下の例が増加することが分かる。
【0117】
これに対し、穿刺部位のナトリウムイオン抽出速度JNa1から非穿刺部位のナトリウムイオン抽出速度JNa2を減じるという発汗補正を行うと、図29に示されるように、24℃と31℃の測定データの分布の偏りは解消し、測定精度が向上した。図29に示したプロット全てを対象として相関係数を求めたところ、相関係数は0.96であった。また、測定誤差は8.6%に減少した。さらに、測定乖離率が0.8を下回る症例がゼロとなった。
【0118】
図30は補正前と補正後のそれぞれの測定値乖離率を示すグラフである。発汗の少ない24℃では大きな変化が見られなかったが、発汗の多い31℃では、補正前の測定値乖離率の平均値は約0.87であったが、補正後の平均値は約1.0であり、測定精度が改善されたことが確認された。
【0119】
〔他の変形例〕
なお、本発明は、前述した実施の形態に限定されるものではなく、種々の変更が可能である。
【0120】
上記実施形態では、測定対象成分としてグルコースを測定した例を示したが、本発明はこれに限らず、組織液中に含まれるグルコース以外の物質の量を測定してもよい。本発明により測定される物質としては、たとえば、生化学成分や被験者に投与された薬剤などが挙げられる。生化学成分としては、生化学成分の一種であるたんぱく質の、アルブミン、グロブリンおよび酵素などが挙げられる。また、たんぱく質以外の生化学成分として、クレアチニン、クレアチン、尿酸、アミノ酸、フルクトース、ガラクトース、ペントース、グリコーゲン、乳酸、ピルビン酸およびケトン体などが挙げられる。また、薬剤としては、ジギタリス製剤、テオフィリン、不整脈用剤、抗てんかん剤、アミノ酸糖体抗生物質、グリコペプチド系抗生物質、抗血栓剤および免疫抑制剤などが挙げられる。
【0121】
また、上述した実施形態では、第1補助成分及び第2補助成分としてナトリウムイオンを用いる例を示したが、本発明はこれに限られない。
例えば、第1補助成分と第2補助成分は、異なる成分であってもよい。
第1補助成分としては、体内に一定の濃度で含まれている成分であって、微細孔の形成状態を反映する成分であればよく、ナトリウムイオンの他に、カリウムイオン、カルシウムイオン、マグネシウムイオンなどの無機イオンを用いることができる。
第2補助成分としては、汗に含まれる成分であればよく、ナトリウムイオンの他に、カリウムイオン、カルシウムイオン、マグネシウムイオンなどの無機イオン、または水分であってもよい。
【0122】
また、前述した実施の形態では、発汗測定装置60と、本測定を行う生体成分分析装置20とは別体であるが、両装置を一体化させることもできる。この場合、本測定用の収集部材10を貼付した本測定用カートリッジ40とは別に、発汗チェック用の収集部材100を貼付するための発汗チェック用カートリッジを設け、これを生体成分分析装置20の配置部22に配置することにより、生体成分分析装置20において、発汗測定及び本測定を行うようにしてもよい。さらなる変形例として、本測定用収集部材10と発汗チェック用収集部材100とを貼付可能な共通のカートリッジを設け、このカートリッジを受け入れ可能な分析装置を設けてもよい。これにより、二つの収集部材に収集された成分を同時に分析することができる。
【0123】
また、前述した実施の形態では、本測定用収集部材10と発汗チェック用収集部材100とを別体とした例を示したが、図24に示すように、これらを一体としてもよい。図24は、共通収集部材300の構成を示す斜視図である。この共通収集部材300は、本測定用の第1収集部310と発汗チェック用の第2収集部320とを備えている。第1収集部310は、前述の本測定用収集部材10と同じ構成からなり、本測定用の収集体312を備えている。第2収集部320は、前述の発汗チェック用収集部材100と同じ構成からなり、発汗チェック用の収集体322を備えている。収集体312及び収集体322は、共通保持シート330に保持されている。共通保持シート330は、前述の保持シートと同じ構成からなっている。共通保持シート330には、第1収集部310と第2収集部320とを分断するためのミシン目340が設けられている。
【0124】
この共通収集部材300は、次のようにして使用される。本測定用の収集体312が微細孔形成領域Sに位置し、発汗チェック用の収集体322が非穿刺部位Rに位置するように、共通保持シート330を被験者の皮膚に貼付する。成分の収集が終了したのち、共通収集部材300は皮膚から取り外され、ミシン目340に沿って第1収集部310と第2収集部320とに分断される。第1収集部310は生体成分分析装置20によって本測定が行われ、第2収集部320は発汗測定装置60によって発汗測定が行われる。
このように、収集部材を一体とすることにより、組織液が抽出される部位(穿刺部位S)に近い位置で汗を収集することができ、第1収集部310と第2収集部320とで、収集される汗の量の差を小さくすることができる。
【0125】
また、前述した実施の形態では、発汗測定装置によって測定されたナトリウムイオン抽出速度JNa2を、ユーザが生体成分分析装置に入力する形態を例示したが、このような形態に限られない。例えば、発汗測定装置と生体成分分析装置とを通信可能に接続し、発汗測定装置で得られた結果(データ)を生体成分分析装置の制御部に送信するように構成することもできる。
【符号の説明】
【0126】
10 収集部材
11 保持シート
12 収集体
20 生体成分分析装置
22 カートリッジ配置部
23 可動天板
24 送液部
25 廃液部
26 タンク
30 検出部
31 グルコース検出部
32 ナトリウムイオン検出部
33 表示部
34 操作ボタン
35 制御部
40 本測定用カートリッジ
100 穿刺具(微細孔形成装置)
200 微細針チップ
201 微細針
300 皮膚
301 微細孔
【特許請求の範囲】
【請求項1】
被験者の皮膚から抽出された組織液に含まれる成分を分析する生体成分分析方法であって、
組織液の抽出を促進する処理を被験者の皮膚の一部に施す工程と、
促進処理が施された皮膚から測定対象成分を収集する工程と、
促進処理が施された皮膚から第1補助成分を収集する工程と、
促進処理が施されていない皮膚から汗に含まれる第2補助成分を収集する工程と、
収集された測定対象成分、第1補助成分及び第2補助成分に基づいて、測定対象成分を分析する工程と
を含むことを特徴とする生体成分分析方法。
【請求項2】
前記第1補助成分と第2補助成分は、同じ期間に収集される、請求項1に記載の生体成分分析方法。
【請求項3】
前記第1補助成分と第2補助成分は、同じ腕において収集される、請求項1又は2に記載の生体成分分析方法。
【請求項4】
前記分析工程は、
収集された第2補助成分を測定して第1測定値を取得する第1測定工程と、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値より小さい場合に、収集された測定対象成分を測定して第2測定値を取得する第2測定工程と、
第1測定値が所定の閾値より小さい場合に、収集された第1補助成分を測定して第3測定値を取得する第3測定工程と、
第2及び第3測定値に基づいて、測定対象成分の量に関する値を含む解析結果を生成する工程を含む、請求項1〜3のいずれか一項に記載の生体成分分析方法。
【請求項5】
前記分析工程は、
収集された第2補助成分を測定して第1測定値を取得する第1測定工程と、
収集された測定対象成分を測定して第2測定値を取得する第2測定工程と、
収集された第1補助成分を測定して第3測定値を取得する第3測定工程と、
第1乃至第3測定値に基づいて、測定対象成分の解析結果を生成する工程と、
を含む、請求項1〜3のいずれか一項に記載の生体成分分析方法。
【請求項6】
前記解析結果を生成する工程は、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値以上である場合に、第2及び第3の測定値に基づく測定対象成分の量に関する値と、この値の信頼性が低いことを示す情報とを含む解析結果を生成する工程を含む、請求項5に記載の生体成分分析方法。
【請求項7】
前記解析結果を生成する工程は、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程を含む、請求項5に記載の生体成分分析方法。
【請求項8】
前記解析結果を生成する工程は、
第1測定値と、第1の閾値及び第1の閾値より大きい第2の閾値とを比較する工程と、
第1測定値が第1の閾値以上であり且つ第2の閾値より小さい場合に、第2及び第3の測定値に基づく測定対象成分の量に関する値と、この値の信頼性が低いことを示す情報とを含む解析結果を生成する工程と、
第1測定値が第2の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程と、
を含む、請求項5に記載の生体成分分析方法。
【請求項9】
第1測定値は、第2補助成分の量に関する値であり、
第2測定値は、測定対象成分の量に関する値であり、且つ
第3測定値は、第1補助成分の量に関する値である、請求項5に記載の生体成分分析方法。
【請求項10】
分析工程は、第1測定値及び第3測定値に基づいて得られる補正値で第2測定値を補正することにより測定対象成分の解析結果を生成する、請求項9に記載の生体成分分析方法。
【請求項11】
補正値は、第3測定値から第1測定値を減ずることにより得られた値である、請求項10に記載の生体成分分析方法。
【請求項12】
量に関する値は、単位時間あたりの補助成分の抽出量である、請求項11に記載の生体成分分析方法。
【請求項13】
前記解析結果を生成する工程は、
第1測定値と、第1の閾値及び第1の閾値より大きい第2の閾値とを比較する工程と、
第1測定値が第1の閾値以上であり且つ第2の閾値より小さい場合に、第1及び第3の測定値に基づく補正値で第2測定値を補正することにより測定対象成分の解析結果を生成する工程と、
第1測定値が第2の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程と、
を含む、請求項9〜12のいずれか一項に記載の生体成分分析方法。
【請求項14】
前記測定対象成分はグルコースである、請求項1〜13のいずれか一項に記載の生体成分分析方法。
【請求項15】
前記第1補助成分及び第2補助成分は無機イオンである、請求項1〜14のいずれか一項に記載の生体成分分析方法。
【請求項16】
前記第1補助成分と第2補助成分は同一種類の成分である、請求項1〜15のいずれか一項に記載の生体成分分析方法。
【請求項17】
前記無機イオンはナトリウムイオンである請求項15に記載の生体成分分析方法。
【請求項18】
前記測定対象成分及び第1補助成分が、被験者の皮膚に貼付可能な貼付面を有する保持シートの当該貼付面に配置された収集体に収集される、請求項1〜17のいずれか一項に記載の生体成分分析方法。
【請求項19】
前記収集体がゲルからなる、請求項18に記載の生体成分分析方法。
【請求項20】
被験者の皮膚から抽出される組織液に含まれる成分を分析する生体成分分析装置であって、
前記成分の抽出を促進する処理が施された被験者の皮膚の一部に所定時間配置された収集部材から測定対象成分及び第1補助成分に関する情報を取得する取得部と、
この取得部において取得された測定対象成分及び第1補助成分に関する情報と、促進処理が施されていない皮膚からの汗に含まれる第2補助成分に関する情報とに基づいて、測定対象成分を分析する解析部と
を備えたことを特徴とする生体成分分析装置。
【請求項21】
前記第2補助成分に関する情報を取得する第2取得部を更に備えている請求項20に記載の生体成分分析装置。
【請求項22】
前記第2補助成分に関する情報を受け付ける情報受付部を更に備えている請求項20に記載の生体成分分析装置。
【請求項1】
被験者の皮膚から抽出された組織液に含まれる成分を分析する生体成分分析方法であって、
組織液の抽出を促進する処理を被験者の皮膚の一部に施す工程と、
促進処理が施された皮膚から測定対象成分を収集する工程と、
促進処理が施された皮膚から第1補助成分を収集する工程と、
促進処理が施されていない皮膚から汗に含まれる第2補助成分を収集する工程と、
収集された測定対象成分、第1補助成分及び第2補助成分に基づいて、測定対象成分を分析する工程と
を含むことを特徴とする生体成分分析方法。
【請求項2】
前記第1補助成分と第2補助成分は、同じ期間に収集される、請求項1に記載の生体成分分析方法。
【請求項3】
前記第1補助成分と第2補助成分は、同じ腕において収集される、請求項1又は2に記載の生体成分分析方法。
【請求項4】
前記分析工程は、
収集された第2補助成分を測定して第1測定値を取得する第1測定工程と、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値より小さい場合に、収集された測定対象成分を測定して第2測定値を取得する第2測定工程と、
第1測定値が所定の閾値より小さい場合に、収集された第1補助成分を測定して第3測定値を取得する第3測定工程と、
第2及び第3測定値に基づいて、測定対象成分の量に関する値を含む解析結果を生成する工程を含む、請求項1〜3のいずれか一項に記載の生体成分分析方法。
【請求項5】
前記分析工程は、
収集された第2補助成分を測定して第1測定値を取得する第1測定工程と、
収集された測定対象成分を測定して第2測定値を取得する第2測定工程と、
収集された第1補助成分を測定して第3測定値を取得する第3測定工程と、
第1乃至第3測定値に基づいて、測定対象成分の解析結果を生成する工程と、
を含む、請求項1〜3のいずれか一項に記載の生体成分分析方法。
【請求項6】
前記解析結果を生成する工程は、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値以上である場合に、第2及び第3の測定値に基づく測定対象成分の量に関する値と、この値の信頼性が低いことを示す情報とを含む解析結果を生成する工程を含む、請求項5に記載の生体成分分析方法。
【請求項7】
前記解析結果を生成する工程は、
第1測定値と所定の閾値とを比較する工程と、
第1測定値が所定の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程を含む、請求項5に記載の生体成分分析方法。
【請求項8】
前記解析結果を生成する工程は、
第1測定値と、第1の閾値及び第1の閾値より大きい第2の閾値とを比較する工程と、
第1測定値が第1の閾値以上であり且つ第2の閾値より小さい場合に、第2及び第3の測定値に基づく測定対象成分の量に関する値と、この値の信頼性が低いことを示す情報とを含む解析結果を生成する工程と、
第1測定値が第2の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程と、
を含む、請求項5に記載の生体成分分析方法。
【請求項9】
第1測定値は、第2補助成分の量に関する値であり、
第2測定値は、測定対象成分の量に関する値であり、且つ
第3測定値は、第1補助成分の量に関する値である、請求項5に記載の生体成分分析方法。
【請求項10】
分析工程は、第1測定値及び第3測定値に基づいて得られる補正値で第2測定値を補正することにより測定対象成分の解析結果を生成する、請求項9に記載の生体成分分析方法。
【請求項11】
補正値は、第3測定値から第1測定値を減ずることにより得られた値である、請求項10に記載の生体成分分析方法。
【請求項12】
量に関する値は、単位時間あたりの補助成分の抽出量である、請求項11に記載の生体成分分析方法。
【請求項13】
前記解析結果を生成する工程は、
第1測定値と、第1の閾値及び第1の閾値より大きい第2の閾値とを比較する工程と、
第1測定値が第1の閾値以上であり且つ第2の閾値より小さい場合に、第1及び第3の測定値に基づく補正値で第2測定値を補正することにより測定対象成分の解析結果を生成する工程と、
第1測定値が第2の閾値以上である場合に、測定対象成分の量に関する値を出力しない旨のメッセージを含む解析結果を生成する工程と、
を含む、請求項9〜12のいずれか一項に記載の生体成分分析方法。
【請求項14】
前記測定対象成分はグルコースである、請求項1〜13のいずれか一項に記載の生体成分分析方法。
【請求項15】
前記第1補助成分及び第2補助成分は無機イオンである、請求項1〜14のいずれか一項に記載の生体成分分析方法。
【請求項16】
前記第1補助成分と第2補助成分は同一種類の成分である、請求項1〜15のいずれか一項に記載の生体成分分析方法。
【請求項17】
前記無機イオンはナトリウムイオンである請求項15に記載の生体成分分析方法。
【請求項18】
前記測定対象成分及び第1補助成分が、被験者の皮膚に貼付可能な貼付面を有する保持シートの当該貼付面に配置された収集体に収集される、請求項1〜17のいずれか一項に記載の生体成分分析方法。
【請求項19】
前記収集体がゲルからなる、請求項18に記載の生体成分分析方法。
【請求項20】
被験者の皮膚から抽出される組織液に含まれる成分を分析する生体成分分析装置であって、
前記成分の抽出を促進する処理が施された被験者の皮膚の一部に所定時間配置された収集部材から測定対象成分及び第1補助成分に関する情報を取得する取得部と、
この取得部において取得された測定対象成分及び第1補助成分に関する情報と、促進処理が施されていない皮膚からの汗に含まれる第2補助成分に関する情報とに基づいて、測定対象成分を分析する解析部と
を備えたことを特徴とする生体成分分析装置。
【請求項21】
前記第2補助成分に関する情報を取得する第2取得部を更に備えている請求項20に記載の生体成分分析装置。
【請求項22】
前記第2補助成分に関する情報を受け付ける情報受付部を更に備えている請求項20に記載の生体成分分析装置。
【図1】


【図2】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図3】


【図4】


【図5】


【図27】


【図28】


【図29】


【図30】




【図2】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図3】


【図4】


【図5】


【図27】


【図28】


【図29】


【図30】


【公開番号】特開2011−227042(P2011−227042A)
【公開日】平成23年11月10日(2011.11.10)
【国際特許分類】
【出願番号】特願2010−217638(P2010−217638)
【出願日】平成22年9月28日(2010.9.28)
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
【公開日】平成23年11月10日(2011.11.10)
【国際特許分類】
【出願日】平成22年9月28日(2010.9.28)
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
[ Back to top ]

