生体計測装置及びその方法
【課題】 電子スピン共鳴や核磁気共鳴など種々の磁気共鳴を利用して生体の組織画像を得るための生体計測装置、並びに方法を提供する。
【解決手段】 所定の大きさの磁場を発生させる第1の磁場発生手段と、前記第1の磁場発生手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段と、計測対象生体を、RFパルスの照射に同期させて前記第1、第2の磁場発生手段の間で移動させる計測対象物移動手段と、前記RFパルスに応じて検出される信号に基づいて計測対象生体中の組織像を計測する計測手段とを有することを特徴とする生体計測装置が提供される。
【解決手段】 所定の大きさの磁場を発生させる第1の磁場発生手段と、前記第1の磁場発生手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段と、計測対象生体を、RFパルスの照射に同期させて前記第1、第2の磁場発生手段の間で移動させる計測対象物移動手段と、前記RFパルスに応じて検出される信号に基づいて計測対象生体中の組織像を計測する計測手段とを有することを特徴とする生体計測装置が提供される。
【発明の詳細な説明】
【技術分野】
【0001】
この発明は、電子スピン共鳴や核磁気共鳴など種々の磁気共鳴を利用して生体の組織画像を得るための生体計測装置に関する。
【背景技術】
【0002】
日本における酸化ストレスに関わる患者予備軍は、いまや数百万人にも上るといわれ、国民健康保険を大きく圧迫するに至っている。ここで、酸化ストレスとは生体の内因性あるいは外因性の原因により生じる活性酸素を生体が十分処理することができなくなるために生じるものである。酸化ストレスはがん、生活習慣病、虚血後再還流障害、炎症など、多くの病態や老化に関与することが知られている。
【0003】
近年、酸化ストレスと活性酸素や活性窒素種などのフリーラジカルとの関係が注目されている。活性酸素・フリーラジカルの過剰な生成等が生じると、生体内においてその生成と消去のバランスを崩し、酸化ストレスの状態となる。活性酸素・フリーラジカルは脂質や、核酸、たんぱく質、糖質などを傷害して各種疾患を誘発する。
【0004】
酸化ストレスは、ほぼすべての疾患に何らかの形でかかわっていると考えられている。しかし、その根拠は、間接的なものがほとんどで、活性酸素の産生が疾患の第一成因であるか、あるいは二次的に障害の進展に関係するのか等に関して明らかとなっていない。生体内で、どのような活性酸素が、何時、どこで、どのように産生し、何と反応するかを酸化ストレスモデル動物で無侵襲画像解析することが可能となれば、酸化ストレス疾患での活性酸素動態の解明と抗酸化性医薬品の開発に有力な情報となりうる。
【0005】
フリーラジカルを検出する装置として、ESR画像装置(ESRI)がある。ESR(Electron Spin Resonance)は、電子スピン共鳴の略称で、フリーラジカルの不対電子スピンの磁気モーメントを電磁波の共鳴吸収で観測することから、フリーラジカルのみを検出する選択性の高い分析機器である。このESR分光器を生体用に改良した生体計測ESRI装置を用いると、実験動物丸ごとで生きたままラジカルを計測し、その分布を画像解析することが可能である。
【0006】
発明者らは抗酸化作用を機序とする医薬品の開発にかかわり、その開発段階で、生体計測ESR・スピンプローブ法を用いて脳虚血−再灌流障害モデルラットでの抗酸化作用発現を明らかにすることに成功している。また、胃潰瘍モデルラットで抗潰瘍薬が胃腔内での・OH生成を抑制することも明らかとした。その他、漢方の胃潰瘍治療薬など、生体計測ESR・スピンプローブ法は抗酸化医薬品の生体内作用評価法として非常に有用である。
【0007】
すなわち、このようなフリーラジカルを検出できる生体計測装置の開発は、国民の健康福祉に直結するもので、きわめて社会的意義が大きい。また本研究は新規抗酸化性医薬品の評価・創出を可能とするもので、その経済的波及効果は計り知れないものである。
【特許文献1】特許第3117847号公報
【発明の開示】
【発明が解決しようとする課題】
【0008】
ところで、上述した従来の方法では、フリーラジカルしか見えないため、活性酸素・フリーラジカルの産生組織・部位が特定できない問題がある。この問題を解決するため、活性酸素・フリーラジカルの画像(ESRI)に臓器のMRI画像を重畳できるESRI・MRI融合型磁気共鳴画像解析装置がある。この装置を用いると、種々のルートで投与したプローブ剤の生体内挙動が画像化できる。
【0009】
また、核・電子二重共鳴装置(PEDRI)もフリーラジカルの動態の解析に有効である。PEDRIは、ESR照射により生体の電子スピンを遷移させ、核スピンへエネルギー遷移が生じさせるものである。その後MRI計測を行うことで、通常の核スピンのボルツマン分布と比較し、最大(理論値)で330倍の核スピンボルツマン分布が増強することができる。すなわち通常のMRI計測に較べ、330倍(理論値)の高感度化を図ることができる。潰瘍性大腸炎モデルに適用した結果、酸化ストレス性疾患のレドックス動態の画像解析に非常に有用であることが明らかとなっている。
【0010】
しかしながら、一般に、このようなPEDRIやERSI/MRIの複合計測装置においては、得られた画像の解像度が低いという問題がある。すなわち、米国で開発中の装置はいずれもMRIの外部磁場が数十mT(ミリテスラ)(Dr.Zweier;Ohio State University,Dr.Halpern;University of Chicago,Dr.Krishna,NIH/NCI,Dr.Swartz;Dartmouth Medical School)であり、MRIの基本特許を取得している英国Aberdeen大学のDr.Lurieの提案において500mT(ミリテスラ)(但し、試料サイズは10mm程度)である。これは、磁気共鳴の感度と解像度は外部磁場の大きさに依存するのに対して、従来の装置はいずれも、1つの磁場発生装置を用い、外部磁場変換をField Cycle法(Dr.Lurieが米国特許取得済)で行っているため、MRI装置の外部磁場を大きくすることができないことに起因するものである。
【0011】
発明者らも、このField Cycle法を参考に数年間装置開発を行ってきたが、上述した感度及び解像度の限界から、従来の装置を使用してさらに高精度の解析を行うことには限界があるとの結論に至った。
【0012】
したがって、この発明の目的とするところは、Field Cycle法を用いず従来の生体計測装置と比較して、電子スピン共鳴及び磁気共鳴の感度及び解像度を飛躍的に向上させることができる複合型生体計測装置を提供することである。
【課題を解決するための手段】
【0013】
上述した課題を解決するため、この発明によれば、所定の大きさの磁場を発生させる第1の磁場発生手段と、前記第1の磁気共鳴手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段と、計測対象生体を、RFパルスの照射に同期させて前記第1、第2の磁場発生装置の間で移動させる計測対象物移動手段と、前記RFパルス応じて検出される信号に基づいて計測対象生体中の組織像を計測する計測手段とを有することを特徴とする生体計測装置が提供される。
【0014】
1の実施形態によれば、前記第2の磁気共鳴手段は、少なくとも1テスラ以上の磁場を発生させ、核磁気共鳴を励起するためのものである。また、前記第1の磁場発生手段は、電子スピン共鳴を励起するためのものである。
【0015】
さらに、前記計測対象物移動手段は、前記計測対象の前記第1、第2の磁場発生手段間の移動を短時間、これに限定するものではないが、好ましくは1秒以内、より好ましくは0.7秒以内で完了するように構成されているものである。
【0016】
このような構成によれば、Field Cycle法を用いる従来の生体計測装置と比較して、電子スピン共鳴及び磁気共鳴の感度及び解像度を飛躍的に向上させることができる複合型生体計測装置を得ることができる。
【0017】
すなわち、発明者らが予備実験をした結果、電子スピン励起後の生体水分子の緩和時間は1秒近くあり、ESRのための電子スピン励起とMRIを同一の外部磁場で行う必要がないことが明らかとなった。この新たな知見に基づいて、MRI用の外部磁場とESR用外部磁場とを独立させた装置の試作及び実験を行ったところ、MRI用の外部磁場を1テスラ以上と大きくし、ESR用磁場(8ミリテスラ)の間を1秒以内(例えば0.5秒程度)で実験動物を移動することで、高感度・高解像度の画像が得られることが示され、Field Cycle法を用いない新たな手法として本発明を完成するに至った。
【0018】
このような構成によれば、第2の外部磁場発生手段をESRIの外部磁場発生装置およびPEDRIの電子スピン励起装置として用い、第1の外部磁場発生手段をMRIおよびPEDRIの外部磁場発生装置として用いることができる。したがって、ラジカル量の時間変化画像はPEDRI、質的変化画像はスペクトル・空間4次元ESRI/MRIで得られることになり、かつ第2の外部磁場発生手段による磁場を大きくできるから、高感度・高分解の画像を得られることになる。さらに、上述したように、PEDRIでの電子スピン励起装置と、ESRIの外部磁場発生装置および共振器とは共用できることから、統合化により、簡単な構成で大きな効果の装置を得ることができる。
【0019】
また、本発明の更なる1の実施形態によれば、前記計測手段は、計測対象生体内に生体内局在性の異なる複数のプローブを適用し、細胞膜を介して分離した微小空間の組織像を分離して同時に画像解析するものである。この場合、前記生体内局在性の異なる複数のプローブは、異なるマーカー(好ましくはN14及びN15)で標識されたニトロキシル化合物である。
【0020】
このような構成によれば、生体内のナノ空間を同時画像解析することが可能になる。
【0021】
本発明の別の1の実施形態によれば、所定の大きさの磁場を発生させる第1の磁場発生手段と、前記第1の磁気共鳴手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段との間で、計測対象生体を、RFパルスの照射に同期させて移動させる計測対象物移動工程と、前記RFパルスに応じて検出される信号に基づいて、計測対象生体内の組織像を計測する計測工程とを有することを特徴とする生体計測方法が提供される。
【0022】
また、計測対象生体内に、N14及びN15で標識された生体内局在性の異なる複数のニトロキシプローブを適用する工程と、前記計測対象を大きさの異なる2つの磁場を適用する工程と、前記標識を基に検出される信号に基づいて、計測対象生体内の異なる組織像を同時に計測する工程とを有することを特徴とする生体計測方法も提供される。
【0023】
このような構成によれば、種々の酸化ストレス病態モデルや統合失調症など脳機能障害モデルに適用・最適化し、レドックス代謝を含む動態解析・脳機能評価を標準化する方法を得ることができる。すなわち、酸化ストレス疾患での活性酸素動態の解明と抗酸化性医薬品の開発に大きく貢献することが可能である。
【0024】
この発明の上記しない他の特徴及び顕著な効果は、次に説明する最良の実施形態の項から、当業者が明確に理解できる。
【発明を実施するための最良の形態】
【0025】
以下、この発明の実施の形態を、図面を参照して説明する。
【0026】
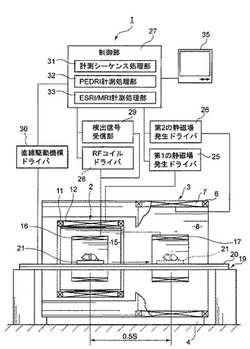
図1は本発明の生体計測装置1を示す概略構成図であり図2は、生体計測装置1の斜視図である。
【0027】
この装置は、基本的に、低磁場用(例えばこの実施形態ではESRI/PEDRI)の第1の外部磁場発生装置2と、高磁場用(例えばこの実施形態ではMRI/PEDRI)用の第2の外部磁場発生装置3とを連結してなるものである。
【0028】
説明の便宜のため、第2の外部磁場発生装置3から説明すると、この第2の外部磁場発生装置3は、支持基部4と、この支持基部4によって支持され大径円筒形の外形を有するハウジング5と、このハウジング5の一端側の内部に設置されこのハウジング5の内径部内8に静磁場を発生させるための円筒形の超伝導磁石6を有する。また、前記ハウジング5の内径面には、磁場勾配コイル7が設置されており、前記で発生された静磁場に所定のMRパルスシーケースに応じた所定規模の磁場勾配を所定の回数で生成するようになっている。この第2の外部磁場発生装置3は、MRI/PEDRI用に外部静磁場を提供するものである。
【0029】
一方、第1の外部磁場発生装置2は、前記ハウジング5の他端内に、このハウジングと同心上に配置された電磁石11と、磁場勾配コイル12と、磁場掃引コイル13とを有する。この第1の外部磁場発生装置2は、前記電磁石11の内径部内15にESRの外部静磁場及びPEDRIにおける励起磁場を提供するものである。
【0030】
前記第1、第2の外部磁場発生装置2、3はその中心軸を一致させて配置され、その内径部内8、15には、円筒形形状の第1のRFコイル16(共振器)及び第2のRFコイル17がそれぞれ同心軸上に設けられている。この第1、第2のRFコイル16,17は、静磁場に直行する方向にラジオ波(RF)の高周波(マイクロ波)磁界を形成するものである。
【0031】
また、前記第1、第2の外部磁場発生装置2、3間には、第1、第2のRFコイル16、17の中心軸線に沿って、直線移動装置19が設置されている。この直線移動装置19は、前記中心軸上に設置されたガイド20と、このガイド20上にスライド自在に設けられた計測対象生体保持部21とを有する。この直線移動装置19は、たとえばリニアモータで駆動されるようになっており、この場合、図3に示すように、前記ガイド20に設けられた永久磁石からなる固定子22と、前記支持部側に設けられ電磁磁石から構成され長手方向に並べられた電磁石からなる可動子23とからなる。この可動子23の極性を所定の周期で切り替えることによって駆動及び停止が行えるようになっている。
【0032】
この装置の制御について説明すると、まず、第1の外部磁場発生装置2は、第1の静磁場発生ドライバ25を介して制御部27に接続されている。この第1の静磁場発生ドライバ25には、前記空芯コイル型電磁石11と、磁場勾配コイル12と、磁場掃引コイル13に給電するための図示しない電源が接続されており、前記制御部27からの指令によって前記空芯コイル型電磁石11と、磁場勾配コイル12と、磁場掃引コイル13を制御するようになっている。この実施形態によれば、これに限定されるものではないが、例えば第1の外部磁場発生装置2による静磁場の強さは8mT、ギャップ幅は15cm、三次元傾斜磁場は100mT/m、磁場掃引コイル13の磁場の強さは2mT/sである。
【0033】
第2の外部磁場発生装置3は、第2の静磁場発生ドライバ26を介して制御部27に接続されている。この第2の静磁場発生ドライバ26には、前記超伝導磁石6、磁場勾配コイル7に給電するための図示しない電源が接続されており、前記制御部27に指令によって超伝導磁石6及び磁場勾配コイル7を駆動するようになっている。この実施形態によれば、この第2の外部磁場発生装置3による静磁場の強さは2T(テスラ)、ギャップ幅20cm、三次元傾斜磁場10mT/mであるが、これに限定されるものではない。なお、後で詳しく説明するがこの静磁場の強さは現在のPEDRIの70倍であり、これにより100倍程度の感度・分解能向上を図ることができる。
【0034】
また、前記第1、第2のRFコイル16、17は、RFコイルドライバ28、検出信号受信部29を介して前記制御部27に接続されている。このRFコイルドライバ28には、RFコイル16、17に給電するための図示しない電源が接続されており、制御部27から指令されるシーケンスに従ってRFコイル16、17を駆動するようになっている。RFコイル16、17に高周波パルスが印加され、前記保持部21上の計測対象に対して高周波磁場が印加される。そして、RFコイル16、17で受信された電子スピン共鳴信号/磁気共鳴信号は、前記検出信号受信部29で受け取られ、前記制御部27に渡されるようになっている。
【0035】
なお、ここで、これに限定されるものではないが、ESRI計測の空間解像度及び撮像時間はFOVを1cmとしたときのスペクトル空間3次元画像及び4次元画像で1mm以内の空間分解能を3次元で1分以内、4次元で10分以内に取得できるものとなっている。
【0036】
前記直線駆動装置19は、直線駆動装置ドライバ30を介して制御部27に接続されている。直線駆動装置19は、計測対象を第1の外部磁場発生装置2と第2の外部磁場発生装置3の間で移動させるものであり、制御部27からの指令されるシーケンスに従い、RFコイル16、17による高周波磁場の印加に同期したタイミングで前記計測対象を駆動する。第1の外部磁場発生装置2から第2の外部磁場発生装置3までの駆動時間は1秒以内であることが好ましく、さらに好ましくは0.7秒以内であり、この実施形態では0.5秒に設定される。
【0037】
一方、前記制御部27には、計測シーケンス処理部31と、PEDRI計測処理部32と、ESRI/MRI計測処理部33とが設けられている。計測シーケンス処理部31は、前記第1、第2の外部磁場発生装置2、3、第1、第2のRFコイル16、17に対する給電シーケンスと、前記第1、第2のRFコイル16、17における計測シーケンスとを有し、上記装置を制御するものである。前記PEDRI計測処理部32及びESRI/MRI計測処理部33は、前記計測シーケンスに従って得られた電子スピン共鳴信号及び磁気共鳴信号に基づいて画像処理を行い、その結果をモニター35上に表示する。
【0038】
また、この画像処理はこの実施形態では、生体内局在性の異なる(例えば、膜透過性の異なる)複数のニトロキシルプローブを合成しておき、これをそれぞれN14とN15で標識することで、細胞膜(厚さナノメートル)あるいは受容体などとの結合を介した微小空間を分離同時画像解析することができるようになっている。
【0039】
なお、上述した制御部27は、実際にはコンピュータシステムからなり、各処理部31〜33は、ハードディスク等に格納されたコンピュータソフトウエアプログラムからなる。これらのコンピュータソフトウエアプログラムはCPUによって適宜呼び出され実行されることで、本発明の構成要素として機能するようになっている。
【0040】
次に、この装置の動作について説明する。
【0041】
まず、前記直線移動装置19の保持部21上に計測対象の小動物、例えばマウスを設置する。この例では、計測対象における、酸化ストレス疾患でのレドックス代謝異常、あるいは統合失調症等での脳機能を空間画像解析する。
【0042】
また、このマウスには、N14、N15で標識したニトロキシルラジカルを誘導体化したプローブ剤を導入しておく。この例では、生体内局在性の異なる(例えば、膜透過性の異なる)複数のプローブをN14とN15で標識することで、細胞膜(厚さナノメートル)あるいは受容体などとの結合を介した微小空間を分離同時画像解析可能にする。
【0043】
すなわち、本実施例のような高感度・高分解能の装置で画像解析を行うには、より高感度・高選択性をもつ造影剤の開発が必須となる。高感度画像を得る一つの要素として、造影剤自身のスペクトル線幅を狭くする手法が考えられる。造影剤の線幅狭小は、造影剤自身の不対電子密度のプロトン局在性を小さくすることで可能となる。一方、生体内でのラジカル反応を追跡するには、それぞれのラジカル種の酸化還元電位に見合った酸化還元電位を有するニトロキシルスピンプローブ造影剤を合成する必要がある。そこで、製薬メーカーが繁用している理論計算科学的手法を駆使して分子設計を行い、新規造影剤の不対電子密度・酸化還元電位を算出し、その分子設計に基づいて有機化学的合成を行い、さらにその造影剤の生物化学的反応性を検証することで、生体内フリーラジカル反応を追跡するに最も適した造影剤を開発したものである。
【0044】
この実施形態では、コンピュータを利用した分子設計手法を用いて、種々の特性を有する置換基を賦したニトロキシルプローブを10種程度新規合成した。これらには、これに限定されるものではないが、a)血管内半減期20分以上、b)細胞内滞留性5分以上の高残留性プローブ、c)細胞膜指向性プローブ、d)血液脳関門通過性プローブが含まれる。さらに、感度を倍増させるために共鳴吸収線幅が0.5ガウス以内(市販ニトロキシルプローブは1.0ガウス以上)になるように合成されたプローブ剤を用いた。
【0045】
ついで、前記直線駆動装置19を駆動し、前記計測対象を前記第1の外部磁場発生装置2による静磁場8内の第1のRFコイル16内に位置させる。ついで、第1のRFコイル16から高周波を照射すると共に、前記掃引コイル13を駆動することで、静磁場を高速掃引する。このことで、計測対象中の不対電子が高周波を吸収し、電子スピンが共鳴励起される。マイクロ波の反射によりESR信号は、前記検出信号受信部29で受信される。
【0046】
第1の外部磁場発生装置2におけるESR計測が終了すると、前記直線駆動装置19を駆動し、0.7秒以内、この例では0.5秒で計測対象を第2の外部磁場発生装置3にまで移動する。このことで、計測対象は1T以上,この実施例では2Tという非常に強い静磁場に置かれる。このことで、共鳴励起された電子スピンが核スピンへエネルギー遷移が生じさせられることになる。ついで、前記第2のRFコイル17を用い、高周波照射により計測対象から得られる信号を前記検出信号受信部29で受信する。
【0047】
このようにして検出信号受信部29で受信された信号は、前記制御部27で受け取られ、計測処理部32、33で処理される。ESRI/MRI計測処理部33は、前記第1のRFコイル16から得られたERS信号と第2のRFコイル17から得られたMRI信号とからERS画像とMRI画像とを重畳させてなる画像を合成する。また、PEDRI計測処理部32は、第2のRFコイル17から得られた信号を処理することで、核スピン分布を示す画像を合成する。
【0048】
このような構成によれば、非常に感度が高く、かつ高分解能の生体計測装置を得ることができる。
【0049】
すなわち、前述したように、発明者らは、予備実験により、電子スピン励起後の生体水分子の緩和時間は1秒近くあり、電子スピン励起とMRIを同一の外部磁場で行う必要がないという知見を得、この新たな知見に基づいて、MRI用の外部磁場とESR用外部磁場とを独立させた装置を完成させたものである。MRI用の外部磁場とESR用外部磁場とが独立しているので、MRI用の外部磁場を非常に大きくしてより高い感度及び空間分解能を得ることができる。この実施形態では、MRI用の第1の外部静磁場発生装置の磁場の大きさを2テスラとし、ESR用磁場(8ミリテスラ)の間を0.5秒程度で計測対象を移動させるようにした。このような構成及び方法によれば、Field Cycle法を用いることなく、より高感度・高解像度のESR/MRI重畳画像が得られる。
【0050】
また、このような構成によれば、第2の外部磁場発生装置3をMRIおよびPEDRIの外部磁場発生装置として用い、第1の外部磁場発生手段2をESRIの外部磁場発生装置およびPEDRIの電子スピン励起装置として用いることができるので、PEDRIも融合することができる。そして上述したようにMRIの外部磁場を大きくすることができるので、高感度・高分解能のPEDRI画像を得ることができる。
【0051】
言い換えると、ラジカル量の時間変化画像はPEDRI、質的変化画像はスペクトル・空間4次元ESRI/MRIで得られることになり、かつ第2の外部磁場発生装置3による磁場を大きくできるから、高感度・高分解の画像を得られることになる。さらに、上述したように、PEDRIでの電子スピン励起装置と、ESRIの外部磁場発生装置および共振器とは共用できることから、統合化により、設置面積を非常に小さくしたコンパクトな装置を得ることができる。
【0052】
さらに、本発明の更なる1の実施形態によれば、前記PEDRI計測処理部32及びESRI/MRI計測処理部33は、計測対象内に生体内局在性の異なる複数のプローブを適用し、細胞膜を介して分離した微小空間の組織像を分離して同時に画像解析するものである。このような構成によれば、生体内のナノ空間を同時画像解析することが可能になる。
【0053】
なお、この発明は上記一実施形態に限定されるものではなく、発明の要旨を変更しない範囲で種々変形可能である。
【0054】
たとえば、上記一実施形態では、第1の外部磁場発生装置の電磁石11と、第2の外部磁場発生装置の超伝導磁石6は、水平方向に離間して設けられていたが、これに限定されるものではない。図4に示すように、高磁場を発生させる超伝導磁石6’を、ハウジング5の全長に亘って設け、電磁石11’を減磁用のものとして第1の外部磁場装置用に磁場を小さくするように構成してもよい。すなわち、この場合、第1の外部磁場発生装置2が発生する低磁場は、前記超伝導磁石6’と、電磁石11’とか生成されることになる。
【0055】
また、上記一実施形態では、上記生体計測装置は、ESRI/MRI/PEDRIであったが、これに限定されるものではない。異なる外部磁場発生装置間で試料を移動させる装置であれば、いかなる装置にも適用可能である。
【図面の簡単な説明】
【0056】
【図1】この発明の実施形態を示す概略構成図。
【図2】同じく、斜視図。
【図3】同じく、直線移動機構を示す縦断面図。
【図4】他の実施形態を示す概略構成図。
【符号の説明】
【0057】
1…生体計測装置
2…第1の外部磁場発生手段
3…第1の外部磁場発生装置
4…支持基部
5…ハウジング
6…超伝導磁石
7…磁場勾配コイル
8…内径部内
11…電磁石
12…磁場勾配コイル
13…磁場掃引コイル
15…内径部内
16…第1のRFコイル
17…第2のRFコイル
19…直線移動装置
20…ガイド
21…保持部
22…固定子
23…可動子
25…第1の静磁場発生ドライバ
26…第2の静磁場発生ドライバ
27…制御部
28…RFコイルドライバ
29…検出信号受信部
30…直線駆動装置ドライバ
31…計測シーケンス処理部
32…PEDRI計測処理部
33…MRI計測処理部
35…モニター
【技術分野】
【0001】
この発明は、電子スピン共鳴や核磁気共鳴など種々の磁気共鳴を利用して生体の組織画像を得るための生体計測装置に関する。
【背景技術】
【0002】
日本における酸化ストレスに関わる患者予備軍は、いまや数百万人にも上るといわれ、国民健康保険を大きく圧迫するに至っている。ここで、酸化ストレスとは生体の内因性あるいは外因性の原因により生じる活性酸素を生体が十分処理することができなくなるために生じるものである。酸化ストレスはがん、生活習慣病、虚血後再還流障害、炎症など、多くの病態や老化に関与することが知られている。
【0003】
近年、酸化ストレスと活性酸素や活性窒素種などのフリーラジカルとの関係が注目されている。活性酸素・フリーラジカルの過剰な生成等が生じると、生体内においてその生成と消去のバランスを崩し、酸化ストレスの状態となる。活性酸素・フリーラジカルは脂質や、核酸、たんぱく質、糖質などを傷害して各種疾患を誘発する。
【0004】
酸化ストレスは、ほぼすべての疾患に何らかの形でかかわっていると考えられている。しかし、その根拠は、間接的なものがほとんどで、活性酸素の産生が疾患の第一成因であるか、あるいは二次的に障害の進展に関係するのか等に関して明らかとなっていない。生体内で、どのような活性酸素が、何時、どこで、どのように産生し、何と反応するかを酸化ストレスモデル動物で無侵襲画像解析することが可能となれば、酸化ストレス疾患での活性酸素動態の解明と抗酸化性医薬品の開発に有力な情報となりうる。
【0005】
フリーラジカルを検出する装置として、ESR画像装置(ESRI)がある。ESR(Electron Spin Resonance)は、電子スピン共鳴の略称で、フリーラジカルの不対電子スピンの磁気モーメントを電磁波の共鳴吸収で観測することから、フリーラジカルのみを検出する選択性の高い分析機器である。このESR分光器を生体用に改良した生体計測ESRI装置を用いると、実験動物丸ごとで生きたままラジカルを計測し、その分布を画像解析することが可能である。
【0006】
発明者らは抗酸化作用を機序とする医薬品の開発にかかわり、その開発段階で、生体計測ESR・スピンプローブ法を用いて脳虚血−再灌流障害モデルラットでの抗酸化作用発現を明らかにすることに成功している。また、胃潰瘍モデルラットで抗潰瘍薬が胃腔内での・OH生成を抑制することも明らかとした。その他、漢方の胃潰瘍治療薬など、生体計測ESR・スピンプローブ法は抗酸化医薬品の生体内作用評価法として非常に有用である。
【0007】
すなわち、このようなフリーラジカルを検出できる生体計測装置の開発は、国民の健康福祉に直結するもので、きわめて社会的意義が大きい。また本研究は新規抗酸化性医薬品の評価・創出を可能とするもので、その経済的波及効果は計り知れないものである。
【特許文献1】特許第3117847号公報
【発明の開示】
【発明が解決しようとする課題】
【0008】
ところで、上述した従来の方法では、フリーラジカルしか見えないため、活性酸素・フリーラジカルの産生組織・部位が特定できない問題がある。この問題を解決するため、活性酸素・フリーラジカルの画像(ESRI)に臓器のMRI画像を重畳できるESRI・MRI融合型磁気共鳴画像解析装置がある。この装置を用いると、種々のルートで投与したプローブ剤の生体内挙動が画像化できる。
【0009】
また、核・電子二重共鳴装置(PEDRI)もフリーラジカルの動態の解析に有効である。PEDRIは、ESR照射により生体の電子スピンを遷移させ、核スピンへエネルギー遷移が生じさせるものである。その後MRI計測を行うことで、通常の核スピンのボルツマン分布と比較し、最大(理論値)で330倍の核スピンボルツマン分布が増強することができる。すなわち通常のMRI計測に較べ、330倍(理論値)の高感度化を図ることができる。潰瘍性大腸炎モデルに適用した結果、酸化ストレス性疾患のレドックス動態の画像解析に非常に有用であることが明らかとなっている。
【0010】
しかしながら、一般に、このようなPEDRIやERSI/MRIの複合計測装置においては、得られた画像の解像度が低いという問題がある。すなわち、米国で開発中の装置はいずれもMRIの外部磁場が数十mT(ミリテスラ)(Dr.Zweier;Ohio State University,Dr.Halpern;University of Chicago,Dr.Krishna,NIH/NCI,Dr.Swartz;Dartmouth Medical School)であり、MRIの基本特許を取得している英国Aberdeen大学のDr.Lurieの提案において500mT(ミリテスラ)(但し、試料サイズは10mm程度)である。これは、磁気共鳴の感度と解像度は外部磁場の大きさに依存するのに対して、従来の装置はいずれも、1つの磁場発生装置を用い、外部磁場変換をField Cycle法(Dr.Lurieが米国特許取得済)で行っているため、MRI装置の外部磁場を大きくすることができないことに起因するものである。
【0011】
発明者らも、このField Cycle法を参考に数年間装置開発を行ってきたが、上述した感度及び解像度の限界から、従来の装置を使用してさらに高精度の解析を行うことには限界があるとの結論に至った。
【0012】
したがって、この発明の目的とするところは、Field Cycle法を用いず従来の生体計測装置と比較して、電子スピン共鳴及び磁気共鳴の感度及び解像度を飛躍的に向上させることができる複合型生体計測装置を提供することである。
【課題を解決するための手段】
【0013】
上述した課題を解決するため、この発明によれば、所定の大きさの磁場を発生させる第1の磁場発生手段と、前記第1の磁気共鳴手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段と、計測対象生体を、RFパルスの照射に同期させて前記第1、第2の磁場発生装置の間で移動させる計測対象物移動手段と、前記RFパルス応じて検出される信号に基づいて計測対象生体中の組織像を計測する計測手段とを有することを特徴とする生体計測装置が提供される。
【0014】
1の実施形態によれば、前記第2の磁気共鳴手段は、少なくとも1テスラ以上の磁場を発生させ、核磁気共鳴を励起するためのものである。また、前記第1の磁場発生手段は、電子スピン共鳴を励起するためのものである。
【0015】
さらに、前記計測対象物移動手段は、前記計測対象の前記第1、第2の磁場発生手段間の移動を短時間、これに限定するものではないが、好ましくは1秒以内、より好ましくは0.7秒以内で完了するように構成されているものである。
【0016】
このような構成によれば、Field Cycle法を用いる従来の生体計測装置と比較して、電子スピン共鳴及び磁気共鳴の感度及び解像度を飛躍的に向上させることができる複合型生体計測装置を得ることができる。
【0017】
すなわち、発明者らが予備実験をした結果、電子スピン励起後の生体水分子の緩和時間は1秒近くあり、ESRのための電子スピン励起とMRIを同一の外部磁場で行う必要がないことが明らかとなった。この新たな知見に基づいて、MRI用の外部磁場とESR用外部磁場とを独立させた装置の試作及び実験を行ったところ、MRI用の外部磁場を1テスラ以上と大きくし、ESR用磁場(8ミリテスラ)の間を1秒以内(例えば0.5秒程度)で実験動物を移動することで、高感度・高解像度の画像が得られることが示され、Field Cycle法を用いない新たな手法として本発明を完成するに至った。
【0018】
このような構成によれば、第2の外部磁場発生手段をESRIの外部磁場発生装置およびPEDRIの電子スピン励起装置として用い、第1の外部磁場発生手段をMRIおよびPEDRIの外部磁場発生装置として用いることができる。したがって、ラジカル量の時間変化画像はPEDRI、質的変化画像はスペクトル・空間4次元ESRI/MRIで得られることになり、かつ第2の外部磁場発生手段による磁場を大きくできるから、高感度・高分解の画像を得られることになる。さらに、上述したように、PEDRIでの電子スピン励起装置と、ESRIの外部磁場発生装置および共振器とは共用できることから、統合化により、簡単な構成で大きな効果の装置を得ることができる。
【0019】
また、本発明の更なる1の実施形態によれば、前記計測手段は、計測対象生体内に生体内局在性の異なる複数のプローブを適用し、細胞膜を介して分離した微小空間の組織像を分離して同時に画像解析するものである。この場合、前記生体内局在性の異なる複数のプローブは、異なるマーカー(好ましくはN14及びN15)で標識されたニトロキシル化合物である。
【0020】
このような構成によれば、生体内のナノ空間を同時画像解析することが可能になる。
【0021】
本発明の別の1の実施形態によれば、所定の大きさの磁場を発生させる第1の磁場発生手段と、前記第1の磁気共鳴手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段との間で、計測対象生体を、RFパルスの照射に同期させて移動させる計測対象物移動工程と、前記RFパルスに応じて検出される信号に基づいて、計測対象生体内の組織像を計測する計測工程とを有することを特徴とする生体計測方法が提供される。
【0022】
また、計測対象生体内に、N14及びN15で標識された生体内局在性の異なる複数のニトロキシプローブを適用する工程と、前記計測対象を大きさの異なる2つの磁場を適用する工程と、前記標識を基に検出される信号に基づいて、計測対象生体内の異なる組織像を同時に計測する工程とを有することを特徴とする生体計測方法も提供される。
【0023】
このような構成によれば、種々の酸化ストレス病態モデルや統合失調症など脳機能障害モデルに適用・最適化し、レドックス代謝を含む動態解析・脳機能評価を標準化する方法を得ることができる。すなわち、酸化ストレス疾患での活性酸素動態の解明と抗酸化性医薬品の開発に大きく貢献することが可能である。
【0024】
この発明の上記しない他の特徴及び顕著な効果は、次に説明する最良の実施形態の項から、当業者が明確に理解できる。
【発明を実施するための最良の形態】
【0025】
以下、この発明の実施の形態を、図面を参照して説明する。
【0026】
図1は本発明の生体計測装置1を示す概略構成図であり図2は、生体計測装置1の斜視図である。
【0027】
この装置は、基本的に、低磁場用(例えばこの実施形態ではESRI/PEDRI)の第1の外部磁場発生装置2と、高磁場用(例えばこの実施形態ではMRI/PEDRI)用の第2の外部磁場発生装置3とを連結してなるものである。
【0028】
説明の便宜のため、第2の外部磁場発生装置3から説明すると、この第2の外部磁場発生装置3は、支持基部4と、この支持基部4によって支持され大径円筒形の外形を有するハウジング5と、このハウジング5の一端側の内部に設置されこのハウジング5の内径部内8に静磁場を発生させるための円筒形の超伝導磁石6を有する。また、前記ハウジング5の内径面には、磁場勾配コイル7が設置されており、前記で発生された静磁場に所定のMRパルスシーケースに応じた所定規模の磁場勾配を所定の回数で生成するようになっている。この第2の外部磁場発生装置3は、MRI/PEDRI用に外部静磁場を提供するものである。
【0029】
一方、第1の外部磁場発生装置2は、前記ハウジング5の他端内に、このハウジングと同心上に配置された電磁石11と、磁場勾配コイル12と、磁場掃引コイル13とを有する。この第1の外部磁場発生装置2は、前記電磁石11の内径部内15にESRの外部静磁場及びPEDRIにおける励起磁場を提供するものである。
【0030】
前記第1、第2の外部磁場発生装置2、3はその中心軸を一致させて配置され、その内径部内8、15には、円筒形形状の第1のRFコイル16(共振器)及び第2のRFコイル17がそれぞれ同心軸上に設けられている。この第1、第2のRFコイル16,17は、静磁場に直行する方向にラジオ波(RF)の高周波(マイクロ波)磁界を形成するものである。
【0031】
また、前記第1、第2の外部磁場発生装置2、3間には、第1、第2のRFコイル16、17の中心軸線に沿って、直線移動装置19が設置されている。この直線移動装置19は、前記中心軸上に設置されたガイド20と、このガイド20上にスライド自在に設けられた計測対象生体保持部21とを有する。この直線移動装置19は、たとえばリニアモータで駆動されるようになっており、この場合、図3に示すように、前記ガイド20に設けられた永久磁石からなる固定子22と、前記支持部側に設けられ電磁磁石から構成され長手方向に並べられた電磁石からなる可動子23とからなる。この可動子23の極性を所定の周期で切り替えることによって駆動及び停止が行えるようになっている。
【0032】
この装置の制御について説明すると、まず、第1の外部磁場発生装置2は、第1の静磁場発生ドライバ25を介して制御部27に接続されている。この第1の静磁場発生ドライバ25には、前記空芯コイル型電磁石11と、磁場勾配コイル12と、磁場掃引コイル13に給電するための図示しない電源が接続されており、前記制御部27からの指令によって前記空芯コイル型電磁石11と、磁場勾配コイル12と、磁場掃引コイル13を制御するようになっている。この実施形態によれば、これに限定されるものではないが、例えば第1の外部磁場発生装置2による静磁場の強さは8mT、ギャップ幅は15cm、三次元傾斜磁場は100mT/m、磁場掃引コイル13の磁場の強さは2mT/sである。
【0033】
第2の外部磁場発生装置3は、第2の静磁場発生ドライバ26を介して制御部27に接続されている。この第2の静磁場発生ドライバ26には、前記超伝導磁石6、磁場勾配コイル7に給電するための図示しない電源が接続されており、前記制御部27に指令によって超伝導磁石6及び磁場勾配コイル7を駆動するようになっている。この実施形態によれば、この第2の外部磁場発生装置3による静磁場の強さは2T(テスラ)、ギャップ幅20cm、三次元傾斜磁場10mT/mであるが、これに限定されるものではない。なお、後で詳しく説明するがこの静磁場の強さは現在のPEDRIの70倍であり、これにより100倍程度の感度・分解能向上を図ることができる。
【0034】
また、前記第1、第2のRFコイル16、17は、RFコイルドライバ28、検出信号受信部29を介して前記制御部27に接続されている。このRFコイルドライバ28には、RFコイル16、17に給電するための図示しない電源が接続されており、制御部27から指令されるシーケンスに従ってRFコイル16、17を駆動するようになっている。RFコイル16、17に高周波パルスが印加され、前記保持部21上の計測対象に対して高周波磁場が印加される。そして、RFコイル16、17で受信された電子スピン共鳴信号/磁気共鳴信号は、前記検出信号受信部29で受け取られ、前記制御部27に渡されるようになっている。
【0035】
なお、ここで、これに限定されるものではないが、ESRI計測の空間解像度及び撮像時間はFOVを1cmとしたときのスペクトル空間3次元画像及び4次元画像で1mm以内の空間分解能を3次元で1分以内、4次元で10分以内に取得できるものとなっている。
【0036】
前記直線駆動装置19は、直線駆動装置ドライバ30を介して制御部27に接続されている。直線駆動装置19は、計測対象を第1の外部磁場発生装置2と第2の外部磁場発生装置3の間で移動させるものであり、制御部27からの指令されるシーケンスに従い、RFコイル16、17による高周波磁場の印加に同期したタイミングで前記計測対象を駆動する。第1の外部磁場発生装置2から第2の外部磁場発生装置3までの駆動時間は1秒以内であることが好ましく、さらに好ましくは0.7秒以内であり、この実施形態では0.5秒に設定される。
【0037】
一方、前記制御部27には、計測シーケンス処理部31と、PEDRI計測処理部32と、ESRI/MRI計測処理部33とが設けられている。計測シーケンス処理部31は、前記第1、第2の外部磁場発生装置2、3、第1、第2のRFコイル16、17に対する給電シーケンスと、前記第1、第2のRFコイル16、17における計測シーケンスとを有し、上記装置を制御するものである。前記PEDRI計測処理部32及びESRI/MRI計測処理部33は、前記計測シーケンスに従って得られた電子スピン共鳴信号及び磁気共鳴信号に基づいて画像処理を行い、その結果をモニター35上に表示する。
【0038】
また、この画像処理はこの実施形態では、生体内局在性の異なる(例えば、膜透過性の異なる)複数のニトロキシルプローブを合成しておき、これをそれぞれN14とN15で標識することで、細胞膜(厚さナノメートル)あるいは受容体などとの結合を介した微小空間を分離同時画像解析することができるようになっている。
【0039】
なお、上述した制御部27は、実際にはコンピュータシステムからなり、各処理部31〜33は、ハードディスク等に格納されたコンピュータソフトウエアプログラムからなる。これらのコンピュータソフトウエアプログラムはCPUによって適宜呼び出され実行されることで、本発明の構成要素として機能するようになっている。
【0040】
次に、この装置の動作について説明する。
【0041】
まず、前記直線移動装置19の保持部21上に計測対象の小動物、例えばマウスを設置する。この例では、計測対象における、酸化ストレス疾患でのレドックス代謝異常、あるいは統合失調症等での脳機能を空間画像解析する。
【0042】
また、このマウスには、N14、N15で標識したニトロキシルラジカルを誘導体化したプローブ剤を導入しておく。この例では、生体内局在性の異なる(例えば、膜透過性の異なる)複数のプローブをN14とN15で標識することで、細胞膜(厚さナノメートル)あるいは受容体などとの結合を介した微小空間を分離同時画像解析可能にする。
【0043】
すなわち、本実施例のような高感度・高分解能の装置で画像解析を行うには、より高感度・高選択性をもつ造影剤の開発が必須となる。高感度画像を得る一つの要素として、造影剤自身のスペクトル線幅を狭くする手法が考えられる。造影剤の線幅狭小は、造影剤自身の不対電子密度のプロトン局在性を小さくすることで可能となる。一方、生体内でのラジカル反応を追跡するには、それぞれのラジカル種の酸化還元電位に見合った酸化還元電位を有するニトロキシルスピンプローブ造影剤を合成する必要がある。そこで、製薬メーカーが繁用している理論計算科学的手法を駆使して分子設計を行い、新規造影剤の不対電子密度・酸化還元電位を算出し、その分子設計に基づいて有機化学的合成を行い、さらにその造影剤の生物化学的反応性を検証することで、生体内フリーラジカル反応を追跡するに最も適した造影剤を開発したものである。
【0044】
この実施形態では、コンピュータを利用した分子設計手法を用いて、種々の特性を有する置換基を賦したニトロキシルプローブを10種程度新規合成した。これらには、これに限定されるものではないが、a)血管内半減期20分以上、b)細胞内滞留性5分以上の高残留性プローブ、c)細胞膜指向性プローブ、d)血液脳関門通過性プローブが含まれる。さらに、感度を倍増させるために共鳴吸収線幅が0.5ガウス以内(市販ニトロキシルプローブは1.0ガウス以上)になるように合成されたプローブ剤を用いた。
【0045】
ついで、前記直線駆動装置19を駆動し、前記計測対象を前記第1の外部磁場発生装置2による静磁場8内の第1のRFコイル16内に位置させる。ついで、第1のRFコイル16から高周波を照射すると共に、前記掃引コイル13を駆動することで、静磁場を高速掃引する。このことで、計測対象中の不対電子が高周波を吸収し、電子スピンが共鳴励起される。マイクロ波の反射によりESR信号は、前記検出信号受信部29で受信される。
【0046】
第1の外部磁場発生装置2におけるESR計測が終了すると、前記直線駆動装置19を駆動し、0.7秒以内、この例では0.5秒で計測対象を第2の外部磁場発生装置3にまで移動する。このことで、計測対象は1T以上,この実施例では2Tという非常に強い静磁場に置かれる。このことで、共鳴励起された電子スピンが核スピンへエネルギー遷移が生じさせられることになる。ついで、前記第2のRFコイル17を用い、高周波照射により計測対象から得られる信号を前記検出信号受信部29で受信する。
【0047】
このようにして検出信号受信部29で受信された信号は、前記制御部27で受け取られ、計測処理部32、33で処理される。ESRI/MRI計測処理部33は、前記第1のRFコイル16から得られたERS信号と第2のRFコイル17から得られたMRI信号とからERS画像とMRI画像とを重畳させてなる画像を合成する。また、PEDRI計測処理部32は、第2のRFコイル17から得られた信号を処理することで、核スピン分布を示す画像を合成する。
【0048】
このような構成によれば、非常に感度が高く、かつ高分解能の生体計測装置を得ることができる。
【0049】
すなわち、前述したように、発明者らは、予備実験により、電子スピン励起後の生体水分子の緩和時間は1秒近くあり、電子スピン励起とMRIを同一の外部磁場で行う必要がないという知見を得、この新たな知見に基づいて、MRI用の外部磁場とESR用外部磁場とを独立させた装置を完成させたものである。MRI用の外部磁場とESR用外部磁場とが独立しているので、MRI用の外部磁場を非常に大きくしてより高い感度及び空間分解能を得ることができる。この実施形態では、MRI用の第1の外部静磁場発生装置の磁場の大きさを2テスラとし、ESR用磁場(8ミリテスラ)の間を0.5秒程度で計測対象を移動させるようにした。このような構成及び方法によれば、Field Cycle法を用いることなく、より高感度・高解像度のESR/MRI重畳画像が得られる。
【0050】
また、このような構成によれば、第2の外部磁場発生装置3をMRIおよびPEDRIの外部磁場発生装置として用い、第1の外部磁場発生手段2をESRIの外部磁場発生装置およびPEDRIの電子スピン励起装置として用いることができるので、PEDRIも融合することができる。そして上述したようにMRIの外部磁場を大きくすることができるので、高感度・高分解能のPEDRI画像を得ることができる。
【0051】
言い換えると、ラジカル量の時間変化画像はPEDRI、質的変化画像はスペクトル・空間4次元ESRI/MRIで得られることになり、かつ第2の外部磁場発生装置3による磁場を大きくできるから、高感度・高分解の画像を得られることになる。さらに、上述したように、PEDRIでの電子スピン励起装置と、ESRIの外部磁場発生装置および共振器とは共用できることから、統合化により、設置面積を非常に小さくしたコンパクトな装置を得ることができる。
【0052】
さらに、本発明の更なる1の実施形態によれば、前記PEDRI計測処理部32及びESRI/MRI計測処理部33は、計測対象内に生体内局在性の異なる複数のプローブを適用し、細胞膜を介して分離した微小空間の組織像を分離して同時に画像解析するものである。このような構成によれば、生体内のナノ空間を同時画像解析することが可能になる。
【0053】
なお、この発明は上記一実施形態に限定されるものではなく、発明の要旨を変更しない範囲で種々変形可能である。
【0054】
たとえば、上記一実施形態では、第1の外部磁場発生装置の電磁石11と、第2の外部磁場発生装置の超伝導磁石6は、水平方向に離間して設けられていたが、これに限定されるものではない。図4に示すように、高磁場を発生させる超伝導磁石6’を、ハウジング5の全長に亘って設け、電磁石11’を減磁用のものとして第1の外部磁場装置用に磁場を小さくするように構成してもよい。すなわち、この場合、第1の外部磁場発生装置2が発生する低磁場は、前記超伝導磁石6’と、電磁石11’とか生成されることになる。
【0055】
また、上記一実施形態では、上記生体計測装置は、ESRI/MRI/PEDRIであったが、これに限定されるものではない。異なる外部磁場発生装置間で試料を移動させる装置であれば、いかなる装置にも適用可能である。
【図面の簡単な説明】
【0056】
【図1】この発明の実施形態を示す概略構成図。
【図2】同じく、斜視図。
【図3】同じく、直線移動機構を示す縦断面図。
【図4】他の実施形態を示す概略構成図。
【符号の説明】
【0057】
1…生体計測装置
2…第1の外部磁場発生手段
3…第1の外部磁場発生装置
4…支持基部
5…ハウジング
6…超伝導磁石
7…磁場勾配コイル
8…内径部内
11…電磁石
12…磁場勾配コイル
13…磁場掃引コイル
15…内径部内
16…第1のRFコイル
17…第2のRFコイル
19…直線移動装置
20…ガイド
21…保持部
22…固定子
23…可動子
25…第1の静磁場発生ドライバ
26…第2の静磁場発生ドライバ
27…制御部
28…RFコイルドライバ
29…検出信号受信部
30…直線駆動装置ドライバ
31…計測シーケンス処理部
32…PEDRI計測処理部
33…MRI計測処理部
35…モニター
【特許請求の範囲】
【請求項1】
所定の大きさの磁場を発生させる第1の磁場発生手段と、
前記第1の磁場発生手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段と、
計測対象生体を、RFパルスの照射に同期させて前記第1、第2の磁場発生手段の間で移動させる計測対象物移動手段と、
前記RFパルスに応じて検出される信号に基づいて計測対象生体中の組織像を計測する計測手段と
を有することを特徴とする生体計測装置。
【請求項2】
請求項1記載の生体計測装置において、
前記第2の磁場発生手段は、少なくとも1テスラ以上の磁場を発生させ、核磁気共鳴を励起するためのものであることを特徴とする生体計測装置。
【請求項3】
請求項1記載の生体計測装置において、
前記計測手段は、
計測対象生体内に生体内局在性の異なる複数のプローブを適用し、異なる生体組織像を分離して同時に画像解析するものであることを特徴とする生体計測装置。
【請求項4】
請求項3記載の生体計測装置において、
前記生体内局在性の異なる複数のプローブは、異なるマーカーで標識されたラベル化合物であることを特徴とする生体計測装置。
【請求項5】
請求項4記載の生体計測装置において、
前記生体内局在性の異なる複数のプローブは、N14及びN15で標識されたニトロキシル化合物であることを特徴とする生体計測装置。
【請求項6】
所定の大きさの磁場を発生させる第1の磁場発生手段と、前記第1の磁気共鳴手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段との間で、計測対象生体を、RFパルスの照射に同期させて移動させる計測対象物移動工程と、
前記RFパルスに応じて検出される信号に基づいて、計測対象生体内の組織像を計測する計測工程と
を有することを特徴とする生体計測方法。
【請求項7】
請求項6記載の生体計測方法において、
前記第2の磁場発生手段は、少なくとも1テスラ以上の磁場を発生させ、核磁気共鳴を励起するためのものであることを特徴とする生体計測方法。
【請求項8】
請求項6記載の生体計測方法において、
前記計測工程は、
計測対象生体内に生体内局在性の異なる複数のプローブを適用し、異なる生体組織像を分離して同時に画像解析するものであることを特徴とする生体計測方法。
【請求項9】
請求項8記載の生体計測方法において、
前記生体内局在性の異なる複数のプローブは、異なるマーカーで標識されたラベル化合物であることを特徴とする生体計測方法。
【請求項10】
請求項9記載の生体計測方法において、
前記生体内局在性の異なる複数のプローブは、N14及びN15で標識されたニトロキシル化合物であることを特徴とする生体計測方法。
【請求項11】
計測対象生体内に、N14及びN15で標識された生体内局在性の異なる複数のニトロキシプローブを適用する工程と、
前記計測対象を大きさの異なる2つの磁場を適用する工程と、
前記標識を基に検出される信号に基づいて、計測対象生体内の異なる組織像を同時に計測する工程と
を有することを特徴とする生体計測方法。
【請求項12】
請求項11記載の生体計測方法において、
前記大きさの異なる2つの磁場を適用する工程は、さらに、前記計測対象を2つの磁場発生装置の間を移動させる計測対象物移動工程を含むことを特徴とする生体計測方法。
【請求項1】
所定の大きさの磁場を発生させる第1の磁場発生手段と、
前記第1の磁場発生手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段と、
計測対象生体を、RFパルスの照射に同期させて前記第1、第2の磁場発生手段の間で移動させる計測対象物移動手段と、
前記RFパルスに応じて検出される信号に基づいて計測対象生体中の組織像を計測する計測手段と
を有することを特徴とする生体計測装置。
【請求項2】
請求項1記載の生体計測装置において、
前記第2の磁場発生手段は、少なくとも1テスラ以上の磁場を発生させ、核磁気共鳴を励起するためのものであることを特徴とする生体計測装置。
【請求項3】
請求項1記載の生体計測装置において、
前記計測手段は、
計測対象生体内に生体内局在性の異なる複数のプローブを適用し、異なる生体組織像を分離して同時に画像解析するものであることを特徴とする生体計測装置。
【請求項4】
請求項3記載の生体計測装置において、
前記生体内局在性の異なる複数のプローブは、異なるマーカーで標識されたラベル化合物であることを特徴とする生体計測装置。
【請求項5】
請求項4記載の生体計測装置において、
前記生体内局在性の異なる複数のプローブは、N14及びN15で標識されたニトロキシル化合物であることを特徴とする生体計測装置。
【請求項6】
所定の大きさの磁場を発生させる第1の磁場発生手段と、前記第1の磁気共鳴手段の磁場よりも大きい磁場を発生させる第2の磁場発生手段との間で、計測対象生体を、RFパルスの照射に同期させて移動させる計測対象物移動工程と、
前記RFパルスに応じて検出される信号に基づいて、計測対象生体内の組織像を計測する計測工程と
を有することを特徴とする生体計測方法。
【請求項7】
請求項6記載の生体計測方法において、
前記第2の磁場発生手段は、少なくとも1テスラ以上の磁場を発生させ、核磁気共鳴を励起するためのものであることを特徴とする生体計測方法。
【請求項8】
請求項6記載の生体計測方法において、
前記計測工程は、
計測対象生体内に生体内局在性の異なる複数のプローブを適用し、異なる生体組織像を分離して同時に画像解析するものであることを特徴とする生体計測方法。
【請求項9】
請求項8記載の生体計測方法において、
前記生体内局在性の異なる複数のプローブは、異なるマーカーで標識されたラベル化合物であることを特徴とする生体計測方法。
【請求項10】
請求項9記載の生体計測方法において、
前記生体内局在性の異なる複数のプローブは、N14及びN15で標識されたニトロキシル化合物であることを特徴とする生体計測方法。
【請求項11】
計測対象生体内に、N14及びN15で標識された生体内局在性の異なる複数のニトロキシプローブを適用する工程と、
前記計測対象を大きさの異なる2つの磁場を適用する工程と、
前記標識を基に検出される信号に基づいて、計測対象生体内の異なる組織像を同時に計測する工程と
を有することを特徴とする生体計測方法。
【請求項12】
請求項11記載の生体計測方法において、
前記大きさの異なる2つの磁場を適用する工程は、さらに、前記計測対象を2つの磁場発生装置の間を移動させる計測対象物移動工程を含むことを特徴とする生体計測方法。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2006−204551(P2006−204551A)
【公開日】平成18年8月10日(2006.8.10)
【国際特許分類】
【出願番号】特願2005−20556(P2005−20556)
【出願日】平成17年1月28日(2005.1.28)
【出願人】(504145342)国立大学法人九州大学 (960)
【Fターム(参考)】
【公開日】平成18年8月10日(2006.8.10)
【国際特許分類】
【出願日】平成17年1月28日(2005.1.28)
【出願人】(504145342)国立大学法人九州大学 (960)
【Fターム(参考)】
[ Back to top ]

