生体高分子精製装置
【課題】分離性能が高く、かつ、多量の生体高分子試料を精製することができる生体高分子精製装置を提供すること。
【解決手段】電源Pと接続される一対の電極である陽極2及び陰極3と、陽極2が配された陽極バッファ容器(第一電極室)5と、陰極3が配された陰極バッファ容器(第二電極室)6と、陽極バッファ容器5及び陰極バッファ容器6に溶液を出入する移送部7と、第一半透膜8を介して陽極バッファ容器5と陰極バッファ容器6との間に配されたタンパク質容器(精製室)10と、を備えている。
【解決手段】電源Pと接続される一対の電極である陽極2及び陰極3と、陽極2が配された陽極バッファ容器(第一電極室)5と、陰極3が配された陰極バッファ容器(第二電極室)6と、陽極バッファ容器5及び陰極バッファ容器6に溶液を出入する移送部7と、第一半透膜8を介して陽極バッファ容器5と陰極バッファ容器6との間に配されたタンパク質容器(精製室)10と、を備えている。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、タンパク質等の生体高分子の精製装置に関する。
【背景技術】
【0002】
タンパク質等の生体高分子試料を精製するための様々な技術が、多くの研究者により開発されており、関連する機器、装置類も多数市販され、多くの研究者が利用している。
【0003】
高品質なタンパク質結晶のための試料の調製という点に関しては、汎用的な調製方法が確立しているわけではないが、一般論として、均一に荷電した状態のタンパク質等生体高分子試料は、良好な結晶を生成することが知られている。そこで、このような状態にタンパク質等生体高分子試料を精製するために、できるだけ緩和な生化学的条件でイオン交換クロマトグラフィーを適用する場合が多い。
【0004】
ただし、現実にはイオン交換クロマトグラフィーの樹脂に所望のタンパク質等生体高分子試料が吸着しない、あるいは高濃度の塩が共存せざるを得ない等の理由により、イオン交換クロマトグラフィーの適用が難しいタンパク質等生体高分子試料が少なからず存在する。
【0005】
このような試料にも対応可能なものとして、タンパク質等生体高分子試料の荷電状態を利用する連続溶出電気泳動法(例えば、非特許文献1参照。)や、プレパラティブな等電点電気泳動法(例えば、非特許文献2参照。)を用いて精製する技術が開発されている。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】「ゲル電気泳動ガイド」、バイオ・ラッド・ラボラトリーズ株式会社、p39
【非特許文献2】ロバートK・スコープス著、塚田欣司訳、「新・タンパク質精製法」、シュプリンガー・フェアラーク東京株式会社、2004年7月3日、p213−p235
【発明の概要】
【発明が解決しようとする課題】
【0007】
しかしながら、例えば、連続溶出電気泳動法は、分離性能が高くなく、条件設定が難しいといった問題がある。また、等電点電気泳動法は、カラムが詰まりやすいといった問題がある。またX線構造解析向け結晶生成のためのタンパク質等生体高分子試料の精製では、一度に数十mgの試料を精製できることが必要であるが、何れの方法も多量の試料処理には向いていない。
【0008】
本発明は上記事情に鑑みて成されたものであり、分離性能が高く、かつ、多量の生体高分子試料を精製することができる生体高分子精製装置を提供することを目的とする。
【課題を解決するための手段】
【0009】
本発明は、上記課題を解決するため、以下の手段を採用する。
本発明に係る生体高分子精製装置は、電源と接続される一対の電極と、前記一対の電極の一方が配された第一電極室と、前記一対の電極の他方が配された第二電極室と、前記第一電極室及び前記第二電極室内に溶液を出入する移送部と、第一半透膜を介して前記第一電極室と前記第二電極室との間に配された精製室と、を備え、前記精製室内を前記第一電極室側の第一精製室と、前記第二電極室側の第二精製室と、に仕切る第二半透膜が前記精製室に配され、精製する生体高分子を含む溶液が、前記第一精製室又は前記第二精製室に導入されることを特徴とする。
【0010】
この生体高分子精製装置は、精製室内に生体高分子試料を含む溶液を導入し、陽極及び陰極間に電圧印加することによって、生体高分子試料が有する電気的特性に基づく電気泳動によって、生体高分子試料を不純物から分離精製する。この際、第一電極室及び第二電極室内の溶液を移送部によって出入しているので、電気分解によって第一電極室及び第二電極室内で発生する気体を移送部によって容器外へ好適に排出する。
【発明の効果】
【0011】
本発明によれば、分離性能が高く、かつ、多量の生体高分子試料を精製することができる。
【図面の簡単な説明】
【0012】
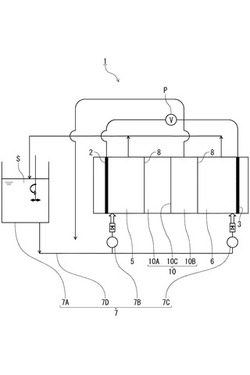
【図1】本発明の一実施形態に係る生体高分子精製装置を示す概要図である。
【図2】本発明の一実施形態に係る生体高分子精製装置の(a)電気泳動前、(b)電気泳動後の状態を示す説明図である。
【発明を実施するための形態】
【0013】
本発明に係る一実施形態について、図1及び図2を参照して説明する。
本実施形態に係る生体高分子精製装置1は、図1に示すように、電源Pと接続される一対の電極である陽極2及び陰極3と、陽極2が配された陽極バッファ容器(第一電極室)5と、陰極3が配された陰極バッファ容器(第二電極室)6と、陽極バッファ容器5及び陰極バッファ容器6に溶液を出入する移送部7と、第一半透膜8を介して陽極バッファ容器5と陰極バッファ容器6との間に配されたタンパク質容器(精製室)10と、を備えている。
【0014】
陽極2及び陰極3は、白金で構成されている。第一半透膜8は、低分子のイオンや化合物は透過するが、タンパク質のような高分子は透過できない膜となっている。
【0015】
移送部7は、精製したいタンパク質を含む溶液Sが貯留された貯留部7Aと、陽極バッファ容器5と連通された第一ポンプ7Bと、陰極バッファ容器6と連通された第二ポンプ7Cと、これらをつなぐ配管7Dと、を備えている。第一ポンプ7B及び第二ポンプ7Cは、溶液Sを一方向に流すようにそれぞれ機能する。
【0016】
タンパク質容器10は、容器内を、陽極バッファ容器5側となる陽極タンパク質容器(第一精製室)10Aと、陰極バッファ容器6側となる陰極タンパク質容器(第二精製室)10Bと、に仕切る第二半透膜10Cと、をさらに備えている。この第二半透膜10Cは、低分子のイオンや化合物及び高分子を透過するが、液体全体は流さない多孔質の膜となっている。
【0017】
次に、本実施形態に係る生体高分子精製装置1の作用について、分離、精製しようとする目的のタンパク質PAと、このタンパク質PAよりも等電点が低い第一不純物PBと、目的とするタンパク質よりも等電点が高い第二不純物PCと、を含む溶液から、目的のタンパク質PAを分離、精製する場合を例として説明する。
【0018】
まずは、上記溶液を陽極タンパク質容器10A内に導入する。次に、目的とするタンパク質PAの等電点よりもpHが低いが、第一不純物PBの等電点よりもpHが高い溶液を、陽極バッファ容器5、陰極タンパク質容器10B、陰極バッファ容器6、貯留部7A内にそれぞれ導入する。
【0019】
そして、移送部7の第一ポンプ7B及び第二ポンプ7Cを駆動して、陽極バッファ容器5及び陰極バッファ容器6内の溶液を交換しながら、陽極2及び陰極3間に電圧を印加する。このとき、目的とするタンパク質PAと第二不純物PCとは、上記pHでは正に電離していることから、電気泳動により、図2(a)に示す状態から、図2(b)に示すように、陽極タンパク質容器10Aから陰極タンパク質容器10Bに移動する。
【0020】
その後、移送部7の第一ポンプ7B及び第二ポンプ7Cをいったん停止するとともに、陽極タンパク質容器10Aから第一不純物PBを排出する。次に、目的とするタンパク質PAと、これよりも等電点が高い第二不純物PCと、を分離、精製する。そのため、陰極タンパク質容器10B中の溶液を残すとともに、陽極バッファ容器5、陽極タンパク質容器10A、陰極バッファ容器6、貯留部7A中に、目的とするタンパク質PAの等電点よりもpHが高いが、第二不純物PCの等電点よりも低いpHとした溶液を導入する。そして、移送部7の第一ポンプ7B及び第二ポンプ7Cを駆動して、陽極バッファ容器5及び陰極バッファ容器6内の溶液を交換しながら、陽極2及び陰極3間に電圧を印加する。
【0021】
この際、目的とするタンパク質PAは負に電離していることから、陰極タンパク質容器10Bから陽極方向となる陽極タンパク質容器10Aに電気泳動により移動する。こうして、目的とするタンパク質PAが、陽極タンパク質容器10Aに集まる。
【0022】
この生体高分子精製装置1によれば、タンパク質試料を緩和な可溶化した溶液条件下で、その電気的特性のみで分離、精製することができ、高品質な結晶に向くタンパク質試料の大量調製を行うことができる。
【0023】
このとき、陽極バッファ容器5及び陰極バッファ容器6内の溶液を移送部7によって出入しているので、電気分解によって陽極バッファ容器5及び陰極バッファ容器6内で発生する気体を移送部7によって容器外へ好適に排出することができる。そのため、電気分解の効率を好適に維持することができる。
【0024】
なお、本発明の技術範囲は上記実施の形態に限定されるものではなく、本発明の趣旨を逸脱しない範囲において種々の変更を加えることが可能である。
例えば、陽極2及び陰極3は、平面状でも線状でも構わない。
【実施例1】
【0025】
生体高分子精製装置1を用いて、表1に示す条件にてタンパク質試料を実際に移動させて分離精製機能を確認した。結果を表2に示す。
【0026】
【表1】

【0027】
【表2】

【0028】
Lysozymeは、pH6.7の条件では正電荷を持っており、陰極側へ移動する。ここで、表3に示す卵白アルブミンの移動度の値から類推して、pH6.7でのLysozymeの移動度は、15×105cm2S−1V−1程度と思われる。この値を用い、上記条件で移動距離を求めると5V印加の10分間では、0.3cmとなるはずである。
【0029】
【表3】

【0030】
本実施例では、タンパク質容器10の第二半透膜10Cの厚みを0.5cmとしていることを考えると、密度差対流がまったくなければ、60%程度のタンパク質が陰極タンパク質容器10Bに移るはずである。実際には対流が生じることから、上記量の1/2〜1/3程度が妥当と思われるところ、1/6程度が移動していた。ただし、最終的に両容器で回収されたタンパク質量は、最初の量の84%であり、概ね良好な結果が得られた。
【符号の説明】
【0031】
1 生体高分子精製装置
2 陽極(一対の電極の一方)
3 陰極(一対の電極の他方)
5 陽極バッファ容器(第一電極室)
6 陰極バッファ容器(第二電極室)
7 移送部
8 第一半透膜
10 タンパク質容器(精製室)
10A 陽極タンパク質容器(第一精製室)
10B 陰極タンパク質容器(第二精製室)
10C 第二半透膜
【技術分野】
【0001】
本発明は、タンパク質等の生体高分子の精製装置に関する。
【背景技術】
【0002】
タンパク質等の生体高分子試料を精製するための様々な技術が、多くの研究者により開発されており、関連する機器、装置類も多数市販され、多くの研究者が利用している。
【0003】
高品質なタンパク質結晶のための試料の調製という点に関しては、汎用的な調製方法が確立しているわけではないが、一般論として、均一に荷電した状態のタンパク質等生体高分子試料は、良好な結晶を生成することが知られている。そこで、このような状態にタンパク質等生体高分子試料を精製するために、できるだけ緩和な生化学的条件でイオン交換クロマトグラフィーを適用する場合が多い。
【0004】
ただし、現実にはイオン交換クロマトグラフィーの樹脂に所望のタンパク質等生体高分子試料が吸着しない、あるいは高濃度の塩が共存せざるを得ない等の理由により、イオン交換クロマトグラフィーの適用が難しいタンパク質等生体高分子試料が少なからず存在する。
【0005】
このような試料にも対応可能なものとして、タンパク質等生体高分子試料の荷電状態を利用する連続溶出電気泳動法(例えば、非特許文献1参照。)や、プレパラティブな等電点電気泳動法(例えば、非特許文献2参照。)を用いて精製する技術が開発されている。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】「ゲル電気泳動ガイド」、バイオ・ラッド・ラボラトリーズ株式会社、p39
【非特許文献2】ロバートK・スコープス著、塚田欣司訳、「新・タンパク質精製法」、シュプリンガー・フェアラーク東京株式会社、2004年7月3日、p213−p235
【発明の概要】
【発明が解決しようとする課題】
【0007】
しかしながら、例えば、連続溶出電気泳動法は、分離性能が高くなく、条件設定が難しいといった問題がある。また、等電点電気泳動法は、カラムが詰まりやすいといった問題がある。またX線構造解析向け結晶生成のためのタンパク質等生体高分子試料の精製では、一度に数十mgの試料を精製できることが必要であるが、何れの方法も多量の試料処理には向いていない。
【0008】
本発明は上記事情に鑑みて成されたものであり、分離性能が高く、かつ、多量の生体高分子試料を精製することができる生体高分子精製装置を提供することを目的とする。
【課題を解決するための手段】
【0009】
本発明は、上記課題を解決するため、以下の手段を採用する。
本発明に係る生体高分子精製装置は、電源と接続される一対の電極と、前記一対の電極の一方が配された第一電極室と、前記一対の電極の他方が配された第二電極室と、前記第一電極室及び前記第二電極室内に溶液を出入する移送部と、第一半透膜を介して前記第一電極室と前記第二電極室との間に配された精製室と、を備え、前記精製室内を前記第一電極室側の第一精製室と、前記第二電極室側の第二精製室と、に仕切る第二半透膜が前記精製室に配され、精製する生体高分子を含む溶液が、前記第一精製室又は前記第二精製室に導入されることを特徴とする。
【0010】
この生体高分子精製装置は、精製室内に生体高分子試料を含む溶液を導入し、陽極及び陰極間に電圧印加することによって、生体高分子試料が有する電気的特性に基づく電気泳動によって、生体高分子試料を不純物から分離精製する。この際、第一電極室及び第二電極室内の溶液を移送部によって出入しているので、電気分解によって第一電極室及び第二電極室内で発生する気体を移送部によって容器外へ好適に排出する。
【発明の効果】
【0011】
本発明によれば、分離性能が高く、かつ、多量の生体高分子試料を精製することができる。
【図面の簡単な説明】
【0012】
【図1】本発明の一実施形態に係る生体高分子精製装置を示す概要図である。
【図2】本発明の一実施形態に係る生体高分子精製装置の(a)電気泳動前、(b)電気泳動後の状態を示す説明図である。
【発明を実施するための形態】
【0013】
本発明に係る一実施形態について、図1及び図2を参照して説明する。
本実施形態に係る生体高分子精製装置1は、図1に示すように、電源Pと接続される一対の電極である陽極2及び陰極3と、陽極2が配された陽極バッファ容器(第一電極室)5と、陰極3が配された陰極バッファ容器(第二電極室)6と、陽極バッファ容器5及び陰極バッファ容器6に溶液を出入する移送部7と、第一半透膜8を介して陽極バッファ容器5と陰極バッファ容器6との間に配されたタンパク質容器(精製室)10と、を備えている。
【0014】
陽極2及び陰極3は、白金で構成されている。第一半透膜8は、低分子のイオンや化合物は透過するが、タンパク質のような高分子は透過できない膜となっている。
【0015】
移送部7は、精製したいタンパク質を含む溶液Sが貯留された貯留部7Aと、陽極バッファ容器5と連通された第一ポンプ7Bと、陰極バッファ容器6と連通された第二ポンプ7Cと、これらをつなぐ配管7Dと、を備えている。第一ポンプ7B及び第二ポンプ7Cは、溶液Sを一方向に流すようにそれぞれ機能する。
【0016】
タンパク質容器10は、容器内を、陽極バッファ容器5側となる陽極タンパク質容器(第一精製室)10Aと、陰極バッファ容器6側となる陰極タンパク質容器(第二精製室)10Bと、に仕切る第二半透膜10Cと、をさらに備えている。この第二半透膜10Cは、低分子のイオンや化合物及び高分子を透過するが、液体全体は流さない多孔質の膜となっている。
【0017】
次に、本実施形態に係る生体高分子精製装置1の作用について、分離、精製しようとする目的のタンパク質PAと、このタンパク質PAよりも等電点が低い第一不純物PBと、目的とするタンパク質よりも等電点が高い第二不純物PCと、を含む溶液から、目的のタンパク質PAを分離、精製する場合を例として説明する。
【0018】
まずは、上記溶液を陽極タンパク質容器10A内に導入する。次に、目的とするタンパク質PAの等電点よりもpHが低いが、第一不純物PBの等電点よりもpHが高い溶液を、陽極バッファ容器5、陰極タンパク質容器10B、陰極バッファ容器6、貯留部7A内にそれぞれ導入する。
【0019】
そして、移送部7の第一ポンプ7B及び第二ポンプ7Cを駆動して、陽極バッファ容器5及び陰極バッファ容器6内の溶液を交換しながら、陽極2及び陰極3間に電圧を印加する。このとき、目的とするタンパク質PAと第二不純物PCとは、上記pHでは正に電離していることから、電気泳動により、図2(a)に示す状態から、図2(b)に示すように、陽極タンパク質容器10Aから陰極タンパク質容器10Bに移動する。
【0020】
その後、移送部7の第一ポンプ7B及び第二ポンプ7Cをいったん停止するとともに、陽極タンパク質容器10Aから第一不純物PBを排出する。次に、目的とするタンパク質PAと、これよりも等電点が高い第二不純物PCと、を分離、精製する。そのため、陰極タンパク質容器10B中の溶液を残すとともに、陽極バッファ容器5、陽極タンパク質容器10A、陰極バッファ容器6、貯留部7A中に、目的とするタンパク質PAの等電点よりもpHが高いが、第二不純物PCの等電点よりも低いpHとした溶液を導入する。そして、移送部7の第一ポンプ7B及び第二ポンプ7Cを駆動して、陽極バッファ容器5及び陰極バッファ容器6内の溶液を交換しながら、陽極2及び陰極3間に電圧を印加する。
【0021】
この際、目的とするタンパク質PAは負に電離していることから、陰極タンパク質容器10Bから陽極方向となる陽極タンパク質容器10Aに電気泳動により移動する。こうして、目的とするタンパク質PAが、陽極タンパク質容器10Aに集まる。
【0022】
この生体高分子精製装置1によれば、タンパク質試料を緩和な可溶化した溶液条件下で、その電気的特性のみで分離、精製することができ、高品質な結晶に向くタンパク質試料の大量調製を行うことができる。
【0023】
このとき、陽極バッファ容器5及び陰極バッファ容器6内の溶液を移送部7によって出入しているので、電気分解によって陽極バッファ容器5及び陰極バッファ容器6内で発生する気体を移送部7によって容器外へ好適に排出することができる。そのため、電気分解の効率を好適に維持することができる。
【0024】
なお、本発明の技術範囲は上記実施の形態に限定されるものではなく、本発明の趣旨を逸脱しない範囲において種々の変更を加えることが可能である。
例えば、陽極2及び陰極3は、平面状でも線状でも構わない。
【実施例1】
【0025】
生体高分子精製装置1を用いて、表1に示す条件にてタンパク質試料を実際に移動させて分離精製機能を確認した。結果を表2に示す。
【0026】
【表1】

【0027】
【表2】

【0028】
Lysozymeは、pH6.7の条件では正電荷を持っており、陰極側へ移動する。ここで、表3に示す卵白アルブミンの移動度の値から類推して、pH6.7でのLysozymeの移動度は、15×105cm2S−1V−1程度と思われる。この値を用い、上記条件で移動距離を求めると5V印加の10分間では、0.3cmとなるはずである。
【0029】
【表3】

【0030】
本実施例では、タンパク質容器10の第二半透膜10Cの厚みを0.5cmとしていることを考えると、密度差対流がまったくなければ、60%程度のタンパク質が陰極タンパク質容器10Bに移るはずである。実際には対流が生じることから、上記量の1/2〜1/3程度が妥当と思われるところ、1/6程度が移動していた。ただし、最終的に両容器で回収されたタンパク質量は、最初の量の84%であり、概ね良好な結果が得られた。
【符号の説明】
【0031】
1 生体高分子精製装置
2 陽極(一対の電極の一方)
3 陰極(一対の電極の他方)
5 陽極バッファ容器(第一電極室)
6 陰極バッファ容器(第二電極室)
7 移送部
8 第一半透膜
10 タンパク質容器(精製室)
10A 陽極タンパク質容器(第一精製室)
10B 陰極タンパク質容器(第二精製室)
10C 第二半透膜
【特許請求の範囲】
【請求項1】
電源と接続される一対の電極と、
前記一対の電極の一方が配された第一電極室と、
前記一対の電極の他方が配された第二電極室と、
前記第一電極室及び前記第二電極室内に溶液を出入する移送部と、
第一半透膜を介して前記第一電極室と前記第二電極室との間に配された精製室と、
を備え、
前記精製室内を前記第一電極室側の第一精製室と、前記第二電極室側の第二精製室と、に仕切る第二半透膜が前記精製室に配され、精製する生体高分子を含む溶液が、前記第一精製室又は前記第二精製室に導入されることを特徴とする生体高分子精製装置。
【請求項1】
電源と接続される一対の電極と、
前記一対の電極の一方が配された第一電極室と、
前記一対の電極の他方が配された第二電極室と、
前記第一電極室及び前記第二電極室内に溶液を出入する移送部と、
第一半透膜を介して前記第一電極室と前記第二電極室との間に配された精製室と、
を備え、
前記精製室内を前記第一電極室側の第一精製室と、前記第二電極室側の第二精製室と、に仕切る第二半透膜が前記精製室に配され、精製する生体高分子を含む溶液が、前記第一精製室又は前記第二精製室に導入されることを特徴とする生体高分子精製装置。
【図1】


【図2】




【図2】


【公開番号】特開2012−41286(P2012−41286A)
【公開日】平成24年3月1日(2012.3.1)
【国際特許分類】
【出願番号】特願2010−182620(P2010−182620)
【出願日】平成22年8月17日(2010.8.17)
【出願人】(507312426)株式会社コンフォーカルサイエンス (1)
【Fターム(参考)】
【公開日】平成24年3月1日(2012.3.1)
【国際特許分類】
【出願日】平成22年8月17日(2010.8.17)
【出願人】(507312426)株式会社コンフォーカルサイエンス (1)
【Fターム(参考)】
[ Back to top ]

