生物分解性ポリエチレングリコール系水不溶性ヒドロゲル
本発明は、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分(ここで、該バックボーン部分は、さらに、反応性官能基を含んでいる)を含んでいる生物分解性ポリエチレングリコール系水不溶性ヒドロゲルに関し、ここで、前記水不溶性ヒドロゲルは、分解可能な結合の加水分解によって前記ヒドロゲルが1以上のバックボーン部分を含んでいる水溶性分解産物に完全に分解されるための時間と前記ヒドロゲルの中のバックボーン部分の総量に基づいて1以上のバックボーン部分を含んでいる水溶性分解産物の最初の10mol-%が放出されるための時間の間の比率が1より大きく且つ2以下であるということをさらに特徴とする。本発明は、さらに、そのようなヒドロゲルとリガンド又は連結基(ligating group)のコンジュゲート、プロドラッグ及び医薬組成物、さらに、薬物中におけるそれらの使用にも関する。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
加水分解的に分解可能な結合によって相互に連結されているバックボーン部分(ここで、該バックボーン部分は、さらに、反応性官能基を含んでいる)を含んでいる生物分解性ポリ(エチレングリコール)系水不溶性ヒドロゲルであって、前記水不溶性ヒドロゲルが、分解可能な結合の加水分解によって前記ヒドロゲルが1以上のバックボーン部分を含んでいる水溶性分解産物に完全に分解されるための時間と前記ヒドロゲルの中のバックボーン部分の総量に基づいて1以上のバックボーン部分を含んでいる水溶性分解産物の最初の10mol-%が放出されるための時間の間の比率が1より大きく且つ2以下であるということをさらに特徴とする、前記生物分解性ポリ(エチレングリコール)系水不溶性ヒドロゲル。
【請求項2】
前記加水分解的に分解可能な結合が、アコニチル類、アセタール類、カルボン酸無水物類、エステル類、イミン類、ヒドラゾン類、マレアミド酸アミド類、オルトエステル類、ホスファミド類、ホスホエステル類、ホスホシリルエステル類、シリルエステル類、スルホン酸エステル類、芳香族カルバメート類及びそれらの組合せからなる群から選択される、請求項1に記載のヒドロゲル。
【請求項3】
前記反応性官能基が、カルボン酸及び活性化誘導体、アミノ、マレイミド、チオール、スルホン酸及び誘導体、カルボネート及び誘導体、カルバメート及び誘導体、ヒドロキシル、アルデヒド、ケトン、ヒドラジン、イソシアネート、イソチオシアネート、リン酸及び誘導体、ホスホン酸及び誘導体、ハロアセチル、アルキルハロゲン化物、アクリロイル及び別のα-β不飽和マイケル受容体、アリール化剤(例えば、フッ化アリール)、ヒドロキシルアミン、ジスルフィド(例えば、ピリジルジスルフィド)、ビニルスルホン、ビニルケトン、ジアゾアルカン、ジアゾアセチル化合物、オキシラン並びにアジリジンからなる群から選択される、請求項1又は2に記載のヒドロゲル。
【請求項4】
前記バックボーン部分が1kDa〜20kDaの範囲内にある分子量を有している、請求項1〜3のいずれかに記載のヒドロゲル。
【請求項5】
前記バックボーン部分がクロスリンカー部分(ここで、各クロスリンカー部分は、加水分解的に分解可能な結合のうちの少なくとも2によって終結されている)を介して互いに結合している、請求項1〜4のいずれかに記載のヒドロゲル。
【請求項6】
前記クロスリンカー部分が0.5kDa〜5kDaの範囲内にある分子量を有している、請求項5に記載のヒドロゲル。
【請求項7】
各クロスリンカー部分がPEG系である、請求項5又は6に記載のヒドロゲル。
【請求項8】
各クロスリンカー部分が1つのPEG系分子鎖によって表される、請求項7に記載のヒドロゲル。
【請求項9】
各バックボーン部分が、合計で少なくとも16の相互に連結されている生物分解性で反応性の官能基を含んでいる、請求項1〜8のいずれかに記載のヒドロゲル。
【請求項10】
前記バックボーン部分が、式
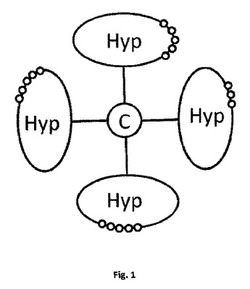
C(A-Hyp)4
〔式中、各Aは、独立して、末端が永久的な共有結合によって当該第4級炭素に結合しているポリ(エチレングリコール)系ポリマー鎖であって、そのポリマー鎖の遠位末端は樹枝状部分Hypに共有結合的に結合しており、ここで、各樹枝状部分Hypは、相互に連結されている官能基及び反応性官能基を表す少なくとも4つの官能基を有している〕
で表される第4級炭素を有している、請求項9に記載のヒドロゲル。
【請求項11】
請求項1〜10のいずれかに記載のヒドロゲルを含んでいるコンジュゲートであって、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分で構成されていること、及び、付加的にスペーサー分子又は遮断基を有していることを特徴とする、前記コンジュゲート。
【請求項12】
請求項1〜10のいずれかに記載のヒドロゲルを含んでいるコンジュゲートであって、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分で構成されていること、及び、付加的にリガンド又はキレート基に対する永久的な結合を有していることを特徴とする、前記コンジュゲート。
【請求項13】
担体として請求項1〜10のいずれかに記載のヒドロゲルを含んでいる担体結合プロドラッグであって、生物学的に活性な部分Dが共有結合的に結合している一時的なプロドラッグリンカーLと一緒に、バックボーン部分の多数の永久的な結合が存在している、前記担体結合プロドラッグ。
【請求項14】
前記生物学的に活性な部分Dが、ポリペプチド、タンパク質、オリゴヌクレオチド又は生物学的に活性な小分子部分である、請求項13に記載の担体結合プロドラッグ。
【請求項15】
前記生物学的に活性な部分Dがアミン基、ヒドロキシル基、カルボキシル基、ホスフェート基又はメルカプト基を含んでいて、前記生物学的に不活性なリンカーLがそのアミン基、ヒドロキシル基、カルボキシル基、ホスフェート基又はメルカプト基と一緒にコンジュゲートD-Lを形成する、請求項14に記載の担体結合プロドラッグ。
【請求項16】
DとLの間の結合が、カルバメート結合、カルボネート結合、アミド結合又はエステル結合である、請求項13〜15のいずれかに記載の担体結合プロドラッグ。
【請求項17】
前記一時的なプロドラッグリンカーLが部分L2で置換されている部分L1を含んでおり、その際、L2は、請求項1〜10のいずれかに記載のヒドロゲルである担体基Zに結合している、請求項12〜14のいずれかに記載の担体結合プロドラッグ。
【請求項18】
L2が、下記構造
【化1】

〔ここで、破線は、それぞれ、L2及びZに結合していることを示している〕
を有する末端基を介してZに結合している、請求項16に記載の担体結合プロドラッグ。
【請求項19】
前記生物学的に活性な部分が芳香族アミンを含んでおり、及び、前記一時的なプロドラッグリンカーが、
(i) 式(VIII)
【化2】

〔式中、
破線は、アミド結合を形成することによってL1が生物学的に活性な部分Dの芳香族アミノ基に結合していることを示しており;
X1は、C(R1R1a)であるか、又は、C3-7シクロアルキル、4〜7員のヘテロシクリル、フェニル、ナフチル、インデニル、インダニル、テトラリニル若しくは9〜11員のヘテロビシクリルから選択される環状フラグメントであり;
X2は、化学結合であるか、又は、C(R3R3a)、N(R3)、O、C(R3R3a)-C(R4R4a)、C(R3R3a)-N(R4)、N(R3)-C(R4R4a)、C(R3R3a)-O若しくはO-C(R3R3a)から選択され;
ここで、X1が環状フラグメントである場合、X2は、化学結合、C(R3R3a)、N(R3)又はOであり;
場合により、X1が環状フラグメントであり且つX2がC(R3R3a)である場合、L1内のX1フラグメントとX2フラグメントの順番は変えられてもよく;
R1、R3及びR4は、独立して、H、C1-4アルキル及び-N(R5R5a)からなる群から選択され;
R1a、R2、R2a、R3a、R4a及びR5aは、独立して、H及びC1-4アルキルからなる群から選択され;
場合により、対R2a/R2、対R2a/R3a、対R2a/R4aのうちの1つは、一緒になって4〜7員の少なくとも部分的に飽和しているヘテロ環を形成してもよく;
R5は、C(O)R6であり;
R6は、C1-4アルキルであり;
場合により、対R1a/R4a、対R3a/R4a又は対R1a/R3aのうちの1つは、化学結合を形成してもよく;
場合により、L1は、さらに置換されていてもよい〕
で表される部分L1;
(ii) 部分L2(ここで、L2は化学結合又はスペーサーであり、及び、L2は請求項1〜10のいずれかに記載のヒドロゲルを表す担体基Zに結合している);
を含んでいる生物学的に不活性なリンカーL〔ここで、L1は1つのL2部分で置換されているが、但し、式(VIII)において星印が付けられている水素はL2で置き換えられず;場合により、Lは、さらに置換されてもよい〕である、請求項17に記載の担体結合プロドラッグ。
【請求項20】
前記生物学的に活性な部分Dが第1級又は第2級の脂肪族アミンを含んでおり、及び、本発明のプロドラッグに関する好ましい構造がプロドラッグコンジュゲートD-Lによって与えられ、ここで、
Dは、第1級又は第2級の脂肪族アミンを含んでいる生物学的に活性な部分であり;及び、
Lは、式(VI)
【化3】

〔式中、
破線は、アミド結合を形成することによって生物学的に活性な部分の第1級又は第2級の脂肪族アミン基に結合していることを示しており;
Xは、C(R4R4a)、N(R4)、O、C(R4R4a)-C(R5R5a)、C(R5R5a)-C(R4R4a)、C(R4R4a)-N(R6)、N(R6)-C(R4R4a)、C(R4R4a)-O又はO-C(R4R4a)であり;
X1は、C又はS(O)であり;
X2は、C(R7,R7a)又はC(R7,R7a)-C(R8,R8a)であり;
R1、R1a、R2、R2a、R3、R3a、R4、R4a、R5、R5a、R6、R7、R7a、R8、R8aは、独立して、H及びC1-4アルキルからなる群から選択され;又は、
場合により、対R1a/R4a、対R1a/R5a、対R4a/R5a、対R4a/R5a、対R7a/R8aのうちの1以上は、化学結合を形成してもよく;
場合により、対R1/R1a、対R2/R2a、対R4/R4a、対R5/R5a、対R7/R7a、対R8/R8aのうちの1以上は、それらが結合している原子と一緒になってC3-7シクロアルキル又は4〜7員のヘテロシクリルを形成してもよく;
場合により、対R1/R4、対R1/R5、対R1/R6、対R4/R5、対R7/R8、対R2/R3のうちの1以上は、それらが結合している原子と一緒になって環Aを形成してもよく;
場合により、R3/R3aは、それらが結合している窒素原子と一緒になって4〜7員のヘテロ環を形成してもよく;
Aは、フェニル、ナフチル、インデニル、インダニル、テトラリニル、C3-10シクロアルキル、4〜7員のヘテロシクリル及び9〜11員のヘテロビシクリルからなる群から選択され;及び、
ここで、L1は、1つの基L2-Zで置換されており、及び、場合によりさらに置換されていてもよいが、但し、式(VI)において星印が付けられている水素は置換基で置き換えられず;
ここで、
L2は、単一の化学結合又はスペーサーであり;及び、
Zは、請求項1〜10のいずれかに記載のヒドロゲルである〕
で表される生物学的に不活性なリンカー部分-L1である;
請求項17に記載の担体結合プロドラッグ。
【請求項21】
前記生物学的に活性な部分Dがヒドロキシル基を含んでおり、及び、当該プロドラッグに関する構造が、式(X)
D-O-Z0 (X)
〔式中、
Dは、ヒドロキシル基の酸素を介して部分Z0に結合している、ヒドロキシル基を含んでいる生物学的に活性な部分であり;
Z0は、C(O)-X0-Z1、C(O)O-X0-Z1、S(O)2-X0-Z1、C(S)-X0-Z1、S(O)2O-X0-Z1、S(O)2N(R1)-X0-Z1、CH(OR1)-X0-Z1、C(OR1)(OR2)-X0-Z1、C(O)N(R1)-X0-Z1、P(=O)(OH)O-X0-Z1、P(=O)(OR1)O-X0-Z1、P(=O)(SH)O-X0-Z1、P(=O)(SR1)O-X0-Z1、P(=O)(OR1)-X0-Z1、P(=S)(OH)O-X0-Z1、P(=S)(OR1)O-X0-Z1、P(=S)(OH)N(R1)-X0-Z1、P(=S)(OR1)N(R2)-X0-Z1、P(=O)(OH)N(R1)-X0-Z1又はP(=O)(OR1)N(R2)-X0-Z1であり;
R1、R2は、独立して、C1-6アルキルからなる群から選択され;又は、R1、R2は、一緒になってC1-6アルキレン架橋基を形成し;
X0は、(X0A)m1-(X0B)m2であり;
m1、m2は、独立して、0又は1であり;
X0Aは、T0であり;
X0Bは、同一であるか若しくは異なっている1以上のR3で置換されているか又は置換されていない分枝鎖又は非分枝鎖のC1-10アルキレン基であり;
R3は、ハロゲン、CN、C(O)R4、C(O)OR4、OR4、C(O)R4、C(O)N(R4R4a)、S(O)2N(R4R4a)、S(O)N(R4R4a)、S(O)2R4、S(O)R4、N(R4)S(O)2N(R4aR4b)、SR4、N(R4R4a)、NO2、OC(O)R4、N(R4)C(O)R4a、N(R4)SO2R4a、N(R4)S(O)R4a、N(R4)C(O)N(R4aR4b)、N(R4)C(O)OR4a、OC(O)N(R4R4a)又はT0であり;
R4、R4a、R4bは、独立して、H、T0、C1-4アルキル、C2-4アルケニル及びC2-4アルキニルからなる群から選択され(ここで、C1-4アルキル、C2-4アルケニル及びC2-4アルキニルは、同一であるか又は異なっている1以上のR5で場合により置換されていてもよい);
R5は、ハロゲン、CN、C(O)R6、C(O)OR6、OR6、C(O)R6、C(O)N(R6R6a)、S(O)2N(R6R6a)、S(O)N(R6R6a)、S(O)2R6、S(O)R6、N(R6)S(O)2N(R6aR6b)、SR6、N(R6R6a)、NO2、OC(O)R6、N(R6)C(O)R6a、N(R6)SO2R6a、N(R6)S(O)R6a、N(R6)C(O)N(R6aR6b)、N(R6)C(O)OR6a、OC(O)N(R6R6a)であり;
R6、R6a、R6bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のハロゲンで場合により置換されていてもよい);
T0は、フェニル、ナフチル、アズレニル、インデニル、インダニル、C3-7シクロアルキル、3〜7員のヘテロシクリル又は8〜11員のヘテロビシクリルであり(ここで、T0は、同一であるか又は異なっている1以上のR7で場合により置換されていてもよい);
R7は、ハロゲン、CN、COOR8、OR8、C(O)R8、C(O)N(R8R8a)、S(O)2N(R8R8a)、S(O)N(R8R8a)、S(O)2R8、S(O)R8、N(R8)S(O)2N(R8aR8b)、SR8、N(R8R8a)、NO2、OC(O)R8、N(R8)C(O)R8a、N(R8)S(O)2R8a、N(R8)S(O)R8a、N(R8)C(O)OR8a、N(R8)C(O)N(R8aR8b)、OC(O)N(R8R8a)、オキソ(=O)(ここで、該環は少なくとも部分的に飽和している)、C1-6アルキル、C2-6アルケニル又はC2-6アルキニルであり(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のR9で場合により置換されていてもよい);
R8、R8a、R8bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のR10で場合により置換されていてもよい);
R9、R10は、独立して、ハロゲン、CN、C(O)R11、C(O)OR11、OR11、C(O)R11、C(O)N(R11R11a)、S(O)2N(R11R11a)、S(O)N(R11R11a)、S(O)2R11、S(O)R11、N(R11)S(O)2N(R11aR11b)、SR11、N(R11R11a)、NO2、OC(O)R11、N(R11)C(O)R11a、N(R11)SO2R11a、N(R11)S(O)R11a、N(R11)C(O)N(R11aR11b)、N(R11)C(O)OR11a及びOC(O)N(R11R11a)からなる群から選択され;
R11、R11a、R11bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のハロゲンで場合により置換されていてもよい);
Z1は、X0に共有結合的に結合している、請求項1〜10のいずれかに記載のヒドロゲルである〕
で表されるプロドラッグコンジュゲートによって与えられる、請求項17に記載の担体結合プロドラッグ。
【請求項22】
前記生物学的に活性な部分Dが芳香族ヒドロキシル基を含んでおり、及び、前記プロドラッグリンカーが、
(i) 式(XI)
【化4】

〔式中、
破線は、カルバメート基を形成することによってL1が生物学的に活性な部分Dの芳香族ヒドロキシル基に結合していることを示しており;
R1は、C1-4アルキル、ヘテロアルキル、C3-7シクロアルキル及び
【化5】

からなる群から選択され;及び、
;
R2、R2a、R3、R3aは、独立して、水素、置換されているか若しくは置換されていない直鎖若しくは分枝鎖若しくは環状のC1-4アルキル又はヘテロアルキルから選択され;
mは、独立して、2、3又は4である〕
で表される部分L1;
(iii) 部分L2(ここで、L2は化学結合又はスペーサーであり、及び、L2は請求項1〜10のいずれかに記載のヒドロゲルに結合している);
を含んでいる生物学的に不活性なリンカーL〔ここで、L1は1つのL2部分で置換されており;場合により、Lは、さらに置換されてもよい〕である、請求項17に記載の担体結合プロドラッグ。
【請求項23】
製薬上許容される賦形剤と一緒に請求項12〜22のいずれかに記載のプロドラッグ又はその薬学的な塩を含んでいる、医薬組成物。
【請求項24】
薬物中で使用するための、請求項12〜22のいずれかに記載のプロドラッグ又は請求項23に記載の医薬組成物。
【請求項25】
1以上の状態を治療することが必要な哺乳類患者において、治療する方法、制御する方法、遅延させる方法又は予防する方法であって、該患者に治療有効量の請求項12〜22のいずれかに記載のプロドラッグ又は請求項23に記載の医薬組成物又はそれらの製薬上許容される塩を投与することを含む、前記方法。
【請求項26】
加水分解的に分解可能な結合によって相互に連結されているバックボーン部分を含んでいる生物分解性ポリ(エチレングリコール)系水不溶性ヒドロゲルであって、該バックボーン部分が、1kDa〜20kDaの範囲内にある分子量を有していること、及び、構造C*-(A-Hyp)x〔ここで、
C*は、分枝コアであり;
Aは、ポリ(エチレングリコール)系ポリマー鎖であり;
Hypは、高分岐樹枝状部分であり;
xは、3〜16の整数であり;
及び、ここで、前記高分岐樹枝状部分は、さらに、反応性官能基及び相互に連結されている官能基を含んでいる〕
を有していることを特徴とする、前記生物分解性ポリ(エチレングリコール)系水不溶性ヒドロゲル。
【請求項27】
前記バックボーン部分がクロスリンカー部分を介して互いに結合しており、各クロスリンカー部分は加水分解的に分解可能な結合のうちの少なくとも2によって終結されている、請求項26に記載の生物分解性ヒドロゲル。
【請求項28】
前記クロスリンカー部分が0.5kDa〜5kDaの範囲内にある分子量を有している、請求項27に記載の生物分解性ヒドロゲル。
【請求項29】
各クロスリンカー部分がPEG系である、請求項27又は28に記載の生物分解性ヒドロゲル。
【請求項30】
各クロスリンカー部分が1つのポリ(エチレングリコール)系ポリマー鎖によって表される、請求項29に記載の生物分解性ヒドロゲル。
【請求項31】
各バックボーン部分が、合計で少なくとも16の相互に連結されている生物分解性で反応性の官能基を含んでいる、請求項26〜30のいずれかに記載の生物分解性ヒドロゲル。
【請求項32】
前記バックボーン部分が、式
C(A-Hyp)4
〔式中、各Aは、独立して、末端が永久的な共有結合によって第4級炭素に結合しているポリ(エチレングリコール)系ポリマー鎖であって、そのポリマー鎖の遠位末端は樹枝状部分Hypに共有結合的に結合しており、ここで、各樹枝状部分Hypは、相互に連結されている官能基及び反応性官能基を表す少なくとも4つの官能基を有している〕
で表される第4級炭素を有している、請求項31に記載の生物分解性ヒドロゲル。
【請求項33】
前記バックボーン部分が、下記式:
【化6】

〔式中、破線は、当該バックボーン部分の残部に結合していることを示している〕
で表される分枝コアを含んでいる、請求項10又は32に記載の生物分解性ヒドロゲル。
【請求項34】
前記バックボーン部分が、下記式:
【化7】

〔式中、nは5〜50の整数であり、及び、破線は、当該分子の残部に結合していることを示している〕
で表される構造を含んでいる、請求項33に記載の生物分解性ヒドロゲル。
【請求項35】
前記バックボーン部分が、下記式:
【化8】

〔式中、破線は、当該分子の残部に結合していることを示しており、及び、星印が付けられている炭素原子はS-立体配置を示している〕
で表される高分岐部分Hypを含んでいる、請求項33又は34に記載の生物分解性ヒドロゲル。
【請求項36】
前記バックボーン部分が、下記式:
【化9】

〔式中、
破線のうちの一方は、高分岐部分Hypに結合していることを示しており、及び、第2の破線は、当該分子の残部に結合していることを示しており;並びに、
mは、2〜4の整数である〕
で表される少なくとも1つのスペーサーを含んでいる、請求項33〜35のいずれかに記載の生物分解性ヒドロゲル。
【請求項37】
前記バックボーン部分が、下記式:
【化10】

〔式中、
星印が付けられている破線は、当該ヒドロゲルと請求項17のチオスクシンイミド基のNの間の結合を示しており;
もう一方の破線は、Hypに結合していることを示しており;及び、
pは、0〜10の整数である〕
で表される少なくとも1つのスペーサーを含んでいる、請求項33〜36のいずれかに記載の生物分解性ヒドロゲル。
【請求項38】
前記バックボーン部分が、下記構造
【化11】

〔ここで、qは、3〜100の整数である〕
を含んでいるクロスリンカー部分を介して互いに結合している、請求項33〜37のいずれかに記載の生物分解性ヒドロゲル。
【請求項39】
請求項26〜38のいずれかに記載のヒドロゲル(ここで、該ヒドロゲルは、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分で構成されている)を含んでおり、及び、付加的にスペーサー分子又は遮断基又はそれらの組合せに対する永久的な結合を有している、コンジュゲート。
【請求項40】
請求項26〜38のいずれかに記載のヒドロゲル(ここで、該ヒドロゲルは、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分で構成されている)を含んでおり、及び、付加的にリガンド又はキレート基に対する永久的な結合を有している、コンジュゲート。
【請求項41】
担体として請求項26〜38のいずれかに記載の生物分解性ヒドロゲルを含んでいる担体結合プロドラッグであって、バックボーン部分の多数の永久的な結合が、それぞれ、生物学的に活性な部分Dが共有結合的に結合している一時的なプロドラッグリンカーLと一緒に存在している、前記担体結合プロドラッグ。
【請求項42】
前記生物学的に活性な部分Dが、ポリペプチド、タンパク質、オリゴヌクレオチド又は生物学的に活性な小分子部分である、請求項41に記載の担体結合プロドラッグ。
【請求項43】
前記生物学的に活性な部分がアミン基、ヒドロキシル基、カルボキシル基、ホスフェート基又はメルカプト基を含んでいて、前記生物学的に不活性なリンカーLがそのアミン基、ヒドロキシル基、カルボキシル基、ホスフェート基又はメルカプト基と一緒にコンジュゲートD-Lを形成する、請求項42に記載の担体結合プロドラッグ。
【請求項44】
DとLの間の一時的な結合が、カルバメート結合、カルボネート結合、アミド結合又はエステル結合である、請求項41〜43のいずれかに記載の担体結合プロドラッグ。
【請求項45】
前記一時的なプロドラッグリンカーLが部分L2で置換されている部分L1を含んでおり、その際、L2は、請求項1〜10のいずれかに記載のヒドロゲルである担体基Zに結合している、請求項41〜44のいずれかに記載の担体結合プロドラッグ。
【請求項46】
L2が、下記構造
【化12】

〔ここで、破線は、それぞれ、L2及びZに結合していることを示している〕
を有する末端基を介してZに結合している、請求項45に記載の担体結合プロドラッグ。
【請求項47】
前記生物学的に活性な部分Dが芳香族アミンを含んでおり、及び、前記一時的なプロドラッグリンカーLが、
(i) 式(VIII)
【化13】

〔式中、
破線は、アミド結合を形成することによってL1が生物学的に活性な部分Dの芳香族アミノ基に結合していることを示しており;
X1は、C(R1R1a)であるか、又は、C3-7シクロアルキル、4〜7員のヘテロシクリル、フェニル、ナフチル、インデニル、インダニル、テトラリニル若しくは9〜11員のヘテロビシクリルから選択される環状フラグメントであり;
X2は、化学結合であるか、又は、C(R3R3a)、N(R3)、O、C(R3R3a)-C(R4R4a)、C(R3R3a)-N(R4)、N(R3)-C(R4R4a)、C(R3R3a)-O若しくはO-C(R3R3a)から選択され;
ここで、X1が環状フラグメントである場合、X2は、化学結合、C(R3R3a)、N(R3)又はOであり;
場合により、X1が環状フラグメントであり且つX2がC(R3R3a)である場合、L1内のX1フラグメントとX2フラグメントの順番は変えられてもよく;
R1、R3及びR4は、独立して、H、C1-4アルキル及び-N(R5R5a)からなる群から選択され;
R1a、R2、R2a、R3a、R4a及びR5aは、独立して、H及びC1-4アルキルからなる群から選択され;
場合により、対R2a/R2、対R2a/R3a、対R2a/R4aのうちの1つは、一緒になって4〜7員の少なくとも部分的に飽和しているヘテロ環を形成してもよく;
R5は、C(O)R6であり;
R6は、C1-4アルキルであり;
場合により、対R1a/R4a、対R3a/R4a又は対R1a/R3aのうちの1つは、化学結合を形成してもよく;
場合により、L1は、さらに置換されていてもよい〕
で表される部分L1;
(ii) 部分L2(ここで、L2は化学結合又はスペーサーであり、及び、L2は請求項25〜31のいずれかに記載のヒドロゲルを表す担体基Zに結合している);
を含んでいる生物学的に不活性なリンカーL〔ここで、L1は1つのL2部分で置換されているが、但し、式(VIII)において星印が付けられている水素はL2で置き換えられず;場合により、Lは、さらに置換されてもよい〕である、請求項46に記載の担体結合プロドラッグ。
【請求項48】
前記生物学的に活性な部分Dが第1級又は第2級の脂肪族アミンを含んでおり、及び、本発明のプロドラッグに関する好ましい構造がプロドラッグコンジュゲートD-Lによって与えられ、ここで、
Dは、第1級又は第2級の脂肪族アミンを含んでいる生物学的に活性な部分であり;及び、
Lは、式(VI)
【化14】

〔式中、
破線は、アミド結合を形成することによって生物学的に活性な部分の第1級又は第2級の脂肪族アミン基に結合していることを示しており;
Xは、C(R4R4a)、N(R4)、O、C(R4R4a)-C(R5R5a)、C(R5R5a)-C(R4R4a)、C(R4R4a)-N(R6)、N(R6)-C(R4R4a)、C(R4R4a)-O又はO-C(R4R4a)であり;
X1は、C又はS(O)であり;
X2は、C(R7,R7a)又はC(R7,R7a)-C(R8,R8a)であり;
R1、R1a、R2、R2a、R3、R3a、R4、R4a、R5、R5a、R6、R7、R7a、R8、R8aは、独立して、H及びC1-4アルキルからなる群から選択され;又は、
場合により、対R1a/R4a、対R1a/R5a、対R4a/R5a、対R4a/R5a、対R7a/R8aのうちの1以上は、化学結合を形成してもよく;
場合により、対R1/R1a、対R2/R2a、対R4/R4a、対R5/R5a、対R7/R7a、対R8/R8aのうちの1以上は、それらが結合している原子と一緒になってC3-7シクロアルキル又は4〜7員のヘテロシクリルを形成してもよく;
場合により、対R1/R4、対R1/R5、対R1/R6、対R4/R5、対R7/R8、対R2/R3のうちの1以上は、それらが結合している原子と一緒になって環Aを形成してもよく;
場合により、R3/R3aは、それらが結合している窒素原子と一緒になって4〜7員のヘテロ環を形成してもよく;
Aは、フェニル、ナフチル、インデニル、インダニル、テトラリニル、C3-10シクロアルキル、4〜7員のヘテロシクリル及び9〜11員のヘテロビシクリルからなる群から選択され;及び、
ここで、L1は、1つの基L2-Zで置換されており、及び、場合によりさらに置換されていてもよいが、但し、式(VI)において星印が付けられている水素は置換基で置き換えられず;
ここで、
L2は、単一の化学結合又はスペーサーであり;及び、
Zは、請求項25〜31のいずれかに記載のヒドロゲルである〕
で表される生物学的に不活性なリンカー部分-L1である;
請求項46に記載の担体結合プロドラッグ。
【請求項49】
前記生物学的に活性な部分Dがヒドロキシル基を含んでおり、及び、当該プロドラッグに関する構造が、式(X)
D-O-Z0 (X)
〔式中、
Dは、ヒドロキシル基の酸素を介して部分Z0に結合している、ヒドロキシル基を含んでいる生物学的に活性な部分であり;
Z0は、C(O)-X0-Z1、C(O)O-X0-Z1、S(O)2-X0-Z1、C(S)-X0-Z1、S(O)2O-X0-Z1、S(O)2N(R1)-X0-Z1、CH(OR1)-X0-Z1、C(OR1)(OR2)-X0-Z1、C(O)N(R1)-X0-Z1、P(=O)(OH)O-X0-Z1、P(=O)(OR1)O-X0-Z1、P(=O)(SH)O-X0-Z1、P(=O)(SR1)O-X0-Z1、P(=O)(OR1)-X0-Z1、P(=S)(OH)O-X0-Z1、P(=S)(OR1)O-X0-Z1、P(=S)(OH)N(R1)-X0-Z1、P(=S)(OR1)N(R2)-X0-Z1、P(=O)(OH)N(R1)-X0-Z1又はP(=O)(OR1)N(R2)-X0-Z1であり;
R1、R2は、独立して、C1-6アルキルからなる群から選択され;又は、R1、R2は、一緒になってC1-6アルキレン架橋基を形成し;
X0は、(X0A)m1-(X0B)m2であり;
m1、m2は、独立して、0又は1であり;
X0Aは、T0であり;
X0Bは、同一であるか若しくは異なっている1以上のR3で置換されているか又は置換されていない分枝鎖又は非分枝鎖のC1-10アルキレン基であり;
R3は、ハロゲン、CN、C(O)R4、C(O)OR4、OR4、C(O)R4、C(O)N(R4R4a)、S(O)2N(R4R4a)、S(O)N(R4R4a)、S(O)2R4、S(O)R4、N(R4)S(O)2N(R4aR4b)、SR4、N(R4R4a)、NO2、OC(O)R4、N(R4)C(O)R4a、N(R4)SO2R4a、N(R4)S(O)R4a、N(R4)C(O)N(R4aR4b)、N(R4)C(O)OR4a、OC(O)N(R4R4a)又はT0であり;
R4、R4a、R4bは、独立して、H、T0、C1-4アルキル、C2-4アルケニル及びC2-4アルキニルからなる群から選択され(ここで、C1-4アルキル、C2-4アルケニル及びC2-4アルキニルは、同一であるか又は異なっている1以上のR5で場合により置換されていてもよい);
R5は、ハロゲン、CN、C(O)R6、C(O)OR6、OR6、C(O)R6、C(O)N(R6R6a)、S(O)2N(R6R6a)、S(O)N(R6R6a)、S(O)2R6、S(O)R6、N(R6)S(O)2N(R6aR6b)、SR6、N(R6R6a)、NO2、OC(O)R6、N(R6)C(O)R6a、N(R6)SO2R6a、N(R6)S(O)R6a、N(R6)C(O)N(R6aR6b)、N(R6)C(O)OR6a、OC(O)N(R6R6a)であり;
R6、R6a、R6bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のハロゲンで場合により置換されていてもよい);
T0は、フェニル、ナフチル、アズレニル、インデニル、インダニル、C3-7シクロアルキル、3〜7員のヘテロシクリル又は8〜11員のヘテロビシクリルであり(ここで、T0は、同一であるか又は異なっている1以上のR7で場合により置換されていてもよい);
R7は、ハロゲン、CN、COOR8、OR8、C(O)R8、C(O)N(R8R8a)、S(O)2N(R8R8a)、S(O)N(R8R8a)、S(O)2R8、S(O)R8、N(R8)S(O)2N(R8aR8b)、SR8、N(R8R8a)、NO2、OC(O)R8、N(R8)C(O)R8a、N(R8)S(O)2R8a、N(R8)S(O)R8a、N(R8)C(O)OR8a、N(R8)C(O)N(R8aR8b)、OC(O)N(R8R8a)、オキソ(=O)(ここで、該環は少なくとも部分的に飽和している)、C1-6アルキル、C2-6アルケニル又はC2-6アルキニルであり(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のR9で場合により置換されていてもよい);
R8、R8a、R8bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のR10で場合により置換されていてもよい);
R9、R10は、独立して、ハロゲン、CN、C(O)R11、C(O)OR11、OR11、C(O)R11、C(O)N(R11R11a)、S(O)2N(R11R11a)、S(O)N(R11R11a)、S(O)2R11、S(O)R11、N(R11)S(O)2N(R11aR11b)、SR11、N(R11R11a)、NO2、OC(O)R11、N(R11)C(O)R11a、N(R11)SO2R11a、N(R11)S(O)R11a、N(R11)C(O)N(R11aR11b)、N(R11)C(O)OR11a及びOC(O)N(R11R11a)からなる群から選択され;
R11、R11a、R11bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のハロゲンで場合により置換されていてもよい);
Z1は、X0に共有結合的に結合している、請求項25〜31のいずれかに記載のヒドロゲルである〕
で表されるプロドラッグコンジュゲートによって与えられる、請求項46に記載の担体結合プロドラッグ。
【請求項50】
前記生物学的に活性な部分Dが芳香族ヒドロキシル基を含んでおり、及び、前記一時的なプロドラッグリンカーLが、
(i) 式(XI)
【化15】

〔式中、
破線は、カルバメート基を形成することによってL1が生物学的に活性な部分Dの芳香族ヒドロキシル基に結合していることを示しており;
R1は、C1-4アルキル、ヘテロアルキル、C3-7シクロアルキル及び
【化16】

からなる群から選択され;及び、
R2、R2a、R3、R3aは、独立して、水素、置換されているか若しくは置換されていない直鎖若しくは分枝鎖若しくは環状のC1-4アルキル又はヘテロアルキルから選択され;
mは、独立して、2、3又は4である〕
で表される部分L1;
(ii) 部分L2(ここで、L2は化学結合又はスペーサーであり、及び、L2は請求項25〜31のいずれかに記載のヒドロゲルに結合している);
を含んでいる生物学的に不活性なリンカーL〔ここで、L1は1つのL2部分で置換されており;場合により、Lは、さらに置換されてもよい〕である、請求項46に記載の担体結合プロドラッグ。
【請求項51】
製薬上許容される賦形剤と一緒に請求項41〜50のいずれかに記載のプロドラッグ又はその薬学的な塩を含んでいる、医薬組成物。
【請求項52】
薬物中で使用するための、請求項41〜50のいずれかに記載のプロドラッグ又は請求項51に記載の医薬組成物。
【請求項53】
1以上の状態を治療することが必要な哺乳類患者において、治療する方法、制御する方法、遅延させる方法又は予防する方法であって、該患者に治療有効量の請求項41〜50のいずれかに記載のプロドラッグ又は請求項51に記載の医薬組成物又はそれらの製薬上許容される塩を投与することを含む、前記方法。
【請求項54】
ヒドロゲルを調製する方法であって、
(a) 式
【化17】

〔式中、nは、3〜100の整数である〕
で表されるバックボーン試薬を下記式
【化18】

〔式中、
qは、3〜100の整数であり;
各mは、独立して、2〜4の整数である〕
で表されるクロスリンカー試薬と2:1〜1.05:1のアミン/活性エステルの比で反応させて、好ましくは、1gのヒドロゲル当たり0.02〜2mmolのアミンがローディングしているヒドロゲルを生じさせる段階を含み;及び、前記試薬は適切な塩基の存在下において非プロトン性溶媒に溶解させる、前記方法。
【請求項55】
前記非プロトン性溶媒がDMSOであり、及び、前記塩基がN,N,N',N'-テトラメチルエチレンジアミンである、請求項54に記載の方法。
【請求項56】
請求項54又は55に記載の調製方法から得ることができるヒドロゲル。
【請求項57】
撹拌、破砕、切削、プレス又は摩砕などの機械的処理によって粉砕し、場合により篩にかけることによって得ることができる、コーティング、メッシュ、ステント又は微粒子の形態にある、請求項1、26又は56のいずれかに記載のヒドロゲル。
【請求項58】
前記試薬を適切な乳化剤の存在下で脂肪族炭化水素の中に分散させる、請求項54に記載の調製方法。
【請求項59】
前記脂肪族炭化水素がn-ヘプタンであり、及び、前記乳化剤がポリ(エチレングリコール)30ジポリヒドロキシステアレートである、請求項58に記載の調製方法。
【請求項60】
微粒子を回収し、洗浄し及び粒径に従って機械的篩によって分別することをさらに特徴とする、請求項54、55、58又は59のいずれかに記載の調製方法。
【請求項61】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) 生物学的に活性な部分を請求項56からのヒドロゲルと反応させて一時的な結合を形成させ、並びに、未反応の生物学的に活性な部分を洗浄及び濾過によって除去する段階;
(b) 場合により、未反応の反応性官能基を適切なキャッピング試薬でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項62】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) スペーサー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲートを生じさせる段階;
(b) 段階(a)からの生物学的に活性な部分-スペーサーコンジュゲートを請求項56のヒドロゲルの反応性官能基と反応させ、並びに、未反応の生物学的に活性な部分-スペーサーコンジュゲートを洗浄及び濾過によって除去する段階;
(c) 場合により、未反応の反応性官能基を適切なキャッピング試薬でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項63】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲートを生じさせる段階;
(b) 段階(a)からの生物学的に活性な部分-リンカーコンジュゲートを請求項56のヒドロゲルの反応性官能基と反応させ、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(c) 場合により、未反応の反応性官能基を適切なキャッピング試薬でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項64】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) 請求項56のヒドロゲルをN-(3-マレイミドプロピル)-21-アミノ-4,7,10,13,16,19-ヘキサオキサ-ヘンエイコサン酸NHSと反応させることにより当該ヒドロゲルを誘導体化してマレイミドで官能基化されたヒドロゲルを生じさせ、並びに、未反応のN-(3-マレイミドプロピル)-21-アミノ-4,7,10,13,16,19-ヘキサオキサ-ヘンエイコサン酸NHSを洗浄及び濾過によって除去する段階;
(b) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲート(ここで、該リンカーは遊離チオール基(-SH)を含んでいる)を生じさせる段階;
(c) 段階(b)からの生物学的に活性な部分-リンカーコンジュゲートをpHが5.5〜8の範囲内にある緩衝化水溶液の中で室温〜4℃の範囲内の温度で段階(a)からのマレイミドで官能基化されたヒドロゲルと反応させ、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(c) 未反応の反応性官能基を34-500Daのチオール含有化合物でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項65】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) 請求項56のヒドロゲルをN-(3-マレイミドプロピル)-21-アミノ-4,7,10,13,16,19-ヘキサオキサ-ヘンエイコサン酸NHSエステルと反応させることにより当該ヒドロゲルを誘導体化してマレイミドで官能基化されたヒドロゲルを生じさせ、並びに、未反応のN-(3-マレイミドプロピル)-21-アミノ-4,7,10,13,16,19-ヘキサオキサ-ヘンエイコサン酸NHSエステルを洗浄及び濾過によって除去する段階;
(b) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲート(ここで、該リンカーは遊離チオール基(-SH)を含んでおり、及び、該生物学的に活性な部分はジスルフィド(-S-S-)結合を含んでいる)を生じさせる段階;
(c) 段階(b)からの生物学的に活性な部分-リンカーコンジュゲートをpHが2〜5の範囲内にある緩衝化水溶液の中で室温〜4℃の範囲内の温度で段階(a)からのマレイミドで官能基化されたヒドロゲルと反応させ(ここで、該リンカーはチオール基に連結されており、及び、該生物学的に活性な部分はジスルフィド(-S-S-)結合を含んでいる)、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(d) 未反応の反応性官能基を34-500Daのチオール含有化合物でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項66】
請求項13〜22又は41〜55のいずれかに記載のプロドラッグを調製する方法であって、
(a) 請求項56のヒドロゲルを保護されたチオール基を含んでいる低分子量スペーサー試薬と反応させることにより当該ヒドロゲルを誘導体化してチオールで官能基化されたヒドロゲル(ここで、該チオール基は保護基に連結されている)を生じさせ、並びに、未反応のスペーサー試薬を洗浄及び濾過によって除去する段階;
(b) 段階(a)からのチオールで官能基化されたヒドロゲルを脱保護し、並びに、放出された保護基を洗浄及び濾過によって除去する段階;
(c) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲート(ここで、該リンカーはマレイミド部分を含んでいる)を生じさせる段階;
(d) 段階(c)からの生物学的に活性な部分-リンカーコンジュゲートをpHが5.5〜8の範囲内にある緩衝化水溶液の中で室温〜4℃の範囲内の温度で段階(b)からのチオールで官能基化されたヒドロゲルと反応させ、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(e) 未反応の反応性官能基を100-300Daのマレイミド含有化合物でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項67】
請求項13〜22及び41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) 請求項56のヒドロゲルを保護されたチオール基を含んでいる低分子量スペーサー試薬と反応させることにより当該ヒドロゲルを誘導体化してチオールで官能基化されたヒドロゲル(ここで、該チオール基は保護基に連結されている)を生じさせ、並びに、未反応のスペーサー試薬を洗浄及び濾過によって除去する段階;
(b) 段階(a)からのチオールで官能基化されたヒドロゲルを脱保護し、並びに、放出された保護基を洗浄及び濾過によって除去する段階;
(c) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲート(ここで、該リンカーはマレイミド部分を含んでおり、及び、該生物学的に活性な部分はジスルフィド(-S-S-)結合を含んでいる)を生じさせる段階;
(d) 段階(b)からの生物学的に活性な部分-リンカーコンジュゲートをpHが2〜5の範囲内にある緩衝化水溶液の中で室温〜4℃の範囲内の温度で段階(a)からのチオールで官能基化されたヒドロゲルと反応させ(ここで、該リンカーはチオール基に連結されており、及び、該生物学的に活性な部分はジスルフィド(-S-S-)結合を含んでいる)、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(e) 未反応の反応性官能基を100-300Daのマレイミド含有化合物でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項68】
請求項61〜67のいずれかに記載の調製方法から得ることができるプロドラッグ。
【請求項69】
注射針で注射可能なプロドラッグを調製する方法であって、
(a) 請求項61〜67のいずれかに記載の調製方法に準じて微粒子の形態にあるプロドラッグを調製する段階;
(b) 前記微粒子を篩にかける段階;
(c) プロドラッグビーズの粒径が25〜80μmであるフラクションを選択する段階;
(d) 段階(c)からのビーズフラクションを注射に適した水性バッファー溶液の中に懸濁させる段階;
を含む、前記方法。
【請求項70】
請求項69に記載の調製方法から得ることができる、注射針で注射可能なプロドラッグ。
【請求項71】
内径が300μm未満である注射針を通して注射することが可能な、請求項69から得られるプロドラッグ。
【請求項72】
内径が225μm未満である注射針を通して注射することが可能な、請求項71に記載のプロドラッグ。
【請求項73】
内径が175μm未満である注射針を通して注射することが可能な、請求項71に記載のプロドラッグ。
【請求項1】
加水分解的に分解可能な結合によって相互に連結されているバックボーン部分(ここで、該バックボーン部分は、さらに、反応性官能基を含んでいる)を含んでいる生物分解性ポリ(エチレングリコール)系水不溶性ヒドロゲルであって、前記水不溶性ヒドロゲルが、分解可能な結合の加水分解によって前記ヒドロゲルが1以上のバックボーン部分を含んでいる水溶性分解産物に完全に分解されるための時間と前記ヒドロゲルの中のバックボーン部分の総量に基づいて1以上のバックボーン部分を含んでいる水溶性分解産物の最初の10mol-%が放出されるための時間の間の比率が1より大きく且つ2以下であるということをさらに特徴とする、前記生物分解性ポリ(エチレングリコール)系水不溶性ヒドロゲル。
【請求項2】
前記加水分解的に分解可能な結合が、アコニチル類、アセタール類、カルボン酸無水物類、エステル類、イミン類、ヒドラゾン類、マレアミド酸アミド類、オルトエステル類、ホスファミド類、ホスホエステル類、ホスホシリルエステル類、シリルエステル類、スルホン酸エステル類、芳香族カルバメート類及びそれらの組合せからなる群から選択される、請求項1に記載のヒドロゲル。
【請求項3】
前記反応性官能基が、カルボン酸及び活性化誘導体、アミノ、マレイミド、チオール、スルホン酸及び誘導体、カルボネート及び誘導体、カルバメート及び誘導体、ヒドロキシル、アルデヒド、ケトン、ヒドラジン、イソシアネート、イソチオシアネート、リン酸及び誘導体、ホスホン酸及び誘導体、ハロアセチル、アルキルハロゲン化物、アクリロイル及び別のα-β不飽和マイケル受容体、アリール化剤(例えば、フッ化アリール)、ヒドロキシルアミン、ジスルフィド(例えば、ピリジルジスルフィド)、ビニルスルホン、ビニルケトン、ジアゾアルカン、ジアゾアセチル化合物、オキシラン並びにアジリジンからなる群から選択される、請求項1又は2に記載のヒドロゲル。
【請求項4】
前記バックボーン部分が1kDa〜20kDaの範囲内にある分子量を有している、請求項1〜3のいずれかに記載のヒドロゲル。
【請求項5】
前記バックボーン部分がクロスリンカー部分(ここで、各クロスリンカー部分は、加水分解的に分解可能な結合のうちの少なくとも2によって終結されている)を介して互いに結合している、請求項1〜4のいずれかに記載のヒドロゲル。
【請求項6】
前記クロスリンカー部分が0.5kDa〜5kDaの範囲内にある分子量を有している、請求項5に記載のヒドロゲル。
【請求項7】
各クロスリンカー部分がPEG系である、請求項5又は6に記載のヒドロゲル。
【請求項8】
各クロスリンカー部分が1つのPEG系分子鎖によって表される、請求項7に記載のヒドロゲル。
【請求項9】
各バックボーン部分が、合計で少なくとも16の相互に連結されている生物分解性で反応性の官能基を含んでいる、請求項1〜8のいずれかに記載のヒドロゲル。
【請求項10】
前記バックボーン部分が、式
C(A-Hyp)4
〔式中、各Aは、独立して、末端が永久的な共有結合によって当該第4級炭素に結合しているポリ(エチレングリコール)系ポリマー鎖であって、そのポリマー鎖の遠位末端は樹枝状部分Hypに共有結合的に結合しており、ここで、各樹枝状部分Hypは、相互に連結されている官能基及び反応性官能基を表す少なくとも4つの官能基を有している〕
で表される第4級炭素を有している、請求項9に記載のヒドロゲル。
【請求項11】
請求項1〜10のいずれかに記載のヒドロゲルを含んでいるコンジュゲートであって、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分で構成されていること、及び、付加的にスペーサー分子又は遮断基を有していることを特徴とする、前記コンジュゲート。
【請求項12】
請求項1〜10のいずれかに記載のヒドロゲルを含んでいるコンジュゲートであって、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分で構成されていること、及び、付加的にリガンド又はキレート基に対する永久的な結合を有していることを特徴とする、前記コンジュゲート。
【請求項13】
担体として請求項1〜10のいずれかに記載のヒドロゲルを含んでいる担体結合プロドラッグであって、生物学的に活性な部分Dが共有結合的に結合している一時的なプロドラッグリンカーLと一緒に、バックボーン部分の多数の永久的な結合が存在している、前記担体結合プロドラッグ。
【請求項14】
前記生物学的に活性な部分Dが、ポリペプチド、タンパク質、オリゴヌクレオチド又は生物学的に活性な小分子部分である、請求項13に記載の担体結合プロドラッグ。
【請求項15】
前記生物学的に活性な部分Dがアミン基、ヒドロキシル基、カルボキシル基、ホスフェート基又はメルカプト基を含んでいて、前記生物学的に不活性なリンカーLがそのアミン基、ヒドロキシル基、カルボキシル基、ホスフェート基又はメルカプト基と一緒にコンジュゲートD-Lを形成する、請求項14に記載の担体結合プロドラッグ。
【請求項16】
DとLの間の結合が、カルバメート結合、カルボネート結合、アミド結合又はエステル結合である、請求項13〜15のいずれかに記載の担体結合プロドラッグ。
【請求項17】
前記一時的なプロドラッグリンカーLが部分L2で置換されている部分L1を含んでおり、その際、L2は、請求項1〜10のいずれかに記載のヒドロゲルである担体基Zに結合している、請求項12〜14のいずれかに記載の担体結合プロドラッグ。
【請求項18】
L2が、下記構造
【化1】

〔ここで、破線は、それぞれ、L2及びZに結合していることを示している〕
を有する末端基を介してZに結合している、請求項16に記載の担体結合プロドラッグ。
【請求項19】
前記生物学的に活性な部分が芳香族アミンを含んでおり、及び、前記一時的なプロドラッグリンカーが、
(i) 式(VIII)
【化2】

〔式中、
破線は、アミド結合を形成することによってL1が生物学的に活性な部分Dの芳香族アミノ基に結合していることを示しており;
X1は、C(R1R1a)であるか、又は、C3-7シクロアルキル、4〜7員のヘテロシクリル、フェニル、ナフチル、インデニル、インダニル、テトラリニル若しくは9〜11員のヘテロビシクリルから選択される環状フラグメントであり;
X2は、化学結合であるか、又は、C(R3R3a)、N(R3)、O、C(R3R3a)-C(R4R4a)、C(R3R3a)-N(R4)、N(R3)-C(R4R4a)、C(R3R3a)-O若しくはO-C(R3R3a)から選択され;
ここで、X1が環状フラグメントである場合、X2は、化学結合、C(R3R3a)、N(R3)又はOであり;
場合により、X1が環状フラグメントであり且つX2がC(R3R3a)である場合、L1内のX1フラグメントとX2フラグメントの順番は変えられてもよく;
R1、R3及びR4は、独立して、H、C1-4アルキル及び-N(R5R5a)からなる群から選択され;
R1a、R2、R2a、R3a、R4a及びR5aは、独立して、H及びC1-4アルキルからなる群から選択され;
場合により、対R2a/R2、対R2a/R3a、対R2a/R4aのうちの1つは、一緒になって4〜7員の少なくとも部分的に飽和しているヘテロ環を形成してもよく;
R5は、C(O)R6であり;
R6は、C1-4アルキルであり;
場合により、対R1a/R4a、対R3a/R4a又は対R1a/R3aのうちの1つは、化学結合を形成してもよく;
場合により、L1は、さらに置換されていてもよい〕
で表される部分L1;
(ii) 部分L2(ここで、L2は化学結合又はスペーサーであり、及び、L2は請求項1〜10のいずれかに記載のヒドロゲルを表す担体基Zに結合している);
を含んでいる生物学的に不活性なリンカーL〔ここで、L1は1つのL2部分で置換されているが、但し、式(VIII)において星印が付けられている水素はL2で置き換えられず;場合により、Lは、さらに置換されてもよい〕である、請求項17に記載の担体結合プロドラッグ。
【請求項20】
前記生物学的に活性な部分Dが第1級又は第2級の脂肪族アミンを含んでおり、及び、本発明のプロドラッグに関する好ましい構造がプロドラッグコンジュゲートD-Lによって与えられ、ここで、
Dは、第1級又は第2級の脂肪族アミンを含んでいる生物学的に活性な部分であり;及び、
Lは、式(VI)
【化3】

〔式中、
破線は、アミド結合を形成することによって生物学的に活性な部分の第1級又は第2級の脂肪族アミン基に結合していることを示しており;
Xは、C(R4R4a)、N(R4)、O、C(R4R4a)-C(R5R5a)、C(R5R5a)-C(R4R4a)、C(R4R4a)-N(R6)、N(R6)-C(R4R4a)、C(R4R4a)-O又はO-C(R4R4a)であり;
X1は、C又はS(O)であり;
X2は、C(R7,R7a)又はC(R7,R7a)-C(R8,R8a)であり;
R1、R1a、R2、R2a、R3、R3a、R4、R4a、R5、R5a、R6、R7、R7a、R8、R8aは、独立して、H及びC1-4アルキルからなる群から選択され;又は、
場合により、対R1a/R4a、対R1a/R5a、対R4a/R5a、対R4a/R5a、対R7a/R8aのうちの1以上は、化学結合を形成してもよく;
場合により、対R1/R1a、対R2/R2a、対R4/R4a、対R5/R5a、対R7/R7a、対R8/R8aのうちの1以上は、それらが結合している原子と一緒になってC3-7シクロアルキル又は4〜7員のヘテロシクリルを形成してもよく;
場合により、対R1/R4、対R1/R5、対R1/R6、対R4/R5、対R7/R8、対R2/R3のうちの1以上は、それらが結合している原子と一緒になって環Aを形成してもよく;
場合により、R3/R3aは、それらが結合している窒素原子と一緒になって4〜7員のヘテロ環を形成してもよく;
Aは、フェニル、ナフチル、インデニル、インダニル、テトラリニル、C3-10シクロアルキル、4〜7員のヘテロシクリル及び9〜11員のヘテロビシクリルからなる群から選択され;及び、
ここで、L1は、1つの基L2-Zで置換されており、及び、場合によりさらに置換されていてもよいが、但し、式(VI)において星印が付けられている水素は置換基で置き換えられず;
ここで、
L2は、単一の化学結合又はスペーサーであり;及び、
Zは、請求項1〜10のいずれかに記載のヒドロゲルである〕
で表される生物学的に不活性なリンカー部分-L1である;
請求項17に記載の担体結合プロドラッグ。
【請求項21】
前記生物学的に活性な部分Dがヒドロキシル基を含んでおり、及び、当該プロドラッグに関する構造が、式(X)
D-O-Z0 (X)
〔式中、
Dは、ヒドロキシル基の酸素を介して部分Z0に結合している、ヒドロキシル基を含んでいる生物学的に活性な部分であり;
Z0は、C(O)-X0-Z1、C(O)O-X0-Z1、S(O)2-X0-Z1、C(S)-X0-Z1、S(O)2O-X0-Z1、S(O)2N(R1)-X0-Z1、CH(OR1)-X0-Z1、C(OR1)(OR2)-X0-Z1、C(O)N(R1)-X0-Z1、P(=O)(OH)O-X0-Z1、P(=O)(OR1)O-X0-Z1、P(=O)(SH)O-X0-Z1、P(=O)(SR1)O-X0-Z1、P(=O)(OR1)-X0-Z1、P(=S)(OH)O-X0-Z1、P(=S)(OR1)O-X0-Z1、P(=S)(OH)N(R1)-X0-Z1、P(=S)(OR1)N(R2)-X0-Z1、P(=O)(OH)N(R1)-X0-Z1又はP(=O)(OR1)N(R2)-X0-Z1であり;
R1、R2は、独立して、C1-6アルキルからなる群から選択され;又は、R1、R2は、一緒になってC1-6アルキレン架橋基を形成し;
X0は、(X0A)m1-(X0B)m2であり;
m1、m2は、独立して、0又は1であり;
X0Aは、T0であり;
X0Bは、同一であるか若しくは異なっている1以上のR3で置換されているか又は置換されていない分枝鎖又は非分枝鎖のC1-10アルキレン基であり;
R3は、ハロゲン、CN、C(O)R4、C(O)OR4、OR4、C(O)R4、C(O)N(R4R4a)、S(O)2N(R4R4a)、S(O)N(R4R4a)、S(O)2R4、S(O)R4、N(R4)S(O)2N(R4aR4b)、SR4、N(R4R4a)、NO2、OC(O)R4、N(R4)C(O)R4a、N(R4)SO2R4a、N(R4)S(O)R4a、N(R4)C(O)N(R4aR4b)、N(R4)C(O)OR4a、OC(O)N(R4R4a)又はT0であり;
R4、R4a、R4bは、独立して、H、T0、C1-4アルキル、C2-4アルケニル及びC2-4アルキニルからなる群から選択され(ここで、C1-4アルキル、C2-4アルケニル及びC2-4アルキニルは、同一であるか又は異なっている1以上のR5で場合により置換されていてもよい);
R5は、ハロゲン、CN、C(O)R6、C(O)OR6、OR6、C(O)R6、C(O)N(R6R6a)、S(O)2N(R6R6a)、S(O)N(R6R6a)、S(O)2R6、S(O)R6、N(R6)S(O)2N(R6aR6b)、SR6、N(R6R6a)、NO2、OC(O)R6、N(R6)C(O)R6a、N(R6)SO2R6a、N(R6)S(O)R6a、N(R6)C(O)N(R6aR6b)、N(R6)C(O)OR6a、OC(O)N(R6R6a)であり;
R6、R6a、R6bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のハロゲンで場合により置換されていてもよい);
T0は、フェニル、ナフチル、アズレニル、インデニル、インダニル、C3-7シクロアルキル、3〜7員のヘテロシクリル又は8〜11員のヘテロビシクリルであり(ここで、T0は、同一であるか又は異なっている1以上のR7で場合により置換されていてもよい);
R7は、ハロゲン、CN、COOR8、OR8、C(O)R8、C(O)N(R8R8a)、S(O)2N(R8R8a)、S(O)N(R8R8a)、S(O)2R8、S(O)R8、N(R8)S(O)2N(R8aR8b)、SR8、N(R8R8a)、NO2、OC(O)R8、N(R8)C(O)R8a、N(R8)S(O)2R8a、N(R8)S(O)R8a、N(R8)C(O)OR8a、N(R8)C(O)N(R8aR8b)、OC(O)N(R8R8a)、オキソ(=O)(ここで、該環は少なくとも部分的に飽和している)、C1-6アルキル、C2-6アルケニル又はC2-6アルキニルであり(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のR9で場合により置換されていてもよい);
R8、R8a、R8bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のR10で場合により置換されていてもよい);
R9、R10は、独立して、ハロゲン、CN、C(O)R11、C(O)OR11、OR11、C(O)R11、C(O)N(R11R11a)、S(O)2N(R11R11a)、S(O)N(R11R11a)、S(O)2R11、S(O)R11、N(R11)S(O)2N(R11aR11b)、SR11、N(R11R11a)、NO2、OC(O)R11、N(R11)C(O)R11a、N(R11)SO2R11a、N(R11)S(O)R11a、N(R11)C(O)N(R11aR11b)、N(R11)C(O)OR11a及びOC(O)N(R11R11a)からなる群から選択され;
R11、R11a、R11bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のハロゲンで場合により置換されていてもよい);
Z1は、X0に共有結合的に結合している、請求項1〜10のいずれかに記載のヒドロゲルである〕
で表されるプロドラッグコンジュゲートによって与えられる、請求項17に記載の担体結合プロドラッグ。
【請求項22】
前記生物学的に活性な部分Dが芳香族ヒドロキシル基を含んでおり、及び、前記プロドラッグリンカーが、
(i) 式(XI)
【化4】

〔式中、
破線は、カルバメート基を形成することによってL1が生物学的に活性な部分Dの芳香族ヒドロキシル基に結合していることを示しており;
R1は、C1-4アルキル、ヘテロアルキル、C3-7シクロアルキル及び
【化5】

からなる群から選択され;及び、
;
R2、R2a、R3、R3aは、独立して、水素、置換されているか若しくは置換されていない直鎖若しくは分枝鎖若しくは環状のC1-4アルキル又はヘテロアルキルから選択され;
mは、独立して、2、3又は4である〕
で表される部分L1;
(iii) 部分L2(ここで、L2は化学結合又はスペーサーであり、及び、L2は請求項1〜10のいずれかに記載のヒドロゲルに結合している);
を含んでいる生物学的に不活性なリンカーL〔ここで、L1は1つのL2部分で置換されており;場合により、Lは、さらに置換されてもよい〕である、請求項17に記載の担体結合プロドラッグ。
【請求項23】
製薬上許容される賦形剤と一緒に請求項12〜22のいずれかに記載のプロドラッグ又はその薬学的な塩を含んでいる、医薬組成物。
【請求項24】
薬物中で使用するための、請求項12〜22のいずれかに記載のプロドラッグ又は請求項23に記載の医薬組成物。
【請求項25】
1以上の状態を治療することが必要な哺乳類患者において、治療する方法、制御する方法、遅延させる方法又は予防する方法であって、該患者に治療有効量の請求項12〜22のいずれかに記載のプロドラッグ又は請求項23に記載の医薬組成物又はそれらの製薬上許容される塩を投与することを含む、前記方法。
【請求項26】
加水分解的に分解可能な結合によって相互に連結されているバックボーン部分を含んでいる生物分解性ポリ(エチレングリコール)系水不溶性ヒドロゲルであって、該バックボーン部分が、1kDa〜20kDaの範囲内にある分子量を有していること、及び、構造C*-(A-Hyp)x〔ここで、
C*は、分枝コアであり;
Aは、ポリ(エチレングリコール)系ポリマー鎖であり;
Hypは、高分岐樹枝状部分であり;
xは、3〜16の整数であり;
及び、ここで、前記高分岐樹枝状部分は、さらに、反応性官能基及び相互に連結されている官能基を含んでいる〕
を有していることを特徴とする、前記生物分解性ポリ(エチレングリコール)系水不溶性ヒドロゲル。
【請求項27】
前記バックボーン部分がクロスリンカー部分を介して互いに結合しており、各クロスリンカー部分は加水分解的に分解可能な結合のうちの少なくとも2によって終結されている、請求項26に記載の生物分解性ヒドロゲル。
【請求項28】
前記クロスリンカー部分が0.5kDa〜5kDaの範囲内にある分子量を有している、請求項27に記載の生物分解性ヒドロゲル。
【請求項29】
各クロスリンカー部分がPEG系である、請求項27又は28に記載の生物分解性ヒドロゲル。
【請求項30】
各クロスリンカー部分が1つのポリ(エチレングリコール)系ポリマー鎖によって表される、請求項29に記載の生物分解性ヒドロゲル。
【請求項31】
各バックボーン部分が、合計で少なくとも16の相互に連結されている生物分解性で反応性の官能基を含んでいる、請求項26〜30のいずれかに記載の生物分解性ヒドロゲル。
【請求項32】
前記バックボーン部分が、式
C(A-Hyp)4
〔式中、各Aは、独立して、末端が永久的な共有結合によって第4級炭素に結合しているポリ(エチレングリコール)系ポリマー鎖であって、そのポリマー鎖の遠位末端は樹枝状部分Hypに共有結合的に結合しており、ここで、各樹枝状部分Hypは、相互に連結されている官能基及び反応性官能基を表す少なくとも4つの官能基を有している〕
で表される第4級炭素を有している、請求項31に記載の生物分解性ヒドロゲル。
【請求項33】
前記バックボーン部分が、下記式:
【化6】

〔式中、破線は、当該バックボーン部分の残部に結合していることを示している〕
で表される分枝コアを含んでいる、請求項10又は32に記載の生物分解性ヒドロゲル。
【請求項34】
前記バックボーン部分が、下記式:
【化7】

〔式中、nは5〜50の整数であり、及び、破線は、当該分子の残部に結合していることを示している〕
で表される構造を含んでいる、請求項33に記載の生物分解性ヒドロゲル。
【請求項35】
前記バックボーン部分が、下記式:
【化8】

〔式中、破線は、当該分子の残部に結合していることを示しており、及び、星印が付けられている炭素原子はS-立体配置を示している〕
で表される高分岐部分Hypを含んでいる、請求項33又は34に記載の生物分解性ヒドロゲル。
【請求項36】
前記バックボーン部分が、下記式:
【化9】

〔式中、
破線のうちの一方は、高分岐部分Hypに結合していることを示しており、及び、第2の破線は、当該分子の残部に結合していることを示しており;並びに、
mは、2〜4の整数である〕
で表される少なくとも1つのスペーサーを含んでいる、請求項33〜35のいずれかに記載の生物分解性ヒドロゲル。
【請求項37】
前記バックボーン部分が、下記式:
【化10】

〔式中、
星印が付けられている破線は、当該ヒドロゲルと請求項17のチオスクシンイミド基のNの間の結合を示しており;
もう一方の破線は、Hypに結合していることを示しており;及び、
pは、0〜10の整数である〕
で表される少なくとも1つのスペーサーを含んでいる、請求項33〜36のいずれかに記載の生物分解性ヒドロゲル。
【請求項38】
前記バックボーン部分が、下記構造
【化11】

〔ここで、qは、3〜100の整数である〕
を含んでいるクロスリンカー部分を介して互いに結合している、請求項33〜37のいずれかに記載の生物分解性ヒドロゲル。
【請求項39】
請求項26〜38のいずれかに記載のヒドロゲル(ここで、該ヒドロゲルは、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分で構成されている)を含んでおり、及び、付加的にスペーサー分子又は遮断基又はそれらの組合せに対する永久的な結合を有している、コンジュゲート。
【請求項40】
請求項26〜38のいずれかに記載のヒドロゲル(ここで、該ヒドロゲルは、加水分解的に分解可能な結合によって相互に連結されているバックボーン部分で構成されている)を含んでおり、及び、付加的にリガンド又はキレート基に対する永久的な結合を有している、コンジュゲート。
【請求項41】
担体として請求項26〜38のいずれかに記載の生物分解性ヒドロゲルを含んでいる担体結合プロドラッグであって、バックボーン部分の多数の永久的な結合が、それぞれ、生物学的に活性な部分Dが共有結合的に結合している一時的なプロドラッグリンカーLと一緒に存在している、前記担体結合プロドラッグ。
【請求項42】
前記生物学的に活性な部分Dが、ポリペプチド、タンパク質、オリゴヌクレオチド又は生物学的に活性な小分子部分である、請求項41に記載の担体結合プロドラッグ。
【請求項43】
前記生物学的に活性な部分がアミン基、ヒドロキシル基、カルボキシル基、ホスフェート基又はメルカプト基を含んでいて、前記生物学的に不活性なリンカーLがそのアミン基、ヒドロキシル基、カルボキシル基、ホスフェート基又はメルカプト基と一緒にコンジュゲートD-Lを形成する、請求項42に記載の担体結合プロドラッグ。
【請求項44】
DとLの間の一時的な結合が、カルバメート結合、カルボネート結合、アミド結合又はエステル結合である、請求項41〜43のいずれかに記載の担体結合プロドラッグ。
【請求項45】
前記一時的なプロドラッグリンカーLが部分L2で置換されている部分L1を含んでおり、その際、L2は、請求項1〜10のいずれかに記載のヒドロゲルである担体基Zに結合している、請求項41〜44のいずれかに記載の担体結合プロドラッグ。
【請求項46】
L2が、下記構造
【化12】

〔ここで、破線は、それぞれ、L2及びZに結合していることを示している〕
を有する末端基を介してZに結合している、請求項45に記載の担体結合プロドラッグ。
【請求項47】
前記生物学的に活性な部分Dが芳香族アミンを含んでおり、及び、前記一時的なプロドラッグリンカーLが、
(i) 式(VIII)
【化13】

〔式中、
破線は、アミド結合を形成することによってL1が生物学的に活性な部分Dの芳香族アミノ基に結合していることを示しており;
X1は、C(R1R1a)であるか、又は、C3-7シクロアルキル、4〜7員のヘテロシクリル、フェニル、ナフチル、インデニル、インダニル、テトラリニル若しくは9〜11員のヘテロビシクリルから選択される環状フラグメントであり;
X2は、化学結合であるか、又は、C(R3R3a)、N(R3)、O、C(R3R3a)-C(R4R4a)、C(R3R3a)-N(R4)、N(R3)-C(R4R4a)、C(R3R3a)-O若しくはO-C(R3R3a)から選択され;
ここで、X1が環状フラグメントである場合、X2は、化学結合、C(R3R3a)、N(R3)又はOであり;
場合により、X1が環状フラグメントであり且つX2がC(R3R3a)である場合、L1内のX1フラグメントとX2フラグメントの順番は変えられてもよく;
R1、R3及びR4は、独立して、H、C1-4アルキル及び-N(R5R5a)からなる群から選択され;
R1a、R2、R2a、R3a、R4a及びR5aは、独立して、H及びC1-4アルキルからなる群から選択され;
場合により、対R2a/R2、対R2a/R3a、対R2a/R4aのうちの1つは、一緒になって4〜7員の少なくとも部分的に飽和しているヘテロ環を形成してもよく;
R5は、C(O)R6であり;
R6は、C1-4アルキルであり;
場合により、対R1a/R4a、対R3a/R4a又は対R1a/R3aのうちの1つは、化学結合を形成してもよく;
場合により、L1は、さらに置換されていてもよい〕
で表される部分L1;
(ii) 部分L2(ここで、L2は化学結合又はスペーサーであり、及び、L2は請求項25〜31のいずれかに記載のヒドロゲルを表す担体基Zに結合している);
を含んでいる生物学的に不活性なリンカーL〔ここで、L1は1つのL2部分で置換されているが、但し、式(VIII)において星印が付けられている水素はL2で置き換えられず;場合により、Lは、さらに置換されてもよい〕である、請求項46に記載の担体結合プロドラッグ。
【請求項48】
前記生物学的に活性な部分Dが第1級又は第2級の脂肪族アミンを含んでおり、及び、本発明のプロドラッグに関する好ましい構造がプロドラッグコンジュゲートD-Lによって与えられ、ここで、
Dは、第1級又は第2級の脂肪族アミンを含んでいる生物学的に活性な部分であり;及び、
Lは、式(VI)
【化14】

〔式中、
破線は、アミド結合を形成することによって生物学的に活性な部分の第1級又は第2級の脂肪族アミン基に結合していることを示しており;
Xは、C(R4R4a)、N(R4)、O、C(R4R4a)-C(R5R5a)、C(R5R5a)-C(R4R4a)、C(R4R4a)-N(R6)、N(R6)-C(R4R4a)、C(R4R4a)-O又はO-C(R4R4a)であり;
X1は、C又はS(O)であり;
X2は、C(R7,R7a)又はC(R7,R7a)-C(R8,R8a)であり;
R1、R1a、R2、R2a、R3、R3a、R4、R4a、R5、R5a、R6、R7、R7a、R8、R8aは、独立して、H及びC1-4アルキルからなる群から選択され;又は、
場合により、対R1a/R4a、対R1a/R5a、対R4a/R5a、対R4a/R5a、対R7a/R8aのうちの1以上は、化学結合を形成してもよく;
場合により、対R1/R1a、対R2/R2a、対R4/R4a、対R5/R5a、対R7/R7a、対R8/R8aのうちの1以上は、それらが結合している原子と一緒になってC3-7シクロアルキル又は4〜7員のヘテロシクリルを形成してもよく;
場合により、対R1/R4、対R1/R5、対R1/R6、対R4/R5、対R7/R8、対R2/R3のうちの1以上は、それらが結合している原子と一緒になって環Aを形成してもよく;
場合により、R3/R3aは、それらが結合している窒素原子と一緒になって4〜7員のヘテロ環を形成してもよく;
Aは、フェニル、ナフチル、インデニル、インダニル、テトラリニル、C3-10シクロアルキル、4〜7員のヘテロシクリル及び9〜11員のヘテロビシクリルからなる群から選択され;及び、
ここで、L1は、1つの基L2-Zで置換されており、及び、場合によりさらに置換されていてもよいが、但し、式(VI)において星印が付けられている水素は置換基で置き換えられず;
ここで、
L2は、単一の化学結合又はスペーサーであり;及び、
Zは、請求項25〜31のいずれかに記載のヒドロゲルである〕
で表される生物学的に不活性なリンカー部分-L1である;
請求項46に記載の担体結合プロドラッグ。
【請求項49】
前記生物学的に活性な部分Dがヒドロキシル基を含んでおり、及び、当該プロドラッグに関する構造が、式(X)
D-O-Z0 (X)
〔式中、
Dは、ヒドロキシル基の酸素を介して部分Z0に結合している、ヒドロキシル基を含んでいる生物学的に活性な部分であり;
Z0は、C(O)-X0-Z1、C(O)O-X0-Z1、S(O)2-X0-Z1、C(S)-X0-Z1、S(O)2O-X0-Z1、S(O)2N(R1)-X0-Z1、CH(OR1)-X0-Z1、C(OR1)(OR2)-X0-Z1、C(O)N(R1)-X0-Z1、P(=O)(OH)O-X0-Z1、P(=O)(OR1)O-X0-Z1、P(=O)(SH)O-X0-Z1、P(=O)(SR1)O-X0-Z1、P(=O)(OR1)-X0-Z1、P(=S)(OH)O-X0-Z1、P(=S)(OR1)O-X0-Z1、P(=S)(OH)N(R1)-X0-Z1、P(=S)(OR1)N(R2)-X0-Z1、P(=O)(OH)N(R1)-X0-Z1又はP(=O)(OR1)N(R2)-X0-Z1であり;
R1、R2は、独立して、C1-6アルキルからなる群から選択され;又は、R1、R2は、一緒になってC1-6アルキレン架橋基を形成し;
X0は、(X0A)m1-(X0B)m2であり;
m1、m2は、独立して、0又は1であり;
X0Aは、T0であり;
X0Bは、同一であるか若しくは異なっている1以上のR3で置換されているか又は置換されていない分枝鎖又は非分枝鎖のC1-10アルキレン基であり;
R3は、ハロゲン、CN、C(O)R4、C(O)OR4、OR4、C(O)R4、C(O)N(R4R4a)、S(O)2N(R4R4a)、S(O)N(R4R4a)、S(O)2R4、S(O)R4、N(R4)S(O)2N(R4aR4b)、SR4、N(R4R4a)、NO2、OC(O)R4、N(R4)C(O)R4a、N(R4)SO2R4a、N(R4)S(O)R4a、N(R4)C(O)N(R4aR4b)、N(R4)C(O)OR4a、OC(O)N(R4R4a)又はT0であり;
R4、R4a、R4bは、独立して、H、T0、C1-4アルキル、C2-4アルケニル及びC2-4アルキニルからなる群から選択され(ここで、C1-4アルキル、C2-4アルケニル及びC2-4アルキニルは、同一であるか又は異なっている1以上のR5で場合により置換されていてもよい);
R5は、ハロゲン、CN、C(O)R6、C(O)OR6、OR6、C(O)R6、C(O)N(R6R6a)、S(O)2N(R6R6a)、S(O)N(R6R6a)、S(O)2R6、S(O)R6、N(R6)S(O)2N(R6aR6b)、SR6、N(R6R6a)、NO2、OC(O)R6、N(R6)C(O)R6a、N(R6)SO2R6a、N(R6)S(O)R6a、N(R6)C(O)N(R6aR6b)、N(R6)C(O)OR6a、OC(O)N(R6R6a)であり;
R6、R6a、R6bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のハロゲンで場合により置換されていてもよい);
T0は、フェニル、ナフチル、アズレニル、インデニル、インダニル、C3-7シクロアルキル、3〜7員のヘテロシクリル又は8〜11員のヘテロビシクリルであり(ここで、T0は、同一であるか又は異なっている1以上のR7で場合により置換されていてもよい);
R7は、ハロゲン、CN、COOR8、OR8、C(O)R8、C(O)N(R8R8a)、S(O)2N(R8R8a)、S(O)N(R8R8a)、S(O)2R8、S(O)R8、N(R8)S(O)2N(R8aR8b)、SR8、N(R8R8a)、NO2、OC(O)R8、N(R8)C(O)R8a、N(R8)S(O)2R8a、N(R8)S(O)R8a、N(R8)C(O)OR8a、N(R8)C(O)N(R8aR8b)、OC(O)N(R8R8a)、オキソ(=O)(ここで、該環は少なくとも部分的に飽和している)、C1-6アルキル、C2-6アルケニル又はC2-6アルキニルであり(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のR9で場合により置換されていてもよい);
R8、R8a、R8bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のR10で場合により置換されていてもよい);
R9、R10は、独立して、ハロゲン、CN、C(O)R11、C(O)OR11、OR11、C(O)R11、C(O)N(R11R11a)、S(O)2N(R11R11a)、S(O)N(R11R11a)、S(O)2R11、S(O)R11、N(R11)S(O)2N(R11aR11b)、SR11、N(R11R11a)、NO2、OC(O)R11、N(R11)C(O)R11a、N(R11)SO2R11a、N(R11)S(O)R11a、N(R11)C(O)N(R11aR11b)、N(R11)C(O)OR11a及びOC(O)N(R11R11a)からなる群から選択され;
R11、R11a、R11bは、独立して、H、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルからなる群から選択され(ここで、C1-6アルキル、C2-6アルケニル及びC2-6アルキニルは、同一であるか又は異なっている1以上のハロゲンで場合により置換されていてもよい);
Z1は、X0に共有結合的に結合している、請求項25〜31のいずれかに記載のヒドロゲルである〕
で表されるプロドラッグコンジュゲートによって与えられる、請求項46に記載の担体結合プロドラッグ。
【請求項50】
前記生物学的に活性な部分Dが芳香族ヒドロキシル基を含んでおり、及び、前記一時的なプロドラッグリンカーLが、
(i) 式(XI)
【化15】

〔式中、
破線は、カルバメート基を形成することによってL1が生物学的に活性な部分Dの芳香族ヒドロキシル基に結合していることを示しており;
R1は、C1-4アルキル、ヘテロアルキル、C3-7シクロアルキル及び
【化16】

からなる群から選択され;及び、
R2、R2a、R3、R3aは、独立して、水素、置換されているか若しくは置換されていない直鎖若しくは分枝鎖若しくは環状のC1-4アルキル又はヘテロアルキルから選択され;
mは、独立して、2、3又は4である〕
で表される部分L1;
(ii) 部分L2(ここで、L2は化学結合又はスペーサーであり、及び、L2は請求項25〜31のいずれかに記載のヒドロゲルに結合している);
を含んでいる生物学的に不活性なリンカーL〔ここで、L1は1つのL2部分で置換されており;場合により、Lは、さらに置換されてもよい〕である、請求項46に記載の担体結合プロドラッグ。
【請求項51】
製薬上許容される賦形剤と一緒に請求項41〜50のいずれかに記載のプロドラッグ又はその薬学的な塩を含んでいる、医薬組成物。
【請求項52】
薬物中で使用するための、請求項41〜50のいずれかに記載のプロドラッグ又は請求項51に記載の医薬組成物。
【請求項53】
1以上の状態を治療することが必要な哺乳類患者において、治療する方法、制御する方法、遅延させる方法又は予防する方法であって、該患者に治療有効量の請求項41〜50のいずれかに記載のプロドラッグ又は請求項51に記載の医薬組成物又はそれらの製薬上許容される塩を投与することを含む、前記方法。
【請求項54】
ヒドロゲルを調製する方法であって、
(a) 式
【化17】

〔式中、nは、3〜100の整数である〕
で表されるバックボーン試薬を下記式
【化18】

〔式中、
qは、3〜100の整数であり;
各mは、独立して、2〜4の整数である〕
で表されるクロスリンカー試薬と2:1〜1.05:1のアミン/活性エステルの比で反応させて、好ましくは、1gのヒドロゲル当たり0.02〜2mmolのアミンがローディングしているヒドロゲルを生じさせる段階を含み;及び、前記試薬は適切な塩基の存在下において非プロトン性溶媒に溶解させる、前記方法。
【請求項55】
前記非プロトン性溶媒がDMSOであり、及び、前記塩基がN,N,N',N'-テトラメチルエチレンジアミンである、請求項54に記載の方法。
【請求項56】
請求項54又は55に記載の調製方法から得ることができるヒドロゲル。
【請求項57】
撹拌、破砕、切削、プレス又は摩砕などの機械的処理によって粉砕し、場合により篩にかけることによって得ることができる、コーティング、メッシュ、ステント又は微粒子の形態にある、請求項1、26又は56のいずれかに記載のヒドロゲル。
【請求項58】
前記試薬を適切な乳化剤の存在下で脂肪族炭化水素の中に分散させる、請求項54に記載の調製方法。
【請求項59】
前記脂肪族炭化水素がn-ヘプタンであり、及び、前記乳化剤がポリ(エチレングリコール)30ジポリヒドロキシステアレートである、請求項58に記載の調製方法。
【請求項60】
微粒子を回収し、洗浄し及び粒径に従って機械的篩によって分別することをさらに特徴とする、請求項54、55、58又は59のいずれかに記載の調製方法。
【請求項61】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) 生物学的に活性な部分を請求項56からのヒドロゲルと反応させて一時的な結合を形成させ、並びに、未反応の生物学的に活性な部分を洗浄及び濾過によって除去する段階;
(b) 場合により、未反応の反応性官能基を適切なキャッピング試薬でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項62】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) スペーサー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲートを生じさせる段階;
(b) 段階(a)からの生物学的に活性な部分-スペーサーコンジュゲートを請求項56のヒドロゲルの反応性官能基と反応させ、並びに、未反応の生物学的に活性な部分-スペーサーコンジュゲートを洗浄及び濾過によって除去する段階;
(c) 場合により、未反応の反応性官能基を適切なキャッピング試薬でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項63】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲートを生じさせる段階;
(b) 段階(a)からの生物学的に活性な部分-リンカーコンジュゲートを請求項56のヒドロゲルの反応性官能基と反応させ、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(c) 場合により、未反応の反応性官能基を適切なキャッピング試薬でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項64】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) 請求項56のヒドロゲルをN-(3-マレイミドプロピル)-21-アミノ-4,7,10,13,16,19-ヘキサオキサ-ヘンエイコサン酸NHSと反応させることにより当該ヒドロゲルを誘導体化してマレイミドで官能基化されたヒドロゲルを生じさせ、並びに、未反応のN-(3-マレイミドプロピル)-21-アミノ-4,7,10,13,16,19-ヘキサオキサ-ヘンエイコサン酸NHSを洗浄及び濾過によって除去する段階;
(b) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲート(ここで、該リンカーは遊離チオール基(-SH)を含んでいる)を生じさせる段階;
(c) 段階(b)からの生物学的に活性な部分-リンカーコンジュゲートをpHが5.5〜8の範囲内にある緩衝化水溶液の中で室温〜4℃の範囲内の温度で段階(a)からのマレイミドで官能基化されたヒドロゲルと反応させ、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(c) 未反応の反応性官能基を34-500Daのチオール含有化合物でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項65】
請求項13〜22又は41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) 請求項56のヒドロゲルをN-(3-マレイミドプロピル)-21-アミノ-4,7,10,13,16,19-ヘキサオキサ-ヘンエイコサン酸NHSエステルと反応させることにより当該ヒドロゲルを誘導体化してマレイミドで官能基化されたヒドロゲルを生じさせ、並びに、未反応のN-(3-マレイミドプロピル)-21-アミノ-4,7,10,13,16,19-ヘキサオキサ-ヘンエイコサン酸NHSエステルを洗浄及び濾過によって除去する段階;
(b) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲート(ここで、該リンカーは遊離チオール基(-SH)を含んでおり、及び、該生物学的に活性な部分はジスルフィド(-S-S-)結合を含んでいる)を生じさせる段階;
(c) 段階(b)からの生物学的に活性な部分-リンカーコンジュゲートをpHが2〜5の範囲内にある緩衝化水溶液の中で室温〜4℃の範囲内の温度で段階(a)からのマレイミドで官能基化されたヒドロゲルと反応させ(ここで、該リンカーはチオール基に連結されており、及び、該生物学的に活性な部分はジスルフィド(-S-S-)結合を含んでいる)、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(d) 未反応の反応性官能基を34-500Daのチオール含有化合物でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項66】
請求項13〜22又は41〜55のいずれかに記載のプロドラッグを調製する方法であって、
(a) 請求項56のヒドロゲルを保護されたチオール基を含んでいる低分子量スペーサー試薬と反応させることにより当該ヒドロゲルを誘導体化してチオールで官能基化されたヒドロゲル(ここで、該チオール基は保護基に連結されている)を生じさせ、並びに、未反応のスペーサー試薬を洗浄及び濾過によって除去する段階;
(b) 段階(a)からのチオールで官能基化されたヒドロゲルを脱保護し、並びに、放出された保護基を洗浄及び濾過によって除去する段階;
(c) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲート(ここで、該リンカーはマレイミド部分を含んでいる)を生じさせる段階;
(d) 段階(c)からの生物学的に活性な部分-リンカーコンジュゲートをpHが5.5〜8の範囲内にある緩衝化水溶液の中で室温〜4℃の範囲内の温度で段階(b)からのチオールで官能基化されたヒドロゲルと反応させ、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(e) 未反応の反応性官能基を100-300Daのマレイミド含有化合物でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項67】
請求項13〜22及び41〜50のいずれかに記載のプロドラッグを調製する方法であって、
(a) 請求項56のヒドロゲルを保護されたチオール基を含んでいる低分子量スペーサー試薬と反応させることにより当該ヒドロゲルを誘導体化してチオールで官能基化されたヒドロゲル(ここで、該チオール基は保護基に連結されている)を生じさせ、並びに、未反応のスペーサー試薬を洗浄及び濾過によって除去する段階;
(b) 段階(a)からのチオールで官能基化されたヒドロゲルを脱保護し、並びに、放出された保護基を洗浄及び濾過によって除去する段階;
(c) リンカー試薬に生物学的に活性な部分を連結して生物学的に活性な部分-リンカーコンジュゲート(ここで、該リンカーはマレイミド部分を含んでおり、及び、該生物学的に活性な部分はジスルフィド(-S-S-)結合を含んでいる)を生じさせる段階;
(d) 段階(b)からの生物学的に活性な部分-リンカーコンジュゲートをpHが2〜5の範囲内にある緩衝化水溶液の中で室温〜4℃の範囲内の温度で段階(a)からのチオールで官能基化されたヒドロゲルと反応させ(ここで、該リンカーはチオール基に連結されており、及び、該生物学的に活性な部分はジスルフィド(-S-S-)結合を含んでいる)、並びに、未反応の生物学的に活性な部分-リンカーコンジュゲートを洗浄及び濾過によって除去する段階;
(e) 未反応の反応性官能基を100-300Daのマレイミド含有化合物でキャッピングし、並びに、未反応のキャッピング試薬を洗浄及び濾過によって除去する段階;
を含む、前記方法。
【請求項68】
請求項61〜67のいずれかに記載の調製方法から得ることができるプロドラッグ。
【請求項69】
注射針で注射可能なプロドラッグを調製する方法であって、
(a) 請求項61〜67のいずれかに記載の調製方法に準じて微粒子の形態にあるプロドラッグを調製する段階;
(b) 前記微粒子を篩にかける段階;
(c) プロドラッグビーズの粒径が25〜80μmであるフラクションを選択する段階;
(d) 段階(c)からのビーズフラクションを注射に適した水性バッファー溶液の中に懸濁させる段階;
を含む、前記方法。
【請求項70】
請求項69に記載の調製方法から得ることができる、注射針で注射可能なプロドラッグ。
【請求項71】
内径が300μm未満である注射針を通して注射することが可能な、請求項69から得られるプロドラッグ。
【請求項72】
内径が225μm未満である注射針を通して注射することが可能な、請求項71に記載のプロドラッグ。
【請求項73】
内径が175μm未満である注射針を通して注射することが可能な、請求項71に記載のプロドラッグ。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【公表番号】特表2013−500950(P2013−500950A)
【公表日】平成25年1月10日(2013.1.10)
【国際特許分類】
【出願番号】特願2012−522186(P2012−522186)
【出願日】平成22年7月30日(2010.7.30)
【国際出願番号】PCT/EP2010/061155
【国際公開番号】WO2011/012715
【国際公開日】平成23年2月3日(2011.2.3)
【出願人】(510209133)アセンディス ファーマ エー/エス (6)
【Fターム(参考)】
【公表日】平成25年1月10日(2013.1.10)
【国際特許分類】
【出願日】平成22年7月30日(2010.7.30)
【国際出願番号】PCT/EP2010/061155
【国際公開番号】WO2011/012715
【国際公開日】平成23年2月3日(2011.2.3)
【出願人】(510209133)アセンディス ファーマ エー/エス (6)
【Fターム(参考)】
[ Back to top ]

