画像取得装置、画像取得方法及び画像取得プログラム
【課題】蛍光標識の検出精度の向上を図ること。
【解決手段】この画像取得装置は、蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射する光源と、生体サンプルの撮像対象を拡大する対物レンズを含む光学系と、対物レンズにより拡大される撮像対象の像が結像される撮像素子と、撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で前記光学系の焦点位置を移動させる移動制御部と、前記光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させる露光制御部とを具備する。
【解決手段】この画像取得装置は、蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射する光源と、生体サンプルの撮像対象を拡大する対物レンズを含む光学系と、対物レンズにより拡大される撮像対象の像が結像される撮像素子と、撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で前記光学系の焦点位置を移動させる移動制御部と、前記光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させる露光制御部とを具備する。
【発明の詳細な説明】
【技術分野】
【0001】
本技術は、顕微鏡を用いて画像を取得する画像取得装置、画像取得方法及び画像取得プログラムに関する。
【背景技術】
【0002】
生物組織など、微細な粒子を分析、分取する手法としてフローサイトメトリーがある。フローサイトメトリー装置(フローサイトメータ)は、細胞などの粒子1個ずつから、大きさなどの形態の情報、DNA/RNA蛍光染色や、タンパクなどを蛍光抗体で染色した蛍光の情報を高速に取得し、それらの相関を解析し、目的の細胞集団などを分取することが可能な装置である。また、細胞の蛍光画像からサイトメトリーを行う手法としてはイメージングサイトメトリーが知られる。イメージングサイトメトリーでは、スライドガラスやシャーレ上の生体サンプルの蛍光像を拡大して撮影し、当該蛍光像中の一つ一つの細胞の情報、例えば細胞を標識する輝点の強度(輝度)やサイズなどの定量・数値化、細胞周期の解析などが行われる。
【0003】
蛍光染色された生体サンプルの蛍光像を取得する場合、生体サンプルの厚み方向に所定間隔ごとに焦点を移動させ、これら焦点での蛍光像それぞれを画像データとして生成することが行われる。これにより、ターゲットの細胞を標識する輝点を取りこぼすことなく取得できる。しかしながらこの場合、1つの生体サンプルに対する蛍光像の枚数が膨大となり、生体サンプルあたりの処理負荷及びデータ容量が増大する傾向を呈する。
【0004】
焦点位置の間隔を広げることで1つの生体サンプルに対する蛍光像の枚数を減らすことはできるが、この場合にはターゲットの細胞を標識する輝点を取りこぼす可能性があり、解析精度が低下する。また、対物レンズのNAを下げるなどの方法により対物レンズの焦点深度を大きくすることも検討されたが、この場合、すべての蛍光像の解像度が均一に落ちてしまうため、やはり解析精度が低下する。
【0005】
このような事情に関連して、例えば特許文献1には、次のような蛍光画像の取得方法が開示されている。この方法では、蛍光像取得部は可動ステージをz軸方向(光軸方向)に移動させ、サンプル部位に対する光学系の焦点を厚み方向に移動させる。蛍光像取得部は、z軸方向への可動ステージの移動が開始された時点から終了する時点まで撮像素子を露光させ、当該終了時点でその露光により得られるサンプル部位の蛍光像を撮像素子から取得する。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2011−017982公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
特許文献1に記載の技術によれば、撮影対象である生体サンプルの厚さ方向の全体にわたって各焦点位置の画像が足し合わされた1つの画像を撮影することができる。これにより、生体サンプルの厚さ方向の全体に存在する各輝点の像がぼけた状態であるものの漏れなく得られる。
【0008】
しかし、このように生体サンプルの厚さ方向の全体にわたって焦点位置を移動させながら撮像素子を連続的に露光することによって得られた画像によると、実際には、生体サンプルの厚さ方向の両端部分に存在する輝点は、中間部分に存在する輝点に比較して、サイズが大きく輝度が低いものなる。このため輝点の輝度、サイズなどの、測定精度が低下するおそれがある。
【0009】
以上のような事情に鑑み、本技術の目的は、蛍光標識の検出精度の向上を図ることのできる画像取得装置、画像取得方法および画像取得プログラムを提供することにある。
【課題を解決するための手段】
【0010】
上述の課題を解決するため、本技術の一形態に係る画像取得装置は、蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射する光源と、前記生体サンプルの撮像対象を拡大する対物レンズを含む光学系と、対物レンズにより拡大される撮像対象の像が結像される撮像素子と、撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で前記光学系の焦点位置を移動させる移動制御部と、前記光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させる露光制御部とを具備する。
【0011】
上記の画像取得装置において、前記撮像対象の厚さの範囲の両側の前記所定のマージンが等しいことが、より望ましい。
【0012】
上記の画像取得装置は、蛍光標識に対する励起光を照射する光源をさらに具備し、
前記露光制御部は、光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させることで前記撮影対象の蛍光像を取得するものとしてもよい。
【0013】
上記の画像取得装置は、前記取得された蛍光像から前記蛍光標識を検出して、当該蛍光標識の輝度およびサイズを求める検出部をさらに具備するものであってよい。
【0014】
本技術の他の形態に係る画像取得方法は、蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射し、前記生体サンプルの撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で、撮像対象を拡大する対物レンズを含む光学系の焦点位置を移動させ、前記光学系の焦点位置を前記延長範囲で移動させる間、撮像素子を露光させることによる。
【0015】
本技術の他の形態に係る画像取得プログラムは、蛍光標識が付された生体サンプルに光源より当該蛍光標識に対する励起光を照射させ、前記生体サンプルの撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で、撮像対象を拡大する対物レンズを含む光学系の焦点位置を移動させ、前記光学系の焦点位置を前記延長範囲で移動させる間、撮像素子を露光させることをコンピュータに実行させるものである。
【発明の効果】
【0016】
以上のように本技術によれば、蛍光標識の検出精度の向上を図れる。
【図面の簡単な説明】
【0017】
【図1】本技術の第1の実施形態に係る画像取得装置を示す模式図である。
【図2】図1の画像取得装置の画像取得対象である生体サンプルを示す図である。
【図3】図1の画像取得装置におけるデータ処理部のハードウェア構成を示すブロック図である。
【図4】典型的な画像取得装置による生体サンプル像取得処理を説明するための図である。
【図5】典型的な画像取得装置により撮影された生体サンプル像の例を示す図である。
【図6】図1の画像取得装置による生体サンプル像取得処理を説明するための図である。
【図7】図1の画像取得装置により撮影された生体サンプル像の例を示す図である。
【図8】図1の画像取得装置による生体サンプル像取得処理のための機能ブロック図である。
【図9】図1の画像取得装置による撮像対象の領域を示す図である。
【図10】図1の画像取得装置による蛍光マーカの検出結果の記録例である。
【図11】図10の蛍光マーカの検出結果の記録例に対応する生体サンプルの例を示す図である。
【図12】図11の生体サンプルから得られる生体サンプル像を示す図である。
【発明を実施するための形態】
【0018】
<第1の実施形態>
[画像取得装置の構成]
図1は、第1の実施形態に係る画像取得装置100を示す模式図である。同図に示すように、本実施形態における画像取得装置100は、顕微鏡10と、データ処理部20とを有する。
【0019】
[顕微鏡の構成]
顕微鏡10は、ステージ11、光学系12、光源13及び撮像素子14を有する。
ステージ11は、例えば組織切片、細胞、染色体等の生体高分子等の生体サンプルSPLを載置可能な載置面を有し、当該載置面に対してその平行方向(x−y平面方向)及び垂直方向(z軸方向)へ移動可能とされている。
【0020】
図2は、上記ステージ11に載置される生体サンプルSPLをステージ11の側面方向から示した図である。同図に示すように、生体サンプルSPLは、Z方向に例えば数μmから数十μmの厚さを有し、スライドガラスSG及びカバーガラスCGに挟まれて所定の固定手法により固定されている。生体サンプルSPLは蛍光染色剤によって染色されている。蛍光染色剤は同一の光源から照射される励起光によって蛍光を発する染色剤である。蛍光染色剤としては、例えば、DAPI(4',6-diamidino-2-phenylindole)、SpAqua、SpGreenなどを挙げることができる。
【0021】
図1に戻り、ステージ11の上方には光学系12が配置される。光学系12は、対物レンズ12A、結像レンズ12B、ダイクロイックミラー12C、エミッションフィルタ12D及び励起フィルタ12Eを有する。光源13は、例えば水銀ランプ等の電球やLED(Light Emitting Diode)など、蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射するものである。
【0022】
励起フィルタ12Eは、生体サンプルSPLの蛍光像を得る場合に、光源13から出射された光のうち蛍光色素を励起する励起波長の光のみを透過させることで励起光を生成する。ダイクロイックミラー12Cは、当該励起フィルタで透過されて入射する励起光を反射させて対物レンズ12Aへ導く。対物レンズ12Aは、当該励起光を生体サンプルSPLへ集光する。そして対物レンズ12A及び結像レンズ12Bは、生体サンプルSPLの像を所定の倍率に拡大し、当該拡大像を撮像素子14の撮像面に結像させる。
【0023】
生体サンプルSPLに励起光が照射されると、生体サンプルSPLの各組織に結合している染色剤が蛍光を発する。この蛍光は、対物レンズ12Aを介してダイクロイックミラー12Cを透過し、エミッションフィルタ12Dを介して結像レンズ12Bへ到達する。エミッションフィルタ12Dは、上記対物レンズ12Aによって拡大された、励起フィルタを透過した光を吸収し、発色光の一部を透過する。当該外光が喪失された発色光の像は、上述のとおり、結像レンズ12Bにより拡大され、撮像素子14上に結像される。
【0024】
撮像素子14としては、例えばCCD(Charge Coupled Device)やCMOS(Complementary Metal Oxide Semiconductor)イメージセンサ等が用いられる。撮像素子14は、RGB(Red、Green、Blue)の色別に光を受けて電気信号に変換する光電変換素子を有し、入射光からカラー画像を得るカラーイメージャである。
【0025】
データ処理部20は、光源13を駆動させ、撮像素子14を用いて生体サンプルSPLの蛍光像を取得し、これをサンプルデータとして保存する。
【0026】
[データ処理部の構成]
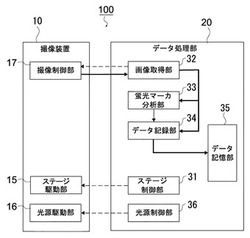
図3は、データ処理部20のハードウェアの構成を示すブロック図である。
データ処理部20は、例えばPC(Personal Computer)により構成され、撮像素子14より取得した生体サンプルSPLの蛍光像を、例えばJPEG(Joint Photographic Experts Group)等の任意形式のデジタル画像データとして保存する。
【0027】
同図に示すようにデータ処理部20は、CPU(Central Processing Unit)21、ROM(Read Only Memory)22、RAM(Random Access Memory)23、操作入力部24、インターフェイス部25、表示部26及び記憶部27を有し、これら各ブロックがバス28を介して接続されている。
【0028】
ROM22は、各種の処理を実行するためのファームウェア等の複数のプログラムやデータを固定的に記憶する。RAM23は、CPU21の作業用領域として用いられ、OS(Operating System)、実行中の各種アプリケーション、処理中の各種データを一時的に保持する。
【0029】
記憶部27は、例えばHDD(Hard Disk Drive)や、フラッシュメモリ、その他の固体メモリ等の不揮発性メモリである。当該記憶部27には、OSや各種アプリケーション、各種データが記憶される。特に本実施形態では、記憶部27には、撮像素子14から取り込まれた蛍光画像データや、蛍光画像データを画像処理する画像処理アプリケーションも記憶される。
【0030】
インターフェイス部25は、顕微鏡10のステージ11、光源13及び撮像素子14をそれぞれ駆動するコントロール基板(ステージ駆動部15、光源駆動部16、撮像制御部17)とそれぞれ接続され、所定の通信規格により当該コントロール基板とデータ処理部20との間で信号のやり取りを行う。
【0031】
CPU21は、ROM22や記憶部27に格納された複数のプログラムのうち、操作入力部24から与えられる命令に対応するプログラムをRAM23に展開し、当該展開されたプログラムにしたがって、表示部26及び記憶部27を適宜制御する。
【0032】
操作入力部24は、例えばマウス等のポインティングデバイス、キーボード、タッチパネル、その他の操作装置である。
【0033】
表示部26は、例えば液晶ディスプレイ、EL(Electro-Luminescence)ディスプレイ、プラズマディスプレイ、CRT(Cathode Ray Tube)ディスプレイ等である。当該表示部26は、データ処理部20に内蔵されていてもよいし、データ処理部20に外部接続されていてもよい。
【0034】
[典型的な生体サンプル像取得処理]
本実施形態の画像取得装置100による生体サンプル像取得処理の説明に入る前に、典型的な生体サンプル像取得処理とその課題について説明する。
【0035】
図4は、典型的な画像取得装置による生体サンプル像取得処理を説明するための図である。
この典型的な画像取得装置は、光学系の焦点位置を生体サンプルSPLの厚み方向に図中下から上へ向けて生体サンプルSPLの厚さの範囲で移動させるとともに、焦点位置の移動開始時点から終了時点まで撮像素子を露光させ、終了時点で撮像素子から画素のデータを取り込む。これにより、生体サンプルSPLの厚さ方向の全体にわたって各焦点位置の画像が足し合わされた1つの蛍光像が得られる。
【0036】
しかし、このように生体サンプルの厚さ方向の全体にわたって焦点位置を移動させながら撮像素子を露光させることによって得られた蛍光像によると、実際には、生体サンプルの厚さ方向の両端部分に存在するターゲットを標識する輝点(以下「蛍光マーカ」と呼ぶ。)の像は、中間部分に存在する蛍光マーカの像に比較して、サイズが大きく輝度が低いものなる。このため蛍光マーカをサイズ及び輝度を基準に検出する場合などに検出精度が低下する。
【0037】
すなわち、図4において、生体サンプルSPLの厚さ方向の中間部分に存在する蛍光マーカP1に着目すると、焦点位置は当該蛍光マーカP1に徐々に近付き、焦点が当該蛍光マーカP1に対して一旦合った状態から次第に離れて行く。すなわち、蛍光マーカP1の像はぼやけた大きな状態から次第にはっきりした小さな状態に変化して行き、その後再びぼやけた大きな状態に変化する。次に、生体サンプルSPLの上部に存在する蛍光マーカP2に着目すると、焦点位置は当該蛍光マーカP2に、蛍光マーカP1の場合よりも遠い位置から近付いて行くことになる。したがって、図5に示すように、生体サンプルSPLの上部に存在する蛍光マーカP1の像は中間部分の蛍光マーカP2の像に比べ、よりぼやけた大きなものになる。同様に、生体サンプルの下部に存在する蛍光マーカP3の場合にも、焦点位置は蛍光マーカP3に一旦合った状態から、蛍光マーカP1の場合よりも遠くまで離れて行くことから、当該蛍光マーカP3の像も中間部の蛍光マーカP1の像に比べ、よりぼやけた大きなものになる。このため蛍光マーカのサイズ及び輝度を基準に蛍光マーカを検出する場合などに検出精度が低下するおそれがある。
【0038】
このような点を改善するために、本実施形態の画像取得装置100は、図6に示すように、生体サンプルSPLの厚さの範囲の両側に所定のマージンDを加えた延長範囲で光学系12の焦点位置を移動させるようにしたものである。これにより、図7に示すように、すべての蛍光マークR1−R4の像がほぼ同様にぼけた生体サンプル像が得られるようにしたものである。すべての蛍光マークR1−R4の像がほぼ同様にぼけた生体サンプル像が得られることで、例えば、蛍光マーカの検出精度の向上、ならびに蛍光マーカの輝度およびサイズの測定精度の向上を期待できる。
【0039】
[生体サンプル像取得処理の具体的な内容]
データ処理部20のCPU21はROM22や記憶部27に格納された複数のプログラムのうち、操作入力部24から与えられる命令に対応するプログラムをRAM23に展開する。CPU21は、この展開されたプログラム(画像取得プログラム)に基づいて生体サンプル像取得処理を実行する。
【0040】
図8はこの生体サンプル像取得処理のための機能ブロック図である。
同図において、ステージ制御部31(移動制御部)は、生体サンプルSPLの対象とすべき部位(以下、これをサンプル部位とも呼ぶ)が撮像範囲に位置するようステージ11を順次移動させて、例えば図9に示すように、該撮像範囲ARに対して生体サンプルSPLを割り当てる。なお、図9では、撮像範囲ARに割り当てるべき生体サンプルSPLの領域が重ならない態様となっているが、隣接する領域の一部が重なる態様であってもよい。
【0041】
また、ステージ制御部31は、対象とすべきサンプル部位が撮像範囲ARに移動されるごとに、ステージ11をz軸方向(対物レンズ12Aの光軸方向)に移動させて、サンプル部位に対する焦点を厚み方向に移動させるように制御を行う。このとき、図6に示したように、生体サンプルSPLの厚さの範囲の下端から下方へ所定のマージンDだけ外れた第1の位置Z1から、当該厚さの範囲の上端から上方へ所定のマージンDだけ外れた第2の位置Z2までの間(延長範囲)を焦点位置が移動するようにステージ11をz軸方向に移動させる。
【0042】
画像取得部32(露光制御部)は、対象とすべきサンプル部位をステージ制御部31が撮像範囲ARに移動するごとに、z軸方向へのステージ11の移動が開始された時点から終了する時点まで撮像素子14を露光させるように撮像制御部17に指令を送る。画像取得部32は、ステージ11におけるz軸方向への移動が終了する時点で、当該移動終了時点と移動開始時点との間の露光により得られるサンプル部位の像を撮像制御部17を介して撮像素子14から取得する。そして画像取得部32は、各撮像範囲ARに割り当てられるサンプル部位の像を、所定の連結アルゴリズムを用いて連結することによって全体の生体サンプル像を生成する。
【0043】
蛍光マーカ分析部33(分析部)は、画像取得部32により生成された生体サンプル像から、ターゲットとされる生体組織を標識する蛍光マーカ(以下「標的マーカ」とも呼ぶ。)を検出する。蛍光マーカ分析部33には、例えば、設定情報として、標的マーカが呈する色(以下「標的マーカ色」と呼ぶ。)と、細胞核を標識する蛍光マーカ(以下「核マーカ」と呼ぶ。)が呈する色(以下「核マーカ色」と呼ぶ。)とが設定される。また、対照とすべき遺伝子を標識する蛍光マーカ(以下「対照マーカ」と呼ぶ。)が用いられている場合、該対照とすべき遺伝子が正常の細胞核内に存在する数が設定される。またこの場合、対照遺伝子を標識する蛍光マーカ(以下「対照マーカ」と呼ぶ。)が呈する色(以下「対照マーカ色」と呼ぶ。)も設定される。
【0044】
これら設定情報は、蛍光染色に使用すべきプローブの製造元や、蛍光マーカの種などの使用条件によって一義的に決まる。具体的には、例えばabbott社のHER−2DNAプローブキットの場合、HER2遺伝子の標的マーカ色は「赤」として設定され、核マーカ色は「青」として設定される。またこの場合、染色体上のHER2遺伝子の隣に位置する遺伝子が対照遺伝子とされ、該対照遺伝子の対照マーカ色は「緑」として設定され、その数は標準的に「2」として設定される。
【0045】
次に、蛍光マーカ分析部33による蛍光マーカの検出方法を説明する。
蛍光マーカ分析部33は、画像取得部32により生成された生体サンプル像から、細胞核が呈するとして設定される核マーカ色に対応する画素であり、閾値以上の輝度となる画素が隣接する領域を細胞核として検出する。
【0046】
続いて、蛍光マーカ分析部33は、検出された細胞核内の標的マーカおよび対照マーカをそれぞれ検出する。ここで、生体サンプル像は、焦点位置を生体サンプルSPLの厚さの方向に延長範囲を移動させる間、撮像素子14を露光させることによって得られたものであることから、生体サンプル像において標的マーカおよび対照マーカはそれぞれほぼ円形状のぼけた輝点として標識される。さらに、生体サンプル像は、図6に示したように、焦点位置を生体サンプルSPLの厚さの範囲の下端から下方へ所定のマージンDだけ外れた第1の位置Z1から当該厚さの範囲の上端から上方へ所定のマージンDだけ外れた第2の位置Z2まで移動させる間、撮像素子14を露光させることによって得られたものである。したがって、生体サンプル像の中に含まれるすべての標的マーカおよび対照マーカはほぼ同様にぼけたものとなる。
【0047】
蛍光マーカ分析部33は、標的マーカに設定されたマーカ色を呈し、かつ閾値以上の輝度の画素がほぼ円形状に所定の数(面積)以上隣接するという条件を満足する領域(輝点)を標的マーカとして検出する。同様に、蛍光マーカ分析部33は、対照マーカに設定されたマーカ色を呈し、かつ閾値以上の輝度の画素がほぼ円形状に所定の数(面積)以上隣接するという条件を満足する領域(輝点)を対照マーカとして検出する。ここで、標的マーカを判定するための条件と、対照マーカを判定するための条件は、呈するマーカ色を除いて、同一としてもよく、相違させてもよい。
【0048】
上記のように、閾値以上の輝度の画素が所定の数(面積)以上隣接するという条件を満足する領域(輝点)が標的マーカおよび対照マーカとして検出されるので、生体サンプル像の中にほぼ同様にぼけた輝点として標識されるすべての標的マーカおよび対照マーカは、蛍光マーカ分析部33によって漏れなく検出されることになる。
【0049】
さらに、蛍光マーカ分析部33は、検出された標的マーカおよび対照マーカのそれぞれについて、輝度の平均値と面積を示す画素数を測定する。
【0050】
一方、データ記録部34は、画像取得部32により生成されたサンプル部位毎の生体サンプル像を連結して1つの生体サンプル画像を生成し、JPEG(Joint Photographic Experts Group)など所定の圧縮形式のサンプルデータに符号化してデータ記憶部35に記録する。この処理は蛍光マーカ分析部33による蛍光マーカの検出の前に行われてもよい。
【0051】
データ記録部34は、蛍光マーカ分析部33による蛍光マーカの測定結果を受けて、その測定結果のデータをデータ記憶部35にサンプルデータと関連付けて記録する。
【0052】
図10は、図11に示す生体サンプルから本実施形態の画像取得装置100により得られた生体サンプル像(図12)からの蛍光マーカ分析部33による蛍光マーカの測定結果の記録例である。
【0053】
この例では、2つの細胞核C1、C2が検出され、一方の細胞核C1には2つの標的マーカR11、R12と2つの対照マーカG11、G12が検出され、他方の細胞核C2にも2つの標的マーカR21、R22と2つの対照マーカG21、G22が検出された場合を示している。それぞれの細胞核C1、C2の中に検出された標的マーカと対照マーカにも、細胞核毎に標的マーカを識別するためのシリアル番号と対照マーカを識別するためのシリアル番号が付与される。なお、マーカの種類は色によって識別可能とされる。そして、それぞれの標的マーカおよび対照マーカには、輝度の平均値と当該マーカの面積を示す画素数が対応付けてデータ記憶部35に記録される。
【0054】
なお、蛍光マーカ分析部33による蛍光マーカの測定結果の記録データには、図10に示す情報の他、例えば、生体サンプルSPLの採取者名、採取者性別、採取者年齢及び採取日付などの情報が付与される。
【0055】
以上のように、本実施形態の構成によれば、画像取得部32は、生体サンプルSPLの厚さの範囲の下端から下方へ所定のマージンDだけ外れた第1の位置Z1から当該厚さの範囲の上端から上方へ所定のマージンDだけ外れた第2の位置Z2までの延長範囲を焦点位置を移動させる間、撮像素子14を露光させることによって生体サンプル像を取得する。
【0056】
このようにして得られた生体サンプル像においては、すべての標的マーカおよび対照マーカがほぼ同様にぼけたものとなる。このため、蛍光マーカ分析部33は、閾値以上の輝度の画素がほぼ円形状に所定の数(面積)以上隣接するという条件を満足する領域(輝点)を標的マーカおよび対照マーカとして検出する場合に、すべての標的マーカおよび対照マーカを漏れなく検出することができる。さらに、蛍光マーカ分析部33は、検出された標的マーカおよび対照マーカのそれぞれについて、輝度の平均値と面積を示す画素数を精度良く測定することができる。
【0057】
マージンDの値に関しては、生体サンプルSPLの厚さの範囲の下端から焦点位置の下端までの距離をD1、同範囲の上端から焦点位置の上端までの距離をD2として、必ずしもD1=D2である必要はない。しかし、生体サンプルSPLの厚さの範囲の上部に存在する蛍光マークと下部に存在する蛍光マークが可及的に同様なぼけが与えられるためにはD1=D2であることが望ましい。
【0058】
また、マージンDの値が小さすぎると、生体サンプルの厚さの範囲において中間部分に存在する蛍光マーカと、同範囲の両端部分に存在する蛍光マーカとの間での輝度の違いおよび面積の違いを十分に縮めることができない。逆にマージンDの値が大きすぎると、蛍光マーカの輝度が全体的に小さくなりすぎることで、蛍光マーカの検出そのものが困難になる。マージンDの好ましい具体的な値やその範囲は、生体サンプルSPLの厚さ、光学系12の対物レンズ12Aの開口数NA(焦点深度)など、様々な条件に依存するため、例えば、各種の条件を変更しながら最適値を見つけ出す方法が1つの手段として考えられる。この方法によると、例えば、開口数NAを0.8、マージンDを3μmとした場合には、各蛍光マーカ間でほぼ同様なぼけを与えられることを確認できた。
【0059】
なお、上述の実施形態の顕微鏡20の構成において、対物レンズ12Aは接眼レンズとすることもできる。
【0060】
また、上述の実施形態では、焦点位置を移動させるためにステージ11を移動させることとしたが、光学系12の対物レンズ12Aを移動させるようにしてもよい。
【0061】
上述の実施の形態では、データ処理部20にデータ記憶部35を設けて、これに生体サンプル像と蛍光マーカの検出結果を記録することとしたが、外部の記憶装置に記録するようにしてもよい。
【0062】
顕微鏡10とデータ処理部20との接続には、バス伝送路の他、ローカルエリアネットワークやインターネット、デジタル衛星放送等の有線又は無線の伝送媒体を用いることができる。
【0063】
なお、本技術は以下のような構成も採ることができる。
(1) 撮像対象を拡大する対物レンズを含む光学系と、
対物レンズにより拡大される撮像対象の像が結像される撮像素子と、
撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で前記光学系の焦点位置を移動させる移動制御部と、
前記光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させる露光制御部と
を具備する画像取得装置。
(2)前記(1)に記載の画像取得装置であって、
前記撮像対象の厚さの範囲の両側の前記所定のマージンが等しい
画像取得装置。
(3)前記(1)から(2)のうちいずれか1つに記載の画像取得装置であって、
蛍光標識に対する励起光を照射する光源をさらに具備し、
前記露光制御部は、光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させることで前記撮影対象の蛍光像を取得する
画像取得装置。
(4)前記(1)から(3)のうちいずれか1つに記載の画像取得装置であって、
前記取得された蛍光像から前記蛍光標識を検出して、当該蛍光標識の輝度およびサイズを求める分析部
をさらに具備する
画像取得装置。
【0064】
本発明はこの実施形態にのみ限定されるものではなく、本発明の要旨を逸脱しない範囲内において変更され得る。
【符号の説明】
【0065】
10…顕微鏡
11…ステージ
12…光学系
13…光源
14…撮像素子
20…データ処理部
31…ステージ制御部
32…画像取得部
33…蛍光マーカ分析部
34…データ記録部
35…データ記憶部
100…画像取得装置
【技術分野】
【0001】
本技術は、顕微鏡を用いて画像を取得する画像取得装置、画像取得方法及び画像取得プログラムに関する。
【背景技術】
【0002】
生物組織など、微細な粒子を分析、分取する手法としてフローサイトメトリーがある。フローサイトメトリー装置(フローサイトメータ)は、細胞などの粒子1個ずつから、大きさなどの形態の情報、DNA/RNA蛍光染色や、タンパクなどを蛍光抗体で染色した蛍光の情報を高速に取得し、それらの相関を解析し、目的の細胞集団などを分取することが可能な装置である。また、細胞の蛍光画像からサイトメトリーを行う手法としてはイメージングサイトメトリーが知られる。イメージングサイトメトリーでは、スライドガラスやシャーレ上の生体サンプルの蛍光像を拡大して撮影し、当該蛍光像中の一つ一つの細胞の情報、例えば細胞を標識する輝点の強度(輝度)やサイズなどの定量・数値化、細胞周期の解析などが行われる。
【0003】
蛍光染色された生体サンプルの蛍光像を取得する場合、生体サンプルの厚み方向に所定間隔ごとに焦点を移動させ、これら焦点での蛍光像それぞれを画像データとして生成することが行われる。これにより、ターゲットの細胞を標識する輝点を取りこぼすことなく取得できる。しかしながらこの場合、1つの生体サンプルに対する蛍光像の枚数が膨大となり、生体サンプルあたりの処理負荷及びデータ容量が増大する傾向を呈する。
【0004】
焦点位置の間隔を広げることで1つの生体サンプルに対する蛍光像の枚数を減らすことはできるが、この場合にはターゲットの細胞を標識する輝点を取りこぼす可能性があり、解析精度が低下する。また、対物レンズのNAを下げるなどの方法により対物レンズの焦点深度を大きくすることも検討されたが、この場合、すべての蛍光像の解像度が均一に落ちてしまうため、やはり解析精度が低下する。
【0005】
このような事情に関連して、例えば特許文献1には、次のような蛍光画像の取得方法が開示されている。この方法では、蛍光像取得部は可動ステージをz軸方向(光軸方向)に移動させ、サンプル部位に対する光学系の焦点を厚み方向に移動させる。蛍光像取得部は、z軸方向への可動ステージの移動が開始された時点から終了する時点まで撮像素子を露光させ、当該終了時点でその露光により得られるサンプル部位の蛍光像を撮像素子から取得する。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2011−017982公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
特許文献1に記載の技術によれば、撮影対象である生体サンプルの厚さ方向の全体にわたって各焦点位置の画像が足し合わされた1つの画像を撮影することができる。これにより、生体サンプルの厚さ方向の全体に存在する各輝点の像がぼけた状態であるものの漏れなく得られる。
【0008】
しかし、このように生体サンプルの厚さ方向の全体にわたって焦点位置を移動させながら撮像素子を連続的に露光することによって得られた画像によると、実際には、生体サンプルの厚さ方向の両端部分に存在する輝点は、中間部分に存在する輝点に比較して、サイズが大きく輝度が低いものなる。このため輝点の輝度、サイズなどの、測定精度が低下するおそれがある。
【0009】
以上のような事情に鑑み、本技術の目的は、蛍光標識の検出精度の向上を図ることのできる画像取得装置、画像取得方法および画像取得プログラムを提供することにある。
【課題を解決するための手段】
【0010】
上述の課題を解決するため、本技術の一形態に係る画像取得装置は、蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射する光源と、前記生体サンプルの撮像対象を拡大する対物レンズを含む光学系と、対物レンズにより拡大される撮像対象の像が結像される撮像素子と、撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で前記光学系の焦点位置を移動させる移動制御部と、前記光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させる露光制御部とを具備する。
【0011】
上記の画像取得装置において、前記撮像対象の厚さの範囲の両側の前記所定のマージンが等しいことが、より望ましい。
【0012】
上記の画像取得装置は、蛍光標識に対する励起光を照射する光源をさらに具備し、
前記露光制御部は、光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させることで前記撮影対象の蛍光像を取得するものとしてもよい。
【0013】
上記の画像取得装置は、前記取得された蛍光像から前記蛍光標識を検出して、当該蛍光標識の輝度およびサイズを求める検出部をさらに具備するものであってよい。
【0014】
本技術の他の形態に係る画像取得方法は、蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射し、前記生体サンプルの撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で、撮像対象を拡大する対物レンズを含む光学系の焦点位置を移動させ、前記光学系の焦点位置を前記延長範囲で移動させる間、撮像素子を露光させることによる。
【0015】
本技術の他の形態に係る画像取得プログラムは、蛍光標識が付された生体サンプルに光源より当該蛍光標識に対する励起光を照射させ、前記生体サンプルの撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で、撮像対象を拡大する対物レンズを含む光学系の焦点位置を移動させ、前記光学系の焦点位置を前記延長範囲で移動させる間、撮像素子を露光させることをコンピュータに実行させるものである。
【発明の効果】
【0016】
以上のように本技術によれば、蛍光標識の検出精度の向上を図れる。
【図面の簡単な説明】
【0017】
【図1】本技術の第1の実施形態に係る画像取得装置を示す模式図である。
【図2】図1の画像取得装置の画像取得対象である生体サンプルを示す図である。
【図3】図1の画像取得装置におけるデータ処理部のハードウェア構成を示すブロック図である。
【図4】典型的な画像取得装置による生体サンプル像取得処理を説明するための図である。
【図5】典型的な画像取得装置により撮影された生体サンプル像の例を示す図である。
【図6】図1の画像取得装置による生体サンプル像取得処理を説明するための図である。
【図7】図1の画像取得装置により撮影された生体サンプル像の例を示す図である。
【図8】図1の画像取得装置による生体サンプル像取得処理のための機能ブロック図である。
【図9】図1の画像取得装置による撮像対象の領域を示す図である。
【図10】図1の画像取得装置による蛍光マーカの検出結果の記録例である。
【図11】図10の蛍光マーカの検出結果の記録例に対応する生体サンプルの例を示す図である。
【図12】図11の生体サンプルから得られる生体サンプル像を示す図である。
【発明を実施するための形態】
【0018】
<第1の実施形態>
[画像取得装置の構成]
図1は、第1の実施形態に係る画像取得装置100を示す模式図である。同図に示すように、本実施形態における画像取得装置100は、顕微鏡10と、データ処理部20とを有する。
【0019】
[顕微鏡の構成]
顕微鏡10は、ステージ11、光学系12、光源13及び撮像素子14を有する。
ステージ11は、例えば組織切片、細胞、染色体等の生体高分子等の生体サンプルSPLを載置可能な載置面を有し、当該載置面に対してその平行方向(x−y平面方向)及び垂直方向(z軸方向)へ移動可能とされている。
【0020】
図2は、上記ステージ11に載置される生体サンプルSPLをステージ11の側面方向から示した図である。同図に示すように、生体サンプルSPLは、Z方向に例えば数μmから数十μmの厚さを有し、スライドガラスSG及びカバーガラスCGに挟まれて所定の固定手法により固定されている。生体サンプルSPLは蛍光染色剤によって染色されている。蛍光染色剤は同一の光源から照射される励起光によって蛍光を発する染色剤である。蛍光染色剤としては、例えば、DAPI(4',6-diamidino-2-phenylindole)、SpAqua、SpGreenなどを挙げることができる。
【0021】
図1に戻り、ステージ11の上方には光学系12が配置される。光学系12は、対物レンズ12A、結像レンズ12B、ダイクロイックミラー12C、エミッションフィルタ12D及び励起フィルタ12Eを有する。光源13は、例えば水銀ランプ等の電球やLED(Light Emitting Diode)など、蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射するものである。
【0022】
励起フィルタ12Eは、生体サンプルSPLの蛍光像を得る場合に、光源13から出射された光のうち蛍光色素を励起する励起波長の光のみを透過させることで励起光を生成する。ダイクロイックミラー12Cは、当該励起フィルタで透過されて入射する励起光を反射させて対物レンズ12Aへ導く。対物レンズ12Aは、当該励起光を生体サンプルSPLへ集光する。そして対物レンズ12A及び結像レンズ12Bは、生体サンプルSPLの像を所定の倍率に拡大し、当該拡大像を撮像素子14の撮像面に結像させる。
【0023】
生体サンプルSPLに励起光が照射されると、生体サンプルSPLの各組織に結合している染色剤が蛍光を発する。この蛍光は、対物レンズ12Aを介してダイクロイックミラー12Cを透過し、エミッションフィルタ12Dを介して結像レンズ12Bへ到達する。エミッションフィルタ12Dは、上記対物レンズ12Aによって拡大された、励起フィルタを透過した光を吸収し、発色光の一部を透過する。当該外光が喪失された発色光の像は、上述のとおり、結像レンズ12Bにより拡大され、撮像素子14上に結像される。
【0024】
撮像素子14としては、例えばCCD(Charge Coupled Device)やCMOS(Complementary Metal Oxide Semiconductor)イメージセンサ等が用いられる。撮像素子14は、RGB(Red、Green、Blue)の色別に光を受けて電気信号に変換する光電変換素子を有し、入射光からカラー画像を得るカラーイメージャである。
【0025】
データ処理部20は、光源13を駆動させ、撮像素子14を用いて生体サンプルSPLの蛍光像を取得し、これをサンプルデータとして保存する。
【0026】
[データ処理部の構成]
図3は、データ処理部20のハードウェアの構成を示すブロック図である。
データ処理部20は、例えばPC(Personal Computer)により構成され、撮像素子14より取得した生体サンプルSPLの蛍光像を、例えばJPEG(Joint Photographic Experts Group)等の任意形式のデジタル画像データとして保存する。
【0027】
同図に示すようにデータ処理部20は、CPU(Central Processing Unit)21、ROM(Read Only Memory)22、RAM(Random Access Memory)23、操作入力部24、インターフェイス部25、表示部26及び記憶部27を有し、これら各ブロックがバス28を介して接続されている。
【0028】
ROM22は、各種の処理を実行するためのファームウェア等の複数のプログラムやデータを固定的に記憶する。RAM23は、CPU21の作業用領域として用いられ、OS(Operating System)、実行中の各種アプリケーション、処理中の各種データを一時的に保持する。
【0029】
記憶部27は、例えばHDD(Hard Disk Drive)や、フラッシュメモリ、その他の固体メモリ等の不揮発性メモリである。当該記憶部27には、OSや各種アプリケーション、各種データが記憶される。特に本実施形態では、記憶部27には、撮像素子14から取り込まれた蛍光画像データや、蛍光画像データを画像処理する画像処理アプリケーションも記憶される。
【0030】
インターフェイス部25は、顕微鏡10のステージ11、光源13及び撮像素子14をそれぞれ駆動するコントロール基板(ステージ駆動部15、光源駆動部16、撮像制御部17)とそれぞれ接続され、所定の通信規格により当該コントロール基板とデータ処理部20との間で信号のやり取りを行う。
【0031】
CPU21は、ROM22や記憶部27に格納された複数のプログラムのうち、操作入力部24から与えられる命令に対応するプログラムをRAM23に展開し、当該展開されたプログラムにしたがって、表示部26及び記憶部27を適宜制御する。
【0032】
操作入力部24は、例えばマウス等のポインティングデバイス、キーボード、タッチパネル、その他の操作装置である。
【0033】
表示部26は、例えば液晶ディスプレイ、EL(Electro-Luminescence)ディスプレイ、プラズマディスプレイ、CRT(Cathode Ray Tube)ディスプレイ等である。当該表示部26は、データ処理部20に内蔵されていてもよいし、データ処理部20に外部接続されていてもよい。
【0034】
[典型的な生体サンプル像取得処理]
本実施形態の画像取得装置100による生体サンプル像取得処理の説明に入る前に、典型的な生体サンプル像取得処理とその課題について説明する。
【0035】
図4は、典型的な画像取得装置による生体サンプル像取得処理を説明するための図である。
この典型的な画像取得装置は、光学系の焦点位置を生体サンプルSPLの厚み方向に図中下から上へ向けて生体サンプルSPLの厚さの範囲で移動させるとともに、焦点位置の移動開始時点から終了時点まで撮像素子を露光させ、終了時点で撮像素子から画素のデータを取り込む。これにより、生体サンプルSPLの厚さ方向の全体にわたって各焦点位置の画像が足し合わされた1つの蛍光像が得られる。
【0036】
しかし、このように生体サンプルの厚さ方向の全体にわたって焦点位置を移動させながら撮像素子を露光させることによって得られた蛍光像によると、実際には、生体サンプルの厚さ方向の両端部分に存在するターゲットを標識する輝点(以下「蛍光マーカ」と呼ぶ。)の像は、中間部分に存在する蛍光マーカの像に比較して、サイズが大きく輝度が低いものなる。このため蛍光マーカをサイズ及び輝度を基準に検出する場合などに検出精度が低下する。
【0037】
すなわち、図4において、生体サンプルSPLの厚さ方向の中間部分に存在する蛍光マーカP1に着目すると、焦点位置は当該蛍光マーカP1に徐々に近付き、焦点が当該蛍光マーカP1に対して一旦合った状態から次第に離れて行く。すなわち、蛍光マーカP1の像はぼやけた大きな状態から次第にはっきりした小さな状態に変化して行き、その後再びぼやけた大きな状態に変化する。次に、生体サンプルSPLの上部に存在する蛍光マーカP2に着目すると、焦点位置は当該蛍光マーカP2に、蛍光マーカP1の場合よりも遠い位置から近付いて行くことになる。したがって、図5に示すように、生体サンプルSPLの上部に存在する蛍光マーカP1の像は中間部分の蛍光マーカP2の像に比べ、よりぼやけた大きなものになる。同様に、生体サンプルの下部に存在する蛍光マーカP3の場合にも、焦点位置は蛍光マーカP3に一旦合った状態から、蛍光マーカP1の場合よりも遠くまで離れて行くことから、当該蛍光マーカP3の像も中間部の蛍光マーカP1の像に比べ、よりぼやけた大きなものになる。このため蛍光マーカのサイズ及び輝度を基準に蛍光マーカを検出する場合などに検出精度が低下するおそれがある。
【0038】
このような点を改善するために、本実施形態の画像取得装置100は、図6に示すように、生体サンプルSPLの厚さの範囲の両側に所定のマージンDを加えた延長範囲で光学系12の焦点位置を移動させるようにしたものである。これにより、図7に示すように、すべての蛍光マークR1−R4の像がほぼ同様にぼけた生体サンプル像が得られるようにしたものである。すべての蛍光マークR1−R4の像がほぼ同様にぼけた生体サンプル像が得られることで、例えば、蛍光マーカの検出精度の向上、ならびに蛍光マーカの輝度およびサイズの測定精度の向上を期待できる。
【0039】
[生体サンプル像取得処理の具体的な内容]
データ処理部20のCPU21はROM22や記憶部27に格納された複数のプログラムのうち、操作入力部24から与えられる命令に対応するプログラムをRAM23に展開する。CPU21は、この展開されたプログラム(画像取得プログラム)に基づいて生体サンプル像取得処理を実行する。
【0040】
図8はこの生体サンプル像取得処理のための機能ブロック図である。
同図において、ステージ制御部31(移動制御部)は、生体サンプルSPLの対象とすべき部位(以下、これをサンプル部位とも呼ぶ)が撮像範囲に位置するようステージ11を順次移動させて、例えば図9に示すように、該撮像範囲ARに対して生体サンプルSPLを割り当てる。なお、図9では、撮像範囲ARに割り当てるべき生体サンプルSPLの領域が重ならない態様となっているが、隣接する領域の一部が重なる態様であってもよい。
【0041】
また、ステージ制御部31は、対象とすべきサンプル部位が撮像範囲ARに移動されるごとに、ステージ11をz軸方向(対物レンズ12Aの光軸方向)に移動させて、サンプル部位に対する焦点を厚み方向に移動させるように制御を行う。このとき、図6に示したように、生体サンプルSPLの厚さの範囲の下端から下方へ所定のマージンDだけ外れた第1の位置Z1から、当該厚さの範囲の上端から上方へ所定のマージンDだけ外れた第2の位置Z2までの間(延長範囲)を焦点位置が移動するようにステージ11をz軸方向に移動させる。
【0042】
画像取得部32(露光制御部)は、対象とすべきサンプル部位をステージ制御部31が撮像範囲ARに移動するごとに、z軸方向へのステージ11の移動が開始された時点から終了する時点まで撮像素子14を露光させるように撮像制御部17に指令を送る。画像取得部32は、ステージ11におけるz軸方向への移動が終了する時点で、当該移動終了時点と移動開始時点との間の露光により得られるサンプル部位の像を撮像制御部17を介して撮像素子14から取得する。そして画像取得部32は、各撮像範囲ARに割り当てられるサンプル部位の像を、所定の連結アルゴリズムを用いて連結することによって全体の生体サンプル像を生成する。
【0043】
蛍光マーカ分析部33(分析部)は、画像取得部32により生成された生体サンプル像から、ターゲットとされる生体組織を標識する蛍光マーカ(以下「標的マーカ」とも呼ぶ。)を検出する。蛍光マーカ分析部33には、例えば、設定情報として、標的マーカが呈する色(以下「標的マーカ色」と呼ぶ。)と、細胞核を標識する蛍光マーカ(以下「核マーカ」と呼ぶ。)が呈する色(以下「核マーカ色」と呼ぶ。)とが設定される。また、対照とすべき遺伝子を標識する蛍光マーカ(以下「対照マーカ」と呼ぶ。)が用いられている場合、該対照とすべき遺伝子が正常の細胞核内に存在する数が設定される。またこの場合、対照遺伝子を標識する蛍光マーカ(以下「対照マーカ」と呼ぶ。)が呈する色(以下「対照マーカ色」と呼ぶ。)も設定される。
【0044】
これら設定情報は、蛍光染色に使用すべきプローブの製造元や、蛍光マーカの種などの使用条件によって一義的に決まる。具体的には、例えばabbott社のHER−2DNAプローブキットの場合、HER2遺伝子の標的マーカ色は「赤」として設定され、核マーカ色は「青」として設定される。またこの場合、染色体上のHER2遺伝子の隣に位置する遺伝子が対照遺伝子とされ、該対照遺伝子の対照マーカ色は「緑」として設定され、その数は標準的に「2」として設定される。
【0045】
次に、蛍光マーカ分析部33による蛍光マーカの検出方法を説明する。
蛍光マーカ分析部33は、画像取得部32により生成された生体サンプル像から、細胞核が呈するとして設定される核マーカ色に対応する画素であり、閾値以上の輝度となる画素が隣接する領域を細胞核として検出する。
【0046】
続いて、蛍光マーカ分析部33は、検出された細胞核内の標的マーカおよび対照マーカをそれぞれ検出する。ここで、生体サンプル像は、焦点位置を生体サンプルSPLの厚さの方向に延長範囲を移動させる間、撮像素子14を露光させることによって得られたものであることから、生体サンプル像において標的マーカおよび対照マーカはそれぞれほぼ円形状のぼけた輝点として標識される。さらに、生体サンプル像は、図6に示したように、焦点位置を生体サンプルSPLの厚さの範囲の下端から下方へ所定のマージンDだけ外れた第1の位置Z1から当該厚さの範囲の上端から上方へ所定のマージンDだけ外れた第2の位置Z2まで移動させる間、撮像素子14を露光させることによって得られたものである。したがって、生体サンプル像の中に含まれるすべての標的マーカおよび対照マーカはほぼ同様にぼけたものとなる。
【0047】
蛍光マーカ分析部33は、標的マーカに設定されたマーカ色を呈し、かつ閾値以上の輝度の画素がほぼ円形状に所定の数(面積)以上隣接するという条件を満足する領域(輝点)を標的マーカとして検出する。同様に、蛍光マーカ分析部33は、対照マーカに設定されたマーカ色を呈し、かつ閾値以上の輝度の画素がほぼ円形状に所定の数(面積)以上隣接するという条件を満足する領域(輝点)を対照マーカとして検出する。ここで、標的マーカを判定するための条件と、対照マーカを判定するための条件は、呈するマーカ色を除いて、同一としてもよく、相違させてもよい。
【0048】
上記のように、閾値以上の輝度の画素が所定の数(面積)以上隣接するという条件を満足する領域(輝点)が標的マーカおよび対照マーカとして検出されるので、生体サンプル像の中にほぼ同様にぼけた輝点として標識されるすべての標的マーカおよび対照マーカは、蛍光マーカ分析部33によって漏れなく検出されることになる。
【0049】
さらに、蛍光マーカ分析部33は、検出された標的マーカおよび対照マーカのそれぞれについて、輝度の平均値と面積を示す画素数を測定する。
【0050】
一方、データ記録部34は、画像取得部32により生成されたサンプル部位毎の生体サンプル像を連結して1つの生体サンプル画像を生成し、JPEG(Joint Photographic Experts Group)など所定の圧縮形式のサンプルデータに符号化してデータ記憶部35に記録する。この処理は蛍光マーカ分析部33による蛍光マーカの検出の前に行われてもよい。
【0051】
データ記録部34は、蛍光マーカ分析部33による蛍光マーカの測定結果を受けて、その測定結果のデータをデータ記憶部35にサンプルデータと関連付けて記録する。
【0052】
図10は、図11に示す生体サンプルから本実施形態の画像取得装置100により得られた生体サンプル像(図12)からの蛍光マーカ分析部33による蛍光マーカの測定結果の記録例である。
【0053】
この例では、2つの細胞核C1、C2が検出され、一方の細胞核C1には2つの標的マーカR11、R12と2つの対照マーカG11、G12が検出され、他方の細胞核C2にも2つの標的マーカR21、R22と2つの対照マーカG21、G22が検出された場合を示している。それぞれの細胞核C1、C2の中に検出された標的マーカと対照マーカにも、細胞核毎に標的マーカを識別するためのシリアル番号と対照マーカを識別するためのシリアル番号が付与される。なお、マーカの種類は色によって識別可能とされる。そして、それぞれの標的マーカおよび対照マーカには、輝度の平均値と当該マーカの面積を示す画素数が対応付けてデータ記憶部35に記録される。
【0054】
なお、蛍光マーカ分析部33による蛍光マーカの測定結果の記録データには、図10に示す情報の他、例えば、生体サンプルSPLの採取者名、採取者性別、採取者年齢及び採取日付などの情報が付与される。
【0055】
以上のように、本実施形態の構成によれば、画像取得部32は、生体サンプルSPLの厚さの範囲の下端から下方へ所定のマージンDだけ外れた第1の位置Z1から当該厚さの範囲の上端から上方へ所定のマージンDだけ外れた第2の位置Z2までの延長範囲を焦点位置を移動させる間、撮像素子14を露光させることによって生体サンプル像を取得する。
【0056】
このようにして得られた生体サンプル像においては、すべての標的マーカおよび対照マーカがほぼ同様にぼけたものとなる。このため、蛍光マーカ分析部33は、閾値以上の輝度の画素がほぼ円形状に所定の数(面積)以上隣接するという条件を満足する領域(輝点)を標的マーカおよび対照マーカとして検出する場合に、すべての標的マーカおよび対照マーカを漏れなく検出することができる。さらに、蛍光マーカ分析部33は、検出された標的マーカおよび対照マーカのそれぞれについて、輝度の平均値と面積を示す画素数を精度良く測定することができる。
【0057】
マージンDの値に関しては、生体サンプルSPLの厚さの範囲の下端から焦点位置の下端までの距離をD1、同範囲の上端から焦点位置の上端までの距離をD2として、必ずしもD1=D2である必要はない。しかし、生体サンプルSPLの厚さの範囲の上部に存在する蛍光マークと下部に存在する蛍光マークが可及的に同様なぼけが与えられるためにはD1=D2であることが望ましい。
【0058】
また、マージンDの値が小さすぎると、生体サンプルの厚さの範囲において中間部分に存在する蛍光マーカと、同範囲の両端部分に存在する蛍光マーカとの間での輝度の違いおよび面積の違いを十分に縮めることができない。逆にマージンDの値が大きすぎると、蛍光マーカの輝度が全体的に小さくなりすぎることで、蛍光マーカの検出そのものが困難になる。マージンDの好ましい具体的な値やその範囲は、生体サンプルSPLの厚さ、光学系12の対物レンズ12Aの開口数NA(焦点深度)など、様々な条件に依存するため、例えば、各種の条件を変更しながら最適値を見つけ出す方法が1つの手段として考えられる。この方法によると、例えば、開口数NAを0.8、マージンDを3μmとした場合には、各蛍光マーカ間でほぼ同様なぼけを与えられることを確認できた。
【0059】
なお、上述の実施形態の顕微鏡20の構成において、対物レンズ12Aは接眼レンズとすることもできる。
【0060】
また、上述の実施形態では、焦点位置を移動させるためにステージ11を移動させることとしたが、光学系12の対物レンズ12Aを移動させるようにしてもよい。
【0061】
上述の実施の形態では、データ処理部20にデータ記憶部35を設けて、これに生体サンプル像と蛍光マーカの検出結果を記録することとしたが、外部の記憶装置に記録するようにしてもよい。
【0062】
顕微鏡10とデータ処理部20との接続には、バス伝送路の他、ローカルエリアネットワークやインターネット、デジタル衛星放送等の有線又は無線の伝送媒体を用いることができる。
【0063】
なお、本技術は以下のような構成も採ることができる。
(1) 撮像対象を拡大する対物レンズを含む光学系と、
対物レンズにより拡大される撮像対象の像が結像される撮像素子と、
撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で前記光学系の焦点位置を移動させる移動制御部と、
前記光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させる露光制御部と
を具備する画像取得装置。
(2)前記(1)に記載の画像取得装置であって、
前記撮像対象の厚さの範囲の両側の前記所定のマージンが等しい
画像取得装置。
(3)前記(1)から(2)のうちいずれか1つに記載の画像取得装置であって、
蛍光標識に対する励起光を照射する光源をさらに具備し、
前記露光制御部は、光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させることで前記撮影対象の蛍光像を取得する
画像取得装置。
(4)前記(1)から(3)のうちいずれか1つに記載の画像取得装置であって、
前記取得された蛍光像から前記蛍光標識を検出して、当該蛍光標識の輝度およびサイズを求める分析部
をさらに具備する
画像取得装置。
【0064】
本発明はこの実施形態にのみ限定されるものではなく、本発明の要旨を逸脱しない範囲内において変更され得る。
【符号の説明】
【0065】
10…顕微鏡
11…ステージ
12…光学系
13…光源
14…撮像素子
20…データ処理部
31…ステージ制御部
32…画像取得部
33…蛍光マーカ分析部
34…データ記録部
35…データ記憶部
100…画像取得装置
【特許請求の範囲】
【請求項1】
蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射する光源と、
前記生体サンプルの撮像対象を拡大する対物レンズを含む光学系と、
対物レンズにより拡大される撮像対象の像が結像される撮像素子と、
撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で前記光学系の焦点位置を移動させる移動制御部と、
前記光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させる露光制御部と
を具備する画像取得装置。
【請求項2】
請求項1に記載の画像取得装置であって、
前記撮像対象の厚さの範囲の両側の前記所定のマージンが等しい
画像取得装置。
【請求項3】
請求項2に記載の画像取得装置であって、
蛍光標識に対する励起光を照射する光源をさらに具備し、
前記露光制御部は、光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させることで前記撮影対象の蛍光像を取得する
画像取得装置。
【請求項4】
請求項3に記載の画像取得装置であって、
前記取得された蛍光像から前記蛍光標識を検出して、当該蛍光標識の輝度およびサイズを求める分析部
をさらに具備する
画像取得装置。
【請求項5】
蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射し、
前記生体サンプルの撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で、撮像対象を拡大する対物レンズを含む光学系の焦点位置を移動させ、
前記光学系の焦点位置を前記延長範囲で移動させる間、撮像素子を露光させる
画像取得方法。
【請求項6】
蛍光標識が付された生体サンプルに光源より当該蛍光標識に対する励起光を照射させ、
前記生体サンプルの撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で、撮像対象を拡大する対物レンズを含む光学系の焦点位置を移動させ、
前記光学系の焦点位置を前記延長範囲で移動させる間、撮像素子を露光させることをコンピュータに実行させる画像取得プログラム。
【請求項1】
蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射する光源と、
前記生体サンプルの撮像対象を拡大する対物レンズを含む光学系と、
対物レンズにより拡大される撮像対象の像が結像される撮像素子と、
撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で前記光学系の焦点位置を移動させる移動制御部と、
前記光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させる露光制御部と
を具備する画像取得装置。
【請求項2】
請求項1に記載の画像取得装置であって、
前記撮像対象の厚さの範囲の両側の前記所定のマージンが等しい
画像取得装置。
【請求項3】
請求項2に記載の画像取得装置であって、
蛍光標識に対する励起光を照射する光源をさらに具備し、
前記露光制御部は、光学系の焦点位置を前記延長範囲で移動させる間、前記撮像素子を露光させることで前記撮影対象の蛍光像を取得する
画像取得装置。
【請求項4】
請求項3に記載の画像取得装置であって、
前記取得された蛍光像から前記蛍光標識を検出して、当該蛍光標識の輝度およびサイズを求める分析部
をさらに具備する
画像取得装置。
【請求項5】
蛍光標識が付された生体サンプルに当該蛍光標識に対する励起光を照射し、
前記生体サンプルの撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で、撮像対象を拡大する対物レンズを含む光学系の焦点位置を移動させ、
前記光学系の焦点位置を前記延長範囲で移動させる間、撮像素子を露光させる
画像取得方法。
【請求項6】
蛍光標識が付された生体サンプルに光源より当該蛍光標識に対する励起光を照射させ、
前記生体サンプルの撮像対象の厚さの範囲の両側に所定のマージンを加えた延長範囲で、撮像対象を拡大する対物レンズを含む光学系の焦点位置を移動させ、
前記光学系の焦点位置を前記延長範囲で移動させる間、撮像素子を露光させることをコンピュータに実行させる画像取得プログラム。
【図1】


【図2】


【図3】


【図4】


【図6】


【図8】


【図9】


【図10】


【図11】


【図5】


【図7】


【図12】




【図2】


【図3】


【図4】


【図6】


【図8】


【図9】


【図10】


【図11】


【図5】


【図7】


【図12】


【公開番号】特開2013−105087(P2013−105087A)
【公開日】平成25年5月30日(2013.5.30)
【国際特許分類】
【出願番号】特願2011−249866(P2011−249866)
【出願日】平成23年11月15日(2011.11.15)
【出願人】(000002185)ソニー株式会社 (34,172)
【Fターム(参考)】
【公開日】平成25年5月30日(2013.5.30)
【国際特許分類】
【出願日】平成23年11月15日(2011.11.15)
【出願人】(000002185)ソニー株式会社 (34,172)
【Fターム(参考)】
[ Back to top ]

