画像形成材料
【課題】鮮明な画像を形成することができる、ロイコ色素を用いた画像形成材料を提供する。
【解決手段】呈色性化合物および顕色剤を、誘電率が5以上7以下である溶媒に溶解させたことを特徴とする画像形成材料。
【解決手段】呈色性化合物および顕色剤を、誘電率が5以上7以下である溶媒に溶解させたことを特徴とする画像形成材料。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はロイコ色素を用いた印刷インキやボールペンなどに使用される画像形成材料に関し、さらに詳しくは、消去可能な画像形成材料やリライタブル画像形成材料の発色成分として用いられる画像形成材料に関する。
【背景技術】
【0002】
地球環境の保護およびCO2による温室効果を抑制するためには森林の保護は絶対条件であり、新たな伐採を最低限に維持し、植林を含めた森林再生とのバランスを保つためには現在すでに保有している紙資源を如何に効率よく利用していくかが大きな課題となっている。現在の紙資源の再利用は、画像形成材料を剥離させる脱墨工程を経た紙繊維を質の悪い紙に漉き直して目的別に使い分ける「リサイクル」であり、脱墨工程のコスト高の問題や廃液の処理による新たな環境汚染の可能性などが指摘されている。
【0003】
その一方で、これまでに古くは鉛筆とケシゴム、筆記用具に修正液にあるように、画像の修正によるハードコピーの再利用に関しては実用化がなされてきた。また、最近ではハードコピー用紙のリユースを目的とした特殊紙リライタブルペーパーなどが提案されてきた。ここで紙質の劣化を極力防ぎ同一の目的に複数回使用する「リユース」は、紙質を落としながら他の目的に使用する「リサイクル」とは異なる概念であり、紙資源の保護の観点からみればより重要な概念であるといえる。それぞれの「リサイクル」の前段階で有効な「リユース」が行われれば新たに必要な紙資源を最小限に抑えることができる。
【0004】
本発明者らはすでに、呈色性化合物と顕色剤との相互作用が増大すると発色状態となり、相互作用が減少すると消色状態になることに着目して、呈色性化合物および顕色剤を含有する組成系に新たに顕色剤を捕獲する消色剤を加えることにより、室温付近の温度で発色状態が安定に存在し、かつ、熱や溶媒による処理で、実用温度において長期に消色状態を固定できる画像形成材料(たとえば特許文献1、2参照)を提案している。これらの画像形成材料は、画像の発色・消色状態の安定性が高く、加えて材料も安全性が高く、インクなどとして用いることができ、しかも大規模消色処理が可能であるという従来の技術にないメリットを有している。このため、これらの画像形成材料を用いれば、現行のリサイクル技術に代わる有効な紙のリユース技術を実現でき、紙ゴミを著しく減少できることから、省資源に大きな効果がある。
【0005】
さらに、本発明者らは、これらの消去可能な画像形成材料の特性向上を検討する過程で紙の構成要素であるセルロースが消色剤の機能を有することを見出し、被記録媒体に紙を用いる用途では消去剤を含有しない画像形成材料でも熱や溶媒による処理で消去できることを立証している。
【0006】
しかし、これらの画像形成材料には、熱消色における発色と消色のコントラストに限界があるという課題があった。これらの画像形成材料では、発色・消色は呈色性化合物と顕色剤との相互作用の平衡によって定まる。そのため、発色と消色のコントラストは、主に呈色性化合物と顕色剤の組み合わせによって決定され、あまり改善の余地がないと考えられていた。
【特許文献1】特開平10−88046号公報
【特許文献2】特開2000−154345号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明の目的は、鮮明な画像を形成することができる、ロイコ色素を用いた画像形成材料を提供することにある。
【課題を解決するための手段】
【0008】
本発明の実施形態に係る画像形成材料は、呈色性化合物および顕色剤を、誘電率が5以上7以下である溶媒に溶解させたことを特徴とする。
【発明の効果】
【0009】
本発明の実施形態に係る画像形成材料は、画像濃度を大幅に改善できる。
【発明を実施するための最良の形態】
【0010】
以下、本発明の実施形態を説明する。
本発明の実施形態に係る画像形成材料では、呈色性化合物であるロイコ色素(L)と顕色剤(D)との間には下記のスキーム1に示す化学平衡が存在し、この平衡がロイコ色素の発色性を支配すると考えられている。
【0011】
スキーム1
L + D ← → [L−D]
そこで、まず溶液中、室温付近におけるスキーム1の平衡に関する詳細な研究を行った。その結果、溶液中、室温付近では、平衡はほとんど解離の方向、すなわち消色側に偏っていることが明らかになった。つまり、ほとんどの色素が発色に寄与していないことが判明した。したがって、スキーム1の平衡を会合の方向、すなわち発色側に偏らせる有効な手段を見出すことができれば、本発明の実施形態に係る画像形成材料の発色濃度を大幅に改善できるという指針も得られた。そこで、どのような条件下において発色性が向上するのか、平衡の状態を理解し易い溶液中での挙動を観測することにより検討した。
【0012】
ロイコ色素の発色は、ラクトン環が開環し分子内の共役が拡大することによると考えられている。スキーム2に、ロイコ色素Aと顕色剤(没食子酸エチル、EG)とが相互作用して発色種Bを生成する化学反応の平衡を示す。スキーム2では発色性中間体Mを想定している。
【化1】

【0013】
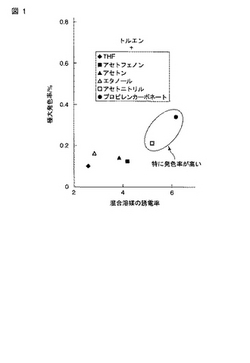
スキーム2に示したように、発色種Bおよび発色性中間体Mでは、分子内で電荷が局在化している。そこで、これら荷電性発色種を安定化することによる平衡制御を試みた。ここでは、極性の低いトルエンをベースとし、ここに種々の極性溶媒を様々な割合で添加し、随時発色の様子を観測した。つまり、極性溶媒とその割合を様々に変え、得られた溶液の紫外可視吸収スペクトルをそのつど測定した。その結果、用いる極性溶媒により、発色の様子が異なることが明らかになった。具体的には、極性溶媒の誘電率が高いほど、より大きい極大発色率が得られるという傾向がみられた。図1に、極大発色率を与える混合溶媒の誘電率(正味の誘電率)と、極大発色率との関係を示す。
【0014】
混合溶媒の誘電率は下記の式(1)を用いて算出した。誘電率は分極可能な部分の密度に依存し、混合により体積が変化しなければ加成性が成り立つので式(1)による算出が妥当である。
正味の誘電率=DpXp+DtXt (1)
(Dp,Dt:極性溶媒,トルエンの誘電率、Xp,Xt:極性溶媒,トルエンの体積分率)。
【0015】
図1から、非常に狭い誘電率範囲において高い極大発色率が得られることがわかった。つまり、誘電率が5以上7以下の溶媒中で特に高い発色率が得られた。一方、誘電率が5未満であるかまたは7を超えると、高い発色率は得られない。すなわち、本発明の実施形態に係る画像形成材料は、ロイコ色素および顕色剤を、誘電率が5以上7以下である溶媒に溶解させたものであり、高い発色率が得られる。
【0016】
また、前記溶媒は、誘電率が2.4以下の溶媒と誘電率が35以上の溶媒との混合溶媒であることが好ましい。誘電率が2.4以下の溶媒としては、たとえばトルエンが挙げられる。誘電率が35以上の溶媒としては、たとえばアセトニトリルやプロピレンカーボネートが挙げられる。
【0017】
以下、本発明の実施形態に係る画像形成材料に用いられる材料について、より詳細に説明する。
【0018】
呈色性化合物としては、ロイコオーラミン類、ジアリールフタリド類、ポリアリールカルビノール類、アシルオーラミン類、アリールオーラミン類、ローダミンBラクタム類、インドリン類、スピロピラン類、フルオラン類などの電子供与性有機物が挙げられる。具体的には、クリスタルバイオレットラクトン(CVL)、マラカイトグリーンラクトン、2−アニリノ−6−(N−シクロヘキシル−N−メチルアミノ)−3−メチルフルオラン、2−アニリノ−3−メチル−6−(N−メチル−N−プロピルアミノ)フルオラン、3−[4−(4−フェニルアミノフェニル)アミノフェニル]アミノ−6−メチル−7−クロロフルオラン、2−アニリノ−6−(N−メチル−N−イソブチルアミノ)−3−メチルフルオラン、2−アニリノ−6−(ジブチルアミノ)−3−メチルフルオラン、3−クロロ−6−(シクロヘキシルアミノ)フルオラン、2−クロロ−6−(ジエチルアミノ)フルオラン、7−(N,N−ジベンジルアミノ)−3−(N,N−ジエチルアミノ)フルオラン、3,6−ビス(ジエチルアミノ)フルオラン−γ−(4’−ニトロ)アニリノラクタム、3−ジエチルアミノベンゾ[a]−フルオラン、3−ジエチルアミノ−6−メチル−7−アミノフルオラン、3−ジエチルアミノ−7−キシリジノフルオラン、3−(4−ジエチルアミノ−2−エトキシフェニル)−3−(1−エチル−2−メチルインドール−3−イル)−4−アザフタリド、3−(4−ジエチルアミノフェニル)−3−(1−エチル−2−メチルインドール−3−イル)フタリド、3−ジエチルアミノ−7−クロロアニリノフルオラン、3−ジエチルアミノ−7,8−ベンゾフルオラン、3,3−ビス(1−n−ブチル−2−メチルインドール−3−イル)フタリド、3,6−ジメチルエトキシフルオラン、3−ジエチルアミノ−6−メソキシ−7−アミノフルオラン、DEPM、ATP,ETAC、2−(2−クロロアニリノ)−6−ジブチルアミノフルオラン、クリスタルバイオレットカルビノール、マラカイトグリーンカルビノール、N−(2、3−ジクロロフェニル)ロイコオーラミン、N−ベンゾイルオーラミン、ローダミンBラクタム、N−アセチルオーラミン、N−フェニルオーラミン、2−(フェニルイミノエタンジリデン)−3,3−ジメチルインドリン、N−3,3−トリメチルインドリノベンゾスピロピラン、8’−メトキシ−N−3,3−トリメチルインドリノベンゾスピロピラン、3−ジエチルアミノ−6−メチル−7−クロロフルオラン、3−ジエチルアミノ−7−メトキシフルオラン、3−ジエチルアミノ−6−ベンジルオキシフルオラン、1,2−ベンゾ−6−ジエチルアミノフルオラン、3,6−ジ−p−トルイジノ−4,5−ジメチルフルオラン−フェニルヒドラジド−γ−ラクタム、3−アミノ−5−メチルフルオランなどが例示される。これらは単独で用いてもよいし2種以上混合して用いてもよい。呈色性化合物を適宜選択すれば多様な色の発色状態が得られることからカラー対応も容易である。これらの中で、特に適している材料は、トリフェニルメタン系、フルオラン系、フェニル−インドール−フタリド系の呈色性化合物である。
【0019】
顕色剤としては、フェノール類、フェノール金属塩類、カルボン酸金属塩類、ベンゾフェノン類、スルホン酸、スルホン酸塩、リン酸類、リン酸金属塩類、酸性リン酸エステル、酸性リン酸エステル金属塩類、亜リン酸類、亜リン酸金属塩類などが挙げられる。これらは単独で用いてもよいし、2種以上混合して用いてもよい。これらのうちでも特に好適な顕色剤は、没食子酸または没食子酸エステル、たとえば没食子酸メチル、没食子酸エチル、没食子酸n−プロピル、没食子酸i−ブチルなど;ジヒドロキシ安息香酸またはそのエステル、たとえば2,3−ジヒドロキシ安息香酸、3,5−ジヒドロキシ安息香酸メチルなど;ヒドロキシアセトフェノン類、たとえば2,4−ジヒドロキシアセトフェノン、2,5−ジヒドロキシアセトフェノン、2,6−ジヒドロキシアセトフェノン、3,5−ジヒドロキシアセトフェノン、2,3,4−トリヒドロキシアセトフェノンなど;ヒドロキシベンゾフェノン類、たとえば2,4−ジヒドロキシベンゾフェノン、4,4’−ジヒドロキシベンゾフェノン、2,3,4−トリヒドロキシベンゾフェノン、2,4,4’−トリヒドロキシベンゾフェノン、2,2’,4,4’−テトラヒドロキシベンゾフェノン、2,3,4,4’−テトラヒドロキシベンゾフェノンなど;ビフェノール類、たとえば2,4’−ビフェノール、4,4’−ビフェノールなど;多価フェノール類、たとえば4−[(4−ヒドロキシフェニル)メチル]−1,2,3−ベンゼントリオール、4−[(3,5−ジメチル−4−ヒドロキシフェニル)メチル]−1,2,3−ベンゼントリオール、4,6−ビス[(3,5−ジメチル−4−ヒドロキシフェニル)メチル]−1,2,3−ベンゼントリオール、4,4’−[1,4−フェニレンビス(1−メチルエチリデン)ビス(ベンゼン−1,2,3−トリオール)]、4,4’−[1,4−フェニレンビス(1−メチルエチリデン)ビス(1,2−ベンゼンジオール)]、4,4’,4’’−エチリデントリスフェノール、4,4’−(1−メチルエチリデン)ビスフェノール、メチレントリス−p−クレゾールなどである。これらの顕色剤のうちで特に好適なものは、没食子酸エステル、たとえば没食子酸エチル、没食子酸n−プロピル、没食子酸i−プロピル、没食子酸ブチルなど;ヒドロキシベンゾフェノン類、たとえば2,4−ジヒドロキシベンゾフェノン、4,4’−ジヒドロキシベンゾフェノン、2,3,4−トリヒドロキシベンゾフェノン、2,4,4’−トリヒドロキシベンゾフェノン、2,2’,4,4’−テトラヒドロキシベンゾフェノン、2,3,4,4’−テトラヒドロキシベンゾフェノンなどである。
【0020】
本発明の実施形態に係る画像形成材料はインクに分類できる。インクの用途では、上で説明した呈色性化合物および顕色剤に加えて、図2に示す成分を添加することができる。
【0021】
本発明の実施形態に係る画像形成材料は、加熱するか、または消去溶媒(消去剤を含む場合もあるし含まない場合もある)と接触させることにより消去することができる。
【0022】
なお、本発明において示した誘電率の好適な範囲は、溶媒だけでなくあらゆる材質に適用される。したがって、誘電率が5以上7以下であれば、呈色性化合物および顕色剤をバインダー樹脂などの固体マトリクスに分散させた画像形成材料でも、同様に高い発色性が期待できる。
【実施例】
【0023】
以下、本発明の実施例を説明する。
実施例1
磁気攪拌子を付したスクリューバイアル(20mL)に、呈色性化合物であるロイコ色素Lとして山田化学製のblue203(3−(4−アミノ−2−ヘキシルオキシフェニル)−3−(1−エチル−2−メチルインドール−3−イル)−4−アザフタリド)を0.027g(5.00×10-5mol)、顕色剤Dとして没食子酸エチル(EG)を0.010g(5.04×10-5mol)、およびアセトニトリルを8、10、14または20体積%含むアセトニトリル(誘電率:37.5)/トルエン(誘電率:2.38)混合溶媒を5mL入れ、よく攪拌し均一溶液とした。
【0024】
また、アセトニトリルを6体積%含有するアセトニトリル/トルエン混合溶媒を用いた場合には、溶解度の関係からblue203 0.019g(3.52×10-5mol)およびEG 0.007g(3.53×10-5mol)を用いて均一溶液を調製した。
【0025】
得られた溶液の吸光度を測定し、モル吸光係数(ε=36000)を用い、それぞれの溶液におけるL−D会合体(発色種、スキーム1参照)の濃度([L−D])を算出した。この[L−D]をblue203の初期濃度([L]0=完全に発色した場合の[L−D])で規格化することにより、各溶液における発色率を求めた。
【0026】
下記表1に、アセトニトリル/トルエン混合溶媒中のアセトニトリル含有率(体積%)、混合溶媒の誘電率、吸光度、発色率(%)を示す。図3に、混合溶媒中のアセトニトリル含有率と発色率との関係を示す。これらの結果からわかるように、アセトニトリル含有率8体積%、誘電率5.19の混合溶媒を用いたインクで極大発色率が得られた。
【表1】

【0027】
[実施例2]
磁気攪拌子を付したスクリューバイアル(20mL)に、呈色性化合物としてblue203 0.025g(4.63×10-5mol)、顕色剤としてEG 0.009g(4.54×10-5mol)、およびプロピレンカーボネートを6、8、14、または20体積%含むプロピレンカーボネート(誘電率:65.1)/トルエン(誘電率:2.38)混合溶媒を5mL入れ、よく攪拌し均一溶液とした。
【0028】
また、プロピレンカーボネートを4体積%含有するプロピレンカーボネート/トルエン混合溶媒を用いた場合には、溶解度の関係からblue203 0.019g(3.52×10-5mol)およびEG 0.007g(3.53×10-5mol)を用いて均一溶液を調製した。
【0029】
下記表2に、プロピレンカーボネート/トルエン混合溶媒中のプロピレンカーボネート含有率(体積%)、混合溶媒の誘電率、吸光度、発色率(%)を示す。図4に、混合溶媒中のプロピレンカーボネート含有率と発色率との関係を示す。これらの結果からわかるように、プロピレンカーボネート含有率6体積%、誘電率6.14の混合溶媒を用いたインクで極大発色率が得られた。
【表2】

【図面の簡単な説明】
【0030】
【図1】極大発色率を与える混合溶媒の誘電率(正味の誘電率)と、極大発色率との関係を示す図。
【図2】インクに添加することができる成分を説明する図。
【図3】実施例1における混合溶媒中のアセトニトリル含有率と発色率との関係を示す図。
【図4】実施例2における混合溶媒中のプロピレンカーボネート含有率と発色率との関係を示す図。
【技術分野】
【0001】
本発明はロイコ色素を用いた印刷インキやボールペンなどに使用される画像形成材料に関し、さらに詳しくは、消去可能な画像形成材料やリライタブル画像形成材料の発色成分として用いられる画像形成材料に関する。
【背景技術】
【0002】
地球環境の保護およびCO2による温室効果を抑制するためには森林の保護は絶対条件であり、新たな伐採を最低限に維持し、植林を含めた森林再生とのバランスを保つためには現在すでに保有している紙資源を如何に効率よく利用していくかが大きな課題となっている。現在の紙資源の再利用は、画像形成材料を剥離させる脱墨工程を経た紙繊維を質の悪い紙に漉き直して目的別に使い分ける「リサイクル」であり、脱墨工程のコスト高の問題や廃液の処理による新たな環境汚染の可能性などが指摘されている。
【0003】
その一方で、これまでに古くは鉛筆とケシゴム、筆記用具に修正液にあるように、画像の修正によるハードコピーの再利用に関しては実用化がなされてきた。また、最近ではハードコピー用紙のリユースを目的とした特殊紙リライタブルペーパーなどが提案されてきた。ここで紙質の劣化を極力防ぎ同一の目的に複数回使用する「リユース」は、紙質を落としながら他の目的に使用する「リサイクル」とは異なる概念であり、紙資源の保護の観点からみればより重要な概念であるといえる。それぞれの「リサイクル」の前段階で有効な「リユース」が行われれば新たに必要な紙資源を最小限に抑えることができる。
【0004】
本発明者らはすでに、呈色性化合物と顕色剤との相互作用が増大すると発色状態となり、相互作用が減少すると消色状態になることに着目して、呈色性化合物および顕色剤を含有する組成系に新たに顕色剤を捕獲する消色剤を加えることにより、室温付近の温度で発色状態が安定に存在し、かつ、熱や溶媒による処理で、実用温度において長期に消色状態を固定できる画像形成材料(たとえば特許文献1、2参照)を提案している。これらの画像形成材料は、画像の発色・消色状態の安定性が高く、加えて材料も安全性が高く、インクなどとして用いることができ、しかも大規模消色処理が可能であるという従来の技術にないメリットを有している。このため、これらの画像形成材料を用いれば、現行のリサイクル技術に代わる有効な紙のリユース技術を実現でき、紙ゴミを著しく減少できることから、省資源に大きな効果がある。
【0005】
さらに、本発明者らは、これらの消去可能な画像形成材料の特性向上を検討する過程で紙の構成要素であるセルロースが消色剤の機能を有することを見出し、被記録媒体に紙を用いる用途では消去剤を含有しない画像形成材料でも熱や溶媒による処理で消去できることを立証している。
【0006】
しかし、これらの画像形成材料には、熱消色における発色と消色のコントラストに限界があるという課題があった。これらの画像形成材料では、発色・消色は呈色性化合物と顕色剤との相互作用の平衡によって定まる。そのため、発色と消色のコントラストは、主に呈色性化合物と顕色剤の組み合わせによって決定され、あまり改善の余地がないと考えられていた。
【特許文献1】特開平10−88046号公報
【特許文献2】特開2000−154345号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明の目的は、鮮明な画像を形成することができる、ロイコ色素を用いた画像形成材料を提供することにある。
【課題を解決するための手段】
【0008】
本発明の実施形態に係る画像形成材料は、呈色性化合物および顕色剤を、誘電率が5以上7以下である溶媒に溶解させたことを特徴とする。
【発明の効果】
【0009】
本発明の実施形態に係る画像形成材料は、画像濃度を大幅に改善できる。
【発明を実施するための最良の形態】
【0010】
以下、本発明の実施形態を説明する。
本発明の実施形態に係る画像形成材料では、呈色性化合物であるロイコ色素(L)と顕色剤(D)との間には下記のスキーム1に示す化学平衡が存在し、この平衡がロイコ色素の発色性を支配すると考えられている。
【0011】
スキーム1
L + D ← → [L−D]
そこで、まず溶液中、室温付近におけるスキーム1の平衡に関する詳細な研究を行った。その結果、溶液中、室温付近では、平衡はほとんど解離の方向、すなわち消色側に偏っていることが明らかになった。つまり、ほとんどの色素が発色に寄与していないことが判明した。したがって、スキーム1の平衡を会合の方向、すなわち発色側に偏らせる有効な手段を見出すことができれば、本発明の実施形態に係る画像形成材料の発色濃度を大幅に改善できるという指針も得られた。そこで、どのような条件下において発色性が向上するのか、平衡の状態を理解し易い溶液中での挙動を観測することにより検討した。
【0012】
ロイコ色素の発色は、ラクトン環が開環し分子内の共役が拡大することによると考えられている。スキーム2に、ロイコ色素Aと顕色剤(没食子酸エチル、EG)とが相互作用して発色種Bを生成する化学反応の平衡を示す。スキーム2では発色性中間体Mを想定している。
【化1】

【0013】
スキーム2に示したように、発色種Bおよび発色性中間体Mでは、分子内で電荷が局在化している。そこで、これら荷電性発色種を安定化することによる平衡制御を試みた。ここでは、極性の低いトルエンをベースとし、ここに種々の極性溶媒を様々な割合で添加し、随時発色の様子を観測した。つまり、極性溶媒とその割合を様々に変え、得られた溶液の紫外可視吸収スペクトルをそのつど測定した。その結果、用いる極性溶媒により、発色の様子が異なることが明らかになった。具体的には、極性溶媒の誘電率が高いほど、より大きい極大発色率が得られるという傾向がみられた。図1に、極大発色率を与える混合溶媒の誘電率(正味の誘電率)と、極大発色率との関係を示す。
【0014】
混合溶媒の誘電率は下記の式(1)を用いて算出した。誘電率は分極可能な部分の密度に依存し、混合により体積が変化しなければ加成性が成り立つので式(1)による算出が妥当である。
正味の誘電率=DpXp+DtXt (1)
(Dp,Dt:極性溶媒,トルエンの誘電率、Xp,Xt:極性溶媒,トルエンの体積分率)。
【0015】
図1から、非常に狭い誘電率範囲において高い極大発色率が得られることがわかった。つまり、誘電率が5以上7以下の溶媒中で特に高い発色率が得られた。一方、誘電率が5未満であるかまたは7を超えると、高い発色率は得られない。すなわち、本発明の実施形態に係る画像形成材料は、ロイコ色素および顕色剤を、誘電率が5以上7以下である溶媒に溶解させたものであり、高い発色率が得られる。
【0016】
また、前記溶媒は、誘電率が2.4以下の溶媒と誘電率が35以上の溶媒との混合溶媒であることが好ましい。誘電率が2.4以下の溶媒としては、たとえばトルエンが挙げられる。誘電率が35以上の溶媒としては、たとえばアセトニトリルやプロピレンカーボネートが挙げられる。
【0017】
以下、本発明の実施形態に係る画像形成材料に用いられる材料について、より詳細に説明する。
【0018】
呈色性化合物としては、ロイコオーラミン類、ジアリールフタリド類、ポリアリールカルビノール類、アシルオーラミン類、アリールオーラミン類、ローダミンBラクタム類、インドリン類、スピロピラン類、フルオラン類などの電子供与性有機物が挙げられる。具体的には、クリスタルバイオレットラクトン(CVL)、マラカイトグリーンラクトン、2−アニリノ−6−(N−シクロヘキシル−N−メチルアミノ)−3−メチルフルオラン、2−アニリノ−3−メチル−6−(N−メチル−N−プロピルアミノ)フルオラン、3−[4−(4−フェニルアミノフェニル)アミノフェニル]アミノ−6−メチル−7−クロロフルオラン、2−アニリノ−6−(N−メチル−N−イソブチルアミノ)−3−メチルフルオラン、2−アニリノ−6−(ジブチルアミノ)−3−メチルフルオラン、3−クロロ−6−(シクロヘキシルアミノ)フルオラン、2−クロロ−6−(ジエチルアミノ)フルオラン、7−(N,N−ジベンジルアミノ)−3−(N,N−ジエチルアミノ)フルオラン、3,6−ビス(ジエチルアミノ)フルオラン−γ−(4’−ニトロ)アニリノラクタム、3−ジエチルアミノベンゾ[a]−フルオラン、3−ジエチルアミノ−6−メチル−7−アミノフルオラン、3−ジエチルアミノ−7−キシリジノフルオラン、3−(4−ジエチルアミノ−2−エトキシフェニル)−3−(1−エチル−2−メチルインドール−3−イル)−4−アザフタリド、3−(4−ジエチルアミノフェニル)−3−(1−エチル−2−メチルインドール−3−イル)フタリド、3−ジエチルアミノ−7−クロロアニリノフルオラン、3−ジエチルアミノ−7,8−ベンゾフルオラン、3,3−ビス(1−n−ブチル−2−メチルインドール−3−イル)フタリド、3,6−ジメチルエトキシフルオラン、3−ジエチルアミノ−6−メソキシ−7−アミノフルオラン、DEPM、ATP,ETAC、2−(2−クロロアニリノ)−6−ジブチルアミノフルオラン、クリスタルバイオレットカルビノール、マラカイトグリーンカルビノール、N−(2、3−ジクロロフェニル)ロイコオーラミン、N−ベンゾイルオーラミン、ローダミンBラクタム、N−アセチルオーラミン、N−フェニルオーラミン、2−(フェニルイミノエタンジリデン)−3,3−ジメチルインドリン、N−3,3−トリメチルインドリノベンゾスピロピラン、8’−メトキシ−N−3,3−トリメチルインドリノベンゾスピロピラン、3−ジエチルアミノ−6−メチル−7−クロロフルオラン、3−ジエチルアミノ−7−メトキシフルオラン、3−ジエチルアミノ−6−ベンジルオキシフルオラン、1,2−ベンゾ−6−ジエチルアミノフルオラン、3,6−ジ−p−トルイジノ−4,5−ジメチルフルオラン−フェニルヒドラジド−γ−ラクタム、3−アミノ−5−メチルフルオランなどが例示される。これらは単独で用いてもよいし2種以上混合して用いてもよい。呈色性化合物を適宜選択すれば多様な色の発色状態が得られることからカラー対応も容易である。これらの中で、特に適している材料は、トリフェニルメタン系、フルオラン系、フェニル−インドール−フタリド系の呈色性化合物である。
【0019】
顕色剤としては、フェノール類、フェノール金属塩類、カルボン酸金属塩類、ベンゾフェノン類、スルホン酸、スルホン酸塩、リン酸類、リン酸金属塩類、酸性リン酸エステル、酸性リン酸エステル金属塩類、亜リン酸類、亜リン酸金属塩類などが挙げられる。これらは単独で用いてもよいし、2種以上混合して用いてもよい。これらのうちでも特に好適な顕色剤は、没食子酸または没食子酸エステル、たとえば没食子酸メチル、没食子酸エチル、没食子酸n−プロピル、没食子酸i−ブチルなど;ジヒドロキシ安息香酸またはそのエステル、たとえば2,3−ジヒドロキシ安息香酸、3,5−ジヒドロキシ安息香酸メチルなど;ヒドロキシアセトフェノン類、たとえば2,4−ジヒドロキシアセトフェノン、2,5−ジヒドロキシアセトフェノン、2,6−ジヒドロキシアセトフェノン、3,5−ジヒドロキシアセトフェノン、2,3,4−トリヒドロキシアセトフェノンなど;ヒドロキシベンゾフェノン類、たとえば2,4−ジヒドロキシベンゾフェノン、4,4’−ジヒドロキシベンゾフェノン、2,3,4−トリヒドロキシベンゾフェノン、2,4,4’−トリヒドロキシベンゾフェノン、2,2’,4,4’−テトラヒドロキシベンゾフェノン、2,3,4,4’−テトラヒドロキシベンゾフェノンなど;ビフェノール類、たとえば2,4’−ビフェノール、4,4’−ビフェノールなど;多価フェノール類、たとえば4−[(4−ヒドロキシフェニル)メチル]−1,2,3−ベンゼントリオール、4−[(3,5−ジメチル−4−ヒドロキシフェニル)メチル]−1,2,3−ベンゼントリオール、4,6−ビス[(3,5−ジメチル−4−ヒドロキシフェニル)メチル]−1,2,3−ベンゼントリオール、4,4’−[1,4−フェニレンビス(1−メチルエチリデン)ビス(ベンゼン−1,2,3−トリオール)]、4,4’−[1,4−フェニレンビス(1−メチルエチリデン)ビス(1,2−ベンゼンジオール)]、4,4’,4’’−エチリデントリスフェノール、4,4’−(1−メチルエチリデン)ビスフェノール、メチレントリス−p−クレゾールなどである。これらの顕色剤のうちで特に好適なものは、没食子酸エステル、たとえば没食子酸エチル、没食子酸n−プロピル、没食子酸i−プロピル、没食子酸ブチルなど;ヒドロキシベンゾフェノン類、たとえば2,4−ジヒドロキシベンゾフェノン、4,4’−ジヒドロキシベンゾフェノン、2,3,4−トリヒドロキシベンゾフェノン、2,4,4’−トリヒドロキシベンゾフェノン、2,2’,4,4’−テトラヒドロキシベンゾフェノン、2,3,4,4’−テトラヒドロキシベンゾフェノンなどである。
【0020】
本発明の実施形態に係る画像形成材料はインクに分類できる。インクの用途では、上で説明した呈色性化合物および顕色剤に加えて、図2に示す成分を添加することができる。
【0021】
本発明の実施形態に係る画像形成材料は、加熱するか、または消去溶媒(消去剤を含む場合もあるし含まない場合もある)と接触させることにより消去することができる。
【0022】
なお、本発明において示した誘電率の好適な範囲は、溶媒だけでなくあらゆる材質に適用される。したがって、誘電率が5以上7以下であれば、呈色性化合物および顕色剤をバインダー樹脂などの固体マトリクスに分散させた画像形成材料でも、同様に高い発色性が期待できる。
【実施例】
【0023】
以下、本発明の実施例を説明する。
実施例1
磁気攪拌子を付したスクリューバイアル(20mL)に、呈色性化合物であるロイコ色素Lとして山田化学製のblue203(3−(4−アミノ−2−ヘキシルオキシフェニル)−3−(1−エチル−2−メチルインドール−3−イル)−4−アザフタリド)を0.027g(5.00×10-5mol)、顕色剤Dとして没食子酸エチル(EG)を0.010g(5.04×10-5mol)、およびアセトニトリルを8、10、14または20体積%含むアセトニトリル(誘電率:37.5)/トルエン(誘電率:2.38)混合溶媒を5mL入れ、よく攪拌し均一溶液とした。
【0024】
また、アセトニトリルを6体積%含有するアセトニトリル/トルエン混合溶媒を用いた場合には、溶解度の関係からblue203 0.019g(3.52×10-5mol)およびEG 0.007g(3.53×10-5mol)を用いて均一溶液を調製した。
【0025】
得られた溶液の吸光度を測定し、モル吸光係数(ε=36000)を用い、それぞれの溶液におけるL−D会合体(発色種、スキーム1参照)の濃度([L−D])を算出した。この[L−D]をblue203の初期濃度([L]0=完全に発色した場合の[L−D])で規格化することにより、各溶液における発色率を求めた。
【0026】
下記表1に、アセトニトリル/トルエン混合溶媒中のアセトニトリル含有率(体積%)、混合溶媒の誘電率、吸光度、発色率(%)を示す。図3に、混合溶媒中のアセトニトリル含有率と発色率との関係を示す。これらの結果からわかるように、アセトニトリル含有率8体積%、誘電率5.19の混合溶媒を用いたインクで極大発色率が得られた。
【表1】

【0027】
[実施例2]
磁気攪拌子を付したスクリューバイアル(20mL)に、呈色性化合物としてblue203 0.025g(4.63×10-5mol)、顕色剤としてEG 0.009g(4.54×10-5mol)、およびプロピレンカーボネートを6、8、14、または20体積%含むプロピレンカーボネート(誘電率:65.1)/トルエン(誘電率:2.38)混合溶媒を5mL入れ、よく攪拌し均一溶液とした。
【0028】
また、プロピレンカーボネートを4体積%含有するプロピレンカーボネート/トルエン混合溶媒を用いた場合には、溶解度の関係からblue203 0.019g(3.52×10-5mol)およびEG 0.007g(3.53×10-5mol)を用いて均一溶液を調製した。
【0029】
下記表2に、プロピレンカーボネート/トルエン混合溶媒中のプロピレンカーボネート含有率(体積%)、混合溶媒の誘電率、吸光度、発色率(%)を示す。図4に、混合溶媒中のプロピレンカーボネート含有率と発色率との関係を示す。これらの結果からわかるように、プロピレンカーボネート含有率6体積%、誘電率6.14の混合溶媒を用いたインクで極大発色率が得られた。
【表2】

【図面の簡単な説明】
【0030】
【図1】極大発色率を与える混合溶媒の誘電率(正味の誘電率)と、極大発色率との関係を示す図。
【図2】インクに添加することができる成分を説明する図。
【図3】実施例1における混合溶媒中のアセトニトリル含有率と発色率との関係を示す図。
【図4】実施例2における混合溶媒中のプロピレンカーボネート含有率と発色率との関係を示す図。
【特許請求の範囲】
【請求項1】
呈色性化合物および顕色剤を、誘電率が5以上7以下である溶媒に溶解させたことを特徴とする画像形成材料。
【請求項2】
前記溶媒は、誘電率が2.4以下の溶媒と誘電率が35以上の溶媒との混合溶媒であることを特徴とする請求項1記載の画像形成材料。
【請求項1】
呈色性化合物および顕色剤を、誘電率が5以上7以下である溶媒に溶解させたことを特徴とする画像形成材料。
【請求項2】
前記溶媒は、誘電率が2.4以下の溶媒と誘電率が35以上の溶媒との混合溶媒であることを特徴とする請求項1記載の画像形成材料。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2006−282680(P2006−282680A)
【公開日】平成18年10月19日(2006.10.19)
【国際特許分類】
【出願番号】特願2005−100310(P2005−100310)
【出願日】平成17年3月31日(2005.3.31)
【出願人】(000003078)株式会社東芝 (54,554)
【Fターム(参考)】
【公開日】平成18年10月19日(2006.10.19)
【国際特許分類】
【出願日】平成17年3月31日(2005.3.31)
【出願人】(000003078)株式会社東芝 (54,554)
【Fターム(参考)】
[ Back to top ]

