病気の研究、予防及び治療のためのアポトーシス活性調節剤としての、MASG−タンパク質結合受容体アゴニスト及びアンタゴニストの使用
【課題】病気の遺伝子治療において使用するための、および老化により生じる器官の変化の治療のための医薬組成物の提供。
【解決手段】アンギオテンシン−(1−7)又はそのアンタゴニストであるA−779に対応するペプチド配列をコードするcDNAを含んでなる、病気の遺伝子治療において使用するための、および老化により生じる器官の変化の治療のための医薬組成物。
【解決手段】アンギオテンシン−(1−7)又はそのアンタゴニストであるA−779に対応するペプチド配列をコードするcDNAを含んでなる、病気の遺伝子治療において使用するための、および老化により生じる器官の変化の治療のための医薬組成物。
【発明の詳細な説明】
【発明の概要】
【0001】
本発明は、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、病気の研究、予防及び治療のためのアポトーシス活性調節剤としての使用を特徴とする。
【0002】
本発明はさらに、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、B/Aktキナーゼタンパク質の活性の変更を含むアポトーシス活性の調節のための使用を特徴とする。
【図面の簡単な説明】
【0003】
【図1】図1は、視床下部の前部切片中のMas Ang-(1-7)受容体の存在を、その免疫反応性によって、異なる領域の組織学的同定のためにニュートラルレッドで染色した多数の領域(図1A)及び隣接切片中で示す(図1B)。
【図2】図2は、視床下部傍室核(PVN、図2A)及び外側視索前野(LPO、図2C)中のMas Ang(1-7)受容体の存在を、免疫反応性によって示す。対照である隣接切片(図2B及び2D)中では合成Masタンパク質で抗体を予め吸収処理した場合にマーキングが消失することを示した。
【図3】図3は、視索上核(CSO、図3A)中のMas、Ang-(1-7)受容体の存在を、免疫反応によって、矢印にて示す。
【図4】図4は、扁桃(図4A)及び視床の背側前核(図4C)中のMas Ang(1-7)受容体の存在を免疫反応によって示す。隣接切片中の対照(図4B及び4D)は、抗体をMas合成タンパク質で予め吸収処理した場合のマーキングの消失を示す。
【図5】図5は、皮質(HL、図5A)及び海馬(HC、図5C)中のMas Ang-(1-7)受容体の存在を免疫反応によって示す。隣接切片中の対照(図5B及び5D)は、抗体をMas合成タンパク質で予め吸収処理した場合のマーキングの消失を示す。
【図6】図6は、Aにおいて、延髄の前部切片を示し、多数の領域中のMas Ang-(1-7)受容体についての免疫反応性を図示する。B及び隣接切片中では、異なる領域の組織学的同定のためにニュートラルレッドで染色した。
【図7】図7は、延髄の尾側腹外側領域(CVLM、図7A)及び吻側腹外側領域(RVLM、図7C)中のMas Ang-(1-7)受容体についての免疫反応性を示す。隣接領域中の対照(図7B及び7D)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。
【図8】図8は、孤束核(NTS、図8A)及び下オリーブ核(IO、図8C)中のMas Ang-(1-7)受容体の存在を免疫反応性によって示す。隣接領域中のその対照(図8B及び8D)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。
【図9】図9は、舌下神経(12、図9A)中のMas Ang-(1-7)受容体の存在を免疫反応性によって示す。隣接切片中のその対照(図9B)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図9Cは、延髄の吻側腹外側領域中のMas 受容体とAKTの免疫共存を示し、この領域の神経性の調節における受容体MasとAKTの相互作用の可能性を示唆している。
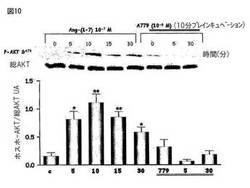
【図10】図10は、CHO-Mas細胞中でのキナーゼB(Akt)のリン酸化においてAng-(1-7)によって生じた刺激を示す。Ang-(1-7)アンタゴニストであるA-779はこの効果をブロックした。
【図11】図11は、CHO-Mas細胞中でAng-(1-7)によって刺激された、内皮のニトリックオキシドシンターゼの刺激部位(S1177)のリン酸化にAktが関与することを示す。ホスファチジルイノシトール3キナーゼアンタゴニスト(PI3K)はこの効果をブロックした。
【図12】図12は、ヒト内皮細胞(HAEC)上のキナーゼB(Akt)のリン酸化におけるAng-(1-7)の刺激効果を示す。Ang-(1-7)アンタゴニストであるA-779は、この効果をブロックした。
【図13】図13は、ヒト内皮細胞(HAEC)中のAng-(1-7)によって刺激されたeNOSの刺激部位(S1177)のリン酸化へのAktの関与を示す。PI3Kアンタゴニストであるワートマニンは、この効果をブロックした。
【図14】図14は、覚醒したウィスターラット(n=7)における、アセチルコリン(ACh)の血管拡張作用の結果を示す。図14Aは、アセチルコリン(ACh)の血管拡張作用が、覚醒したウィスターラット(n=7)において生理食塩水の静脈内輸注(NaCl 0.9%、0.4mL/時間)によって変化しないことを示す。しかしながら、Ang-(1-7)の静脈内輸注(7.0ピコモル/分)は、覚醒したウィスターラット(n=9)においてアセチルコリン(ACh)の血管拡張作用を増強する(図14B)。図14Cは、ワートマニン(10-6M)のボーラス静脈内注射において、Ang-(1-7)(7.0ピコモル/分)に伴うワートマニン(10-6M)の静脈内ボーラス注射の前のPI3K阻害剤が、覚醒したウィスターラット(n=7)におけるアセチルコリン(ACh)の血管拡張作用のAng-(1-7)による増強をブロックすることを示す。
【図15】図15は、ヒト内皮細胞(HAEC)中のAng IIによって刺激されたc-SRCのリン酸化におけるAng-(1-7)の調節効果を示す。
【図16】図16は、Ang II(10-7M、10分)によって刺激されたHAECにおける、NAD(P)Hオキシダーゼの活性に対するAng-(1-7)(10-7M、プレインキュベーション15分)の効果を示す。
【図17】図17は、Mas G-タンパク質−結合受容体アンタゴニストであるA-779で処置された動物が、対照群に対して、横断面当たりのアポトーシスの数が多いが、生殖腺指数においては相違がなかったことを示す。
【図18】図18は、Mas受容体の存在がアポトーシス活性の調節に寄与しているかもしれない多数の組織におけるMas受容体の発現を、RT-PCRによって示す。
【発明を実施するための形態】
【0004】
本発明の他の特徴は、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含む、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、病気の研究、予防及び治療において使用するためのアポトーシス活性調節剤としての使用である。
【0005】
本発明はさらに、薬学的に又は薬理学的に許容可能な担体とともに製剤された、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニスト、そして、アンギオテンシン−(1−7)ペプチド並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含む、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、アポトーシス活性調節剤としての使用も権利請求する。
【0006】
他の権利請求される特徴は、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含む、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの製剤の、マイクロ及びナノ粒子である、埋め込み型又は注射用デバイスの、アポトーシス活性調節剤としての使用である。
【0007】
ここに記載される投与形態は、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニスト、そしてそれらの製剤を含む、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、経口、筋肉内、静脈内、皮下、局所、経皮、肛門内、吸入(肺内、鼻腔内、口腔内)投与経路のいずれかを介する使用、或いは埋め込み型又は注射用のデバイスとしての使用を含むが、これらに限定されない。
【0008】
体液及び血圧のホメオスタシスの調節物質としてのレニン−アンギオテンシン系(RAS)の役割は、かなり知られている。RASは、生理学的及び病理学的状態の両方における、血圧、循環器のホメオスタシス及び水分電解質バランスの調節に関与する(Santos, R.A.S.; Campagnole-Santos, M.J.; Andrade, S.P. Angiotensin-(1-7): an update. Regul Pept. 91:45−62, 2000)。最近、血液循環中のAng IIを生成する系のほかに、異なる組織が、局所的にこの系の様々な生理活性ペプチドを生成しうることが発見された(組織のRAS)。組織のRASの成分は、心臓、管、腎臓、男性及び女性生殖系、内分泌腺、脊髄及び脳を含む様々な器官及び組織中に見出される。異なる組織中のこれらのRASの機能は、完全には明らかにされていない(Santos, RAS, Campagnole-Santos, MJ, Andrade, SP, Angiotensin-(1-7): an update. Regul Pept. 91:45-62, 2000; Yoshimura, Y. The ovarian rennin-angiotensin system in reproductive physiology. Front Neuroendocrinol.; 18: 247-291, 1997)。
【0009】
古典的なRASの主要成分は、以下の:アンギオテンシノーゲンのアンギオテンシンI(Ang I)へのタンパク分解による変換を触媒する酵素である、レニン;レニンの主要な基質でありアンギオテンシンII(Ang II)の前駆体であるアンギオテンシノーゲン;2つのカルボキシ末端アミノ酸を加水分解することによりAng IをAng IIに変換する、アンギオテンシン変換酵素(ACE);この系の主要な生理活性ペプチドであるアンギオテンシンII;及びAng IIの細胞における作用の開始に関与する、AT1及びAT2受容体である。この周知の系に、アンギオテンシンIII(Ang III)、アンギオテンシンIV(Ang IV)及びアンギオテンシン−(1−7)[(Ang-(1-7)]などの他のペプチドが追加された。Ang-(1-7)は、組織のエンドペプチダーゼによってAng I又はAng IIから生成されることができる(Santos, R.A. Brosnihan, K.B. Cappell, M. C., Pesquero, J., Chernicky, C.L., Greene, L. J., ;Ferrario, C.M. Converting enzyme activity and angiotensin metabolism in the dog brainstem. Hypertension (11(2-Pt-2): l153-l1537, 1988)。
【0010】
Ang-(1-7)は、血漿中並びに雌性ラット卵巣(Costa APR, Fagundes-Moura CR, Pereira VM., Silva LF, Vieira MA, Santos RA, Reis AM. Angiotensin-(1-7): a novel peptide in the ovary. Endocrinology. 144:1942-1948, 2003)を含む様々なヒト及び動物の器官及び組織中で確認されている(Santos, R.A.S.; Campagnole-Santos, M.J.; Andrade,S.P. Angiotensin-(1-7): an update. Regul Pept. 91:45-62, 2000)。その独立したACE産生が、Santos et al., 1988(Santos, R.A., Brosnihan, K.B., Cappell, M.C., Pesquero, J., Chernicky, C.L., Greene, L.J.; Ferrario, C.M. Converting enzyme activity and angiotensin metabolism in the dog brainstem. Hypertension, 11(2-Pt 2): l153-l153-l1537, 1988)によって実証され、特異的受容体へのその結合がSantos et al., 1994(Santos, RAS, Campagnole-Santos, M.J., Baracho, N.C., Fontes, M.A., Silva, L.C., Neves, L.A., Oliveira, D.R., Caligiorne, S.M., Rodrigues, A.R., Gropen Junior, C. Characterization of a new angiotensin antagonist selective for angiotensin-(1-7): evidence that the actions of angiotensin-(1-7) are mediated by specific angiotensin receptors. Brain Res Bull. 35(4):293-298, 1994)及びTallant et al., 1997, (Tallant, E.A., Lu, X., Weiss, R.B., Cappell, M. C.; Ferrario, C.M. Bovine aortic endothelial cells contain an angiotensin-(1-7) receptor. Hypertension 29:388-393, 1997)によって示唆された。これらの発見は、特に、Ang-(1-7)のための選択的アンタゴニストであるA-779(Asp1-Arg2-Val3-Tir4-Lle5-His6-D-Ala7;Santos, R.A., Campagnole-Santos, M.J. Barracho, N.C., Fontes, M.A. Silva, L.C., Neves, L.A. Oliveira, D.R., Caligione, S.M., Rodrigues, A.R., Groppen Junior, C. Characterization of a new angiotensin antagonist selective for angiotensin-(1-7) : evidence that the actions of angiotensin-(1-7) are mediated by specific angiotensin receptors. Brain Res Bull. 35(4):293-298, 1994; Ambuhl, P, Felix, D. Khosla, M.C. [7-D-ALA]-Angiotensin-(1-7): selective antagonism of angiotensin-(1-7) in the rat paraventricular nucleus. Brain Res Bull. 1994; 35(4):289-91)の利用可能性によって得られた。
【0011】
様々な酵素がRASカスケードのいくつかのステップに関与し、ここでそれらはいくつかのペプチド断片の分解並びに他のものの生成に関与する。ACEは、Ang IのAng IIへの変換に関与し;PEP(プロリルエンドペプチダーゼ)がAng I及びAng IIからAng(1-7)を生成し、そしてNEP(ニュートラルエンドペプチダーゼ)がAng IのAng-(1-7)への変換を触媒する。ACEはまた、Ang-(1-7)を加水分解し、Ang-(1-5)を生成する(Chappell MC, Pirro NT, Sykes, A, Ferrario CM. Metabolism of angiotensin-(1-7) by angiotensin-converting enzyme. Hypertension. 31:362-367, 1998)。したがって、ACE経路は、循環中及び組織のRASの生理活性ペプチドの生成及び分解の両方にとって重要である。より最近には、他の酵素、ACE2が記載され、これはAng-(1-7)の形成にとって重要である(SR Tipnis, NM Hooper, R Hyde, E Karran and G Christie. The human homolog of angiotensin-converting enzyme. Cloning and functional expression as a captopril-insensitive carboxypeptidase. J. Biol Chem. 275(43):33238-33243, 200)。この酵素は、Ang-(1-7)を、特にAng IIから生成する。
【0012】
アンギオテンシン−(1−7)及びアンギオテンシンIIは、主要なRASエフェクターである。2つの重要な特徴がAng-(1-7)をAng IIから識別する:最初のAng(1-7)は非常に特異的な生理活性を有し、Ang-(1-7)の生成経路によって、ACEから完全に独立しうる(Santos, R.A.S.; Campagnole-Santos, M. J.; Andrade, S.P. Angiotensin-(1-7): an update. Regulatory Peptides. 91: 45−62, 2000)。
【0013】
Mas調節物質は最初、インビボでのその弱い腫瘍形成活性によってプロトオンコジーンとして記載された(Young D. Waitches G, Birchmeier C. Fasano O. Wigler M. Isolation and characterization of a new cellular oncogene encoding a protein with multiple potential transmembrane domains. Cell. 1986; 45:711-71)。
【0014】
哺乳動物においては、その遺伝子の発現は圧倒的に精巣及び海馬を含む脳の様々な区域及び扁桃で検出され、より弱いが、顕著なレベルで腎臓及び心臓で検出された(Bunnemann B, Fuxe K, Metzger R, Mullins J, Jackson TR, Hanley MR, Ganten D. Autoradiographic localization of Mas proto-oncogene mRNA in adult rat brain using in situ hybridization. Neurosci Lett 114:147-153, 1990; Alenina N, Bader M, Walther T. Imprinting of the murine MAS proto-oncogene is restricted to its antisense RNA. Biochem Biophys Res Commun. 290:1072-1078, 2002)。
【0015】
その遺伝子は、G-タンパク質結合受容体のクラスIの特徴を有する、7つの膜貫通ドメインを有するタンパク質を調節する。初期の研究においては、この遺伝子は、オクタペプチドであるアンギオテンシンIIの受容体の調節因子として示唆された(Jackson TR, Blair LA, Marshall J, Goedert M, Hanley MR. The Mas oncogene encodes an angiotensin receptor. Nature 335:437-440, 1988)。しかしながら、Ambrozと共同研究者そして後のArdaillouは、Masによりトランスフェクトされた細胞におけるAng IIによる細胞内カルシウムの上昇が、Ang IIのAT1受容体を内因的に発現する細胞のみにおいておこることを示した(Ambroz C, Clark A, Catt KJ. The Mas oncogene enhances angiotensin-induced [Ca2+]i responses in cells with pre-existing angiotensin II receptors. Biochem Biophys Acta. 1133: 107-111, 1991; Ardaillou R. Angiotensin II receptors. J Am Soc Nephrol. 10:S30-S39, 1999)。より最近には、実際に、MasがAng-(1-7)の受容体であることが観察された(Santos, R.A., Simoes e Silva A C, Maric, C., Silva, D.M., Machado, R.P., de Buhr, I., Heringer-Walther, S., Pinheiro, S.V., Lopes, M.T., Bader, M., Mendes, E.P., Lemos, V.S., Campagnole-Santos, M.J., Schultheiss, H.P., Speth, R.; Walther, T. Angiotensin-(1-7) is an endogenous ligand for the G protein-coupled receptor Mas Proc Natl. Acad Sci USA, 100(14):8258-8263, 2003)。
【0016】
内皮の機能不全は、標的器官(中でも、心臓、腎臓、脳、血管、生殖器官)の病巣に関連する様々な病理の設置及び進行においてより早期に発生する事象である(Goligorsky MS. Endothelial cell dysfunction: can't live with it, how to live without it. Am J. Physiol Renal Physilo. 288(5):F871-80, 2005)。窒素酸化物のバイオアベイラビリティーの減少は、内皮の機能不全の開始のための決定的因子であり、それは、この分子が血管拡張性、抗増殖性、抗凝固性、アテローム産生抑制性の性質を有し、かつ活性酸素種の産生を中和するからである(Ogita H, Liao J. Endothelial function and oxidative stress. Endothelium. 11(2):123-32, 2004)。最近、カルシウムに依存する古典的経路のほかに、窒素酸化物が、内皮のニトリックオキシドシンターゼ(eNOS)の1177セリンなどの部位のB/Aktキナーゼタンパク質を介する直接的リン酸化によって形成されることができることが実証された。このメカニズムは、内皮の完全性の維持に大いに貢献する。eNOSのリン酸化によるAktの活性化は、ヒト内皮中でAnt-(1-7)によって刺激される窒素酸化物の放出に関与し、結局、本発明の特徴である、内皮の機能性の改善に関与する。本発明の他の特徴は、Ang-(1-7)が、c-SRCなどの活性酸素種の産生に関与する近位の細胞内経路を阻害することによって、ヒト内皮中のAng IIの作用の負の調節を行うことを実証することである。さらに、Ang-(1-7)は、血管壁中の最大の活性酸素種産生源であるNAD(P)Hオキシダーゼの活性を阻害する(Touyz RM. Reactive oxygen species and angiotensin II signaling in vascular cells-implications in cardiovascular disease. Braz J Med Bio Res. 37(8): 1263-73, 2004)。Ang IIによるNAD(P)Hの活性化は、該酵素のサブユニットp47phoxのリン酸化及び膜への移動のためにc-SRCを必要とする。さらに、Ang IIによる慢性の刺激においては、c-SRCは、NAD(P)Hオキシダーゼのサブユニットgp91phox、p22phox、及びp47phoxのタンパク質発現の増加に関与する(Touyz RM, Yao G, Schiffrin EL. c-Src induces phosphorylation and translocation of p47pho role in super oxide generation by angiotensin II in human vascular smooth muscles cells. Arterioscler Thromb Vasc Biol 23(6):981-7, 2003)。酸化促進因子及び抗酸化因子間のアンバランスが内皮の機能不全開始の決定因子の1つであるため、この事実は特に重要である。したがって、窒素酸化物の放出によって内皮の完全性を維持することに直接寄与するほかに、Ang-(1-7)は酸化フリーラジカルの生成も中和する。そして、活性酸素種の産生はアポトーシス活性と密接に関連し、なぜなら、それはMAPK、カスパーゼなどの細胞死の決定因子を含むシグナルカスケードを刺激するからである(Matuzawa, A. Ichijo, H. Stress-responsive protein kinases in redox-regulated apoptosis signaling. Antioxid Redos Signal 7(3-4):472-81;2005)。しかしながら、循環器、腎臓の病気、多重メタボリック症候群(plurimetabolic syndrome)、勃起不全、中枢神経系の病気などの、しかしこれらに限らない内皮の機能不全を含む病理の予防及び治療のために、Mas受容体を介してPI3K/Akt/eNOSカスケードを活性化し、並びにNAD(P)Hオキシダーゼを不活性化し、そして活性酸素種の産生及び内皮のアポトーシスに関与するメカニズムを低下させる、Ang-(1-7)又はそのペプチド若しくは非ペプチド類似体の製剤を使用することに関する発明は従来技術においてなかった。
【0017】
Ant-(1-7)は、探索行動を増加させ、かつ記憶を促進する(Santos, RA, Campagnole-Santos, MJ. Central and Peripheral actions of Angiotensin-(1-7). Braz J Med Bio Res. 27(4):1033-47, 1994; Hellner, K., Walther, T., Schubert, M., Albrecht, D. Angiotensin-(1-7) enhances LTP in the hippocampus through the G-protein-coupled receptor Mas. Mol Cell Neurosci 29(3):427-35, 2005)。Mas受容体は、海馬、扁桃体及び脳皮質を含む、これらの機能に関与する脳の領域に位置する(K. A Martin, S. G. Grant, S. Hockfield. The Mas proto-oncogene is developmentally regulated in the rat central nervous system. Brain Res Dev Brain Res 68(1): 75-82, 1992)。Mas受容体とAng-(1-7)との相互作用は、抗アポトーシス特性を有するシグナリング経路、より特別にはPKI3/Aktの経路を活性化する。Ang-(1-7)により増加する、B(Akt)キナーゼタンパク質によるリン酸化は、細胞のアポトーシスを減少させる(Z.-Z. Yang, O. Tschopp, A. Baudry, B. Dummler, D. Hynx and B. A Hemmings. Physiological functions of protein kinase B Akt Biochem Soc Trans. 32:350-354, 2004)。Aktの脳の亜型であるAktγについてのノックアウトマウスは、脳重量の劇的な減少を示す(Z.-Z. Yang, O. Tschopp, A. Baudry, B. Dummler, D. Hynx and B. A Hemmings. Physiological functions of protein kinase B Akt Biochem Soc Trans. 32:350-354, 2004)。脳内のAktの発現部位のいくつかは、Mas 受容体のためのRNAMにも富む領域である、海馬及び脳皮質である。しかしながら、従来技術においては、Ang-(1-7)とMas受容体との相互作用によって誘導される、Aktにより仲介される抗アポトーシス活性の刺激に基づく、変性脳疾患、或いは記憶又は学習障害の制御又は予防のためのアンギオテンシン−(1−7)の製剤に関する発明はない。同様に、Mas受容体のペプチド又は非ペプチドアゴニストと該受容体との相互作用により誘導される、Aktにより仲介される抗アポトーシス活性の刺激に基づく、変性脳疾患、或いは記憶又は学習障害の研究、予防又は治療のためのMas 受容体アゴニスト又はアンタゴニストの製剤の使用に関する発明はない。
【0018】
本発明は、Mas Gタンパク質結合受容体との相互作用へのアクセスを促進する、Ang-(1-7)、Ang-(1-7)の類似体又は誘導体を含む放出制御系の使用に特徴を有する。Gタンパク質、Mas 及びAng-(1-7)、類似体又は誘導体間の相互作用は、中でもアルツハイマー、パーキンソン、ハンチントン病などの変性脳疾患を含む、アポトーシス活性の増加に特徴を有する変性脳疾患の制御又は予防を可能とする。満足のいく放出制御系は、シクロデキストリン、生物適合性ポリマー、生物分解性ポリマー、他のポリマーマトリックス、カプセル、マイクロカプセル、微小粒子、ボーラス製剤、浸透圧ポンプ、分散デバイス、リポソーム、リポスフィア、及び経皮投与システムを含むが、これらに限定されない。
【0019】
最近、様々な文献が、IP3k/AKT経路がインスリン受容体とその基質とのシグナル伝達を仲介する決定的な役割を演じることを示した(Zdychova J, Komers R. Emerging role of Akt kinase/protein kinase B signaling in pathophysiology of diabetes and its complications. Physiol Res; 54(1):1-16, 2005)。成長因子、アンギオテンシンII、活性酸素種、コルチコステロイド、エストロゲンなどの、このカスケードを変化させるメディエーター及びその血糖状態の変化は、PI3K/Akt経路が本質的に抗アポトーシス経路であるため、糖尿病に固有の内皮の機能不全から糖尿病の妊娠女性における胎児の催奇形性変化にまで導くであろう(Reece EA, Ma XD, Zhao Z, Wu YK, Dhanasekaran D. Aberrant patterns of cellular communication in diabetes-induced embryopathy in rats: II, apoptotic pathways Am J. Obstet Gynecol. 192(3):967-972, 2005)。Aktは、この経路によって仲介されるシグナル伝達を方向付ける様々な因子によって制御されることができる。例えば、D-グルコースは、Aktのリン酸化を制御し、高血糖は、糖尿病における内皮の機能不全に関連付けられてきた(現在印刷中のVarma S, Lal BK, Zhen R, Breslin JW, Saito S, Pappas PJ, Hobson li RW, DuranWN. Hyperglycemia Alters PI3K and Akt Signaling and Leads to Endothelial Cell Proliferative Dysfunction. Am J Physiol Heart Circ Physiol. 2005)。さらに、セリンのリン酸化は、e-NOSの活性化に関連し(Kobayashi T, Taguchi K, Yasuhiro T, Matsumoto T, Kamata K, Impairment of PI3K/Akt pathway underlies attenuated endothelial function in aorta of type 2 diabetic mouse model. Hypertension. 44(6):956-962, 2004)、そして脂肪レベルの増加によって阻害されることができ、これは、内皮の保存及び循環する内皮前駆細胞(EPC)の活性化のほかに、Aktがアテローム保護作用に関係するかもしれないことを示唆している。骨格筋においては、Aktのリン酸化における変化が2型糖尿病におけるGLUt4を介する輸送の調節に関連する(Karlsson HK, Zierath JR, Kane S, Krook A, Lienhard GE, Wallberg-Henriksson H. Insulin-Stimulated Phosphorylation of the Akt Substrate AS160 Is Impaired in Skeletal Muscle of Type 2 Diabetic Subjects. Diabetes. 54(6):1692-7, 2005)。他の興味深い側面は、このカスケードがβ細胞自体の増殖及び生存に関与するようであること、及びセラミドにより活性化されるホスファターゼ(CAPP)によるその不活性化がI型糖尿病におけるインスリン分泌の変化を引き起こすかもしれないということである(Kowluru A. Novel regulatory roles for protein phosphatase-2A in the islet beta cell. Biochem Pharmacol. 69(12): 1681-1691, 2005)。PI3K/Akt/TOR経路によって仲介されるネガティブフィードバックプロセスの存在は、インスリン耐性及び腫瘍新生のための決定的事象であると指摘された(Manning BD, Balancing Akt with S6K: implications for both metabolic diseases and tumorigenesis, J. Cell Biol, 167(3): 399-403, 2004)。したがって、糖尿病の原因因子及びそれにより生じる脈管障害などの合併症の両方へのAktの関与は明らかである。
【0020】
レニン−アンギオテンシン系とインスリン受容体シグナル伝達との間には密接な関係があるようである。Ang IIが、インスリン受容体を介するAktのリン酸化を阻害することは実証済みである。さらに、Ang IIにより刺激される酸化的ストレスも、インスリンにより活性化される細胞内カスケードの様々な段階を変化させる(Taniyama, Y, Hitomi H, Shah A, Alexander RW, Griendling KK. Mechanisms of reactive oxygen species-dependent downregulation of insulin receptor substrate 1 by angiotensin II. Arterioscler Thromb Vasc. Biol. 25(6): 1142-1147, 2005)。これは、部分的に、なぜAng II阻害剤の使用が、インスリン耐性を改善し、結果として微小血管の病変のような糖尿病に関連する合併症を改善するかを説明する。Ang-(1-7)は、強力な生物学的Ang IIアンタゴニストであり、かつ内皮機能の改善に関連する様々な作用を有する。そのレベルは、系の薬理学的遮断の間に上昇し、Ang-(1-7)がACE阻害剤及びAT1受容体アンタゴニストの両方の有益な効果の重要なメディエーターであることを示している。上記で既に述べたとおり、Ang-(1-7)のMas受容体への結合がAktの強いリン酸化に導く。しかしながら、従来技術においては、インスリン耐性又はこのホルモンの産生の欠乏の結果の研究、予防又は治療のための、アンギオテンシン−(1−7)又はそのペプチド若しくは非ペプチド類似体の製剤の使用に関する発明はない。
【0021】
アンギオテンシン−(1−7)は、心臓に存在し、そして収縮性の増加及び不整脈の減少などの心臓への重要な効果を有する(Ferreira, AJ and Santos, RAS. Cardiovascular actions of Angiotensin-(1-7). Braz. J. Med. Biol Res. 38(4):499-507, 2005)。Mas受容体も、心臓内で発現され、そしてその欠乏は心臓機能の重大な低下を引き起こす(Ferreira,AJ Santos, RAS. Cardiovascular actions of Angiotensin-(1-7), Braz. J. Med. Biol Res. 38(4):499-507, 2005)。キナーゼAktタンパク質も、心臓、特に心筋細胞中で発現される。これらの細胞中では、AktはPIK3を介してリン酸化もされ、心筋の収縮性を増加させ、そして再灌流不整脈を減少させる。心臓中でのAkt発現が増加したマウスは、「インスリン様成長因子結合タンパク質−5」の増加のような、解糖系に関与するタンパク質の合成の変化を示し、これは、この経路をの活性を高める結果となる(Latronico, MGV, Costinean, S., Lavitrano, M.L. Peschle, C., Condorelli, G. Regulation of Cell Size and Contractile Function by AKT in Cardiomyocytes, Ann. N.Y. Acad. Sci. 1015: 250-260, 2004; Cook, S.A. Matsui, T., Li, L., Rosenzweig, A. Transcriptional Effects of Chronic Akt Activation in the Heart. J Biol Chem: 277(25): 22528-22533, 2002)。Ang-(1-7)の投与は、心筋梗塞に対して心臓を保護することとなる(Loot A. E. Roks A. J., HENNING, R.H., Tio, R.A., Suurmeijer, A. J., Boomsma, F, van Gilst, W.H., Angiotensin-(1-7) attenuates the develpment of heart failure after myocardial infarction in rats. Circulation. 2002:105 (13):1548-50)。Ang-(1-7)を生成する融合タンパク質を発現するトランスジェニックラットは、イソプロテレノールによる治療に応答して心臓肥大が低下し、そして再灌流不整脈の発生及び持続時間がより短い(Santos, R. A., Ferreira, A. J., Nadu, A. P., Braga, A. N., de A.meida, A.P., Campagnole-Santos, M.J., Baltatu. O., Iliescu, R., Reudelhuber, T. L., Bader, M. Expression of an angiotensin-(1-7)-producing fusion protein produces cardioprotective effects in rats. Physiol Genomics. 2004; 19(7):292-9)。一方、アデノウイルスを介するAkt遺伝子の心内投与は、ラットにおける梗塞域のサイズの減少を生じた(W. Miao, Z. Luo, R. N. Kitsis and K. Walsh, Intracoronary, Adenovirus-mediated Akt Gene Transfer in Heart Limits Infarct Size Following Ischemia-reperfusion Injury in vivo. J. Mol Cell Cardiol. 32:2397-2402, 2000)。Aktで改変された幹細胞は、ラットにおいてリモデリングを予防し、そして梗塞心臓の機能を回復する(Mangi, A. A, Noiseux, N., Kong, D., He, H., Rezvani, M., Ingwall, J. S., Dzau, V. J. Mesenchymal stem cells modified with Akt prevent remodeling and restore performance of infacted hearts Nat Med. 9:1195-1201, 2003)。しかしながら、従来技術においては、PIK3/Akt経路の刺激によって生じる抗アポトーシス活性のような細胞内情報伝達経路の刺激に基づいて、Ang-(1-7)とMas受容体との相互作用によって、心内投与後に心臓機能を増加させるか、或いは心筋変性疾患を制御又は予防するか、幹細胞のバイアビリティーを増加させるか、或いは心臓のリモデリングまたは心臓の電気生理学的障害を減少させるための、アンギオテンシン−(1−7)又はそのペプチド若しくは非ペプチド類似体の製剤の使用に関する発明はない。
【0022】
筋萎縮症は、悪液質、癌、AIDS、多くの原因によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性使用及び様々な神経学的症候群及び外傷などの多様な状態によって引き起こされる深刻な病的状態である(Lai KM, Gonzalez M. Poueymirou WT, Kline WO, Na E, Zlotchenko E, Stitt tN, Ecomonides An, Yancopoulos GD, Glass DJ. Conditional activation of act in adult skeletal muscle induces rapid hypertrophy. Mol Cell Biol. (21):9295-304, 2004)。最近、骨格筋におけるシグナリング経路を活性化することのできる戦略であって、筋肉のトロピズムを回復することのできるものが研究された。これらの経路の中で、Aktは、嫌気的経路を活性化し、そして同時にかつ圧倒的に異化経路を抑制することができるため、注目に値する(Stitt TN, Duran D., Clarke BA, Planar F, Timofeyva Y, Kline WO, Gonzalez M, Yancopoulos GD, Glass DJ. Mol Cell. 14(3):395-403, 2004)。IGF-1/PI3K/Akt経路は、FOXO転写因子を阻害することによって、筋萎縮により誘導されるユビキチンリガーゼの発現を阻止する(Mol Cell; 14(3):395-403、2004)。末梢筋肉組織中のAng-(1-7)の作用は、骨格筋内の血流の増加(Sampaio WO, Nascimento AAS, Santos RAS, Systemic and regional hemodynamic effects of angiotensin-(1-7) in rats. Am J Physiol Heart Circ Physiol., 284(6):H1985-94, 2003)及びシナプスの円滑化(Bevilaqua ER, Kushmerick C, Beirao PS, Naves LA. Angiotensin 1-7 increases quantal content and facilitation at the frog neuromuscular junction. Brain Res.; 927(2)208-11, 2002)。さらに、Ang-(1-7)はAktを活性化する。しかしながら、従来技術においては、Ang-(1-7)/Mas/Akt軸を活性化する、Ang-(1-7)又はそのペプチド若しくは非ペプチド類似体の、筋肉の分化、成熟及び再生における変化を含む病理の予防及び治療のための使用、並びにエルゴジェニックな資源としての使用に関する発明はない。
【0023】
Ang-(1-7)又は他のアゴニストとMas受容体との相互作用によって仲介されるAktの活性化に基づく抗アポトーシス活性の活性化は、中でも、皮膚、内分泌腺、肝臓、腎臓、胃腸管及び泌尿生殖器管を含む他の組織及び器官においても起こることができる。
【0024】
本発明は、非限定的な以下の実施例及び詳細な説明の助けによってより良く理解されることができる。
【実施例】
【0025】
実施例1
この実施例は、生理学的機能の中枢制御に関与する脳の領域中のMAS受容体の同定を記載する。
【0026】
動物をトリブロモエタノール(0.25g/Kg)で麻酔し、そしてPBS(0.02M、pH7.4)で2分間、そして、PBS中10%パラホルムアルデヒド溶液で15分間、経心的に灌流した。脳を取り出し、そして同じ固定液中に2時間置いた。そして、組織をPBS溶液中で3回洗浄し、その後、シュークロース溶液(PBS中30%)中に一夜置いた。−18℃の温度の凍結ミクロトーム中で、30μmの脳切片を、前額面内で作製した。延髄及び視床下部の切片を、PBS、トゥイーン0.5%及びBSA5%中で「フリーフローティング」法によってそれぞれ15分間インキュベートし、そして切片をMas一次抗体(1:500)とともに、4℃で48時間インキュベートした。隣接する切片において、Masタンパク質で予め吸収処理した一次抗体とともにインキュベートした陰性対照を実施した。48時間後、切片をPBS溶液中で5分間、3回洗浄し、蛍光化合物に結合した二次抗体とともに室温で60分間インキュベートした。この期間の後、切片をPBS中で5分間、3回洗浄し、乾燥したゼラチンコートしたスライドガラス内に保持し、そして1:3のグリセロール及びPBSを含むマウンティング溶液中でそれぞれスライドガラスで覆った。使用した各蛍光化合物に特異的な励起及び発光フィルターを有する共焦点顕微鏡下でブレード(blade)を分析する。免疫蛍光アッセイに供する、隣接切片を含むスライドガラスを、組織の構造分析及び様々な領域の同定のためにニュートラルレッド法で染色した。あるものは、脳内の観察した領域を定義するためにAtlas de G. Paxinos, C. Watson, The rat brain in stereotaxic coordinates, 2nd Edition, Academic Press, New York, 1986を使用した。図1は、視床下部の前部切片中のMas Ang-(1-7)受容体の存在を、その免疫反応性によって、異なる領域の組織学的同定のためにニュートラルレッドで染色した多数の領域(図1A)及び隣接切片中で示す(図1B)。図2は、視床下部傍室核(PVN、図2A)及び外側視索前野(LPO、図2C)中のMas Ang(1-7)受容体の存在を、免疫反応性によって示し、そして対照である隣接切片(図2B及び2D)中では合成Masタンパク質で抗体を予め吸収処理した場合にマーキングが消失することを示した。図3においては、矢印は、視索上核(CSO、図3A)中のMas、Ang-(1-7)受容体の存在を、免疫反応によって示した。隣接切片(図3B及び3D)は、合成Masタンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図4は、扁桃(図4A)及び視床の背側前核(図4C)中のMas Ang(1-7)受容体の存在を免疫反応によって示し、そして、隣接切片中の対照(図4B及び4D)は、抗体をMas合成タンパク質で予め吸収処理した場合のマーキングの消失を示す。図5は、皮質(HL、図5A)及び海馬(HC、図5C)中のMas Ang-(1-7)受容体の存在を免疫反応によって示し、そして、隣接切片中の対照(図5B及び5D)は、抗体をMas合成タンパク質で予め吸収処理した場合のマーキングの消失を示す。図6は、Aにおいて、延髄の前部切片を示し、多数の領域中のMas Ang-(1-7)受容体についての免疫反応性を図示する。B及び隣接切片中では、異なる領域の組織学的同定のためにニュートラルレッドで染色した。図7は、延髄の尾側腹外側領域(CVLM、図7A)及び吻側腹外側領域(RVLM、図7C)中のMas Ang-(1-7)受容体についての免疫反応性を示し、そして、隣接領域中の対照(図7B及び7D)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図8は、孤束核(NTS、図8A)及び下オリーブ核(IO、図8C)中のMas Ang-(1-7)受容体の存在を免疫反応性によって示し、そして、隣接領域中のその対照(図8B及び8D)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図9は、舌下神経(12、図9A)中のMas Ang-(1-7)受容体の存在を免疫反応性によって示し、そして、隣接切片中のその対照(図9B)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図9Cは、延髄の吻側腹外側領域中のMas 受容体とAKTの免疫共存を示し、この領域の神経性の調節における受容体MasとAKTの相互作用の可能性を示唆している。
【0027】
実施例2
この実施例は、Ang-(1-7)とそのMas受容体との相互作用によるPIK3/Akt経路の活性化の同定を記載する。
【0028】
Mas受容体(CHO-Mas)でトランスフェクトしたCHO細胞とヒトの胸部大動脈の内皮細胞(HAEC)を、約80%のコンフルエンスまで培養し、そしてウエスタンブロッティングのための溶解バッファーで処理した。処理後、タンパク質濃度を測定し、そしてライセートをポリアクリルアミド/SDSゲル中の電気泳動に供し、そしてニトロセルロース膜に転写した。膜を特異的な抗体(抗−ホスホ−Akt、抗−Akt、抗−ホスホ−eNOS及び抗−βアクチン)とともにインキュベートした。展開後にケミルミネッセンスによってバンドを観察した。図10は、CHO-Mas細胞中でのキナーゼB(Akt)のリン酸化においてAng-(1-7)によって生じた刺激を示す。Ang-(1-7)アンタゴニストであるA-779はこの効果をブロックした。図11は、CHO-Mas細胞中でAng-(1-7)によって刺激された、内皮のニトリックオキシドシンターゼの刺激部位(S1177)のリン酸化にAktが関与することを示す。ホスファチジルイノシトール3キナーゼアンタゴニスト(PI3K)はこの効果をブロックした。図12は、ヒト内皮細胞(HAEC)上のキナーゼB(Akt)のリン酸化におけるAng-(1-7)の刺激効果を示す。Ang-(1-7)アンタゴニストであるA-779は、この効果をブロックした。図13は、ヒト内皮細胞(HAEC)中のAng-(1-7)によって刺激されたeNOSの刺激部位(S1177)のリン酸化へのAktの関与を示す。PI3Kアンタゴニストであるワートマニンは、この効果をブロックした。
【0029】
実施例3
この実施例は、覚醒したラットにおける、Ang-(1-7)によって刺激された内皮の機能の改善へのPI3K/Akt経路の関与の同定を記載する。
【0030】
実験の24時間前に、ウィスターラットに、(血圧及び心拍数の分析のために)大腿動脈、(薬物の注射及び輸注のために)大腿静脈、そして(薬物の注射のために)左頚動脈中にカテーテルを外科的に埋め込んだ。血圧及び心拍数の記録を、マイクロコンピュータに接続したデータ取得システム(BIOPAC System、Inc.)を介して得た。図14Aは、アセチルコリン(ACh)の血管拡張作用が、覚醒したウィスターラット(n=7)において生理食塩水の静脈内輸注(NaCl 0.9%、0.4mL/時間)によって変化しないことを示す。しかしながら、Ang-(1-7)の静脈内輸注(7.0ピコモル/分)は、覚醒したウィスターラット(n=9)においてアセチルコリン(ACh)の血管拡張作用を増強する(図14B)。図14Cは、ワートマニン(10-6M)のボーラス静脈内注射において、Ang-(1-7)(7.0ピコモル/分)に伴うワートマニン(10-6M)の静脈内ボーラス注射の前のPI3K阻害剤が、覚醒したウィスターラット(n=7)におけるアセチルコリン(ACh)の血管拡張作用のAng-(1-7)による増強をブロックすることを示す。どの群においても、われわれは圧反射における変化を観察しなかった。
【0031】
実施例4
この実施例は、NADPHオキシダーゼの活性におけるAng-(1-7)とMas受容体の相互作用によるPIK3/Akt経路の活性化の同定を示す。
【0032】
NAD(P)Hオキシダーゼの活性を定量するために、アンギオテンシンII(10-7M)で10分間、ヒト動脈内皮細胞(HAEC)を刺激した。いくつかの実験においては、予め、細胞をAT1受容体アンタゴニストであるイベサルタン(Ibesartan)(10-5M)に30分間、又はAng-(1-7)(10-7M)に15分間露出した。ルシゲニンからの化学発光を、細胞のホモジェネート中のNAD(P)Hオキシダーゼの活性を測定するために使用した。c-SRCのリン酸化におけるAng-(1-7)の調節を定量するために、HAECを約80%のコンフルエンスに達するまで培養し、そしてウエスタンブロッティングのための溶解バッファーで処理した。処理後、タンパク質濃度を測定し、そしてライセートをポリアクリルアミド/SDSのゲル電気泳動に供し、そしてニトロセルロース膜に転写した。膜を特異的な抗体(抗−ホスホ−c-SRC、抗−c-SRC)とともにインキュベートした。展開後、ケモルミネッセンスによってバンドを可視化した。図15は、ヒト内皮細胞(HAEC)中のAng IIによって刺激されたc-SRCのリン酸化におけるAng-(1-7)の調節効果を示す。棒グラフは、4つの実験の平均±EPMを示す。対照に対して、*P<0.05及び**P<0.001。図16は、Ang II(10-7M、10分)によって刺激されたHAECにおける、NAD(P)Hオキシダーゼの活性に対するAng-(1-7)(10-7M、プレインキュベーション15分)の効果を示す。いくつかの実験においては、細胞をイベサルタン(10-5M、30分)とともにプレインキュベーションした。データを、4つの実験の平均±EPMとして表す。対照に対して、*p<0.05。AngII+Ang(1-7)に対して、+p<0.05。
【0033】
実施例5
この実施例は、Mas、G-タンパク質結合受容体アンタゴニストの精子形成における効果を記載する。
【0034】
MasG-タンパク質−結合受容体アンタゴニストであるA-779(2.5μg/時間、14日、n=5)又は担体(NaCl 0.9%、1μl/時間、14日、n=6)を含む浸透圧ミニポンプ(ALZET、モデル2002)を、トリブロモエタノール(2.5%、1ml/100g体重)の麻酔下のC57マウスの背部領域中の皮下に埋め込んだ。この後、動物を体重測定し、そして腹腔内経路で125U/kg体重の濃度でヘパリンを注射した。15分後、これらの動物をチオペンタールナトリウム(50mg/kg体重)で鎮静させ、そして左心室を介して灌流した。第一のステップにおいては、約80mmHgの圧力下で室温において、約5分間、0.9%食塩水溶液で血管床の洗浄を行った。この手順後ただちに、リン酸バッファー(0.05M、pH7.2〜7.4)中、4%グルタルアルデヒド固定液で約25分間、動物を灌流した。このステップの後、精巣を除去し、そしてそれぞれの精巣上体から分離して重量測定した。精巣重量及び体重から、各動物についての生殖腺指数(精巣重量と体重の間のパーセンテージ関係)を推定した。顕微鏡分析のために、約3mm以下の厚さの精巣断片を収集し、これを4%グルタルアルデヒドのバッファー中に2〜4時間、4℃で浸漬した。そして、断片を、それらが組織学的分析(アポトーシスの存在)のために処理されるまで、4℃のリン酸バッファー中に保存した。精巣のこれらの断片を、増加する濃度のアルコール(30分ごとに70°、80°、90°、100°に交換する)で脱水した。脱水後、断片をメタクリレートグリコール(Leica Historesin Embedding Kit, Leica Instruments)中に入れ、その後、ガラスカッターを備えたミクロトームで4μmの厚さに区分した。得られた切片を1%ホウ酸トルイジンブルーナトリウムで染色し、エンテラン(Merk)を載せ、そしてOlympus顕微鏡下で分析した。図17は、Mas G-タンパク質−結合受容体アンタゴニストであるA-779で処置された動物が、対照群に対して、横断面当たりのアポトーシスの数が多いが、生殖腺指数においては相違がなかったことを示す。
【0035】
実施例6
この実施例は、Mas-KOマウスの卵巣における形態学的変化を記載する。
【0036】
未成熟の雌性マウス(30日、11〜14g)WT(野生型;n=4)及びMas-KO(n=3)を断頭してと殺した。卵巣を除去し、PBS0.1m中、4%グルタルアルデヒド中で固定し、そしてグリコールメタクリレート中に入れた。5つの切片(5μm)ごとに、組織学用スライド上に集め、トルイジンブルーで染色した。増殖する胞状一次濾胞及び閉鎖一次濾胞の数を確定するために、形態学的分析を用いた。KOの卵巣は、WTの卵巣よりも、顕著に低い濾胞総数を示し(1494対3332)、始原濾胞においては特別であった(418対1930)。さらに、KO雌性マウスの閉鎖濾胞のパーセンテージは、WTマウスと比べると、約50%高かった。これらのデータは、Mas受容体の除去の結果としての卵巣のアポトーシス活性の増加を示唆する。
【0037】
実施例7
この実施例は、Mas受容体の存在がアポトーシス活性の調節に寄与しているかもしれない多数の組織におけるMas受容体の発現を、RT-PCRによって示す(図18)。
【発明の概要】
【0001】
本発明は、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、病気の研究、予防及び治療のためのアポトーシス活性調節剤としての使用を特徴とする。
【0002】
本発明はさらに、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、B/Aktキナーゼタンパク質の活性の変更を含むアポトーシス活性の調節のための使用を特徴とする。
【図面の簡単な説明】
【0003】
【図1】図1は、視床下部の前部切片中のMas Ang-(1-7)受容体の存在を、その免疫反応性によって、異なる領域の組織学的同定のためにニュートラルレッドで染色した多数の領域(図1A)及び隣接切片中で示す(図1B)。
【図2】図2は、視床下部傍室核(PVN、図2A)及び外側視索前野(LPO、図2C)中のMas Ang(1-7)受容体の存在を、免疫反応性によって示す。対照である隣接切片(図2B及び2D)中では合成Masタンパク質で抗体を予め吸収処理した場合にマーキングが消失することを示した。
【図3】図3は、視索上核(CSO、図3A)中のMas、Ang-(1-7)受容体の存在を、免疫反応によって、矢印にて示す。
【図4】図4は、扁桃(図4A)及び視床の背側前核(図4C)中のMas Ang(1-7)受容体の存在を免疫反応によって示す。隣接切片中の対照(図4B及び4D)は、抗体をMas合成タンパク質で予め吸収処理した場合のマーキングの消失を示す。
【図5】図5は、皮質(HL、図5A)及び海馬(HC、図5C)中のMas Ang-(1-7)受容体の存在を免疫反応によって示す。隣接切片中の対照(図5B及び5D)は、抗体をMas合成タンパク質で予め吸収処理した場合のマーキングの消失を示す。
【図6】図6は、Aにおいて、延髄の前部切片を示し、多数の領域中のMas Ang-(1-7)受容体についての免疫反応性を図示する。B及び隣接切片中では、異なる領域の組織学的同定のためにニュートラルレッドで染色した。
【図7】図7は、延髄の尾側腹外側領域(CVLM、図7A)及び吻側腹外側領域(RVLM、図7C)中のMas Ang-(1-7)受容体についての免疫反応性を示す。隣接領域中の対照(図7B及び7D)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。
【図8】図8は、孤束核(NTS、図8A)及び下オリーブ核(IO、図8C)中のMas Ang-(1-7)受容体の存在を免疫反応性によって示す。隣接領域中のその対照(図8B及び8D)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。
【図9】図9は、舌下神経(12、図9A)中のMas Ang-(1-7)受容体の存在を免疫反応性によって示す。隣接切片中のその対照(図9B)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図9Cは、延髄の吻側腹外側領域中のMas 受容体とAKTの免疫共存を示し、この領域の神経性の調節における受容体MasとAKTの相互作用の可能性を示唆している。
【図10】図10は、CHO-Mas細胞中でのキナーゼB(Akt)のリン酸化においてAng-(1-7)によって生じた刺激を示す。Ang-(1-7)アンタゴニストであるA-779はこの効果をブロックした。
【図11】図11は、CHO-Mas細胞中でAng-(1-7)によって刺激された、内皮のニトリックオキシドシンターゼの刺激部位(S1177)のリン酸化にAktが関与することを示す。ホスファチジルイノシトール3キナーゼアンタゴニスト(PI3K)はこの効果をブロックした。
【図12】図12は、ヒト内皮細胞(HAEC)上のキナーゼB(Akt)のリン酸化におけるAng-(1-7)の刺激効果を示す。Ang-(1-7)アンタゴニストであるA-779は、この効果をブロックした。
【図13】図13は、ヒト内皮細胞(HAEC)中のAng-(1-7)によって刺激されたeNOSの刺激部位(S1177)のリン酸化へのAktの関与を示す。PI3Kアンタゴニストであるワートマニンは、この効果をブロックした。
【図14】図14は、覚醒したウィスターラット(n=7)における、アセチルコリン(ACh)の血管拡張作用の結果を示す。図14Aは、アセチルコリン(ACh)の血管拡張作用が、覚醒したウィスターラット(n=7)において生理食塩水の静脈内輸注(NaCl 0.9%、0.4mL/時間)によって変化しないことを示す。しかしながら、Ang-(1-7)の静脈内輸注(7.0ピコモル/分)は、覚醒したウィスターラット(n=9)においてアセチルコリン(ACh)の血管拡張作用を増強する(図14B)。図14Cは、ワートマニン(10-6M)のボーラス静脈内注射において、Ang-(1-7)(7.0ピコモル/分)に伴うワートマニン(10-6M)の静脈内ボーラス注射の前のPI3K阻害剤が、覚醒したウィスターラット(n=7)におけるアセチルコリン(ACh)の血管拡張作用のAng-(1-7)による増強をブロックすることを示す。
【図15】図15は、ヒト内皮細胞(HAEC)中のAng IIによって刺激されたc-SRCのリン酸化におけるAng-(1-7)の調節効果を示す。
【図16】図16は、Ang II(10-7M、10分)によって刺激されたHAECにおける、NAD(P)Hオキシダーゼの活性に対するAng-(1-7)(10-7M、プレインキュベーション15分)の効果を示す。
【図17】図17は、Mas G-タンパク質−結合受容体アンタゴニストであるA-779で処置された動物が、対照群に対して、横断面当たりのアポトーシスの数が多いが、生殖腺指数においては相違がなかったことを示す。
【図18】図18は、Mas受容体の存在がアポトーシス活性の調節に寄与しているかもしれない多数の組織におけるMas受容体の発現を、RT-PCRによって示す。
【発明を実施するための形態】
【0004】
本発明の他の特徴は、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含む、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、病気の研究、予防及び治療において使用するためのアポトーシス活性調節剤としての使用である。
【0005】
本発明はさらに、薬学的に又は薬理学的に許容可能な担体とともに製剤された、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニスト、そして、アンギオテンシン−(1−7)ペプチド並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含む、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、アポトーシス活性調節剤としての使用も権利請求する。
【0006】
他の権利請求される特徴は、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含む、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの製剤の、マイクロ及びナノ粒子である、埋め込み型又は注射用デバイスの、アポトーシス活性調節剤としての使用である。
【0007】
ここに記載される投与形態は、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニスト、そしてそれらの製剤を含む、Mas、Gタンパク質結合受容体アゴニスト及びアンタゴニストの、経口、筋肉内、静脈内、皮下、局所、経皮、肛門内、吸入(肺内、鼻腔内、口腔内)投与経路のいずれかを介する使用、或いは埋め込み型又は注射用のデバイスとしての使用を含むが、これらに限定されない。
【0008】
体液及び血圧のホメオスタシスの調節物質としてのレニン−アンギオテンシン系(RAS)の役割は、かなり知られている。RASは、生理学的及び病理学的状態の両方における、血圧、循環器のホメオスタシス及び水分電解質バランスの調節に関与する(Santos, R.A.S.; Campagnole-Santos, M.J.; Andrade, S.P. Angiotensin-(1-7): an update. Regul Pept. 91:45−62, 2000)。最近、血液循環中のAng IIを生成する系のほかに、異なる組織が、局所的にこの系の様々な生理活性ペプチドを生成しうることが発見された(組織のRAS)。組織のRASの成分は、心臓、管、腎臓、男性及び女性生殖系、内分泌腺、脊髄及び脳を含む様々な器官及び組織中に見出される。異なる組織中のこれらのRASの機能は、完全には明らかにされていない(Santos, RAS, Campagnole-Santos, MJ, Andrade, SP, Angiotensin-(1-7): an update. Regul Pept. 91:45-62, 2000; Yoshimura, Y. The ovarian rennin-angiotensin system in reproductive physiology. Front Neuroendocrinol.; 18: 247-291, 1997)。
【0009】
古典的なRASの主要成分は、以下の:アンギオテンシノーゲンのアンギオテンシンI(Ang I)へのタンパク分解による変換を触媒する酵素である、レニン;レニンの主要な基質でありアンギオテンシンII(Ang II)の前駆体であるアンギオテンシノーゲン;2つのカルボキシ末端アミノ酸を加水分解することによりAng IをAng IIに変換する、アンギオテンシン変換酵素(ACE);この系の主要な生理活性ペプチドであるアンギオテンシンII;及びAng IIの細胞における作用の開始に関与する、AT1及びAT2受容体である。この周知の系に、アンギオテンシンIII(Ang III)、アンギオテンシンIV(Ang IV)及びアンギオテンシン−(1−7)[(Ang-(1-7)]などの他のペプチドが追加された。Ang-(1-7)は、組織のエンドペプチダーゼによってAng I又はAng IIから生成されることができる(Santos, R.A. Brosnihan, K.B. Cappell, M. C., Pesquero, J., Chernicky, C.L., Greene, L. J., ;Ferrario, C.M. Converting enzyme activity and angiotensin metabolism in the dog brainstem. Hypertension (11(2-Pt-2): l153-l1537, 1988)。
【0010】
Ang-(1-7)は、血漿中並びに雌性ラット卵巣(Costa APR, Fagundes-Moura CR, Pereira VM., Silva LF, Vieira MA, Santos RA, Reis AM. Angiotensin-(1-7): a novel peptide in the ovary. Endocrinology. 144:1942-1948, 2003)を含む様々なヒト及び動物の器官及び組織中で確認されている(Santos, R.A.S.; Campagnole-Santos, M.J.; Andrade,S.P. Angiotensin-(1-7): an update. Regul Pept. 91:45-62, 2000)。その独立したACE産生が、Santos et al., 1988(Santos, R.A., Brosnihan, K.B., Cappell, M.C., Pesquero, J., Chernicky, C.L., Greene, L.J.; Ferrario, C.M. Converting enzyme activity and angiotensin metabolism in the dog brainstem. Hypertension, 11(2-Pt 2): l153-l153-l1537, 1988)によって実証され、特異的受容体へのその結合がSantos et al., 1994(Santos, RAS, Campagnole-Santos, M.J., Baracho, N.C., Fontes, M.A., Silva, L.C., Neves, L.A., Oliveira, D.R., Caligiorne, S.M., Rodrigues, A.R., Gropen Junior, C. Characterization of a new angiotensin antagonist selective for angiotensin-(1-7): evidence that the actions of angiotensin-(1-7) are mediated by specific angiotensin receptors. Brain Res Bull. 35(4):293-298, 1994)及びTallant et al., 1997, (Tallant, E.A., Lu, X., Weiss, R.B., Cappell, M. C.; Ferrario, C.M. Bovine aortic endothelial cells contain an angiotensin-(1-7) receptor. Hypertension 29:388-393, 1997)によって示唆された。これらの発見は、特に、Ang-(1-7)のための選択的アンタゴニストであるA-779(Asp1-Arg2-Val3-Tir4-Lle5-His6-D-Ala7;Santos, R.A., Campagnole-Santos, M.J. Barracho, N.C., Fontes, M.A. Silva, L.C., Neves, L.A. Oliveira, D.R., Caligione, S.M., Rodrigues, A.R., Groppen Junior, C. Characterization of a new angiotensin antagonist selective for angiotensin-(1-7) : evidence that the actions of angiotensin-(1-7) are mediated by specific angiotensin receptors. Brain Res Bull. 35(4):293-298, 1994; Ambuhl, P, Felix, D. Khosla, M.C. [7-D-ALA]-Angiotensin-(1-7): selective antagonism of angiotensin-(1-7) in the rat paraventricular nucleus. Brain Res Bull. 1994; 35(4):289-91)の利用可能性によって得られた。
【0011】
様々な酵素がRASカスケードのいくつかのステップに関与し、ここでそれらはいくつかのペプチド断片の分解並びに他のものの生成に関与する。ACEは、Ang IのAng IIへの変換に関与し;PEP(プロリルエンドペプチダーゼ)がAng I及びAng IIからAng(1-7)を生成し、そしてNEP(ニュートラルエンドペプチダーゼ)がAng IのAng-(1-7)への変換を触媒する。ACEはまた、Ang-(1-7)を加水分解し、Ang-(1-5)を生成する(Chappell MC, Pirro NT, Sykes, A, Ferrario CM. Metabolism of angiotensin-(1-7) by angiotensin-converting enzyme. Hypertension. 31:362-367, 1998)。したがって、ACE経路は、循環中及び組織のRASの生理活性ペプチドの生成及び分解の両方にとって重要である。より最近には、他の酵素、ACE2が記載され、これはAng-(1-7)の形成にとって重要である(SR Tipnis, NM Hooper, R Hyde, E Karran and G Christie. The human homolog of angiotensin-converting enzyme. Cloning and functional expression as a captopril-insensitive carboxypeptidase. J. Biol Chem. 275(43):33238-33243, 200)。この酵素は、Ang-(1-7)を、特にAng IIから生成する。
【0012】
アンギオテンシン−(1−7)及びアンギオテンシンIIは、主要なRASエフェクターである。2つの重要な特徴がAng-(1-7)をAng IIから識別する:最初のAng(1-7)は非常に特異的な生理活性を有し、Ang-(1-7)の生成経路によって、ACEから完全に独立しうる(Santos, R.A.S.; Campagnole-Santos, M. J.; Andrade, S.P. Angiotensin-(1-7): an update. Regulatory Peptides. 91: 45−62, 2000)。
【0013】
Mas調節物質は最初、インビボでのその弱い腫瘍形成活性によってプロトオンコジーンとして記載された(Young D. Waitches G, Birchmeier C. Fasano O. Wigler M. Isolation and characterization of a new cellular oncogene encoding a protein with multiple potential transmembrane domains. Cell. 1986; 45:711-71)。
【0014】
哺乳動物においては、その遺伝子の発現は圧倒的に精巣及び海馬を含む脳の様々な区域及び扁桃で検出され、より弱いが、顕著なレベルで腎臓及び心臓で検出された(Bunnemann B, Fuxe K, Metzger R, Mullins J, Jackson TR, Hanley MR, Ganten D. Autoradiographic localization of Mas proto-oncogene mRNA in adult rat brain using in situ hybridization. Neurosci Lett 114:147-153, 1990; Alenina N, Bader M, Walther T. Imprinting of the murine MAS proto-oncogene is restricted to its antisense RNA. Biochem Biophys Res Commun. 290:1072-1078, 2002)。
【0015】
その遺伝子は、G-タンパク質結合受容体のクラスIの特徴を有する、7つの膜貫通ドメインを有するタンパク質を調節する。初期の研究においては、この遺伝子は、オクタペプチドであるアンギオテンシンIIの受容体の調節因子として示唆された(Jackson TR, Blair LA, Marshall J, Goedert M, Hanley MR. The Mas oncogene encodes an angiotensin receptor. Nature 335:437-440, 1988)。しかしながら、Ambrozと共同研究者そして後のArdaillouは、Masによりトランスフェクトされた細胞におけるAng IIによる細胞内カルシウムの上昇が、Ang IIのAT1受容体を内因的に発現する細胞のみにおいておこることを示した(Ambroz C, Clark A, Catt KJ. The Mas oncogene enhances angiotensin-induced [Ca2+]i responses in cells with pre-existing angiotensin II receptors. Biochem Biophys Acta. 1133: 107-111, 1991; Ardaillou R. Angiotensin II receptors. J Am Soc Nephrol. 10:S30-S39, 1999)。より最近には、実際に、MasがAng-(1-7)の受容体であることが観察された(Santos, R.A., Simoes e Silva A C, Maric, C., Silva, D.M., Machado, R.P., de Buhr, I., Heringer-Walther, S., Pinheiro, S.V., Lopes, M.T., Bader, M., Mendes, E.P., Lemos, V.S., Campagnole-Santos, M.J., Schultheiss, H.P., Speth, R.; Walther, T. Angiotensin-(1-7) is an endogenous ligand for the G protein-coupled receptor Mas Proc Natl. Acad Sci USA, 100(14):8258-8263, 2003)。
【0016】
内皮の機能不全は、標的器官(中でも、心臓、腎臓、脳、血管、生殖器官)の病巣に関連する様々な病理の設置及び進行においてより早期に発生する事象である(Goligorsky MS. Endothelial cell dysfunction: can't live with it, how to live without it. Am J. Physiol Renal Physilo. 288(5):F871-80, 2005)。窒素酸化物のバイオアベイラビリティーの減少は、内皮の機能不全の開始のための決定的因子であり、それは、この分子が血管拡張性、抗増殖性、抗凝固性、アテローム産生抑制性の性質を有し、かつ活性酸素種の産生を中和するからである(Ogita H, Liao J. Endothelial function and oxidative stress. Endothelium. 11(2):123-32, 2004)。最近、カルシウムに依存する古典的経路のほかに、窒素酸化物が、内皮のニトリックオキシドシンターゼ(eNOS)の1177セリンなどの部位のB/Aktキナーゼタンパク質を介する直接的リン酸化によって形成されることができることが実証された。このメカニズムは、内皮の完全性の維持に大いに貢献する。eNOSのリン酸化によるAktの活性化は、ヒト内皮中でAnt-(1-7)によって刺激される窒素酸化物の放出に関与し、結局、本発明の特徴である、内皮の機能性の改善に関与する。本発明の他の特徴は、Ang-(1-7)が、c-SRCなどの活性酸素種の産生に関与する近位の細胞内経路を阻害することによって、ヒト内皮中のAng IIの作用の負の調節を行うことを実証することである。さらに、Ang-(1-7)は、血管壁中の最大の活性酸素種産生源であるNAD(P)Hオキシダーゼの活性を阻害する(Touyz RM. Reactive oxygen species and angiotensin II signaling in vascular cells-implications in cardiovascular disease. Braz J Med Bio Res. 37(8): 1263-73, 2004)。Ang IIによるNAD(P)Hの活性化は、該酵素のサブユニットp47phoxのリン酸化及び膜への移動のためにc-SRCを必要とする。さらに、Ang IIによる慢性の刺激においては、c-SRCは、NAD(P)Hオキシダーゼのサブユニットgp91phox、p22phox、及びp47phoxのタンパク質発現の増加に関与する(Touyz RM, Yao G, Schiffrin EL. c-Src induces phosphorylation and translocation of p47pho role in super oxide generation by angiotensin II in human vascular smooth muscles cells. Arterioscler Thromb Vasc Biol 23(6):981-7, 2003)。酸化促進因子及び抗酸化因子間のアンバランスが内皮の機能不全開始の決定因子の1つであるため、この事実は特に重要である。したがって、窒素酸化物の放出によって内皮の完全性を維持することに直接寄与するほかに、Ang-(1-7)は酸化フリーラジカルの生成も中和する。そして、活性酸素種の産生はアポトーシス活性と密接に関連し、なぜなら、それはMAPK、カスパーゼなどの細胞死の決定因子を含むシグナルカスケードを刺激するからである(Matuzawa, A. Ichijo, H. Stress-responsive protein kinases in redox-regulated apoptosis signaling. Antioxid Redos Signal 7(3-4):472-81;2005)。しかしながら、循環器、腎臓の病気、多重メタボリック症候群(plurimetabolic syndrome)、勃起不全、中枢神経系の病気などの、しかしこれらに限らない内皮の機能不全を含む病理の予防及び治療のために、Mas受容体を介してPI3K/Akt/eNOSカスケードを活性化し、並びにNAD(P)Hオキシダーゼを不活性化し、そして活性酸素種の産生及び内皮のアポトーシスに関与するメカニズムを低下させる、Ang-(1-7)又はそのペプチド若しくは非ペプチド類似体の製剤を使用することに関する発明は従来技術においてなかった。
【0017】
Ant-(1-7)は、探索行動を増加させ、かつ記憶を促進する(Santos, RA, Campagnole-Santos, MJ. Central and Peripheral actions of Angiotensin-(1-7). Braz J Med Bio Res. 27(4):1033-47, 1994; Hellner, K., Walther, T., Schubert, M., Albrecht, D. Angiotensin-(1-7) enhances LTP in the hippocampus through the G-protein-coupled receptor Mas. Mol Cell Neurosci 29(3):427-35, 2005)。Mas受容体は、海馬、扁桃体及び脳皮質を含む、これらの機能に関与する脳の領域に位置する(K. A Martin, S. G. Grant, S. Hockfield. The Mas proto-oncogene is developmentally regulated in the rat central nervous system. Brain Res Dev Brain Res 68(1): 75-82, 1992)。Mas受容体とAng-(1-7)との相互作用は、抗アポトーシス特性を有するシグナリング経路、より特別にはPKI3/Aktの経路を活性化する。Ang-(1-7)により増加する、B(Akt)キナーゼタンパク質によるリン酸化は、細胞のアポトーシスを減少させる(Z.-Z. Yang, O. Tschopp, A. Baudry, B. Dummler, D. Hynx and B. A Hemmings. Physiological functions of protein kinase B Akt Biochem Soc Trans. 32:350-354, 2004)。Aktの脳の亜型であるAktγについてのノックアウトマウスは、脳重量の劇的な減少を示す(Z.-Z. Yang, O. Tschopp, A. Baudry, B. Dummler, D. Hynx and B. A Hemmings. Physiological functions of protein kinase B Akt Biochem Soc Trans. 32:350-354, 2004)。脳内のAktの発現部位のいくつかは、Mas 受容体のためのRNAMにも富む領域である、海馬及び脳皮質である。しかしながら、従来技術においては、Ang-(1-7)とMas受容体との相互作用によって誘導される、Aktにより仲介される抗アポトーシス活性の刺激に基づく、変性脳疾患、或いは記憶又は学習障害の制御又は予防のためのアンギオテンシン−(1−7)の製剤に関する発明はない。同様に、Mas受容体のペプチド又は非ペプチドアゴニストと該受容体との相互作用により誘導される、Aktにより仲介される抗アポトーシス活性の刺激に基づく、変性脳疾患、或いは記憶又は学習障害の研究、予防又は治療のためのMas 受容体アゴニスト又はアンタゴニストの製剤の使用に関する発明はない。
【0018】
本発明は、Mas Gタンパク質結合受容体との相互作用へのアクセスを促進する、Ang-(1-7)、Ang-(1-7)の類似体又は誘導体を含む放出制御系の使用に特徴を有する。Gタンパク質、Mas 及びAng-(1-7)、類似体又は誘導体間の相互作用は、中でもアルツハイマー、パーキンソン、ハンチントン病などの変性脳疾患を含む、アポトーシス活性の増加に特徴を有する変性脳疾患の制御又は予防を可能とする。満足のいく放出制御系は、シクロデキストリン、生物適合性ポリマー、生物分解性ポリマー、他のポリマーマトリックス、カプセル、マイクロカプセル、微小粒子、ボーラス製剤、浸透圧ポンプ、分散デバイス、リポソーム、リポスフィア、及び経皮投与システムを含むが、これらに限定されない。
【0019】
最近、様々な文献が、IP3k/AKT経路がインスリン受容体とその基質とのシグナル伝達を仲介する決定的な役割を演じることを示した(Zdychova J, Komers R. Emerging role of Akt kinase/protein kinase B signaling in pathophysiology of diabetes and its complications. Physiol Res; 54(1):1-16, 2005)。成長因子、アンギオテンシンII、活性酸素種、コルチコステロイド、エストロゲンなどの、このカスケードを変化させるメディエーター及びその血糖状態の変化は、PI3K/Akt経路が本質的に抗アポトーシス経路であるため、糖尿病に固有の内皮の機能不全から糖尿病の妊娠女性における胎児の催奇形性変化にまで導くであろう(Reece EA, Ma XD, Zhao Z, Wu YK, Dhanasekaran D. Aberrant patterns of cellular communication in diabetes-induced embryopathy in rats: II, apoptotic pathways Am J. Obstet Gynecol. 192(3):967-972, 2005)。Aktは、この経路によって仲介されるシグナル伝達を方向付ける様々な因子によって制御されることができる。例えば、D-グルコースは、Aktのリン酸化を制御し、高血糖は、糖尿病における内皮の機能不全に関連付けられてきた(現在印刷中のVarma S, Lal BK, Zhen R, Breslin JW, Saito S, Pappas PJ, Hobson li RW, DuranWN. Hyperglycemia Alters PI3K and Akt Signaling and Leads to Endothelial Cell Proliferative Dysfunction. Am J Physiol Heart Circ Physiol. 2005)。さらに、セリンのリン酸化は、e-NOSの活性化に関連し(Kobayashi T, Taguchi K, Yasuhiro T, Matsumoto T, Kamata K, Impairment of PI3K/Akt pathway underlies attenuated endothelial function in aorta of type 2 diabetic mouse model. Hypertension. 44(6):956-962, 2004)、そして脂肪レベルの増加によって阻害されることができ、これは、内皮の保存及び循環する内皮前駆細胞(EPC)の活性化のほかに、Aktがアテローム保護作用に関係するかもしれないことを示唆している。骨格筋においては、Aktのリン酸化における変化が2型糖尿病におけるGLUt4を介する輸送の調節に関連する(Karlsson HK, Zierath JR, Kane S, Krook A, Lienhard GE, Wallberg-Henriksson H. Insulin-Stimulated Phosphorylation of the Akt Substrate AS160 Is Impaired in Skeletal Muscle of Type 2 Diabetic Subjects. Diabetes. 54(6):1692-7, 2005)。他の興味深い側面は、このカスケードがβ細胞自体の増殖及び生存に関与するようであること、及びセラミドにより活性化されるホスファターゼ(CAPP)によるその不活性化がI型糖尿病におけるインスリン分泌の変化を引き起こすかもしれないということである(Kowluru A. Novel regulatory roles for protein phosphatase-2A in the islet beta cell. Biochem Pharmacol. 69(12): 1681-1691, 2005)。PI3K/Akt/TOR経路によって仲介されるネガティブフィードバックプロセスの存在は、インスリン耐性及び腫瘍新生のための決定的事象であると指摘された(Manning BD, Balancing Akt with S6K: implications for both metabolic diseases and tumorigenesis, J. Cell Biol, 167(3): 399-403, 2004)。したがって、糖尿病の原因因子及びそれにより生じる脈管障害などの合併症の両方へのAktの関与は明らかである。
【0020】
レニン−アンギオテンシン系とインスリン受容体シグナル伝達との間には密接な関係があるようである。Ang IIが、インスリン受容体を介するAktのリン酸化を阻害することは実証済みである。さらに、Ang IIにより刺激される酸化的ストレスも、インスリンにより活性化される細胞内カスケードの様々な段階を変化させる(Taniyama, Y, Hitomi H, Shah A, Alexander RW, Griendling KK. Mechanisms of reactive oxygen species-dependent downregulation of insulin receptor substrate 1 by angiotensin II. Arterioscler Thromb Vasc. Biol. 25(6): 1142-1147, 2005)。これは、部分的に、なぜAng II阻害剤の使用が、インスリン耐性を改善し、結果として微小血管の病変のような糖尿病に関連する合併症を改善するかを説明する。Ang-(1-7)は、強力な生物学的Ang IIアンタゴニストであり、かつ内皮機能の改善に関連する様々な作用を有する。そのレベルは、系の薬理学的遮断の間に上昇し、Ang-(1-7)がACE阻害剤及びAT1受容体アンタゴニストの両方の有益な効果の重要なメディエーターであることを示している。上記で既に述べたとおり、Ang-(1-7)のMas受容体への結合がAktの強いリン酸化に導く。しかしながら、従来技術においては、インスリン耐性又はこのホルモンの産生の欠乏の結果の研究、予防又は治療のための、アンギオテンシン−(1−7)又はそのペプチド若しくは非ペプチド類似体の製剤の使用に関する発明はない。
【0021】
アンギオテンシン−(1−7)は、心臓に存在し、そして収縮性の増加及び不整脈の減少などの心臓への重要な効果を有する(Ferreira, AJ and Santos, RAS. Cardiovascular actions of Angiotensin-(1-7). Braz. J. Med. Biol Res. 38(4):499-507, 2005)。Mas受容体も、心臓内で発現され、そしてその欠乏は心臓機能の重大な低下を引き起こす(Ferreira,AJ Santos, RAS. Cardiovascular actions of Angiotensin-(1-7), Braz. J. Med. Biol Res. 38(4):499-507, 2005)。キナーゼAktタンパク質も、心臓、特に心筋細胞中で発現される。これらの細胞中では、AktはPIK3を介してリン酸化もされ、心筋の収縮性を増加させ、そして再灌流不整脈を減少させる。心臓中でのAkt発現が増加したマウスは、「インスリン様成長因子結合タンパク質−5」の増加のような、解糖系に関与するタンパク質の合成の変化を示し、これは、この経路をの活性を高める結果となる(Latronico, MGV, Costinean, S., Lavitrano, M.L. Peschle, C., Condorelli, G. Regulation of Cell Size and Contractile Function by AKT in Cardiomyocytes, Ann. N.Y. Acad. Sci. 1015: 250-260, 2004; Cook, S.A. Matsui, T., Li, L., Rosenzweig, A. Transcriptional Effects of Chronic Akt Activation in the Heart. J Biol Chem: 277(25): 22528-22533, 2002)。Ang-(1-7)の投与は、心筋梗塞に対して心臓を保護することとなる(Loot A. E. Roks A. J., HENNING, R.H., Tio, R.A., Suurmeijer, A. J., Boomsma, F, van Gilst, W.H., Angiotensin-(1-7) attenuates the develpment of heart failure after myocardial infarction in rats. Circulation. 2002:105 (13):1548-50)。Ang-(1-7)を生成する融合タンパク質を発現するトランスジェニックラットは、イソプロテレノールによる治療に応答して心臓肥大が低下し、そして再灌流不整脈の発生及び持続時間がより短い(Santos, R. A., Ferreira, A. J., Nadu, A. P., Braga, A. N., de A.meida, A.P., Campagnole-Santos, M.J., Baltatu. O., Iliescu, R., Reudelhuber, T. L., Bader, M. Expression of an angiotensin-(1-7)-producing fusion protein produces cardioprotective effects in rats. Physiol Genomics. 2004; 19(7):292-9)。一方、アデノウイルスを介するAkt遺伝子の心内投与は、ラットにおける梗塞域のサイズの減少を生じた(W. Miao, Z. Luo, R. N. Kitsis and K. Walsh, Intracoronary, Adenovirus-mediated Akt Gene Transfer in Heart Limits Infarct Size Following Ischemia-reperfusion Injury in vivo. J. Mol Cell Cardiol. 32:2397-2402, 2000)。Aktで改変された幹細胞は、ラットにおいてリモデリングを予防し、そして梗塞心臓の機能を回復する(Mangi, A. A, Noiseux, N., Kong, D., He, H., Rezvani, M., Ingwall, J. S., Dzau, V. J. Mesenchymal stem cells modified with Akt prevent remodeling and restore performance of infacted hearts Nat Med. 9:1195-1201, 2003)。しかしながら、従来技術においては、PIK3/Akt経路の刺激によって生じる抗アポトーシス活性のような細胞内情報伝達経路の刺激に基づいて、Ang-(1-7)とMas受容体との相互作用によって、心内投与後に心臓機能を増加させるか、或いは心筋変性疾患を制御又は予防するか、幹細胞のバイアビリティーを増加させるか、或いは心臓のリモデリングまたは心臓の電気生理学的障害を減少させるための、アンギオテンシン−(1−7)又はそのペプチド若しくは非ペプチド類似体の製剤の使用に関する発明はない。
【0022】
筋萎縮症は、悪液質、癌、AIDS、多くの原因によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性使用及び様々な神経学的症候群及び外傷などの多様な状態によって引き起こされる深刻な病的状態である(Lai KM, Gonzalez M. Poueymirou WT, Kline WO, Na E, Zlotchenko E, Stitt tN, Ecomonides An, Yancopoulos GD, Glass DJ. Conditional activation of act in adult skeletal muscle induces rapid hypertrophy. Mol Cell Biol. (21):9295-304, 2004)。最近、骨格筋におけるシグナリング経路を活性化することのできる戦略であって、筋肉のトロピズムを回復することのできるものが研究された。これらの経路の中で、Aktは、嫌気的経路を活性化し、そして同時にかつ圧倒的に異化経路を抑制することができるため、注目に値する(Stitt TN, Duran D., Clarke BA, Planar F, Timofeyva Y, Kline WO, Gonzalez M, Yancopoulos GD, Glass DJ. Mol Cell. 14(3):395-403, 2004)。IGF-1/PI3K/Akt経路は、FOXO転写因子を阻害することによって、筋萎縮により誘導されるユビキチンリガーゼの発現を阻止する(Mol Cell; 14(3):395-403、2004)。末梢筋肉組織中のAng-(1-7)の作用は、骨格筋内の血流の増加(Sampaio WO, Nascimento AAS, Santos RAS, Systemic and regional hemodynamic effects of angiotensin-(1-7) in rats. Am J Physiol Heart Circ Physiol., 284(6):H1985-94, 2003)及びシナプスの円滑化(Bevilaqua ER, Kushmerick C, Beirao PS, Naves LA. Angiotensin 1-7 increases quantal content and facilitation at the frog neuromuscular junction. Brain Res.; 927(2)208-11, 2002)。さらに、Ang-(1-7)はAktを活性化する。しかしながら、従来技術においては、Ang-(1-7)/Mas/Akt軸を活性化する、Ang-(1-7)又はそのペプチド若しくは非ペプチド類似体の、筋肉の分化、成熟及び再生における変化を含む病理の予防及び治療のための使用、並びにエルゴジェニックな資源としての使用に関する発明はない。
【0023】
Ang-(1-7)又は他のアゴニストとMas受容体との相互作用によって仲介されるAktの活性化に基づく抗アポトーシス活性の活性化は、中でも、皮膚、内分泌腺、肝臓、腎臓、胃腸管及び泌尿生殖器管を含む他の組織及び器官においても起こることができる。
【0024】
本発明は、非限定的な以下の実施例及び詳細な説明の助けによってより良く理解されることができる。
【実施例】
【0025】
実施例1
この実施例は、生理学的機能の中枢制御に関与する脳の領域中のMAS受容体の同定を記載する。
【0026】
動物をトリブロモエタノール(0.25g/Kg)で麻酔し、そしてPBS(0.02M、pH7.4)で2分間、そして、PBS中10%パラホルムアルデヒド溶液で15分間、経心的に灌流した。脳を取り出し、そして同じ固定液中に2時間置いた。そして、組織をPBS溶液中で3回洗浄し、その後、シュークロース溶液(PBS中30%)中に一夜置いた。−18℃の温度の凍結ミクロトーム中で、30μmの脳切片を、前額面内で作製した。延髄及び視床下部の切片を、PBS、トゥイーン0.5%及びBSA5%中で「フリーフローティング」法によってそれぞれ15分間インキュベートし、そして切片をMas一次抗体(1:500)とともに、4℃で48時間インキュベートした。隣接する切片において、Masタンパク質で予め吸収処理した一次抗体とともにインキュベートした陰性対照を実施した。48時間後、切片をPBS溶液中で5分間、3回洗浄し、蛍光化合物に結合した二次抗体とともに室温で60分間インキュベートした。この期間の後、切片をPBS中で5分間、3回洗浄し、乾燥したゼラチンコートしたスライドガラス内に保持し、そして1:3のグリセロール及びPBSを含むマウンティング溶液中でそれぞれスライドガラスで覆った。使用した各蛍光化合物に特異的な励起及び発光フィルターを有する共焦点顕微鏡下でブレード(blade)を分析する。免疫蛍光アッセイに供する、隣接切片を含むスライドガラスを、組織の構造分析及び様々な領域の同定のためにニュートラルレッド法で染色した。あるものは、脳内の観察した領域を定義するためにAtlas de G. Paxinos, C. Watson, The rat brain in stereotaxic coordinates, 2nd Edition, Academic Press, New York, 1986を使用した。図1は、視床下部の前部切片中のMas Ang-(1-7)受容体の存在を、その免疫反応性によって、異なる領域の組織学的同定のためにニュートラルレッドで染色した多数の領域(図1A)及び隣接切片中で示す(図1B)。図2は、視床下部傍室核(PVN、図2A)及び外側視索前野(LPO、図2C)中のMas Ang(1-7)受容体の存在を、免疫反応性によって示し、そして対照である隣接切片(図2B及び2D)中では合成Masタンパク質で抗体を予め吸収処理した場合にマーキングが消失することを示した。図3においては、矢印は、視索上核(CSO、図3A)中のMas、Ang-(1-7)受容体の存在を、免疫反応によって示した。隣接切片(図3B及び3D)は、合成Masタンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図4は、扁桃(図4A)及び視床の背側前核(図4C)中のMas Ang(1-7)受容体の存在を免疫反応によって示し、そして、隣接切片中の対照(図4B及び4D)は、抗体をMas合成タンパク質で予め吸収処理した場合のマーキングの消失を示す。図5は、皮質(HL、図5A)及び海馬(HC、図5C)中のMas Ang-(1-7)受容体の存在を免疫反応によって示し、そして、隣接切片中の対照(図5B及び5D)は、抗体をMas合成タンパク質で予め吸収処理した場合のマーキングの消失を示す。図6は、Aにおいて、延髄の前部切片を示し、多数の領域中のMas Ang-(1-7)受容体についての免疫反応性を図示する。B及び隣接切片中では、異なる領域の組織学的同定のためにニュートラルレッドで染色した。図7は、延髄の尾側腹外側領域(CVLM、図7A)及び吻側腹外側領域(RVLM、図7C)中のMas Ang-(1-7)受容体についての免疫反応性を示し、そして、隣接領域中の対照(図7B及び7D)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図8は、孤束核(NTS、図8A)及び下オリーブ核(IO、図8C)中のMas Ang-(1-7)受容体の存在を免疫反応性によって示し、そして、隣接領域中のその対照(図8B及び8D)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図9は、舌下神経(12、図9A)中のMas Ang-(1-7)受容体の存在を免疫反応性によって示し、そして、隣接切片中のその対照(図9B)は、Mas合成タンパク質で抗体を予め吸収処理した場合のマーキングの消失を示す。図9Cは、延髄の吻側腹外側領域中のMas 受容体とAKTの免疫共存を示し、この領域の神経性の調節における受容体MasとAKTの相互作用の可能性を示唆している。
【0027】
実施例2
この実施例は、Ang-(1-7)とそのMas受容体との相互作用によるPIK3/Akt経路の活性化の同定を記載する。
【0028】
Mas受容体(CHO-Mas)でトランスフェクトしたCHO細胞とヒトの胸部大動脈の内皮細胞(HAEC)を、約80%のコンフルエンスまで培養し、そしてウエスタンブロッティングのための溶解バッファーで処理した。処理後、タンパク質濃度を測定し、そしてライセートをポリアクリルアミド/SDSゲル中の電気泳動に供し、そしてニトロセルロース膜に転写した。膜を特異的な抗体(抗−ホスホ−Akt、抗−Akt、抗−ホスホ−eNOS及び抗−βアクチン)とともにインキュベートした。展開後にケミルミネッセンスによってバンドを観察した。図10は、CHO-Mas細胞中でのキナーゼB(Akt)のリン酸化においてAng-(1-7)によって生じた刺激を示す。Ang-(1-7)アンタゴニストであるA-779はこの効果をブロックした。図11は、CHO-Mas細胞中でAng-(1-7)によって刺激された、内皮のニトリックオキシドシンターゼの刺激部位(S1177)のリン酸化にAktが関与することを示す。ホスファチジルイノシトール3キナーゼアンタゴニスト(PI3K)はこの効果をブロックした。図12は、ヒト内皮細胞(HAEC)上のキナーゼB(Akt)のリン酸化におけるAng-(1-7)の刺激効果を示す。Ang-(1-7)アンタゴニストであるA-779は、この効果をブロックした。図13は、ヒト内皮細胞(HAEC)中のAng-(1-7)によって刺激されたeNOSの刺激部位(S1177)のリン酸化へのAktの関与を示す。PI3Kアンタゴニストであるワートマニンは、この効果をブロックした。
【0029】
実施例3
この実施例は、覚醒したラットにおける、Ang-(1-7)によって刺激された内皮の機能の改善へのPI3K/Akt経路の関与の同定を記載する。
【0030】
実験の24時間前に、ウィスターラットに、(血圧及び心拍数の分析のために)大腿動脈、(薬物の注射及び輸注のために)大腿静脈、そして(薬物の注射のために)左頚動脈中にカテーテルを外科的に埋め込んだ。血圧及び心拍数の記録を、マイクロコンピュータに接続したデータ取得システム(BIOPAC System、Inc.)を介して得た。図14Aは、アセチルコリン(ACh)の血管拡張作用が、覚醒したウィスターラット(n=7)において生理食塩水の静脈内輸注(NaCl 0.9%、0.4mL/時間)によって変化しないことを示す。しかしながら、Ang-(1-7)の静脈内輸注(7.0ピコモル/分)は、覚醒したウィスターラット(n=9)においてアセチルコリン(ACh)の血管拡張作用を増強する(図14B)。図14Cは、ワートマニン(10-6M)のボーラス静脈内注射において、Ang-(1-7)(7.0ピコモル/分)に伴うワートマニン(10-6M)の静脈内ボーラス注射の前のPI3K阻害剤が、覚醒したウィスターラット(n=7)におけるアセチルコリン(ACh)の血管拡張作用のAng-(1-7)による増強をブロックすることを示す。どの群においても、われわれは圧反射における変化を観察しなかった。
【0031】
実施例4
この実施例は、NADPHオキシダーゼの活性におけるAng-(1-7)とMas受容体の相互作用によるPIK3/Akt経路の活性化の同定を示す。
【0032】
NAD(P)Hオキシダーゼの活性を定量するために、アンギオテンシンII(10-7M)で10分間、ヒト動脈内皮細胞(HAEC)を刺激した。いくつかの実験においては、予め、細胞をAT1受容体アンタゴニストであるイベサルタン(Ibesartan)(10-5M)に30分間、又はAng-(1-7)(10-7M)に15分間露出した。ルシゲニンからの化学発光を、細胞のホモジェネート中のNAD(P)Hオキシダーゼの活性を測定するために使用した。c-SRCのリン酸化におけるAng-(1-7)の調節を定量するために、HAECを約80%のコンフルエンスに達するまで培養し、そしてウエスタンブロッティングのための溶解バッファーで処理した。処理後、タンパク質濃度を測定し、そしてライセートをポリアクリルアミド/SDSのゲル電気泳動に供し、そしてニトロセルロース膜に転写した。膜を特異的な抗体(抗−ホスホ−c-SRC、抗−c-SRC)とともにインキュベートした。展開後、ケモルミネッセンスによってバンドを可視化した。図15は、ヒト内皮細胞(HAEC)中のAng IIによって刺激されたc-SRCのリン酸化におけるAng-(1-7)の調節効果を示す。棒グラフは、4つの実験の平均±EPMを示す。対照に対して、*P<0.05及び**P<0.001。図16は、Ang II(10-7M、10分)によって刺激されたHAECにおける、NAD(P)Hオキシダーゼの活性に対するAng-(1-7)(10-7M、プレインキュベーション15分)の効果を示す。いくつかの実験においては、細胞をイベサルタン(10-5M、30分)とともにプレインキュベーションした。データを、4つの実験の平均±EPMとして表す。対照に対して、*p<0.05。AngII+Ang(1-7)に対して、+p<0.05。
【0033】
実施例5
この実施例は、Mas、G-タンパク質結合受容体アンタゴニストの精子形成における効果を記載する。
【0034】
MasG-タンパク質−結合受容体アンタゴニストであるA-779(2.5μg/時間、14日、n=5)又は担体(NaCl 0.9%、1μl/時間、14日、n=6)を含む浸透圧ミニポンプ(ALZET、モデル2002)を、トリブロモエタノール(2.5%、1ml/100g体重)の麻酔下のC57マウスの背部領域中の皮下に埋め込んだ。この後、動物を体重測定し、そして腹腔内経路で125U/kg体重の濃度でヘパリンを注射した。15分後、これらの動物をチオペンタールナトリウム(50mg/kg体重)で鎮静させ、そして左心室を介して灌流した。第一のステップにおいては、約80mmHgの圧力下で室温において、約5分間、0.9%食塩水溶液で血管床の洗浄を行った。この手順後ただちに、リン酸バッファー(0.05M、pH7.2〜7.4)中、4%グルタルアルデヒド固定液で約25分間、動物を灌流した。このステップの後、精巣を除去し、そしてそれぞれの精巣上体から分離して重量測定した。精巣重量及び体重から、各動物についての生殖腺指数(精巣重量と体重の間のパーセンテージ関係)を推定した。顕微鏡分析のために、約3mm以下の厚さの精巣断片を収集し、これを4%グルタルアルデヒドのバッファー中に2〜4時間、4℃で浸漬した。そして、断片を、それらが組織学的分析(アポトーシスの存在)のために処理されるまで、4℃のリン酸バッファー中に保存した。精巣のこれらの断片を、増加する濃度のアルコール(30分ごとに70°、80°、90°、100°に交換する)で脱水した。脱水後、断片をメタクリレートグリコール(Leica Historesin Embedding Kit, Leica Instruments)中に入れ、その後、ガラスカッターを備えたミクロトームで4μmの厚さに区分した。得られた切片を1%ホウ酸トルイジンブルーナトリウムで染色し、エンテラン(Merk)を載せ、そしてOlympus顕微鏡下で分析した。図17は、Mas G-タンパク質−結合受容体アンタゴニストであるA-779で処置された動物が、対照群に対して、横断面当たりのアポトーシスの数が多いが、生殖腺指数においては相違がなかったことを示す。
【0035】
実施例6
この実施例は、Mas-KOマウスの卵巣における形態学的変化を記載する。
【0036】
未成熟の雌性マウス(30日、11〜14g)WT(野生型;n=4)及びMas-KO(n=3)を断頭してと殺した。卵巣を除去し、PBS0.1m中、4%グルタルアルデヒド中で固定し、そしてグリコールメタクリレート中に入れた。5つの切片(5μm)ごとに、組織学用スライド上に集め、トルイジンブルーで染色した。増殖する胞状一次濾胞及び閉鎖一次濾胞の数を確定するために、形態学的分析を用いた。KOの卵巣は、WTの卵巣よりも、顕著に低い濾胞総数を示し(1494対3332)、始原濾胞においては特別であった(418対1930)。さらに、KO雌性マウスの閉鎖濾胞のパーセンテージは、WTマウスと比べると、約50%高かった。これらのデータは、Mas受容体の除去の結果としての卵巣のアポトーシス活性の増加を示唆する。
【0037】
実施例7
この実施例は、Mas受容体の存在がアポトーシス活性の調節に寄与しているかもしれない多数の組織におけるMas受容体の発現を、RT-PCRによって示す(図18)。
【特許請求の範囲】
【請求項1】
プロテインキナーゼB/Aktの活性の変更を含むアポトーシス活性の調節を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項2】
活性酸素種の産生の調節を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項3】
アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストの、病気の予防及び治療におけるアポトーシス活性の調節物質としての使用を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項4】
アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストの、老化により生じる器官の変化の予防又は治療において使用するためのアポトーシス活性の調節物質としての使用を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項5】
薬学的及び薬理学的に許容可能な賦形剤又は担体を含む、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの製剤の、アポトーシス活性の調節物質としての使用を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項6】
請求項1、2、3、4、5に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、少なくとも1つのさらなる薬理学的に活性な化合物及び/又は薬学的に許容可能な担体及び/又は賦形剤の使用を特徴とし、ここで、前記担体及び/又は賦形剤が、ポリエチレングリコール、非水性ビヒクル、ゴマ油、オレイン酸エチル、又はトリグリセリドなどの固定油、カルボキシメチルセルロースナトリウム、ソルビトール、又はデキストラン、チメロサール、m-若しくはo-クレゾール、ホルマリン及びベンジルアルコール、ヒト血清アルブミン、シクロデキストリン、リポソーム、環状若しくは非環状オリゴサッカライドを含有するか又は含有しない、水、食塩水溶液、緩衝液、リンゲル液、デキストロース溶液、Hank溶液、生物適合性食塩水溶液を含む、前記使用。
【請求項7】
請求項1、2、3、4、5、6に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの製剤の埋め込み型又は注射用のマイクロ−及びナノ粒子デバイスのアポトーシス活性調節物質としての使用を特徴とする、前記使用。
【請求項8】
請求項7に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、PLGA、PLA、PGA、カプロラクトン、これらのポリマーとリポソームの組み合わせなどの、生物分解性ポリマーの使用を特徴とする、前記使用。
【請求項9】
請求項1、2、3、4、5、6、7、8に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、悪液質、癌、AIDS、多数の因子によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性的使用並びに筋萎縮に導く様々な神経学的症候群、外傷及び変性疾患などの、筋萎縮における筋肉分化、成熟、及び、再生における変化を含む病気の予防及び治療、そして老化により生じる器官の変化の予防又は治療におけるアポトーシス活性の調節物質として、そしてエルゴジェニックな援助としての使用に特徴を有する、前記使用。
【請求項10】
請求項1、2、3、4、5、6、7、8に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、アンギオテンシン−(1−7)並びにその類似体、アゴニスト及びアンタゴニストに対応するペプチド配列をコードするcDNAの、病気及び老化により生じる器官の変化の遺伝子治療における使用のためのアポトーシス活性調節物質としての使用を特徴とする、前記使用。
【請求項11】
病気及び老化により生じる器官の変化の遺伝子治療における使用のための、請求項1、2、3、4、5、6、7、8に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストのアポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項12】
請求項1〜6に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、病気及び老化により生じる器官の変化の遺伝子治療における使用のための、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストのアポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項13】
Mas受容体の発現の減少並びにMas受容体アゴニストの血漿及び組織レベルの減少に関連する、循環器疾患及びその合併症、自己免疫疾患、アンギオテンシン変換酵素のDD型などの遺伝子多型の結果としての病気、心筋梗塞などの器官及び組織における虚血事象に関連した合併症、創傷、やけど、紅斑症、腫瘍、I型及びII型糖尿病並びにその合併症、男性の生殖系(精子形成、精子の運動性、勃起の機能不全)及び女性生殖系及び胚形成の障害、呼吸器疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス、及び血管形成後の再狭窄)、放射線治療後などの血液の急性発作の障害、記憶及び学習障害、並びに中枢及び末梢の変性ニューロパチーの研究、予防及び治療のための、そして温血動物における老化により生じる器官の変化の研究、予防又は治療のための、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、アポトーシス活性の調節物質としての使用を特徴とする、請求項8に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項14】
請求項2〜6に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、循環器疾患(高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全及び中枢神経系の病気などの、しかしこれらに限定されない、内皮の機能不全を結果として伴う病気の、活性酸素種の減少を含む、研究、予防及び治療における、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする、前記使用。
【請求項15】
循環器疾患(高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全)、腎臓病、多重メタボリック症候群、勃起不全及び中枢神経系の病気などを含むがこれらに限定されない、内皮の機能不全を結果として伴う病気の、活性酸素種の減少を含む、予防及び治療における、Mas Gタンパク質結合受容体アゴニスト及びアンタゴニストの使用であって、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アゴニスト及びアンタゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項16】
アンギオテンシン−(1−7)ペプチド、並びにその類似体、アゴニスト及びアンタゴニストを含む、請求項1、2、3、4、5に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、循環器疾患(全身性及び肺の高血圧、妊娠高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全、中枢神経系の病気、血管炎などの、活性酸素種の減少と結果としての内皮の機能不全の改善を含む遺伝子治療のための、アンギオテンシン−(1−7)並びにその類似体、アゴニスト及びアンタゴニストに対応するペプチド配列をコードするcDNAの使用を特徴とする、前記使用。
【請求項17】
Mas受容体の発現の減少並びにMas受容体アゴニストの血漿及び組織レベルの減少に関連する、循環器疾患及びその合併症、自己免疫疾患、アンギオテンシン変換酵素のDD型などの遺伝子多型の結果としての病気、心筋梗塞などの器官及び組織における虚血事象に関連した合併症、創傷、やけど、紅斑症、腫瘍、I型及びII型糖尿病及びそれらの合併症、男性の生殖系(精子形成、精子の運動性、勃起の機能不全)及び女性生殖系及び胚形成の障害、呼吸器疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後などの血液の急性発作の障害、記憶及び学習障害、並びに中枢及び末梢の変性ニューロパチーの予防及び治療のための、そして温血動物における老化により生じる器官の変化の研究、予防又は治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、アポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項18】
Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとして、Mas受容体の発現の減少並びにMas受容体アゴニストの血漿及び組織レベルの減少に関連する、循環器疾患及びその合併症、自己免疫疾患、アンギオテンシン変換酵素のDD型などの遺伝子多型の結果としての病気、器官及び組織における虚血事象に関連した合併症、創傷、やけど、紅斑症、腫瘍、I型及びII型糖尿病及びそれらの合併症、男性の生殖系(精子形成、精子の運動性、勃起の機能不全)及び女性生殖系及び胚形成の障害、呼吸器疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス、及び血管形成後の再狭窄)、放射線治療後などの血液の急性発作の障害、記憶及び学習障害、並びに中枢及び末梢の変性ニューロパチーの研究、予防及び治療のため、そして温血動物における老化により生じる器官の変化の研究、予防又は治療において使用される、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項19】
Mas受容体の発現の減少並びにMas受容体アゴニストの血漿及び組織レベルの減少に関連する、循環器疾患及びその合併症、自己免疫疾患、アンギオテンシン変換酵素のDD型などの遺伝子多型の結果としての病気、器官及び創傷を受けた組織における虚血事象に関連した合併症、やけど、紅斑症、腫瘍、I型及びII型糖尿病及びそれらの合併症、男性の生殖系(精子形成、精子の運動性、勃起の機能不全)及び女性生殖系及び胚形成の障害、呼吸器疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス、及び血管形成後の再狭窄)、放射線治療後などの血液の急性発作の障害、記憶及び学習障害、並びに中枢及び末梢の変性ニューロパチーの予防及び治療のための、そして温血動物における老化により生じる器官の変化の研究、予防又は治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする、前記使用。
【請求項20】
皮膚の損傷、創傷、火傷、紅斑症、腫瘍の研究、予防及び治療のため、器官移植、胚性又は非胚性幹細胞による治療、器官及び他の組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、生殖系の障害(精子形成、精子の運動性、勃起不全)、気管支疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後の血液の急性発作の障害、記憶及び学習障害の研究、予防及び治療のための、そして温血動物における老化により生じる器官の変化の予防又は治療における、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、アポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項21】
請求項1、2、3、4、5に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、皮膚の損傷、創傷、紅斑症、腫瘍の治療及びアポトーシス活性の一時的又は慢性的な低下を必要とする他の治療、並びに、生殖系の障害(精子形成、精子の運動性、勃起不全)、気管支疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後の血液の急性発作の障害、記憶及び学習障害の治療、そして温血動物における老化により生じる器官の変化の予防又は治療において使用されることを特徴とする、前記使用。
【請求項22】
請求項1、2、3、4、5、6に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、器官移植、胚性又は非胚性幹細胞による治療、器官及び組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、そして、温血動物における老化により生じる器官の変化の予防又は治療において使用されることを特徴とする、前記使用。
【請求項23】
器官移植、胚性又は非胚性幹細胞による治療、器官及び組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、そして、温血動物における老化により生じる器官の変化の予防又は治療における使用のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト、並びにその製剤の使用を特徴とする、前記使用。
【請求項24】
皮膚の損傷、創傷、火傷、紅斑症、腫瘍の研究、予防又は治療のため、器官移植、胚性又は非胚性幹細胞による治療、器官及び組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、生殖系の障害(精子形成、精子の運動性、勃起不全)、気管支疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後の血液の急性発作の障害、記憶及び学習障害、そして温血動物における老化により生じる器官の変化の予防又は治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、アポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項25】
Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、皮膚の損傷、創傷、火傷、紅斑症、腫瘍の研究、予防及び治療のため、器官移植、胚性又は非胚性幹細胞による治療、器官及び組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、生殖系の障害(精子形成、精子の運動性、勃起不全)、気管支疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後の血液の急性発作の障害、記憶及び学習障害の研究、予防及び治療のための、そして温血動物における老化により生じる器官の変化の予防又は治療のための、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト、並びにその製剤の使用を特徴とする、前記使用。
【請求項26】
Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、悪液質、癌、AIDS、多数の因子によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性的使用、並びに筋萎縮に導く様々な神経学的症候群、外傷及び変性疾患などの、筋萎縮における筋肉分化、成熟、及び、再生における変化を含む病気の研究、予防又は治療のため、そして老化により生じる器官の変化の予防又は治療のため、そしてエルゴジェニックな援助としての、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項27】
悪液質、癌、AIDS、多数の因子によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性的使用、並びに筋萎縮に導く様々な神経学的症候群、外傷及び変性疾患などの、筋萎縮における筋肉分化、成熟、及び、再生における変化を含む病気の予防及び治療のため、そして、老化により生じる器官の変化の予防又は治療のため、そして、エルゴジェニックな援助としての、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項28】
活性酸素種の減少と結果としての内皮の機能不全の改善を含む、循環器疾患(全身性及び肺の高血圧、妊娠高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全、中枢神経系の疾患、血管炎などの病気の予防及び治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする前記使用。
【請求項29】
Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、活性酸素種の減少と結果としての内皮の機能不全の改善を含む、循環器疾患(全身性及び肺の高血圧、妊娠高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全、中枢神経系の疾患、血管炎などの病気の研究、予防及び治療のための、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項30】
悪液質、癌、AIDS、多数の因子によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性的使用、並びに筋萎縮に導く様々な神経学的症候群、外傷及び変性疾患などの、筋肉分化、成熟、及び筋萎縮における再生における変化を含む病気の研究、予防又は治療のため、そして、老化により生じる器官の変化の予防又は治療のため、そして、エルゴジェニックな援助としての、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする、前記使用。
【請求項31】
活性酸素種の減少と結果としての内皮の機能不全の改善を含む、循環器疾患(全身性及び肺の高血圧、妊娠性高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全、中枢神経系の疾患、血管炎などの病気の研究、予防又は治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする、前記使用。
【請求項1】
プロテインキナーゼB/Aktの活性の変更を含むアポトーシス活性の調節を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項2】
活性酸素種の産生の調節を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項3】
アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストの、病気の予防及び治療におけるアポトーシス活性の調節物質としての使用を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項4】
アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストの、老化により生じる器官の変化の予防又は治療において使用するためのアポトーシス活性の調節物質としての使用を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項5】
薬学的及び薬理学的に許容可能な賦形剤又は担体を含む、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの製剤の、アポトーシス活性の調節物質としての使用を特徴とする、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項6】
請求項1、2、3、4、5に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、少なくとも1つのさらなる薬理学的に活性な化合物及び/又は薬学的に許容可能な担体及び/又は賦形剤の使用を特徴とし、ここで、前記担体及び/又は賦形剤が、ポリエチレングリコール、非水性ビヒクル、ゴマ油、オレイン酸エチル、又はトリグリセリドなどの固定油、カルボキシメチルセルロースナトリウム、ソルビトール、又はデキストラン、チメロサール、m-若しくはo-クレゾール、ホルマリン及びベンジルアルコール、ヒト血清アルブミン、シクロデキストリン、リポソーム、環状若しくは非環状オリゴサッカライドを含有するか又は含有しない、水、食塩水溶液、緩衝液、リンゲル液、デキストロース溶液、Hank溶液、生物適合性食塩水溶液を含む、前記使用。
【請求項7】
請求項1、2、3、4、5、6に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの製剤の埋め込み型又は注射用のマイクロ−及びナノ粒子デバイスのアポトーシス活性調節物質としての使用を特徴とする、前記使用。
【請求項8】
請求項7に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、PLGA、PLA、PGA、カプロラクトン、これらのポリマーとリポソームの組み合わせなどの、生物分解性ポリマーの使用を特徴とする、前記使用。
【請求項9】
請求項1、2、3、4、5、6、7、8に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、悪液質、癌、AIDS、多数の因子によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性的使用並びに筋萎縮に導く様々な神経学的症候群、外傷及び変性疾患などの、筋萎縮における筋肉分化、成熟、及び、再生における変化を含む病気の予防及び治療、そして老化により生じる器官の変化の予防又は治療におけるアポトーシス活性の調節物質として、そしてエルゴジェニックな援助としての使用に特徴を有する、前記使用。
【請求項10】
請求項1、2、3、4、5、6、7、8に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、アンギオテンシン−(1−7)並びにその類似体、アゴニスト及びアンタゴニストに対応するペプチド配列をコードするcDNAの、病気及び老化により生じる器官の変化の遺伝子治療における使用のためのアポトーシス活性調節物質としての使用を特徴とする、前記使用。
【請求項11】
病気及び老化により生じる器官の変化の遺伝子治療における使用のための、請求項1、2、3、4、5、6、7、8に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストのアポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項12】
請求項1〜6に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、病気及び老化により生じる器官の変化の遺伝子治療における使用のための、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストのアポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項13】
Mas受容体の発現の減少並びにMas受容体アゴニストの血漿及び組織レベルの減少に関連する、循環器疾患及びその合併症、自己免疫疾患、アンギオテンシン変換酵素のDD型などの遺伝子多型の結果としての病気、心筋梗塞などの器官及び組織における虚血事象に関連した合併症、創傷、やけど、紅斑症、腫瘍、I型及びII型糖尿病並びにその合併症、男性の生殖系(精子形成、精子の運動性、勃起の機能不全)及び女性生殖系及び胚形成の障害、呼吸器疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス、及び血管形成後の再狭窄)、放射線治療後などの血液の急性発作の障害、記憶及び学習障害、並びに中枢及び末梢の変性ニューロパチーの研究、予防及び治療のための、そして温血動物における老化により生じる器官の変化の研究、予防又は治療のための、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、アポトーシス活性の調節物質としての使用を特徴とする、請求項8に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用。
【請求項14】
請求項2〜6に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、循環器疾患(高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全及び中枢神経系の病気などの、しかしこれらに限定されない、内皮の機能不全を結果として伴う病気の、活性酸素種の減少を含む、研究、予防及び治療における、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする、前記使用。
【請求項15】
循環器疾患(高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全)、腎臓病、多重メタボリック症候群、勃起不全及び中枢神経系の病気などを含むがこれらに限定されない、内皮の機能不全を結果として伴う病気の、活性酸素種の減少を含む、予防及び治療における、Mas Gタンパク質結合受容体アゴニスト及びアンタゴニストの使用であって、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アゴニスト及びアンタゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項16】
アンギオテンシン−(1−7)ペプチド、並びにその類似体、アゴニスト及びアンタゴニストを含む、請求項1、2、3、4、5に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、循環器疾患(全身性及び肺の高血圧、妊娠高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全、中枢神経系の病気、血管炎などの、活性酸素種の減少と結果としての内皮の機能不全の改善を含む遺伝子治療のための、アンギオテンシン−(1−7)並びにその類似体、アゴニスト及びアンタゴニストに対応するペプチド配列をコードするcDNAの使用を特徴とする、前記使用。
【請求項17】
Mas受容体の発現の減少並びにMas受容体アゴニストの血漿及び組織レベルの減少に関連する、循環器疾患及びその合併症、自己免疫疾患、アンギオテンシン変換酵素のDD型などの遺伝子多型の結果としての病気、心筋梗塞などの器官及び組織における虚血事象に関連した合併症、創傷、やけど、紅斑症、腫瘍、I型及びII型糖尿病及びそれらの合併症、男性の生殖系(精子形成、精子の運動性、勃起の機能不全)及び女性生殖系及び胚形成の障害、呼吸器疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後などの血液の急性発作の障害、記憶及び学習障害、並びに中枢及び末梢の変性ニューロパチーの予防及び治療のための、そして温血動物における老化により生じる器官の変化の研究、予防又は治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、アポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項18】
Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとして、Mas受容体の発現の減少並びにMas受容体アゴニストの血漿及び組織レベルの減少に関連する、循環器疾患及びその合併症、自己免疫疾患、アンギオテンシン変換酵素のDD型などの遺伝子多型の結果としての病気、器官及び組織における虚血事象に関連した合併症、創傷、やけど、紅斑症、腫瘍、I型及びII型糖尿病及びそれらの合併症、男性の生殖系(精子形成、精子の運動性、勃起の機能不全)及び女性生殖系及び胚形成の障害、呼吸器疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス、及び血管形成後の再狭窄)、放射線治療後などの血液の急性発作の障害、記憶及び学習障害、並びに中枢及び末梢の変性ニューロパチーの研究、予防及び治療のため、そして温血動物における老化により生じる器官の変化の研究、予防又は治療において使用される、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項19】
Mas受容体の発現の減少並びにMas受容体アゴニストの血漿及び組織レベルの減少に関連する、循環器疾患及びその合併症、自己免疫疾患、アンギオテンシン変換酵素のDD型などの遺伝子多型の結果としての病気、器官及び創傷を受けた組織における虚血事象に関連した合併症、やけど、紅斑症、腫瘍、I型及びII型糖尿病及びそれらの合併症、男性の生殖系(精子形成、精子の運動性、勃起の機能不全)及び女性生殖系及び胚形成の障害、呼吸器疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス、及び血管形成後の再狭窄)、放射線治療後などの血液の急性発作の障害、記憶及び学習障害、並びに中枢及び末梢の変性ニューロパチーの予防及び治療のための、そして温血動物における老化により生じる器官の変化の研究、予防又は治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする、前記使用。
【請求項20】
皮膚の損傷、創傷、火傷、紅斑症、腫瘍の研究、予防及び治療のため、器官移植、胚性又は非胚性幹細胞による治療、器官及び他の組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、生殖系の障害(精子形成、精子の運動性、勃起不全)、気管支疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後の血液の急性発作の障害、記憶及び学習障害の研究、予防及び治療のための、そして温血動物における老化により生じる器官の変化の予防又は治療における、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、アポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項21】
請求項1、2、3、4、5に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、皮膚の損傷、創傷、紅斑症、腫瘍の治療及びアポトーシス活性の一時的又は慢性的な低下を必要とする他の治療、並びに、生殖系の障害(精子形成、精子の運動性、勃起不全)、気管支疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後の血液の急性発作の障害、記憶及び学習障害の治療、そして温血動物における老化により生じる器官の変化の予防又は治療において使用されることを特徴とする、前記使用。
【請求項22】
請求項1、2、3、4、5、6に記載のMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、器官移植、胚性又は非胚性幹細胞による治療、器官及び組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、そして、温血動物における老化により生じる器官の変化の予防又は治療において使用されることを特徴とする、前記使用。
【請求項23】
器官移植、胚性又は非胚性幹細胞による治療、器官及び組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、そして、温血動物における老化により生じる器官の変化の予防又は治療における使用のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト、並びにその製剤の使用を特徴とする、前記使用。
【請求項24】
皮膚の損傷、創傷、火傷、紅斑症、腫瘍の研究、予防又は治療のため、器官移植、胚性又は非胚性幹細胞による治療、器官及び組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、生殖系の障害(精子形成、精子の運動性、勃起不全)、気管支疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後の血液の急性発作の障害、記憶及び学習障害、そして温血動物における老化により生じる器官の変化の予防又は治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの、アポトーシス活性の調節物質としての使用を特徴とする、前記使用。
【請求項25】
Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、皮膚の損傷、創傷、火傷、紅斑症、腫瘍の研究、予防及び治療のため、器官移植、胚性又は非胚性幹細胞による治療、器官及び組織の再移植、並びに、アポトーシス活性の一時的又は慢性的な低下を必要とする他の治療のための補助的処置として、生殖系の障害(精子形成、精子の運動性、勃起不全)、気管支疾患、腎障害、胃腸障害、婦人科の障害、血管新生、脱毛症、血液疾患及び血管形成(腔内プロステーシス及び血管形成後の再狭窄)、放射線治療後の血液の急性発作の障害、記憶及び学習障害の研究、予防及び治療のための、そして温血動物における老化により生じる器官の変化の予防又は治療のための、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト、並びにその製剤の使用を特徴とする、前記使用。
【請求項26】
Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、悪液質、癌、AIDS、多数の因子によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性的使用、並びに筋萎縮に導く様々な神経学的症候群、外傷及び変性疾患などの、筋萎縮における筋肉分化、成熟、及び、再生における変化を含む病気の研究、予防又は治療のため、そして老化により生じる器官の変化の予防又は治療のため、そしてエルゴジェニックな援助としての、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項27】
悪液質、癌、AIDS、多数の因子によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性的使用、並びに筋萎縮に導く様々な神経学的症候群、外傷及び変性疾患などの、筋萎縮における筋肉分化、成熟、及び、再生における変化を含む病気の予防及び治療のため、そして、老化により生じる器官の変化の予防又は治療のため、そして、エルゴジェニックな援助としての、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項28】
活性酸素種の減少と結果としての内皮の機能不全の改善を含む、循環器疾患(全身性及び肺の高血圧、妊娠高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全、中枢神経系の疾患、血管炎などの病気の予防及び治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする前記使用。
【請求項29】
Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、活性酸素種の減少と結果としての内皮の機能不全の改善を含む、循環器疾患(全身性及び肺の高血圧、妊娠高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全、中枢神経系の疾患、血管炎などの病気の研究、予防及び治療のための、経口、筋肉内、静脈内、皮下、局所、経皮、肛門、吸入(肺内、鼻腔内、頬側)投与経路のいずれかによるか又は埋め込まれるか若しくは注射されてよいデバイスとしての、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニスト並びにその製剤の使用を特徴とする、前記使用。
【請求項30】
悪液質、癌、AIDS、多数の因子によるベッドへの長期の拘束、糖尿病、コルチコイドの慢性的使用、並びに筋萎縮に導く様々な神経学的症候群、外傷及び変性疾患などの、筋肉分化、成熟、及び筋萎縮における再生における変化を含む病気の研究、予防又は治療のため、そして、老化により生じる器官の変化の予防又は治療のため、そして、エルゴジェニックな援助としての、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする、前記使用。
【請求項31】
活性酸素種の減少と結果としての内皮の機能不全の改善を含む、循環器疾患(全身性及び肺の高血圧、妊娠性高血圧、アテローム性動脈硬化、血栓症、心筋梗塞、心不全など)、腎臓病、多重メタボリック症候群、勃起不全、中枢神経系の疾患、血管炎などの病気の研究、予防又は治療のための、Mas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用であって、薬学的又は薬理学的に許容可能な賦形剤又は担体とともに製剤された、アンギオテンシン−(1−7)ペプチド、並びにペプチド又は非ペプチドである、その類似体、アゴニスト及びアンタゴニストを含むMas Gタンパク質結合受容体アンタゴニスト及びアゴニストの使用を特徴とする、前記使用。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【公開番号】特開2013−75911(P2013−75911A)
【公開日】平成25年4月25日(2013.4.25)
【国際特許分類】
【外国語出願】
【出願番号】特願2013−248(P2013−248)
【出願日】平成25年1月4日(2013.1.4)
【分割の表示】特願2008−518575(P2008−518575)の分割
【原出願日】平成18年6月28日(2006.6.28)
【出願人】(508000652)ウニベルシダーヂ フェデラル ヂ ミナス ジェライス (2)
【Fターム(参考)】
【公開日】平成25年4月25日(2013.4.25)
【国際特許分類】
【出願番号】特願2013−248(P2013−248)
【出願日】平成25年1月4日(2013.1.4)
【分割の表示】特願2008−518575(P2008−518575)の分割
【原出願日】平成18年6月28日(2006.6.28)
【出願人】(508000652)ウニベルシダーヂ フェデラル ヂ ミナス ジェライス (2)
【Fターム(参考)】
[ Back to top ]

