瘢痕治療用シリコーン製剤
1)シロキサンマトリクス形成の製剤中の有用な活性の溶解度を増進させる方法と、2)その製剤に関することを開示する。揮発助剤は、シロキサンに不溶の添加剤を含有する、新規なゲルを提供するために利用される。
【発明の詳細な説明】
【技術分野】
【0001】
[関連出願の参照]
本出願は、2009年6月18日出願、米国特許出願第12/487,498号の優先権を主張する。
【背景技術】
【0002】
皮膚の完全性を損なう裂傷及びその他の創傷は、ほとんどの人が経験したことがあるありふれたものであり、擦りむいた膝といった日常的なものから、刺し傷又は重度の火傷といった命にかかわるものまである。多くの皮膚の破損は、瘢痕を経て美観を損なう可能性がある。
【0003】
瘢痕組織の発生は、損傷に対する防御反応であり、皮膚の破損箇所を修復し、潜在的な感染及び再損傷部位を除去する。しかし、瘢痕組織の過剰な形成は、周囲の皮膚の色素又は粘稠性を欠く、固い真皮表面を生じさせることがある。普通の皮膚とは異なる瘢痕組織の柔軟性と弾力性のため、瘢痕組織は、傷を受けた者の生活を最終的に制限することがある。瘢痕組織は、一般的に周辺の皮膚組織より丈夫である。このことは、膝又は肘の上あるいは後ろなど、皮膚が変形応力と弾性応力にさらされる瘢痕組織に特に当てはまる。このような場所は、皮膚/瘢痕組織の境界で、裂傷を受ける可能性がある。掌線などの曲げることを容易にする生来の溝を有する場所を覆う瘢痕組織、特に新しい瘢痕組織は、多くの場合これらの屈曲する線においては弱い。手を開いたり閉じたりすることで生じる伸縮が、これらの生来の溝で瘢痕組織を破裂させることがあり、溝の両側に瘢痕組織の蓄積をもたらし、手を動かしただけで裂けてしまう、更に高い脆弱性を有する組織を、溝の中に新たに形成させる要因になる。一般的に、創傷部位の生来の組織分布が、再裂傷の可能性を高めて、治癒時間を長引かせることになる。
【0004】
瘢痕が、分厚く、硬く、及び非弾性になるにつれて、形成の間及び後に瘢痕化した部位が自然に収縮するので、瘢痕組織の柔軟性と弾力性が更に失われてしまう。結果として、火傷の犠牲者など広範囲の皮膚損傷を負った者の動作は、かなり制限されることがある。重篤な火傷を負った手は、握りしめたまま動かせなくなることがある。火傷による腰周辺の瘢痕組織は、多くの人が当たり前だと思うねじれ運動を妨げることがある。
【0005】
創傷を治療するいくつかの製剤が処方され、治癒する間に形成される瘢痕組織の特性に良い効果を与えている。例えば、いくつかの創傷ドレッシングは、創傷の乾燥を減少させる若しくは紫外線暴露を防止するといった機能を有する。このような調合物は、度重なる亀裂と乾燥を防ぐことができ、その結果、とりわけ、この調合物を欠いて形成された瘢痕組織と比べて、改善された柔軟性、弾力性、及び色特性を有する瘢痕組織が形成される。
【0006】
いくつかの調合物は、ゲルなど、厳密に言えば有機物質で作られている。ゲルは、創傷ドレッシングとして適する特性を有する。ゲルは、創傷に直接接触させて冷やすことができ、更に創傷が汚染を受けない状態にしておくことができる。ゲルのその他の有用な特性は、その粘稠度である:多くのゲルは、弾力性や変形能が、皮膚と類似しているので、皮膚及び組織表面に付着したゲルは、治癒創傷の部位で裂けることなく又は応力を生じさせることなく、皮膚及び組織表面と共に曲がり、まとまり、及び伸縮することができる。
【0007】
しかし、ゲルは、時間がたつと急速に乾燥し、構造的に及び/又は化学的に崩壊するので、通常ゲルを再度塗布しなければならない。このことは、特に乾燥によりドレッシングの粘稠度が固くなった場合は、患者にとって痛みを伴うプロセスになることがある。いくかのゲルは、水分を吸収して柔らかな又は液体の粘稠度になる。ゲルの粘稠度が損なわれると、バクテリア感染の可能性が高まる。
【0008】
一般的に、シロキサンゲルは、他のゲル製品より創傷組織と瘢痕組織の治療において優れていることが、わかっている。シロキサンゲルは、創傷部位の上にシリコーンベースのポリママトリクスを形成することにより機能する。例えば、ジメチコン、ジメチコンクロスポリマ、及びその他のシロキサン誘導体といったポリマ前駆体は、創傷部位に塗布される塗り広げることができる製剤に含有されている。いくつかのポリマ前駆体の調合物は、ヒュームドシリカを含む。この製剤は、創傷部位へ製剤を塗布すると蒸発し始める揮発性成分も含む。この塗り広げることができる製剤から揮発性化合物が蒸発すると、ポリママトリクスが形成を始める。多くの場合、特に、この調合物がヒュームドシリカを含む場合は、この製剤はチキソトロピックである。チキソトロピックの調合物は、創傷への塗布など応力がかかると、固い粘稠度から噛みタバコのような粘稠度に変化し、応力がなくなると、流動性の少ない固さに戻る。この特性によって、シロキサンゲル前駆体の調合物は、創傷を覆う比較的薄い層に容易に広がり、この創傷部位で最小の応力とずれで、この創傷部位から流れ出ることなく場所に留まることができる。
【0009】
シロキサンゲルの他の利点は、いくつかのゲルが瘢痕の形成時に、瘢痕組織の特性に対する有益な効果を有することを示したものであり、瘢痕の度合いを減少させて、瘢痕組織の質感を改善し、治癒した創傷の最終的な外見が、より周囲の皮膚に類似することである。例えば、いくつかのシロキサン製剤は、成長中の又は新しく形成される瘢痕組織に塗布すると、瘢痕を見事に消して、持続的に塗布することにより、ほとんど消滅させる能力があることが証明されている。
【0010】
創傷の治癒を補助する、市場に出ている他の塗り広げることができる製剤とは違い、ある程度の重合が起きてシロキサンポリママトリクスを形成すると、結果として得られたゲルは、一般的に、長時間にわたりその粘稠度を保持する能力を有する。その上、塗布されない製品は、塗布されるまで「硬化」しないシロキサンポリママトリクス前駆体として適用することができるので、他のタイプのゲルよりも保管し易く、使い易い。
【0011】
シロキサンゲルは、成長中の瘢痕組織に対してこのような有益な効果を有するので、このような製剤は、ゲルに更なる有用な機能を与える添加剤を包含する能力も有することが望ましい。例えば、上述のシリコーンベースの調合物は、瘢痕を減少させる優れた特性を示すが、成長中の瘢痕組織は、紫外線及びその他の波長の放射線にさらされると、色及び/又は質感の変化、並びに熱損傷といった他のタイプの損傷の影響を受け易い。マトリクス形成時に保持される調合物に、日焼け止め作用のある化合物を組み込むことが望ましい。また、ゲルの局所塗布により最適に手当てされた火傷及びその他の損傷は、創傷が瘢痕になり始めてもなお、非常な痛みを伴うことがある。しかし、マトリクス形成製剤の塗布は、鎮痛剤の局所塗布を妨げることがある大部分の包帯タイプの被覆剤とは違って、局所ゲルは簡単にはずしたり再度置いたりできない。したがって、マトリクス形成製剤は、少なくとも一の疼痛緩和化合物を含むことが望ましい。
【0012】
残念なことに、シロキサンマトリクス前駆体の使用は、シリコーン創傷ドレッシングに含まれ得るさまざまな添加剤を、大幅に制限してきた。多くの望ましい添加剤は、塗り広げることができる製剤を含むジメチコンとその他のシロキサン誘導体といったマトリクス前駆体の混合物中に容易に溶媒和されない。例えば、オクトクリレン、オクチノキサート、オクチサレート、及びオキシベンゾンといった、多くの効果的で一般的に用いられる日焼け止め添加剤は、予め重合された製剤中に十分に溶解しないことがある。予め重合された製剤中の溶解度が低い、望ましい添加剤の他の例は、例えば、酢酸ヒドロコルチゾンなど疼痛や炎症を減少させる、コルチドンタイプの化合物を含む。
【0013】
シロキサンマトリクスを形成する創傷製剤の利点を生かし、更に、シリコーン創傷ドレッシング調合物中に不溶性添加剤を包含させる方法は、創傷ドレッシング製剤の技術の大幅な進歩として歓迎されるであろう。
【発明の概要】
【0014】
驚くべきことに、制限されている又はマトリクス前駆体中に不溶である、所定の活性を有する所定の揮発性助剤を(揮発性成分に加えて)使用すると、シリコーンマトリクスへこの活性を取り込むことができることを見出した。更に驚くべきことに、成形マトリクスへこの活性を組み込むことを可能にするこの複合体は、この活性と複合されるにもかかわらず、かつ成長中のマトリクスが、この複合助剤が蒸発する能力を妨げることが予想されるにもかかわらず、優れた揮発性を実際に維持する。驚くべきことに、この揮発性助剤は、この活性を有するマトリクス内に取り込まれない。代わりに、助剤なしではマトリクス前駆体中に溶けない不溶性活性は、揮発性助剤がこの活性に複合されたままでなく、分離し、蒸発して失われるにもかかわらず、マトリクス形成中にマトリクス内に取り込まれたままである。更に驚くべきことに、鎮痛添加剤の効果から明らかなように、この活性は、マトリクス内で移動性を有し、ゲルを通って創傷部位に移動する能力をもたらす。更に、揮発性助剤の蒸気圧は、活性と複合すると、及び成長中のシロキサンマトリクス内に活性とともに取り込まれることによって減少することが予想される。また、十分な蒸気圧を維持しており、きれいに蒸発する。ここに特定されるような揮発性助剤を使用すると、シリコーンマトリクス形成の調合物に、さまざまな添加剤のタイプを組み込むことができる。本発明は、シリコン前駆体混合物への不溶性活性の取り込みを可能にして、シロキサンゲルの創傷治癒技術の有用性を大幅に拡げる。
【図面の簡単な説明】
【0015】
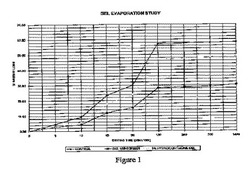
【図1】図1は、乾燥試験の結果である。一番下、真ん中、及び一番上の曲線は、日焼け止め剤含有のゲル、鎮痛剤含有のゲル、及びコントロールのゲルの乾燥結果を、それぞれグラフを使って示したものである。
【発明を実施するための形態】
【0016】
[シロキサンマトリクス前駆体]
本発明のマトリクス形成組成物は、シロキサンマトリクス前駆体、揮発性成分、活性成分、及び揮発性助剤を含む。この組成物を創傷又は瘢痕部位に適用すると、揮発性成分及び揮発性助剤は、1)マトリクス形成に関与する成分、並びに2)マトリクスに存在する一又はそれ以上の活性成分を残して、この組成物から部分的に又は完全に蒸発する。一般的に、マトリクス形成に関与する成分は、一又はそれ以上のシロキサンを有し、一又はそれ以上のシロキサンは、環状ヒドロカルビル基などの有機成分を含有するといった有機特性を有する。ジメチコン及びジメチコンクロスポリマといったポリジメチルシロキサンが好ましい。ジメチコンやジメチコンクロスポリマの代わりに又はこれらに加えて、他のポリジメチルシロキサンを用いてポリママトリクスを形成してもよい。他のポリシロキサンや他のジアルキルポリシロキサンを含む重合反応は特に、以下に挙げる揮発性成分、揮発性助剤、及び活性と共に用いるときに、本発明の利点を示すマトリクスを形成することができると考えられている。このようなマトリクスは、本発明の範囲内である。ヒュームドシリカは、予め重合された組成物に、チキソトロピックな粘稠性を与える。ヒュームドシリカは、ゲルの構造にも関与するが、重合プロセスにおけるヒュームドシリカの貢献又は関与は、たとえあったとしても明らかではない。揮発性成分を有する場合は、一般的に製剤中のマトリクス前駆体は、例えば、1、2、4、6、12ヶ月又はそれ以上の長期間、顕著な重合を受けることなく、室温(25K)で保管可能である。マトリクス前駆体は、ジメチコンクロスオポリマ、並びにジメチコンといったクロスポロマ成分を含むことが好ましい。いくつかの実施態様では、シロキサン成分が、約25乃至60重量%の重量パーセントの範囲で存在する。好ましい実施態様では、シロキサン成分は、30乃至50重量%の範囲で存在する。より好ましい実施態様では、シロキサン成分は、約35乃至45重量%の範囲の量で存在する。シロキサン成分は、ジメチコンが好ましい。 クロスポリマ成分は、約0.5乃至8重量%の範囲の量で存在するのが好ましく、約1.5乃至5重量%の範囲で存在するのがより好ましい。
【0017】
[揮発性成分]
本発明の組成物は、(以下に述べる揮発性助剤と区別される)揮発性成分を含む。一般的に、揮発性成分は、組成物を創傷部位に塗布すると蒸発を始める。いくつかの実施態様では、蒸発が始まるとシロキサンマトリクスの形成は直ちに始まり、蒸発は更に進行する。他の実施態様では、揮発性成分が蒸発する間のある時期には、シロキサンマトリクスは、かなり形成し始めるが、その時期より前には、ほんの少ししか形成しない。好ましい実施態様では、揮発性成分の重合への関与は、制限されているかまったくないが、マトリクス前駆体中に容易に溶媒和又は溶解する。好ましい例は、シロキサン重合における反応物としてほとんど又は全く関与しない揮発性シロキサン化合物である。例えば、環状シクロヘキサンは、一般的に、シクロヘキサン中に高い溶媒和と揮発性特性を示し、全てのシラン酸素原子が重合に利用できない事実により、一般的に、マトリクス形成における環状シクロヘキサンの関与は比較的低い。水素又は4未満の炭素原子のヒドロカルビル基を含む構成物質を有する、シクロペンタシロキサンがより好ましい。水素又は1の炭素原子のヒドロカルビル基を含む構成物質が最も好ましい。約12乃至45重量%の範囲の揮発性成分の量が好ましい。約15乃至28重量%の範囲の量がより好ましく、約20乃至25重量%の範囲の量が最も好ましい。
【0018】
揮発性成分は、約30乃至40℃の範囲の一又はそれ以上の温度で15分後に、揮発成分の50パーセント超が蒸発されるような量で存在することが好ましい。
【0019】
一般的に、この揮発性成分は、その一部又は全体が蒸発すると、ポリママトリクスが形成を始めるように機能する。従って、いくつかの実施態様では、揮発性物質の存在は、揮発を開始すると重合速度が上がるように作用し、重合プロセスを完全に又は部分的に阻害することがある。一般的に、本発明の組成は、上記の化合物に特に限定されるものではなく、創傷に塗布する前はシロキサンマトリクスの形成を完全に又は部分的に阻害するが、創傷に製剤を塗布すると蒸発し始め、シロキサンマトリクス形成の完了によって完全に又は部分的に蒸発されるような相対量で使用され得る化合物を広く含む。いくつかの実施態様では、揮発性成分の蒸発は、完全な蒸発の前に経時的に停滞する。他の実施態様では、揮発性成分の蒸発は、シロキサンマトリクスが完全に形成された後も継続する。揮発性成分の蒸発は、3時間以内で原重量(保管の濃度)の5%未満が好ましいが、いくつかの実施態様では、揮発成分の蒸発は、3時間以内で原重量の10、20、及び30%を超える範囲内である。いくつかの実施態様では、使用前及び保管中の揮発性成分濃度の重量パーセントは、約5乃至約40%の範囲である。別の実施態様では、使用前及び保管中の揮発性成分濃度の重量パーセントは、約15乃至約35%の範囲である。好ましい実施態様では、使用前及び保管中の揮発性成分濃度は、約18乃至約30%の範囲である。
【0020】
[活性剤及び揮発性助剤]
本発明の創傷治癒の製剤は、揮発性助剤を含有する。理論に拘束されるのを望むものではないが、揮発性助剤は、マトリクス前駆体中に活性を溶媒和するのを補助すると考えられている。特定の活性を具える揮発性助剤として機能する特定の化合物は、成長中のマトリクスに取り囲まれ、それ自身は最終的には揮発されない活性と化学的に関連があるという事実にもかかわらず、かなり揮発させる能力を有することが見出されてきた。
【0021】
一般的な紫外線吸収剤は、シロキサンマトリクス前駆体を含む溶液中に容易に溶解しない。しかし、多くの紫外線吸収剤は、ミリスチン酸エステルが存在するシロキサンマトリクス前駆体溶液中に溶媒和することがある。例えば、以下のさまざまな化学構造を有するエスカロール紫外線吸収剤は、シロキサンマトリクスに導入されることができる。

【0022】
一実施態様では、活性は、少なくとも一の芳香環を含む紫外線吸収化合物である。より好ましい実施態様では、この活性は、ISPケミカルから入手可能な一又はそれ以上のエスカロール化合物であり、この揮発性助剤は、1)約6乃至13の炭素原子の炭素鎖長を有する直鎖酸と、2)メタノール、エタノール、又は約3乃至約8の炭素原子の全炭素含有量を有する第二アルコールと、のエステルである。より好ましい実施態様では、揮発性助剤は、メタノール、エタノール、又は約3乃至約8の炭素原子の全炭素含有量を有する第二アルコールからのミリスチン酸エステルであり、活性は、エスカロール化合物である。更に好ましい実施態様では、揮発性助剤は、ミリスチン酸イソプロピルであり、活性は、オクトクリレン(ISPエスカロール597)、オクチノキサート(ISPエスカロール557)、オクチサレート(ISPエスカロール587)、又はオキシベンゾン(ISPエスカロール567)である。調合物中の日焼け止め活性は、約5乃至40重量%の範囲の総計量で存在するが、約15乃至35重量%の範囲の量がより好ましい。いくつかの実施態様では、日焼け止め活性は、約25乃至30重量%の範囲の量で存在する。
【0023】
一般に、揮発性剤は、1)約6乃至13の炭素原子の炭素鎖を有する直鎖酸と2)メタノール、エタノール、又は約3乃至約8の炭素原子の全炭素含有量を有する第二アルコールとのエステルであり、より好ましくは、ミリスチン酸イソプロピル;3又はそれ以上の炭素の直鎖及び一又はそれ以上のヒドロキシル基を具えるグリコールであり;全てのヒドロキシル基は、終末炭素を含む炭素に隣接し;ペンチレングリコールがより好ましく;又は置換若しくは非置換イソソルビド;及びジメチルイソソルビドが好ましい。
【0024】
一般の抗炎症化合物の多くは、ステロイド化合物構造に基づいている。シロキサンマトリクス前駆体の溶液中に難溶解性を有するいくつかのステロイドは、グリコール及び/又はイソソルビド化合物が存在するシロキサンマトリクス前駆体溶液中に溶媒和され得ることが見出されてきた。
【0025】
一実施態様では、活性は、ステロイド化合物であり、揮発性助剤は、3又はそれ以上の炭素の直鎖と、一又はそれ以上のヒドロキシル基とを含むグリコールであり、全てのヒドロキシル基は、終末炭素を含む隣接する炭素に上にある。より好ましい実施態様では、揮発性助剤は、3乃至7の炭素の直鎖と、一つが末端炭素に結合された2つのヒドロキシル基とを具えるグリコールであり、その活性は、ステロイド化合物である。更に好ましい実施態様では、揮発性助剤は、ペンチレングリコールであり、その活性は、酢酸ジヒドロコルチゾンである。
【0026】
一実施態様では、活性は、ステロイド化合物であり、揮発性助剤は、置換又は非置換イソソルビドを含む。更に好ましい実施態様では、活性は、コルチゾンであり、揮発性助剤は、二置換イソソルビドを含む。更に好ましい実施態様では、揮発性助剤は、ジメチルイソソルビドであり、その活性は、酢酸ジヒドロコルチゾンである。
【0027】
一実施態様では、活性は、ヒドロコルチゾン化合物であり、グリコール化合物とイソソルビド化合物との両方を含む活性を用いる。好ましい化合物においては、その活性は、酢酸ヒドロコルチゾンである。
【0028】
ステロイド化合物は、0.1乃至8重量%の範囲の量で存在するのが好ましい。約0.5乃至3重量%の範囲の量が、更に好ましい。
【0029】
グリコール及びイソソルビドは、5乃至40重量%のパーセントの範囲(両方存在する場合は総合重量)の量で存在する。好ましい実施態様では、双方それぞれ5乃至50重量%の範囲の量で存在する。別の実施態様では、グリコールとイソソルビドは、10乃至25重量%の範囲で存在し、0乃至15合計重量%となる。
【0030】
より深い浸透が要求される場合は、ミリスチン酸イソプロピルの代わり、日焼け止め活性とともにグリコール及びイソソルビド成分を用いてもよいことに留意すべきである。
【0031】
本発明の組成物は、例えば、ヒュームドシリカ、ジメチコン、及びジメチコンクロスポリマといったマトリクス前駆体と、例えば、シクロペンタシロキサンといった揮発性成分とを互いに混合することにより調製してもよい。前述の化合物を、互いに混合し、シロキサンのベースを形成させた。一般的に、活性成分は、揮発性助剤と混合されて混合物を形成するが、この混合物は、組成物のバランスにそれを導入する前にシロキサンのベースに添加される。一実施態様では、このベースは、シクロペンタシロキサン及びジメチコンクロスポリマのみを含有する。次いで、混合物をベースと混ぜ合わせる。一般的に、活性と揮発性助剤とを予め混合するのが望ましい。しかし、いくつかのケースでは、揮発性助剤と活性以外の全ての成分とを組み合わせ、活性を最終ステップにおいて製剤に添加してもよい。
【実施例1】
【0032】
[30SPFの日焼け止め含有の瘢痕用ゲル]
瘢痕用ゲルは、10.0%のオクトクリレン、7.5%のオクチノキサート、5.0%のオクチサレート、6.0%のオキシベンゾン、8.0%のミリスチン酸イソプロピル、36%のジメチコン、3.5%ヒュームドシリカ、2%のジメチコンクロスポリマ、及び22%のシクロペンタシロキサンを含む。全てのパーセンテージは重量/重量である。オクトクリレン、オクチノキサート、オクチサレート、オキシベンゾンは、UVA及びUVB抵抗を提供する。これらを、ミリスチン酸イソプロピルと予め混合した。シクロペンタシロキサンとジメチコンクロスポリマを混ぜ合わせたものに、この混合物を添加した。次に高せん断混合プロセス(排出装置)を用いて、ヒュームドシリカを混合物全体に添加した。最後にジメチコンを添加して、均質になるまで混合物を混合しダマや目に見える分離がない粘性のある不透明のゲルを得た。調合物は、30又はそれ以上のSPF評価を有する。乾燥試験(一定重量に到達するのにかかる時間)(図1を参照されたい)を行ったところ、この調合物は、オクトクリレン、オクチノキサート、オクチサレート、オキシベンゾン、及びミリスチン酸イソプロピル(コントロールの調合物)のない調合物と、本質的に同じ時間で乾燥した。日焼け止め添加剤を添加しても、調合物の乾燥は、感知できるほどには遅くならない。
【実施例2】
【0033】
[酢酸ヒドロコルチゾン含有の瘢痕用ゲル]
瘢痕用ゲルは、1.0%の酢酸ヒドロコルチゾン、5.0%のプロピレングリコール、8.0%のジメチルイソソルビド、12.0%のペンチレングリコール、45.0%のジメチコン、3.0%のヒュームドシリカ、2.0%のジメチコンクロスポリマ、及び24.0%のシクロペンタシロキサンを含む。全てのパーセンテージは、重量/重量である。酢酸ヒドロコルチゾンを、ペンチレングリコール、ジメチルイソソルビド、及びプロピレングリコールに予め混合し、メインバッチに添加する前に、少し温めて十分に混合させた。高せん断混合プロセス(排出装置)を用いて、メインバッチを調製した。ダマや目に見える分離は観察されなかった。得られたバッチは、均一で少し不透明であった。乾燥試験を行ったところ(図1を参照されたい)、この調合物は、酢酸ジヒドロコルチゾン、プロピレングリコール、及びジメチルイソソルビド(コントロールの調合物)のない調合物と、実質的に同じ時間で乾燥した。疼痛/掻痒緩和剤を添加しても、調合物の乾燥は、感知できるほどには遅くならない。
【実施例3】
【0034】
[乾燥試験の実験の詳細]
「30SPFの日焼け止め含有の瘢痕用シリコーンゲル」の詳細
上の実施例1に記載の「30SPF日焼け止めシリコーン瘢痕用ゲル」は、以下のFDAに認可された日焼け止め活性:10.0%のオクトクリレン、7.5%のオクチノキサート、5.0%のオクチサレート、及び6.0%のオキシベンゾン、を添加した「瘢痕を制御処方するゲル」の成分を含有する。更に、エモリエントエステルである、8.0%のミリスチレン酸イソプロピルを分散剤として添加した。
【0035】
「1%の酢酸ヒドロコルチゾン含有の瘢痕用シリコーンゲル」の詳細
上の実施例2に記載の「1%のヒドロコルチゾンシリコーン含有の瘢痕用ゲル」は、FDAに認可された抗炎症薬、1%重量/重量の酢酸ヒドロコルチゾンを添加した「瘢痕を制御処方するゲル」の成分を含有する。また、5.0%のプロピレングリコール(保湿剤と皮膚調整剤)及びソルビトールの異性体の無水物のジメチルエーテルである溶媒である10.0%のジメチルイソソルビドを、酢酸ヒドロコルチゾンの皮膚浸透をより良くするのに用いた。
【0036】
[手順]
30個のプラスチックの秤量ボートにラベルを貼り、O’Haus EPI 14化学てんびんで正確に計量した。「瘢痕を制御処方するゲル」のサンプルを、プラスチックの秤量ボート上の薄膜に塗り広げ、初期重量を記録した(T=0)。35℃に設定したLunaire社の人工気候室に、このサンプルを置き、それから取り出して、5、10、40、60、180、240、300及び1440分間隔で秤量した。このプロセスを、「30SPF日焼け止め剤含有の瘢痕用シリコーンゲル」と「1%の酢酸ヒドロコルチゾン含有の瘢痕用シリコーンゲル」について繰り返した。この比較試験の結果を、以下の表1−瘢痕を制御処方するゲルの蒸発試験の結果;表2−30SPF日焼け止め剤含有のシリコーンゲルの蒸発試験の結果、及び表3−1%の酢酸ヒドロコルチゾンシリコーン含有のゲルの蒸発試験の結果に載せた。各表から得られたデータは、図1に一覧にして示した。
【0037】
[使用した器具]
(30)5.25”×3.50”×1.0”のプラスチックの秤量ボート
(1)目盛り付きのO’Haus EPI 14 Explorer Pro 化学てんびん
(1)35℃に設定したLunaire社の型番号GEO932M−4の人工気候室
【0038】
[結果]
【表1】

【0039】
【表2】

【0040】
【表3】

【0041】
[計算]
以下のように重量損失パーセントの値を計算した:

【0042】
nは、5、10、40、60、180、240、300、及び1440分に記録した重量である。
【0043】
例:「T=5分のときの1%の酢酸ヒドロコルチゾンシリコーンゲル」の重量損失パーセントを、これに沿って決定する。

【0044】
適切な時間間隔(5,10、40、60、180、240、300、及び1440)における、3つの製品のそれぞれの重量損失パーセントの値の平均値を求め、図に示した、図1を参照されたい。
【0045】
[計算]
1.瘢痕を制御処方するゲル、「30SPFの日焼け止め含有の瘢痕用シリコーンゲル」及び「1%の酢酸ヒドロコルチゾン含有の瘢痕用シリコーンゲル」は、全て180分のところで比較的安定な乾燥重量に達した。
【実施例4】
【0046】
[SPF試験の実験の詳細]
タイトル: 日焼け止め剤を含有する処方箋の静的日焼け防止指数(SPF)の評価
目 的: FDAの最終医薬品基準に準じて、店頭販売(OTC)の日焼け止め剤を含有する処方箋と8%のホモサラート規格(HMS)の静的SPFを、ボランティア人材において測定する。
試験製品: 試験調合物−SPF30と予想される
試験様式: 非ランダム化、盲検評価
結 果: 5対象が試験を完了した。試験の調合物である、試験製品の平均SPFは、33.1(n=5,標準偏差=2.0)であった。試験製品は、静的SPF30+1とラベルする条件である、FDAの最終医薬品基準を満たす。
有害事象: 有害事象は報告されなかった。
【0047】
[概要]
試験の一日目に、各対象に、キセノンアーク太陽シミュレータから背中の非保護の部位に、一連のUVを投与した。二日目に、暴露部位の周辺に伸びる、軽度の紅斑を生成するUV最小投与量として、最小紅斑量(MED)を決定した。次いで、100mgの試験製品と100mgのHMS規格品を、背中の隣接する50cm2面積に塗り広げた(8%のホモサラート(HMS)規格品は、ニュージャージー州、フェアフィールド、コスメテック ラボラトリーズ株式会社により提供された)。
【0048】
試験製品は、SPF30と予想され、HMS規格の日焼け止め剤は、SPF4と予想された。15分の乾燥期間の後、日焼け止め剤で保護した試験領域に、SPF30を塗布したときのMEDの0.76乃至1.32倍のUV線量を投与した。HMS規格の日焼け止め剤で保護した領域に、MEDと4の製品の0.64乃至1.56倍のUV線量を投与した。第二の保護されていない部位にも、一連のUV線量を投与した。三日目に、日焼け止めで保護した部位と保護しない部位のMEDを測定した。各日焼け止め剤のSPFは、最終的なMEDに対する、各日焼け止め剤で保護した部位のMEDの比として計算する。
【0049】
FDA日焼け止め医薬品基準1に準じる、静的な日焼け止め指数を決定する詳細な手順をプロトコルで述べる。
【0050】
ランプ1、2、7、8、10、13及び14に関する較正の詳細をランプ較正に示す。
【0051】
FDA最終医薬品基準に準じて、ラベル表示されたSPFを、以下のように計算する:
ラベル表示されたSPF=平均SPF値−A
小数点一位を切り捨てる。
SPF値>31のときは、試験製品を、SPF30+とラベル表示する。
ここでは、A=ts/sqrt(n)であり、95%の信頼区間を意味する。
t=生徒の分布の上位5%
s=標準偏差
n=対象の数
【0052】
パネルが有効なときは、HMS規格の日焼け止め剤のSPFが、予想されるSPF(すなわち、4.47±1.279)の標準偏差内にあり、HMS規格の日焼け止めの平均SPFに関して95%の信頼区間は、値4を含むはずである。
【0053】
[結果]
インフォームドコンセントを書面で提出した、男性2人と女性3人の5人の対象が、試験を終えた。全ての手順を終えた対象は、皮膚のタイプがIの人を2人、皮膚のタイプがIIの人を2人、及び皮膚のタイプがIIIの人を1人含んでいた。年齢は、21才乃至38才で、平均年齢は30.4才であった(n=5、標準偏差=7.1)。対象の層と静的SPFの結果を表4に挙げる。
【0054】
試験の調合物である、試験製品の平均静的SPFは、33.1であった(n=5、標準偏差=2.0)。HMS規格の平均SPFは、4.4(n=5、標準偏差=0.4)であった。
【0055】
[プロトコルからの逸脱]
プロトコルからの逸脱が、対象04で報告された。反復MEDと最終SPF評価は、22時乃至24時以外の時間枠(各々21時50分と21時54分と)で行った。プロトコルからの逸脱は、試験の結果に影響を与えなかった。
【0056】
[登録]
対象03は、一日目の手順中に、禁止薬物を理由に資格を剥奪され、対象05と対象06は、手順誤りを理由に資格を剥奪された。これらの対象のデータを、この報告に含まなかった。
【0057】
【表4】

対象03−禁止薬物服用により資格剥奪
対象05−手順誤りにより資格剥奪
対象06−手順誤りにより資格剥奪
【0058】
[結論]
参考文献の試験調合物である試験製品は、静的SPF30+1とラベルする条件である、FDAの最終医薬品基準を満たす。
【0059】
[参考文献]
1.米国の食品及び薬物の投与;店頭販売のヒト用日焼け止め薬物製品;最終医薬品基準;21CRF部分310、352、700及び740。Federal Register 64(98)、1999年5月21日、27666−27693頁。
【0060】
[プロトコル]
目 的: FDAの最終医薬品基準1に準じる、店頭販売(OTC)の日焼け止め剤含有の処方箋の静的SPFを測定する。
試験製品: SPF30と予測
試験様式: 非ランダム化、盲検評価
対 象: 皮膚のタイプI、II及び/又はIII1を有する、5人の男性及び/又は女性の条件を満たしたボランティアが、試験製品を終える。スポンサから許可を得て、最大20人の追加の対象を登録し、FDA最終医薬品基準試験1の条件を満たした。
【0061】
[序論]
FDA最終医薬品基準1には、静的日焼け防止指数を決定する手順が記載されている。静的SPFは、日焼け止めで保護された皮膚と保護されていない皮膚の紫外線放射の最小紅斑量の比率により定義される。最小紅斑量(MED)は、投与の22乃至24時間後に、境界がはっきりと明確な軽度の紅斑(日光皮膚炎)を生じさせる紫外線(UV)の吸収量である。太陽放射を模したキセノンアークランプを用いて、時間を決めてUV放射量を投与した。技術者は、較正済みの放射計を用いて太陽シミュレータの出力を測定して、紅斑的に効果的な放射照度が一定であることを保証した。紅斑に効果的な放射照度の測定値を記録した。
【0062】
[目的]
この試験の目的は、FDA最終医薬品基準1に準じて、店頭販売(OTC)の日焼け止め剤含有の処方箋の静的SPFを測定することであった。
【0063】
[様式]
非ランダム化、盲検評価をした。
【0064】
[対象]
最大25人の健康な男性と女性のボランティアを含む対象は、1製品につき皮膚タイプI、II及び/又はIII1に関して試験を終えた(下記を参照されたい)。

*対象によって報告された、1時間の夏の日光暴露に対する反応
【0065】
対象は、試験に参加する前1週間内及び試験参加中に使用したOTC又は処方薬を報告した。対象は、以下の基準も満たした。
【0066】
[試験対象患者基準]
・法的効力のある書面によるインフォームドコンセントを提出する、18才以上の者
・試験の約束を守り、指示に従う意思があり、かつこれらをできる者
・全般的に健康である者
・試験の間は、日光や日焼けランプを避ける意思のある者
【0067】
[除外基準]
・UV放射に対する異常反応歴又は試験製品の任意の成分に対して異常な反応歴を有する者
・日光皮膚炎、日焼け、活発な真皮の病変、まだらな肌の色合い、又は母斑、傷、若しくはホクロなど試験の手順を妨害する可能性のある任意の疾患を有する者
・例えば、光感受性物質、抗ヒスタミン、鎮痛薬、又は抗炎症薬など、試験結果に影響を及ぼす可能性のある任意の薬物を使用する者
・妊娠、授乳、又は試験に参加することにより危険性が高まる可能性のある状態にある者
・過去3ヶ月において、日焼け用ベッド又は日焼けランプに暴露した者
【0068】
[試験手順]
全ての手順(製品塗布、UV線量、及び評価)を、対象の同じ部位で行なった。
【0069】
[1日目]
[対象の登録]
候補となった対象は、試験室に出向いて、試験の手順について完全な説明を受けた。対象が、この試験の条件に賛同し、参加を希望した場合は、同意書及び健康に関する個人情報の公開を承認する署名を行い、簡単な薬物歴書を提供した。まだらな皮膚色及び傷はないか、背中、ベルトライン、及び肩甲骨を、ウッドランプを用いて検査した。技術者は、対象の問診票に記入し、条件を満たす対象を試験に登録した。対象の番号を試験の登録順に割り当てた。
【0070】
[MED線量投与]
時間を定めたUV線量を5回連続で、25パーセントずつ増量して、背中、肩甲骨の真下、及びベルトラインの上に投与した。MEDのUV線量、時間線量が終わったら、ランプの測定値をMEDフォームに表示した。
【0071】
UV暴露、光感受性物質、鎮痛剤、抗ヒスタミン剤、及び抗炎症剤を避けるよう、対象に指示し、かつUV線量完了の22時乃至24時間後に試験室に戻るよう指示した。
【0072】
[2日目]
[MED決定]
対象は、反応の評価のために、MED線量の完了の22時乃至24時間以内に試験室に戻り、非指示的に質問されて、服薬順守を評価され、併用薬を同定され、有事事象を観察される。訓練を受けた評価者による、UVの暴露部位の反応を、450乃至550ルクスの温蛍光又はタングステン照明下で、表5に示す評価基準を用いて等級分けした。
【0073】
表5:未処理の部位及び日焼け止め剤で処理した部位へのUV線量の投与に対する、紅斑反応の評価基準
0 紅斑反応なし
1 わずかに認知できる紅斑
2 明らかに明確な境界を有する軽度の紅斑
3 はっきりとした境界を有する中度の紅斑*
4 はっきりとした境界を有するどす黒い紅斑*
5 はっきりとした境界を有して浮腫の可能性のある、どす黒い紅斑*
6 はっきりとした境界と浮腫を有する、はっきりと認知できる紅斑*
*中度、どす黒い、又ははっきりと認知できる紅斑が、暴露部位の境界に届かない場合は、説明が評価形式の所見欄に提供された。
【0074】
少なくとも2(明らかに明確な境界を有する軽度の紅斑)の等級の紅斑を生じさせる、一連のうちの第一暴露部位としてMEDを決定した。紅斑の等級の進行は、投与されたUV線量と一致した。
【0075】
日焼け反応があると判断されたら、対象は、おそらくタイプIVであり、試験に適任ではない。このケースでは、この対象を、試験から除外し、交替させた。各UV暴露部位の等級、すべてのコメント、及び評価時間を記録した。
【0076】
実際のスケジュールで必要であれば、対象は、その時に試験室を離れ、2日目の処置を終えるべく1週間以内に戻ることが許可された。
【0077】
[SPF決定のための製品の塗布]
試験の参加を中断していた場合は、この対象は、非指示的に質問されて、服薬順守を評価され、併用薬を同定され、有事事象を観察される。
【0078】
試験の技術者は、テンプレートと消えないマーカーを用いて、ベルトラインと肩甲骨の間の、対象の背中上の指定箇所に50cm2の矩形を複数描いた。次いで技術者は、100mgの試験製品をその指定された矩形内に塗布し、100mgのHMS規格を隣接する矩形に塗布した。材料を領域全域にわたり「点々と」をつけ指サックを用いて全域に均一な膜が塗布されるまで優しく伸ばすことにより、この日焼け止め剤を塗布した。
【0079】
技術者は、製品処方指示書、試験の部位の位置、及び塗布した時間を記録した。
【0080】
[静的SPF決定用のUV線量]
少なくとも15分かけて、技術者は、時間を定めたUV線量を、徐々に増やしながら続けて7回、試験製品で処理した部位に投与した。この一連の線量は、各試験製品の予想されるSPFの製品、対象のMED、及び以下の数字によって決定した。

【0081】
技術者は、各試験製品につき、完了した回数及びランプの効果的な放射照度の測定値を記録した。
【0082】
[HMS規格用UV線量]
少なくとも15分かけて、技術者は、時間を定めたUV線量を、徐々に増やしながら続けて7回、HMS規格部位に投与した。一連の線量は、HMS規格SPF(4)の製品、対象のMED、及び以下の数字により決定した。

【0083】
技術者は、HMS規格用のUV線量、完了した回数及びランプの効果的な放射照度の測定値を記録した。
【0084】
[反復MED決定用のUV線量]
技術者は、背中の非保護領域に、時間を定めたUV線量を続けて5回、25パーセントずつ増やして投与した。一連の5回の線量は、以下に示す中心の当初MEDを含んでいた。

【0085】
反復MED用のUV線量、完了した回数及びランプの効果的な放射照度測定値を記録した。
【0086】
技術者は、静的SPF用のUV線量、HMS規格のSPF、及び反復MEDの完了後22時間乃至24時間以内に、評価のために試験室に戻るよう対象に指示した。
【0087】
[3日目]
[静的SPF及び反復MED用のUV線量に対する反応の評価]
対象は、試験室に戻ると、非指示的に質問されて、服薬順守を評価され、併用薬を同定され、有事事象を観察された。製品の塗布又はUV線量の投与に関与していない、訓練を受けた評価者が、表5に表示した基準を用いて、UV線量を受けた全ての部位を等級分けした。試験製品を塗布して、UV線量を投与した技術者は、評価者を補助することは許可されたが、この技術者が、UV反応の等級について、評価者に影響を与えることは許可されなかった。日焼け止め剤が処理された全ての部位の反応の等級を記録した。
【0088】
[SPFの計算]
技術者は、上記のように反復MEDを決定して、各対象のSPF値を計算した。
【0089】
反復MEDが決定できない場合、最終MEDが反復MEDされた。このケースでは、初期MEDを、最終MEDとして使用する。
【0090】
SPF値を、最終MEDに対する、日焼け止め剤で保護した部位のMEDの比率として計算した。
【0091】
ラベルされたSPFを、20人の対象に基づいて、以下のように算出した。
平均SPF値−A
(小数第一位を切り捨てる)
ここでは、A=ts/sqrt(n)
t=生徒の分布の上位5%
s=標準偏差
n=対象の数
【0092】
パネルが有効であるときは、HMS規格の日焼け止め剤のSPFが、予想されるSPF(すなわち、4.47±1.279)の標準偏差内にあり、HMS規格の日焼け止め剤の平均SPFに関する95%の信頼区間は、値4を含むはずである。
【0093】
[有事事象]
あらゆる有事事象を、対象のファイルと、必要に応じて得られる即時の治療において記録した。致命傷である又は緊急処置と定義されるいかなる深刻な有事事象も、24時間以内にスポンサーに報告した。全ての有事事象を、スポンサーに報告した。
【0094】
[対象の交替]
服薬順守をしない又は有事事象により不適格と見なされた対象を全て交替させた。対象のデータに、SPF値に関して望み通りの計算ができない理由がある場合は、その対象を交替させることになっていた。
【0095】
[参考文献]
1.米国の食品及び薬物の投与;店頭販売のヒト用日焼け止め薬物製品;最終医薬品基準;21CRF部分310、352、700、及び740。Federal Register 64(98)、1999年5月21日、27666−27693頁。
【0096】

【技術分野】
【0001】
[関連出願の参照]
本出願は、2009年6月18日出願、米国特許出願第12/487,498号の優先権を主張する。
【背景技術】
【0002】
皮膚の完全性を損なう裂傷及びその他の創傷は、ほとんどの人が経験したことがあるありふれたものであり、擦りむいた膝といった日常的なものから、刺し傷又は重度の火傷といった命にかかわるものまである。多くの皮膚の破損は、瘢痕を経て美観を損なう可能性がある。
【0003】
瘢痕組織の発生は、損傷に対する防御反応であり、皮膚の破損箇所を修復し、潜在的な感染及び再損傷部位を除去する。しかし、瘢痕組織の過剰な形成は、周囲の皮膚の色素又は粘稠性を欠く、固い真皮表面を生じさせることがある。普通の皮膚とは異なる瘢痕組織の柔軟性と弾力性のため、瘢痕組織は、傷を受けた者の生活を最終的に制限することがある。瘢痕組織は、一般的に周辺の皮膚組織より丈夫である。このことは、膝又は肘の上あるいは後ろなど、皮膚が変形応力と弾性応力にさらされる瘢痕組織に特に当てはまる。このような場所は、皮膚/瘢痕組織の境界で、裂傷を受ける可能性がある。掌線などの曲げることを容易にする生来の溝を有する場所を覆う瘢痕組織、特に新しい瘢痕組織は、多くの場合これらの屈曲する線においては弱い。手を開いたり閉じたりすることで生じる伸縮が、これらの生来の溝で瘢痕組織を破裂させることがあり、溝の両側に瘢痕組織の蓄積をもたらし、手を動かしただけで裂けてしまう、更に高い脆弱性を有する組織を、溝の中に新たに形成させる要因になる。一般的に、創傷部位の生来の組織分布が、再裂傷の可能性を高めて、治癒時間を長引かせることになる。
【0004】
瘢痕が、分厚く、硬く、及び非弾性になるにつれて、形成の間及び後に瘢痕化した部位が自然に収縮するので、瘢痕組織の柔軟性と弾力性が更に失われてしまう。結果として、火傷の犠牲者など広範囲の皮膚損傷を負った者の動作は、かなり制限されることがある。重篤な火傷を負った手は、握りしめたまま動かせなくなることがある。火傷による腰周辺の瘢痕組織は、多くの人が当たり前だと思うねじれ運動を妨げることがある。
【0005】
創傷を治療するいくつかの製剤が処方され、治癒する間に形成される瘢痕組織の特性に良い効果を与えている。例えば、いくつかの創傷ドレッシングは、創傷の乾燥を減少させる若しくは紫外線暴露を防止するといった機能を有する。このような調合物は、度重なる亀裂と乾燥を防ぐことができ、その結果、とりわけ、この調合物を欠いて形成された瘢痕組織と比べて、改善された柔軟性、弾力性、及び色特性を有する瘢痕組織が形成される。
【0006】
いくつかの調合物は、ゲルなど、厳密に言えば有機物質で作られている。ゲルは、創傷ドレッシングとして適する特性を有する。ゲルは、創傷に直接接触させて冷やすことができ、更に創傷が汚染を受けない状態にしておくことができる。ゲルのその他の有用な特性は、その粘稠度である:多くのゲルは、弾力性や変形能が、皮膚と類似しているので、皮膚及び組織表面に付着したゲルは、治癒創傷の部位で裂けることなく又は応力を生じさせることなく、皮膚及び組織表面と共に曲がり、まとまり、及び伸縮することができる。
【0007】
しかし、ゲルは、時間がたつと急速に乾燥し、構造的に及び/又は化学的に崩壊するので、通常ゲルを再度塗布しなければならない。このことは、特に乾燥によりドレッシングの粘稠度が固くなった場合は、患者にとって痛みを伴うプロセスになることがある。いくかのゲルは、水分を吸収して柔らかな又は液体の粘稠度になる。ゲルの粘稠度が損なわれると、バクテリア感染の可能性が高まる。
【0008】
一般的に、シロキサンゲルは、他のゲル製品より創傷組織と瘢痕組織の治療において優れていることが、わかっている。シロキサンゲルは、創傷部位の上にシリコーンベースのポリママトリクスを形成することにより機能する。例えば、ジメチコン、ジメチコンクロスポリマ、及びその他のシロキサン誘導体といったポリマ前駆体は、創傷部位に塗布される塗り広げることができる製剤に含有されている。いくつかのポリマ前駆体の調合物は、ヒュームドシリカを含む。この製剤は、創傷部位へ製剤を塗布すると蒸発し始める揮発性成分も含む。この塗り広げることができる製剤から揮発性化合物が蒸発すると、ポリママトリクスが形成を始める。多くの場合、特に、この調合物がヒュームドシリカを含む場合は、この製剤はチキソトロピックである。チキソトロピックの調合物は、創傷への塗布など応力がかかると、固い粘稠度から噛みタバコのような粘稠度に変化し、応力がなくなると、流動性の少ない固さに戻る。この特性によって、シロキサンゲル前駆体の調合物は、創傷を覆う比較的薄い層に容易に広がり、この創傷部位で最小の応力とずれで、この創傷部位から流れ出ることなく場所に留まることができる。
【0009】
シロキサンゲルの他の利点は、いくつかのゲルが瘢痕の形成時に、瘢痕組織の特性に対する有益な効果を有することを示したものであり、瘢痕の度合いを減少させて、瘢痕組織の質感を改善し、治癒した創傷の最終的な外見が、より周囲の皮膚に類似することである。例えば、いくつかのシロキサン製剤は、成長中の又は新しく形成される瘢痕組織に塗布すると、瘢痕を見事に消して、持続的に塗布することにより、ほとんど消滅させる能力があることが証明されている。
【0010】
創傷の治癒を補助する、市場に出ている他の塗り広げることができる製剤とは違い、ある程度の重合が起きてシロキサンポリママトリクスを形成すると、結果として得られたゲルは、一般的に、長時間にわたりその粘稠度を保持する能力を有する。その上、塗布されない製品は、塗布されるまで「硬化」しないシロキサンポリママトリクス前駆体として適用することができるので、他のタイプのゲルよりも保管し易く、使い易い。
【0011】
シロキサンゲルは、成長中の瘢痕組織に対してこのような有益な効果を有するので、このような製剤は、ゲルに更なる有用な機能を与える添加剤を包含する能力も有することが望ましい。例えば、上述のシリコーンベースの調合物は、瘢痕を減少させる優れた特性を示すが、成長中の瘢痕組織は、紫外線及びその他の波長の放射線にさらされると、色及び/又は質感の変化、並びに熱損傷といった他のタイプの損傷の影響を受け易い。マトリクス形成時に保持される調合物に、日焼け止め作用のある化合物を組み込むことが望ましい。また、ゲルの局所塗布により最適に手当てされた火傷及びその他の損傷は、創傷が瘢痕になり始めてもなお、非常な痛みを伴うことがある。しかし、マトリクス形成製剤の塗布は、鎮痛剤の局所塗布を妨げることがある大部分の包帯タイプの被覆剤とは違って、局所ゲルは簡単にはずしたり再度置いたりできない。したがって、マトリクス形成製剤は、少なくとも一の疼痛緩和化合物を含むことが望ましい。
【0012】
残念なことに、シロキサンマトリクス前駆体の使用は、シリコーン創傷ドレッシングに含まれ得るさまざまな添加剤を、大幅に制限してきた。多くの望ましい添加剤は、塗り広げることができる製剤を含むジメチコンとその他のシロキサン誘導体といったマトリクス前駆体の混合物中に容易に溶媒和されない。例えば、オクトクリレン、オクチノキサート、オクチサレート、及びオキシベンゾンといった、多くの効果的で一般的に用いられる日焼け止め添加剤は、予め重合された製剤中に十分に溶解しないことがある。予め重合された製剤中の溶解度が低い、望ましい添加剤の他の例は、例えば、酢酸ヒドロコルチゾンなど疼痛や炎症を減少させる、コルチドンタイプの化合物を含む。
【0013】
シロキサンマトリクスを形成する創傷製剤の利点を生かし、更に、シリコーン創傷ドレッシング調合物中に不溶性添加剤を包含させる方法は、創傷ドレッシング製剤の技術の大幅な進歩として歓迎されるであろう。
【発明の概要】
【0014】
驚くべきことに、制限されている又はマトリクス前駆体中に不溶である、所定の活性を有する所定の揮発性助剤を(揮発性成分に加えて)使用すると、シリコーンマトリクスへこの活性を取り込むことができることを見出した。更に驚くべきことに、成形マトリクスへこの活性を組み込むことを可能にするこの複合体は、この活性と複合されるにもかかわらず、かつ成長中のマトリクスが、この複合助剤が蒸発する能力を妨げることが予想されるにもかかわらず、優れた揮発性を実際に維持する。驚くべきことに、この揮発性助剤は、この活性を有するマトリクス内に取り込まれない。代わりに、助剤なしではマトリクス前駆体中に溶けない不溶性活性は、揮発性助剤がこの活性に複合されたままでなく、分離し、蒸発して失われるにもかかわらず、マトリクス形成中にマトリクス内に取り込まれたままである。更に驚くべきことに、鎮痛添加剤の効果から明らかなように、この活性は、マトリクス内で移動性を有し、ゲルを通って創傷部位に移動する能力をもたらす。更に、揮発性助剤の蒸気圧は、活性と複合すると、及び成長中のシロキサンマトリクス内に活性とともに取り込まれることによって減少することが予想される。また、十分な蒸気圧を維持しており、きれいに蒸発する。ここに特定されるような揮発性助剤を使用すると、シリコーンマトリクス形成の調合物に、さまざまな添加剤のタイプを組み込むことができる。本発明は、シリコン前駆体混合物への不溶性活性の取り込みを可能にして、シロキサンゲルの創傷治癒技術の有用性を大幅に拡げる。
【図面の簡単な説明】
【0015】
【図1】図1は、乾燥試験の結果である。一番下、真ん中、及び一番上の曲線は、日焼け止め剤含有のゲル、鎮痛剤含有のゲル、及びコントロールのゲルの乾燥結果を、それぞれグラフを使って示したものである。
【発明を実施するための形態】
【0016】
[シロキサンマトリクス前駆体]
本発明のマトリクス形成組成物は、シロキサンマトリクス前駆体、揮発性成分、活性成分、及び揮発性助剤を含む。この組成物を創傷又は瘢痕部位に適用すると、揮発性成分及び揮発性助剤は、1)マトリクス形成に関与する成分、並びに2)マトリクスに存在する一又はそれ以上の活性成分を残して、この組成物から部分的に又は完全に蒸発する。一般的に、マトリクス形成に関与する成分は、一又はそれ以上のシロキサンを有し、一又はそれ以上のシロキサンは、環状ヒドロカルビル基などの有機成分を含有するといった有機特性を有する。ジメチコン及びジメチコンクロスポリマといったポリジメチルシロキサンが好ましい。ジメチコンやジメチコンクロスポリマの代わりに又はこれらに加えて、他のポリジメチルシロキサンを用いてポリママトリクスを形成してもよい。他のポリシロキサンや他のジアルキルポリシロキサンを含む重合反応は特に、以下に挙げる揮発性成分、揮発性助剤、及び活性と共に用いるときに、本発明の利点を示すマトリクスを形成することができると考えられている。このようなマトリクスは、本発明の範囲内である。ヒュームドシリカは、予め重合された組成物に、チキソトロピックな粘稠性を与える。ヒュームドシリカは、ゲルの構造にも関与するが、重合プロセスにおけるヒュームドシリカの貢献又は関与は、たとえあったとしても明らかではない。揮発性成分を有する場合は、一般的に製剤中のマトリクス前駆体は、例えば、1、2、4、6、12ヶ月又はそれ以上の長期間、顕著な重合を受けることなく、室温(25K)で保管可能である。マトリクス前駆体は、ジメチコンクロスオポリマ、並びにジメチコンといったクロスポロマ成分を含むことが好ましい。いくつかの実施態様では、シロキサン成分が、約25乃至60重量%の重量パーセントの範囲で存在する。好ましい実施態様では、シロキサン成分は、30乃至50重量%の範囲で存在する。より好ましい実施態様では、シロキサン成分は、約35乃至45重量%の範囲の量で存在する。シロキサン成分は、ジメチコンが好ましい。 クロスポリマ成分は、約0.5乃至8重量%の範囲の量で存在するのが好ましく、約1.5乃至5重量%の範囲で存在するのがより好ましい。
【0017】
[揮発性成分]
本発明の組成物は、(以下に述べる揮発性助剤と区別される)揮発性成分を含む。一般的に、揮発性成分は、組成物を創傷部位に塗布すると蒸発を始める。いくつかの実施態様では、蒸発が始まるとシロキサンマトリクスの形成は直ちに始まり、蒸発は更に進行する。他の実施態様では、揮発性成分が蒸発する間のある時期には、シロキサンマトリクスは、かなり形成し始めるが、その時期より前には、ほんの少ししか形成しない。好ましい実施態様では、揮発性成分の重合への関与は、制限されているかまったくないが、マトリクス前駆体中に容易に溶媒和又は溶解する。好ましい例は、シロキサン重合における反応物としてほとんど又は全く関与しない揮発性シロキサン化合物である。例えば、環状シクロヘキサンは、一般的に、シクロヘキサン中に高い溶媒和と揮発性特性を示し、全てのシラン酸素原子が重合に利用できない事実により、一般的に、マトリクス形成における環状シクロヘキサンの関与は比較的低い。水素又は4未満の炭素原子のヒドロカルビル基を含む構成物質を有する、シクロペンタシロキサンがより好ましい。水素又は1の炭素原子のヒドロカルビル基を含む構成物質が最も好ましい。約12乃至45重量%の範囲の揮発性成分の量が好ましい。約15乃至28重量%の範囲の量がより好ましく、約20乃至25重量%の範囲の量が最も好ましい。
【0018】
揮発性成分は、約30乃至40℃の範囲の一又はそれ以上の温度で15分後に、揮発成分の50パーセント超が蒸発されるような量で存在することが好ましい。
【0019】
一般的に、この揮発性成分は、その一部又は全体が蒸発すると、ポリママトリクスが形成を始めるように機能する。従って、いくつかの実施態様では、揮発性物質の存在は、揮発を開始すると重合速度が上がるように作用し、重合プロセスを完全に又は部分的に阻害することがある。一般的に、本発明の組成は、上記の化合物に特に限定されるものではなく、創傷に塗布する前はシロキサンマトリクスの形成を完全に又は部分的に阻害するが、創傷に製剤を塗布すると蒸発し始め、シロキサンマトリクス形成の完了によって完全に又は部分的に蒸発されるような相対量で使用され得る化合物を広く含む。いくつかの実施態様では、揮発性成分の蒸発は、完全な蒸発の前に経時的に停滞する。他の実施態様では、揮発性成分の蒸発は、シロキサンマトリクスが完全に形成された後も継続する。揮発性成分の蒸発は、3時間以内で原重量(保管の濃度)の5%未満が好ましいが、いくつかの実施態様では、揮発成分の蒸発は、3時間以内で原重量の10、20、及び30%を超える範囲内である。いくつかの実施態様では、使用前及び保管中の揮発性成分濃度の重量パーセントは、約5乃至約40%の範囲である。別の実施態様では、使用前及び保管中の揮発性成分濃度の重量パーセントは、約15乃至約35%の範囲である。好ましい実施態様では、使用前及び保管中の揮発性成分濃度は、約18乃至約30%の範囲である。
【0020】
[活性剤及び揮発性助剤]
本発明の創傷治癒の製剤は、揮発性助剤を含有する。理論に拘束されるのを望むものではないが、揮発性助剤は、マトリクス前駆体中に活性を溶媒和するのを補助すると考えられている。特定の活性を具える揮発性助剤として機能する特定の化合物は、成長中のマトリクスに取り囲まれ、それ自身は最終的には揮発されない活性と化学的に関連があるという事実にもかかわらず、かなり揮発させる能力を有することが見出されてきた。
【0021】
一般的な紫外線吸収剤は、シロキサンマトリクス前駆体を含む溶液中に容易に溶解しない。しかし、多くの紫外線吸収剤は、ミリスチン酸エステルが存在するシロキサンマトリクス前駆体溶液中に溶媒和することがある。例えば、以下のさまざまな化学構造を有するエスカロール紫外線吸収剤は、シロキサンマトリクスに導入されることができる。

【0022】
一実施態様では、活性は、少なくとも一の芳香環を含む紫外線吸収化合物である。より好ましい実施態様では、この活性は、ISPケミカルから入手可能な一又はそれ以上のエスカロール化合物であり、この揮発性助剤は、1)約6乃至13の炭素原子の炭素鎖長を有する直鎖酸と、2)メタノール、エタノール、又は約3乃至約8の炭素原子の全炭素含有量を有する第二アルコールと、のエステルである。より好ましい実施態様では、揮発性助剤は、メタノール、エタノール、又は約3乃至約8の炭素原子の全炭素含有量を有する第二アルコールからのミリスチン酸エステルであり、活性は、エスカロール化合物である。更に好ましい実施態様では、揮発性助剤は、ミリスチン酸イソプロピルであり、活性は、オクトクリレン(ISPエスカロール597)、オクチノキサート(ISPエスカロール557)、オクチサレート(ISPエスカロール587)、又はオキシベンゾン(ISPエスカロール567)である。調合物中の日焼け止め活性は、約5乃至40重量%の範囲の総計量で存在するが、約15乃至35重量%の範囲の量がより好ましい。いくつかの実施態様では、日焼け止め活性は、約25乃至30重量%の範囲の量で存在する。
【0023】
一般に、揮発性剤は、1)約6乃至13の炭素原子の炭素鎖を有する直鎖酸と2)メタノール、エタノール、又は約3乃至約8の炭素原子の全炭素含有量を有する第二アルコールとのエステルであり、より好ましくは、ミリスチン酸イソプロピル;3又はそれ以上の炭素の直鎖及び一又はそれ以上のヒドロキシル基を具えるグリコールであり;全てのヒドロキシル基は、終末炭素を含む炭素に隣接し;ペンチレングリコールがより好ましく;又は置換若しくは非置換イソソルビド;及びジメチルイソソルビドが好ましい。
【0024】
一般の抗炎症化合物の多くは、ステロイド化合物構造に基づいている。シロキサンマトリクス前駆体の溶液中に難溶解性を有するいくつかのステロイドは、グリコール及び/又はイソソルビド化合物が存在するシロキサンマトリクス前駆体溶液中に溶媒和され得ることが見出されてきた。
【0025】
一実施態様では、活性は、ステロイド化合物であり、揮発性助剤は、3又はそれ以上の炭素の直鎖と、一又はそれ以上のヒドロキシル基とを含むグリコールであり、全てのヒドロキシル基は、終末炭素を含む隣接する炭素に上にある。より好ましい実施態様では、揮発性助剤は、3乃至7の炭素の直鎖と、一つが末端炭素に結合された2つのヒドロキシル基とを具えるグリコールであり、その活性は、ステロイド化合物である。更に好ましい実施態様では、揮発性助剤は、ペンチレングリコールであり、その活性は、酢酸ジヒドロコルチゾンである。
【0026】
一実施態様では、活性は、ステロイド化合物であり、揮発性助剤は、置換又は非置換イソソルビドを含む。更に好ましい実施態様では、活性は、コルチゾンであり、揮発性助剤は、二置換イソソルビドを含む。更に好ましい実施態様では、揮発性助剤は、ジメチルイソソルビドであり、その活性は、酢酸ジヒドロコルチゾンである。
【0027】
一実施態様では、活性は、ヒドロコルチゾン化合物であり、グリコール化合物とイソソルビド化合物との両方を含む活性を用いる。好ましい化合物においては、その活性は、酢酸ヒドロコルチゾンである。
【0028】
ステロイド化合物は、0.1乃至8重量%の範囲の量で存在するのが好ましい。約0.5乃至3重量%の範囲の量が、更に好ましい。
【0029】
グリコール及びイソソルビドは、5乃至40重量%のパーセントの範囲(両方存在する場合は総合重量)の量で存在する。好ましい実施態様では、双方それぞれ5乃至50重量%の範囲の量で存在する。別の実施態様では、グリコールとイソソルビドは、10乃至25重量%の範囲で存在し、0乃至15合計重量%となる。
【0030】
より深い浸透が要求される場合は、ミリスチン酸イソプロピルの代わり、日焼け止め活性とともにグリコール及びイソソルビド成分を用いてもよいことに留意すべきである。
【0031】
本発明の組成物は、例えば、ヒュームドシリカ、ジメチコン、及びジメチコンクロスポリマといったマトリクス前駆体と、例えば、シクロペンタシロキサンといった揮発性成分とを互いに混合することにより調製してもよい。前述の化合物を、互いに混合し、シロキサンのベースを形成させた。一般的に、活性成分は、揮発性助剤と混合されて混合物を形成するが、この混合物は、組成物のバランスにそれを導入する前にシロキサンのベースに添加される。一実施態様では、このベースは、シクロペンタシロキサン及びジメチコンクロスポリマのみを含有する。次いで、混合物をベースと混ぜ合わせる。一般的に、活性と揮発性助剤とを予め混合するのが望ましい。しかし、いくつかのケースでは、揮発性助剤と活性以外の全ての成分とを組み合わせ、活性を最終ステップにおいて製剤に添加してもよい。
【実施例1】
【0032】
[30SPFの日焼け止め含有の瘢痕用ゲル]
瘢痕用ゲルは、10.0%のオクトクリレン、7.5%のオクチノキサート、5.0%のオクチサレート、6.0%のオキシベンゾン、8.0%のミリスチン酸イソプロピル、36%のジメチコン、3.5%ヒュームドシリカ、2%のジメチコンクロスポリマ、及び22%のシクロペンタシロキサンを含む。全てのパーセンテージは重量/重量である。オクトクリレン、オクチノキサート、オクチサレート、オキシベンゾンは、UVA及びUVB抵抗を提供する。これらを、ミリスチン酸イソプロピルと予め混合した。シクロペンタシロキサンとジメチコンクロスポリマを混ぜ合わせたものに、この混合物を添加した。次に高せん断混合プロセス(排出装置)を用いて、ヒュームドシリカを混合物全体に添加した。最後にジメチコンを添加して、均質になるまで混合物を混合しダマや目に見える分離がない粘性のある不透明のゲルを得た。調合物は、30又はそれ以上のSPF評価を有する。乾燥試験(一定重量に到達するのにかかる時間)(図1を参照されたい)を行ったところ、この調合物は、オクトクリレン、オクチノキサート、オクチサレート、オキシベンゾン、及びミリスチン酸イソプロピル(コントロールの調合物)のない調合物と、本質的に同じ時間で乾燥した。日焼け止め添加剤を添加しても、調合物の乾燥は、感知できるほどには遅くならない。
【実施例2】
【0033】
[酢酸ヒドロコルチゾン含有の瘢痕用ゲル]
瘢痕用ゲルは、1.0%の酢酸ヒドロコルチゾン、5.0%のプロピレングリコール、8.0%のジメチルイソソルビド、12.0%のペンチレングリコール、45.0%のジメチコン、3.0%のヒュームドシリカ、2.0%のジメチコンクロスポリマ、及び24.0%のシクロペンタシロキサンを含む。全てのパーセンテージは、重量/重量である。酢酸ヒドロコルチゾンを、ペンチレングリコール、ジメチルイソソルビド、及びプロピレングリコールに予め混合し、メインバッチに添加する前に、少し温めて十分に混合させた。高せん断混合プロセス(排出装置)を用いて、メインバッチを調製した。ダマや目に見える分離は観察されなかった。得られたバッチは、均一で少し不透明であった。乾燥試験を行ったところ(図1を参照されたい)、この調合物は、酢酸ジヒドロコルチゾン、プロピレングリコール、及びジメチルイソソルビド(コントロールの調合物)のない調合物と、実質的に同じ時間で乾燥した。疼痛/掻痒緩和剤を添加しても、調合物の乾燥は、感知できるほどには遅くならない。
【実施例3】
【0034】
[乾燥試験の実験の詳細]
「30SPFの日焼け止め含有の瘢痕用シリコーンゲル」の詳細
上の実施例1に記載の「30SPF日焼け止めシリコーン瘢痕用ゲル」は、以下のFDAに認可された日焼け止め活性:10.0%のオクトクリレン、7.5%のオクチノキサート、5.0%のオクチサレート、及び6.0%のオキシベンゾン、を添加した「瘢痕を制御処方するゲル」の成分を含有する。更に、エモリエントエステルである、8.0%のミリスチレン酸イソプロピルを分散剤として添加した。
【0035】
「1%の酢酸ヒドロコルチゾン含有の瘢痕用シリコーンゲル」の詳細
上の実施例2に記載の「1%のヒドロコルチゾンシリコーン含有の瘢痕用ゲル」は、FDAに認可された抗炎症薬、1%重量/重量の酢酸ヒドロコルチゾンを添加した「瘢痕を制御処方するゲル」の成分を含有する。また、5.0%のプロピレングリコール(保湿剤と皮膚調整剤)及びソルビトールの異性体の無水物のジメチルエーテルである溶媒である10.0%のジメチルイソソルビドを、酢酸ヒドロコルチゾンの皮膚浸透をより良くするのに用いた。
【0036】
[手順]
30個のプラスチックの秤量ボートにラベルを貼り、O’Haus EPI 14化学てんびんで正確に計量した。「瘢痕を制御処方するゲル」のサンプルを、プラスチックの秤量ボート上の薄膜に塗り広げ、初期重量を記録した(T=0)。35℃に設定したLunaire社の人工気候室に、このサンプルを置き、それから取り出して、5、10、40、60、180、240、300及び1440分間隔で秤量した。このプロセスを、「30SPF日焼け止め剤含有の瘢痕用シリコーンゲル」と「1%の酢酸ヒドロコルチゾン含有の瘢痕用シリコーンゲル」について繰り返した。この比較試験の結果を、以下の表1−瘢痕を制御処方するゲルの蒸発試験の結果;表2−30SPF日焼け止め剤含有のシリコーンゲルの蒸発試験の結果、及び表3−1%の酢酸ヒドロコルチゾンシリコーン含有のゲルの蒸発試験の結果に載せた。各表から得られたデータは、図1に一覧にして示した。
【0037】
[使用した器具]
(30)5.25”×3.50”×1.0”のプラスチックの秤量ボート
(1)目盛り付きのO’Haus EPI 14 Explorer Pro 化学てんびん
(1)35℃に設定したLunaire社の型番号GEO932M−4の人工気候室
【0038】
[結果]
【表1】

【0039】
【表2】

【0040】
【表3】

【0041】
[計算]
以下のように重量損失パーセントの値を計算した:

【0042】
nは、5、10、40、60、180、240、300、及び1440分に記録した重量である。
【0043】
例:「T=5分のときの1%の酢酸ヒドロコルチゾンシリコーンゲル」の重量損失パーセントを、これに沿って決定する。

【0044】
適切な時間間隔(5,10、40、60、180、240、300、及び1440)における、3つの製品のそれぞれの重量損失パーセントの値の平均値を求め、図に示した、図1を参照されたい。
【0045】
[計算]
1.瘢痕を制御処方するゲル、「30SPFの日焼け止め含有の瘢痕用シリコーンゲル」及び「1%の酢酸ヒドロコルチゾン含有の瘢痕用シリコーンゲル」は、全て180分のところで比較的安定な乾燥重量に達した。
【実施例4】
【0046】
[SPF試験の実験の詳細]
タイトル: 日焼け止め剤を含有する処方箋の静的日焼け防止指数(SPF)の評価
目 的: FDAの最終医薬品基準に準じて、店頭販売(OTC)の日焼け止め剤を含有する処方箋と8%のホモサラート規格(HMS)の静的SPFを、ボランティア人材において測定する。
試験製品: 試験調合物−SPF30と予想される
試験様式: 非ランダム化、盲検評価
結 果: 5対象が試験を完了した。試験の調合物である、試験製品の平均SPFは、33.1(n=5,標準偏差=2.0)であった。試験製品は、静的SPF30+1とラベルする条件である、FDAの最終医薬品基準を満たす。
有害事象: 有害事象は報告されなかった。
【0047】
[概要]
試験の一日目に、各対象に、キセノンアーク太陽シミュレータから背中の非保護の部位に、一連のUVを投与した。二日目に、暴露部位の周辺に伸びる、軽度の紅斑を生成するUV最小投与量として、最小紅斑量(MED)を決定した。次いで、100mgの試験製品と100mgのHMS規格品を、背中の隣接する50cm2面積に塗り広げた(8%のホモサラート(HMS)規格品は、ニュージャージー州、フェアフィールド、コスメテック ラボラトリーズ株式会社により提供された)。
【0048】
試験製品は、SPF30と予想され、HMS規格の日焼け止め剤は、SPF4と予想された。15分の乾燥期間の後、日焼け止め剤で保護した試験領域に、SPF30を塗布したときのMEDの0.76乃至1.32倍のUV線量を投与した。HMS規格の日焼け止め剤で保護した領域に、MEDと4の製品の0.64乃至1.56倍のUV線量を投与した。第二の保護されていない部位にも、一連のUV線量を投与した。三日目に、日焼け止めで保護した部位と保護しない部位のMEDを測定した。各日焼け止め剤のSPFは、最終的なMEDに対する、各日焼け止め剤で保護した部位のMEDの比として計算する。
【0049】
FDA日焼け止め医薬品基準1に準じる、静的な日焼け止め指数を決定する詳細な手順をプロトコルで述べる。
【0050】
ランプ1、2、7、8、10、13及び14に関する較正の詳細をランプ較正に示す。
【0051】
FDA最終医薬品基準に準じて、ラベル表示されたSPFを、以下のように計算する:
ラベル表示されたSPF=平均SPF値−A
小数点一位を切り捨てる。
SPF値>31のときは、試験製品を、SPF30+とラベル表示する。
ここでは、A=ts/sqrt(n)であり、95%の信頼区間を意味する。
t=生徒の分布の上位5%
s=標準偏差
n=対象の数
【0052】
パネルが有効なときは、HMS規格の日焼け止め剤のSPFが、予想されるSPF(すなわち、4.47±1.279)の標準偏差内にあり、HMS規格の日焼け止めの平均SPFに関して95%の信頼区間は、値4を含むはずである。
【0053】
[結果]
インフォームドコンセントを書面で提出した、男性2人と女性3人の5人の対象が、試験を終えた。全ての手順を終えた対象は、皮膚のタイプがIの人を2人、皮膚のタイプがIIの人を2人、及び皮膚のタイプがIIIの人を1人含んでいた。年齢は、21才乃至38才で、平均年齢は30.4才であった(n=5、標準偏差=7.1)。対象の層と静的SPFの結果を表4に挙げる。
【0054】
試験の調合物である、試験製品の平均静的SPFは、33.1であった(n=5、標準偏差=2.0)。HMS規格の平均SPFは、4.4(n=5、標準偏差=0.4)であった。
【0055】
[プロトコルからの逸脱]
プロトコルからの逸脱が、対象04で報告された。反復MEDと最終SPF評価は、22時乃至24時以外の時間枠(各々21時50分と21時54分と)で行った。プロトコルからの逸脱は、試験の結果に影響を与えなかった。
【0056】
[登録]
対象03は、一日目の手順中に、禁止薬物を理由に資格を剥奪され、対象05と対象06は、手順誤りを理由に資格を剥奪された。これらの対象のデータを、この報告に含まなかった。
【0057】
【表4】

対象03−禁止薬物服用により資格剥奪
対象05−手順誤りにより資格剥奪
対象06−手順誤りにより資格剥奪
【0058】
[結論]
参考文献の試験調合物である試験製品は、静的SPF30+1とラベルする条件である、FDAの最終医薬品基準を満たす。
【0059】
[参考文献]
1.米国の食品及び薬物の投与;店頭販売のヒト用日焼け止め薬物製品;最終医薬品基準;21CRF部分310、352、700及び740。Federal Register 64(98)、1999年5月21日、27666−27693頁。
【0060】
[プロトコル]
目 的: FDAの最終医薬品基準1に準じる、店頭販売(OTC)の日焼け止め剤含有の処方箋の静的SPFを測定する。
試験製品: SPF30と予測
試験様式: 非ランダム化、盲検評価
対 象: 皮膚のタイプI、II及び/又はIII1を有する、5人の男性及び/又は女性の条件を満たしたボランティアが、試験製品を終える。スポンサから許可を得て、最大20人の追加の対象を登録し、FDA最終医薬品基準試験1の条件を満たした。
【0061】
[序論]
FDA最終医薬品基準1には、静的日焼け防止指数を決定する手順が記載されている。静的SPFは、日焼け止めで保護された皮膚と保護されていない皮膚の紫外線放射の最小紅斑量の比率により定義される。最小紅斑量(MED)は、投与の22乃至24時間後に、境界がはっきりと明確な軽度の紅斑(日光皮膚炎)を生じさせる紫外線(UV)の吸収量である。太陽放射を模したキセノンアークランプを用いて、時間を決めてUV放射量を投与した。技術者は、較正済みの放射計を用いて太陽シミュレータの出力を測定して、紅斑的に効果的な放射照度が一定であることを保証した。紅斑に効果的な放射照度の測定値を記録した。
【0062】
[目的]
この試験の目的は、FDA最終医薬品基準1に準じて、店頭販売(OTC)の日焼け止め剤含有の処方箋の静的SPFを測定することであった。
【0063】
[様式]
非ランダム化、盲検評価をした。
【0064】
[対象]
最大25人の健康な男性と女性のボランティアを含む対象は、1製品につき皮膚タイプI、II及び/又はIII1に関して試験を終えた(下記を参照されたい)。

*対象によって報告された、1時間の夏の日光暴露に対する反応
【0065】
対象は、試験に参加する前1週間内及び試験参加中に使用したOTC又は処方薬を報告した。対象は、以下の基準も満たした。
【0066】
[試験対象患者基準]
・法的効力のある書面によるインフォームドコンセントを提出する、18才以上の者
・試験の約束を守り、指示に従う意思があり、かつこれらをできる者
・全般的に健康である者
・試験の間は、日光や日焼けランプを避ける意思のある者
【0067】
[除外基準]
・UV放射に対する異常反応歴又は試験製品の任意の成分に対して異常な反応歴を有する者
・日光皮膚炎、日焼け、活発な真皮の病変、まだらな肌の色合い、又は母斑、傷、若しくはホクロなど試験の手順を妨害する可能性のある任意の疾患を有する者
・例えば、光感受性物質、抗ヒスタミン、鎮痛薬、又は抗炎症薬など、試験結果に影響を及ぼす可能性のある任意の薬物を使用する者
・妊娠、授乳、又は試験に参加することにより危険性が高まる可能性のある状態にある者
・過去3ヶ月において、日焼け用ベッド又は日焼けランプに暴露した者
【0068】
[試験手順]
全ての手順(製品塗布、UV線量、及び評価)を、対象の同じ部位で行なった。
【0069】
[1日目]
[対象の登録]
候補となった対象は、試験室に出向いて、試験の手順について完全な説明を受けた。対象が、この試験の条件に賛同し、参加を希望した場合は、同意書及び健康に関する個人情報の公開を承認する署名を行い、簡単な薬物歴書を提供した。まだらな皮膚色及び傷はないか、背中、ベルトライン、及び肩甲骨を、ウッドランプを用いて検査した。技術者は、対象の問診票に記入し、条件を満たす対象を試験に登録した。対象の番号を試験の登録順に割り当てた。
【0070】
[MED線量投与]
時間を定めたUV線量を5回連続で、25パーセントずつ増量して、背中、肩甲骨の真下、及びベルトラインの上に投与した。MEDのUV線量、時間線量が終わったら、ランプの測定値をMEDフォームに表示した。
【0071】
UV暴露、光感受性物質、鎮痛剤、抗ヒスタミン剤、及び抗炎症剤を避けるよう、対象に指示し、かつUV線量完了の22時乃至24時間後に試験室に戻るよう指示した。
【0072】
[2日目]
[MED決定]
対象は、反応の評価のために、MED線量の完了の22時乃至24時間以内に試験室に戻り、非指示的に質問されて、服薬順守を評価され、併用薬を同定され、有事事象を観察される。訓練を受けた評価者による、UVの暴露部位の反応を、450乃至550ルクスの温蛍光又はタングステン照明下で、表5に示す評価基準を用いて等級分けした。
【0073】
表5:未処理の部位及び日焼け止め剤で処理した部位へのUV線量の投与に対する、紅斑反応の評価基準
0 紅斑反応なし
1 わずかに認知できる紅斑
2 明らかに明確な境界を有する軽度の紅斑
3 はっきりとした境界を有する中度の紅斑*
4 はっきりとした境界を有するどす黒い紅斑*
5 はっきりとした境界を有して浮腫の可能性のある、どす黒い紅斑*
6 はっきりとした境界と浮腫を有する、はっきりと認知できる紅斑*
*中度、どす黒い、又ははっきりと認知できる紅斑が、暴露部位の境界に届かない場合は、説明が評価形式の所見欄に提供された。
【0074】
少なくとも2(明らかに明確な境界を有する軽度の紅斑)の等級の紅斑を生じさせる、一連のうちの第一暴露部位としてMEDを決定した。紅斑の等級の進行は、投与されたUV線量と一致した。
【0075】
日焼け反応があると判断されたら、対象は、おそらくタイプIVであり、試験に適任ではない。このケースでは、この対象を、試験から除外し、交替させた。各UV暴露部位の等級、すべてのコメント、及び評価時間を記録した。
【0076】
実際のスケジュールで必要であれば、対象は、その時に試験室を離れ、2日目の処置を終えるべく1週間以内に戻ることが許可された。
【0077】
[SPF決定のための製品の塗布]
試験の参加を中断していた場合は、この対象は、非指示的に質問されて、服薬順守を評価され、併用薬を同定され、有事事象を観察される。
【0078】
試験の技術者は、テンプレートと消えないマーカーを用いて、ベルトラインと肩甲骨の間の、対象の背中上の指定箇所に50cm2の矩形を複数描いた。次いで技術者は、100mgの試験製品をその指定された矩形内に塗布し、100mgのHMS規格を隣接する矩形に塗布した。材料を領域全域にわたり「点々と」をつけ指サックを用いて全域に均一な膜が塗布されるまで優しく伸ばすことにより、この日焼け止め剤を塗布した。
【0079】
技術者は、製品処方指示書、試験の部位の位置、及び塗布した時間を記録した。
【0080】
[静的SPF決定用のUV線量]
少なくとも15分かけて、技術者は、時間を定めたUV線量を、徐々に増やしながら続けて7回、試験製品で処理した部位に投与した。この一連の線量は、各試験製品の予想されるSPFの製品、対象のMED、及び以下の数字によって決定した。

【0081】
技術者は、各試験製品につき、完了した回数及びランプの効果的な放射照度の測定値を記録した。
【0082】
[HMS規格用UV線量]
少なくとも15分かけて、技術者は、時間を定めたUV線量を、徐々に増やしながら続けて7回、HMS規格部位に投与した。一連の線量は、HMS規格SPF(4)の製品、対象のMED、及び以下の数字により決定した。

【0083】
技術者は、HMS規格用のUV線量、完了した回数及びランプの効果的な放射照度の測定値を記録した。
【0084】
[反復MED決定用のUV線量]
技術者は、背中の非保護領域に、時間を定めたUV線量を続けて5回、25パーセントずつ増やして投与した。一連の5回の線量は、以下に示す中心の当初MEDを含んでいた。

【0085】
反復MED用のUV線量、完了した回数及びランプの効果的な放射照度測定値を記録した。
【0086】
技術者は、静的SPF用のUV線量、HMS規格のSPF、及び反復MEDの完了後22時間乃至24時間以内に、評価のために試験室に戻るよう対象に指示した。
【0087】
[3日目]
[静的SPF及び反復MED用のUV線量に対する反応の評価]
対象は、試験室に戻ると、非指示的に質問されて、服薬順守を評価され、併用薬を同定され、有事事象を観察された。製品の塗布又はUV線量の投与に関与していない、訓練を受けた評価者が、表5に表示した基準を用いて、UV線量を受けた全ての部位を等級分けした。試験製品を塗布して、UV線量を投与した技術者は、評価者を補助することは許可されたが、この技術者が、UV反応の等級について、評価者に影響を与えることは許可されなかった。日焼け止め剤が処理された全ての部位の反応の等級を記録した。
【0088】
[SPFの計算]
技術者は、上記のように反復MEDを決定して、各対象のSPF値を計算した。
【0089】
反復MEDが決定できない場合、最終MEDが反復MEDされた。このケースでは、初期MEDを、最終MEDとして使用する。
【0090】
SPF値を、最終MEDに対する、日焼け止め剤で保護した部位のMEDの比率として計算した。
【0091】
ラベルされたSPFを、20人の対象に基づいて、以下のように算出した。
平均SPF値−A
(小数第一位を切り捨てる)
ここでは、A=ts/sqrt(n)
t=生徒の分布の上位5%
s=標準偏差
n=対象の数
【0092】
パネルが有効であるときは、HMS規格の日焼け止め剤のSPFが、予想されるSPF(すなわち、4.47±1.279)の標準偏差内にあり、HMS規格の日焼け止め剤の平均SPFに関する95%の信頼区間は、値4を含むはずである。
【0093】
[有事事象]
あらゆる有事事象を、対象のファイルと、必要に応じて得られる即時の治療において記録した。致命傷である又は緊急処置と定義されるいかなる深刻な有事事象も、24時間以内にスポンサーに報告した。全ての有事事象を、スポンサーに報告した。
【0094】
[対象の交替]
服薬順守をしない又は有事事象により不適格と見なされた対象を全て交替させた。対象のデータに、SPF値に関して望み通りの計算ができない理由がある場合は、その対象を交替させることになっていた。
【0095】
[参考文献]
1.米国の食品及び薬物の投与;店頭販売のヒト用日焼け止め薬物製品;最終医薬品基準;21CRF部分310、352、700、及び740。Federal Register 64(98)、1999年5月21日、27666−27693頁。
【0096】

【特許請求の範囲】
【請求項1】
創傷の治癒を促進させるとともに、前記創傷の部位において後に創成される皮膚組織の特性を向上させる、塗り広げることができる製剤であって、当該製剤が:
a)揮発性成分と;
b)前記揮発性成分が蒸発する間に、約95乃至100華氏温度の範囲で、シロキサンマトリクスを形成することができるシロキサンマトリクス前駆体と;
c)前記シロキサンマトリクス前駆体に低混和性及び低溶解性を有する活性成分と;
d)揮発性助剤と;を含み、
前記揮発性助剤が、前記活性成分とともに複合体を形成して、可溶性の活性成分を形成することができ、前記複合体が、前記シロキサンマトリクス前駆体に混和性であり、前記シロキサンマトリクスの形成時に、前記揮発性助剤の全部又は一部分が、前記製剤から蒸発することを特徴とする製剤。
【請求項2】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、約6乃至13個の範囲の炭素原子の炭素鎖長を有する直鎖酸と、メタノール、エタノール、又は約3乃至8個の範囲の炭素原子の総炭素含有量を有する第二アルコールとのエステルであることを特徴とする製剤。
【請求項3】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、三又はそれ以上の炭素の直鎖と、一又はそれ以上のヒドロキシル基でなるグリコールであり;全てのヒドロキシル基が、終末炭素を含む隣接する炭素上にあることを特徴とする製剤。
【請求項4】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、置換イソソルビド又は非置換イソソルビドであることを特徴とする製剤。
【請求項5】
請求項1に記載の塗り広げることができる製剤において、前記活性成分が、日焼け止め作用を有する薬剤を含むことを特徴とする製剤。
【請求項6】
請求項1に記載の塗り広げることができる製剤において、前記活性成分が、抗ヒスタミン作用又は鎮痛作用を有する薬剤を含むことを特徴とする製剤。
【請求項7】
請求項5に記載の塗り広げることができる製剤において、前記活性成分が、オクトクリレン(ISPエスカロール597)、オクチノキサート(ISPエスカロール557)、オクチサレート(ISPエスカロール587)、又はオキシベンゾン(ISPエスカロール567)の一又はそれ以上を含むことを特徴とする製剤。
【請求項8】
請求項6に記載の塗り広げることができる製剤において、前記成分が、米国薬局方の酢酸ヒドロコルチゾンを含むことを特徴とする製剤。
【請求項9】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、ジメチルイソソルビドを含むことを特徴とする製剤。
【請求項10】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、ミリスチン酸イソプロピルを含むことを特徴とする製剤。
【請求項11】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、ペンチレングリコールを含むことを特徴とする製剤。
【請求項12】
請求項6に記載の塗り広げることができる製剤において、前記揮発性助剤が、ミリスチン酸イソプロピルを含むことを特徴とする製剤。
【請求項13】
請求項8に記載の塗り広げることができる製剤において、前記揮発性助剤が、ジメチルイソソルビドを含むことを特徴とする製剤。
【請求項14】
請求項13に記載の塗り広げることができる製剤において、前記揮発性助剤が、ペンチレングリコールを含むことを特徴とする製剤。
【請求項15】
請求項1に記載の塗り広げることができる製剤において、前記シロキサンマトリクス前駆体が、ジメチコンクロスポリマ、ヒュームドシリカ、及びジメチコンを含むことを特徴とする製剤。
【請求項16】
請求項1に記載の方法において、前記揮発性成分が、シクロペンタシロキソンであることを特徴とする方法。
【請求項17】
創傷の治癒を促進させ、瘢痕組織を回復させる、塗り広げることができる製剤の調製方法であって、前記製剤が;
a)揮発性成分と;
b)前記揮発性成分が蒸発する間に、約95乃至100華氏温度の範囲で、シロキサンマトリクスを形成することができるシロキサンマトリクス前駆体と;
c)前記シロキサンマトリクス前駆体に低混和性及び低溶解性を有する活性成分と;
d)揮発性助剤と;を含み、
前記揮発性助剤が、前記活性成分とともに複合体を形成して、可溶性の活性成分を形成することができ、前記複合体が、前記シロキサンマトリクス前駆体に混和性であり、前記シロキサンマトリクスの形成時に、前記揮発性助剤の全部又は一部分が、前記製剤から蒸発するものであり、
前記方法が、
a)前記活性成分を提供するステップと;
b)前記揮発性助剤を提供するステップと;
c)シロキサンマトリクス前駆体を提供するステップと;
d)混和性を有する、前記揮発性助剤と前記活性成分との複合体を形成するステップと;
を具えることを特徴とする方法。
【請求項18】
請求項17に記載の方法であって、前記シロキサンマトリクス前駆体が、ジメチルクロスポリマ、ヒュームドシリカ、及びジメチコンを含み、前記揮発性成分が、シクロペンタシロキサンを含むことを特徴とする方法。
【請求項19】
請求項17に記載の方法であって、前記揮発性助剤が、ミリスチン酸イソプロピルを含み、前記活性成分が、オクトクリレン(ISPエスカロール597)、オクチノキサート(ISPエスカロール557)、オクチサレート(ISPエスカロール587)、又はオキシベンゾン(ISPエスカロール567)の一又はそれ以上を含むことを特徴とする方法。
【請求項20】
請求項17に記載の方法であって、前記揮発性助剤が、ペンチレングリコール及び/又はジメチルイソソルビドを含み、前記活性成分が、酢酸ヒドロコルチゾンを含むことを特徴とする方法。
【請求項1】
創傷の治癒を促進させるとともに、前記創傷の部位において後に創成される皮膚組織の特性を向上させる、塗り広げることができる製剤であって、当該製剤が:
a)揮発性成分と;
b)前記揮発性成分が蒸発する間に、約95乃至100華氏温度の範囲で、シロキサンマトリクスを形成することができるシロキサンマトリクス前駆体と;
c)前記シロキサンマトリクス前駆体に低混和性及び低溶解性を有する活性成分と;
d)揮発性助剤と;を含み、
前記揮発性助剤が、前記活性成分とともに複合体を形成して、可溶性の活性成分を形成することができ、前記複合体が、前記シロキサンマトリクス前駆体に混和性であり、前記シロキサンマトリクスの形成時に、前記揮発性助剤の全部又は一部分が、前記製剤から蒸発することを特徴とする製剤。
【請求項2】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、約6乃至13個の範囲の炭素原子の炭素鎖長を有する直鎖酸と、メタノール、エタノール、又は約3乃至8個の範囲の炭素原子の総炭素含有量を有する第二アルコールとのエステルであることを特徴とする製剤。
【請求項3】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、三又はそれ以上の炭素の直鎖と、一又はそれ以上のヒドロキシル基でなるグリコールであり;全てのヒドロキシル基が、終末炭素を含む隣接する炭素上にあることを特徴とする製剤。
【請求項4】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、置換イソソルビド又は非置換イソソルビドであることを特徴とする製剤。
【請求項5】
請求項1に記載の塗り広げることができる製剤において、前記活性成分が、日焼け止め作用を有する薬剤を含むことを特徴とする製剤。
【請求項6】
請求項1に記載の塗り広げることができる製剤において、前記活性成分が、抗ヒスタミン作用又は鎮痛作用を有する薬剤を含むことを特徴とする製剤。
【請求項7】
請求項5に記載の塗り広げることができる製剤において、前記活性成分が、オクトクリレン(ISPエスカロール597)、オクチノキサート(ISPエスカロール557)、オクチサレート(ISPエスカロール587)、又はオキシベンゾン(ISPエスカロール567)の一又はそれ以上を含むことを特徴とする製剤。
【請求項8】
請求項6に記載の塗り広げることができる製剤において、前記成分が、米国薬局方の酢酸ヒドロコルチゾンを含むことを特徴とする製剤。
【請求項9】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、ジメチルイソソルビドを含むことを特徴とする製剤。
【請求項10】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、ミリスチン酸イソプロピルを含むことを特徴とする製剤。
【請求項11】
請求項1に記載の塗り広げることができる製剤において、前記揮発性助剤が、ペンチレングリコールを含むことを特徴とする製剤。
【請求項12】
請求項6に記載の塗り広げることができる製剤において、前記揮発性助剤が、ミリスチン酸イソプロピルを含むことを特徴とする製剤。
【請求項13】
請求項8に記載の塗り広げることができる製剤において、前記揮発性助剤が、ジメチルイソソルビドを含むことを特徴とする製剤。
【請求項14】
請求項13に記載の塗り広げることができる製剤において、前記揮発性助剤が、ペンチレングリコールを含むことを特徴とする製剤。
【請求項15】
請求項1に記載の塗り広げることができる製剤において、前記シロキサンマトリクス前駆体が、ジメチコンクロスポリマ、ヒュームドシリカ、及びジメチコンを含むことを特徴とする製剤。
【請求項16】
請求項1に記載の方法において、前記揮発性成分が、シクロペンタシロキソンであることを特徴とする方法。
【請求項17】
創傷の治癒を促進させ、瘢痕組織を回復させる、塗り広げることができる製剤の調製方法であって、前記製剤が;
a)揮発性成分と;
b)前記揮発性成分が蒸発する間に、約95乃至100華氏温度の範囲で、シロキサンマトリクスを形成することができるシロキサンマトリクス前駆体と;
c)前記シロキサンマトリクス前駆体に低混和性及び低溶解性を有する活性成分と;
d)揮発性助剤と;を含み、
前記揮発性助剤が、前記活性成分とともに複合体を形成して、可溶性の活性成分を形成することができ、前記複合体が、前記シロキサンマトリクス前駆体に混和性であり、前記シロキサンマトリクスの形成時に、前記揮発性助剤の全部又は一部分が、前記製剤から蒸発するものであり、
前記方法が、
a)前記活性成分を提供するステップと;
b)前記揮発性助剤を提供するステップと;
c)シロキサンマトリクス前駆体を提供するステップと;
d)混和性を有する、前記揮発性助剤と前記活性成分との複合体を形成するステップと;
を具えることを特徴とする方法。
【請求項18】
請求項17に記載の方法であって、前記シロキサンマトリクス前駆体が、ジメチルクロスポリマ、ヒュームドシリカ、及びジメチコンを含み、前記揮発性成分が、シクロペンタシロキサンを含むことを特徴とする方法。
【請求項19】
請求項17に記載の方法であって、前記揮発性助剤が、ミリスチン酸イソプロピルを含み、前記活性成分が、オクトクリレン(ISPエスカロール597)、オクチノキサート(ISPエスカロール557)、オクチサレート(ISPエスカロール587)、又はオキシベンゾン(ISPエスカロール567)の一又はそれ以上を含むことを特徴とする方法。
【請求項20】
請求項17に記載の方法であって、前記揮発性助剤が、ペンチレングリコール及び/又はジメチルイソソルビドを含み、前記活性成分が、酢酸ヒドロコルチゾンを含むことを特徴とする方法。
【図1】




【公表番号】特表2012−530719(P2012−530719A)
【公表日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願番号】特願2012−516337(P2012−516337)
【出願日】平成22年6月18日(2010.6.18)
【国際出願番号】PCT/US2010/039181
【国際公開番号】WO2010/148310
【国際公開日】平成22年12月23日(2010.12.23)
【出願人】(511307100)アドバンスド バイオ−テクノロジーズ,インコーポレイテッド (1)
【氏名又は名称原語表記】ADVANCED BIO−TECHNOLOGIES,INC.
【Fターム(参考)】
【公表日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願日】平成22年6月18日(2010.6.18)
【国際出願番号】PCT/US2010/039181
【国際公開番号】WO2010/148310
【国際公開日】平成22年12月23日(2010.12.23)
【出願人】(511307100)アドバンスド バイオ−テクノロジーズ,インコーポレイテッド (1)
【氏名又は名称原語表記】ADVANCED BIO−TECHNOLOGIES,INC.
【Fターム(参考)】
[ Back to top ]

