癌の治療法
本発明は、癌の治療に使用される組成物、キット及び方法を提供する。特に、本発明は、ポリ−ADP−リボースポリメラーゼを阻害することにより対象における癌を治療する組成物及び方法、並びにかかる組成物を投与する剤形及び方式を提供する。
【発明の詳細な説明】
【背景技術】
【0001】
本出願は2006年9月5日出願の米国仮特許出願の利益を請求する。本出願はその全体が参照により本明細書に組み込まれる。
【0002】
癌は現代社会における深刻な脅威である。悪性癌増殖は、その独自の特徴ゆえに、現代医学の重大な課題となっている。その特徴としては、悪性組織の無秩序な増殖をもたらす制御できない細胞増殖、局所組織やさらには遠隔組織を侵入する能力、分化の欠乏、検出できる症状の欠乏、最も重要な点としては、効果的治療及び予防の欠乏が挙げられる。
【0003】
癌は任意の年齢で、且つ、任意の器官の組織又は任意の組織で進行する。癌の病因は明確には定義されていないが、遺伝的感受性、染色体破損障害、ウィルス、環境因子及び免疫学的障害等の機構が、何れも悪性細胞増殖及び悪性化と関連付けられてきた。癌は、世界数百万人に広く影響を及ぼす多くの種類の医学的状態を包含する。癌が発症するのは、身体の一部の細胞が未分化となり始め、或いは無制御下で増殖し始める場合である。何れの癌型も異常細胞の無制御な増殖と共に開始する。
【0004】
癌には多くの種類、例えば乳癌、肺癌、卵巣癌、膀胱癌、前立腺癌、膵臓癌、頸癌及び白血病が存在する。現在、利用できる主な治療としては、手術、放射線療法、及び化学療法が挙げられる。手術は多くの場合、抜本的な治療であり、深刻な結果をもたらす。例えば、卵巣癌の処理は何れも、不妊症及び/又は性的機能障害をもたらし得る。頸癌及び膀胱癌の処理には、不妊症を引き起すものがある。膵臓癌を治療する手術は、膵臓の部分的又は全体の除去をもたらし、患者に対する重度の危険性を有する。前立腺癌の手術の中には、尿失禁及び性的不能の危険性を有するものがある。肺癌患者の手術は多くの場合、癌性肺組織に接近してこれを除去する必要上、肋骨を切除せねばならず、術後に激しい痛みを生ぜさせる。さらに、肺癌及び肺疾患、例えば気腫又は慢性気管支炎を有する患者には通常、術後に息切れの増加が見られる。
【0005】
放射線療法は、癌細胞殺害の利点を有するものの、同時に非癌性組織に損傷を与える。化学療法は、患者への種々の抗癌剤の投与を包含するが、副作用を伴う場合が多い。
【0006】
世界で1千万人以上の人々が毎年、癌保有患者との診断を受けており、この数は2020年まで新規患者が毎年1千5百万人ずつ上昇することが予測される。癌によって死亡する人は毎年6百万人と、全世界の死亡数の12%を占めている。癌を治療し得る方法が依然として求められている。かかる方法によって、ヒト及び他の哺乳類における癌の予防及び治療に有用な医薬組成物の基礎が提供され得る。
【0007】
一連の抗腫瘍薬物が同定されている。それらの薬物は、ニトロ及びニトロソ化合物及びそれらの代謝物を含み、それらは、“抗ウィルス及び抗腫瘍剤として有用な芳香族ニトロ及びニトロソ化合物及びそれらの代謝物”の名称の1995年11月7日に発行されたアメリカ特許第5,454,871号、“抗ウィルス及び抗腫瘍剤として有用な芳香族ニトロ及びニトロソ化合物及びそれらの代謝物”の名称の1997年9月23日に発行されたアメリカ特許第5,670,518号、“芳香族ニトロ及びニトロソ化合物、及びそれらの代謝物による癌の治療方法”の名称の1999年12月21日に発行されたアメリカ特許第6,004,978号の主題であり、それらの開示は引用により本明細書に組込まれる。それらの化合物の使用は、乳腺癌、乳腺管癌、リンパ性白血病、AIDSを有する免疫制御された患者におけるカポジ肉腫、及び新形成増殖、例えば非ホドキシのリンパ腫、及び一次リンパ腫の処理において有用なものとして当業界において記載されている。しかし、抗腫瘍活性を有する追加の化合物を同定する必要がある。前駆体化合物から単離された代謝物は、個々に、又は種々の癌細胞を標的化する他の化合物と組合せて使用され得る抗腫瘍剤を提供する。
【発明の概要】
【課題を解決するための手段】
【0008】
本発明は一般的に、芳香族ニトロベンズアミド代謝化合物を用いての腫瘍形成疾病の治療方法に関する。より特定には、それは、ニトロ化合物ベンズアミド前駆体分子由来のニトロベンズアミド代謝化合物、及び哺乳類における腫瘍増殖の抑制及び阻害への、前記代謝物、又はその塩、溶媒化合物、異性体、互変異体、代謝物、類似体又はプロドラッグの使用に関する。
【0009】
本発明の1つの観点においては、式(Ia)の化合物及び1又は2以上の追加の薬理学的活性剤を含んでなる医薬組成物の投与を含んでなる、癌及び癌に関する阻害の処理方法が提供される。もう1つの観点においては、式(Ia)の化合物由来の代謝化合物及びブチオニンスルホキシミン(BSO)の組合せの投与を含んでなる、癌及び癌に関連する阻害の処理方法が提供される。前記代謝物はまた、BSOを伴って又はそれを伴わないで、式(II)のベンゾヒロン化合物と組合せても投与され得る。
【0010】
それらの観点の態様は、種々の癌、例えば白血病、乳癌、卵巣癌、膀胱癌、前立腺癌、膵臓癌及び頸癌、並びに本明細書に記載される他の癌タイプの処理方法を包含する。
【0011】
本発明は、物質の組成物及び医薬組成物、及び癌の治療へのそれらの使用方法に関する。例えば、本発明の組成物は、本明細書に記載される複数の化合物の組合せ、及び/又は本明細書に記載される複数形の化合物の組合せであり得る。本発明の医薬組成物は、対象への投与のために適切な組成物であり得る。
【図面の簡単な説明】
【0012】
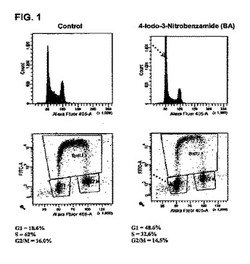
【図1】図1(FACSドットプロット及びヒストグラム)は、PARP−1阻害剤(4−ヨード−3−ニトロベンズアミド又は“BA”)により19時間、処理されたHTC116細胞における細胞周期分析を示す。BA処理は、対照(18.6%)に比較して、S期細胞周期の同時低下と共に、G1期における細胞数の低下(48.6%)を引起した。
【図2】図2(FACSドットプロット及びヒストグラム)は、PARP−1阻害剤BA、4−ヨード−3−ニトロベンズアミド(BNO)及び4−ヨード−3−ヒドロキシアミノベンズアミド(BNHOH)により24時間、処理されたHela細胞の周期分析を示す。細胞周期のS期におけるBrdU染色ラベル細胞。有糸分裂におけるGF7染色ラベル細胞。
【図3】図3(FACSドットプロット及びヒストグラム)は、PARP−1阻害剤BA、4−ヨード−3−ニトロベンズアミド(BNO)及び4−ヨード−3−ヒドロキシアミノベンズアミド(BNHOH)により72時間、処理されたHela細胞の周期分析を示す。細胞周期のS期におけるBrdU染色ラベル細胞。有糸分裂におけるGF7染色ラベル細胞。
【図4】図4は、雌SCIDマウスにおけるヒトOVCAR−3卵巣腺癌異種移植片におけるBA活性を示す。BAは、50mg/kg/用量で経口b.i.d.投与されるか、又は25mg/kg/週の用量で浸透ポンプによりs.c.投与される。
【図5】図5は、BAが、MDR1をアップレギュレートする多薬物耐性細胞、及びMDR1−陰性細胞を標的化することを示す。図5Aは、KB3−1細胞におけるMDR1発現のレベルを示す。図5Bは、KB V−1細胞におけるMDR1発現のレベルを示す。FACSヒストグラムは、KB V−1細胞におけるMDR1の過剰発現を示す。MDR1の過剰発現は、多薬物耐性に関連しているので、図5Cに示されるように、BAがK3−1及びKB V−1細胞の両者において用量依存性細胞死をもたらすことは注目に値する。
【発明を実施するための形態】
【0013】
本明細書で言及される出版物及び特許出願は何れも、各出版物又は特許出願について個別具体的に参照により本明細書に組込まれる旨を記載したのと同様に、参照により本明細書に組込まれる。
【0014】
「ニトロベンズアミド前駆体化合物」は、下記式(Ia):
【化1】

[式中、R1、R2、R3、R4及びR5は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C4)シクロアルキル及びフェニルからなる群から独立して選択され、ここで5種のR1、R2、R3、R4及びR5置換基の少なくとも2つは常に水素であり、5種の置換基の少なくとも1つは常にニトロであり、ニトロに隣接して位置する少なくとも1つの置換基は常にヨードである]で表される化合物、及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグを意味する。R1、R2、R3、R4及びR5はまた、ハロゲン化物、例えばクロロ、フルオロ又はブロモであり得る。“前駆体化合物”とは、代謝化合物をもたらす、1又は2以上の化学的又は生化学的工程(例えば、細胞又は生物における)を受ける化合物である。用語“前駆体”、“前駆体化合物”、“ベンズアミド前駆体”又は“ニトロベンズアミド前駆体”とは本明細書において、交換可能的に使用される。
【0015】
“代謝物”とは、出発化合物の生成物とは、構造的に異なる生成物をもたらすいずれかのインビトロ又はインビボ代謝工程を通して生成される化合物を意味する。用語“代謝物”とは、ニトロベンズアミド代謝化合物を包含する。代謝物は、前駆体化合物、例えば式(Ia)で示される前駆体化合物に対していずれかの位置で存在する種々の数又はタイプの置換基を含むことができる。さらに、代謝物は、本明細書に示される化合物に対していずれかの位置で存在する多くのタイプの置換基で異なることができる。さらに、用語“代謝物”、“代謝化合物”、“ベンズアミド代謝化合物”又はニトロペンズアミド代謝的化合物“は、本明細書において交換可能的に使用される。
【0016】
“手術”とは、治癒、治療又は診断効果を得るために、ヒト又は他の哺乳類の身体に対する手動的又は器具を伴っての手動的作用を包含するいずれかの治療又は診断方法を意味する。
【0017】
“放射線療法”とは、高エネルギー放射線、例えばX−線、γ−線及び中性子(但し、それらだけには制限されない)への患者の照射を意味する。このタイプの治療は、外部放射線療法、内部放射線療法、移植物放射線、近接照射療法、全身性放射線療法及び放射線療法を包含するが、但しそれらだけには限定されない。
【0018】
“化学療法”とは、種々の方法、例えば静脈、経口、筋肉内、腹腔内、膀胱内、皮膚、経皮、頬内又は吸入によるか又は坐薬の形での癌患者への1又は2以上の抗癌剤及び/又は他の剤の投与を意味する。化学療法は、大きな腫瘍を縮小するために手術の前、その腫瘍を除去するために手術工程の前、身体におけるいずれかの残存する癌細胞の増殖を妨げるために手術又は放射線療法の後、与えられ得る。
【0019】
用語“有効量”又は“医薬的有効量”とは、所望する生物学的、治療及び/又は予防結果を提供するために、非毒性であるが、しかし十分な量の剤を言及する。この結果は、疾病の微候、症状又は原因の低減及び/又は軽減、又は生物学的システムのいずれか他の所望する変更であり得る。例えば、治療使用のための“有効量”とは、それ自体、本明細書に開示しているようなニトロベンズアミド代謝化合物、又は疾病において臨床学的に有意な低下をもたらすのに必要とされる本明細書におけるニトロベンズアミド代謝化合物を含んでなる組成物の量である。いずれか個々の場合、高められた有効量は、通常の実験を用いて当業者により決定され得る。
【0020】
“医薬的に許容し得る”又は“薬理学的に許容できる”とは、生物学的に又は他方では所望の材料を意味し、すなわち、前記材料は、いずれの所望しない生物学的効果も引起さないで、又は組成物に含まれるいずれかの成分とも、有害な態様で相互作用しないで、個人に投与され得る。
【0021】
用語“処理する”及びその文法的同義語は、本明細書で使用される場合、治療的有益性及び/又は予防的有益性を達成することを包含する。治療的有益性とは、処理される、基礎をなす障害の根絶又は改善を意味する。例えば疾患者においては、治療的有益性は、基礎をなす癌の根絶又は改善を包含する。また、治療的有益性は、患者が基礎をなす障害によりまだ苦しめられている事実にもかかわらず、患者に改善が観察されるよう、その基礎をなす障害に関連する1又は2以上の生理学的症状の根絶又は改善により達成される。予防的有益性に関しては、本発明の方法は、癌の進行の危険性での患者に、又は病状の診断が行われていなかったとしても、そのような病状の1又は2以上の生理学的症状を報告する患者に投与される本発明に組成物に基づいて実施され得る。
【0022】
本明細書で使用される場合、“BA”とは、4−ヨード−ニトロベンズアミドを意味し;“BNO”とは、4−ヨード−3−ニトロソベンズアミドを意味し;“BNHOH”とは、4−ヨード−3−ヒドロキシアミノベンズアミドを意味する。
【0023】
(i)ニトロベンズアミド代謝化合物:
本発明において有用な前駆体化合物は、下記式(Ia):
【化2】

[式中、R1、R2、R3、R4及びR5は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C7)シクロアルキル及びフェニルからなる群から独立して選択され、ここで5種のR1、R2、R3、R4及びR5置換基の少なくとも2つは常に水素であり、前記5種の置換基の少なくとも1つは常に、ニトロであり、ニトロに隣接して位置する少なくとも1つの置換基は常にヨードである]で表される化合物、及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグである。R1、R2、R3、R4及びR5はまた、ハロゲン化物、例えばクロロ、フルオロ、又はブロモ置換基でもあり得る。
【0024】
式Iaの好ましい前駆体化合物は、下記式の化合物である。
【化3】

【0025】
本発明において有用な代謝物は、下記式(IIa):
【化4】

[式中、(1)R1、R2、R3、R4及びR5置換基の少なくとも1つは常に硫黄含有置換基であり、残る置換基R1、R2、R3、R4及びR5は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、ブロモ、フルオロ、クロロ、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C7)シクロアルキル及びフェニルからなる群から独立して選択され、ここで5種のR1、R2、R3、R4及びR5置換基の少なくとも2つが常に水素であり;又は(2)R1、R2、R3、R4及びR5置換基の少なくとも1つは硫黄含有置換基ではなく、5種の置換基R1、R2、R3、R4及びR5の少なくとも1つは常にヨードであり、前記ヨードは、ニトロ、ニトロソ、ヒドロキシアミノ、ヒドロキシ又はアミノ基のいずれかであるR1、R2、R3、R4及びR5基に常に隣接している]で表される化合物、及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグである。幾つかの態様においては、(2)の化合物は、ヨード基が、ニトロソ、ヒドロキシアミン、ヒドロキシ又はアミノ基であるR1、R2、R3、R4及びR5基に常に隣接するようなものである。
【0026】
次の組成物は好ましい代謝化合物であり、個々は、下記化学式により表される。
【化5】

[前記式中、R6は、水素、アルキル(C1−C8)、アルコキシ(C1−C8)、イソキノリノン、インドール、チアゾール、オキサゾール、オキサジアゾール、チフェン又はフェニルからなる群から選択される]
【化6】

【0027】
【化7】

【0028】
いずれか1つの特定の機構に限定されないが、次のスキームは例えば、ニトロレダクターゼ又はグルタチオン接合機構を通してのMS292代謝を提供する。
【化8】

【0029】
BAグルタチオン接合及び代謝:
【化9】

【0030】
本発明は、他の乳癌、例えば乳腺における腺管癌、他の形の白血病、例えば末梢血液における急性前骨髄細胞性白血病、卵巣癌、肺癌、膀胱癌、前立腺癌、膵臓癌及び頸癌、並びに本明細書に記載される他の癌型の処理のためへの前述のニトロベンズアミド代謝化合物の使用を提供する。
【0031】
ニトロベンズアミド代謝化合物は悪性癌細胞に対して選択的細胞毒性を有するが、しかし非悪性癌細胞に対してはそうではないことが報告されている。Rice et at , Proc Natl Acad Sci USA 89-7703-7707 (1992)を参照のこと。1つの態様においては、本発明の方法に使用されるニトロベンズアミド代謝化合物は、非腫瘍細胞よりも腫瘍細胞に対してより選択的毒性を示すことができる。
【0032】
ニトロベンズアミド及びニトロソベンズアミド化合物の腫瘍形成性が、BSOが癌細胞に同時投与される場合、増強されることは報告されている。Mendeleyev et al , Biochemical Pharmacol 50(5) 705- 714 (1995)を参照のこと。ブチオニンスルホキシミン(BSO)は、化学療法に対する細胞耐性を一部、担当するγ−グルタミルシステインシンセターゼ、すなわちグルタチオンの生合成におけるキー酵素を阻害する。Chen et al , Chem Biol Interact Apr 24,111-112 263-75 (1998)を参照のこと。本発明はまた、BSOと組合せてのニトロベンズアミド代謝化合物及び/又はベンゾピロン化合物の投与を含んでなる、癌の治療方法も提供する。他方では、代謝化合物は、前駆体化合物及び/又はベンゾピロンと共に投与され得る。
【0033】
BSOの他に、γ−グルタミルシステインシンセターゼの他の阻害剤は、ニトロベンズアミド及び/又はベンゾピロン化合物と組合せて使用され得る。BSOの他の適切な類似体は、プロプロチオニンスルホキシミン、メチオニンスルホキシミン、エチオニンスルホキシミン、メチルブチオニンスルホキシミン、γ−グルタミル−α−アミノブチレート及びγ−グルタミルシステインを包含するが、但しそれらだけには限定されない。
【0034】
ベンゾピロン化合物:
幾つかの態様において、代謝化合物は、ベンズアミド化合物及び/又は式IIのベンゾピロンと組合せて投与される。式IIのベンゾピロン化合物は、下記式:
【化10】

[式中、R1、R2、R3及びR4は、H、ハロゲン、任意に置換されたヒドロキシ、任意に置換されたアミン、任意に置換された低級アルキル、任意に置換されたフェニル、任意に置換されたC1−C10へテロアリール、及び任意に置換されたC3−C8シクロアルキルからなる群から独立して選択される]で表される化合物、又はその塩、溶媒化合物、異性体、互変異体、代謝物又はプロドラッグである。
【0035】
好ましい態様においては、本発明は、下記式IIのベンゾピロン化合物に関する。
【化11】

【0036】
(ii)ニトロベンズアミド代謝化合物の機構:
作用の1つの機構により制限されるものではないが、本明細書に記載される化合物は、ポリ(ADP−リボース)ポリメラーゼ酵素の調整を通して抗癌性質を有すると思われる。薬物の作用機構は、核酵素ポリ(ADP−リボース)ポリメラーゼ(PARP−1)のためのリガンドとして作用するそれらの能力に関連している。Mendeleyevなど、前記(1995)を参照のこと。PARP−1は、核において発現され、ニコチンアミド及びポリ−ADP−リボース(PAR)へのβ−ニコチンアミドアデニンジヌクレオチド(NAD+)の転換を触媒する。恒常性条件下でのPARP−1の役割は、DNA転写及び修復に制限されると思われる。しかし、細胞ストレスがDNA損傷を引き起す場合、PARP−1活性は劇的に上昇し、これはゲノム結合性のために必要であると思われる。Shall et at., Mutat Res. Jun 30;460(l):l-15 (2000)を参照のこと。さらに、PARP−1は酵素のPARPフェミリーの最良の既知メンバーであるが、作用の機構はPARPファミリーのいずれかのメンバー(例えば、PARP−2〜PARP−18、又は作用の類似する機構により作用することが発見された追加のメンバー、又はPARP−1の共有する類似機構体)に同等に適用できる。
【0037】
PARP−1の1つの機構は、生ポリマーポリ(ADP−リボース)の合成である。ポリ(ADP−リボース)及びPARP−1の両者は、DNA修復、アポプトシス、ゲノム安定性の維持及び発癌の修復に連結されて来た。Masutani et al., Genes, Chromosomes, and Cancer 38:339-348 (2003)を参照のこと。PARP−1は、DNA修復、特に塩基除去修復(BER)において役割を演じる。BERは単一塩基DNA破壊のための哺乳類細胞における保護機構である。PARP−1は、高い親和性で、その亜鉛フィンガードメインを通してDNAフラグメントの端に結合し、それにより、DNA損傷センサーとして作用する。Gradwohl et al., Proc. Natl. Acad. Sci. USA 87:2990-2994を参照のこと。DNAにおける破壊は、破壊の部位へのPARP−1による結合応答を誘発する。次に、PARP−1は、その触媒活性を数百倍、高め(Gradwohl et al., Proc. Natl. Acad. Sci. USA 87:2990-2994 (1990); Murcia et al., Trends Biochem. Sci 19: 172-176 (1994)を参照のこと)、自然にポリADP−リボシル化(Simonin et al., J Biol. Chem. 278: 13454-13461 (1993))及びBERタンパク質、例えばDNA−依存性タンパク質キナーゼ(DNA−PKcs)及び分子骨格タンパク質XRCC−1を転換し始める。Ruscetti et al., J. Biol. Chem. Jun 5;273(23):14461- 14467 (1998)を参照のこと。BERタンパク質は、DNA損傷の部位に急速に補充される。El-Kaminsy et al., Nucleic Acid Res. 31(19):5526-5533 (2003); Okano et al., MoI Cell Biol. 23(11):3974-3981 (2003)を参照のこと。PARP−1は、DNA分解部位から解離するが、しかしDNA修復現象の付近に依存する。
【0038】
PARP分子の活性の阻害は、それらの分子の活性の低減を包含する。用語“阻害する”及びその分法的な語形変化、例えば“阻害の”とは、PARP活性の完全な低減を必要とするものではない。そのような低減は好ましくは、阻害効果の不在下で、例えば阻害剤、例えば本発明のニトロベンズアミド代謝化合物の不在下で、分子の活性の少なくとも約50%、少なくとも約75%、少なくとも約90%及びより好ましくは少なくとも95%である。最も好ましくは、この用語は、活性における観察できるか又は測定できる低減を言及する。処理シナリオにおいては、好ましくは、阻害は、処理される病状において治療及び/又は予防有益性を生成するのに十分である。用語“阻害しない”及びその文法的な語形変化は、活性に対する効果の完全な結合を必要としない。例えば、それは、阻害剤、例えば本発明のニトロベンズアミド代謝化合物の存在下で、PARP活性の約20%以下、約10%以下及び好ましくは約5%以下である情況を言及する。
【0039】
作用のもう1つの機構は、イノシン一リン酸デヒドロゲナーゼ(IMPDH)の阻害を包含する。IMPDHは、グアニレート、例えばGTP及びdGTPを供給する枝分かれプリンヌクレオチド合成路の律速酵素である。2種のIMPDHイソフォーム、すなわち全ての細胞に構成的に存在するタイプI、及び高増殖性細胞、例えば癌において誘発でき、存在するタイプIIが存在する。後者の酵素の阻害は、腫瘍細胞増殖及び複製のために必要である細胞内グアノシン分子の完全な消耗を引き起す。本発明の1又は2以上の代謝化合物は、IMPDHを標的化し、従って腫瘍細胞増殖を阻害し得る。
【0040】
作用のさらにもう1つの機構は、ヒストンデアシテラーゼ(HDAC)の阻害を包含する。転写因子プールにおける腫瘍関連の変更が、正常な増殖及び成長において重要な遺伝子の誤調節を導くことができる。キメラ性転写因子は、転写補リプレッサー及びそれらの関連するHDAC活性の異常補充により増殖調節標的遺伝子の転写抑制を引き起す。ヒト急性前骨髄細胞性白血病においては、レチノイン酸重要体を包含するキメラ性転写因子(PML−RARα及びPLZF−RARα)は、標的遺伝子、例えばRARβ遺伝子の転写を抑制すると思われている。転写補リプレッサー複合体は、HDAC活性を含み、転写補活性化因子複合体はヒストンアセチルトランスフェラーゼ活性を含む。HDAC阻害剤、例えばトリコスタチンA又はNaBuは、キメラ性転写因子PML−RARα及びPLZFRARαにより引起される転写抑制リプレッションを軽減し得る。HDAC阻害剤は単独で又はレチノイドと組合せて、明白な副作用を伴わないで、急性前骨髄細胞性白血病の動物も出るにおいて白血病緩解及び延長された生存性を誘発することが示されている。
【0041】
ヒストンのアセチル化及び脱アセチル化は、DNAとのヒストンの相互作用に影響を及ぼすことにより、高次クロマチン構造を変更する。転写因子はまたアセチル化され得、アセチル化されたそれらのタンパク質の状態は、DNAとのそれらの相互反応、及び他の転写補調節タンパク質と相互反応するそれらの能力に影響を及ぼすことができる。例えば、p53のアセチル化は、その配列特異的DNA結合活性を増強する。脱アセチル化されたヒストンは、細胞増殖に関連するが、ところが超アセチル化されたヒストンは細胞増殖阻止、分化及び/次にアポプトシスに関連している。
【0042】
例えば、Saitoなどは、MS−27−275、すなわちHDACを阻害する合成ベンゼン誘導体の効率を評価した。Saito et al. Proc Natl Acad Sci , 1999; 96: 4592-4597。多くの成熟腫瘍細胞系においては、MS−27−275は、μモル以下の範囲でのIC50を伴って腫瘍細胞増殖を阻害した。細胞増殖は、細胞周期阻止、及び細胞周期阻害剤p21の誘発を付随する。p.o.投与されたMS−27−275は、s.c.増殖されたヌードマウスにおける確立された完熟腫瘍系の増殖を最少の毒性を伴って阻害した。Jaboin et al Cancer Research, 2002, 62:6108-6115を参照のこと。
【0043】
HDAC阻害剤としての本発明の化合物は、転写活性を調節し得る。従って、本発明の化合物はまた、脈管形成及び細胞周期阻止し、アポプトシス及び分化を促進するよう作用し得る。腫瘍増殖のそれらのキー成分を標的化することにより、HDAC阻害剤は、高速移動細胞増殖抑制性市場において明確な位置を示す能力を有する。HDAC阻害剤がそのようなキー役割を演じる2つの主要理由は、それらが例えば存在する細胞増殖抑制物(例えば、レチノイド)の効率を改良するために他の処理レジメと当時に使用され得、さらに、それらが特定疾病を引き起す遺伝子の転写を標的化できることであり、それらは癌治療への前例のない治療窓を付与する。
【0044】
ベンズアミド代謝化合物の使用:
癌型:
【0045】
本発明は、幾つかの特定癌又は腫瘍を処理するための方法を提供する。例えば、癌型は、副腎皮層癌腫、肛門癌、再生不良性貧血、胆管癌、膀胱癌、骨癌、骨転移、成人CNS脳腫瘍、子供CNS脳腫瘍、乳癌、カースルマン疾患、子宮頚部腫瘍、幼児期非ホジキンリンパ腫、結腸及び直腸癌、子宮内膜癌、食道癌、Ewingファミリーの腫瘍、眼癌、胆嚢癌、胃腸の類癌腫、消化管間質腫瘍、妊娠期間絨毛性疾患、悪性リンパ腫、カポジ肉腫、腎癌、喉頭及び下咽頭癌、急性リンパ球性白血病、急性骨髄白血病、小児白血病、慢性リンパ球性白血病、慢性骨髄性白血病、肝臓癌、肺癌、肺カルチノイド腫瘍、非ホジキンリンパ腫、男性乳癌、悪性黒子症候群、多発性骨髄腫、骨髄形成異常症候群、鼻腔及び副鼻腔癌、上咽頭癌、神経芽、口腔及び中咽頭癌、骨肉腫、卵巣癌、膵臓癌、陰茎癌、脳下垂体腫瘍、前立腺癌、網膜胚種細胞腫、横紋筋肉腫、唾液腺癌、肉腫(成人軟組織癌腫)、黒色腫皮膚癌、非黒色腫皮膚癌、胃癌、精巣癌、胸腺癌腫、甲状腺癌、子宮肉腫、腟癌、外陰部癌及びワルデンストロームマクログロブリン血症を包含する。
【0046】
甲状腺癌は、内分泌系の最も通常の悪性疾患である。甲状腺癌は、分化された腫瘍(乳頭又は小胞)及び不十分に分化された腫瘍(骨髄又は退形成)を包含する。膣癌は、鱗状細胞癌、腺癌、メラノーマ及び肉腫を包含する。精巣癌は、セミノーマ及び非セミノーマ型に広く分けられる。
【0047】
胸腺腫は、非新生物リンパ細胞により集中的に浸潤され得るか又は浸潤され得ない、胸腺の上皮腫瘍である。用語、胸腺腫は、上皮成分の明確な異型性を示さない新生物を説明するために通常使用される。もはや胸腺に対して特異的ではない、明確な細胞学的異型性及び組織学的特徴を示す胸腺上皮腫瘍は、胸腺癌(また、Cタイプ胸腺腫としても知られている)として知られている。
【0048】
本発明により提供される方法は、他の治療剤と組合せてのベンズアミド代謝化合物の投与を含んでなる。本発明の組成物と共に同時投与され得る治療の選択は、処理される状態に一部、依存するであろう。例えば、急性骨髄性白血病の処理に関しては、本発明の幾つかの態様のベンズアミド化合物が、放射線治療法、モノクローナル抗体療法、化学療法、骨髄移植、遺伝子療法、免疫学的療法、又はそれらの組合せと組合せて使用され得る。
【0049】
乳癌:
1つの観点においては、本発明は、乳癌、好ましくは乳腺における管組織における管癌を治療するための方法を提供する。
【0050】
本発明により提供される方法により処理され得る幾つかのタイプの乳癌が存在する。本来の位置での小葉癌及び管癌は、それぞれ小葉及び管において進行するが、しかし乳房を取囲む脂肪組織又は身体の他の領域には拡散しない癌である。浸潤性(又は侵入性)小葉及び管癌は、それぞれ小葉及び管において進行し、乳房の脂肪組織又は身体の他の部分のいずれかに拡散する癌である。本発明により提供される方法による処理から有益である乳房の他の癌は、骨髄性癌、コロイド状癌、管状癌及び炎症性乳癌である。
【0051】
乳癌患者のために利用できる処理は、手術、免疫療法、放射線療法、化学療法、内分泌療法又はそれらの組合せである。腫瘍摘除及び乳房切除は、乳癌患者のために利用できる2種の可能性ある手術法である。
【0052】
化学療法は、癌細胞の患者における増加、侵入、転移及び患者の殺害を妨げるために高腫瘍剤を利用する。幾つかの薬物、例えば細胞毒性薬物、例えばドキソルビシン、シクロホスファミド、メトトレキセート、パクリタキセル、チオテパ、ミトキサントロン、ビンクリスチン又はそれらの組合せが、乳癌を治療するために利用できる。この療法のために投与される剤は、タモキシフェン、酢酸メガストロール、アミノグルテチミド、フルオキシメステロン、ロイプロリド、ゴセレリン及びプレドニソンを包含する。
【0053】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法又は内分泌療法の組合せにより、乳癌患者に有益な効果を提供し得る。
【0054】
幾つかの態様においては、本発明は、いわゆる“三重陰性”乳癌の治療を提供する。従来のバイオマーカーにより同定される幾つかのサブクラスの乳癌、例えばエストロゲン受容体(ER)及び/又はプロゲステロン受容体(PR)陽性腫瘍、HER2増幅された腫瘍及びER/PR/HER2−陰性腫瘍が存在する。それらの3種のサブタイプは、多重乳癌における遺伝子発現フロフィーリングにより再現的に同定されており、基礎−様サブタイプの発現プロフィール及び不十分な予後を示す。三重陰性乳癌は、ER/PR/HER2−陰性腫瘍により特徴付けられる。
【0055】
卵巣癌:
もう1つの観点においては、本発明は、卵巣癌、例えば上皮卵巣腫瘍の処理方法を提供する。好ましくは、本発明は、次のものから選択された卵巣癌の治療方法を提供する:卵巣における腺癌、及び腹腔中への卵巣から移動した腺癌。手術、免疫療法、化学療法、ホルモン療法、放射線療法又はそれらの組合せが、卵巣癌のために利用できる幾つかの可能性ある処理法である。幾つかの可能性ある手術法は、減量化(debulking)、及び一側性卵巣摘除及び/又は一側性又はニ側性卵巣摘除を包含する。
【0056】
使用され得る抗癌剤は、シクロホスファミド、エトポシド、アルドレタミン及びイホスファミドを包含する。薬物タモキシフェンによるホルモン療法は、卵巣腫瘍を縮小するために使用され得る。放射線療法は、外部放射線療法及び/又は近接照射療法であり得る。
【0057】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、内分泌療法又はそれらのの組合せにより、卵巣癌患者に有益な効果を提供し得る。
【0058】
頸癌:
もう1つの観点においては、本発明は、頸癌、好ましくは頸部上皮における腺癌の治療方法を提供する。この癌の2種の主要型が存在する:鱗状細胞癌及び腺癌。前者は、全ての頸癌の80〜90%を構成し、子宮膣部(膣に近い部分)及び子宮頸内膜(子宮に近い部分)が連結する部分で進行する。後者は子宮頸内膜の粘膜生成腺細胞において進行する。幾つかの頸癌は、それらの両者の特徴を有しそして腺鱗状癌又は混合された癌と呼ばれる。
【0059】
頸癌のために利用できる主要処理は、手術、免疫療法、放射線療法及び化学療法である。幾つかの可能性ある手術選択は、冷凍手術、子宮摘出、及び膣上部摘出である。頸癌患者のための放射線療法は、外部放射線療法又は近接照射療法を包含する。頸癌を治療するために化学療法の一部として投与され得る抗癌薬物は、シスプラチン、カルボプラチン、ヒドロキシウレア、イリノテカン、ブレオマイシン、ビンクリスチン、マイトマイシン、イホスファミド、フルオロウラシル、エトポシド、メトトレキセート及びそれらの組合わせを包含する。
【0060】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、又はそれらのの組合せにより、頸癌患者に有益な効果を提供し得る。
【0061】
前立腺癌:
1つの他の観点においては、本発明は、前立腺癌、好ましくは次のものから選択された前立腺癌を治療するための方法を提供する:腺癌、又は骨に転移した腺癌。前立腺癌は、尿道の最初の部分を取囲む、男性における前立腺器官において進行する。前立腺は、幾つかの細胞型を有するが、しかし腫瘍の99%は、精液の生成を担当する腺細胞において進行する。
【0062】
手術、免疫療法、放射線療法、凍結外科、ホルモン療法及び化学療法は、前立腺癌患者のために利用できる幾つかの処理である。前立腺癌を治療するための可能性ある手術は、基本的恥骨後前立腺切除、基本的会陰前立腺切除及び腹腔鏡による基本的前立腺切除を包含する。幾つかの放射線療法選択は、外部ビーム放線、例えば三次元等角放射性療法、強度変調放射線療法及び等角プロトンビーム放射線療法である。近接照射療法(種子移植又は組織間腔放射線療法)がまた、前立腺癌についての利用できる処理方法である。凍結外科は、局在化する前立腺癌細胞を処理するために使用されるもう1つの可能性ある方法である。
【0063】
アンドロゲン妨害療法又はアンドロゲン抑制療法とも呼ばれるホルモン療法が、前立腺癌を治療するために使用され得る。この療法の幾つかの方法、例えばアンドロゲンの90%が生成される睾丸摘除法が利用できる。もう1つの方法は、低いアンドロゲンレベルへの黄体形成ホルモン放出ホルモン(LHRH)類似体の投与である。入手できるLHRH類似体は、ロイプロリド、ゴセレリン、トリプトレリンを包含する。LHRHアンタゴニスト、例えばアバレリックス(abarelix)もまた投与され得る。
【0064】
身体におけるアンドロゲン活性を阻止する抗アンドロゲン剤による処理は、もう1つの入手できる療法である。そのような剤は、フルタミド、ビカルタミド及びニルタミドを包含する。この療法は典型的には、LHRH類似体投与又は睾丸摘除と組合わされ、これは組合されたアンドロゲン遮断(CAB)と呼ばれる。
【0065】
化学療法異は、前立腺腫瘍が前立腺外に広がり、ホルモン処理が効果的でない場合、適切である。抗癌薬剤、例えばドキソルビジン、エストラムスチン、エトポシド、ミトキサントロン、ビンブラスチン、パクリタキセル、ドセタクセル、カルボプラチン及びプレドニソンが、前立腺癌の増殖を遅め、症状を軽減し、生存の性質を改良するために、投与され得る。
【0066】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、ホルモン療法又はそれらの組合せにより、前立腺癌患者に有益な効果を提供し得る。
【0067】
膵臓癌:
もう1つの観点においては、本発明は、膵臓癌、好ましくは膵管組織における上皮(epitheloid)癌及び膵管における腺癌から選択された膵臓癌の治療方法を提供する。
【0068】
最も通常型の膵臓癌は、膵管の内層において発症する腺癌である。膵臓癌のために利用できる可能な処理は、手術、免疫療法、放射線療法及び化学療法である。可能性ある手術処理の選択は、遠位又は全膵臓切除及び膵十二指腸切除(ウィップル方法)を包含する。
【0069】
放射線療法、特に体外機械によって腫瘍に焦点を合わせられる外部ブーム放射線放線が膵臓癌患者のためのオプションである。もう1つのオプションは、手術の間に投与される手術内電子ビーム照射である。
【0070】
化学療法は、膵臓癌患者を処理するために使用され得る。適切な抗癌剤は、5−フルオロウラシル(5−FU)、マイトマイシン、イホスファミド、ドキソルビシン、スルレプトゾシン、クロロゾトシン及びそれらの組合せを包含する。
【0071】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、又は化学療法により、膵臓癌患者に有益な効果を提供し得る。
【0072】
膀胱癌:
もう1つの観点においては、本発明は、膀胱癌、好ましくは膀胱における移行細胞癌の治療方法を提供する。膀胱癌は、尿路上皮癌(移行細胞癌)、又は膀胱の内表面になる尿路上皮細胞における腫瘍である。膀胱癌の残る事例は、扁平上皮細胞癌、腺癌及び小細胞癌である。幾つかのサブタイプの尿路癌は、それらが非侵襲性か又は侵襲性のいずれかであるか、及びそれらが乳頭状であるか又は平らであるかどうかに依存して存在する。非侵襲性腫瘍は尿路上皮、すなわち膀胱の最も内部層に存在し、侵襲性腫瘍は尿路上皮から膀胱の主要筋肉壁のより深い層まで広がる。侵襲性乳頭状尿路上皮癌は、膀胱の空洞中心に分岐し、また、膀胱壁中に外側から増殖する細長いフィンガー様隆起物である。非侵襲性乳頭状尿路上皮腫瘍は、膀胱の中心部の方に増殖する。非侵襲性の平らな尿路上皮腫瘍(また、平らな上皮癌とも呼ばれる)は、膀胱の内部中空部分に最も隣接する細胞層に限定されるが、侵襲性の平らな尿路上皮癌は、膀胱のより深い層、特に筋肉層に侵入する。
【0073】
膀胱癌を治療するためには、手術、放射線療法、免疫療法、化学療法又はそれらの組合せが適用される。幾つかの可能性ある手術オプションは、経尿道切除、膀胱切除又は根治的膀胱切除である。膀胱癌についての放射線療法は、外部ビーム放射線及び近接照射療法を包含する。
【0074】
免疫療法は、膀胱癌患者を処理するために使用され得るもう1つの方法である。典型的には、これは膀胱内的に達成され、すなわちカテーテルにより膀胱中に直接的に処理剤が投与される。1つの方法は、結核種痘において時々使用される細菌カテーテルを通して膀胱に直接的に与えられる、Bacillus Calmete-Guerin(BCG)である。身体は、細菌に対する免疫応答を開始し、それにより、癌細胞を攻撃し、殺害する。
【0075】
免疫療法のもう1つの方法は、インターフェロン、すなわち免疫応答を調節する糖タンパク質の投与である。インターフェロンαはしばしば、膀胱癌を治療するために使用される。
【0076】
膀胱癌を治療するために化学療法において使用され得る抗癌剤は、チテパ、メトトレキセート、ビンブラスチン、ドキソルビシン、シクロホスファミド、パクリタキセル、カルボプラチン、シスプラチン、イホスファミド、ゲムシタビン又はそれらの組合せを包含する。
【0077】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、免疫療法、化学療法、又はそれらの組合せにより、膀胱癌患者に有益な効果を提供し得る。
【0078】
血液癌:
リンパ腫:
【0079】
B−細胞リンパ腫:
悪性(癌性)B−細胞リンパ腫により引起される非ホジキンリンパ腫は、多くのサブセット(アメリカにおいて約85%)の既知型リンパ腫を表す(他の2種のサブセットは、T−細胞リンパ腫、及び細胞型がナチュラルキラー細胞であるか又は未知であるリンパ腫である)。細胞は、細胞と、身体における外来性物質との相互作用との間の複雑なシグナル化工程に依存して、それらの生活環において多くの変化を受ける。種々のタイプのリンパ腫又は白血病が、B細胞生活環において生じることができる。
急性骨髄性白血病:
【0080】
もう1つの観点においては、本発明は、急性骨髄性白血病(AML)、好ましくは末梢血液における急性前骨髄細胞白血病の治療方法を提供する。AMLは骨髄において始まるが、しかし身体の他の部分、例えばリンパ節、肝臓、脾臓、中枢神経系、及び精巣へも広がる。それは、すばやく進行することを意味する急性であり、数ヶ月以内に処理されなければ、致命的である。AMLは、再生し、蓄積し続ける、未熟の骨髄細胞、通常顆粒球又は単球により特徴づけられる。
【0081】
AMLは、免疫療法、放射線療法、化学療法、骨髄又は末梢血液幹細胞移植、又はそれらの組合せにより処理され得る。放射線療法は、外部ビーム放射線を包含し、副作用を有する。AMLを処理するために化学療法に使用され得る抗癌剤は、シタラビン、アントラサイクリン、アントラセンジオン、イダルビシン、ダウノルビシン、イダルビシン、ミトキサントロン、チオグアニン、ビンクリスチン、プレドニソン、エトポシド、又はそれらの組合せを包含する。
【0082】
モノクローナル抗体療法は、AML患者を処理するために使用され得る。小分子又は放射性化学物質が、身体において白血病細胞を殺害する手段を提供するために投与の前、それらの抗体に結合され得る。AML細胞上のCD33を結合するモノクローナル抗体、すなわちゲムツズマブ・オゾガミシン(gemtuzumab ozogamicin)が、化学療法レジメの前、耐えることができないAML患者を処理するために使用され得る。
【0083】
骨髄又は末梢血液幹細胞移植が、AML患者を処理するために使用され得る。幾つかの可能性ある移植方法は、同種又は自己移植である。
【0084】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、又は移植療法より、白血病患者に有益な効果を提供し得る。
【0085】
本発明により提供される方法により処理され得る他のタイプの白血病、例えば急性リンパ性白血病、急性骨髄性白血病、慢性リンパ球性白血病、慢性骨髄性白血病、ヘアリー細胞白血病、骨髄形成異常及び骨髄増殖性疾患が存在するが、但しそれらだけには限定されない。
【0086】
肺癌:
もう1つの観点においては、本発明は肺癌を治療するための方法を提供する。最も通常のタイプの肺癌は、非小細胞肺癌(NSCLC)であり、肺癌の約80〜85%を占め、扁平上皮癌、腺癌及び大細胞末分化癌に分けられる。小細胞肺癌は、肺癌の15〜20%を占める。
【0087】
肺癌治療の選択肢としては、手術、免疫療法、放射線療法、化学療法、光力学療法、又はそれらの組合せが挙げられる。肺癌の治療のために幾つかの可能性ある手術オプションは、分節性又はくさび性切除、葉切除法又は一側肺全摘除である。放射線療法は、外部ビーム放射線療法及び近接照射療法であり得る。
【0088】
肺癌を治療するために化学療法に使用され得る幾つかの抗がん剤は、シスプラチン、カルボプラチン、パクリタキセル、ドセタクセル、ゲムシタビン、ピノレルビン、イリノテカン、エトポスデ、ビンブラスチン、ゲフィチニブ、イソスファミド、メトトレキセート、又はそれらの混合物を包含する。光力学療法(PDT)が、肺癌患者を処理するために使用され得る。
【0089】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、光力学療法、又はそれらの組合せにより、肺癌患者に有益な効果を提供し得る。
【0090】
皮膚癌:
もう1つの観点においては、本発明は、皮膚において開始する幾つかのタイプの癌が存在する。最も通常のタイプは、非メラノーマ性皮膚癌である基底細胞癌及び扁平上皮細胞癌である。光線性角化症は、時々、扁平上皮細胞癌に進行する皮膚状態である。非メラノーマは、近くの組織に侵入し、身体の他の部分に広がる。異なったタイプの処理、例えば手術、放射線療法、化学療法及び光力学療法は、非メラノーマ及びメラノーマ性皮膚癌及び光線性角化症を有する患者のために利用できる。皮膚癌の治療のための幾つかの可能性である手術オプションは、Mohs顕微鏡検査手術(MMS)、単純な切除、電気乾燥及び掻爬、凍結外科、レーザー手術である。放射線療法は、外部ビーム放射線療法又は近接照射療法であり得る。臨床試験において試験される他のタイプの処理は、生物学的療法又は免疫療法、化学免疫療法、フルオロウラシルによる局部化学療法及び光力学療法である。
【0091】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、光力学療法、又はそれらの組合せにより、皮膚癌患者に有益な効果を提供し得る。
【0092】
眼の癌、網膜芽腫:
もう1つの観点においては、本発明は、網膜芽腫を処理するための方法を提供する。網膜芽腫は、網膜の悪性腫瘍である。網膜芽腫はいずれの年齢でも発症するが、それはしばしば、より若い子供、通常5歳前に発症する。腫瘍は、片眼においてのみ、又は両眼において存在し得る。網膜芽腫は通常、眼に制限され、身体の近くの組織又は他の部分には広がらない。患者を治癒し、ビジョンを保持するための処理オプションは、脱核(眼を除去する手術)、放射線療法、凍結外科、光凝固、免疫療法、熱療法及び化学療法を包含する。放射線療法は、外部ビーム放射線療法又は近接照射線療法であり得る。
【0093】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、凍結外科、光凝固、熱療法、及び熱療法、又はそれらの組合せにより、眼の網膜芽腫患者に有益な効果を提供し得る。
【0094】
眼癌、眼球内メラノーマ:
もう1つの観点においては、本発明は、眼球内メラノーマの処理方法を提供する。まれな癌である眼球内メラノーマは、癌細胞がブドウ膜と呼ばれる眼の部分に見出される疾病である。眼球内メラノーマは、中年の人々において最もしばしば発症する。眼球内メラノーマについての処理は、手術、免疫療法、放射線療法及びレーザー療法を包含する。手術は、眼球内メラノーマの最も通常の処理である。幾つかの可能性ある手術オプションは、虹彩切除、虹彩柵状組織切除、虹彩毛様体切除、脈絡膜切除、脱核及び眼窩内容除去である。放射線療法は、外部ビーム放射線療法又は近接照射療法であり得る。レーザー療法は、腫瘍を破壊するための強力な光のビーム、熱療法又は光凝集法であり得る。
【0095】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法及びレーザー療法、又はそれらの組合せにより、眼球内メラノーマ患者に有益な効果を提供し得る。
【0096】
子宮内膜癌:
もう1つの観点においては、本発明は子宮膜癌を治療するための方法を提供する。子宮内膜癌は、子宮内膜、すなわち子宮内膜において開始する癌である。子宮及び子宮内膜の癌の幾つかの例は、次のものを包含するが、但しそれらだけには限定されない:腺癌、腺類癌、腺扁平細胞癌、乳頭状漿液性腺癌、明細胞線癌、子宮内肉腫、間質性肉腫、悪性混合ミュラー腫瘍及び平滑筋肉腫。
【0097】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、遺伝子療法、光力学的療法、抗脈管形成療法、及び免疫療法、又はそれらの組合せにより、子宮内膜癌患者に有益な効果を提供し得る。
【0098】
肝臓癌:
もう1つの観点においては、本発明は、原発性肝癌(肝臓において開始する癌)の処理方法を提供する。原発性肝癌は、成人及び子供の両者において発症する。異なったタイプの処理が、原発性肝癌を有する個人のために利用できる。それらは、手術、免疫療法、放射線療法、化学療法及び経皮エタノール注入を包含する。使用され得るこのタイプの手術は、凍結外科、部分肝切除、全肝切除及び高周波アブレーションである。放射線療法は、外部ビーム放射線療法、近接照射療法、放射線増感剤又は放射性ラベルされた抗体であり得る。他のタイプの処理は、温熱療法及び免疫療法を包含する。
【0099】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、経皮エタノール注入、温熱療法及び免疫療法、又はそれらの組合せにより、肝臓癌患者に有益な効果を提供し得る。
【0100】
腎臓癌:
もう1つの観点においては、本発明は、腎臓癌の治療方法を提供する。腎臓癌(または、腎細胞癌又は腎臓腺癌とも呼ばれる)は、悪性細胞が腎臓における細管の内層に見出される疾病である。腎臓癌は、手術、放射線療法、化学療法及び免疫療法により処理され得る。腎臓癌を治療するための幾つかの可能性ある手術オプションは、部分腎摘出、単純腎切除、及び根治的腎摘出である。放射線療法は、外部ビーム放射線療法又は近接照射法であり得る。幹細胞移植が、腎臓癌を治療するために使用され得る。
【0101】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、免疫療法、及び幹細胞移植、又はそれらの組合せにより、腎臓癌患者に有益な効果を提供し得る。
【0102】
甲状腺癌:
もう1つの観点においては、本発明は甲状腺癌の治療方法を提供する。甲状腺癌は、癌(悪性)細胞が甲状腺の組織に見出される疾病である。次の4種の主要型の甲状腺癌が存在する:乳頭状性、小胞性、髄質性及び退形性。甲状腺癌は、手術、免疫療法、放射線療法、ホルモン療法及び化学療法により処理され得る。手術は、甲状腺癌の最も通常の処理である。甲状腺癌の治療のための幾つかの可能性ある手術オプションは、葉切除、甲状腺のほぼ全摘、甲状腺全切除及びリンパ節切除である。放射線療法は、外部放射線療法であり得、又は放射性ヨウ素を含む液体の摂取を必要とする。ホルモン療法は、癌細胞の増殖を停止するために使用する。甲状腺癌の治療においては、ホルモンは、癌細胞を増殖する他のホルモンの身体における製造を停止するために使用され得る。
【0103】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、ホルモン療法、及び化学療法、又はそれらの組合せにより、甲状腺癌患者に有益な効果を提供し得る。
【0104】
AIDS関連癌:
AIDS関連のリンパ腫:
もう1つの観点においては、本発明はAIDS関連のリンパ腫の処理方法を提供する。AIDS関連のリンパ腫は、後天性免疫欠損症候群(AIDS)を有する患者のリンパ系において悪性細胞が形成する疾病である。次に、免疫系は、身体に侵入する感染及び疾病を攻撃することができない。HIV疾病を有する人々は、感染、リンパ腫及び他のタイプの癌を進行する高められた危険性を有する。リンパ腫は、リンパ系の白血球に影響を及ぼす癌である。リンパ腫は次の2種の一般的タイプに分けられる:ホジギンリンパ腫及び非ホジギンリンパ腫。ホジキンリンパ腫及び非ホジキンリンパ腫の両者はAIDS患者において発症するが、しかし非ホジキンリンパ腫がより一般的である。AIDSを有する個人が非ホジキンリンパ腫を有する場合、それはAIDS関連リンパ腫と呼ばれる。非ホジキンリンパ腫は、無活性(遅い増殖)又は攻撃的(早い増殖)であり得る。AIDS関連リンパ腫は通常、攻撃的である。3種の主要タイプのAIDS関連リンパ腫が拡散する:大B細胞リンパ腫、B細胞免疫芽球リンパ腫及び小非分裂細胞リンパ腫。
【0105】
AIDS関連のリンパ腫の処理は、リンパ腫の処理と、AIDSについての処理とを兼ねる。AIDSを有する患者は弱体化された免疫系を有し、処理はさらなる損傷を引き起すことができる。この理由のために、AIDS関連のリンパ腫を有する患者は通常、AIDSを有さないリンパ腫患者よりも低い用量の薬物により処理される。高い活性の抗レトロウィルス療法(HAART)は、HIVの進行を遅めるために使用される。重症である感染を予防し、処理するための薬剤がまた使用される。AIDS関連リンパ腫は、化学療法、免疫療法、放射線療法及び幹細胞移植による高用量化学療法により処理され得る。放射線療法は、外部ビーム放射線療法又は近接照射療法による。AIDS関連のリンパ腫は、モノクローナル抗体療法により処理され得る。
【0106】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、化学療法、放射線療法及び高−用量化学療法、又はそれらの組合せにより、AIDS関連リンパ腫患者に有益な効果を提供し得る。
【0107】
カポジ肉腫:
もう1つの観点においては、本発明はカポジ肉腫の処理方法を提供する。カポジ肉腫は、癌細胞が口、鼻及び肛門の内表面になる、皮膚又は粘膜下の組織において見出される疾病である。従来のカポジ肉腫は通常、イスラエル人、イタリア人又は地中海先祖の男性老人において発症する。このタイプのカポジ肉腫は、ゆっくり、時々10〜15年にわたって進行する。カポジ肉腫は、免疫抑制剤を摂取している人々において発症する。後天性免疫欠損症候群(AIDS)を有する患者におけるカポジ肉腫は、伝染性カポジ肉腫と呼ばれる。AIDSを有する人々におけるカポジ肉腫は通常、他の種類のカポジ肉腫よりもすばやく広がり、しばしば、身体の多くの部分に見出される。カポジ肉腫は、手術、化学療法、放射線療法及び免疫療法により処理され得る。外部放射線療法は、カポジ肉腫の通常の処理である。カポジ肉腫を処理するための幾つかの可能性ある手術オプションは、局部切除、電気乾燥及び掻爬、及び寒冷療法である。
【0108】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、化学療法、放射線療法及び免疫療法、又はそれらの組合せにより、カポジ肉腫患者に有益な効果を提供し得る。
【0109】
ウィルス誘発された癌:
もう1つの観点においては、本発明はウィルス誘発された癌の治療方法を提供する。幾つかの通常のウィルスが、特定悪性腫の病因学において明らかな、又は問題のある原因要素である。それらのウィルスは通常、潜伏期を確立し、又は数種は感染耐性になる。腫瘍形成はたぶん、感染された宿主において増強されたレベルのウィルス活性化に連結され、重度のウィルス用量又は易感染性免疫制御に影響を及ぼす。主要ウィルス悪性腫系は、B型肝炎ウィルス(HBV)、C型肝炎ウィルス(HCV)及び原発性肝細胞癌;ヒト向リンパ性ウィルス型1(HTLV−1)及び成人T−細胞白血病/リンパ腫;及びヒト乳頭腫ウィルス(HPV)及び頸癌を包含する。一般的にそれらの悪性腫は比較的、生命の初期において発症し、典型的には中年期か又はそれよりも早くピークに達する。
【0110】
ウィルス誘発された肝細胞癌:
HBV及びHCVの両者と肝細胞癌との間の因果関係は、実質的な流行学的出来事を通して確立される。両者は、細胞死及び続く再生を引き起すことにより、肝臓において慢性的再現を通して作用するように思える。異なったタイプの処理が、肝臓癌を有する患者のために利用できる。それらは、手術、免疫療法、放射線療法、化学療法及び経皮エタノール注入を包含する。使用され得る手術のタイプは、凍結外科、部分肝切除、全肝切除及び高周波アブレーションである。放射線療法は、外部ビーム放射線療法、近接照射療法、放射線増感剤又は放射性ラベルされた抗体であり得る。他のタイプの処理は、温熱療法及び免疫療法を包含する。
【0111】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、経皮エタノール注入、温熱療法及び免疫療法、又はそれらの組合せにより、ウィルス誘発された肝細胞癌患者に有益な効果を提供し得る。
【0112】
ウィルス誘発された成人T細胞白血病/リンパ腫:
レンチウィルス(例えば、HTLV−1)と成人T細胞白血病(ATL)との間の関係は確立されている。世界中に見出される他の腫瘍形成ウィルスとは異なって、HTLV−1は高く地理的に制限され、主として南日本、カリブ海、西及び中央アフリカ、及び南太平洋諸島において見出される。因果関係の証拠は、キャリヤーにおけるATLのほとんど全ての場合、ウィルスゲノムのモノクローナル統合を包含する。HTLV−1関連の悪性腫についての危険因子は、周産期感染、高ウィルス量及び雄性生殖であるように思える。
成人T細胞白血病は、血液及び骨髄の癌である。成人T細胞白血病/リンパ腫についての標準処理は、放射線療法、免疫療法及び化学療法である。放射線療法は、外部ビーム放射線療法又は近接照射療法であり得る。成人T細胞白血病/リンパ腫を処理するための他の方法は、免疫療法、及び幹細胞移植による高用量化学療法を包含する。
【0113】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、免疫療法、及び幹細胞移植による高用量化学療法、又はそれらの組合せにより、成人T細胞白血病患者に有益な効果を提供し得る。
【0114】
ウィルス−誘発された頸癌:
ヒト乳頭腫ウィルス(HPV)による頸部の感染は、頸癌の最も共通した原因である。しかし、HPV感染を有する全ての女性が必ずしも頸癌を進行しないであろう。頸癌は通常、時間にわたってゆっくり進行する。癌が頸部に出現する前、頸部の細胞は、正常ではない細胞が頸部組織に出現し始める、形成異常として知られている変化を受ける。後に、癌細胞は増殖し、頸部中に及び周囲領域に、より深く広がり始める。頸部癌のための標準処理は、手術、免疫療法、放射線療法及び化学療法である。使用され得る手術のタイプは、円錐切除、子宮全摘出、双方の卵管卵巣摘出、広汎性子宮全摘出、骨髄内容除去、凍結外科、レーザー手術及びループ電子切除方法である。放射線療法は、外部ビーム放射線療法又は近接照射療法である。
【0115】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、成人頸癌患者に有益な効果を提供し得る。
【0116】
CNS癌:
脳及び脊髄腫瘍は、中枢神経系(CNS)の主成分である、頭蓋骨又は脊椎骨の内部に見出される組織の異常増殖である。良性腫瘍は、非癌性であり、悪性腫瘍は癌性である。CNSは堅い骨の四分体(すなわち、頭蓋骨及び脊椎骨)に収容され、その結果、良性であろうと又は悪性であろうと、いずれの異常増殖でも感受性組織に対して圧力を付与し、機能を損なう。脳又は脊髄において起因する腫瘍は一次腫瘍と呼ばれる。ほとんどの一次腫瘍は、ニューロンを取囲み、支持する細胞間の制御不能により引起される。少数の個人においては、一次腫瘍は、特定の遺伝的疾患(例えば、神経線維腫症、結節性硬化症)、又は放射線又は癌を引き起す化学物質に起因する。ほとんどの一次腫瘍の原因は、未知のままである。
【0117】
脳及び脊髄腫瘍を診断するための最初の試験は、神経学的試験である。特定のイメージング技法(断層エックス線撮影及び磁気共鳴イメージングが、ポジトロン放射断層撮影に比較して)がまた使用される。実験試験はEEG及び腰椎穿刺を包含する。生検、すなわち組織のサンプルが懸濁された腫瘍から取られる手術法は、医師による腫瘍のタイプの診断を助ける。
【0118】
腫瘍は、その巣葉ガ起因すると思われる細胞の種類に従って分類される。成人における最も共通する脳腫瘍は、血液−脳バリヤーを構成し、中枢神経系の栄養に寄与する星状細胞と呼ばれる脳における細胞に由来する。それらの腫瘍神経膠腫(星状細胞腫、退形成星細胞腫又は多形膠芽腫)と呼ばれ、全ての一次中枢神経系腫瘍の65%を占める。腫瘍の幾つかは、乏突起細胞腫、脳室上皮腫、髄膜腫、リンパ腫、神経鞘腫及び髄芽腫であるが、但しそれらだけには限定されない。
【0119】
CNSの感覚上皮腫瘍:
星状細胞腫瘍、例えば星状細胞腫;末分化(悪性)星状細胞腫、例えば半球状、間脳性、視覚性、脳幹性、小脳性;多形膠芽腫;毛様細胞性星状細胞腫、例えば半球状、間脳性、視覚性、脳幹性、小脳性;上衣下巨細胞神経膠星状細胞腫;及び多形性黄色星状膠細胞腫。稀突起膠細胞腫瘍、例えば稀突起膠腫;及び末分化(悪性)乏突起細胞腫。脳室上衣細胞腫瘍、例えば脳室上皮腫;末分化脳室上皮腫;粘液乳頭脳室上皮腫;及び上衣下細胞腫。混合された神経膠腫、例えば混合された稀星状細胞腫;末分化(悪性)稀星状細胞腫;及び他のもの(例えば、上衣−星状細胞腫)。確信できない起源の感覚上皮腫瘍、例えば極性海綿細胞腫;星状芽細胞腫;及び大脳神経膠腫症。脈絡膜叢の腫瘍、例えば脈絡膜叢乳頭腫;及び脈絡膜叢癌(末分化脈絡膜叢乳頭腫)。ニューロン性及び混合されたニューロン−膠腫瘍、例えば節神経腫;小脳の形成異常性節神経腫(Lhermitte-Duclos);神経節膠腫;末分化(悪性)神経節膠腫;癒着性乳児神経節膠腫、例えば癒着性乳児星状細胞腫;中枢神経細胞腫;胎生期発育不全性神経上皮腫瘍;嗅神経芽細胞腫(鼻腔神経芽細胞)。松果実質腫瘍、例えばピネオサイトーマ;松果体芽腫;及び混合されたピネオサイトーマ/松果体芽腫。神経芽細胞又はグリア芽細胞要素を有する腫瘍(胚芽腫)、例えば髄様上皮腫;多分化能分化を有する末分化神経外胚芽性腫瘍、例えば髄芽腫;脳末分化神経外胚芽性腫瘍;神経芽細胞腫;網膜胚種細胞腫;及び上衣芽腫。
【0120】
他のCNS腫瘍:
Sellar領域の腫瘍、例えば脳下垂体腺腫;下垂体癌;及び頭蓋咽頭腫。造血性腫瘍、例えば原発性悪性リンパ腫;プラズマ細胞腫;及び顆粒球性肉腫。胚細胞腫、例えば胚芽腫;胎生期癌;卵黄嚢腫瘍(内皮性静脈洞炎腫瘍);絨毛膜癌;奇形腫;及び混合された胚細胞腫。膜の腫瘍、例えば髄膜腫;非定型的髄膜腫;及び末分化(悪性)髄膜腫。膜の非髄膜細胞層腫瘍、例えば良性間葉;悪性間葉;一次メラニン細胞病巣;造血腫瘍;及び不確定組織形成、例えば血管芽細胞腫(毛細管血管芽細胞腫)。頭側及び背骨神経の腫瘍、例えば(神経鞘腫);神経繊維腫;悪性末梢神経鞘腫(悪性神経鞘腫)、例えば類上皮、分岐間葉又は上皮性分化、及びメラニン性。局所腫瘍からの局部拡張;例えば傍神経節腫(頸静脈小体腫瘍);背索腫;軟骨肉腫;及び癌。転移性腫瘍、末分類腫瘍及び包嚢、及び腫瘍様病巣、例えばラケト嚢腫;類表皮;類皮腫;第三脳室のコロイド状包嚢;腸性嚢胞;神経膠嚢胞;顆粒細胞腫(迷芽腫、下垂体細胞腫);視床下部ニューロン性過誤腫;鼻神経膠異所性;及びプラズマ細胞肉腫。
【0121】
利用できる化学療法剤は、次のものであるが、但しそれらだけには限定されない:アルキル化剤、例えばシクロホスファミド、イホスファミド、メルファラン、クロラムブシル、CCNU、デカルバジン、プロカルバジン、ブスルファン及びチオデパ;代謝拮抗剤、例えばメトトレキサート、5−フルオロウラシル、シタラビン、ゲムシタビン(Gemzar(登録商標))、6−メルカプトプリン、6−チオグラニン、フルダラビン及びクラドリビン;アントラサイクリン、例えばダウノルビシン、ドキソルビシン、イダルビシン、エビルビシン及びミトキサントロン;抗生物質、例えばブレオマイシン;カンブトテンシン類、例えばイリノテカン及びトポテカン;タキサン類、例えばパクリタキセル及びドセタクセル;及びプラチナ類、例えばシスプラチン、カルボプラチン及びオキサリプラチン。
【0122】
処理法は手術、放射線療法、免疫療法、高体温、遺伝子療法、化学療法、及びそれらの組合せである。医者はまた、CNS内部の膨張を低めるためにステロイドを処方できる。
【0123】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、成人頸癌患者に有益な効果を提供し得る。
【0124】
PNS癌:
末梢神経系は、脳及び脊髄から枝分かれする神経からなる。それらの神経は、CNSと身体部分との間で連結網を形成する。末梢神経系はさらに、体性神経系及び付随神経系に細分される。体性神経系は、皮膚及び筋肉に進行する神経から成り、意識活性に関与される。不随神経系は、内臓、例えば心臓、胃及び腸にCNSを連結する神経からなる。それは無意識の活性を仲介する。
【0125】
聴神経腫は、8番目の脳神経又は内耳神経とも呼ばれる、平衡神経から生じる良性線維性増殖である。それらの腫瘍は、非悪性であり、すなわち、それらは身体の他の部分に拡散も又は転移もしないことを意味する。それらの腫瘍の局在化は、脳幹における生体脳に隣接して、頭蓋骨内深部である。腫瘍が拡大するにつれて、それらは、生体機能と関係する構造体を取囲む。大部分の場合、それらの腫瘍は数年間にわたってゆっくり増殖する。
【0126】
悪性末梢神経鞘腫瘍(MPNST)は、良性柔組織腫瘍、例えば神経繊維腫及び神経鞘腫に対する悪性対抗物である。それは最も通常には、深部の柔組織において、通常、神経幹に密接して存在する。最も通常の部位は、坐骨神経、腕神経叢及び仙骨神経叢を包含する。それは、成人において三叉神経核の知覚ブランチから通常生じる、まれで、攻撃的で、且つ致死性の眼窩腫瘍である。悪性PNS腫瘍は、脳を包含するよう神経に沿って拡張し、ほとんどの患者が臨床学的診断の5年以内に死亡する。MPNSTは、類上皮、間葉又腺特徴により3種の主要カテゴリーに分類され得る。MPNSTのいつかは、次のものを包含するが、但しそれらだけに限定されない:軟骨質分化を有する皮下悪性類上皮神経鞘腫、腺悪性神経鞘腫、神経周膜を有する悪性末梢神経鞘腫、杆状機能を有する皮膚類上皮悪性骨髄鞘腫、皮相類上皮MPNST、トリトン腫瘍(横紋筋芽細胞分化を有するMPNST)、横紋筋芽細胞分化を有する神経鞘腫。稀なMPNSTは、複数の肉腫性組織型、特に骨肉腫、軟骨肉腫及び血管肉腫を含む。それらは時々、柔組織の悪性間葉組織腫瘍とは区別できない。
【0127】
他のタイプのPNS癌は、悪性線維性細胞腫、悪性線維性組織球腫、悪性髄膜腫、悪性黒子症候群、及び悪性の混合されたMullerian腫瘍を包含するが、但しそれらだけには限定されない。
【0128】
その処理は、手術、放射線療法、免疫療法、化学療法、及び放射線療法及び化学療法の組合せである。
【0129】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、PNS癌に有益な効果を提供し得る。
【0130】
口腔及び中咽頭癌:
中枢神経(CNS)癌を有する患者の管理は、困難な課題として残っている。癌、例えば下咽頭癌、喉頭癌、上咽頭癌、中因頭癌及び同様のものは、手術、免疫療法、化学療法、化学療法及び放射線療法の組合せにより処理されて来た。エトポシド及びアクチノマイシンD(トポイソメラーゼIIを阻害する、2種の通常使用される腫瘍学的剤)は、有用な量で血液−脳バリヤーを交差できない。
【0131】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、口腔及び中咽頭癌に有益な効果を提供し得る。
【0132】
胃癌:
胃癌は、胃の内層における細胞変化の結果である。次の3種の主要型の胃癌が存在する:リンパ腫、胃の間質腫瘍及び類癌腫。リンパ腫は、時々胃の壁に見出される免疫組織の癌である。胃の間質腫瘍は、胃壁の組織から進行する。類癌腫は胃のホルモン生成細胞の腫瘍である。
【0133】
胃癌の原因は、議論され続けている。遺伝及び環境(食餌、喫煙、等)の組合せが全て、一部原因であるように思える。処理への共通するアプローチは、手術、免疫療法、化学療法、放射線療法、化学療法及び放射線療法の組み合わせ、又は生物学的療法を包含する。
【0134】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、胃癌に有益な効果を提供し得る。
【0135】
精巣癌:
精巣癌は、典型的には、若い男性における1つの又は両睾丸において進行する癌である。睾丸の癌は、生殖細胞として知られている一定の細胞において進行する。男性において発症する2種の主要型の生殖細胞腫瘍(GCT)は、セミノーマ(60%)及び非セミノーマ(40%)である。腫瘍はまた、睾丸の支持及びホルモン生成組織又は間質において発症する。そのような腫瘍は、生殖腺間質腫としても知られている。2種の主要タイプの癌は、Leydig細胞腫瘍及びセルトリ細胞腫である。二次睾丸腫瘍は、他の器官において開始し、次に、睾丸に広がる腫瘍である。リンパ腫は、最も共通する二次精巣癌である。
【0136】
処理のためへの共通するアプローチは、手術、免疫療法、化学療法、放射線療法、化学療法及び放射線療法の組合せ、又は生物学的療法を包含する。次の幾つかの薬物が典型的には、精巣癌を治療するために使用される:プラチノール(シスプラチン)、Vepesid又はVP−16(エトポシド)及びブレノキサン(硫酸ブレオマイシン)。さらに、Ifex(イフォサミド)、Velban(硫酸ビンブラスチン)及び他のものが使用され得る。
【0137】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、精巣癌に有益な効果を提供し得る。
【0138】
胸腺癌:
胸腺は、喉の基部から心臓の前部に延長する、胸の上部/前部に位置する小器官である。胸腺は次の2種の主要型細胞を含む:胸腺上皮細胞及びリンパ球。胸腺上皮細胞に、胸腺腫及び胸腺癌は起因する。リンパ球は、胸腺においても又はリンパ節においても、悪性になり、ホジギン病及び非ホジキンリンパ腫と呼ばれる癌に進行する。胸腺はまた、通常一定のホルモンを放出する、Kulchitsky細胞又は神経内分泌細胞と呼ばれる、もう1つの低い共通型の細胞を含む。それらの細胞は、しばしば同じ型のホルモンを放出し、身体の他の部分における神経分泌細胞から発生する他の腫瘍に類似する、カルチノイド又はカルチノイド腫瘍と呼ばれる癌を生ぜしめることができる。
【0139】
処理への共通するアプローチは、手術、免疫療法、化学療法、放射線療法、化学療法及び放射線療法の組合せ、又は生物学的療法を包含する。胸腺腫及び胸腺癌の治療に使用されて来た抗癌薬物は、ドキソルビシン(アドリアマイシン)、シスプラチン、イホスファミド及びコルチコイド(プレドニゾン)である。しばしば、それらの薬物は、それらの有効性を高めるために、組合せて与えられる。胸腺癌を治療するために使用される組合せは、シスプラチン、ドキソルビシン、エトポシド及びシクロホスファミド、及びシスプラチン、ドキソルビシン、シクロホスファミド及びビンクリスチンの組合せを包含する。
【0140】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、胸腺癌に有益な効果を提供し得る。
【0141】
併用療法:
本発明の1つの観点は、処理管理の異なった組み合わせを用いての癌の治療方法を提供する。例えば、そのような組合せは、1又は2以上の種々の抗腫瘍化学療法剤、化学予防薬及び/又は副作用制限剤と共に1又は2以上のニトロベンズアミド化合物の使用を包含するが、但しそれらだけには限定されない。
【0142】
抗腫瘍化学療法剤:
本発明に使用される適切な抗腫瘍化学療法剤は、次のものを包含するが、但しそれらだけには限定されない:アルキル化剤、代謝拮抗剤、天然の抗腫瘍剤、ホルモン性抗癌剤、脈管形成阻害剤、分化試薬、RNA阻害剤、DNA阻害剤、ウィルス複製の阻害剤、抗体又は免疫療法剤、ペプチド剤、遺伝子療法剤、小分子酵素阻害剤、生物学的応答変性剤、及び抗−転移剤。
【0143】
アルキル化剤:
アルキル化剤は、高分子、例えば癌細胞のDNAのアルキル化を通して作用することが知られており、通常、強い求電子体である。この活性は、DNA合成及び細胞分裂を破壊し得る。本明細書への使用のために適切なアルキル化剤の例は、ナイトロジェンマスタード及びそれらの類似体及び誘導体、例えばシクロホスファミド、イホスファミド、クロラムブシル、エストラムスチン、メクロエタミン塩酸塩、メルファラン及びウラシルマスタードを包含する。アルキル化剤の他の例は、スルホン酸アルキル(例えば、ブスルファン)、ニトロソ尿素(例えば、カルムスチン、ロムスチン及びストレプトゾシン)、トリアゼン(例えば、ダカルバジン及びテモゾロミド)、エチレンイミン/メチルメラミン(例えば、アルトレタミン及びチオテパ)、及びメチルヒドラジン誘導体(例えば、プロカルバジン)を包含する。カルボプラチン、シスプラチン及びオキサリプラチンを含んでなるアルキル化様プラチナ含有薬物が、アルキル化剤グループに包含される。
【0144】
抗代謝物:
抗代謝抗癌剤は天然の代謝物に構造的に類似し、癌細胞の通常の代謝工程、例えば核酸及びタンパク質の合成に包含される。それらは天然の代謝物とは十分に異なり、その結果、それらは癌細胞の代謝工程を妨げる。本発明に使用されるべき適切な抗代謝抗癌剤は、それらが影響を及ぼす代謝工程に従って分類され得、葉酸の類似体及び誘導体、ピリミジン、プリン及びシチジンを包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な剤の葉酸グループのメンバーは、メトトレキセート(アメトプテリン)、ペメトレキシド及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なピリミジン剤は、シタラビン、フロキシウリジン、フルオロウラシル(5−フルオロウラシル)、カペシタビン、ゲムシタビン、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なプリン剤は、メルカプトプリン(6−メルカプトプリン)、ペントスタチン、チオグラニン、クラドリビン、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なシチジン剤は、シタラビン(シトシンアラビノドシド)、アザシチジン(5−アザシチジン)、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0145】
天然の抗癌剤:
天然の抗癌剤は、抗分裂剤、抗生物質抗癌剤、カンプトテシン類似体及び酵素を含んでなる。本明細書への使用のために適切な抗分裂剤は、ビンカアルカロイド、例えばビンプラスチン、ビンクリスチン、ビンデシン、ビノレルビン、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。それらは、ニチニチソウ植物から誘導され、通常、癌細胞の微小管におけるチューブリンに結合する、M期に対して細胞周期特異的である。本明細書における使用のために適切な他の抗分裂剤は、ポドフィロトキシンであり、これはエトポシド、テニポシド、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。それらの試薬は、細胞周期のG2及びS期を優先的に標的化する。
【0146】
抗生物質抗癌剤がまた、天然の抗癌剤に包含される。抗生物質抗癌剤は、癌細胞DNAとの相互作用を通して、通常抗腫瘍性質を有する抗微生物薬物である。本明細における使用のために適切な抗生物質抗癌剤は、ベロマイシン、ダクチノマイシン、ドキソルビシン、イダルビシン、エピルビシン、マイトマイシン、ミトキサントロン、ペントスタチン、プリカマイシン、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0147】
天然の抗癌剤分類はまた、本明細書に使用するために適切な、カプトテシン類似体及び誘導体を包含し、カプトテシン、トポテカン及びイリノテカンを包含する。それらの剤は主に、核酵素トポイソメラーゼIを標的化することにより作用する。天然の抗癌剤下でのもう1つのサブクラスは、酵素、L−アスパラギナーゼ及びその変異体である。L−アスパラギナーゼは、アスパラギン酸及びアンモニアへの循環アスパラギンの加水分解を触媒することにより、いくらかの癌細胞からL−アスパラギンを奪うことにより作用する。
【0148】
ホルモン抗癌剤:
ホルモン抗癌剤は、前立腺組織、乳房組織、子宮内膜組織、卵巣組織、リンパ腫及び白血病に関連するホルモン−依存性癌細胞に対して優先的に作用する。そのような組織は、グルココルチコイド、黄体ホルモン、エストロゲン及びアンドロゲンのような種類の剤に対して敏感であり、依存性であり得る。アゴニスト又は拮抗物質である類似体及び誘導体の両者は、腫瘍を処理するために本発明への使用に適切である。本明細書における使用のために適切なグルココルチコイドアゴニスト/拮抗物質の例は、デキサメサゾン、コルチゾール、コルチコステロン、プレドニソン、ミフェプリストン(RU486)、それらの類似体及び誘導体である。本明細書における使用のための適切な剤の黄体ホルモンアゴニスト/拮抗物質サブクラスは、ヒドロキシプロゲステロン、メドロキシプロゲステロン、酢酸メゲステロール、ミフェプリストン(RU486)、ZK98299、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のための適切な剤のエストロゲンアゴニスト/拮抗物質サブクラスの例は、エストロゲン、タモキシフェン、トレミフェン、RU58668、SR16234、ZD164384、ZK191703、フルベストラント、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。エストロゲン生成を阻害する、本明細書における使用のために適切なアロマターゼ阻害剤の例は、アンドロステンジオン、ホルメスタン、エキセメスタン、アミノグルテチミド、アナストロゾール、レトロゾール、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な剤のアンドロゲンアゴニスト/拮抗物質サブクラスからの例は、テストステロン、ジヒドロテストステロン、フルオキシメステロン、テストラクトン、エナント酸テストステロン、、プロピオン酸テストステロン、生殖腺刺激ホルモン放出ホルモンアゴニスト/拮抗物質(例えば、ロイプロリド、ゴセレリン、トリプトレリン、ブセレリン)、ジエチルスチルベストロール、アバレリックス、シプロテロン、フルタミド、ニルタミド、ビカルタミド、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0149】
脈管形成阻害剤:
脈管形成阻害剤は、腫瘍の血管形成化を阻害することにより作動する。脈管形成阻害剤は、広範囲の種類の剤、例えば小分子剤、抗体剤、及びRNA機能を標的化する剤を包含する。本明細書における使用のために適切な脈管形成阻害剤の例は、ラニビズマブ、ベバシズマブ、SUl1248、PTK787、ZK222584、CEP−7055、アンジオザイム、ダルテパリン、サリドマイド、スラミン、CC−5013、コンブレタスタチンAホスフェート、LY317615、大豆イソフラボン、AE−941、インターフェロンα、PTK787/ZK222584、ZD6474、EMD121974、ZD6474、BAY543−9006、セレコキシブ、ハロフジノン臭化水素、ベバシズマブ、それらの類似体、変異体又は誘導体を包含するが、但しそれらだけには限定されない。
【0150】
分化試薬:
分化剤は、癌細胞の分化を誘発する機構を通して腫瘍増殖を阻害する。本明細書における使用のために適切なそれらの剤の1つのそのようなサブクラスは、ビタミンA類似体又はレチノイド、及びペロキシソーム増殖活性化受容体アゴニスト(PPAR)を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なレチノイドは、ビタミンA、ビタミンAアルデヒド(レチナール)、レチノイン酸、フェンレチニド、9−シス−レチノイン酸、13−シス−レチノイン酸、全てのトランス−レチノイン酸、イソトレチノイン、トレチノイン、レチニルパルミテート、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なPPARのアゴニストは、トログリタゾン、シダリタゾン、テサグリタザー、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0151】
RNA阻害剤:
一定のRNA阻害剤が、癌表現型に関連するメッセンジャーRNA(“mRNa”)の発現又は翻訳を阻害するために利用され得る。本明細書における使用のために適切なそのような剤の例は、短い干渉性RNA(“siRNA”)、マイクロRNA(“miRNA”)、リボザイム及びアンチセンスオリゴヌクレオチドを包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なRNA阻害剤の特定例は、Cand5、Sirna−027、フォミビルセン及びアンギオザイムを包含するが、但しそれらだけには限定されない。
【0152】
抗体/免疫療法剤:
抗体剤は、癌細胞において選択的に発現される標的物を結合し、その標的物に結合される細胞を殺害するために接合体を利用するか、又は癌細胞を破壊するために身体の免疫応答を誘発し得る。免疫療法剤は、ポリクローナル又はモノクローナル抗体からなることができる。抗体は、非ヒト動物(例えば、マウス)及びヒト成分からなるか、又は完全にヒト成分(“ヒト適合された抗体”)から構成される。本明細書における使用のために適切なモノクローナル免疫療法剤の例は、CD−20タンパク質を標的化する、リツキシマブ、トシブツモマブ、イブリツモマブを包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な他の例は、トランスツズマブ、エドレコロマブ、ベバシズマブ、セツキシマブ、癌胎児性抗原抗体、ゲムツヅマブ、アレムツヅマブ、マパツムマブ、パニツムマブ、EMD72000、TheraCIM hR3、2C4、HGS−TR2J及びHGS−ETR2を包含するが、但しそれらだけには限定されない。
【0153】
遺伝子療法剤:
遺伝子療法剤は、遺伝子のコピーを、特定組の患者の細胞中に挿入し、癌及び非癌細胞の両者を標的化し得る。遺伝子療法の目的は、変更された遺伝子を、機能的遺伝子により置換し、癌に対する患者の免疫応答を刺激し、癌細胞を化学療法に対してより感受性にし、癌細胞中に“自殺”遺伝子を配置し、又は脈管形成を阻害することであり得る。遺伝子は、ウィルス、リポソーム、又は他のキャリヤー又はベクターを用いて、標的細胞に供給され得る。これは、遺伝子−キャリヤー組成物を、患者中に直接、注入することにより、又はエクストビボで実施され、感染された細胞が患者中に戻される。このような組成物は、本発明での使用のために適切である。
【0154】
小分子酵素阻害剤:
一定の小分子療法が、チロシンキナーゼ酵素活性、又は一定の細胞受容体、例えば上皮増殖因子受容体(“GGFR”)又は血管の内皮増殖因子受容体(“VEGFR”)の下流のシグナルトランスダクションシグナルを標的化し得る。小分子療法剤によるそのような標的化は、抗癌効果ともたらすことができる。本明細書における使用のために適切なそのような剤の例は、イマチニブ、ゲフィチニブ、エルロチニブ、ラパチニブ、カネルチニブ、ZD6474、フォラフェニブ(BAY43−9006)、ERB−569、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0155】
生物学的応答調節剤:
一定のタンパク質又は小分子剤は、直接的な抗腫瘍効果又は間接的効果を通して抗癌療法に使用され得る。本明細書における使用のために適切な直接的作用剤の例は、分化試薬、例えばレチノイド及びレチノイド誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な作用剤は、免疫又は他のシステムを調節するか又は増強する剤、例えばインターフェロン、インターロイキン、造血成長因子(例えば、エリスロポイエチン)、及び抗体(モノクローナル及びポリクローナル)を包含するが、但しそれらだけには限定されない。
【0156】
抗転移剤:
癌細胞が元の腫瘍の部位から身体周囲の他の位置に広がる工程が、癌移転と呼ばれる。一定の剤は、癌細胞の広がりを阻害するよう企画された抗転移性質を有する。本明細書における使用のために適切なそのような剤の例は、マリマスタット、ベバシズマブ、トラスヅマブ、リツキシマブ、エルロチニブ、MMI−166、GRN163L、ハンターキラーペプチド、メタロプロテイナーゼの組織阻害剤(TIMP)、それらの類似体、誘導体及び変異体を包含するが、但しそれらだけには限定されない。
【0157】
化学予防剤:
一定の医薬剤が、癌の初期発症を妨げるために、又は転移の再発を妨げるために使用され得る。1又は2以上の他の抗症剤、例えばニトロベンズアミド化合物と組合せてのそのような化学予防剤の投与は、癌の再発を処理し、予防するよう作用し得る。本明細書における使用のために適切な化学予防剤の例は、次のものを包含するが、但しそれらだけには限定されない:タモキシフェン、ラロキシフェン、チボロン、ビスホスホネート、イバンドロネート、エストロゲン受容体モジュレーター、アロマターゼ阻害剤(レトロゾール、アナストロゾール)、黄体形成ホルモン放出ホルモンアゴニスト、ゴセレリン、ビタミンA、レタノイン酸、フェンレチニド、9−シス−レチノイド酸、13−シス−レチノイド酸、全てのトランス−レチノイン酸、イソトレチノメン、トレチノイド、ビタミンB6、ビタミンB12、ビタミンC、ビタミンD、ビタミンE、シクロオキシゲナーゼ阻害剤、非ステロイド性抗炎症薬物(NSAID)、アスピリン、イブプロフェン、セレコキシア、ポリフェノール、ポリフェノールE、緑茶抽出物、葉酸、グルカル酸、インターフェロンα、アネトールジチオールエチオン、亜鉛、ヒリドキシン、フィナステリド、ドキサゾジン、セレニウム、インドール−3−カルビナール、α−ジフルオロメチルオルニチン、カロテノイド、β−カロテン、リコペン、酸化防止剤、補酵素Q10、フラボノイド、ケルセチン、クルクミン、カテキン、エピガロカテキンガレート、N−アセチルシステイン、インドール−3−カルビノール、イソシトール六リン酸、イソフラボン、グルカン酸、ローズマリー、大豆、ノコギリパルメット及びカルシウム。本発明への使用のために適切な化学予防剤の追加の例は、癌用ワクチンである。それらは、ワクチン接種工程により標的化される癌細胞型の全て又は一部により患者を免疫化することにより製造され得る。
【0158】
副作用制限剤:
ニトロベンズアミド化合物単独による又は他の抗癌化合物と組合せての癌の治療は、抗癌剤により生成される副作用を緩和できる医薬剤の投与により達成され得る。本明細書における使用のために適切なそのような剤は、鎮吐薬、抗粘膜炎薬剤、疼痛処理薬剤、感染抑制剤及び抗貧血/抗血小板減少剤を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な鎮吐薬の例は、5−ヒドロキシトリプタミン3受容体拮抗薬、メトクロプラミド、ステロイド、ロラゼパム、オンダンセトロン、カンナビノイ、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な抗粘膜炎薬剤の例は、パリフェミン(ケラチン細胞成長因子)、グルカゴン様ペプチド2、テジュクルチド、L−グルタミン、アミホスチン及び繊維芽細胞成長因子20を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な疼痛処理薬剤の例は、オピイオイド、オピエート及び非ステロイド性抗炎症化合物を包含する。本明細書における使用のために適切な感染を制御するために使用される剤の例は、次のものを包含するが、但しそれらだけには限定されない:抗菌剤、例えばアミノグリコシド、ペニシリン、セファロスポリン、テトラサイクリン、クリンダマイシン、リンコマイシン、マクロライド、バンコマイシン、カルバペネム、モノバクタム、フルオロキノロン、スルホンアミド、ニトロフラントイン、それらの類似体及び誘導体。本明細書における使用のために適切な化学療法に関連する貧血又は血小板減少症を処理できる剤の例は、エリスロポイエチン及びトロンボポイエチンを包含するが、但しそれらだけには限定されない。
【0159】
ニトロベンズアミド化合物及び本明細書に記載される他の化合物と組合せての使用のための幾つかの他の適切な療法がまた利用できる。例えば、Goodman & Gilman's The Pharmacological Basis of Therapeutics 1 lth ed. Brunton LL, Lazo JS, and Parker KL, ed. McGraw-Hill, New York, 2006を参照のこと。
【0160】
製剤、投与路及び有効用量:
本発明のもう1つの観点は、ニトロベンズアミド代謝化合物を含んでなる医薬組成物のための配合及び投与路に関する。そのような医薬組成物は、上記に詳細に記載された方法により癌を治療するために使用され得る。
【0161】
幾つかの態様においては、上記に示される代謝化合物は、個々の、又はプロドラッグとして組合せて供給され、/又は投与の後、インビボでニトロソベンズアミド形に相互転換され得る。さらに、前記代謝化合物は、プロドラッグとして供給され、/又は投与の後、インビボでニトロソベンズアミド形に相互転換され得る、式Iaのニトロベンズアミドと共に投与され得る。すなわち、ニトロベンズアミド形及び/又はニトロソベンズアミド形のいずれか、又は医薬的に許容し得る塩が、本発明への使用のための製剤の開発に使用され得る。さらに、幾つかの態様においては、代謝化合物は、1又は2以上の他の化合物、又は1又は2以上の他の形と組合せて使用され得る。例えば、製剤は、ニトロベンズアミド代謝化合物及び酸形の両者を、特定の割合で、個々の相対的能力及び意図される指標に依存して、含んでなる。前記2種の形は、同じ投与量単位で、例えば1つのクリーム、坐薬、錠剤、カプセル又は飲料水に溶解される粉末のパケットに、一緒に配合され得;又は個々の形は、別々の単位、例えば2種のクリーム、2種の坐薬、2種の錠剤、2種のカプセル、錠剤及び錠剤を溶解するための液体、粉末のパケット及び粉末を溶解するための溶液、等に配合され得る。
【0162】
ニトロベンズアミド代謝化合物及びもう1つの活性剤の組合せを含んでなる組成物は効果的である。2種の化合物及び/又は化合物形は、同じ投与量単位、例えば1つのクリーム、坐薬、錠剤、カプセル又は飲料水に溶解される粉末のパケットに一緒に配合され得;又は個々の形が、別々の単位、例えば2種のクリーム、坐薬、錠剤、2種のカプセル、錠剤及び錠剤を溶解するための液体、粉末ぱっと及び粉末を溶解するための液体、等に配合され得る。
【0163】
用語“医薬的に許容し得る塩”とは、本発明に使用される化合物の生物学的有効性及び性質を保持し、生物学的に又は他方では所望であるそれらの塩を意味する。例えば、医薬的に許容し得る塩は、癌の治療において本発明の化合物の有益な効果を妨げない。
【0164】
典型的な塩は、無機イオン、例えばナトリウム、カリウム、カルシウム及びマグネシウムイオンのそれらの塩である。そのような塩は、無機又は有機酸、例えば塩酸、臭酸、リン酸、硝酸、硫酸、メタンスルホン酸、p−トルエンスルホン酸、酢酸、フマル酸、琥珀酸、乳酸、マンデル酸、リンゴ酸、クエン酸、酒石酸又はマレイン酸との塩を包含する。さらに、本発明に使用される化合物がカルボキシ基又は他の酸性基を含む場合、それは無機又は有機塩基による医薬的に許容し得る付加塩に転換され得る。適切な塩基の例は、水酸化ナトリウム、水酸化カリウム、アンモニア、シクロヘキシルアミン、ジシクロヘキシル−アミン、エタノールアミン、ジエタノールアミン及びトリエタノールアミンを包含する。
【0165】
経口投与に関しては、代謝化合物は、活性化合物と、当業界において良く知られている医薬的に許容し得るキャリヤーとを組合すことにより容易に配合され得る。そのようなキャリヤーは、処理される患者による経口摂取のための、錠剤、咀嚼錠剤、ピル、糖剤、カプセル、トローチ、ハードキャンデー、液体、ゲル、シロップ、スラリー、粉末、懸濁液、エリキシル、ウェハー及び同様のものとしての本発明の化合物の配合を可能にする。そのような製剤は、医薬的に許容し得るキャリヤー、例えば固体希釈剤又は充填剤、無菌水性媒体及び種々の非毒性有機溶媒を含んでなる。一般的に、本発明の化合物は、所望する投与量単位を提供するのに十分な量で、経口投与形の合計組成物の約0.5重量%、約5重量%、約10重量%、約20重量%、又は約30重量%〜約50重量%、約60重量%、約70重量%、約80重量%又は90重量%の濃度レベルで含まれるであろう。
【0166】
水性懸濁液は、ニトロベンズアミド代謝化合物、及び医薬的に許容し得る賦形剤、例えば沈殿防止剤(例えば、メチルセルロース)、湿潤剤(例えば、レシチン、リソレシチン及び/又は長鎖脂肪アルコール)、並びに着色剤、保存剤、風味剤及び同様のものを含むことができる。
【0167】
幾つかの態様においては、油又は非水性溶媒は、例えば大きな親油性成分の存在のために、代謝化合物を溶液にすることが必要とされる。他方では、エマルジョン、懸濁液、又は他の調製物、例えばリポソーム調製物が使用され得る。リポソーム調製物に関しては、病状の処理のためのポリマーを調製するためのいずれの既知方法でも使用され得る。例えば、Bangham et al., J. MoI. Biol, 23: 238-252 (1965)及び Szoka et al., Proc. Natl Acad. Sci 75: 4194-4198 (1978)(引用により本明細書に組込まれる)を参照のこと。リガンドはまた、作用の特定部位にそれらの組成物を向けるためにリポソームに結合され得る。本発明の化合物はまた、食品、例えばクリームチーズ、バター、サラダドレッシング、又はアイスクリームに、一定の患者集団における溶解性、投与及び/又はコンプライアンスを促進するために組込まれ得る。
【0168】
経口使用のための医薬製剤は、任意には、得られる混合物を粉砕し、所望には、錠剤又は糖剤コアーを得るために、適切な助剤の添加の後、顆粒の混合物を処理することにより、固体賦形剤として得られる。適切な賦形剤は特に、充填剤、例えば糖、例えばラクトース、スクロース、マンニトール、又はソルビトール;風味要素、セルロース調製物、例えばトウモロコシ澱粉、小麦澱粉、米澱粉、ジャガイモ澱粉、ゼラチン、トラガカントガム、メチルセルロース、ヒドロキシプロピルメチルセルロース、ナトリウムカルボキシメチルセルロース、及び/又はポリビニルピロリドン(PVP)である。所望には、砕解剤、例えば架橋されたポリビニルピロリドン、寒天、又はアルギン酸、又はその塩、例えばアルギン酸ナトリウムが添加され得る。前記化合物はまた、持効性製剤としても配合され得る。
【0169】
糖剤コアーは、適切な被覆が供給され得る。このためには、任意にはアラビアゴム、タルク、ポリビニルピロリドン、カルボポールゲル、ポリエチレングリコール、及び/又は二酸化チタン、ラッカー溶液及び適切な有機溶媒又は溶媒混合物を含むことができる、濃縮された糖溶液が使用され得る。染料又は色素が、識別のために、又は活性化合物用量の異なった組合せを特徴づけるために、錠剤又は糖剤被膜に添加され得る。
【0170】
経口使用され得る医薬製剤は、ゼラチンから製造された押込嵌めカプセル、及びゼラチン及び可塑剤、例えばグリセロール又はソルビトールから製造される、密封された軟質カプセルを包含する。押込嵌めカプセルは、活性成分、並びに充填剤、例えばラクトース、結合剤、例えば澱粉、及び/又は滑剤、例えばタルク又はステアリン酸マグネシウム、及び任意には安定剤を含むことができる。軟質カプセルにおいては、活性化合物は、適切な液体、例えば脂肪油、液体パラフィン又は液体ポリエチレングリコールに溶解されるか又は懸濁され得る。さらに、安定剤が添加され得る。経口投与のための全ての製剤は、投与のために適切な投与量で存在すべきである。
【0171】
注射に関しては、本発明の阻害剤は、水溶液、好ましくは生理学的に適合できる懸濁液、例えばハンクス溶液、リンガー溶液又は生理学的塩緩衝液において配合され得る。そのような組成物はまた、1又は2以上の賦形剤、例えば保存剤、溶解剤、充填剤、滑剤、安定剤、アルブミン及び同様のものを含むことができる。例えば、Remington's Pharmaceutical Sciences, latest edition, Mack Publishing Co., Easton Pに開示されるような配合方法は、当業界において知られている。それらの化合物はまた、経粘膜投与、口腔内投与、吸入による投与、非経口投与、経皮投与及び直腸投与のためにも配合され得る。
【0172】
これまで記載された製剤の他に、代謝化合物はまた、デポ製剤としても配合され得る。そのような長期作用性製剤は、移植又は経皮供給(例えば、皮下又は筋肉内)、筋肉内注射又は経皮用パッチの使用により投与され得る。従って、例えば化合物は、適切なポリマー又は親水性材料(例えば、許容できる油中、エマルジョンとして)、又はイオン交換樹脂と共に、又は親水性材料(例えば、許容できる油中、エマルジョンとして)、又はイオン交換樹脂と共に、又は低溶解性誘導体として、例えば低溶解性塩として配合され得る。
【0173】
本発明における使用のために適切な医薬組成物は、活性成分が有効量で、すなわち本明細書に記載される少なくとも1つの癌において治療及び/又は予防的有益性を達成するの有効な量で存在する組成物を包含する。特定の用途のために効果的な実際の量は、処理される状態、対象の状態、配合及び投与路、並びに当業者に知られている他の要因に依存するであろう。ニトロベンズアミド代謝化合物の有効量の決定は、本明細書における開示の点から、当業者の能力内であり、通常の最適化技法を用いて決定されるであろう。
【実施例】
【0174】
実施例1:ベンズアミド代謝物の同定:
血漿サンプルを、イヌ、ラット及びマウス研究から得、ここで動物は4−ヨード−3−ニトロベンズアミド(BA)を投与されている。血漿及び腫瘍サンプルを、血漿(40μl)を、3倍体積(150μl)のアセトニトリルにより沈殿することにより、HPLC注入のために調製した。組織サンプルを、組織1mg当たり1μlのアセトニトリルを添加し、次に電気ホモナイザーにより均質化することにより、HPLC注入のために調製した。遠心分離に続いて、150μlの個々の上清液を蒸発乾燥し、水中、0.2%蟻酸50μlにおいて再構成し、クロマトグラフィー及び質量分光技法(LC/MS/MS条件)により分析した。LC/MS/MS条件は次の通りである:HPLC(Shimadzu VP System);移動相:水中、0.2%蟻酸(A)及びメタノール中、0.18%蟻酸(B);カラム:1×50mmのThermo Betabasic C18カラム;注入体積:25μl;グラジエント:30分での0〜6%B;流速:100μl/分;質量分光計:Applied Biosystems/MDS SCIEX Q-STAR;インターフェイス:1/10でのIonSprayスプリット;親イオン走査:200〜900amuのTOF陽性;生成物イオン走査:親イオン走査における最も強いイオンの60〜900amuのTOP生成物イオン;TOP検量:Renin基質を用いて外部的に検量された。イヌ及びマウス血漿からの代謝物同定の結果が、次の通りに表1〜3に示される。
【0175】
表1:イヌ血漿からのLC/MS/MSによるBA代謝物同定の要約:
【表1】

*:近似ng/ml等価値は、対照標準として1μg/mlのスパイクサンプルにおけるBSI−201を用いて測定された。
【0176】
明確化のため、上記表1における名称は、次の通りに上記に開示される化合物に対応する(名称:化合物);M2:MS472、M3:MS213及びM4:MS263。
【0177】
表2:ネズミ血漿からのLC/MS/MSによるBA代謝物同定の要約:
【表2】

*:近似ng/ml等価値は、対照標準として1μg/mlのスパイクサンプルにおけるBSI−201を用いて測定された。
【0178】
明確化のため、上記表2における名称は、次の通りに本明細書に開示される化合物に対応する(名称:化合物);M3:MS472、M6:MS328、M7:MS213及びM8:MS263。
【0179】
表3:イヌ血漿及び赤血球細胞からのLC/MS/MSによるBA代謝物同定の要約:
【表3】

*近似ng/ml等価値は、対照標準として5μg/mlのスパイクサンプルにおけるBSI−201の270nmUVピーク領域を用いて測定された。
【0180】
明確化のため、上記表3における名称は、次の通りに本明細書に開示される化合物に対応する(名称:化合物);M2:MS472及び第2のM2:MS601。
【0181】
実施例2:インビトロ研究−細胞毒性アッセイ:
異なった起源の異なったタイプの癌細胞系又は一次細胞を、48ウェルプレート(5×104)又は96ウェルプレート(2×104)上に接種する。細胞を適切な培地において培養し得る。培養を、95%O2/5%CO2の湿潤された雰囲気下で37℃のインキュベーターにおいて維持し得る。細胞の接種の後(24時間)、培地を除き、200μMのBSOの存在又は不在下で、種々の濃度のINO2BA又はINH2BPの存在下で培養培地により置換する。37℃での6日間のインキュベーションの後、細胞生存度を、Cell Titer-Blue, Cell Viability Assay (Promega) (O'Brien, J.et al. (2000) Investigation of the Alamar Blue (resazurin) fluorescent dye for the assessment of mammalian cell cytotoxicity. Eur.J.Biochem.267, 5421-26 and Gonzalez, R.J.and Tarloff, J.B. (2001) Evaluation of hepatic subcellular fractions for Alamar Blue and MTT reductaseを参照のこと)を用いて測定する。このアッセイは、活性色素還元による検出に基づかれる蛍光測定/比色成長インジケーターを組込む。細胞毒性を、成長阻害により測定される。
【0182】
細胞毒性をまた、生存細胞の数を計数することにより評価し得る。細胞をPBSにより単層を洗浄することにより収穫し、続いて0.25%のトリプシン及び0.02%のEDTAにおいて短時間インキュベーションした。次に、細胞を集め、遠心分離により2度、洗浄し、PBSに再懸濁する。細胞数及び生存度を、0.2%トリパンブルー塩溶液により小体積の細胞懸濁液を染色し、血球計算機により細胞を試験することにより決定する。Kerley-Hamilton et al. (2005) p53-dominant transcriptional response to cisplatin in testicular germ cell tumor-derived human embryonal carcinoma及びCheol et al. (2005) Induction of apoptosis and inhibition of cyclooxygenase-2 expression by N-methyl-N'-nitro-N-nitrosoguanidine in human leukemia cellsを参照のこと。
【0183】
実施例3:BrdU−ELISAにより測定される細胞増殖:
細胞を、37℃で湿潤された雰囲気下でウェル当たり100μlの最終体積で、ブラック96ウェルMultiplate(組織培養品種:平らな透明底)において種々の濃度の試験物質(薬物)の存在下でインキュベートし得る。10μl/ウェルのBrdUラベリング溶液を、細胞を100μl/ウェルにおいて培養した後(最終濃度:10μMのBrdU)、添加し、細胞を37℃でさらに2〜24時間、再インキュベートする(細胞が200μl/ウェルで培養される場合、20μl/ウェルのBrdUラベリング溶液を添加した)。MPを、300m×gで10分間、遠心分離し、ラベリング培地をカニューレを用いて吸引により除去した。細胞を、ヘアードライヤーを用いて、約15分間、又は他方では、60℃で1時間、乾燥する。200μl/ウェルのFixDenatを細胞に添加し、15〜25℃で30分間インキュベートする。FixDenat溶液を、軽くはね飛ばし、タッピングすることにより十分に除去する。100μl/ウェルの抗−BrdU−POD作業溶液を添加し、15〜25℃で約90分間インキュベートする。他方では、このインキュベーション時間は、個々の必要条件に依存して、30〜120分、変動する。抗体接合体を、軽くはね飛ばすことにより除去し、ウェルを200〜300μl/ウェルの洗浄溶液により3度、すすいだ。洗浄溶液をタッピングすることにより除去する。次に、100μl/ウェルの基質溶液を個々のウェルに添加する。サンプルの発光を、光電増倍管によりマイクロプレートルミノメーターにより測定し得る。
【0184】
実施例4:インビボ移植及び腫瘍増殖:
100匹の雌NU/NU−nuBRマウス(Charles River、生後5〜6週)を、0.72mgの17β−エストラジオール(ヒト)ペレットにより移植し、耳をクリップを用いて標識し、腫瘍細胞移植の24〜48時間前、計量する。腫瘍細胞BT472(2×107個の細胞/マウス)を、肩甲下乳房脂肪パッド(0.2mlの体積)中に注入する。キャリパー測定を、21日目、及びその後、毎週3度(月、水、金)始める。動物を、腫瘍の存在及び不在に従って、及び次に、腫瘍体積により分離する。移植後第3週から初めて、動物を週当たり2度、計量する(月及び金)。薬物処理を、腫瘍サイズが150〜250kmm3(L×W×H)である場合、開始する。薬物及びビークル投与は、5日間、胃管栄養法(BP+BSO)によるBID及びIP(BA)によるSIDである。次のサイクルが開始する前、2日の自発休眠期が存在する。動物は、予測できない毒性が存在しない限り、3回のサイクル(それぞれ5日)を受けることができる。初期値又は一定の微候の表示の15%を越える体重の低下が、動物安楽死のための基準として使用さえ得る。薬物は、5mg/kgの体積で、胃管栄養法及びIPにより投与される。薬物及びビークルを、箔−被覆されたボトルにおいて4℃で貯蔵する。
【0185】
【表4】

*:BP+BSO及びBAの組合せ。
【0186】
実施例4:異種移植片研究:
代謝化合物の効果を、ヌードマウスにおける卵巣ヒト癌細胞(OVCAR)異種移植片に対して評価する。
【0187】
雌NU/NU37−BU−04−BACマウス(Charles River, 生後5〜6週)の耳を、クリップを用いて標識し、腫瘍細胞移植の24〜48時間前、計量する。腫瘍細胞Ovcar3(5×106個の細胞/マウス)を、雌ヌードマウス宿主の肩甲下の乳房脂肪パッド中に皮下移植する。キャリパー測定を、腫瘍細胞移植後、7日目、その後、週2度(月及び金)開始する。動物を、腫瘍の存在又は不在に従って、及び次に腫瘍体積に従って分離する。動物を週1度、計量する。薬物処理を、サイズが最大直径0.4〜0.5cmになる場合、開始する。4−ヨード−3−ニトロベンズアミド(BA)(50μlの100%DMSO/マウスにおける)及びビークル(50μlの100%DMSO/マウスにおける)を、5日間、1日当たり2度、IPにより、注入する。次のサイクルが始まる前、2日の自発休眠期間が存在する。
【0188】
【表5】

【0189】
実施例5:代謝化合物の効力の評価:
一般的方法:
MDA MB231ヒト乳癌細胞を、雌ヌードマウスの右側面中に皮下注入し得る。作業1に関しては、BPを、腫瘍細胞移植の前、5日間連続して投与し、その後、薬物投与を、4〜8週間、週5日続ける。作業2に関しては、癌細胞を、腫瘍が50〜60mm3の平均腫瘍体積に達する場合、注入し、マウスを8匹のグループに分け、トウモロコシ油:PEG400(対照)、BP, 又はCTX(MDA MB231陽性対照)により処理する。腫瘍体積を、処理の開始の後、90日間モニターする(MDA MB231に関する)。
【0190】
細胞系:
MDA MB231は、細胞系が開始する前3ヶ月で、5−RU, ドキソルビシン、メトトレキセート及びCTXにより処理された患者の胸膜浸出液から1973年、確立されたヒト乳癌細胞系である。この細胞系は、エストロゲン受容体陰性であり、ホルモン拮抗薬として標的化されない抗癌薬物のスクリーニングに使用されて来た。MDA MB231は、NaHCO3/l、10%ウシ胎児血清(FBS)及び2mMのL−グルタミンを含むダルベッコ変性イーグル培地(DMEM)において増殖し、湿潤された5%CO2/空気インキュベーターにおいて37℃で維持した。抗体を、培地に添加しなかった。
【0191】
動物腫瘍モデル:
マウス:
雌CB.17SCIDマウス(Charles River)は、生後8〜11週であり、研究のD1で、12.6〜23.0gの範囲の体重(BW)を有した。動物は、水(逆浸透、1ppmのCl)、及び18.0%の粗タンパク質、5.0%の粗脂肪及び5.0%の粗繊維からなるNIH 31 Modified and Irradiated Lab Diet*を、自由に供給された。マウスは、実験動物の保護及び使用について、許容された標準とのコンプライアンスを確かにする、Assessment and Accreditation of Laboratory (AAALAC) Internationalにより認定された実験所において、21〜22℃(70〜72°F)及び40〜60%湿度で12時間の光サイクルに基づいて、静的にマイクロアイソレーターにおける照射されたALPHA-dri(登録商標) bed-o-cobs* Laboratory Animal Beddingに収容された。
【0192】
腫瘍移植:
この研究に使用されるヒトOVCAR−3(NIH−OVCAR−3)卵巣腺癌を、一連の移植により無胸腺ヌードマウスにおいて維持した。腫瘍フラグメント(1mm3)を、個々の試験マウスの右側部中に皮下(s.c.)移植した。腫瘍を週2度モニターし、それらの体積が80〜120mm3に達する場合、毎日モニターした。研究のD1で、動物を、63〜221mm3の腫瘍サイズを有する処理グループ及び約105mm3の平均腫瘍サイズのグループに分類した。
【0193】
腫瘍サイズ(mm3)は、下記式から計算された:
【数1】

【0194】
腫瘍重量を、1mgが1mm3の腫瘍体積に等しい仮定に基づいて評価する。
【0195】
処理:
マウスを9のグループ(n=10)に分類し、前記プロトコールに従って処理した。経口グループは、D68a.m.(最後までb.i.d.(毎日2度))まで、D1p.m.から、毎日2度、BAを経口的(p.o.)に受けた。Alzetモデルの浸透ポンプを、1,15及び29日目に移植した。ポンプは、37℃で約1時間、予備的に暖められ、次に、イソフルオラン麻酔されたマウスの左側部にs.c.移植された。個々のポンプは、14日間にわたって合計用量の25mgの/kg/週のBAを供給した。
【0196】
エンドポイント:
腫瘍は、研究の期間、週2度カリパスにより測定された。個々の動物は、その腫瘍が予定されたエンドポイントサイズ(1,000mm3)に達した場合、安楽死された。個々のマウスについてのエンドポイントの時間(TTE)は、次の等式により計算された:
【数2】

ここでTTEは日で表され、エンドポイント体積はmm3で示され、bは切片であり、mはlog−転換された腫瘍増殖データ組の線状回帰により得られた直線の傾斜である。
【0197】
そのデータ組は、研究エンドポイント体積を越える最初の観察、及びエンドポイント体積の到達の直後、3回の連続した観察から構成される。計算されたTTEは通常、動物が腫瘍サイズに関して安定死される日以下である。エンドポイントに達しない動物は、研究の最後で安定死され、最後の日(68日)に等しいTTE値を割り当てられる。処理効力を、対照のグループに比較して、処理グループについてのメジアンTTEの上昇として定義される、腫瘍増殖遅延(TGD)から決定した:TGD=日で表され、又は対照グループのメジアンTTEの百分率として表される、T−C:
【数3】

式中、T=処理グループについてのメジアンTTE、C=対照グループ1についてのメジアンTTE。
それらの研究の結果は図4に示される。
【0198】
生後4〜5週の雌Swiss NGヌード(nu/nu)マウスを、Taconic (Germantown, NY)から入手する。動物は、Bio Bubble, Inc. (Fort Collins, CO)から購入されたバリアクリーンルームにおいて無菌フィルターを上部に付けられたゲージにおいて、ケージ当たり3匹で収容される。達着後、それらは、使用の前、4日の作業目の間、検疫される。処理は、72±5°F及び35〜70%の相対湿度で維持され、12時間の明/暗サイクルが使用された。マウスは、無菌でオートクレーブできる、保証されたPurina齧歯動物用食事を自由に供給される。飲料水は酸性にされ、オートクレーブ処理され、水源を再循環され、脱イオン化され、UV−処理され、5μmのフィルター処理される。
【0199】
動物を検疫から開放した後、マウスは、1又は5×106個のMDA MB231細胞(0.1mlの注入体積)を、右側部に皮下注入される。タスク1に関するマウスは、細胞注入の前5日間、前処理を受けた。腫瘍寸法及び体重を、週2度、測定する。ノギスを用いて、腫瘍を3面から測定し、腫瘍体積(V)を次の通りに計算する:V=π(x×y×z)/6、ここでx、y及びzは腫瘍測定値−皮膚の厚さである。実験の最後で、マウスを、CO2吸入、続く頸部転移により殺す。
【0200】
医薬:
MS472を、30mg/ml及び100mg/mlの濃度で、トウモロコシ油:PEG400(2:1、v/v)において製造し得る。薬物は、それらの濃度での懸濁液であり得る。陽性対照薬物は、リン酸緩衝溶液(PBS)及びCTXに基づいて、15mg/mlで製造される。両薬物は、使用の前、フィルター殺菌され得る(0.2μmのフィルター)。
【0201】
処理プロトコール:
タスク1に関しては、MDA MB231腫瘍細胞により移植されたマウスを、MS472(300又は1000mg/kg)により5日間、前処理し、細胞懸濁液の皮下注入に続いて、薬物処理を、最少4週間、週5日間(月〜金)、続ける。
【0202】
タスク2に関しては、腫瘍体積が予定されたサイズ(50〜60mm3の平均腫瘍体積)に達した後、マウスをそれぞれ8匹のマウスの処理グループに分ける。BPの全ての処理を、少なくとも4週間、週当たり5度(月〜金)、行う。CTXは、150mg/kgの用量で1度、腹腔内投与される。全てのBP処理は経口的に行われ;投与量は、MDA MB231細胞により移植されたそれらに関しては、1000又は2000mg/kgであった。個々のタスクに関して、全ての処理は同じ日に開始した。
【0203】
腫瘍は、最初の処理の後、少なくとも9週間、週2度、測定される(MDA MB231)。個々のグループについての平均腫瘍体積を、個々の時点について計算する。特定時間でのグループ間の比較を、非対両側t検定を用いて行い、結果を、分散分析(ANOVA)を用いて分析する。タスク2に関しては、個々の腫瘍体積(V)を、0日、すなわち処理の最初の日(VO)での腫瘍体積の割合として表す。個々のグループに関しては、VNO比率の平均を、処理の後の時間の関数としてプロットする。処理に対する応答を、処理に対する腫瘍応答に依存して、2種の手段で測定する。腫瘍体積倍増化時間(VDT)及び体積4倍化時間(VQT)を、処理に対する応答が存在するグループにおけるlog(腫瘍体積)の関数としての時間のプロットに基づく線状回帰法により、個々の腫瘍について決定する。個々の処理グループについての腫瘍倍増遅延を決定し、グループ間の比較をANOVAを用いて分析する。
【0204】
全身毒性を、処理後の体重の低下から評価する。マウスは、追跡期間の最後で、又は腫瘍体積が早く1600mm3に達するか又は腫瘍が潰瘍化した場合、殺害される。
統計学的分析:
【0205】
統計学的分析を、InStat(Graphpad Software, San Diego, CA)を用いて行う。
【0206】
腫瘍増殖:
MDA MB231腫瘍は、腫瘍細胞注入の3週間以内に測定可能であり、通常、よりゆっくり増殖し、倍増化時間は7日である。値は、対照のグループから計算され得る。処理の開始での平均腫瘍体積及び体重が、タスク1に関して表4日及びタスク2に関して表5に示されるフォーマット下で示され得る。
【0207】
表4:
処理の開始でのマウスパラメーター−タスク1:
【表6】

*SEM=標準誤差
【0208】
表5:
処理の開始でのマウスパラメーター−タスク2:
【表7】

*SEM=標準誤差
【0209】
上記実施例は、本発明の範囲を制限するものではない。さらに、多くの変更及び修飾が本発明の範囲内で行われることは、当業者に明らかである。
【0210】
実施例6:細胞周期分析:
HCT116及びHela細胞を、ATCCから入手した。DNA含量分析に関しては、2×105個の細胞を、PBSにより2度、洗浄し、70%エタノールに固定した。細胞を、37℃で20分間、100単位/mlのRNアーゼAにより処理し、Alexa Fluor(登録商標)405蛍光染色(Invitrogen)を含む冷PBSに、その製造業者のプロトコールに従って再懸濁した。細胞を流動細胞計測法により分析した。図1は、PARP−1阻害剤(4−ヨード−3−ニトロベンズアミド又は“BA”)により19時間、処理されたHTC16細胞における(FACSドットプロット及びヒストグラム)細胞周期分析を示す。BA処理は、S期細胞周期の同時低下を伴って、対照に比較して(18.6%)、G1期における細胞数の上昇(48.6%)を引起した。
【0211】
DNA複製分析に関しては、2×105個の細胞を、50μモル/lのブロモデオキシウリジン(BrdUrd)と共に30分間インキュベートした。細胞を70%エタノールに固定し、BrdUrd組込めを、抗−BrdUrd−FITC 抗体(Becton Dickinson, Franklin Lakes, NJ)を用いて、その製造業者のプロトコールに従って、流動細胞計測法により決定した。G2/Mチェックポイントの程度を評価するために、有糸分裂細胞を、有糸分裂−特異的抗体GF−7を用いて、流動細胞計測法により検出した。固定された細胞を、GF7−フィコエリトリン(PE)抗体(BD Biosciences Pharmingen)と共に30分間インキュベートし、PBSにより洗浄し、流動細胞計測法により分析した。図2は、24時間のインキュベーションで、BA、BNO(4−ヨード−3−ニトロソベンズアミド)及びBNHOH(4−ヨード−3−ヒドロキシアミノベンズアミド)により得られた結果を比較し;図3は72時間でのBA、BNO及びBNHOHに関する結果を示す。
【0212】
像分析及び顕微鏡法:カバーガラス上で増殖する細胞を、PBS中、4%パラホルムアルデヒドにより10分間、固定し、70%エタノールに浸透した。洗浄の後、カバーガラスを、50%PBS/50%グリセロール中、スライド上に積層した。像を顕微鏡により分析した。
【0213】
MDR1発現FACSアッセイ:
KB−V1は、KB−3−1ヒト癌細胞のビンブラスチン耐性クローンである(Fojo, A T , J Whang-Peng, M M Gottesman, and I Pastan 1985 Amplification of DNA sequences in human multidrugresistant KB carcinoma cells Proc Natl Acad Sa USA 82 7661-7665 , Shen, D -W, C Cardarelli, J Iwang, M Cornwell, N Richert, S Is fin, I Pastan, and M M Gottesman 1986 Multiple drug-resistant human KB carcinoma cells independently selected for high-level resistance to colchicine, Adnamycin, or vinblastine show changes in expression of specific proteins J Biol Chem 261 7762-7770)。細胞を、10%ウシ胎児血清を含むイーグル最少必須培地において増殖した。
【0214】
MDR1に関しては、染色細胞をトリプシン処理により収穫し、5%FBSにより補充されたIscoveの変性ダルベッコ培地により洗浄し、次に、抗−Mdr1抗体UIC2を含むIMDM/5%FBSに再懸濁した。一次抗体のとのインキュベーションの後、細胞を洗浄し、次に、フィコエリトリン(PE)抗体(BD Biosciences Pharmingen)に結合される二次抗体と共に、インキュベートした。抗体処理された細胞を洗浄し、次に、FACS Calibur(登録商標)計測期(Becton, Dickinson)上で分析した。FACS分析に使用される対照は、抗体と共にインキュベートされなかった細胞、すなわちイソタイプ対照抗体と共にインキュベートされた細胞であった。三重反復試験サンプルを分析し、それらのヒストグラムを分析した。メジアン蛍光を、log尺度でプロットした。図6A及び6Bは、それぞれ、KB3−1及びKBV−1細胞のレベルを示す:従って、FACFヒストグラムは、KBV−1細胞におけるMDR1の過剰発現を示す。MDR1の過剰発現は、多薬物耐性に関連している。
【0215】
コロニー形成アッセイ:
細胞をトリプシン処理し、計数し、106個の細胞/mlの最終濃度に希釈した。コロニー形成アッセイを、適切な数の細胞を培養皿中にプレートすることにより、三重反復して実施し、0〜100μMの化合物により処理した。14日後、細胞を固定し、1%クリスタルバイオレットにより染色し、コロニーを計数した。図5Cは、KB3−1及びKBV−1細胞におけるこの実験の結果を示す。図5Cに見られるように、BAはMDR1過剰発現及びMDR1正常細胞に関して、用量依存性態様で細胞コロニー数を減じる。MDR1過剰発現は多薬剤耐性に関連するので、この結果は、BAが多薬剤耐性腫瘍に対して効果的であろうことを示唆する。
【0216】
本発明の好ましい態様を本明細書において示し、記載して来たが、そのような態様が単なる例によって提供されることは当業者に明白であろう。現在、本発明から逸脱しないで、多くの変動、変更及び置換が、当業者に明らかになるであろう。本明細書に記載される本発明の態様に対する種々の選択が本発明の実施に使用され得ることは理解されるべきである。次の請求項が本発明の範囲を定義し、それらの請求項の範囲内の方法及び構造体並びにそれらの同等物は保護される。
【背景技術】
【0001】
本出願は2006年9月5日出願の米国仮特許出願の利益を請求する。本出願はその全体が参照により本明細書に組み込まれる。
【0002】
癌は現代社会における深刻な脅威である。悪性癌増殖は、その独自の特徴ゆえに、現代医学の重大な課題となっている。その特徴としては、悪性組織の無秩序な増殖をもたらす制御できない細胞増殖、局所組織やさらには遠隔組織を侵入する能力、分化の欠乏、検出できる症状の欠乏、最も重要な点としては、効果的治療及び予防の欠乏が挙げられる。
【0003】
癌は任意の年齢で、且つ、任意の器官の組織又は任意の組織で進行する。癌の病因は明確には定義されていないが、遺伝的感受性、染色体破損障害、ウィルス、環境因子及び免疫学的障害等の機構が、何れも悪性細胞増殖及び悪性化と関連付けられてきた。癌は、世界数百万人に広く影響を及ぼす多くの種類の医学的状態を包含する。癌が発症するのは、身体の一部の細胞が未分化となり始め、或いは無制御下で増殖し始める場合である。何れの癌型も異常細胞の無制御な増殖と共に開始する。
【0004】
癌には多くの種類、例えば乳癌、肺癌、卵巣癌、膀胱癌、前立腺癌、膵臓癌、頸癌及び白血病が存在する。現在、利用できる主な治療としては、手術、放射線療法、及び化学療法が挙げられる。手術は多くの場合、抜本的な治療であり、深刻な結果をもたらす。例えば、卵巣癌の処理は何れも、不妊症及び/又は性的機能障害をもたらし得る。頸癌及び膀胱癌の処理には、不妊症を引き起すものがある。膵臓癌を治療する手術は、膵臓の部分的又は全体の除去をもたらし、患者に対する重度の危険性を有する。前立腺癌の手術の中には、尿失禁及び性的不能の危険性を有するものがある。肺癌患者の手術は多くの場合、癌性肺組織に接近してこれを除去する必要上、肋骨を切除せねばならず、術後に激しい痛みを生ぜさせる。さらに、肺癌及び肺疾患、例えば気腫又は慢性気管支炎を有する患者には通常、術後に息切れの増加が見られる。
【0005】
放射線療法は、癌細胞殺害の利点を有するものの、同時に非癌性組織に損傷を与える。化学療法は、患者への種々の抗癌剤の投与を包含するが、副作用を伴う場合が多い。
【0006】
世界で1千万人以上の人々が毎年、癌保有患者との診断を受けており、この数は2020年まで新規患者が毎年1千5百万人ずつ上昇することが予測される。癌によって死亡する人は毎年6百万人と、全世界の死亡数の12%を占めている。癌を治療し得る方法が依然として求められている。かかる方法によって、ヒト及び他の哺乳類における癌の予防及び治療に有用な医薬組成物の基礎が提供され得る。
【0007】
一連の抗腫瘍薬物が同定されている。それらの薬物は、ニトロ及びニトロソ化合物及びそれらの代謝物を含み、それらは、“抗ウィルス及び抗腫瘍剤として有用な芳香族ニトロ及びニトロソ化合物及びそれらの代謝物”の名称の1995年11月7日に発行されたアメリカ特許第5,454,871号、“抗ウィルス及び抗腫瘍剤として有用な芳香族ニトロ及びニトロソ化合物及びそれらの代謝物”の名称の1997年9月23日に発行されたアメリカ特許第5,670,518号、“芳香族ニトロ及びニトロソ化合物、及びそれらの代謝物による癌の治療方法”の名称の1999年12月21日に発行されたアメリカ特許第6,004,978号の主題であり、それらの開示は引用により本明細書に組込まれる。それらの化合物の使用は、乳腺癌、乳腺管癌、リンパ性白血病、AIDSを有する免疫制御された患者におけるカポジ肉腫、及び新形成増殖、例えば非ホドキシのリンパ腫、及び一次リンパ腫の処理において有用なものとして当業界において記載されている。しかし、抗腫瘍活性を有する追加の化合物を同定する必要がある。前駆体化合物から単離された代謝物は、個々に、又は種々の癌細胞を標的化する他の化合物と組合せて使用され得る抗腫瘍剤を提供する。
【発明の概要】
【課題を解決するための手段】
【0008】
本発明は一般的に、芳香族ニトロベンズアミド代謝化合物を用いての腫瘍形成疾病の治療方法に関する。より特定には、それは、ニトロ化合物ベンズアミド前駆体分子由来のニトロベンズアミド代謝化合物、及び哺乳類における腫瘍増殖の抑制及び阻害への、前記代謝物、又はその塩、溶媒化合物、異性体、互変異体、代謝物、類似体又はプロドラッグの使用に関する。
【0009】
本発明の1つの観点においては、式(Ia)の化合物及び1又は2以上の追加の薬理学的活性剤を含んでなる医薬組成物の投与を含んでなる、癌及び癌に関する阻害の処理方法が提供される。もう1つの観点においては、式(Ia)の化合物由来の代謝化合物及びブチオニンスルホキシミン(BSO)の組合せの投与を含んでなる、癌及び癌に関連する阻害の処理方法が提供される。前記代謝物はまた、BSOを伴って又はそれを伴わないで、式(II)のベンゾヒロン化合物と組合せても投与され得る。
【0010】
それらの観点の態様は、種々の癌、例えば白血病、乳癌、卵巣癌、膀胱癌、前立腺癌、膵臓癌及び頸癌、並びに本明細書に記載される他の癌タイプの処理方法を包含する。
【0011】
本発明は、物質の組成物及び医薬組成物、及び癌の治療へのそれらの使用方法に関する。例えば、本発明の組成物は、本明細書に記載される複数の化合物の組合せ、及び/又は本明細書に記載される複数形の化合物の組合せであり得る。本発明の医薬組成物は、対象への投与のために適切な組成物であり得る。
【図面の簡単な説明】
【0012】
【図1】図1(FACSドットプロット及びヒストグラム)は、PARP−1阻害剤(4−ヨード−3−ニトロベンズアミド又は“BA”)により19時間、処理されたHTC116細胞における細胞周期分析を示す。BA処理は、対照(18.6%)に比較して、S期細胞周期の同時低下と共に、G1期における細胞数の低下(48.6%)を引起した。
【図2】図2(FACSドットプロット及びヒストグラム)は、PARP−1阻害剤BA、4−ヨード−3−ニトロベンズアミド(BNO)及び4−ヨード−3−ヒドロキシアミノベンズアミド(BNHOH)により24時間、処理されたHela細胞の周期分析を示す。細胞周期のS期におけるBrdU染色ラベル細胞。有糸分裂におけるGF7染色ラベル細胞。
【図3】図3(FACSドットプロット及びヒストグラム)は、PARP−1阻害剤BA、4−ヨード−3−ニトロベンズアミド(BNO)及び4−ヨード−3−ヒドロキシアミノベンズアミド(BNHOH)により72時間、処理されたHela細胞の周期分析を示す。細胞周期のS期におけるBrdU染色ラベル細胞。有糸分裂におけるGF7染色ラベル細胞。
【図4】図4は、雌SCIDマウスにおけるヒトOVCAR−3卵巣腺癌異種移植片におけるBA活性を示す。BAは、50mg/kg/用量で経口b.i.d.投与されるか、又は25mg/kg/週の用量で浸透ポンプによりs.c.投与される。
【図5】図5は、BAが、MDR1をアップレギュレートする多薬物耐性細胞、及びMDR1−陰性細胞を標的化することを示す。図5Aは、KB3−1細胞におけるMDR1発現のレベルを示す。図5Bは、KB V−1細胞におけるMDR1発現のレベルを示す。FACSヒストグラムは、KB V−1細胞におけるMDR1の過剰発現を示す。MDR1の過剰発現は、多薬物耐性に関連しているので、図5Cに示されるように、BAがK3−1及びKB V−1細胞の両者において用量依存性細胞死をもたらすことは注目に値する。
【発明を実施するための形態】
【0013】
本明細書で言及される出版物及び特許出願は何れも、各出版物又は特許出願について個別具体的に参照により本明細書に組込まれる旨を記載したのと同様に、参照により本明細書に組込まれる。
【0014】
「ニトロベンズアミド前駆体化合物」は、下記式(Ia):
【化1】

[式中、R1、R2、R3、R4及びR5は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C4)シクロアルキル及びフェニルからなる群から独立して選択され、ここで5種のR1、R2、R3、R4及びR5置換基の少なくとも2つは常に水素であり、5種の置換基の少なくとも1つは常にニトロであり、ニトロに隣接して位置する少なくとも1つの置換基は常にヨードである]で表される化合物、及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグを意味する。R1、R2、R3、R4及びR5はまた、ハロゲン化物、例えばクロロ、フルオロ又はブロモであり得る。“前駆体化合物”とは、代謝化合物をもたらす、1又は2以上の化学的又は生化学的工程(例えば、細胞又は生物における)を受ける化合物である。用語“前駆体”、“前駆体化合物”、“ベンズアミド前駆体”又は“ニトロベンズアミド前駆体”とは本明細書において、交換可能的に使用される。
【0015】
“代謝物”とは、出発化合物の生成物とは、構造的に異なる生成物をもたらすいずれかのインビトロ又はインビボ代謝工程を通して生成される化合物を意味する。用語“代謝物”とは、ニトロベンズアミド代謝化合物を包含する。代謝物は、前駆体化合物、例えば式(Ia)で示される前駆体化合物に対していずれかの位置で存在する種々の数又はタイプの置換基を含むことができる。さらに、代謝物は、本明細書に示される化合物に対していずれかの位置で存在する多くのタイプの置換基で異なることができる。さらに、用語“代謝物”、“代謝化合物”、“ベンズアミド代謝化合物”又はニトロペンズアミド代謝的化合物“は、本明細書において交換可能的に使用される。
【0016】
“手術”とは、治癒、治療又は診断効果を得るために、ヒト又は他の哺乳類の身体に対する手動的又は器具を伴っての手動的作用を包含するいずれかの治療又は診断方法を意味する。
【0017】
“放射線療法”とは、高エネルギー放射線、例えばX−線、γ−線及び中性子(但し、それらだけには制限されない)への患者の照射を意味する。このタイプの治療は、外部放射線療法、内部放射線療法、移植物放射線、近接照射療法、全身性放射線療法及び放射線療法を包含するが、但しそれらだけには限定されない。
【0018】
“化学療法”とは、種々の方法、例えば静脈、経口、筋肉内、腹腔内、膀胱内、皮膚、経皮、頬内又は吸入によるか又は坐薬の形での癌患者への1又は2以上の抗癌剤及び/又は他の剤の投与を意味する。化学療法は、大きな腫瘍を縮小するために手術の前、その腫瘍を除去するために手術工程の前、身体におけるいずれかの残存する癌細胞の増殖を妨げるために手術又は放射線療法の後、与えられ得る。
【0019】
用語“有効量”又は“医薬的有効量”とは、所望する生物学的、治療及び/又は予防結果を提供するために、非毒性であるが、しかし十分な量の剤を言及する。この結果は、疾病の微候、症状又は原因の低減及び/又は軽減、又は生物学的システムのいずれか他の所望する変更であり得る。例えば、治療使用のための“有効量”とは、それ自体、本明細書に開示しているようなニトロベンズアミド代謝化合物、又は疾病において臨床学的に有意な低下をもたらすのに必要とされる本明細書におけるニトロベンズアミド代謝化合物を含んでなる組成物の量である。いずれか個々の場合、高められた有効量は、通常の実験を用いて当業者により決定され得る。
【0020】
“医薬的に許容し得る”又は“薬理学的に許容できる”とは、生物学的に又は他方では所望の材料を意味し、すなわち、前記材料は、いずれの所望しない生物学的効果も引起さないで、又は組成物に含まれるいずれかの成分とも、有害な態様で相互作用しないで、個人に投与され得る。
【0021】
用語“処理する”及びその文法的同義語は、本明細書で使用される場合、治療的有益性及び/又は予防的有益性を達成することを包含する。治療的有益性とは、処理される、基礎をなす障害の根絶又は改善を意味する。例えば疾患者においては、治療的有益性は、基礎をなす癌の根絶又は改善を包含する。また、治療的有益性は、患者が基礎をなす障害によりまだ苦しめられている事実にもかかわらず、患者に改善が観察されるよう、その基礎をなす障害に関連する1又は2以上の生理学的症状の根絶又は改善により達成される。予防的有益性に関しては、本発明の方法は、癌の進行の危険性での患者に、又は病状の診断が行われていなかったとしても、そのような病状の1又は2以上の生理学的症状を報告する患者に投与される本発明に組成物に基づいて実施され得る。
【0022】
本明細書で使用される場合、“BA”とは、4−ヨード−ニトロベンズアミドを意味し;“BNO”とは、4−ヨード−3−ニトロソベンズアミドを意味し;“BNHOH”とは、4−ヨード−3−ヒドロキシアミノベンズアミドを意味する。
【0023】
(i)ニトロベンズアミド代謝化合物:
本発明において有用な前駆体化合物は、下記式(Ia):
【化2】

[式中、R1、R2、R3、R4及びR5は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C7)シクロアルキル及びフェニルからなる群から独立して選択され、ここで5種のR1、R2、R3、R4及びR5置換基の少なくとも2つは常に水素であり、前記5種の置換基の少なくとも1つは常に、ニトロであり、ニトロに隣接して位置する少なくとも1つの置換基は常にヨードである]で表される化合物、及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグである。R1、R2、R3、R4及びR5はまた、ハロゲン化物、例えばクロロ、フルオロ、又はブロモ置換基でもあり得る。
【0024】
式Iaの好ましい前駆体化合物は、下記式の化合物である。
【化3】

【0025】
本発明において有用な代謝物は、下記式(IIa):
【化4】

[式中、(1)R1、R2、R3、R4及びR5置換基の少なくとも1つは常に硫黄含有置換基であり、残る置換基R1、R2、R3、R4及びR5は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、ブロモ、フルオロ、クロロ、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C7)シクロアルキル及びフェニルからなる群から独立して選択され、ここで5種のR1、R2、R3、R4及びR5置換基の少なくとも2つが常に水素であり;又は(2)R1、R2、R3、R4及びR5置換基の少なくとも1つは硫黄含有置換基ではなく、5種の置換基R1、R2、R3、R4及びR5の少なくとも1つは常にヨードであり、前記ヨードは、ニトロ、ニトロソ、ヒドロキシアミノ、ヒドロキシ又はアミノ基のいずれかであるR1、R2、R3、R4及びR5基に常に隣接している]で表される化合物、及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグである。幾つかの態様においては、(2)の化合物は、ヨード基が、ニトロソ、ヒドロキシアミン、ヒドロキシ又はアミノ基であるR1、R2、R3、R4及びR5基に常に隣接するようなものである。
【0026】
次の組成物は好ましい代謝化合物であり、個々は、下記化学式により表される。
【化5】

[前記式中、R6は、水素、アルキル(C1−C8)、アルコキシ(C1−C8)、イソキノリノン、インドール、チアゾール、オキサゾール、オキサジアゾール、チフェン又はフェニルからなる群から選択される]
【化6】

【0027】
【化7】

【0028】
いずれか1つの特定の機構に限定されないが、次のスキームは例えば、ニトロレダクターゼ又はグルタチオン接合機構を通してのMS292代謝を提供する。
【化8】

【0029】
BAグルタチオン接合及び代謝:
【化9】

【0030】
本発明は、他の乳癌、例えば乳腺における腺管癌、他の形の白血病、例えば末梢血液における急性前骨髄細胞性白血病、卵巣癌、肺癌、膀胱癌、前立腺癌、膵臓癌及び頸癌、並びに本明細書に記載される他の癌型の処理のためへの前述のニトロベンズアミド代謝化合物の使用を提供する。
【0031】
ニトロベンズアミド代謝化合物は悪性癌細胞に対して選択的細胞毒性を有するが、しかし非悪性癌細胞に対してはそうではないことが報告されている。Rice et at , Proc Natl Acad Sci USA 89-7703-7707 (1992)を参照のこと。1つの態様においては、本発明の方法に使用されるニトロベンズアミド代謝化合物は、非腫瘍細胞よりも腫瘍細胞に対してより選択的毒性を示すことができる。
【0032】
ニトロベンズアミド及びニトロソベンズアミド化合物の腫瘍形成性が、BSOが癌細胞に同時投与される場合、増強されることは報告されている。Mendeleyev et al , Biochemical Pharmacol 50(5) 705- 714 (1995)を参照のこと。ブチオニンスルホキシミン(BSO)は、化学療法に対する細胞耐性を一部、担当するγ−グルタミルシステインシンセターゼ、すなわちグルタチオンの生合成におけるキー酵素を阻害する。Chen et al , Chem Biol Interact Apr 24,111-112 263-75 (1998)を参照のこと。本発明はまた、BSOと組合せてのニトロベンズアミド代謝化合物及び/又はベンゾピロン化合物の投与を含んでなる、癌の治療方法も提供する。他方では、代謝化合物は、前駆体化合物及び/又はベンゾピロンと共に投与され得る。
【0033】
BSOの他に、γ−グルタミルシステインシンセターゼの他の阻害剤は、ニトロベンズアミド及び/又はベンゾピロン化合物と組合せて使用され得る。BSOの他の適切な類似体は、プロプロチオニンスルホキシミン、メチオニンスルホキシミン、エチオニンスルホキシミン、メチルブチオニンスルホキシミン、γ−グルタミル−α−アミノブチレート及びγ−グルタミルシステインを包含するが、但しそれらだけには限定されない。
【0034】
ベンゾピロン化合物:
幾つかの態様において、代謝化合物は、ベンズアミド化合物及び/又は式IIのベンゾピロンと組合せて投与される。式IIのベンゾピロン化合物は、下記式:
【化10】

[式中、R1、R2、R3及びR4は、H、ハロゲン、任意に置換されたヒドロキシ、任意に置換されたアミン、任意に置換された低級アルキル、任意に置換されたフェニル、任意に置換されたC1−C10へテロアリール、及び任意に置換されたC3−C8シクロアルキルからなる群から独立して選択される]で表される化合物、又はその塩、溶媒化合物、異性体、互変異体、代謝物又はプロドラッグである。
【0035】
好ましい態様においては、本発明は、下記式IIのベンゾピロン化合物に関する。
【化11】

【0036】
(ii)ニトロベンズアミド代謝化合物の機構:
作用の1つの機構により制限されるものではないが、本明細書に記載される化合物は、ポリ(ADP−リボース)ポリメラーゼ酵素の調整を通して抗癌性質を有すると思われる。薬物の作用機構は、核酵素ポリ(ADP−リボース)ポリメラーゼ(PARP−1)のためのリガンドとして作用するそれらの能力に関連している。Mendeleyevなど、前記(1995)を参照のこと。PARP−1は、核において発現され、ニコチンアミド及びポリ−ADP−リボース(PAR)へのβ−ニコチンアミドアデニンジヌクレオチド(NAD+)の転換を触媒する。恒常性条件下でのPARP−1の役割は、DNA転写及び修復に制限されると思われる。しかし、細胞ストレスがDNA損傷を引き起す場合、PARP−1活性は劇的に上昇し、これはゲノム結合性のために必要であると思われる。Shall et at., Mutat Res. Jun 30;460(l):l-15 (2000)を参照のこと。さらに、PARP−1は酵素のPARPフェミリーの最良の既知メンバーであるが、作用の機構はPARPファミリーのいずれかのメンバー(例えば、PARP−2〜PARP−18、又は作用の類似する機構により作用することが発見された追加のメンバー、又はPARP−1の共有する類似機構体)に同等に適用できる。
【0037】
PARP−1の1つの機構は、生ポリマーポリ(ADP−リボース)の合成である。ポリ(ADP−リボース)及びPARP−1の両者は、DNA修復、アポプトシス、ゲノム安定性の維持及び発癌の修復に連結されて来た。Masutani et al., Genes, Chromosomes, and Cancer 38:339-348 (2003)を参照のこと。PARP−1は、DNA修復、特に塩基除去修復(BER)において役割を演じる。BERは単一塩基DNA破壊のための哺乳類細胞における保護機構である。PARP−1は、高い親和性で、その亜鉛フィンガードメインを通してDNAフラグメントの端に結合し、それにより、DNA損傷センサーとして作用する。Gradwohl et al., Proc. Natl. Acad. Sci. USA 87:2990-2994を参照のこと。DNAにおける破壊は、破壊の部位へのPARP−1による結合応答を誘発する。次に、PARP−1は、その触媒活性を数百倍、高め(Gradwohl et al., Proc. Natl. Acad. Sci. USA 87:2990-2994 (1990); Murcia et al., Trends Biochem. Sci 19: 172-176 (1994)を参照のこと)、自然にポリADP−リボシル化(Simonin et al., J Biol. Chem. 278: 13454-13461 (1993))及びBERタンパク質、例えばDNA−依存性タンパク質キナーゼ(DNA−PKcs)及び分子骨格タンパク質XRCC−1を転換し始める。Ruscetti et al., J. Biol. Chem. Jun 5;273(23):14461- 14467 (1998)を参照のこと。BERタンパク質は、DNA損傷の部位に急速に補充される。El-Kaminsy et al., Nucleic Acid Res. 31(19):5526-5533 (2003); Okano et al., MoI Cell Biol. 23(11):3974-3981 (2003)を参照のこと。PARP−1は、DNA分解部位から解離するが、しかしDNA修復現象の付近に依存する。
【0038】
PARP分子の活性の阻害は、それらの分子の活性の低減を包含する。用語“阻害する”及びその分法的な語形変化、例えば“阻害の”とは、PARP活性の完全な低減を必要とするものではない。そのような低減は好ましくは、阻害効果の不在下で、例えば阻害剤、例えば本発明のニトロベンズアミド代謝化合物の不在下で、分子の活性の少なくとも約50%、少なくとも約75%、少なくとも約90%及びより好ましくは少なくとも95%である。最も好ましくは、この用語は、活性における観察できるか又は測定できる低減を言及する。処理シナリオにおいては、好ましくは、阻害は、処理される病状において治療及び/又は予防有益性を生成するのに十分である。用語“阻害しない”及びその文法的な語形変化は、活性に対する効果の完全な結合を必要としない。例えば、それは、阻害剤、例えば本発明のニトロベンズアミド代謝化合物の存在下で、PARP活性の約20%以下、約10%以下及び好ましくは約5%以下である情況を言及する。
【0039】
作用のもう1つの機構は、イノシン一リン酸デヒドロゲナーゼ(IMPDH)の阻害を包含する。IMPDHは、グアニレート、例えばGTP及びdGTPを供給する枝分かれプリンヌクレオチド合成路の律速酵素である。2種のIMPDHイソフォーム、すなわち全ての細胞に構成的に存在するタイプI、及び高増殖性細胞、例えば癌において誘発でき、存在するタイプIIが存在する。後者の酵素の阻害は、腫瘍細胞増殖及び複製のために必要である細胞内グアノシン分子の完全な消耗を引き起す。本発明の1又は2以上の代謝化合物は、IMPDHを標的化し、従って腫瘍細胞増殖を阻害し得る。
【0040】
作用のさらにもう1つの機構は、ヒストンデアシテラーゼ(HDAC)の阻害を包含する。転写因子プールにおける腫瘍関連の変更が、正常な増殖及び成長において重要な遺伝子の誤調節を導くことができる。キメラ性転写因子は、転写補リプレッサー及びそれらの関連するHDAC活性の異常補充により増殖調節標的遺伝子の転写抑制を引き起す。ヒト急性前骨髄細胞性白血病においては、レチノイン酸重要体を包含するキメラ性転写因子(PML−RARα及びPLZF−RARα)は、標的遺伝子、例えばRARβ遺伝子の転写を抑制すると思われている。転写補リプレッサー複合体は、HDAC活性を含み、転写補活性化因子複合体はヒストンアセチルトランスフェラーゼ活性を含む。HDAC阻害剤、例えばトリコスタチンA又はNaBuは、キメラ性転写因子PML−RARα及びPLZFRARαにより引起される転写抑制リプレッションを軽減し得る。HDAC阻害剤は単独で又はレチノイドと組合せて、明白な副作用を伴わないで、急性前骨髄細胞性白血病の動物も出るにおいて白血病緩解及び延長された生存性を誘発することが示されている。
【0041】
ヒストンのアセチル化及び脱アセチル化は、DNAとのヒストンの相互作用に影響を及ぼすことにより、高次クロマチン構造を変更する。転写因子はまたアセチル化され得、アセチル化されたそれらのタンパク質の状態は、DNAとのそれらの相互反応、及び他の転写補調節タンパク質と相互反応するそれらの能力に影響を及ぼすことができる。例えば、p53のアセチル化は、その配列特異的DNA結合活性を増強する。脱アセチル化されたヒストンは、細胞増殖に関連するが、ところが超アセチル化されたヒストンは細胞増殖阻止、分化及び/次にアポプトシスに関連している。
【0042】
例えば、Saitoなどは、MS−27−275、すなわちHDACを阻害する合成ベンゼン誘導体の効率を評価した。Saito et al. Proc Natl Acad Sci , 1999; 96: 4592-4597。多くの成熟腫瘍細胞系においては、MS−27−275は、μモル以下の範囲でのIC50を伴って腫瘍細胞増殖を阻害した。細胞増殖は、細胞周期阻止、及び細胞周期阻害剤p21の誘発を付随する。p.o.投与されたMS−27−275は、s.c.増殖されたヌードマウスにおける確立された完熟腫瘍系の増殖を最少の毒性を伴って阻害した。Jaboin et al Cancer Research, 2002, 62:6108-6115を参照のこと。
【0043】
HDAC阻害剤としての本発明の化合物は、転写活性を調節し得る。従って、本発明の化合物はまた、脈管形成及び細胞周期阻止し、アポプトシス及び分化を促進するよう作用し得る。腫瘍増殖のそれらのキー成分を標的化することにより、HDAC阻害剤は、高速移動細胞増殖抑制性市場において明確な位置を示す能力を有する。HDAC阻害剤がそのようなキー役割を演じる2つの主要理由は、それらが例えば存在する細胞増殖抑制物(例えば、レチノイド)の効率を改良するために他の処理レジメと当時に使用され得、さらに、それらが特定疾病を引き起す遺伝子の転写を標的化できることであり、それらは癌治療への前例のない治療窓を付与する。
【0044】
ベンズアミド代謝化合物の使用:
癌型:
【0045】
本発明は、幾つかの特定癌又は腫瘍を処理するための方法を提供する。例えば、癌型は、副腎皮層癌腫、肛門癌、再生不良性貧血、胆管癌、膀胱癌、骨癌、骨転移、成人CNS脳腫瘍、子供CNS脳腫瘍、乳癌、カースルマン疾患、子宮頚部腫瘍、幼児期非ホジキンリンパ腫、結腸及び直腸癌、子宮内膜癌、食道癌、Ewingファミリーの腫瘍、眼癌、胆嚢癌、胃腸の類癌腫、消化管間質腫瘍、妊娠期間絨毛性疾患、悪性リンパ腫、カポジ肉腫、腎癌、喉頭及び下咽頭癌、急性リンパ球性白血病、急性骨髄白血病、小児白血病、慢性リンパ球性白血病、慢性骨髄性白血病、肝臓癌、肺癌、肺カルチノイド腫瘍、非ホジキンリンパ腫、男性乳癌、悪性黒子症候群、多発性骨髄腫、骨髄形成異常症候群、鼻腔及び副鼻腔癌、上咽頭癌、神経芽、口腔及び中咽頭癌、骨肉腫、卵巣癌、膵臓癌、陰茎癌、脳下垂体腫瘍、前立腺癌、網膜胚種細胞腫、横紋筋肉腫、唾液腺癌、肉腫(成人軟組織癌腫)、黒色腫皮膚癌、非黒色腫皮膚癌、胃癌、精巣癌、胸腺癌腫、甲状腺癌、子宮肉腫、腟癌、外陰部癌及びワルデンストロームマクログロブリン血症を包含する。
【0046】
甲状腺癌は、内分泌系の最も通常の悪性疾患である。甲状腺癌は、分化された腫瘍(乳頭又は小胞)及び不十分に分化された腫瘍(骨髄又は退形成)を包含する。膣癌は、鱗状細胞癌、腺癌、メラノーマ及び肉腫を包含する。精巣癌は、セミノーマ及び非セミノーマ型に広く分けられる。
【0047】
胸腺腫は、非新生物リンパ細胞により集中的に浸潤され得るか又は浸潤され得ない、胸腺の上皮腫瘍である。用語、胸腺腫は、上皮成分の明確な異型性を示さない新生物を説明するために通常使用される。もはや胸腺に対して特異的ではない、明確な細胞学的異型性及び組織学的特徴を示す胸腺上皮腫瘍は、胸腺癌(また、Cタイプ胸腺腫としても知られている)として知られている。
【0048】
本発明により提供される方法は、他の治療剤と組合せてのベンズアミド代謝化合物の投与を含んでなる。本発明の組成物と共に同時投与され得る治療の選択は、処理される状態に一部、依存するであろう。例えば、急性骨髄性白血病の処理に関しては、本発明の幾つかの態様のベンズアミド化合物が、放射線治療法、モノクローナル抗体療法、化学療法、骨髄移植、遺伝子療法、免疫学的療法、又はそれらの組合せと組合せて使用され得る。
【0049】
乳癌:
1つの観点においては、本発明は、乳癌、好ましくは乳腺における管組織における管癌を治療するための方法を提供する。
【0050】
本発明により提供される方法により処理され得る幾つかのタイプの乳癌が存在する。本来の位置での小葉癌及び管癌は、それぞれ小葉及び管において進行するが、しかし乳房を取囲む脂肪組織又は身体の他の領域には拡散しない癌である。浸潤性(又は侵入性)小葉及び管癌は、それぞれ小葉及び管において進行し、乳房の脂肪組織又は身体の他の部分のいずれかに拡散する癌である。本発明により提供される方法による処理から有益である乳房の他の癌は、骨髄性癌、コロイド状癌、管状癌及び炎症性乳癌である。
【0051】
乳癌患者のために利用できる処理は、手術、免疫療法、放射線療法、化学療法、内分泌療法又はそれらの組合せである。腫瘍摘除及び乳房切除は、乳癌患者のために利用できる2種の可能性ある手術法である。
【0052】
化学療法は、癌細胞の患者における増加、侵入、転移及び患者の殺害を妨げるために高腫瘍剤を利用する。幾つかの薬物、例えば細胞毒性薬物、例えばドキソルビシン、シクロホスファミド、メトトレキセート、パクリタキセル、チオテパ、ミトキサントロン、ビンクリスチン又はそれらの組合せが、乳癌を治療するために利用できる。この療法のために投与される剤は、タモキシフェン、酢酸メガストロール、アミノグルテチミド、フルオキシメステロン、ロイプロリド、ゴセレリン及びプレドニソンを包含する。
【0053】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法又は内分泌療法の組合せにより、乳癌患者に有益な効果を提供し得る。
【0054】
幾つかの態様においては、本発明は、いわゆる“三重陰性”乳癌の治療を提供する。従来のバイオマーカーにより同定される幾つかのサブクラスの乳癌、例えばエストロゲン受容体(ER)及び/又はプロゲステロン受容体(PR)陽性腫瘍、HER2増幅された腫瘍及びER/PR/HER2−陰性腫瘍が存在する。それらの3種のサブタイプは、多重乳癌における遺伝子発現フロフィーリングにより再現的に同定されており、基礎−様サブタイプの発現プロフィール及び不十分な予後を示す。三重陰性乳癌は、ER/PR/HER2−陰性腫瘍により特徴付けられる。
【0055】
卵巣癌:
もう1つの観点においては、本発明は、卵巣癌、例えば上皮卵巣腫瘍の処理方法を提供する。好ましくは、本発明は、次のものから選択された卵巣癌の治療方法を提供する:卵巣における腺癌、及び腹腔中への卵巣から移動した腺癌。手術、免疫療法、化学療法、ホルモン療法、放射線療法又はそれらの組合せが、卵巣癌のために利用できる幾つかの可能性ある処理法である。幾つかの可能性ある手術法は、減量化(debulking)、及び一側性卵巣摘除及び/又は一側性又はニ側性卵巣摘除を包含する。
【0056】
使用され得る抗癌剤は、シクロホスファミド、エトポシド、アルドレタミン及びイホスファミドを包含する。薬物タモキシフェンによるホルモン療法は、卵巣腫瘍を縮小するために使用され得る。放射線療法は、外部放射線療法及び/又は近接照射療法であり得る。
【0057】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、内分泌療法又はそれらのの組合せにより、卵巣癌患者に有益な効果を提供し得る。
【0058】
頸癌:
もう1つの観点においては、本発明は、頸癌、好ましくは頸部上皮における腺癌の治療方法を提供する。この癌の2種の主要型が存在する:鱗状細胞癌及び腺癌。前者は、全ての頸癌の80〜90%を構成し、子宮膣部(膣に近い部分)及び子宮頸内膜(子宮に近い部分)が連結する部分で進行する。後者は子宮頸内膜の粘膜生成腺細胞において進行する。幾つかの頸癌は、それらの両者の特徴を有しそして腺鱗状癌又は混合された癌と呼ばれる。
【0059】
頸癌のために利用できる主要処理は、手術、免疫療法、放射線療法及び化学療法である。幾つかの可能性ある手術選択は、冷凍手術、子宮摘出、及び膣上部摘出である。頸癌患者のための放射線療法は、外部放射線療法又は近接照射療法を包含する。頸癌を治療するために化学療法の一部として投与され得る抗癌薬物は、シスプラチン、カルボプラチン、ヒドロキシウレア、イリノテカン、ブレオマイシン、ビンクリスチン、マイトマイシン、イホスファミド、フルオロウラシル、エトポシド、メトトレキセート及びそれらの組合わせを包含する。
【0060】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、又はそれらのの組合せにより、頸癌患者に有益な効果を提供し得る。
【0061】
前立腺癌:
1つの他の観点においては、本発明は、前立腺癌、好ましくは次のものから選択された前立腺癌を治療するための方法を提供する:腺癌、又は骨に転移した腺癌。前立腺癌は、尿道の最初の部分を取囲む、男性における前立腺器官において進行する。前立腺は、幾つかの細胞型を有するが、しかし腫瘍の99%は、精液の生成を担当する腺細胞において進行する。
【0062】
手術、免疫療法、放射線療法、凍結外科、ホルモン療法及び化学療法は、前立腺癌患者のために利用できる幾つかの処理である。前立腺癌を治療するための可能性ある手術は、基本的恥骨後前立腺切除、基本的会陰前立腺切除及び腹腔鏡による基本的前立腺切除を包含する。幾つかの放射線療法選択は、外部ビーム放線、例えば三次元等角放射性療法、強度変調放射線療法及び等角プロトンビーム放射線療法である。近接照射療法(種子移植又は組織間腔放射線療法)がまた、前立腺癌についての利用できる処理方法である。凍結外科は、局在化する前立腺癌細胞を処理するために使用されるもう1つの可能性ある方法である。
【0063】
アンドロゲン妨害療法又はアンドロゲン抑制療法とも呼ばれるホルモン療法が、前立腺癌を治療するために使用され得る。この療法の幾つかの方法、例えばアンドロゲンの90%が生成される睾丸摘除法が利用できる。もう1つの方法は、低いアンドロゲンレベルへの黄体形成ホルモン放出ホルモン(LHRH)類似体の投与である。入手できるLHRH類似体は、ロイプロリド、ゴセレリン、トリプトレリンを包含する。LHRHアンタゴニスト、例えばアバレリックス(abarelix)もまた投与され得る。
【0064】
身体におけるアンドロゲン活性を阻止する抗アンドロゲン剤による処理は、もう1つの入手できる療法である。そのような剤は、フルタミド、ビカルタミド及びニルタミドを包含する。この療法は典型的には、LHRH類似体投与又は睾丸摘除と組合わされ、これは組合されたアンドロゲン遮断(CAB)と呼ばれる。
【0065】
化学療法異は、前立腺腫瘍が前立腺外に広がり、ホルモン処理が効果的でない場合、適切である。抗癌薬剤、例えばドキソルビジン、エストラムスチン、エトポシド、ミトキサントロン、ビンブラスチン、パクリタキセル、ドセタクセル、カルボプラチン及びプレドニソンが、前立腺癌の増殖を遅め、症状を軽減し、生存の性質を改良するために、投与され得る。
【0066】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、ホルモン療法又はそれらの組合せにより、前立腺癌患者に有益な効果を提供し得る。
【0067】
膵臓癌:
もう1つの観点においては、本発明は、膵臓癌、好ましくは膵管組織における上皮(epitheloid)癌及び膵管における腺癌から選択された膵臓癌の治療方法を提供する。
【0068】
最も通常型の膵臓癌は、膵管の内層において発症する腺癌である。膵臓癌のために利用できる可能な処理は、手術、免疫療法、放射線療法及び化学療法である。可能性ある手術処理の選択は、遠位又は全膵臓切除及び膵十二指腸切除(ウィップル方法)を包含する。
【0069】
放射線療法、特に体外機械によって腫瘍に焦点を合わせられる外部ブーム放射線放線が膵臓癌患者のためのオプションである。もう1つのオプションは、手術の間に投与される手術内電子ビーム照射である。
【0070】
化学療法は、膵臓癌患者を処理するために使用され得る。適切な抗癌剤は、5−フルオロウラシル(5−FU)、マイトマイシン、イホスファミド、ドキソルビシン、スルレプトゾシン、クロロゾトシン及びそれらの組合せを包含する。
【0071】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、又は化学療法により、膵臓癌患者に有益な効果を提供し得る。
【0072】
膀胱癌:
もう1つの観点においては、本発明は、膀胱癌、好ましくは膀胱における移行細胞癌の治療方法を提供する。膀胱癌は、尿路上皮癌(移行細胞癌)、又は膀胱の内表面になる尿路上皮細胞における腫瘍である。膀胱癌の残る事例は、扁平上皮細胞癌、腺癌及び小細胞癌である。幾つかのサブタイプの尿路癌は、それらが非侵襲性か又は侵襲性のいずれかであるか、及びそれらが乳頭状であるか又は平らであるかどうかに依存して存在する。非侵襲性腫瘍は尿路上皮、すなわち膀胱の最も内部層に存在し、侵襲性腫瘍は尿路上皮から膀胱の主要筋肉壁のより深い層まで広がる。侵襲性乳頭状尿路上皮癌は、膀胱の空洞中心に分岐し、また、膀胱壁中に外側から増殖する細長いフィンガー様隆起物である。非侵襲性乳頭状尿路上皮腫瘍は、膀胱の中心部の方に増殖する。非侵襲性の平らな尿路上皮腫瘍(また、平らな上皮癌とも呼ばれる)は、膀胱の内部中空部分に最も隣接する細胞層に限定されるが、侵襲性の平らな尿路上皮癌は、膀胱のより深い層、特に筋肉層に侵入する。
【0073】
膀胱癌を治療するためには、手術、放射線療法、免疫療法、化学療法又はそれらの組合せが適用される。幾つかの可能性ある手術オプションは、経尿道切除、膀胱切除又は根治的膀胱切除である。膀胱癌についての放射線療法は、外部ビーム放射線及び近接照射療法を包含する。
【0074】
免疫療法は、膀胱癌患者を処理するために使用され得るもう1つの方法である。典型的には、これは膀胱内的に達成され、すなわちカテーテルにより膀胱中に直接的に処理剤が投与される。1つの方法は、結核種痘において時々使用される細菌カテーテルを通して膀胱に直接的に与えられる、Bacillus Calmete-Guerin(BCG)である。身体は、細菌に対する免疫応答を開始し、それにより、癌細胞を攻撃し、殺害する。
【0075】
免疫療法のもう1つの方法は、インターフェロン、すなわち免疫応答を調節する糖タンパク質の投与である。インターフェロンαはしばしば、膀胱癌を治療するために使用される。
【0076】
膀胱癌を治療するために化学療法において使用され得る抗癌剤は、チテパ、メトトレキセート、ビンブラスチン、ドキソルビシン、シクロホスファミド、パクリタキセル、カルボプラチン、シスプラチン、イホスファミド、ゲムシタビン又はそれらの組合せを包含する。
【0077】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、免疫療法、化学療法、又はそれらの組合せにより、膀胱癌患者に有益な効果を提供し得る。
【0078】
血液癌:
リンパ腫:
【0079】
B−細胞リンパ腫:
悪性(癌性)B−細胞リンパ腫により引起される非ホジキンリンパ腫は、多くのサブセット(アメリカにおいて約85%)の既知型リンパ腫を表す(他の2種のサブセットは、T−細胞リンパ腫、及び細胞型がナチュラルキラー細胞であるか又は未知であるリンパ腫である)。細胞は、細胞と、身体における外来性物質との相互作用との間の複雑なシグナル化工程に依存して、それらの生活環において多くの変化を受ける。種々のタイプのリンパ腫又は白血病が、B細胞生活環において生じることができる。
急性骨髄性白血病:
【0080】
もう1つの観点においては、本発明は、急性骨髄性白血病(AML)、好ましくは末梢血液における急性前骨髄細胞白血病の治療方法を提供する。AMLは骨髄において始まるが、しかし身体の他の部分、例えばリンパ節、肝臓、脾臓、中枢神経系、及び精巣へも広がる。それは、すばやく進行することを意味する急性であり、数ヶ月以内に処理されなければ、致命的である。AMLは、再生し、蓄積し続ける、未熟の骨髄細胞、通常顆粒球又は単球により特徴づけられる。
【0081】
AMLは、免疫療法、放射線療法、化学療法、骨髄又は末梢血液幹細胞移植、又はそれらの組合せにより処理され得る。放射線療法は、外部ビーム放射線を包含し、副作用を有する。AMLを処理するために化学療法に使用され得る抗癌剤は、シタラビン、アントラサイクリン、アントラセンジオン、イダルビシン、ダウノルビシン、イダルビシン、ミトキサントロン、チオグアニン、ビンクリスチン、プレドニソン、エトポシド、又はそれらの組合せを包含する。
【0082】
モノクローナル抗体療法は、AML患者を処理するために使用され得る。小分子又は放射性化学物質が、身体において白血病細胞を殺害する手段を提供するために投与の前、それらの抗体に結合され得る。AML細胞上のCD33を結合するモノクローナル抗体、すなわちゲムツズマブ・オゾガミシン(gemtuzumab ozogamicin)が、化学療法レジメの前、耐えることができないAML患者を処理するために使用され得る。
【0083】
骨髄又は末梢血液幹細胞移植が、AML患者を処理するために使用され得る。幾つかの可能性ある移植方法は、同種又は自己移植である。
【0084】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、又は移植療法より、白血病患者に有益な効果を提供し得る。
【0085】
本発明により提供される方法により処理され得る他のタイプの白血病、例えば急性リンパ性白血病、急性骨髄性白血病、慢性リンパ球性白血病、慢性骨髄性白血病、ヘアリー細胞白血病、骨髄形成異常及び骨髄増殖性疾患が存在するが、但しそれらだけには限定されない。
【0086】
肺癌:
もう1つの観点においては、本発明は肺癌を治療するための方法を提供する。最も通常のタイプの肺癌は、非小細胞肺癌(NSCLC)であり、肺癌の約80〜85%を占め、扁平上皮癌、腺癌及び大細胞末分化癌に分けられる。小細胞肺癌は、肺癌の15〜20%を占める。
【0087】
肺癌治療の選択肢としては、手術、免疫療法、放射線療法、化学療法、光力学療法、又はそれらの組合せが挙げられる。肺癌の治療のために幾つかの可能性ある手術オプションは、分節性又はくさび性切除、葉切除法又は一側肺全摘除である。放射線療法は、外部ビーム放射線療法及び近接照射療法であり得る。
【0088】
肺癌を治療するために化学療法に使用され得る幾つかの抗がん剤は、シスプラチン、カルボプラチン、パクリタキセル、ドセタクセル、ゲムシタビン、ピノレルビン、イリノテカン、エトポスデ、ビンブラスチン、ゲフィチニブ、イソスファミド、メトトレキセート、又はそれらの混合物を包含する。光力学療法(PDT)が、肺癌患者を処理するために使用され得る。
【0089】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、光力学療法、又はそれらの組合せにより、肺癌患者に有益な効果を提供し得る。
【0090】
皮膚癌:
もう1つの観点においては、本発明は、皮膚において開始する幾つかのタイプの癌が存在する。最も通常のタイプは、非メラノーマ性皮膚癌である基底細胞癌及び扁平上皮細胞癌である。光線性角化症は、時々、扁平上皮細胞癌に進行する皮膚状態である。非メラノーマは、近くの組織に侵入し、身体の他の部分に広がる。異なったタイプの処理、例えば手術、放射線療法、化学療法及び光力学療法は、非メラノーマ及びメラノーマ性皮膚癌及び光線性角化症を有する患者のために利用できる。皮膚癌の治療のための幾つかの可能性である手術オプションは、Mohs顕微鏡検査手術(MMS)、単純な切除、電気乾燥及び掻爬、凍結外科、レーザー手術である。放射線療法は、外部ビーム放射線療法又は近接照射療法であり得る。臨床試験において試験される他のタイプの処理は、生物学的療法又は免疫療法、化学免疫療法、フルオロウラシルによる局部化学療法及び光力学療法である。
【0091】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、光力学療法、又はそれらの組合せにより、皮膚癌患者に有益な効果を提供し得る。
【0092】
眼の癌、網膜芽腫:
もう1つの観点においては、本発明は、網膜芽腫を処理するための方法を提供する。網膜芽腫は、網膜の悪性腫瘍である。網膜芽腫はいずれの年齢でも発症するが、それはしばしば、より若い子供、通常5歳前に発症する。腫瘍は、片眼においてのみ、又は両眼において存在し得る。網膜芽腫は通常、眼に制限され、身体の近くの組織又は他の部分には広がらない。患者を治癒し、ビジョンを保持するための処理オプションは、脱核(眼を除去する手術)、放射線療法、凍結外科、光凝固、免疫療法、熱療法及び化学療法を包含する。放射線療法は、外部ビーム放射線療法又は近接照射線療法であり得る。
【0093】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、凍結外科、光凝固、熱療法、及び熱療法、又はそれらの組合せにより、眼の網膜芽腫患者に有益な効果を提供し得る。
【0094】
眼癌、眼球内メラノーマ:
もう1つの観点においては、本発明は、眼球内メラノーマの処理方法を提供する。まれな癌である眼球内メラノーマは、癌細胞がブドウ膜と呼ばれる眼の部分に見出される疾病である。眼球内メラノーマは、中年の人々において最もしばしば発症する。眼球内メラノーマについての処理は、手術、免疫療法、放射線療法及びレーザー療法を包含する。手術は、眼球内メラノーマの最も通常の処理である。幾つかの可能性ある手術オプションは、虹彩切除、虹彩柵状組織切除、虹彩毛様体切除、脈絡膜切除、脱核及び眼窩内容除去である。放射線療法は、外部ビーム放射線療法又は近接照射療法であり得る。レーザー療法は、腫瘍を破壊するための強力な光のビーム、熱療法又は光凝集法であり得る。
【0095】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法及びレーザー療法、又はそれらの組合せにより、眼球内メラノーマ患者に有益な効果を提供し得る。
【0096】
子宮内膜癌:
もう1つの観点においては、本発明は子宮膜癌を治療するための方法を提供する。子宮内膜癌は、子宮内膜、すなわち子宮内膜において開始する癌である。子宮及び子宮内膜の癌の幾つかの例は、次のものを包含するが、但しそれらだけには限定されない:腺癌、腺類癌、腺扁平細胞癌、乳頭状漿液性腺癌、明細胞線癌、子宮内肉腫、間質性肉腫、悪性混合ミュラー腫瘍及び平滑筋肉腫。
【0097】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、遺伝子療法、光力学的療法、抗脈管形成療法、及び免疫療法、又はそれらの組合せにより、子宮内膜癌患者に有益な効果を提供し得る。
【0098】
肝臓癌:
もう1つの観点においては、本発明は、原発性肝癌(肝臓において開始する癌)の処理方法を提供する。原発性肝癌は、成人及び子供の両者において発症する。異なったタイプの処理が、原発性肝癌を有する個人のために利用できる。それらは、手術、免疫療法、放射線療法、化学療法及び経皮エタノール注入を包含する。使用され得るこのタイプの手術は、凍結外科、部分肝切除、全肝切除及び高周波アブレーションである。放射線療法は、外部ビーム放射線療法、近接照射療法、放射線増感剤又は放射性ラベルされた抗体であり得る。他のタイプの処理は、温熱療法及び免疫療法を包含する。
【0099】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、経皮エタノール注入、温熱療法及び免疫療法、又はそれらの組合せにより、肝臓癌患者に有益な効果を提供し得る。
【0100】
腎臓癌:
もう1つの観点においては、本発明は、腎臓癌の治療方法を提供する。腎臓癌(または、腎細胞癌又は腎臓腺癌とも呼ばれる)は、悪性細胞が腎臓における細管の内層に見出される疾病である。腎臓癌は、手術、放射線療法、化学療法及び免疫療法により処理され得る。腎臓癌を治療するための幾つかの可能性ある手術オプションは、部分腎摘出、単純腎切除、及び根治的腎摘出である。放射線療法は、外部ビーム放射線療法又は近接照射法であり得る。幹細胞移植が、腎臓癌を治療するために使用され得る。
【0101】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、免疫療法、及び幹細胞移植、又はそれらの組合せにより、腎臓癌患者に有益な効果を提供し得る。
【0102】
甲状腺癌:
もう1つの観点においては、本発明は甲状腺癌の治療方法を提供する。甲状腺癌は、癌(悪性)細胞が甲状腺の組織に見出される疾病である。次の4種の主要型の甲状腺癌が存在する:乳頭状性、小胞性、髄質性及び退形性。甲状腺癌は、手術、免疫療法、放射線療法、ホルモン療法及び化学療法により処理され得る。手術は、甲状腺癌の最も通常の処理である。甲状腺癌の治療のための幾つかの可能性ある手術オプションは、葉切除、甲状腺のほぼ全摘、甲状腺全切除及びリンパ節切除である。放射線療法は、外部放射線療法であり得、又は放射性ヨウ素を含む液体の摂取を必要とする。ホルモン療法は、癌細胞の増殖を停止するために使用する。甲状腺癌の治療においては、ホルモンは、癌細胞を増殖する他のホルモンの身体における製造を停止するために使用され得る。
【0103】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、ホルモン療法、及び化学療法、又はそれらの組合せにより、甲状腺癌患者に有益な効果を提供し得る。
【0104】
AIDS関連癌:
AIDS関連のリンパ腫:
もう1つの観点においては、本発明はAIDS関連のリンパ腫の処理方法を提供する。AIDS関連のリンパ腫は、後天性免疫欠損症候群(AIDS)を有する患者のリンパ系において悪性細胞が形成する疾病である。次に、免疫系は、身体に侵入する感染及び疾病を攻撃することができない。HIV疾病を有する人々は、感染、リンパ腫及び他のタイプの癌を進行する高められた危険性を有する。リンパ腫は、リンパ系の白血球に影響を及ぼす癌である。リンパ腫は次の2種の一般的タイプに分けられる:ホジギンリンパ腫及び非ホジギンリンパ腫。ホジキンリンパ腫及び非ホジキンリンパ腫の両者はAIDS患者において発症するが、しかし非ホジキンリンパ腫がより一般的である。AIDSを有する個人が非ホジキンリンパ腫を有する場合、それはAIDS関連リンパ腫と呼ばれる。非ホジキンリンパ腫は、無活性(遅い増殖)又は攻撃的(早い増殖)であり得る。AIDS関連リンパ腫は通常、攻撃的である。3種の主要タイプのAIDS関連リンパ腫が拡散する:大B細胞リンパ腫、B細胞免疫芽球リンパ腫及び小非分裂細胞リンパ腫。
【0105】
AIDS関連のリンパ腫の処理は、リンパ腫の処理と、AIDSについての処理とを兼ねる。AIDSを有する患者は弱体化された免疫系を有し、処理はさらなる損傷を引き起すことができる。この理由のために、AIDS関連のリンパ腫を有する患者は通常、AIDSを有さないリンパ腫患者よりも低い用量の薬物により処理される。高い活性の抗レトロウィルス療法(HAART)は、HIVの進行を遅めるために使用される。重症である感染を予防し、処理するための薬剤がまた使用される。AIDS関連リンパ腫は、化学療法、免疫療法、放射線療法及び幹細胞移植による高用量化学療法により処理され得る。放射線療法は、外部ビーム放射線療法又は近接照射療法による。AIDS関連のリンパ腫は、モノクローナル抗体療法により処理され得る。
【0106】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、化学療法、放射線療法及び高−用量化学療法、又はそれらの組合せにより、AIDS関連リンパ腫患者に有益な効果を提供し得る。
【0107】
カポジ肉腫:
もう1つの観点においては、本発明はカポジ肉腫の処理方法を提供する。カポジ肉腫は、癌細胞が口、鼻及び肛門の内表面になる、皮膚又は粘膜下の組織において見出される疾病である。従来のカポジ肉腫は通常、イスラエル人、イタリア人又は地中海先祖の男性老人において発症する。このタイプのカポジ肉腫は、ゆっくり、時々10〜15年にわたって進行する。カポジ肉腫は、免疫抑制剤を摂取している人々において発症する。後天性免疫欠損症候群(AIDS)を有する患者におけるカポジ肉腫は、伝染性カポジ肉腫と呼ばれる。AIDSを有する人々におけるカポジ肉腫は通常、他の種類のカポジ肉腫よりもすばやく広がり、しばしば、身体の多くの部分に見出される。カポジ肉腫は、手術、化学療法、放射線療法及び免疫療法により処理され得る。外部放射線療法は、カポジ肉腫の通常の処理である。カポジ肉腫を処理するための幾つかの可能性ある手術オプションは、局部切除、電気乾燥及び掻爬、及び寒冷療法である。
【0108】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、化学療法、放射線療法及び免疫療法、又はそれらの組合せにより、カポジ肉腫患者に有益な効果を提供し得る。
【0109】
ウィルス誘発された癌:
もう1つの観点においては、本発明はウィルス誘発された癌の治療方法を提供する。幾つかの通常のウィルスが、特定悪性腫の病因学において明らかな、又は問題のある原因要素である。それらのウィルスは通常、潜伏期を確立し、又は数種は感染耐性になる。腫瘍形成はたぶん、感染された宿主において増強されたレベルのウィルス活性化に連結され、重度のウィルス用量又は易感染性免疫制御に影響を及ぼす。主要ウィルス悪性腫系は、B型肝炎ウィルス(HBV)、C型肝炎ウィルス(HCV)及び原発性肝細胞癌;ヒト向リンパ性ウィルス型1(HTLV−1)及び成人T−細胞白血病/リンパ腫;及びヒト乳頭腫ウィルス(HPV)及び頸癌を包含する。一般的にそれらの悪性腫は比較的、生命の初期において発症し、典型的には中年期か又はそれよりも早くピークに達する。
【0110】
ウィルス誘発された肝細胞癌:
HBV及びHCVの両者と肝細胞癌との間の因果関係は、実質的な流行学的出来事を通して確立される。両者は、細胞死及び続く再生を引き起すことにより、肝臓において慢性的再現を通して作用するように思える。異なったタイプの処理が、肝臓癌を有する患者のために利用できる。それらは、手術、免疫療法、放射線療法、化学療法及び経皮エタノール注入を包含する。使用され得る手術のタイプは、凍結外科、部分肝切除、全肝切除及び高周波アブレーションである。放射線療法は、外部ビーム放射線療法、近接照射療法、放射線増感剤又は放射性ラベルされた抗体であり得る。他のタイプの処理は、温熱療法及び免疫療法を包含する。
【0111】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び手術、放射線療法、化学療法、経皮エタノール注入、温熱療法及び免疫療法、又はそれらの組合せにより、ウィルス誘発された肝細胞癌患者に有益な効果を提供し得る。
【0112】
ウィルス誘発された成人T細胞白血病/リンパ腫:
レンチウィルス(例えば、HTLV−1)と成人T細胞白血病(ATL)との間の関係は確立されている。世界中に見出される他の腫瘍形成ウィルスとは異なって、HTLV−1は高く地理的に制限され、主として南日本、カリブ海、西及び中央アフリカ、及び南太平洋諸島において見出される。因果関係の証拠は、キャリヤーにおけるATLのほとんど全ての場合、ウィルスゲノムのモノクローナル統合を包含する。HTLV−1関連の悪性腫についての危険因子は、周産期感染、高ウィルス量及び雄性生殖であるように思える。
成人T細胞白血病は、血液及び骨髄の癌である。成人T細胞白血病/リンパ腫についての標準処理は、放射線療法、免疫療法及び化学療法である。放射線療法は、外部ビーム放射線療法又は近接照射療法であり得る。成人T細胞白血病/リンパ腫を処理するための他の方法は、免疫療法、及び幹細胞移植による高用量化学療法を包含する。
【0113】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、免疫療法、及び幹細胞移植による高用量化学療法、又はそれらの組合せにより、成人T細胞白血病患者に有益な効果を提供し得る。
【0114】
ウィルス−誘発された頸癌:
ヒト乳頭腫ウィルス(HPV)による頸部の感染は、頸癌の最も共通した原因である。しかし、HPV感染を有する全ての女性が必ずしも頸癌を進行しないであろう。頸癌は通常、時間にわたってゆっくり進行する。癌が頸部に出現する前、頸部の細胞は、正常ではない細胞が頸部組織に出現し始める、形成異常として知られている変化を受ける。後に、癌細胞は増殖し、頸部中に及び周囲領域に、より深く広がり始める。頸部癌のための標準処理は、手術、免疫療法、放射線療法及び化学療法である。使用され得る手術のタイプは、円錐切除、子宮全摘出、双方の卵管卵巣摘出、広汎性子宮全摘出、骨髄内容除去、凍結外科、レーザー手術及びループ電子切除方法である。放射線療法は、外部ビーム放射線療法又は近接照射療法である。
【0115】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、成人頸癌患者に有益な効果を提供し得る。
【0116】
CNS癌:
脳及び脊髄腫瘍は、中枢神経系(CNS)の主成分である、頭蓋骨又は脊椎骨の内部に見出される組織の異常増殖である。良性腫瘍は、非癌性であり、悪性腫瘍は癌性である。CNSは堅い骨の四分体(すなわち、頭蓋骨及び脊椎骨)に収容され、その結果、良性であろうと又は悪性であろうと、いずれの異常増殖でも感受性組織に対して圧力を付与し、機能を損なう。脳又は脊髄において起因する腫瘍は一次腫瘍と呼ばれる。ほとんどの一次腫瘍は、ニューロンを取囲み、支持する細胞間の制御不能により引起される。少数の個人においては、一次腫瘍は、特定の遺伝的疾患(例えば、神経線維腫症、結節性硬化症)、又は放射線又は癌を引き起す化学物質に起因する。ほとんどの一次腫瘍の原因は、未知のままである。
【0117】
脳及び脊髄腫瘍を診断するための最初の試験は、神経学的試験である。特定のイメージング技法(断層エックス線撮影及び磁気共鳴イメージングが、ポジトロン放射断層撮影に比較して)がまた使用される。実験試験はEEG及び腰椎穿刺を包含する。生検、すなわち組織のサンプルが懸濁された腫瘍から取られる手術法は、医師による腫瘍のタイプの診断を助ける。
【0118】
腫瘍は、その巣葉ガ起因すると思われる細胞の種類に従って分類される。成人における最も共通する脳腫瘍は、血液−脳バリヤーを構成し、中枢神経系の栄養に寄与する星状細胞と呼ばれる脳における細胞に由来する。それらの腫瘍神経膠腫(星状細胞腫、退形成星細胞腫又は多形膠芽腫)と呼ばれ、全ての一次中枢神経系腫瘍の65%を占める。腫瘍の幾つかは、乏突起細胞腫、脳室上皮腫、髄膜腫、リンパ腫、神経鞘腫及び髄芽腫であるが、但しそれらだけには限定されない。
【0119】
CNSの感覚上皮腫瘍:
星状細胞腫瘍、例えば星状細胞腫;末分化(悪性)星状細胞腫、例えば半球状、間脳性、視覚性、脳幹性、小脳性;多形膠芽腫;毛様細胞性星状細胞腫、例えば半球状、間脳性、視覚性、脳幹性、小脳性;上衣下巨細胞神経膠星状細胞腫;及び多形性黄色星状膠細胞腫。稀突起膠細胞腫瘍、例えば稀突起膠腫;及び末分化(悪性)乏突起細胞腫。脳室上衣細胞腫瘍、例えば脳室上皮腫;末分化脳室上皮腫;粘液乳頭脳室上皮腫;及び上衣下細胞腫。混合された神経膠腫、例えば混合された稀星状細胞腫;末分化(悪性)稀星状細胞腫;及び他のもの(例えば、上衣−星状細胞腫)。確信できない起源の感覚上皮腫瘍、例えば極性海綿細胞腫;星状芽細胞腫;及び大脳神経膠腫症。脈絡膜叢の腫瘍、例えば脈絡膜叢乳頭腫;及び脈絡膜叢癌(末分化脈絡膜叢乳頭腫)。ニューロン性及び混合されたニューロン−膠腫瘍、例えば節神経腫;小脳の形成異常性節神経腫(Lhermitte-Duclos);神経節膠腫;末分化(悪性)神経節膠腫;癒着性乳児神経節膠腫、例えば癒着性乳児星状細胞腫;中枢神経細胞腫;胎生期発育不全性神経上皮腫瘍;嗅神経芽細胞腫(鼻腔神経芽細胞)。松果実質腫瘍、例えばピネオサイトーマ;松果体芽腫;及び混合されたピネオサイトーマ/松果体芽腫。神経芽細胞又はグリア芽細胞要素を有する腫瘍(胚芽腫)、例えば髄様上皮腫;多分化能分化を有する末分化神経外胚芽性腫瘍、例えば髄芽腫;脳末分化神経外胚芽性腫瘍;神経芽細胞腫;網膜胚種細胞腫;及び上衣芽腫。
【0120】
他のCNS腫瘍:
Sellar領域の腫瘍、例えば脳下垂体腺腫;下垂体癌;及び頭蓋咽頭腫。造血性腫瘍、例えば原発性悪性リンパ腫;プラズマ細胞腫;及び顆粒球性肉腫。胚細胞腫、例えば胚芽腫;胎生期癌;卵黄嚢腫瘍(内皮性静脈洞炎腫瘍);絨毛膜癌;奇形腫;及び混合された胚細胞腫。膜の腫瘍、例えば髄膜腫;非定型的髄膜腫;及び末分化(悪性)髄膜腫。膜の非髄膜細胞層腫瘍、例えば良性間葉;悪性間葉;一次メラニン細胞病巣;造血腫瘍;及び不確定組織形成、例えば血管芽細胞腫(毛細管血管芽細胞腫)。頭側及び背骨神経の腫瘍、例えば(神経鞘腫);神経繊維腫;悪性末梢神経鞘腫(悪性神経鞘腫)、例えば類上皮、分岐間葉又は上皮性分化、及びメラニン性。局所腫瘍からの局部拡張;例えば傍神経節腫(頸静脈小体腫瘍);背索腫;軟骨肉腫;及び癌。転移性腫瘍、末分類腫瘍及び包嚢、及び腫瘍様病巣、例えばラケト嚢腫;類表皮;類皮腫;第三脳室のコロイド状包嚢;腸性嚢胞;神経膠嚢胞;顆粒細胞腫(迷芽腫、下垂体細胞腫);視床下部ニューロン性過誤腫;鼻神経膠異所性;及びプラズマ細胞肉腫。
【0121】
利用できる化学療法剤は、次のものであるが、但しそれらだけには限定されない:アルキル化剤、例えばシクロホスファミド、イホスファミド、メルファラン、クロラムブシル、CCNU、デカルバジン、プロカルバジン、ブスルファン及びチオデパ;代謝拮抗剤、例えばメトトレキサート、5−フルオロウラシル、シタラビン、ゲムシタビン(Gemzar(登録商標))、6−メルカプトプリン、6−チオグラニン、フルダラビン及びクラドリビン;アントラサイクリン、例えばダウノルビシン、ドキソルビシン、イダルビシン、エビルビシン及びミトキサントロン;抗生物質、例えばブレオマイシン;カンブトテンシン類、例えばイリノテカン及びトポテカン;タキサン類、例えばパクリタキセル及びドセタクセル;及びプラチナ類、例えばシスプラチン、カルボプラチン及びオキサリプラチン。
【0122】
処理法は手術、放射線療法、免疫療法、高体温、遺伝子療法、化学療法、及びそれらの組合せである。医者はまた、CNS内部の膨張を低めるためにステロイドを処方できる。
【0123】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、成人頸癌患者に有益な効果を提供し得る。
【0124】
PNS癌:
末梢神経系は、脳及び脊髄から枝分かれする神経からなる。それらの神経は、CNSと身体部分との間で連結網を形成する。末梢神経系はさらに、体性神経系及び付随神経系に細分される。体性神経系は、皮膚及び筋肉に進行する神経から成り、意識活性に関与される。不随神経系は、内臓、例えば心臓、胃及び腸にCNSを連結する神経からなる。それは無意識の活性を仲介する。
【0125】
聴神経腫は、8番目の脳神経又は内耳神経とも呼ばれる、平衡神経から生じる良性線維性増殖である。それらの腫瘍は、非悪性であり、すなわち、それらは身体の他の部分に拡散も又は転移もしないことを意味する。それらの腫瘍の局在化は、脳幹における生体脳に隣接して、頭蓋骨内深部である。腫瘍が拡大するにつれて、それらは、生体機能と関係する構造体を取囲む。大部分の場合、それらの腫瘍は数年間にわたってゆっくり増殖する。
【0126】
悪性末梢神経鞘腫瘍(MPNST)は、良性柔組織腫瘍、例えば神経繊維腫及び神経鞘腫に対する悪性対抗物である。それは最も通常には、深部の柔組織において、通常、神経幹に密接して存在する。最も通常の部位は、坐骨神経、腕神経叢及び仙骨神経叢を包含する。それは、成人において三叉神経核の知覚ブランチから通常生じる、まれで、攻撃的で、且つ致死性の眼窩腫瘍である。悪性PNS腫瘍は、脳を包含するよう神経に沿って拡張し、ほとんどの患者が臨床学的診断の5年以内に死亡する。MPNSTは、類上皮、間葉又腺特徴により3種の主要カテゴリーに分類され得る。MPNSTのいつかは、次のものを包含するが、但しそれらだけに限定されない:軟骨質分化を有する皮下悪性類上皮神経鞘腫、腺悪性神経鞘腫、神経周膜を有する悪性末梢神経鞘腫、杆状機能を有する皮膚類上皮悪性骨髄鞘腫、皮相類上皮MPNST、トリトン腫瘍(横紋筋芽細胞分化を有するMPNST)、横紋筋芽細胞分化を有する神経鞘腫。稀なMPNSTは、複数の肉腫性組織型、特に骨肉腫、軟骨肉腫及び血管肉腫を含む。それらは時々、柔組織の悪性間葉組織腫瘍とは区別できない。
【0127】
他のタイプのPNS癌は、悪性線維性細胞腫、悪性線維性組織球腫、悪性髄膜腫、悪性黒子症候群、及び悪性の混合されたMullerian腫瘍を包含するが、但しそれらだけには限定されない。
【0128】
その処理は、手術、放射線療法、免疫療法、化学療法、及び放射線療法及び化学療法の組合せである。
【0129】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、PNS癌に有益な効果を提供し得る。
【0130】
口腔及び中咽頭癌:
中枢神経(CNS)癌を有する患者の管理は、困難な課題として残っている。癌、例えば下咽頭癌、喉頭癌、上咽頭癌、中因頭癌及び同様のものは、手術、免疫療法、化学療法、化学療法及び放射線療法の組合せにより処理されて来た。エトポシド及びアクチノマイシンD(トポイソメラーゼIIを阻害する、2種の通常使用される腫瘍学的剤)は、有用な量で血液−脳バリヤーを交差できない。
【0131】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、口腔及び中咽頭癌に有益な効果を提供し得る。
【0132】
胃癌:
胃癌は、胃の内層における細胞変化の結果である。次の3種の主要型の胃癌が存在する:リンパ腫、胃の間質腫瘍及び類癌腫。リンパ腫は、時々胃の壁に見出される免疫組織の癌である。胃の間質腫瘍は、胃壁の組織から進行する。類癌腫は胃のホルモン生成細胞の腫瘍である。
【0133】
胃癌の原因は、議論され続けている。遺伝及び環境(食餌、喫煙、等)の組合せが全て、一部原因であるように思える。処理への共通するアプローチは、手術、免疫療法、化学療法、放射線療法、化学療法及び放射線療法の組み合わせ、又は生物学的療法を包含する。
【0134】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、胃癌に有益な効果を提供し得る。
【0135】
精巣癌:
精巣癌は、典型的には、若い男性における1つの又は両睾丸において進行する癌である。睾丸の癌は、生殖細胞として知られている一定の細胞において進行する。男性において発症する2種の主要型の生殖細胞腫瘍(GCT)は、セミノーマ(60%)及び非セミノーマ(40%)である。腫瘍はまた、睾丸の支持及びホルモン生成組織又は間質において発症する。そのような腫瘍は、生殖腺間質腫としても知られている。2種の主要タイプの癌は、Leydig細胞腫瘍及びセルトリ細胞腫である。二次睾丸腫瘍は、他の器官において開始し、次に、睾丸に広がる腫瘍である。リンパ腫は、最も共通する二次精巣癌である。
【0136】
処理のためへの共通するアプローチは、手術、免疫療法、化学療法、放射線療法、化学療法及び放射線療法の組合せ、又は生物学的療法を包含する。次の幾つかの薬物が典型的には、精巣癌を治療するために使用される:プラチノール(シスプラチン)、Vepesid又はVP−16(エトポシド)及びブレノキサン(硫酸ブレオマイシン)。さらに、Ifex(イフォサミド)、Velban(硫酸ビンブラスチン)及び他のものが使用され得る。
【0137】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、精巣癌に有益な効果を提供し得る。
【0138】
胸腺癌:
胸腺は、喉の基部から心臓の前部に延長する、胸の上部/前部に位置する小器官である。胸腺は次の2種の主要型細胞を含む:胸腺上皮細胞及びリンパ球。胸腺上皮細胞に、胸腺腫及び胸腺癌は起因する。リンパ球は、胸腺においても又はリンパ節においても、悪性になり、ホジギン病及び非ホジキンリンパ腫と呼ばれる癌に進行する。胸腺はまた、通常一定のホルモンを放出する、Kulchitsky細胞又は神経内分泌細胞と呼ばれる、もう1つの低い共通型の細胞を含む。それらの細胞は、しばしば同じ型のホルモンを放出し、身体の他の部分における神経分泌細胞から発生する他の腫瘍に類似する、カルチノイド又はカルチノイド腫瘍と呼ばれる癌を生ぜしめることができる。
【0139】
処理への共通するアプローチは、手術、免疫療法、化学療法、放射線療法、化学療法及び放射線療法の組合せ、又は生物学的療法を包含する。胸腺腫及び胸腺癌の治療に使用されて来た抗癌薬物は、ドキソルビシン(アドリアマイシン)、シスプラチン、イホスファミド及びコルチコイド(プレドニゾン)である。しばしば、それらの薬物は、それらの有効性を高めるために、組合せて与えられる。胸腺癌を治療するために使用される組合せは、シスプラチン、ドキソルビシン、エトポシド及びシクロホスファミド、及びシスプラチン、ドキソルビシン、シクロホスファミド及びビンクリスチンの組合せを包含する。
【0140】
本発明により提供される方法は、ニトロベンズアミド代謝化合物の投与、又はニトロベンズ代謝化合物の投与及び放射線療法、化学療法、又はそれらの組合せにより、胸腺癌に有益な効果を提供し得る。
【0141】
併用療法:
本発明の1つの観点は、処理管理の異なった組み合わせを用いての癌の治療方法を提供する。例えば、そのような組合せは、1又は2以上の種々の抗腫瘍化学療法剤、化学予防薬及び/又は副作用制限剤と共に1又は2以上のニトロベンズアミド化合物の使用を包含するが、但しそれらだけには限定されない。
【0142】
抗腫瘍化学療法剤:
本発明に使用される適切な抗腫瘍化学療法剤は、次のものを包含するが、但しそれらだけには限定されない:アルキル化剤、代謝拮抗剤、天然の抗腫瘍剤、ホルモン性抗癌剤、脈管形成阻害剤、分化試薬、RNA阻害剤、DNA阻害剤、ウィルス複製の阻害剤、抗体又は免疫療法剤、ペプチド剤、遺伝子療法剤、小分子酵素阻害剤、生物学的応答変性剤、及び抗−転移剤。
【0143】
アルキル化剤:
アルキル化剤は、高分子、例えば癌細胞のDNAのアルキル化を通して作用することが知られており、通常、強い求電子体である。この活性は、DNA合成及び細胞分裂を破壊し得る。本明細書への使用のために適切なアルキル化剤の例は、ナイトロジェンマスタード及びそれらの類似体及び誘導体、例えばシクロホスファミド、イホスファミド、クロラムブシル、エストラムスチン、メクロエタミン塩酸塩、メルファラン及びウラシルマスタードを包含する。アルキル化剤の他の例は、スルホン酸アルキル(例えば、ブスルファン)、ニトロソ尿素(例えば、カルムスチン、ロムスチン及びストレプトゾシン)、トリアゼン(例えば、ダカルバジン及びテモゾロミド)、エチレンイミン/メチルメラミン(例えば、アルトレタミン及びチオテパ)、及びメチルヒドラジン誘導体(例えば、プロカルバジン)を包含する。カルボプラチン、シスプラチン及びオキサリプラチンを含んでなるアルキル化様プラチナ含有薬物が、アルキル化剤グループに包含される。
【0144】
抗代謝物:
抗代謝抗癌剤は天然の代謝物に構造的に類似し、癌細胞の通常の代謝工程、例えば核酸及びタンパク質の合成に包含される。それらは天然の代謝物とは十分に異なり、その結果、それらは癌細胞の代謝工程を妨げる。本発明に使用されるべき適切な抗代謝抗癌剤は、それらが影響を及ぼす代謝工程に従って分類され得、葉酸の類似体及び誘導体、ピリミジン、プリン及びシチジンを包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な剤の葉酸グループのメンバーは、メトトレキセート(アメトプテリン)、ペメトレキシド及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なピリミジン剤は、シタラビン、フロキシウリジン、フルオロウラシル(5−フルオロウラシル)、カペシタビン、ゲムシタビン、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なプリン剤は、メルカプトプリン(6−メルカプトプリン)、ペントスタチン、チオグラニン、クラドリビン、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なシチジン剤は、シタラビン(シトシンアラビノドシド)、アザシチジン(5−アザシチジン)、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0145】
天然の抗癌剤:
天然の抗癌剤は、抗分裂剤、抗生物質抗癌剤、カンプトテシン類似体及び酵素を含んでなる。本明細書への使用のために適切な抗分裂剤は、ビンカアルカロイド、例えばビンプラスチン、ビンクリスチン、ビンデシン、ビノレルビン、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。それらは、ニチニチソウ植物から誘導され、通常、癌細胞の微小管におけるチューブリンに結合する、M期に対して細胞周期特異的である。本明細書における使用のために適切な他の抗分裂剤は、ポドフィロトキシンであり、これはエトポシド、テニポシド、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。それらの試薬は、細胞周期のG2及びS期を優先的に標的化する。
【0146】
抗生物質抗癌剤がまた、天然の抗癌剤に包含される。抗生物質抗癌剤は、癌細胞DNAとの相互作用を通して、通常抗腫瘍性質を有する抗微生物薬物である。本明細における使用のために適切な抗生物質抗癌剤は、ベロマイシン、ダクチノマイシン、ドキソルビシン、イダルビシン、エピルビシン、マイトマイシン、ミトキサントロン、ペントスタチン、プリカマイシン、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0147】
天然の抗癌剤分類はまた、本明細書に使用するために適切な、カプトテシン類似体及び誘導体を包含し、カプトテシン、トポテカン及びイリノテカンを包含する。それらの剤は主に、核酵素トポイソメラーゼIを標的化することにより作用する。天然の抗癌剤下でのもう1つのサブクラスは、酵素、L−アスパラギナーゼ及びその変異体である。L−アスパラギナーゼは、アスパラギン酸及びアンモニアへの循環アスパラギンの加水分解を触媒することにより、いくらかの癌細胞からL−アスパラギンを奪うことにより作用する。
【0148】
ホルモン抗癌剤:
ホルモン抗癌剤は、前立腺組織、乳房組織、子宮内膜組織、卵巣組織、リンパ腫及び白血病に関連するホルモン−依存性癌細胞に対して優先的に作用する。そのような組織は、グルココルチコイド、黄体ホルモン、エストロゲン及びアンドロゲンのような種類の剤に対して敏感であり、依存性であり得る。アゴニスト又は拮抗物質である類似体及び誘導体の両者は、腫瘍を処理するために本発明への使用に適切である。本明細書における使用のために適切なグルココルチコイドアゴニスト/拮抗物質の例は、デキサメサゾン、コルチゾール、コルチコステロン、プレドニソン、ミフェプリストン(RU486)、それらの類似体及び誘導体である。本明細書における使用のための適切な剤の黄体ホルモンアゴニスト/拮抗物質サブクラスは、ヒドロキシプロゲステロン、メドロキシプロゲステロン、酢酸メゲステロール、ミフェプリストン(RU486)、ZK98299、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のための適切な剤のエストロゲンアゴニスト/拮抗物質サブクラスの例は、エストロゲン、タモキシフェン、トレミフェン、RU58668、SR16234、ZD164384、ZK191703、フルベストラント、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。エストロゲン生成を阻害する、本明細書における使用のために適切なアロマターゼ阻害剤の例は、アンドロステンジオン、ホルメスタン、エキセメスタン、アミノグルテチミド、アナストロゾール、レトロゾール、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な剤のアンドロゲンアゴニスト/拮抗物質サブクラスからの例は、テストステロン、ジヒドロテストステロン、フルオキシメステロン、テストラクトン、エナント酸テストステロン、、プロピオン酸テストステロン、生殖腺刺激ホルモン放出ホルモンアゴニスト/拮抗物質(例えば、ロイプロリド、ゴセレリン、トリプトレリン、ブセレリン)、ジエチルスチルベストロール、アバレリックス、シプロテロン、フルタミド、ニルタミド、ビカルタミド、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0149】
脈管形成阻害剤:
脈管形成阻害剤は、腫瘍の血管形成化を阻害することにより作動する。脈管形成阻害剤は、広範囲の種類の剤、例えば小分子剤、抗体剤、及びRNA機能を標的化する剤を包含する。本明細書における使用のために適切な脈管形成阻害剤の例は、ラニビズマブ、ベバシズマブ、SUl1248、PTK787、ZK222584、CEP−7055、アンジオザイム、ダルテパリン、サリドマイド、スラミン、CC−5013、コンブレタスタチンAホスフェート、LY317615、大豆イソフラボン、AE−941、インターフェロンα、PTK787/ZK222584、ZD6474、EMD121974、ZD6474、BAY543−9006、セレコキシブ、ハロフジノン臭化水素、ベバシズマブ、それらの類似体、変異体又は誘導体を包含するが、但しそれらだけには限定されない。
【0150】
分化試薬:
分化剤は、癌細胞の分化を誘発する機構を通して腫瘍増殖を阻害する。本明細書における使用のために適切なそれらの剤の1つのそのようなサブクラスは、ビタミンA類似体又はレチノイド、及びペロキシソーム増殖活性化受容体アゴニスト(PPAR)を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なレチノイドは、ビタミンA、ビタミンAアルデヒド(レチナール)、レチノイン酸、フェンレチニド、9−シス−レチノイン酸、13−シス−レチノイン酸、全てのトランス−レチノイン酸、イソトレチノイン、トレチノイン、レチニルパルミテート、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なPPARのアゴニストは、トログリタゾン、シダリタゾン、テサグリタザー、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0151】
RNA阻害剤:
一定のRNA阻害剤が、癌表現型に関連するメッセンジャーRNA(“mRNa”)の発現又は翻訳を阻害するために利用され得る。本明細書における使用のために適切なそのような剤の例は、短い干渉性RNA(“siRNA”)、マイクロRNA(“miRNA”)、リボザイム及びアンチセンスオリゴヌクレオチドを包含するが、但しそれらだけには限定されない。本明細書における使用のために適切なRNA阻害剤の特定例は、Cand5、Sirna−027、フォミビルセン及びアンギオザイムを包含するが、但しそれらだけには限定されない。
【0152】
抗体/免疫療法剤:
抗体剤は、癌細胞において選択的に発現される標的物を結合し、その標的物に結合される細胞を殺害するために接合体を利用するか、又は癌細胞を破壊するために身体の免疫応答を誘発し得る。免疫療法剤は、ポリクローナル又はモノクローナル抗体からなることができる。抗体は、非ヒト動物(例えば、マウス)及びヒト成分からなるか、又は完全にヒト成分(“ヒト適合された抗体”)から構成される。本明細書における使用のために適切なモノクローナル免疫療法剤の例は、CD−20タンパク質を標的化する、リツキシマブ、トシブツモマブ、イブリツモマブを包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な他の例は、トランスツズマブ、エドレコロマブ、ベバシズマブ、セツキシマブ、癌胎児性抗原抗体、ゲムツヅマブ、アレムツヅマブ、マパツムマブ、パニツムマブ、EMD72000、TheraCIM hR3、2C4、HGS−TR2J及びHGS−ETR2を包含するが、但しそれらだけには限定されない。
【0153】
遺伝子療法剤:
遺伝子療法剤は、遺伝子のコピーを、特定組の患者の細胞中に挿入し、癌及び非癌細胞の両者を標的化し得る。遺伝子療法の目的は、変更された遺伝子を、機能的遺伝子により置換し、癌に対する患者の免疫応答を刺激し、癌細胞を化学療法に対してより感受性にし、癌細胞中に“自殺”遺伝子を配置し、又は脈管形成を阻害することであり得る。遺伝子は、ウィルス、リポソーム、又は他のキャリヤー又はベクターを用いて、標的細胞に供給され得る。これは、遺伝子−キャリヤー組成物を、患者中に直接、注入することにより、又はエクストビボで実施され、感染された細胞が患者中に戻される。このような組成物は、本発明での使用のために適切である。
【0154】
小分子酵素阻害剤:
一定の小分子療法が、チロシンキナーゼ酵素活性、又は一定の細胞受容体、例えば上皮増殖因子受容体(“GGFR”)又は血管の内皮増殖因子受容体(“VEGFR”)の下流のシグナルトランスダクションシグナルを標的化し得る。小分子療法剤によるそのような標的化は、抗癌効果ともたらすことができる。本明細書における使用のために適切なそのような剤の例は、イマチニブ、ゲフィチニブ、エルロチニブ、ラパチニブ、カネルチニブ、ZD6474、フォラフェニブ(BAY43−9006)、ERB−569、及びそれらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。
【0155】
生物学的応答調節剤:
一定のタンパク質又は小分子剤は、直接的な抗腫瘍効果又は間接的効果を通して抗癌療法に使用され得る。本明細書における使用のために適切な直接的作用剤の例は、分化試薬、例えばレチノイド及びレチノイド誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な作用剤は、免疫又は他のシステムを調節するか又は増強する剤、例えばインターフェロン、インターロイキン、造血成長因子(例えば、エリスロポイエチン)、及び抗体(モノクローナル及びポリクローナル)を包含するが、但しそれらだけには限定されない。
【0156】
抗転移剤:
癌細胞が元の腫瘍の部位から身体周囲の他の位置に広がる工程が、癌移転と呼ばれる。一定の剤は、癌細胞の広がりを阻害するよう企画された抗転移性質を有する。本明細書における使用のために適切なそのような剤の例は、マリマスタット、ベバシズマブ、トラスヅマブ、リツキシマブ、エルロチニブ、MMI−166、GRN163L、ハンターキラーペプチド、メタロプロテイナーゼの組織阻害剤(TIMP)、それらの類似体、誘導体及び変異体を包含するが、但しそれらだけには限定されない。
【0157】
化学予防剤:
一定の医薬剤が、癌の初期発症を妨げるために、又は転移の再発を妨げるために使用され得る。1又は2以上の他の抗症剤、例えばニトロベンズアミド化合物と組合せてのそのような化学予防剤の投与は、癌の再発を処理し、予防するよう作用し得る。本明細書における使用のために適切な化学予防剤の例は、次のものを包含するが、但しそれらだけには限定されない:タモキシフェン、ラロキシフェン、チボロン、ビスホスホネート、イバンドロネート、エストロゲン受容体モジュレーター、アロマターゼ阻害剤(レトロゾール、アナストロゾール)、黄体形成ホルモン放出ホルモンアゴニスト、ゴセレリン、ビタミンA、レタノイン酸、フェンレチニド、9−シス−レチノイド酸、13−シス−レチノイド酸、全てのトランス−レチノイン酸、イソトレチノメン、トレチノイド、ビタミンB6、ビタミンB12、ビタミンC、ビタミンD、ビタミンE、シクロオキシゲナーゼ阻害剤、非ステロイド性抗炎症薬物(NSAID)、アスピリン、イブプロフェン、セレコキシア、ポリフェノール、ポリフェノールE、緑茶抽出物、葉酸、グルカル酸、インターフェロンα、アネトールジチオールエチオン、亜鉛、ヒリドキシン、フィナステリド、ドキサゾジン、セレニウム、インドール−3−カルビナール、α−ジフルオロメチルオルニチン、カロテノイド、β−カロテン、リコペン、酸化防止剤、補酵素Q10、フラボノイド、ケルセチン、クルクミン、カテキン、エピガロカテキンガレート、N−アセチルシステイン、インドール−3−カルビノール、イソシトール六リン酸、イソフラボン、グルカン酸、ローズマリー、大豆、ノコギリパルメット及びカルシウム。本発明への使用のために適切な化学予防剤の追加の例は、癌用ワクチンである。それらは、ワクチン接種工程により標的化される癌細胞型の全て又は一部により患者を免疫化することにより製造され得る。
【0158】
副作用制限剤:
ニトロベンズアミド化合物単独による又は他の抗癌化合物と組合せての癌の治療は、抗癌剤により生成される副作用を緩和できる医薬剤の投与により達成され得る。本明細書における使用のために適切なそのような剤は、鎮吐薬、抗粘膜炎薬剤、疼痛処理薬剤、感染抑制剤及び抗貧血/抗血小板減少剤を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な鎮吐薬の例は、5−ヒドロキシトリプタミン3受容体拮抗薬、メトクロプラミド、ステロイド、ロラゼパム、オンダンセトロン、カンナビノイ、それらの類似体及び誘導体を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な抗粘膜炎薬剤の例は、パリフェミン(ケラチン細胞成長因子)、グルカゴン様ペプチド2、テジュクルチド、L−グルタミン、アミホスチン及び繊維芽細胞成長因子20を包含するが、但しそれらだけには限定されない。本明細書における使用のために適切な疼痛処理薬剤の例は、オピイオイド、オピエート及び非ステロイド性抗炎症化合物を包含する。本明細書における使用のために適切な感染を制御するために使用される剤の例は、次のものを包含するが、但しそれらだけには限定されない:抗菌剤、例えばアミノグリコシド、ペニシリン、セファロスポリン、テトラサイクリン、クリンダマイシン、リンコマイシン、マクロライド、バンコマイシン、カルバペネム、モノバクタム、フルオロキノロン、スルホンアミド、ニトロフラントイン、それらの類似体及び誘導体。本明細書における使用のために適切な化学療法に関連する貧血又は血小板減少症を処理できる剤の例は、エリスロポイエチン及びトロンボポイエチンを包含するが、但しそれらだけには限定されない。
【0159】
ニトロベンズアミド化合物及び本明細書に記載される他の化合物と組合せての使用のための幾つかの他の適切な療法がまた利用できる。例えば、Goodman & Gilman's The Pharmacological Basis of Therapeutics 1 lth ed. Brunton LL, Lazo JS, and Parker KL, ed. McGraw-Hill, New York, 2006を参照のこと。
【0160】
製剤、投与路及び有効用量:
本発明のもう1つの観点は、ニトロベンズアミド代謝化合物を含んでなる医薬組成物のための配合及び投与路に関する。そのような医薬組成物は、上記に詳細に記載された方法により癌を治療するために使用され得る。
【0161】
幾つかの態様においては、上記に示される代謝化合物は、個々の、又はプロドラッグとして組合せて供給され、/又は投与の後、インビボでニトロソベンズアミド形に相互転換され得る。さらに、前記代謝化合物は、プロドラッグとして供給され、/又は投与の後、インビボでニトロソベンズアミド形に相互転換され得る、式Iaのニトロベンズアミドと共に投与され得る。すなわち、ニトロベンズアミド形及び/又はニトロソベンズアミド形のいずれか、又は医薬的に許容し得る塩が、本発明への使用のための製剤の開発に使用され得る。さらに、幾つかの態様においては、代謝化合物は、1又は2以上の他の化合物、又は1又は2以上の他の形と組合せて使用され得る。例えば、製剤は、ニトロベンズアミド代謝化合物及び酸形の両者を、特定の割合で、個々の相対的能力及び意図される指標に依存して、含んでなる。前記2種の形は、同じ投与量単位で、例えば1つのクリーム、坐薬、錠剤、カプセル又は飲料水に溶解される粉末のパケットに、一緒に配合され得;又は個々の形は、別々の単位、例えば2種のクリーム、2種の坐薬、2種の錠剤、2種のカプセル、錠剤及び錠剤を溶解するための液体、粉末のパケット及び粉末を溶解するための溶液、等に配合され得る。
【0162】
ニトロベンズアミド代謝化合物及びもう1つの活性剤の組合せを含んでなる組成物は効果的である。2種の化合物及び/又は化合物形は、同じ投与量単位、例えば1つのクリーム、坐薬、錠剤、カプセル又は飲料水に溶解される粉末のパケットに一緒に配合され得;又は個々の形が、別々の単位、例えば2種のクリーム、坐薬、錠剤、2種のカプセル、錠剤及び錠剤を溶解するための液体、粉末ぱっと及び粉末を溶解するための液体、等に配合され得る。
【0163】
用語“医薬的に許容し得る塩”とは、本発明に使用される化合物の生物学的有効性及び性質を保持し、生物学的に又は他方では所望であるそれらの塩を意味する。例えば、医薬的に許容し得る塩は、癌の治療において本発明の化合物の有益な効果を妨げない。
【0164】
典型的な塩は、無機イオン、例えばナトリウム、カリウム、カルシウム及びマグネシウムイオンのそれらの塩である。そのような塩は、無機又は有機酸、例えば塩酸、臭酸、リン酸、硝酸、硫酸、メタンスルホン酸、p−トルエンスルホン酸、酢酸、フマル酸、琥珀酸、乳酸、マンデル酸、リンゴ酸、クエン酸、酒石酸又はマレイン酸との塩を包含する。さらに、本発明に使用される化合物がカルボキシ基又は他の酸性基を含む場合、それは無機又は有機塩基による医薬的に許容し得る付加塩に転換され得る。適切な塩基の例は、水酸化ナトリウム、水酸化カリウム、アンモニア、シクロヘキシルアミン、ジシクロヘキシル−アミン、エタノールアミン、ジエタノールアミン及びトリエタノールアミンを包含する。
【0165】
経口投与に関しては、代謝化合物は、活性化合物と、当業界において良く知られている医薬的に許容し得るキャリヤーとを組合すことにより容易に配合され得る。そのようなキャリヤーは、処理される患者による経口摂取のための、錠剤、咀嚼錠剤、ピル、糖剤、カプセル、トローチ、ハードキャンデー、液体、ゲル、シロップ、スラリー、粉末、懸濁液、エリキシル、ウェハー及び同様のものとしての本発明の化合物の配合を可能にする。そのような製剤は、医薬的に許容し得るキャリヤー、例えば固体希釈剤又は充填剤、無菌水性媒体及び種々の非毒性有機溶媒を含んでなる。一般的に、本発明の化合物は、所望する投与量単位を提供するのに十分な量で、経口投与形の合計組成物の約0.5重量%、約5重量%、約10重量%、約20重量%、又は約30重量%〜約50重量%、約60重量%、約70重量%、約80重量%又は90重量%の濃度レベルで含まれるであろう。
【0166】
水性懸濁液は、ニトロベンズアミド代謝化合物、及び医薬的に許容し得る賦形剤、例えば沈殿防止剤(例えば、メチルセルロース)、湿潤剤(例えば、レシチン、リソレシチン及び/又は長鎖脂肪アルコール)、並びに着色剤、保存剤、風味剤及び同様のものを含むことができる。
【0167】
幾つかの態様においては、油又は非水性溶媒は、例えば大きな親油性成分の存在のために、代謝化合物を溶液にすることが必要とされる。他方では、エマルジョン、懸濁液、又は他の調製物、例えばリポソーム調製物が使用され得る。リポソーム調製物に関しては、病状の処理のためのポリマーを調製するためのいずれの既知方法でも使用され得る。例えば、Bangham et al., J. MoI. Biol, 23: 238-252 (1965)及び Szoka et al., Proc. Natl Acad. Sci 75: 4194-4198 (1978)(引用により本明細書に組込まれる)を参照のこと。リガンドはまた、作用の特定部位にそれらの組成物を向けるためにリポソームに結合され得る。本発明の化合物はまた、食品、例えばクリームチーズ、バター、サラダドレッシング、又はアイスクリームに、一定の患者集団における溶解性、投与及び/又はコンプライアンスを促進するために組込まれ得る。
【0168】
経口使用のための医薬製剤は、任意には、得られる混合物を粉砕し、所望には、錠剤又は糖剤コアーを得るために、適切な助剤の添加の後、顆粒の混合物を処理することにより、固体賦形剤として得られる。適切な賦形剤は特に、充填剤、例えば糖、例えばラクトース、スクロース、マンニトール、又はソルビトール;風味要素、セルロース調製物、例えばトウモロコシ澱粉、小麦澱粉、米澱粉、ジャガイモ澱粉、ゼラチン、トラガカントガム、メチルセルロース、ヒドロキシプロピルメチルセルロース、ナトリウムカルボキシメチルセルロース、及び/又はポリビニルピロリドン(PVP)である。所望には、砕解剤、例えば架橋されたポリビニルピロリドン、寒天、又はアルギン酸、又はその塩、例えばアルギン酸ナトリウムが添加され得る。前記化合物はまた、持効性製剤としても配合され得る。
【0169】
糖剤コアーは、適切な被覆が供給され得る。このためには、任意にはアラビアゴム、タルク、ポリビニルピロリドン、カルボポールゲル、ポリエチレングリコール、及び/又は二酸化チタン、ラッカー溶液及び適切な有機溶媒又は溶媒混合物を含むことができる、濃縮された糖溶液が使用され得る。染料又は色素が、識別のために、又は活性化合物用量の異なった組合せを特徴づけるために、錠剤又は糖剤被膜に添加され得る。
【0170】
経口使用され得る医薬製剤は、ゼラチンから製造された押込嵌めカプセル、及びゼラチン及び可塑剤、例えばグリセロール又はソルビトールから製造される、密封された軟質カプセルを包含する。押込嵌めカプセルは、活性成分、並びに充填剤、例えばラクトース、結合剤、例えば澱粉、及び/又は滑剤、例えばタルク又はステアリン酸マグネシウム、及び任意には安定剤を含むことができる。軟質カプセルにおいては、活性化合物は、適切な液体、例えば脂肪油、液体パラフィン又は液体ポリエチレングリコールに溶解されるか又は懸濁され得る。さらに、安定剤が添加され得る。経口投与のための全ての製剤は、投与のために適切な投与量で存在すべきである。
【0171】
注射に関しては、本発明の阻害剤は、水溶液、好ましくは生理学的に適合できる懸濁液、例えばハンクス溶液、リンガー溶液又は生理学的塩緩衝液において配合され得る。そのような組成物はまた、1又は2以上の賦形剤、例えば保存剤、溶解剤、充填剤、滑剤、安定剤、アルブミン及び同様のものを含むことができる。例えば、Remington's Pharmaceutical Sciences, latest edition, Mack Publishing Co., Easton Pに開示されるような配合方法は、当業界において知られている。それらの化合物はまた、経粘膜投与、口腔内投与、吸入による投与、非経口投与、経皮投与及び直腸投与のためにも配合され得る。
【0172】
これまで記載された製剤の他に、代謝化合物はまた、デポ製剤としても配合され得る。そのような長期作用性製剤は、移植又は経皮供給(例えば、皮下又は筋肉内)、筋肉内注射又は経皮用パッチの使用により投与され得る。従って、例えば化合物は、適切なポリマー又は親水性材料(例えば、許容できる油中、エマルジョンとして)、又はイオン交換樹脂と共に、又は親水性材料(例えば、許容できる油中、エマルジョンとして)、又はイオン交換樹脂と共に、又は低溶解性誘導体として、例えば低溶解性塩として配合され得る。
【0173】
本発明における使用のために適切な医薬組成物は、活性成分が有効量で、すなわち本明細書に記載される少なくとも1つの癌において治療及び/又は予防的有益性を達成するの有効な量で存在する組成物を包含する。特定の用途のために効果的な実際の量は、処理される状態、対象の状態、配合及び投与路、並びに当業者に知られている他の要因に依存するであろう。ニトロベンズアミド代謝化合物の有効量の決定は、本明細書における開示の点から、当業者の能力内であり、通常の最適化技法を用いて決定されるであろう。
【実施例】
【0174】
実施例1:ベンズアミド代謝物の同定:
血漿サンプルを、イヌ、ラット及びマウス研究から得、ここで動物は4−ヨード−3−ニトロベンズアミド(BA)を投与されている。血漿及び腫瘍サンプルを、血漿(40μl)を、3倍体積(150μl)のアセトニトリルにより沈殿することにより、HPLC注入のために調製した。組織サンプルを、組織1mg当たり1μlのアセトニトリルを添加し、次に電気ホモナイザーにより均質化することにより、HPLC注入のために調製した。遠心分離に続いて、150μlの個々の上清液を蒸発乾燥し、水中、0.2%蟻酸50μlにおいて再構成し、クロマトグラフィー及び質量分光技法(LC/MS/MS条件)により分析した。LC/MS/MS条件は次の通りである:HPLC(Shimadzu VP System);移動相:水中、0.2%蟻酸(A)及びメタノール中、0.18%蟻酸(B);カラム:1×50mmのThermo Betabasic C18カラム;注入体積:25μl;グラジエント:30分での0〜6%B;流速:100μl/分;質量分光計:Applied Biosystems/MDS SCIEX Q-STAR;インターフェイス:1/10でのIonSprayスプリット;親イオン走査:200〜900amuのTOF陽性;生成物イオン走査:親イオン走査における最も強いイオンの60〜900amuのTOP生成物イオン;TOP検量:Renin基質を用いて外部的に検量された。イヌ及びマウス血漿からの代謝物同定の結果が、次の通りに表1〜3に示される。
【0175】
表1:イヌ血漿からのLC/MS/MSによるBA代謝物同定の要約:
【表1】

*:近似ng/ml等価値は、対照標準として1μg/mlのスパイクサンプルにおけるBSI−201を用いて測定された。
【0176】
明確化のため、上記表1における名称は、次の通りに上記に開示される化合物に対応する(名称:化合物);M2:MS472、M3:MS213及びM4:MS263。
【0177】
表2:ネズミ血漿からのLC/MS/MSによるBA代謝物同定の要約:
【表2】

*:近似ng/ml等価値は、対照標準として1μg/mlのスパイクサンプルにおけるBSI−201を用いて測定された。
【0178】
明確化のため、上記表2における名称は、次の通りに本明細書に開示される化合物に対応する(名称:化合物);M3:MS472、M6:MS328、M7:MS213及びM8:MS263。
【0179】
表3:イヌ血漿及び赤血球細胞からのLC/MS/MSによるBA代謝物同定の要約:
【表3】

*近似ng/ml等価値は、対照標準として5μg/mlのスパイクサンプルにおけるBSI−201の270nmUVピーク領域を用いて測定された。
【0180】
明確化のため、上記表3における名称は、次の通りに本明細書に開示される化合物に対応する(名称:化合物);M2:MS472及び第2のM2:MS601。
【0181】
実施例2:インビトロ研究−細胞毒性アッセイ:
異なった起源の異なったタイプの癌細胞系又は一次細胞を、48ウェルプレート(5×104)又は96ウェルプレート(2×104)上に接種する。細胞を適切な培地において培養し得る。培養を、95%O2/5%CO2の湿潤された雰囲気下で37℃のインキュベーターにおいて維持し得る。細胞の接種の後(24時間)、培地を除き、200μMのBSOの存在又は不在下で、種々の濃度のINO2BA又はINH2BPの存在下で培養培地により置換する。37℃での6日間のインキュベーションの後、細胞生存度を、Cell Titer-Blue, Cell Viability Assay (Promega) (O'Brien, J.et al. (2000) Investigation of the Alamar Blue (resazurin) fluorescent dye for the assessment of mammalian cell cytotoxicity. Eur.J.Biochem.267, 5421-26 and Gonzalez, R.J.and Tarloff, J.B. (2001) Evaluation of hepatic subcellular fractions for Alamar Blue and MTT reductaseを参照のこと)を用いて測定する。このアッセイは、活性色素還元による検出に基づかれる蛍光測定/比色成長インジケーターを組込む。細胞毒性を、成長阻害により測定される。
【0182】
細胞毒性をまた、生存細胞の数を計数することにより評価し得る。細胞をPBSにより単層を洗浄することにより収穫し、続いて0.25%のトリプシン及び0.02%のEDTAにおいて短時間インキュベーションした。次に、細胞を集め、遠心分離により2度、洗浄し、PBSに再懸濁する。細胞数及び生存度を、0.2%トリパンブルー塩溶液により小体積の細胞懸濁液を染色し、血球計算機により細胞を試験することにより決定する。Kerley-Hamilton et al. (2005) p53-dominant transcriptional response to cisplatin in testicular germ cell tumor-derived human embryonal carcinoma及びCheol et al. (2005) Induction of apoptosis and inhibition of cyclooxygenase-2 expression by N-methyl-N'-nitro-N-nitrosoguanidine in human leukemia cellsを参照のこと。
【0183】
実施例3:BrdU−ELISAにより測定される細胞増殖:
細胞を、37℃で湿潤された雰囲気下でウェル当たり100μlの最終体積で、ブラック96ウェルMultiplate(組織培養品種:平らな透明底)において種々の濃度の試験物質(薬物)の存在下でインキュベートし得る。10μl/ウェルのBrdUラベリング溶液を、細胞を100μl/ウェルにおいて培養した後(最終濃度:10μMのBrdU)、添加し、細胞を37℃でさらに2〜24時間、再インキュベートする(細胞が200μl/ウェルで培養される場合、20μl/ウェルのBrdUラベリング溶液を添加した)。MPを、300m×gで10分間、遠心分離し、ラベリング培地をカニューレを用いて吸引により除去した。細胞を、ヘアードライヤーを用いて、約15分間、又は他方では、60℃で1時間、乾燥する。200μl/ウェルのFixDenatを細胞に添加し、15〜25℃で30分間インキュベートする。FixDenat溶液を、軽くはね飛ばし、タッピングすることにより十分に除去する。100μl/ウェルの抗−BrdU−POD作業溶液を添加し、15〜25℃で約90分間インキュベートする。他方では、このインキュベーション時間は、個々の必要条件に依存して、30〜120分、変動する。抗体接合体を、軽くはね飛ばすことにより除去し、ウェルを200〜300μl/ウェルの洗浄溶液により3度、すすいだ。洗浄溶液をタッピングすることにより除去する。次に、100μl/ウェルの基質溶液を個々のウェルに添加する。サンプルの発光を、光電増倍管によりマイクロプレートルミノメーターにより測定し得る。
【0184】
実施例4:インビボ移植及び腫瘍増殖:
100匹の雌NU/NU−nuBRマウス(Charles River、生後5〜6週)を、0.72mgの17β−エストラジオール(ヒト)ペレットにより移植し、耳をクリップを用いて標識し、腫瘍細胞移植の24〜48時間前、計量する。腫瘍細胞BT472(2×107個の細胞/マウス)を、肩甲下乳房脂肪パッド(0.2mlの体積)中に注入する。キャリパー測定を、21日目、及びその後、毎週3度(月、水、金)始める。動物を、腫瘍の存在及び不在に従って、及び次に、腫瘍体積により分離する。移植後第3週から初めて、動物を週当たり2度、計量する(月及び金)。薬物処理を、腫瘍サイズが150〜250kmm3(L×W×H)である場合、開始する。薬物及びビークル投与は、5日間、胃管栄養法(BP+BSO)によるBID及びIP(BA)によるSIDである。次のサイクルが開始する前、2日の自発休眠期が存在する。動物は、予測できない毒性が存在しない限り、3回のサイクル(それぞれ5日)を受けることができる。初期値又は一定の微候の表示の15%を越える体重の低下が、動物安楽死のための基準として使用さえ得る。薬物は、5mg/kgの体積で、胃管栄養法及びIPにより投与される。薬物及びビークルを、箔−被覆されたボトルにおいて4℃で貯蔵する。
【0185】
【表4】

*:BP+BSO及びBAの組合せ。
【0186】
実施例4:異種移植片研究:
代謝化合物の効果を、ヌードマウスにおける卵巣ヒト癌細胞(OVCAR)異種移植片に対して評価する。
【0187】
雌NU/NU37−BU−04−BACマウス(Charles River, 生後5〜6週)の耳を、クリップを用いて標識し、腫瘍細胞移植の24〜48時間前、計量する。腫瘍細胞Ovcar3(5×106個の細胞/マウス)を、雌ヌードマウス宿主の肩甲下の乳房脂肪パッド中に皮下移植する。キャリパー測定を、腫瘍細胞移植後、7日目、その後、週2度(月及び金)開始する。動物を、腫瘍の存在又は不在に従って、及び次に腫瘍体積に従って分離する。動物を週1度、計量する。薬物処理を、サイズが最大直径0.4〜0.5cmになる場合、開始する。4−ヨード−3−ニトロベンズアミド(BA)(50μlの100%DMSO/マウスにおける)及びビークル(50μlの100%DMSO/マウスにおける)を、5日間、1日当たり2度、IPにより、注入する。次のサイクルが始まる前、2日の自発休眠期間が存在する。
【0188】
【表5】

【0189】
実施例5:代謝化合物の効力の評価:
一般的方法:
MDA MB231ヒト乳癌細胞を、雌ヌードマウスの右側面中に皮下注入し得る。作業1に関しては、BPを、腫瘍細胞移植の前、5日間連続して投与し、その後、薬物投与を、4〜8週間、週5日続ける。作業2に関しては、癌細胞を、腫瘍が50〜60mm3の平均腫瘍体積に達する場合、注入し、マウスを8匹のグループに分け、トウモロコシ油:PEG400(対照)、BP, 又はCTX(MDA MB231陽性対照)により処理する。腫瘍体積を、処理の開始の後、90日間モニターする(MDA MB231に関する)。
【0190】
細胞系:
MDA MB231は、細胞系が開始する前3ヶ月で、5−RU, ドキソルビシン、メトトレキセート及びCTXにより処理された患者の胸膜浸出液から1973年、確立されたヒト乳癌細胞系である。この細胞系は、エストロゲン受容体陰性であり、ホルモン拮抗薬として標的化されない抗癌薬物のスクリーニングに使用されて来た。MDA MB231は、NaHCO3/l、10%ウシ胎児血清(FBS)及び2mMのL−グルタミンを含むダルベッコ変性イーグル培地(DMEM)において増殖し、湿潤された5%CO2/空気インキュベーターにおいて37℃で維持した。抗体を、培地に添加しなかった。
【0191】
動物腫瘍モデル:
マウス:
雌CB.17SCIDマウス(Charles River)は、生後8〜11週であり、研究のD1で、12.6〜23.0gの範囲の体重(BW)を有した。動物は、水(逆浸透、1ppmのCl)、及び18.0%の粗タンパク質、5.0%の粗脂肪及び5.0%の粗繊維からなるNIH 31 Modified and Irradiated Lab Diet*を、自由に供給された。マウスは、実験動物の保護及び使用について、許容された標準とのコンプライアンスを確かにする、Assessment and Accreditation of Laboratory (AAALAC) Internationalにより認定された実験所において、21〜22℃(70〜72°F)及び40〜60%湿度で12時間の光サイクルに基づいて、静的にマイクロアイソレーターにおける照射されたALPHA-dri(登録商標) bed-o-cobs* Laboratory Animal Beddingに収容された。
【0192】
腫瘍移植:
この研究に使用されるヒトOVCAR−3(NIH−OVCAR−3)卵巣腺癌を、一連の移植により無胸腺ヌードマウスにおいて維持した。腫瘍フラグメント(1mm3)を、個々の試験マウスの右側部中に皮下(s.c.)移植した。腫瘍を週2度モニターし、それらの体積が80〜120mm3に達する場合、毎日モニターした。研究のD1で、動物を、63〜221mm3の腫瘍サイズを有する処理グループ及び約105mm3の平均腫瘍サイズのグループに分類した。
【0193】
腫瘍サイズ(mm3)は、下記式から計算された:
【数1】

【0194】
腫瘍重量を、1mgが1mm3の腫瘍体積に等しい仮定に基づいて評価する。
【0195】
処理:
マウスを9のグループ(n=10)に分類し、前記プロトコールに従って処理した。経口グループは、D68a.m.(最後までb.i.d.(毎日2度))まで、D1p.m.から、毎日2度、BAを経口的(p.o.)に受けた。Alzetモデルの浸透ポンプを、1,15及び29日目に移植した。ポンプは、37℃で約1時間、予備的に暖められ、次に、イソフルオラン麻酔されたマウスの左側部にs.c.移植された。個々のポンプは、14日間にわたって合計用量の25mgの/kg/週のBAを供給した。
【0196】
エンドポイント:
腫瘍は、研究の期間、週2度カリパスにより測定された。個々の動物は、その腫瘍が予定されたエンドポイントサイズ(1,000mm3)に達した場合、安楽死された。個々のマウスについてのエンドポイントの時間(TTE)は、次の等式により計算された:
【数2】

ここでTTEは日で表され、エンドポイント体積はmm3で示され、bは切片であり、mはlog−転換された腫瘍増殖データ組の線状回帰により得られた直線の傾斜である。
【0197】
そのデータ組は、研究エンドポイント体積を越える最初の観察、及びエンドポイント体積の到達の直後、3回の連続した観察から構成される。計算されたTTEは通常、動物が腫瘍サイズに関して安定死される日以下である。エンドポイントに達しない動物は、研究の最後で安定死され、最後の日(68日)に等しいTTE値を割り当てられる。処理効力を、対照のグループに比較して、処理グループについてのメジアンTTEの上昇として定義される、腫瘍増殖遅延(TGD)から決定した:TGD=日で表され、又は対照グループのメジアンTTEの百分率として表される、T−C:
【数3】

式中、T=処理グループについてのメジアンTTE、C=対照グループ1についてのメジアンTTE。
それらの研究の結果は図4に示される。
【0198】
生後4〜5週の雌Swiss NGヌード(nu/nu)マウスを、Taconic (Germantown, NY)から入手する。動物は、Bio Bubble, Inc. (Fort Collins, CO)から購入されたバリアクリーンルームにおいて無菌フィルターを上部に付けられたゲージにおいて、ケージ当たり3匹で収容される。達着後、それらは、使用の前、4日の作業目の間、検疫される。処理は、72±5°F及び35〜70%の相対湿度で維持され、12時間の明/暗サイクルが使用された。マウスは、無菌でオートクレーブできる、保証されたPurina齧歯動物用食事を自由に供給される。飲料水は酸性にされ、オートクレーブ処理され、水源を再循環され、脱イオン化され、UV−処理され、5μmのフィルター処理される。
【0199】
動物を検疫から開放した後、マウスは、1又は5×106個のMDA MB231細胞(0.1mlの注入体積)を、右側部に皮下注入される。タスク1に関するマウスは、細胞注入の前5日間、前処理を受けた。腫瘍寸法及び体重を、週2度、測定する。ノギスを用いて、腫瘍を3面から測定し、腫瘍体積(V)を次の通りに計算する:V=π(x×y×z)/6、ここでx、y及びzは腫瘍測定値−皮膚の厚さである。実験の最後で、マウスを、CO2吸入、続く頸部転移により殺す。
【0200】
医薬:
MS472を、30mg/ml及び100mg/mlの濃度で、トウモロコシ油:PEG400(2:1、v/v)において製造し得る。薬物は、それらの濃度での懸濁液であり得る。陽性対照薬物は、リン酸緩衝溶液(PBS)及びCTXに基づいて、15mg/mlで製造される。両薬物は、使用の前、フィルター殺菌され得る(0.2μmのフィルター)。
【0201】
処理プロトコール:
タスク1に関しては、MDA MB231腫瘍細胞により移植されたマウスを、MS472(300又は1000mg/kg)により5日間、前処理し、細胞懸濁液の皮下注入に続いて、薬物処理を、最少4週間、週5日間(月〜金)、続ける。
【0202】
タスク2に関しては、腫瘍体積が予定されたサイズ(50〜60mm3の平均腫瘍体積)に達した後、マウスをそれぞれ8匹のマウスの処理グループに分ける。BPの全ての処理を、少なくとも4週間、週当たり5度(月〜金)、行う。CTXは、150mg/kgの用量で1度、腹腔内投与される。全てのBP処理は経口的に行われ;投与量は、MDA MB231細胞により移植されたそれらに関しては、1000又は2000mg/kgであった。個々のタスクに関して、全ての処理は同じ日に開始した。
【0203】
腫瘍は、最初の処理の後、少なくとも9週間、週2度、測定される(MDA MB231)。個々のグループについての平均腫瘍体積を、個々の時点について計算する。特定時間でのグループ間の比較を、非対両側t検定を用いて行い、結果を、分散分析(ANOVA)を用いて分析する。タスク2に関しては、個々の腫瘍体積(V)を、0日、すなわち処理の最初の日(VO)での腫瘍体積の割合として表す。個々のグループに関しては、VNO比率の平均を、処理の後の時間の関数としてプロットする。処理に対する応答を、処理に対する腫瘍応答に依存して、2種の手段で測定する。腫瘍体積倍増化時間(VDT)及び体積4倍化時間(VQT)を、処理に対する応答が存在するグループにおけるlog(腫瘍体積)の関数としての時間のプロットに基づく線状回帰法により、個々の腫瘍について決定する。個々の処理グループについての腫瘍倍増遅延を決定し、グループ間の比較をANOVAを用いて分析する。
【0204】
全身毒性を、処理後の体重の低下から評価する。マウスは、追跡期間の最後で、又は腫瘍体積が早く1600mm3に達するか又は腫瘍が潰瘍化した場合、殺害される。
統計学的分析:
【0205】
統計学的分析を、InStat(Graphpad Software, San Diego, CA)を用いて行う。
【0206】
腫瘍増殖:
MDA MB231腫瘍は、腫瘍細胞注入の3週間以内に測定可能であり、通常、よりゆっくり増殖し、倍増化時間は7日である。値は、対照のグループから計算され得る。処理の開始での平均腫瘍体積及び体重が、タスク1に関して表4日及びタスク2に関して表5に示されるフォーマット下で示され得る。
【0207】
表4:
処理の開始でのマウスパラメーター−タスク1:
【表6】

*SEM=標準誤差
【0208】
表5:
処理の開始でのマウスパラメーター−タスク2:
【表7】

*SEM=標準誤差
【0209】
上記実施例は、本発明の範囲を制限するものではない。さらに、多くの変更及び修飾が本発明の範囲内で行われることは、当業者に明らかである。
【0210】
実施例6:細胞周期分析:
HCT116及びHela細胞を、ATCCから入手した。DNA含量分析に関しては、2×105個の細胞を、PBSにより2度、洗浄し、70%エタノールに固定した。細胞を、37℃で20分間、100単位/mlのRNアーゼAにより処理し、Alexa Fluor(登録商標)405蛍光染色(Invitrogen)を含む冷PBSに、その製造業者のプロトコールに従って再懸濁した。細胞を流動細胞計測法により分析した。図1は、PARP−1阻害剤(4−ヨード−3−ニトロベンズアミド又は“BA”)により19時間、処理されたHTC16細胞における(FACSドットプロット及びヒストグラム)細胞周期分析を示す。BA処理は、S期細胞周期の同時低下を伴って、対照に比較して(18.6%)、G1期における細胞数の上昇(48.6%)を引起した。
【0211】
DNA複製分析に関しては、2×105個の細胞を、50μモル/lのブロモデオキシウリジン(BrdUrd)と共に30分間インキュベートした。細胞を70%エタノールに固定し、BrdUrd組込めを、抗−BrdUrd−FITC 抗体(Becton Dickinson, Franklin Lakes, NJ)を用いて、その製造業者のプロトコールに従って、流動細胞計測法により決定した。G2/Mチェックポイントの程度を評価するために、有糸分裂細胞を、有糸分裂−特異的抗体GF−7を用いて、流動細胞計測法により検出した。固定された細胞を、GF7−フィコエリトリン(PE)抗体(BD Biosciences Pharmingen)と共に30分間インキュベートし、PBSにより洗浄し、流動細胞計測法により分析した。図2は、24時間のインキュベーションで、BA、BNO(4−ヨード−3−ニトロソベンズアミド)及びBNHOH(4−ヨード−3−ヒドロキシアミノベンズアミド)により得られた結果を比較し;図3は72時間でのBA、BNO及びBNHOHに関する結果を示す。
【0212】
像分析及び顕微鏡法:カバーガラス上で増殖する細胞を、PBS中、4%パラホルムアルデヒドにより10分間、固定し、70%エタノールに浸透した。洗浄の後、カバーガラスを、50%PBS/50%グリセロール中、スライド上に積層した。像を顕微鏡により分析した。
【0213】
MDR1発現FACSアッセイ:
KB−V1は、KB−3−1ヒト癌細胞のビンブラスチン耐性クローンである(Fojo, A T , J Whang-Peng, M M Gottesman, and I Pastan 1985 Amplification of DNA sequences in human multidrugresistant KB carcinoma cells Proc Natl Acad Sa USA 82 7661-7665 , Shen, D -W, C Cardarelli, J Iwang, M Cornwell, N Richert, S Is fin, I Pastan, and M M Gottesman 1986 Multiple drug-resistant human KB carcinoma cells independently selected for high-level resistance to colchicine, Adnamycin, or vinblastine show changes in expression of specific proteins J Biol Chem 261 7762-7770)。細胞を、10%ウシ胎児血清を含むイーグル最少必須培地において増殖した。
【0214】
MDR1に関しては、染色細胞をトリプシン処理により収穫し、5%FBSにより補充されたIscoveの変性ダルベッコ培地により洗浄し、次に、抗−Mdr1抗体UIC2を含むIMDM/5%FBSに再懸濁した。一次抗体のとのインキュベーションの後、細胞を洗浄し、次に、フィコエリトリン(PE)抗体(BD Biosciences Pharmingen)に結合される二次抗体と共に、インキュベートした。抗体処理された細胞を洗浄し、次に、FACS Calibur(登録商標)計測期(Becton, Dickinson)上で分析した。FACS分析に使用される対照は、抗体と共にインキュベートされなかった細胞、すなわちイソタイプ対照抗体と共にインキュベートされた細胞であった。三重反復試験サンプルを分析し、それらのヒストグラムを分析した。メジアン蛍光を、log尺度でプロットした。図6A及び6Bは、それぞれ、KB3−1及びKBV−1細胞のレベルを示す:従って、FACFヒストグラムは、KBV−1細胞におけるMDR1の過剰発現を示す。MDR1の過剰発現は、多薬物耐性に関連している。
【0215】
コロニー形成アッセイ:
細胞をトリプシン処理し、計数し、106個の細胞/mlの最終濃度に希釈した。コロニー形成アッセイを、適切な数の細胞を培養皿中にプレートすることにより、三重反復して実施し、0〜100μMの化合物により処理した。14日後、細胞を固定し、1%クリスタルバイオレットにより染色し、コロニーを計数した。図5Cは、KB3−1及びKBV−1細胞におけるこの実験の結果を示す。図5Cに見られるように、BAはMDR1過剰発現及びMDR1正常細胞に関して、用量依存性態様で細胞コロニー数を減じる。MDR1過剰発現は多薬剤耐性に関連するので、この結果は、BAが多薬剤耐性腫瘍に対して効果的であろうことを示唆する。
【0216】
本発明の好ましい態様を本明細書において示し、記載して来たが、そのような態様が単なる例によって提供されることは当業者に明白であろう。現在、本発明から逸脱しないで、多くの変動、変更及び置換が、当業者に明らかになるであろう。本明細書に記載される本発明の態様に対する種々の選択が本発明の実施に使用され得ることは理解されるべきである。次の請求項が本発明の範囲を定義し、それらの請求項の範囲内の方法及び構造体並びにそれらの同等物は保護される。
【特許請求の範囲】
【請求項1】
下記構造式(IIa):
【化1】

[式中、R1、R2、R3、R4及びR5置換基の少なくとも1つは常に硫黄であり、R基は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、ブロモ、フルオロ、クロロ、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C7)シクロアルキル及びフェニルからなる群から独立して選択され、5種のR1、R2、R3、R4及びR5置換基の少なくとも2つは常に水素であり;或いは、R1、R2、R3、R4及びR5置換基の少なくとも1つが硫黄でない場合、前記5種の置換基の少なくとも1つは常にヨードであり、前記ヨードは、酸化窒素、ヒドロキシルアミン、ヒドロキシル又はアミノ基のいずれかであるR基に常に隣接する]で表される化合物;及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグ。
【請求項2】
MS213、MS472、MS601、MS328、MS263、MS276、MS278、MS456、MS183、MS261、MS182、MS635a、MS635b、MS471、MS414及びMS692からなる群から選択される化合物。
【請求項3】
前記化合物が、医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグの形態である、請求項2記載の化合物。
【請求項4】
癌を治療する方法であって、
下記式(IIa):
【化2】

[式中、R1、R2、R3、R4及びR5置換基の少なくとも1つは常に硫黄であり、R基は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、ブロモ、フルオロ、クロロ、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C7)シクロアルキル及びフェニルからなる群から独立して選択され、ここで5種のR1、R2、R3、R4及びR5置換基の少なくとも2つが常に水素であり;或いは、R1、R2、R3、R4及びR5置換基の少なくとも1つが硫黄でない場合、前記5種の置換基の少なくとも1つは常にヨードであり、前記ヨードは、酸化窒素、ヒドロキシルアミン、ヒドロキシル又はアミノ基のいずれかであるR基に常に隣接している]で表される化合物;及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグを含んでなる、有効量の組成物を、それを必要とする対象に投与することを含んでなる方法。
【請求項5】
MS213、MS472、MS601、MS328、MS263、MS276、MS278、MS456、MS183、MS261、MS182、MS635a、MS635b、MS471、MS414及びMS692からなる群から選択される化合物を含んでなる、有効量の組成物を、それを必要とする対象に投与することを含んでなる癌の治療方法。
【請求項6】
有効量のブチオニンスルホキシミンを投与することをさらに含んでなる、請求項4又は5記載の方法。
【請求項7】
ポリ−ADP−リボースポリメラーゼ(PARP)分子が、患者において式(Ia)及び/又は式(IIa)の化合物により阻害される、請求項4又は5記載の方法。
【請求項8】
前記腫瘍細胞が、患者においてアポプトシス、細胞周期阻止、及び/又は壊死を受ける、請求項4又は5記載の方法。
【請求項9】
有効量の式(II)のベンゾピロン化合物を投与することをさらに含んでなる、請求項4又は5記載の方法。
【請求項10】
癌を治療する方法であって、有効量の1又は2以上の組成物を、それを必要とする対象に投与することを含んでなるとともに、前記1又は2以上の組成物が各々、MS213、MS472、MS601、MS328、MS263、MS276、MS278、MS456、MS183、MS261、MS182、MS635a、MS635b、MS471、MS414、MS692、又はそれらの組合せである方法。
【請求項1】
下記構造式(IIa):
【化1】

[式中、R1、R2、R3、R4及びR5置換基の少なくとも1つは常に硫黄であり、R基は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、ブロモ、フルオロ、クロロ、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C7)シクロアルキル及びフェニルからなる群から独立して選択され、5種のR1、R2、R3、R4及びR5置換基の少なくとも2つは常に水素であり;或いは、R1、R2、R3、R4及びR5置換基の少なくとも1つが硫黄でない場合、前記5種の置換基の少なくとも1つは常にヨードであり、前記ヨードは、酸化窒素、ヒドロキシルアミン、ヒドロキシル又はアミノ基のいずれかであるR基に常に隣接する]で表される化合物;及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグ。
【請求項2】
MS213、MS472、MS601、MS328、MS263、MS276、MS278、MS456、MS183、MS261、MS182、MS635a、MS635b、MS471、MS414及びMS692からなる群から選択される化合物。
【請求項3】
前記化合物が、医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグの形態である、請求項2記載の化合物。
【請求項4】
癌を治療する方法であって、
下記式(IIa):
【化2】

[式中、R1、R2、R3、R4及びR5置換基の少なくとも1つは常に硫黄であり、R基は、水素、ヒドロキシ、アミノ、ニトロ、ヨード、ブロモ、フルオロ、クロロ、(C1−C6)アルキル、(C1−C6)アルコキシ、(C3−C7)シクロアルキル及びフェニルからなる群から独立して選択され、ここで5種のR1、R2、R3、R4及びR5置換基の少なくとも2つが常に水素であり;或いは、R1、R2、R3、R4及びR5置換基の少なくとも1つが硫黄でない場合、前記5種の置換基の少なくとも1つは常にヨードであり、前記ヨードは、酸化窒素、ヒドロキシルアミン、ヒドロキシル又はアミノ基のいずれかであるR基に常に隣接している]で表される化合物;及び医薬的に許容し得るその塩、溶媒化合物、異性体、互異性体、代謝物、類似体又はプロドラッグを含んでなる、有効量の組成物を、それを必要とする対象に投与することを含んでなる方法。
【請求項5】
MS213、MS472、MS601、MS328、MS263、MS276、MS278、MS456、MS183、MS261、MS182、MS635a、MS635b、MS471、MS414及びMS692からなる群から選択される化合物を含んでなる、有効量の組成物を、それを必要とする対象に投与することを含んでなる癌の治療方法。
【請求項6】
有効量のブチオニンスルホキシミンを投与することをさらに含んでなる、請求項4又は5記載の方法。
【請求項7】
ポリ−ADP−リボースポリメラーゼ(PARP)分子が、患者において式(Ia)及び/又は式(IIa)の化合物により阻害される、請求項4又は5記載の方法。
【請求項8】
前記腫瘍細胞が、患者においてアポプトシス、細胞周期阻止、及び/又は壊死を受ける、請求項4又は5記載の方法。
【請求項9】
有効量の式(II)のベンゾピロン化合物を投与することをさらに含んでなる、請求項4又は5記載の方法。
【請求項10】
癌を治療する方法であって、有効量の1又は2以上の組成物を、それを必要とする対象に投与することを含んでなるとともに、前記1又は2以上の組成物が各々、MS213、MS472、MS601、MS328、MS263、MS276、MS278、MS456、MS183、MS261、MS182、MS635a、MS635b、MS471、MS414、MS692、又はそれらの組合せである方法。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公表番号】特表2010−502730(P2010−502730A)
【公表日】平成22年1月28日(2010.1.28)
【国際特許分類】
【出願番号】特願2009−527544(P2009−527544)
【出願日】平成19年9月5日(2007.9.5)
【国際出願番号】PCT/US2007/077651
【国際公開番号】WO2008/030883
【国際公開日】平成20年3月13日(2008.3.13)
【出願人】(507401258)バイパー サイエンシズ,インコーポレイティド (13)
【Fターム(参考)】
【公表日】平成22年1月28日(2010.1.28)
【国際特許分類】
【出願日】平成19年9月5日(2007.9.5)
【国際出願番号】PCT/US2007/077651
【国際公開番号】WO2008/030883
【国際公開日】平成20年3月13日(2008.3.13)
【出願人】(507401258)バイパー サイエンシズ,インコーポレイティド (13)
【Fターム(参考)】
[ Back to top ]

