癌高発現遺伝子
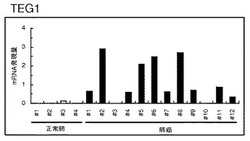
【課題】癌の診断および治療剤として用いることができる遺伝子およびタンパク質を提供する。
【解決手段】特定のヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント、これらを認識する抗体またはその抗原結合性フラグメント、または特定のヌクレオチド配列の少なくとも12個の連続するヌクレオチド配列もしくはこれに相補的なヌクレオチド配列を有するポリヌクレオチド。
【解決手段】特定のヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント、これらを認識する抗体またはその抗原結合性フラグメント、または特定のヌクレオチド配列の少なくとも12個の連続するヌクレオチド配列もしくはこれに相補的なヌクレオチド配列を有するポリヌクレオチド。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
配列番号1−65のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項2】
配列番号1、2、28、29、30、31、32、51、52、60および61のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項3】
請求項2記載のタンパク質またはそのフラグメントを含む、肺癌を診断または治療する為の組成物。
【請求項4】
配列番号3、4、5、6、7、8、9、10、11、12、13、22、23、24、25、26、27、33、34、35、36、37、38、39、40、41、42、53、54および55のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項5】
請求項4記載のタンパク質またはそのフラグメントを含む、胃癌を診断または治療する為の組成物。
【請求項6】
配列番号3、7、20、21、46、47、48、49および50のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項7】
請求項6記載のタンパク質またはそのフラグメントを含む、大腸癌を診断または治療する為の組成物。
【請求項8】
配列番号14、15、16、17、18、19、43、44、45、56、57、58、59、62、63、64および65のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項9】
請求項8記載のタンパク質またはそのフラグメントを含む、肝癌を診断または治療する為の組成物。
【請求項10】
前記遺伝子が、配列番号1、9、10、14、20、22、24、25、26、27、28、29、32、38、39、40、44、51、52、53、54および58のいずれかに記載されるヌクレオチド配列を有する、請求項1記載のタンパク質またはそのフラグメント。
【請求項11】
前記遺伝子が、配列番号1、9、10、14、20、22、24、25および26のいずれかに記載されるヌクレオチド配列を有する、請求項1記載のタンパク質またはそのフラグメント。
【請求項12】
配列番号66−123のいずれかに記載されるアミノ酸配列を有する、請求項1記載のタンパク質またはそのフラグメント。
【請求項13】
請求項1,2,4,6,8,10,11および12のいずかに記載のタンパク質またはそのフラグメントを認識する抗体。
【請求項14】
配列番号1−65のいずれかに記載されるヌクレオチド配列もしくはこれに相補的なヌクレオチド配列を有するポリヌクレオチド、およびこれらのポリヌクレオチドと高ストリンジェントな条件下でハイブリダイズするポリヌクレオチド。
【請求項15】
配列番号1−65のいずれかに記載されるヌクレオチド配列の少なくとも12個の連続するヌクレオチド配列もしくはこれに相補的なヌクレオチド配列を有するポリヌクレオチド、およびこれらのポリヌクレオチドと高ストリンジェントな条件下でハイブリダイズする少なくとも12個のヌクレオチドを有するポリヌクレオチド。
【請求項16】
配列番号が1、2、28、29、30、31、32、51、52、60および61のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項17】
請求項16記載のポリヌクレオチドを含む、肺癌を診断または治療する為の組成物。
【請求項18】
配列番号が3、4、5、6、7、8、9、10、11、12、13、22、23、24、25、26、27、33、34、35、36、37、38、39、40、41、42、53、54および55のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項19】
請求項18記載のポリヌクレオチドを含む、胃癌を診断または治療する為の組成物。
【請求項20】
配列番号が3、7、20、21、46、47、48、49および50のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項21】
請求項20記載のポリヌクレオチドを含む、大腸癌を診断または治療する為の組成物。
【請求項22】
配列番号が14、15、16、17、18、19、43、44、45、56、57、58、59、62、63、64および65のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項23】
請求項22記載のポリヌクレオチドを含む、肝癌を診断または治療する為の組成物。
【請求項24】
配列番号が1、9、10、14、20、22、24、25、26、27、28、29、32、38、39、40、44、51、52、53、54および58のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項25】
請求項14,15,16,18,20,22および24のいずれかに記載のポリヌクレオチドを含むベクター。
【請求項26】
請求項25記載のベクターを含む細胞。
【請求項27】
抗癌活性を有する化合物を同定する方法であって、
培養ヒト細胞を試験化合物と接触させ、そして
前記細胞において配列番号1−65のいずれかに記載されるヌクレオチド配列を含む遺伝子の発現量の変化を引き起こす化合物を抗癌活性を有する化合物として同定する
の各工程を含む方法。
【請求項28】
請求項1,2,4,6,8,10,11および12のいずかに記載のタンパク質、または請求項14,15,16,18,20,22および24のいずれかに記載のポリヌクレオチドの発現量を測定することを特徴とする癌の診断方法。
【請求項29】
C20orf102タンパク質を検出することを特徴とする癌の診断方法。
【請求項30】
癌が肺癌、肝癌、または膵癌である請求項29記載の診断方法。
【請求項31】
分泌されたC20orf102タンパク質を検出することを特徴とする請求項29記載の診断方法。
【請求項32】
C20orf102タンパク質を認識する抗体を用いることを特徴とする請求項29記載の診断方法。
【請求項33】
血液中、血清中、または血漿中のC20orf102タンパク質を検出することを特徴とする請求項29記載の診断方法。
【請求項34】
以下の工程:
(a) 被験者から試料を採取する工程;
(b) 採取された試料に含まれるC20orf102タンパク質を検出する工程
を含む癌の診断方法。
【請求項35】
被験者から採取される試料が血液、血清、または血漿である請求項34記載の診断方法。
【請求項36】
C20orf102タンパク質細胞外領域を検出することを特徴とする請求項34記載の診断方法。
【請求項37】
C20orf102タンパク質を認識する抗体を用いることを特徴とする請求項34記載の診断方法。
【請求項1】
配列番号1−65のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項2】
配列番号1、2、28、29、30、31、32、51、52、60および61のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項3】
請求項2記載のタンパク質またはそのフラグメントを含む、肺癌を診断または治療する為の組成物。
【請求項4】
配列番号3、4、5、6、7、8、9、10、11、12、13、22、23、24、25、26、27、33、34、35、36、37、38、39、40、41、42、53、54および55のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項5】
請求項4記載のタンパク質またはそのフラグメントを含む、胃癌を診断または治療する為の組成物。
【請求項6】
配列番号3、7、20、21、46、47、48、49および50のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項7】
請求項6記載のタンパク質またはそのフラグメントを含む、大腸癌を診断または治療する為の組成物。
【請求項8】
配列番号14、15、16、17、18、19、43、44、45、56、57、58、59、62、63、64および65のいずれかに記載されるヌクレオチド配列を有する遺伝子によりコードされるタンパク質またはそのフラグメント。
【請求項9】
請求項8記載のタンパク質またはそのフラグメントを含む、肝癌を診断または治療する為の組成物。
【請求項10】
前記遺伝子が、配列番号1、9、10、14、20、22、24、25、26、27、28、29、32、38、39、40、44、51、52、53、54および58のいずれかに記載されるヌクレオチド配列を有する、請求項1記載のタンパク質またはそのフラグメント。
【請求項11】
前記遺伝子が、配列番号1、9、10、14、20、22、24、25および26のいずれかに記載されるヌクレオチド配列を有する、請求項1記載のタンパク質またはそのフラグメント。
【請求項12】
配列番号66−123のいずれかに記載されるアミノ酸配列を有する、請求項1記載のタンパク質またはそのフラグメント。
【請求項13】
請求項1,2,4,6,8,10,11および12のいずかに記載のタンパク質またはそのフラグメントを認識する抗体。
【請求項14】
配列番号1−65のいずれかに記載されるヌクレオチド配列もしくはこれに相補的なヌクレオチド配列を有するポリヌクレオチド、およびこれらのポリヌクレオチドと高ストリンジェントな条件下でハイブリダイズするポリヌクレオチド。
【請求項15】
配列番号1−65のいずれかに記載されるヌクレオチド配列の少なくとも12個の連続するヌクレオチド配列もしくはこれに相補的なヌクレオチド配列を有するポリヌクレオチド、およびこれらのポリヌクレオチドと高ストリンジェントな条件下でハイブリダイズする少なくとも12個のヌクレオチドを有するポリヌクレオチド。
【請求項16】
配列番号が1、2、28、29、30、31、32、51、52、60および61のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項17】
請求項16記載のポリヌクレオチドを含む、肺癌を診断または治療する為の組成物。
【請求項18】
配列番号が3、4、5、6、7、8、9、10、11、12、13、22、23、24、25、26、27、33、34、35、36、37、38、39、40、41、42、53、54および55のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項19】
請求項18記載のポリヌクレオチドを含む、胃癌を診断または治療する為の組成物。
【請求項20】
配列番号が3、7、20、21、46、47、48、49および50のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項21】
請求項20記載のポリヌクレオチドを含む、大腸癌を診断または治療する為の組成物。
【請求項22】
配列番号が14、15、16、17、18、19、43、44、45、56、57、58、59、62、63、64および65のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項23】
請求項22記載のポリヌクレオチドを含む、肝癌を診断または治療する為の組成物。
【請求項24】
配列番号が1、9、10、14、20、22、24、25、26、27、28、29、32、38、39、40、44、51、52、53、54および58のいずれかである、請求項14または15記載のポリヌクレオチド。
【請求項25】
請求項14,15,16,18,20,22および24のいずれかに記載のポリヌクレオチドを含むベクター。
【請求項26】
請求項25記載のベクターを含む細胞。
【請求項27】
抗癌活性を有する化合物を同定する方法であって、
培養ヒト細胞を試験化合物と接触させ、そして
前記細胞において配列番号1−65のいずれかに記載されるヌクレオチド配列を含む遺伝子の発現量の変化を引き起こす化合物を抗癌活性を有する化合物として同定する
の各工程を含む方法。
【請求項28】
請求項1,2,4,6,8,10,11および12のいずかに記載のタンパク質、または請求項14,15,16,18,20,22および24のいずれかに記載のポリヌクレオチドの発現量を測定することを特徴とする癌の診断方法。
【請求項29】
C20orf102タンパク質を検出することを特徴とする癌の診断方法。
【請求項30】
癌が肺癌、肝癌、または膵癌である請求項29記載の診断方法。
【請求項31】
分泌されたC20orf102タンパク質を検出することを特徴とする請求項29記載の診断方法。
【請求項32】
C20orf102タンパク質を認識する抗体を用いることを特徴とする請求項29記載の診断方法。
【請求項33】
血液中、血清中、または血漿中のC20orf102タンパク質を検出することを特徴とする請求項29記載の診断方法。
【請求項34】
以下の工程:
(a) 被験者から試料を採取する工程;
(b) 採取された試料に含まれるC20orf102タンパク質を検出する工程
を含む癌の診断方法。
【請求項35】
被験者から採取される試料が血液、血清、または血漿である請求項34記載の診断方法。
【請求項36】
C20orf102タンパク質細胞外領域を検出することを特徴とする請求項34記載の診断方法。
【請求項37】
C20orf102タンパク質を認識する抗体を用いることを特徴とする請求項34記載の診断方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】


【図46】


【図47】


【図48】


【図49】


【図50】


【図51】


【図52】


【図53】


【図54】


【図55】


【図56】


【図57】


【図58】


【図59】


【図60】


【図61】


【図62】


【図63】


【図64】


【図65】


【図66】


【図67−1】


【図67−2】


【図67−3】


【図67−4】


【図68−1】


【図68−2】


【図68−3】


【図68−4】


【図68−5】


【図69】


【図70−1】


【図70−2】


【図70−3】


【図71−1】


【図71−2】


【図71−3】


【図72】


【図73】


【図74】


【図75】


【図76】


【図77】


【図78】


【図79】


【図80】


【図81】


【図82】


【図83】


【図84】


【図85】


【図86】


【図87】


【図88】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】


【図46】


【図47】


【図48】


【図49】


【図50】


【図51】


【図52】


【図53】


【図54】


【図55】


【図56】


【図57】


【図58】


【図59】


【図60】


【図61】


【図62】


【図63】


【図64】


【図65】


【図66】


【図67−1】


【図67−2】


【図67−3】


【図67−4】


【図68−1】


【図68−2】


【図68−3】


【図68−4】


【図68−5】


【図69】


【図70−1】


【図70−2】


【図70−3】


【図71−1】


【図71−2】


【図71−3】


【図72】


【図73】


【図74】


【図75】


【図76】


【図77】


【図78】


【図79】


【図80】


【図81】


【図82】


【図83】


【図84】


【図85】


【図86】


【図87】


【図88】


【公開番号】特開2011−15681(P2011−15681A)
【公開日】平成23年1月27日(2011.1.27)
【国際特許分類】
【出願番号】特願2010−162552(P2010−162552)
【出願日】平成22年7月20日(2010.7.20)
【分割の表示】特願2005−513023(P2005−513023)の分割
【原出願日】平成16年8月6日(2004.8.6)
【出願人】(503196776)株式会社ペルセウスプロテオミクス (25)
【出願人】(000003311)中外製薬株式会社 (228)
【出願人】(501251758)
【Fターム(参考)】
【公開日】平成23年1月27日(2011.1.27)
【国際特許分類】
【出願日】平成22年7月20日(2010.7.20)
【分割の表示】特願2005−513023(P2005−513023)の分割
【原出願日】平成16年8月6日(2004.8.6)
【出願人】(503196776)株式会社ペルセウスプロテオミクス (25)
【出願人】(000003311)中外製薬株式会社 (228)
【出願人】(501251758)

【Fターム(参考)】
[ Back to top ]

