発電装置
【課題】発生させた水素を燃料電池に供給して、外部からの電力供給なし余剰電力を出力できる発電装置を提供する。
【解決手段】電圧の印加による電気分解反応及び電極11の自己反応の両者で水素を発生させる水素発生手段10と、発生した水素を供給して発電を行う燃料電池20と、その燃料電池20からの電力を利用して、直接的又は間接的に前記水素発生手段10に電圧を印加する電圧印加回路30と、前記燃料電池20で発電した余剰の電力を出力する出力回路40と、を備える。
【解決手段】電圧の印加による電気分解反応及び電極11の自己反応の両者で水素を発生させる水素発生手段10と、発生した水素を供給して発電を行う燃料電池20と、その燃料電池20からの電力を利用して、直接的又は間接的に前記水素発生手段10に電圧を印加する電圧印加回路30と、前記燃料電池20で発電した余剰の電力を出力する出力回路40と、を備える。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、電気分解反応を利用して発生させた水素を、燃料電池に供給して発電を行う発電装置に関し、特に電極の自己反応を伴うことで余剰電力を電力供給なしに出力できる技術として極めて有用である。
【背景技術】
【0002】
この種の発電装置としては、特許文献1の従来技術に記載されているように、水の電気分解反応で水素を発生させる水素発生手段と、発生した水素を貯蔵する貯蔵手段と、貯蔵手段から導入した水素で発電を行う燃料電池とを備えた発電装置が知られていた。
【0003】
この発電装置で使用する水素発生手段は、常法による水の電気分解を行う装置であるため、電気分解の消費電力が、発生した水素を利用した燃料電池による発電電力を超えているので、外部から供給した電力を超える電力を出力することはできなかった。このため、この発電装置では、水素を貯蔵する貯蔵手段を設けて、一旦貯蔵した水素で発電を行う装置構成を採用しており、一旦貯蔵した貯蔵手段からの水素が、水素発生手段による水素発生量より十分多い場合に限り、燃料電池で発電を行いながら、電気分解と外部への出力を行うことができる。
【0004】
このため、特許文献1の発明では、自然エネルギー発電装置から水素発生手段に電力を供給する方法を採用して、外部電力の消費を少なくしている。また、特許文献1の発明では、自然エネルギー発電装置からの電力を充電して、負荷に供給する二次電池を併用することが開示されているが、この二次電池は、発電の初期に前記水素発生手段に電力を供給するものではない。
【0005】
また、特許文献2には、水の電気分解反応で水素を発生させる際に、電解層に通電する電力のデューティ比で水素発生量を制御する方法が開示されている。
【0006】
一方、特許文献3には、アルミニウム等をアノード極とし、アルミニウムをカソード極として、両極を電解質水溶液に浸漬して電気分解を行うことで、水素を発生させる水素製造方法が開示されている。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2003−257443号公報
【特許文献2】特開2004−197211号公報
【特許文献3】特表2008−544084号公報
【発明の概要】
【発明が解決しようとする課題】
【0008】
特許文献3の水素製造方法では、他の金属を電極に使用した場合に比べて、水素発生量が増加することが開示されているものの、発生した水素を燃料電池による発電に使用した場合、電気分解の消費電力と、燃料電池による発電電力との大小関係がどのようになるかは不明であった。
【0009】
そこで、本発明の目的は、発生させた水素を燃料電池に供給して、外部からの電力供給なし余剰電力を出力できる発電装置を提供することにある。
【課題を解決するための手段】
【0010】
本発明者らは、水の電気分解反応を利用して水素を発生させる際に、アルミニウム等をカソード極に使用することで、電極の自己反応が生じて、電気分解の消費電力と水素供給による燃料電池の発電電力との電力収支がプラスになることを見出し、本発明を完成するに至った。
【0011】
即ち、本発明の発電装置は、電圧の印加による電気分解反応及び電極の自己反応の両者で水素を発生させる水素発生手段と、発生した水素を供給して発電を行う燃料電池と、その燃料電池からの電力を利用して、直接的又は間接的に前記水素発生手段に電圧を印加する電圧印加回路と、前記燃料電池で発電した余剰の電力を出力する出力回路と、を備えることを特徴とする。
【0012】
本発明の発電装置によると、電圧の印加による電気分解反応及び電極の自己反応の両者で水素を発生させる水素発生手段を用いることで、電気分解の消費電力と水素供給による燃料電池の発電電力との電力収支をプラスにすることができる。このため、発生した水素を供給して発電を行う燃料電池の電力を利用して、電圧印加回路により水素発生手段に電圧を印加する一方で、余剰の電力を出力回路を経て出力することができる。その結果、発生させた水素を燃料電池に供給して、外部からの電力供給なし余剰電力を出力できる発電装置を提供することができる。
【0013】
上記において、前記水素発生手段に供給される初期の電力が、定常状態における電力と比較して大きくなるように構成されているのが好ましい。ここで、定常状態とは、水素発生手段による消費電力が、最小の状態から最小プラス50%の状態までの状態を指す。
【0014】
この構成によると、電力収支がプラスである定常状態における水素発生手段に供給される電力より、初期に供給される電力が大きくなるため、初期に電極が活性化され易くなり、電極の自己反応が早急に開始することで、トータルの電力収支を高めることができると共に、電力収支がプラスになる時点を早めることができる。
【0015】
また、前記水素発生手段は、少なくともカソード極がアルミニウムを含有するものであることが好ましい。カソード極がアルミニウムを含有することによって、カソード極でも電極の自己反応を生じさせることができ、電力収支をよりプラスにして、より大きな余剰電力を出力できるようになる。
【0016】
また、少なくとも発電の初期に前記水素発生手段に電力を供給する蓄電手段、及び/又は少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段を備えることが好ましい。
【0017】
一旦、燃料電池による発電が生じると、継続的に余剰電力を出力できるので、発電の初期に電力を供給する蓄電手段、及び/又は水素を供給するための水素供給手段を設けることで、初期の発電をスムーズに行うことができる。
【0018】
その際、少なくとも発電の初期に前記水素発生手段に電力を供給し、前記燃料電池から供給された電力を蓄電する蓄電手段と、前記燃料電池から前記蓄電手段に供給する電力を制御する制御手段とを備えることが好ましい。蓄電手段を設ける場合には、燃料電池から供給された電力を蓄電して利用することが好ましいため、燃料電池から前記蓄電手段に供給する電力を制御する制御手段を設けることで、初期に使用する電力を蓄電手段に確保できる。
【0019】
また、少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段と、前記燃料電池から前記水素発生手段に供給する電力及び前記出力回路から出力される電力を制御する制御手段とを備えることが好ましい。このような水素供給手段を設けることで、初期に使用する蓄電手段を不要にすることができるが、その場合、制御手段を設けて、燃料電池から水素発生手段に供給する電力及び出力回路から出力される電力を制御することで、余剰電力を出力する際の電力配分の適正化が図り易くなる。
【0020】
その際、前記制御手段がデューティ比の制御により電力を制御することが好ましい。デューティ比の制御を行うことで、電圧降下等による系全体の不安定化を回避しながら、電力を効率良く供給することができ、余剰電力を出力する際の電力配分の適正化が図り易くなる。
【図面の簡単な説明】
【0021】
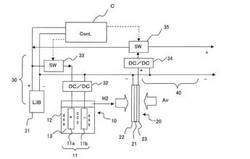
【図1】本発明の発電装置の一例を示すブロック図
【図2】本発明の発電装置の他の例を示すブロック図
【図3】本発明の発電装置の他の例を示すブロック図
【図4】本発明の発電装置の他の例を示すブロック図
【図5】実施例1における結果を示すグラフ
【図6】実施例1〜2及び比較例1における結果を示すグラフ
【図7】実施例3及び比較例2における結果を示すグラフ
【図8】実施例4及び比較例3における結果を示すグラフ
【図9】実施例5及び比較例4における結果を示すグラフ
【図10】実施例3−1、4−1、及び5−1における結果を示すグラフ
【図11】実施例で使用した燃料電池を示す図であり、(a)は上面図、(b)は(a)のI−I矢視断面図、(c)は(a)のII−II矢視断面図、(d)は底面図
【発明を実施するための形態】
【0022】
本発明の発電装置は、図1に示すように、電圧の印加による電気分解反応及び電極11の自己反応の両者で水素を発生させる水素発生手段10と、発生した水素を供給して発電を行う燃料電池20と、その燃料電池20からの電力を利用して、直接的又は間接的に前記水素発生手段10に電圧を印加する電圧印加回路30と、前記燃料電池20で発電した余剰の電力を出力する出力回路40と、を備える。
【0023】
(水素発生手段)
水素発生手段10は、少なくとも2つの電極11を有し、電圧の印加による電気分解反応が可能となっている。本実施形態では、電極11が一対のアノード極11aとカソード極11bとで構成されている例を示すが、更に複数のアノード極11aとカソード極11bが直列及び/又は並列に接続されていてもよい。
【0024】
本発明では、水素発生手段10により、電気分解反応及び電極11の自己反応の両者で水素を発生させるが、電極11の自己反応は、標準電極電位の低い金属(イオン化し易い金属)をアノード極11a及び/又はカソード極11bに用いることで生じさせることができる。標準電極電位の低い金属は、何れの極に使用してもよいが、両極に使用することが、電力収支を大きくする観点から好ましい。なお、従来の水の電気分解は不活性電極を使用するため、電極11の自己反応が生じないことが知られている。
【0025】
本発明では、アノード極11aとカソード極11bが同じ金属でもよく、異なる金属でもよい。標準電極電位の低い金属としては、カリウム、カルシウム、ナトリウム、マグネシウム、アルミニウム、亜鉛、鉄、ニッケル、錫、鉛が挙げられるが、自己反応の生じ易さの観点から、カリウム、カルシウム、ナトリウム、マグネシウム、アルミニウムが好ましく、コストとハンドリング性の観点から、マグネシウム、アルミニウムがより好ましい。
【0026】
これらの金属は、合金や混合金属としても使用することができる。その場合の純度は、90〜100重量%が好ましく、99〜99.9重量%がより好ましい。電極11に含まれる他の元素としては、Al,Mg,Mn,Zn,Cu,Si,Fe,Ti,Cr,V,Bi,Pb,Zr,Bなどが挙げられる。
【0027】
本発明では、特に、マグネシウムを含むアノード極とマグネシウムを含むカソード極との組合せ、又はアルミニウムを含むアノード極とアルミニウムを含むカソード極との組合せが好ましいが、マグネシウムを含むアノード極とアルミニウムを含むカソード極との組合せでも、自己反応を活発に生じさせることができる。
【0028】
本発明では、電極からの電子の授受を伴う電極反応(電気分解反応)と、電子の授受を伴わない電極の自己反応(自発反応)との両者が生じる。電子の授受を伴う電極反応は、印加する電力の消費を伴うため、両電極での水素発生反応を効率良く行うためには、自己反応の比率を高めることが重要になる。これらの反応は、例えば次の通りである。
【0029】
例えば、両極がアルミニウムの場合、アノード極では、
Al+3OH−→Al(OH)3+3e−(水の電気分解)と、
2Al+6H2O→2Al(OH)3+3H2↑(Al活性化による自己反応)
が生じると考えられる。
【0030】
また、カソード極では
2H++2e−→H2↑(水の電気分解)と、
2Al+6H2O→2Al(OH)3+3H2↑(Al活性化による自己反応)
が生じると考えられる。
【0031】
マグネシウムを使用する場合、アノード極では、
Mg+2OH−→Mg(OH)2+2e−(水の電気分解)と、
Mg+2H2O→Mg(OH)2+H2↑(Mg活性化による自己反応)
が生じると考えられる。カソード極に使用する場合は、同様の自己反応と、アルミニウムの場合と同じ水の電気分解反応が生じると考えられる。
【0032】
本実施形態では、説明を簡易にするため、電極11が容器12の電解液13に浸漬されている例を示すが、アノード極11aとカソード極11bとに、多孔質体を接触させて両極間に介在させ、その多孔質体に電解質水溶液を保持させた状態で、両極に電圧を印加することが好ましい。
【0033】
このような水素発生手段10では、電極に多孔質体を接触させて両極間に介在させているため、多孔質体が接触しない場合と比較して、アノード極での反応に伴う酸性度と、カソード極での反応に伴うアルカリ性度とが維持されやすくなり、酸性条件での電極の自己反応(水素発生反応)や、アルカリ性条件での電極の自己反応(水素発生反応)が促進されて、水素発生反応が効率良く生じると考えられる。また、反応で生成する成分(例えば金属水酸化物)が、電極表面に付着せずに多孔質体の空孔内部に取り込まれるため、副生成物による反応阻害を抑制することができ、長時間の水素発生が行えると考えられる。その結果、両電極での水素発生反応を、効率良く長時間生じさせることができる。
【0034】
アルミニウムの自己反応による水素発生は、アルカリ性条件および酸性条件で生じるため、このように酸性度とアルカリ性度とを維持することが、水素発生反応の効率を向上させる。また、マグネシウムの自己反応による水素発生は酸性条件の方が有利であるため、酸性度を維持することが、水素発生反応の効率を向上させる。この観点から、マグネシウムはアノード極に使用するのが好ましい。
アノード極11a及び/又はカソード極11bの形状は、柱状、板状、塊状など何れでも良いが、電極面積を広くする上で、板状のものが好ましい。板状の場合、パンチングメタルのような有孔タイプ、櫛状電極のようなスリットを有するタイプ、メッシュタイプ、不織布状物などでもよい。板状の電極は、平板状の他、板状物を円筒状、四角筒状、スパイラル状、ジグザク状、プリーツ状などに加工したものなどでもよい。
【0035】
アルミニウムを用いる場合の電極の厚みは、十分な水素発生量を確保しつつ金属の反応率を高める観点から、0.03〜5mmが好ましく、0.1〜1mmがより好ましい。マグネシウムを用いる場合の電極の厚みは、同様の観点から、0.3〜10mmが好ましく、0.5〜5mmがより好ましい。一方の電極に不活性な金属を用いる場合など、その他の金属を用いた電極の厚みは0.01〜10mmが好ましく、0.05〜5mmがより好ましい。
【0036】
アノード極11aとカソード極11bとに、多孔質体を接触させて両極間に介在させる場合、多孔質体としては、連通孔を有するものであれば何れでもよく、スポンジ(フォーム)、不織布、織布、紙類、多孔質膜、焼結体、多孔板などが挙げられる。
【0037】
多孔質体の空孔率は、副生成物を取り込む空間を確保しつつ、電極との接触状態を維持する観点から、空孔率が30〜99.9%であることが好ましく、80〜99.5%であることがより好ましい。なお、空孔率(%)は、(1−(多孔質体の密度/材質の密度))×100で計算した値である。
【0038】
多孔質体表面の平均孔径としては、空孔の目詰まりを抑制しつつ、電極との接触状態を確保する観点から、1〜3000μmが好ましく、50〜100μmがより好ましい。平均孔径は、表面の顕微鏡観察により測定し、数平均により求めた値である。
【0039】
多孔質体の材質としては、樹脂、セラミックスなどの絶縁物質や、これらに導電性物質を添加して導電性を向上させたもの、など何れでもよい。但し、電解質水溶液を保持する観点から、親水性の材料が好ましい。樹脂製の多孔質体の場合、弾性変形可能なもの、塑性変形可能なもの、殆ど変形しないものなどが挙げられるが、弾性変形可能なスポンジ状樹脂からなる多孔質体が特に好ましい。
【0040】
多孔質体を構成する樹脂としては、メラミン樹脂、ウレタン樹脂、フェノール樹脂、ポリプロピレン樹脂、ポリエチレン樹脂、ポリエステル樹脂、ポリアミド樹脂、エポキシ樹脂、セルロース系樹脂、などが挙げられる。なかでも、適当な空孔率、孔径、弾性を有する多孔質体が得られ易い観点から、メラミン樹脂、ウレタン樹脂、ポリエステル樹脂、セルロース系樹脂が好ましい。
【0041】
多孔質体の厚み(運転状態)又は電極間の距離は、電解質水溶液を保持しつつ副生成物を取り込む空間を確保する観点から、1〜10mmが好ましく、2〜5mmがより好ましい。多孔質体は、単層であっても複数層であってもよく、複数層の場合、各層の孔径を変えるなど、異なる種類のものを積層してもよい。弾性変形可能な多孔質体を用いる場合、接触性を向上させる観点から、配置する電極間の距離に対して、1〜3倍が好ましく、1.2〜2倍がより好ましい。
【0042】
多孔質体には、電解質水溶液を保持させている。電解質水溶液は、酸性又はアルカリ性でもよいが、両極で酸性度とアルカリ性度とを発現する観点から、中性、例えばpH5〜9が好ましく、pH6〜8がより好ましい。
【0043】
電解質水溶液に含有される電解質としては、アルカリ金属塩、アルカリ土類金属塩、その他の金属塩、アンモニウム塩、ホスホニウム塩など何れでも良いが、取扱い性の観点から、塩化ナトリウム、塩化カリウム、塩化リチウムが好ましい。電解質は2種以上混合することも可能であり、酸性塩や塩基性塩との併用も可能である。また、アルカリ性物質や酸性物質を併用することも可能である。
【0044】
電解質の濃度としては、電気抵抗を適度に調整して、効率よく電極反応を生じさせる観点から、5〜30重量%が好ましく、20〜26重量%がより好ましい。なお、水素発生反応の途中で、水を別途添加したり、電解質を別途添加してもよい。また、多孔質体に予め電解質等を添着(含浸・乾燥)しておき、反応の初期に水等を供給して、多孔質体に電解質水溶液を保持させてもよい。また、完全に溶解しない電解質が存在する状態(飽和状態)で反応を行ってもよい。
【0045】
電解質水溶液は、少なくともその一部が多孔質体に保持されていればよく、残部は容器内に存在してもよい。また、電解質水溶液の全体が多孔質体に保持されるようにしてもよい。電解質水溶液を水素発生反応の途中で別途添加することも可能である。
【0046】
電解質水溶液の量は、できるだけ過不足無く水素発生反応を行う観点から、電極の総重量100重量部に対して、1500〜10000重量部が好ましく、2000〜5000重量部がより好ましい。
【0047】
(燃料電池)
燃料電池20としては、水素を供給して発電を行うものが何れも使用できる。本発明では、装置の小型化・軽量化の観点から、燃料電池20として固体高分子電解質層21とその両側に設けられた電極22、23とを備えるものが好ましい。なお、燃料電池20は、複数の単位セルを備えるものでよく、その場合、単位セル同士は接続部により直列又は並列に電気的に接続される。
【0048】
燃料電池20のアノード側には、水素発生手段10で発生した水素が供給される。その際の経路には、バッファタンクなどを設けてもよいが、直接供給することも可能である。燃料電池20のカソード側には空気などの酸素含有ガスが供給される。
【0049】
単位セルは、例えば、固体高分子電解質層21と、この固体高分子電解質層21の両側に設けられた第1電極層22及び第2電極層23と、これら電極層22,23の更に外側に各々配置された第1導電層及び第2導電層とを有する。本実施形態では、第1導電層及び第2導電層が、第1電極層22及び第2電極層23を部分的に露出させる露出部を有する第1金属層及び第2金属層とからなる例を示す。これらの各層は、インサート成形により樹脂で一体化されていることが好ましい。インサート成形により単位セルを製造する方法は、国際公開WO2009/145090号公報に詳述されている。
【0050】
固体高分子電解質層21としては、従来の固体高分子膜型の燃料電池に用いられるものであれば何れでもよいが、化学的安定性及び導電性の点から、超強酸であるスルホン酸基を有するパーフルオロカーボン重合体からなる陽イオン交換膜が好適に用いられる。このような陽イオン交換膜としては、ナフィオン(登録商標)が好適に用いられる。その他、例えば、ポリテトラフルオロエチレン等のフッ素樹脂からなる多孔質膜に上記ナフィオンや他のイオン伝導性物質を含浸させたものや、ポリエチレンやポリプロピレン等のポリオレフィン樹脂からなる多孔質膜や不織布に上記ナフィオンや他のイオン伝導性物質を担持させたものでもよい。
【0051】
固体高分子電解質層21の厚みは、薄くするほど全体の薄型化に有効であるが、イオン伝導機能、強度、ハンドリング性などを考慮すると、10〜300μmが使用可能であるが、25〜50μmが好ましい。
【0052】
電極層22,23は、固体高分子電解質層21の表面付近でアノード側およびカソード側の電極反応を生じさせるものであれば何れでもよい。なかでも、ガス拡散層としての機能を発揮して、燃料ガス、燃料液、酸化ガス及び水蒸気の供給・排出を行なうと同時に、集電の機能を発揮するものが好適に使用できる。電極層22,23としては、同一又は異なるものが使用でき、その基材には電極触媒作用を有する触媒を担持させることが好ましい。触媒は、固体高分子電解質層21と接する内面側に少なくとも担持させるのが好ましい。
【0053】
電極層22,23の電極基材としては、例えば、カーボンペーパー、カーボン繊維不織布などの繊維質カーボン、導電性高分子繊維の集合体などの電導性多孔質材が使用できる。また、固体高分子電解質層21に触媒を直接付着させたり、カーボンブラックなどの導電性粒子に担持させて固体高分子電解質層21に付着させた電極層22,23を用いることも可能である。
【0054】
一般に、電極層22,23は、このような電導性多孔質材にフッ素樹脂等の撥水性物質を添加して作製されるものであって、触媒を担持させる場合、白金微粒子などの触媒とフッ素樹脂等の撥水性物質とを混合し、これに溶媒を混合して、ペースト状或いはインク状とした後、これを固体高分子電解質膜と対向すべき電極基材の片面に塗布して形成される。
【0055】
一般に、電極層22,23や固体高分子電解質層21は、燃料電池に供給される還元ガスと酸化ガスに応じた設計がなされる。本発明では、酸化ガスとして空気が用いられると共に、還元ガスとして水素ガスを用いる。
【0056】
空気が自然供給される側のカソード側の第2電極層23(本明細書では、アノード側を第1電極層、カソード側を第2電極層と仮定する)では、酸素と水素イオンの反応が生じて水が生成するため、かかる電極反応に応じた設計をするのが好ましい。
【0057】
触媒としては、白金、パラジウム、ルテニウム、ロジウム、銀、ニッケル、鉄、銅、コバルト及びモリブデンから選ばれる少なくとも1種の金属か、又はその酸化物が使用でき、これらの触媒をカーボンブラック等に予め担持させたものも使用できる。
【0058】
電極層22,23の厚みは、薄くするほど全体の薄型化に有効であるが、電極反応、強度、ハンドリング性などを考慮すると、1〜500μmが好ましく、100〜300μmがより好ましい。電極層22,23と固体高分子電解質層21とは、予め接着、融着、又は塗布形成等を行って積層一体化しておいてもよいが、単に積層配置されているだけでもよい。このような積層体は、膜/電極接合体(Membrane Electrode Assembly:MEA)として入手することもでき、これを使用してもよい。
【0059】
アノード側電極層22の表面にはアノード側の第1金属層が配置され、カソード側電極層23の表面にはカソード側の第2金属層が配置される(本明細書では、アノード側を第1金属層、カソード側を第2金属層と仮定する)。第1金属層は、第1電極層22を部分的に露出させる露出部を有するが、本実施形態では、アノード側金属層には燃料ガス等を供給するための開孔が設けられている例を示す。
【0060】
第1金属層の露出部は、アノード側電極層22が露出可能であれば、その個数、形状、大きさ、形成位置などは何れでもよい。アノード側金属層の開孔は、例えば、規則的又はランダムに複数の円孔やスリット等を設けたり、または金属メッシュによって開孔を設けてもよい。開孔部分の面積が締める割合(開孔率)は、電極との接触面積とガスの供給面積のバランスなどの観点から、10〜50%が好ましく、15〜30%がより好ましい。
【0061】
また、カソード側の第2金属層は、第2電極層23を部分的に露出させる露出部を有するが、本実施形態では、カソード側金属層には、空気中の酸素を供給(自然吸気)するための多数の開孔が設けられている例を示す。開孔の形状、大きさ、開孔率等は、アノード側の第1金属層と同様である。
【0062】
金属層としては、電極反応に悪影響がないものであれば何れの金属も使用でき、例えばステンレス板、ニッケル、銅、銅合金などが挙げられる。但し、導電性、コスト、形状付与性、加圧のための強度などの観点から、銅、銅合金、ステンレス板などが好ましい。また、上記の金属に金メッキなどの金属メッキを施したものでもよい。
【0063】
なお、金属層の厚みは、薄くするほど全体の薄型化に有効であるが、導電性、コスト、重量、形状付与性、加圧のための強度などを考慮すると、10〜1000μmが好ましく、50〜200μmがより好ましい。
【0064】
第1金属層及び第2金属層は、少なくとも一部が樹脂から露出することにより、その部分を電極として電気を外部に取り出すことができる。このため、樹脂成形体に対して、第1金属層及び第2金属層を一部露出させた端子部を設けてもよい。金属層及び金属層の形成や開孔の形成は、プレス加工(プレス打ち抜き加工)を利用して行うことができる。
【0065】
以上では、小型の燃料電池として、アノード側とカソード側の両側に、燃料、酸素等を供給するための開口を有する燃料電池の例を示したが、少なくとも一方の側に、燃料等を供給するための流路を設けた単位セルが独立して構成された構成燃料電池、又はセパレータを介在させたスタックタイプの燃料電池などを使用することも可能である。
【0066】
(電圧印加回路)
電圧印加回路30は、燃料電池20からの電力を利用して、直接的又は間接的に水素発生手段10に電圧を印加するものである。本実施形態では、電圧印加回路30が蓄電手段31を介して、間接的に水素発生手段10に電圧を印加する例を示す。
【0067】
アルミニウムを含むアノード極11aと、アルミニウムを含むカソード極11bとに電圧を印加する場合、適度な自己反応率を実現する上で、一対の電極に対して0.1〜5Vで印加するのが好ましく、0.5〜1.5Vで印加するのがより好ましい。マグネシウムを含むアノード極と、マグネシウムを含むカソード極とに電圧を印加する場合、適度な自己反応率を実現する上で、一対の電極に対して0.3〜5Vで印加するのが好ましく、1〜3Vで印加するのがより好ましい。マグネシウムを含むアノード極と、アルミニウムを含むカソード極とに電圧を印加する場合、適度な自己反応率を実現する上で、一対の電極に対して0〜2Vで印加するのが好ましく、0〜0.5Vで印加するのがより好ましい。
【0068】
上記印加を行う際の電流は、上記電圧値と系の抵抗とによって決まるが、系の抵抗は、電極面積、電解質濃度、電極間距離、電極の数、多孔質体の空孔率などにより変化する。電圧の印加の際には、定電圧による印加の他、一定電流への電圧制御、一定水素発生量への電圧制御、あるいはこれらに対応する電流制御などを行っても良い。本発明では、水素発生の効率が高く、発生した水素を燃料電池に供給する場合の発電電力が、電気分解の消費電力を超えること、即ち電力収支をプラスにすることが可能となる。このため、発生した水素を供給した燃料電池により、電圧の印加を行うことができる。
【0069】
水素発生手段10に電圧を印加する回路には、電圧を昇圧又は降圧させるために、必要に応じてDC/DCコンバータ32を設けてもよい。蓄電手段31の出力電圧と、水素発生手段10で要求される電位が、同程度であれば、DC/DCコンバータ32は必要ないが、両者に電圧差がある場合には、これに応じた電圧変化がなされる。例えば、リチウムイオン二次電池を蓄電手段31として使用する場合、出力電圧は4V前後であるため、DC/DCコンバータ32などを用いて降圧を行うのが好ましい。
【0070】
蓄電手段31から水素発生手段10に印加する電圧は、制御手段Cにより制御するのが好ましいが、制御の方法としては、スイッチング素子33を用いて、デューティー比で電力供給量を制御する方法やオンオフ制御を行う方法の他、DC/DCコンバータ32に対して制御信号を送ることで、DC/DCコンバータ32からの出力電圧を制御する方法でもよい。
【0071】
本実施形態では、燃料電池20から蓄電手段31に電力を供給する回路にも、DC/DCコンバータ34を設けられているが、これは燃料電池20からの出力電圧を、蓄電手段31を充電するための電圧に調整するために設けている。本実施形態では、燃料電池20から出力回路40を経て出力される電力が、DC/DCコンバータ34を介して出力されるため、蓄電手段31の充電電圧とほぼ同じ電位になる。
【0072】
燃料電池20から蓄電手段31に電力を供給する回路には、制御手段Cにより制御されるスイッチング素子35などが設けられ、蓄電手段31に供給する電力と、出力回路40を経て出力する電力とを、制御手段Cにより配分することができる。制御手段Cによる配分は、デューティー比で制御する方法の他、配分される電流を検出して両者の電流の比で、電力の配分を行うようにしてもよい。この制御手段Cによりスイッチング素子35などを制御して、燃料電池20から蓄電手段31に供給する電力を制御することができる。
【0073】
デューティー比でスイッチング素子35を制御する場合、スイッチング素子33と同期させることで、スイッチング素子35により蓄電手段31を充電するタイミングを避けて、スイッチング素子33で水素発生手段10に電圧を印加するタイミングを制御してもよい。
【0074】
なお、デューティー比で制御する場合、スイッチング素子35と蓄電手段31との間、又はスイッチング素子35の出力回路40側には、直流化のための整流回路や平滑化回路を設けてもよい。
【0075】
本実施形態では、少なくとも発電の初期に水素発生手段10に電力を供給する蓄電手段31を備える例を示すが、少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段を備えていてもよい(図3参照)。
【0076】
蓄電手段31は、発電の初期に水素発生手段10に電力を供給するためにも使用することができる。図示した例では、発電の初期には、蓄電手段31以外に電力の供給源が特に存在しない。このため、発電の初期に、スイッチング素子33がオンになる状態で、蓄電手段31から水素発生手段10に電力を供給することが好ましい。
【0077】
本発明では、水素発生手段10に供給される初期の電力が、定常状態における電力と比較して大きくなるように構成されているのが好ましい。ここで、定常状態とは、水素発生手段による消費電力が、最小の状態から最小プラス50%の状態までの状態を指すが、初期に供給する最大電力が、定常状態における最小電力の1.1〜50倍が好ましく、2〜20倍がより好ましく、4〜10倍が好ましい。
【0078】
初期の電力又は電力量を大きくする方法としては、蓄電手段31からの電圧を変換するDC/DCコンバータ32の設定電圧を高くする制御、スイッチング素子33のデューティー比を高くする制御などが挙げられる。また、タイマ制御により設定電圧を変える制御、プログラムにより設定電圧を変える制御、電流等を検出してフィードバック制御で設定値に調節する際に設定値を変える制御などにより、上記制御を行うことが可能である。
【0079】
制御手段Cは、蓄電手段31から電源を取っているが、燃料電池20からこれを行うことも可能である。燃料電池20から電源を取る場合、燃料電池20とDC/DCコンバータ34との間に電気的に接続することが好ましい。
【0080】
制御手段Cとしては、汎用のマイクロプロセッサ又は専用のマイクロコントローラを用いることができる。一般にマイクロコントローラは、メモリと用途に応じたI/Oを内蔵しているが、汎用マイクロプロセッサの場合、それらの機能を有する周辺チップを追加して用いることができる。
【0081】
マイクロコントローラは、一般にクロックジェネレータ付きのCPU、プログラムを格納するためのメモリ、ウォッチドッグタイマー等のタイマー、外部周辺機器などと通信するための入出力部を有しており、これらが一つの集積回路に組み込まれているものもある(ワンチップマイコン)。
【0082】
マイクロコントローラを動作できるようにするには、ソフトウェアをROMに格納して、クロック制御による演算を行えばよい。マイクロコントローラは様々な入出力デバイスを内蔵しており、アナログ-デジタル変換回路、汎用非同期シリアル通信などである。
【0083】
マイクロコントローラを用いて、デューティー比の制御を行う場合、例えばカウンタを利用したPWM(Pulse Width Modulation)モードのプログラムを用いればよい。また、電流値又は電圧値などをフィードバック制御する場合、例えば、検出値と設定値とを比較して、制御信号をオンオフしたり、偏差に基づいて制御信号を演算するプログラムを用いればよい。
【0084】
ここで、PWM方式は、周期を一定としてパルス幅の割合を可変することにより、通電する時間の平均のエネルギーを可変制御する方式であるが、電圧そのものを変えてエネルギーを可変するPAM方式(Pulse Amplitude Modulation) を採用したり、両者を併用することも可能である。このようなPWM/PAM複合制御を行う場合、例えば、電力が低い領域では、電圧変換効率の問題により、一定以下に電圧が下げられないため、パルスモードを使用し、電力が必要な領域では、降圧型コンバータを制御し、デューティ100%で電圧値そのものを可変させて、電力を制御することができる。
【0085】
(出力回路)
出力回路40は、燃料電池20で発電した余剰の電力を出力するものである。本実施形態では、燃料電池20から蓄電手段31に電力を供給する回路のDC/DCコンバータ34が、出力回路40のDC/DCコンバータと兼用されているが、別のDC/DCコンバータを設けても良い。その場合、スイッチング素子35の両側にDC/DCコンバータを設けてもよい。これにより、充電側の電圧と出力側の電圧とを変えることが出来る。
【0086】
本発明において「余剰の電力を出力する」とは、トータルとしての余剰分を出力すると言う意味であり、常時、余剰分を出力すると言う意味ではない。例えば、ある期間は、燃料電池20からの出力を全て出力回路40を経て必要な負荷に出力し、負荷のない時に、出力を止めて全ての電力を蓄電手段31に充電しながら、蓄電手段31から水素発生手段10に電力を供給してもよい。
【0087】
出力回路40には、蓄電手段31とは別の蓄電手段を設けてもよく、この蓄電手段の充放電を行いながら系外に出力することができる。また、別の蓄電手段を設けずに、蓄電手段31を充電しながら、蓄電手段31から系外に電力を出力できるように構成してもよい。
【0088】
また、図2に示す他の実施形態のように、出力回路40に対し、蓄電手段31からの出力をスイッチング素子41などを介して電気的に接続してもよい。その場合、例えば燃料電池20からの出力回路40に、電流センサ42などを設けて、電流の変化勾配に基づいて、スイッチング素子41を制御することができる。スイッチング素子41としては、オンオフだけでなく、電流制御を行えるものでもよい。
【0089】
(他の実施形態1)
本発明の発電装置は、図3に示すように、少なくとも発電の初期に燃料電池20に水素を供給するための水素供給手段50を備えていてもよい。水素供給手段50としては、水素貯蔵合金などを用いた水素タンク、水素化金属などの水素発生剤を用いたもの、電極反応を利用したものなど、何れでもよい。図示した実施形態では、電極反応を利用した水素供給手段50の例を示す。
【0090】
この水素供給手段50は、電極51間をスイッチング素子55などで導通させるだけで、電極反応により水素を発生させることができる。その際、導通回路54に抵抗を設けたり、スイッチング素子55などで電流を調整するなどにより、水素発生量を制御することができ。
【0091】
水素供給手段50に用いる電極51としては、アノード極51aが水素より標準電極電位の低い金属であり、カソード極11bがそれより標準電極電位の高い金属であれば、いずれも使用することができる。但し、水素発生の純度と量、コスト、及びハンドリング性の観点より、マグネシウムとアルミニウム、マグネシウムとニッケル、マグネシウムと亜鉛、マグネシウムと鉄、マグネシウムとスズ、マグネシウムとSUS、マグネシウムと銅、マグネシウムとカーボンの組合せが好ましい。その他の構成、即ち、電解液53、容器52、多孔質体などは、前述した水素発生手段10と同様のものが使用可能である。
【0092】
水素供給手段50は、発電の開始時点で、手動によりスイッチオンするのが好ましい。これにより発生した水素は、燃料電池20のアノード側に供給され、発電が開始する。この実施形態では、蓄電手段31を有しないため、電圧印加回路30により、燃料電池20からの電力を利用して、直接的に水素発生手段10に電圧を印加する。電圧の印加により、水素発生手段10は水素を発生し、これが燃料電池20に供給され、二系統からの水素供給により発電が行われる。
【0093】
電圧印加回路30には、先の実施形態と同様に、燃料電池20からの電力を配分するスイッチング素子35と、DC/DCコンバータ32とが設けられている。電圧印加回路30を経て、水素発生手段10に供給できる電力が十分(例えば電力収支がプラス)になると、スイッチング素子55をオフすることで、水素供給手段50からの水素供給を停止することができる。また、水素供給手段50を使い切りにして、スイッチング素子55をオフする制御を省略することも可能である。
【0094】
出力回路40は、スイッチング素子35の負荷側にDC/DCコンバータ34が設けられている他は、先の実施形態と同様である。制御手段Cは、燃料電池20から電源を取っており、燃料電池20とスイッチング素子35との間に電気的に接続することが好ましい。
【0095】
(他の実施形態2)
図4に示す実施形態は、他の実施形態1において、水素供給手段50で発生する水素を利用するだけでなく、水素供給手段50で発生する電力を利用して、発電の初期に水素発生手段10に電圧を印加するものである。つまり、この実施形態では、少なくとも発電の初期に水素発生手段10に電力を供給する蓄電手段を、少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段50が兼用している。
【0096】
この実施形態では、電圧印加回路30を経て、水素発生手段10に供給できる電力が十分(例えば電力収支がプラス)になると、スイッチング素子55をオフすることが好ましい。また、逆電流を防止するために、導通回路54に整流素子を用いるのが好ましい。
【0097】
(他の実施形態3)
他の実施形態1では、燃料電池20から水素発生手段10に電力を供給する際に、DC/DCコンバータ32を設ける例を示したが、これを設けずに電力を供給することも可能である。その場合、燃料電池20の出力電圧と、水素発生手段10の印加電圧とを近づけることが好ましい。例えば、単位セルの直列接続の数を少なくすることで燃料電池20の出力電圧を下げることができ、その場合、電極面積を増加させたり、又は並列接続の数を増加させることで、電力を維持することができる。また、水素発生手段10の両電極11a,11bを直列に接続して、両端の電極間に印加することで、印加電圧水素発生手段10の印加電圧を低下させることができる。
【実施例】
【0098】
以下、本発明の構成と効果を具体的に示す実施例等について説明する。
【0099】
燃料電池の製造例1
厚み0.2mmのニッケル板を金メッキしたものを、図11に示す形状(矩形状部の長径33mm、短径12mm、)にプレスして打ち抜き、金属層4(開口率14%)と金属層5(開口率31%)となるニッケル板を2枚作製した。金属層4,5の突出部4b,5bは、電極端子となる。また、金属層4,5の開口部は、樹脂成形後に、電極層2,3の表面を部分的に露出させる露出部4a(開口率7%)と露出部5a(開口率22%)となる。
【0100】
固体高分子電解質層1(陽イオン交換膜)としてナフィオンフィルム(デュポン社製ナフィオン112、33mm×12mm、厚み15μm)を用いた。この固体高分子電解質層1の両面の周縁部に、図11に示すように補強層8としてPEN樹脂(ポリエチレンナフタレート)を幅500μm、厚み40μmで設けた。
【0101】
また、固体高分子電解質層1の両面の中央部には、図11に示すように、触媒層9を補強層8とほぼ同じ厚みで設けた。白金触媒は、米国エレクトロケム社製20%白金担持カーボン触媒(EC−20−PTC)を用いた。この白金触媒と、カーボンブラック(アクゾ社ケッチェンブラックEC)、ポリフッ化ビニリデン(カイナー)を、それぞれ75重量%、15重量%、10重量%の割合で混合し、ジメチルホルムアミドを、2.5重量%のポリフッ化ビニリデン溶液となるような割合で、上記白金触媒、カーボンブラック、ポリフッ化ビニリデンの混合物中に加え、乳鉢中で溶解・混合して、触媒ペーストを作製し、固体高分子電解質層1の表面に塗布した。電極層2,3としては、カーボンペーパー(東レ製TGP−H−90、厚み370μm)を33mm×12mmに切断して用いた。
【0102】
固体高分子電解質層1、触媒層9、補強層8、電極層2,3の積層物を、上記のニッケル板2枚の中央で挟み込み、樹脂の開口形状に対応する凸部を内表面に有する金型を用いて、2枚のニッケル板の両側から圧力(1トン)がかかる状態で、金型内に配置した。その状態で、樹脂((株)プライムポリマー製、ポリプロピレン樹脂、J−700GP)を195℃で型内に注入して(射出圧力400kgf/cm2)、冷却した後に金型から取り出すことで、樹脂成形体の外寸35mm×14mm×2.2mm厚の単位セルを作成した。この単位セルでは、アノード側の電極層2と樹脂成形体6の樹脂が接触する接触部6aが、カソード側に比べて多くなっている。
【0103】
この単位セルの4つを用いて、アノード側を内側にして四角柱の四つの側面を形成し、これらの突出部4b,5bを電気的に直列に接続して、内側に水素供給空間を有し、外側から空気供給が可能な四角柱の燃料電池を得た。
【0104】
実施例1
電極となるアルミニウム板(純度99.5%、縦35×横50×厚み0.3mm、1.44g)を2枚用意し、2枚の間に多孔質体(BASF社製、メラミンフォーム、縦35×横50×厚み5mm、密度0.0093g/cm3、空孔率99.4%、平均孔径70μm)を挟み、電極間の距離が5mmになるような平型ケース(約8mL)に入れて、20重量%NaCl水溶液を約8mL注入した。ケースの上部空間を閉空間とし、発生した水素ガスを排出する流路に、膜式流量計(堀場製作所社製)を接続して、常時、水素発生流量をモニターした。各々の電極を安定化電源に正極および負極として接続し、水素発生流量が約10mL/minになるように、手動で電源の電流値を変化させながら1時間運転を行った。その際の水素発生量を図5(a)に、電圧と電流の関係を図5(b)、これらから計算される発生電力と消費電力を図5(c)に示す。
【0105】
発生電力については、製造例1の燃料電池を用いて、水素流量10mL/minで発電を行った場合、燃料電池の出力電圧が約3V(4セル分)、電流が約0.33Aであり、これをDC/DCコンバーター(電力効率85%)で、約5Vまで昇圧すると、発生電力が約0.83Wであったため、これを基準に発生電力を計算した。
【0106】
図5(c)に示す結果から、電極の自己反応により、消費電力以上の発電が可能(1.14〜5.2倍)なことが分かった。電圧印加により、電極のアルミが活性化され、電気分解以外の自己反応により水素発生が生じていると考えられる。なお、消費電力0.5W以下の持続時間は約90minであった。
【0107】
実施例2
実施例1において、使用した多孔質体を下記の多孔質体に代える以外は、実施例1と全く同じ条件で水素発生流量が約10mL/minになるように、手動で電源の電流値を変化させながら1時間運転を行った。その際の電圧と電流から計算される消費電力を、実施例1の結果と併せて図6に示す。
(実施例2−1)ソフラス(ポリウレタン、0.22g/cm3、空孔率82%、平均孔径1μm)5mm厚み
(実施例2−2)ポリウレタン(食器洗いスポンジ0.028g/cm3、空孔率98%、平均孔径2000μm)5mm厚み
(実施例2−3)蒸発紙(ポリエステル樹脂、0.26g/cm3、空孔率78%、平均孔径50μm)1mm厚み×5枚
(実施例2−4)ベルイーター(ポリビニルアルコールスポンジ、0.089g/cm3、空孔率95%、平均孔径70μm)1.8mm厚み×2枚。
【0108】
比較例1
実施例1において、多孔質体を使用せずに、同量のNaCl水溶液のみが電極間に存在するようにした以外は、実施例1と全く同じ条件で水素発生流量が約10mL/minになるように、手動で電源の電流値を変化させながら1時間運転を行った。その際の電圧と電流から計算される消費電力を、図6に併せて示す。その結果、多孔質体を用いない場合には、初期に消費電力が非常に大きくなり、電力収支がマイナスになる部分(消費電力0.8W以上)が生じた。
【0109】
実施例3−1
電極となるアルミニウム板(純度99.5%、縦35×横20×厚み0.3mm、0.57g)を2枚用意し、2枚の間と両外側とに多孔質体(BASF社製、メラミンフォーム、縦35×横50×厚み5mm、密度0.0093g/cm3、空孔率99.4%)を1枚ずつ配置し、これを容器(深さ35×横50×幅15mm、容積約27mL)に入れて、20重量%NaCl水溶液を約15mL注入した。容器の上部空間を閉空間とし、発生した水素ガスを排出する流路に、膜式流量計(堀場製作所社製)を接続して測定した。各々の電極を安定化電源に正極および負極として接続し、電源の電流値を0.5Aに制御して2時間運転を行った。その際の消費電力を図7(a)に、消費電力量を図7(b)、利用可能電力を図7(c)に、利用可能電力量を図7(d)に示す。
【0110】
実施例3−2
実施例3−1において、使用した多孔質体の厚みを10mmに代える以外は、実施例3−1と全く同じ条件で2時間運転を行った。その際の消費電力を図7(a)に、消費電力量を図7(b)、利用可能電力を図7(c)に、利用可能電力量を図7(d)に併せて示す。
【0111】
比較例2
実施例3−1において、使用した3枚の多孔質体の厚みを3mmに代え、多孔質体と電極との間に厚さ1mmのシリコーンゴムよりなる枠状スペーサ(電極とは上端と下端とでのみ幅2mmで接する)を介在させて、電極と多孔質体との距離を1mmにしたこと以外は、実施例3−1と全く同じ条件で2時間運転を行った。その際の消費電力を図7(a)に、消費電力量を図7(b)、利用可能電力を図7(c)に、利用可能電力量を図7(d)に併せて示す。
【0112】
実施例3−1、3−2と比較例2の結果を対比すると、アルミ電極とスポンジの接触が良いほど、反応効率は向上し、特に非接触の場合は反応が鈍化し、消費電力が跳ね上がっていることが分かった。
【0113】
実施例4−1
電極となるマグネシウム板(AZ31,純度96%、縦35×横20×厚み0.3mm、0.36g)を2枚用意し、2枚の間と両外側とに多孔質体(BASF社製、メラミンフォーム、縦35×横50×厚み5mm、密度0.0093g/cm3、空孔率99.4%)を1枚ずつ配置し、これを容器(深さ35×横50×幅15mm、容積約27mL)に入れて、20重量%NaCl水溶液を約15mL注入した。容器の上部空間を閉空間とし、発生した水素ガスを排出する流路に、膜式流量計(堀場製作所社製)を接続して測定した。各々の電極を安定化電源に正極および負極として接続し、電源の電流値を0.5Aに制御して1時間運転を行った。その際の消費電力を図8(a)に、消費電力量を図8(b)、利用可能電力を図8(c)に、利用可能電力量を図8(d)に示す。
【0114】
実施例4−2
実施例4−1において、使用した多孔質体の厚みを10mmに代える以外は、実施例4−1と全く同じ条件で1時間運転を行った。その際の消費電力を図8(a)に、消費電力量を図8(b)、利用可能電力を図8(c)に、利用可能電力量を図8(d)に併せて示す。
【0115】
比較例3
実施例4−1において、使用した3枚の多孔質体の厚みを3mmに代え、多孔質体と電極との間に厚さ1mmのシリコーンゴムよりなる枠状スペーサ(電極とは上端と下端とでのみ幅2mmで接する)を介在させて、電極と多孔質体との距離を1mmにしたこと以外は、実施例4−1と全く同じ条件で1時間運転を行った。その際の消費電力を図8(a)に、消費電力量を図8(b)、利用可能電力を図8(c)に、利用可能電力量を図8(d)に併せて示す。
【0116】
実施例4−1、4−2と比較例3の結果を対比すると、非接触の場合は反応が鈍化し、消費電力が大きくなることが分かった。マグネシウム電極とスポンジの接触が弱いほど、反応効率は向上しており、これは接触が強いほど、マグネシウムの副生成物(酸化物、水酸化物)による堆積を許容しにくくなるためであると考えられる。
【0117】
実施例5−1
アノード極となるマグネシウム板(純度96%、縦35×横20×厚み0.3mm、0.36g)と、カソード極となるアルミニウム板(純度99.5%、縦35×横20×厚み0.3mm、0.57g)とを用意し、2枚の間と両外側とに多孔質体(BASF社製、メラミンフォーム、縦35×横50×厚み5mm、密度0.0093g/cm3、空孔率99.4%)を1枚ずつ配置し、これを容器(深さ35×横50×幅15mm、容積約27mL)に入れて、20重量%NaCl水溶液を約15mL注入した。容器の上部空間を閉空間とし、発生した水素ガスを排出する流路に、膜式流量計(堀場製作所社製)を接続して測定した。各々の電極を銅板(幅10mm、厚み0.5mm、抵抗5〜8mΩ)で導通させ、水素発生流量が約6mL/min以下になるまで運転を行った。その際の利用可能電力を図9(a)に、利用可能電力量を図9(b)に示す。
【0118】
この系を利用することで、初期に水素を供給する水素供給手段、及び/又は初期に電力を供給する蓄電手段として、利用することができる。
【0119】
実施例5−2
実施例5−1において、使用した多孔質体の厚みを10mmに代える以外は、実施例5−1と全く同じ条件で1時間運転を行った。その際の利用可能電力を図9(a)に、利用可能電力量を図9(b)に併せて示す。
【0120】
比較例4
実施例5−1において、使用した3枚の多孔質体の厚みを3mmに代え、多孔質体と電極との間に厚さ1mmのシリコーンゴムよりなる枠状スペーサ(電極とは上端と下端とでのみ幅2mmで接する)を介在させて、電極と多孔質体との距離を1mmにしたこと以外は、実施例5−1と全く同じ条件で1時間運転を行った。その際の利用可能電力を図9(a)に、利用可能電力量を図9(b)に併せて示す。
【0121】
実施例5−1、5−2と比較例4の結果を対比すると、水素発生反応の効率はほとんど変わらないものの、非接触の場合は副生成物による反応阻害が早く生じるため、利用可能電力量はより小さくなった。
【0122】
(自己反応率の対比)
実施例3−1、4−1、及び5−1の結果から、次のようにして自己反応率を計算した。即ち、電流から求めた、「移動した電子量」から電気分解反応で発生した水素量を算出し、これを実際の水素発生量から差し引き、各々の電極で自己反応と、電気分解反応の比率を求めた。
【数1】

その結果を図10(a)に示す。また、計算に使用した電流値と電圧値のデータを、それぞれ図10(b)と図10(c)とに示す。図10の結果から、Al−Mg、Al−Al、Mg−Mgの順序で、自己反応の比率が高いことが分かった。
【0123】
実施例6
実施例1で用いた水素発生手段等の装置を用いて、安定化電源から電力供給を開始し、製造例1の燃料電池に水素供給して発電(出力電圧約3V)を行った。開始から10分後(水素発生量約10mL/min)に電力供給を停止し、燃料電池の出力電圧を0.7VまでDC/DCコンバーター(電力効率85%)で降圧して水素発生手段の正極および負極に印加しつつ、DC/DCコンバーター(電力効率85%、出力電圧5V)を介して、一定電流(0.12A)に設定した外部負荷(菊水電子工業株式会社製、PLZ70UA)による電力利用を試みた。その結果、水素流量をほぼ一定に保ちながら、外部負荷に対して電力を90分間にわたり出力(電力量0.9Wh、平均電力約0.6W)することができた。
【符号の説明】
【0124】
10 水素発生手段
11 電極
20 燃料電池
30 電圧印加回路
31 蓄電手段
40 出力回路
50 水素供給手段
C 制御手段
【技術分野】
【0001】
本発明は、電気分解反応を利用して発生させた水素を、燃料電池に供給して発電を行う発電装置に関し、特に電極の自己反応を伴うことで余剰電力を電力供給なしに出力できる技術として極めて有用である。
【背景技術】
【0002】
この種の発電装置としては、特許文献1の従来技術に記載されているように、水の電気分解反応で水素を発生させる水素発生手段と、発生した水素を貯蔵する貯蔵手段と、貯蔵手段から導入した水素で発電を行う燃料電池とを備えた発電装置が知られていた。
【0003】
この発電装置で使用する水素発生手段は、常法による水の電気分解を行う装置であるため、電気分解の消費電力が、発生した水素を利用した燃料電池による発電電力を超えているので、外部から供給した電力を超える電力を出力することはできなかった。このため、この発電装置では、水素を貯蔵する貯蔵手段を設けて、一旦貯蔵した水素で発電を行う装置構成を採用しており、一旦貯蔵した貯蔵手段からの水素が、水素発生手段による水素発生量より十分多い場合に限り、燃料電池で発電を行いながら、電気分解と外部への出力を行うことができる。
【0004】
このため、特許文献1の発明では、自然エネルギー発電装置から水素発生手段に電力を供給する方法を採用して、外部電力の消費を少なくしている。また、特許文献1の発明では、自然エネルギー発電装置からの電力を充電して、負荷に供給する二次電池を併用することが開示されているが、この二次電池は、発電の初期に前記水素発生手段に電力を供給するものではない。
【0005】
また、特許文献2には、水の電気分解反応で水素を発生させる際に、電解層に通電する電力のデューティ比で水素発生量を制御する方法が開示されている。
【0006】
一方、特許文献3には、アルミニウム等をアノード極とし、アルミニウムをカソード極として、両極を電解質水溶液に浸漬して電気分解を行うことで、水素を発生させる水素製造方法が開示されている。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2003−257443号公報
【特許文献2】特開2004−197211号公報
【特許文献3】特表2008−544084号公報
【発明の概要】
【発明が解決しようとする課題】
【0008】
特許文献3の水素製造方法では、他の金属を電極に使用した場合に比べて、水素発生量が増加することが開示されているものの、発生した水素を燃料電池による発電に使用した場合、電気分解の消費電力と、燃料電池による発電電力との大小関係がどのようになるかは不明であった。
【0009】
そこで、本発明の目的は、発生させた水素を燃料電池に供給して、外部からの電力供給なし余剰電力を出力できる発電装置を提供することにある。
【課題を解決するための手段】
【0010】
本発明者らは、水の電気分解反応を利用して水素を発生させる際に、アルミニウム等をカソード極に使用することで、電極の自己反応が生じて、電気分解の消費電力と水素供給による燃料電池の発電電力との電力収支がプラスになることを見出し、本発明を完成するに至った。
【0011】
即ち、本発明の発電装置は、電圧の印加による電気分解反応及び電極の自己反応の両者で水素を発生させる水素発生手段と、発生した水素を供給して発電を行う燃料電池と、その燃料電池からの電力を利用して、直接的又は間接的に前記水素発生手段に電圧を印加する電圧印加回路と、前記燃料電池で発電した余剰の電力を出力する出力回路と、を備えることを特徴とする。
【0012】
本発明の発電装置によると、電圧の印加による電気分解反応及び電極の自己反応の両者で水素を発生させる水素発生手段を用いることで、電気分解の消費電力と水素供給による燃料電池の発電電力との電力収支をプラスにすることができる。このため、発生した水素を供給して発電を行う燃料電池の電力を利用して、電圧印加回路により水素発生手段に電圧を印加する一方で、余剰の電力を出力回路を経て出力することができる。その結果、発生させた水素を燃料電池に供給して、外部からの電力供給なし余剰電力を出力できる発電装置を提供することができる。
【0013】
上記において、前記水素発生手段に供給される初期の電力が、定常状態における電力と比較して大きくなるように構成されているのが好ましい。ここで、定常状態とは、水素発生手段による消費電力が、最小の状態から最小プラス50%の状態までの状態を指す。
【0014】
この構成によると、電力収支がプラスである定常状態における水素発生手段に供給される電力より、初期に供給される電力が大きくなるため、初期に電極が活性化され易くなり、電極の自己反応が早急に開始することで、トータルの電力収支を高めることができると共に、電力収支がプラスになる時点を早めることができる。
【0015】
また、前記水素発生手段は、少なくともカソード極がアルミニウムを含有するものであることが好ましい。カソード極がアルミニウムを含有することによって、カソード極でも電極の自己反応を生じさせることができ、電力収支をよりプラスにして、より大きな余剰電力を出力できるようになる。
【0016】
また、少なくとも発電の初期に前記水素発生手段に電力を供給する蓄電手段、及び/又は少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段を備えることが好ましい。
【0017】
一旦、燃料電池による発電が生じると、継続的に余剰電力を出力できるので、発電の初期に電力を供給する蓄電手段、及び/又は水素を供給するための水素供給手段を設けることで、初期の発電をスムーズに行うことができる。
【0018】
その際、少なくとも発電の初期に前記水素発生手段に電力を供給し、前記燃料電池から供給された電力を蓄電する蓄電手段と、前記燃料電池から前記蓄電手段に供給する電力を制御する制御手段とを備えることが好ましい。蓄電手段を設ける場合には、燃料電池から供給された電力を蓄電して利用することが好ましいため、燃料電池から前記蓄電手段に供給する電力を制御する制御手段を設けることで、初期に使用する電力を蓄電手段に確保できる。
【0019】
また、少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段と、前記燃料電池から前記水素発生手段に供給する電力及び前記出力回路から出力される電力を制御する制御手段とを備えることが好ましい。このような水素供給手段を設けることで、初期に使用する蓄電手段を不要にすることができるが、その場合、制御手段を設けて、燃料電池から水素発生手段に供給する電力及び出力回路から出力される電力を制御することで、余剰電力を出力する際の電力配分の適正化が図り易くなる。
【0020】
その際、前記制御手段がデューティ比の制御により電力を制御することが好ましい。デューティ比の制御を行うことで、電圧降下等による系全体の不安定化を回避しながら、電力を効率良く供給することができ、余剰電力を出力する際の電力配分の適正化が図り易くなる。
【図面の簡単な説明】
【0021】
【図1】本発明の発電装置の一例を示すブロック図
【図2】本発明の発電装置の他の例を示すブロック図
【図3】本発明の発電装置の他の例を示すブロック図
【図4】本発明の発電装置の他の例を示すブロック図
【図5】実施例1における結果を示すグラフ
【図6】実施例1〜2及び比較例1における結果を示すグラフ
【図7】実施例3及び比較例2における結果を示すグラフ
【図8】実施例4及び比較例3における結果を示すグラフ
【図9】実施例5及び比較例4における結果を示すグラフ
【図10】実施例3−1、4−1、及び5−1における結果を示すグラフ
【図11】実施例で使用した燃料電池を示す図であり、(a)は上面図、(b)は(a)のI−I矢視断面図、(c)は(a)のII−II矢視断面図、(d)は底面図
【発明を実施するための形態】
【0022】
本発明の発電装置は、図1に示すように、電圧の印加による電気分解反応及び電極11の自己反応の両者で水素を発生させる水素発生手段10と、発生した水素を供給して発電を行う燃料電池20と、その燃料電池20からの電力を利用して、直接的又は間接的に前記水素発生手段10に電圧を印加する電圧印加回路30と、前記燃料電池20で発電した余剰の電力を出力する出力回路40と、を備える。
【0023】
(水素発生手段)
水素発生手段10は、少なくとも2つの電極11を有し、電圧の印加による電気分解反応が可能となっている。本実施形態では、電極11が一対のアノード極11aとカソード極11bとで構成されている例を示すが、更に複数のアノード極11aとカソード極11bが直列及び/又は並列に接続されていてもよい。
【0024】
本発明では、水素発生手段10により、電気分解反応及び電極11の自己反応の両者で水素を発生させるが、電極11の自己反応は、標準電極電位の低い金属(イオン化し易い金属)をアノード極11a及び/又はカソード極11bに用いることで生じさせることができる。標準電極電位の低い金属は、何れの極に使用してもよいが、両極に使用することが、電力収支を大きくする観点から好ましい。なお、従来の水の電気分解は不活性電極を使用するため、電極11の自己反応が生じないことが知られている。
【0025】
本発明では、アノード極11aとカソード極11bが同じ金属でもよく、異なる金属でもよい。標準電極電位の低い金属としては、カリウム、カルシウム、ナトリウム、マグネシウム、アルミニウム、亜鉛、鉄、ニッケル、錫、鉛が挙げられるが、自己反応の生じ易さの観点から、カリウム、カルシウム、ナトリウム、マグネシウム、アルミニウムが好ましく、コストとハンドリング性の観点から、マグネシウム、アルミニウムがより好ましい。
【0026】
これらの金属は、合金や混合金属としても使用することができる。その場合の純度は、90〜100重量%が好ましく、99〜99.9重量%がより好ましい。電極11に含まれる他の元素としては、Al,Mg,Mn,Zn,Cu,Si,Fe,Ti,Cr,V,Bi,Pb,Zr,Bなどが挙げられる。
【0027】
本発明では、特に、マグネシウムを含むアノード極とマグネシウムを含むカソード極との組合せ、又はアルミニウムを含むアノード極とアルミニウムを含むカソード極との組合せが好ましいが、マグネシウムを含むアノード極とアルミニウムを含むカソード極との組合せでも、自己反応を活発に生じさせることができる。
【0028】
本発明では、電極からの電子の授受を伴う電極反応(電気分解反応)と、電子の授受を伴わない電極の自己反応(自発反応)との両者が生じる。電子の授受を伴う電極反応は、印加する電力の消費を伴うため、両電極での水素発生反応を効率良く行うためには、自己反応の比率を高めることが重要になる。これらの反応は、例えば次の通りである。
【0029】
例えば、両極がアルミニウムの場合、アノード極では、
Al+3OH−→Al(OH)3+3e−(水の電気分解)と、
2Al+6H2O→2Al(OH)3+3H2↑(Al活性化による自己反応)
が生じると考えられる。
【0030】
また、カソード極では
2H++2e−→H2↑(水の電気分解)と、
2Al+6H2O→2Al(OH)3+3H2↑(Al活性化による自己反応)
が生じると考えられる。
【0031】
マグネシウムを使用する場合、アノード極では、
Mg+2OH−→Mg(OH)2+2e−(水の電気分解)と、
Mg+2H2O→Mg(OH)2+H2↑(Mg活性化による自己反応)
が生じると考えられる。カソード極に使用する場合は、同様の自己反応と、アルミニウムの場合と同じ水の電気分解反応が生じると考えられる。
【0032】
本実施形態では、説明を簡易にするため、電極11が容器12の電解液13に浸漬されている例を示すが、アノード極11aとカソード極11bとに、多孔質体を接触させて両極間に介在させ、その多孔質体に電解質水溶液を保持させた状態で、両極に電圧を印加することが好ましい。
【0033】
このような水素発生手段10では、電極に多孔質体を接触させて両極間に介在させているため、多孔質体が接触しない場合と比較して、アノード極での反応に伴う酸性度と、カソード極での反応に伴うアルカリ性度とが維持されやすくなり、酸性条件での電極の自己反応(水素発生反応)や、アルカリ性条件での電極の自己反応(水素発生反応)が促進されて、水素発生反応が効率良く生じると考えられる。また、反応で生成する成分(例えば金属水酸化物)が、電極表面に付着せずに多孔質体の空孔内部に取り込まれるため、副生成物による反応阻害を抑制することができ、長時間の水素発生が行えると考えられる。その結果、両電極での水素発生反応を、効率良く長時間生じさせることができる。
【0034】
アルミニウムの自己反応による水素発生は、アルカリ性条件および酸性条件で生じるため、このように酸性度とアルカリ性度とを維持することが、水素発生反応の効率を向上させる。また、マグネシウムの自己反応による水素発生は酸性条件の方が有利であるため、酸性度を維持することが、水素発生反応の効率を向上させる。この観点から、マグネシウムはアノード極に使用するのが好ましい。
アノード極11a及び/又はカソード極11bの形状は、柱状、板状、塊状など何れでも良いが、電極面積を広くする上で、板状のものが好ましい。板状の場合、パンチングメタルのような有孔タイプ、櫛状電極のようなスリットを有するタイプ、メッシュタイプ、不織布状物などでもよい。板状の電極は、平板状の他、板状物を円筒状、四角筒状、スパイラル状、ジグザク状、プリーツ状などに加工したものなどでもよい。
【0035】
アルミニウムを用いる場合の電極の厚みは、十分な水素発生量を確保しつつ金属の反応率を高める観点から、0.03〜5mmが好ましく、0.1〜1mmがより好ましい。マグネシウムを用いる場合の電極の厚みは、同様の観点から、0.3〜10mmが好ましく、0.5〜5mmがより好ましい。一方の電極に不活性な金属を用いる場合など、その他の金属を用いた電極の厚みは0.01〜10mmが好ましく、0.05〜5mmがより好ましい。
【0036】
アノード極11aとカソード極11bとに、多孔質体を接触させて両極間に介在させる場合、多孔質体としては、連通孔を有するものであれば何れでもよく、スポンジ(フォーム)、不織布、織布、紙類、多孔質膜、焼結体、多孔板などが挙げられる。
【0037】
多孔質体の空孔率は、副生成物を取り込む空間を確保しつつ、電極との接触状態を維持する観点から、空孔率が30〜99.9%であることが好ましく、80〜99.5%であることがより好ましい。なお、空孔率(%)は、(1−(多孔質体の密度/材質の密度))×100で計算した値である。
【0038】
多孔質体表面の平均孔径としては、空孔の目詰まりを抑制しつつ、電極との接触状態を確保する観点から、1〜3000μmが好ましく、50〜100μmがより好ましい。平均孔径は、表面の顕微鏡観察により測定し、数平均により求めた値である。
【0039】
多孔質体の材質としては、樹脂、セラミックスなどの絶縁物質や、これらに導電性物質を添加して導電性を向上させたもの、など何れでもよい。但し、電解質水溶液を保持する観点から、親水性の材料が好ましい。樹脂製の多孔質体の場合、弾性変形可能なもの、塑性変形可能なもの、殆ど変形しないものなどが挙げられるが、弾性変形可能なスポンジ状樹脂からなる多孔質体が特に好ましい。
【0040】
多孔質体を構成する樹脂としては、メラミン樹脂、ウレタン樹脂、フェノール樹脂、ポリプロピレン樹脂、ポリエチレン樹脂、ポリエステル樹脂、ポリアミド樹脂、エポキシ樹脂、セルロース系樹脂、などが挙げられる。なかでも、適当な空孔率、孔径、弾性を有する多孔質体が得られ易い観点から、メラミン樹脂、ウレタン樹脂、ポリエステル樹脂、セルロース系樹脂が好ましい。
【0041】
多孔質体の厚み(運転状態)又は電極間の距離は、電解質水溶液を保持しつつ副生成物を取り込む空間を確保する観点から、1〜10mmが好ましく、2〜5mmがより好ましい。多孔質体は、単層であっても複数層であってもよく、複数層の場合、各層の孔径を変えるなど、異なる種類のものを積層してもよい。弾性変形可能な多孔質体を用いる場合、接触性を向上させる観点から、配置する電極間の距離に対して、1〜3倍が好ましく、1.2〜2倍がより好ましい。
【0042】
多孔質体には、電解質水溶液を保持させている。電解質水溶液は、酸性又はアルカリ性でもよいが、両極で酸性度とアルカリ性度とを発現する観点から、中性、例えばpH5〜9が好ましく、pH6〜8がより好ましい。
【0043】
電解質水溶液に含有される電解質としては、アルカリ金属塩、アルカリ土類金属塩、その他の金属塩、アンモニウム塩、ホスホニウム塩など何れでも良いが、取扱い性の観点から、塩化ナトリウム、塩化カリウム、塩化リチウムが好ましい。電解質は2種以上混合することも可能であり、酸性塩や塩基性塩との併用も可能である。また、アルカリ性物質や酸性物質を併用することも可能である。
【0044】
電解質の濃度としては、電気抵抗を適度に調整して、効率よく電極反応を生じさせる観点から、5〜30重量%が好ましく、20〜26重量%がより好ましい。なお、水素発生反応の途中で、水を別途添加したり、電解質を別途添加してもよい。また、多孔質体に予め電解質等を添着(含浸・乾燥)しておき、反応の初期に水等を供給して、多孔質体に電解質水溶液を保持させてもよい。また、完全に溶解しない電解質が存在する状態(飽和状態)で反応を行ってもよい。
【0045】
電解質水溶液は、少なくともその一部が多孔質体に保持されていればよく、残部は容器内に存在してもよい。また、電解質水溶液の全体が多孔質体に保持されるようにしてもよい。電解質水溶液を水素発生反応の途中で別途添加することも可能である。
【0046】
電解質水溶液の量は、できるだけ過不足無く水素発生反応を行う観点から、電極の総重量100重量部に対して、1500〜10000重量部が好ましく、2000〜5000重量部がより好ましい。
【0047】
(燃料電池)
燃料電池20としては、水素を供給して発電を行うものが何れも使用できる。本発明では、装置の小型化・軽量化の観点から、燃料電池20として固体高分子電解質層21とその両側に設けられた電極22、23とを備えるものが好ましい。なお、燃料電池20は、複数の単位セルを備えるものでよく、その場合、単位セル同士は接続部により直列又は並列に電気的に接続される。
【0048】
燃料電池20のアノード側には、水素発生手段10で発生した水素が供給される。その際の経路には、バッファタンクなどを設けてもよいが、直接供給することも可能である。燃料電池20のカソード側には空気などの酸素含有ガスが供給される。
【0049】
単位セルは、例えば、固体高分子電解質層21と、この固体高分子電解質層21の両側に設けられた第1電極層22及び第2電極層23と、これら電極層22,23の更に外側に各々配置された第1導電層及び第2導電層とを有する。本実施形態では、第1導電層及び第2導電層が、第1電極層22及び第2電極層23を部分的に露出させる露出部を有する第1金属層及び第2金属層とからなる例を示す。これらの各層は、インサート成形により樹脂で一体化されていることが好ましい。インサート成形により単位セルを製造する方法は、国際公開WO2009/145090号公報に詳述されている。
【0050】
固体高分子電解質層21としては、従来の固体高分子膜型の燃料電池に用いられるものであれば何れでもよいが、化学的安定性及び導電性の点から、超強酸であるスルホン酸基を有するパーフルオロカーボン重合体からなる陽イオン交換膜が好適に用いられる。このような陽イオン交換膜としては、ナフィオン(登録商標)が好適に用いられる。その他、例えば、ポリテトラフルオロエチレン等のフッ素樹脂からなる多孔質膜に上記ナフィオンや他のイオン伝導性物質を含浸させたものや、ポリエチレンやポリプロピレン等のポリオレフィン樹脂からなる多孔質膜や不織布に上記ナフィオンや他のイオン伝導性物質を担持させたものでもよい。
【0051】
固体高分子電解質層21の厚みは、薄くするほど全体の薄型化に有効であるが、イオン伝導機能、強度、ハンドリング性などを考慮すると、10〜300μmが使用可能であるが、25〜50μmが好ましい。
【0052】
電極層22,23は、固体高分子電解質層21の表面付近でアノード側およびカソード側の電極反応を生じさせるものであれば何れでもよい。なかでも、ガス拡散層としての機能を発揮して、燃料ガス、燃料液、酸化ガス及び水蒸気の供給・排出を行なうと同時に、集電の機能を発揮するものが好適に使用できる。電極層22,23としては、同一又は異なるものが使用でき、その基材には電極触媒作用を有する触媒を担持させることが好ましい。触媒は、固体高分子電解質層21と接する内面側に少なくとも担持させるのが好ましい。
【0053】
電極層22,23の電極基材としては、例えば、カーボンペーパー、カーボン繊維不織布などの繊維質カーボン、導電性高分子繊維の集合体などの電導性多孔質材が使用できる。また、固体高分子電解質層21に触媒を直接付着させたり、カーボンブラックなどの導電性粒子に担持させて固体高分子電解質層21に付着させた電極層22,23を用いることも可能である。
【0054】
一般に、電極層22,23は、このような電導性多孔質材にフッ素樹脂等の撥水性物質を添加して作製されるものであって、触媒を担持させる場合、白金微粒子などの触媒とフッ素樹脂等の撥水性物質とを混合し、これに溶媒を混合して、ペースト状或いはインク状とした後、これを固体高分子電解質膜と対向すべき電極基材の片面に塗布して形成される。
【0055】
一般に、電極層22,23や固体高分子電解質層21は、燃料電池に供給される還元ガスと酸化ガスに応じた設計がなされる。本発明では、酸化ガスとして空気が用いられると共に、還元ガスとして水素ガスを用いる。
【0056】
空気が自然供給される側のカソード側の第2電極層23(本明細書では、アノード側を第1電極層、カソード側を第2電極層と仮定する)では、酸素と水素イオンの反応が生じて水が生成するため、かかる電極反応に応じた設計をするのが好ましい。
【0057】
触媒としては、白金、パラジウム、ルテニウム、ロジウム、銀、ニッケル、鉄、銅、コバルト及びモリブデンから選ばれる少なくとも1種の金属か、又はその酸化物が使用でき、これらの触媒をカーボンブラック等に予め担持させたものも使用できる。
【0058】
電極層22,23の厚みは、薄くするほど全体の薄型化に有効であるが、電極反応、強度、ハンドリング性などを考慮すると、1〜500μmが好ましく、100〜300μmがより好ましい。電極層22,23と固体高分子電解質層21とは、予め接着、融着、又は塗布形成等を行って積層一体化しておいてもよいが、単に積層配置されているだけでもよい。このような積層体は、膜/電極接合体(Membrane Electrode Assembly:MEA)として入手することもでき、これを使用してもよい。
【0059】
アノード側電極層22の表面にはアノード側の第1金属層が配置され、カソード側電極層23の表面にはカソード側の第2金属層が配置される(本明細書では、アノード側を第1金属層、カソード側を第2金属層と仮定する)。第1金属層は、第1電極層22を部分的に露出させる露出部を有するが、本実施形態では、アノード側金属層には燃料ガス等を供給するための開孔が設けられている例を示す。
【0060】
第1金属層の露出部は、アノード側電極層22が露出可能であれば、その個数、形状、大きさ、形成位置などは何れでもよい。アノード側金属層の開孔は、例えば、規則的又はランダムに複数の円孔やスリット等を設けたり、または金属メッシュによって開孔を設けてもよい。開孔部分の面積が締める割合(開孔率)は、電極との接触面積とガスの供給面積のバランスなどの観点から、10〜50%が好ましく、15〜30%がより好ましい。
【0061】
また、カソード側の第2金属層は、第2電極層23を部分的に露出させる露出部を有するが、本実施形態では、カソード側金属層には、空気中の酸素を供給(自然吸気)するための多数の開孔が設けられている例を示す。開孔の形状、大きさ、開孔率等は、アノード側の第1金属層と同様である。
【0062】
金属層としては、電極反応に悪影響がないものであれば何れの金属も使用でき、例えばステンレス板、ニッケル、銅、銅合金などが挙げられる。但し、導電性、コスト、形状付与性、加圧のための強度などの観点から、銅、銅合金、ステンレス板などが好ましい。また、上記の金属に金メッキなどの金属メッキを施したものでもよい。
【0063】
なお、金属層の厚みは、薄くするほど全体の薄型化に有効であるが、導電性、コスト、重量、形状付与性、加圧のための強度などを考慮すると、10〜1000μmが好ましく、50〜200μmがより好ましい。
【0064】
第1金属層及び第2金属層は、少なくとも一部が樹脂から露出することにより、その部分を電極として電気を外部に取り出すことができる。このため、樹脂成形体に対して、第1金属層及び第2金属層を一部露出させた端子部を設けてもよい。金属層及び金属層の形成や開孔の形成は、プレス加工(プレス打ち抜き加工)を利用して行うことができる。
【0065】
以上では、小型の燃料電池として、アノード側とカソード側の両側に、燃料、酸素等を供給するための開口を有する燃料電池の例を示したが、少なくとも一方の側に、燃料等を供給するための流路を設けた単位セルが独立して構成された構成燃料電池、又はセパレータを介在させたスタックタイプの燃料電池などを使用することも可能である。
【0066】
(電圧印加回路)
電圧印加回路30は、燃料電池20からの電力を利用して、直接的又は間接的に水素発生手段10に電圧を印加するものである。本実施形態では、電圧印加回路30が蓄電手段31を介して、間接的に水素発生手段10に電圧を印加する例を示す。
【0067】
アルミニウムを含むアノード極11aと、アルミニウムを含むカソード極11bとに電圧を印加する場合、適度な自己反応率を実現する上で、一対の電極に対して0.1〜5Vで印加するのが好ましく、0.5〜1.5Vで印加するのがより好ましい。マグネシウムを含むアノード極と、マグネシウムを含むカソード極とに電圧を印加する場合、適度な自己反応率を実現する上で、一対の電極に対して0.3〜5Vで印加するのが好ましく、1〜3Vで印加するのがより好ましい。マグネシウムを含むアノード極と、アルミニウムを含むカソード極とに電圧を印加する場合、適度な自己反応率を実現する上で、一対の電極に対して0〜2Vで印加するのが好ましく、0〜0.5Vで印加するのがより好ましい。
【0068】
上記印加を行う際の電流は、上記電圧値と系の抵抗とによって決まるが、系の抵抗は、電極面積、電解質濃度、電極間距離、電極の数、多孔質体の空孔率などにより変化する。電圧の印加の際には、定電圧による印加の他、一定電流への電圧制御、一定水素発生量への電圧制御、あるいはこれらに対応する電流制御などを行っても良い。本発明では、水素発生の効率が高く、発生した水素を燃料電池に供給する場合の発電電力が、電気分解の消費電力を超えること、即ち電力収支をプラスにすることが可能となる。このため、発生した水素を供給した燃料電池により、電圧の印加を行うことができる。
【0069】
水素発生手段10に電圧を印加する回路には、電圧を昇圧又は降圧させるために、必要に応じてDC/DCコンバータ32を設けてもよい。蓄電手段31の出力電圧と、水素発生手段10で要求される電位が、同程度であれば、DC/DCコンバータ32は必要ないが、両者に電圧差がある場合には、これに応じた電圧変化がなされる。例えば、リチウムイオン二次電池を蓄電手段31として使用する場合、出力電圧は4V前後であるため、DC/DCコンバータ32などを用いて降圧を行うのが好ましい。
【0070】
蓄電手段31から水素発生手段10に印加する電圧は、制御手段Cにより制御するのが好ましいが、制御の方法としては、スイッチング素子33を用いて、デューティー比で電力供給量を制御する方法やオンオフ制御を行う方法の他、DC/DCコンバータ32に対して制御信号を送ることで、DC/DCコンバータ32からの出力電圧を制御する方法でもよい。
【0071】
本実施形態では、燃料電池20から蓄電手段31に電力を供給する回路にも、DC/DCコンバータ34を設けられているが、これは燃料電池20からの出力電圧を、蓄電手段31を充電するための電圧に調整するために設けている。本実施形態では、燃料電池20から出力回路40を経て出力される電力が、DC/DCコンバータ34を介して出力されるため、蓄電手段31の充電電圧とほぼ同じ電位になる。
【0072】
燃料電池20から蓄電手段31に電力を供給する回路には、制御手段Cにより制御されるスイッチング素子35などが設けられ、蓄電手段31に供給する電力と、出力回路40を経て出力する電力とを、制御手段Cにより配分することができる。制御手段Cによる配分は、デューティー比で制御する方法の他、配分される電流を検出して両者の電流の比で、電力の配分を行うようにしてもよい。この制御手段Cによりスイッチング素子35などを制御して、燃料電池20から蓄電手段31に供給する電力を制御することができる。
【0073】
デューティー比でスイッチング素子35を制御する場合、スイッチング素子33と同期させることで、スイッチング素子35により蓄電手段31を充電するタイミングを避けて、スイッチング素子33で水素発生手段10に電圧を印加するタイミングを制御してもよい。
【0074】
なお、デューティー比で制御する場合、スイッチング素子35と蓄電手段31との間、又はスイッチング素子35の出力回路40側には、直流化のための整流回路や平滑化回路を設けてもよい。
【0075】
本実施形態では、少なくとも発電の初期に水素発生手段10に電力を供給する蓄電手段31を備える例を示すが、少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段を備えていてもよい(図3参照)。
【0076】
蓄電手段31は、発電の初期に水素発生手段10に電力を供給するためにも使用することができる。図示した例では、発電の初期には、蓄電手段31以外に電力の供給源が特に存在しない。このため、発電の初期に、スイッチング素子33がオンになる状態で、蓄電手段31から水素発生手段10に電力を供給することが好ましい。
【0077】
本発明では、水素発生手段10に供給される初期の電力が、定常状態における電力と比較して大きくなるように構成されているのが好ましい。ここで、定常状態とは、水素発生手段による消費電力が、最小の状態から最小プラス50%の状態までの状態を指すが、初期に供給する最大電力が、定常状態における最小電力の1.1〜50倍が好ましく、2〜20倍がより好ましく、4〜10倍が好ましい。
【0078】
初期の電力又は電力量を大きくする方法としては、蓄電手段31からの電圧を変換するDC/DCコンバータ32の設定電圧を高くする制御、スイッチング素子33のデューティー比を高くする制御などが挙げられる。また、タイマ制御により設定電圧を変える制御、プログラムにより設定電圧を変える制御、電流等を検出してフィードバック制御で設定値に調節する際に設定値を変える制御などにより、上記制御を行うことが可能である。
【0079】
制御手段Cは、蓄電手段31から電源を取っているが、燃料電池20からこれを行うことも可能である。燃料電池20から電源を取る場合、燃料電池20とDC/DCコンバータ34との間に電気的に接続することが好ましい。
【0080】
制御手段Cとしては、汎用のマイクロプロセッサ又は専用のマイクロコントローラを用いることができる。一般にマイクロコントローラは、メモリと用途に応じたI/Oを内蔵しているが、汎用マイクロプロセッサの場合、それらの機能を有する周辺チップを追加して用いることができる。
【0081】
マイクロコントローラは、一般にクロックジェネレータ付きのCPU、プログラムを格納するためのメモリ、ウォッチドッグタイマー等のタイマー、外部周辺機器などと通信するための入出力部を有しており、これらが一つの集積回路に組み込まれているものもある(ワンチップマイコン)。
【0082】
マイクロコントローラを動作できるようにするには、ソフトウェアをROMに格納して、クロック制御による演算を行えばよい。マイクロコントローラは様々な入出力デバイスを内蔵しており、アナログ-デジタル変換回路、汎用非同期シリアル通信などである。
【0083】
マイクロコントローラを用いて、デューティー比の制御を行う場合、例えばカウンタを利用したPWM(Pulse Width Modulation)モードのプログラムを用いればよい。また、電流値又は電圧値などをフィードバック制御する場合、例えば、検出値と設定値とを比較して、制御信号をオンオフしたり、偏差に基づいて制御信号を演算するプログラムを用いればよい。
【0084】
ここで、PWM方式は、周期を一定としてパルス幅の割合を可変することにより、通電する時間の平均のエネルギーを可変制御する方式であるが、電圧そのものを変えてエネルギーを可変するPAM方式(Pulse Amplitude Modulation) を採用したり、両者を併用することも可能である。このようなPWM/PAM複合制御を行う場合、例えば、電力が低い領域では、電圧変換効率の問題により、一定以下に電圧が下げられないため、パルスモードを使用し、電力が必要な領域では、降圧型コンバータを制御し、デューティ100%で電圧値そのものを可変させて、電力を制御することができる。
【0085】
(出力回路)
出力回路40は、燃料電池20で発電した余剰の電力を出力するものである。本実施形態では、燃料電池20から蓄電手段31に電力を供給する回路のDC/DCコンバータ34が、出力回路40のDC/DCコンバータと兼用されているが、別のDC/DCコンバータを設けても良い。その場合、スイッチング素子35の両側にDC/DCコンバータを設けてもよい。これにより、充電側の電圧と出力側の電圧とを変えることが出来る。
【0086】
本発明において「余剰の電力を出力する」とは、トータルとしての余剰分を出力すると言う意味であり、常時、余剰分を出力すると言う意味ではない。例えば、ある期間は、燃料電池20からの出力を全て出力回路40を経て必要な負荷に出力し、負荷のない時に、出力を止めて全ての電力を蓄電手段31に充電しながら、蓄電手段31から水素発生手段10に電力を供給してもよい。
【0087】
出力回路40には、蓄電手段31とは別の蓄電手段を設けてもよく、この蓄電手段の充放電を行いながら系外に出力することができる。また、別の蓄電手段を設けずに、蓄電手段31を充電しながら、蓄電手段31から系外に電力を出力できるように構成してもよい。
【0088】
また、図2に示す他の実施形態のように、出力回路40に対し、蓄電手段31からの出力をスイッチング素子41などを介して電気的に接続してもよい。その場合、例えば燃料電池20からの出力回路40に、電流センサ42などを設けて、電流の変化勾配に基づいて、スイッチング素子41を制御することができる。スイッチング素子41としては、オンオフだけでなく、電流制御を行えるものでもよい。
【0089】
(他の実施形態1)
本発明の発電装置は、図3に示すように、少なくとも発電の初期に燃料電池20に水素を供給するための水素供給手段50を備えていてもよい。水素供給手段50としては、水素貯蔵合金などを用いた水素タンク、水素化金属などの水素発生剤を用いたもの、電極反応を利用したものなど、何れでもよい。図示した実施形態では、電極反応を利用した水素供給手段50の例を示す。
【0090】
この水素供給手段50は、電極51間をスイッチング素子55などで導通させるだけで、電極反応により水素を発生させることができる。その際、導通回路54に抵抗を設けたり、スイッチング素子55などで電流を調整するなどにより、水素発生量を制御することができ。
【0091】
水素供給手段50に用いる電極51としては、アノード極51aが水素より標準電極電位の低い金属であり、カソード極11bがそれより標準電極電位の高い金属であれば、いずれも使用することができる。但し、水素発生の純度と量、コスト、及びハンドリング性の観点より、マグネシウムとアルミニウム、マグネシウムとニッケル、マグネシウムと亜鉛、マグネシウムと鉄、マグネシウムとスズ、マグネシウムとSUS、マグネシウムと銅、マグネシウムとカーボンの組合せが好ましい。その他の構成、即ち、電解液53、容器52、多孔質体などは、前述した水素発生手段10と同様のものが使用可能である。
【0092】
水素供給手段50は、発電の開始時点で、手動によりスイッチオンするのが好ましい。これにより発生した水素は、燃料電池20のアノード側に供給され、発電が開始する。この実施形態では、蓄電手段31を有しないため、電圧印加回路30により、燃料電池20からの電力を利用して、直接的に水素発生手段10に電圧を印加する。電圧の印加により、水素発生手段10は水素を発生し、これが燃料電池20に供給され、二系統からの水素供給により発電が行われる。
【0093】
電圧印加回路30には、先の実施形態と同様に、燃料電池20からの電力を配分するスイッチング素子35と、DC/DCコンバータ32とが設けられている。電圧印加回路30を経て、水素発生手段10に供給できる電力が十分(例えば電力収支がプラス)になると、スイッチング素子55をオフすることで、水素供給手段50からの水素供給を停止することができる。また、水素供給手段50を使い切りにして、スイッチング素子55をオフする制御を省略することも可能である。
【0094】
出力回路40は、スイッチング素子35の負荷側にDC/DCコンバータ34が設けられている他は、先の実施形態と同様である。制御手段Cは、燃料電池20から電源を取っており、燃料電池20とスイッチング素子35との間に電気的に接続することが好ましい。
【0095】
(他の実施形態2)
図4に示す実施形態は、他の実施形態1において、水素供給手段50で発生する水素を利用するだけでなく、水素供給手段50で発生する電力を利用して、発電の初期に水素発生手段10に電圧を印加するものである。つまり、この実施形態では、少なくとも発電の初期に水素発生手段10に電力を供給する蓄電手段を、少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段50が兼用している。
【0096】
この実施形態では、電圧印加回路30を経て、水素発生手段10に供給できる電力が十分(例えば電力収支がプラス)になると、スイッチング素子55をオフすることが好ましい。また、逆電流を防止するために、導通回路54に整流素子を用いるのが好ましい。
【0097】
(他の実施形態3)
他の実施形態1では、燃料電池20から水素発生手段10に電力を供給する際に、DC/DCコンバータ32を設ける例を示したが、これを設けずに電力を供給することも可能である。その場合、燃料電池20の出力電圧と、水素発生手段10の印加電圧とを近づけることが好ましい。例えば、単位セルの直列接続の数を少なくすることで燃料電池20の出力電圧を下げることができ、その場合、電極面積を増加させたり、又は並列接続の数を増加させることで、電力を維持することができる。また、水素発生手段10の両電極11a,11bを直列に接続して、両端の電極間に印加することで、印加電圧水素発生手段10の印加電圧を低下させることができる。
【実施例】
【0098】
以下、本発明の構成と効果を具体的に示す実施例等について説明する。
【0099】
燃料電池の製造例1
厚み0.2mmのニッケル板を金メッキしたものを、図11に示す形状(矩形状部の長径33mm、短径12mm、)にプレスして打ち抜き、金属層4(開口率14%)と金属層5(開口率31%)となるニッケル板を2枚作製した。金属層4,5の突出部4b,5bは、電極端子となる。また、金属層4,5の開口部は、樹脂成形後に、電極層2,3の表面を部分的に露出させる露出部4a(開口率7%)と露出部5a(開口率22%)となる。
【0100】
固体高分子電解質層1(陽イオン交換膜)としてナフィオンフィルム(デュポン社製ナフィオン112、33mm×12mm、厚み15μm)を用いた。この固体高分子電解質層1の両面の周縁部に、図11に示すように補強層8としてPEN樹脂(ポリエチレンナフタレート)を幅500μm、厚み40μmで設けた。
【0101】
また、固体高分子電解質層1の両面の中央部には、図11に示すように、触媒層9を補強層8とほぼ同じ厚みで設けた。白金触媒は、米国エレクトロケム社製20%白金担持カーボン触媒(EC−20−PTC)を用いた。この白金触媒と、カーボンブラック(アクゾ社ケッチェンブラックEC)、ポリフッ化ビニリデン(カイナー)を、それぞれ75重量%、15重量%、10重量%の割合で混合し、ジメチルホルムアミドを、2.5重量%のポリフッ化ビニリデン溶液となるような割合で、上記白金触媒、カーボンブラック、ポリフッ化ビニリデンの混合物中に加え、乳鉢中で溶解・混合して、触媒ペーストを作製し、固体高分子電解質層1の表面に塗布した。電極層2,3としては、カーボンペーパー(東レ製TGP−H−90、厚み370μm)を33mm×12mmに切断して用いた。
【0102】
固体高分子電解質層1、触媒層9、補強層8、電極層2,3の積層物を、上記のニッケル板2枚の中央で挟み込み、樹脂の開口形状に対応する凸部を内表面に有する金型を用いて、2枚のニッケル板の両側から圧力(1トン)がかかる状態で、金型内に配置した。その状態で、樹脂((株)プライムポリマー製、ポリプロピレン樹脂、J−700GP)を195℃で型内に注入して(射出圧力400kgf/cm2)、冷却した後に金型から取り出すことで、樹脂成形体の外寸35mm×14mm×2.2mm厚の単位セルを作成した。この単位セルでは、アノード側の電極層2と樹脂成形体6の樹脂が接触する接触部6aが、カソード側に比べて多くなっている。
【0103】
この単位セルの4つを用いて、アノード側を内側にして四角柱の四つの側面を形成し、これらの突出部4b,5bを電気的に直列に接続して、内側に水素供給空間を有し、外側から空気供給が可能な四角柱の燃料電池を得た。
【0104】
実施例1
電極となるアルミニウム板(純度99.5%、縦35×横50×厚み0.3mm、1.44g)を2枚用意し、2枚の間に多孔質体(BASF社製、メラミンフォーム、縦35×横50×厚み5mm、密度0.0093g/cm3、空孔率99.4%、平均孔径70μm)を挟み、電極間の距離が5mmになるような平型ケース(約8mL)に入れて、20重量%NaCl水溶液を約8mL注入した。ケースの上部空間を閉空間とし、発生した水素ガスを排出する流路に、膜式流量計(堀場製作所社製)を接続して、常時、水素発生流量をモニターした。各々の電極を安定化電源に正極および負極として接続し、水素発生流量が約10mL/minになるように、手動で電源の電流値を変化させながら1時間運転を行った。その際の水素発生量を図5(a)に、電圧と電流の関係を図5(b)、これらから計算される発生電力と消費電力を図5(c)に示す。
【0105】
発生電力については、製造例1の燃料電池を用いて、水素流量10mL/minで発電を行った場合、燃料電池の出力電圧が約3V(4セル分)、電流が約0.33Aであり、これをDC/DCコンバーター(電力効率85%)で、約5Vまで昇圧すると、発生電力が約0.83Wであったため、これを基準に発生電力を計算した。
【0106】
図5(c)に示す結果から、電極の自己反応により、消費電力以上の発電が可能(1.14〜5.2倍)なことが分かった。電圧印加により、電極のアルミが活性化され、電気分解以外の自己反応により水素発生が生じていると考えられる。なお、消費電力0.5W以下の持続時間は約90minであった。
【0107】
実施例2
実施例1において、使用した多孔質体を下記の多孔質体に代える以外は、実施例1と全く同じ条件で水素発生流量が約10mL/minになるように、手動で電源の電流値を変化させながら1時間運転を行った。その際の電圧と電流から計算される消費電力を、実施例1の結果と併せて図6に示す。
(実施例2−1)ソフラス(ポリウレタン、0.22g/cm3、空孔率82%、平均孔径1μm)5mm厚み
(実施例2−2)ポリウレタン(食器洗いスポンジ0.028g/cm3、空孔率98%、平均孔径2000μm)5mm厚み
(実施例2−3)蒸発紙(ポリエステル樹脂、0.26g/cm3、空孔率78%、平均孔径50μm)1mm厚み×5枚
(実施例2−4)ベルイーター(ポリビニルアルコールスポンジ、0.089g/cm3、空孔率95%、平均孔径70μm)1.8mm厚み×2枚。
【0108】
比較例1
実施例1において、多孔質体を使用せずに、同量のNaCl水溶液のみが電極間に存在するようにした以外は、実施例1と全く同じ条件で水素発生流量が約10mL/minになるように、手動で電源の電流値を変化させながら1時間運転を行った。その際の電圧と電流から計算される消費電力を、図6に併せて示す。その結果、多孔質体を用いない場合には、初期に消費電力が非常に大きくなり、電力収支がマイナスになる部分(消費電力0.8W以上)が生じた。
【0109】
実施例3−1
電極となるアルミニウム板(純度99.5%、縦35×横20×厚み0.3mm、0.57g)を2枚用意し、2枚の間と両外側とに多孔質体(BASF社製、メラミンフォーム、縦35×横50×厚み5mm、密度0.0093g/cm3、空孔率99.4%)を1枚ずつ配置し、これを容器(深さ35×横50×幅15mm、容積約27mL)に入れて、20重量%NaCl水溶液を約15mL注入した。容器の上部空間を閉空間とし、発生した水素ガスを排出する流路に、膜式流量計(堀場製作所社製)を接続して測定した。各々の電極を安定化電源に正極および負極として接続し、電源の電流値を0.5Aに制御して2時間運転を行った。その際の消費電力を図7(a)に、消費電力量を図7(b)、利用可能電力を図7(c)に、利用可能電力量を図7(d)に示す。
【0110】
実施例3−2
実施例3−1において、使用した多孔質体の厚みを10mmに代える以外は、実施例3−1と全く同じ条件で2時間運転を行った。その際の消費電力を図7(a)に、消費電力量を図7(b)、利用可能電力を図7(c)に、利用可能電力量を図7(d)に併せて示す。
【0111】
比較例2
実施例3−1において、使用した3枚の多孔質体の厚みを3mmに代え、多孔質体と電極との間に厚さ1mmのシリコーンゴムよりなる枠状スペーサ(電極とは上端と下端とでのみ幅2mmで接する)を介在させて、電極と多孔質体との距離を1mmにしたこと以外は、実施例3−1と全く同じ条件で2時間運転を行った。その際の消費電力を図7(a)に、消費電力量を図7(b)、利用可能電力を図7(c)に、利用可能電力量を図7(d)に併せて示す。
【0112】
実施例3−1、3−2と比較例2の結果を対比すると、アルミ電極とスポンジの接触が良いほど、反応効率は向上し、特に非接触の場合は反応が鈍化し、消費電力が跳ね上がっていることが分かった。
【0113】
実施例4−1
電極となるマグネシウム板(AZ31,純度96%、縦35×横20×厚み0.3mm、0.36g)を2枚用意し、2枚の間と両外側とに多孔質体(BASF社製、メラミンフォーム、縦35×横50×厚み5mm、密度0.0093g/cm3、空孔率99.4%)を1枚ずつ配置し、これを容器(深さ35×横50×幅15mm、容積約27mL)に入れて、20重量%NaCl水溶液を約15mL注入した。容器の上部空間を閉空間とし、発生した水素ガスを排出する流路に、膜式流量計(堀場製作所社製)を接続して測定した。各々の電極を安定化電源に正極および負極として接続し、電源の電流値を0.5Aに制御して1時間運転を行った。その際の消費電力を図8(a)に、消費電力量を図8(b)、利用可能電力を図8(c)に、利用可能電力量を図8(d)に示す。
【0114】
実施例4−2
実施例4−1において、使用した多孔質体の厚みを10mmに代える以外は、実施例4−1と全く同じ条件で1時間運転を行った。その際の消費電力を図8(a)に、消費電力量を図8(b)、利用可能電力を図8(c)に、利用可能電力量を図8(d)に併せて示す。
【0115】
比較例3
実施例4−1において、使用した3枚の多孔質体の厚みを3mmに代え、多孔質体と電極との間に厚さ1mmのシリコーンゴムよりなる枠状スペーサ(電極とは上端と下端とでのみ幅2mmで接する)を介在させて、電極と多孔質体との距離を1mmにしたこと以外は、実施例4−1と全く同じ条件で1時間運転を行った。その際の消費電力を図8(a)に、消費電力量を図8(b)、利用可能電力を図8(c)に、利用可能電力量を図8(d)に併せて示す。
【0116】
実施例4−1、4−2と比較例3の結果を対比すると、非接触の場合は反応が鈍化し、消費電力が大きくなることが分かった。マグネシウム電極とスポンジの接触が弱いほど、反応効率は向上しており、これは接触が強いほど、マグネシウムの副生成物(酸化物、水酸化物)による堆積を許容しにくくなるためであると考えられる。
【0117】
実施例5−1
アノード極となるマグネシウム板(純度96%、縦35×横20×厚み0.3mm、0.36g)と、カソード極となるアルミニウム板(純度99.5%、縦35×横20×厚み0.3mm、0.57g)とを用意し、2枚の間と両外側とに多孔質体(BASF社製、メラミンフォーム、縦35×横50×厚み5mm、密度0.0093g/cm3、空孔率99.4%)を1枚ずつ配置し、これを容器(深さ35×横50×幅15mm、容積約27mL)に入れて、20重量%NaCl水溶液を約15mL注入した。容器の上部空間を閉空間とし、発生した水素ガスを排出する流路に、膜式流量計(堀場製作所社製)を接続して測定した。各々の電極を銅板(幅10mm、厚み0.5mm、抵抗5〜8mΩ)で導通させ、水素発生流量が約6mL/min以下になるまで運転を行った。その際の利用可能電力を図9(a)に、利用可能電力量を図9(b)に示す。
【0118】
この系を利用することで、初期に水素を供給する水素供給手段、及び/又は初期に電力を供給する蓄電手段として、利用することができる。
【0119】
実施例5−2
実施例5−1において、使用した多孔質体の厚みを10mmに代える以外は、実施例5−1と全く同じ条件で1時間運転を行った。その際の利用可能電力を図9(a)に、利用可能電力量を図9(b)に併せて示す。
【0120】
比較例4
実施例5−1において、使用した3枚の多孔質体の厚みを3mmに代え、多孔質体と電極との間に厚さ1mmのシリコーンゴムよりなる枠状スペーサ(電極とは上端と下端とでのみ幅2mmで接する)を介在させて、電極と多孔質体との距離を1mmにしたこと以外は、実施例5−1と全く同じ条件で1時間運転を行った。その際の利用可能電力を図9(a)に、利用可能電力量を図9(b)に併せて示す。
【0121】
実施例5−1、5−2と比較例4の結果を対比すると、水素発生反応の効率はほとんど変わらないものの、非接触の場合は副生成物による反応阻害が早く生じるため、利用可能電力量はより小さくなった。
【0122】
(自己反応率の対比)
実施例3−1、4−1、及び5−1の結果から、次のようにして自己反応率を計算した。即ち、電流から求めた、「移動した電子量」から電気分解反応で発生した水素量を算出し、これを実際の水素発生量から差し引き、各々の電極で自己反応と、電気分解反応の比率を求めた。
【数1】

その結果を図10(a)に示す。また、計算に使用した電流値と電圧値のデータを、それぞれ図10(b)と図10(c)とに示す。図10の結果から、Al−Mg、Al−Al、Mg−Mgの順序で、自己反応の比率が高いことが分かった。
【0123】
実施例6
実施例1で用いた水素発生手段等の装置を用いて、安定化電源から電力供給を開始し、製造例1の燃料電池に水素供給して発電(出力電圧約3V)を行った。開始から10分後(水素発生量約10mL/min)に電力供給を停止し、燃料電池の出力電圧を0.7VまでDC/DCコンバーター(電力効率85%)で降圧して水素発生手段の正極および負極に印加しつつ、DC/DCコンバーター(電力効率85%、出力電圧5V)を介して、一定電流(0.12A)に設定した外部負荷(菊水電子工業株式会社製、PLZ70UA)による電力利用を試みた。その結果、水素流量をほぼ一定に保ちながら、外部負荷に対して電力を90分間にわたり出力(電力量0.9Wh、平均電力約0.6W)することができた。
【符号の説明】
【0124】
10 水素発生手段
11 電極
20 燃料電池
30 電圧印加回路
31 蓄電手段
40 出力回路
50 水素供給手段
C 制御手段
【特許請求の範囲】
【請求項1】
電圧の印加による電気分解反応及び電極の自己反応の両者で水素を発生させる水素発生手段と、
発生した水素を供給して発電を行う燃料電池と、
その燃料電池からの電力を利用して、直接的又は間接的に前記水素発生手段に電圧を印加する電圧印加回路と、
前記燃料電池で発電した余剰の電力を出力する出力回路と、を備える発電装置。
【請求項2】
前記水素発生手段に供給される初期の電力が、定常状態における電力と比較して大きくなるように構成されている請求項1に記載の発電装置。
【請求項3】
前記水素発生手段は、少なくともカソード極がアルミニウムを含有するものである請求項1又は2に記載の発電装置。
【請求項4】
少なくとも発電の初期に前記水素発生手段に電力を供給する蓄電手段、及び/又は少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段を備える請求項1〜3いずれかに記載の発電装置。
【請求項5】
少なくとも発電の初期に前記水素発生手段に電力を供給し、前記燃料電池から供給された電力を蓄電する蓄電手段と、
前記燃料電池から前記蓄電手段に供給する電力を制御する制御手段とを備える請求項1〜4いずれかに記載の発電装置。
【請求項6】
少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段と、
前記燃料電池から前記水素発生手段に供給する電力及び前記出力回路から出力される電力を制御する制御手段とを備える請求項1〜4いずれかに記載の発電装置。
【請求項7】
前記制御手段がデューティ比の制御により電力を制御する請求項6に記載の発電装置。
【請求項1】
電圧の印加による電気分解反応及び電極の自己反応の両者で水素を発生させる水素発生手段と、
発生した水素を供給して発電を行う燃料電池と、
その燃料電池からの電力を利用して、直接的又は間接的に前記水素発生手段に電圧を印加する電圧印加回路と、
前記燃料電池で発電した余剰の電力を出力する出力回路と、を備える発電装置。
【請求項2】
前記水素発生手段に供給される初期の電力が、定常状態における電力と比較して大きくなるように構成されている請求項1に記載の発電装置。
【請求項3】
前記水素発生手段は、少なくともカソード極がアルミニウムを含有するものである請求項1又は2に記載の発電装置。
【請求項4】
少なくとも発電の初期に前記水素発生手段に電力を供給する蓄電手段、及び/又は少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段を備える請求項1〜3いずれかに記載の発電装置。
【請求項5】
少なくとも発電の初期に前記水素発生手段に電力を供給し、前記燃料電池から供給された電力を蓄電する蓄電手段と、
前記燃料電池から前記蓄電手段に供給する電力を制御する制御手段とを備える請求項1〜4いずれかに記載の発電装置。
【請求項6】
少なくとも発電の初期に前記燃料電池に水素を供給するための水素供給手段と、
前記燃料電池から前記水素発生手段に供給する電力及び前記出力回路から出力される電力を制御する制御手段とを備える請求項1〜4いずれかに記載の発電装置。
【請求項7】
前記制御手段がデューティ比の制御により電力を制御する請求項6に記載の発電装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【公開番号】特開2011−249161(P2011−249161A)
【公開日】平成23年12月8日(2011.12.8)
【国際特許分類】
【出願番号】特願2010−121733(P2010−121733)
【出願日】平成22年5月27日(2010.5.27)
【出願人】(506239784)アクアフェアリー株式会社 (40)
【Fターム(参考)】
【公開日】平成23年12月8日(2011.12.8)
【国際特許分類】
【出願日】平成22年5月27日(2010.5.27)
【出願人】(506239784)アクアフェアリー株式会社 (40)
【Fターム(参考)】
[ Back to top ]

