皮膚熱傷を治療するための医薬組成物
本発明は、オクタン酸セテアリルおよびヘキサン酸から選択される活性成分を組成物の全重量に対して少なくとも4重量%、蜜ろう、および任意選択的に1種または複数種の薬学的に許容される賦形剤を含有することを特徴とする医薬組成物、ならびに皮膚のプレバーンまたは熱傷を治療するため、かつ熱衝撃後の痛みを低減するためのその使用に関する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、熱傷により生じる皮膚の損傷および収縮を治療するのに有用な医薬組成物の分野、ならびにその使用および関連する治療的処置法にも関する。
【背景技術】
【0002】
化学的熱傷の場合を除く皮膚熱傷は、皮膚への熱的攻撃として定義することができる。皮膚熱傷は、皮膚、軟部組織、耳および眼、頭髪および体毛、爪、および骨さえの部分的または全体的な破壊を引き起こし得る。熱傷のほとんどは皮膚のみ、つまり表皮と真皮のみに影響を及ぼす。熱傷の重症度を評価するために、いくつかの因子、つまり患部表面領域、深さ、所在および熱傷の原因も考慮される。
【0003】
皮膚熱傷は通常、重症度に従って示される。第1度熱傷は一般に、紅斑に限定され、表皮の表面層のみ影響を受けている。第2度熱傷「A」は、表皮および真皮の一部にも影響する。これらの熱傷は、その表面の紅斑および水泡の出現によってそれ自体が顕在化する。この種類の熱傷は、神経が影響を受けるその程度に応じて、多少とも急性疼痛の原因となり得る。毛細血管の破断は既に、それと関連し得る。深部第2度熱傷「B」は、真皮を越えて、皮下軟部組織に達する。第3度熱傷は、表皮および真皮の全体的な破壊または溶融固化を生じさせる。この種類の熱傷は、血管組織、筋肉および神経などの皮下組織に損傷を与えることが多い。この種類の熱傷を治療するため、表皮の瘢痕化が理論的に可能ではないことから、皮膚移植を実施するのが慣行である。第4度熱傷は筋肉に影響し、骨にさえ及び得る。この場合には、皮膚の外観が、「炭化」していると言われ、推奨される処置は切断術である。この場合、患者の生命予後は、患者の年齢および患部表面領域に関係することが多い。
【0004】
熱傷は、
−固体、液体または気体熱源との接触(熱的熱傷)、
−熱源からの照射(熱的熱傷)、
−放射線治療などの特定の医学的治療、
−寒冷との接触(凍傷)、
−感電死(電気的熱傷)、
−化学製品との接触(化学的熱傷)、
−摩擦(一般に熱的熱傷にたとえられる摩擦熱傷)
などの様々な原因によって起こり得る。
【0005】
世界保健機関によると、熱傷は、世界中で毎年300,000人を超える死亡の原因である(戦争のケースを除いて)。フランスでは、2005年に、Direction Generale de l’Offre de Soins(DGOS)[Directorate General for Care Provision]は、医療的ケアの必要がある熱傷は400,000件を超えると列記しており、その70%が、家庭内の事故に関連すると思われる。鎮痛治療が必要な熱傷は、その集団の10%を含み得る。したがって、皮膚熱傷を治療するための医薬組成物を提案することが実際に必要とされている。
【0006】
熱傷の治療を目的とする医薬組成物は既に知られている。例えば、NL9101053号明細書には、ほぼ不溶性かつ不透過性である連続フィルムを形成する、水中油型エマルジョンが記述されている。この水中油型エマルジョンは、ステアリン酸セテアリルも含有し、炎症のある皮膚および治癒した熱傷の治療に有用である。
【0007】
それにもかかわらず、一般に第1度または第2度皮膚熱傷が完全治癒する時間は、最大2週間かかり得ることが確認されている。
【0008】
したがって、皮膚熱傷を治療するための他の医薬組成物および治療的処置法も提案することが必要であると思われる。
【発明の概要】
【0009】
本発明は、蜜ろうおよび任意選択的に1種または複数種の賦形剤と併せて、組成物の全重量に対して、オクタン酸セテアリルおよび/またはヘキサン酸から選択される活性成分を少なくとも約4重量%含む医薬組成物に関する。
【0010】
本発明の文脈において行われる研究は、熱傷形成プロセス中に、いくつかの段階、すなわち、
−1)熱傷の原因との接触(熱衝撃とも呼ばれる)、
−2)表皮、次いで真皮、皮下軟部組織、もしくは血管組織、またはさらには臓器の変形(または変化)の開始;この変形は、組織の縮小または収縮に関連し得る、
−3)熱の連続的な放射および組織に含まれる水の蒸発と平行する様々な局所または隣接組織の連続的な変形、
−4)組織の壊死および変形の安定化(皮膚熱傷の安定化は、重篤な症例では数ヶ月間かかる)、
を確認することができることを実証することを可能にした。
【0011】
これを考慮して、既に公知の医薬組成物は、組織壊死および変形が安定化した(ステージ4)後に、熱傷によって生じた皮膚損傷のみを治療すると考えられていることは意外であると思われる。その理由の1つは間違いなく、組織の内部変形(ステージ2および3)の変遷中ではなく、安定化段階(ステージ4)中に、医師が診察しているからである。
【0012】
しかしながら、したがって、熱傷形成プロセスの様々な段階(例えば、ステージ2、3および/または4)にて介入を想定することは可能であると思われる。本発明の利点の1つは、皮膚熱傷形成プロセス中の特定の状態、つまり上述されるステージ2および3に相当するプレバーン状態を確認することが可能となることである。本発明の目的では、「プレバーン」という用語は、表皮、真皮、およびその中に含有される水の蒸発と関連する組織の変形に相当する皮膚損傷であって、熱傷の原因との接触から始まって、一般に60秒以下の時間内、特に45秒以下の時間内で生じる皮膚損傷を意味する。
【0013】
したがって、本発明による医薬組成物は、それがまだプレバーンの問題(上記で定義されるステージ2および3)であるときに、皮膚損傷および変形を治療することを提案する。本発明のもう1つの利点は、プレバーン段階での皮膚損傷および変形の治療によって、安定化の前にそれが行われることから、より速く完全な治癒が可能となることが実証されることである。この治癒は、大部分の場合において300〜500%速いと考えられる。
【0014】
さらに、本発明による医薬組成物は、特定の脂質成分の内部供給による安定化された皮膚熱傷(ステージ4)の治療に有効であるだけでなく、特にプレバーン(ステージ2および3)の治療にも有効であることが実証されている。
【0015】
驚くべきことに、本発明による医薬組成物の使用によって、皮膚熱傷またはプレバーンの総治癒時間を大幅に低減することが可能となることが注目されている。
【0016】
いずれの理論にも束縛されることなく、熱源の衝撃によって生じる脱水は、本発明による医薬組成物の塗布によって即座に補われると思われる。本発明による組成物は、患部領域の細胞内に蒸発水を取り戻し、したがって血液または生理学的液体の流入を制限するために、患部領域を即座に水和することを可能にする。このようにして、紅斑または水疱の形成はかなり制限される。さらに、この急速な組織の再水和によって、その壊死またはその悪化を低減することが可能となる。また、正常な体温と比較して、プレバーン段階で観察される、皮膚損傷によって示される温度が高いほど、医薬組成物の浸透がよくなると思われる。したがって、熱傷が完全に治癒するための時間は著しく低減される。さらに、この完全な、かつ急速な治癒によって、局所血流の状態に応じて、7日後に現れることが多い微生物感染のリスクに伴う問題を避けることが可能となる。さらに、神経終末の圧迫が少ないため、感じる痛みが低減される。重篤ではない症例では、収縮した組織により神経が圧迫されないために、それは10分後に消失する。したがって、本発明の医薬組成物を使用することによって、熱傷した肢の使用を妨げ、かつ感染を予防するための治療を必要とする、皮膚の後遺症を低減することが可能となる。さらに、本発明による組成物の使用によって、通常数ヶ月間、目に見える状態である瘢痕化を低減することも可能となる。
【0017】
驚くべきことに、本発明による組成物は、急速な皮膚浸透を示すことが確認されている。
【0018】
本発明の主題は、皮膚熱傷を治療するために、特に皮膚プレバーンを治療するための、本発明による医薬組成物の使用にも関する。
【0019】
本発明の他の主題は、前記医薬組成物を皮膚熱傷と、特に皮膚プレバーンと接触させることを特徴とする、治療的方法に関する。
【図面の簡単な説明】
【0020】
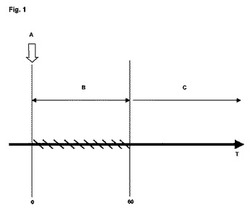
【図1】図1は、本発明による医薬組成物の作用機序を図解するスキームである。
【0021】
(T)は、時間(秒)の軸を表す。(A)は、熱の原因(または熱衝撃)との接触を表す。(B)は、その期間中に本発明による組成物が優先的に作用し、かつ0〜60秒である、皮膚プレバーンの期間に相当する。(C)は、組織壊死および変形の安定化の期間に相当する(安定化された熱傷)。
【発明を実施するための形態】
【0022】
本発明は、蜜ろうおよび任意選択的に1種または複数種の薬学的に許容される賦形剤と併せて、組成物の全重量に対して、オクタン酸セテアリルまたはヘキサン酸またはその両方の組み合わせから選択される活性成分を少なくとも4重量%含むことを特徴とする医薬組成物に関する。
【0023】
本発明に従うと、「オクタン酸セテアリル」という用語は、セチルアルコールのオクタン酸エステルおよび実験式C24H48O2のステアリルアルコールのオクタン酸エステルを意味する。
【0024】
本発明に従うと、「ヘキサン酸」という用語は、一般式C6H12O2の化合物を意味する。
【0025】
本発明に従うと、「蜜ろう」という用語は、天然の蜜ろうまたは合成蜜ろう(CAS 71243−51−1)またはサラシ蜜ろうを意味する。
【0026】
本発明において、「薬学的に許容される」という用語は、一般に安全な、非毒性の、生物学的にも他の点でも望ましくないものではなく、かつ特に局所適用による治療的使用に対して許容可能である、医薬組成物の製造で使用されるものを示すことが意図される。
【0027】
有利には、本発明による医薬組成物は、組成物の全重量に対して活性成分を4〜15重量%含む。本発明の一実施形態に従うと、医薬組成物は、組成物の全重量に対して活性成分を少なくとも4重量%、好ましくは少なくとも5重量%、好ましくは少なくとも6.5重量%、好ましくは少なくとも8重量%、好ましくは少なくとも10重量%、好ましくは少なくとも12重量%、またさらに好ましくは少なくとも14.5重量%含む。本発明の他の実施形態に従うと、医薬組成物は、組成物の全重量に対して活性成分を最大で15重量%、好ましくは最大で12重量%、好ましくは最大で10重量%、好ましくは最大で8重量%、好ましくは最大で6.5重量%、好ましくは最大で5重量%含む。優先的には、医薬組成物は、組成物の全重量に対して活性成分を4〜12重量%、好ましくは5〜10重量%、好ましくは6.5〜8重量%含む。
【0028】
好ましくは、医薬組成物は、医薬組成物の全重量に対して蜜ろうを2〜5重量%含む。本発明の一実施形態に従うと、医薬組成物は、医薬組成物の全重量に対して蜜ろうを少なくとも2重量%、好ましくは少なくとも2.2重量%、好ましくは少なくとも2.5重量%、好ましくは少なくとも3重量%、好ましくは少なくとも3.5重量%、および一実施形態に従うと少なくとも4重量%含む。本発明の他の実施形態に従うと、医薬組成物は、医薬組成物の全重量に対して蜜ろうを最大で5重量%、好ましくは最大で4重量%、好ましくは最大で重量3%、好ましくは少なくとも2.5重量%、かつ好ましくは少なくとも2.2重量%含む。有利には、医薬組成物は、本発明の全重量に対して蜜ろうを2〜5重量%、好ましくは2〜4重量%含む。
【0029】
有利には、活性成分と蜜ろうの比は0.8〜7.5である。一実施形態に従うと、前記比は、1.5〜5、好ましくは2〜4である。
【0030】
本発明の一実施形態に従うと、医薬組成物の活性成分は、オクタン酸セテアリルである。
【0031】
さらに、医薬組成物は、とりわけ医薬組成物の保湿性を高める目的で、デクスパンテノール(ビタミンB5)および/またはポリジメチルシロキサン(ジメチコーン)から選択される1種または複数種の添加剤も含有し得る。
【0032】
本発明の一実施形態に従うと、医薬組成物は、デクスパンテノールも含み得る。好ましくは、医薬組成物は、組成物の全重量に対してデクスパンテノールを0.1〜5重量%含む。本発明の一実施形態に従うと、医薬組成物は、組成物の全重量に対してデクスパンテノールを少なくとも0.1重量%、好ましくは少なくとも0.2重量%、好ましくは少なくとも0.3重量%、好ましくは少なくとも0.4重量%、好ましくは少なくとも1重量%、好ましくは少なくとも2重量%、好ましくは少なくとも3重量%、好ましくは少なくとも4重量%および好ましくは少なくとも4.5重量%含む。本発明の他の実施形態に従うと、医薬組成物は、組成物の全重量に対してデクスパンテノールを最大で5重量%、好ましくは最大で4重量%、好ましくは最大で3重量%、好ましくは最大で2重量%、好ましくは最大で0.4重量%、好ましくは最大で0.3重量%および好ましくは最大で0.2重量%含む。有利には、医薬組成物は、組成物の全重量に対してデクスパンテノールを0.2〜3重量%含む。
【0033】
本発明の一実施形態に従うと、医薬組成物はポリジメチルシロキサン(ジメチコーン)も含み得る。好ましくは、医薬組成物は、医薬組成物の全重量に対してポリジメチルシロキサンを2〜5重量%含む。本発明の一実施形態に従うと、医薬組成物は、医薬組成物の全重量に対してポリジメチルシロキサンを少なくとも2%重量、好ましくは少なくとも2.2重量%、好ましくは少なくとも2.5重量%、好ましくは少なくとも3重量%、好ましくは少なくとも4重量%、および一実施形態に従うと少なくとも4.5重量%含む。本発明の他の実施形態に従うと、医薬組成物は、医薬組成物の全重量に対してポリジメチルシロキサンを最大で5重量%、好ましくは最大で4重量%、好ましくは最大で3重量%、好ましくは最大で2.5重量%、および好ましくは最大で2.2重量%含む。有利には、医薬組成物は、本発明の全重量に対してポリジメチルシロキサンを2〜4重量%、好ましくは2〜3重量%含む。
【0034】
本発明の一実施形態に従うと、医薬組成物は、オクタン酸セテアリル、蜜ろう、デクスパンテノールおよびポリジメチルシロキサンを含む。
【0035】
医薬組成物は、細菌または真菌が原因の可能性のある感染を防ぐために、例えば消毒性および皮膚の鎮静および保湿性を有する1種または複数種の精油またはその誘導体も含み得る。精油は任意選択的に、精製されていてもよい。精油の誘導体は、例えば、精油のグリコール抽出物、チンキまたは温浸生成物である。この、またはこれらの精油またはその誘導体は、メラルーカ・アルターニフォリア(Melaleuca alterniflora)精油またはその誘導体、テペズコヒテ(Tepezcohuite)精油またはその誘導体、ユーカリ(eucalyptus)精油またはその誘導体、タイム精油またはその誘導体、ローズマリー精油またはその誘導体、レモン精油またはその誘導体、クローバ精油またはその誘導体、シナモン精油またはその誘導体、マツ精油またはその誘導体、ラベンダー精油またはその誘導体、ロックローズ(Cistus ladaniferus)精油またはその誘導体、セントジョンズワート(St John’s Wort)精油またはその誘導体およびジャコウバラ精油またはその誘導体からなる群から選択することができる。
【0036】
好ましくは、精油またはその誘導体は、メラルーカ・アルターニフォリア(Melaleuca alterniflora)精油またはその誘導体、テペズコヒテ(Tepezcohuite)精油またはその誘導体、セントジョンズワート(St John’s Wort)精油またはその誘導体、およびジャコウバラ精油またはその誘導体からなる群から選択される。
【0037】
精油の誘導体に関して、特に、テペズコヒテ(Tepezcohuite)のグリコール抽出物またはチンキまたは温浸生成物が挙げられる。セントジョンズワート(St John’s Wort)のグリコール抽出物またはチンキまたは温浸生成物も挙げられる。
【0038】
本発明の一実施形態に従うと、医薬組成物は、組成物の全重量に対して精油またはその誘導体を0.01〜10重量%、好ましくは組成物の全重量に対して精油またはその誘導体を0.1〜5重量%含む。
【0039】
医薬組成物は、以下の群、すなわち、リドカイン、プリロカイン、スカンジカイン、エチドカイン、ブピバカイン、ロピバカイン、レボブピバカイン、アルチカインおよびメピバカインから選択される1種または複数種の局所麻酔薬も含有し得る。本発明の一実施形態に従うと、それはリドカインである。好ましくは、医薬組成物は、医薬組成物の全重量に対して局所麻酔薬を10〜20重量%含む。一実施形態に従うと、医薬組成物は、医薬組成物の全重量に対して局所麻酔薬を少なくとも10重量%、好ましくは少なくとも15重量%、好ましくは少なくとも18重量%含む。他の実施形態に従うと、医薬組成物は、医薬組成物の全重量に対して局所麻酔薬を最大で20重量%、好ましくは最大で15重量%、好ましくは最大で12重量%含む。有利には、医薬組成物は、医薬組成物の全重量に対して局所麻酔薬を10〜15重量%含む。
【0040】
一実施形態に従うと、医薬組成物はアラントインも含み得る。
【0041】
医薬組成物は、活性成分の特性および利便性を向上させるために、特に皮膚浸透を可能にする賦形剤を有する、局所投与で通常知られている形態、特にローション、フォーム、ジェル、分散液、油中水型もしくは水中油型エマルジョンまたはマルチプルエマルション、スプレー、漿液、マスク、ボディーミルクまたはクリームの形をとり得る。医薬組成物は、注射による投与で通常知られている形態をとり得る。「注射」という用語は、皮下または皮内投与を意味することが意図される。この場合、医薬組成物は、例えば滅菌シリンジに組み込まれた注射可能な形態をとる。シリンジは、例えばベータ線またはガンマ線で処理することによって滅菌することができる。
【0042】
有利には、医薬組成物は、油中水型エマルジョンまたは水中油型エマルジョンである。
【0043】
医薬組成物は、局所的に(例えば、皮膚用組成物)、または注射によって投与されることが意図される医薬組成物の分野で通常使用される賦形剤も含み得る。
【0044】
本発明の医薬組成物の脂肪相は、油、ガム、ペーストおよびワックスなどの親油性化合物も含み得る。
【0045】
油は好ましくは、植物油、動物油、鉱油、合成油、シリコーン油、液体脂肪酸エステル、液体脂肪酸および液体脂肪酸アミドから選択される。
【0046】
植物油として、特に甘扁桃油(Prunus amygdalus dulcis)油、アボガド油、ヒマシ油、オリーブ油、ホホバ液体ワックス、ヒマワリ油、麦芽油、ゴマ油、ラッカセイ油、グレープシード油、ダイズ油、ナタネ油、サフラワー油、ヤシ油、トウモロコシ油、ヘイゼルナッツ油、杏仁油およびビューティー・リーフ油が挙げられる。
【0047】
動物油として、特にパーヒドロスクアレンが挙げられる。
【0048】
合成油として、スクアレン、イソドデカンまたはイソヘキサデカンなどのポリ(α−オレフィン)、エステル交換された植物油およびフルオロ油が挙げられる。
【0049】
シリコーン油として、デカメチルペンタシロキサンなどの環状ポリジメチルシロキサン(例えば、シクロメチコーンまたはジメチコーン)および低粘度直鎖状ポリメチルシロキサン(150〜500cst)が挙げられる。
【0050】
医薬組成物で使用される蜜ろうに加えて、使用することができるワックス、例えば動物、植物、鉱物または合成起源のワックス、例えばフルオロもしくはパーフルオロワックス、ラノリンワックス、カンデリラ、カカオ脂およびシアバターワックス、ファーツリーワックス、綿実ろう;マイクロクリスタリンワックス、パラフィンワックス、ペトロラタム、石油ゼリー、地蝋;水素化ホホバ油などの40℃を超える融点を有する水素化油、およびポリエチレンワックスを任意に含有し得る。
【0051】
医薬組成物は、通常使用される乳化剤も含有し得る。乳化システムは特に、エトキシ化脂肪アルコール、脂肪酸のエステルおよびPEGのエステル、エトキシ化脂肪酸部分グリセリド、ポリグリセロール化脂肪酸トリグリセリドおよびそのエトキシ化誘導体から選択される1種または複数種の化合物を含み得る。挙げられる適切なエトキシ化脂肪アルコールは、エチレンオキシドとベヘニルアルコールとの付加生成物、特にオキシエチレン基6〜12個を含む生成物(例えば、Beheneth−9またはBeheneth−10);エチレンオキシドとステアリルアルコールとの付加生成物、特にオキシエチレン基6〜12個を含む生成物(例えば、steareth−9);エチレンオキシドとイソステアリルアルコールとの付加生成物、例えばオキシエチレン基6〜12個を含む生成物(isosteareth−9)、およびその混合物である。
【0052】
医薬組成物は、非イオン界面活性剤、上述のものと異なるオキシエチレン化脂肪アルコール、つまりエチレンオキシドとラウリルアルコールとの付加生成物(laureth−9〜laureth−50);エチレンオキシドとセテアリルまたはセチルステアリルアルコールとの付加生成物(ceteareth−9〜ceteareth−30)、エチレンオキシドとセチルアルコールとの付加生成物(ceteth−9〜ceteth−30);およびその混合物を含み得る。
【0053】
更なる界面活性剤が、組成物中に任意に含まれ得る。これらの更なる界面活性剤は、炭素原子8〜30個を有する脂肪酸の塩、例えばパルミチン酸、ステアリン酸またはベヘン酸の塩、グリセロールの脂肪酸エステル、例えばステアリン酸グリセリル;エチレンオキシド基2〜8個を有する、脂肪酸塩のオキシエチレン化誘導体およびグリセロールの脂肪酸エステルのオキシエチレン化誘導体、およびその混合であり得る。
【0054】
医薬組成物は、医薬組成物の分野で通常使用される防腐剤も含み得る。それらは、特に、1つまたは複数の芳香族置換基を含有し得るアルコール、例えば2−フェノキシエタノールなどのフェノキシエタノールまたは1−フェノキシ−2−プロパノール、ベンジルアルコール、2−ヒドロキシビフェニル、メチルパラベン、エチルパラベン、プロピルパラベン、ブチルパラベン、イソブチルパラベン、ナトリウムメチルパラベン、ナトリウムエチルパラベン、ナトリウムプロピルパラベン、ナトリウムブチルパラベンまたはナトリウムイソブチルパラベンなどのパラベン、エチル、ブチル、プロピルまたはメチルp−ヒドロキシベンゾエート、イミダゾリジニル尿素、ジアゾリジニル尿素、ヒドロキシメチルグリシン酸ナトリウム、ハロゲン化誘導体、例えばヨードプロピニルブチルカルバメート、2−ブロモ−2−ニトロプロパン−1,3−ジオール、2,4,4’−トリクロロ−2’−ヒドロキシジフェニルエーテル(トリクロサン)、3,4,4’−トリクロロカルバニリド(トリクロカルバン)、クロルブタヌルム、2,4−ジクロロベンジルアルコール、N−(4−クロロフェニル)−N’−(3,4−ジクロロフェニル)尿素、1,2−ジブロモ−2,4−ジシアノブタン、クロロキシレノール、ケトコナゾール、オキシコナゾール、ブトコナゾール、クロトリマゾール、エコナゾール、エニルコナゾール、フェンチコナゾール、ミコナゾール、スルコナゾール、チオコナゾール、フルコナゾール、イトラコナゾール、テルコナゾール、1つまたは複数のカチオン性窒素を含有する作用薬、例えば塩化セチルトリメチルアンモニウム、塩化セチルピリジニウム、塩化ベンゼトニウムまたは塩化ベンザルコニウム(過ホウ酸塩安定化過酸化水素と任意に組み合わせられる)、ジイソブチルエトキシエチルジメチルベンジルアンモニウムクロリド、ジイソブチルフェノキシエトキシエチルジメチルベンジルアンモニウムクロリド、N−アルキル−N,N−ジメチルベンジルアンモニウムクロリド、ブロミドまたはサッカリネート、トリメチルアンモニウムクロリド、クロロヒドロキシ酢酸ナトリウムアルミニウム、塩化トリセチルメチルアンモニウム、ジアミノアルキルアミド、クエン酸などの有機酸およびその塩から選択される、防腐剤などの抗菌剤または抗真菌剤、ファルネソール、テルビナフィンまたはナフチフィンなどの不飽和抗菌剤、ビフォナゾール、クロコナゾールまたはイソコナゾールなどの複素環式芳香族剤、当業者に公知の他のいずれかの抗菌剤または抗真菌剤;およびその混合物であることができる。
【0055】
さらに、医薬組成物は、前記医薬組成物のpH範囲を調節するための酸および塩基も含み得る。その塩基は、無機(水酸化ナトリウム、水酸化カリウム、アンモニア水)またはモノ−、ジ−またはトリエタノールアミン、アミノメチルプロパンジオール、N−メチルグルカミン、アルギニンおよびリジンなどの塩基性アミノ酸などの有機塩基;およびその混合物であることができる。
【0056】
本発明は、皮膚熱傷を治療するための、特に皮膚のプレバーンを治療するための、上述の医薬組成物の使用にも関する。
【0057】
本発明による医薬組成物は、異なる原因の皮膚のプレバーンまたは熱傷、すなわち、熱源と接触または熱源からの放射によって生じる皮膚のプレバーンまたは熱傷、放射線治療などの医学的処置によって生じる皮膚のプレバーンまたは熱傷、寒冷との接触から生じる皮膚のプレバーンまたは熱傷、摩擦によって生じる皮膚のプレバーンまたは熱傷、太陽光への短時間の曝露によって生じる皮膚のプレバーンまたは熱傷を治療するのに有用である。有利なことには、本発明による医薬組成物は、熱源との接触または熱源からの放射によって生じる、放射線治療などの医学的処置によって生じる、または摩擦によって生じる、皮膚のプレバーンまたは熱傷に特に有用である。本発明の他の態様に従うと、医薬組成物は、粘膜(例えば、食道などの消化器系の壁または唇、泌尿生殖器領域等)のプレバーンまたは熱傷を治療するのに有用であり得る。本発明による医薬組成物は、第1度、第2度または第3度のプレバーンまたは熱傷を治療するのに有用である。
【0058】
本発明の一態様に従うと、この使用は、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり60秒以下の時間内で、あるいは注射による投与の場合にはプレバーンまたは熱傷の原因との接触から始まり30分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0059】
好ましくは、この使用は、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり45秒以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0060】
本発明の一実施形態に従うと、この使用は、注射による投与の場合にはプレバーンまたは熱傷の原因との接触から始まり25分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0061】
本発明の一実施形態に従うと、医薬組成物の使用は、60分間の間に続いて30回、または60分間に20回、または30分間に10回、または15分間に5回投与されることを特徴とする。
【0062】
本発明は、本発明による医薬組成物を皮膚熱傷と、特に皮膚のプレバーンと接触させることを特徴とする治療的処置法にも関する。
【0063】
有利には、この治療的処置法は、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり60秒以下の時間内で、または注射による投与の場合には30分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0064】
好ましくは、本発明による治療的処置法は、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり45秒以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0065】
一実施形態に従うと、本発明による治療的処置法は、注射による投与の場合にはプレバーンまたは熱傷の原因との接触から始まり25分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0066】
本発明は、熱衝撃により生じる痛みの強さを低減する治療的処置法であって、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり60秒以下の時間内で、あるいは注射による投与の場合には30分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする治療的処置法にも関する。
【実施例】
【0067】
−実施例1:臨床試験
−a)臨床試験プロトコル
異なる原因のプレバーンおよび異なる重症度を有する数名の患者に関して、本発明による医薬組成物を試験した。以下の場合のそれぞれに関して、熱傷の原因との接触から始まり45秒の時間内に、次いで定義された期間中に定期的に、医薬組成物を皮膚のプレバーンに直接適用した。
【0068】
−b)臨床試験の結果
−患者1:この患者は、第2度プレバーンを示し、その原因は、350℃に加熱されたオーブン発熱体に腕を直接接触させたことから生じた。350℃に加熱されたオーブン発熱体との接触から開始して45秒の時間内に、本発明による医薬組成物を適用し、次いで15分間で3分毎に適用し、次いで2日間定期的に適用した。この期間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。痛みは3時間後に消失した。
【0069】
−患者2:この患者は、400℃の赤熱ドリルビットに手掌を接触させたことによって生じた第2度プレバーンを示した。赤熱ドリルビットとの接触から開始して45秒の時間内に本発明による医薬組成物を適用し、次いで2日間定期的に適用した。この期間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。痛みは2時間後に消失した。
【0070】
−患者3:この患者は、蒸気に手が接触したことによって生じた第1度プレバーンを示した。蒸気との接触から開始して45秒の時間内に本発明による医薬組成物を適用し、次いで3時間定期的に適用した。この期間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。このケースは他の患者5名についても繰り返した。痛みは10分後に消失した。
【0071】
−患者4:この患者は、熱を持ったチェーンソーの鎖からの患者の大腿への摩擦によって生じた第2度「A」プレバーンを示した。チェーンソーの鎖との接触から開始して45秒の時間内に、本発明による医薬組成物を適用し、次いで3日間定期的に適用した。この期間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。痛みは10時間後に消失した。
【0072】
−患者5:この患者は、オートバイの排気管に足を接触したことから生じた第2度「B」プレバーンを示した。オートバイの排気管との接触から開始して45秒の時間内に本発明による医薬組成物を適用し、次いで3日間定期的に適用した。5日間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。痛みは24時間後に消失した。
【0073】
これらの結果から、本発明による医薬組成物が、皮膚のプレバーンを治療し、それによって生じた皮膚損傷を著しく低減するのに特に有効であることが実証されている。第2度熱傷により生じた皮膚損傷が消失するのに必要な時間はおよそ2週間であると通常は確認されているが、本発明による医薬組成物を使用した場合には、この時間は2または3日間に低減される。治癒時間のこの有意な減少によって、熱傷により起こる皮膚損傷の場合には7日後に現れることが多い微生物(細菌または真菌起源)による感染のリスクも低減することが可能となる。さらに、本発明による医薬組成物を使用することによって、皮膚損傷が原因の痛みが著しく低減されることに留意されたい。
【0074】
−実施例2:本発明による医薬組成物

【技術分野】
【0001】
本発明は、熱傷により生じる皮膚の損傷および収縮を治療するのに有用な医薬組成物の分野、ならびにその使用および関連する治療的処置法にも関する。
【背景技術】
【0002】
化学的熱傷の場合を除く皮膚熱傷は、皮膚への熱的攻撃として定義することができる。皮膚熱傷は、皮膚、軟部組織、耳および眼、頭髪および体毛、爪、および骨さえの部分的または全体的な破壊を引き起こし得る。熱傷のほとんどは皮膚のみ、つまり表皮と真皮のみに影響を及ぼす。熱傷の重症度を評価するために、いくつかの因子、つまり患部表面領域、深さ、所在および熱傷の原因も考慮される。
【0003】
皮膚熱傷は通常、重症度に従って示される。第1度熱傷は一般に、紅斑に限定され、表皮の表面層のみ影響を受けている。第2度熱傷「A」は、表皮および真皮の一部にも影響する。これらの熱傷は、その表面の紅斑および水泡の出現によってそれ自体が顕在化する。この種類の熱傷は、神経が影響を受けるその程度に応じて、多少とも急性疼痛の原因となり得る。毛細血管の破断は既に、それと関連し得る。深部第2度熱傷「B」は、真皮を越えて、皮下軟部組織に達する。第3度熱傷は、表皮および真皮の全体的な破壊または溶融固化を生じさせる。この種類の熱傷は、血管組織、筋肉および神経などの皮下組織に損傷を与えることが多い。この種類の熱傷を治療するため、表皮の瘢痕化が理論的に可能ではないことから、皮膚移植を実施するのが慣行である。第4度熱傷は筋肉に影響し、骨にさえ及び得る。この場合には、皮膚の外観が、「炭化」していると言われ、推奨される処置は切断術である。この場合、患者の生命予後は、患者の年齢および患部表面領域に関係することが多い。
【0004】
熱傷は、
−固体、液体または気体熱源との接触(熱的熱傷)、
−熱源からの照射(熱的熱傷)、
−放射線治療などの特定の医学的治療、
−寒冷との接触(凍傷)、
−感電死(電気的熱傷)、
−化学製品との接触(化学的熱傷)、
−摩擦(一般に熱的熱傷にたとえられる摩擦熱傷)
などの様々な原因によって起こり得る。
【0005】
世界保健機関によると、熱傷は、世界中で毎年300,000人を超える死亡の原因である(戦争のケースを除いて)。フランスでは、2005年に、Direction Generale de l’Offre de Soins(DGOS)[Directorate General for Care Provision]は、医療的ケアの必要がある熱傷は400,000件を超えると列記しており、その70%が、家庭内の事故に関連すると思われる。鎮痛治療が必要な熱傷は、その集団の10%を含み得る。したがって、皮膚熱傷を治療するための医薬組成物を提案することが実際に必要とされている。
【0006】
熱傷の治療を目的とする医薬組成物は既に知られている。例えば、NL9101053号明細書には、ほぼ不溶性かつ不透過性である連続フィルムを形成する、水中油型エマルジョンが記述されている。この水中油型エマルジョンは、ステアリン酸セテアリルも含有し、炎症のある皮膚および治癒した熱傷の治療に有用である。
【0007】
それにもかかわらず、一般に第1度または第2度皮膚熱傷が完全治癒する時間は、最大2週間かかり得ることが確認されている。
【0008】
したがって、皮膚熱傷を治療するための他の医薬組成物および治療的処置法も提案することが必要であると思われる。
【発明の概要】
【0009】
本発明は、蜜ろうおよび任意選択的に1種または複数種の賦形剤と併せて、組成物の全重量に対して、オクタン酸セテアリルおよび/またはヘキサン酸から選択される活性成分を少なくとも約4重量%含む医薬組成物に関する。
【0010】
本発明の文脈において行われる研究は、熱傷形成プロセス中に、いくつかの段階、すなわち、
−1)熱傷の原因との接触(熱衝撃とも呼ばれる)、
−2)表皮、次いで真皮、皮下軟部組織、もしくは血管組織、またはさらには臓器の変形(または変化)の開始;この変形は、組織の縮小または収縮に関連し得る、
−3)熱の連続的な放射および組織に含まれる水の蒸発と平行する様々な局所または隣接組織の連続的な変形、
−4)組織の壊死および変形の安定化(皮膚熱傷の安定化は、重篤な症例では数ヶ月間かかる)、
を確認することができることを実証することを可能にした。
【0011】
これを考慮して、既に公知の医薬組成物は、組織壊死および変形が安定化した(ステージ4)後に、熱傷によって生じた皮膚損傷のみを治療すると考えられていることは意外であると思われる。その理由の1つは間違いなく、組織の内部変形(ステージ2および3)の変遷中ではなく、安定化段階(ステージ4)中に、医師が診察しているからである。
【0012】
しかしながら、したがって、熱傷形成プロセスの様々な段階(例えば、ステージ2、3および/または4)にて介入を想定することは可能であると思われる。本発明の利点の1つは、皮膚熱傷形成プロセス中の特定の状態、つまり上述されるステージ2および3に相当するプレバーン状態を確認することが可能となることである。本発明の目的では、「プレバーン」という用語は、表皮、真皮、およびその中に含有される水の蒸発と関連する組織の変形に相当する皮膚損傷であって、熱傷の原因との接触から始まって、一般に60秒以下の時間内、特に45秒以下の時間内で生じる皮膚損傷を意味する。
【0013】
したがって、本発明による医薬組成物は、それがまだプレバーンの問題(上記で定義されるステージ2および3)であるときに、皮膚損傷および変形を治療することを提案する。本発明のもう1つの利点は、プレバーン段階での皮膚損傷および変形の治療によって、安定化の前にそれが行われることから、より速く完全な治癒が可能となることが実証されることである。この治癒は、大部分の場合において300〜500%速いと考えられる。
【0014】
さらに、本発明による医薬組成物は、特定の脂質成分の内部供給による安定化された皮膚熱傷(ステージ4)の治療に有効であるだけでなく、特にプレバーン(ステージ2および3)の治療にも有効であることが実証されている。
【0015】
驚くべきことに、本発明による医薬組成物の使用によって、皮膚熱傷またはプレバーンの総治癒時間を大幅に低減することが可能となることが注目されている。
【0016】
いずれの理論にも束縛されることなく、熱源の衝撃によって生じる脱水は、本発明による医薬組成物の塗布によって即座に補われると思われる。本発明による組成物は、患部領域の細胞内に蒸発水を取り戻し、したがって血液または生理学的液体の流入を制限するために、患部領域を即座に水和することを可能にする。このようにして、紅斑または水疱の形成はかなり制限される。さらに、この急速な組織の再水和によって、その壊死またはその悪化を低減することが可能となる。また、正常な体温と比較して、プレバーン段階で観察される、皮膚損傷によって示される温度が高いほど、医薬組成物の浸透がよくなると思われる。したがって、熱傷が完全に治癒するための時間は著しく低減される。さらに、この完全な、かつ急速な治癒によって、局所血流の状態に応じて、7日後に現れることが多い微生物感染のリスクに伴う問題を避けることが可能となる。さらに、神経終末の圧迫が少ないため、感じる痛みが低減される。重篤ではない症例では、収縮した組織により神経が圧迫されないために、それは10分後に消失する。したがって、本発明の医薬組成物を使用することによって、熱傷した肢の使用を妨げ、かつ感染を予防するための治療を必要とする、皮膚の後遺症を低減することが可能となる。さらに、本発明による組成物の使用によって、通常数ヶ月間、目に見える状態である瘢痕化を低減することも可能となる。
【0017】
驚くべきことに、本発明による組成物は、急速な皮膚浸透を示すことが確認されている。
【0018】
本発明の主題は、皮膚熱傷を治療するために、特に皮膚プレバーンを治療するための、本発明による医薬組成物の使用にも関する。
【0019】
本発明の他の主題は、前記医薬組成物を皮膚熱傷と、特に皮膚プレバーンと接触させることを特徴とする、治療的方法に関する。
【図面の簡単な説明】
【0020】
【図1】図1は、本発明による医薬組成物の作用機序を図解するスキームである。
【0021】
(T)は、時間(秒)の軸を表す。(A)は、熱の原因(または熱衝撃)との接触を表す。(B)は、その期間中に本発明による組成物が優先的に作用し、かつ0〜60秒である、皮膚プレバーンの期間に相当する。(C)は、組織壊死および変形の安定化の期間に相当する(安定化された熱傷)。
【発明を実施するための形態】
【0022】
本発明は、蜜ろうおよび任意選択的に1種または複数種の薬学的に許容される賦形剤と併せて、組成物の全重量に対して、オクタン酸セテアリルまたはヘキサン酸またはその両方の組み合わせから選択される活性成分を少なくとも4重量%含むことを特徴とする医薬組成物に関する。
【0023】
本発明に従うと、「オクタン酸セテアリル」という用語は、セチルアルコールのオクタン酸エステルおよび実験式C24H48O2のステアリルアルコールのオクタン酸エステルを意味する。
【0024】
本発明に従うと、「ヘキサン酸」という用語は、一般式C6H12O2の化合物を意味する。
【0025】
本発明に従うと、「蜜ろう」という用語は、天然の蜜ろうまたは合成蜜ろう(CAS 71243−51−1)またはサラシ蜜ろうを意味する。
【0026】
本発明において、「薬学的に許容される」という用語は、一般に安全な、非毒性の、生物学的にも他の点でも望ましくないものではなく、かつ特に局所適用による治療的使用に対して許容可能である、医薬組成物の製造で使用されるものを示すことが意図される。
【0027】
有利には、本発明による医薬組成物は、組成物の全重量に対して活性成分を4〜15重量%含む。本発明の一実施形態に従うと、医薬組成物は、組成物の全重量に対して活性成分を少なくとも4重量%、好ましくは少なくとも5重量%、好ましくは少なくとも6.5重量%、好ましくは少なくとも8重量%、好ましくは少なくとも10重量%、好ましくは少なくとも12重量%、またさらに好ましくは少なくとも14.5重量%含む。本発明の他の実施形態に従うと、医薬組成物は、組成物の全重量に対して活性成分を最大で15重量%、好ましくは最大で12重量%、好ましくは最大で10重量%、好ましくは最大で8重量%、好ましくは最大で6.5重量%、好ましくは最大で5重量%含む。優先的には、医薬組成物は、組成物の全重量に対して活性成分を4〜12重量%、好ましくは5〜10重量%、好ましくは6.5〜8重量%含む。
【0028】
好ましくは、医薬組成物は、医薬組成物の全重量に対して蜜ろうを2〜5重量%含む。本発明の一実施形態に従うと、医薬組成物は、医薬組成物の全重量に対して蜜ろうを少なくとも2重量%、好ましくは少なくとも2.2重量%、好ましくは少なくとも2.5重量%、好ましくは少なくとも3重量%、好ましくは少なくとも3.5重量%、および一実施形態に従うと少なくとも4重量%含む。本発明の他の実施形態に従うと、医薬組成物は、医薬組成物の全重量に対して蜜ろうを最大で5重量%、好ましくは最大で4重量%、好ましくは最大で重量3%、好ましくは少なくとも2.5重量%、かつ好ましくは少なくとも2.2重量%含む。有利には、医薬組成物は、本発明の全重量に対して蜜ろうを2〜5重量%、好ましくは2〜4重量%含む。
【0029】
有利には、活性成分と蜜ろうの比は0.8〜7.5である。一実施形態に従うと、前記比は、1.5〜5、好ましくは2〜4である。
【0030】
本発明の一実施形態に従うと、医薬組成物の活性成分は、オクタン酸セテアリルである。
【0031】
さらに、医薬組成物は、とりわけ医薬組成物の保湿性を高める目的で、デクスパンテノール(ビタミンB5)および/またはポリジメチルシロキサン(ジメチコーン)から選択される1種または複数種の添加剤も含有し得る。
【0032】
本発明の一実施形態に従うと、医薬組成物は、デクスパンテノールも含み得る。好ましくは、医薬組成物は、組成物の全重量に対してデクスパンテノールを0.1〜5重量%含む。本発明の一実施形態に従うと、医薬組成物は、組成物の全重量に対してデクスパンテノールを少なくとも0.1重量%、好ましくは少なくとも0.2重量%、好ましくは少なくとも0.3重量%、好ましくは少なくとも0.4重量%、好ましくは少なくとも1重量%、好ましくは少なくとも2重量%、好ましくは少なくとも3重量%、好ましくは少なくとも4重量%および好ましくは少なくとも4.5重量%含む。本発明の他の実施形態に従うと、医薬組成物は、組成物の全重量に対してデクスパンテノールを最大で5重量%、好ましくは最大で4重量%、好ましくは最大で3重量%、好ましくは最大で2重量%、好ましくは最大で0.4重量%、好ましくは最大で0.3重量%および好ましくは最大で0.2重量%含む。有利には、医薬組成物は、組成物の全重量に対してデクスパンテノールを0.2〜3重量%含む。
【0033】
本発明の一実施形態に従うと、医薬組成物はポリジメチルシロキサン(ジメチコーン)も含み得る。好ましくは、医薬組成物は、医薬組成物の全重量に対してポリジメチルシロキサンを2〜5重量%含む。本発明の一実施形態に従うと、医薬組成物は、医薬組成物の全重量に対してポリジメチルシロキサンを少なくとも2%重量、好ましくは少なくとも2.2重量%、好ましくは少なくとも2.5重量%、好ましくは少なくとも3重量%、好ましくは少なくとも4重量%、および一実施形態に従うと少なくとも4.5重量%含む。本発明の他の実施形態に従うと、医薬組成物は、医薬組成物の全重量に対してポリジメチルシロキサンを最大で5重量%、好ましくは最大で4重量%、好ましくは最大で3重量%、好ましくは最大で2.5重量%、および好ましくは最大で2.2重量%含む。有利には、医薬組成物は、本発明の全重量に対してポリジメチルシロキサンを2〜4重量%、好ましくは2〜3重量%含む。
【0034】
本発明の一実施形態に従うと、医薬組成物は、オクタン酸セテアリル、蜜ろう、デクスパンテノールおよびポリジメチルシロキサンを含む。
【0035】
医薬組成物は、細菌または真菌が原因の可能性のある感染を防ぐために、例えば消毒性および皮膚の鎮静および保湿性を有する1種または複数種の精油またはその誘導体も含み得る。精油は任意選択的に、精製されていてもよい。精油の誘導体は、例えば、精油のグリコール抽出物、チンキまたは温浸生成物である。この、またはこれらの精油またはその誘導体は、メラルーカ・アルターニフォリア(Melaleuca alterniflora)精油またはその誘導体、テペズコヒテ(Tepezcohuite)精油またはその誘導体、ユーカリ(eucalyptus)精油またはその誘導体、タイム精油またはその誘導体、ローズマリー精油またはその誘導体、レモン精油またはその誘導体、クローバ精油またはその誘導体、シナモン精油またはその誘導体、マツ精油またはその誘導体、ラベンダー精油またはその誘導体、ロックローズ(Cistus ladaniferus)精油またはその誘導体、セントジョンズワート(St John’s Wort)精油またはその誘導体およびジャコウバラ精油またはその誘導体からなる群から選択することができる。
【0036】
好ましくは、精油またはその誘導体は、メラルーカ・アルターニフォリア(Melaleuca alterniflora)精油またはその誘導体、テペズコヒテ(Tepezcohuite)精油またはその誘導体、セントジョンズワート(St John’s Wort)精油またはその誘導体、およびジャコウバラ精油またはその誘導体からなる群から選択される。
【0037】
精油の誘導体に関して、特に、テペズコヒテ(Tepezcohuite)のグリコール抽出物またはチンキまたは温浸生成物が挙げられる。セントジョンズワート(St John’s Wort)のグリコール抽出物またはチンキまたは温浸生成物も挙げられる。
【0038】
本発明の一実施形態に従うと、医薬組成物は、組成物の全重量に対して精油またはその誘導体を0.01〜10重量%、好ましくは組成物の全重量に対して精油またはその誘導体を0.1〜5重量%含む。
【0039】
医薬組成物は、以下の群、すなわち、リドカイン、プリロカイン、スカンジカイン、エチドカイン、ブピバカイン、ロピバカイン、レボブピバカイン、アルチカインおよびメピバカインから選択される1種または複数種の局所麻酔薬も含有し得る。本発明の一実施形態に従うと、それはリドカインである。好ましくは、医薬組成物は、医薬組成物の全重量に対して局所麻酔薬を10〜20重量%含む。一実施形態に従うと、医薬組成物は、医薬組成物の全重量に対して局所麻酔薬を少なくとも10重量%、好ましくは少なくとも15重量%、好ましくは少なくとも18重量%含む。他の実施形態に従うと、医薬組成物は、医薬組成物の全重量に対して局所麻酔薬を最大で20重量%、好ましくは最大で15重量%、好ましくは最大で12重量%含む。有利には、医薬組成物は、医薬組成物の全重量に対して局所麻酔薬を10〜15重量%含む。
【0040】
一実施形態に従うと、医薬組成物はアラントインも含み得る。
【0041】
医薬組成物は、活性成分の特性および利便性を向上させるために、特に皮膚浸透を可能にする賦形剤を有する、局所投与で通常知られている形態、特にローション、フォーム、ジェル、分散液、油中水型もしくは水中油型エマルジョンまたはマルチプルエマルション、スプレー、漿液、マスク、ボディーミルクまたはクリームの形をとり得る。医薬組成物は、注射による投与で通常知られている形態をとり得る。「注射」という用語は、皮下または皮内投与を意味することが意図される。この場合、医薬組成物は、例えば滅菌シリンジに組み込まれた注射可能な形態をとる。シリンジは、例えばベータ線またはガンマ線で処理することによって滅菌することができる。
【0042】
有利には、医薬組成物は、油中水型エマルジョンまたは水中油型エマルジョンである。
【0043】
医薬組成物は、局所的に(例えば、皮膚用組成物)、または注射によって投与されることが意図される医薬組成物の分野で通常使用される賦形剤も含み得る。
【0044】
本発明の医薬組成物の脂肪相は、油、ガム、ペーストおよびワックスなどの親油性化合物も含み得る。
【0045】
油は好ましくは、植物油、動物油、鉱油、合成油、シリコーン油、液体脂肪酸エステル、液体脂肪酸および液体脂肪酸アミドから選択される。
【0046】
植物油として、特に甘扁桃油(Prunus amygdalus dulcis)油、アボガド油、ヒマシ油、オリーブ油、ホホバ液体ワックス、ヒマワリ油、麦芽油、ゴマ油、ラッカセイ油、グレープシード油、ダイズ油、ナタネ油、サフラワー油、ヤシ油、トウモロコシ油、ヘイゼルナッツ油、杏仁油およびビューティー・リーフ油が挙げられる。
【0047】
動物油として、特にパーヒドロスクアレンが挙げられる。
【0048】
合成油として、スクアレン、イソドデカンまたはイソヘキサデカンなどのポリ(α−オレフィン)、エステル交換された植物油およびフルオロ油が挙げられる。
【0049】
シリコーン油として、デカメチルペンタシロキサンなどの環状ポリジメチルシロキサン(例えば、シクロメチコーンまたはジメチコーン)および低粘度直鎖状ポリメチルシロキサン(150〜500cst)が挙げられる。
【0050】
医薬組成物で使用される蜜ろうに加えて、使用することができるワックス、例えば動物、植物、鉱物または合成起源のワックス、例えばフルオロもしくはパーフルオロワックス、ラノリンワックス、カンデリラ、カカオ脂およびシアバターワックス、ファーツリーワックス、綿実ろう;マイクロクリスタリンワックス、パラフィンワックス、ペトロラタム、石油ゼリー、地蝋;水素化ホホバ油などの40℃を超える融点を有する水素化油、およびポリエチレンワックスを任意に含有し得る。
【0051】
医薬組成物は、通常使用される乳化剤も含有し得る。乳化システムは特に、エトキシ化脂肪アルコール、脂肪酸のエステルおよびPEGのエステル、エトキシ化脂肪酸部分グリセリド、ポリグリセロール化脂肪酸トリグリセリドおよびそのエトキシ化誘導体から選択される1種または複数種の化合物を含み得る。挙げられる適切なエトキシ化脂肪アルコールは、エチレンオキシドとベヘニルアルコールとの付加生成物、特にオキシエチレン基6〜12個を含む生成物(例えば、Beheneth−9またはBeheneth−10);エチレンオキシドとステアリルアルコールとの付加生成物、特にオキシエチレン基6〜12個を含む生成物(例えば、steareth−9);エチレンオキシドとイソステアリルアルコールとの付加生成物、例えばオキシエチレン基6〜12個を含む生成物(isosteareth−9)、およびその混合物である。
【0052】
医薬組成物は、非イオン界面活性剤、上述のものと異なるオキシエチレン化脂肪アルコール、つまりエチレンオキシドとラウリルアルコールとの付加生成物(laureth−9〜laureth−50);エチレンオキシドとセテアリルまたはセチルステアリルアルコールとの付加生成物(ceteareth−9〜ceteareth−30)、エチレンオキシドとセチルアルコールとの付加生成物(ceteth−9〜ceteth−30);およびその混合物を含み得る。
【0053】
更なる界面活性剤が、組成物中に任意に含まれ得る。これらの更なる界面活性剤は、炭素原子8〜30個を有する脂肪酸の塩、例えばパルミチン酸、ステアリン酸またはベヘン酸の塩、グリセロールの脂肪酸エステル、例えばステアリン酸グリセリル;エチレンオキシド基2〜8個を有する、脂肪酸塩のオキシエチレン化誘導体およびグリセロールの脂肪酸エステルのオキシエチレン化誘導体、およびその混合であり得る。
【0054】
医薬組成物は、医薬組成物の分野で通常使用される防腐剤も含み得る。それらは、特に、1つまたは複数の芳香族置換基を含有し得るアルコール、例えば2−フェノキシエタノールなどのフェノキシエタノールまたは1−フェノキシ−2−プロパノール、ベンジルアルコール、2−ヒドロキシビフェニル、メチルパラベン、エチルパラベン、プロピルパラベン、ブチルパラベン、イソブチルパラベン、ナトリウムメチルパラベン、ナトリウムエチルパラベン、ナトリウムプロピルパラベン、ナトリウムブチルパラベンまたはナトリウムイソブチルパラベンなどのパラベン、エチル、ブチル、プロピルまたはメチルp−ヒドロキシベンゾエート、イミダゾリジニル尿素、ジアゾリジニル尿素、ヒドロキシメチルグリシン酸ナトリウム、ハロゲン化誘導体、例えばヨードプロピニルブチルカルバメート、2−ブロモ−2−ニトロプロパン−1,3−ジオール、2,4,4’−トリクロロ−2’−ヒドロキシジフェニルエーテル(トリクロサン)、3,4,4’−トリクロロカルバニリド(トリクロカルバン)、クロルブタヌルム、2,4−ジクロロベンジルアルコール、N−(4−クロロフェニル)−N’−(3,4−ジクロロフェニル)尿素、1,2−ジブロモ−2,4−ジシアノブタン、クロロキシレノール、ケトコナゾール、オキシコナゾール、ブトコナゾール、クロトリマゾール、エコナゾール、エニルコナゾール、フェンチコナゾール、ミコナゾール、スルコナゾール、チオコナゾール、フルコナゾール、イトラコナゾール、テルコナゾール、1つまたは複数のカチオン性窒素を含有する作用薬、例えば塩化セチルトリメチルアンモニウム、塩化セチルピリジニウム、塩化ベンゼトニウムまたは塩化ベンザルコニウム(過ホウ酸塩安定化過酸化水素と任意に組み合わせられる)、ジイソブチルエトキシエチルジメチルベンジルアンモニウムクロリド、ジイソブチルフェノキシエトキシエチルジメチルベンジルアンモニウムクロリド、N−アルキル−N,N−ジメチルベンジルアンモニウムクロリド、ブロミドまたはサッカリネート、トリメチルアンモニウムクロリド、クロロヒドロキシ酢酸ナトリウムアルミニウム、塩化トリセチルメチルアンモニウム、ジアミノアルキルアミド、クエン酸などの有機酸およびその塩から選択される、防腐剤などの抗菌剤または抗真菌剤、ファルネソール、テルビナフィンまたはナフチフィンなどの不飽和抗菌剤、ビフォナゾール、クロコナゾールまたはイソコナゾールなどの複素環式芳香族剤、当業者に公知の他のいずれかの抗菌剤または抗真菌剤;およびその混合物であることができる。
【0055】
さらに、医薬組成物は、前記医薬組成物のpH範囲を調節するための酸および塩基も含み得る。その塩基は、無機(水酸化ナトリウム、水酸化カリウム、アンモニア水)またはモノ−、ジ−またはトリエタノールアミン、アミノメチルプロパンジオール、N−メチルグルカミン、アルギニンおよびリジンなどの塩基性アミノ酸などの有機塩基;およびその混合物であることができる。
【0056】
本発明は、皮膚熱傷を治療するための、特に皮膚のプレバーンを治療するための、上述の医薬組成物の使用にも関する。
【0057】
本発明による医薬組成物は、異なる原因の皮膚のプレバーンまたは熱傷、すなわち、熱源と接触または熱源からの放射によって生じる皮膚のプレバーンまたは熱傷、放射線治療などの医学的処置によって生じる皮膚のプレバーンまたは熱傷、寒冷との接触から生じる皮膚のプレバーンまたは熱傷、摩擦によって生じる皮膚のプレバーンまたは熱傷、太陽光への短時間の曝露によって生じる皮膚のプレバーンまたは熱傷を治療するのに有用である。有利なことには、本発明による医薬組成物は、熱源との接触または熱源からの放射によって生じる、放射線治療などの医学的処置によって生じる、または摩擦によって生じる、皮膚のプレバーンまたは熱傷に特に有用である。本発明の他の態様に従うと、医薬組成物は、粘膜(例えば、食道などの消化器系の壁または唇、泌尿生殖器領域等)のプレバーンまたは熱傷を治療するのに有用であり得る。本発明による医薬組成物は、第1度、第2度または第3度のプレバーンまたは熱傷を治療するのに有用である。
【0058】
本発明の一態様に従うと、この使用は、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり60秒以下の時間内で、あるいは注射による投与の場合にはプレバーンまたは熱傷の原因との接触から始まり30分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0059】
好ましくは、この使用は、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり45秒以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0060】
本発明の一実施形態に従うと、この使用は、注射による投与の場合にはプレバーンまたは熱傷の原因との接触から始まり25分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0061】
本発明の一実施形態に従うと、医薬組成物の使用は、60分間の間に続いて30回、または60分間に20回、または30分間に10回、または15分間に5回投与されることを特徴とする。
【0062】
本発明は、本発明による医薬組成物を皮膚熱傷と、特に皮膚のプレバーンと接触させることを特徴とする治療的処置法にも関する。
【0063】
有利には、この治療的処置法は、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり60秒以下の時間内で、または注射による投与の場合には30分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0064】
好ましくは、本発明による治療的処置法は、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり45秒以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0065】
一実施形態に従うと、本発明による治療的処置法は、注射による投与の場合にはプレバーンまたは熱傷の原因との接触から始まり25分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする。
【0066】
本発明は、熱衝撃により生じる痛みの強さを低減する治療的処置法であって、局所投与の場合にはプレバーンまたは熱傷の原因との接触から始まり60秒以下の時間内で、あるいは注射による投与の場合には30分以下の時間内で、医薬組成物を皮膚損傷と接触させることを特徴とする治療的処置法にも関する。
【実施例】
【0067】
−実施例1:臨床試験
−a)臨床試験プロトコル
異なる原因のプレバーンおよび異なる重症度を有する数名の患者に関して、本発明による医薬組成物を試験した。以下の場合のそれぞれに関して、熱傷の原因との接触から始まり45秒の時間内に、次いで定義された期間中に定期的に、医薬組成物を皮膚のプレバーンに直接適用した。
【0068】
−b)臨床試験の結果
−患者1:この患者は、第2度プレバーンを示し、その原因は、350℃に加熱されたオーブン発熱体に腕を直接接触させたことから生じた。350℃に加熱されたオーブン発熱体との接触から開始して45秒の時間内に、本発明による医薬組成物を適用し、次いで15分間で3分毎に適用し、次いで2日間定期的に適用した。この期間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。痛みは3時間後に消失した。
【0069】
−患者2:この患者は、400℃の赤熱ドリルビットに手掌を接触させたことによって生じた第2度プレバーンを示した。赤熱ドリルビットとの接触から開始して45秒の時間内に本発明による医薬組成物を適用し、次いで2日間定期的に適用した。この期間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。痛みは2時間後に消失した。
【0070】
−患者3:この患者は、蒸気に手が接触したことによって生じた第1度プレバーンを示した。蒸気との接触から開始して45秒の時間内に本発明による医薬組成物を適用し、次いで3時間定期的に適用した。この期間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。このケースは他の患者5名についても繰り返した。痛みは10分後に消失した。
【0071】
−患者4:この患者は、熱を持ったチェーンソーの鎖からの患者の大腿への摩擦によって生じた第2度「A」プレバーンを示した。チェーンソーの鎖との接触から開始して45秒の時間内に、本発明による医薬組成物を適用し、次いで3日間定期的に適用した。この期間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。痛みは10時間後に消失した。
【0072】
−患者5:この患者は、オートバイの排気管に足を接触したことから生じた第2度「B」プレバーンを示した。オートバイの排気管との接触から開始して45秒の時間内に本発明による医薬組成物を適用し、次いで3日間定期的に適用した。5日間の終わりに、目に見える皮膚損傷が全て消失していた、すなわち、皮膚患部は紅斑または水疱を全く示さず、剥離しなかった。痛みは24時間後に消失した。
【0073】
これらの結果から、本発明による医薬組成物が、皮膚のプレバーンを治療し、それによって生じた皮膚損傷を著しく低減するのに特に有効であることが実証されている。第2度熱傷により生じた皮膚損傷が消失するのに必要な時間はおよそ2週間であると通常は確認されているが、本発明による医薬組成物を使用した場合には、この時間は2または3日間に低減される。治癒時間のこの有意な減少によって、熱傷により起こる皮膚損傷の場合には7日後に現れることが多い微生物(細菌または真菌起源)による感染のリスクも低減することが可能となる。さらに、本発明による医薬組成物を使用することによって、皮膚損傷が原因の痛みが著しく低減されることに留意されたい。
【0074】
−実施例2:本発明による医薬組成物

【特許請求の範囲】
【請求項1】
蜜ろうおよび任意選択的に1種または複数種の薬学的に許容される賦形剤と組み合わせて、オクタン酸セテアリルおよび/またはヘキサン酸から選択される活性成分を、組成物の全重量に対して少なくとも4重量%含むことを特徴とする、医薬組成物。
【請求項2】
請求項1に記載の医薬組成物において、前記活性成分がオクタン酸セテアリルであることを特徴とする医薬組成物。
【請求項3】
請求項1または2に記載の医薬組成物において、前記組成物の全重量に対して活性成分を4〜15重量%含むことを特徴とする医薬組成物。
【請求項4】
請求項1乃至3の何れか一項に記載の医薬組成物において、前記組成物の全重量に対して蜜ろうを2〜5重量%含むことを特徴とする医薬組成物。
【請求項5】
請求項1乃至4の何れか一項に記載の組成物において、前記活性成分と前記蜜ろうの比が0.8〜7.5であることを特徴とする組成物。
【請求項6】
請求項1乃至5の何れか一項に記載の医薬組成物において、油中水型エマルジョンまたは水中油型エマルジョンであることを特徴とする医薬組成物。
【請求項7】
請求項1乃至6の何れか一項に記載の医薬組成物において、デクスパンテノールおよび/またはポリジメチルシロキサン(ジメチコーン)から選択される1種または複数種の更なる添加剤を含むことを特徴とする医薬組成物。
【請求項8】
請求項1乃至7の何れか一項に記載の医薬組成物において、リドカイン、プリロカイン、スカンジカイン、エチドカイン、ブピバカイン、ロピバカイン、レボブピバカイン、アルチカインおよびメピバカインから選択される1種または複数種の局所麻酔薬を含むことを特徴とする医薬組成物。
【請求項9】
請求項1乃至8の何れか一項に記載の医薬組成物において、メラルーカ・アルターニフォリア(Melaleuca alterniflora)精油またはその誘導体、テペズコヒテ(Tepezcohuite)精油またはその誘導体、ユーカリ(eucalyptus)精油またはその誘導体、タイム精油またはその誘導体、ローズマリー精油またはその誘導体、レモン精油またはその誘導体、クローバ精油またはその誘導体、シナモン精油またはその誘導体、マツ精油またはその誘導体、ラベンダー精油またはその誘導体、ロックローズ(Cistus ladaniferus)精油またはその誘導体、セントジョンズワート(St John’s Wort)精油またはその誘導体およびジャコウバラ精油またはその誘導体からなる群から選択される、1種または複数種の精油またはその誘導体も含むことを特徴とする医薬組成物。
【請求項10】
請求項1乃至9の何れか一項に記載の医薬組成物において、メラルーカ・アルターニフォリア(Melaleuca alterniflora)精油またはその誘導体、テペズコヒテ(Tepezcohuite)精油またはその誘導体、セントジョンズワート(St John’s Wort)精油またはその誘導体およびジャコウバラ精油またはその誘導体からなる群から選択される、1種または複数種の精油またはその誘導体も含むことを特徴とする医薬組成物。
【請求項11】
請求項1乃至10の何れか一項に記載の医薬組成物において、局所的にまたは注射によって投与されることを特徴とする医薬組成物。
【請求項12】
請求項1乃至11の何れか一項に記載の医薬組成物の使用において、皮膚のプレバーンまたは熱傷を治療するためであることを特徴とする使用。
【請求項13】
請求項12に記載の使用において、局所投与の場合にはプレバーンまたは熱傷の原因との接触から開始して60秒以下の時間内にまたは注射による投与の場合にはプレバーンまたは熱傷の原因との接触から開始して30分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする使用。
【請求項14】
請求項12または13に記載の使用において、局所投与の場合にプレバーンまたは熱傷の原因との接触から開始して45秒以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする使用。
【請求項15】
請求項12または13に記載の使用において、注射による投与の場合にプレバーンまたは熱傷の原因との接触から開始して25分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする使用。
【請求項16】
請求項12乃至15の何れか一項に記載の使用において、前記医薬組成物が、60分間に30回続いて投与されることを特徴とする使用。
【請求項17】
請求項1乃至11の何れか一項に記載の医薬組成物を皮膚のプレバーンまたは熱傷と接触させることを特徴とする治療的処置法。
【請求項18】
請求項17に記載の治療的処置法において、局所投与の場合にはプレバーンまたは熱傷の原因との接触から開始して60秒以下の時間内に、または注射による投与の場合にはプレバーンまたは熱傷の原因との接触から開始して30分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする治療的処置法。
【請求項19】
請求項17または18に記載の治療的処置法において、局所投与の場合にプレバーンまたは熱傷の原因との接触から開始して45秒以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする治療的処置法。
【請求項20】
請求項17または18に記載の治療的処置法において、注射による投与の場合にプレバーンまたは熱傷の原因との接触から開始して25分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする治療的処置法。
【請求項21】
熱衝撃によって生じる痛みの強さを低減する治療的処置法において、局所投与の場合にはプレバーンまたは熱傷の原因との接触から開始して60秒以下の時間内に、または注射による投与の場合にはプレバーンまたは熱傷の原因との接触から開始して30分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする治療的処置法。
【請求項1】
蜜ろうおよび任意選択的に1種または複数種の薬学的に許容される賦形剤と組み合わせて、オクタン酸セテアリルおよび/またはヘキサン酸から選択される活性成分を、組成物の全重量に対して少なくとも4重量%含むことを特徴とする、医薬組成物。
【請求項2】
請求項1に記載の医薬組成物において、前記活性成分がオクタン酸セテアリルであることを特徴とする医薬組成物。
【請求項3】
請求項1または2に記載の医薬組成物において、前記組成物の全重量に対して活性成分を4〜15重量%含むことを特徴とする医薬組成物。
【請求項4】
請求項1乃至3の何れか一項に記載の医薬組成物において、前記組成物の全重量に対して蜜ろうを2〜5重量%含むことを特徴とする医薬組成物。
【請求項5】
請求項1乃至4の何れか一項に記載の組成物において、前記活性成分と前記蜜ろうの比が0.8〜7.5であることを特徴とする組成物。
【請求項6】
請求項1乃至5の何れか一項に記載の医薬組成物において、油中水型エマルジョンまたは水中油型エマルジョンであることを特徴とする医薬組成物。
【請求項7】
請求項1乃至6の何れか一項に記載の医薬組成物において、デクスパンテノールおよび/またはポリジメチルシロキサン(ジメチコーン)から選択される1種または複数種の更なる添加剤を含むことを特徴とする医薬組成物。
【請求項8】
請求項1乃至7の何れか一項に記載の医薬組成物において、リドカイン、プリロカイン、スカンジカイン、エチドカイン、ブピバカイン、ロピバカイン、レボブピバカイン、アルチカインおよびメピバカインから選択される1種または複数種の局所麻酔薬を含むことを特徴とする医薬組成物。
【請求項9】
請求項1乃至8の何れか一項に記載の医薬組成物において、メラルーカ・アルターニフォリア(Melaleuca alterniflora)精油またはその誘導体、テペズコヒテ(Tepezcohuite)精油またはその誘導体、ユーカリ(eucalyptus)精油またはその誘導体、タイム精油またはその誘導体、ローズマリー精油またはその誘導体、レモン精油またはその誘導体、クローバ精油またはその誘導体、シナモン精油またはその誘導体、マツ精油またはその誘導体、ラベンダー精油またはその誘導体、ロックローズ(Cistus ladaniferus)精油またはその誘導体、セントジョンズワート(St John’s Wort)精油またはその誘導体およびジャコウバラ精油またはその誘導体からなる群から選択される、1種または複数種の精油またはその誘導体も含むことを特徴とする医薬組成物。
【請求項10】
請求項1乃至9の何れか一項に記載の医薬組成物において、メラルーカ・アルターニフォリア(Melaleuca alterniflora)精油またはその誘導体、テペズコヒテ(Tepezcohuite)精油またはその誘導体、セントジョンズワート(St John’s Wort)精油またはその誘導体およびジャコウバラ精油またはその誘導体からなる群から選択される、1種または複数種の精油またはその誘導体も含むことを特徴とする医薬組成物。
【請求項11】
請求項1乃至10の何れか一項に記載の医薬組成物において、局所的にまたは注射によって投与されることを特徴とする医薬組成物。
【請求項12】
請求項1乃至11の何れか一項に記載の医薬組成物の使用において、皮膚のプレバーンまたは熱傷を治療するためであることを特徴とする使用。
【請求項13】
請求項12に記載の使用において、局所投与の場合にはプレバーンまたは熱傷の原因との接触から開始して60秒以下の時間内にまたは注射による投与の場合にはプレバーンまたは熱傷の原因との接触から開始して30分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする使用。
【請求項14】
請求項12または13に記載の使用において、局所投与の場合にプレバーンまたは熱傷の原因との接触から開始して45秒以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする使用。
【請求項15】
請求項12または13に記載の使用において、注射による投与の場合にプレバーンまたは熱傷の原因との接触から開始して25分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする使用。
【請求項16】
請求項12乃至15の何れか一項に記載の使用において、前記医薬組成物が、60分間に30回続いて投与されることを特徴とする使用。
【請求項17】
請求項1乃至11の何れか一項に記載の医薬組成物を皮膚のプレバーンまたは熱傷と接触させることを特徴とする治療的処置法。
【請求項18】
請求項17に記載の治療的処置法において、局所投与の場合にはプレバーンまたは熱傷の原因との接触から開始して60秒以下の時間内に、または注射による投与の場合にはプレバーンまたは熱傷の原因との接触から開始して30分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする治療的処置法。
【請求項19】
請求項17または18に記載の治療的処置法において、局所投与の場合にプレバーンまたは熱傷の原因との接触から開始して45秒以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする治療的処置法。
【請求項20】
請求項17または18に記載の治療的処置法において、注射による投与の場合にプレバーンまたは熱傷の原因との接触から開始して25分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする治療的処置法。
【請求項21】
熱衝撃によって生じる痛みの強さを低減する治療的処置法において、局所投与の場合にはプレバーンまたは熱傷の原因との接触から開始して60秒以下の時間内に、または注射による投与の場合にはプレバーンまたは熱傷の原因との接触から開始して30分以下の時間内に、前記医薬組成物を前記皮膚損傷と接触させることを特徴とする治療的処置法。
【図1】




【公表番号】特表2013−513579(P2013−513579A)
【公表日】平成25年4月22日(2013.4.22)
【国際特許分類】
【出願番号】特願2012−542567(P2012−542567)
【出願日】平成22年12月10日(2010.12.10)
【国際出願番号】PCT/EP2010/069412
【国際公開番号】WO2011/070168
【国際公開日】平成23年6月16日(2011.6.16)
【出願人】(512149606)45 セック.エルエルシー (1)
【氏名又は名称原語表記】45 Sec.LLC
【Fターム(参考)】
【公表日】平成25年4月22日(2013.4.22)
【国際特許分類】
【出願日】平成22年12月10日(2010.12.10)
【国際出願番号】PCT/EP2010/069412
【国際公開番号】WO2011/070168
【国際公開日】平成23年6月16日(2011.6.16)
【出願人】(512149606)45 セック.エルエルシー (1)
【氏名又は名称原語表記】45 Sec.LLC
【Fターム(参考)】
[ Back to top ]

