磁性炭素ナノチューブに基づく生体検出
生物学的及び医学的感知に応用のための磁性炭素ナノチューブを含む新規なハイブリッドシステムであるmCNTが提供される。或る実施形態の場合、このシステムには炭素ナノチューブ(CNT)内部の磁性物質が含まれる。CNT内の磁性物質の量は、mCNTが小型で安価の携帯用磁石に応答可能な程度である。CNTの外面は生体分子的付着、又はその他の機能化のためにそのまま残されている。この新規な物質による性能の向上の例には、感度の向上、応答時間の短縮、及びサンプル体積の減少がある。種々の実施形態の場合、mCNTはこれらのアッセイに関与する、又は活性感知用要素としての分子の密着用下地層である。印刷された電極上の二次元的mCNT及びCNTネットワークの製造法も開示される。
【発明の詳細な説明】
【背景技術】
【0001】
[他の出願との関係]
本出願は米国特許法U.S.C.§119(e)により、2009年8月7日に提出された米国特許暫定出願61/232,242号に基づいて優先権を主張するものである。この出願はその全体を此処に参照して合同するものとする。
【0002】
単壁型の複ラベル二次抗体ナノチューブ生体接合体を有するCNTフォレストプラットホームに基づく電気化学的免疫センサは高感度の検出プラットホームであることが報告されている。(Xin et al.“Carbon Nanotube Amplification Strategies for Highly Sensitive Immunodetection of Cancer Biomarkers”, Journal of the American Chemical Society 2006 128(34), pp 11199−11205, 此処に参照して合同するものとする。)この場合、SWNTフォレストはナフィオン-酸化鉄の装飾導電面上に直立した束として立つものであった。感度の向上は単ラベル二次抗体に替えて山葵ペルオキシダーゼ(HRP)ラベル及び二次抗体(Ab2)とがHRPとAb2との間の高い比で連接されて複壁CNTを特色とする生体接合体を使用することで達成された。CNTフォレストの製造プロセスが複雑なので、高密度に詰められたAuNPを使用する代行的プラットホームが最近報告されている。(Vigneshwaran Mani et al. ”Ultrasensitive Immunosensor for Cancer Biomarker Proteins Using Gold Nanoparticle Film Electrode and Multienzyme−Particle Amplification“,ACS Nano Letters, 2009, 3(3) pp 585−594,此処に参照して合同するものとする。)この研究において、HRPラベルは感度及び検出限度を向上させるために磁性ビーズの表面に生成されたカルボキシル基に付けられた。HRP及びAb2の生体接合の後、遊離抗体及びHRPは試験管底部のビーズを局地化するのに磁石を使用し、非反応の蛋白質を除去するために洗浄することによってAb2磁性ビーズ−HRPから容易に分離された。医学的応用のための磁性粒子は開発されている。磁性粒子にはその他の物質にない特異な磁性特性があるので、特殊な医学的技術に応用可能である。(例えばChoi,J−W et al. ”An integrated microfluidic biochemical detection system with magnetic bead−based sampling and analysis capabilities.“ Electrochemistry Communications. 2001,9,pp 1547−1552 及び R.E.Thilwind, et al. ”Measurement of the concentration of magnetic nanoparticles in a fluid using a giant magnetoresistance sensor with a trench.” J. Maagntism and Magnetic Materials, 2008, 320, pp486−489 を参照、共に此処に参照して合同するものとする。)
【0003】
分離、免疫検定、磁気共鳴結像処理(MRI)、薬品配送、及び高体温は磁性粒子の使用で向上する。関心箇所での診断を可能にする生体検出に使用される磁性粒子の一例がPhilipsのMagnotech携帯技術によって開示された。Magnotechは携帯用解析器に挿入される使い捨ての生体センサのカートリッジに合同された磁性ナノ粒子を使用してピコモル単位の対象分子をただの数分間で測定する。液体洗浄工程を簡素化することによって、この技術は更に使用を容易にしている。磁性ビーズは種々の生体検出の応用に使用されているが、これには屡複雑な表面の機能化が伴う。表面コーティングの適合性及び安定性は結合の毒性及び堅牢性に影響することがある。
【発明の概要】
【0004】
此処に提供されるのは、生物学及び医学的検出に応用される磁性炭素ナノチューブを含む新規なハイブリッド物質システムmCNTである。或る実施形態の場合、システムには炭素ナノチューブ(CNT)の内部に磁性物質が含まれる。CNT内の磁性粒子の量はmCNTが小型,廉価、携帯可能の磁石に呼応出来るものであってよい。CNTの外面は生体分子的付着又はその他の機能化用にそのままに保持される。この新規な物質による性能向上には、感度の向上、応答時間の短縮、及びサンプル量の減少が含まれる。種々の実施形態の場合、mCNTはこれらのアッセイにおいて、又は活性検知要素として関与する分子に密着する下地層である。更に提供されるものは、印刷された電極上の二次元的なmCNT及びCNTのネットワークの製法である。
【0005】
本発明はその一面において内部空洞と外面、内部空洞内に位置される磁性物質、及び外面に付着する複数の捕獲因子を有する炭素ナノチューブを含むmCNT物質に関する。捕獲因子は対象物に結合、又はそれ以外の様相で捕獲可能な分子であってよい。捕獲因子は合成因子及び非合成因子を含む有機又は無機の捕獲因子であってよい。生体分子捕獲因子の例には抗体、酵素、オリゴヌクレチド、アプタマー、抗体断片、及び分子的にインプリントされた高分子がある。或る実施形態の場合、ナノチューブに付着する捕獲因子は選択的又は非選択的に対象物に結合するように構成された抗体のようなリポーター因子であってよい。多くの実施形態の場合、磁性物質は例えばナノクラスターのような粒子の形態の鉄、コバルト、ニッケル、又はそれらの合金或は混合物のような強磁性物質である。種々の実施形態の場合、mCNT物質には複数のかような炭素ナノチューブが含まれる。或る実施形態の場合、例えば粉末とかタブレットの形態で供給される。他の実施形態の場合、mCNT物質は溶液の中に在る。溶液の中で複数の炭素ナノチューブは或る実施形態の磁界の応用によってメッシュネットワークを形成する。或る実施形態の場合、磁性物質はナノチューブの空洞内に閉鎖され、ナノチューブ外面、又はナノチューブの内部空洞の中以外には実質上磁性物質が存在しない。空洞の端部は開いていても、閉じていてもよい。
【0006】
別の面において、本発明はサンプル内の生体分子対象物を感知する方法に関する。或る実施形態の場合、この方法は内部空洞,内部空洞内に位置される磁性物質を有する外面、及び外面に付着する対象物に結合するように構成された複数の捕獲因子を有する複数の炭素ナノチューブを供給する工程と、これら複数の炭素ナノチューブを溶液に分散する工程と、これら複数の炭素ナノチューブをサンプルに接触させてサンプル内の生体分子対象物を溶液内の捕獲因子と結合させる工程と、磁界を印加して溶液内の複数の炭素ナノチューブを感知電極に移送する工程と、対象物の存在を感知する工程とから成る。
【0007】
更に別の面において、本発明はサンプル容器、サンプル容器内のサンプルに接触するように構成された電極、内部空洞、内部空洞内に位置される磁性物質を有する外面、及び外面に付着する対象物に結合するように構成された複数の捕獲因子を有する複数の炭素ナノチューブ、及び複数の炭素ナノチューブに磁力を及ぼして電極に関して移動するように構成された磁石を含む溶液内の生体分子対象物を感知するシステムに関する。
【0008】
本発明のこれら及びその他の面は以下において図を参照して説明される。
【図面の簡単な説明】
【0009】
【図1】強磁性粒子を中に有する炭素ナノチューブを含む或る実施形態のmCNTを図示する。
【図2】或る実施形態のmCNTを使用するアッセイの代表的図示である。
【図3】或る実施形態の場合の活性結核(TB)のような条件の為の新規な診断用生体センサの一実施形態を示す。
【図4】CNT404を含む電極402を有する装置400の像を示す。
【図5】ランダムに分布されたCNTネットワークのSEM像である。
【図6】磁界が印加された溶液に吊るされたmCNTの像である。
【発明を実施するための形態】
【0010】
本発明は表面特性及び磁性特性の独立制御を可能とする新しいシステムを提供する。種々の実施形態の場合、本発明は炭素ナノチューブ(CNT)を使用する高性能の化学的及び生物学的検出に関する。或る実施形態の場合、生物学的及び他の対象物の検出の為、CNT内にナノ磁性物質が埋め込まれた新規なハイブリッド物質システムが提供される。ここでは、このハイブリッド物質をmCNTと称する。この新規な物質は、向上された感度、短縮された応答時間、及び減少されたサンプル体積など、多くの面で向上された特性を提供する。更にこの新規な物質及び此処に記載される観念は種々の製品構成に応用可能である。その例は以下のごとくである。
【0011】
或る実施形態の場合、mCNTは免疫学的又は他の生物学的アッセイに使用される。mCNTはこれらのアッセイに関与する複数の分子が密着する下地層の物質として役立つ。この物質は機能的面積を有意義的に向上するので、磁性ビーズ及び粒子で生成される有用な特性が向上する。mCNTは生物学的捕獲を使用するすべてのタイプの対象物(核酸、蛋白質、抗体、グリカン)及び検出プラットホーム(例えば光学的、電気測定的、電気化学的、ラベル無し)に使用可能である。
【0012】
或る実施形態の場合、mCNTには鉄、コバルト、ガドリニウム、ジスプロシウム、又は強磁性を有するその他の物質のような強磁性物質の一種以上で充填されたナノチューブが含まれる。金属を包み込んだり、金属又は金属の炭化物及び酸化物をCNTに導入する種々の技術により電子的及び力学的特性は有意義的に変更可能であろう。例えば、個々の炭素ナノチューブの電気伝導度はそれに埋め込まれたナノスケールの磁石の磁性遷移に敏感であることが示されている。強磁性物質で充填されたナノチューブも、その磁性データ貯蔵技術への応用の可能性故に可成り興味を惹かれている。
【0013】
或る実施形態の場合、mCNTにはナノチューブの外面に実質上磁性物質のないナノチューブシェルが含まれる。ナノチューブシェルとは内部の強磁性クラスターの酸化を防止し、長期間に亘る安定性を向上させるものである。或る実施形態の場合、mCNTの製造プロセスでナノチューブの端部が開かれる。例えば或る実施形態の場合、CNTの精製及び酸処理(例えば濃硝酸及び硫酸による酸化)によってナノチューブ端部にカルボキシ基(−COOH)のような機能基が生成される。これは対応する金属塩を還元する電気化学的方法によってナノチューブ内に金属(強磁性)粒子を堆積するのに有用である。或る実施形態の場合、CNTの磁性化の後、金属粒子の露出を防止して更に安定性を向上するように端部がカバーされる。
【0014】
CNTの内部に磁性クラスターが埋め込まれたCNTを生成する製造のアプローチはSoldano et alによって開示されている。(”Detection of nanoscale magnetic activity using a single carbon nanotube”, Nano Letters. 2008;8(12), pp4498−4505,此処に参照して合同されるものとする。)この中で、物質は単一の炭素ナノチューブによってナノスケールの磁性活性の検査に使用された。
【0015】
種々の実施形態の場合、この物質は磁性ビーズの代わりに生物学的及び医学的応用において使用される。この物質はCNTの内部に磁性物質を有する。もし磁性物質のあるのがCNTの外側であったなら、この物質は対象物の検出中に測定される電気化学的信号に関与することとなり、場合によっては毒性を増加させることになろう。磁性クラスターがCNTの内部のみに位置するので、CNTの表面はそのままであり、興味の対象である対象物に特殊性を与える化学物質で容易に機能化可能である。例えば、生体分子捕獲因子には抗体、酵素、オリゴヌクレオチド、アパタマー及び抗体断片が含まれる。非生体分子捕獲因子には分子的にインプリントされた高分子が含まれてよい。
【0016】
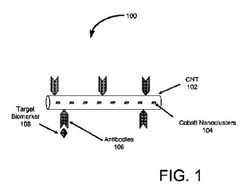
図1は或る実施形態の場合のmCNT100の略図である。mCNT100には中にコバルトナノクラスター104を有する炭素ナノチューブ102が含まれる。種々の実施形態の場合、応用面によりmCNTの直径は約1nmから20nmの間であり、長さは約50nmから数ミリメートルの間であるが、これらの特定された範囲に限定されるものではない。図示の実施形態の場合、mCNT100には外面上に抗体機能化が含まれ、抗体106がCNT102の側壁に付着している。抗体106はmCNT100を機能化して対象の抗原108を捕獲する。種々の実施形態の場合、mCNTに適応される捕獲化学形態の例として、酵素、核酸、抗体、アプタマー、オリゴヌクレオチド、抗原、及びグリカンがある。付着の方法には吸着、共有性結合、ストレプトアビジン/ビオチン、及びその他の既知のCNTを機能化する方法が含まれる。
【0017】
mCNTの機能化及び使用の一例が以下のように記載される:
1.生体分子が物理的吸着又はカルボジイミド又はグルタアルデヒド交差結合のような選択的化学形式を使用してmCNTに付着される。例えば電気化学的酵素―結合された免疫吸着アッセイ(ELISA)の中で、心臓トロポニンIのような捕獲抗体が付着されてよい。対象に特定的な酵素がグルコース又はクレアチニン検出のような酵素アッセイに付着される。どのような既知の捕獲化学形態が使用されてもよいことは、当業者には自明であろう。
2.mCNTの非機能化面はサンプルやリポーター物質の非特定的な付着を防止するように、ウシ血清アルブミン(BSA)又はツイーン−20のような界面活性剤のような蛋白質で封鎖されている。mCNTと蛋白質/抗体/界面活性剤の間の疎水性反応はこれに有用である。
3.機能化されたmCNTは溶液に入れられる。この溶液は例えば水、エタノール、ジメチルフォルムアミド(DMF)、テトラヒドロフラン(THF)、又は水中のドデシル硫酸ナトリウム(SDS)のような界面活性剤のようなCNT分散用の普通の液体であってよい。生体分子との適合性のため、水性溶媒が好適である。分散液とmCNTの溶液には電気化学的反応に関与したリポーター化学形態が含まれてもよい。或る実施形態の場合、リポーターは必要でなく、これは典型的に「ラベル無し」と呼ばれる。典型的な電気化学的ELISAの場合、ラベルは信号の増幅に必要である。ラベルは対象物(即ちリポーター)用の二次抗体に付着された山葵ペルオキシダーゼ(HRP)にような酵素であってよい。
4.溶液はサンプルに混合される。サンプルの例には尿、痰、唾液、血液、呼気凝縮液などがある。これは種々の状態で実行可能である。チューブ、微小ウエル板、又は好適に携帯用リーダーにはまるカートリジの中で可能である。
【0018】
図2は或る実施形態の場合のmCNTを使用するアッセイの略図である。捕獲抗体206はスクリーン印刷された電極の近くに磁力(図示せず)で保持されるmCNT201に付着されている。捕獲抗体206はリポーター抗体209にも結合する対象物208を捕獲するように構成されている。酵素211は報告用リポーター抗体209に付着している。
【0019】
mCNTが無い場合、ラベルが捕獲抗体、対象物、及び二次抗体(リポーター)サンドイッチの為電極から或る距離に位置すると言う事実の理由で酵素活性地域211と電極201の間に電子を移動させる電子往復運動が必要である。mCNTを使用すると、或る実施形態の場合、サンドイッチ形成が溶液の中で起こる。磁界が印加された後、リポーターを含めてサンドイッチ集合体の全部が物理的に電極の近くに移動され、これによりラベルと電極の間の直接の電子的交信の可能性が向上する。これにより、ラベルの検出用の下地層の必要性が除去される。製品カートリッジに貯蔵されるべき試薬もより少なくなる。アッセイ工程が少なくなり、アッセイ速度が改善する。流体工学、バルブ、及びポンプに関する要求も簡素化される。酵素と電極の間の直接電子的交信がmCNTの使用で確立される酵素のアッセイにもこの原則は応用され、電子の往復運度の必要性が除去される。
【0020】
酵素の活性地域又は他のラベルがCNTでアクセス不可能であるか、別の組成物(又は伝達物質)の或る反応の触媒作用がより高速或は低エネルギイである場合、活性地域への交信に伝達物質が使用可能である。典型的な伝達物質(例えば2,2’−アジノビス(3−エチルベンゾチアゾリン−6−スルフォネート)(ABTS)又は3,3’,5,5’−テトラメチルベンジディン(TMBB))はCNTの上に吸着し、この目的に有用である。ラベル無しのアプローチは選択的に高濃度を要求するアッセイ(例えばC−活性蛋白質(CRP)−ng/mlから g/mlの範囲)へカートリッジ上で使用可能なアッセイのメニュから適応可能である。酵素に加えて、シトクローム−C(Fe(III)(Cytc) Fe(II)(Cyt−c)のような電気化学的活性を示す他のラベル、ZnS,CdS,PbS,CuSのようなコロイド状金属結晶も使用可能であり、上記のアプローチに適当である。
【0021】
溶液内の活性要素が磁性成分を含むと言う事実は、磁性攪拌が対象物の分散/遭遇の割合及び捕獲の向上に使用可能であることを意味する。リポーター及び捕獲抗体の間のサンドイッチ形成はアッセイを速くするバルク相で起こる。これは捕獲抗体が電極上で不動化されている電気化学的ELISAの中で典型的に起こる2相反応と比較される。攪拌には例えば回転的、側方的、前後的など多種の運動のいずれも使用可能である。全体の扇動の度合も例えば乳液の生成の抑制であるとか、mCNTの機能化を退化させるため(低攪拌)とか、多くの理由の中のいくつかによって制御されてもよい。
【0022】
サンプルの配達及び流れの経路に関する製品構成において、mCNT/捕獲/対象物/リポータコンプレックスを感知地区に移動するのに磁石が使用可能である。例えば、カートリッジの下に位置する電磁石によって捕獲された対象物分子を含めてmCNTを生体センサの活性検出面へと移動させることが可能である。測定は光学的技術で実施可能である、測定は更に外部回路に接続されたベース電極にmCNTを接触させることにより電気的に実施可能である。
【0023】
mCNTには分子を容易に付着するため複数の経路がある。対照的に、複数酵素ラベル付けのアプローチで使用されるビーズや粒子の多くには例えばアミン又はカルボキシル基のような単一の化学的配合部分が存在する。二種以上の異なるタイプの機能グループが存在しないと言うことは、異なるタイプの分子を付着させる容易な経路がないと言うことを意味する。均一的化学構成のこれらの物質の場合、各分子の支持体への特別なローディングを得るため、適当な動的制御(即ち反応のタイミング)又は複数の結合体の適当なモル比が要求される。対照的に、単一の炭素ナノチューブが異なる分子を付着する複数の化学的部分をもつことがある。つまり、炭素ナノチューブの端部はナノチューブの中央部とは異なる化学的構成である。或る実施形態の場合、CNTの側壁はsp2結合構成で特徴付けされる一方、チューブの端部は懸垂的結合を有して側壁部より反応性である。向上された反応性は欠陥によって中央部に向かって伸びることもあるが、これは端部から数個の原子の範囲である。端部での懸垂的結合の存在により、例えば酸処理によるCNTの精製及び機能化の期間中に機能基が生成されることもある。このことは、第二の異なる化学的部分がナノチューブの中央部に亘って拡散する一方、炭素ナノチューブのより反応的な端部は選択的に或る機能的部分に変換される可能性があることを意味する。代行的に、本体が機能化されないまま残されて分子の簡単な物理吸着的付着に使用される一方、端部が機能化されてもよい。二つの異なる付着経路があるということは、物質上の異なるタイプの分子の量の制御の向上を含め、これらの物質の容易な構成を供するものである。
【0024】
或る実施形態の場合、磁性粒子の置換に加え、mCNTは活性的な感知用要素として使用可能である。実施形態の中の一つの場合、mCNTは下地層の上に堆積されて電極を形成する。その構成と直径とは所望の電気的特性を達成するために独立的に最適化可能である。上記のような化学的及び磁石のデザインの進歩のみならず、mCNTの高度の縦横比によって直接の読み出し用に電気的に接続可能なネットワーク構成が可能にされる。図3は或る実施形態の場合例えば活性結核(TB)のような状態用の新規な診断用生体センサの実施例を示すものである。この生体センサには本発明の面が含まれて居り、最小の流体処理及び高感度を有するように構成されている。これにはサンプル容器302、その下側に付着されて容器302内のサンプルにまで伸びている電極305を含む蓋304、可動性及び/又は容器に対してスイッチ可能な磁石308、及びリーダー310が含まれている。磁石308は容器に対して移動可能な永久磁石であっても、又はオンとオフにスイッチ可能な電磁石であってもよい。必要とされる試薬を分散させるための試薬タブレット306がサンプル容器302内に位置されてもよい。下記のように、これにはmCNTが含まれていてもよい。
【0025】
このような装置を使用する試験のプロトコルの一例は以下のようなものである:
1.容器にサンプルを収集する
2.蓋をつける
3.内容物(対象物がmCNTを結合)を旋回させる
4.磁界を印加する(サンドイッチ形成)
5.磁界及び旋回を反転(非結合のmCNTは容器の底に密着)
6.静電容量を測定
【0026】
一実施形態の場合、捕獲抗体は静電容量の測定に構成された標準的な導電性カーボンインク電極(即ちグルコースの試験片)の上に不動化される。リポーター抗体はmCNTの上に不動化される。磁気特性はチューブの核部に電気化学的に堆積されたコバルトナノクラスターによって付与される。リポーター抗体はバルク溶液内の対象物と結合し、溶液の緩慢な旋回で動特性が向上する。その後、このコンプレクスを急速に電極表面に移動してサンドイッチの形成を完了すべく磁石が位置される。抗体は対象物にとって特殊なので、サンドイッチ構成の形成には対象物が必要である。サンドイッチの形成後、非結合のリポーター抗体が静電容量電極の近辺から除去されて対象物特殊性を付与するように磁石の位置及び/又は方向が変更される。残留するmCNT(対象物と通じて結合)は電極静電容量を増加させ、対象物の存在を示す。CNTは実質的に電気化学的キャパシタ(例えば尿のような電解質の中の多孔質のメッシュ構成)を形成するものであるから、電極の静電容量を増加するものである。このような種類のメッシュ構成は磁性ビーズとか他の試験で通常使用される他のナノ粒子で形成することはできないが、高縦横比のCNTの幾何学的形状でこの発明のアプローチは可能とされる。CNTはそのナノスケール次元の為に表面積が大きい。このために検出の感度が向上される。CNTに存在する機能基(例えば−COOH)はいずれもCNTと電極の結合に関連する静電容量の変化を更に増加する。
【0027】
典型的な尿サンプルには酵素免疫アッセイ(EIA)及び免疫色彩側方流動(ICLF)テストで使用されるものより体積で殆ど3桁よけいに大きい。この非慣習的テストは使用可能なサンプル体積の全体を使用するようにデザインされたものであり、バルク溶液の中の対象物を捕獲するのに効率的な方法を使用し、トランスジューサ表面にそれを集中する。このテストは並み以下の体積で収集され、又は並み以下の体積に希釈された生物学的又は環境的サンプル(例えば尿、飲料水、その他)内の低含量分子の検出に広く応用される。提案されたこのテストは既に容認されている数々の化学的検出法で使用される成分を集めたものである。この新規なテストでは、対象物認識にEIAやICLFで使用されると同じ抗体サンドイッチ手法(リポーター+対象物+捕獲)が使用される。但し、対象物の光学的リポーティングの代わり、テストを更に簡素化するために直接な電子的測定が使用されている。
【0028】
或る実施形態の場合、テストは全体的に標準的な尿サンプル収集用容器の中で実施され、必要なのは永久磁石の旋回と移動のみである。代行的に無ステップのアッセイに電磁石が使用されてもよい。ビンの中には既にリポーター抗体によって接合されたmCNTの乾燥粉末を入れた小型の水/尿溶解性のカプセルが入れられる。サンプルはシステムを再水和するので、液体試薬は不必要である。有意義的なことであるが、非結合mCNTは一度電極から数マイクロメートル離れるとすでに局地的容量には影響しないので、この磁性的分離では「洗浄」工程が不必要となる。従って、このテストでは追加的液体試薬とか流体処理が不必要である。
【0029】
図3に示される構成の場合、電極305は蓋304の下側に付けられてあり、蓋の上部に付けられた安価な太陽光線で充電される時計に似た簡単な再使用可能なリーダー310で計測される。このリーダーは結果をデジタル出力として提供する。測定は電子的なので、正負の制御又は複数個の対象物のマルチプレクス検出が容易に実施される。
【0030】
此処に記載される生体センサはmCNTが如何に対象物捕獲及び感知要素として使用可能であるかの多くの例の一つである。免疫学的要素による広範囲に亘る種々の抗原及び抗体検出に加えて、本発明の実施形態に従ってmCNTを使用可能の種々のタイプのアッセイには、以下のものが含まれる:
1)例えばCD4(例えば此処に参照により合同されるものとするGao et al.,Magnetic based immunoassay for enumeration of CD4(+)T lymphocytes on a microfluidic device. Talanta 82:528−533(2010)を参照)又は癌(例えば此処に参照により合同されるものとするMa et al.,Magnetization of large polystyrene peptide beads for capturing and expanding cancer cells. J.of Magnetism and Magnetic Materials 264:153−157(2003)を参照)のような溶液からの捕獲及び検出に特殊な細胞
2)核酸異種交配アッセイ例えば此処に参照により合同されるものとするShepard,A.R and J.L.Rae.,Magnetic capture of cDNAs from double−stranded plasmid cDNA libraries. Nucleic Acids Research 25:3183−3185(1997)を参照)
3)核酸増幅システムに応答するサンプルへの統合(例えば此処に参照により合同されるものとするDill et al. Fully integrated device for direct sample−to−answer genetic analysis. Integrated Analytical Systems;Microarrays, Springer New Yorl(2009)を参照)
4)流体血球計算(例えば此処に参照により合同されるものとするm Yang et al,Biosensors and Bioelectronics 24:855−862(2008)を参照)
5)膠着接合アッセイ(例えば此処に参照により合同されるものとするMoser et al.m On−chip immuno−agglutination assay with analyte capture by dynamic manipulation of superparmagnetic beads. Lab on a Chip 9:3261−3267(2009)を参照);及び
6)脂質解析(例えば此処に参照により合同されるものとするNauck et al., New Immunoseparation−based homogeneous assay for HDL−cholesterol compared with three homogeneous and two heterogeneous methods for HDL−cholesterol., Clinical Chemistry 44:1443−1451 (1998)を参照)
【0031】
此処に記載された教示を基にして、当業者には如何にして磁性ビーズやその他の磁性要素の代わりにmCNTがこれらのアッセイに、又免疫学的要素で種々の抗原及び抗体の検出に応用されるか、理解されることであろう。
【0032】
本発明はその他の面においてCNTに基づく増幅機構と結合されるCNTネットワークに関するものである。単壁型のCNTフォレストプラットホームに複ラベル二次抗体ナノチューブ生体接合体を結合することは既に示されたことである。SWNTフォレストはナフィオン-酸化鉄の装飾導電面上に直立した束として立つものであった。感度の向上は達成された。しかし、技術の実現は電極製造のプロセスが複雑なので阻止されていた。或る実施形態の場合、CNT及び/又はmCNTネットワークが電極として使用される。基盤電極はスクリーン印刷のような通常の手段で製造可能である。CNT及び/又はmCNTネットワークは例えばBiodotのような市場で入手可能な基盤電極の上に堆積可能である。図4はCNT404を含む電極402を有する装置400の像を示す。Biodotによって最終的装置の上に堆積されたCNTのSEM(走査型電子顕微鏡)像の一例が図5に示されている。その結果として、スクリーン印刷された炭素インクで定義された電極の上に炭素ナノチューブネットワークが均一的に分配されていることが示されている。
【0033】
電気化学的検出に種々の方法が使用される。異なる酵素ラベル、金属ナノ粒子、その他の電子的活性ラベルが多重化に使用される。リポーター抗体への酵素ラベルと共に、酵素下地層の存在のもとで伝達物質用のレドクス電流が電流測定法による対象物の定量化に使用される。結合イベントごとに得られる酵素分子を増大させるためにリポーター抗体と共に複数の酵素ラベルがCNTに付着可能である。工程数を減少させるために、シトクローム−C(Fe(III)(Cyt c)→Fe(II)(Cyt−c))のような電気化学的活性を示すその他のラベルが使用されてもよい。CNT又はリポーター抗体はZnS,CdS,PbS,CuSのようなコロイド状金属結晶でラベル付けされ、陽極ストリッピング法ボルタメトリによって検出されてもよい。
【0034】
例
CNTは陽極酸化されたアルミナテンプレートの中で化学蒸着(CVD)によって成長された。CNTの直径はテンプレートの孔サイズによって容易に制御された。次いで、電気化学的堆積によってナノチューブ(mCNT)内で強磁性ナノ粒子が形成された。埋め込まれた何千もの磁性ナノ粒子の集合的動作及びこれらがCNTに強力な強磁性動作を付与する能力が調査された。その結果、mCNTは 埋め込まれた磁性ナノクラスターが良好な分離特性を提供するのに十分であることを示すことが分かった。図6は永久磁石を使用することによってバルク溶液から分離されたmCNTの像である。mCNTは超純水の中でガラスの小瓶の背後に位置された永久磁石(印付き)によって溶液から分離されている。対照的に、非磁性のCNTは小瓶の底に沈殿する。
【0035】
本発明による方法及び装置の好適な実施形態がこのように記載された後、当業者にはこのシステムが有利であることが自明であろう。これらの種々の変更、応用、代行実施形態も本発明の範囲及び精神の範囲内であることが理解されよう。異なるラベル及び電気化学的測定法も磁性CNTに基づくシステムに応用可能であり、これも当業者には自明であろう。従って、装置の感度及び特殊性などの性能の度合は特殊な応用面で要求される追加的流体処理及び測定工程での必要性でバランス可能である。
【背景技術】
【0001】
[他の出願との関係]
本出願は米国特許法U.S.C.§119(e)により、2009年8月7日に提出された米国特許暫定出願61/232,242号に基づいて優先権を主張するものである。この出願はその全体を此処に参照して合同するものとする。
【0002】
単壁型の複ラベル二次抗体ナノチューブ生体接合体を有するCNTフォレストプラットホームに基づく電気化学的免疫センサは高感度の検出プラットホームであることが報告されている。(Xin et al.“Carbon Nanotube Amplification Strategies for Highly Sensitive Immunodetection of Cancer Biomarkers”, Journal of the American Chemical Society 2006 128(34), pp 11199−11205, 此処に参照して合同するものとする。)この場合、SWNTフォレストはナフィオン-酸化鉄の装飾導電面上に直立した束として立つものであった。感度の向上は単ラベル二次抗体に替えて山葵ペルオキシダーゼ(HRP)ラベル及び二次抗体(Ab2)とがHRPとAb2との間の高い比で連接されて複壁CNTを特色とする生体接合体を使用することで達成された。CNTフォレストの製造プロセスが複雑なので、高密度に詰められたAuNPを使用する代行的プラットホームが最近報告されている。(Vigneshwaran Mani et al. ”Ultrasensitive Immunosensor for Cancer Biomarker Proteins Using Gold Nanoparticle Film Electrode and Multienzyme−Particle Amplification“,ACS Nano Letters, 2009, 3(3) pp 585−594,此処に参照して合同するものとする。)この研究において、HRPラベルは感度及び検出限度を向上させるために磁性ビーズの表面に生成されたカルボキシル基に付けられた。HRP及びAb2の生体接合の後、遊離抗体及びHRPは試験管底部のビーズを局地化するのに磁石を使用し、非反応の蛋白質を除去するために洗浄することによってAb2磁性ビーズ−HRPから容易に分離された。医学的応用のための磁性粒子は開発されている。磁性粒子にはその他の物質にない特異な磁性特性があるので、特殊な医学的技術に応用可能である。(例えばChoi,J−W et al. ”An integrated microfluidic biochemical detection system with magnetic bead−based sampling and analysis capabilities.“ Electrochemistry Communications. 2001,9,pp 1547−1552 及び R.E.Thilwind, et al. ”Measurement of the concentration of magnetic nanoparticles in a fluid using a giant magnetoresistance sensor with a trench.” J. Maagntism and Magnetic Materials, 2008, 320, pp486−489 を参照、共に此処に参照して合同するものとする。)
【0003】
分離、免疫検定、磁気共鳴結像処理(MRI)、薬品配送、及び高体温は磁性粒子の使用で向上する。関心箇所での診断を可能にする生体検出に使用される磁性粒子の一例がPhilipsのMagnotech携帯技術によって開示された。Magnotechは携帯用解析器に挿入される使い捨ての生体センサのカートリッジに合同された磁性ナノ粒子を使用してピコモル単位の対象分子をただの数分間で測定する。液体洗浄工程を簡素化することによって、この技術は更に使用を容易にしている。磁性ビーズは種々の生体検出の応用に使用されているが、これには屡複雑な表面の機能化が伴う。表面コーティングの適合性及び安定性は結合の毒性及び堅牢性に影響することがある。
【発明の概要】
【0004】
此処に提供されるのは、生物学及び医学的検出に応用される磁性炭素ナノチューブを含む新規なハイブリッド物質システムmCNTである。或る実施形態の場合、システムには炭素ナノチューブ(CNT)の内部に磁性物質が含まれる。CNT内の磁性粒子の量はmCNTが小型,廉価、携帯可能の磁石に呼応出来るものであってよい。CNTの外面は生体分子的付着又はその他の機能化用にそのままに保持される。この新規な物質による性能向上には、感度の向上、応答時間の短縮、及びサンプル量の減少が含まれる。種々の実施形態の場合、mCNTはこれらのアッセイにおいて、又は活性検知要素として関与する分子に密着する下地層である。更に提供されるものは、印刷された電極上の二次元的なmCNT及びCNTのネットワークの製法である。
【0005】
本発明はその一面において内部空洞と外面、内部空洞内に位置される磁性物質、及び外面に付着する複数の捕獲因子を有する炭素ナノチューブを含むmCNT物質に関する。捕獲因子は対象物に結合、又はそれ以外の様相で捕獲可能な分子であってよい。捕獲因子は合成因子及び非合成因子を含む有機又は無機の捕獲因子であってよい。生体分子捕獲因子の例には抗体、酵素、オリゴヌクレチド、アプタマー、抗体断片、及び分子的にインプリントされた高分子がある。或る実施形態の場合、ナノチューブに付着する捕獲因子は選択的又は非選択的に対象物に結合するように構成された抗体のようなリポーター因子であってよい。多くの実施形態の場合、磁性物質は例えばナノクラスターのような粒子の形態の鉄、コバルト、ニッケル、又はそれらの合金或は混合物のような強磁性物質である。種々の実施形態の場合、mCNT物質には複数のかような炭素ナノチューブが含まれる。或る実施形態の場合、例えば粉末とかタブレットの形態で供給される。他の実施形態の場合、mCNT物質は溶液の中に在る。溶液の中で複数の炭素ナノチューブは或る実施形態の磁界の応用によってメッシュネットワークを形成する。或る実施形態の場合、磁性物質はナノチューブの空洞内に閉鎖され、ナノチューブ外面、又はナノチューブの内部空洞の中以外には実質上磁性物質が存在しない。空洞の端部は開いていても、閉じていてもよい。
【0006】
別の面において、本発明はサンプル内の生体分子対象物を感知する方法に関する。或る実施形態の場合、この方法は内部空洞,内部空洞内に位置される磁性物質を有する外面、及び外面に付着する対象物に結合するように構成された複数の捕獲因子を有する複数の炭素ナノチューブを供給する工程と、これら複数の炭素ナノチューブを溶液に分散する工程と、これら複数の炭素ナノチューブをサンプルに接触させてサンプル内の生体分子対象物を溶液内の捕獲因子と結合させる工程と、磁界を印加して溶液内の複数の炭素ナノチューブを感知電極に移送する工程と、対象物の存在を感知する工程とから成る。
【0007】
更に別の面において、本発明はサンプル容器、サンプル容器内のサンプルに接触するように構成された電極、内部空洞、内部空洞内に位置される磁性物質を有する外面、及び外面に付着する対象物に結合するように構成された複数の捕獲因子を有する複数の炭素ナノチューブ、及び複数の炭素ナノチューブに磁力を及ぼして電極に関して移動するように構成された磁石を含む溶液内の生体分子対象物を感知するシステムに関する。
【0008】
本発明のこれら及びその他の面は以下において図を参照して説明される。
【図面の簡単な説明】
【0009】
【図1】強磁性粒子を中に有する炭素ナノチューブを含む或る実施形態のmCNTを図示する。
【図2】或る実施形態のmCNTを使用するアッセイの代表的図示である。
【図3】或る実施形態の場合の活性結核(TB)のような条件の為の新規な診断用生体センサの一実施形態を示す。
【図4】CNT404を含む電極402を有する装置400の像を示す。
【図5】ランダムに分布されたCNTネットワークのSEM像である。
【図6】磁界が印加された溶液に吊るされたmCNTの像である。
【発明を実施するための形態】
【0010】
本発明は表面特性及び磁性特性の独立制御を可能とする新しいシステムを提供する。種々の実施形態の場合、本発明は炭素ナノチューブ(CNT)を使用する高性能の化学的及び生物学的検出に関する。或る実施形態の場合、生物学的及び他の対象物の検出の為、CNT内にナノ磁性物質が埋め込まれた新規なハイブリッド物質システムが提供される。ここでは、このハイブリッド物質をmCNTと称する。この新規な物質は、向上された感度、短縮された応答時間、及び減少されたサンプル体積など、多くの面で向上された特性を提供する。更にこの新規な物質及び此処に記載される観念は種々の製品構成に応用可能である。その例は以下のごとくである。
【0011】
或る実施形態の場合、mCNTは免疫学的又は他の生物学的アッセイに使用される。mCNTはこれらのアッセイに関与する複数の分子が密着する下地層の物質として役立つ。この物質は機能的面積を有意義的に向上するので、磁性ビーズ及び粒子で生成される有用な特性が向上する。mCNTは生物学的捕獲を使用するすべてのタイプの対象物(核酸、蛋白質、抗体、グリカン)及び検出プラットホーム(例えば光学的、電気測定的、電気化学的、ラベル無し)に使用可能である。
【0012】
或る実施形態の場合、mCNTには鉄、コバルト、ガドリニウム、ジスプロシウム、又は強磁性を有するその他の物質のような強磁性物質の一種以上で充填されたナノチューブが含まれる。金属を包み込んだり、金属又は金属の炭化物及び酸化物をCNTに導入する種々の技術により電子的及び力学的特性は有意義的に変更可能であろう。例えば、個々の炭素ナノチューブの電気伝導度はそれに埋め込まれたナノスケールの磁石の磁性遷移に敏感であることが示されている。強磁性物質で充填されたナノチューブも、その磁性データ貯蔵技術への応用の可能性故に可成り興味を惹かれている。
【0013】
或る実施形態の場合、mCNTにはナノチューブの外面に実質上磁性物質のないナノチューブシェルが含まれる。ナノチューブシェルとは内部の強磁性クラスターの酸化を防止し、長期間に亘る安定性を向上させるものである。或る実施形態の場合、mCNTの製造プロセスでナノチューブの端部が開かれる。例えば或る実施形態の場合、CNTの精製及び酸処理(例えば濃硝酸及び硫酸による酸化)によってナノチューブ端部にカルボキシ基(−COOH)のような機能基が生成される。これは対応する金属塩を還元する電気化学的方法によってナノチューブ内に金属(強磁性)粒子を堆積するのに有用である。或る実施形態の場合、CNTの磁性化の後、金属粒子の露出を防止して更に安定性を向上するように端部がカバーされる。
【0014】
CNTの内部に磁性クラスターが埋め込まれたCNTを生成する製造のアプローチはSoldano et alによって開示されている。(”Detection of nanoscale magnetic activity using a single carbon nanotube”, Nano Letters. 2008;8(12), pp4498−4505,此処に参照して合同されるものとする。)この中で、物質は単一の炭素ナノチューブによってナノスケールの磁性活性の検査に使用された。
【0015】
種々の実施形態の場合、この物質は磁性ビーズの代わりに生物学的及び医学的応用において使用される。この物質はCNTの内部に磁性物質を有する。もし磁性物質のあるのがCNTの外側であったなら、この物質は対象物の検出中に測定される電気化学的信号に関与することとなり、場合によっては毒性を増加させることになろう。磁性クラスターがCNTの内部のみに位置するので、CNTの表面はそのままであり、興味の対象である対象物に特殊性を与える化学物質で容易に機能化可能である。例えば、生体分子捕獲因子には抗体、酵素、オリゴヌクレオチド、アパタマー及び抗体断片が含まれる。非生体分子捕獲因子には分子的にインプリントされた高分子が含まれてよい。
【0016】
図1は或る実施形態の場合のmCNT100の略図である。mCNT100には中にコバルトナノクラスター104を有する炭素ナノチューブ102が含まれる。種々の実施形態の場合、応用面によりmCNTの直径は約1nmから20nmの間であり、長さは約50nmから数ミリメートルの間であるが、これらの特定された範囲に限定されるものではない。図示の実施形態の場合、mCNT100には外面上に抗体機能化が含まれ、抗体106がCNT102の側壁に付着している。抗体106はmCNT100を機能化して対象の抗原108を捕獲する。種々の実施形態の場合、mCNTに適応される捕獲化学形態の例として、酵素、核酸、抗体、アプタマー、オリゴヌクレオチド、抗原、及びグリカンがある。付着の方法には吸着、共有性結合、ストレプトアビジン/ビオチン、及びその他の既知のCNTを機能化する方法が含まれる。
【0017】
mCNTの機能化及び使用の一例が以下のように記載される:
1.生体分子が物理的吸着又はカルボジイミド又はグルタアルデヒド交差結合のような選択的化学形式を使用してmCNTに付着される。例えば電気化学的酵素―結合された免疫吸着アッセイ(ELISA)の中で、心臓トロポニンIのような捕獲抗体が付着されてよい。対象に特定的な酵素がグルコース又はクレアチニン検出のような酵素アッセイに付着される。どのような既知の捕獲化学形態が使用されてもよいことは、当業者には自明であろう。
2.mCNTの非機能化面はサンプルやリポーター物質の非特定的な付着を防止するように、ウシ血清アルブミン(BSA)又はツイーン−20のような界面活性剤のような蛋白質で封鎖されている。mCNTと蛋白質/抗体/界面活性剤の間の疎水性反応はこれに有用である。
3.機能化されたmCNTは溶液に入れられる。この溶液は例えば水、エタノール、ジメチルフォルムアミド(DMF)、テトラヒドロフラン(THF)、又は水中のドデシル硫酸ナトリウム(SDS)のような界面活性剤のようなCNT分散用の普通の液体であってよい。生体分子との適合性のため、水性溶媒が好適である。分散液とmCNTの溶液には電気化学的反応に関与したリポーター化学形態が含まれてもよい。或る実施形態の場合、リポーターは必要でなく、これは典型的に「ラベル無し」と呼ばれる。典型的な電気化学的ELISAの場合、ラベルは信号の増幅に必要である。ラベルは対象物(即ちリポーター)用の二次抗体に付着された山葵ペルオキシダーゼ(HRP)にような酵素であってよい。
4.溶液はサンプルに混合される。サンプルの例には尿、痰、唾液、血液、呼気凝縮液などがある。これは種々の状態で実行可能である。チューブ、微小ウエル板、又は好適に携帯用リーダーにはまるカートリジの中で可能である。
【0018】
図2は或る実施形態の場合のmCNTを使用するアッセイの略図である。捕獲抗体206はスクリーン印刷された電極の近くに磁力(図示せず)で保持されるmCNT201に付着されている。捕獲抗体206はリポーター抗体209にも結合する対象物208を捕獲するように構成されている。酵素211は報告用リポーター抗体209に付着している。
【0019】
mCNTが無い場合、ラベルが捕獲抗体、対象物、及び二次抗体(リポーター)サンドイッチの為電極から或る距離に位置すると言う事実の理由で酵素活性地域211と電極201の間に電子を移動させる電子往復運動が必要である。mCNTを使用すると、或る実施形態の場合、サンドイッチ形成が溶液の中で起こる。磁界が印加された後、リポーターを含めてサンドイッチ集合体の全部が物理的に電極の近くに移動され、これによりラベルと電極の間の直接の電子的交信の可能性が向上する。これにより、ラベルの検出用の下地層の必要性が除去される。製品カートリッジに貯蔵されるべき試薬もより少なくなる。アッセイ工程が少なくなり、アッセイ速度が改善する。流体工学、バルブ、及びポンプに関する要求も簡素化される。酵素と電極の間の直接電子的交信がmCNTの使用で確立される酵素のアッセイにもこの原則は応用され、電子の往復運度の必要性が除去される。
【0020】
酵素の活性地域又は他のラベルがCNTでアクセス不可能であるか、別の組成物(又は伝達物質)の或る反応の触媒作用がより高速或は低エネルギイである場合、活性地域への交信に伝達物質が使用可能である。典型的な伝達物質(例えば2,2’−アジノビス(3−エチルベンゾチアゾリン−6−スルフォネート)(ABTS)又は3,3’,5,5’−テトラメチルベンジディン(TMBB))はCNTの上に吸着し、この目的に有用である。ラベル無しのアプローチは選択的に高濃度を要求するアッセイ(例えばC−活性蛋白質(CRP)−ng/mlから g/mlの範囲)へカートリッジ上で使用可能なアッセイのメニュから適応可能である。酵素に加えて、シトクローム−C(Fe(III)(Cytc) Fe(II)(Cyt−c)のような電気化学的活性を示す他のラベル、ZnS,CdS,PbS,CuSのようなコロイド状金属結晶も使用可能であり、上記のアプローチに適当である。
【0021】
溶液内の活性要素が磁性成分を含むと言う事実は、磁性攪拌が対象物の分散/遭遇の割合及び捕獲の向上に使用可能であることを意味する。リポーター及び捕獲抗体の間のサンドイッチ形成はアッセイを速くするバルク相で起こる。これは捕獲抗体が電極上で不動化されている電気化学的ELISAの中で典型的に起こる2相反応と比較される。攪拌には例えば回転的、側方的、前後的など多種の運動のいずれも使用可能である。全体の扇動の度合も例えば乳液の生成の抑制であるとか、mCNTの機能化を退化させるため(低攪拌)とか、多くの理由の中のいくつかによって制御されてもよい。
【0022】
サンプルの配達及び流れの経路に関する製品構成において、mCNT/捕獲/対象物/リポータコンプレックスを感知地区に移動するのに磁石が使用可能である。例えば、カートリッジの下に位置する電磁石によって捕獲された対象物分子を含めてmCNTを生体センサの活性検出面へと移動させることが可能である。測定は光学的技術で実施可能である、測定は更に外部回路に接続されたベース電極にmCNTを接触させることにより電気的に実施可能である。
【0023】
mCNTには分子を容易に付着するため複数の経路がある。対照的に、複数酵素ラベル付けのアプローチで使用されるビーズや粒子の多くには例えばアミン又はカルボキシル基のような単一の化学的配合部分が存在する。二種以上の異なるタイプの機能グループが存在しないと言うことは、異なるタイプの分子を付着させる容易な経路がないと言うことを意味する。均一的化学構成のこれらの物質の場合、各分子の支持体への特別なローディングを得るため、適当な動的制御(即ち反応のタイミング)又は複数の結合体の適当なモル比が要求される。対照的に、単一の炭素ナノチューブが異なる分子を付着する複数の化学的部分をもつことがある。つまり、炭素ナノチューブの端部はナノチューブの中央部とは異なる化学的構成である。或る実施形態の場合、CNTの側壁はsp2結合構成で特徴付けされる一方、チューブの端部は懸垂的結合を有して側壁部より反応性である。向上された反応性は欠陥によって中央部に向かって伸びることもあるが、これは端部から数個の原子の範囲である。端部での懸垂的結合の存在により、例えば酸処理によるCNTの精製及び機能化の期間中に機能基が生成されることもある。このことは、第二の異なる化学的部分がナノチューブの中央部に亘って拡散する一方、炭素ナノチューブのより反応的な端部は選択的に或る機能的部分に変換される可能性があることを意味する。代行的に、本体が機能化されないまま残されて分子の簡単な物理吸着的付着に使用される一方、端部が機能化されてもよい。二つの異なる付着経路があるということは、物質上の異なるタイプの分子の量の制御の向上を含め、これらの物質の容易な構成を供するものである。
【0024】
或る実施形態の場合、磁性粒子の置換に加え、mCNTは活性的な感知用要素として使用可能である。実施形態の中の一つの場合、mCNTは下地層の上に堆積されて電極を形成する。その構成と直径とは所望の電気的特性を達成するために独立的に最適化可能である。上記のような化学的及び磁石のデザインの進歩のみならず、mCNTの高度の縦横比によって直接の読み出し用に電気的に接続可能なネットワーク構成が可能にされる。図3は或る実施形態の場合例えば活性結核(TB)のような状態用の新規な診断用生体センサの実施例を示すものである。この生体センサには本発明の面が含まれて居り、最小の流体処理及び高感度を有するように構成されている。これにはサンプル容器302、その下側に付着されて容器302内のサンプルにまで伸びている電極305を含む蓋304、可動性及び/又は容器に対してスイッチ可能な磁石308、及びリーダー310が含まれている。磁石308は容器に対して移動可能な永久磁石であっても、又はオンとオフにスイッチ可能な電磁石であってもよい。必要とされる試薬を分散させるための試薬タブレット306がサンプル容器302内に位置されてもよい。下記のように、これにはmCNTが含まれていてもよい。
【0025】
このような装置を使用する試験のプロトコルの一例は以下のようなものである:
1.容器にサンプルを収集する
2.蓋をつける
3.内容物(対象物がmCNTを結合)を旋回させる
4.磁界を印加する(サンドイッチ形成)
5.磁界及び旋回を反転(非結合のmCNTは容器の底に密着)
6.静電容量を測定
【0026】
一実施形態の場合、捕獲抗体は静電容量の測定に構成された標準的な導電性カーボンインク電極(即ちグルコースの試験片)の上に不動化される。リポーター抗体はmCNTの上に不動化される。磁気特性はチューブの核部に電気化学的に堆積されたコバルトナノクラスターによって付与される。リポーター抗体はバルク溶液内の対象物と結合し、溶液の緩慢な旋回で動特性が向上する。その後、このコンプレクスを急速に電極表面に移動してサンドイッチの形成を完了すべく磁石が位置される。抗体は対象物にとって特殊なので、サンドイッチ構成の形成には対象物が必要である。サンドイッチの形成後、非結合のリポーター抗体が静電容量電極の近辺から除去されて対象物特殊性を付与するように磁石の位置及び/又は方向が変更される。残留するmCNT(対象物と通じて結合)は電極静電容量を増加させ、対象物の存在を示す。CNTは実質的に電気化学的キャパシタ(例えば尿のような電解質の中の多孔質のメッシュ構成)を形成するものであるから、電極の静電容量を増加するものである。このような種類のメッシュ構成は磁性ビーズとか他の試験で通常使用される他のナノ粒子で形成することはできないが、高縦横比のCNTの幾何学的形状でこの発明のアプローチは可能とされる。CNTはそのナノスケール次元の為に表面積が大きい。このために検出の感度が向上される。CNTに存在する機能基(例えば−COOH)はいずれもCNTと電極の結合に関連する静電容量の変化を更に増加する。
【0027】
典型的な尿サンプルには酵素免疫アッセイ(EIA)及び免疫色彩側方流動(ICLF)テストで使用されるものより体積で殆ど3桁よけいに大きい。この非慣習的テストは使用可能なサンプル体積の全体を使用するようにデザインされたものであり、バルク溶液の中の対象物を捕獲するのに効率的な方法を使用し、トランスジューサ表面にそれを集中する。このテストは並み以下の体積で収集され、又は並み以下の体積に希釈された生物学的又は環境的サンプル(例えば尿、飲料水、その他)内の低含量分子の検出に広く応用される。提案されたこのテストは既に容認されている数々の化学的検出法で使用される成分を集めたものである。この新規なテストでは、対象物認識にEIAやICLFで使用されると同じ抗体サンドイッチ手法(リポーター+対象物+捕獲)が使用される。但し、対象物の光学的リポーティングの代わり、テストを更に簡素化するために直接な電子的測定が使用されている。
【0028】
或る実施形態の場合、テストは全体的に標準的な尿サンプル収集用容器の中で実施され、必要なのは永久磁石の旋回と移動のみである。代行的に無ステップのアッセイに電磁石が使用されてもよい。ビンの中には既にリポーター抗体によって接合されたmCNTの乾燥粉末を入れた小型の水/尿溶解性のカプセルが入れられる。サンプルはシステムを再水和するので、液体試薬は不必要である。有意義的なことであるが、非結合mCNTは一度電極から数マイクロメートル離れるとすでに局地的容量には影響しないので、この磁性的分離では「洗浄」工程が不必要となる。従って、このテストでは追加的液体試薬とか流体処理が不必要である。
【0029】
図3に示される構成の場合、電極305は蓋304の下側に付けられてあり、蓋の上部に付けられた安価な太陽光線で充電される時計に似た簡単な再使用可能なリーダー310で計測される。このリーダーは結果をデジタル出力として提供する。測定は電子的なので、正負の制御又は複数個の対象物のマルチプレクス検出が容易に実施される。
【0030】
此処に記載される生体センサはmCNTが如何に対象物捕獲及び感知要素として使用可能であるかの多くの例の一つである。免疫学的要素による広範囲に亘る種々の抗原及び抗体検出に加えて、本発明の実施形態に従ってmCNTを使用可能の種々のタイプのアッセイには、以下のものが含まれる:
1)例えばCD4(例えば此処に参照により合同されるものとするGao et al.,Magnetic based immunoassay for enumeration of CD4(+)T lymphocytes on a microfluidic device. Talanta 82:528−533(2010)を参照)又は癌(例えば此処に参照により合同されるものとするMa et al.,Magnetization of large polystyrene peptide beads for capturing and expanding cancer cells. J.of Magnetism and Magnetic Materials 264:153−157(2003)を参照)のような溶液からの捕獲及び検出に特殊な細胞
2)核酸異種交配アッセイ例えば此処に参照により合同されるものとするShepard,A.R and J.L.Rae.,Magnetic capture of cDNAs from double−stranded plasmid cDNA libraries. Nucleic Acids Research 25:3183−3185(1997)を参照)
3)核酸増幅システムに応答するサンプルへの統合(例えば此処に参照により合同されるものとするDill et al. Fully integrated device for direct sample−to−answer genetic analysis. Integrated Analytical Systems;Microarrays, Springer New Yorl(2009)を参照)
4)流体血球計算(例えば此処に参照により合同されるものとするm Yang et al,Biosensors and Bioelectronics 24:855−862(2008)を参照)
5)膠着接合アッセイ(例えば此処に参照により合同されるものとするMoser et al.m On−chip immuno−agglutination assay with analyte capture by dynamic manipulation of superparmagnetic beads. Lab on a Chip 9:3261−3267(2009)を参照);及び
6)脂質解析(例えば此処に参照により合同されるものとするNauck et al., New Immunoseparation−based homogeneous assay for HDL−cholesterol compared with three homogeneous and two heterogeneous methods for HDL−cholesterol., Clinical Chemistry 44:1443−1451 (1998)を参照)
【0031】
此処に記載された教示を基にして、当業者には如何にして磁性ビーズやその他の磁性要素の代わりにmCNTがこれらのアッセイに、又免疫学的要素で種々の抗原及び抗体の検出に応用されるか、理解されることであろう。
【0032】
本発明はその他の面においてCNTに基づく増幅機構と結合されるCNTネットワークに関するものである。単壁型のCNTフォレストプラットホームに複ラベル二次抗体ナノチューブ生体接合体を結合することは既に示されたことである。SWNTフォレストはナフィオン-酸化鉄の装飾導電面上に直立した束として立つものであった。感度の向上は達成された。しかし、技術の実現は電極製造のプロセスが複雑なので阻止されていた。或る実施形態の場合、CNT及び/又はmCNTネットワークが電極として使用される。基盤電極はスクリーン印刷のような通常の手段で製造可能である。CNT及び/又はmCNTネットワークは例えばBiodotのような市場で入手可能な基盤電極の上に堆積可能である。図4はCNT404を含む電極402を有する装置400の像を示す。Biodotによって最終的装置の上に堆積されたCNTのSEM(走査型電子顕微鏡)像の一例が図5に示されている。その結果として、スクリーン印刷された炭素インクで定義された電極の上に炭素ナノチューブネットワークが均一的に分配されていることが示されている。
【0033】
電気化学的検出に種々の方法が使用される。異なる酵素ラベル、金属ナノ粒子、その他の電子的活性ラベルが多重化に使用される。リポーター抗体への酵素ラベルと共に、酵素下地層の存在のもとで伝達物質用のレドクス電流が電流測定法による対象物の定量化に使用される。結合イベントごとに得られる酵素分子を増大させるためにリポーター抗体と共に複数の酵素ラベルがCNTに付着可能である。工程数を減少させるために、シトクローム−C(Fe(III)(Cyt c)→Fe(II)(Cyt−c))のような電気化学的活性を示すその他のラベルが使用されてもよい。CNT又はリポーター抗体はZnS,CdS,PbS,CuSのようなコロイド状金属結晶でラベル付けされ、陽極ストリッピング法ボルタメトリによって検出されてもよい。
【0034】
例
CNTは陽極酸化されたアルミナテンプレートの中で化学蒸着(CVD)によって成長された。CNTの直径はテンプレートの孔サイズによって容易に制御された。次いで、電気化学的堆積によってナノチューブ(mCNT)内で強磁性ナノ粒子が形成された。埋め込まれた何千もの磁性ナノ粒子の集合的動作及びこれらがCNTに強力な強磁性動作を付与する能力が調査された。その結果、mCNTは 埋め込まれた磁性ナノクラスターが良好な分離特性を提供するのに十分であることを示すことが分かった。図6は永久磁石を使用することによってバルク溶液から分離されたmCNTの像である。mCNTは超純水の中でガラスの小瓶の背後に位置された永久磁石(印付き)によって溶液から分離されている。対照的に、非磁性のCNTは小瓶の底に沈殿する。
【0035】
本発明による方法及び装置の好適な実施形態がこのように記載された後、当業者にはこのシステムが有利であることが自明であろう。これらの種々の変更、応用、代行実施形態も本発明の範囲及び精神の範囲内であることが理解されよう。異なるラベル及び電気化学的測定法も磁性CNTに基づくシステムに応用可能であり、これも当業者には自明であろう。従って、装置の感度及び特殊性などの性能の度合は特殊な応用面で要求される追加的流体処理及び測定工程での必要性でバランス可能である。
【特許請求の範囲】
【請求項1】
内部空洞及び外面を有する炭素ナノチューブと、
前記内部空洞の内部に位置する磁性物質と、
前記外面に付着する複数の捕獲因子と、
を備える、mCNT物質。
【請求項2】
請求項1に記載のmCNT物質であって、
各々が、内部空洞と、前記内部空洞内に位置する磁性物質を有する外面と、前記外面に付着する複数の捕獲因子と、を有する複数の炭素ナノチューブを備える、mCNT物質。
【請求項3】
請求項1または請求項2に記載のmCNT物質であって、
前記磁性物質は強磁性物質である、mCNT物質。
【請求項4】
請求項3に記載のmCNT物質であって、
前記強磁性物質はコバルト、鉄、及びニッケルの中の少なくともの一つである、mCNT物質。
【請求項5】
請求項2または請求項3に記載のmCNT物質であって、
前記物質は粉末の形状である、mCNT物質。
【請求項6】
請求項5に記載のmCNT物質であって、
前記物質は溶液の外にある、mCNT物質。
【請求項7】
請求項2または請求項5に記載のmCNT物質であって、
前記物質は溶液の中にある、mCNT物質。
【請求項8】
請求項7に記載のmCNT物質であって、
前記複数の炭素ナノチューブは、磁界の印加のもとで前記溶液の中にメッシュを形成する、mCNT物質。
【請求項9】
請求項1に記載のmCNT物質であって、
前記外面上に実質上磁性物質が存在しない、mCNT物質。
【請求項10】
請求項1に記載のmCNT物質であって、
一つ以上の空洞端部が開いている、mCNT物質。
【請求項11】
請求項1に記載のmCNT物質であって、
一つ以上の空洞端部が閉じている、mCNT物質。
【請求項12】
サンプル内の生体分子対象物を感知する方法であって、
内部空洞と、前記内部空洞内に位置される磁性物質を有する外面と、前記外面に付着する対象物に結合するように構成された複数の捕獲因子と、を有する複数の炭素ナノチューブを供給する工程と、
前記複数の炭素ナノチューブを溶液に分散する工程と、
前記複数の炭素ナノチューブを前記サンプルに接触させて前記サンプル内の生体分子対象物を溶液内の捕獲因子と結合させる工程と、
磁界を印加して前記溶液内の前記複数の炭素ナノチューブを感知電極に移送する工程と、
前記対象物の存在を感知する工程と、
を備える、方法。
【請求項13】
サンプル内の生体分子対象物を感知する方法であって、
内部空洞と、前記内部空洞内に位置される磁性物質を有する外面と、前記外面に付着する複数のリポーター因子と、を有する複数の炭素ナノチューブを供給する工程と、
電極の上に複数の捕獲因子を供給する工程と、
前記複数の炭素ナノチューブを溶液に分散する工程と、
前記複数の炭素ナノチューブを前記サンプルに接触させて前記サンプル内の生体分子対象物を溶液内のリポーター因子と結合させる工程と、
磁界を印加して、それにより前記溶液内の前記複数の炭素ナノチューブを前記電極に移送し、リポーター因子−対象物−捕獲因子のサンドイッチ構成を形成する工程と、
前記対象物を感知する工程と、
を備える、方法。
【請求項14】
溶液の中の生体分子対象物を感知するシステムであって、
サンプル容器と、
前記サンプル容器の中のサンプルに接触するように構成された電極と、
内部空洞と、前記内部空洞内に位置される磁性物質を有する外面と、前記外面に付着する対象物に結合するように構成された複数の捕獲因子と、を有する複数の炭素ナノチューブと、
前記複数の炭素ナノチューブに磁界を作用してこれらを前記電極に対して移動させるように構成された磁石と、
を備える、システム。
【請求項1】
内部空洞及び外面を有する炭素ナノチューブと、
前記内部空洞の内部に位置する磁性物質と、
前記外面に付着する複数の捕獲因子と、
を備える、mCNT物質。
【請求項2】
請求項1に記載のmCNT物質であって、
各々が、内部空洞と、前記内部空洞内に位置する磁性物質を有する外面と、前記外面に付着する複数の捕獲因子と、を有する複数の炭素ナノチューブを備える、mCNT物質。
【請求項3】
請求項1または請求項2に記載のmCNT物質であって、
前記磁性物質は強磁性物質である、mCNT物質。
【請求項4】
請求項3に記載のmCNT物質であって、
前記強磁性物質はコバルト、鉄、及びニッケルの中の少なくともの一つである、mCNT物質。
【請求項5】
請求項2または請求項3に記載のmCNT物質であって、
前記物質は粉末の形状である、mCNT物質。
【請求項6】
請求項5に記載のmCNT物質であって、
前記物質は溶液の外にある、mCNT物質。
【請求項7】
請求項2または請求項5に記載のmCNT物質であって、
前記物質は溶液の中にある、mCNT物質。
【請求項8】
請求項7に記載のmCNT物質であって、
前記複数の炭素ナノチューブは、磁界の印加のもとで前記溶液の中にメッシュを形成する、mCNT物質。
【請求項9】
請求項1に記載のmCNT物質であって、
前記外面上に実質上磁性物質が存在しない、mCNT物質。
【請求項10】
請求項1に記載のmCNT物質であって、
一つ以上の空洞端部が開いている、mCNT物質。
【請求項11】
請求項1に記載のmCNT物質であって、
一つ以上の空洞端部が閉じている、mCNT物質。
【請求項12】
サンプル内の生体分子対象物を感知する方法であって、
内部空洞と、前記内部空洞内に位置される磁性物質を有する外面と、前記外面に付着する対象物に結合するように構成された複数の捕獲因子と、を有する複数の炭素ナノチューブを供給する工程と、
前記複数の炭素ナノチューブを溶液に分散する工程と、
前記複数の炭素ナノチューブを前記サンプルに接触させて前記サンプル内の生体分子対象物を溶液内の捕獲因子と結合させる工程と、
磁界を印加して前記溶液内の前記複数の炭素ナノチューブを感知電極に移送する工程と、
前記対象物の存在を感知する工程と、
を備える、方法。
【請求項13】
サンプル内の生体分子対象物を感知する方法であって、
内部空洞と、前記内部空洞内に位置される磁性物質を有する外面と、前記外面に付着する複数のリポーター因子と、を有する複数の炭素ナノチューブを供給する工程と、
電極の上に複数の捕獲因子を供給する工程と、
前記複数の炭素ナノチューブを溶液に分散する工程と、
前記複数の炭素ナノチューブを前記サンプルに接触させて前記サンプル内の生体分子対象物を溶液内のリポーター因子と結合させる工程と、
磁界を印加して、それにより前記溶液内の前記複数の炭素ナノチューブを前記電極に移送し、リポーター因子−対象物−捕獲因子のサンドイッチ構成を形成する工程と、
前記対象物を感知する工程と、
を備える、方法。
【請求項14】
溶液の中の生体分子対象物を感知するシステムであって、
サンプル容器と、
前記サンプル容器の中のサンプルに接触するように構成された電極と、
内部空洞と、前記内部空洞内に位置される磁性物質を有する外面と、前記外面に付着する対象物に結合するように構成された複数の捕獲因子と、を有する複数の炭素ナノチューブと、
前記複数の炭素ナノチューブに磁界を作用してこれらを前記電極に対して移動させるように構成された磁石と、
を備える、システム。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公表番号】特表2013−501921(P2013−501921A)
【公表日】平成25年1月17日(2013.1.17)
【国際特許分類】
【出願番号】特願2012−523989(P2012−523989)
【出願日】平成22年8月6日(2010.8.6)
【国際出願番号】PCT/US2010/044778
【国際公開番号】WO2011/017660
【国際公開日】平成23年2月10日(2011.2.10)
【出願人】(504468470)ナノミックス・インコーポレーテッド (12)
【Fターム(参考)】
【公表日】平成25年1月17日(2013.1.17)
【国際特許分類】
【出願日】平成22年8月6日(2010.8.6)
【国際出願番号】PCT/US2010/044778
【国際公開番号】WO2011/017660
【国際公開日】平成23年2月10日(2011.2.10)
【出願人】(504468470)ナノミックス・インコーポレーテッド (12)
【Fターム(参考)】
[ Back to top ]

