神経活動計測装置及びその方法
【課題】一般的な細胞、細胞膜そのものの応答ではなく、神経細胞そのものの応答(電気的な応答)を計測する装置を提供し、神経活動そのものの電気的計測を実現することで、神経細胞の疾病の予測、診断の実現などを提供する。
【解決手段】神経伝達時に電圧が発生することを鑑み、神経細胞1へ電気的な刺激を与えることを特徴とする刺激装置14と、該神経細胞を伝播した電気信号を検出することを特徴とするカンチレバー4を具備することを特徴とするケルビンプローブ。
【解決手段】神経伝達時に電圧が発生することを鑑み、神経細胞1へ電気的な刺激を与えることを特徴とする刺激装置14と、該神経細胞を伝播した電気信号を検出することを特徴とするカンチレバー4を具備することを特徴とするケルビンプローブ。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、生体神経細胞の活動の計測法及び計測装置に関わるものである。
【背景技術】
【0002】
従来の研究では、例えば精神疾患を患う患者に対して、近赤外分光法により脳活動を計測し、得られた波形に応じて精神疾患を分別する方法が非特許文献1に開示されている。この方法では、被検査体へ光照射用プローブと光検出プローブを被検査体の頭部に代表する皮膚上へ装着させる。そして、被検査体へ問いかけのタスクを課し、そのタスクを課した期間に対応する時間帯での生体組織を通過した光の強度の変化を、そのタスクを課した期間の前後での生体組織を通過した光の強度を基準に算出し、血液量変化を算出する。この血液量変化は、大凡100msの時間分解能を有し、時刻に対する波形として、また、被検査体へ照射する光を複数波長とすることで、酸素化ヘモグロビンに関する血液量変化と脱酸素化ヘモグロビンに関する血液量変化を同時に計測することが出来る。
【0003】
これらの波形を疾病群毎に比較すると、健常者、統合失調症、双極性障がい、うつ病群へ弁別することが出来、その時点での被検査体の精神状態を推定することが出来る。
【0004】
この計測方法は、罹患中の被検査体に限らず、健常な状態の被検査体へも適用でき、また、投薬による疾病からの緩和状態を追跡することも出来る。このため、適用可能な応用範囲は幅広い。
一方で、より早期から、言い換えれば出生直後から、疾患へ罹患する可能性を検出することが出来れば、子供に対して適切なケアを早期に取り組むことが出来、その効果は高い。
【0005】
また、走査プローブ顕微鏡(以下SPMともいう)を用いて生物試料を観察する試みが近年活発となってきている。
【0006】
走査プローブ顕微鏡は、金属探針を用いて物性像と形状が同時に得られることが可能であり、形状と物性の相関を解析することが高い空間分解能で容易にできるという特徴がある。
SPMに係わる従来の技術においては、特許文献1により、外部刺激(物理的、化学的)に対する細胞内の電位変化の測定による細胞の機能解析、また、特許文献2では、がん細胞を含む細胞サンプル(培養細胞、神経細胞)に対して、生化学反応などの外部刺激を加えて、AFM(原子間力顕微鏡)でその応答としての細胞膜の変異などから細胞の特性を測定し、薬剤のスクリーニングを行い、もしくは診断を行うものなどが開示されている。
また、近年Rett症候群に罹患した生体より神経細胞を培養し、その機能等についての検討がなされている(非特許文献2)。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2008−079608号公報
【特許文献2】特表2008−539697号公報
【非特許文献】
【0008】
【非特許文献1】精神疾患とNIRS、福田正人編、中山書店(pp.79-102)
【非特許文献2】A Model for Neural Development and Treatment of Rett Syndrome Using Human Induced Pluripotent Stem Cells 、 Maria C.N.Marchetto他、Cell 143、527-539頁
【発明の概要】
【発明が解決しようとする課題】
【0009】
しかし、上記のように近赤外光を用いた脳機能計測においては、出生直後の被検査体の精神疾患の状態を早期に検出する手段についての報告はなされておらず、細胞レベルでの神経活動の評価を行うことはその特性上困難である。
【0010】
また、SPMを用いた計測においても、神経細胞そのものを計測対象とする技術についてはその計測手法を含め確立されていないのが現状である。
【0011】
そこで本発明では、一般的な細胞、細胞膜そのものの応答ではなく、神経細胞そのものの応答(電気的な応答)を計測する装置を提供し、神経活動そのものの電気的計測を実現することで、神経細胞の疾病の予測、診断の実現などを提供することを目的とする。
【課題を解決するための手段】
【0012】
本発明は、神経伝達時に電圧が発生することを鑑み、神経細胞へ電気的な刺激を与えることを特徴とする刺激装置と、該神経細胞を伝播した電気信号を検出することを特徴とするカンチレバーを具備することを特徴とするケルビンプローブを提供する。
【発明の効果】
【0013】
細胞レベルでの神経活動の計測を行うことにより、神経活動に由来する精神疾患の診断、並びに、将来の精神疾患の発症予測などの実現可能性がある。
また本計測手法によれば、被検者の状態に寄らず簡便に神経活動計測が可能となる。
【図面の簡単な説明】
【0014】
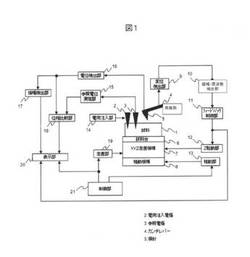
【図1】装置全体構成を示す図である。
【図2】計測の一例を示す図である。
【発明を実施するための形態】
【実施例1】
【0015】
図1は、本発明にて使用する神経活動計測装置の実施形態を示す構成図であり、図2は神経細胞の測定例である。これらを用いて以下説明する。
【0016】
測定試料1は神経細胞を想定しており、測定試料1の表面に対向する様にカンチレバー4が配置され、その先端には探針5が設けられている。
カンチレバー4および探針5は発振部に接続されており、固有振動数かその近傍の周波数で、測定試料1の表面に対して垂直方向に振動させられる。当該発振部は制御部21においてその動作が制御されている。
【0017】
測定試料1は試料台6を介してXYZ走査機構7および粗動機構8上に固定されており、XYZ走査機構7により探針5に対して3次元方位方向に移動させることができ、また、粗動機構8により測定試料1と探針8の間の距離を大きく変化させることができる。
【0018】
測定時に際して、まず、制御部21が粗動部13を用いて粗動機構8を駆動し、測定試料1の表面を探針8に接近させる。測定試料1と探針8が十分に接近すると、測定試料1の表面との相互作用によりカンチレバー4の振動状態が変化する。カンチレバー4の変位を変位検出部9を用いて検出し、さらに、振幅・周波数検出部10によりカンチレバー4の振動振幅あるいは周波数が検出される。
フィードバック制御部11は、カンチレバー4の振動振幅あるいは周波数が制御部21により設定された一定値となるように、Z駆動部12によりXYZ走査機構7をZ方向に駆動し、探針5と測定試料1表面との間の距離を一定に保つ。
【0019】
この状態において、制御部21が走査部19を用いてXYZ走査機構7をXY面内で走査すると、測定試料1の表面形状に合わせてXYZ走査機構7がZ方向位置を調整し、測定試料1の表面と探針5の先端の距離は常に一定に保たれる。
【0020】
測定においては、測定試料1の表面と探針8の先端の距離を常に一定に保ちながら行う。まず電荷注入部14を通じて電荷注入電極2より測定試料1に対して所定の電荷を注入することにより神経細胞である測定試料1に電圧を印加する。
電荷注入電極2により測定試料1に電圧(数mV〜数百mV程度)が印加されると、測定試料1上に配置されている参照電極3を通じて参照電位測定部15においてレファレンスデータとなる参照電位を測定する。当該参照電位は図示しない記憶部に格納される。
【0021】
電荷注入部14を通じて神経細胞である測定試料1に電圧を印加すると、パルス状の電流が生じ、測定試料の所望位置に金属探針5を接触、もしくは近接させることで、パルス的に流れる電流の影響により変化するカンチレバー4の変位量を変位検出部9において時系列的に検出する。
検出した変位量から、当該探針が接触もしくは近接する位置までに流れる電流を時系列的に計測することができる。
当該検出を測定試料1上の多点において行い、導通不良個所を特定することが可能となる。
不良個所の特定は、制御部21内に格納されるか、独立に存在する図示しない演算装置によって、予め記憶部において記憶されている上述の参照電位との比較を行い、参照電位とのかい離具合が所定値を超えた場合に不良と判定するものとする。また、参照電位との比較を例に示したが、順に計測する計測点における計測結果を順次比較することも可能である。
またここで、所定値の基準については、制御部に接続された図示しない入力部において任意に設定可能であることは言うまでもない。
【0022】
比較の具体的方法については、測定された結果について、振幅検出部17及び位相比較部18において夫々位相、振幅を算出し、それらと参照電位測定部の結果とを比較するものとする。
当該比較結果、もしくは、所定値を超える導通不良が見つかった箇所については、表示部20においてその結果を表示する様に構成しても良い。
【0023】
本実施例に記載の計測装置及び方法によれば、神経活動を簡便に測定することが可能となるだけでなく、細胞レベルでの導通不良を特定出来ることから、神経活動に由来する精神疾患の診断、並びに、将来の精神疾患の発症予測などの実現可能性がある。
【実施例2】
【0024】
上述の実施例1においては、事前の観察手段を設けていないが、事前に観察・測定する対象を目視できることは、計測をする際に有効であり、また、測定を自動化する際には形状測定は必要となる。
そこで、図1に示した構成において、形状観察モードを搭載する場合について、以下説明する。ここでは、実施例1と重複する内容については省略ものとする。
【0025】
まず、試料台6に測定試料1を載置した後に、カンチレバー4及び探針5に測定試料1を極近傍に接近させる。このとき、カンチレバー4は固有振動数かその近傍の周波数で、測定試料1の表面に対して垂直方向に振動させられる。カンチレバー4に接続された発振部は制御部21においてその動作が制御されている。
この状態で測定試料1上を探針5が走査し、探針5と測定試料1に作用する原子間力を検出する。この探針5と測定試料1表面を微小な力で接触させるか、近接させ、カンチレバーのたわみ量が一定になるように探針・試料間距離をフィードバック制御しながら走査することで、当該走査範囲における検出情報をもとに、演算装置において表面形状を取得する。
【0026】
取得した表面形状については、図示しない記憶部においてその形状を記憶し、制御部21において、表示部20にその形状を表示させる。
当該表示内容に基づき、ユーザが電荷注入電極2を与える場所を設定し、探針5の走査範囲、計測位置等を入力部を介して指定することが可能となる。
【0027】
また、神経細胞は表面形状に表れない場合もある。このため、以下の方法において形状を求めることもできる。
実施例1の内容と同様に、電荷注入電極2を介して電荷を注入し、測定試料1に対して所定の電圧を印加する。このとき、実施例1においては、所定の計測点に対する導通を計測したが、本例においては、所定範囲についてカンチレバー4を、探針5−測定試料1間の高さを保ちつつ、X-Y方向に2次元走査を行い界面電位分布を計測する。
【0028】
界面電位(接触電位差)は仕事関数の差を表すことが知られており、探針5−測定試料1の様に2つの仕事関数の異なる物質を接触もしくは近接させる際に、フェルミ準位が同じになるように電流が流れ、平衡状態では電位差が生じる。この差が探針5−測定試料1の仕事関数の差に相当する。
従って、仕事関数が既知の探針5と仕事関数が未知である測定試料1とを互いに対向させ、発振部においてカンチレバーを振動させると、交流電流が流れるためにその際の電圧を測定することで測定試料1の仕事関数が測定できる。
上記方法に基づいて2次元的に試料表面を走査することで、試料の所定範囲における電位分布が可視化されることになる。
このように電位分布が可視化されることで、表面には現れない神経細胞の形態が特定できる。
【0029】
本実施例においては、神経細胞の形状、形態の特定手法について2つを挙げたが、これらは独立したモードとして個々に実施例1の構成に組み込むことが可能であることは言うまでもない。
【0030】
実施例1、2において上述した測定試料である神経細胞は、動物より採取してきたものであっても良いし、在宅の被検査体から採取された粘膜を郵送などで培養工場へ送付され、送付されたサンプルを工場で細胞培養技術により培養したものであっても良いし、病院、研究室などで培養されたものであってもよい。また、iPS細胞、ES細胞、MUSE細胞の様な様々な細胞に変化する万能型細胞等から形成したものであっても良い。
この場合、採取可能な細胞は、成人に限らず、背景技術に記載した出生直後の被検査体であっても構わない。また、胎児についても取得が可能である。このため、これらの細胞を培養し、その神経活動を分析することで、精神疾患等神経活動に由来する疾病を早期に実現することが可能となる。
【符号の説明】
【0031】
1・・・測定試料、2・・・電荷注入電極、3・・・参照電極、4・・・カンチレバー、5・・・探針、6・・・試料台、7・・・XYZ走査機構、8・・・粗動機構、9・・・変位検出部、10・・・振幅・周波数検出部、11・・・フィードバック制御部、201・・・細胞体、202・・・軸索
【技術分野】
【0001】
本発明は、生体神経細胞の活動の計測法及び計測装置に関わるものである。
【背景技術】
【0002】
従来の研究では、例えば精神疾患を患う患者に対して、近赤外分光法により脳活動を計測し、得られた波形に応じて精神疾患を分別する方法が非特許文献1に開示されている。この方法では、被検査体へ光照射用プローブと光検出プローブを被検査体の頭部に代表する皮膚上へ装着させる。そして、被検査体へ問いかけのタスクを課し、そのタスクを課した期間に対応する時間帯での生体組織を通過した光の強度の変化を、そのタスクを課した期間の前後での生体組織を通過した光の強度を基準に算出し、血液量変化を算出する。この血液量変化は、大凡100msの時間分解能を有し、時刻に対する波形として、また、被検査体へ照射する光を複数波長とすることで、酸素化ヘモグロビンに関する血液量変化と脱酸素化ヘモグロビンに関する血液量変化を同時に計測することが出来る。
【0003】
これらの波形を疾病群毎に比較すると、健常者、統合失調症、双極性障がい、うつ病群へ弁別することが出来、その時点での被検査体の精神状態を推定することが出来る。
【0004】
この計測方法は、罹患中の被検査体に限らず、健常な状態の被検査体へも適用でき、また、投薬による疾病からの緩和状態を追跡することも出来る。このため、適用可能な応用範囲は幅広い。
一方で、より早期から、言い換えれば出生直後から、疾患へ罹患する可能性を検出することが出来れば、子供に対して適切なケアを早期に取り組むことが出来、その効果は高い。
【0005】
また、走査プローブ顕微鏡(以下SPMともいう)を用いて生物試料を観察する試みが近年活発となってきている。
【0006】
走査プローブ顕微鏡は、金属探針を用いて物性像と形状が同時に得られることが可能であり、形状と物性の相関を解析することが高い空間分解能で容易にできるという特徴がある。
SPMに係わる従来の技術においては、特許文献1により、外部刺激(物理的、化学的)に対する細胞内の電位変化の測定による細胞の機能解析、また、特許文献2では、がん細胞を含む細胞サンプル(培養細胞、神経細胞)に対して、生化学反応などの外部刺激を加えて、AFM(原子間力顕微鏡)でその応答としての細胞膜の変異などから細胞の特性を測定し、薬剤のスクリーニングを行い、もしくは診断を行うものなどが開示されている。
また、近年Rett症候群に罹患した生体より神経細胞を培養し、その機能等についての検討がなされている(非特許文献2)。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2008−079608号公報
【特許文献2】特表2008−539697号公報
【非特許文献】
【0008】
【非特許文献1】精神疾患とNIRS、福田正人編、中山書店(pp.79-102)
【非特許文献2】A Model for Neural Development and Treatment of Rett Syndrome Using Human Induced Pluripotent Stem Cells 、 Maria C.N.Marchetto他、Cell 143、527-539頁
【発明の概要】
【発明が解決しようとする課題】
【0009】
しかし、上記のように近赤外光を用いた脳機能計測においては、出生直後の被検査体の精神疾患の状態を早期に検出する手段についての報告はなされておらず、細胞レベルでの神経活動の評価を行うことはその特性上困難である。
【0010】
また、SPMを用いた計測においても、神経細胞そのものを計測対象とする技術についてはその計測手法を含め確立されていないのが現状である。
【0011】
そこで本発明では、一般的な細胞、細胞膜そのものの応答ではなく、神経細胞そのものの応答(電気的な応答)を計測する装置を提供し、神経活動そのものの電気的計測を実現することで、神経細胞の疾病の予測、診断の実現などを提供することを目的とする。
【課題を解決するための手段】
【0012】
本発明は、神経伝達時に電圧が発生することを鑑み、神経細胞へ電気的な刺激を与えることを特徴とする刺激装置と、該神経細胞を伝播した電気信号を検出することを特徴とするカンチレバーを具備することを特徴とするケルビンプローブを提供する。
【発明の効果】
【0013】
細胞レベルでの神経活動の計測を行うことにより、神経活動に由来する精神疾患の診断、並びに、将来の精神疾患の発症予測などの実現可能性がある。
また本計測手法によれば、被検者の状態に寄らず簡便に神経活動計測が可能となる。
【図面の簡単な説明】
【0014】
【図1】装置全体構成を示す図である。
【図2】計測の一例を示す図である。
【発明を実施するための形態】
【実施例1】
【0015】
図1は、本発明にて使用する神経活動計測装置の実施形態を示す構成図であり、図2は神経細胞の測定例である。これらを用いて以下説明する。
【0016】
測定試料1は神経細胞を想定しており、測定試料1の表面に対向する様にカンチレバー4が配置され、その先端には探針5が設けられている。
カンチレバー4および探針5は発振部に接続されており、固有振動数かその近傍の周波数で、測定試料1の表面に対して垂直方向に振動させられる。当該発振部は制御部21においてその動作が制御されている。
【0017】
測定試料1は試料台6を介してXYZ走査機構7および粗動機構8上に固定されており、XYZ走査機構7により探針5に対して3次元方位方向に移動させることができ、また、粗動機構8により測定試料1と探針8の間の距離を大きく変化させることができる。
【0018】
測定時に際して、まず、制御部21が粗動部13を用いて粗動機構8を駆動し、測定試料1の表面を探針8に接近させる。測定試料1と探針8が十分に接近すると、測定試料1の表面との相互作用によりカンチレバー4の振動状態が変化する。カンチレバー4の変位を変位検出部9を用いて検出し、さらに、振幅・周波数検出部10によりカンチレバー4の振動振幅あるいは周波数が検出される。
フィードバック制御部11は、カンチレバー4の振動振幅あるいは周波数が制御部21により設定された一定値となるように、Z駆動部12によりXYZ走査機構7をZ方向に駆動し、探針5と測定試料1表面との間の距離を一定に保つ。
【0019】
この状態において、制御部21が走査部19を用いてXYZ走査機構7をXY面内で走査すると、測定試料1の表面形状に合わせてXYZ走査機構7がZ方向位置を調整し、測定試料1の表面と探針5の先端の距離は常に一定に保たれる。
【0020】
測定においては、測定試料1の表面と探針8の先端の距離を常に一定に保ちながら行う。まず電荷注入部14を通じて電荷注入電極2より測定試料1に対して所定の電荷を注入することにより神経細胞である測定試料1に電圧を印加する。
電荷注入電極2により測定試料1に電圧(数mV〜数百mV程度)が印加されると、測定試料1上に配置されている参照電極3を通じて参照電位測定部15においてレファレンスデータとなる参照電位を測定する。当該参照電位は図示しない記憶部に格納される。
【0021】
電荷注入部14を通じて神経細胞である測定試料1に電圧を印加すると、パルス状の電流が生じ、測定試料の所望位置に金属探針5を接触、もしくは近接させることで、パルス的に流れる電流の影響により変化するカンチレバー4の変位量を変位検出部9において時系列的に検出する。
検出した変位量から、当該探針が接触もしくは近接する位置までに流れる電流を時系列的に計測することができる。
当該検出を測定試料1上の多点において行い、導通不良個所を特定することが可能となる。
不良個所の特定は、制御部21内に格納されるか、独立に存在する図示しない演算装置によって、予め記憶部において記憶されている上述の参照電位との比較を行い、参照電位とのかい離具合が所定値を超えた場合に不良と判定するものとする。また、参照電位との比較を例に示したが、順に計測する計測点における計測結果を順次比較することも可能である。
またここで、所定値の基準については、制御部に接続された図示しない入力部において任意に設定可能であることは言うまでもない。
【0022】
比較の具体的方法については、測定された結果について、振幅検出部17及び位相比較部18において夫々位相、振幅を算出し、それらと参照電位測定部の結果とを比較するものとする。
当該比較結果、もしくは、所定値を超える導通不良が見つかった箇所については、表示部20においてその結果を表示する様に構成しても良い。
【0023】
本実施例に記載の計測装置及び方法によれば、神経活動を簡便に測定することが可能となるだけでなく、細胞レベルでの導通不良を特定出来ることから、神経活動に由来する精神疾患の診断、並びに、将来の精神疾患の発症予測などの実現可能性がある。
【実施例2】
【0024】
上述の実施例1においては、事前の観察手段を設けていないが、事前に観察・測定する対象を目視できることは、計測をする際に有効であり、また、測定を自動化する際には形状測定は必要となる。
そこで、図1に示した構成において、形状観察モードを搭載する場合について、以下説明する。ここでは、実施例1と重複する内容については省略ものとする。
【0025】
まず、試料台6に測定試料1を載置した後に、カンチレバー4及び探針5に測定試料1を極近傍に接近させる。このとき、カンチレバー4は固有振動数かその近傍の周波数で、測定試料1の表面に対して垂直方向に振動させられる。カンチレバー4に接続された発振部は制御部21においてその動作が制御されている。
この状態で測定試料1上を探針5が走査し、探針5と測定試料1に作用する原子間力を検出する。この探針5と測定試料1表面を微小な力で接触させるか、近接させ、カンチレバーのたわみ量が一定になるように探針・試料間距離をフィードバック制御しながら走査することで、当該走査範囲における検出情報をもとに、演算装置において表面形状を取得する。
【0026】
取得した表面形状については、図示しない記憶部においてその形状を記憶し、制御部21において、表示部20にその形状を表示させる。
当該表示内容に基づき、ユーザが電荷注入電極2を与える場所を設定し、探針5の走査範囲、計測位置等を入力部を介して指定することが可能となる。
【0027】
また、神経細胞は表面形状に表れない場合もある。このため、以下の方法において形状を求めることもできる。
実施例1の内容と同様に、電荷注入電極2を介して電荷を注入し、測定試料1に対して所定の電圧を印加する。このとき、実施例1においては、所定の計測点に対する導通を計測したが、本例においては、所定範囲についてカンチレバー4を、探針5−測定試料1間の高さを保ちつつ、X-Y方向に2次元走査を行い界面電位分布を計測する。
【0028】
界面電位(接触電位差)は仕事関数の差を表すことが知られており、探針5−測定試料1の様に2つの仕事関数の異なる物質を接触もしくは近接させる際に、フェルミ準位が同じになるように電流が流れ、平衡状態では電位差が生じる。この差が探針5−測定試料1の仕事関数の差に相当する。
従って、仕事関数が既知の探針5と仕事関数が未知である測定試料1とを互いに対向させ、発振部においてカンチレバーを振動させると、交流電流が流れるためにその際の電圧を測定することで測定試料1の仕事関数が測定できる。
上記方法に基づいて2次元的に試料表面を走査することで、試料の所定範囲における電位分布が可視化されることになる。
このように電位分布が可視化されることで、表面には現れない神経細胞の形態が特定できる。
【0029】
本実施例においては、神経細胞の形状、形態の特定手法について2つを挙げたが、これらは独立したモードとして個々に実施例1の構成に組み込むことが可能であることは言うまでもない。
【0030】
実施例1、2において上述した測定試料である神経細胞は、動物より採取してきたものであっても良いし、在宅の被検査体から採取された粘膜を郵送などで培養工場へ送付され、送付されたサンプルを工場で細胞培養技術により培養したものであっても良いし、病院、研究室などで培養されたものであってもよい。また、iPS細胞、ES細胞、MUSE細胞の様な様々な細胞に変化する万能型細胞等から形成したものであっても良い。
この場合、採取可能な細胞は、成人に限らず、背景技術に記載した出生直後の被検査体であっても構わない。また、胎児についても取得が可能である。このため、これらの細胞を培養し、その神経活動を分析することで、精神疾患等神経活動に由来する疾病を早期に実現することが可能となる。
【符号の説明】
【0031】
1・・・測定試料、2・・・電荷注入電極、3・・・参照電極、4・・・カンチレバー、5・・・探針、6・・・試料台、7・・・XYZ走査機構、8・・・粗動機構、9・・・変位検出部、10・・・振幅・周波数検出部、11・・・フィードバック制御部、201・・・細胞体、202・・・軸索
【特許請求の範囲】
【請求項1】
神経細胞を載置する試料台と、
当該神経細胞の所定箇所に電圧を印加する電極と、
前記試料台と対向する位置に配置され、前記神経細胞に接触もしくは近接させるカンチレバーと、
前記神経細胞に所定の時間間隔で電圧を印加する様に制御する制御部と、
当該電圧の印加により前記神経細胞に流れる電流を前記カンチレバーの変位量により検出する変位検出部と、
前記神経細胞に流れる前記電流の時系列データを参照情報として記憶する記憶手段とを備え、
前記検出した結果と、予め記憶された参照情報とを比較し、不良判定する演算装置を備えることを特徴とする神経活動計測装置。
【請求項2】
請求項1に記載の神経活動計測装置において、
前記演算装置は、前記カンチレバーの走査により得られる前記神経細胞の表面形状を算出することを特徴とする神経活動計測装置。
【請求項3】
請求項2に記載の神経活動計測装置において、
前記カンチレバーの走査は前記制御部により制御されることを特徴とする神経活動計測装置。
【請求項4】
請求項2に記載の神経活動計測装置において、
前記表面形状を表示する表示部を備えることを特徴とする神経活動計測装置。
【請求項5】
請求項1に記載の神経活動計測装置において、
前記電極と、前記カンチレバーとの間に参照電極を備え、
当該参照電極において取得される、前記神経細胞を流れる電流を前記参照情報として前記記憶手段に記憶することを特徴とする神経活動計測装置。
【請求項6】
請求項1に記載の神経活動計測装置において、
前記カンチレバーを前記神経細胞に順次接触もしくは近接させることにより、前記神経細胞の前記電極からカンチレバーが接触もしくは近接する範囲までに流れる電流を順次取得することを特徴とする神経活動計測装置。
【請求項7】
請求項6に記載の神経活動計測装置において、
前記演算部は、取得した結果を順次、前記参照情報として、後に取得された結果と夫々比較し、不良個所を特定することを特徴とする神経活動計測装置。
【請求項8】
請求項1に記載の神経活動計測装置において、
前記参照情報は、予め前記記憶部に記憶された情報であることを特徴とする神経活動計測装置。
【請求項9】
請求項1に記載の神経活動計測装置において、
前記神経細胞は、培養された細胞であることを特徴とする神経活動計測装置。
【請求項10】
電極を介して神経細胞に電圧を印加し、カンチレバーを神経細胞に順次接触もしくは近接させ、前記神経細胞の前記電極からカンチレバーが接触もしくは近接する範囲までに流れる電流を順次取得し、当該取得した結果を後に取得された結果と夫々比較し、不良個所を特定することを特徴とする神経活動計測方法。
【請求項11】
被検査体からサンプルを採取し、
当該採取したサンプルを培養して細胞を形成し、
当該培養した細胞を試料台に載置し、
当該細胞の所定箇所に電極を用いて所定の時間間隔で電圧を印加し、
前記試料台と対向する位置に配置されたカンチレバーにより、前記細胞に接触もしくは近接させ、
当該電圧の印加により前記細胞に流れる電流を前記カンチレバーの変位量により検出し、
前記細胞に流れる前記電流の時系列データを参照情報として記憶手段に記憶させ、
前記検出した結果と、予め記憶された参照情報とを比較し、不良判定することを特徴とする生体活動計測方法。
【請求項1】
神経細胞を載置する試料台と、
当該神経細胞の所定箇所に電圧を印加する電極と、
前記試料台と対向する位置に配置され、前記神経細胞に接触もしくは近接させるカンチレバーと、
前記神経細胞に所定の時間間隔で電圧を印加する様に制御する制御部と、
当該電圧の印加により前記神経細胞に流れる電流を前記カンチレバーの変位量により検出する変位検出部と、
前記神経細胞に流れる前記電流の時系列データを参照情報として記憶する記憶手段とを備え、
前記検出した結果と、予め記憶された参照情報とを比較し、不良判定する演算装置を備えることを特徴とする神経活動計測装置。
【請求項2】
請求項1に記載の神経活動計測装置において、
前記演算装置は、前記カンチレバーの走査により得られる前記神経細胞の表面形状を算出することを特徴とする神経活動計測装置。
【請求項3】
請求項2に記載の神経活動計測装置において、
前記カンチレバーの走査は前記制御部により制御されることを特徴とする神経活動計測装置。
【請求項4】
請求項2に記載の神経活動計測装置において、
前記表面形状を表示する表示部を備えることを特徴とする神経活動計測装置。
【請求項5】
請求項1に記載の神経活動計測装置において、
前記電極と、前記カンチレバーとの間に参照電極を備え、
当該参照電極において取得される、前記神経細胞を流れる電流を前記参照情報として前記記憶手段に記憶することを特徴とする神経活動計測装置。
【請求項6】
請求項1に記載の神経活動計測装置において、
前記カンチレバーを前記神経細胞に順次接触もしくは近接させることにより、前記神経細胞の前記電極からカンチレバーが接触もしくは近接する範囲までに流れる電流を順次取得することを特徴とする神経活動計測装置。
【請求項7】
請求項6に記載の神経活動計測装置において、
前記演算部は、取得した結果を順次、前記参照情報として、後に取得された結果と夫々比較し、不良個所を特定することを特徴とする神経活動計測装置。
【請求項8】
請求項1に記載の神経活動計測装置において、
前記参照情報は、予め前記記憶部に記憶された情報であることを特徴とする神経活動計測装置。
【請求項9】
請求項1に記載の神経活動計測装置において、
前記神経細胞は、培養された細胞であることを特徴とする神経活動計測装置。
【請求項10】
電極を介して神経細胞に電圧を印加し、カンチレバーを神経細胞に順次接触もしくは近接させ、前記神経細胞の前記電極からカンチレバーが接触もしくは近接する範囲までに流れる電流を順次取得し、当該取得した結果を後に取得された結果と夫々比較し、不良個所を特定することを特徴とする神経活動計測方法。
【請求項11】
被検査体からサンプルを採取し、
当該採取したサンプルを培養して細胞を形成し、
当該培養した細胞を試料台に載置し、
当該細胞の所定箇所に電極を用いて所定の時間間隔で電圧を印加し、
前記試料台と対向する位置に配置されたカンチレバーにより、前記細胞に接触もしくは近接させ、
当該電圧の印加により前記細胞に流れる電流を前記カンチレバーの変位量により検出し、
前記細胞に流れる前記電流の時系列データを参照情報として記憶手段に記憶させ、
前記検出した結果と、予め記憶された参照情報とを比較し、不良判定することを特徴とする生体活動計測方法。
【図1】


【図2】




【図2】


【公開番号】特開2012−143196(P2012−143196A)
【公開日】平成24年8月2日(2012.8.2)
【国際特許分類】
【出願番号】特願2011−4460(P2011−4460)
【出願日】平成23年1月13日(2011.1.13)
【出願人】(000005108)株式会社日立製作所 (27,607)
【Fターム(参考)】
【公開日】平成24年8月2日(2012.8.2)
【国際特許分類】
【出願日】平成23年1月13日(2011.1.13)
【出願人】(000005108)株式会社日立製作所 (27,607)
【Fターム(参考)】
[ Back to top ]

