窒素代謝微生物の活性化方法及びバイオリアクタ
【課題】亜硝酸イオンを窒素ガスに還元する亜硝酸還元微生物または亜硝酸イオンを硝酸イオンに酸化する亜硝酸酸化微生物について、選択的に且つ高濃度に処理槽等に存在させて機能させる。
【解決手段】亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と有機物と酸化還元物質とを含む培養液に電極を浸し、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が電極へ電位を印加していない場合よりも向上する電位を電極に印加しながら窒素代謝微生物を培養するようにした。
【解決手段】亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と有機物と酸化還元物質とを含む培養液に電極を浸し、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が電極へ電位を印加していない場合よりも向上する電位を電極に印加しながら窒素代謝微生物を培養するようにした。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、窒素代謝微生物の活性化方法及びバイオリアクタに関する。さらに詳述すると、本発明は、窒素代謝微生物である亜硝酸還元能を有する亜硝酸還元微生物または亜硝酸酸化能を有する亜硝酸酸化微生物を活性化するのに好適な方法、さらには、亜硝酸還元微生物または亜硝酸酸化微生物を活性化しながら亜硝酸イオン含有廃水等の亜硝酸イオン含有液を処理するのに好適なバイオリアクタに関する。
【背景技術】
【0002】
自然環境中の微生物による窒素サイクルを図20に示す。図20に示されるように、窒素は自然環境中において多様な酸化還元反応を得て、様々な形態で存在している。
【0003】
現在では、このような微生物による窒素サイクルを利用して、廃水(排水)に含まれるアンモニウムイオンや硝酸イオン、亜硝酸イオンを処理する方法が各種提案されている(例えば、特許文献1を参照)。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2000−237791号
【発明の概要】
【発明が解決しようとする課題】
【0005】
微生物による窒素サイクルを利用して廃水処理を行う場合、処理効率を高める上では、
処理に必要な機能を有する微生物を選択的に且つ高濃度に処理槽に存在させて機能させることが重要となる。しかしながら、微生物による窒素サイクルを利用した従来の廃水処理方法では、処理に必要な機能を有する微生物を選択的に且つ高濃度に処理槽に存在させて機能させることには限界があり、その改善が望まれていた。
【0006】
そこで、本発明は、微生物による窒素サイクルの中でも特に重要な窒素代謝微生物である、亜硝酸イオンを窒素ガスに還元する亜硝酸還元微生物または亜硝酸イオンを硝酸イオンに酸化する亜硝酸酸化微生物について、選択的に且つ高濃度に処理槽等に存在させて機能させることができる窒素代謝微生物の活性化方法を提供することを目的とする。
【0007】
また、本発明は、亜硝酸イオンを窒素ガスに還元する亜硝酸還元微生物または亜硝酸イオンを硝酸イオンに酸化する亜硝酸酸化微生物について、選択的に且つ高濃度に処理槽等に存在させて機能させ、亜硝酸イオン含有廃水等の亜硝酸イオン含有液を効率よく処理することのできる方法及びバイオリアクタを提供することを目的とする。
【課題を解決するための手段】
【0008】
かかる課題を解決するため、本願発明者等が鋭意検討を行った結果、培養液に水田土壌を添加し、酸化還元物質を添加した培養液に電極を浸して電極の電位をある値に制御することで、電極に電位を印加しない場合と比較して亜硝酸イオンが窒素ガスに還元される速度が顕著に促進されることが明らかとなった。また、電極の電位を上記とは別の値に制御することで、電極に電位を印加しない場合と比較して亜硝酸イオンが硝酸イオンに酸化される速度が顕著に促進されることも明らかとなった。
【0009】
そして、亜硝酸イオンが窒素ガスに還元される速度が顕著に促進された電位に制御して培養を行った場合の培養液の微生物叢と亜硝酸イオンが硝酸イオンに酸化される速度が顕著に促進された電位に制御して培養を行った場合の培養液の微生物叢について解析を遺伝子学的な解析を行った。その結果、亜硝酸イオンが窒素ガスに還元される速度が顕著に促進された電位に制御して培養を行った場合の培養液の微生物叢においては、亜硝酸還元能(脱窒能)を有する微生物群が優占化していると共に微生物の数自体も電位を印加しない場合と比較して増加することが明らかとなった。また、亜硝酸イオンが硝酸イオンに酸化される速度が顕著に促進された電位に制御して培養を行った場合の培養液の微生物叢においては、亜硝酸酸化能を有する微生物群が優占化していると共に微生物の数自体も電位を印加しない場合と比較して増加することが明らかとなった。
【0010】
これらの結果から、培養液に亜硝酸イオンが溶解しているときの亜硝酸イオンの窒素ガスへの還元速度または亜硝酸イオンの硝酸イオンの酸化速度を指標として、培養液に浸した電極の電位を制御することで、窒素代謝微生物である亜硝酸還元能を有する微生物と亜硝酸酸化能を有する微生物を選択的に活性化(生育促進、さらには機能向上)できることを知見するに至り、さらに種々検討を重ねて本発明を完成するに至った。
【0011】
かかる知見に基づく、本発明の窒素代謝微生物の活性化方法は、亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と有機物と酸化還元物質とを含む培養液に電極を浸し、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が電極へ電位を印加していない場合よりも向上する電位を電極に印加しながら窒素代謝微生物を培養するようにしている。
【0012】
ここで、本発明の窒素代謝微生物の活性化方法において、培養液にイオン交換膜を介して電解液を接触させ、培養液に浸漬した電極と対をなす電極を電解液に浸漬することが好ましい。また、培養液にイオン交換膜を介して培養液に浸漬した電極と対をなす電極を接触させることが好ましい。この場合、培養液中の酸化還元物質が培養液に浸漬した電極と対をなす電極に接触するのを抑制して、培養液の電位(酸化還元電位)を制御させ易いものとできる。
【0013】
また、本発明の窒素代謝微生物の活性化方法においては、電極に印加する電位を、亜硝酸イオンの低減速度が向上する結果として窒素ガスの生成速度が向上する電位とすることにより、亜硝酸還元微生物を活性化することができる。電極に印加する電位は、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位とすることが好ましい。
【0014】
また、本発明の窒素代謝微生物の活性化方法においては、電極に印加する電位を、亜硝酸イオンの低減速度が向上する結果として硝酸イオン生成速度が向上する電位とすることにより、亜硝酸酸化微生物を活性化することができる。電極に印加する電位は、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とすることが好ましい。
【0015】
次に、本発明の亜硝酸イオン含有液の処理方法は、本発明の窒素代謝微生物の活性化方法により活性化された窒素代謝微生物を含む培養液中で亜硝酸イオン含有廃水等の亜硝酸イオン含有液を処理するようにしている。したがって、亜硝酸イオンが効率よく窒素ガスあるいは硝酸イオンに変換(還元または酸化)される。
【0016】
また、本発明の亜硝酸生成微生物の培養方法は、本発明の窒素代謝微生物の活性化方法により活性化された窒素代謝微生物を含む培養液中に亜硝酸イオンを生成する亜硝酸生成微生物を添加し、亜硝酸生成微生物により生成された亜硝酸イオンを活性化された窒素代謝微生物に還元または酸化させて低減し、亜硝酸イオンの毒性による生育阻害を回避しながら亜硝酸生成微生物を培養するようにしている。したがって、亜硝酸生成微生物が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、亜硝酸生成微生物を良好に培養することができる。
【0017】
次に、本発明のバイオリアクタは、イオン交換膜によって仕切られた対電極槽及び密閉構造の培養槽と、培養槽に収容された培養液と、対電極槽に収容された電解液と、培養液に浸された作用電極と、電解液に浸された対電極と、作用電極と対電極とが結線されて作用電極と対電極との間に電位差を与えて作用電極の電位を設定する定電位設定装置と、培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、培養槽から処理液を排出する処理液排出手段とを有し、培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極に電位を印加しない場合よりも向上する電位が作用電極に印加されながら窒素代謝微生物が培養されるものとしている。
【0018】
また、本発明のバイオリアクタは、培養槽としての密閉構造の容器と、容器に収容可能な対電極槽としての密閉構造の小容器と、培養槽に収容された培養液と、対電極槽に収容された電解液と、培養液に浸された作用電極と、電解液に浸された対電極と、作用電極と対電極とが結線されて作用電極と対電極との間に電位差を与えて作用電極の電位を設定する定電位設定装置と、培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、培養槽から処理液を排出する処理液排出手段とを有し、小容器は培養液と接触する位置の少なくとも一部にイオン交換膜を備えるものとし、培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極に電位を印加しない場合よりも向上する電位が作用電極に印加されながら窒素代謝微生物が培養されるものとしている。
【0019】
さらに、本発明のバイオリアクタは、イオン交換膜を少なくとも一部に備える容器と、容器に収容された培養液と、培養液に浸された作用電極と、イオン交換膜の容器の外側の面の少なくとも一部に接触している対電極と、作用電極と対電極とが結線されて作用電極と対電極との間に電位差を与えて作用電極の電位を設定する定電位設定装置と、培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、培養槽から処理液を排出する処理液排出手段とを有し、イオン交換膜は容器の培養液と接触する位置に備えるものとし、培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極に電位を印加しない場合よりも向上する電位が作用電極に印加されながら窒素代謝微生物が培養されるものとしている。
【0020】
本発明のバイオリアクタにおいては、作用電極に印加される電位が、亜硝酸イオンの低減速度が向上する結果として窒素ガスの生成速度が向上する電位とされて亜硝酸還元微生物が活性化され、亜硝酸イオンが還元されて生じた窒素ガスを培養槽から排出する窒素ガス排出手段が備えられているものとすることが好ましい。作用電極に印加される電位は、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位であることが好ましい。
【0021】
また、本発明のバイオリアクタにおいては、作用電極に印加される電位が、亜硝酸イオンの低減速度が向上する結果として硝酸イオン生成速度が向上する電位とされて亜硝酸酸化微生物が活性化されているものとすることが好ましい。作用電極に印加される電位は、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とすることが好ましい。
【発明の効果】
【0022】
本発明の窒素代謝微生物の活性化方法によれば、亜硝酸還元微生物または亜硝酸酸化微生物の生育を選択的に促進させ、さらには亜硝酸還元微生物の亜硝酸還元能または亜硝酸酸化微生物の亜硝酸酸化能を選択的に向上させることが可能となる。したがって、例えば土壌サンプル等のように雑多な微生物を含む試料を用いて、亜硝酸還元微生物または亜硝酸酸化微生物を選択的に増殖させて培養液中に高濃度に存在させ、さらには亜硝酸還元微生物の亜硝酸還元能または亜硝酸酸化微生物の亜硝酸酸化能を選択的に向上させることによって、培養液自体の微生物処理槽としての機能を極めて高いものとすることが可能となる。
【0023】
本発明の亜硝酸イオン含有液の処理方法によれば、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物または亜硝酸酸化微生物を利用して亜硝酸イオン含有液に含まれる亜硝酸イオンを効率よく還元または酸化してその濃度を低減することができる。したがって、亜硝酸イオン含有廃水(排水)を効率よく処理することが可能となる。
【0024】
本発明の亜硝酸生成微生物の培養方法によれば、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物または亜硝酸酸化微生物を利用して亜硝酸生成微生物により生成される亜硝酸イオンを酸化または還元してその濃度を低減するようにしているので、亜硝酸生成微生物が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、亜硝酸生成微生物を良好に培養することが可能となる。例えば、呼吸により硝酸イオンを亜硝酸イオンに還元する硝酸呼吸能を有する微生物(例えば、大腸菌等)は、硝酸呼吸により自らが生成した亜硝酸イオンによってその生育が阻害されるが、本発明の培養方法を利用することによって、亜硝酸イオンによる生育阻害を抑えて、良好に培養することが可能となる。
【0025】
本発明のバイオリアクタによれば、亜硝酸還元微生物または亜硝酸酸化微生物の生育を選択的に促進させ、さらには亜硝酸還元微生物の亜硝酸還元能または亜硝酸酸化微生物の亜硝酸酸化能を選択的に向上させて、培養槽の亜硝酸イオン処理能力を極めて高いものとすることが可能となる。したがって、亜硝酸イオン含有廃水等の亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することが可能となる。
【図面の簡単な説明】
【0026】
【図1】本発明の窒素代謝微生物の活性化方法の概念を示す図である。
【図2】第一の実施形態Aにかかるバイオリアクタの一例を示す断面図である。
【図3】第一の実施形態Bにかかるバイオリアクタの一例を示す断面図である。
【図4】第一の実施形態Cにかかるバイオリアクタの一例を示す断面図である。
【図5】第一の実施形態Dにかかるバイオリアクタの一例を示す断面図である。
【図6】第二の実施形態にかかるバイオリアクタの一例を示す断面図である。
【図7】バイオリアクタの他の構成の一例を示す断面図である。
【図8】実験に使用した装置の概念図である。
【図9】実験に使用した装置の小容器の構成を示す図である。
【図10】アンモニウムイオンの酸化還元特性を示す図である。
【図11】亜硝酸イオンの酸化還元特性を示す図である。
【図12】実施例3における、通電無しの場合の各種物質の経時変化を示す図である。
【図13】実施例3における、+0.2Vの場合の各種物質の経時変化を示す図である。
【図14】実施例3における、+0.6Vの場合の各種物質の経時変化を示す図である。
【図15】実施例3における、−0.6Vの場合の各種物質の経時変化を示す図である。
【図16】実施例4における、全菌数の定量結果を示す図である。
【図17】実施例4における、nirK遺伝子の定量結果を示す図である。
【図18】実施例4における、nirS遺伝子の定量結果を示す図である。
【図19】実施例5における、培養液中の微生物叢解析の結果を示す図である。
【図20】自然環境中の微生物による窒素サイクルに関わる酸化還元反応を示す図である。
【発明を実施するための形態】
【0027】
以下、本発明を実施するための形態について、図面に基づいて詳細に説明する。
【0028】
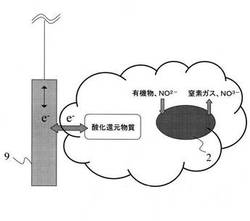
図1に、本発明の窒素代謝微生物の活性化方法の実施形態の一例を概念的に示す。本発明の窒素代謝微生物の活性化方法は、亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方の窒素代謝微生物2と有機物5と酸化還元物質3とを含む培養液4に電極9(作用電極9)を浸し、培養液4に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が電極9へ電位を印加していない場合よりも向上する電位を電極9に印加しながら窒素代謝微生物2を培養するようにしている。
【0029】
本発明では、窒素代謝微生物2として、亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方を培養液4に含ませる。
【0030】
亜硝酸還元能を有する微生物2aは、亜硝酸イオンを還元する能力を有する微生物であれば特に限定されるものではないが、亜硝酸イオンを窒素ガスに還元(脱窒)する能力を有する微生物が特に好適であり、例えば、シュードモナス(Pseudomonas)属、アリシクリフィルス(Alicycliphilus)属及びティシエレラ(Tissierella)属の微生物を用いることが好適である。
【0031】
亜硝酸酸化能を有する微生物2bは、亜硝酸イオンを硝酸イオンに酸化する能力を有する微生物であれば特に限定されるものではないが、ブルクホルデリア(Burkholderia)属の微生物を用いることが好適である。
【0032】
尚、本発明においては、窒素代謝微生物2として、単離された微生物の市販品や培養品を用いてもよいが、水田土壌のような微生物含有土壌試料や汚泥試料等を用いることができる。即ち、亜硝酸還元能を有する微生物2aや亜硝酸酸化能を有する微生物2bは、通常、土壌や汚泥等に一般的に存在するものであることから、土壌試料や汚泥試料を培養液4に添加することで、窒素代謝微生物2を選択的に増殖させて培養液4に高濃度に存在させることができる。換言すれば、土壌試料や汚泥試料から、窒素代謝微生物を集積培養することができる。
【0033】
培養液4の組成は、窒素代謝微生物2の培養に一般的に用いられている培地の組成とすればよく、特に限定されるものではないが、一例を挙げると、KH2PO4、MgSO4・7H2O、CaCl2・2H2O、微量元素(Zn、Co、Mn、Cu、Mo、Ni、Se、B、Fe)を含む培地を用いることができる。
【0034】
有機物5は、窒素代謝微生物2の炭素源となり得る物質であれば特に限定されるものではないが、例えば炭酸塩やプロピオン酸等を好適に使用することができる。
【0035】
酸化還元物質3は、培養液4に浸されている電極9と可逆的に酸化還元反応を生じる物質であり、且つ窒素代謝微生物2に対して毒性を呈さない物質であればよい。また、窒素代謝微生物の代謝等に直接関与しない物質とすることが好ましい。例えば、キレート剤であるジエチレントリアミンペンタ酢酸(DTPA)、エチレンジアミンテトラ酢酸(EDTA)、テトラエチレントリアミン(TET)、エチレンジアミン(EDA)、ジエチレントリアミン(DETA)、クエン酸、シュウ酸、クラウンエーテル、ニトリロテトラ酢酸、エデト酸二ナトリウム、エデト酸ナトリウム、エデト酸三ナトリウム、ペニシラミン、ペンテテートカルシウム三ナトリウム、ペンテト酸、スクシメルおよびエデト酸トリエンチン、好ましくはEDTAに配位させた鉄イオン、フェロシアン化カリウム、アントラキノンジスルホン酸ナトリウムなどのキノン化合物、メチルビオロゲン等のビオロゲン誘導体等を用いることができるが、これらに限定されるものではない。
【0036】
尚、キノン化合物は土壌成分の一つとして知られている物質であることから、土壌試料や汚泥試料を添加することで、酸化還元物質3を培養液4に存在させることができる場合がある。つまり、土壌試料や汚泥試料に酸化還元物質3が十分に含まれている場合があり、このような場合には、別途酸化還元物質3を培養液4に添加する必要は無くなる。
【0037】
尚、酸化還元物質3の培養液4への添加量は、好適には0.1〜100mM、より好適には1〜10mM、さらに好適には数mMである。酸化還元物質3の添加量が少なすぎると培養液4の酸化還元電位を制御し難くなる場合がある。また、多すぎると培養液4に溶解しなかったり、微生物の生育に悪影響を及ぼす場合もある。
【0038】
本発明においては、電極9の電位を制御することにより酸化還元物質3の酸化体と還元体の比を制御し、培養液4の電位(酸化還元電位)を制御するようにしている。培養液4の酸化還元電位は、数式1のネルンストの式により表される。
[数式1] E=E0+RT/nF×ln(Cox/Cred)
【0039】
数式1において、Eは培養液4の酸化還元電位、E0は酸化還元物質3の標準酸化還元電位、Rは気体定数、Tは絶対温度、nは反応電子数、Fはファラデー定数、Coxは酸化還元物質3の酸化体の濃度、Credは酸化還元物質3の還元体の濃度である。つまり、培養液4に含まれる酸化還元物質3の酸化体の濃度と還元体の濃度の比を電極9の電位を制御して一定に制御することにより、培養液4自体の酸化還元電位を制御することができる。
【0040】
電極9には、酸化還元物質3を可逆的に酸化還元させることが可能な材質のものが適宜用いられる。具体的には、炭素板やグラッシーカーボン等の炭素電極、白金電極等を用いることができるが、これらに限定されるものではない。
【0041】
電極9に与える電位(培養液4の酸化還元電位)は、以下の手順により決定される。即ち、培養液4に亜硝酸イオンを溶解させ、電極9に電位を与えることなく培養試験を行い、亜硝酸イオンの低減速度を決定する。亜硝酸イオンの低減速度は培養過程にて亜硝酸イオンの経時変化を測定することで決定することができる。そして、電極9に各種電位を印加して同様の培養試験を行い、亜硝酸イオンの低減速度を決定する。亜硝酸イオンの低減速度が電極9に電位を与えずに培養試験を行った場合よりも向上していれば、その電位が窒素代謝微生物2を活性化させることのできる電位に該当する。そして、亜硝酸イオンの低減速度が向上した結果として窒素ガスの生成速度が向上している場合には、その電位は、窒素代謝微生物2のうち亜硝酸還元微生物2aを活性化させることのできる電位に該当する。また、亜硝酸イオンの低減速度が向上した結果として硝酸イオンの生成速度が向上している場合には、その電位は、窒素代謝微生物2のうち亜硝酸酸化微生物2bを活性化させることのできる電位に該当する。
【0042】
本願発明者等の実験によると、窒素代謝微生物2のうち亜硝酸還元微生物2aを活性化させ始めることのできる電位は、銀・塩化銀電極電位基準で−0.6V〜+0.2V未満に存在し、−0.6Vとすれば、窒素代謝微生物2のうち亜硝酸還元微生物2aを確実に活性化できることが確認されている。また、−0.6Vで亜硝酸還元微生物2aを活性化できることが確認されたことから、電極9から培養液4に電子を与えやすい電位とすることで、亜硝酸還元微生物2aを活性化できるものと考えられる。したがって、電極9の電位を、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位とすることが好適であるが、電位をマイナス側に大きくし過ぎると水の電気分解が生じて培養液4のpHに変動が生じ、亜硝酸還元微生物2の生育を阻害する虞があるので、−0.6V〜−1.0Vとすることがより好適である。
【0043】
また、本願発明者等の実験によると、窒素代謝微生物2のうち亜硝酸酸化微生物2bを活性化させ始めることのできる電位は、銀・塩化銀電極電位基準で+0.2V超〜+0.6Vに存在し、+0.6Vとすれば、窒素代謝微生物2のうち亜硝酸酸化微生物2bを確実に活性化できることが確認されている。また、+0.6Vで亜硝酸酸化微生物2bを活性化できることが確認されたことから、電極9により培養液4から電子を引き抜きやすい電位とすることで、酸化還元微生物2aを活性化できるものと考えられる。したがって、電極9の電位を、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とすることが好適であるが、電位をプラス側に大きくし過ぎると水の電気分解が生じて培養液4のpHに変動が生じ、亜硝酸酸化微生物2の生育を阻害する虞があるので、+0.6V〜+1.0Vとすることがより好適である。ここで、+0.7Vよりもプラス側に大きな電位とすると、亜硝酸イオンが電気的に酸化されて減少するので、亜硝酸イオンが不足し易くなる。したがって、亜硝酸酸化微生物2bを増殖させる際には、+0.6V〜+0.7Vとすることが好適である。但し、亜硝酸酸化微生物2bが培養液4中に十分に高濃度に存在している場合には、+0.7Vよりもプラス側に大きな電位ととして、亜硝酸酸化微生物2bによる酸化と電気的な酸化とを併用し、亜硝酸イオンを低減してもよい。
【0044】
したがって、本発明の窒素代謝微生物の活性化方法によると、例えば土壌試料や汚泥試料のように、窒素代謝微生物2として亜硝酸還元微生物2aと亜硝酸酸化微生物2bが混在し得る微生物試料を用いた場合においても、亜硝酸還元微生物2aと亜硝酸酸化微生物2bのいずれか一方を選択的に活性化させることができる。
【0045】
尚、本発明の窒素代謝微生物の活性化方法においては、培養液4に亜硝酸イオンを添加しながら窒素代謝微生物2の活性化を図るようにしてもよいが、培養液4中の窒素代謝微生物2の菌体密度が十分に高く、増殖させる必要が無い場合には、亜硝酸イオンを添加せずに電位だけを印加して窒素代謝微生物2を活性化するようにしてもよい。例えば、窒素代謝微生物2の菌体密度が高濃度に維持された培養液4に電位を印加して窒素代謝微生物2を活性化させておき、亜硝酸イオン含有廃液などの亜硝酸イオン含有液を培養液4に投入して亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減するようにしてもよい。
【0046】
尚、本発明の窒素代謝微生物の活性化方法においては、電極9(作用電極9)の電位を制御するためには、電極9と対をなす電極10(対電極10)が必要となる。ここで、酸化還元物質3が対電極10に接触すると培養液4の酸化還元電位の制御性が低下することから、酸化還元物質3が対電極10に接触するのを抑制して培養液4の電位を制御し易いものとするために、作用電極9と対電極10の間にイオン交換膜6を設けることが好ましい。
【0047】
以降の説明では、作用電極9と対電極10の間にイオン交換膜6を設けた場合の本発明の窒素代謝微生物の活性化方法と共に、この方法を利用した亜硝酸イオン含有液処理用のバイオリアクタの構成について、第一の実施形態を図2〜5に基づいて説明し、第二の実施形態を図6に基づいて説明する。
【0048】
<第一の実施形態>
第一の実施形態にかかる窒素代謝微生物の活性化方法は、亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方の窒素代謝微生物2と有機物5と酸化還元物質3とを含む培養液4に作用電極9を浸し、培養液4に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極9へ電位を印加していない場合よりも向上する電位を作用電極9に印加しながら窒素代謝微生物2を培養するようにしている。本実施形態では、培養液4にイオン交換膜6を介して電解液4aを接触させ、作用電極9と対をなす電極10(対電極10)を電解液4aに浸すようにしている。
【0049】
第一の実施形態にかかる窒素代謝微生物の活性化方法を利用したバイオリアクタの構成を図2〜5に例示する。図2〜5に示すバイオリアクタ1は、イオン交換膜6によって仕切られた二つの槽のうちの一方の槽を培養槽7とし、他方の槽を対電極槽8とし、培養槽7には培養液4が収容されると共に作用電極9と参照電極11が浸され、対電極槽8には電解液4aが収容されると共に対電極10が浸され、作用電極9と対電極10と参照電極11は定電位設定装置12に結線されている。そして、培養液4に亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方の窒素代謝微生物2と酸化還元物質3と有機物5とが含まれ、培養液4に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極9に電位を印加しない場合よりも向上する電位が作用電極9に印加されながら窒素代謝微生物が培養されるものとしている。
【0050】
このように、3電極方式で作用電極9の電位を制御することで、作用電極9の電位を厳密に設定電位に制御することができ、培養液4の電位(酸化還元電位)を所望の値に厳密に制御することができる。詳細には、定電位設定装置(ポテンシオスタット)12により、作用電極9と参照電極11との間の電位差を測定し、この電位差が設定電位に達するように作用電極9と対電極10との間に電流を流し、基準となる参照電極11には一切電流が流れないようにしている。尚、3電極方式による電位制御については、例えば、電気化学測定法(上)、技報動出版株式会社、第1版15刷、2004年6月発行の6〜9ページにその詳細が記載されている。但し、作用電極9と対電極10の極間電圧のみで作用電極9の電位を制御できる場合には、3電極方式とせずともよい。
【0051】
また、イオン交換膜6は、培養液4に含まれる酸化還元物質3のみならず、窒素代謝微生物2や有機物5を対電極槽8に透過させることなく、培養液4中に留まらせ、且つ培養液4に含まれるイオンまたは電解液4aに含まれるイオンを透過させてイオン電流を生じさせ、作用電極9において生じる酸化還元反応を補完する反応を対電極10で生じさせるものである。これにより、培養液4において酸化還元物質3の酸化体と還元体の比が安定に保持されて、長期に亘って培養液4の電位を制御し易くなる。イオン交換膜6としては、酸化還元物質3(酸化体と還元体)を透過させることのないものを適宜選択して用いる。
【0052】
ここで、図2〜図5に示すバイオリアクタ1では、培養槽7を密閉構造としている。したがって、培養液4の嫌気性雰囲気を制御し易い。即ち、培養槽7を密閉構造とすることで、遊離酸素の進入が起こらないので、培養を開始する前に培養槽7の遊離酸素を実質的に無くせば、培養期間中は嫌気状態を維持し続けて、窒素代謝微生物2の機能を良好に機能させることができる。
【0053】
また、図2〜図5に示すバイオリアクタ1では、培養槽7に、亜硝酸イオン含有液を導入する被処理液導入部18を備え、培養槽7の培養液4に亜硝酸イオン含有液を導入するようにしている。但し、亜硝酸イオン含有液を培養槽7に導入する方法は、この方法に限定されるものではない。
【0054】
さらに、図2〜図5に示すバイオリアクタ1では、培養槽7内の培養液4の液面よりも下部に、培養槽7内の処理液(亜硝酸イオン含有液の亜硝酸イオン濃度が低減された液)を培養液4と共に外に導く処理液排出管16aを備え、この処理液排出管16aをバルブ16bにより開閉可能とした処理液排出手段16により、培養槽7内から処理液を培養液4と共に排出するようにしている。但し、処理液の排出方法は、この方法に限定されるものではない。
【0055】
ここで、本発明のバイオリアクタにおいて、培養液4に窒素代謝微生物2を担持し得る担体を入れることが好適である。この場合、担体に窒素代謝微生物2を担持させて、この担体を培養液4に留めるようにして処理液と培養液4を排出することで、活性化された窒素代謝微生物2を培養槽7の外に排出させることなく、長期に亘ってその機能を活用することができる。また、処理液排出手段16から排出される前に処理液と培養液4とが通過する位置に、担体を処理液及び培養液4から分離する濾過膜または濾過装置を備えるようにして、処理液排出手段16から排出される処理液と培養液4から担体が濾過分離されるようにすることが好適である。尚、担体としては、窒素代謝微生物2を担持し得ると共に吸水し易い素材、例えばスポンジ等を用いることができるが、これに限定されるものではない。例えば、予め窒素代謝微生物2を光硬化性樹脂などのゲル等で固定化する包括固定化法により、微生物を担持させた担体を作製し、これを培養液4に投入するようにしてもよい。
【0056】
また、図2〜図5に示すバイオリアクタ1では、培養槽7を密閉構造とし、培養槽7の培養液4の液面よりも上部の空間(ヘッドスペース)に滞留する窒素ガスを培養槽7の外へ導く窒素ガス排出管15aを備え、この窒素ガス排出管15aをバルブ15bにより開閉可能とした窒素ガス排出手段15を有している。このガス回収手段15により、ヘッドスペースに滞留し得る窒素ガスを排出するようにしている。但し、亜硝酸酸化微生物2bを活性化させる場合には、窒素ガスは発生しないので、この場合には窒素ガス排出手段15は設けずともよい。また、窒素ガス排出管15aのみでヘッドスペースに滞留する窒素ガスを培養槽7の外へ導くようにしてもよい。
【0057】
尚、被処理液導入部18とは別に、培養液4に物質を添加・供給する手段を設けるようにしてもよい。具体的には、培養槽7の外部から培養液4に物質を添加・供給することのできる開閉可能な物質導入管を備えるようにしてもよい。この場合には、培養液4に栄養源、中和剤、物質生産に必要な物質等を必要に応じて添加することができる。勿論、微生物2をこの導入管から供給することもできるし、酸化還元物質3や有機物5を導入することもできる。また、嫌気条件とするためのガス(窒素ガス等)を供給することもできる。但し、培養液4に物質を添加・供給する手段は必ずしも備える必要はなく、被処理液導入部18を培養液4に物質を添加・供給する手段として併用するようにしてもよい。また、被処理液に添加・供給した物質を混合して培養槽7に供給するようにしてもよい。また、電解液4aに物質を添加・供給する手段を設けるようにしてもよい。
【0058】
また、図2〜図5に示すバイオリアクタ1では、対電極槽8を密閉構造とし、対電極槽8の電解液4aの液面よりも上部の空間(ヘッドスペース)に滞留するガスを対電極槽8の外へ導くガス排出管17aを備え、このガス排出管17aをバルブ17bにより開閉可能としたガス放出手段17により、対電極10から発生したガスを培養槽7に漏洩させることなく放出するようにしている。但し、対電極槽8におけるガス発生量が少ない場合には、ガス放出手段17を設けずともよい。また、バルブ17bを省略して、ガス排出管17aから常時ガスが放出される構成としても勿論よい。また、対電極槽8を密閉構造とすることは必須条件ではなく、培養槽7の密閉性を阻害しない範囲で開放構造としても構わない。
【0059】
以下、図2に示すバイオリアクタを用いた場合を第一の実施形態Aとして説明し、図3に示すバイオリアクタを用いた場合を第一の実施形態Bとして説明し、図4に示すバイオリアクタを用いた場合を第一の実施形態Cとして説明し、図5に示すバイオリアクタを用いた場合を第一の実施形態Dとして説明する。
【0060】
(第一の実施形態A)
図2に示すバイオリアクタ1は、密閉構造の容器20を培養槽7とし、容器20に収容可能な密閉構造の小容器21を対電極槽8とし、小容器21は少なくとも一部にイオン交換膜6を備え、培養槽7には被処理液導入部18、処理液排出手段16及び窒素ガス排出手段15を備えるものとしている。
【0061】
容器20に小容器21を収容することで、容器20に収容されている培養液4に小容器21が浸され、小容器21の少なくとも一部に備えられているイオン交換膜6は培養液4と接触する。換言すれば、培養液4はイオン交換膜6を介して電解液4aと接触する。
【0062】
培養槽7としての密閉構造の容器20は、対電極槽8としての密閉構造の小容器21を収容可能な大きさの容器であり、形状は特に限定されない。容器の材質としては、例えば、ガラス、プラスチック、絶縁処理を施した金属、コンクリート等が挙げられるがこれらに限定されるものではない。また、ガス不透過性の膜材をヒートシール等により袋状に形成した容器を培養槽7として用いるようにしてもよい。
【0063】
対電極槽8としての密閉構造の小容器21は、培養槽7としての容器20に収容可能な大きさの容器であり、少なくとも一部にイオン交換膜6を備えるものとしている。ここで、小容器21はその全体をイオン交換膜6で形成した袋状の容器としてもよいが、袋状の容器の片面だけをイオン交換膜6で構成したり、一つの面のさらに一部分をイオン交換膜6のみで構成するようにしてもよい。部分的にイオン交換膜6を用いる場合には、その他の部分は容器20と同様の上記材質で構成してもよいし、イオン交換膜6以外の膜材、例えばガス不透過性の膜材により構成し、小容器21で発生するガスが容器20の内部に漏洩しないようにしてもよい。
【0064】
対電極10としては、作用電極9における酸化還元反応に対して電子の授受を補完する反応が生じ得る材質の電極、例えば炭素電極等を用いることができるが、これに限定されるものではない。
【0065】
図2に示すバイオリアクタ1によれば、活性化された窒素代謝微生物2を含む培養液4中で亜硝酸イオン含有液を処理することができるので、亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することができる。
【0066】
(第一の実施形態B)
図3に示すバイオリアクタ1は、上方が開放されている容器23をイオン交換膜6で仕切ることにより開放された二つの槽が形成され、培養槽7としての一方の槽の上方開放部がガス不透過膜またはガス不透過部材24により塞がれているものとしている。同様に、対電極槽8としての他方の槽の上方開放部もガス不透過膜またはガス不透過性部材24により塞がれているものとしている。培養槽7には被処理液導入部18、処理液排出手段16及び窒素ガス排出手段15を備えるものとしている。尚、図3に示すバイオリアクタ1においては、容器23の密閉性が確保されていれば、培養槽7のヘッドスペースと対電極槽8のヘッドスペースとを完全に仕切る必要はない。
【0067】
ガス不透過膜またはガス不透過部材24としては、各種分野で一般に用いられているものを適宜用いることができる。例えば、ガス不透過部材としては、ガラス、プラスチック、絶縁処理を施した金属、コンクリート等が挙げられるがこれらに限定されるものではない。また、ガス不透過膜としては、例えばイオン交換膜6を用いることができるがこれに限定されるものではない。
【0068】
図3に示すバイオリアクタ1によれば、図2に示すバイオリアクタ1と同様、活性化された窒素代謝微生物2を含む培養液4中で亜硝酸イオン含有液を処理することができるので、亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することができる。
【0069】
(第一の実施形態C)
図4に示すバイオリアクタ1は、収容される液体の液面よりも下部に開口部を備える二つの容器25aと25bがイオン交換膜6を介して開口部で連結されてU字型の容器25が形成され、一方の容器25aを密閉構造として培養槽7とし、他方の容器25bも密閉して対電極槽8としている。この場合、培養液4と電解液4aがイオン交換膜6を介して接触すると共に、培養槽7の培養液4の液面よりも上部の空間と対電極槽8の電解液4aの液面よりも上部の空間とが容器25自体のU字型構造によって隔てて配置される。図4に示すバイオリアクタ1によれば、図2に示すバイオリアクタ1と同様、活性化された窒素代謝微生物2を含む培養液4中で亜硝酸イオン含有液を処理することができるので、亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することができる。
【0070】
(第一の実施形態D)
図5に示すバイオリアクタ1は、収容される液体の液面よりも下部に開口部を備える二つの容器26aと26bがイオン交換膜6を介して開口部で連結されてH字型の容器26が形成され、一方の容器26aを密閉構造として培養槽7とし、他方の容器26bも密閉して対電極槽8としている。この場合にも、培養液4と電解液4aがイオン交換膜6を介して接触すると共に、培養槽7の培養液4の液面よりも上部の空間と対電極槽8の電解液4aの液面よりも上部の空間とが容器26自体のH字型構造によって隔てて配置される。図5に示すバイオリアクタ1によれば、図2に示すバイオリアクタ1と同様、活性化された窒素代謝微生物2を含む培養液4中で亜硝酸イオン含有液を処理することができるので、亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することができる。
【0071】
<第二の実施形態>
第二の実施形態にかかる窒素代謝微生物の活性化方法は、亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方の窒素代謝微生物2と有機物5と酸化還元物質3とを含む培養液4に作用電極9を浸し、培養液4に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極9へ電位を印加していない場合よりも向上する電位を作用電極9に印加しながら窒素代謝微生物2を培養するようにしている。本実施形態では、培養液4にイオン交換膜6を介して対電極9を接触させるようにしている。つまり、第一の実施形態における窒素代謝微生物の活性化方法とは、電解液4aを用いることなく対電極10を直接イオン交換膜6に接触させている点が異なっている。しかしながら、第一の実施形態のように電解液4aを用いずとも、作用電極9と対電極10との間でイオン交換膜6を介してイオン電流は流れるので、第二の実施形態にかかる窒素代謝微生物の活性化方法によれば、第一の実施形態と同様に作用電極9の電位を制御して、同様の効果を得ることが可能である。
【0072】
第二の実施形態にかかる窒素代謝微生物の活性化方法を利用したバイオリアクタの構成を図6に例示する。図6に示すバイオリアクタ1は、イオン交換膜6を少なくとも一部に備える密閉構造の容器50内に作用電極9と参照電極11が配置され、容器50の外側に対電極10が配置され、容器50に培養液4が収容されると共に作用電極9と参照電極11が培養液4に浸され、容器50のイオン交換膜6は容器50に培養液4が収容されたときに少なくともその一部がイオン交換膜6と接触しうる位置に備えられ、イオン交換膜6の培養液4の接触面とは反対側の面の少なくとも一部に対電極10が接触して配置されているものとしている。図6に示すバイオリアクタ1では、容器50の培養液4の液面よりも下部に開口部50aが設けられ、開口部50aがイオン交換膜6で塞がれ、容器50の外側のイオン交換膜6の表面の少なくとも一部に対電極10が接触して配置されているものとしている。つまり、図6に示すバイオリアクタ1では、容器50全体が培養槽7として機能することとなる。
【0073】
したがって、図6に示すバイオリアクタ1によれば、容器50を密閉構造としているので、第一の実施形態と同様、培養槽7の嫌気性雰囲気を制御し易い。
【0074】
尚、図6に示すバイオリアクタ1においては、第一の実施形態と同様に、被処理液導入部18、処理液排出手段16及び窒素ガス排出手段15を備えるようにしているが、上記の通り、被処理液導入方法、処理液排出方法、窒素ガス排出方法はこれらの手段を利用したものには限定されない。また、第一の実施形態と同様に、培養液4に窒素代謝微生物2を担持し得る担体を入れるようにしてもよいし、処理液排出手段16から排出される前に処理液と培養液4とが通過する位置に、担体を処理液及び培養液4から分離する濾過膜または濾過装置を備えるようにして、処理液排出手段16から排出される処理液と培養液4から担体が濾過分離されるようにしてもよい。さらに、第一の実施形態と同様、培養液4に物質を添加・供給する手段を設けるようにしてもよい。
【0075】
以下、図6に示すバイオリアクタ1の詳細について説明する。但し、以下に説明する以外の構成については、第一の実施形態と実質的に同一であり、説明は省略する。
【0076】
容器50は、イオン交換膜6を少なくとも一部に備える密閉構造としている。容器50の材質としては、例えば、ガラス、プラスチック、絶縁処理を施した金属、コンクリート等が挙げられるがこれらに限定されるものではない。尚、図6では、密閉構造の容器50の培養液4の液面よりも下部に設けられた開口部50aをイオン交換膜6により塞ぐようにしているが、容器50の形態や構造は特に限定されない。例えば容器50全体をイオン交換膜6で形成した袋状の容器としてもよいし、袋状の容器の片面だけをイオン交換膜6で構成してもよいし、一つの面のさらに一部分をイオン交換膜6のみで構成するようにしてもよい。部分的にイオン交換膜6を用いる場合には、その他の部分はガラス等の上記材質で構成してもよいし、イオン交換膜6以外の膜材、例えば培養液4と培養液4中の成分の双方を透過させることがない膜材により構成してもよい。要は、容器50に収容される培養液4が容器50の少なくとも一部を構成するイオン交換膜6と接触しうる構造の容器とすればよい。
【0077】
対電極10は、イオン交換膜6の培養液4との接触面とは反対側の面の少なくとも一部に接触させるようにしている。本実施形態において、対電極10は板状の炭素電極としているが、対電極10の形状と材質はこれに限定されるものではなく、要は、イオン交換膜6との接触が可能な形状であり、且つ作用電極9における酸化還元反応に対して電子の授受を補完する反応を進行させることが可能な材質の電極とすればよい。また、本実施形態では、対電極10の面積をイオン交換膜6の面積よりも大きなものとしてイオン交換膜6全体を対電極10で完全に覆うようにし、イオン交換膜6と対電極10とを接触させるようにしているが、イオン交換膜6の培養液4との接触面とは反対側の面の少なくとも一部に対電極10を接触させればよく、必ずしもイオン交換膜6全体を対電極10で完全に覆うようにしてイオン交換膜6と対電極10とを接触させずともよい。但し、イオン交換膜6全体を対電極10で完全に覆うことで、対電極10をイオン交換膜6の保護材としても機能させることができると共に、培養液4からのイオンの伝達面が増大する結果として、培養液4の電位制御性を高めることができる利点があり、好適である。イオン交換膜6全体を対電極10で完全に覆う方法としては、例えば、容器50の開口部50aの周囲に接着剤を塗布して対電極10を接着することにより、開口部50aを塞ぐイオン交換膜6全体と対電極10とを接触させるようにしてもよいし、容器50の開口部50aの周囲に接着剤を塗布して対電極10の表面の少なくとも一部に塗布形成されたイオン交換膜6を接着することにより、開口部50aをイオン交換膜6で塞ぎつつ、開口部50aを塞ぐイオン交換膜6全体と対電極10とを接触させるようにしてもよい。イオン交換膜6を塗布形成するための薬剤としては、例えばナフィオン分散液が挙げられるが、これに限定されるものではない。また、対電極10の表面にナフィオン分散液を塗布し、ナフィオン分散液が乾燥する前にイオン交換膜6を貼り付けるようにしてもよい。この場合には、イオン交換膜6の対電極10の表面への接着性と接触性とを十分なものとすることができる。
【0078】
ここで、対電極10は多孔質体とすることが好適である。この場合には、イオン交換膜6と対電極10との接触面で発生したガスを接触面とは反対側の面に通過させやすくなる。尚、対電極10を多孔質体とし、ナフィオン分散液を用いてイオン交換膜6を貼り付けることで、ナフィオン分散液の多孔質体の孔への侵入によりイオン交換膜6と対電極10との接触面積を増大させて電気化学反応をより進行させやすくすることができ、好適である。
【0079】
上述の形態は本発明の好適な形態の一例ではあるがこれに限定されるものではなく本発明の要旨を逸脱しない範囲において種々変形実施可能である。
【0080】
例えば、図7に示すように、培養液4と電解質4aをイオン交換膜6ではなく、イオンや微生物を一切透過させることのない不透過部材40で隔て、あるいは培養槽7と対電極槽8を別の容器で形成し、塩橋41(寒天等にKCl等の飽和電解質溶液を入れたもの)を介して培養液4と電解質4aを接触(液絡)させるようにしてもよい。この場合にも、塩橋41によってイオン電流の流れが許容されると共に、酸化還元物質3の対電極槽8への透過を防ぐことができるので、上述の実施形態と同様の効果が得られる。
【0081】
また、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aを含む培養液4中で亜硝酸イオン含有液を処理する場合、亜硝酸イオン含有液には、硝酸イオンが含まれていてもよい。この場合には、亜硝酸還元微生物2aにより、亜硝酸イオンと硝酸イオンの双方を効率よく窒素ガスに還元することができる。また、亜硝酸イオン含有液には、窒素代謝微生物2の炭素源となる有機物5が含まれていてもよい。この場合、亜硝酸イオン含有液に含まれる有機物5を窒素代謝微生物2が炭素源として利用して分解しながら、亜硝酸イオンの還元または酸化を行うことができ、亜硝酸イオン含有液に含まれる亜硝酸イオン濃度の低減と同時にTOC濃度の低減を図ることもできる。
【0082】
また、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aまたは亜硝酸酸化微生物2bを利用して、亜硝酸生成微生物により生成される亜硝酸イオンを酸化または還元してその濃度を低減することで、亜硝酸生成微生物が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、亜硝酸生成微生物を良好に培養することが可能となる。例えば、硝酸イオンを最終電子受容体として硝酸呼吸を行うことにより亜硝酸イオンを生成する硝酸呼吸能を有する微生物は自然界に広く存在している。具体的には、例えば、アルカリゲネス(Alcaligenes)属、アグロバクテリウム(Agrobacterium)属、アクアスピリラム(Aquaspirillum)属、アゾスピリラム(Azospirillum)属、バチルス(Bacillus)属、ブラストバクター(Blastobacter)属、ブラディリゾビウム(Bradyrhizobium)属、ブランハメラ(Branhamella)属、クロモバクテリウム(Chromobacterium)属、サイトファーガ(Cytophaga)属、エンテロバクター(Enterobacter)属、エシェリキア(Escherichia)属、フラボバクテリウム(Flavobacterium)属、フレキシバクター(Flexibacter)属、ハロバクテリウム(Halobacterium)属、ヒポミクロビウム(Hyphomicrobium)属、キンゲラ(Kingella)属、クレブシエラ(Klebsiella)属、リソバクター(Lysobacter)属、ネイセイリア(Neisseiria)属、パラコッカス(Paracoccus)属、プロピオニバクテリウム(Propionibacterium)属、シュードモナス(Pseudomonas)属、リゾビウム(Rhizobium)属、ウォリネラ(Wolinella)属、ロドシュードモナス(Rhodopseudomonas)属、チオバチルス(Thiobacillus)属、ニトロソモナス(Nitrosomonas)属、チオミクロスピラ(Thiomicrospira)属、チオスフェラ(Thiosphera)属等が挙げられる。ここで、大腸菌(Escherichia coli)、ブラディリゾビウム ジャポニカム(Bradyrhyzobium japonicum)、クレブシエラ プネウモニア(Klebsiella pneumonia)、エンテロバクター エアロゲネス(Enterobacter aerogenes)、チオバチルス チオパラス(Thiobacillus thioparus)、リゾバクター アンチビオティカム(Lysobacter antibioticum)等は、硝酸呼吸能を有する微生物の中でも特に、硝酸呼吸により培養液に亜硝酸イオンが蓄積されやすい微生物であり、亜硝酸イオンの生物毒性によって、生育が阻害されやすく、培養し難い。しかしながら、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aまたは亜硝酸酸化微生物2bを利用してこれらの微生物により生成される亜硝酸イオンを酸化または還元してその濃度を低減することで、これらの微生物が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、従来は培養が難しかったこれらの微生物を良好に培養(集積培養)することが可能となる。
【0083】
特に、本発明の窒素代謝微生物の活性化方法により亜硝酸酸化微生物2bを活性化させた場合には、この微生物の機能により、亜硝酸イオンを硝酸イオンに酸化することができるので、この硝酸イオンを上記硝酸呼吸能を有する微生物に供給して硝酸呼吸を行わせ、硝酸呼吸により生じた亜硝酸イオンを亜硝酸酸化微生物2bに供給して亜硝酸イオンを硝酸イオンに酸化させるといった、いわば硝酸イオンと亜硝酸イオンの循環経路を確立することができる。したがって、亜硝酸酸化微生物2bと共に硝酸呼吸能を有する微生物を効率よく培養することができる。本発明の窒素代謝微生物の活性化方法により亜硝酸還元微生物2aを活性化させた場合には、上記循環経路は確立されないものの、硝酸イオンを定期的に又は随意に培養液に供給することで、硝酸呼吸能を有する微生物に硝酸呼吸を行わせて、亜硝酸還元微生物2aと共に培養することができる。
【0084】
また、亜硝酸生成微生物は、単独で硝酸イオンを亜硝酸イオン経由で窒素に変換する菌(脱窒菌)としてもよい。即ち、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aまたは亜硝酸酸化微生物2bを利用して、単独で硝酸イオンを亜硝酸イオン経由で窒素に変換する菌(脱窒菌)により硝酸イオンが還元されて生成される亜硝酸イオンを還元または酸化してその濃度を低減することで、脱窒菌が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、脱窒菌を良好に培養することが可能となる。したがって、従来は培養が難しかった一部の脱窒菌を良好に培養(集積培養)することが可能となる。また、培養液4に単独で硝酸イオンを亜硝酸イオン経由で窒素に変換する菌(脱窒菌)と亜硝酸還元微生物2aを含ませ、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aを利用して亜硝酸還元反応を促進させることで、脱窒菌の生育を良好なものとして、さらには従来は培養が難しかった一部の脱窒菌を良好に培養し得ることによって、脱窒プロセス全体を促進し得るので、脱窒反応を利用した硝酸イオン及び亜硝酸イオンを含む廃水等の水処理プロセスの効率化を図ることも可能となる。
【実施例】
【0085】
以下に本発明の実施例を説明するが、本発明はこれら実施例に限られるものではない。
【0086】
尚、本実施例における電位は、全て銀・塩化銀電極電位を基準とするものである。
【0087】
<実験装置>
図8に示す電気培養装置1により実験を行った。培養槽7としての容器20は250mL容のガラスバイアル瓶(Duran製)とした。培養液4は200mL収容した。容器20には蓋30をした。蓋30の上面30aにはシリコーンゴム栓を設けて、配線や電極、管と通した際の密閉性を確保した。
【0088】
対電極槽8としての小容器21は、イオン交換膜6を成型して袋状(以下、袋21と呼ぶ)とした。実験で用いた小容器21の形態を図9に示す。具体的には、陽イオン交換膜(デュポン製、ナフィオンK)をヒートシーラーで熱圧着により加工して上部が開口した袋状の容器21とし、袋21の内部には電解液4aを収容すると共に対電極10を収容して電解液4aに浸した。そして、対電極10と電位制御装置12を結線するための配線31をガス排出管22に通した。ガス排出管22は両端が開口されており、一端を小容器21の内部に、他端を容器20の外側に配置するようにして、小容器21内で発生するガスが容器20の外側に排出されるようにした。袋状の小容器21の上部の開口部は、シリコン接着剤32で塞いだ。
【0089】
小容器21と作用電極9とを培養液4に浸漬し、小容器21のガス排出管22と作用電極9の配線は蓋30に設けたシリコーンゴム栓に通して容器20の外側に引き出した。参照電極11(RE-1B, ビー・エー・エス株式会社)は容器20の外側からシリコーンゴム栓に通して差し込むことにより培養液4と接触させた。処理液排出管16は容器20の外側からシリコーンゴム栓に通して差し込むことによりその一端を培養液4と接触させた。作用電極9と対電極10と参照電極11とを3電極式の電位制御装置(ポテンシオスタット)12に結線して、培養液4の電位を厳密に制御可能とした。処理液排出管16の他端は注射器と接続して培養液4を採取可能とした。
【0090】
<培養液>
培養槽7には、以下の組成の培養液を収容した。尚、以下の組成のうち、KHCO3とプロピオン酸が微生物2の炭素源として機能する。
[培養液組成]
・KHCO3 :500ppm
・KH2PO4 :27ppm
・MgSO4・7H2O :300ppm
・CaCl2・2H2O :180ppm
・プロピオン酸 :1mM
・微量元素(Zn、Co、Mn、Cu、Mo、Ni、Se、B、Fe) :1mL
【0091】
<電解液>
後述する酸化還元物質3(アントラキノン2,6−ジスルホン酸:AQDS)を含まないことを除いて培養液4と同一成分とした。
【0092】
(実施例1)
アンモニウムイオンの酸化還元特性について検討した。
【0093】
培養液4にアンモニウムイオンとしてNH4Clを10mM添加し、作用電極9を炭素電極(BAS社製)とし、対電極10を白金棒電極(自作)として、上記実験装置を用いてサイクリックボルタンメトリーにより酸化還元特性を測定した(掃引速度100mV/s)。結果を図10に示す。図10に示される結果から、アンモニウムイオンは、−1.5V〜+1.5Vの範囲では酸化還元されないことが明らかとなった。
【0094】
(実施例2)
亜硝酸イオンの酸化還元特性について検討した。
【0095】
培養液4に亜硝酸イオンとしてKNO2を10mM添加し、作用電極9を炭素電極(BAS社製)とし、対電極10を白金棒電極(自作)として、上記実験装置を用いてサイクリックボルタンメトリーにより酸化還元特性を測定した(掃引速度100mV/s)。結果を図11に示す。図11に示される結果から、亜硝酸イオンは、+0.7V以上で酸化されるが、−1.5V〜+0.7V未満の範囲では酸化還元されないことが明らかとなった。
【0096】
(実施例3)
培養液4に、微生物2として(九十九里、2009年04月18日)から採取した水田土壌を 2g、酸化還元物質3としてアントラキノン2,6−ジスルホン酸(AQDS)を2mM添加した。作用電極9と対電極10は炭素電極とした。また、培養液4にはスポンジ(東和産業株式会社製、商品名:ピカるちゃんキューブ)を200mLの培養液4に対して10mm×10mm×15mmに切ったスポンジ16個を添加して、試験期間中の培養液4の抜き取りの際の微生物2の流出や減少を抑制した。
【0097】
培養液4には、亜硝酸イオン源としてKNO2を50ppm添加し、アンモニウムイオン源として(NH4)2SO4を50ppm添加した。また、試験期間中には、定期的にKNO2、(NH4)2SO4、炭素源であるKHCO3とプロピオン酸、微量元素を添加するようにした。KHCO3、プロピオン酸、微量元素は定期的に初期値と同一量を添加した(18日、40日、60日)。アンモニウムイオンは5日後に約100ppmに設定した後は添加しなかった。亜硝酸イオンは約5日ごとにサンプリングおよび測定を行い、低下が見られたら添加する方針で運転を行い、段階的にKNO2負荷を上昇させた。具体的には、5日目:50ppm, 5日目〜20日目:17.5ppm, 21日目〜32日目35ppm、33日目〜48日目:70ppm、49日目以降210ppmとし、56日目のみは525ppmとして大幅に負荷を上昇させた。
【0098】
蓋30に備えられたシリコーンゴム栓に注射針を2本刺し、一方の注射針からN2ガスを1時間通気することにより、培養液4の液面上部のヘッドスペースをN2ガスで置換した。培養液4は攪拌子34で攪拌させ、37℃で培養試験を実施した。
【0099】
培養試験の条件は以下の通りとした。
・通電無し(73mV)
・+0.2V
・+0.6V
・−0.6V
【0100】
試験期間中の培養液のアンモニウムイオン濃度、亜硝酸イオン濃度、硝酸イオン濃度はイオンクロマトグラフィー(製品名:ICS-1500、メーカー:DIONEX)、TOC濃度はTOCアナライザー(型番TNC-6000、装置名Automatic TOC analyzer, メーカー:Toray)にて測定した。
【0101】
通電無しにおける試験結果を図12に示し、+0.2Vにおける試験結果を図13に示し、+0.6Vにおける試験結果を図14に示し、−0.6Vにおける試験結果を図15に示す。尚、図12〜図15中、◆がアンモニウムイオン濃度、×がTOC濃度、■が硝酸イオン濃度、▲が亜硝酸イオン濃度を表している。
【0102】
通電無しの条件及び+0.2Vの場合には、添加した亜硝酸イオンの量に応じて亜硝酸イオンの濃度が増加するのみであった。これに対し、+0.6Vでは亜硝酸イオン濃度の減少に対応して、硝酸イオン濃度が増加する傾向が見られた。また、−0.6Vでは亜硝酸イオン濃度の減少に対応して、培養液4からの顕著な泡発生がみられた。これらの結果から、+0.6Vでは培養液4中の亜硝酸酸化細菌が活性化して亜硝酸イオンが硝酸イオンに酸化され、−0.6Vでは亜硝酸還元細菌が活性化して亜硝酸イオンが窒素ガスに還元されていることが考えられた。
【0103】
(実施例4)
培養液中の菌数、亜硝酸還元反応を担う遺伝子であるnirK及びnirSについて、遺伝子学的に解析を実施した。
【0104】
<培養液からのDNA抽出>
試験終了後に培養液4を50mL採取し、遠心分離して菌体を回収した。そして回収した菌体からPowerMicrobial Maxi DNA isolation kit (MO BIO)を用いてゲノムDNAの抽出を行い、最終的に2mlの精製DNAを得た。また、参照データとして、試験開始前の培養液4を50mL採取して、上記と同様、ゲノムDNAの抽出を行った。
【0105】
<微生物の定量>
培養液中に含まれる亜硝酸還元(脱窒プロセス)に関わる微生物の定量を行うために、Light Cycler ST300(Roche)を用いてリアルタイムPCRを行った。
【0106】
まず、培養液に含まれる全菌量を測定するために、LightCycler TaqMan Master(Roche)を用い、Taq−Man probe法により16Sr DNAを定量した。
【0107】
亜硝酸還元反応を担う遺伝子であるnirK、nirS遺伝子は、Light Cycler Fast start DNA Master SYBR Green I (Roche)を用いSYBR Green法により定量した。
【0108】
定量はSecond derivative maximum法によりCp値(Crossing point、蛍光強度増加曲線の二次導関数が最大に達した点)を算出し、全菌数については検量線と照らし合わせて絶対定量を行い、nirK、nirSについては通電せずに培養を行った場合を1とした相対定量を行った。
【0109】
検量線はリアルタイムPCRに用いたプライマーで増幅した大腸菌JM109株の16Sr RNA遺伝子をクローニングしたプラスミド(pT7Blue)を標準物質として10倍希釈の希釈系列をサンプルとしてリアルタイムPCRを行うことにより作成した。
【0110】
各実験に用いたプライマー及びプローブ、PCR条件は以下の通りとした。
【0111】
(1)全菌
プライマー及びプローブは以下の通りとした。
・Uni340F:CCTACGGGRBGCASCAG(配列番号1)
・Uni806R:GGACTACNNGGGTATCTAAT(配列番号2)
・Uni516F (TaqMan probe):TGYCAGCMGCCGCGGTAAHACVNRS(配列番号3)
(5'6-FAM、3'TAMRA)
PCR条件は、以下の通りとし、(ii)〜(iv)を40サイクル実施した。
・(i)95℃10分→(ii)95℃10秒→(iii)50℃45秒→(iv)72℃1秒
【0112】
(2)nirK遺伝子
プライマーは以下の通りとした。
・nirK876 : ATYGGCGGVAYGGCGA(配列番号4)
・nirK1040 : GCCTCGATCAGRTTRTGGTT(配列番号5)
PCR条件は、以下の通りとし、(ii)〜(iv)を32サイクル実施した。
・(i)95℃10分→(ii)95℃10秒→(iii)60℃30秒→(iv)72℃30秒
【0113】
(3)nirS遺伝子
プライマーは以下の通りとした。
・nirSCd3aF : AACGYSAAGGARACSGG(配列番号6)
・nirSR3cd : GASTTCGGRTGSGTCTTSAYGAA(配列番号7)
PCR条件は、以下の通りとし、(ii)〜(iii)を40サイクル実施した。
・(i)95℃10分→(ii)95℃10秒→(iii)65℃20秒
【0114】
全菌の定量結果を図16に示し、nirK遺伝子の定量結果を図17に示し、nirS遺伝子の定量結果を図18に示す。
【0115】
図16に示される結果から、通電した全ての場合において、通電無しの場合と比較して菌数が増大することが明らかとなり、特に−0.6Vにおいて菌数の増大が顕著であった。
【0116】
また、図17及び図18に示される結果から、電した全ての場合において、通電無しの場合と比較してnirK及びnirSの増加が見られ、特に−0.6Vにおいてその傾向が顕著であった。
【0117】
(実施例5)
試験終了後の培養液の微生物叢解析を実施した。
【0118】
PCRにより16S rRNA遺伝子のV3領域(約200bp)を増幅した。PCRはEx-taq polymerase (Takara bio, Japan)及び以下のEscherichia coli由来16S rRNA 遺伝子 (EMBL/GenBank/DDBJ accession number X80721) の配列を元に作成した以下のプライマーを用いて行った。
・forward primer 5’-CCTACGGGAGGCAGCAG-3’
(Escherichia coli 由来16S rRNA 遺伝子における341番目に相当、配列番号8)
・reverse primer 5’-ATTACCGCGGCTGCTGG-3’
(Escherichia coli 由来16S rRNA 遺伝子における517番目に相当、配列番号9)
【0119】
PCRにより増幅した約200bp の16S rDNAの部分DNA断片をアガロース電気泳動により分離、精製した。精製DNA断片はpT7Blue -T vector (Novagen) に挿入し、JM109の形質転換を行った。得られた形質転換体をランダムに約50個取得し、16S rRNA遺伝子クローンの塩基配列解析を行った。塩基配列解析はABI PRISM BigDye terminator v3.0 cycle sequencing kitとABI PRISM 310 Genetic Analyzer (Applied Biosystems) を使用し、dideoxy nucleotide chain termination法により決定した。得られた16S rRNA遺伝子の塩基配列について国際塩基配列データベース (GeneBank/EMBL/DDBJ) からDNA塩基配列データベースに対する相同性検索を行い、類縁微生物の推定を行った。
【0120】
解析結果を図19に示す。植菌試料から検出された微生物種は37種と非常に雑多であったにも関わらず、通電しながら培養を行うことで、ある種の微生物が優占化する傾向が見られた。具体的には、−0.6Vにおいては、シュードモナス(Pseudomonas)属、アリシクリフィルス(Alicycliphilus)属及びティシエレラ(Tissierella)属の微生物が優占化している傾向が見られ、これらの微生物の優占化によって亜硝酸イオンを窒素ガスに還元する速度が促進されたものと考えられた。また、+0.6Vでは、シュードモナス(Pseudomonas)属、ブルクホルデリア(Burkholderia)属及びシュードキサントモナス(Pseudoxanthomonas)属の微生物が優占化している傾向が見られた。ここで、シュードモナス(Pseudomonas)属及びシュードキサントモナス(Pseudoxanthomonas)属の微生物は、硝酸還元能及び亜硝酸還元能を有することが知られており、ブルクホルデリア(Burkholderia)属の微生物は亜硝酸酸化能を有することが知られていることから、+0.6Vによる亜硝酸酸化反応の促進は、+0.6Vにおいては、シュードモナス(Pseudomonas)属及びシュードキサントモナス(Pseudoxanthomonas)属の微生物の生育は促進されるものの硝酸還元及び亜硝酸還元活性は弱く、ブルクホルデリア(Burkholderia)属の微生物の生育が促進されて亜硝酸酸化活性が向上し、全体として亜硝酸酸化反応が促進されたものと考えられる。
【0121】
以上の結果から、本発明の窒素代謝微生物の活性化方法により、亜硝酸還元能を有する微生物または亜硝酸酸化能を有する微生物を選択的に増殖させて培養液中に優占化させて存在させることができ、これにより培養液の亜硝酸イオン処理能力(還元または酸化能力)を大きく向上できることが明らかとなった。
【産業上の利用可能性】
【0122】
本発明の窒素代謝微生物の活性化方法を利用することで、土壌サンプル等のように雑多な微生物を含む試料から、亜硝酸還元微生物または亜硝酸酸化微生物を選択的に増殖させて、集積的に培養を行うことができる。したがって、通常の培養方法では増殖させにくい微生物を増殖させやすいものとして、新たな機能性微生物の探索に資する。即ち、本発明は、自然界に存在する膨大な微生物資源から新規なあるいは従来よりも優れた機能を有する微生物の探索に貢献し得るものである。
【符号の説明】
【0123】
1 バイオリアクタ
2 窒素代謝微生物
2a 亜硝酸還元微生物
2b 亜硝酸酸化微生物
3 酸化還元物質
4 培養液
4a 電解液
5 有機物
6 イオン交換膜
7 培養槽
8 対電極槽
9 作用電極
10 対電極
12 定電位設定装置
15 窒素ガス排出手段
16 処理液排出手段
18 被処理液導入部
【技術分野】
【0001】
本発明は、窒素代謝微生物の活性化方法及びバイオリアクタに関する。さらに詳述すると、本発明は、窒素代謝微生物である亜硝酸還元能を有する亜硝酸還元微生物または亜硝酸酸化能を有する亜硝酸酸化微生物を活性化するのに好適な方法、さらには、亜硝酸還元微生物または亜硝酸酸化微生物を活性化しながら亜硝酸イオン含有廃水等の亜硝酸イオン含有液を処理するのに好適なバイオリアクタに関する。
【背景技術】
【0002】
自然環境中の微生物による窒素サイクルを図20に示す。図20に示されるように、窒素は自然環境中において多様な酸化還元反応を得て、様々な形態で存在している。
【0003】
現在では、このような微生物による窒素サイクルを利用して、廃水(排水)に含まれるアンモニウムイオンや硝酸イオン、亜硝酸イオンを処理する方法が各種提案されている(例えば、特許文献1を参照)。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2000−237791号
【発明の概要】
【発明が解決しようとする課題】
【0005】
微生物による窒素サイクルを利用して廃水処理を行う場合、処理効率を高める上では、
処理に必要な機能を有する微生物を選択的に且つ高濃度に処理槽に存在させて機能させることが重要となる。しかしながら、微生物による窒素サイクルを利用した従来の廃水処理方法では、処理に必要な機能を有する微生物を選択的に且つ高濃度に処理槽に存在させて機能させることには限界があり、その改善が望まれていた。
【0006】
そこで、本発明は、微生物による窒素サイクルの中でも特に重要な窒素代謝微生物である、亜硝酸イオンを窒素ガスに還元する亜硝酸還元微生物または亜硝酸イオンを硝酸イオンに酸化する亜硝酸酸化微生物について、選択的に且つ高濃度に処理槽等に存在させて機能させることができる窒素代謝微生物の活性化方法を提供することを目的とする。
【0007】
また、本発明は、亜硝酸イオンを窒素ガスに還元する亜硝酸還元微生物または亜硝酸イオンを硝酸イオンに酸化する亜硝酸酸化微生物について、選択的に且つ高濃度に処理槽等に存在させて機能させ、亜硝酸イオン含有廃水等の亜硝酸イオン含有液を効率よく処理することのできる方法及びバイオリアクタを提供することを目的とする。
【課題を解決するための手段】
【0008】
かかる課題を解決するため、本願発明者等が鋭意検討を行った結果、培養液に水田土壌を添加し、酸化還元物質を添加した培養液に電極を浸して電極の電位をある値に制御することで、電極に電位を印加しない場合と比較して亜硝酸イオンが窒素ガスに還元される速度が顕著に促進されることが明らかとなった。また、電極の電位を上記とは別の値に制御することで、電極に電位を印加しない場合と比較して亜硝酸イオンが硝酸イオンに酸化される速度が顕著に促進されることも明らかとなった。
【0009】
そして、亜硝酸イオンが窒素ガスに還元される速度が顕著に促進された電位に制御して培養を行った場合の培養液の微生物叢と亜硝酸イオンが硝酸イオンに酸化される速度が顕著に促進された電位に制御して培養を行った場合の培養液の微生物叢について解析を遺伝子学的な解析を行った。その結果、亜硝酸イオンが窒素ガスに還元される速度が顕著に促進された電位に制御して培養を行った場合の培養液の微生物叢においては、亜硝酸還元能(脱窒能)を有する微生物群が優占化していると共に微生物の数自体も電位を印加しない場合と比較して増加することが明らかとなった。また、亜硝酸イオンが硝酸イオンに酸化される速度が顕著に促進された電位に制御して培養を行った場合の培養液の微生物叢においては、亜硝酸酸化能を有する微生物群が優占化していると共に微生物の数自体も電位を印加しない場合と比較して増加することが明らかとなった。
【0010】
これらの結果から、培養液に亜硝酸イオンが溶解しているときの亜硝酸イオンの窒素ガスへの還元速度または亜硝酸イオンの硝酸イオンの酸化速度を指標として、培養液に浸した電極の電位を制御することで、窒素代謝微生物である亜硝酸還元能を有する微生物と亜硝酸酸化能を有する微生物を選択的に活性化(生育促進、さらには機能向上)できることを知見するに至り、さらに種々検討を重ねて本発明を完成するに至った。
【0011】
かかる知見に基づく、本発明の窒素代謝微生物の活性化方法は、亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と有機物と酸化還元物質とを含む培養液に電極を浸し、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が電極へ電位を印加していない場合よりも向上する電位を電極に印加しながら窒素代謝微生物を培養するようにしている。
【0012】
ここで、本発明の窒素代謝微生物の活性化方法において、培養液にイオン交換膜を介して電解液を接触させ、培養液に浸漬した電極と対をなす電極を電解液に浸漬することが好ましい。また、培養液にイオン交換膜を介して培養液に浸漬した電極と対をなす電極を接触させることが好ましい。この場合、培養液中の酸化還元物質が培養液に浸漬した電極と対をなす電極に接触するのを抑制して、培養液の電位(酸化還元電位)を制御させ易いものとできる。
【0013】
また、本発明の窒素代謝微生物の活性化方法においては、電極に印加する電位を、亜硝酸イオンの低減速度が向上する結果として窒素ガスの生成速度が向上する電位とすることにより、亜硝酸還元微生物を活性化することができる。電極に印加する電位は、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位とすることが好ましい。
【0014】
また、本発明の窒素代謝微生物の活性化方法においては、電極に印加する電位を、亜硝酸イオンの低減速度が向上する結果として硝酸イオン生成速度が向上する電位とすることにより、亜硝酸酸化微生物を活性化することができる。電極に印加する電位は、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とすることが好ましい。
【0015】
次に、本発明の亜硝酸イオン含有液の処理方法は、本発明の窒素代謝微生物の活性化方法により活性化された窒素代謝微生物を含む培養液中で亜硝酸イオン含有廃水等の亜硝酸イオン含有液を処理するようにしている。したがって、亜硝酸イオンが効率よく窒素ガスあるいは硝酸イオンに変換(還元または酸化)される。
【0016】
また、本発明の亜硝酸生成微生物の培養方法は、本発明の窒素代謝微生物の活性化方法により活性化された窒素代謝微生物を含む培養液中に亜硝酸イオンを生成する亜硝酸生成微生物を添加し、亜硝酸生成微生物により生成された亜硝酸イオンを活性化された窒素代謝微生物に還元または酸化させて低減し、亜硝酸イオンの毒性による生育阻害を回避しながら亜硝酸生成微生物を培養するようにしている。したがって、亜硝酸生成微生物が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、亜硝酸生成微生物を良好に培養することができる。
【0017】
次に、本発明のバイオリアクタは、イオン交換膜によって仕切られた対電極槽及び密閉構造の培養槽と、培養槽に収容された培養液と、対電極槽に収容された電解液と、培養液に浸された作用電極と、電解液に浸された対電極と、作用電極と対電極とが結線されて作用電極と対電極との間に電位差を与えて作用電極の電位を設定する定電位設定装置と、培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、培養槽から処理液を排出する処理液排出手段とを有し、培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極に電位を印加しない場合よりも向上する電位が作用電極に印加されながら窒素代謝微生物が培養されるものとしている。
【0018】
また、本発明のバイオリアクタは、培養槽としての密閉構造の容器と、容器に収容可能な対電極槽としての密閉構造の小容器と、培養槽に収容された培養液と、対電極槽に収容された電解液と、培養液に浸された作用電極と、電解液に浸された対電極と、作用電極と対電極とが結線されて作用電極と対電極との間に電位差を与えて作用電極の電位を設定する定電位設定装置と、培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、培養槽から処理液を排出する処理液排出手段とを有し、小容器は培養液と接触する位置の少なくとも一部にイオン交換膜を備えるものとし、培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極に電位を印加しない場合よりも向上する電位が作用電極に印加されながら窒素代謝微生物が培養されるものとしている。
【0019】
さらに、本発明のバイオリアクタは、イオン交換膜を少なくとも一部に備える容器と、容器に収容された培養液と、培養液に浸された作用電極と、イオン交換膜の容器の外側の面の少なくとも一部に接触している対電極と、作用電極と対電極とが結線されて作用電極と対電極との間に電位差を与えて作用電極の電位を設定する定電位設定装置と、培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、培養槽から処理液を排出する処理液排出手段とを有し、イオン交換膜は容器の培養液と接触する位置に備えるものとし、培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極に電位を印加しない場合よりも向上する電位が作用電極に印加されながら窒素代謝微生物が培養されるものとしている。
【0020】
本発明のバイオリアクタにおいては、作用電極に印加される電位が、亜硝酸イオンの低減速度が向上する結果として窒素ガスの生成速度が向上する電位とされて亜硝酸還元微生物が活性化され、亜硝酸イオンが還元されて生じた窒素ガスを培養槽から排出する窒素ガス排出手段が備えられているものとすることが好ましい。作用電極に印加される電位は、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位であることが好ましい。
【0021】
また、本発明のバイオリアクタにおいては、作用電極に印加される電位が、亜硝酸イオンの低減速度が向上する結果として硝酸イオン生成速度が向上する電位とされて亜硝酸酸化微生物が活性化されているものとすることが好ましい。作用電極に印加される電位は、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とすることが好ましい。
【発明の効果】
【0022】
本発明の窒素代謝微生物の活性化方法によれば、亜硝酸還元微生物または亜硝酸酸化微生物の生育を選択的に促進させ、さらには亜硝酸還元微生物の亜硝酸還元能または亜硝酸酸化微生物の亜硝酸酸化能を選択的に向上させることが可能となる。したがって、例えば土壌サンプル等のように雑多な微生物を含む試料を用いて、亜硝酸還元微生物または亜硝酸酸化微生物を選択的に増殖させて培養液中に高濃度に存在させ、さらには亜硝酸還元微生物の亜硝酸還元能または亜硝酸酸化微生物の亜硝酸酸化能を選択的に向上させることによって、培養液自体の微生物処理槽としての機能を極めて高いものとすることが可能となる。
【0023】
本発明の亜硝酸イオン含有液の処理方法によれば、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物または亜硝酸酸化微生物を利用して亜硝酸イオン含有液に含まれる亜硝酸イオンを効率よく還元または酸化してその濃度を低減することができる。したがって、亜硝酸イオン含有廃水(排水)を効率よく処理することが可能となる。
【0024】
本発明の亜硝酸生成微生物の培養方法によれば、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物または亜硝酸酸化微生物を利用して亜硝酸生成微生物により生成される亜硝酸イオンを酸化または還元してその濃度を低減するようにしているので、亜硝酸生成微生物が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、亜硝酸生成微生物を良好に培養することが可能となる。例えば、呼吸により硝酸イオンを亜硝酸イオンに還元する硝酸呼吸能を有する微生物(例えば、大腸菌等)は、硝酸呼吸により自らが生成した亜硝酸イオンによってその生育が阻害されるが、本発明の培養方法を利用することによって、亜硝酸イオンによる生育阻害を抑えて、良好に培養することが可能となる。
【0025】
本発明のバイオリアクタによれば、亜硝酸還元微生物または亜硝酸酸化微生物の生育を選択的に促進させ、さらには亜硝酸還元微生物の亜硝酸還元能または亜硝酸酸化微生物の亜硝酸酸化能を選択的に向上させて、培養槽の亜硝酸イオン処理能力を極めて高いものとすることが可能となる。したがって、亜硝酸イオン含有廃水等の亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することが可能となる。
【図面の簡単な説明】
【0026】
【図1】本発明の窒素代謝微生物の活性化方法の概念を示す図である。
【図2】第一の実施形態Aにかかるバイオリアクタの一例を示す断面図である。
【図3】第一の実施形態Bにかかるバイオリアクタの一例を示す断面図である。
【図4】第一の実施形態Cにかかるバイオリアクタの一例を示す断面図である。
【図5】第一の実施形態Dにかかるバイオリアクタの一例を示す断面図である。
【図6】第二の実施形態にかかるバイオリアクタの一例を示す断面図である。
【図7】バイオリアクタの他の構成の一例を示す断面図である。
【図8】実験に使用した装置の概念図である。
【図9】実験に使用した装置の小容器の構成を示す図である。
【図10】アンモニウムイオンの酸化還元特性を示す図である。
【図11】亜硝酸イオンの酸化還元特性を示す図である。
【図12】実施例3における、通電無しの場合の各種物質の経時変化を示す図である。
【図13】実施例3における、+0.2Vの場合の各種物質の経時変化を示す図である。
【図14】実施例3における、+0.6Vの場合の各種物質の経時変化を示す図である。
【図15】実施例3における、−0.6Vの場合の各種物質の経時変化を示す図である。
【図16】実施例4における、全菌数の定量結果を示す図である。
【図17】実施例4における、nirK遺伝子の定量結果を示す図である。
【図18】実施例4における、nirS遺伝子の定量結果を示す図である。
【図19】実施例5における、培養液中の微生物叢解析の結果を示す図である。
【図20】自然環境中の微生物による窒素サイクルに関わる酸化還元反応を示す図である。
【発明を実施するための形態】
【0027】
以下、本発明を実施するための形態について、図面に基づいて詳細に説明する。
【0028】
図1に、本発明の窒素代謝微生物の活性化方法の実施形態の一例を概念的に示す。本発明の窒素代謝微生物の活性化方法は、亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方の窒素代謝微生物2と有機物5と酸化還元物質3とを含む培養液4に電極9(作用電極9)を浸し、培養液4に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が電極9へ電位を印加していない場合よりも向上する電位を電極9に印加しながら窒素代謝微生物2を培養するようにしている。
【0029】
本発明では、窒素代謝微生物2として、亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方を培養液4に含ませる。
【0030】
亜硝酸還元能を有する微生物2aは、亜硝酸イオンを還元する能力を有する微生物であれば特に限定されるものではないが、亜硝酸イオンを窒素ガスに還元(脱窒)する能力を有する微生物が特に好適であり、例えば、シュードモナス(Pseudomonas)属、アリシクリフィルス(Alicycliphilus)属及びティシエレラ(Tissierella)属の微生物を用いることが好適である。
【0031】
亜硝酸酸化能を有する微生物2bは、亜硝酸イオンを硝酸イオンに酸化する能力を有する微生物であれば特に限定されるものではないが、ブルクホルデリア(Burkholderia)属の微生物を用いることが好適である。
【0032】
尚、本発明においては、窒素代謝微生物2として、単離された微生物の市販品や培養品を用いてもよいが、水田土壌のような微生物含有土壌試料や汚泥試料等を用いることができる。即ち、亜硝酸還元能を有する微生物2aや亜硝酸酸化能を有する微生物2bは、通常、土壌や汚泥等に一般的に存在するものであることから、土壌試料や汚泥試料を培養液4に添加することで、窒素代謝微生物2を選択的に増殖させて培養液4に高濃度に存在させることができる。換言すれば、土壌試料や汚泥試料から、窒素代謝微生物を集積培養することができる。
【0033】
培養液4の組成は、窒素代謝微生物2の培養に一般的に用いられている培地の組成とすればよく、特に限定されるものではないが、一例を挙げると、KH2PO4、MgSO4・7H2O、CaCl2・2H2O、微量元素(Zn、Co、Mn、Cu、Mo、Ni、Se、B、Fe)を含む培地を用いることができる。
【0034】
有機物5は、窒素代謝微生物2の炭素源となり得る物質であれば特に限定されるものではないが、例えば炭酸塩やプロピオン酸等を好適に使用することができる。
【0035】
酸化還元物質3は、培養液4に浸されている電極9と可逆的に酸化還元反応を生じる物質であり、且つ窒素代謝微生物2に対して毒性を呈さない物質であればよい。また、窒素代謝微生物の代謝等に直接関与しない物質とすることが好ましい。例えば、キレート剤であるジエチレントリアミンペンタ酢酸(DTPA)、エチレンジアミンテトラ酢酸(EDTA)、テトラエチレントリアミン(TET)、エチレンジアミン(EDA)、ジエチレントリアミン(DETA)、クエン酸、シュウ酸、クラウンエーテル、ニトリロテトラ酢酸、エデト酸二ナトリウム、エデト酸ナトリウム、エデト酸三ナトリウム、ペニシラミン、ペンテテートカルシウム三ナトリウム、ペンテト酸、スクシメルおよびエデト酸トリエンチン、好ましくはEDTAに配位させた鉄イオン、フェロシアン化カリウム、アントラキノンジスルホン酸ナトリウムなどのキノン化合物、メチルビオロゲン等のビオロゲン誘導体等を用いることができるが、これらに限定されるものではない。
【0036】
尚、キノン化合物は土壌成分の一つとして知られている物質であることから、土壌試料や汚泥試料を添加することで、酸化還元物質3を培養液4に存在させることができる場合がある。つまり、土壌試料や汚泥試料に酸化還元物質3が十分に含まれている場合があり、このような場合には、別途酸化還元物質3を培養液4に添加する必要は無くなる。
【0037】
尚、酸化還元物質3の培養液4への添加量は、好適には0.1〜100mM、より好適には1〜10mM、さらに好適には数mMである。酸化還元物質3の添加量が少なすぎると培養液4の酸化還元電位を制御し難くなる場合がある。また、多すぎると培養液4に溶解しなかったり、微生物の生育に悪影響を及ぼす場合もある。
【0038】
本発明においては、電極9の電位を制御することにより酸化還元物質3の酸化体と還元体の比を制御し、培養液4の電位(酸化還元電位)を制御するようにしている。培養液4の酸化還元電位は、数式1のネルンストの式により表される。
[数式1] E=E0+RT/nF×ln(Cox/Cred)
【0039】
数式1において、Eは培養液4の酸化還元電位、E0は酸化還元物質3の標準酸化還元電位、Rは気体定数、Tは絶対温度、nは反応電子数、Fはファラデー定数、Coxは酸化還元物質3の酸化体の濃度、Credは酸化還元物質3の還元体の濃度である。つまり、培養液4に含まれる酸化還元物質3の酸化体の濃度と還元体の濃度の比を電極9の電位を制御して一定に制御することにより、培養液4自体の酸化還元電位を制御することができる。
【0040】
電極9には、酸化還元物質3を可逆的に酸化還元させることが可能な材質のものが適宜用いられる。具体的には、炭素板やグラッシーカーボン等の炭素電極、白金電極等を用いることができるが、これらに限定されるものではない。
【0041】
電極9に与える電位(培養液4の酸化還元電位)は、以下の手順により決定される。即ち、培養液4に亜硝酸イオンを溶解させ、電極9に電位を与えることなく培養試験を行い、亜硝酸イオンの低減速度を決定する。亜硝酸イオンの低減速度は培養過程にて亜硝酸イオンの経時変化を測定することで決定することができる。そして、電極9に各種電位を印加して同様の培養試験を行い、亜硝酸イオンの低減速度を決定する。亜硝酸イオンの低減速度が電極9に電位を与えずに培養試験を行った場合よりも向上していれば、その電位が窒素代謝微生物2を活性化させることのできる電位に該当する。そして、亜硝酸イオンの低減速度が向上した結果として窒素ガスの生成速度が向上している場合には、その電位は、窒素代謝微生物2のうち亜硝酸還元微生物2aを活性化させることのできる電位に該当する。また、亜硝酸イオンの低減速度が向上した結果として硝酸イオンの生成速度が向上している場合には、その電位は、窒素代謝微生物2のうち亜硝酸酸化微生物2bを活性化させることのできる電位に該当する。
【0042】
本願発明者等の実験によると、窒素代謝微生物2のうち亜硝酸還元微生物2aを活性化させ始めることのできる電位は、銀・塩化銀電極電位基準で−0.6V〜+0.2V未満に存在し、−0.6Vとすれば、窒素代謝微生物2のうち亜硝酸還元微生物2aを確実に活性化できることが確認されている。また、−0.6Vで亜硝酸還元微生物2aを活性化できることが確認されたことから、電極9から培養液4に電子を与えやすい電位とすることで、亜硝酸還元微生物2aを活性化できるものと考えられる。したがって、電極9の電位を、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位とすることが好適であるが、電位をマイナス側に大きくし過ぎると水の電気分解が生じて培養液4のpHに変動が生じ、亜硝酸還元微生物2の生育を阻害する虞があるので、−0.6V〜−1.0Vとすることがより好適である。
【0043】
また、本願発明者等の実験によると、窒素代謝微生物2のうち亜硝酸酸化微生物2bを活性化させ始めることのできる電位は、銀・塩化銀電極電位基準で+0.2V超〜+0.6Vに存在し、+0.6Vとすれば、窒素代謝微生物2のうち亜硝酸酸化微生物2bを確実に活性化できることが確認されている。また、+0.6Vで亜硝酸酸化微生物2bを活性化できることが確認されたことから、電極9により培養液4から電子を引き抜きやすい電位とすることで、酸化還元微生物2aを活性化できるものと考えられる。したがって、電極9の電位を、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とすることが好適であるが、電位をプラス側に大きくし過ぎると水の電気分解が生じて培養液4のpHに変動が生じ、亜硝酸酸化微生物2の生育を阻害する虞があるので、+0.6V〜+1.0Vとすることがより好適である。ここで、+0.7Vよりもプラス側に大きな電位とすると、亜硝酸イオンが電気的に酸化されて減少するので、亜硝酸イオンが不足し易くなる。したがって、亜硝酸酸化微生物2bを増殖させる際には、+0.6V〜+0.7Vとすることが好適である。但し、亜硝酸酸化微生物2bが培養液4中に十分に高濃度に存在している場合には、+0.7Vよりもプラス側に大きな電位ととして、亜硝酸酸化微生物2bによる酸化と電気的な酸化とを併用し、亜硝酸イオンを低減してもよい。
【0044】
したがって、本発明の窒素代謝微生物の活性化方法によると、例えば土壌試料や汚泥試料のように、窒素代謝微生物2として亜硝酸還元微生物2aと亜硝酸酸化微生物2bが混在し得る微生物試料を用いた場合においても、亜硝酸還元微生物2aと亜硝酸酸化微生物2bのいずれか一方を選択的に活性化させることができる。
【0045】
尚、本発明の窒素代謝微生物の活性化方法においては、培養液4に亜硝酸イオンを添加しながら窒素代謝微生物2の活性化を図るようにしてもよいが、培養液4中の窒素代謝微生物2の菌体密度が十分に高く、増殖させる必要が無い場合には、亜硝酸イオンを添加せずに電位だけを印加して窒素代謝微生物2を活性化するようにしてもよい。例えば、窒素代謝微生物2の菌体密度が高濃度に維持された培養液4に電位を印加して窒素代謝微生物2を活性化させておき、亜硝酸イオン含有廃液などの亜硝酸イオン含有液を培養液4に投入して亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減するようにしてもよい。
【0046】
尚、本発明の窒素代謝微生物の活性化方法においては、電極9(作用電極9)の電位を制御するためには、電極9と対をなす電極10(対電極10)が必要となる。ここで、酸化還元物質3が対電極10に接触すると培養液4の酸化還元電位の制御性が低下することから、酸化還元物質3が対電極10に接触するのを抑制して培養液4の電位を制御し易いものとするために、作用電極9と対電極10の間にイオン交換膜6を設けることが好ましい。
【0047】
以降の説明では、作用電極9と対電極10の間にイオン交換膜6を設けた場合の本発明の窒素代謝微生物の活性化方法と共に、この方法を利用した亜硝酸イオン含有液処理用のバイオリアクタの構成について、第一の実施形態を図2〜5に基づいて説明し、第二の実施形態を図6に基づいて説明する。
【0048】
<第一の実施形態>
第一の実施形態にかかる窒素代謝微生物の活性化方法は、亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方の窒素代謝微生物2と有機物5と酸化還元物質3とを含む培養液4に作用電極9を浸し、培養液4に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極9へ電位を印加していない場合よりも向上する電位を作用電極9に印加しながら窒素代謝微生物2を培養するようにしている。本実施形態では、培養液4にイオン交換膜6を介して電解液4aを接触させ、作用電極9と対をなす電極10(対電極10)を電解液4aに浸すようにしている。
【0049】
第一の実施形態にかかる窒素代謝微生物の活性化方法を利用したバイオリアクタの構成を図2〜5に例示する。図2〜5に示すバイオリアクタ1は、イオン交換膜6によって仕切られた二つの槽のうちの一方の槽を培養槽7とし、他方の槽を対電極槽8とし、培養槽7には培養液4が収容されると共に作用電極9と参照電極11が浸され、対電極槽8には電解液4aが収容されると共に対電極10が浸され、作用電極9と対電極10と参照電極11は定電位設定装置12に結線されている。そして、培養液4に亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方の窒素代謝微生物2と酸化還元物質3と有機物5とが含まれ、培養液4に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極9に電位を印加しない場合よりも向上する電位が作用電極9に印加されながら窒素代謝微生物が培養されるものとしている。
【0050】
このように、3電極方式で作用電極9の電位を制御することで、作用電極9の電位を厳密に設定電位に制御することができ、培養液4の電位(酸化還元電位)を所望の値に厳密に制御することができる。詳細には、定電位設定装置(ポテンシオスタット)12により、作用電極9と参照電極11との間の電位差を測定し、この電位差が設定電位に達するように作用電極9と対電極10との間に電流を流し、基準となる参照電極11には一切電流が流れないようにしている。尚、3電極方式による電位制御については、例えば、電気化学測定法(上)、技報動出版株式会社、第1版15刷、2004年6月発行の6〜9ページにその詳細が記載されている。但し、作用電極9と対電極10の極間電圧のみで作用電極9の電位を制御できる場合には、3電極方式とせずともよい。
【0051】
また、イオン交換膜6は、培養液4に含まれる酸化還元物質3のみならず、窒素代謝微生物2や有機物5を対電極槽8に透過させることなく、培養液4中に留まらせ、且つ培養液4に含まれるイオンまたは電解液4aに含まれるイオンを透過させてイオン電流を生じさせ、作用電極9において生じる酸化還元反応を補完する反応を対電極10で生じさせるものである。これにより、培養液4において酸化還元物質3の酸化体と還元体の比が安定に保持されて、長期に亘って培養液4の電位を制御し易くなる。イオン交換膜6としては、酸化還元物質3(酸化体と還元体)を透過させることのないものを適宜選択して用いる。
【0052】
ここで、図2〜図5に示すバイオリアクタ1では、培養槽7を密閉構造としている。したがって、培養液4の嫌気性雰囲気を制御し易い。即ち、培養槽7を密閉構造とすることで、遊離酸素の進入が起こらないので、培養を開始する前に培養槽7の遊離酸素を実質的に無くせば、培養期間中は嫌気状態を維持し続けて、窒素代謝微生物2の機能を良好に機能させることができる。
【0053】
また、図2〜図5に示すバイオリアクタ1では、培養槽7に、亜硝酸イオン含有液を導入する被処理液導入部18を備え、培養槽7の培養液4に亜硝酸イオン含有液を導入するようにしている。但し、亜硝酸イオン含有液を培養槽7に導入する方法は、この方法に限定されるものではない。
【0054】
さらに、図2〜図5に示すバイオリアクタ1では、培養槽7内の培養液4の液面よりも下部に、培養槽7内の処理液(亜硝酸イオン含有液の亜硝酸イオン濃度が低減された液)を培養液4と共に外に導く処理液排出管16aを備え、この処理液排出管16aをバルブ16bにより開閉可能とした処理液排出手段16により、培養槽7内から処理液を培養液4と共に排出するようにしている。但し、処理液の排出方法は、この方法に限定されるものではない。
【0055】
ここで、本発明のバイオリアクタにおいて、培養液4に窒素代謝微生物2を担持し得る担体を入れることが好適である。この場合、担体に窒素代謝微生物2を担持させて、この担体を培養液4に留めるようにして処理液と培養液4を排出することで、活性化された窒素代謝微生物2を培養槽7の外に排出させることなく、長期に亘ってその機能を活用することができる。また、処理液排出手段16から排出される前に処理液と培養液4とが通過する位置に、担体を処理液及び培養液4から分離する濾過膜または濾過装置を備えるようにして、処理液排出手段16から排出される処理液と培養液4から担体が濾過分離されるようにすることが好適である。尚、担体としては、窒素代謝微生物2を担持し得ると共に吸水し易い素材、例えばスポンジ等を用いることができるが、これに限定されるものではない。例えば、予め窒素代謝微生物2を光硬化性樹脂などのゲル等で固定化する包括固定化法により、微生物を担持させた担体を作製し、これを培養液4に投入するようにしてもよい。
【0056】
また、図2〜図5に示すバイオリアクタ1では、培養槽7を密閉構造とし、培養槽7の培養液4の液面よりも上部の空間(ヘッドスペース)に滞留する窒素ガスを培養槽7の外へ導く窒素ガス排出管15aを備え、この窒素ガス排出管15aをバルブ15bにより開閉可能とした窒素ガス排出手段15を有している。このガス回収手段15により、ヘッドスペースに滞留し得る窒素ガスを排出するようにしている。但し、亜硝酸酸化微生物2bを活性化させる場合には、窒素ガスは発生しないので、この場合には窒素ガス排出手段15は設けずともよい。また、窒素ガス排出管15aのみでヘッドスペースに滞留する窒素ガスを培養槽7の外へ導くようにしてもよい。
【0057】
尚、被処理液導入部18とは別に、培養液4に物質を添加・供給する手段を設けるようにしてもよい。具体的には、培養槽7の外部から培養液4に物質を添加・供給することのできる開閉可能な物質導入管を備えるようにしてもよい。この場合には、培養液4に栄養源、中和剤、物質生産に必要な物質等を必要に応じて添加することができる。勿論、微生物2をこの導入管から供給することもできるし、酸化還元物質3や有機物5を導入することもできる。また、嫌気条件とするためのガス(窒素ガス等)を供給することもできる。但し、培養液4に物質を添加・供給する手段は必ずしも備える必要はなく、被処理液導入部18を培養液4に物質を添加・供給する手段として併用するようにしてもよい。また、被処理液に添加・供給した物質を混合して培養槽7に供給するようにしてもよい。また、電解液4aに物質を添加・供給する手段を設けるようにしてもよい。
【0058】
また、図2〜図5に示すバイオリアクタ1では、対電極槽8を密閉構造とし、対電極槽8の電解液4aの液面よりも上部の空間(ヘッドスペース)に滞留するガスを対電極槽8の外へ導くガス排出管17aを備え、このガス排出管17aをバルブ17bにより開閉可能としたガス放出手段17により、対電極10から発生したガスを培養槽7に漏洩させることなく放出するようにしている。但し、対電極槽8におけるガス発生量が少ない場合には、ガス放出手段17を設けずともよい。また、バルブ17bを省略して、ガス排出管17aから常時ガスが放出される構成としても勿論よい。また、対電極槽8を密閉構造とすることは必須条件ではなく、培養槽7の密閉性を阻害しない範囲で開放構造としても構わない。
【0059】
以下、図2に示すバイオリアクタを用いた場合を第一の実施形態Aとして説明し、図3に示すバイオリアクタを用いた場合を第一の実施形態Bとして説明し、図4に示すバイオリアクタを用いた場合を第一の実施形態Cとして説明し、図5に示すバイオリアクタを用いた場合を第一の実施形態Dとして説明する。
【0060】
(第一の実施形態A)
図2に示すバイオリアクタ1は、密閉構造の容器20を培養槽7とし、容器20に収容可能な密閉構造の小容器21を対電極槽8とし、小容器21は少なくとも一部にイオン交換膜6を備え、培養槽7には被処理液導入部18、処理液排出手段16及び窒素ガス排出手段15を備えるものとしている。
【0061】
容器20に小容器21を収容することで、容器20に収容されている培養液4に小容器21が浸され、小容器21の少なくとも一部に備えられているイオン交換膜6は培養液4と接触する。換言すれば、培養液4はイオン交換膜6を介して電解液4aと接触する。
【0062】
培養槽7としての密閉構造の容器20は、対電極槽8としての密閉構造の小容器21を収容可能な大きさの容器であり、形状は特に限定されない。容器の材質としては、例えば、ガラス、プラスチック、絶縁処理を施した金属、コンクリート等が挙げられるがこれらに限定されるものではない。また、ガス不透過性の膜材をヒートシール等により袋状に形成した容器を培養槽7として用いるようにしてもよい。
【0063】
対電極槽8としての密閉構造の小容器21は、培養槽7としての容器20に収容可能な大きさの容器であり、少なくとも一部にイオン交換膜6を備えるものとしている。ここで、小容器21はその全体をイオン交換膜6で形成した袋状の容器としてもよいが、袋状の容器の片面だけをイオン交換膜6で構成したり、一つの面のさらに一部分をイオン交換膜6のみで構成するようにしてもよい。部分的にイオン交換膜6を用いる場合には、その他の部分は容器20と同様の上記材質で構成してもよいし、イオン交換膜6以外の膜材、例えばガス不透過性の膜材により構成し、小容器21で発生するガスが容器20の内部に漏洩しないようにしてもよい。
【0064】
対電極10としては、作用電極9における酸化還元反応に対して電子の授受を補完する反応が生じ得る材質の電極、例えば炭素電極等を用いることができるが、これに限定されるものではない。
【0065】
図2に示すバイオリアクタ1によれば、活性化された窒素代謝微生物2を含む培養液4中で亜硝酸イオン含有液を処理することができるので、亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することができる。
【0066】
(第一の実施形態B)
図3に示すバイオリアクタ1は、上方が開放されている容器23をイオン交換膜6で仕切ることにより開放された二つの槽が形成され、培養槽7としての一方の槽の上方開放部がガス不透過膜またはガス不透過部材24により塞がれているものとしている。同様に、対電極槽8としての他方の槽の上方開放部もガス不透過膜またはガス不透過性部材24により塞がれているものとしている。培養槽7には被処理液導入部18、処理液排出手段16及び窒素ガス排出手段15を備えるものとしている。尚、図3に示すバイオリアクタ1においては、容器23の密閉性が確保されていれば、培養槽7のヘッドスペースと対電極槽8のヘッドスペースとを完全に仕切る必要はない。
【0067】
ガス不透過膜またはガス不透過部材24としては、各種分野で一般に用いられているものを適宜用いることができる。例えば、ガス不透過部材としては、ガラス、プラスチック、絶縁処理を施した金属、コンクリート等が挙げられるがこれらに限定されるものではない。また、ガス不透過膜としては、例えばイオン交換膜6を用いることができるがこれに限定されるものではない。
【0068】
図3に示すバイオリアクタ1によれば、図2に示すバイオリアクタ1と同様、活性化された窒素代謝微生物2を含む培養液4中で亜硝酸イオン含有液を処理することができるので、亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することができる。
【0069】
(第一の実施形態C)
図4に示すバイオリアクタ1は、収容される液体の液面よりも下部に開口部を備える二つの容器25aと25bがイオン交換膜6を介して開口部で連結されてU字型の容器25が形成され、一方の容器25aを密閉構造として培養槽7とし、他方の容器25bも密閉して対電極槽8としている。この場合、培養液4と電解液4aがイオン交換膜6を介して接触すると共に、培養槽7の培養液4の液面よりも上部の空間と対電極槽8の電解液4aの液面よりも上部の空間とが容器25自体のU字型構造によって隔てて配置される。図4に示すバイオリアクタ1によれば、図2に示すバイオリアクタ1と同様、活性化された窒素代謝微生物2を含む培養液4中で亜硝酸イオン含有液を処理することができるので、亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することができる。
【0070】
(第一の実施形態D)
図5に示すバイオリアクタ1は、収容される液体の液面よりも下部に開口部を備える二つの容器26aと26bがイオン交換膜6を介して開口部で連結されてH字型の容器26が形成され、一方の容器26aを密閉構造として培養槽7とし、他方の容器26bも密閉して対電極槽8としている。この場合にも、培養液4と電解液4aがイオン交換膜6を介して接触すると共に、培養槽7の培養液4の液面よりも上部の空間と対電極槽8の電解液4aの液面よりも上部の空間とが容器26自体のH字型構造によって隔てて配置される。図5に示すバイオリアクタ1によれば、図2に示すバイオリアクタ1と同様、活性化された窒素代謝微生物2を含む培養液4中で亜硝酸イオン含有液を処理することができるので、亜硝酸イオン含有液の亜硝酸イオン濃度を効率よく低減することができる。
【0071】
<第二の実施形態>
第二の実施形態にかかる窒素代謝微生物の活性化方法は、亜硝酸還元能を有する亜硝酸還元微生物2a及び亜硝酸酸化能を有する亜硝酸酸化微生物2bの少なくともいずれか一方の窒素代謝微生物2と有機物5と酸化還元物質3とを含む培養液4に作用電極9を浸し、培養液4に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が作用電極9へ電位を印加していない場合よりも向上する電位を作用電極9に印加しながら窒素代謝微生物2を培養するようにしている。本実施形態では、培養液4にイオン交換膜6を介して対電極9を接触させるようにしている。つまり、第一の実施形態における窒素代謝微生物の活性化方法とは、電解液4aを用いることなく対電極10を直接イオン交換膜6に接触させている点が異なっている。しかしながら、第一の実施形態のように電解液4aを用いずとも、作用電極9と対電極10との間でイオン交換膜6を介してイオン電流は流れるので、第二の実施形態にかかる窒素代謝微生物の活性化方法によれば、第一の実施形態と同様に作用電極9の電位を制御して、同様の効果を得ることが可能である。
【0072】
第二の実施形態にかかる窒素代謝微生物の活性化方法を利用したバイオリアクタの構成を図6に例示する。図6に示すバイオリアクタ1は、イオン交換膜6を少なくとも一部に備える密閉構造の容器50内に作用電極9と参照電極11が配置され、容器50の外側に対電極10が配置され、容器50に培養液4が収容されると共に作用電極9と参照電極11が培養液4に浸され、容器50のイオン交換膜6は容器50に培養液4が収容されたときに少なくともその一部がイオン交換膜6と接触しうる位置に備えられ、イオン交換膜6の培養液4の接触面とは反対側の面の少なくとも一部に対電極10が接触して配置されているものとしている。図6に示すバイオリアクタ1では、容器50の培養液4の液面よりも下部に開口部50aが設けられ、開口部50aがイオン交換膜6で塞がれ、容器50の外側のイオン交換膜6の表面の少なくとも一部に対電極10が接触して配置されているものとしている。つまり、図6に示すバイオリアクタ1では、容器50全体が培養槽7として機能することとなる。
【0073】
したがって、図6に示すバイオリアクタ1によれば、容器50を密閉構造としているので、第一の実施形態と同様、培養槽7の嫌気性雰囲気を制御し易い。
【0074】
尚、図6に示すバイオリアクタ1においては、第一の実施形態と同様に、被処理液導入部18、処理液排出手段16及び窒素ガス排出手段15を備えるようにしているが、上記の通り、被処理液導入方法、処理液排出方法、窒素ガス排出方法はこれらの手段を利用したものには限定されない。また、第一の実施形態と同様に、培養液4に窒素代謝微生物2を担持し得る担体を入れるようにしてもよいし、処理液排出手段16から排出される前に処理液と培養液4とが通過する位置に、担体を処理液及び培養液4から分離する濾過膜または濾過装置を備えるようにして、処理液排出手段16から排出される処理液と培養液4から担体が濾過分離されるようにしてもよい。さらに、第一の実施形態と同様、培養液4に物質を添加・供給する手段を設けるようにしてもよい。
【0075】
以下、図6に示すバイオリアクタ1の詳細について説明する。但し、以下に説明する以外の構成については、第一の実施形態と実質的に同一であり、説明は省略する。
【0076】
容器50は、イオン交換膜6を少なくとも一部に備える密閉構造としている。容器50の材質としては、例えば、ガラス、プラスチック、絶縁処理を施した金属、コンクリート等が挙げられるがこれらに限定されるものではない。尚、図6では、密閉構造の容器50の培養液4の液面よりも下部に設けられた開口部50aをイオン交換膜6により塞ぐようにしているが、容器50の形態や構造は特に限定されない。例えば容器50全体をイオン交換膜6で形成した袋状の容器としてもよいし、袋状の容器の片面だけをイオン交換膜6で構成してもよいし、一つの面のさらに一部分をイオン交換膜6のみで構成するようにしてもよい。部分的にイオン交換膜6を用いる場合には、その他の部分はガラス等の上記材質で構成してもよいし、イオン交換膜6以外の膜材、例えば培養液4と培養液4中の成分の双方を透過させることがない膜材により構成してもよい。要は、容器50に収容される培養液4が容器50の少なくとも一部を構成するイオン交換膜6と接触しうる構造の容器とすればよい。
【0077】
対電極10は、イオン交換膜6の培養液4との接触面とは反対側の面の少なくとも一部に接触させるようにしている。本実施形態において、対電極10は板状の炭素電極としているが、対電極10の形状と材質はこれに限定されるものではなく、要は、イオン交換膜6との接触が可能な形状であり、且つ作用電極9における酸化還元反応に対して電子の授受を補完する反応を進行させることが可能な材質の電極とすればよい。また、本実施形態では、対電極10の面積をイオン交換膜6の面積よりも大きなものとしてイオン交換膜6全体を対電極10で完全に覆うようにし、イオン交換膜6と対電極10とを接触させるようにしているが、イオン交換膜6の培養液4との接触面とは反対側の面の少なくとも一部に対電極10を接触させればよく、必ずしもイオン交換膜6全体を対電極10で完全に覆うようにしてイオン交換膜6と対電極10とを接触させずともよい。但し、イオン交換膜6全体を対電極10で完全に覆うことで、対電極10をイオン交換膜6の保護材としても機能させることができると共に、培養液4からのイオンの伝達面が増大する結果として、培養液4の電位制御性を高めることができる利点があり、好適である。イオン交換膜6全体を対電極10で完全に覆う方法としては、例えば、容器50の開口部50aの周囲に接着剤を塗布して対電極10を接着することにより、開口部50aを塞ぐイオン交換膜6全体と対電極10とを接触させるようにしてもよいし、容器50の開口部50aの周囲に接着剤を塗布して対電極10の表面の少なくとも一部に塗布形成されたイオン交換膜6を接着することにより、開口部50aをイオン交換膜6で塞ぎつつ、開口部50aを塞ぐイオン交換膜6全体と対電極10とを接触させるようにしてもよい。イオン交換膜6を塗布形成するための薬剤としては、例えばナフィオン分散液が挙げられるが、これに限定されるものではない。また、対電極10の表面にナフィオン分散液を塗布し、ナフィオン分散液が乾燥する前にイオン交換膜6を貼り付けるようにしてもよい。この場合には、イオン交換膜6の対電極10の表面への接着性と接触性とを十分なものとすることができる。
【0078】
ここで、対電極10は多孔質体とすることが好適である。この場合には、イオン交換膜6と対電極10との接触面で発生したガスを接触面とは反対側の面に通過させやすくなる。尚、対電極10を多孔質体とし、ナフィオン分散液を用いてイオン交換膜6を貼り付けることで、ナフィオン分散液の多孔質体の孔への侵入によりイオン交換膜6と対電極10との接触面積を増大させて電気化学反応をより進行させやすくすることができ、好適である。
【0079】
上述の形態は本発明の好適な形態の一例ではあるがこれに限定されるものではなく本発明の要旨を逸脱しない範囲において種々変形実施可能である。
【0080】
例えば、図7に示すように、培養液4と電解質4aをイオン交換膜6ではなく、イオンや微生物を一切透過させることのない不透過部材40で隔て、あるいは培養槽7と対電極槽8を別の容器で形成し、塩橋41(寒天等にKCl等の飽和電解質溶液を入れたもの)を介して培養液4と電解質4aを接触(液絡)させるようにしてもよい。この場合にも、塩橋41によってイオン電流の流れが許容されると共に、酸化還元物質3の対電極槽8への透過を防ぐことができるので、上述の実施形態と同様の効果が得られる。
【0081】
また、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aを含む培養液4中で亜硝酸イオン含有液を処理する場合、亜硝酸イオン含有液には、硝酸イオンが含まれていてもよい。この場合には、亜硝酸還元微生物2aにより、亜硝酸イオンと硝酸イオンの双方を効率よく窒素ガスに還元することができる。また、亜硝酸イオン含有液には、窒素代謝微生物2の炭素源となる有機物5が含まれていてもよい。この場合、亜硝酸イオン含有液に含まれる有機物5を窒素代謝微生物2が炭素源として利用して分解しながら、亜硝酸イオンの還元または酸化を行うことができ、亜硝酸イオン含有液に含まれる亜硝酸イオン濃度の低減と同時にTOC濃度の低減を図ることもできる。
【0082】
また、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aまたは亜硝酸酸化微生物2bを利用して、亜硝酸生成微生物により生成される亜硝酸イオンを酸化または還元してその濃度を低減することで、亜硝酸生成微生物が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、亜硝酸生成微生物を良好に培養することが可能となる。例えば、硝酸イオンを最終電子受容体として硝酸呼吸を行うことにより亜硝酸イオンを生成する硝酸呼吸能を有する微生物は自然界に広く存在している。具体的には、例えば、アルカリゲネス(Alcaligenes)属、アグロバクテリウム(Agrobacterium)属、アクアスピリラム(Aquaspirillum)属、アゾスピリラム(Azospirillum)属、バチルス(Bacillus)属、ブラストバクター(Blastobacter)属、ブラディリゾビウム(Bradyrhizobium)属、ブランハメラ(Branhamella)属、クロモバクテリウム(Chromobacterium)属、サイトファーガ(Cytophaga)属、エンテロバクター(Enterobacter)属、エシェリキア(Escherichia)属、フラボバクテリウム(Flavobacterium)属、フレキシバクター(Flexibacter)属、ハロバクテリウム(Halobacterium)属、ヒポミクロビウム(Hyphomicrobium)属、キンゲラ(Kingella)属、クレブシエラ(Klebsiella)属、リソバクター(Lysobacter)属、ネイセイリア(Neisseiria)属、パラコッカス(Paracoccus)属、プロピオニバクテリウム(Propionibacterium)属、シュードモナス(Pseudomonas)属、リゾビウム(Rhizobium)属、ウォリネラ(Wolinella)属、ロドシュードモナス(Rhodopseudomonas)属、チオバチルス(Thiobacillus)属、ニトロソモナス(Nitrosomonas)属、チオミクロスピラ(Thiomicrospira)属、チオスフェラ(Thiosphera)属等が挙げられる。ここで、大腸菌(Escherichia coli)、ブラディリゾビウム ジャポニカム(Bradyrhyzobium japonicum)、クレブシエラ プネウモニア(Klebsiella pneumonia)、エンテロバクター エアロゲネス(Enterobacter aerogenes)、チオバチルス チオパラス(Thiobacillus thioparus)、リゾバクター アンチビオティカム(Lysobacter antibioticum)等は、硝酸呼吸能を有する微生物の中でも特に、硝酸呼吸により培養液に亜硝酸イオンが蓄積されやすい微生物であり、亜硝酸イオンの生物毒性によって、生育が阻害されやすく、培養し難い。しかしながら、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aまたは亜硝酸酸化微生物2bを利用してこれらの微生物により生成される亜硝酸イオンを酸化または還元してその濃度を低減することで、これらの微生物が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、従来は培養が難しかったこれらの微生物を良好に培養(集積培養)することが可能となる。
【0083】
特に、本発明の窒素代謝微生物の活性化方法により亜硝酸酸化微生物2bを活性化させた場合には、この微生物の機能により、亜硝酸イオンを硝酸イオンに酸化することができるので、この硝酸イオンを上記硝酸呼吸能を有する微生物に供給して硝酸呼吸を行わせ、硝酸呼吸により生じた亜硝酸イオンを亜硝酸酸化微生物2bに供給して亜硝酸イオンを硝酸イオンに酸化させるといった、いわば硝酸イオンと亜硝酸イオンの循環経路を確立することができる。したがって、亜硝酸酸化微生物2bと共に硝酸呼吸能を有する微生物を効率よく培養することができる。本発明の窒素代謝微生物の活性化方法により亜硝酸還元微生物2aを活性化させた場合には、上記循環経路は確立されないものの、硝酸イオンを定期的に又は随意に培養液に供給することで、硝酸呼吸能を有する微生物に硝酸呼吸を行わせて、亜硝酸還元微生物2aと共に培養することができる。
【0084】
また、亜硝酸生成微生物は、単独で硝酸イオンを亜硝酸イオン経由で窒素に変換する菌(脱窒菌)としてもよい。即ち、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aまたは亜硝酸酸化微生物2bを利用して、単独で硝酸イオンを亜硝酸イオン経由で窒素に変換する菌(脱窒菌)により硝酸イオンが還元されて生成される亜硝酸イオンを還元または酸化してその濃度を低減することで、脱窒菌が自ら生成した亜硝酸イオンの毒性によってその生育が阻害されることがなく、脱窒菌を良好に培養することが可能となる。したがって、従来は培養が難しかった一部の脱窒菌を良好に培養(集積培養)することが可能となる。また、培養液4に単独で硝酸イオンを亜硝酸イオン経由で窒素に変換する菌(脱窒菌)と亜硝酸還元微生物2aを含ませ、本発明の窒素代謝微生物の活性化方法により活性化された亜硝酸還元微生物2aを利用して亜硝酸還元反応を促進させることで、脱窒菌の生育を良好なものとして、さらには従来は培養が難しかった一部の脱窒菌を良好に培養し得ることによって、脱窒プロセス全体を促進し得るので、脱窒反応を利用した硝酸イオン及び亜硝酸イオンを含む廃水等の水処理プロセスの効率化を図ることも可能となる。
【実施例】
【0085】
以下に本発明の実施例を説明するが、本発明はこれら実施例に限られるものではない。
【0086】
尚、本実施例における電位は、全て銀・塩化銀電極電位を基準とするものである。
【0087】
<実験装置>
図8に示す電気培養装置1により実験を行った。培養槽7としての容器20は250mL容のガラスバイアル瓶(Duran製)とした。培養液4は200mL収容した。容器20には蓋30をした。蓋30の上面30aにはシリコーンゴム栓を設けて、配線や電極、管と通した際の密閉性を確保した。
【0088】
対電極槽8としての小容器21は、イオン交換膜6を成型して袋状(以下、袋21と呼ぶ)とした。実験で用いた小容器21の形態を図9に示す。具体的には、陽イオン交換膜(デュポン製、ナフィオンK)をヒートシーラーで熱圧着により加工して上部が開口した袋状の容器21とし、袋21の内部には電解液4aを収容すると共に対電極10を収容して電解液4aに浸した。そして、対電極10と電位制御装置12を結線するための配線31をガス排出管22に通した。ガス排出管22は両端が開口されており、一端を小容器21の内部に、他端を容器20の外側に配置するようにして、小容器21内で発生するガスが容器20の外側に排出されるようにした。袋状の小容器21の上部の開口部は、シリコン接着剤32で塞いだ。
【0089】
小容器21と作用電極9とを培養液4に浸漬し、小容器21のガス排出管22と作用電極9の配線は蓋30に設けたシリコーンゴム栓に通して容器20の外側に引き出した。参照電極11(RE-1B, ビー・エー・エス株式会社)は容器20の外側からシリコーンゴム栓に通して差し込むことにより培養液4と接触させた。処理液排出管16は容器20の外側からシリコーンゴム栓に通して差し込むことによりその一端を培養液4と接触させた。作用電極9と対電極10と参照電極11とを3電極式の電位制御装置(ポテンシオスタット)12に結線して、培養液4の電位を厳密に制御可能とした。処理液排出管16の他端は注射器と接続して培養液4を採取可能とした。
【0090】
<培養液>
培養槽7には、以下の組成の培養液を収容した。尚、以下の組成のうち、KHCO3とプロピオン酸が微生物2の炭素源として機能する。
[培養液組成]
・KHCO3 :500ppm
・KH2PO4 :27ppm
・MgSO4・7H2O :300ppm
・CaCl2・2H2O :180ppm
・プロピオン酸 :1mM
・微量元素(Zn、Co、Mn、Cu、Mo、Ni、Se、B、Fe) :1mL
【0091】
<電解液>
後述する酸化還元物質3(アントラキノン2,6−ジスルホン酸:AQDS)を含まないことを除いて培養液4と同一成分とした。
【0092】
(実施例1)
アンモニウムイオンの酸化還元特性について検討した。
【0093】
培養液4にアンモニウムイオンとしてNH4Clを10mM添加し、作用電極9を炭素電極(BAS社製)とし、対電極10を白金棒電極(自作)として、上記実験装置を用いてサイクリックボルタンメトリーにより酸化還元特性を測定した(掃引速度100mV/s)。結果を図10に示す。図10に示される結果から、アンモニウムイオンは、−1.5V〜+1.5Vの範囲では酸化還元されないことが明らかとなった。
【0094】
(実施例2)
亜硝酸イオンの酸化還元特性について検討した。
【0095】
培養液4に亜硝酸イオンとしてKNO2を10mM添加し、作用電極9を炭素電極(BAS社製)とし、対電極10を白金棒電極(自作)として、上記実験装置を用いてサイクリックボルタンメトリーにより酸化還元特性を測定した(掃引速度100mV/s)。結果を図11に示す。図11に示される結果から、亜硝酸イオンは、+0.7V以上で酸化されるが、−1.5V〜+0.7V未満の範囲では酸化還元されないことが明らかとなった。
【0096】
(実施例3)
培養液4に、微生物2として(九十九里、2009年04月18日)から採取した水田土壌を 2g、酸化還元物質3としてアントラキノン2,6−ジスルホン酸(AQDS)を2mM添加した。作用電極9と対電極10は炭素電極とした。また、培養液4にはスポンジ(東和産業株式会社製、商品名:ピカるちゃんキューブ)を200mLの培養液4に対して10mm×10mm×15mmに切ったスポンジ16個を添加して、試験期間中の培養液4の抜き取りの際の微生物2の流出や減少を抑制した。
【0097】
培養液4には、亜硝酸イオン源としてKNO2を50ppm添加し、アンモニウムイオン源として(NH4)2SO4を50ppm添加した。また、試験期間中には、定期的にKNO2、(NH4)2SO4、炭素源であるKHCO3とプロピオン酸、微量元素を添加するようにした。KHCO3、プロピオン酸、微量元素は定期的に初期値と同一量を添加した(18日、40日、60日)。アンモニウムイオンは5日後に約100ppmに設定した後は添加しなかった。亜硝酸イオンは約5日ごとにサンプリングおよび測定を行い、低下が見られたら添加する方針で運転を行い、段階的にKNO2負荷を上昇させた。具体的には、5日目:50ppm, 5日目〜20日目:17.5ppm, 21日目〜32日目35ppm、33日目〜48日目:70ppm、49日目以降210ppmとし、56日目のみは525ppmとして大幅に負荷を上昇させた。
【0098】
蓋30に備えられたシリコーンゴム栓に注射針を2本刺し、一方の注射針からN2ガスを1時間通気することにより、培養液4の液面上部のヘッドスペースをN2ガスで置換した。培養液4は攪拌子34で攪拌させ、37℃で培養試験を実施した。
【0099】
培養試験の条件は以下の通りとした。
・通電無し(73mV)
・+0.2V
・+0.6V
・−0.6V
【0100】
試験期間中の培養液のアンモニウムイオン濃度、亜硝酸イオン濃度、硝酸イオン濃度はイオンクロマトグラフィー(製品名:ICS-1500、メーカー:DIONEX)、TOC濃度はTOCアナライザー(型番TNC-6000、装置名Automatic TOC analyzer, メーカー:Toray)にて測定した。
【0101】
通電無しにおける試験結果を図12に示し、+0.2Vにおける試験結果を図13に示し、+0.6Vにおける試験結果を図14に示し、−0.6Vにおける試験結果を図15に示す。尚、図12〜図15中、◆がアンモニウムイオン濃度、×がTOC濃度、■が硝酸イオン濃度、▲が亜硝酸イオン濃度を表している。
【0102】
通電無しの条件及び+0.2Vの場合には、添加した亜硝酸イオンの量に応じて亜硝酸イオンの濃度が増加するのみであった。これに対し、+0.6Vでは亜硝酸イオン濃度の減少に対応して、硝酸イオン濃度が増加する傾向が見られた。また、−0.6Vでは亜硝酸イオン濃度の減少に対応して、培養液4からの顕著な泡発生がみられた。これらの結果から、+0.6Vでは培養液4中の亜硝酸酸化細菌が活性化して亜硝酸イオンが硝酸イオンに酸化され、−0.6Vでは亜硝酸還元細菌が活性化して亜硝酸イオンが窒素ガスに還元されていることが考えられた。
【0103】
(実施例4)
培養液中の菌数、亜硝酸還元反応を担う遺伝子であるnirK及びnirSについて、遺伝子学的に解析を実施した。
【0104】
<培養液からのDNA抽出>
試験終了後に培養液4を50mL採取し、遠心分離して菌体を回収した。そして回収した菌体からPowerMicrobial Maxi DNA isolation kit (MO BIO)を用いてゲノムDNAの抽出を行い、最終的に2mlの精製DNAを得た。また、参照データとして、試験開始前の培養液4を50mL採取して、上記と同様、ゲノムDNAの抽出を行った。
【0105】
<微生物の定量>
培養液中に含まれる亜硝酸還元(脱窒プロセス)に関わる微生物の定量を行うために、Light Cycler ST300(Roche)を用いてリアルタイムPCRを行った。
【0106】
まず、培養液に含まれる全菌量を測定するために、LightCycler TaqMan Master(Roche)を用い、Taq−Man probe法により16Sr DNAを定量した。
【0107】
亜硝酸還元反応を担う遺伝子であるnirK、nirS遺伝子は、Light Cycler Fast start DNA Master SYBR Green I (Roche)を用いSYBR Green法により定量した。
【0108】
定量はSecond derivative maximum法によりCp値(Crossing point、蛍光強度増加曲線の二次導関数が最大に達した点)を算出し、全菌数については検量線と照らし合わせて絶対定量を行い、nirK、nirSについては通電せずに培養を行った場合を1とした相対定量を行った。
【0109】
検量線はリアルタイムPCRに用いたプライマーで増幅した大腸菌JM109株の16Sr RNA遺伝子をクローニングしたプラスミド(pT7Blue)を標準物質として10倍希釈の希釈系列をサンプルとしてリアルタイムPCRを行うことにより作成した。
【0110】
各実験に用いたプライマー及びプローブ、PCR条件は以下の通りとした。
【0111】
(1)全菌
プライマー及びプローブは以下の通りとした。
・Uni340F:CCTACGGGRBGCASCAG(配列番号1)
・Uni806R:GGACTACNNGGGTATCTAAT(配列番号2)
・Uni516F (TaqMan probe):TGYCAGCMGCCGCGGTAAHACVNRS(配列番号3)
(5'6-FAM、3'TAMRA)
PCR条件は、以下の通りとし、(ii)〜(iv)を40サイクル実施した。
・(i)95℃10分→(ii)95℃10秒→(iii)50℃45秒→(iv)72℃1秒
【0112】
(2)nirK遺伝子
プライマーは以下の通りとした。
・nirK876 : ATYGGCGGVAYGGCGA(配列番号4)
・nirK1040 : GCCTCGATCAGRTTRTGGTT(配列番号5)
PCR条件は、以下の通りとし、(ii)〜(iv)を32サイクル実施した。
・(i)95℃10分→(ii)95℃10秒→(iii)60℃30秒→(iv)72℃30秒
【0113】
(3)nirS遺伝子
プライマーは以下の通りとした。
・nirSCd3aF : AACGYSAAGGARACSGG(配列番号6)
・nirSR3cd : GASTTCGGRTGSGTCTTSAYGAA(配列番号7)
PCR条件は、以下の通りとし、(ii)〜(iii)を40サイクル実施した。
・(i)95℃10分→(ii)95℃10秒→(iii)65℃20秒
【0114】
全菌の定量結果を図16に示し、nirK遺伝子の定量結果を図17に示し、nirS遺伝子の定量結果を図18に示す。
【0115】
図16に示される結果から、通電した全ての場合において、通電無しの場合と比較して菌数が増大することが明らかとなり、特に−0.6Vにおいて菌数の増大が顕著であった。
【0116】
また、図17及び図18に示される結果から、電した全ての場合において、通電無しの場合と比較してnirK及びnirSの増加が見られ、特に−0.6Vにおいてその傾向が顕著であった。
【0117】
(実施例5)
試験終了後の培養液の微生物叢解析を実施した。
【0118】
PCRにより16S rRNA遺伝子のV3領域(約200bp)を増幅した。PCRはEx-taq polymerase (Takara bio, Japan)及び以下のEscherichia coli由来16S rRNA 遺伝子 (EMBL/GenBank/DDBJ accession number X80721) の配列を元に作成した以下のプライマーを用いて行った。
・forward primer 5’-CCTACGGGAGGCAGCAG-3’
(Escherichia coli 由来16S rRNA 遺伝子における341番目に相当、配列番号8)
・reverse primer 5’-ATTACCGCGGCTGCTGG-3’
(Escherichia coli 由来16S rRNA 遺伝子における517番目に相当、配列番号9)
【0119】
PCRにより増幅した約200bp の16S rDNAの部分DNA断片をアガロース電気泳動により分離、精製した。精製DNA断片はpT7Blue -T vector (Novagen) に挿入し、JM109の形質転換を行った。得られた形質転換体をランダムに約50個取得し、16S rRNA遺伝子クローンの塩基配列解析を行った。塩基配列解析はABI PRISM BigDye terminator v3.0 cycle sequencing kitとABI PRISM 310 Genetic Analyzer (Applied Biosystems) を使用し、dideoxy nucleotide chain termination法により決定した。得られた16S rRNA遺伝子の塩基配列について国際塩基配列データベース (GeneBank/EMBL/DDBJ) からDNA塩基配列データベースに対する相同性検索を行い、類縁微生物の推定を行った。
【0120】
解析結果を図19に示す。植菌試料から検出された微生物種は37種と非常に雑多であったにも関わらず、通電しながら培養を行うことで、ある種の微生物が優占化する傾向が見られた。具体的には、−0.6Vにおいては、シュードモナス(Pseudomonas)属、アリシクリフィルス(Alicycliphilus)属及びティシエレラ(Tissierella)属の微生物が優占化している傾向が見られ、これらの微生物の優占化によって亜硝酸イオンを窒素ガスに還元する速度が促進されたものと考えられた。また、+0.6Vでは、シュードモナス(Pseudomonas)属、ブルクホルデリア(Burkholderia)属及びシュードキサントモナス(Pseudoxanthomonas)属の微生物が優占化している傾向が見られた。ここで、シュードモナス(Pseudomonas)属及びシュードキサントモナス(Pseudoxanthomonas)属の微生物は、硝酸還元能及び亜硝酸還元能を有することが知られており、ブルクホルデリア(Burkholderia)属の微生物は亜硝酸酸化能を有することが知られていることから、+0.6Vによる亜硝酸酸化反応の促進は、+0.6Vにおいては、シュードモナス(Pseudomonas)属及びシュードキサントモナス(Pseudoxanthomonas)属の微生物の生育は促進されるものの硝酸還元及び亜硝酸還元活性は弱く、ブルクホルデリア(Burkholderia)属の微生物の生育が促進されて亜硝酸酸化活性が向上し、全体として亜硝酸酸化反応が促進されたものと考えられる。
【0121】
以上の結果から、本発明の窒素代謝微生物の活性化方法により、亜硝酸還元能を有する微生物または亜硝酸酸化能を有する微生物を選択的に増殖させて培養液中に優占化させて存在させることができ、これにより培養液の亜硝酸イオン処理能力(還元または酸化能力)を大きく向上できることが明らかとなった。
【産業上の利用可能性】
【0122】
本発明の窒素代謝微生物の活性化方法を利用することで、土壌サンプル等のように雑多な微生物を含む試料から、亜硝酸還元微生物または亜硝酸酸化微生物を選択的に増殖させて、集積的に培養を行うことができる。したがって、通常の培養方法では増殖させにくい微生物を増殖させやすいものとして、新たな機能性微生物の探索に資する。即ち、本発明は、自然界に存在する膨大な微生物資源から新規なあるいは従来よりも優れた機能を有する微生物の探索に貢献し得るものである。
【符号の説明】
【0123】
1 バイオリアクタ
2 窒素代謝微生物
2a 亜硝酸還元微生物
2b 亜硝酸酸化微生物
3 酸化還元物質
4 培養液
4a 電解液
5 有機物
6 イオン交換膜
7 培養槽
8 対電極槽
9 作用電極
10 対電極
12 定電位設定装置
15 窒素ガス排出手段
16 処理液排出手段
18 被処理液導入部
【特許請求の範囲】
【請求項1】
亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と有機物と酸化還元物質とを含む培養液に電極を浸し、前記培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が前記電極へ電位を印加していない場合よりも向上する電位を前記電極に印加しながら前記窒素代謝微生物を培養することを特徴とする窒素代謝微生物の活性化方法。
【請求項2】
前記培養液にイオン交換膜を介して電解液を接触させ、前記電極と対をなす電極を前記電解液に浸漬する請求項1に記載の窒素代謝微生物の活性化方法。
【請求項3】
前記培養液にイオン交換膜を介して前記電極と対をなす電極を接触させる請求項1に記載の窒素代謝微生物の活性化方法。
【請求項4】
前記電極に印加する電位を、亜硝酸イオンの低減速度が向上する結果として窒素ガスの生成速度が向上する電位とすることにより、前記亜硝酸還元微生物を活性化する請求項1〜3のいずれか1つに記載の窒素代謝微生物の活性化方法。
【請求項5】
前記電位を、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位とする請求項4に記載の窒素代謝微生物の活性化方法。
【請求項6】
前記電極に印加する電位を、亜硝酸イオンの低減速度が向上する結果として硝酸イオン生成速度が向上する電位とすることにより、前記亜硝酸酸化微生物を活性化する請求項1〜3のいずれか1つに記載の窒素代謝微生物の活性化方法。
【請求項7】
前記電位を、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とする請求項6に記載の窒素代謝微生物の活性化方法。
【請求項8】
請求項1〜7のいずれか1つに記載の方法により活性化された窒素代謝微生物を含む培養液中で亜硝酸イオン含有液を処理することを特徴とする亜硝酸イオン含有液の処理方法。
【請求項9】
請求項1〜7のいずれか1つに記載の方法により活性化された窒素代謝微生物を含む培養液中に亜硝酸イオンを生成する亜硝酸生成微生物を添加し、前記亜硝酸生成微生物により生成された亜硝酸イオンを前記活性化された窒素代謝微生物に還元または酸化させて低減し、亜硝酸イオンの毒性による生育阻害を回避しながら前記亜硝酸生成微生物を培養することを特徴とする亜硝酸生成微生物の培養方法。
【請求項10】
イオン交換膜によって仕切られた対電極槽及び密閉構造の培養槽と、前記培養槽に収容された培養液と、前記対電極槽に収容された電解液と、前記培養液に浸された作用電極と、前記電解液に浸された対電極と、前記作用電極と前記対電極とが結線されて前記作用電極と前記対電極との間に電位差を与えて前記作用電極の電位を設定する定電位設定装置と、前記培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、前記培養槽から処理液を排出する処理液排出手段とを有し、前記培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、前記培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が前記作用電極に電位を印加しない場合よりも向上する電位が前記作用電極に印加されながら前記窒素代謝微生物が培養されるものとしたことを特徴とするバイオリアクタ。
【請求項11】
培養槽としての密閉構造の容器と、前記容器に収容可能な対電極槽としての密閉構造の小容器と、前記培養槽に収容された培養液と、前記対電極槽に収容された電解液と、前記培養液に浸された作用電極と、前記電解液に浸された対電極と、前記作用電極と前記対電極とが結線されて前記作用電極と前記対電極との間に電位差を与えて前記作用電極の電位を設定する定電位設定装置と、前記培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、前記培養槽から処理液を排出する処理液排出手段とを有し、前記小容器は前記培養液と接触する位置の少なくとも一部にイオン交換膜を備えるものとし、前記培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、前記培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が前記作用電極に電位を印加しない場合よりも向上する電位が前記作用電極に印加されながら前記窒素代謝微生物が培養されるものとしたことを特徴とするバイオリアクタ。
【請求項12】
イオン交換膜を少なくとも一部に備える容器と、前記容器に収容された培養液と、前記培養液に浸された作用電極と、前記イオン交換膜の前記容器の外側の面の少なくとも一部に接触している対電極と、前記作用電極と前記対電極とが結線されて前記作用電極と前記対電極との間に電位差を与えて前記作用電極の電位を設定する定電位設定装置と、前記培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、前記培養槽から処理液を排出する処理液排出手段とを有し、前記イオン交換膜は前記容器の前記培養液と接触する位置に備えるものとし、前記培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、前記培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が前記作用電極に電位を印加しない場合よりも向上する電位が前記作用電極に印加されながら前記窒素代謝微生物が培養されるものとしたことを特徴とするバイオリアクタ。
【請求項13】
前記作用電極に印加される電位が、亜硝酸イオンの低減速度が向上する結果として窒素ガスの生成速度が向上する電位とされて前記亜硝酸還元微生物が活性化され、亜硝酸イオンが還元されて生じた窒素ガスを前記培養槽から排出する窒素ガス排出手段が備えられている請求項10〜12のいずれか1つに記載のバイオリアクタ。
【請求項14】
前記電位は、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位である請求項13に記載のバイオリアクタ。
【請求項15】
前記作用電極に印加される電位が、亜硝酸イオンの低減速度が向上する結果として硝酸イオン生成速度が向上する電位とされて前記亜硝酸酸化微生物が活性化されている請求項10〜12のいずれか1つに記載のバイオリアクタ。
【請求項16】
前記電位は、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とする請求項13に記載のバイオリアクタ。
【請求項1】
亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と有機物と酸化還元物質とを含む培養液に電極を浸し、前記培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が前記電極へ電位を印加していない場合よりも向上する電位を前記電極に印加しながら前記窒素代謝微生物を培養することを特徴とする窒素代謝微生物の活性化方法。
【請求項2】
前記培養液にイオン交換膜を介して電解液を接触させ、前記電極と対をなす電極を前記電解液に浸漬する請求項1に記載の窒素代謝微生物の活性化方法。
【請求項3】
前記培養液にイオン交換膜を介して前記電極と対をなす電極を接触させる請求項1に記載の窒素代謝微生物の活性化方法。
【請求項4】
前記電極に印加する電位を、亜硝酸イオンの低減速度が向上する結果として窒素ガスの生成速度が向上する電位とすることにより、前記亜硝酸還元微生物を活性化する請求項1〜3のいずれか1つに記載の窒素代謝微生物の活性化方法。
【請求項5】
前記電位を、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位とする請求項4に記載の窒素代謝微生物の活性化方法。
【請求項6】
前記電極に印加する電位を、亜硝酸イオンの低減速度が向上する結果として硝酸イオン生成速度が向上する電位とすることにより、前記亜硝酸酸化微生物を活性化する請求項1〜3のいずれか1つに記載の窒素代謝微生物の活性化方法。
【請求項7】
前記電位を、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とする請求項6に記載の窒素代謝微生物の活性化方法。
【請求項8】
請求項1〜7のいずれか1つに記載の方法により活性化された窒素代謝微生物を含む培養液中で亜硝酸イオン含有液を処理することを特徴とする亜硝酸イオン含有液の処理方法。
【請求項9】
請求項1〜7のいずれか1つに記載の方法により活性化された窒素代謝微生物を含む培養液中に亜硝酸イオンを生成する亜硝酸生成微生物を添加し、前記亜硝酸生成微生物により生成された亜硝酸イオンを前記活性化された窒素代謝微生物に還元または酸化させて低減し、亜硝酸イオンの毒性による生育阻害を回避しながら前記亜硝酸生成微生物を培養することを特徴とする亜硝酸生成微生物の培養方法。
【請求項10】
イオン交換膜によって仕切られた対電極槽及び密閉構造の培養槽と、前記培養槽に収容された培養液と、前記対電極槽に収容された電解液と、前記培養液に浸された作用電極と、前記電解液に浸された対電極と、前記作用電極と前記対電極とが結線されて前記作用電極と前記対電極との間に電位差を与えて前記作用電極の電位を設定する定電位設定装置と、前記培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、前記培養槽から処理液を排出する処理液排出手段とを有し、前記培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、前記培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が前記作用電極に電位を印加しない場合よりも向上する電位が前記作用電極に印加されながら前記窒素代謝微生物が培養されるものとしたことを特徴とするバイオリアクタ。
【請求項11】
培養槽としての密閉構造の容器と、前記容器に収容可能な対電極槽としての密閉構造の小容器と、前記培養槽に収容された培養液と、前記対電極槽に収容された電解液と、前記培養液に浸された作用電極と、前記電解液に浸された対電極と、前記作用電極と前記対電極とが結線されて前記作用電極と前記対電極との間に電位差を与えて前記作用電極の電位を設定する定電位設定装置と、前記培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、前記培養槽から処理液を排出する処理液排出手段とを有し、前記小容器は前記培養液と接触する位置の少なくとも一部にイオン交換膜を備えるものとし、前記培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、前記培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が前記作用電極に電位を印加しない場合よりも向上する電位が前記作用電極に印加されながら前記窒素代謝微生物が培養されるものとしたことを特徴とするバイオリアクタ。
【請求項12】
イオン交換膜を少なくとも一部に備える容器と、前記容器に収容された培養液と、前記培養液に浸された作用電極と、前記イオン交換膜の前記容器の外側の面の少なくとも一部に接触している対電極と、前記作用電極と前記対電極とが結線されて前記作用電極と前記対電極との間に電位差を与えて前記作用電極の電位を設定する定電位設定装置と、前記培養槽に亜硝酸イオン含有液を導入する被処理液導入部と、前記培養槽から処理液を排出する処理液排出手段とを有し、前記イオン交換膜は前記容器の前記培養液と接触する位置に備えるものとし、前記培養液には亜硝酸還元能を有する亜硝酸還元微生物及び亜硝酸酸化能を有する亜硝酸酸化微生物の少なくともいずれか一方の窒素代謝微生物と酸化還元物質と有機物とが含まれ、前記培養液に亜硝酸イオンを溶解させたときの亜硝酸イオンの低減速度が前記作用電極に電位を印加しない場合よりも向上する電位が前記作用電極に印加されながら前記窒素代謝微生物が培養されるものとしたことを特徴とするバイオリアクタ。
【請求項13】
前記作用電極に印加される電位が、亜硝酸イオンの低減速度が向上する結果として窒素ガスの生成速度が向上する電位とされて前記亜硝酸還元微生物が活性化され、亜硝酸イオンが還元されて生じた窒素ガスを前記培養槽から排出する窒素ガス排出手段が備えられている請求項10〜12のいずれか1つに記載のバイオリアクタ。
【請求項14】
前記電位は、銀・塩化銀電極電位基準で−0.6Vを含んで−0.6Vよりもマイナス側に大きな電位である請求項13に記載のバイオリアクタ。
【請求項15】
前記作用電極に印加される電位が、亜硝酸イオンの低減速度が向上する結果として硝酸イオン生成速度が向上する電位とされて前記亜硝酸酸化微生物が活性化されている請求項10〜12のいずれか1つに記載のバイオリアクタ。
【請求項16】
前記電位は、銀・塩化銀電極電位基準で+0.6Vを含んで+0.6Vよりもプラス側に大きな電位とする請求項13に記載のバイオリアクタ。
【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図1】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】




【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図1】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【公開番号】特開2012−50381(P2012−50381A)
【公開日】平成24年3月15日(2012.3.15)
【国際特許分類】
【出願番号】特願2010−195395(P2010−195395)
【出願日】平成22年9月1日(2010.9.1)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成22年3月5日 社団法人日本農芸化学会発行の「大会講演要旨集 2010年度(平成22年度)大会[東京]」に発表
【出願人】(000173809)財団法人電力中央研究所 (1,040)
【Fターム(参考)】
【公開日】平成24年3月15日(2012.3.15)
【国際特許分類】
【出願日】平成22年9月1日(2010.9.1)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成22年3月5日 社団法人日本農芸化学会発行の「大会講演要旨集 2010年度(平成22年度)大会[東京]」に発表
【出願人】(000173809)財団法人電力中央研究所 (1,040)
【Fターム(参考)】
[ Back to top ]

