筋萎縮抑制剤、及びその使用方法
【課題】廃用性筋萎縮を抑制する筋萎縮抑制剤、及びその使用方法を提供する。
【解決手段】筋萎縮抑制剤は、プレニル化フラバノンを有効成分として含有する。プレニル化フラバノンは、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含むことが好ましい。筋萎縮抑制剤の使用方法は、筋萎縮抑制剤を飲食品に配合して摂取させる。
【解決手段】筋萎縮抑制剤は、プレニル化フラバノンを有効成分として含有する。プレニル化フラバノンは、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含むことが好ましい。筋萎縮抑制剤の使用方法は、筋萎縮抑制剤を飲食品に配合して摂取させる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、廃用性筋萎縮を抑制する筋萎縮抑制剤、及びその使用方法に関する。
【背景技術】
【0002】
筋萎縮としては、例えば老化や寝たきりを要因として筋肉が萎縮する筋萎縮(廃用性筋萎縮)が知られ、こうした廃用性筋萎縮を抑制する飲食品が提案されている(特許文献1参照)。特許文献1は、果実ポリフェノールを有効成分として含有する筋萎縮抑制組成物を開示している。同文献1では、リンゴポリフェノールを含有する筋萎縮抑制組成物の実施例が開示されている。ここで、廃用性筋萎縮については、酸化ストレスが要因であるという報告がある(非特許文献1参照)。非特許文献1は、酸化ストレスを抗酸化剤又は鉄キレート剤の投与により防止することで、筋萎縮の進行が抑制できることを報告している。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開2001−89387号公報
【非特許文献】
【0004】
【非特許文献1】体力研究,1993年,No.83,pp.73−81
【発明の概要】
【発明が解決しようとする課題】
【0005】
特許文献1に記載されるリンゴポリフェノールは、抗酸化活性を有するカテキンを含有している。抗酸化活性を有するカテキンは、非特許文献1に記載されるように、酸化ストレスを低減し、その結果、廃用性筋萎縮を抑制すると考えられる。カテキンは、フラバノールの一種であり、このフラバノールはフラボノイドの一種である。
【0006】
フラボノイドに分類される化合物群として、フラバノール以外にフラバノンが知られている。ここで、代表的なフラバノンであるナリンゲニンについても、抗酸化活性を有するため、廃用性筋萎縮を抑制する効果が期待される。ところが、本発明者らは、ナリンゲニンを含有する飲食品を摂取させた場合には、廃用性筋萎縮を抑制する効果が得られないことを確認した。こうした実情の下、本発明は、プレニル基を付加したフラバノンが廃用性筋萎縮を抑制することを見出すことでなされたものである。
【0007】
本発明の目的は、廃用性筋萎縮を抑制する筋萎縮抑制剤、及びその使用方法を提供することにある。
【課題を解決するための手段】
【0008】
上記の目的を達成するために、請求項1に記載の発明の筋萎縮抑制剤は、廃用性筋萎縮を抑制する筋萎縮抑制剤であって、プレニル化フラバノンを有効成分として含有することを特徴とする。
【0009】
請求項2に記載の発明は、請求項1に記載の筋萎縮抑制剤において、前記プレニル化フラバノンが、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含むことを特徴とする。
【0010】
請求項3に記載の発明は、請求項2に記載の筋萎縮抑制剤において、前記プレニル化フラバノンが、オオバギ抽出物由来であることを特徴とする。
請求項4に記載の発明は、請求項3に記載の筋萎縮抑制剤において、前記オオバギ抽出物が、果実より抽出して得られたことを特徴とする。
【0011】
請求項5に記載の発明の筋萎縮抑制剤の使用方法は、請求項1から請求項4のいずれか一項に記載の筋萎縮抑制剤を飲食品に配合して摂取させることを特徴とする。
【発明の効果】
【0012】
本発明によれば、廃用性筋萎縮を抑制する筋萎縮抑制剤、及びその使用方法が提供される。
【図面の簡単な説明】
【0013】
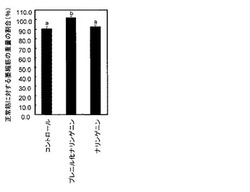
【図1】実施例1及び比較例1における正常筋に対する萎縮筋の重量の割合を示すグラフ。
【図2】実施例1及び比較例1におけるマウスの飼育機関に対する摂餌量を示すグラフ。
【図3】実施例3における正常筋に対する萎縮筋の重量の割合を示すグラフ。
【発明を実施するための形態】
【0014】
本発明の筋萎縮抑制剤、及びその使用方法を具体化した実施形態を詳細に説明する。
本実施形態の筋萎縮抑制剤は、プレニル化フラバノンを有効成分として含有することで、廃用性筋萎縮を抑制する。筋萎縮は、進行性筋萎縮と、廃用性筋萎縮とに分類される。進行性筋萎縮は、四肢等の骨格筋が進行的に萎縮する疾患群である一方、廃用性筋萎縮は、筋肉を使わないことによって生じる筋萎縮である。
【0015】
プレニル化フラバノンの具体例は、プレニル化ナリンゲニン、プレニル化エリオディクティオール、及びプレニル化ヘスペレチンを含む。これらのプレニル化フラバノンは、一種のみを用いてもよいし、複数種のプレニル化フラバノンを組み合わせて用いてもよい。
【0016】
プレニル基の具体例は、ジメチルアリル基(C5)、ゲラニル基(C10)、ファルネシル基(C15)、ゲラニルゲラニル基(C20)、ゲラニルファルネシル基(C25)、ヘキサプレニル基(C30)、オクタプレニル基(C40)、及びデカプレニル基(C50)を含む。
【0017】
プレニル化フラバノンのうち、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールは、オオバギ(大葉木)に含有される成分である。このため、プレニル化ナリンゲニン、又はプレニル化エリオディクティオールを筋萎縮抑制剤に含有させる場合、オオバギを用いることができる。
【0018】
オオバギは、マカランガ・タナリウス(Macaranga tanarius)とも呼ばれる植物であって、トウダイグサ科オオバギ属に属する常緑広葉樹(雌雄異株)である。オオバギは、沖縄、台湾、中国南部、マレー半島、フィリピン、マレーシア、インドネシア、タイなどの東南アジア、オーストラリア北部などに生育している。また、オオバギは、樹木の中でも成長が極めて早く、荒廃地における成長も可能である。このため、プレニル化フラバノンとして、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含む筋萎縮抑制剤によれば、例えば、上述したオオバギを有効利用することができる。
【0019】
オオバギは、プレニル化ナリンゲニンとして、5,7,4´-トリヒドロキシ-3´-ゲラニルフラバノン(5,7,4´-trihydroxy-3´-geranylflavanone)を含む。
オオバギに含まれるプレニル化エリオディクティオールとしては、ニムフェオール−A、ニムフェオール−B、イソニムフェオール−B及びニムフェオール−Cが挙げられる。ニムフェオール−A(nymphaeol−A)は、5,7,3´,4´-テトラヒドロキシ-6-ゲラニルフラバノン(5,7,3´,4´-tetrahydroxy-6-geranylflavanone)である。ニムフェオール−B(nymphaeol−B)は、5,7,3´,4´-テトラヒドロキシ-2´-ゲラニルフラバノン(5,7,3´,4´-tetrahydroxy-2´-geranylflavanone)である。イソニムフェオール−B(isonymphaeol−B)は、5,7,3´,4´-テトラヒドロキシ-5´-ゲラニルフラバノン(5,7,3´,4´-tetrahydroxy-5´-geranylflavanone)である。ニムフェオール−C(nymphaeol−C)は、5,7,3´,4´-テトラヒドロキシ-6-(3´´´,3´´´-ジメチルアリル)-2´-ゲラニルフラバノン(5,7,3´,4´-tetrahydroxy-6-(3´´´,3´´´-dimethylallyl)-2´-geranylflavanone)である。
【0020】
プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方の濃度を高めることが容易であるという観点から、オオバギは、抽出物として筋萎縮抑制剤に配合されることが好ましい。
【0021】
オオバギ抽出物の原料としては、オオバギの各器官やそれらの構成成分を用いることができる。原料としては、単独の器官又は構成成分を用いてもよいし、二種以上の器官や構成成分を混合して用いてもよい。原料の具体例は、果実、種子、花、根、幹、茎の先端部、葉身、及び分泌物(ワックス等)を含む。茎の先端部は、茎の成長点及び葉芽を含んでおり、葉身に比べて柔軟であるため、抽出操作を効率的に行うことが容易である。また、オオバギの全体に対して各器官が占める割合を比較すると、幹、根、及び葉の占める割合は高い。このため、オオバギの葉身をオオバギ抽出物の原料として用いることは、原料確保が容易であるという観点から、工業的に好適である。また、オオバギの各部位の中でも、花、種子及び果実(ワックスを含む)には、ニムフェオール−A,B,C及びイソニムフェオール−Bが高濃度で含有される。このため、プレニル化エリオディクティオールの濃度を高めるためには、花、種子及び果実(ワックスを含む)を用いることが好ましく、果実を用いることがより好ましい。
【0022】
オオバギ抽出物の原料は、採取したままの状態、採取後に破砕、粉砕若しくはすり潰した状態、採取・乾燥後に粉砕、破砕若しくはすり潰した状態、又は、採取後に粉砕、破砕若しくはすり潰した後に乾燥させた状態として用いられる。抽出操作を効率的に行うという観点からは、破砕した原料を用いることが好ましい。こうした破砕には、例えばカッター、裁断機、クラッシャー等を用いることができる。また、粉砕した原料を調製する際には、例えばミル、クラッシャー、グラインダー等を用いることができる。すり潰した原料を調製する際には、ニーダー、乳鉢等を用いることができる。
【0023】
オオバギ抽出物を抽出するための抽出溶媒としては、少なくとも有機溶媒を含む抽出溶媒であることが好ましい。抽出溶媒としては、例えば水と有機溶媒との混合溶媒、低級アルコール、ジメチルスルホキシド、アセトニトリル、アセトン、酢酸エチル、ヘキサン、グリセリン、プロピレングリコール等の有機溶媒が好ましい。低級アルコールとしては、メタノール、エタノール、プロパノール、イソプロパノール、ブタノール等が挙げられる。有機溶媒としては、単独種を用いてもよいし、複数種を混合した混合溶媒を用いてもよい。抽出溶媒として水と有機溶媒の混合溶媒を用いる場合、混合溶媒中における有機溶媒の含有量は、好ましくは50体積%以上、より好ましくは80体積%以上である。混合溶媒中における有機溶媒の含有量が50体積%未満の場合、プレニル化ナリンゲニン、又はプレニル化エリオディクティオールを効率的に抽出することが困難となるおそれがある。なお、有機溶媒としては、低級アルコールが好ましく、エタノールがより好ましい。
【0024】
なお、抽出溶媒中に、有機塩、無機塩、緩衝剤、乳化剤、デキストリン等を溶解させてもよい。
抽出操作としては、抽出溶媒中に上記原料を所定時間浸漬させる。こうした抽出操作においては、抽出効率を高めるべく、必要に応じて攪拌操作、加温等を行ってもよい。また、原料から抽出される夾雑物を削減すべく、抽出操作に先だって、別途水抽出操作又は熱水抽出操作を行ってもよい。プレニル化ナリンゲニン、及びプレニル化エリオディクティオールは、水に対して不溶の成分であるため、オオバギを例えば熱湯で煮沸することで、不必要な侠雑物を効率的に除去することができる。
【0025】
抽出操作の後には固液分離操作が行われることで、オオバギ抽出液と原料の残渣とを分離することができる。固液分離操作の分離法としては、例えばろ過、遠心分離等の公知の分離法を利用することができる。
【0026】
ここで、オオバギには、上記のプレニル化フラバノン以外のフラバノンが含まれる。この点、例えばカラムを用いてオオバギ抽出液を分離することにより、プレニル化ナリンゲニン、又はプレニル化エリオディクティオールを高濃度で含有した抽出液(抽出物)を容易に得ることができる。カラムを用いた分離操作に用いられる充填材としては、周知の充填材から適宜選択して用いることができる。充填材としては、例えば、オクタデシル基を結合したシリカゲルが好適である。抽出液中に含まれるプレニル化ナリンゲニン、又はプレニル化エリオディクティオールの確認及び定量は、例えば、周知の高速液体クロマトグラフィーにより行うことができる。
【0027】
得られたオオバギ抽出液は、必要に応じて濃縮してもよい。オオバギ抽出液に含まれる抽出溶媒を必要に応じて除去することにより、粘度を有する油状や固体状のオオバギ抽出物を得ることができる。こうした溶媒の除去は、例えば減圧下で加熱することにより行ってもよいし、凍結乾燥により行ってもよい。
【0028】
筋萎縮抑制剤には、例えば、賦形剤、添加剤、副素材、増量剤等を適宜添加することもできる。筋萎縮抑制剤は、医薬品、又は、医薬品に配合して用いることができる。医薬品として用いる場合、又は医薬品中に配合させて用いる場合の投与方法としては、例えば、服用(経口摂取)により投与する方法(経口投与)、腸内投与(経腸投与)、皮膚湿布(経皮投与)、筋肉注射等が挙げられる。医薬品の剤型の具体例は、例えば、ガム製剤、散剤、粉剤、顆粒剤、錠剤、カプセル剤、丸剤、坐剤、液剤、塗布剤、貼付剤、注射剤等が挙げられる。
【0029】
次に、筋萎縮抑制剤の使用方法について説明する。
筋萎縮抑制剤の使用方法は、上述した筋萎縮抑制剤を飲食品に配合して摂取させる。
飲食品の具体例は、通常の飲食品に加えて、医薬部外品、健康食品、特定保健用食品、健康飲料、栄養補助食品等を含む。飲食品の形態としては、例えば、ガム、粉末、錠剤、顆粒、液状(ドリンク剤等)、カプセル状、シロップ、キャンディー等が挙げられる。飲食品としては、より具体的には、スポーツドリンク、茶葉やハーブなどから抽出した茶類飲料、牛乳やヨーグルト等の乳製品、ペクチンやカラギーナン等のゲル化剤含有食品、グルコース、ショ糖、果糖、乳糖やデキストリン等の糖類、香料、ステビア、アスパルテーム、糖アルコール等の甘味料、植物性油脂及び動物性油脂等の油脂等を含有する飲料品や食料品が挙げられる。
【0030】
プレニル化フラバノンは、常法に従って、例えば、飲食品の基材にプレニル化フラバノンを混合することで飲食品に配合される。飲食品には、本発明の目的を損なわない範囲において、賦形剤、添加剤、副素材、増量剤等を適宜添加してもよい。
【0031】
飲食品中におけるプレニル化フラバノンの含有量は、例えば0.0001〜5質量%の範囲とされる。飲食品の摂取量は、特に限定されないが、成人1日当たりのプレニル化フラバノンの摂取量として、好ましくは1〜1000mg、より好ましくは10〜200mgとされる。
【0032】
次に、筋萎縮抑制剤、及びその使用方法の作用について説明する。
代表的なフラバノンであるナリンゲニンは抗酸化活性を有するものの、ナリンゲニンを摂取させた場合には廃用性筋萎縮を抑制する効果が確認されない。このことから、廃用性萎縮を抑制するのは、必ずしも上述した非特許文献1に記載される抗酸化能により酸化ストレスを低減させることに基づくものではないと推察される。また、ナリンゲニンにプレニル基を導入しても、抗酸化活性が著しく高まることはない。このため、プレニル化フラバノンによる廃用性筋萎縮を抑制する効果は、抗酸化能に基づくものではなく、他の作用機序によると推測される。この点、プレニル化フラバノンでは、例えばプレニル基により親油性が高まることで、フラバノンでは得られない新たな作用機序に基づき廃用性筋萎縮の抑制効果が発揮されると推測される。
【0033】
筋萎縮抑制剤、及びその使用方法は、例えば、怪我、病気、老化、運動不足等に基づく廃用性筋萎縮を容易に抑制することができる。筋萎縮抑制剤の使用方法は、筋萎縮抑制剤を宇宙食へ配合することで、例えば、無重力条件下の宇宙滞在者の廃用性筋萎縮を抑制することが容易となるため、宇宙滞在の長期化に寄与することができる。
【0034】
筋萎縮抑制剤に含まれるプレニル化フラバノンは、難水溶性のため、そのまま摂取した場合、体内での吸収率が十分に得られないおそれがある。また、筋萎縮抑制剤を水で摂取した場合、プレニル化フラバノンが難水溶性であることから、口腔に残留したり、口腔にべたつき感が生じたりすることで、摂取時に違和感が生じるおそれがある。この点、筋萎縮抑制剤の使用方法によれば、筋萎縮抑制剤を飲食品に配合して摂取させるため、例えば、飲料に分散させたり、飲食品に混合したりすることで、体内でのプレニル化フラバノンの吸収率を高めたり、筋萎縮抑制剤の摂取時の違和感を軽減したりすることが容易となる。
【0035】
本実施形態によって発揮される効果について、以下に記載する。
(1)プレニル化フラバノンを有効成分として含有させることで、廃用性筋萎縮を抑制する筋萎縮抑制剤が提供される。
【0036】
(2)プレニル化フラバノンが、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含むことで、例えば、オオバギを有効に利用することができるようになる。
【0037】
(3)プレニル化フラバノンは、オオバギ抽出物由来であることが好ましい。この場合、オオバギを有効利用することができる。
(4)オオバギ抽出物として、果実より抽出して得られたものを用いることで、プレニル化エリオディクティオールの濃度を高めることが容易となる。
【0038】
(5)筋萎縮抑制剤を飲食品に配合して摂取させる筋萎縮抑制剤の使用方法によれば、体内でのプレニル化フラバノンの吸収率を高めたり、筋萎縮抑制剤の摂取時の違和感を軽減したりすることが容易となる。
【0039】
なお、前記実施形態を次のように変更することもできる。
・筋萎縮抑制剤、及びその使用方法は、ヒトへの適用に限定されず、例えば、馬、牛、犬、猫等の動物に適用してもよい。
【0040】
・前記使用方法は、例えば、運動トレーニング、リハビリテーション、一般的な食事療法と合わせて実施してもよい。
・前記筋萎縮抑制剤、及びその使用方法は、廃用性筋萎縮の予防に適用する他に、発症した廃用性筋萎縮の進行の阻止に適用してもよい。
【実施例】
【0041】
次に、実施例及び比較例を挙げて前記実施形態を具体的に説明する。
(実施例1)
プレニル化フラバノンを添加した飼料をマウスに与える試験を行った。プレニル化フラバノンとしては、8−プレニルナリンゲニン(以下、プレニル化ナリンゲニンという)を用いた。プレニル化ナリンゲニンは、国立大学法人徳島大学大学院、ヘルスバイオサイエンス研究部、機能分子合成薬学分野において人工的に化学合成した純度95%以上のものである。
【0042】
標準精製飼料AIN−93M(米国国立栄養研究所(AIN)から1993年に発表されたマウス・ラットを用いた栄養研究のための標準精製飼料)にプレニル化ナリンゲニンを添加することで、飼料を調製した。プレニル化ナリンゲニンの添加量は、標準精製飼料100g中にプレニル化ナリンゲニン(分子量340.37)がフラバノン当量で5.6mmol含まれる量(純度95%として算出)とした。すなわち、標準精製飼料100g中に0.2gのプレニル化ナリンゲニン(純度95%以上)が含有されるように添加した。なお、プレニル化ナリンゲニンを添加する前記標準精製飼料は、予めセルロース量を減じることで、対照(コントロール)とする前記標準精製飼料と組成を調整した。
【0043】
プレニル化ナリンゲニンを添加した飼料と対照の飼料とを、投与群と対照群の各群4匹のC57BL/6マウス(7週齢、オス、日本エスエルシー社より購入)に3g/匹/日となるように与えた。なお、飲水については、水道水の自由摂取とした。なお、各群のマウスは、1週間の予備飼育後、各群に分けている。
【0044】
18日間の摂食の後、マウス右後肢の坐骨神経を切除する手術を施すことで廃用性筋萎縮の誘導を行った。なお、左後肢に偽手術を施すことで、左後肢を対照とした。
手術から4日間、マウスに上記と同様に飼料を与えるとともに水道水を自由摂取させた。手術から4日後、マウスの左右後肢の腓腹筋を摘出し、その腓腹筋の重量を測定した。
【0045】
腓腹筋重量を左右後肢の腓腹筋のそれぞれについて体重当たりとして計算し、左肢の腓腹筋重量を100%としたときの右肢の腓腹筋重量の割合を算出することで、正常筋に対する萎縮筋の重量の割合を求めた。
【0046】
(比較例1)
プレニル化ナリンゲニンの代わりに、ナリンゲニン(東京化成工業株式会社製、純度90%)を用いて、実施例1と同様に飼料をマウスに与える試験を行った。標準精製飼料AIN−93Mにナリンゲニンを添加することで、飼料を調製した。ナリンゲニンの添加量は、100gの標準精製飼料中にナリンゲニン(分子量270.5)がフラバノン当量で5.6mmol含まれる量とした。すなわち、標準精製飼料100g中に0.17gのナリンゲニン(純度90%)が含有されるように添加した。なお、ナリンゲニンを添加する標準精製飼料は、予めセルロースの量を減じることで、対照の飼料と組成を合わせた。
【0047】
(実施例1及び比較例1の結果)
対照群における筋萎縮の割合は、90.3%であった。これに対して、ナリンゲニン食群における筋萎縮の割合は、92.9%であり、プレニル化ナリンゲニン食群は102.1%であった。これらの結果を図1に示している。そして、各群の結果について、Tukey法を用いて統計処理を行った結果、プレニル化ナリンゲニン食群と、その他の群との間に有意な差があった。従って、プレニル化ナリンゲニンに廃用性筋萎縮の抑制効果が認められた。また、ナリンゲニンでは、廃用性筋萎縮の抑制効果が認められないことから、前記抑制効果は、プレニル化に基づいて得られることが分かった。
【0048】
次に、腓腹筋の摘出時における体重及び摂餌量を表1に示す。
【0049】
【表1】

表1に示すように、体重及び摂餌量について、プレニル化ナリンゲニンを与えた群がその他の群よりも低いことが分かった。さらに、試験期間中の摂餌量の変化について図2に示す。実験の開始から1週間程度の間は、各群において摂餌量の差が認められるものの、その後は各群間で概ね同程度の摂餌量であった。なお、プレニル化ナリンゲニン食群の摂餌量がその他の群の摂餌量よりも低い結果は、試験期間の初期においてプレニル化ナリンゲニン食群の摂餌量が他の群の摂餌量よりも少ないことに起因していることが分かる。この点、試験期間の経過に伴って摂餌量が安定してその他の群と同等になることから、著しく腓腹筋重量へ影響することは無いと考えられる。また、同一個体での正常筋に対する萎縮筋の重量の割合により効果を確認しているため、体重の影響も無いと考えられる。
【0050】
すなわち、プレニル化ナリンゲニン食群とナリンゲニン食群間においてフラバノン摂取量(mmol/匹/day)には大差なく、飼料摂取量の違いによる腓腹筋重量への影響もないことから、廃用性筋萎縮の抑制効果は、プレニル化ナリンゲニンの作用によるものと考えられる。
【0051】
(実施例3)
沖縄県国頭郡において、2009年6月に採取し、冷凍保存していたオオバギ(Macaranga tanarius)の果実を原料として用いた。このオオバギの果実1kgを3Lのエタノールに24時間浸漬した。その浸漬物を濾材として珪藻土を用いてろ過することでろ液を得た後、そのろ液をエバポレーターで濃縮することで濃縮液を得た。次に、分取用ODSカラムを用いて濃縮液を分画することで、プレニル化フラバノンを多く含む分画液を得た。得られた分画液をエバポレーターにて濃縮し、エタノール及び水を除去することで、粘性を有する油状の抽出物を得た。
【0052】
得られた油状の抽出物に含まれる成分を高速液体クロマトグラフィーにより分析した結果、プレニル化フラバノンを約80w/w%含有していた。プレニル化フラバノンの化合物名と含有量を表2に示す。
【0053】
【表2】

次に、得られた抽出物を添加した飼料をマウスに与える試験を行った。
【0054】
標準精製飼料AIN−93M(米国国立栄養研究所(AIN)から1993年に発表されたマウス・ラットを用いた栄養研究のための標準精製飼料)に抽出物を添加することで、飼料を調製した。抽出物の添加量は、標準精製飼料100g中に0.2gの抽出物が含有されるように添加した飼料中における抽出物の濃度が0.2w/w%となる量とした。なお、抽出物を添加する前記標準精製飼料は、予めセルロースの量を減じることで、対照となる前記標準精製飼料と組成を調整した。
【0055】
抽出物を添加した飼料と対照となる前記標準精製飼料とを、オオバギ食群と対照群の各群5匹のC57BL/6マウス(7週齢、オス、日本エスエルシー社より購入)に2週間自由摂食させた。なお、飲水については、水道水の自由摂取とした。
【0056】
2週間の自由摂食の後、マウス右後肢の坐骨神経を切除する手術を施すことで廃用性筋萎縮の誘導を行った。なお、左後肢に偽手術を施すことで、左後肢を対照とした。
手術から4日間、マウスに上記と同様に飼料を与えるとともに水道水を自由摂取させた。手術から4日後、マウスの左右後肢の腓腹筋を摘出し、その腓腹筋の重量を測定した。
【0057】
腓腹筋重量を左右後肢の腓腹筋のそれぞれについて体重当たりとして計算し、左肢の腓腹筋重量を100%としたときの右肢の腓腹筋重量の割合を算出することで、正常筋に対する萎縮筋の重量の割合を求めた。
【0058】
(実施例3の結果)
表3及び図3には、各群における正常筋に対する萎縮筋の重量割合(%)についての結果を示している。
【0059】
【表3】

この結果について、t−検定を行った結果、オオバギ食群と対照群との間に有意な差があった。これにより、プレニル化フラバノンを含有するオオバギ抽出物が廃用性筋萎縮を抑制できることが分かる。
【技術分野】
【0001】
本発明は、廃用性筋萎縮を抑制する筋萎縮抑制剤、及びその使用方法に関する。
【背景技術】
【0002】
筋萎縮としては、例えば老化や寝たきりを要因として筋肉が萎縮する筋萎縮(廃用性筋萎縮)が知られ、こうした廃用性筋萎縮を抑制する飲食品が提案されている(特許文献1参照)。特許文献1は、果実ポリフェノールを有効成分として含有する筋萎縮抑制組成物を開示している。同文献1では、リンゴポリフェノールを含有する筋萎縮抑制組成物の実施例が開示されている。ここで、廃用性筋萎縮については、酸化ストレスが要因であるという報告がある(非特許文献1参照)。非特許文献1は、酸化ストレスを抗酸化剤又は鉄キレート剤の投与により防止することで、筋萎縮の進行が抑制できることを報告している。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開2001−89387号公報
【非特許文献】
【0004】
【非特許文献1】体力研究,1993年,No.83,pp.73−81
【発明の概要】
【発明が解決しようとする課題】
【0005】
特許文献1に記載されるリンゴポリフェノールは、抗酸化活性を有するカテキンを含有している。抗酸化活性を有するカテキンは、非特許文献1に記載されるように、酸化ストレスを低減し、その結果、廃用性筋萎縮を抑制すると考えられる。カテキンは、フラバノールの一種であり、このフラバノールはフラボノイドの一種である。
【0006】
フラボノイドに分類される化合物群として、フラバノール以外にフラバノンが知られている。ここで、代表的なフラバノンであるナリンゲニンについても、抗酸化活性を有するため、廃用性筋萎縮を抑制する効果が期待される。ところが、本発明者らは、ナリンゲニンを含有する飲食品を摂取させた場合には、廃用性筋萎縮を抑制する効果が得られないことを確認した。こうした実情の下、本発明は、プレニル基を付加したフラバノンが廃用性筋萎縮を抑制することを見出すことでなされたものである。
【0007】
本発明の目的は、廃用性筋萎縮を抑制する筋萎縮抑制剤、及びその使用方法を提供することにある。
【課題を解決するための手段】
【0008】
上記の目的を達成するために、請求項1に記載の発明の筋萎縮抑制剤は、廃用性筋萎縮を抑制する筋萎縮抑制剤であって、プレニル化フラバノンを有効成分として含有することを特徴とする。
【0009】
請求項2に記載の発明は、請求項1に記載の筋萎縮抑制剤において、前記プレニル化フラバノンが、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含むことを特徴とする。
【0010】
請求項3に記載の発明は、請求項2に記載の筋萎縮抑制剤において、前記プレニル化フラバノンが、オオバギ抽出物由来であることを特徴とする。
請求項4に記載の発明は、請求項3に記載の筋萎縮抑制剤において、前記オオバギ抽出物が、果実より抽出して得られたことを特徴とする。
【0011】
請求項5に記載の発明の筋萎縮抑制剤の使用方法は、請求項1から請求項4のいずれか一項に記載の筋萎縮抑制剤を飲食品に配合して摂取させることを特徴とする。
【発明の効果】
【0012】
本発明によれば、廃用性筋萎縮を抑制する筋萎縮抑制剤、及びその使用方法が提供される。
【図面の簡単な説明】
【0013】
【図1】実施例1及び比較例1における正常筋に対する萎縮筋の重量の割合を示すグラフ。
【図2】実施例1及び比較例1におけるマウスの飼育機関に対する摂餌量を示すグラフ。
【図3】実施例3における正常筋に対する萎縮筋の重量の割合を示すグラフ。
【発明を実施するための形態】
【0014】
本発明の筋萎縮抑制剤、及びその使用方法を具体化した実施形態を詳細に説明する。
本実施形態の筋萎縮抑制剤は、プレニル化フラバノンを有効成分として含有することで、廃用性筋萎縮を抑制する。筋萎縮は、進行性筋萎縮と、廃用性筋萎縮とに分類される。進行性筋萎縮は、四肢等の骨格筋が進行的に萎縮する疾患群である一方、廃用性筋萎縮は、筋肉を使わないことによって生じる筋萎縮である。
【0015】
プレニル化フラバノンの具体例は、プレニル化ナリンゲニン、プレニル化エリオディクティオール、及びプレニル化ヘスペレチンを含む。これらのプレニル化フラバノンは、一種のみを用いてもよいし、複数種のプレニル化フラバノンを組み合わせて用いてもよい。
【0016】
プレニル基の具体例は、ジメチルアリル基(C5)、ゲラニル基(C10)、ファルネシル基(C15)、ゲラニルゲラニル基(C20)、ゲラニルファルネシル基(C25)、ヘキサプレニル基(C30)、オクタプレニル基(C40)、及びデカプレニル基(C50)を含む。
【0017】
プレニル化フラバノンのうち、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールは、オオバギ(大葉木)に含有される成分である。このため、プレニル化ナリンゲニン、又はプレニル化エリオディクティオールを筋萎縮抑制剤に含有させる場合、オオバギを用いることができる。
【0018】
オオバギは、マカランガ・タナリウス(Macaranga tanarius)とも呼ばれる植物であって、トウダイグサ科オオバギ属に属する常緑広葉樹(雌雄異株)である。オオバギは、沖縄、台湾、中国南部、マレー半島、フィリピン、マレーシア、インドネシア、タイなどの東南アジア、オーストラリア北部などに生育している。また、オオバギは、樹木の中でも成長が極めて早く、荒廃地における成長も可能である。このため、プレニル化フラバノンとして、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含む筋萎縮抑制剤によれば、例えば、上述したオオバギを有効利用することができる。
【0019】
オオバギは、プレニル化ナリンゲニンとして、5,7,4´-トリヒドロキシ-3´-ゲラニルフラバノン(5,7,4´-trihydroxy-3´-geranylflavanone)を含む。
オオバギに含まれるプレニル化エリオディクティオールとしては、ニムフェオール−A、ニムフェオール−B、イソニムフェオール−B及びニムフェオール−Cが挙げられる。ニムフェオール−A(nymphaeol−A)は、5,7,3´,4´-テトラヒドロキシ-6-ゲラニルフラバノン(5,7,3´,4´-tetrahydroxy-6-geranylflavanone)である。ニムフェオール−B(nymphaeol−B)は、5,7,3´,4´-テトラヒドロキシ-2´-ゲラニルフラバノン(5,7,3´,4´-tetrahydroxy-2´-geranylflavanone)である。イソニムフェオール−B(isonymphaeol−B)は、5,7,3´,4´-テトラヒドロキシ-5´-ゲラニルフラバノン(5,7,3´,4´-tetrahydroxy-5´-geranylflavanone)である。ニムフェオール−C(nymphaeol−C)は、5,7,3´,4´-テトラヒドロキシ-6-(3´´´,3´´´-ジメチルアリル)-2´-ゲラニルフラバノン(5,7,3´,4´-tetrahydroxy-6-(3´´´,3´´´-dimethylallyl)-2´-geranylflavanone)である。
【0020】
プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方の濃度を高めることが容易であるという観点から、オオバギは、抽出物として筋萎縮抑制剤に配合されることが好ましい。
【0021】
オオバギ抽出物の原料としては、オオバギの各器官やそれらの構成成分を用いることができる。原料としては、単独の器官又は構成成分を用いてもよいし、二種以上の器官や構成成分を混合して用いてもよい。原料の具体例は、果実、種子、花、根、幹、茎の先端部、葉身、及び分泌物(ワックス等)を含む。茎の先端部は、茎の成長点及び葉芽を含んでおり、葉身に比べて柔軟であるため、抽出操作を効率的に行うことが容易である。また、オオバギの全体に対して各器官が占める割合を比較すると、幹、根、及び葉の占める割合は高い。このため、オオバギの葉身をオオバギ抽出物の原料として用いることは、原料確保が容易であるという観点から、工業的に好適である。また、オオバギの各部位の中でも、花、種子及び果実(ワックスを含む)には、ニムフェオール−A,B,C及びイソニムフェオール−Bが高濃度で含有される。このため、プレニル化エリオディクティオールの濃度を高めるためには、花、種子及び果実(ワックスを含む)を用いることが好ましく、果実を用いることがより好ましい。
【0022】
オオバギ抽出物の原料は、採取したままの状態、採取後に破砕、粉砕若しくはすり潰した状態、採取・乾燥後に粉砕、破砕若しくはすり潰した状態、又は、採取後に粉砕、破砕若しくはすり潰した後に乾燥させた状態として用いられる。抽出操作を効率的に行うという観点からは、破砕した原料を用いることが好ましい。こうした破砕には、例えばカッター、裁断機、クラッシャー等を用いることができる。また、粉砕した原料を調製する際には、例えばミル、クラッシャー、グラインダー等を用いることができる。すり潰した原料を調製する際には、ニーダー、乳鉢等を用いることができる。
【0023】
オオバギ抽出物を抽出するための抽出溶媒としては、少なくとも有機溶媒を含む抽出溶媒であることが好ましい。抽出溶媒としては、例えば水と有機溶媒との混合溶媒、低級アルコール、ジメチルスルホキシド、アセトニトリル、アセトン、酢酸エチル、ヘキサン、グリセリン、プロピレングリコール等の有機溶媒が好ましい。低級アルコールとしては、メタノール、エタノール、プロパノール、イソプロパノール、ブタノール等が挙げられる。有機溶媒としては、単独種を用いてもよいし、複数種を混合した混合溶媒を用いてもよい。抽出溶媒として水と有機溶媒の混合溶媒を用いる場合、混合溶媒中における有機溶媒の含有量は、好ましくは50体積%以上、より好ましくは80体積%以上である。混合溶媒中における有機溶媒の含有量が50体積%未満の場合、プレニル化ナリンゲニン、又はプレニル化エリオディクティオールを効率的に抽出することが困難となるおそれがある。なお、有機溶媒としては、低級アルコールが好ましく、エタノールがより好ましい。
【0024】
なお、抽出溶媒中に、有機塩、無機塩、緩衝剤、乳化剤、デキストリン等を溶解させてもよい。
抽出操作としては、抽出溶媒中に上記原料を所定時間浸漬させる。こうした抽出操作においては、抽出効率を高めるべく、必要に応じて攪拌操作、加温等を行ってもよい。また、原料から抽出される夾雑物を削減すべく、抽出操作に先だって、別途水抽出操作又は熱水抽出操作を行ってもよい。プレニル化ナリンゲニン、及びプレニル化エリオディクティオールは、水に対して不溶の成分であるため、オオバギを例えば熱湯で煮沸することで、不必要な侠雑物を効率的に除去することができる。
【0025】
抽出操作の後には固液分離操作が行われることで、オオバギ抽出液と原料の残渣とを分離することができる。固液分離操作の分離法としては、例えばろ過、遠心分離等の公知の分離法を利用することができる。
【0026】
ここで、オオバギには、上記のプレニル化フラバノン以外のフラバノンが含まれる。この点、例えばカラムを用いてオオバギ抽出液を分離することにより、プレニル化ナリンゲニン、又はプレニル化エリオディクティオールを高濃度で含有した抽出液(抽出物)を容易に得ることができる。カラムを用いた分離操作に用いられる充填材としては、周知の充填材から適宜選択して用いることができる。充填材としては、例えば、オクタデシル基を結合したシリカゲルが好適である。抽出液中に含まれるプレニル化ナリンゲニン、又はプレニル化エリオディクティオールの確認及び定量は、例えば、周知の高速液体クロマトグラフィーにより行うことができる。
【0027】
得られたオオバギ抽出液は、必要に応じて濃縮してもよい。オオバギ抽出液に含まれる抽出溶媒を必要に応じて除去することにより、粘度を有する油状や固体状のオオバギ抽出物を得ることができる。こうした溶媒の除去は、例えば減圧下で加熱することにより行ってもよいし、凍結乾燥により行ってもよい。
【0028】
筋萎縮抑制剤には、例えば、賦形剤、添加剤、副素材、増量剤等を適宜添加することもできる。筋萎縮抑制剤は、医薬品、又は、医薬品に配合して用いることができる。医薬品として用いる場合、又は医薬品中に配合させて用いる場合の投与方法としては、例えば、服用(経口摂取)により投与する方法(経口投与)、腸内投与(経腸投与)、皮膚湿布(経皮投与)、筋肉注射等が挙げられる。医薬品の剤型の具体例は、例えば、ガム製剤、散剤、粉剤、顆粒剤、錠剤、カプセル剤、丸剤、坐剤、液剤、塗布剤、貼付剤、注射剤等が挙げられる。
【0029】
次に、筋萎縮抑制剤の使用方法について説明する。
筋萎縮抑制剤の使用方法は、上述した筋萎縮抑制剤を飲食品に配合して摂取させる。
飲食品の具体例は、通常の飲食品に加えて、医薬部外品、健康食品、特定保健用食品、健康飲料、栄養補助食品等を含む。飲食品の形態としては、例えば、ガム、粉末、錠剤、顆粒、液状(ドリンク剤等)、カプセル状、シロップ、キャンディー等が挙げられる。飲食品としては、より具体的には、スポーツドリンク、茶葉やハーブなどから抽出した茶類飲料、牛乳やヨーグルト等の乳製品、ペクチンやカラギーナン等のゲル化剤含有食品、グルコース、ショ糖、果糖、乳糖やデキストリン等の糖類、香料、ステビア、アスパルテーム、糖アルコール等の甘味料、植物性油脂及び動物性油脂等の油脂等を含有する飲料品や食料品が挙げられる。
【0030】
プレニル化フラバノンは、常法に従って、例えば、飲食品の基材にプレニル化フラバノンを混合することで飲食品に配合される。飲食品には、本発明の目的を損なわない範囲において、賦形剤、添加剤、副素材、増量剤等を適宜添加してもよい。
【0031】
飲食品中におけるプレニル化フラバノンの含有量は、例えば0.0001〜5質量%の範囲とされる。飲食品の摂取量は、特に限定されないが、成人1日当たりのプレニル化フラバノンの摂取量として、好ましくは1〜1000mg、より好ましくは10〜200mgとされる。
【0032】
次に、筋萎縮抑制剤、及びその使用方法の作用について説明する。
代表的なフラバノンであるナリンゲニンは抗酸化活性を有するものの、ナリンゲニンを摂取させた場合には廃用性筋萎縮を抑制する効果が確認されない。このことから、廃用性萎縮を抑制するのは、必ずしも上述した非特許文献1に記載される抗酸化能により酸化ストレスを低減させることに基づくものではないと推察される。また、ナリンゲニンにプレニル基を導入しても、抗酸化活性が著しく高まることはない。このため、プレニル化フラバノンによる廃用性筋萎縮を抑制する効果は、抗酸化能に基づくものではなく、他の作用機序によると推測される。この点、プレニル化フラバノンでは、例えばプレニル基により親油性が高まることで、フラバノンでは得られない新たな作用機序に基づき廃用性筋萎縮の抑制効果が発揮されると推測される。
【0033】
筋萎縮抑制剤、及びその使用方法は、例えば、怪我、病気、老化、運動不足等に基づく廃用性筋萎縮を容易に抑制することができる。筋萎縮抑制剤の使用方法は、筋萎縮抑制剤を宇宙食へ配合することで、例えば、無重力条件下の宇宙滞在者の廃用性筋萎縮を抑制することが容易となるため、宇宙滞在の長期化に寄与することができる。
【0034】
筋萎縮抑制剤に含まれるプレニル化フラバノンは、難水溶性のため、そのまま摂取した場合、体内での吸収率が十分に得られないおそれがある。また、筋萎縮抑制剤を水で摂取した場合、プレニル化フラバノンが難水溶性であることから、口腔に残留したり、口腔にべたつき感が生じたりすることで、摂取時に違和感が生じるおそれがある。この点、筋萎縮抑制剤の使用方法によれば、筋萎縮抑制剤を飲食品に配合して摂取させるため、例えば、飲料に分散させたり、飲食品に混合したりすることで、体内でのプレニル化フラバノンの吸収率を高めたり、筋萎縮抑制剤の摂取時の違和感を軽減したりすることが容易となる。
【0035】
本実施形態によって発揮される効果について、以下に記載する。
(1)プレニル化フラバノンを有効成分として含有させることで、廃用性筋萎縮を抑制する筋萎縮抑制剤が提供される。
【0036】
(2)プレニル化フラバノンが、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含むことで、例えば、オオバギを有効に利用することができるようになる。
【0037】
(3)プレニル化フラバノンは、オオバギ抽出物由来であることが好ましい。この場合、オオバギを有効利用することができる。
(4)オオバギ抽出物として、果実より抽出して得られたものを用いることで、プレニル化エリオディクティオールの濃度を高めることが容易となる。
【0038】
(5)筋萎縮抑制剤を飲食品に配合して摂取させる筋萎縮抑制剤の使用方法によれば、体内でのプレニル化フラバノンの吸収率を高めたり、筋萎縮抑制剤の摂取時の違和感を軽減したりすることが容易となる。
【0039】
なお、前記実施形態を次のように変更することもできる。
・筋萎縮抑制剤、及びその使用方法は、ヒトへの適用に限定されず、例えば、馬、牛、犬、猫等の動物に適用してもよい。
【0040】
・前記使用方法は、例えば、運動トレーニング、リハビリテーション、一般的な食事療法と合わせて実施してもよい。
・前記筋萎縮抑制剤、及びその使用方法は、廃用性筋萎縮の予防に適用する他に、発症した廃用性筋萎縮の進行の阻止に適用してもよい。
【実施例】
【0041】
次に、実施例及び比較例を挙げて前記実施形態を具体的に説明する。
(実施例1)
プレニル化フラバノンを添加した飼料をマウスに与える試験を行った。プレニル化フラバノンとしては、8−プレニルナリンゲニン(以下、プレニル化ナリンゲニンという)を用いた。プレニル化ナリンゲニンは、国立大学法人徳島大学大学院、ヘルスバイオサイエンス研究部、機能分子合成薬学分野において人工的に化学合成した純度95%以上のものである。
【0042】
標準精製飼料AIN−93M(米国国立栄養研究所(AIN)から1993年に発表されたマウス・ラットを用いた栄養研究のための標準精製飼料)にプレニル化ナリンゲニンを添加することで、飼料を調製した。プレニル化ナリンゲニンの添加量は、標準精製飼料100g中にプレニル化ナリンゲニン(分子量340.37)がフラバノン当量で5.6mmol含まれる量(純度95%として算出)とした。すなわち、標準精製飼料100g中に0.2gのプレニル化ナリンゲニン(純度95%以上)が含有されるように添加した。なお、プレニル化ナリンゲニンを添加する前記標準精製飼料は、予めセルロース量を減じることで、対照(コントロール)とする前記標準精製飼料と組成を調整した。
【0043】
プレニル化ナリンゲニンを添加した飼料と対照の飼料とを、投与群と対照群の各群4匹のC57BL/6マウス(7週齢、オス、日本エスエルシー社より購入)に3g/匹/日となるように与えた。なお、飲水については、水道水の自由摂取とした。なお、各群のマウスは、1週間の予備飼育後、各群に分けている。
【0044】
18日間の摂食の後、マウス右後肢の坐骨神経を切除する手術を施すことで廃用性筋萎縮の誘導を行った。なお、左後肢に偽手術を施すことで、左後肢を対照とした。
手術から4日間、マウスに上記と同様に飼料を与えるとともに水道水を自由摂取させた。手術から4日後、マウスの左右後肢の腓腹筋を摘出し、その腓腹筋の重量を測定した。
【0045】
腓腹筋重量を左右後肢の腓腹筋のそれぞれについて体重当たりとして計算し、左肢の腓腹筋重量を100%としたときの右肢の腓腹筋重量の割合を算出することで、正常筋に対する萎縮筋の重量の割合を求めた。
【0046】
(比較例1)
プレニル化ナリンゲニンの代わりに、ナリンゲニン(東京化成工業株式会社製、純度90%)を用いて、実施例1と同様に飼料をマウスに与える試験を行った。標準精製飼料AIN−93Mにナリンゲニンを添加することで、飼料を調製した。ナリンゲニンの添加量は、100gの標準精製飼料中にナリンゲニン(分子量270.5)がフラバノン当量で5.6mmol含まれる量とした。すなわち、標準精製飼料100g中に0.17gのナリンゲニン(純度90%)が含有されるように添加した。なお、ナリンゲニンを添加する標準精製飼料は、予めセルロースの量を減じることで、対照の飼料と組成を合わせた。
【0047】
(実施例1及び比較例1の結果)
対照群における筋萎縮の割合は、90.3%であった。これに対して、ナリンゲニン食群における筋萎縮の割合は、92.9%であり、プレニル化ナリンゲニン食群は102.1%であった。これらの結果を図1に示している。そして、各群の結果について、Tukey法を用いて統計処理を行った結果、プレニル化ナリンゲニン食群と、その他の群との間に有意な差があった。従って、プレニル化ナリンゲニンに廃用性筋萎縮の抑制効果が認められた。また、ナリンゲニンでは、廃用性筋萎縮の抑制効果が認められないことから、前記抑制効果は、プレニル化に基づいて得られることが分かった。
【0048】
次に、腓腹筋の摘出時における体重及び摂餌量を表1に示す。
【0049】
【表1】

表1に示すように、体重及び摂餌量について、プレニル化ナリンゲニンを与えた群がその他の群よりも低いことが分かった。さらに、試験期間中の摂餌量の変化について図2に示す。実験の開始から1週間程度の間は、各群において摂餌量の差が認められるものの、その後は各群間で概ね同程度の摂餌量であった。なお、プレニル化ナリンゲニン食群の摂餌量がその他の群の摂餌量よりも低い結果は、試験期間の初期においてプレニル化ナリンゲニン食群の摂餌量が他の群の摂餌量よりも少ないことに起因していることが分かる。この点、試験期間の経過に伴って摂餌量が安定してその他の群と同等になることから、著しく腓腹筋重量へ影響することは無いと考えられる。また、同一個体での正常筋に対する萎縮筋の重量の割合により効果を確認しているため、体重の影響も無いと考えられる。
【0050】
すなわち、プレニル化ナリンゲニン食群とナリンゲニン食群間においてフラバノン摂取量(mmol/匹/day)には大差なく、飼料摂取量の違いによる腓腹筋重量への影響もないことから、廃用性筋萎縮の抑制効果は、プレニル化ナリンゲニンの作用によるものと考えられる。
【0051】
(実施例3)
沖縄県国頭郡において、2009年6月に採取し、冷凍保存していたオオバギ(Macaranga tanarius)の果実を原料として用いた。このオオバギの果実1kgを3Lのエタノールに24時間浸漬した。その浸漬物を濾材として珪藻土を用いてろ過することでろ液を得た後、そのろ液をエバポレーターで濃縮することで濃縮液を得た。次に、分取用ODSカラムを用いて濃縮液を分画することで、プレニル化フラバノンを多く含む分画液を得た。得られた分画液をエバポレーターにて濃縮し、エタノール及び水を除去することで、粘性を有する油状の抽出物を得た。
【0052】
得られた油状の抽出物に含まれる成分を高速液体クロマトグラフィーにより分析した結果、プレニル化フラバノンを約80w/w%含有していた。プレニル化フラバノンの化合物名と含有量を表2に示す。
【0053】
【表2】

次に、得られた抽出物を添加した飼料をマウスに与える試験を行った。
【0054】
標準精製飼料AIN−93M(米国国立栄養研究所(AIN)から1993年に発表されたマウス・ラットを用いた栄養研究のための標準精製飼料)に抽出物を添加することで、飼料を調製した。抽出物の添加量は、標準精製飼料100g中に0.2gの抽出物が含有されるように添加した飼料中における抽出物の濃度が0.2w/w%となる量とした。なお、抽出物を添加する前記標準精製飼料は、予めセルロースの量を減じることで、対照となる前記標準精製飼料と組成を調整した。
【0055】
抽出物を添加した飼料と対照となる前記標準精製飼料とを、オオバギ食群と対照群の各群5匹のC57BL/6マウス(7週齢、オス、日本エスエルシー社より購入)に2週間自由摂食させた。なお、飲水については、水道水の自由摂取とした。
【0056】
2週間の自由摂食の後、マウス右後肢の坐骨神経を切除する手術を施すことで廃用性筋萎縮の誘導を行った。なお、左後肢に偽手術を施すことで、左後肢を対照とした。
手術から4日間、マウスに上記と同様に飼料を与えるとともに水道水を自由摂取させた。手術から4日後、マウスの左右後肢の腓腹筋を摘出し、その腓腹筋の重量を測定した。
【0057】
腓腹筋重量を左右後肢の腓腹筋のそれぞれについて体重当たりとして計算し、左肢の腓腹筋重量を100%としたときの右肢の腓腹筋重量の割合を算出することで、正常筋に対する萎縮筋の重量の割合を求めた。
【0058】
(実施例3の結果)
表3及び図3には、各群における正常筋に対する萎縮筋の重量割合(%)についての結果を示している。
【0059】
【表3】

この結果について、t−検定を行った結果、オオバギ食群と対照群との間に有意な差があった。これにより、プレニル化フラバノンを含有するオオバギ抽出物が廃用性筋萎縮を抑制できることが分かる。
【特許請求の範囲】
【請求項1】
廃用性筋萎縮を抑制する筋萎縮抑制剤であって、プレニル化フラバノンを有効成分として含有することを特徴とする筋萎縮抑制剤。
【請求項2】
前記プレニル化フラバノンが、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含むことを特徴とする請求項1に記載の筋萎縮抑制剤。
【請求項3】
前記プレニル化フラバノンが、オオバギ抽出物由来であることを特徴とする請求項2に記載の筋萎縮抑制剤。
【請求項4】
前記オオバギ抽出物が、果実より抽出して得られたことを特徴とする請求項3に記載の筋萎縮抑制剤。
【請求項5】
請求項1から請求項4のいずれか一項に記載の筋萎縮抑制剤を飲食品に配合して摂取させることを特徴とする筋萎縮抑制剤の使用方法。
【請求項1】
廃用性筋萎縮を抑制する筋萎縮抑制剤であって、プレニル化フラバノンを有効成分として含有することを特徴とする筋萎縮抑制剤。
【請求項2】
前記プレニル化フラバノンが、プレニル化ナリンゲニン、及びプレニル化エリオディクティオールの少なくとも一方を含むことを特徴とする請求項1に記載の筋萎縮抑制剤。
【請求項3】
前記プレニル化フラバノンが、オオバギ抽出物由来であることを特徴とする請求項2に記載の筋萎縮抑制剤。
【請求項4】
前記オオバギ抽出物が、果実より抽出して得られたことを特徴とする請求項3に記載の筋萎縮抑制剤。
【請求項5】
請求項1から請求項4のいずれか一項に記載の筋萎縮抑制剤を飲食品に配合して摂取させることを特徴とする筋萎縮抑制剤の使用方法。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2013−35811(P2013−35811A)
【公開日】平成25年2月21日(2013.2.21)
【国際特許分類】
【出願番号】特願2011−175303(P2011−175303)
【出願日】平成23年8月10日(2011.8.10)
【出願人】(308009277)株式会社ポッカコーポレーション (31)
【出願人】(304020292)国立大学法人徳島大学 (307)
【Fターム(参考)】
【公開日】平成25年2月21日(2013.2.21)
【国際特許分類】
【出願日】平成23年8月10日(2011.8.10)
【出願人】(308009277)株式会社ポッカコーポレーション (31)
【出願人】(304020292)国立大学法人徳島大学 (307)
【Fターム(参考)】
[ Back to top ]

