粘着性マイクロベシクルの除去方法
【課題】血液試料中における、人為的操作により活性化血小板より放出されるマイクロベシクルの特異的除去方法および血液中マイクロベシクルの適正な測定方法を提供。
【解決手段】血液由来試料のアルブミン前処理により、人為的操作により活性化された血小板より放出されるマイクロベシクルのみを排除し、血液中マイクロベシクルのみを測定。
【解決手段】血液由来試料のアルブミン前処理により、人為的操作により活性化された血小板より放出されるマイクロベシクルのみを排除し、血液中マイクロベシクルのみを測定。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、マイクロベシクル測定用の血液由来試料中において発生する粘着性マイクロベシクルを、採血前の血液中に存在する循環性マイクロベシクルの測定に影響しないように前処理する方法および循環性マイクロベシクルの適正な測定方法およびその測定試薬ないし測定キットに関する。
【背景技術】
【0002】
マイクロベシクルは、アテローム硬化症、播種性血管内血液凝固症候群などの血栓形成時において活性化した血小板から放出される。しかし、該マイクロベシクルは、膜表面のリン脂質に凝固因子が結合・濃縮されることによる血液凝固促進作用、単球・血小板・血管内皮細胞の活性化作用、或いは白血球−血小板・白血球−白血球・内皮細胞−白血球の接着促進作用などが知られており、単なる血小板活性化マーカーではなく、血栓形成、動脈硬化進展に深く関わっていると考えられている(非特許文献1参照)。従って、血液中のマイクロベシクルの量を測定することは、前記疾患の病状を経時的に推定する上での有力な診断手法の1つとして重要な位置を占めている。ところが、血小板は物理的刺激などにより容易に活性化され、これに伴いマイクロベシクルも活性化後の血小板から放出される。例えば、採血時の物理的ショックや血漿または血清の分離操作中に混在する血小板の活性化などにより臨床状態を反映しないマイクロベシクルが採血後の血液由来試料中に増加することがある。このようなマイクロベシクルは血液由来試料中のマイクロベシクル量を押し上げ、患者の病状を正確に判定する上で障害となる。従って、採血後に発生するマイクロベシクルの影響を排除して、採血前の血液中のマイクロベシクルを正確に測定する方法が求められていた。
【非特許文献1】Nomura S. Int. J.Hematol. 74, 397-404, (2001)
【発明の開示】
【発明が解決しようとする課題】
【0003】
本発明は、上記採血後の血液由来試料の調製時に発生するマイクロベシクル(粘着性マイクロベシクル)による問題点を解決するために、上記粘着性マイクロベシクルの除去方法、これを利用した血液中の循環性マイクロベシクルの適正な測定方法および測定試薬を提供することを目的としている。
【課題を解決するための手段】
【0004】
本発明者らは、斯かる実情に鑑み、鋭意研究を行った結果、BSA(ウシ血清アルブミン)を代表とするアルブミンが採血後に発生するマイクロベシクル(粘着性マイクロベシクル)と特異的に相互作用して免疫学的測定におけるその影響を排除し、採血前に存在したマイクロベシクル(循環性マイクロベシクル)のみを免疫学的手法により適正に測定し得ることを見出した。本発明は、前述成果に基づいて完成されたものであり、具体的には以下の発明を提供するものである。
項1. 血液由来試料中にアルブミンを添加することを特徴とする、採血後に発生した血液由来試料中の粘着性マイクロベシクルの影響を排除するための血液由来試料の前処理方法。
項2. アルブミンがBSAである項1に記載の方法。
項3. 血液由来試料にアルブミンを添加して採血後に発生した血液由来試料中の粘着性マイクロベシクルの影響を排除する工程、血液由来試料中の循環性マイクロベシクルを免疫学的に測定する工程を含む、血液由来試料中の循環性マイクロベシクルの免疫学的測定方法。
項4. 循環性マイクロベシクルに対する抗体をマイクロベシクル特異的表面エピトープに結合させ、その結果結合した抗体レベルを測定することにより、循環性マイクロベシクルの免疫学的測定を行う、項3に記載の方法。
項5. 前記表面エピトープが循環性マイクロベシクルの糖蛋白質上にある項4に記載の方法。
項6. 前記表面糖蛋白質がGpIb−IXである項5に記載の方法。
項7. 抗体の検出を、抗体に結合された標識または酵素に基づいて行うことを特徴とする項6記載の測定方法。
項8. 固層化したGpIXに対する抗体に循環性マイクロベシクルを結合させたのち、該マイクロベシクル上のGpIbを認識する抗体を作用させる手順を含むことを特徴とする項7に記載の方法。
項9. 少なくともアルブミン、抗GpIb標識抗体および抗GpIX抗体を含む血液由来試料中の循環性マイクロベシクル測定キット。
項10. アルブミンがBSAである項9記載のキット。
項11. 抗GpIX抗体をプレートにコーティングしてなる項9または10に記載のキット。
【0005】
本明細書において、患者血液中に存在するマイクロベシクルを「循環性マイクロベシクル」と呼び、採血時または採血後に人為的操作により活性化された血小板から放出されたマイクロベシクルをアルブミンに対する親和性より「粘着性マイクロベシクル」と呼ぶ。
【0006】
本発明において対象となる血液由来試料とは、血液又は血液から調製された血液成分を含む溶液を指し、血小板の除去操作を行なった試料が好ましい。具体的には、血漿を挙げることができ、該血液画分を測定上の観点から生理食塩水又は緩衝液などで希釈した溶液も含む。
【0007】
アルブミンは、ヒト又はヒト以外の哺乳動物又は鳥類由来アルブミンを指し、ヒト以外の哺乳動物としては、例えばウシ、ウマ、サル、イヌ、ウサギ、マウスなどを、鳥類としてはニワトリを代表例として上げることができる。特に、ウシ血清アルブミン(BSA)を代表例として上げることができ、この他にも、ヒト血清アルブミン(HSA)、卵白アルブミンなどを好適な例として挙げることができる。
【0008】
また、アルブミンの添加時期に関しては、測定前に血液由来試料に添加しても良く、ELISA法を例にとると、プレート上に抗体を固定化した後でも良い。また、添加形態としては特に制限はないが、液体状態で添加するのが望ましく、前もって生理食塩水又は、等張の緩衝液に溶解した後添加することができる。該アルブミン添加量としては、終濃度5%以上であることが望ましく、例えば終濃度5〜10%程度が例示される。また、添加後粘着性マイクロベシクルをアルブミンに吸着させるために静置または振盪処理することが好ましく、処理時間としては1時間以上、好適には4時間以上アルブミン処理を行なうことが望ましい。かくして、人為的に活性化された血小板より放出された粘着性マイクロベシクルはアルブミンと相互作用し、マイクロベシクル膜表面抗原を利用した抗体による免疫学的測定方法に対して、系外に排除され、循環性マイクロベシクルの測定に実質的に影響しないものとなる。
【0009】
本来の血液由来試料中の循環性マイクロベシクルに関しては、該アルブミン処理によっては実質的に影響を受けることなく、通常のマイクロベシクルの特性を利用した免疫学的測定方法により測定することが可能である。
【0010】
免疫学的測定方法としては、マイクロベシクルの膜表面の抗原性分子(エピトープ)に基づき、該エピトープに対する抗体を利用し、該分子を定量することによるマイクロベシクルを測定・定量する手法であれば制限なく用いることができる。例えば、ELISA法、RIA法、或いは凝集法を例示することができる。
【0011】
本発明による好ましい抗体としては、GpIb−GPIX複合体および/または個々の糖タンパク質GpIbおよびGpIXを含む糖タンパク質に対する抗体を挙げることができる。マイクロベシクル上にみられる他の血小板特異的糖タンパク質にはGpIa−IIa 、GpIIb−III aおよびGpIII bが含まれる。
【0012】
また、循環性マイクロベシクルに結合する抗体をそれ自体標識してもよく、あるいは第2抗体、例えばマウスモノクローナル抗体(第1抗体)に特異的に結合する標識された抗−マウス免疫グロブリンを用いてもよい。特に、ポリクローナル抗体およびモノクローナル抗体を問わないが、好ましくはモノクローナル抗体を使用することができる。 使用される標識は、信号を発することのできる任意の成分、例えば酵素(ペルオキシダーゼ、アルカリフォスファターゼ等)、発色団、発蛍光団(FITC等)、放射性同位元素、着色粒子、色素、コロイド状金属などであってよい。
【0013】
さらに、本発明の好ましい一態様としてBSAを用いたELISA法を例に取り以下に詳述する。
【0014】
前述の如く調製した血液由来成分を、予め抗GpIX抗体をコーティングしスキムミルク等によりブロッキング操作を行った96穴プレートの各ウエル上に、例えば10〜150μl添加し、次いで、BSA溶液を最終濃度5%以上になるように添加する。その後、新たに発生した粘着性マイクロベシクルをBSAに吸着させるために、室温又は、37℃にて例えば1時間以上、好ましくは4時間以上振盪下インキュベートする。その後、洗浄液例えば、0.02〜0.1%程度の Tween20/PBSで十分に洗浄を行う。次いで、ペルオキシダーゼ標識抗GpIb抗体を添加し、同洗浄液にて十分洗浄後、該酵素に対する基質を添加し、発色操作を行なう。かくして、循環性マイクロベシクルの量を膜表面エピトープGpIb−GpIX複合体にもとづく抗体を利用し、酵素反応により生じる発色基質量として、定量することが可能となる。該操作を通じて、人為的操作により発生した粘着性マイクロベシクルはBSAにトラップされた後は、当該一連の免疫操作を通じて、使用抗体には未反応となり、目的の本来血液中に存在する循環性マイクロベシクルのみを測定することが可能となる。
【0015】
また、上述操作上使用する各種抗体、試薬などを含む循環性マイクロベシクル測定キットを提供することができる。具体的には、人為的操作により発生する粘着性マイクロベシクルを効率よく除去するために、BSAを代表とするアルブミン、または該溶液、さらにはGpIbおよびGpIXに対する抗体に代表されるマイクロベシクル膜表面タンパク複合体に対する認識抗体(該認識抗体は、いずれか一方もしくは両方が標識化されている)、さらには必要に応じて2次抗体、酵素の基質(標識として酵素を使用した場合)などが該キットに含まれる。例えば、認識抗体がビオチン標識GpIbであれば、該測定キットには2次抗体としてペルオキシダーゼ標識アビジンを含み得る。また、該ペルオキシダーゼに対する基質等を含む循環性マイクロベシクル測定キットが提供できる。
【発明の効果】
【0016】
以下の実施例から明らかなように、本発明により従来血液処理操作の段階で、混在する血小板の活性化により放出される粘着性マイクロベシクルを、アルブミンで前処理することにより効率的に免疫測定系から除去でき、血液中に元々存在する循環性マイクロベシクルを測定できることが判明した。
【発明を実施するための最良の形態】
【0017】
以上の本発明を更に詳しく説明するため実施例を挙げる。なお、これらの実施例は、単なる例示目的として記載されており、本発明を限定するものではない。
【0018】
実施例1
方法:
1.擬陽性(活性化)サンプルの作製
循環性マイクロベシクル(PDMP)正常値を示す健常成人男性より3.8%クエン酸(チトラート)にて採血した全血を4℃の冷蔵庫に12時間保管し、新生PDMP(粘着性マイクロベシクル)を生成させた。冷蔵全血(2ml)を卓上遠心器にて3000rpm/20min遠心し、上清(600μl)を回収し、活性化サンプルとした。活性化サンプルはsalineでx2とx4倍に希釈し、ELISA測定を行った。
2.高値検体の調製
PDMP高値を示す被験者(成人男性)よりEDTA/ACD(クエン酸−デキストロース溶液)採血(2ml)を行い、卓上遠心器にて3000rpm/20min室温で遠心し、上清(600μl)を回収した。高値検体はsalineでx2とx4倍に希釈し、ELISA測定を行った。
3.正常検体の調製
PDMP正常値を示す健常成人男性よりEDTA/ACD採血(2ml)を行い、卓上遠心器にて3000rpm/20min室温で遠心し、上清(600μl)を回収し、ELISA測定を行った。
4.ELISA測定
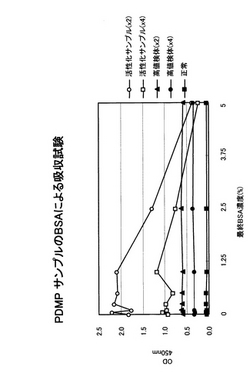
血小板膜表面に存在する糖蛋白質のうち、血小板特異的な分子であるCD42b(GpIb)とCD42a(GpIX)に対する抗体(抗CD42b抗体;NNKY5-5、抗CD42a抗体;KMP-9)を用いたサンドイッチELISA測定系を作成した。抗CD42a抗体をコーティングしたELISA用の96穴タイタープレート(コーニング社製:MaxiSorb)に、活性化サンプルおよび高値検体50μlを添加後、各サンプルに50μlのPBSおよび2.5%、5%、7.5%、10%のBSAを添加し、終濃度1.25%、2.5%、3.75%、5%のBSAが添加されたwellを作成した。室温で振盪下4時間インキュベーションした後、サンプルを洗浄液(0.05% Tween 20/ PBS)で洗浄した。ビオチン化した抗CD42b抗体を添加し、ペルオキシダーゼ標識アビジンで発色させ、450nmの吸光度をイムノリーダーで測定した(図1)。
結果:
擬陽性を示す活性化サンプルは、測定時にwellに添加されたBSA濃度依存的に測定値が低下し、その値はBSAの最終濃度が5%の時に正常検体近くまで下がった。一方、元々高いPDMP値を示す高値検体は、BSAの濃度に関係なく一定の値を示した。これらの結果より、採血後の操作によって生じる新生PDMPのみを、測定時終濃度5%のBSAを添加する事により除去できる事が確認できた。
【図面の簡単な説明】
【0019】
【図1】図1は、人為的に活性化させたサンプル、マイクロベシクル高値患者由来サンプルおよび正常サンプルを用いたBSAによる粘着性マイクロベシクルの吸収試験を示した図である。
【技術分野】
【0001】
本発明は、マイクロベシクル測定用の血液由来試料中において発生する粘着性マイクロベシクルを、採血前の血液中に存在する循環性マイクロベシクルの測定に影響しないように前処理する方法および循環性マイクロベシクルの適正な測定方法およびその測定試薬ないし測定キットに関する。
【背景技術】
【0002】
マイクロベシクルは、アテローム硬化症、播種性血管内血液凝固症候群などの血栓形成時において活性化した血小板から放出される。しかし、該マイクロベシクルは、膜表面のリン脂質に凝固因子が結合・濃縮されることによる血液凝固促進作用、単球・血小板・血管内皮細胞の活性化作用、或いは白血球−血小板・白血球−白血球・内皮細胞−白血球の接着促進作用などが知られており、単なる血小板活性化マーカーではなく、血栓形成、動脈硬化進展に深く関わっていると考えられている(非特許文献1参照)。従って、血液中のマイクロベシクルの量を測定することは、前記疾患の病状を経時的に推定する上での有力な診断手法の1つとして重要な位置を占めている。ところが、血小板は物理的刺激などにより容易に活性化され、これに伴いマイクロベシクルも活性化後の血小板から放出される。例えば、採血時の物理的ショックや血漿または血清の分離操作中に混在する血小板の活性化などにより臨床状態を反映しないマイクロベシクルが採血後の血液由来試料中に増加することがある。このようなマイクロベシクルは血液由来試料中のマイクロベシクル量を押し上げ、患者の病状を正確に判定する上で障害となる。従って、採血後に発生するマイクロベシクルの影響を排除して、採血前の血液中のマイクロベシクルを正確に測定する方法が求められていた。
【非特許文献1】Nomura S. Int. J.Hematol. 74, 397-404, (2001)
【発明の開示】
【発明が解決しようとする課題】
【0003】
本発明は、上記採血後の血液由来試料の調製時に発生するマイクロベシクル(粘着性マイクロベシクル)による問題点を解決するために、上記粘着性マイクロベシクルの除去方法、これを利用した血液中の循環性マイクロベシクルの適正な測定方法および測定試薬を提供することを目的としている。
【課題を解決するための手段】
【0004】
本発明者らは、斯かる実情に鑑み、鋭意研究を行った結果、BSA(ウシ血清アルブミン)を代表とするアルブミンが採血後に発生するマイクロベシクル(粘着性マイクロベシクル)と特異的に相互作用して免疫学的測定におけるその影響を排除し、採血前に存在したマイクロベシクル(循環性マイクロベシクル)のみを免疫学的手法により適正に測定し得ることを見出した。本発明は、前述成果に基づいて完成されたものであり、具体的には以下の発明を提供するものである。
項1. 血液由来試料中にアルブミンを添加することを特徴とする、採血後に発生した血液由来試料中の粘着性マイクロベシクルの影響を排除するための血液由来試料の前処理方法。
項2. アルブミンがBSAである項1に記載の方法。
項3. 血液由来試料にアルブミンを添加して採血後に発生した血液由来試料中の粘着性マイクロベシクルの影響を排除する工程、血液由来試料中の循環性マイクロベシクルを免疫学的に測定する工程を含む、血液由来試料中の循環性マイクロベシクルの免疫学的測定方法。
項4. 循環性マイクロベシクルに対する抗体をマイクロベシクル特異的表面エピトープに結合させ、その結果結合した抗体レベルを測定することにより、循環性マイクロベシクルの免疫学的測定を行う、項3に記載の方法。
項5. 前記表面エピトープが循環性マイクロベシクルの糖蛋白質上にある項4に記載の方法。
項6. 前記表面糖蛋白質がGpIb−IXである項5に記載の方法。
項7. 抗体の検出を、抗体に結合された標識または酵素に基づいて行うことを特徴とする項6記載の測定方法。
項8. 固層化したGpIXに対する抗体に循環性マイクロベシクルを結合させたのち、該マイクロベシクル上のGpIbを認識する抗体を作用させる手順を含むことを特徴とする項7に記載の方法。
項9. 少なくともアルブミン、抗GpIb標識抗体および抗GpIX抗体を含む血液由来試料中の循環性マイクロベシクル測定キット。
項10. アルブミンがBSAである項9記載のキット。
項11. 抗GpIX抗体をプレートにコーティングしてなる項9または10に記載のキット。
【0005】
本明細書において、患者血液中に存在するマイクロベシクルを「循環性マイクロベシクル」と呼び、採血時または採血後に人為的操作により活性化された血小板から放出されたマイクロベシクルをアルブミンに対する親和性より「粘着性マイクロベシクル」と呼ぶ。
【0006】
本発明において対象となる血液由来試料とは、血液又は血液から調製された血液成分を含む溶液を指し、血小板の除去操作を行なった試料が好ましい。具体的には、血漿を挙げることができ、該血液画分を測定上の観点から生理食塩水又は緩衝液などで希釈した溶液も含む。
【0007】
アルブミンは、ヒト又はヒト以外の哺乳動物又は鳥類由来アルブミンを指し、ヒト以外の哺乳動物としては、例えばウシ、ウマ、サル、イヌ、ウサギ、マウスなどを、鳥類としてはニワトリを代表例として上げることができる。特に、ウシ血清アルブミン(BSA)を代表例として上げることができ、この他にも、ヒト血清アルブミン(HSA)、卵白アルブミンなどを好適な例として挙げることができる。
【0008】
また、アルブミンの添加時期に関しては、測定前に血液由来試料に添加しても良く、ELISA法を例にとると、プレート上に抗体を固定化した後でも良い。また、添加形態としては特に制限はないが、液体状態で添加するのが望ましく、前もって生理食塩水又は、等張の緩衝液に溶解した後添加することができる。該アルブミン添加量としては、終濃度5%以上であることが望ましく、例えば終濃度5〜10%程度が例示される。また、添加後粘着性マイクロベシクルをアルブミンに吸着させるために静置または振盪処理することが好ましく、処理時間としては1時間以上、好適には4時間以上アルブミン処理を行なうことが望ましい。かくして、人為的に活性化された血小板より放出された粘着性マイクロベシクルはアルブミンと相互作用し、マイクロベシクル膜表面抗原を利用した抗体による免疫学的測定方法に対して、系外に排除され、循環性マイクロベシクルの測定に実質的に影響しないものとなる。
【0009】
本来の血液由来試料中の循環性マイクロベシクルに関しては、該アルブミン処理によっては実質的に影響を受けることなく、通常のマイクロベシクルの特性を利用した免疫学的測定方法により測定することが可能である。
【0010】
免疫学的測定方法としては、マイクロベシクルの膜表面の抗原性分子(エピトープ)に基づき、該エピトープに対する抗体を利用し、該分子を定量することによるマイクロベシクルを測定・定量する手法であれば制限なく用いることができる。例えば、ELISA法、RIA法、或いは凝集法を例示することができる。
【0011】
本発明による好ましい抗体としては、GpIb−GPIX複合体および/または個々の糖タンパク質GpIbおよびGpIXを含む糖タンパク質に対する抗体を挙げることができる。マイクロベシクル上にみられる他の血小板特異的糖タンパク質にはGpIa−IIa 、GpIIb−III aおよびGpIII bが含まれる。
【0012】
また、循環性マイクロベシクルに結合する抗体をそれ自体標識してもよく、あるいは第2抗体、例えばマウスモノクローナル抗体(第1抗体)に特異的に結合する標識された抗−マウス免疫グロブリンを用いてもよい。特に、ポリクローナル抗体およびモノクローナル抗体を問わないが、好ましくはモノクローナル抗体を使用することができる。 使用される標識は、信号を発することのできる任意の成分、例えば酵素(ペルオキシダーゼ、アルカリフォスファターゼ等)、発色団、発蛍光団(FITC等)、放射性同位元素、着色粒子、色素、コロイド状金属などであってよい。
【0013】
さらに、本発明の好ましい一態様としてBSAを用いたELISA法を例に取り以下に詳述する。
【0014】
前述の如く調製した血液由来成分を、予め抗GpIX抗体をコーティングしスキムミルク等によりブロッキング操作を行った96穴プレートの各ウエル上に、例えば10〜150μl添加し、次いで、BSA溶液を最終濃度5%以上になるように添加する。その後、新たに発生した粘着性マイクロベシクルをBSAに吸着させるために、室温又は、37℃にて例えば1時間以上、好ましくは4時間以上振盪下インキュベートする。その後、洗浄液例えば、0.02〜0.1%程度の Tween20/PBSで十分に洗浄を行う。次いで、ペルオキシダーゼ標識抗GpIb抗体を添加し、同洗浄液にて十分洗浄後、該酵素に対する基質を添加し、発色操作を行なう。かくして、循環性マイクロベシクルの量を膜表面エピトープGpIb−GpIX複合体にもとづく抗体を利用し、酵素反応により生じる発色基質量として、定量することが可能となる。該操作を通じて、人為的操作により発生した粘着性マイクロベシクルはBSAにトラップされた後は、当該一連の免疫操作を通じて、使用抗体には未反応となり、目的の本来血液中に存在する循環性マイクロベシクルのみを測定することが可能となる。
【0015】
また、上述操作上使用する各種抗体、試薬などを含む循環性マイクロベシクル測定キットを提供することができる。具体的には、人為的操作により発生する粘着性マイクロベシクルを効率よく除去するために、BSAを代表とするアルブミン、または該溶液、さらにはGpIbおよびGpIXに対する抗体に代表されるマイクロベシクル膜表面タンパク複合体に対する認識抗体(該認識抗体は、いずれか一方もしくは両方が標識化されている)、さらには必要に応じて2次抗体、酵素の基質(標識として酵素を使用した場合)などが該キットに含まれる。例えば、認識抗体がビオチン標識GpIbであれば、該測定キットには2次抗体としてペルオキシダーゼ標識アビジンを含み得る。また、該ペルオキシダーゼに対する基質等を含む循環性マイクロベシクル測定キットが提供できる。
【発明の効果】
【0016】
以下の実施例から明らかなように、本発明により従来血液処理操作の段階で、混在する血小板の活性化により放出される粘着性マイクロベシクルを、アルブミンで前処理することにより効率的に免疫測定系から除去でき、血液中に元々存在する循環性マイクロベシクルを測定できることが判明した。
【発明を実施するための最良の形態】
【0017】
以上の本発明を更に詳しく説明するため実施例を挙げる。なお、これらの実施例は、単なる例示目的として記載されており、本発明を限定するものではない。
【0018】
実施例1
方法:
1.擬陽性(活性化)サンプルの作製
循環性マイクロベシクル(PDMP)正常値を示す健常成人男性より3.8%クエン酸(チトラート)にて採血した全血を4℃の冷蔵庫に12時間保管し、新生PDMP(粘着性マイクロベシクル)を生成させた。冷蔵全血(2ml)を卓上遠心器にて3000rpm/20min遠心し、上清(600μl)を回収し、活性化サンプルとした。活性化サンプルはsalineでx2とx4倍に希釈し、ELISA測定を行った。
2.高値検体の調製
PDMP高値を示す被験者(成人男性)よりEDTA/ACD(クエン酸−デキストロース溶液)採血(2ml)を行い、卓上遠心器にて3000rpm/20min室温で遠心し、上清(600μl)を回収した。高値検体はsalineでx2とx4倍に希釈し、ELISA測定を行った。
3.正常検体の調製
PDMP正常値を示す健常成人男性よりEDTA/ACD採血(2ml)を行い、卓上遠心器にて3000rpm/20min室温で遠心し、上清(600μl)を回収し、ELISA測定を行った。
4.ELISA測定
血小板膜表面に存在する糖蛋白質のうち、血小板特異的な分子であるCD42b(GpIb)とCD42a(GpIX)に対する抗体(抗CD42b抗体;NNKY5-5、抗CD42a抗体;KMP-9)を用いたサンドイッチELISA測定系を作成した。抗CD42a抗体をコーティングしたELISA用の96穴タイタープレート(コーニング社製:MaxiSorb)に、活性化サンプルおよび高値検体50μlを添加後、各サンプルに50μlのPBSおよび2.5%、5%、7.5%、10%のBSAを添加し、終濃度1.25%、2.5%、3.75%、5%のBSAが添加されたwellを作成した。室温で振盪下4時間インキュベーションした後、サンプルを洗浄液(0.05% Tween 20/ PBS)で洗浄した。ビオチン化した抗CD42b抗体を添加し、ペルオキシダーゼ標識アビジンで発色させ、450nmの吸光度をイムノリーダーで測定した(図1)。
結果:
擬陽性を示す活性化サンプルは、測定時にwellに添加されたBSA濃度依存的に測定値が低下し、その値はBSAの最終濃度が5%の時に正常検体近くまで下がった。一方、元々高いPDMP値を示す高値検体は、BSAの濃度に関係なく一定の値を示した。これらの結果より、採血後の操作によって生じる新生PDMPのみを、測定時終濃度5%のBSAを添加する事により除去できる事が確認できた。
【図面の簡単な説明】
【0019】
【図1】図1は、人為的に活性化させたサンプル、マイクロベシクル高値患者由来サンプルおよび正常サンプルを用いたBSAによる粘着性マイクロベシクルの吸収試験を示した図である。
【特許請求の範囲】
【請求項1】
血液由来試料中にアルブミンを添加することを特徴とする、採血後に発生した血液由来試料中の粘着性マイクロベシクルの影響を排除するための血液由来試料の前処理方法。
【請求項2】
アルブミンがBSAである請求項1に記載の方法。
【請求項3】
血液由来試料にアルブミンを添加して採血後に発生した血液由来試料中の粘着性マイクロベシクルの影響を排除する工程、血液由来試料中の循環性マイクロベシクルを免疫学的に測定する工程を含む、血液由来試料中の循環性マイクロベシクルの免疫学的測定方法。
【請求項4】
循環性マイクロベシクルに対する抗体をマイクロベシクル特異的表面エピトープに結合させ、その結果結合した抗体レベルを測定することにより、循環性マイクロベシクルの免疫学的測定を行う、請求項3に記載の方法。
【請求項5】
前記表面エピトープが循環性マイクロベシクルの糖蛋白質上にある請求項4に記載の方法。
【請求項6】
前記表面糖蛋白質がGpIb−IXである請求項5に記載の方法。
【請求項7】
抗体の検出を、抗体に結合された標識または酵素に基づいて行うことを特徴とする請求項6記載の測定方法。
【請求項8】
固層化したGpIXに対する抗体に循環性マイクロベシクルを結合させたのち、該マイクロベシクル上のGpIbを認識する抗体を作用させる手順を含むことを特徴とする請求項7に記載の方法。
【請求項9】
少なくともアルブミン、抗GpIb標識抗体および抗GpIX抗体を含む血液由来試料中の循環性マイクロベシクル測定キット。
【請求項10】
アルブミンがBSAである請求項9記載のキット。
【請求項11】
抗GpIX抗体をプレートにコーティングしてなる請求項9または10に記載のキット。
【請求項1】
血液由来試料中にアルブミンを添加することを特徴とする、採血後に発生した血液由来試料中の粘着性マイクロベシクルの影響を排除するための血液由来試料の前処理方法。
【請求項2】
アルブミンがBSAである請求項1に記載の方法。
【請求項3】
血液由来試料にアルブミンを添加して採血後に発生した血液由来試料中の粘着性マイクロベシクルの影響を排除する工程、血液由来試料中の循環性マイクロベシクルを免疫学的に測定する工程を含む、血液由来試料中の循環性マイクロベシクルの免疫学的測定方法。
【請求項4】
循環性マイクロベシクルに対する抗体をマイクロベシクル特異的表面エピトープに結合させ、その結果結合した抗体レベルを測定することにより、循環性マイクロベシクルの免疫学的測定を行う、請求項3に記載の方法。
【請求項5】
前記表面エピトープが循環性マイクロベシクルの糖蛋白質上にある請求項4に記載の方法。
【請求項6】
前記表面糖蛋白質がGpIb−IXである請求項5に記載の方法。
【請求項7】
抗体の検出を、抗体に結合された標識または酵素に基づいて行うことを特徴とする請求項6記載の測定方法。
【請求項8】
固層化したGpIXに対する抗体に循環性マイクロベシクルを結合させたのち、該マイクロベシクル上のGpIbを認識する抗体を作用させる手順を含むことを特徴とする請求項7に記載の方法。
【請求項9】
少なくともアルブミン、抗GpIb標識抗体および抗GpIX抗体を含む血液由来試料中の循環性マイクロベシクル測定キット。
【請求項10】
アルブミンがBSAである請求項9記載のキット。
【請求項11】
抗GpIX抗体をプレートにコーティングしてなる請求項9または10に記載のキット。
【図1】




【公開番号】特開2006−38567(P2006−38567A)
【公開日】平成18年2月9日(2006.2.9)
【国際特許分類】
【出願番号】特願2004−217387(P2004−217387)
【出願日】平成16年7月26日(2004.7.26)
【出願人】(000206956)大塚製薬株式会社 (230)
【出願人】(000153258)株式会社JIMRO (6)
【公開日】平成18年2月9日(2006.2.9)
【国際特許分類】
【出願日】平成16年7月26日(2004.7.26)
【出願人】(000206956)大塚製薬株式会社 (230)
【出願人】(000153258)株式会社JIMRO (6)
[ Back to top ]

