細胞凝集塊の形成方法
【課題】接着性細胞の細胞凝集塊の形成方法、該方法を用いる物質のスクリーニング方法及び細胞の機能探索方法、細胞凝集塊並びに培養容器の提供。
【解決手段】細胞凝集塊用培養容器Dは、アミノ基、カルボキシル基及び/又はヒドロキシル基が表面近傍に存在する領域と、一般式

で表される基を底面に有する。
【解決手段】細胞凝集塊用培養容器Dは、アミノ基、カルボキシル基及び/又はヒドロキシル基が表面近傍に存在する領域と、一般式

で表される基を底面に有する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、細胞凝集塊の形成方法、物質のスクリーニング方法、細胞の機能探索方法、細胞凝集塊及び培養容器に関する。
【背景技術】
【0002】
従来、接着性細胞及び非接着性細胞を培養することにより、細胞凝集塊が形成されている。
【0003】
特許文献1には、多能性神経幹細胞を含む組織を少なくとも一種の幹細胞増殖因子を含む培地に懸濁し、神経幹細胞凝集塊形成用容器に播種、培養する事により神経幹細胞凝集塊を形成させる方法が開示されている。このとき、神経幹細胞凝集塊形成用容器は、内面に非水溶性硬化皮膜層を有し、水溶性樹脂を容器内面に被覆させて水溶性樹脂被覆層を形成した後に、水溶性樹脂被覆層を硬化させて非水溶性硬化皮膜層に変性することにより製造される。また、水溶性樹脂として、2−メタクリロイルオキシエチルホスホリルコリンと他のモノマー(例えば、ブチルメタクリレート等)との共重合体が例示されている。
【0004】
しかしながら、このような神経幹細胞凝集塊形成用容器を用いて、接着性細胞を培養しても、非水溶性硬化皮膜層が接着性細胞の接着を阻害するため、接着性細胞が死滅し、接着性細胞の細胞凝集塊を形成することができないという問題がある。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2008−220205号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明は、上記の従来技術が有する問題に鑑み、接着性細胞の細胞凝集塊を形成することが可能な細胞凝集塊の形成方法、該細胞凝集塊の形成方法を用いる物質のスクリーニング方法及び細胞の機能探索方法、細胞凝集塊並びに培養容器を提供することを目的とする。
【課題を解決するための手段】
【0007】
本発明の細胞凝集塊の形成方法は、培養容器を用いて、接着性細胞を培養して細胞凝集塊を形成する方法であって、前記培養容器は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式
【0008】
【化1】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1以上6以下のアルキル基であり、mは、2以上6以下の整数である。)
で表される基が表面近傍に存在し、前記接着性細胞は、間葉系幹細胞、肝細胞又はガン細胞である。
【0009】
本発明の物質のスクリーニング方法は、本発明の細胞凝集塊の形成方法を用いて、細胞凝集塊を形成する工程と、該細胞凝集塊を用いて物質をスクリーニングする工程を有する。
【0010】
本発明の細胞の機能探索方法は、本発明の細胞凝集塊の形成方法を用いて、細胞凝集塊を形成する工程と、該細胞凝集塊を用いて細胞の機能を探索する工程を有する。
【0011】
本発明の細胞凝集塊は、接着性細胞が増殖して自律的に凝集した細胞凝集塊であって、前記接着性細胞は、間葉系幹細胞、肝細胞又はガン細胞である。
【0012】
本発明の培養容器は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式
【0013】
【化2】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1以上6以下のアルキル基であり、mは、2以上6以下の整数である。)
で表される基が表面近傍に存在する。
【発明の効果】
【0014】
本発明によれば、接着性細胞の細胞凝集塊を形成することが可能な細胞凝集塊の形成方法、該細胞凝集塊の形成方法を用いる物質のスクリーニング方法及び細胞の機能探索方法、細胞凝集塊並びに培養容器を提供することができる。
【図面の簡単な説明】
【0015】
【図1A】本発明の細胞凝集塊を形成する方法の一例を示す図(その1)である。
【図1B】本発明の細胞凝集塊を形成する方法の一例を示す図(その2)である。
【図2A】実施例1の細胞凝集塊(2日間培養した場合)を示す光学顕微鏡写真である。
【図2B】実施例1の細胞凝集塊(5日間培養した場合)を示す光学顕微鏡写真である。
【図3】比較例1の培養細胞(5日間培養した場合)を示す光学顕微鏡写真である。
【図4A】実施例1の細胞凝集塊のアルカリホスファターゼ活性の評価結果を示す光学顕微鏡写真である。
【図4B】比較例1の培養細胞のアルカリホスファターゼ活性の評価結果を示す光学顕微鏡写真である。
【図5】実施例1の細胞凝集塊の免疫二重染色の評価結果(その1)を示す蛍光顕微鏡写真である。
【図6】実施例1の細胞凝集塊の免疫二重染色の評価結果(その2)を示す蛍光顕微鏡写真である。
【図7】実施例1の細胞凝集塊の免疫二重染色の評価結果(その3)を示す蛍光顕微鏡写真である。
【図8】実施例1の細胞凝集塊の免疫二重染色の評価結果(その4)を示す蛍光顕微鏡写真である。
【図9】実施例2−1の細胞凝集塊(2日間培養した場合)を示す光学顕微鏡写真である。
【図10】実施例2−2の細胞凝集塊(7日間培養した場合)を示す光学顕微鏡写真である。
【図11】実施例2−3の細胞凝集塊(7日間培養した場合)を示す光学顕微鏡写真である。
【図12】比較例2の培養細胞(7日間培養した場合)を示す光学顕微鏡写真である。
【図13】実施例2−2の細胞凝集塊の免疫染色の評価結果を示す写真である。
【図14】実施例3の細胞凝集塊(11日間培養した場合)を示す光学顕微鏡写真である。
【図15】比較例3の培養細胞(11日間培養した場合)を示す光学顕微鏡写真である。
【図16】実施例3の細胞凝集塊及び比較例3の培養細胞のアルブミンの産生量の評価結果を示す図である。
【図17】実施例3の細胞凝集塊及び比較例3の培養細胞のCYP1A1の活性の評価結果を示す図である。
【図18】実施例3の細胞凝集塊及び比較例3の培養細胞の遺伝子発現の評価結果を示す図である。
【図19】実施例4の細胞凝集塊(8日間培養した場合)を示す光学顕微鏡写真である。
【図20】比較例4の培養細胞(8日間培養した場合)を示す光学顕微鏡写真である。
【図21A】実施例4の細胞凝集塊のアルカリホスファターゼ活性の評価結果を示す光学顕微鏡写真である。
【図21B】比較例4の培養細胞のアルカリホスファターゼ活性の評価結果を示す光学顕微鏡写真である。
【図22】実施例4の細胞凝集塊及び比較例4の培養細胞の遺伝子発現の評価結果を示す図である。
【発明を実施するための形態】
【0016】
次に、本発明を実施するための形態を図面と共に説明する。
【0017】
図1に、本発明の細胞凝集塊を形成する方法の一例を示す。
【0018】
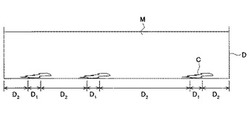
培養容器Dは、アミノ基、カルボキシル基及び/又はヒドロキシル基が表面近傍に存在する領域D1と、一般式(1)で表される基が表面近傍に存在する領域D2を底面に有する。
【0019】
培養容器Dに、接着性細胞C及び培地Mを添加すると、培養容器Dの底面に接着性細胞Cが接着する(図1A参照)。これは、培養容器Dの底面のアミノ基、カルボキシル基及び/又はヒドロキシル基が表面近傍に存在する領域D1に接着性細胞Cが接着するためであると考えられる。次に、接着性細胞Cを培養すると、接着性細胞Cが増殖して自律的に凝集し、細胞凝集塊C'が形成される(図1B参照)。これは、培養容器Dの底面の一般式(1)で表される基が表面近傍に存在する領域D2は、接着性細胞Cの接着を抑制するため、接着性細胞C上に、増殖した接着性細胞Cが形成されるためであると考えられる。このため、培養容器Dを用いて、接着性細胞Cを培養すると、接着性細胞Cが増殖して自律的に凝集した細胞凝集塊C'を形成することができる。
【0020】
接着性細胞Cとしては、特に限定されないが、間葉系幹細胞、肝細胞、肝幹細胞、心筋細胞、ガン細胞、ガン幹細胞、繊維芽細胞、神経細胞、血管内皮前駆細胞、上皮細胞等が挙げられる。
【0021】
培養容器Dの形態としては、特に限定されないが、ディッシュ、マルチウェルプレート、フラスコ、ローラーボトル、細胞培養プロセスを有するデバイスのユニット等が挙げられる。
【0022】
[培養容器Dの第一の実施形態]
培養容器Dの第一の実施形態は、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器に、カルボキシル基、アミノ基又はヒドロキシル基に対して反応性を有する基と、一般式(1)で表される基を有する表面改質剤を反応させることにより製造されている。このとき、表面改質剤の分子量は、225〜650である。これにより、一般式(1)で表される基を高密度で導入することができる。
【0023】
容器の表面近傍にアミノ基を導入する方法としては、特に限定されないが、窒素プラズマ処理、アンモニアプラズマ処理、表面処理剤を反応させる方法、シリコーン気相処理等が挙げられる。
【0024】
窒素プラズマ処理では、窒素ガス雰囲気下、低温プラズマを発生させることにより、容器の表面近傍にアミノ基を導入する(例えば、Surface and Coatings Technology 116−119(1999)802−807,Colloids and Surfaces A:Physicochem.Eng.Aspects 195(2001)81−95,Macromol.Chem.Phys.200.989−996(1999)参照)。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、窒素ガスを導入し、グロー放電を行う。
【0025】
アンモニアプラズマ処理では、アンモニアガス雰囲気下、低温プラズマを発生させることにより、容器の表面近傍にアミノ基を導入する。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、アンモニアガスを導入し、グロー放電を行う。
【0026】
容器を構成する材料としては、特に限定されないが、ポリ塩化ビニル、アクリル樹脂、ポリスチレン、ポリプロピレン、ポリエチレン、ポリエステル、シクロオレフィン樹脂、ポリカーボネート、ガラス等が挙げられる。
【0027】
表面処理剤を反応させる方法では、アミノ基を有するアルコキシシラン、クロロシラン、シラザン等の表面処理剤を用いて、アルコキシシリル基等の加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器の表面近傍にアミノ基を導入する。具体的には、まず、容器内に水/2−プロパノール混合液を仕込み、3−アミノプロピルトリメトキシシランを添加した後、100℃に加熱し、6時間反応させる。次に、室温に冷却した後、メタノールで洗浄し、乾燥する。
【0028】
容器を構成する材料としては、特に限定されないが、メタクリル酸3−トリメトキシシリルプロピル−メタクリル酸メチル−ジビニルベンゼン共重合体、ポリ塩化ビニル、アクリル樹脂、ポリスチレン、ポリプロピレン、ポリエチレン、ポリエステル、シクロオレフィン樹脂、ポリカーボネート、シリカ、ガラス、アルミナ、タルク、クレー、マイカ、アスベスト、酸化チタン、亜鉛華、酸化鉄等が挙げられる。
【0029】
シリコーン気相処理では、1,3,5,7−テトラメチルシクロテトラシロキサンを用いて、容器の表面近傍にヒドロシリル基を導入した後、アミノ基を有するアルケンを反応させることにより、容器の表面近傍にアミノ基を導入する(例えば、特公平1−54379号公報、特公平1−54380号公報、特公平1−54381号公報参照)。具体的には、まず、1,3,5,7−テトラメチルシクロテトラシロキサンと、容器をデシケーター中に入れ、アスピレーターで脱気する。次に、80℃で16時間反応させた後、容器を取り出し、120℃で乾燥させる。さらに、得られた容器をエタノール中に浸し、アリルアミンを添加した後、塩化白金酸のエタノール溶液を添加し、60℃で2時間攪拌する。反応が終了した後、エタノールで洗浄し、減圧乾燥する。
【0030】
容器を構成する材料としては、特に限定されないが、スチレン−ジビニルベンゼン共重合体、ポリ塩化ビニル、アクリル樹脂、ポリスチレン、ポリプロピレン、ポリエチレン、ポリエステル、シクロオレフィン樹脂、ポリカーボネート、マイカ、タルク、カオリン、アルミナ、酸化チタン、酸化亜鉛、酸化鉄等が挙げられる。
【0031】
アミノ基を有するアルケンとしては、アリルアミンに限定されず、ビニル基を有するアミン、アクリル基を有するアミン等であればよい。また、アミノ基は、ブトキシカルボニル基、ベンジルオキシカルボニル基等により保護されていてもよい。さらに、アミノ基を有するアルケンの代わりに、エポキシ基等の、例えば、ジアミンとの反応により、アミノ基を導入することが可能な基を有するアルケンを用いてもよい。
【0032】
容器の表面近傍にカルボキシル基及び/又はヒドロキシル基を導入する方法としては、特に限定されないが、酸素プラズマ処理、オゾン処理、水蒸気プラズマ処理等が挙げられる。
【0033】
酸素プラズマ処理では、酸素ガスの雰囲気下、低温プラズマを発生させることにより、容器の表面近傍にカルボキシル基及びヒドロキシル基を導入する。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、酸素ガスを導入し、グロー放電する。
【0034】
オゾン処理では、容器にオゾン水溶液を仕込むことにより、容器の表面近傍にカルボキシル基及びヒドロキシル基を導入する。具体的には、容器に40ppmのオゾン水溶液を仕込み、室温で15分間処理する。
【0035】
水蒸気プラズマ処理では、水蒸気の雰囲気下、低温プラズマを発生させることにより、容器の表面近傍にヒドロキシル基を導入する。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、水蒸気を導入し、グロー放電する。
【0036】
容器を構成する材料としては、特に限定されないが、ポリスチレン、ポリエチレンテレフタレート、ポリカーボネート、ポリメタクリル酸メチル、ポリテトラフルオロエチレン、ポリエーテルエーテルケトン、シクロオレフィン樹脂、ポリカーボネート等が挙げられる。
【0037】
容器の表面近傍にカルボキシル基を導入する方法としては、特に限定されないが、表面処理剤を反応させる方法、シリコーン気相処理等が挙げられる。
【0038】
表面処理剤を反応させる方法では、カルボキシル基を有するアルコキシシラン、クロロシラン、シラザン等の表面処理剤を用いて、アルコキシシリル基等の加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器の表面近傍にカルボキシル基を導入する。具体的には、まず、トリエトキシシリルプロピル無水コハク酸をN,N−ジメチルホルムアミドに溶解させ、蒸留水と4−ジメチルアミノピリジンを添加し、16時間室温で撹拌し、カルボンキシル基を有するシランカップリング剤を合成する。次に、容器に水/2−プロパノール混合液を仕込み、カルボキシル基を有するシランカップリング剤を添加した後、100℃に加熱し、6時間反応させる。さらに、室温に冷却した後、メタノールで洗浄し、乾燥する。
【0039】
容器を構成する材料としては、特に限定されないが、メタクリル酸3−トリメトキシシリルプロピル−メタクリル酸メチル−ジビニルベンゼン共重合体、シリカ、ガラス、アルミナ、タルク、クレー、マイカ、アスベスト、酸化チタン、亜鉛華、酸化鉄等が挙げられる。
【0040】
シリコーン気相処理では、1,3,5,7−テトラメチルシクロテトラシロキサンを用いて、容器の表面近傍にヒドロシリル基を導入した後、カルボキシル基を有するアルケンを反応させることにより、容器の表面近傍にカルボキシル基を導入する(例えば、特公平1−54379号公報、特公平1−54380号公報、特公平1−54381号公報参照)。具体的には、まず、1,3,5,7−テトラメチルシクロテトラシロキサンを入れた容器をデシケーター中に入れ、アスピレーターで脱気する。次に、80℃で16時間反応させた後、容器を取り出し、120℃で乾燥させる。さらに、得られた容器をエタノール中に浸し、アリルカルボン酸を添加した後、塩化白金酸のエタノール溶液を添加し、60℃で2時間攪拌する。反応が終了した後、エタノールで洗浄し、減圧乾燥する。
【0041】
容器を構成する材料としては、特に限定されないが、スチレン−ジビニルベンゼン共重合体、マイカ、タルク、カオリン、アルミナ、酸化チタン、酸化亜鉛、酸化鉄等が挙げられる。
【0042】
カルボキシル基を有するアルケンとしては、アリルカルボン酸に限定されず、ビニル基を有するカルボン酸、アクリル基を有するカルボン酸等であればよい。
【0043】
容器の表面近傍にアミノ基、カルボキシル基及びヒドロキシル基を導入する方法としては、特に限定されないが、酸素ガス及びアンモニアガスを含む雰囲気下でプラズマ処理する方法等が挙げられる。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、酸素ガス及びアンモニアガスを導入し、グロー放電を行い、低温プラズマを発生させる。
【0044】
カルボキシル基に対して反応性を有する基としては、アミノ基、ヒドロキシル基等が挙げられるが、反応性が高いことから、アミノ基が好ましい。
【0045】
アミノ基又はヒドロキシル基に対して反応性を有する基としては、カルボキシル基、アルデヒド基等が挙げられるが、反応性が高いことから、カルボキシル基が好ましい。
【0046】
また、表面改質剤は、カルボキシル基、アミノ基又はヒドロキシル基に対して反応性を有する基がスペーサーを介して、一般式(1)で表される基に結合されていることが好ましい。スペーサーとしては、特に限定されないが、メチレン基、オキシエチレン基、アミノ基を1個以上有するアルキレン基等が挙げられる。
【0047】
次に、アミノ基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0048】
アミノ基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、特開2006−7203号公報、特開2006−7204号公報、特開2008−174491号公報に開示されている化合物等が挙げられる。
【0049】
容器の表面近傍に存在するカルボキシル基と、表面改質剤が有するアミノ基は、一般的な反応により縮合させると、アミド結合を形成する。具体的には、容器にN−ヒドロキシスクシンイミド、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミドの溶液を仕込み、容器の表面近傍に存在するカルボキシル基を活性エステル化させた後、表面改質剤を容器に仕込む。
【0050】
次に、ヒドロキシル基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0051】
ヒドロキシル基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、L−α−グリセロホスホリルコリン等が挙げられる。
【0052】
容器の表面近傍に存在するカルボキシル基と、表面改質剤が有するヒドロキシル基は、一般的な反応により縮合させると、エステル結合を形成する。具体的には、臭化シアンを用いて、ヒドロキシル基を活性化させた表面改質剤を容器に仕込む。
【0053】
次に、カルボキシル基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0054】
カルボキシル基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、特開2006−11381号公報に開示されている化合物等が挙げられる。
【0055】
容器の表面近傍に存在するアミノ基と、表面改質剤が有するカルボキシル基は、一般的な反応によりを縮合させると、アミド結合を形成する。具体的には、N−ヒドロキシスクシンイミド、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミドの溶液を用いて、カルボキシル基を活性エステル化させた表面改質剤を容器に仕込む。
【0056】
容器の表面近傍に存在するヒドロキシル基と、表面改質剤が有するカルボキシル基は、一般的な反応により縮合させると、エステル結合を形成する。具体的には、臭化シアンを用いて、容器の表面近傍に存在するヒドロキシル基を活性化させた後、表面改質剤を添加する。
【0057】
次に、アルデヒド基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0058】
アルデヒド基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、特開2006−11383号公報に開示されている化合物等が挙げられる。
【0059】
容器の表面近傍に存在するアミノ基と、表面改質剤が有するアルデヒド基は、一般的な反応により縮合させると、イミノ結合を形成する。具体的には、容器に表面改質剤及びメタノールを仕込み、室温で6時間放置した後、シアノトリヒドロホウ素酸ナトリウムを0℃で添加して、一晩加熱攪拌する。反応溶媒としては、メタノール以外にも、水、エタノール、2−プロパノール等のプロトン性溶媒を使用することができるが、メタノールを用いた場合の導入率が高い傾向にある。
【0060】
容器の表面近傍に存在するヒドロキシル基と、表面改質剤が有するアルデヒド基は、一般的な反応により付加させると、アセタール結合を形成する。具体的には、容器に表面改質剤及びメタノールを仕込み、室温で6時間放置した後、シアノトリヒドロホウ素酸ナトリウムを0℃で添加して、一晩加熱攪拌する。反応溶媒としては、メタノール以外にも、水、エタノール、2−プロパノール等のプロトン性溶媒を使用することができるが、メタノールを用いた場合の導入率が高い傾向にある。
【0061】
なお、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器の代わりに、アルデヒド基と、アミノ基及び/又はヒドロキシル基とが表面近傍に存在する容器を用いて、アルデヒド基に対して反応性を有する基と、一般式(1)で表される基を有する表面改質剤を反応させてもよい。
【0062】
容器の表面近傍にアルデヒド基を導入する方法としては、特に限定されないが、表面近傍にアミノ基が存在する容器にグルタルアルデヒドを反応させる方法等が挙げられる。
【0063】
アルデヒド基に対して反応性を有する基としては、アミノ基、ヒドロキシル基等が挙げられるが、反応性が高いことから、アミノ基が好ましい。
【0064】
また、表面改質剤は、アルデヒド基に対して反応性を有する基がスペーサーを介して、一般式(1)で表される基に結合されていることが好ましい。スペーサーとしては、特に限定されないが、メチレン基、オキシエチレン基、アミノ基を1個以上有するアルキレン基等が挙げられる。
【0065】
次に、アミノ基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0066】
アミノ基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、特開2006−7203号公報、特開2006−7204号公報、特開2008−174491号公報に開示されている化合物等が挙げられる。
【0067】
容器の表面近傍に存在するアルデヒド基と、表面改質剤が有するアミノ基は、一般的な反応により縮合させると、イミノ結合を形成する。具体的には、容器に表面改質剤及びメタノールを仕込み、室温で6時間放置した後、シアノトリヒドロホウ素酸ナトリウムを0℃で添加して、一晩加熱攪拌する。反応溶媒としては、メタノール以外にも、水、エタノール、2−プロパノール等のプロトン性溶媒を使用することができるが、メタノールを用いた場合の導入率が高い傾向にある。
【0068】
次に、ヒドロキシル基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0069】
ヒドロキシル基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、L−α−グリセロホスホリルコリン等が挙げられる。
【0070】
容器の表面近傍に存在するアルデヒド基と、表面改質剤が有するヒドロキシル基は、一般的な反応により付加させると、アセタール結合を形成する。具体的には、容器に表面改質剤及びメタノールを仕込み、室温で6時間放置した後、シアノトリヒドロホウ素酸ナトリウムを0℃で添加して、一晩加熱攪拌する。反応溶媒としては、メタノール以外にも、水、エタノール、2−プロパノール等のプロトン性溶媒を使用することができるが、メタノールを用いた場合の導入率が高い傾向にある。
【0071】
また、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器の代わりに、アミノ基又はヒドロキシル基と、カルボキシル基が表面近傍に存在する容器を用いて、アミノ基又はヒドロキシル基に対して反応性を有する基と、一般式(1)で表される基を有する表面改質剤を反応させてもよい。
【0072】
さらに、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器の代わりに、アミノ基及びヒドロキシル基が表面近傍に存在する容器を用いて、アミノ基又はヒドロキシル基に対して反応性を有する基と、ホリルコリン類似基を有する表面改質剤を、容器の表面近傍に未反応のアミノ基及び/又はヒドロキシル基が残留するように反応させてもよい。
【0073】
また、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器の代わりに、カルボキシル基、アミノ基又はヒドロキシル基が表面近傍に存在する容器を用いて、カルボキシル基、アミノ基又はヒドロキシル基に対して反応性を有する基と、一般式(1)で表される基を有する表面改質剤を、容器の表面近傍に未反応のカルボキシル基、アミノ基又はヒドロキシル基が残留するように反応させてもよい。
【0074】
[培養容器Dの第二の実施形態]
培養容器Dの第二の実施形態は、加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器に、加水分解によりシラノール基を生成することが可能な基と、一般式(1)で表される基を有する第一の表面改質剤と、アミノ基、カルボキシル基及び/又はヒドロキシル基と、加水分解によりシラノール基を生成することが可能な基を有する第二の表面改質剤を反応させることにより製造されている。このとき、第一の表面改質剤の分子量は、315〜650である。これにより、一般式(1)で表される基を高密度で導入することができる。
【0075】
なお、接着性細胞Cが間葉系幹細胞である場合は、第一の表面改質剤が有する一般式(1)で表される基に対する第二の表面改質剤が有するアミノ基、カルボキシル基及び/又はヒドロキシル基のモル比は、0.001〜2.4であることが好ましい。モル比が0.001未満であると、細胞が接着しないことがあり、2.4を超えると、細胞が単層の状態で増殖し、凝集しないことがある。
【0076】
容器の表面近傍に加水分解によりシラノール基を生成することが可能な基及び/又はシラノール基を導入する方法としては、加水分解によりシラノール基を生成することが可能な基を有するポリマー(以下、加水分解性ポリマーという)と、アルコキシシランを含有する塗布液を容器に塗布する方法が挙げられる。
【0077】
加水分解性ポリマーと、アルコキシシランを含有する塗布液を容器に塗布すると、加水分解性ポリマーとアルコキシシランが加水分解され、シラノール基が生成する。さらに、シラノール基同士の脱水縮合により、加水分解性ポリマーが架橋され、シラノール基が導入された架橋ポリマー層が形成される。具体的には、材料に塗布液を塗布した後に、水、酸又はアルカリを塗布したり、加熱したりする。また、水、酸又はアルカリを材料に塗布した後に、塗布液を塗布してもよい。さらに、塗布液に、水、酸又はアルカリを混合してもよい。この場合、塗布液中で加水分解が起こるため、塗布時に塗布液を適宜調製することが好ましい。なお、水、酸又はアルカリを用いる場合は、加熱してもよいが、通常、室温で十分反応が進行する。また、水、酸又はアルカリを用いなくても、大気中の水分により緩やかに反応が進行する。
【0078】
加水分解に用いられる酸又はアルカリとしては、加水分解させることが可能なものであれば、特に限定されず、二種以上混合して用いることができ、水溶液として用いてもよい。
【0079】
塗布液としては、有機溶媒中に、加水分解性ポリマーと、アルコキシシランを溶解又は分散させたものを用いることができる。有機溶媒としては、特に限定されないが、脂肪族炭化水素、芳香族炭化水素、塩素化炭化水素、エーテル、炭素数が1〜4の1〜4価の脂肪族アルコール等のアルコール、エチルセロソルブ、ブチルセロソルブ等のセロソルブ、ジオキサン、酢酸メチル、ジホルムアミド等が挙げられ、二種以上併用してもよい。
【0080】
塗布液中の加水分解性ポリマーの含有量は、通常、0.001〜20質量%であり、0.1〜5質量%が好ましい。塗布液中の加水分解性ポリマーの含有量が0.001質量%未満であると、1回の塗布で十分な効果が得られないことがあり、20質量%を超えると、塗布性が低下することがある。
【0081】
また、アルコキシシランに対する加水分解性ポリマーの質量比は、通常、0.01〜20%であり、0.2〜5%が好ましい。アルコキシシランに対する加水分解性ポリマーの質量比が0.01%未満であると、架橋ポリマー層の強度が不十分になることがあり、20%を超えると、架橋ポリマー層に導入されるシラノール基の量が不十分になることがある。
【0082】
塗布液を塗布する方法としては、特に限定されないが、浸漬塗布法、スプレー塗布法、スピンキャスト法等が挙げられる。
【0083】
容器を構成する材料としては、特に限定されないが、PP(ポリプロピレン)、シクロオレフィン樹脂、ポリカーボネート、PET(ポリエチレンテレフタレート)、PEEK、フッ素系樹脂、ポリスチレン、ポリ塩化ビニル等の有機材料;金、チタン、アルミ、鉄、銅、ステンレス、アルミナ、酸化チタン、酸化亜鉛等の無機材料等が挙げられる。
【0084】
加水分解性ポリマーとしては、加水分解によりシラノール基を生成することが可能な基を有するポリマーであれば、特に限定されないが、一般式
【0085】
【化3】

(式中、R1は、水素原子又はメチル基であり、R2は、炭素数が1〜6のアルキレン基、好ましくはプロピレン基であり、R3、R4及びR5は、それぞれ独立に、炭素数が1〜6のアルコキシル基、好ましくはメトキシル基又はエトキシル基である。)
で表されるモノマー(A−1)を重合することにより得られるホモポリマー又はコポリマー(以下、ポリマー(A)という)を用いることができる。このとき、モノマー(A−1)を二種以上用いてもよい。
【0086】
また、ポリマー(A)を合成する際に、一般式
【0087】
【化4】

(式中、R1は、水素原子又はメチル基であり、R2は、炭素数が1〜18の直鎖状、分岐状又は環状のアルキル基、好ましくは炭素数1〜6のアルキル基、特に好ましくはメチル基である。)
で表されるモノマー(A−2)を共重合してもよい。このとき、モノマー(A−2)を二種以上用いてもよい。
【0088】
また、ポリマー(A)を合成する際に、一般式
【0089】
【化5】

(式中、R1は、水素原子又はメチル基であり、R2は、炭素数が1〜6のアルキレン基、好ましくはエチレン基、プロピレン基又は2−ヒドロキシプロピレン基であり、Xは、一般式
【0090】
【化6】

(式中、R1、R2、R3、R4、R5、R6、R7、R8及びR9は、それぞれ独立に、炭素数が1〜6の直鎖又は分岐状のアルキル基、好ましくはメチル基である。)
で表される基(X−1)、一般式
【0091】
【化7】

(式中、R1、R2、R3、R4、R5及びR6は、それぞれ独立に、炭素数が1〜6の直鎖又は分岐状のアルキル基、好ましくはメチル基であり、R7は、炭素数が1〜6の直鎖又は分岐状のアルキル基、好ましくはブチル基であり、xは、正の整数である。)
で表される基(X−2)又は一般式
【0092】
【化8】

(式中、R1、R2、R3、R4、R5及びR6は、それぞれ独立に、炭素数が1〜6の直鎖又は分岐状のアルキル基、好ましくはメチル基であり、R7は、炭素数が1〜6のアルキレン基、好ましくはエチレン基、プロピレン基又は2−ヒドロキシプロピレン基であり、R8は、水素原子又はメチル基であり、yは、正の整数である。)
で表される基(X−3)である。)
で表されるモノマー(A−3)を共重合してもよい。なお、Xが基(X−2)又は(X−3)である場合、モノマー(A−3)は、分子量が1000〜100000であることが好ましく、2000〜20000が特に好ましい。このとき、モノマー(A−3)を二種以上用いてもよい。
【0093】
また、ポリマー(A)を合成する際に、一般式
【0094】
【化9】

(式中、R1は、水素原子又はメチル基であり、R2は、炭素数が1〜6のアルキレン基、好ましくはエチレン基又はプロピレン基であり、Yは、一般式
【0095】
【化10】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1〜6のアルキル基、好ましくはメチル基であり、Z−は、ハロゲン化物イオン又は有機酸若しくは無機酸の共役イオンである。)
で表される基(Y−1)又は一般式
【0096】
【化11】

(式中、R1及びR2は、それぞれ独立に、炭素数が1〜6のアルキル基、好ましくはメチル基である。)
で表される基(Y−2)である。)
で表されるモノマー(A−4)を共重合してもよい。このとき、モノマー(A−4)を二種以上用いてもよい。
【0097】
すなわち、ポリマー(A)を合成する際に、モノマー(A−1)と共に、モノマー(A−2)、モノマー(A−3)及び/又はモノマー(A−4)を共重合してもよい。
【0098】
ポリマー(A)を合成する際に用いられる全モノマー中のモノマー(A−1)の含有量が40〜85質量%であることが好ましい。全モノマー中のモノマー(A−1)の含有量が40質量%未満であると、架橋密度が低下して、親水化の効果が十分に持続しないことがあり、85質量%を超えると、架橋ポリマー層の均一性が低下することがある。
【0099】
また、ポリマー(A)を合成する際に用いられる全モノマー中のモノマー(A−2)の含有量は、通常、1〜75質量%であり、10〜60質量%が好ましい。全モノマー中のモノマー(A−2)の含有量が1質量%未満であると、架橋ポリマー層の耐水性が低下することがあり、75質量%を超えると、ポリマー(A)がアルコールに難溶性となることがある。
【0100】
さらに、ポリマー(A)を合成する際に用いられる全モノマー中のモノマー(A−3)の含有量は、通常、1〜70質量%であり、5〜60質量%が好ましい。全モノマー中のモノマー(A−3)の含有量が1質量%未満であると、架橋ポリマー層の耐水性が低下することがあり、70質量%を超えると、ポリマー(A)がアルコールに難溶性となることがある。
【0101】
また、モノマー(A−1)、モノマー(A−2)及びモノマー(A−3)の総質量に対するモノマー(A−4)の質量の比は、通常、0.01〜1であり、0.05〜0.5が好ましい。この比が0.01未満であると、架橋ポリマー層の柔軟性が低下することがあり、1を超えると、架橋ポリマー層の耐水性が低下することがある。
【0102】
ポリマー(A)の数平均分子量は2000〜150000であることが好ましい。ポリマー(A)の数平均分子量が2000未満であると、架橋ポリマー層を形成する時間が長くなることがあり、150000を超えると、塗布液の粘度が高くなって、塗布性や作業性に劣ることがある。
【0103】
なお、ポリマー(A)の具体例及び製造方法は、特開平11−302129号公報等に開示されている。
【0104】
また、加水分解性ポリマーとしては、一般式
【0105】
【化12】

(式中、R1は、炭素数が1〜22のアルキル基又はフェニル基、好ましくは、メチル基である。)
で表される構成単位(B−1)を有するホモポリマー又はコポリマー(以下、ポリマー(B)という)を用いることができる。このとき、ポリマー(B)は、構成単位(B−1)を二種以上有してもよい。
【0106】
また、ポリマー(B)は、一般式
【0107】
【化13】

(式中、R1及びR2は、それぞれ独立に、炭素数が1〜22のアルキル基又はフェニル基、好ましくは、メチル基である。)
で表される構成単位(B−2)を有してもよい。このとき、ポリマー(B)は、構成単位(B−2)を二種以上有してもよい。
【0108】
ポリマー(B)は、構成単位(B−1)の含有量が1〜90質量%であることが好ましい。構成単位(B−1)の含有量が1質量%未満であると、架橋密度が低下して、親水化の効果が十分に持続しないことがあり、90質量%を超えると、架橋ポリマー層の均一性が低下することがある。
【0109】
さらに、ポリマー(B)は、構成単位(B−2)の含有量が10〜99質量%であることが好ましい。構成単位(B−2)の含有量が10質量%未満であると、架橋ポリマー層の均一性が低下することがあり、99質量%を超えると、架橋密度が低下して、親水化の効果が十分に持続しないことがある。
【0110】
ポリマー(B)の数平均分子量は2000〜500000であることが好ましい。数平均分子量が2000未満であると、架橋ポリマー層を形成する時間が長くなることがあり、500000を超えると、塗布液の粘度が高くなって、塗布性や作業性に劣ることがある。
【0111】
加水分解性ポリマーとして、ポリマー(A)及びポリマー(B)を併用してもよいし、加水分解性ポリマーと非加水分解性ポリマーを併用してもよい。非加水分解性ポリマーとしては、特に限定されないが、加水分解によりシラノール基を生成することが可能な基を有さないポリマー(A)、ポリマー(B)等が挙げられる。
【0112】
容器の表面近傍にシラノール基を導入する方法としては、特に限定されないが、シリコーン樹脂を含む塗布液を容器に塗布することにより、シラノール基を有するシリコーン樹脂を含む膜を形成する方法等が挙げられる。
【0113】
シラノール基を有するシリコーン樹脂を含む膜は、水の接触角が3〜8°であることが好ましい。水の接触角が3°未満である膜を形成することは困難であり、水の接触角が8°を超える膜を形成すると、一般式(1)で表される基を高密度で導入できなくなることがある。
【0114】
塗布液に含まれるシリコーン樹脂としては、特に限定されないが、一般式
(R1O)nSi(R2)4−n
(式中、R1及びR2は、それぞれ独立に、炭素数が1〜8のアルキル基であり、nは、1〜4の整数であり、nが1又は2である場合、複数のR2は、同一であっても異なっていてもよく、nが2又は3である場合、複数のR1は、同一であっても異なっていてもよい。)
で表されるアルコキシシランを加水分解した後、縮合することにより得られる樹脂が挙げられ、二種以上併用してもよい。このとき、水の接触角が3〜8°である膜に含まれるシラノール基を有するシリコーン樹脂は、塗布液に含まれるシリコーン樹脂と同一であってもよいし、異なっていてもよい。
【0115】
塗布液に含まれる有機溶媒としては、特に限定されないが、脂肪族炭化水素、芳香族炭化水素、塩素化炭化水素、エーテル、炭素数が1〜4の1〜4価の脂肪族アルコール等のアルコール、エチルセロソルブ、ブチルセロソルブ等のセロソルブ、ジオキサン、酢酸メチル、ジホルムアミド等が挙げられ、二種以上併用してもよい。
【0116】
塗布液中のシリコーン樹脂の含有量は、通常、0.001〜1質量%であり、0.1〜1質量%が好ましい。塗布液中のシリコーン樹脂の含有量が0.001質量%未満であると、均一な膜が形成されないことがあり、20質量%を超えると、塗布性が低下することがある。
【0117】
塗布液を塗布する方法としては、特に限定されないが、浸漬塗布法、スプレー塗布法、スピンキャスト法等が挙げられる。
【0118】
容器を構成する材料としては、特に限定されないが、ポリカーボネート、PET(ポリエチレンテレフタレート)、ポリスチレン、アクリル樹脂等の有機材料;金、チタン、アルミ、鉄、銅、ステンレス、アルミナ、酸化チタン、酸化亜鉛等の無機材料等が挙げられる。
【0119】
また、シラノール基が表面近傍に存在する容器として、ガラス製の容器を用いてもよい。
【0120】
金属酸化物由来のヒドロキシル基が表面近傍に存在する容器を構成する金属酸化物としては、特に限定されないが、酸化チタン、酸化亜鉛、酸化鉄、酸化クロム、酸化アルミニウム等が挙げられる。
【0121】
半金属酸化物由来のヒドロキシル基が表面近傍に存在する容器を構成する金属酸化物としては、特に限定されないが、酸化ゲルマニウム、酸化ヒ素、酸化ホウ素等が挙げられる。
【0122】
加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基に対して反応性を有する基としては、加水分解によりシラノール基を生成することが可能な基が挙げられる。
【0123】
また、第一の表面改質剤は、加水分解によりシラノール基を生成することが可能な基がスペーサーを介して、一般式(1)で表される基に結合されていることが好ましい。スペーサーとしては、特に限定されないが、メチレン基、オキシエチレン基、アミノ基を1個以上有するアルキレン基等が挙げられる。
【0124】
加水分解によりシラノール基を生成することが可能な基としては、ヒドロシリル基、アルコキシシリル基、ハロシリル基、アシルオキシシリル基、アミノシリル基等が挙げられるが、安定性、反応性等の点から、炭素数が1〜6のアルコキシシリル基又はヒドロシリル基が好ましい。
【0125】
第一の表面改質剤としては、加水分解によりシラノール基を生成することが可能な基と、一般式(1)で表される基を有していれば、特に限定されないが、特開2006−11380号公報に開示されている化合物が挙げられる。
【0126】
第二の表面改質剤としては、アミノ基、加水分解によりカルボキシル基を生成することが可能な基及び/又は加水分解によりヒドロキシル基を生成することが可能な基と、加水分解によりシラノール基を生成することが可能な基を有していれば、特に限定されないが、3−アミノプロピルトリメトキシシラン、p−アミノフェニルトリメトキシシラン等のアミノ基を有する化合物;3−(トリエトキシシリル)プロピルスクシニックアンハイドライド等の加水分解によりカルボキシル基を生成することが可能な基を有する化合物;3−グリシドキシプロピルトリメトキシシラン、3−グリシドキシプロピルメチルジエトキシシラン等の加水分解によりヒドロキシル基を生成することが可能な基を有する化合物等が挙げられ、二種以上併用してもよい。
【0127】
第二の表面改質剤が加水分解によりカルボキシル基及び/又はヒドロキシル基を生成することが可能な基を有する場合は、加水分解によりカルボキシル基及び/又はヒドロキシル基を生成することが可能な基を容器の表面近傍に導入した後に、加水分解によりカルボキシル基及び/又はヒドロキシル基を生成させればよい。
【0128】
なお、第二の表面改質剤が有するアミノ基は、保護基により保護されていてもよい。また、第二の表面改質剤は、加水分解によりカルボキシル基又はヒドロキシル基を生成することが可能な基の代わりに、加水分解以外の反応により脱保護することが可能な保護基により保護されているカルボキシル基又はヒドロキシル基を有していてもよい。
【0129】
第二の表面改質剤が保護基により保護されているアミノ基、カルボキシル基及び/又はヒドロキシル基を有する場合は、保護基により保護されているアミノ基、カルボキシル基及び/又はヒドロキシル基を容器の表面近傍に導入した後に、脱保護によりアミノ基、カルボキシル基及び/又はヒドロキシル基を生成させればよい。
【0130】
次に、加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器に、アミノ基、加水分解によりカルボキシル基を生成することが可能な基及び/又は加水分解によりヒドロキシル基を生成することが可能な基と、一般式(1)で表される基を導入する方法について説明する。
【0131】
まず、加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器に、第一の表面改質剤及び第二の表面改質剤を含む塗布液を塗布する。このとき、加水分解によりシラノール基を生成することが可能な基が加水分解され、シラノール基が生成する。さらに、容器の表面近傍に存在するシラノール基、半金属酸化物の加水分解により生成したヒドロキシル基及び/又は金属酸化物の加水分解により生成したヒドロキシル基と、表面改質剤の加水分解により生成したシラノール基の脱水縮合により、容器の表面が改質される。具体的には、容器に塗布液を塗布した後に、水、酸又はアルカリを塗布したり、加熱したりする。また、水、酸又はアルカリを容器に塗布した後に、塗布液を塗布してもよい。さらに、塗布液に、水、酸又はアルカリを混合してもよい。この場合、塗布液中で加水分解が起こるため、塗布時に塗布液を適宜調製することが好ましい。なお、水、酸又はアルカリを用いる場合は、加熱してもよいが、通常、室温で十分反応が進行する。また、水、酸又はアルカリを用いなくても、大気中の水分により緩やかに反応が進行する。
【0132】
酸又はアルカリとしては、加水分解によりシラノール基を生成することが可能な基を加水分解させることが可能であれば、特に限定されず、二種以上併用してもよい。なお、加水分解に用いられる酸又はアルカリは、水溶液として用いてもよい。
【0133】
塗布液としては、有機溶媒中に、第一の表面改質剤及び第二の表面処理剤を溶解又は分散させたものを用いることができる。有機溶媒としては、脂肪族炭化水素、芳香族炭化水素、塩素化炭化水素、エーテル、炭素数が1〜4の1〜4価の脂肪族アルコール等のアルコール、エチルセロソルブ、ブチルセロソルブ等のセロソルブ、ジオキサン、酢酸メチル、ジホルムアミド等が挙げられる。
【0134】
塗布液中の第一の表面改質剤の含有量は、通常、0.1〜30質量%であり、1〜10質量%が好ましい。塗布液中の第一の表面改質剤の含有量が0.1質量%未満であると、1回の塗布で第一の表面改質剤を十分に塗布できないことがあり、30質量%を超えると、塗布性が低下することがある。
【0135】
塗布液を塗布する方法としては、特に限定されないが、浸漬塗布法、スプレー塗布法、スピンキャスト法等が挙げられる。
【0136】
なお、第一の表面処理剤を含む塗布液及び第二の表面処理剤を含む塗布液を、それぞれ容器に塗布してもよい。
【0137】
また、容器の表面近傍に未反応のシラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が残留するように、表面改質剤由来のシラノール基と、容器由来のシラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基を反応させてもよい。
【0138】
[培養容器Dの第三の実施形態]
培養容器Dの第三の実施形態は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式(1)で表される基を有する樹脂を含む層が表面に形成されている。
【0139】
アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式(1)で表される基を有する樹脂としては、特に限定されないが、一般式(1)で表される基を有するモノマーと、アミノ基を有するモノマー、カルボキシル基を有するモノマー及び/又はヒドロキシル基を有するモノマーを共重合することにより得られる樹脂が挙げられる(例えば、特開平7−184990号公報参照)。
【0140】
容器を構成する材料としては、特に限定されないが、シクロオレフィン樹脂、ポリカーボネート、PET(ポリエチレンテレフタレート)、ポリスチレン、アクリル樹脂等の有機材料;金、チタン、アルミ、鉄、銅、ステンレス、アルミナ、酸化チタン、酸化亜鉛等の無機材料等が挙げられる。
【0141】
なお、有機材料から構成される容器を用いる場合、容器に対する接着性を考慮すると、一般式(1)で表される基を有するモノマーと、アミノ基、カルボキシル基及び/又はヒドロキシル基を有するモノマーと、疎水性基を有するモノマーを共重合することにより得られる樹脂を用いることが好ましい。
【0142】
疎水性基を有するモノマーとしては、特に限定されないが、メタクリル酸ブチル等が挙げられる。
【0143】
容器の表面近傍に、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式(1)で表される基を有する樹脂を含む層を形成する方法としては、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式(1)で表される基を有する樹脂を含む塗布液を容器に塗布する方法が挙げられる。
【0144】
塗布液としては、有機溶媒中に、樹脂を溶解又は分散させたものを用いることができる。有機溶媒としては、脂肪族炭化水素、芳香族炭化水素、塩素化炭化水素、エーテル、炭素数が1〜4の1〜4価の脂肪族アルコール等のアルコール、エチルセロソルブ、ブチルセロソルブ等のセロソルブ、ジオキサン、酢酸メチル、ジホルムアミド等が挙げられる。
【0145】
塗布液中の樹脂の含有量は、通常、0.1〜30質量%であり、1〜10質量%が好ましい。塗布液中の樹脂の含有量が0.1質量%未満であると、1回の塗布で樹脂を十分に塗布できないことがあり、30質量%を超えると、塗布性が低下することがある。
【0146】
塗布液を塗布する方法としては、特に限定されないが、浸漬塗布法、スプレー塗布法、スピンキャスト法等が挙げられる。
【0147】
本発明の細胞凝集塊の形成方法に、ヒト、ラット、マウス、霊長類等の哺乳類に由来する接着性細胞を適用すると、後述する物質のスクリーニング方法及び細胞の機能探索方法に有用である。
【0148】
本発明において、接着性細胞を培養する方法としては、特に限定されず、接着性細胞に応じて、公知の条件を適用することができるが、10質量%のウシ胎児血清(FBS)、1mMのグルタミン、適量の抗生物質を含むダルベッコ改変培地(DMEM)を用いて、5体積%の二酸化炭素を含む雰囲気下、37℃で接着性細胞を培養する方法等が挙げられる。
【0149】
本発明の物質のスクリーニング方法は、本発明の細胞凝集塊の形成方法により形成されている細胞凝集塊を用いて物質をスクリーニングする。このとき、本発明の物質のスクリーニング方法は、肝細胞や心筋細胞を用いて物質の毒性を評価する方法、ガン細胞を用いて薬剤の効果を試験する方法等の公知の物質のスクリーニング方法に適用することができる。物質の毒性を評価する方法としては、MTTアッセイ、アラマーブルーアッセイ等の細胞増殖を基準とする方法が挙げられる。また、RT−PCR、ELISA等の方法により、炎症性サイトカインの産生放出、癌化に関連する因子であるSDF−1、LIF、EGFR等の量を定量することもできる。
【0150】
また、本発明の物質のスクリーニング方法は、個体毎の接着性細胞の細胞凝集塊を用いて物質をスクリーニングすることにより、テーラーメイド医療に応用することができる。
【0151】
本発明の細胞の機能探索方法は、本発明の細胞凝集塊の形成方法により形成されている細胞凝集塊を用いて細胞の機能を探索する。このとき、本発明の細胞の機能探索方法は、接着性細胞の生化学的機能を解明する方法、バイオマーカーを探索する方法等の公知の細胞の機能探索方法に適用することができる。
【実施例】
【0152】
[実施例1]
プライマリアディッシュ(日本ベクトン・ディッキンソン社製)に、N−ヒドロキシスクシンイミド1g、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド1gの1質量%水溶液を仕込んだ後、化学式
【0153】
【化14】

で表される化合物(A)1gを水100mlに溶解させた溶液を添加し、アミド化した。次に、プライマリアディッシュから液を取り出し、室温で5時間乾燥させた後、水洗し、乾燥させ、培養容器を得た。なお、プライマリアディッシュは、酸素とアンモニアを含む雰囲気下でプラズマ処理されているポリスチレン製のディッシュである。
【0154】
培養容器に、MensenPRO RS培地(Invitrogen社製)10ml及び間葉系幹細胞としてのヒト脂肪由来幹細胞(Invitrogen社製)1×106個/容器を添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図2A及び図2B参照)。
【0155】
[比較例1]
表面処理されていないポリスチレン製のペトリディッシュ(日本ベクトン・ディッキンソン社製)に、MensenPRO RS培地(Invitrogen社製)10ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×106個/ディッシュを添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が単層の状態で増殖し、細胞凝集塊を形成しなかった(図3参照)。
【0156】
[アルカリホスファターゼ活性]
実施例1の細胞凝集塊及び比較例1の培養細胞に4質量%パラホルムアルデヒド・リン酸緩衝液を添加して5分間処理した後、TBS緩衝液及びTBST緩衝液を用いて洗浄した。次に、BMパープルAP基質(Roche社製)を添加して、37℃で1時間反応させた後、TBST緩衝液を用いて洗浄した。評価結果を図4A及び図4Bに示す。図4A及び図4Bから、実施例1の細胞凝集塊は、アルカリホスファターゼ活性が陽性であるが、比較例1の培養細胞は、アルカリホスファターゼ活性が陰性であることがわかる。
【0157】
[免疫二重染色]
実施例1の細胞凝集塊及び比較例1の培養細胞に4質量%パラホルムアルデヒド・リン酸緩衝液を添加して5分間処理した後、TBS緩衝液及びTBST緩衝液を用いて洗浄した。次に、第一の一次抗体を、カタログに記載されている方法で希釈し、細胞に反応させた後、第一のAlexa Fluor標識二次抗体(Invitrogen社製)を細胞に反応させ、TBST緩衝液を用いて洗浄した。さらに、第二の一次抗体を、カタログに記載されている方法で希釈し、細胞に反応させた後、第二のAlexa Fluor標識二次抗体(Invitrogen社製)を細胞に反応させ、TBST緩衝液を用いて洗浄した。評価結果を表1に示す。
【0158】
【表1】

なお、Nestin(Abcam社製)、CD271(Abcam社製)及びCD133(Abcam社製)は、それぞれ神経由来幹細胞マーカー、脂肪由来幹細胞マーカー及び幹細胞マーカーであり、PDGFRa(R&D社製)及びPDGFRb(R&D社製)は、間葉系幹細胞マーカーである。また、実施例1の細胞凝集塊の評価結果を図5〜8に示す。表1から、実施例1の細胞凝集塊は、Nestinが陽性であるため、脂肪由来幹細胞がin vitroで神経由来幹細胞の性質を獲得できることがわかる。
【0159】
[実施例2−1]
3−アミノプロピルトリメトキシシランの0.15mol/Lメタノール溶液0.01mL、化学式
【0160】
【化15】

で表される化合物(B)の0.15mol/Lメタノール溶液9.99mL及びメタノール10mLからなる塗布液を得た。
【0161】
得られた塗布液をガラスボトムディッシュ(松浪硝子工業社製)に塗布し、室温で乾燥させた。次に、加熱乾燥し、室温で乾燥させた後、水洗し、乾燥させ、培養容器を得た。
【0162】
培養容器に、MensenPRO RS培地(Invitrogen社製)2.5ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×105個/容器を添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図9参照)。
【0163】
[実施例2−2]
3−アミノプロピルトリメトキシシランの0.15mol/Lメタノール溶液0.5mL、化合物(B)の0.15mol/Lメタノール溶液9.5mL及びメタノール10mLからなる塗布液を得た。
【0164】
得られた塗布液をガラスボトムディッシュ(松浪硝子工業社製)に塗布し、室温で乾燥させた。次に、加熱乾燥し、室温で乾燥させた後、水洗し、乾燥させ、培養容器を得た。
【0165】
培養容器に、MensenPRO RS培地(Invitrogen社製)2.5ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×105個/容器を添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図10参照)。
【0166】
[実施例2−3]
3−アミノプロピルトリメトキシシランの0.15mol/Lメタノール溶液7mL、化合物(B)の0.15mol/Lメタノール溶液3mL及びメタノール10mLからなる塗布液を得た。
【0167】
得られた塗布液をガラスボトムディッシュ(松浪硝子工業社製)に塗布し、室温で乾燥させた。次に、加熱乾燥し、室温で乾燥させた後、水洗し、乾燥させ、培養容器を得た。
【0168】
培養容器に、MensenPRO RS培地(Invitrogen社製)2.5ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×105個/容器を添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図11参照)。
【0169】
[比較例2]
表面処理されていないガラスボトムディッシュ(松浪硝子工業社製)に、MensenPRO RS培地(Invitrogen社製)2.5ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×105個/ディッシュを添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が単層の状態で増殖し、細胞凝集塊を形成しなかった(図12参照)。
【0170】
[免疫染色]
実施例2−2の細胞凝集塊に4質量%パラホルムアルデヒド・リン酸緩衝液を添加して5分間処理した後、0.2質量%Triton X−100(ロシュ・ダイアグノスティックス社製)/TBS緩衝液及び0.2質量%Tween20(東京化成工業社製)/TBS緩衝液を用いて洗浄した。次に、Protein Block(DAKO社製)で非特異反応をブロッキングした。さらに、200倍に希釈した一次抗体の抗CD271ラビットポリクローナル抗体(abcam社製)及びCD90マウスモノクローナル抗体(abcam社製)を細胞に一晩反応させた後、0.2質量%Tween20(東京化成工業社製)/TBS緩衝液を用いて洗浄した。次に、250倍に希釈したそれぞれ緑色及び赤色に発色する蛍光二次抗体のAlexa488 抗ラビット抗体(Invitrogen社製)及びAlexa594 抗マウス抗体(Invitrogen社製)を細胞に2時間反応させた後、0.2質量%Tween20(東京化成工業社製)/TBS緩衝液を用いて洗浄した。さらに、青色に発色するVectorshield−DAPI(Vector社製)で核を染色した後、共焦点レーザー顕微鏡LSM 5 PASCAL(Carl Zeiss社製)を用いて観察した。その結果、実施例2−2の細胞凝集塊が緑色に発色していたことから、CD271が陽性であることがわかった(図13参照)。
【0171】
なお、実施例2−1及び実施例2−3の細胞凝集塊も、実施例2−2の細胞凝集塊と同様に緑色に発色し、CD271が陽性であった。
【0172】
[実施例3]
プライマリアディッシュ(日本ベクトン・ディッキンソン社製)に、N−ヒドロキシスクシンイミド89mg、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド149mgを水10mLに溶解させた水溶液を仕込んだ後、化合物(A)200mgを水10mlに溶解させた溶液を添加し、アミド化した。次に、プライマリアディッシュから液を取り出した後、水洗し、乾燥させ、培養容器を得た。
【0173】
培養容器に、10質量%のウシ胎児血清(FBS)を含むMEM培地(SIGMA−ALDRICH社製)3ml及びガン細胞としてのヒト肝ガン細胞(プライマリーセル社製)1×105個/容器を添加し、ヒト肝ガン細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図14参照)。
【0174】
[比較例3]
プライマリアディッシュ(日本ベクトン・ディッキンソン社製)に、10質量%のウシ胎児血清(FBS)を含むMEM培地(SIGMA−ALDRICH社製)3ml及びガン細胞としてのヒト肝ガン細胞(プライマリーセル社製)1×105個/容器を添加し、ヒト肝ガン細胞を培養したところ、細胞が単層の状態で増殖し、細胞凝集塊を形成しなかった(図15参照)。
【0175】
[アルブミンの産生量]
実施例3及び比較例3のヒト肝ガン細胞を培養した培地中のアルブミンの産生量を、ヒトアルブミン定量キット(コスモバイオ社製)を用いて、ELISA法により定量した。評価結果を図16に示す。図16から、実施例3の細胞凝集塊は、アルブミンの産生量が比較例3の培養細胞よりも大きいことがわかる。
【0176】
[CYP1A1の活性]
実施例3の細胞凝集塊及び比較例3の培養細胞を10質量%のウシ胎児血清(FBS)、8μMの7−エトキシレゾルフィン及び10μMのジクマロールを含むMEM培地(SIGMA−ALDRICH社製)中、37℃で30分間培養した。次に、培養上清に、β−グルクロニダーゼ及びアリルスルファターゼを含む酢酸緩衝液を添加して37℃で2時間反応させた。さらに、溶液中のレゾルフィン量を蛍光測定(励起波長530nm、蛍光波長590nm)により、定量し、細胞が産生したCYP1A1の活性を評価した。評価結果を図17に示す。図17から、実施例3の細胞凝集塊は、CYP1A1の活性が比較例3の培養細胞よりも大きいことがわかる。
【0177】
[遺伝子発現]
実施例3の細胞凝集塊及び比較例3の培養細胞の遺伝子発現を、Lightcycler 480−II(Roche社製)を用いて、PCR法により、定量した。評価結果を図18に示す。図18から、実施例3の細胞凝集塊は、CYP1A1、ALB、LDLR、ATP51及びCol1A1の遺伝子発現が比較例3の培養細胞よりも大きいことがわかる。なお、内部標準としては、GAPDHを用いた。
【0178】
[実施例4]
ヒト肝ガン細胞(プライマリーセル社製)の代わりに、ヒト乳腺由来ガン細胞(理研BRC製)を用いた以外は、実施例3と同様にして、ヒト乳腺由来ガン細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図19参照)。
【0179】
[比較例4]
ヒト肝ガン細胞(プライマリーセル社製)の代わりに、ヒト乳腺由来ガン細胞(理研BRC製)を用いた以外は、比較例3と同様にして、ヒト乳腺由来ガン細胞を培養したところ、細胞が単層の状態で増殖し、細胞凝集塊を形成しなかった(図20参照)。
【0180】
[アルカリホスファターゼ活性]
実施例4の細胞凝集塊及び比較例4の培養細胞に4質量%パラホルムアルデヒド・リン酸緩衝液を添加して5分間処理した後、TBS緩衝液及びTBST緩衝液を用いて洗浄した。次に、BMパープルAP基質(Roche社製)を添加して、37℃で1時間反応させた後、TBST緩衝液を用いて洗浄した。評価結果を図21A及び図21Bに示す。図21A及び図21Bから、実施例4の細胞凝集塊は、アルカリホスファターゼ活性が陽性であるが、比較例4の培養細胞は、アルカリホスファターゼ活性が陰性であることがわかる。
【0181】
[遺伝子発現]
実施例4の細胞凝集塊及び比較例4の培養細胞の遺伝子発現を、Lightcycler 480−II(Roche社製)を用いて、PCR法により、定量した。評価結果を図22に示す。図22から、実施例4の細胞凝集塊は、VEGF−Aの遺伝子発現が比較例4の培養細胞よりも大きいことがわかる。なお、内部標準としては、GAPDHを用いた。
【符号の説明】
【0182】
C 接着性細胞
C' 細胞凝集塊
D 培養容器
M 培地
【技術分野】
【0001】
本発明は、細胞凝集塊の形成方法、物質のスクリーニング方法、細胞の機能探索方法、細胞凝集塊及び培養容器に関する。
【背景技術】
【0002】
従来、接着性細胞及び非接着性細胞を培養することにより、細胞凝集塊が形成されている。
【0003】
特許文献1には、多能性神経幹細胞を含む組織を少なくとも一種の幹細胞増殖因子を含む培地に懸濁し、神経幹細胞凝集塊形成用容器に播種、培養する事により神経幹細胞凝集塊を形成させる方法が開示されている。このとき、神経幹細胞凝集塊形成用容器は、内面に非水溶性硬化皮膜層を有し、水溶性樹脂を容器内面に被覆させて水溶性樹脂被覆層を形成した後に、水溶性樹脂被覆層を硬化させて非水溶性硬化皮膜層に変性することにより製造される。また、水溶性樹脂として、2−メタクリロイルオキシエチルホスホリルコリンと他のモノマー(例えば、ブチルメタクリレート等)との共重合体が例示されている。
【0004】
しかしながら、このような神経幹細胞凝集塊形成用容器を用いて、接着性細胞を培養しても、非水溶性硬化皮膜層が接着性細胞の接着を阻害するため、接着性細胞が死滅し、接着性細胞の細胞凝集塊を形成することができないという問題がある。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2008−220205号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明は、上記の従来技術が有する問題に鑑み、接着性細胞の細胞凝集塊を形成することが可能な細胞凝集塊の形成方法、該細胞凝集塊の形成方法を用いる物質のスクリーニング方法及び細胞の機能探索方法、細胞凝集塊並びに培養容器を提供することを目的とする。
【課題を解決するための手段】
【0007】
本発明の細胞凝集塊の形成方法は、培養容器を用いて、接着性細胞を培養して細胞凝集塊を形成する方法であって、前記培養容器は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式
【0008】
【化1】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1以上6以下のアルキル基であり、mは、2以上6以下の整数である。)
で表される基が表面近傍に存在し、前記接着性細胞は、間葉系幹細胞、肝細胞又はガン細胞である。
【0009】
本発明の物質のスクリーニング方法は、本発明の細胞凝集塊の形成方法を用いて、細胞凝集塊を形成する工程と、該細胞凝集塊を用いて物質をスクリーニングする工程を有する。
【0010】
本発明の細胞の機能探索方法は、本発明の細胞凝集塊の形成方法を用いて、細胞凝集塊を形成する工程と、該細胞凝集塊を用いて細胞の機能を探索する工程を有する。
【0011】
本発明の細胞凝集塊は、接着性細胞が増殖して自律的に凝集した細胞凝集塊であって、前記接着性細胞は、間葉系幹細胞、肝細胞又はガン細胞である。
【0012】
本発明の培養容器は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式
【0013】
【化2】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1以上6以下のアルキル基であり、mは、2以上6以下の整数である。)
で表される基が表面近傍に存在する。
【発明の効果】
【0014】
本発明によれば、接着性細胞の細胞凝集塊を形成することが可能な細胞凝集塊の形成方法、該細胞凝集塊の形成方法を用いる物質のスクリーニング方法及び細胞の機能探索方法、細胞凝集塊並びに培養容器を提供することができる。
【図面の簡単な説明】
【0015】
【図1A】本発明の細胞凝集塊を形成する方法の一例を示す図(その1)である。
【図1B】本発明の細胞凝集塊を形成する方法の一例を示す図(その2)である。
【図2A】実施例1の細胞凝集塊(2日間培養した場合)を示す光学顕微鏡写真である。
【図2B】実施例1の細胞凝集塊(5日間培養した場合)を示す光学顕微鏡写真である。
【図3】比較例1の培養細胞(5日間培養した場合)を示す光学顕微鏡写真である。
【図4A】実施例1の細胞凝集塊のアルカリホスファターゼ活性の評価結果を示す光学顕微鏡写真である。
【図4B】比較例1の培養細胞のアルカリホスファターゼ活性の評価結果を示す光学顕微鏡写真である。
【図5】実施例1の細胞凝集塊の免疫二重染色の評価結果(その1)を示す蛍光顕微鏡写真である。
【図6】実施例1の細胞凝集塊の免疫二重染色の評価結果(その2)を示す蛍光顕微鏡写真である。
【図7】実施例1の細胞凝集塊の免疫二重染色の評価結果(その3)を示す蛍光顕微鏡写真である。
【図8】実施例1の細胞凝集塊の免疫二重染色の評価結果(その4)を示す蛍光顕微鏡写真である。
【図9】実施例2−1の細胞凝集塊(2日間培養した場合)を示す光学顕微鏡写真である。
【図10】実施例2−2の細胞凝集塊(7日間培養した場合)を示す光学顕微鏡写真である。
【図11】実施例2−3の細胞凝集塊(7日間培養した場合)を示す光学顕微鏡写真である。
【図12】比較例2の培養細胞(7日間培養した場合)を示す光学顕微鏡写真である。
【図13】実施例2−2の細胞凝集塊の免疫染色の評価結果を示す写真である。
【図14】実施例3の細胞凝集塊(11日間培養した場合)を示す光学顕微鏡写真である。
【図15】比較例3の培養細胞(11日間培養した場合)を示す光学顕微鏡写真である。
【図16】実施例3の細胞凝集塊及び比較例3の培養細胞のアルブミンの産生量の評価結果を示す図である。
【図17】実施例3の細胞凝集塊及び比較例3の培養細胞のCYP1A1の活性の評価結果を示す図である。
【図18】実施例3の細胞凝集塊及び比較例3の培養細胞の遺伝子発現の評価結果を示す図である。
【図19】実施例4の細胞凝集塊(8日間培養した場合)を示す光学顕微鏡写真である。
【図20】比較例4の培養細胞(8日間培養した場合)を示す光学顕微鏡写真である。
【図21A】実施例4の細胞凝集塊のアルカリホスファターゼ活性の評価結果を示す光学顕微鏡写真である。
【図21B】比較例4の培養細胞のアルカリホスファターゼ活性の評価結果を示す光学顕微鏡写真である。
【図22】実施例4の細胞凝集塊及び比較例4の培養細胞の遺伝子発現の評価結果を示す図である。
【発明を実施するための形態】
【0016】
次に、本発明を実施するための形態を図面と共に説明する。
【0017】
図1に、本発明の細胞凝集塊を形成する方法の一例を示す。
【0018】
培養容器Dは、アミノ基、カルボキシル基及び/又はヒドロキシル基が表面近傍に存在する領域D1と、一般式(1)で表される基が表面近傍に存在する領域D2を底面に有する。
【0019】
培養容器Dに、接着性細胞C及び培地Mを添加すると、培養容器Dの底面に接着性細胞Cが接着する(図1A参照)。これは、培養容器Dの底面のアミノ基、カルボキシル基及び/又はヒドロキシル基が表面近傍に存在する領域D1に接着性細胞Cが接着するためであると考えられる。次に、接着性細胞Cを培養すると、接着性細胞Cが増殖して自律的に凝集し、細胞凝集塊C'が形成される(図1B参照)。これは、培養容器Dの底面の一般式(1)で表される基が表面近傍に存在する領域D2は、接着性細胞Cの接着を抑制するため、接着性細胞C上に、増殖した接着性細胞Cが形成されるためであると考えられる。このため、培養容器Dを用いて、接着性細胞Cを培養すると、接着性細胞Cが増殖して自律的に凝集した細胞凝集塊C'を形成することができる。
【0020】
接着性細胞Cとしては、特に限定されないが、間葉系幹細胞、肝細胞、肝幹細胞、心筋細胞、ガン細胞、ガン幹細胞、繊維芽細胞、神経細胞、血管内皮前駆細胞、上皮細胞等が挙げられる。
【0021】
培養容器Dの形態としては、特に限定されないが、ディッシュ、マルチウェルプレート、フラスコ、ローラーボトル、細胞培養プロセスを有するデバイスのユニット等が挙げられる。
【0022】
[培養容器Dの第一の実施形態]
培養容器Dの第一の実施形態は、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器に、カルボキシル基、アミノ基又はヒドロキシル基に対して反応性を有する基と、一般式(1)で表される基を有する表面改質剤を反応させることにより製造されている。このとき、表面改質剤の分子量は、225〜650である。これにより、一般式(1)で表される基を高密度で導入することができる。
【0023】
容器の表面近傍にアミノ基を導入する方法としては、特に限定されないが、窒素プラズマ処理、アンモニアプラズマ処理、表面処理剤を反応させる方法、シリコーン気相処理等が挙げられる。
【0024】
窒素プラズマ処理では、窒素ガス雰囲気下、低温プラズマを発生させることにより、容器の表面近傍にアミノ基を導入する(例えば、Surface and Coatings Technology 116−119(1999)802−807,Colloids and Surfaces A:Physicochem.Eng.Aspects 195(2001)81−95,Macromol.Chem.Phys.200.989−996(1999)参照)。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、窒素ガスを導入し、グロー放電を行う。
【0025】
アンモニアプラズマ処理では、アンモニアガス雰囲気下、低温プラズマを発生させることにより、容器の表面近傍にアミノ基を導入する。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、アンモニアガスを導入し、グロー放電を行う。
【0026】
容器を構成する材料としては、特に限定されないが、ポリ塩化ビニル、アクリル樹脂、ポリスチレン、ポリプロピレン、ポリエチレン、ポリエステル、シクロオレフィン樹脂、ポリカーボネート、ガラス等が挙げられる。
【0027】
表面処理剤を反応させる方法では、アミノ基を有するアルコキシシラン、クロロシラン、シラザン等の表面処理剤を用いて、アルコキシシリル基等の加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器の表面近傍にアミノ基を導入する。具体的には、まず、容器内に水/2−プロパノール混合液を仕込み、3−アミノプロピルトリメトキシシランを添加した後、100℃に加熱し、6時間反応させる。次に、室温に冷却した後、メタノールで洗浄し、乾燥する。
【0028】
容器を構成する材料としては、特に限定されないが、メタクリル酸3−トリメトキシシリルプロピル−メタクリル酸メチル−ジビニルベンゼン共重合体、ポリ塩化ビニル、アクリル樹脂、ポリスチレン、ポリプロピレン、ポリエチレン、ポリエステル、シクロオレフィン樹脂、ポリカーボネート、シリカ、ガラス、アルミナ、タルク、クレー、マイカ、アスベスト、酸化チタン、亜鉛華、酸化鉄等が挙げられる。
【0029】
シリコーン気相処理では、1,3,5,7−テトラメチルシクロテトラシロキサンを用いて、容器の表面近傍にヒドロシリル基を導入した後、アミノ基を有するアルケンを反応させることにより、容器の表面近傍にアミノ基を導入する(例えば、特公平1−54379号公報、特公平1−54380号公報、特公平1−54381号公報参照)。具体的には、まず、1,3,5,7−テトラメチルシクロテトラシロキサンと、容器をデシケーター中に入れ、アスピレーターで脱気する。次に、80℃で16時間反応させた後、容器を取り出し、120℃で乾燥させる。さらに、得られた容器をエタノール中に浸し、アリルアミンを添加した後、塩化白金酸のエタノール溶液を添加し、60℃で2時間攪拌する。反応が終了した後、エタノールで洗浄し、減圧乾燥する。
【0030】
容器を構成する材料としては、特に限定されないが、スチレン−ジビニルベンゼン共重合体、ポリ塩化ビニル、アクリル樹脂、ポリスチレン、ポリプロピレン、ポリエチレン、ポリエステル、シクロオレフィン樹脂、ポリカーボネート、マイカ、タルク、カオリン、アルミナ、酸化チタン、酸化亜鉛、酸化鉄等が挙げられる。
【0031】
アミノ基を有するアルケンとしては、アリルアミンに限定されず、ビニル基を有するアミン、アクリル基を有するアミン等であればよい。また、アミノ基は、ブトキシカルボニル基、ベンジルオキシカルボニル基等により保護されていてもよい。さらに、アミノ基を有するアルケンの代わりに、エポキシ基等の、例えば、ジアミンとの反応により、アミノ基を導入することが可能な基を有するアルケンを用いてもよい。
【0032】
容器の表面近傍にカルボキシル基及び/又はヒドロキシル基を導入する方法としては、特に限定されないが、酸素プラズマ処理、オゾン処理、水蒸気プラズマ処理等が挙げられる。
【0033】
酸素プラズマ処理では、酸素ガスの雰囲気下、低温プラズマを発生させることにより、容器の表面近傍にカルボキシル基及びヒドロキシル基を導入する。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、酸素ガスを導入し、グロー放電する。
【0034】
オゾン処理では、容器にオゾン水溶液を仕込むことにより、容器の表面近傍にカルボキシル基及びヒドロキシル基を導入する。具体的には、容器に40ppmのオゾン水溶液を仕込み、室温で15分間処理する。
【0035】
水蒸気プラズマ処理では、水蒸気の雰囲気下、低温プラズマを発生させることにより、容器の表面近傍にヒドロキシル基を導入する。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、水蒸気を導入し、グロー放電する。
【0036】
容器を構成する材料としては、特に限定されないが、ポリスチレン、ポリエチレンテレフタレート、ポリカーボネート、ポリメタクリル酸メチル、ポリテトラフルオロエチレン、ポリエーテルエーテルケトン、シクロオレフィン樹脂、ポリカーボネート等が挙げられる。
【0037】
容器の表面近傍にカルボキシル基を導入する方法としては、特に限定されないが、表面処理剤を反応させる方法、シリコーン気相処理等が挙げられる。
【0038】
表面処理剤を反応させる方法では、カルボキシル基を有するアルコキシシラン、クロロシラン、シラザン等の表面処理剤を用いて、アルコキシシリル基等の加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器の表面近傍にカルボキシル基を導入する。具体的には、まず、トリエトキシシリルプロピル無水コハク酸をN,N−ジメチルホルムアミドに溶解させ、蒸留水と4−ジメチルアミノピリジンを添加し、16時間室温で撹拌し、カルボンキシル基を有するシランカップリング剤を合成する。次に、容器に水/2−プロパノール混合液を仕込み、カルボキシル基を有するシランカップリング剤を添加した後、100℃に加熱し、6時間反応させる。さらに、室温に冷却した後、メタノールで洗浄し、乾燥する。
【0039】
容器を構成する材料としては、特に限定されないが、メタクリル酸3−トリメトキシシリルプロピル−メタクリル酸メチル−ジビニルベンゼン共重合体、シリカ、ガラス、アルミナ、タルク、クレー、マイカ、アスベスト、酸化チタン、亜鉛華、酸化鉄等が挙げられる。
【0040】
シリコーン気相処理では、1,3,5,7−テトラメチルシクロテトラシロキサンを用いて、容器の表面近傍にヒドロシリル基を導入した後、カルボキシル基を有するアルケンを反応させることにより、容器の表面近傍にカルボキシル基を導入する(例えば、特公平1−54379号公報、特公平1−54380号公報、特公平1−54381号公報参照)。具体的には、まず、1,3,5,7−テトラメチルシクロテトラシロキサンを入れた容器をデシケーター中に入れ、アスピレーターで脱気する。次に、80℃で16時間反応させた後、容器を取り出し、120℃で乾燥させる。さらに、得られた容器をエタノール中に浸し、アリルカルボン酸を添加した後、塩化白金酸のエタノール溶液を添加し、60℃で2時間攪拌する。反応が終了した後、エタノールで洗浄し、減圧乾燥する。
【0041】
容器を構成する材料としては、特に限定されないが、スチレン−ジビニルベンゼン共重合体、マイカ、タルク、カオリン、アルミナ、酸化チタン、酸化亜鉛、酸化鉄等が挙げられる。
【0042】
カルボキシル基を有するアルケンとしては、アリルカルボン酸に限定されず、ビニル基を有するカルボン酸、アクリル基を有するカルボン酸等であればよい。
【0043】
容器の表面近傍にアミノ基、カルボキシル基及びヒドロキシル基を導入する方法としては、特に限定されないが、酸素ガス及びアンモニアガスを含む雰囲気下でプラズマ処理する方法等が挙げられる。具体的には、容器を反応容器内に収容し、反応容器内を真空ポンプで真空にした後、酸素ガス及びアンモニアガスを導入し、グロー放電を行い、低温プラズマを発生させる。
【0044】
カルボキシル基に対して反応性を有する基としては、アミノ基、ヒドロキシル基等が挙げられるが、反応性が高いことから、アミノ基が好ましい。
【0045】
アミノ基又はヒドロキシル基に対して反応性を有する基としては、カルボキシル基、アルデヒド基等が挙げられるが、反応性が高いことから、カルボキシル基が好ましい。
【0046】
また、表面改質剤は、カルボキシル基、アミノ基又はヒドロキシル基に対して反応性を有する基がスペーサーを介して、一般式(1)で表される基に結合されていることが好ましい。スペーサーとしては、特に限定されないが、メチレン基、オキシエチレン基、アミノ基を1個以上有するアルキレン基等が挙げられる。
【0047】
次に、アミノ基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0048】
アミノ基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、特開2006−7203号公報、特開2006−7204号公報、特開2008−174491号公報に開示されている化合物等が挙げられる。
【0049】
容器の表面近傍に存在するカルボキシル基と、表面改質剤が有するアミノ基は、一般的な反応により縮合させると、アミド結合を形成する。具体的には、容器にN−ヒドロキシスクシンイミド、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミドの溶液を仕込み、容器の表面近傍に存在するカルボキシル基を活性エステル化させた後、表面改質剤を容器に仕込む。
【0050】
次に、ヒドロキシル基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0051】
ヒドロキシル基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、L−α−グリセロホスホリルコリン等が挙げられる。
【0052】
容器の表面近傍に存在するカルボキシル基と、表面改質剤が有するヒドロキシル基は、一般的な反応により縮合させると、エステル結合を形成する。具体的には、臭化シアンを用いて、ヒドロキシル基を活性化させた表面改質剤を容器に仕込む。
【0053】
次に、カルボキシル基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0054】
カルボキシル基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、特開2006−11381号公報に開示されている化合物等が挙げられる。
【0055】
容器の表面近傍に存在するアミノ基と、表面改質剤が有するカルボキシル基は、一般的な反応によりを縮合させると、アミド結合を形成する。具体的には、N−ヒドロキシスクシンイミド、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミドの溶液を用いて、カルボキシル基を活性エステル化させた表面改質剤を容器に仕込む。
【0056】
容器の表面近傍に存在するヒドロキシル基と、表面改質剤が有するカルボキシル基は、一般的な反応により縮合させると、エステル結合を形成する。具体的には、臭化シアンを用いて、容器の表面近傍に存在するヒドロキシル基を活性化させた後、表面改質剤を添加する。
【0057】
次に、アルデヒド基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0058】
アルデヒド基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、特開2006−11383号公報に開示されている化合物等が挙げられる。
【0059】
容器の表面近傍に存在するアミノ基と、表面改質剤が有するアルデヒド基は、一般的な反応により縮合させると、イミノ結合を形成する。具体的には、容器に表面改質剤及びメタノールを仕込み、室温で6時間放置した後、シアノトリヒドロホウ素酸ナトリウムを0℃で添加して、一晩加熱攪拌する。反応溶媒としては、メタノール以外にも、水、エタノール、2−プロパノール等のプロトン性溶媒を使用することができるが、メタノールを用いた場合の導入率が高い傾向にある。
【0060】
容器の表面近傍に存在するヒドロキシル基と、表面改質剤が有するアルデヒド基は、一般的な反応により付加させると、アセタール結合を形成する。具体的には、容器に表面改質剤及びメタノールを仕込み、室温で6時間放置した後、シアノトリヒドロホウ素酸ナトリウムを0℃で添加して、一晩加熱攪拌する。反応溶媒としては、メタノール以外にも、水、エタノール、2−プロパノール等のプロトン性溶媒を使用することができるが、メタノールを用いた場合の導入率が高い傾向にある。
【0061】
なお、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器の代わりに、アルデヒド基と、アミノ基及び/又はヒドロキシル基とが表面近傍に存在する容器を用いて、アルデヒド基に対して反応性を有する基と、一般式(1)で表される基を有する表面改質剤を反応させてもよい。
【0062】
容器の表面近傍にアルデヒド基を導入する方法としては、特に限定されないが、表面近傍にアミノ基が存在する容器にグルタルアルデヒドを反応させる方法等が挙げられる。
【0063】
アルデヒド基に対して反応性を有する基としては、アミノ基、ヒドロキシル基等が挙げられるが、反応性が高いことから、アミノ基が好ましい。
【0064】
また、表面改質剤は、アルデヒド基に対して反応性を有する基がスペーサーを介して、一般式(1)で表される基に結合されていることが好ましい。スペーサーとしては、特に限定されないが、メチレン基、オキシエチレン基、アミノ基を1個以上有するアルキレン基等が挙げられる。
【0065】
次に、アミノ基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0066】
アミノ基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、特開2006−7203号公報、特開2006−7204号公報、特開2008−174491号公報に開示されている化合物等が挙げられる。
【0067】
容器の表面近傍に存在するアルデヒド基と、表面改質剤が有するアミノ基は、一般的な反応により縮合させると、イミノ結合を形成する。具体的には、容器に表面改質剤及びメタノールを仕込み、室温で6時間放置した後、シアノトリヒドロホウ素酸ナトリウムを0℃で添加して、一晩加熱攪拌する。反応溶媒としては、メタノール以外にも、水、エタノール、2−プロパノール等のプロトン性溶媒を使用することができるが、メタノールを用いた場合の導入率が高い傾向にある。
【0068】
次に、ヒドロキシル基と、一般式(1)で表される基を有する表面改質剤について説明する。
【0069】
ヒドロキシル基と、一般式(1)で表される基を有する表面改質剤としては、特に限定されないが、L−α−グリセロホスホリルコリン等が挙げられる。
【0070】
容器の表面近傍に存在するアルデヒド基と、表面改質剤が有するヒドロキシル基は、一般的な反応により付加させると、アセタール結合を形成する。具体的には、容器に表面改質剤及びメタノールを仕込み、室温で6時間放置した後、シアノトリヒドロホウ素酸ナトリウムを0℃で添加して、一晩加熱攪拌する。反応溶媒としては、メタノール以外にも、水、エタノール、2−プロパノール等のプロトン性溶媒を使用することができるが、メタノールを用いた場合の導入率が高い傾向にある。
【0071】
また、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器の代わりに、アミノ基又はヒドロキシル基と、カルボキシル基が表面近傍に存在する容器を用いて、アミノ基又はヒドロキシル基に対して反応性を有する基と、一般式(1)で表される基を有する表面改質剤を反応させてもよい。
【0072】
さらに、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器の代わりに、アミノ基及びヒドロキシル基が表面近傍に存在する容器を用いて、アミノ基又はヒドロキシル基に対して反応性を有する基と、ホリルコリン類似基を有する表面改質剤を、容器の表面近傍に未反応のアミノ基及び/又はヒドロキシル基が残留するように反応させてもよい。
【0073】
また、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器の代わりに、カルボキシル基、アミノ基又はヒドロキシル基が表面近傍に存在する容器を用いて、カルボキシル基、アミノ基又はヒドロキシル基に対して反応性を有する基と、一般式(1)で表される基を有する表面改質剤を、容器の表面近傍に未反応のカルボキシル基、アミノ基又はヒドロキシル基が残留するように反応させてもよい。
【0074】
[培養容器Dの第二の実施形態]
培養容器Dの第二の実施形態は、加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器に、加水分解によりシラノール基を生成することが可能な基と、一般式(1)で表される基を有する第一の表面改質剤と、アミノ基、カルボキシル基及び/又はヒドロキシル基と、加水分解によりシラノール基を生成することが可能な基を有する第二の表面改質剤を反応させることにより製造されている。このとき、第一の表面改質剤の分子量は、315〜650である。これにより、一般式(1)で表される基を高密度で導入することができる。
【0075】
なお、接着性細胞Cが間葉系幹細胞である場合は、第一の表面改質剤が有する一般式(1)で表される基に対する第二の表面改質剤が有するアミノ基、カルボキシル基及び/又はヒドロキシル基のモル比は、0.001〜2.4であることが好ましい。モル比が0.001未満であると、細胞が接着しないことがあり、2.4を超えると、細胞が単層の状態で増殖し、凝集しないことがある。
【0076】
容器の表面近傍に加水分解によりシラノール基を生成することが可能な基及び/又はシラノール基を導入する方法としては、加水分解によりシラノール基を生成することが可能な基を有するポリマー(以下、加水分解性ポリマーという)と、アルコキシシランを含有する塗布液を容器に塗布する方法が挙げられる。
【0077】
加水分解性ポリマーと、アルコキシシランを含有する塗布液を容器に塗布すると、加水分解性ポリマーとアルコキシシランが加水分解され、シラノール基が生成する。さらに、シラノール基同士の脱水縮合により、加水分解性ポリマーが架橋され、シラノール基が導入された架橋ポリマー層が形成される。具体的には、材料に塗布液を塗布した後に、水、酸又はアルカリを塗布したり、加熱したりする。また、水、酸又はアルカリを材料に塗布した後に、塗布液を塗布してもよい。さらに、塗布液に、水、酸又はアルカリを混合してもよい。この場合、塗布液中で加水分解が起こるため、塗布時に塗布液を適宜調製することが好ましい。なお、水、酸又はアルカリを用いる場合は、加熱してもよいが、通常、室温で十分反応が進行する。また、水、酸又はアルカリを用いなくても、大気中の水分により緩やかに反応が進行する。
【0078】
加水分解に用いられる酸又はアルカリとしては、加水分解させることが可能なものであれば、特に限定されず、二種以上混合して用いることができ、水溶液として用いてもよい。
【0079】
塗布液としては、有機溶媒中に、加水分解性ポリマーと、アルコキシシランを溶解又は分散させたものを用いることができる。有機溶媒としては、特に限定されないが、脂肪族炭化水素、芳香族炭化水素、塩素化炭化水素、エーテル、炭素数が1〜4の1〜4価の脂肪族アルコール等のアルコール、エチルセロソルブ、ブチルセロソルブ等のセロソルブ、ジオキサン、酢酸メチル、ジホルムアミド等が挙げられ、二種以上併用してもよい。
【0080】
塗布液中の加水分解性ポリマーの含有量は、通常、0.001〜20質量%であり、0.1〜5質量%が好ましい。塗布液中の加水分解性ポリマーの含有量が0.001質量%未満であると、1回の塗布で十分な効果が得られないことがあり、20質量%を超えると、塗布性が低下することがある。
【0081】
また、アルコキシシランに対する加水分解性ポリマーの質量比は、通常、0.01〜20%であり、0.2〜5%が好ましい。アルコキシシランに対する加水分解性ポリマーの質量比が0.01%未満であると、架橋ポリマー層の強度が不十分になることがあり、20%を超えると、架橋ポリマー層に導入されるシラノール基の量が不十分になることがある。
【0082】
塗布液を塗布する方法としては、特に限定されないが、浸漬塗布法、スプレー塗布法、スピンキャスト法等が挙げられる。
【0083】
容器を構成する材料としては、特に限定されないが、PP(ポリプロピレン)、シクロオレフィン樹脂、ポリカーボネート、PET(ポリエチレンテレフタレート)、PEEK、フッ素系樹脂、ポリスチレン、ポリ塩化ビニル等の有機材料;金、チタン、アルミ、鉄、銅、ステンレス、アルミナ、酸化チタン、酸化亜鉛等の無機材料等が挙げられる。
【0084】
加水分解性ポリマーとしては、加水分解によりシラノール基を生成することが可能な基を有するポリマーであれば、特に限定されないが、一般式
【0085】
【化3】

(式中、R1は、水素原子又はメチル基であり、R2は、炭素数が1〜6のアルキレン基、好ましくはプロピレン基であり、R3、R4及びR5は、それぞれ独立に、炭素数が1〜6のアルコキシル基、好ましくはメトキシル基又はエトキシル基である。)
で表されるモノマー(A−1)を重合することにより得られるホモポリマー又はコポリマー(以下、ポリマー(A)という)を用いることができる。このとき、モノマー(A−1)を二種以上用いてもよい。
【0086】
また、ポリマー(A)を合成する際に、一般式
【0087】
【化4】

(式中、R1は、水素原子又はメチル基であり、R2は、炭素数が1〜18の直鎖状、分岐状又は環状のアルキル基、好ましくは炭素数1〜6のアルキル基、特に好ましくはメチル基である。)
で表されるモノマー(A−2)を共重合してもよい。このとき、モノマー(A−2)を二種以上用いてもよい。
【0088】
また、ポリマー(A)を合成する際に、一般式
【0089】
【化5】

(式中、R1は、水素原子又はメチル基であり、R2は、炭素数が1〜6のアルキレン基、好ましくはエチレン基、プロピレン基又は2−ヒドロキシプロピレン基であり、Xは、一般式
【0090】
【化6】

(式中、R1、R2、R3、R4、R5、R6、R7、R8及びR9は、それぞれ独立に、炭素数が1〜6の直鎖又は分岐状のアルキル基、好ましくはメチル基である。)
で表される基(X−1)、一般式
【0091】
【化7】

(式中、R1、R2、R3、R4、R5及びR6は、それぞれ独立に、炭素数が1〜6の直鎖又は分岐状のアルキル基、好ましくはメチル基であり、R7は、炭素数が1〜6の直鎖又は分岐状のアルキル基、好ましくはブチル基であり、xは、正の整数である。)
で表される基(X−2)又は一般式
【0092】
【化8】

(式中、R1、R2、R3、R4、R5及びR6は、それぞれ独立に、炭素数が1〜6の直鎖又は分岐状のアルキル基、好ましくはメチル基であり、R7は、炭素数が1〜6のアルキレン基、好ましくはエチレン基、プロピレン基又は2−ヒドロキシプロピレン基であり、R8は、水素原子又はメチル基であり、yは、正の整数である。)
で表される基(X−3)である。)
で表されるモノマー(A−3)を共重合してもよい。なお、Xが基(X−2)又は(X−3)である場合、モノマー(A−3)は、分子量が1000〜100000であることが好ましく、2000〜20000が特に好ましい。このとき、モノマー(A−3)を二種以上用いてもよい。
【0093】
また、ポリマー(A)を合成する際に、一般式
【0094】
【化9】

(式中、R1は、水素原子又はメチル基であり、R2は、炭素数が1〜6のアルキレン基、好ましくはエチレン基又はプロピレン基であり、Yは、一般式
【0095】
【化10】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1〜6のアルキル基、好ましくはメチル基であり、Z−は、ハロゲン化物イオン又は有機酸若しくは無機酸の共役イオンである。)
で表される基(Y−1)又は一般式
【0096】
【化11】

(式中、R1及びR2は、それぞれ独立に、炭素数が1〜6のアルキル基、好ましくはメチル基である。)
で表される基(Y−2)である。)
で表されるモノマー(A−4)を共重合してもよい。このとき、モノマー(A−4)を二種以上用いてもよい。
【0097】
すなわち、ポリマー(A)を合成する際に、モノマー(A−1)と共に、モノマー(A−2)、モノマー(A−3)及び/又はモノマー(A−4)を共重合してもよい。
【0098】
ポリマー(A)を合成する際に用いられる全モノマー中のモノマー(A−1)の含有量が40〜85質量%であることが好ましい。全モノマー中のモノマー(A−1)の含有量が40質量%未満であると、架橋密度が低下して、親水化の効果が十分に持続しないことがあり、85質量%を超えると、架橋ポリマー層の均一性が低下することがある。
【0099】
また、ポリマー(A)を合成する際に用いられる全モノマー中のモノマー(A−2)の含有量は、通常、1〜75質量%であり、10〜60質量%が好ましい。全モノマー中のモノマー(A−2)の含有量が1質量%未満であると、架橋ポリマー層の耐水性が低下することがあり、75質量%を超えると、ポリマー(A)がアルコールに難溶性となることがある。
【0100】
さらに、ポリマー(A)を合成する際に用いられる全モノマー中のモノマー(A−3)の含有量は、通常、1〜70質量%であり、5〜60質量%が好ましい。全モノマー中のモノマー(A−3)の含有量が1質量%未満であると、架橋ポリマー層の耐水性が低下することがあり、70質量%を超えると、ポリマー(A)がアルコールに難溶性となることがある。
【0101】
また、モノマー(A−1)、モノマー(A−2)及びモノマー(A−3)の総質量に対するモノマー(A−4)の質量の比は、通常、0.01〜1であり、0.05〜0.5が好ましい。この比が0.01未満であると、架橋ポリマー層の柔軟性が低下することがあり、1を超えると、架橋ポリマー層の耐水性が低下することがある。
【0102】
ポリマー(A)の数平均分子量は2000〜150000であることが好ましい。ポリマー(A)の数平均分子量が2000未満であると、架橋ポリマー層を形成する時間が長くなることがあり、150000を超えると、塗布液の粘度が高くなって、塗布性や作業性に劣ることがある。
【0103】
なお、ポリマー(A)の具体例及び製造方法は、特開平11−302129号公報等に開示されている。
【0104】
また、加水分解性ポリマーとしては、一般式
【0105】
【化12】

(式中、R1は、炭素数が1〜22のアルキル基又はフェニル基、好ましくは、メチル基である。)
で表される構成単位(B−1)を有するホモポリマー又はコポリマー(以下、ポリマー(B)という)を用いることができる。このとき、ポリマー(B)は、構成単位(B−1)を二種以上有してもよい。
【0106】
また、ポリマー(B)は、一般式
【0107】
【化13】

(式中、R1及びR2は、それぞれ独立に、炭素数が1〜22のアルキル基又はフェニル基、好ましくは、メチル基である。)
で表される構成単位(B−2)を有してもよい。このとき、ポリマー(B)は、構成単位(B−2)を二種以上有してもよい。
【0108】
ポリマー(B)は、構成単位(B−1)の含有量が1〜90質量%であることが好ましい。構成単位(B−1)の含有量が1質量%未満であると、架橋密度が低下して、親水化の効果が十分に持続しないことがあり、90質量%を超えると、架橋ポリマー層の均一性が低下することがある。
【0109】
さらに、ポリマー(B)は、構成単位(B−2)の含有量が10〜99質量%であることが好ましい。構成単位(B−2)の含有量が10質量%未満であると、架橋ポリマー層の均一性が低下することがあり、99質量%を超えると、架橋密度が低下して、親水化の効果が十分に持続しないことがある。
【0110】
ポリマー(B)の数平均分子量は2000〜500000であることが好ましい。数平均分子量が2000未満であると、架橋ポリマー層を形成する時間が長くなることがあり、500000を超えると、塗布液の粘度が高くなって、塗布性や作業性に劣ることがある。
【0111】
加水分解性ポリマーとして、ポリマー(A)及びポリマー(B)を併用してもよいし、加水分解性ポリマーと非加水分解性ポリマーを併用してもよい。非加水分解性ポリマーとしては、特に限定されないが、加水分解によりシラノール基を生成することが可能な基を有さないポリマー(A)、ポリマー(B)等が挙げられる。
【0112】
容器の表面近傍にシラノール基を導入する方法としては、特に限定されないが、シリコーン樹脂を含む塗布液を容器に塗布することにより、シラノール基を有するシリコーン樹脂を含む膜を形成する方法等が挙げられる。
【0113】
シラノール基を有するシリコーン樹脂を含む膜は、水の接触角が3〜8°であることが好ましい。水の接触角が3°未満である膜を形成することは困難であり、水の接触角が8°を超える膜を形成すると、一般式(1)で表される基を高密度で導入できなくなることがある。
【0114】
塗布液に含まれるシリコーン樹脂としては、特に限定されないが、一般式
(R1O)nSi(R2)4−n
(式中、R1及びR2は、それぞれ独立に、炭素数が1〜8のアルキル基であり、nは、1〜4の整数であり、nが1又は2である場合、複数のR2は、同一であっても異なっていてもよく、nが2又は3である場合、複数のR1は、同一であっても異なっていてもよい。)
で表されるアルコキシシランを加水分解した後、縮合することにより得られる樹脂が挙げられ、二種以上併用してもよい。このとき、水の接触角が3〜8°である膜に含まれるシラノール基を有するシリコーン樹脂は、塗布液に含まれるシリコーン樹脂と同一であってもよいし、異なっていてもよい。
【0115】
塗布液に含まれる有機溶媒としては、特に限定されないが、脂肪族炭化水素、芳香族炭化水素、塩素化炭化水素、エーテル、炭素数が1〜4の1〜4価の脂肪族アルコール等のアルコール、エチルセロソルブ、ブチルセロソルブ等のセロソルブ、ジオキサン、酢酸メチル、ジホルムアミド等が挙げられ、二種以上併用してもよい。
【0116】
塗布液中のシリコーン樹脂の含有量は、通常、0.001〜1質量%であり、0.1〜1質量%が好ましい。塗布液中のシリコーン樹脂の含有量が0.001質量%未満であると、均一な膜が形成されないことがあり、20質量%を超えると、塗布性が低下することがある。
【0117】
塗布液を塗布する方法としては、特に限定されないが、浸漬塗布法、スプレー塗布法、スピンキャスト法等が挙げられる。
【0118】
容器を構成する材料としては、特に限定されないが、ポリカーボネート、PET(ポリエチレンテレフタレート)、ポリスチレン、アクリル樹脂等の有機材料;金、チタン、アルミ、鉄、銅、ステンレス、アルミナ、酸化チタン、酸化亜鉛等の無機材料等が挙げられる。
【0119】
また、シラノール基が表面近傍に存在する容器として、ガラス製の容器を用いてもよい。
【0120】
金属酸化物由来のヒドロキシル基が表面近傍に存在する容器を構成する金属酸化物としては、特に限定されないが、酸化チタン、酸化亜鉛、酸化鉄、酸化クロム、酸化アルミニウム等が挙げられる。
【0121】
半金属酸化物由来のヒドロキシル基が表面近傍に存在する容器を構成する金属酸化物としては、特に限定されないが、酸化ゲルマニウム、酸化ヒ素、酸化ホウ素等が挙げられる。
【0122】
加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基に対して反応性を有する基としては、加水分解によりシラノール基を生成することが可能な基が挙げられる。
【0123】
また、第一の表面改質剤は、加水分解によりシラノール基を生成することが可能な基がスペーサーを介して、一般式(1)で表される基に結合されていることが好ましい。スペーサーとしては、特に限定されないが、メチレン基、オキシエチレン基、アミノ基を1個以上有するアルキレン基等が挙げられる。
【0124】
加水分解によりシラノール基を生成することが可能な基としては、ヒドロシリル基、アルコキシシリル基、ハロシリル基、アシルオキシシリル基、アミノシリル基等が挙げられるが、安定性、反応性等の点から、炭素数が1〜6のアルコキシシリル基又はヒドロシリル基が好ましい。
【0125】
第一の表面改質剤としては、加水分解によりシラノール基を生成することが可能な基と、一般式(1)で表される基を有していれば、特に限定されないが、特開2006−11380号公報に開示されている化合物が挙げられる。
【0126】
第二の表面改質剤としては、アミノ基、加水分解によりカルボキシル基を生成することが可能な基及び/又は加水分解によりヒドロキシル基を生成することが可能な基と、加水分解によりシラノール基を生成することが可能な基を有していれば、特に限定されないが、3−アミノプロピルトリメトキシシラン、p−アミノフェニルトリメトキシシラン等のアミノ基を有する化合物;3−(トリエトキシシリル)プロピルスクシニックアンハイドライド等の加水分解によりカルボキシル基を生成することが可能な基を有する化合物;3−グリシドキシプロピルトリメトキシシラン、3−グリシドキシプロピルメチルジエトキシシラン等の加水分解によりヒドロキシル基を生成することが可能な基を有する化合物等が挙げられ、二種以上併用してもよい。
【0127】
第二の表面改質剤が加水分解によりカルボキシル基及び/又はヒドロキシル基を生成することが可能な基を有する場合は、加水分解によりカルボキシル基及び/又はヒドロキシル基を生成することが可能な基を容器の表面近傍に導入した後に、加水分解によりカルボキシル基及び/又はヒドロキシル基を生成させればよい。
【0128】
なお、第二の表面改質剤が有するアミノ基は、保護基により保護されていてもよい。また、第二の表面改質剤は、加水分解によりカルボキシル基又はヒドロキシル基を生成することが可能な基の代わりに、加水分解以外の反応により脱保護することが可能な保護基により保護されているカルボキシル基又はヒドロキシル基を有していてもよい。
【0129】
第二の表面改質剤が保護基により保護されているアミノ基、カルボキシル基及び/又はヒドロキシル基を有する場合は、保護基により保護されているアミノ基、カルボキシル基及び/又はヒドロキシル基を容器の表面近傍に導入した後に、脱保護によりアミノ基、カルボキシル基及び/又はヒドロキシル基を生成させればよい。
【0130】
次に、加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器に、アミノ基、加水分解によりカルボキシル基を生成することが可能な基及び/又は加水分解によりヒドロキシル基を生成することが可能な基と、一般式(1)で表される基を導入する方法について説明する。
【0131】
まず、加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器に、第一の表面改質剤及び第二の表面改質剤を含む塗布液を塗布する。このとき、加水分解によりシラノール基を生成することが可能な基が加水分解され、シラノール基が生成する。さらに、容器の表面近傍に存在するシラノール基、半金属酸化物の加水分解により生成したヒドロキシル基及び/又は金属酸化物の加水分解により生成したヒドロキシル基と、表面改質剤の加水分解により生成したシラノール基の脱水縮合により、容器の表面が改質される。具体的には、容器に塗布液を塗布した後に、水、酸又はアルカリを塗布したり、加熱したりする。また、水、酸又はアルカリを容器に塗布した後に、塗布液を塗布してもよい。さらに、塗布液に、水、酸又はアルカリを混合してもよい。この場合、塗布液中で加水分解が起こるため、塗布時に塗布液を適宜調製することが好ましい。なお、水、酸又はアルカリを用いる場合は、加熱してもよいが、通常、室温で十分反応が進行する。また、水、酸又はアルカリを用いなくても、大気中の水分により緩やかに反応が進行する。
【0132】
酸又はアルカリとしては、加水分解によりシラノール基を生成することが可能な基を加水分解させることが可能であれば、特に限定されず、二種以上併用してもよい。なお、加水分解に用いられる酸又はアルカリは、水溶液として用いてもよい。
【0133】
塗布液としては、有機溶媒中に、第一の表面改質剤及び第二の表面処理剤を溶解又は分散させたものを用いることができる。有機溶媒としては、脂肪族炭化水素、芳香族炭化水素、塩素化炭化水素、エーテル、炭素数が1〜4の1〜4価の脂肪族アルコール等のアルコール、エチルセロソルブ、ブチルセロソルブ等のセロソルブ、ジオキサン、酢酸メチル、ジホルムアミド等が挙げられる。
【0134】
塗布液中の第一の表面改質剤の含有量は、通常、0.1〜30質量%であり、1〜10質量%が好ましい。塗布液中の第一の表面改質剤の含有量が0.1質量%未満であると、1回の塗布で第一の表面改質剤を十分に塗布できないことがあり、30質量%を超えると、塗布性が低下することがある。
【0135】
塗布液を塗布する方法としては、特に限定されないが、浸漬塗布法、スプレー塗布法、スピンキャスト法等が挙げられる。
【0136】
なお、第一の表面処理剤を含む塗布液及び第二の表面処理剤を含む塗布液を、それぞれ容器に塗布してもよい。
【0137】
また、容器の表面近傍に未反応のシラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が残留するように、表面改質剤由来のシラノール基と、容器由来のシラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基を反応させてもよい。
【0138】
[培養容器Dの第三の実施形態]
培養容器Dの第三の実施形態は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式(1)で表される基を有する樹脂を含む層が表面に形成されている。
【0139】
アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式(1)で表される基を有する樹脂としては、特に限定されないが、一般式(1)で表される基を有するモノマーと、アミノ基を有するモノマー、カルボキシル基を有するモノマー及び/又はヒドロキシル基を有するモノマーを共重合することにより得られる樹脂が挙げられる(例えば、特開平7−184990号公報参照)。
【0140】
容器を構成する材料としては、特に限定されないが、シクロオレフィン樹脂、ポリカーボネート、PET(ポリエチレンテレフタレート)、ポリスチレン、アクリル樹脂等の有機材料;金、チタン、アルミ、鉄、銅、ステンレス、アルミナ、酸化チタン、酸化亜鉛等の無機材料等が挙げられる。
【0141】
なお、有機材料から構成される容器を用いる場合、容器に対する接着性を考慮すると、一般式(1)で表される基を有するモノマーと、アミノ基、カルボキシル基及び/又はヒドロキシル基を有するモノマーと、疎水性基を有するモノマーを共重合することにより得られる樹脂を用いることが好ましい。
【0142】
疎水性基を有するモノマーとしては、特に限定されないが、メタクリル酸ブチル等が挙げられる。
【0143】
容器の表面近傍に、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式(1)で表される基を有する樹脂を含む層を形成する方法としては、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式(1)で表される基を有する樹脂を含む塗布液を容器に塗布する方法が挙げられる。
【0144】
塗布液としては、有機溶媒中に、樹脂を溶解又は分散させたものを用いることができる。有機溶媒としては、脂肪族炭化水素、芳香族炭化水素、塩素化炭化水素、エーテル、炭素数が1〜4の1〜4価の脂肪族アルコール等のアルコール、エチルセロソルブ、ブチルセロソルブ等のセロソルブ、ジオキサン、酢酸メチル、ジホルムアミド等が挙げられる。
【0145】
塗布液中の樹脂の含有量は、通常、0.1〜30質量%であり、1〜10質量%が好ましい。塗布液中の樹脂の含有量が0.1質量%未満であると、1回の塗布で樹脂を十分に塗布できないことがあり、30質量%を超えると、塗布性が低下することがある。
【0146】
塗布液を塗布する方法としては、特に限定されないが、浸漬塗布法、スプレー塗布法、スピンキャスト法等が挙げられる。
【0147】
本発明の細胞凝集塊の形成方法に、ヒト、ラット、マウス、霊長類等の哺乳類に由来する接着性細胞を適用すると、後述する物質のスクリーニング方法及び細胞の機能探索方法に有用である。
【0148】
本発明において、接着性細胞を培養する方法としては、特に限定されず、接着性細胞に応じて、公知の条件を適用することができるが、10質量%のウシ胎児血清(FBS)、1mMのグルタミン、適量の抗生物質を含むダルベッコ改変培地(DMEM)を用いて、5体積%の二酸化炭素を含む雰囲気下、37℃で接着性細胞を培養する方法等が挙げられる。
【0149】
本発明の物質のスクリーニング方法は、本発明の細胞凝集塊の形成方法により形成されている細胞凝集塊を用いて物質をスクリーニングする。このとき、本発明の物質のスクリーニング方法は、肝細胞や心筋細胞を用いて物質の毒性を評価する方法、ガン細胞を用いて薬剤の効果を試験する方法等の公知の物質のスクリーニング方法に適用することができる。物質の毒性を評価する方法としては、MTTアッセイ、アラマーブルーアッセイ等の細胞増殖を基準とする方法が挙げられる。また、RT−PCR、ELISA等の方法により、炎症性サイトカインの産生放出、癌化に関連する因子であるSDF−1、LIF、EGFR等の量を定量することもできる。
【0150】
また、本発明の物質のスクリーニング方法は、個体毎の接着性細胞の細胞凝集塊を用いて物質をスクリーニングすることにより、テーラーメイド医療に応用することができる。
【0151】
本発明の細胞の機能探索方法は、本発明の細胞凝集塊の形成方法により形成されている細胞凝集塊を用いて細胞の機能を探索する。このとき、本発明の細胞の機能探索方法は、接着性細胞の生化学的機能を解明する方法、バイオマーカーを探索する方法等の公知の細胞の機能探索方法に適用することができる。
【実施例】
【0152】
[実施例1]
プライマリアディッシュ(日本ベクトン・ディッキンソン社製)に、N−ヒドロキシスクシンイミド1g、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド1gの1質量%水溶液を仕込んだ後、化学式
【0153】
【化14】

で表される化合物(A)1gを水100mlに溶解させた溶液を添加し、アミド化した。次に、プライマリアディッシュから液を取り出し、室温で5時間乾燥させた後、水洗し、乾燥させ、培養容器を得た。なお、プライマリアディッシュは、酸素とアンモニアを含む雰囲気下でプラズマ処理されているポリスチレン製のディッシュである。
【0154】
培養容器に、MensenPRO RS培地(Invitrogen社製)10ml及び間葉系幹細胞としてのヒト脂肪由来幹細胞(Invitrogen社製)1×106個/容器を添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図2A及び図2B参照)。
【0155】
[比較例1]
表面処理されていないポリスチレン製のペトリディッシュ(日本ベクトン・ディッキンソン社製)に、MensenPRO RS培地(Invitrogen社製)10ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×106個/ディッシュを添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が単層の状態で増殖し、細胞凝集塊を形成しなかった(図3参照)。
【0156】
[アルカリホスファターゼ活性]
実施例1の細胞凝集塊及び比較例1の培養細胞に4質量%パラホルムアルデヒド・リン酸緩衝液を添加して5分間処理した後、TBS緩衝液及びTBST緩衝液を用いて洗浄した。次に、BMパープルAP基質(Roche社製)を添加して、37℃で1時間反応させた後、TBST緩衝液を用いて洗浄した。評価結果を図4A及び図4Bに示す。図4A及び図4Bから、実施例1の細胞凝集塊は、アルカリホスファターゼ活性が陽性であるが、比較例1の培養細胞は、アルカリホスファターゼ活性が陰性であることがわかる。
【0157】
[免疫二重染色]
実施例1の細胞凝集塊及び比較例1の培養細胞に4質量%パラホルムアルデヒド・リン酸緩衝液を添加して5分間処理した後、TBS緩衝液及びTBST緩衝液を用いて洗浄した。次に、第一の一次抗体を、カタログに記載されている方法で希釈し、細胞に反応させた後、第一のAlexa Fluor標識二次抗体(Invitrogen社製)を細胞に反応させ、TBST緩衝液を用いて洗浄した。さらに、第二の一次抗体を、カタログに記載されている方法で希釈し、細胞に反応させた後、第二のAlexa Fluor標識二次抗体(Invitrogen社製)を細胞に反応させ、TBST緩衝液を用いて洗浄した。評価結果を表1に示す。
【0158】
【表1】

なお、Nestin(Abcam社製)、CD271(Abcam社製)及びCD133(Abcam社製)は、それぞれ神経由来幹細胞マーカー、脂肪由来幹細胞マーカー及び幹細胞マーカーであり、PDGFRa(R&D社製)及びPDGFRb(R&D社製)は、間葉系幹細胞マーカーである。また、実施例1の細胞凝集塊の評価結果を図5〜8に示す。表1から、実施例1の細胞凝集塊は、Nestinが陽性であるため、脂肪由来幹細胞がin vitroで神経由来幹細胞の性質を獲得できることがわかる。
【0159】
[実施例2−1]
3−アミノプロピルトリメトキシシランの0.15mol/Lメタノール溶液0.01mL、化学式
【0160】
【化15】

で表される化合物(B)の0.15mol/Lメタノール溶液9.99mL及びメタノール10mLからなる塗布液を得た。
【0161】
得られた塗布液をガラスボトムディッシュ(松浪硝子工業社製)に塗布し、室温で乾燥させた。次に、加熱乾燥し、室温で乾燥させた後、水洗し、乾燥させ、培養容器を得た。
【0162】
培養容器に、MensenPRO RS培地(Invitrogen社製)2.5ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×105個/容器を添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図9参照)。
【0163】
[実施例2−2]
3−アミノプロピルトリメトキシシランの0.15mol/Lメタノール溶液0.5mL、化合物(B)の0.15mol/Lメタノール溶液9.5mL及びメタノール10mLからなる塗布液を得た。
【0164】
得られた塗布液をガラスボトムディッシュ(松浪硝子工業社製)に塗布し、室温で乾燥させた。次に、加熱乾燥し、室温で乾燥させた後、水洗し、乾燥させ、培養容器を得た。
【0165】
培養容器に、MensenPRO RS培地(Invitrogen社製)2.5ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×105個/容器を添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図10参照)。
【0166】
[実施例2−3]
3−アミノプロピルトリメトキシシランの0.15mol/Lメタノール溶液7mL、化合物(B)の0.15mol/Lメタノール溶液3mL及びメタノール10mLからなる塗布液を得た。
【0167】
得られた塗布液をガラスボトムディッシュ(松浪硝子工業社製)に塗布し、室温で乾燥させた。次に、加熱乾燥し、室温で乾燥させた後、水洗し、乾燥させ、培養容器を得た。
【0168】
培養容器に、MensenPRO RS培地(Invitrogen社製)2.5ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×105個/容器を添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図11参照)。
【0169】
[比較例2]
表面処理されていないガラスボトムディッシュ(松浪硝子工業社製)に、MensenPRO RS培地(Invitrogen社製)2.5ml及びヒト脂肪由来幹細胞(Invitrogen社製)1×105個/ディッシュを添加し、ヒト脂肪由来幹細胞を培養したところ、細胞が単層の状態で増殖し、細胞凝集塊を形成しなかった(図12参照)。
【0170】
[免疫染色]
実施例2−2の細胞凝集塊に4質量%パラホルムアルデヒド・リン酸緩衝液を添加して5分間処理した後、0.2質量%Triton X−100(ロシュ・ダイアグノスティックス社製)/TBS緩衝液及び0.2質量%Tween20(東京化成工業社製)/TBS緩衝液を用いて洗浄した。次に、Protein Block(DAKO社製)で非特異反応をブロッキングした。さらに、200倍に希釈した一次抗体の抗CD271ラビットポリクローナル抗体(abcam社製)及びCD90マウスモノクローナル抗体(abcam社製)を細胞に一晩反応させた後、0.2質量%Tween20(東京化成工業社製)/TBS緩衝液を用いて洗浄した。次に、250倍に希釈したそれぞれ緑色及び赤色に発色する蛍光二次抗体のAlexa488 抗ラビット抗体(Invitrogen社製)及びAlexa594 抗マウス抗体(Invitrogen社製)を細胞に2時間反応させた後、0.2質量%Tween20(東京化成工業社製)/TBS緩衝液を用いて洗浄した。さらに、青色に発色するVectorshield−DAPI(Vector社製)で核を染色した後、共焦点レーザー顕微鏡LSM 5 PASCAL(Carl Zeiss社製)を用いて観察した。その結果、実施例2−2の細胞凝集塊が緑色に発色していたことから、CD271が陽性であることがわかった(図13参照)。
【0171】
なお、実施例2−1及び実施例2−3の細胞凝集塊も、実施例2−2の細胞凝集塊と同様に緑色に発色し、CD271が陽性であった。
【0172】
[実施例3]
プライマリアディッシュ(日本ベクトン・ディッキンソン社製)に、N−ヒドロキシスクシンイミド89mg、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド149mgを水10mLに溶解させた水溶液を仕込んだ後、化合物(A)200mgを水10mlに溶解させた溶液を添加し、アミド化した。次に、プライマリアディッシュから液を取り出した後、水洗し、乾燥させ、培養容器を得た。
【0173】
培養容器に、10質量%のウシ胎児血清(FBS)を含むMEM培地(SIGMA−ALDRICH社製)3ml及びガン細胞としてのヒト肝ガン細胞(プライマリーセル社製)1×105個/容器を添加し、ヒト肝ガン細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図14参照)。
【0174】
[比較例3]
プライマリアディッシュ(日本ベクトン・ディッキンソン社製)に、10質量%のウシ胎児血清(FBS)を含むMEM培地(SIGMA−ALDRICH社製)3ml及びガン細胞としてのヒト肝ガン細胞(プライマリーセル社製)1×105個/容器を添加し、ヒト肝ガン細胞を培養したところ、細胞が単層の状態で増殖し、細胞凝集塊を形成しなかった(図15参照)。
【0175】
[アルブミンの産生量]
実施例3及び比較例3のヒト肝ガン細胞を培養した培地中のアルブミンの産生量を、ヒトアルブミン定量キット(コスモバイオ社製)を用いて、ELISA法により定量した。評価結果を図16に示す。図16から、実施例3の細胞凝集塊は、アルブミンの産生量が比較例3の培養細胞よりも大きいことがわかる。
【0176】
[CYP1A1の活性]
実施例3の細胞凝集塊及び比較例3の培養細胞を10質量%のウシ胎児血清(FBS)、8μMの7−エトキシレゾルフィン及び10μMのジクマロールを含むMEM培地(SIGMA−ALDRICH社製)中、37℃で30分間培養した。次に、培養上清に、β−グルクロニダーゼ及びアリルスルファターゼを含む酢酸緩衝液を添加して37℃で2時間反応させた。さらに、溶液中のレゾルフィン量を蛍光測定(励起波長530nm、蛍光波長590nm)により、定量し、細胞が産生したCYP1A1の活性を評価した。評価結果を図17に示す。図17から、実施例3の細胞凝集塊は、CYP1A1の活性が比較例3の培養細胞よりも大きいことがわかる。
【0177】
[遺伝子発現]
実施例3の細胞凝集塊及び比較例3の培養細胞の遺伝子発現を、Lightcycler 480−II(Roche社製)を用いて、PCR法により、定量した。評価結果を図18に示す。図18から、実施例3の細胞凝集塊は、CYP1A1、ALB、LDLR、ATP51及びCol1A1の遺伝子発現が比較例3の培養細胞よりも大きいことがわかる。なお、内部標準としては、GAPDHを用いた。
【0178】
[実施例4]
ヒト肝ガン細胞(プライマリーセル社製)の代わりに、ヒト乳腺由来ガン細胞(理研BRC製)を用いた以外は、実施例3と同様にして、ヒト乳腺由来ガン細胞を培養したところ、細胞が増殖して自律的に凝集し、細胞凝集塊を形成した(図19参照)。
【0179】
[比較例4]
ヒト肝ガン細胞(プライマリーセル社製)の代わりに、ヒト乳腺由来ガン細胞(理研BRC製)を用いた以外は、比較例3と同様にして、ヒト乳腺由来ガン細胞を培養したところ、細胞が単層の状態で増殖し、細胞凝集塊を形成しなかった(図20参照)。
【0180】
[アルカリホスファターゼ活性]
実施例4の細胞凝集塊及び比較例4の培養細胞に4質量%パラホルムアルデヒド・リン酸緩衝液を添加して5分間処理した後、TBS緩衝液及びTBST緩衝液を用いて洗浄した。次に、BMパープルAP基質(Roche社製)を添加して、37℃で1時間反応させた後、TBST緩衝液を用いて洗浄した。評価結果を図21A及び図21Bに示す。図21A及び図21Bから、実施例4の細胞凝集塊は、アルカリホスファターゼ活性が陽性であるが、比較例4の培養細胞は、アルカリホスファターゼ活性が陰性であることがわかる。
【0181】
[遺伝子発現]
実施例4の細胞凝集塊及び比較例4の培養細胞の遺伝子発現を、Lightcycler 480−II(Roche社製)を用いて、PCR法により、定量した。評価結果を図22に示す。図22から、実施例4の細胞凝集塊は、VEGF−Aの遺伝子発現が比較例4の培養細胞よりも大きいことがわかる。なお、内部標準としては、GAPDHを用いた。
【符号の説明】
【0182】
C 接着性細胞
C' 細胞凝集塊
D 培養容器
M 培地
【特許請求の範囲】
【請求項1】
培養容器を用いて、接着性細胞を培養して細胞凝集塊を形成する方法であって、
前記培養容器は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式
【化1】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1以上6以下のアルキル基であり、mは、2以上6以下の整数である。)
で表される基が表面近傍に存在し、
前記接着性細胞は、間葉系幹細胞、肝細胞又はガン細胞であることを特徴とする細胞凝集塊の形成方法。
【請求項2】
前記培養容器は、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器に、カルボキシル基、アミノ基又はヒドロキシル基に対して反応性を有する基と、前記一般式で表される基を有し、分子量が225以上650以下である化合物を反応させることにより製造されていることを特徴とする請求項1に記載の細胞凝集塊の形成方法。
【請求項3】
前記カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器は、酸素、オゾン及び/又は水蒸気と、アンモニア及び/又は窒素を含む雰囲気下でプラズマ処理することにより製造されていることを特徴とする請求項2に記載の細胞凝集塊の形成方法。
【請求項4】
前記培養容器は、加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器に、加水分解によりシラノール基を生成することが可能な基と、前記一般式で表される基を有し、分子量が315以上650以下である第一の化合物と、アミノ基、加水分解によりカルボキシル基を生成することが可能な基及び/又は加水分解によりヒドロキシル基を生成することが可能な基と、加水分解によりシラノール基を生成することが可能な基を有する第二の化合物を反応させることにより製造されていることを特徴とする請求項1に記載の細胞凝集塊の形成方法。
【請求項5】
前記培養容器は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、前記一般式で表される基を有する樹脂を含む層が表面に形成されていることを特徴とする請求項1に記載の細胞凝集塊の形成方法。
【請求項6】
請求項1乃至5のいずれか一項に記載の細胞凝集塊の形成方法を用いて、細胞凝集塊を形成する工程と、
該細胞凝集塊を用いて物質をスクリーニングする工程を有することを特徴とする物質のスクリーニング方法。
【請求項7】
請求項1乃至5のいずれか一項に記載の細胞凝集塊の形成方法を用いて、細胞凝集塊を形成する工程と、
該細胞凝集塊を用いて細胞の機能を探索する工程を有することを特徴とする細胞の機能探索方法。
【請求項8】
接着性細胞が増殖して自律的に凝集した細胞凝集塊であって、
前記接着性細胞は、間葉系幹細胞、肝細胞又はガン細胞であることを特徴とする細胞凝集塊。
【請求項9】
アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式
【化2】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1以上6以下のアルキル基であり、mは、2以上6以下の整数である。)
で表される基が表面近傍に存在することを特徴とする培養容器。
【請求項1】
培養容器を用いて、接着性細胞を培養して細胞凝集塊を形成する方法であって、
前記培養容器は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式
【化1】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1以上6以下のアルキル基であり、mは、2以上6以下の整数である。)
で表される基が表面近傍に存在し、
前記接着性細胞は、間葉系幹細胞、肝細胞又はガン細胞であることを特徴とする細胞凝集塊の形成方法。
【請求項2】
前記培養容器は、カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器に、カルボキシル基、アミノ基又はヒドロキシル基に対して反応性を有する基と、前記一般式で表される基を有し、分子量が225以上650以下である化合物を反応させることにより製造されていることを特徴とする請求項1に記載の細胞凝集塊の形成方法。
【請求項3】
前記カルボキシル基、アミノ基及びヒドロキシル基が表面近傍に存在する容器は、酸素、オゾン及び/又は水蒸気と、アンモニア及び/又は窒素を含む雰囲気下でプラズマ処理することにより製造されていることを特徴とする請求項2に記載の細胞凝集塊の形成方法。
【請求項4】
前記培養容器は、加水分解によりシラノール基を生成することが可能な基、シラノール基、半金属酸化物由来のヒドロキシル基及び/又は金属酸化物由来のヒドロキシル基が表面近傍に存在する容器に、加水分解によりシラノール基を生成することが可能な基と、前記一般式で表される基を有し、分子量が315以上650以下である第一の化合物と、アミノ基、加水分解によりカルボキシル基を生成することが可能な基及び/又は加水分解によりヒドロキシル基を生成することが可能な基と、加水分解によりシラノール基を生成することが可能な基を有する第二の化合物を反応させることにより製造されていることを特徴とする請求項1に記載の細胞凝集塊の形成方法。
【請求項5】
前記培養容器は、アミノ基、カルボキシル基及び/又はヒドロキシル基と、前記一般式で表される基を有する樹脂を含む層が表面に形成されていることを特徴とする請求項1に記載の細胞凝集塊の形成方法。
【請求項6】
請求項1乃至5のいずれか一項に記載の細胞凝集塊の形成方法を用いて、細胞凝集塊を形成する工程と、
該細胞凝集塊を用いて物質をスクリーニングする工程を有することを特徴とする物質のスクリーニング方法。
【請求項7】
請求項1乃至5のいずれか一項に記載の細胞凝集塊の形成方法を用いて、細胞凝集塊を形成する工程と、
該細胞凝集塊を用いて細胞の機能を探索する工程を有することを特徴とする細胞の機能探索方法。
【請求項8】
接着性細胞が増殖して自律的に凝集した細胞凝集塊であって、
前記接着性細胞は、間葉系幹細胞、肝細胞又はガン細胞であることを特徴とする細胞凝集塊。
【請求項9】
アミノ基、カルボキシル基及び/又はヒドロキシル基と、一般式
【化2】

(式中、R1、R2及びR3は、それぞれ独立に、炭素数が1以上6以下のアルキル基であり、mは、2以上6以下の整数である。)
で表される基が表面近傍に存在することを特徴とする培養容器。
【図1A】


【図1B】


【図16】


【図17】


【図18】


【図22】


【図2A】


【図2B】


【図3】


【図4A】


【図4B】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図19】


【図20】


【図21A】


【図21B】




【図1B】


【図16】


【図17】


【図18】


【図22】


【図2A】


【図2B】


【図3】


【図4A】


【図4B】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図19】


【図20】


【図21A】


【図21B】


【公開番号】特開2012−187097(P2012−187097A)
【公開日】平成24年10月4日(2012.10.4)
【国際特許分類】
【出願番号】特願2011−265210(P2011−265210)
【出願日】平成23年12月2日(2011.12.2)
【出願人】(000001959)株式会社 資生堂 (1,748)
【Fターム(参考)】
【公開日】平成24年10月4日(2012.10.4)
【国際特許分類】
【出願日】平成23年12月2日(2011.12.2)
【出願人】(000001959)株式会社 資生堂 (1,748)
【Fターム(参考)】
[ Back to top ]

