細胞分析の進歩した方法および装置
本発明の実施例は、細胞、細胞凝集塊、固形腫瘍などを解析するための進歩した方法および装置を目的としている。斯かる方法および装置は、例えば、病理学の分野で有用であり、進歩した細胞処理術および解析結果を提供することができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明の実施例は、細胞、細胞凝集塊、または、固形腫瘍を分析する進歩した方法および装置に関するものである。このような方法および装置は、例えば、病理学の分野で有用であり、進歩した細胞処理および分析結果を提供することができる。
【背景技術】
【0002】
従来からの病理学的試料を大量処理するのに、細胞を殺傷することに関与したり試料処理時間が冗長である方法を採用してきた。このような方法は、治療の時点からかなり経てから実験室で実施されるのが一般的である。このような従来からの方法は、治療の時点で生細胞に対する動的生体マーカー法などのような生細胞検査を行うことができないうえに、治療の時点で迅速に試料処理したり分析結果生成を行うことができない。完全かつ即時取得された情報をこのように逸しているせいで、医者は適切な治療管理法を指定することができないか、或いは、少なくとも処理を遅延させてしまい、患者の生活の質に悪影響を及ぼすことになる。従来の処理を幾つかの進歩した実施例と対比させた一例を図9に示した。
【0003】
例えば、腫瘍学者は、治療の標準と特色づけられる、複数薬剤を各種組合わせて使用する方法とか、特定癌について承認を得ているという評判は得ていないがその特定の癌に有効であると実証されている多数の薬剤を使用する方法とかいった多様な治療選択肢を採用することができる。良好な治療成果を得る最も高い見込みを実現する要件として、患者に利用できる最適癌治療を施すこと、および、このような施療指定が診断後に極力迅速に行われることが挙げられる。
【0004】
或る種の癌はゲノムマーカーを利用して容易に同定することができ、癌は1種類または多数種類(通例は多数種類である)の正常な遺伝子が異常な発現をしたものであるという言い方が特徴をより適切に表していると思われるが、そのような癌の全てについて信頼できるゲノムマーカーが入手できるわけではない。癌を特定種類別に診断してから遺伝子発現に基づいて複数の異なる治療戦略の見込みのある効力を評価するのに目下利用できる診断試験には欠点があって、例えば、(1)斯かる試験は血液検査用に設計されたものであって、固形腫瘍を検査するのに適合させるのは容易ではないこと、(2)細胞解離処理などのような固形腫瘍試料の調製方法は、生細胞を処理したり、その後でマーカー発現を測定するのには好適とは言えない場合があること、(3)穿刺生検法などを利用して得られた小型試料は完全な分析を行うのに十分な組織として作用し得ないこと、(4)斯かる試験は生体外で細胞を培養する必要があるうえに、より長い培養期間を必要とし、患者から被験細胞を採取してから細胞を検査するまでに相当な遅延を見込む必要があり、または、これら全部を要件とするため、多様な外的影響がマーカー発現に及ぼされる潜在的可能性を生じてしまうこと、(5)斯かる試験は、発現を異常であると認識して特性を定めるのに重要である多数の遺伝子、多数の燐蛋白質、または、それ以外の多数のマーカーの発現を同時平行式に測定するのには不適となる場合があること、(6)斯かる試験は定量検査ではなく、或る蛋白質が存在していることまたは不在であることが複数遺伝子の相対発現レベルに反するものであると判定するのに原則的には免疫組織化学法に依存していること、(7)試薬および細胞処理条件が厳密に抑制されることなく、検査ごとに、更にまた、検査所ごとにかなりの差異を生じること、(8)斯かる試験は、RNAが不安定であるうえに患者から十分に新鮮な試料を採取するのが実際上困難であるせいで、RNAレベルの解析には不適切であること、(9)斯かる試験は、遺伝子発現解析を実施する前に、例えば、選択された試薬の存在下で、または、選択された試薬の不在時に細胞を固定する処理を含んでいる場合があること等の欠点がある。
【0005】
近年、マイクロアレイ遺伝子発現解析による多様な癌種類の分類に関する研究が公開されている(例えば、ガループ(Golub)ほか著の1999年刊行『サイエンス(Science)』286号531-537掲載論文、バタカルヤエ(Bhattacharjae)ほか著の2001年刊行『米国科学アカデミー(National Academy of Science, USA)会報』98号13790-13795掲載論文、チェンシャン(Chen-Hsiang)ほか著の2001年刊行『生物情報科学(Bioinformatics)』17号の別冊1のセクション316-322、ラマスウォミー(Ramaswamy)ほか著の2001年刊行『米国科学アカデミー会報』98号15149-15154掲載論文などを参照のこと)。遺伝子発現パターンに基づいて行ったヒトの乳癌の或る種の分類も報告されている(マーチン(Martin)ほか著の2000年刊行『癌研究(Cancer Research)』60号2232-2238掲載論文、ウエスト(West)ほか著の2001年刊行『米国科学アカデミー会報』98号11462-11467掲載論文、ソーリー(Sorlie)ほか著の2001年刊行『米国科学アカデミー会報』98号10869-10874掲載論文、ヤン(Yan)ほか著の2001年刊行『癌研究』61号8375-8380掲載論文を参照のこと)。しかしながら、上述の各研究はもっぱら多様な種類の癌についての既存の分類の改良と精査のし直しに主眼を置き、互いに異なる発現をした複数遺伝子の関係に新たな洞察を行ったものとは凡そ言い難い。このような研究は新たな発見を治療戦略と結びつけて癌治療の臨床的成果を進展させるものではないうえに、細胞の処理・解析の既存の技術を向上させ標準化するという問題に対処するものでもない。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】ガループ(Golub)ほか著、『サイエンス(Science)』286号531-537掲載論文、1999年刊
【非特許文献2】バタカルヤエ(Bhattacharjae)ほか著、『米国科学アカデミー(National Academy of Science, USA)会報』98号13790-13795掲載論文、2001年刊
【非特許文献3】チェンシャン(Chen-Hsiang)ほか著、『生物情報科学(Bioinformatics)』17号の別冊1のセクション316-322、2001年刊
【非特許文献4】ラマスウォミー(Ramaswamy)ほか著、『米国科学アカデミー会報』98号15149-15154掲載論文、2001年刊
【非特許文献5】マーチン(Martin)ほか著、『癌研究(Cancer Research)』60号2232-2238掲載論文、2000年刊
【非特許文献6】ウエスト(West)ほか著、『米国科学アカデミー会報』98号11462-11467掲載論文、2001年刊
【非特許文献7】ソーリー(Sorlie)ほか著、『米国科学アカデミー会報』98号10869-10874掲載論文、2001年刊
【非特許文献8】ヤン(Yan)ほか著、『癌研究』61号8375-8380掲載論文、2001年刊
【発明の概要】
【発明が解決しようとする課題】
【0007】
近年の分子生物学および生体化学は100種類を超える遺伝子とその活動の影響を受けた腫瘍細胞それぞれの動向、腫瘍細胞それぞれの分化状態、および、或る種の治療薬に対する腫瘍細胞それぞれの感度または耐性などを解明してきたが、このような遺伝子の状態を薬物治療に関わる臨床上の判断を定常的に行う目的で利用することは、2〜3の例外を除いてこれまで皆無であった。注目に値する一例外として、乳癌においてタモキシフェンなどのような抗エストロゲン剤を使った治療を施すにあたり患者の適否選別にエストロゲン受容体(ER)蛋白質発現を利用する方法がある。もう1つの例外的な具体例として、乳癌においてHer2拮抗薬ヘルセプチンを使うにあたり患者の適否選別にErbB2 (Her2) 蛋白質発現を利用する方法がある(ヘルセプチン(Herceptin)は米国カリフォルニア州サウスサンフランシスコのジェネンテク・インコーポレーティッド(Genentech, Inc.)登録商標である)。しかし、大半の癌について、遺伝子発現の病理は微妙さを増すことがあるうえに、多数遺伝子の発現パターンまたは特定の刺激に反応した遺伝子発現のパターンに関与することがある。
【0008】
癌治療への困難な取組みは依然として、特定治療管理を目標に掲げて腫瘍種類を病理学的に弁別することであり、更にまた、出来るだけ早期に最適治療を見極めて最適成果を得ることである。このため、多様な治療選択肢に対する患者の反応に関する予後、予報、または、その両方を同時に供与する検査が必要である。
【0009】
上述の各種欠点に対処するとともに組織試料を処理して調製する機能を単体の小型装置に統合して実施するにあたり、組織試料の生存力を維持して、組織試料が生存力を喪失する前に、または、生体外複製により培養されなくとも、同じ組織試料を刺激することができるようにする、同じ組織試料から得られた複数の互いに異なる生体マーカー反応を保存することができるようにする、または、同じ組織試料を刺激して尚且つ生体マーカー反応の保存も行うことができるようにするよく管理されて一貫性があるうえに効率的でもある幾つかの処理工程を採用した、固形腫瘍またはそれ以外の細胞凝集塊の生検材料調製装置および生検材料調製方法が必要である。
【課題を解決するための手段】
【0010】
本発明の実施例は、被検体から採取した細胞凝集塊を処理または調製して生組織試料にする方法を目的としている。この方法は、被検体から採取された生細胞凝集塊を水性溶液中に解離および分散させて生細胞凝集塊を含有している少なくとも1分割量の部分標本を第1隔離室内に入れる工程と、任意で、混入細胞を除去することにより標的細胞の残余の混入細胞に対する割合を増大させるようにこの部分標本を高純度化する工程と、任意で高純度化された生細胞を解析に付すために1個以上の第2隔離室内に分配する工程と、分配済みの細胞の細胞解析、分子解析、または、その両方の解析を行えるようにするために分配済みの細胞を安定させる工程とを含んでいるとよい。
【0011】
本発明はまた、或る実施例においては、固形腫瘍から採取した癌細胞を処理または調製する方法を目的としており、斯かる方法は固形腫瘍から得られた癌の生細胞を解離および分散させて少なくとも1分割量の部分試験標本を少なくとも1個の第1隔離室に入れる工程と、任意で混入物を除去するように癌の生細胞を高純度化する工程と、癌の生細胞を解析に付すために1個以上の第2隔離室に分配する工程と、分配済みの細胞の細胞解析、分子解析、または、その両方の解析を行えるようにするために分配済みの細胞を安定させる工程とを含んでいる。
【0012】
更に、本発明の或る実施例は細胞処理用のカートリッジを目的としている。例えば、複数の無菌室が設けられた、癌の生細胞を処理または調製する用途に付されるカートリッジにおいては、無菌室は互いに隔絶されているようにするとよい。他の実施例はまた、細胞を分散させる室、細胞を高純度化する室、および、隔離室である室などから構成された複数の小室が設けられているカートリッジを目的とする。
【0013】
本発明はまた、本発明のカートリッジと解析デバイスから構成されているシステムを目的としている。本発明のカートリッジを含んでいるキットも本発明に包含されている。
【図面の簡単な説明】
【0014】
【図1】図1は本発明のカートリッジの具体的な実施例を示した図である。
【図2】図2はカートリッジ内部に設けられて試料を受容して処理するための具体的な隔離室を例示した図である。
【図3】図3は本発明による具体的な解離プロセスを例示した図である。
【図4】図4は本発明のカートリッジのもう1つ別な実施例を示した図である。
【図5】図5は本発明のカートリッジに設置することができる硝子スライドホルダーの具体的実施例の縦断面図および頂面図である。
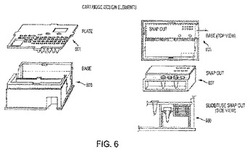
【図6】図6は本発明のカートリッジのもう1つ別な実施例の具体的特性を例示した図である。
【図7】図7は本発明のカートリッジの一実施例においてカートリッジの小室のうちの幾つかを互いから隔絶させることができるのを例示した図である。
【図8】図8は本発明のカートリッジのもう1つ別な実施例の具体的特性を例示した図である。
【図9】図9は従来の病理学的試料処理方法(左側)と本発明の具体的な処理方法(右側)との比較例を例示した図である。
【図10】図10は本発明の方法でRNA試料を生成した場合のほうがホルマリン固定・パラフィン埋設プロセスよりも無欠RNA個体数(RIN)が多いことを例示した図である。
【図11】図11は従来の腫瘍試料処理方法が生体マーカーを破損したことにより、利用できる細胞情報が低減する恐れがあることを例示した図である。
【図12】図12は穿刺吸引法(FNA)を利用した吸引法で始まる本発明の試料処理方法を例示した図である。
【図13】図13Aは無欠RNA個体数(RIN)評点を示したグラフであり、図13Bは生成RNAの量をマイクログラム(μg)単位で示したグラフであり、図13CはHCT-116細胞の細胞個数が変動している条件における260/280値を示したグラフである。
【図14】図14Aは無欠RNA個体数(RIN)評点を示したグラフであり、図14Bは生成RNAの量をマイクログラム(μg)単位で示したグラフであり、図14CはMCF-7 細胞の細胞個数が変動している条件における260/280値を示したグラフである。
【図15】図15はMCF-7細胞およびHCT-116細胞が分散してダイン/平方センチメートル(dyne/cm2)単位で変動した場合に細胞集団寸法に及ぼす影響を示したグラフである。
【図16】図16はMCF-7細胞およびHCT-116細胞が分散してダイン/平方センチメートル(dyne/cm2)単位で変動した場合に細胞生存力に及ぼす影響を示したグラフである。
【図17】図17はMCF-7細胞が分散して上皮細胞成長因子(EGF)刺激を受けたことによりFOS蛋白誘導レベルが変動するのを示したグラフである。
【図18】図18はHCT-116 細胞が分散して上皮細胞成長因子(EGF)刺激を受けたことによりFOS蛋白誘導レベルが変動するのを示したグラフである。
【図19】図19はMCF-7細胞およびHCT-116細胞において本発明の方法を利用して腫瘍細胞を集積培養したグラフである。
【図20A】図20Aは本発明の方法を利用して調製したMCF-7細胞に生細胞指標剤を導入した結果を示した図である。
【図20B】図20Bは3時間のホルマリン固定処置を利用して調製したMCF-7細胞に生細胞指標剤を導入した結果を示した図である。
【図21A】図21Aは本発明の方法を利用して調製したHCT-116細胞に生細胞指標剤を導入した結果を示した図である。
【図21B】図21Bは3時間のホルマリン固定処置を利用して調製したHCT-116細胞に生細胞指標剤を導入した結果を示した図である。
【図22】本明細書に記載されている解離技術を利用してMCF-7細胞およびHCT-116細胞を分散させた具体例を示した図である。
【発明を実施するための形態】
【0015】
本明細書に記載されている発明の実施例は、目標に掲げた各種治療と分子診断検査の開発利用を促進する自動自蔵式流体腫瘍細胞処理試験fシステムに関与しているが、これに限定されるものではない。本発明の実施例はまた、斯かるシステムを利用した方法であって、例えば、生細胞に対して生体外で実施することのできる進歩した病理学的処理方法を含んでいる。本発明はまた、本明細書に記載されているシステムおよび方法と併用するためのキットを目的としている。
【0016】
本発明は、固形細胞試料を体外で採集し、取扱い、処理するための、安全、効果的、高精度、正確、再生可能、廉価、コスト効率が良い、効率的、迅速、尚且つ、便利な方法および「カートリッジ式の」システムを提案している。このような方法およびカートリッジは、処理中も試料の生存力を維持して生体マーカーを無欠に保つことができるとともに、任意で、体外刺激により元の試料には存在していなかった各種燐蛋白質およびRNAなどのような生体マーカーを誘発するようにしてもよい。本発明は、完璧な診断細胞学実験室システムと生検後の管理された諸条件で完全無欠な試料と情報管理を提供するものであり、これにより或る検査から次の検査までの間の変化を最小限に抑え、生体混入の危険を最小限に抑え、尚且つ、試料調製プロセスそれ自体が生体マーカーの発現に及ぼす影響を最小限に抑えことができる。本発明の実施例を利用して、目標に掲げた腫瘍治療を容易にすることができるうえに、任意で、細胞計数機能、それ以外の関連解析、または、その両方を具体例とする組織試料の適性評価を行うこともできる。
【0017】
図9に例示されているように、従来の細胞処理技術は、組織処理前にホルマリン固定術を採用し、最終的には細胞をパラフィンに埋設する。この結果、図11に例示されているように、多数の潜在的な細胞情報が「喪失して」しまう。しかしながら、本明細書に記載されているとともに図9や図12などに描かれている進歩した方法は生細胞の自動処理、自動処理済みの生細胞の刺激、および、それに続く、本件後段に記載した各種方法を利用した細胞解析を行うことができる。
【0018】
当業者なら正しく認識することであるが、このような新規な装置、システム、キット、および、方法は臨床現場または研究現場で多数の利点を供することができる。例えば、これらを利用することで試料を遠隔の研究施設に発送する必要無しに、目の前にいる患者に直ちに生検処理を施すことができる。これらを利用することで生検処理をコスト効率の良い態様で標準化および自動化することもできる。本発明は、現行の病理学的処理が許容する以上に細胞についてより詳細な分子情報を提供することができ、これにより、任意で新規な体外における生体マーカー検査および診断検査を利用して、生検に付した細胞(例えば、癌細胞)をより細かく小分類することができるようにしている。本発明の各種利点は、それぞれ一緒に採択することで、治療の時点で迅速な診断を行えるようにするうえに、その後でより有効な患者ごとの固有治療管理計画を立てることを可能にする。
【0019】
本発明の装置、システム、および、方法のために利用される具体例のプロセス(限定するものではない)は、後段により詳細に説明されており、図12のフローチャートに例示されている。このプロセスは、図12に例示されている穿刺吸引(FNA)工程1201などのような方法で細胞凝集塊の試料を採取することで開始される。次に、試料は本明細書に記載されている新規な技術を利用して解離されてから、分散工程1203により複数の隔離室に分配される。試料が興味の対象である細胞とそうではない他の細胞とを混交して含有している場合は、任意で、混入物と興味の対象ではない細胞とを除去することにより、試料を高純度化して、試料中の興味の対象である全部の細胞を集積培養工程1205にまわしてもよい。次に、任意で、試料は体外刺激工程1207を受けるか、またそうでなければ、検査試薬と混合されてから、1分割量ずつの部分標本を新たな隔絶室に入れる工程1209にまわす。これら部分標本も、任意で、実施されるアッセイ次第で、体外刺激を受けるか、またそうでなければ、検査試薬と混合されるようにしてもよい。次に、これら部分標本は興味の対象となる特性について解析される。例えば、顕微鏡解析工程1211に備えて部分標本からスライドを準備するか、または、部分標本はそれぞれ1分割量ずつの細胞が核酸、RNA,および、DNAに溶解分離され、RNAは工程1213で、DNAは工程1215でそれぞれに解析される。解析結果は、穿刺吸引(FNA)の試料提供者である患者の治療管理の編成などの適切な行為を行うことができる研究者または臨床医に連絡される。更に、図11に例示されているように、本明細書に開示されている進歩した方法および装置により、従来の病理学的細胞処理技術中に「喪失され」ていた新情報を研究者または臨床医が得ることができるようになる。
【0020】
<1. 装置、システム、および、キット>
<<A. 装置>>
更に別な実施例では、本発明は、本明細書に記載されている生細胞の処理方法、生細胞の調製方法、または、その両方の方法などにおいて有用な装置またはプラットフォームを提案している。この装置はカートリッジとも称される。本発明の装置の幾つかの実施例が後段により詳細に説明され、図1から図8に描かれている。
【0021】
このようなカートリッジは1個以上の隔離室を備えている。隔離室は何らかの区画、区分、または、それら以外の実利的容器であって、生細胞の試料、固定済み細胞の試料、処理済み細胞の試料、安定化済み細胞の試料、または、それら全処理を完了した細胞の試料を保管することができる。具体例を挙げると、隔離室という用語の具体例としてはウエル、バイアル、管、スライド(例えば、硝子スライド)、プレートなどがあるが、これらに限定されるものではない。
【0022】
本発明の隔離室または区画は以下に列挙する機能のうちの1つ、複数、または、全部に好適である。すなわち、(1)隔壁またはそれ以外の方法により封鎖された小室に生体試料を受容する機能、(2)内蔵収納式注射針を保管する機能、(3)隔壁から取出しができる液体試薬を保管する機能、(4)隔壁内に廃棄物を受容・保管する機能、(5)液体剪断または機械剪断により試料を粉砕する機能、(6)細胞計数機能および細胞視覚化機能、(7)ビーズ分離機能、および、(8)固形樹脂含有機能のうちの1つ、幾つか、または、全部に好適である。
【0023】
カートリッジは各々がその用途次第で1個以上の隔離室を備えているようにするとよい。例えば、カートリッジには1個から約200個までの隔離室が設けられていてもよいし、1個から約100個までの隔離室が設けられていてもよいし、または、1個から約50個までの隔離室が設けられているようにしてもよい。或る実施例では隔離室の数は約24、約48、または、約96である。
【0024】
或る実施例においては、カートリッジには1個以上の第1隔離室と1個以上の第2隔離室が設けられている。カートリッジには細胞の試料を保有するための第1隔離室が設けられているようにしてもよい。このようなカートリッジは、分散された1分割量ずつの細胞試料の部分標本を保有する1個以上の第2隔離室を特徴としているようにしてもよい。或る実施例においては、第2隔離室は、分散された1分割量分の細胞の部分標本が添加される前に、そこに所定量の検査試薬を包含しているようにしてもよい。図2は、試料を受容して処理するためにあってもよい具体的な各種隔離室を例示している。
【0025】
或る実施例においては、本発明は、複数の区画(例えば、隔離室)が互いに分離して設けられているカートリッジを提案している。図7に例示されているように、区画は分離して設けられ、その内側の試料は複数の相互に異なる分析検査の用途に付すことができる。例えば、1区画がDNA解析のために回され、また別な区画はRNA解析のために回され、更にもう1つ別な区画は顕微鏡解析のため、更にもう1つの区画は免疫組織化学解析のために回されるようにしてもよい。或る実施例では、例えば、カートリッジに設けられた第2隔離室は第1隔離室とは別個に設けられていてもよい。
【0026】
本発明の装置は加熱部材を備えており、カートリッジの温度を摂氏約30度から40度まで、摂氏約36度から約38度まで、またはそれ以外の温度範囲の所望温度に維持することができる。
【0027】
本発明の装置は、装置内のカートリッジ、細胞試料源、または、その両方を識別するバーコードまたはそれ以外の手段を有しているようにしてもよい。カートリッジを識別するバーコードまたはそれ以外の手段を使って、試料識別、患者の安全、または、その両方を容易にすることができる。このような識別手段はコンピュータによるデータ保管システム、自動細胞処理システム、アッセイ、携帯用情報端末(PDA)、または、それらの各種組合わせと相互作用するようにしてもよい。バーコードが設けられたカートリッジの具体的実施例が図4に描かれている。
【0028】
例えば図2Fに描かれているように、装置の或る実施例には細胞計数機構が設けられていてもよい。このような機構は自動システムでも手動システムでも、いずれでもよい。例えば、細胞計数機構は血球計またはセロミター(登録商標Cellometer、ネクセロム・バイオサイエンシズ・エル・エル・シー(Nexcelom Biosciences, LLC)から購入可能)でもよいが、ディジタル計数装置または光学計数装置が使用される見込みである。当業者なら正しく認識することであるが、上記以外の細胞計数手段も当該技術で周知であり、本発明と併用するようにしてもよい。
【0029】
本発明のいずれの実施例のカートリッジであれ、1個以上のモジュールまたは1個以上の隔離室が設けられて、そこに樹脂、試薬、溶剤、それ以外の物質が保有されるようにしてもよい。モジュールは特定の目的で使用される1個の隔離室または1組の複数の隔離室のいずれであってもよい。例えば、多数の操作(例えば、溶解分離と染色など)が特定の検査に関与している場合は、その検査の「モジュール」の一部として2個以上の隔離室を利用してもよい。例えば、1個以上の隔離室が樹脂に核酸、蛋白質、天然重合体、合成重合体、小型分子などを付着させて保有しているようにしてもよい。1個以上の隔離室が緩衝剤、分子生物酵素、核酸または蛋白質などの生体分子、小分子化学物質などの液体を保有しているようにしてもよい。1個以上の隔離室がカートリッジ内可溶化処理用の乾燥試薬を保有しているようにしてもよいが、その場合、乾燥試薬の具体例としては核酸、蛋白質、天然重合体、合成重合体、小型分子などが挙げられる。
【0030】
或る実施例においては、カメラまたはそれ以外のディジタル結像装置がカートリッジの一部となっているか、または、カートリッジと併用される。従って、本発明のいずれの実施例のカートリッジであれ、10マイクロリットルから500マイクロリットルの間の量の試料に対して細胞視覚化とディジタル画像化による細胞計数処理を行うことができるようにした画像化モジュールを備えているようにしてもよいが(図2Fを参照のこと)、上述の量の試料は容積流動または毛細管作用によって画像化モジュール内に分配される。結像装置を利用して、例えば、蛋白質局在化データとなるような試料中の細胞成分などの試料写真を撮影するようにしてもよい。
【0031】
本発明のいずれの実施例のカートリッジであれ、直径が10ミクロンから500ミクロンである微細通路により細胞を通過させる流体モジュールが設けられて、10マイクロリットルから1000マイクロリットルの量を利用して100ダイン/平方センチメートルから800ダイン/平方センチメートルの壁剪断応力を生じるようにしてもよい。
【0032】
本発明のいずれの実施例のカートリッジであれ、免疫除去モジュールまたは免疫除去隔離室が設けられているようにしてもよい。このような免疫除去モジュールまたは免疫除去離室は磁気ビーズまたはそれ以外の方法を利用するとよい。例えば、磁気ビーズ製品はノルウエイのオスロに居所を置くダイナル・バイオテク(Dynal Biotech)から購入できる。このような実施例は方法解説部分でより詳細に説明している。
【0033】
本発明のいずれの実施例のカートリッジであれ、生体試料を含有する、または、生体試料を含有するように設計された1個以上のモジュールまたは1個以上の隔離室が設けらているようにしてもよく、斯かる生体試料の具体例として、穿刺吸引生検試料、コア生検試料、生体液試料(唾液、血液、精液、膣液など)、有機生物体由来の採取組織、細胞培養試料などがある。このようなモジュールは第1隔離室とも呼ばれ、例えば、図2の(A)および図4に描かれている。
【0034】
更に別な実施例においては、本発明は、本明細書に記載された方法および装置で使用するのに好適で、例えば、複数の個別の自蔵モジュールが設けられているようなカートリッジを提案しており、斯かるモジュールは細胞処理に好適な培地を保有しているとともに各々が隔壁またはそれ以外のシール機構によって封鎖されており、隔壁またはシール機構は針などの管による副側路形成や穿孔を行うことができるとともに管を取り出した際に再封鎖を行うことができる。或る実施例においては、液体試薬、生検試料、先鋭部材(すなわち、針)などを全部一括してカートリッジまたはカートリッジを封入した解析デバイスに投入したりそこから取出したりするのが十分可能なモジュールまたは隔離室が設けられており、この場合、解析デバイスは解析作業中の生物災害封じ込み作用を果たしている。モジュールには、細胞計数または細胞生存度アッセイなどの特殊検査や特殊活動を実施する試薬および装置を付随させた多数の隔離室が設けられている。上述の実施例は、例えば、図1、図2、図4、図6、図7、および、図8に描かれている。
【0035】
図5の参照番号501Bで示されているように、本発明のカートリッジは階段形状部501Aに複数スライドが積載される構成になっており、階段形状部のおかげで、これらスライドは細胞物質を収容した後で接近して取出すのに単に手動手段またはロボット手段を使って効率よく利用することができるようになる。図5は階段形状部501A、501Bを例示した断面図である。従って、更に別な実施例においては、本発明は、例えば硝子スライドなどのような多数の平坦な基板が階段状に配置されたホルダーを備えている装置を提案しており、斯かる装置においては、ホルダーは基板が左右上下に移動するのを抑制している。好適な基板としては、硝子スライドなどのような平坦な矩形板片、金属プレート、または、マイクロ流体装置などが挙げられるが、これらに限定されない。基板の厚みは0.1 mmから3 mm、縦横の寸法は2 cmから3 cmの幅に7 cmから9 cmの長さ、または、これら全部の条件を備えているとよい。当業者には分かることであるが、上記以外の基板または隔離室をカートリッジ上に同様の態様で配置してもよいが、そのような各種実施例も本件の範囲に含まれる。
【0036】
或る実施例においては、カートリッジ上のホルダーには底面部と上蓋部が設けられており、これら両部分は各々に階段が設けられて、複数の個別の基板を階段状に積載したものがホルダー内に設置され、または、ホルダーに相関的に位置決めされて、ホルダー内で、または、ホルダーに相関的に移動することがないように図っている。ホルダー内に保管されている間は、基板の遠位端は最も低い部位が積載部を越えた先まで突出している(図5の501Bを参照のこと)。この遠位端は機能上の特徴を印刷したもの、ウエル、または、刻印が1個以上設けられているようにしてもよい。特徴を印刷したものは、使用済み時または使用前に基板を識別するための付箋であってもよい。或る実施例では、ホルダーには上蓋が設けられており、基板の遠位端は露出状態になっており、上蓋の1個または複数個の隔壁を通り抜けて接近することができるようになっている。ホルダーはフレームの中に出し入れ自在であり、例えば、国際分子生物科学協会(SBS)推奨規格の設置面積を有するフレームへ出し入れ自在であるようにするとよい。任意で、ホルダーは底面に1個の小さな穴または複数の穴が設けられているようにしてもよい。
【0037】
図5は具体的なホルダーの頂面図である。スライドの積載部は、自動化用途または手動化用途に付すのに理想的なシステム構築をしている標準的な行列間隔設定に従って、上部から特定位置の認識が行えるようになっている。ホルダーが備えている上蓋には1個の基板ごとにその真上に隔壁が設けられており、真上から1個の基板ごとに個別の特定位置を割当てている。例えば、ホルダーにおいては、1個の基板ごとの識別できる特定位置の真上に1個のO字型リングまたはガスケットにより封鎖可能な密室が設けられているようにしてもよい。このようなO字型リングまたはガスケットにより封鎖可能な密室は所望に応じてどのような形状であってもよいが、例えば、円形、矩形、または、正方形であってもよい。
【0038】
所定の態様でホルダーと多数基板を設置することにより、ピペット、注射針、または、ピン型ツールを使って1ナノリットルから0.5ミリリットルまでの範囲の量の流体試料を基板に並列分配することができるようになる。或る実施例では、ホルダーは流体分配中に基板が左右方向または上下方向にずれるのを抑制しているとともに、流体分配中に基板が移動するのも抑制している。他の実施例においては、ホルダーにより基板は上下方向に回転するのは許容されるが、左右方向に移動するのを抑制されている。このような柔軟性により、多様な方法および多様なシステムを利用して個々の隔離室への並列流体搬入とそこからの並列流体搬出を自動または手動で行うことができるようになる。
【0039】
或る実施例においては、ホルダーの分解は上蓋の部分を取り外すことで行われ、底面部はホルダーの底面部に設けられた穴を突き抜けている突出位置に在るスタンドに載せて置くことができるようになっている。基板は本発明特有の態様でスタンド突出部に置かれた状態で差し出され、人の手で、または、ロボット型把握ツールにより連続して把握動作を行えるようになっている。これにより基板を連続して取り外すことができるようになり、例えば、最下位のスライドを真っ先に取り外して最後に最上位スライドを取出すことができるため、スライド上に堆積させた試料を基板が掠めて切り崩す事故を回避することにより、スライド標本式の細胞物質を安定して搬送することができるようになる。上述のホルダーの各種実施例を保有しているカートリッジの具体的な分解図が図6および図8に開示されている。
【0040】
流体試料は自動システムまたは手動のいずれで基板に分配されてもよい。或る実施例においては、流体サンプルは所定の順番で連続して基板に分配される。好適な流体試料として、各種の溶液、エマルジョン、懸濁液、重合体含有混合液などが挙げられるが、これらに限定されない。例えば、流体試料は各種の生物学的物質または化学物質であって、例えば、小型有機分子または小型無機分子、蛋白質、核酸、細胞、粒子、揮発性溶剤、不揮発性溶剤、重合体、定着剤などであればよいが、これらに限定されない。
【0041】
更に別な実施例においては、本発明は、本発明のカートリッジで有用となるウエルプレートを更に提案している。目下のところ、各構成部材(導通管、密封管、注射器、ピペット先端具など)を適所に固定することができるようにすることでプレートが斜交いまたは上下逆にされても構成部材が適所から脱落することがないようにしたウエルプレート技術が必要である。更に、ウエルプレート技術により、標準的な(デカルト空間内)ピペットツールを使用して固定済み構成部材を取外して使用してから元の固定位置に戻すのに、ピペットツールに取り付けられた先端具排出装置さえ必要とせずに行えるようになる。或る実施例では、本発明の狙いは、平坦面に多数のウエルが設けられているウエルプレートを製造するにあたり、ウエルプレート上の互いに隣接する2点の位置(「2重ウエル」と呼ぶ)がそれら2点の間に介在している空間によって接続されて、構成部材を左右方向に移動させることができるようにすることである。
【0042】
上述の構成部材は、導通管、密封管、隔壁が設けられた管、透明管、何らかの容器、注射器、針、刃、ピペット先端具などであればよい。或る実施例では、この構成部材は、固定機構を通り抜けるのに好適な厚みの正方形、円形、または、それ以外の形状の物質の剛性部材片を備えており、固定ウエルの固定機構の形状と一致している。
【0043】
2重ウエルプレートの或る実施例においては、2重ウエル(「固定ウエル」と称する)の互いに隣接し合う第1位置として複数の小型タブを含んでおり、これらタブにより各構成部材を適所に固定して移動できないようにし、とりわけ、プレートが上向きである場合に構成部材が上下方向に引き出されるのを阻止することができる。このような2重ウエルプレートには従属ガスケットを有している固定ウエルが設けられており、斯かるガスケットは、構成部材が固定ウエル内に固定されてガスケットが固定された構成部材の移動を阻止している間に限って一部が圧搾される。
【0044】
或る実施例においては、上述の構成部材はツール(例えば、ピペットまたは注射器)によって特定位置割当てができる「取付け部材」を備えており、この場合、取付け部材(例えば、ルアーロック)により構成部材は上記ツールと気密嵌合状態になることができる。上記ツールは固定ウエル内に固定されている構成部材の上に載せられてから構成部材を押下げることで更にガスケットを圧搾することができるが、これにより、構成部材を適所に置くことで2重ウエルの介在空間内で2重ウエルの第1位置(固定ウエル状態)から2重ウエルの第2位置(「解放ウエル」と称する状態)まで左右方向への移動を行えるようにすることができる。或る実施例においては、この構成部材はツールによって上下方向に移動させられると解放ウエルへの出入りを自由に行うことができる。ツールは構成部材を固定ウエルの十分内奥まで搬入することができ、ウエルプレートが表面に係留されるとツールがウエルプレートから垂直方向に離れる方向に移動することにより、構成部材を固定ウエル内に固定したままでツールから構成部材を切り離すことができる。
【0045】
上述のツールとプレートは各々がコンピュータ制御のガントリーシステム上に搭載されており、ツール、プレート、または、その両方がデカルト座標(x, y, z)空間内を移動することができるようにすることにより、ツールが構成部材を固定ウエルに搬入してから固定ウエル内に構成部材を放置し、固定ウエル位置で構成部材を乗せてから構成部材を解放ウエル位置まで移動させ、解放ウエルから構成部材を取出して、更に構成部材をウエルプレートから放免することができるようになる。このような装備によって、ツールが構成部材を解放ウエルに搬入してから、先端具排出装置により構成部材を解放ウエル内に放置することができるようにしてもよい。
【0046】
上述のツールとプレートを利用したコンピュータ制御のシステムの或るものは、角度運動(シータ軸中心)を採用する必要がないように構築されているため、構成部材がウエルプレートに存在したままでも、または、構成部材がウエルプレートから取外されていても、いずれの場合であれ、構成部材をウエルプレートに対して相関的に位置回転して配向し直しをするのを回避することができる。
【0047】
或る実施例においては、2重ウエルを利用して、試料から混入物を除去するように予め設計されている所定の経路を通って液体を流動させることができるようにしている。このような2重ウエルシステムは、例えば、図2においてはウエルCおよびウエルDとして例示されている。
【0048】
<<B. システム>>
本発明の狙いは、本明細書に記載されているカートリッジおよび方法を利用するシステムでもある。例えば、システムは本発明のカートリッジを個別的にまたはキットの一部として1個以上備えているとともに、カートリッジと相互作用して少なくとも1つの解析結果を得ることができるようにした解析デバイス(本明細書では解析装置とも称する)を備えている。例えば、斯かるシステムは治療中に使用して患者の医療診断を得ることができる。
【0049】
従って、本発明の或る実施例の狙いは複数の個別モジュール(例えば、複数の隔離室)が設けられたカートリッジにおいて各種操作を実施するための解析デバイスであり、この場合、解析デバイスは1個以上の注射器用の1個以上のホルダーを備えており、注射器は中空針を備えているとともにカートリッジが配置されているプラットフォームの真上で配向されて、針の尖点をカートリッジの個別モジュールに向けて当てるのにコンピュータ制御の運動制御によるデカルト座標システム(x, y, z)を採用することでカートリッジのモジュールから内容物を吸引したりモジュールに内容物を分配することができるように図っており、モジュールは各々に針で刺し通すことができる隔壁が設けられているが、そうでない限り、隔壁はモジュールの内容物を環境から隔絶している。これらカートリッジの或る実施例の態様が図1、図4、および、図8に描かれている。或る実施例においては、カートリッジによって調製された注射器またはツールをホルダーが持ち上げることができるようになっている。
【0050】
解析デバイスは、本発明のカートリッジを受容する手段を備えている。例えば、スロット、開口、穴、または、それ以外の、カートリッジを受容することができる領域を挙げることができる。或る実施例においては、カートリッジを受容手段内に設置完了すると、扉が閉まって受容手段を封鎖することにより、解析デバイス内にカートリッジを完全に封入する。このような扉閉鎖は手動で実施されてもよいし、自動であってもよい。このような完全密封実施態様が特に有用と言い得るのは、潜在的生物災害を撒き散らすのを防いでいる点、またそうでなくとも、研究室や臨床環境に放散させてしまうのを回避している点である。
【0051】
或る実施例においては、解析デバイスおよびカートリッジを利用するためのシステムは真空設備、空気供給設備、天然ガス設備を必要とせず利用もしないが、更に、試薬給送ライン(処理液流、分析用試薬流、および、廃棄物流)とそれぞれの付属ボトルも全く無用である。すなわち、デバイスは完全自蔵式である。
【0052】
このようなシステムで使用されるカートリッジ、或いは、単独で使用されるカートリッジも自蔵式であってもよい。これは、手動であれ自動システムを利用するのであれ、いずれにせよ、所望のアッセイを実施するのに必要なあらゆる必需ツール(例えば、ピペット先端具など)と試薬(例えば、検査試薬、顔料、または、それ以外の化合物)をカートリッジが事前装填した状態になっているということを意味する。例えば、カートリッジは癌療法のパネル(例えば、プレートに設けられたウエルなどの隔離室ごとに1療法ずつ)と試料を解離して複数のウエルに分散させるのに必要なあらゆるツールとを事前装填しているようにしてもよい。
【0053】
本発明のシステムはカートリッジのモジュールの特定位置を割当てることができる内部画像化機能を備えているようにしてもよい。このシステムを利用してデータを生成し、生成データをユーザーまたは他の装置に出力することができる。
【0054】
解析デバイスは、試料に対して検査が実施されている間も細胞生存力を保つための温熱培養に必要な各種構成部材を備えているようにしてもよい。このような解析デバイスの培養部は1個以上のカートリッジを保有しており、任意でカートリッジは所定の順序に配置される(例えば、試料採収時期に基づく時間順など)。
【0055】
前述の各種解析デバイスのいずれも、カートリッジのモジュールに試料識別子を付着させ、試料情報を伝達し、更には、通信ラインにより処理情報を他の装置に転送するかまたは検査を実施しているユーザーのために結果を表示することができる。
【0056】
<<C. キット>>
本発明はまた、本発明の装置を包含しているキットを目的としている。具体的なキットでは、本明細書に記載されている1個以上のカートリッジが1個の容器に梱包されている。キットは使用上の指示書きを印刷したもの、試薬、緩衝剤、分子指標剤、後段で説明するような1種類以上の検査試薬、ピペットまたは針などの解離または分配用のツール、および、後段で説明する方法を実施する際に有用となる上記以外の物品を更に含んでいるようにしてもよい。
【0057】
或る実施例においては、キットは当該技術で周知の方法を利用して殺菌されてから、無菌状態を保つ態様で梱包される。キットは個別キットとして販売されてもよいし、多数を一括梱包したセットとして販売されてもよい。キットはまた、包装物の中身を誰かにいじくられることがないように設計されるか、または、そのような事態が生じた場合に、それを表示する設計にされるか、いずれかの設計にされているとよい。
【0058】
キットは、本明細書に記載されているような、自動装置を使用するよりはむしろ手作業で利用することができる解析用カートリッジを包含しているようにしてもよい。この場合、検査を遂行する、または、カートリッジの特定目的を遂行するのに必要な試薬と器具がキットの一部として提供されるようにするとよい。斯かる器具としては、例えば、注射針やピペットなどがあるが、これらはカートリッジに事前装填されていてもよいし、或いは、カートリッジの外側に置かれて、キットの一部として提供されるようにしてもよい。他の実施例においては、器具はユーザーが準備するようにして、キットの一部に含まれていないようにしてもよい。同様に、キットと併用される検査試薬は、カートリッジの特定の隔離室内に事前装填されているようにしてもよいし、或いは、ユーザーの実用に適合するようにカートリッジの外側に梱包されているようにしてもよい。上述の各実施例によるキットは、1回きりの検査用の1個のカートリッジとして梱包されてもよいし、多数回の検査用に装填または準備された1個のカートリッジとして梱包されてもよいし、或いは、多数回の検査用の多数カートリッジとして梱包されてもよい。
【0059】
任意で、キットは、カートリッジやそれ以外の試薬などの必需品を適性に使用する指示書きを、本明細書に記載されているようなアッセイまたは方法の一部として包含していてもよい。例えば、キットはお知らせまたは印刷した指示書を含んでいるようにしてもよい。このような印刷した指示書は、医薬品または生体学製品の製造、使用、または、販売を管理指導する政府機関によって規定された形式を呈しているようにするとよいが、そのような通知は、本明細書に記載されているアッセイ、方法、および、装置から得られた情報を利用して扱うことができる症状を診断または治療するための人的管理について、製造、使用、または、販売を管理指導する政府機関の承諾を反映したものである。或る実施例においては、キットは、細胞を処理する目的でキットを使用する際の情報を提供する印刷物、或いは、細胞を処理する目的でキットを使用する際の情報を提供する事前記録媒体装置を更に含んでいるようにしてもよい。
【0060】
「印刷物」は、例えば、本、冊子、パンフレット、ちらし等のうちのいずれかであるとよい。印刷物は、本発明の方法に従って細胞を処理するための実験評価分析書、培検計画案、または、その両方を説明しているようにするとよい。考えられる様式として、段階的指示、箇条書きリスト、よくある質問(FAQ)リスト、図表などがあるが、これらに限定されない。更に、供与される情報は、写真、図画、または、これら以外の表象を利用した原文に典拠しない表現で例示されているようにしてもよい。
【0061】
「事前記録媒体装置」とは視覚媒体装置のことであり、例えば、ビデオテープカセット、DVD(ディジタルビデオディスク)、フィルムストリップ、35ミリ映画、または、それ以外の何らかの視覚媒体装置であるとよい。これに代わる例として、事前記録媒体装置は対話型ソフトウエアアプリケーションであってもよいが、その具体例として、CD−ROM(コンパクトディスク型リードオンリーメモリ)やフロッピー(登録商標)ディスクなどがある。これに代わる例として、事前記録媒体装置は、例えば、レコード、オーディオカセット、オーディオコンパクトディスクなどのようなオーディオ媒体装置であってもよい。事前記録媒体装置に保有されている情報は、本発明の方法に従って細胞を処理するための実験評価分析書、培検計画案、または、その両方を説明しているようにするとよい。
【0062】
<2. 方法>
本発明は細胞試料を処理する新規な方法を目的としており、特に、臨床現場または研究現場で使用することができる細胞凝集塊または固形腫瘍を処理する新規な方法を狙いとしている。このような方法は、被検体から得た癌の生細胞を水性溶液中に解離・分散させて少なくとも1分割量の部分検査標本にして第1隔離室に入れる工程を含んでおり、任意で、混入細胞を除去することにより標的細胞の残余の混入細胞に対する割合を増大させるようにこの部分標本を高純度化または操作する工程と、任意で高純度化された癌の生細胞を解析に付すために1個以上の第2隔離室内に分配する工程と、分配済みの生細胞を安定させることで分配済みの細胞の細胞解析、分子解析、または、その両方の解析を行えるようにする工程とを含んでいるとよい。或る実施例においては、安定化された分配済みの細胞は生細胞でもよいし死細胞でもよいが、これは所望の結果と興味の対象である細胞アッセイ次第である。
【0063】
本発明のまた別な実施例は、固形腫瘍から採取した癌細胞を処理または調製する方法を含んでおり、斯かる方法は固形腫瘍から得られた癌の生細胞を解離および分散させて少なくとも1分割量の部分試験標本を少なくとも1個の第1隔離室に入れる工程と、任意で、混入物を除去するように癌の生細胞を高純度化または操作する工程と、高純度化された癌の生細胞を解析に付すために1個以上の第2隔離室に分配する工程と、分配済みの細胞の細胞解析、分子解析、または、その両方の解析を行えるようにするために分配済みの細胞を安定させる工程とを含んでいる。
【0064】
本発明の方法は、生細胞を迅速に処理することができるようにする。細胞は生きた状態で最小限の細胞活性化または最小限の応力で処理される(例えば、環境応力、温度誘導応力、代謝応力、化学誘導応力など)。「最小限の細胞活性化または最小限の応力」という語は、刺激と比較して、細胞シグナリングのバックグラウンドノイズ変動量を最小限にすること、および、細胞応力経路の変化を最小限にすることと定義される。例えば、図17で分かるように、解離、分散、または、その両方処理の前後の細胞へのFOS蛋白(または、C-FOS)誘導を比較することで、FOSまたはそれ以外の早期反応遺伝子もしくは生体応力指標物質の誘導が最小限になる(3倍から5倍)になるのを、刺激を与えられた試料(上記物質が20倍から30倍増量する)と比較して示すことができる。
【0065】
本発明の方法のもう1つ別な利点は、元の試料中に存在する極めて少数の細胞を使用するだけでよいことである。例えば、或る実施例においては、処理された細胞凝集塊または固形腫瘍の総数は1×103個から1×107個の間である。
【0066】
本発明の方法はまた、迅速な試料処理を行えるようにする。或る実施例においては、分配済みの生細胞の安定化は、被検体から試料を得た後、約1時間以内、約2時間以内、約3時間以内、または、約4時間以内に完了する。このような驚くべき短い処理時間により細胞培養の必要性を排除しながら、細胞生存度は、例えば、約50%を越える、約60%を越える、約70%を越える、約75%を越える、約80%を越える、約85%を越える、約90%を越える、または、約95%を越える高い割合に維持することができる。或る実施例においては、細胞生存度の割合は約70%または約75%である。「約」という語は、例えば、百分率などのような数に関連づけて使用されている場合は、その数値プラスマイナス10%の増減幅を意味している。例えば、「約60%」という語は54%から66%の間を意味している。
【0067】
<<A. 試料採収>>
本明細書に記載されている各方法で使用される試料は多様な方法で得ることができる。試料は、哺乳類(例えば、ヒト)またはそれ以外の生きている有機生物体などのような被検体から採取された生細胞であればよい。具体的には、臨床現場で人間患者から解析を目的として採取された生検材料であって、最終的には、適切な臨床診断と治療方針を判断するのに役立てるために利用されるものであればよい。
【0068】
或る実施例の試料は、凝集状態であれ解離状態であれ、研究現場または臨床現場における興味の対象である何らかの群細胞または単一細胞であればよい。試料の具体例を挙げると、固形腫瘍は元より、トリプシンを使用するといったような、本明細書に記載されているものとは異なる手段を利用してリンパ腫または細胞塊を解離した個々の単一細胞でもよい。このような試料は既存の細胞株、異種移植片、または、臨床診断に付す目的とは異なる理由で検査される患者試料に由来するものとなる可能性がある。このような試料は解析に供されて、細胞と特定の検査試薬に対してそれぞれの細胞が示す反応とを更に特徴づけることができる。このような適用例は、新規な調製剤を識別したり既存の調製剤の投与を改善する目的で、薬品開発と分析評価法選別作業の一部として有用である。
【0069】
或る実施例においては、本明細書に記載されている方法は、どのような種類の解離細胞または解離腫瘍細胞とでも併用することができる。例えば、本発明の方法は癌種または肉腫を検査して処理することができる。本発明の方法を利用して検査することができる具体的な癌としては、大腸癌、膵臓癌、乳癌、卵巣癌、前立腺癌、扁平上皮細胞癌、子宮頸癌、肺癌、小細胞肺癌、腎臓癌、肝臓癌、脳腫瘍、皮膚癌、膀胱癌などが挙げられるが、これらに限定されない。このような各種癌はヒト、ヒト以外の哺乳類、または、ヒト以外の哺乳類(例えば、マウス)から除去されたヒト癌細胞の異種移植片に由来するものである。
【0070】
或る実施例においては、組織試料は固形腫瘍の一部、または、全腫瘍である。本発明で使用する腫瘍細胞を含んでいるこのような組織試料は、例えば、患者から生検材料を採取する等といったような、当該技術で周知の何らかの手段により得ることができる。本発明で採用することができる好適な生検法としては、切開生検、コア生検、パンチ生検、穿刺吸引生検のほかに、切除生検などが挙げられるが、これらに限定されない。或る実施例においては、生検材料は腫瘍の穿刺吸引術(FNA)によって採集される。
【0071】
穿刺吸引(FNA)生検は細い針を使って実施されるが、針は注射器に取り付けられている場合もあれば、単独で使用される場合もある。穿刺吸引生検すなわちFNAは、本発明においては、癌試料を得るために採用される。穿刺吸引生検は経皮(皮膚を貫通させる)生検法であってもよいし、或いはこれに代わる例として、気管支、食道、胃、または、腸などの器官の管腔を貫通させる生検法であってもよい。穿刺吸引生検は、通例は、ファインゲージ針(21ゲージまたはもっと細い針で、22ゲージまたは25ゲージなど)を使って達成される。穿刺領域がまず洗浄されてから、普通は、局所麻酔で麻痺状態にされる。針は興味の対象となる器官または組織の領域に穿刺される。針を刺した後、注射器を使って真空を設けるか、これに代わる例として、針の内部の毛細管作用のみを利用するようにしてもよいが、何度も針を刺し抜きする動作が実施される。採取される細胞は針の管腔内に入り込み、場合によっては、組織を刺し通した時に針の斜面の微細標本抜取り作用により針の円筒中心部に入り込む。通常は3個乃至6個の別個の試料が作られる。リンパ節や肝臓などの癌の転移部位は穿刺吸引生検のよい候補となる。穿刺吸引処置は、通例、超音波画像処理法またはコンピューター断層撮影法(CT)を採用して行われる。
【0072】
コアニードル生検(コア生検)は、小型の中空針で皮膚を貫いて器官の中に針を挿入することにより実施される。次いで、針は細胞層の内部に進入させられて、試料または標本を取出す。針は切断用先端部が設けられて組織の試料を除去するのを助ける設計になっている。コア生検は、組織試料を除去するのを支援するのに、バネを装填した銃型装置を使用して実施されることが多い。コア生検は、通例は、CT画像処理、超音波、または、マンモグラフィーなどの画像誘導下で実施される。針は手で刺すか、または、試料採取装置の支援で刺すか、いずれかの態様で行われる。十分な組織を得るために何度も挿入されることが多く、多数の試料が採取される。コア生検は、真空装置支援式の吸引法(真空支援生検)である場合がある。この方法により、1度しか針を挿入しないのに多数の試料を抜き取ることができる。コア生検とは異なり、真空支援式生検探針は、小さな皮膚の刺し傷から組織の中に1回のみ挿入される。試料採集用の針穴(開口)の回転を利用しながら、吸引支援を受けて多数試料が採取される。従って、コアニードル生検または真空支援式ニードル生検を本発明に採用することで、組織試料を採集することができる。
【0073】
内視鏡生検は、試料採集を目的として本発明に採用することができるありふれたタイプの生検法である。内視鏡生検は、試料採取器具と一緒に体内に挿入される内視鏡(体内を視認するための光ファイバーケーブル)によって行われる。内視鏡により、興味の対象である器官の内側の領域を直接視認することができるようになるうえに、試料の内部を貫いて延びている長いケーブルに取付けられた鉗子を使って少量の組織を採取し、または、切り取る。内視鏡生検は、例えば、胃腸管(消化管内視鏡検査)、膀胱(膀胱鏡検査)、腹腔(腹腔鏡検査)、関節腔(関節鏡検査)、胸部中間部(縦隔鏡検査)、気管および気管支系(咽頭鏡および気管支鏡検査)などに対して実施されるが、いずれも天然の肉体開口部または小さな外科手術切開部を通す。内視鏡超音波誘導式穿刺吸引生検法も肺、縦隔リンパ節、膵臓、肝臓などに対して、経食道アプローチ、経消化管アプローチ、経十二指腸アプローチなどの経路を利用して実施することもできる。
【0074】
癌試料を採集する目的で、表層生検が本発明に取り入れられてもよい。この技術は組織または器官の表面から試料抽出する、または、それらの表面を掻爬することで細胞を抜き取る処理に関与している。表層生検は皮膚の小片を抜き取る目的で実施されることが多い。
【0075】
<<B. 細胞の解離・分散>>
処理用に採取された試料は、細胞を互いから分離してから(凝集している場合は)分離した細胞を分散させて1分割量の部分標本ごとに本明細書に記載のカートリッジまたはそれ以外の好適な容器に入れる。このようなプロセスは、分散工程、計数工程、生存度評価検査、または、これらの各種組合わせを含んでいる多数の工程から構成されているとよい。
【0076】
外科手術で切除された腫瘍に由来する試料と比較した場合、本発明の方法で使用される試料は比較的少数の細胞(例えば、腫瘍細胞)しか含有していなくても済み、本明細書に開示されている各方法無しには、大半の現行の分子診断技術においてはこのような少量細胞しか含まない試料の利用が制限されてしまう場合がある。更に、固形腫瘍由来の穿刺吸引試料または他の方法を利用して採取された固形腫瘍細胞は極度に大きな塊の細胞(細胞数にして500個を越える)を含有していることがあり、多数の検査用隔離室に試料を均一に分配するのを阻害してしまう恐れがある。
【0077】
細胞を殺傷せずに、または、細胞内の応力反応経路を過度に活性化させてしまわずに、上述のような細胞を解離させて分散させる処理は、厳密な方法および厳密な技術を必要とする細心の注意を要するプロセスである。本件で採用されているように、解離手段は細胞を分離させたり細胞のほぼ均質な試料を供与する血用として、複数の細胞を含有している試料を分散させて多数の比較的均一な試料を生じることができるような態様を取っている。例えば、内皮細胞などのような付着依存性細胞においては、大動脈レベルの持続する一方向層流剪断力(10 dyne/cm2から25 dyne/cm2)は代謝の急変(プロスタシクリンおよび一酸化窒素NOの生成)を生じるばかりか、FOS mRNAおよびFOS蛋白質が1時間経過しないうちに上昇した状態での遺伝子発現の急変も生じることがある。これ以外の幾つかの細胞株で、例えば、CHOおよびHELAなどの細胞株も、一方向剪断応力に持続して晒された後にはFOS誘導を示す。このような研究は通例はフローチャンバーを配備して、数分間から数時間更に数日間に亘って細胞が剪断応力に晒されることで遺伝子表現型が変化するのを観る環境で実施される。例えば、エス・エル・ディアマンド(S.L. Diamond)、エス・ジー・エスキン(S.G. Eskin)、エル・ヴィー・マッキンタイア(L.V. McIntire)共著、「流体フローの刺激によるヒトの培養内皮細胞からの組織プラスミノゲン活性化因子分泌促進(Fluid Flow Stimulates Tissue Plasminogen Activator Secretion by Cultured Human Endothelial Cells)」という題の1989年3月17日刊行のサイエンス(Science)243 (4897)号1483-1485を参照のこと。流体剪断研究とは別に、機械的摂動(基板の伸展または誘導変形)が伸展活性イオンチャネルを活性化させることができるとともに、カルシウム流動化を生じることがある。摂動剪断応力は、通例、破裂する酸素気泡が膜を破壊することとの相互作用が特に細胞溶解反応的であるという点で、層流剪断応力に比べて好ましくない。プルロニックF68(登録商標Pluronic F68)またはウシ血清などのような添加剤は細胞保護性を示すが、細胞が気泡と結合するのを防ぐ界面活性剤効果により、作用は部分的にすぎない。
【0078】
本発明の驚嘆に値する発見は、所定量の層流剪断応力を利用すれば細胞には最小の応力反応しか誘発しない、または、応力反応を全く誘発しないことで細胞を殺傷せずに細胞の凝集を破断することができることである。このような解離作用は、例えば、細胞を所定寸法の針または管の中に引き入れてからウエル等の中に細胞を注入し、これを必要に応じて反復することにより実施される。層流剪断応力への露出時間を最小限に抑えることで、試料を流体機械的破壊処理に付している最中も細胞の剪断活性化を低減している。
【0079】
試料を解離させるための適性条件を予め考慮することで、必要な装備と培検計画案を認識することができるようになる。いかなる刹那であれ細胞系の凝集状態は、細胞個体数規模分布によって明確にされる。細胞系は、単一分散であってもよいし(例えば、単体または凝集塊がいずれも、例えば、全部20-mer以下の小さい量体数の細胞だけから構成されている)、或いは、凝集塊が複数の単体から構成されたものから単体と多様なk-merから構成されたものにまで及んでおり、kの値が大きく、例えば、20よりも大きい多重分散であってもよい。細胞培養株では、凝集塊は同型である。しかしながら、穿刺吸引法は、多数の細胞型を含んでいるという意味で異型である。時機を得て進化する凝集プロセスおよび細分化プロセスの数学は良好な発展を見た。複雑に応じて、個体数バランス等式の解を分析的に求めてもよいし(単純な同型凝集の場合)、解を数値的に求めてもよいし(複雑な同型凝集の場合)、或いは、モンテカルロシミュレーション法に従って求めてもよい(異型の凝集と細分化について)。穿刺吸引による細胞破壊については、基本プロセスは細分化断片の核Fによって必然的に決まるが、細分化断片の核Fは一般的なフロー場、細胞集団寸法、緩衝条件で決まる。細分化(1つの成分が、1個の粒子ごとに分断されて2個のより小さな粒子になる)を受ける各寸法ごとの個体数については、細分化バランスは次のように表すことができる。
【0080】

但し、

は時間tにおけるk-量体数の大きさに設定された粒子(または、k-mers)の濃度であり、

はk-mersの正味分割率であり、

はk-mersの分割時に生成されたi-mersの平均数である。従って、

で (i+j)-mersがi-mersとj-mersに分かれる正味の割合が求められる。細分化断片の核Fは管内フローにおいては空間に依存しており(管の壁の近辺では高く、管中央部ではゼロである)、尚且つ、細胞集団寸法の管直径に対する割合にも依存している。生検後に操作するにあたり、穿刺吸引採取試料は高度に希釈されることになるため(細胞容量/試料容量 << 1)、最小粒子が壁に向けて放射方向に移動することに関与する懸濁液中浮遊物の動力学は重要ではなくなる。凝集塊の細分化の範囲は二分裂から全くの粉砕(細胞凝集塊から得られた細胞単体の喪失)にまで及んでいる。細分化断片の核は穿刺吸引採取試料中の腫瘍凝集塊ゆえに周知なのではない。当業者には分かることであるが、剪断フローにおける細胞群の実験による細分化率は、平均剪断率Gavgと凝集塊の水力学的半径または衝突半径Rhydとに基づく冪法則の関係である。例えば、共通様式は次のとおりである。すなわち、

であり、Aとyは実験的に決まり、γ=2を満たしている。i-細胞の腫瘍凝集塊については、1個の細胞ごとにその半径がR0であれば、

であり、但し、Dfは分数寸法である(Dfは1.7から2.5)。
【0081】
穿刺吸引採取試料およびそれ以外の細胞凝集塊は複雑な物体であり、多数の細胞型と多様な細胞基質組成を有している場合がある。穿刺吸引採取試料の分断を考慮するにあたり、患者から得た大型組織試料を細分化して部分集団にすることは、主として、腫瘍細胞相互の接合を分断するという問題であり、第2に、腫瘍細胞とその下の基質層との間のインテグリン依存性癒着を破断するという問題である。
【0082】
例えば、穿刺吸引採取試料などのような生検試料を管の中で剪断誘導により解離させるとする。細胞を解離する方法の1つとして、剪断応力を利用することによる方法がある。上述のように、層流剪断応力が好ましい。層流剪断応力は管の内部で生成される。
【0083】
管内の剪断層流については(レイノルズ数 < 2100)、剪断応力は管壁の付近で最大となり、流体が単純に下流側に移動している管の中央部ではゼロである。壁剪断応力 twおよび推移時間ttransitは次のように定義することができる。すなわち、

であり、断面積A=πR2の管を通る容積流量Qについては

であるが、但し、

であり、この等式におけるQの単位はcm3/sであり、vavgの単位はcm/sであり、Aの単位はcm2である。管材の長さLを横断する平均推移時間は

を満たすようなvavg=L/ttransitに基づいて定められる。水の粘性は室温で0.01ポアズである。グリセロール、プルロニックF68、デキストラン、ポリエチレングリコール(PEG)などのような添加剤は全て液相の粘性を高める可能性がある。一定の流量と一定の幾何学的形状の元では、粘性を増すことで剪断力も上昇する。入口長さの効果は小径の管では相当に極限まで小さくなる。広く使用されている1インチ注射器の長さ、注射器ゲージ(G)、水の灌注緩衝(1センチポアズ)、壁剪断応力(dpc、ダイン/平方センチメートル)、および、推移時間が表1に列挙されている。
【0084】
【表1】

1mL/s(粘性=1 cP)の水緩衝で灌流された1インチ針について、針ゲージ、壁剪断応力(dpc、ダイン/平方センチメートル)、および、推移時間(msec)の関係
【0085】
管内の層流は適度な伸張性フローの一例である。管などの内部流で近傍平坦面に向かって当たる衝突フローの伸張性は高い。細胞懸濁液は、低剪断環境に入る前に管の出口付近を通るほんの短い瞬間に伸張力を受ける。伸張力の大きさは管直径、流量、および、平面からの距離によって容易に制御される。定常運動制御および微調整操作は10ミクロン以内の精度で距離を制御することができる。また、液体の針への流入または針からの流出は強く細長い流れを生じることができる。多様な長さと内径(ゲージ)を採用することにより、壁剪断応力に晒されたせいで生じた解離を針への流入または針からの流出が原因で生じた解離と区別することができる。
【0086】
必要と算定された力および装備に基づいて、祖h式試料の細胞を直径10ミクロンから500ミクロンの管に通し、この時に10マイクロリットルから2000マイクロリットルまでの間の容量を利用して100ダイン/平方センチメートルから800ダイン/平方センチメートルの壁剪断応力を生じるようにする。或る実施例では、細胞は22ゲージ針または18ゲージ針に通される。或る実施例では、細胞が晒される層流による壁剪断応力は約100ダイン/平方センチメートルから約800ダイン/平方センチメートル、約300ダイン/平方センチメートルから約500ダイン/平方センチメートル、または、約350ダイン/平方センチメートルから約450ダイン/平方センチメートルである。必要な力の量と細胞の種類に応じて、細胞が層流による壁剪断応力に晒される期間は約10ミリ秒から約500ミリ秒、もしくは、それよりも長くてもよい。
【0087】
或る実施例においては、媒体の粘性を調節して、適正な剪断力を供与している。
【0088】
解析に適した試料が生成されるまで、上述の解離工程を必要に応じて反復するとよい。或る実施例では、少なくとも約70%、約80%、約90%、または、約90%を越える細胞が分散により1個から100個の細胞を含んでいる凝集塊にされる。凝集塊は5個から100個の細胞群、10個から100個の細胞群、10個から25個の細胞群、または、5個から25個の細胞群であってもよい。凝集固まりは1凝集塊あたりの含有細胞の個数が15個よりも少なく、例えば、1個から10個の細胞を含有しているのが好ましい。
【0089】
解離工程はまた、解離を支援する化合物を添加する工程、または、細胞の応力反応の活性化を阻害する化合物を添加する工程を含んでいるようにしてもよい。例えば、解離工程の最中に以下に列挙するいずれかの物質を細胞に添加するとよく、すなわち、生理学的に容認できる抗酸化剤、ムコリチック剤、ジスルフィド結合を減じることができる、N-アセチル-L-システインまたはジチオトレイトール等のような薬剤、生理学的に容認できる、エチレンジアミン四酢酸(EDTA)等のようなキレート剤、1種類以上の膜組織を保護する界面活性剤、または、これらの各種組合わせを添加するとよいが、膜組織を保護する界面活性剤の具体例としては非イオン性界面活性剤があり、その具体例としては、ポリエチレングリコール、ポリエトキシレート型脂肪酸、エチレンオキシドブロック共重合体、プルロニックF68(BASF)などのようなプロピレンオキシドブロック共重合体などがある。
【0090】
分散工程は、例えば、約0.9 % w/vの塩化ナトリウムの無菌水溶液などのような血清が全く含まれていない等張性生理食塩水中に複数の細胞または細胞凝集塊を懸濁させる工程を含んでいるが、等張性生理食塩水は、任意で、生理学に容認できる緩衝剤や塩を更に含有していることもあり、例えば、ラクトリンゲル液、アセトリンゲル液、燐酸緩衝生理食塩水、トリス緩衝生理食塩水、ハンク平衡塩溶液、アール平衡塩溶液、標準的なクエン酸生理食塩水、ヘペス緩衝生理食塩水などを含有していることもある。
【0091】
当業者には分かることであるが、細胞解離プロセスは手作業で実施されてもよく、例えば、ピペットまたは針を使用して人が行うか、または、空気駆動式または流体駆動式の自動流体処理装置などの自動プロセスを利用して行ってもよい。手動解離プロセスと自動化入りプロセスのいずれも、本発明の多様な実施例が網羅している。
【0092】
或る実施例においては、組織試料が解離および分散されている間、細胞シグナル伝達路や応力反応経路など(これらに限定されない)の反応経路がリガンド刺激に比べて活性化していない状態にあるが、具体的には、EGF刺激に比べて分散処理がFOS発現を活性化しない。
【0093】
<<C. 試料の高純度化と集積培養>>
凝集塊状の細胞は多数の細胞型を含んでいることがあるが、そのような多数の細胞型のうちの極めて少数またはわずか1種類のみしか検査や解析の対象とならないことも多い。このような場合、細胞は解離処理に付されてより小型の複数の凝集塊、個々の単一細胞、または、その両方に離解されてから、それらの混合物を高純度化処理に付して、興味の対象ではない細胞などの混入物を除去することで試料を高純度化し、更に、元の混交細胞試料中に含まれている興味の対象である細胞の割合よりも高い割合で興味の対象である細胞を調製することにより、試料を集積培養する。本明細書中で使用されているような「高純度化」または「集積培養」という用語は、標的細胞(例えば、腫瘍細胞、それ以外の解析に付されている細胞など)の個体数の、高純度化や集積培養の処理に付して除去しておかなければ解析の妨げとなる恐れのある標的ではない細胞または細胞の各部分の個体数に対する割合を増大させることを意味している。
【0094】
例えば、固形腫瘍から採取された生検試料は、興味の対象である細胞(例えば、腫瘍細胞)と混入した正常な細胞成分(血液生成細胞、肝細胞、脈管構造細胞など)の両方を含有している細胞混合物から構成されている。具体的な実施例においては、混入成分を除去する方法としては培検計画案に応じて、混入成分に固有の抗体を利用する方法か、または、標的細胞に固有の抗体を利用する方法が取られる。抗体は、プレート壁面や磁気ビーズなどの可塑性ビーズまたは可塑材被膜ビーズなどの可塑性表面を具体例とする基板に直接結着されるか、または、第1抗体を認識する第2抗体により基板に間接結着されて、興味の対象である細胞から混入物質を除去することができる。
【0095】
<<D. 細胞分配>>
細胞の解離処理と任意の高純度化処理(必要な場合のみ実施)が完了すると、細胞の試料は、本発明のカートリッジ内の1個以上の隔離室(例えば、上述の1個以上の第2隔離室)またはそれ以外の何か好適な容器に分配される。
【0096】
興味の対象である細胞は、所望されれば、前項Bに記載されていたような各種技術を利用して分散されてから、1分割量ごとの部分標本に分配されて、検査試薬と反応させられ、他の解析・検査に回され、または、その両方が実施される。或る実施例においては、1分割量ごとの部分標本が特別に誂えたカートリッジのウエルのうちの幾つかまたは全部に分配される。部分標本は所望の検査試薬と反応させられるが、例えば、刺激により細胞増殖やシグナル伝達を促す1種類以上のリガンドが適用される。
【0097】
第2隔離室またはそれ以外の検査用基板に分配された部分標本は、必要な細胞の個数およびそれ以外の当業者には周知の実験条件次第で変容可能である。或る実施例では、検査用部分標本の1分割量は2ミリリットル未満であるが、200マイクロリットル未満であるか、または、1マイクロリットルから200マイクロリットルの間か、いずれかである。当業者には分かることであるが、この量は、検査用の懸濁液中に好適な数の細胞が獲得されたさえ、必要に応じて上述の具体的範囲とは異なる値であってもよい。
【0098】
或る実施例においては、1分割量ずつの検査用部分標本を受容している少なくとも1個の隔離室は対照試料と指定される。このような対照試料は細胞生存度および応力レベルごとに再度評価分析し直されてもよいし、細胞計数処理を受けるようにしてもよいし、更に別な添加剤か対照物質が加えられて、他の隔離室のデータ解析結果とプラスマイナスの対照を行うようにしてもよい。
【0099】
分配された細胞は、その細胞型に好適な何らかの培地中に懸濁状態にされる。例えば、分配された細胞の検査用部分標本は血清が全く含まれていない養分を最小限に抑えた培地内に置かれている。血清が全く含まれていない養分を最小限に抑えた培地とは、必須アミノ酸、塩(例えば、塩化カリウム、硫酸マグネシウム、塩化ナトリウム、燐酸二水素ナトリウムなど)、グルコース、各種ビタミン(例えば、葉酸、ニコチンアミド、リボフラビン、B-12など)、それ以外の、細胞を適切に処理したり解析するのに必要な成分などを含んでいる。血清が全く含まれていない好適な栄養培地の具体例としては、ダルベッコ・フォークト変法イーグル最小必須培地(DMEM)やRPMI培地などがある。
【0100】
或る実施例においては、検査用部分標本は、96ウエルプレートなどのような可塑性プレートのウエルに分配されるが、この場合のウエルの壁は、ポリエチレングリコール、デキストラン、アルギネート、シリコーンなどのような、生理学的に容認可能なヒドロゲルまたはオイルで被膜されている。
【0101】
<<E. 検査試薬および検査>>
検査用部分標本は多様な検査試薬と反応させられるが、カートリッジ内で実施されるか、または、1個以上の隔離室をカートリッジから分離させた後で実施されるか、いずれかである。本明細書における方法および装置の利点は、検査試薬が治療の時点で添加されてもよいこと、検査試薬がカートリッジの特定のウエルに事前装填されていてもよいこと、または、その両方を満たしていてもよいことである。これにより、体外生体マーカーの検査は生細胞を利用して、任意で治療の時点で行うことができるようになる。このような方法および装置を特定の検査試薬と併用することで試料を体外で操作し、新規な予測生体マーカーの開発を容易にし、特定の薬剤に対する細胞感度の監視および測定と当業者が認識する上記以外の用途を監視および測定することができるようになる。
【0102】
例えば、患者から採取した固形腫瘍の試料は解離され、分配されてから、治療の時点で目下利用できる癌治療法のパネルに対して検査が行われる。次に、試料は安定化処理され、必要なら固定処理され、または、安定化と固定化の両方の処理が行われてから、解析が実施される。検査試薬は各々についての結果次第で、個々の患者の腫瘍にどの治療が最も効果的であるかを治療の時点で医者が即時判断することができる。この個人ごとに誂えた衣料は幾多の恩恵を施すものであり、特に、迅速かつコスト効率のよい態様で標的癌の治療法と培検計画案を採用できるという恩恵がある。
【0103】
本発明の実施例は、少なくとも1種類の薬剤を投与することにより標的である体外生体マーカーまたは体外生体分子に測定可能な定量効果または定性効果を生じることにより、分配済みの細胞(例えば、癌細胞)を解析することを目標としている。定量効果または定性効果は細胞経路の活性化であってもよいし、細胞経路の抑制であってもよい。具体的な細胞経路として、代謝経路、複製経路、細胞シグナル発生経路、腫瘍形成シグナル発生経路、アポトーシス経路、血管新生誘導経路などがあるが、これらに限定されない。例えば、定量効果または定性効果とは、G蛋白質共役受容体、または、上皮細胞成長因子受容体(EGFR)などの受容体型チロシンキナーゼに対するアゴニスト的代用効果またはアンタゴニスト的拮抗効果、更に、下流経路に対するアゴニスト的代用効果またはアンタゴニスト的拮抗効果の測定値のことである。
【0104】
測定される定量効果または定性効果とは、即時型または遅延型の初期遺伝子系統のメンバーなどの遺伝子の発現レベルのことである。好適な即時型または遅延型の初期遺伝子系統メンバーの具体例として、FOS、JUN、DUSP 1-28などがあるが、これらに限定されない。
【0105】
検査試薬の存在または不在の効果も、遺伝子情報翻訳後修飾蛋白質、イオン、酵素などの体外生体マーカーを検出することにより判定することができる。
【0106】
好適な検査試薬は、次に列挙するもののうちの1種類または各種組合わせを含んでいる(それらに限定されないが)。すなわち、医薬品、化合物、細胞刺激剤、ポリペプチド、ポリヌクレオチド、抗体、Fab分屑、Fc分屑、RNA、miRNA、siRNA、燐蛋白質などのうちの1種類または各種組合わせを含んでいる。上述のように、試薬の投与の後に続いて、分散細胞または分配細胞の標的体外生体マーカーまたは標的体外生体分子に対する定量効果または定性効果の測定が行われる。
【0107】
或る解析方法について、検査試薬は検出可能な薬剤であるとよい。検出可能な薬剤は個別に使用してもよいし、或いは、もう1つ別な化合物(例えば、抗体と共役した検出可能な薬剤など)と共役状態またはそれ以外の結合状態になるようにして使用してもよい。好適な検出可能な薬剤の具体例として、酵素、蛍光物質、発光物質、生体発光物質、放射性物質、陽電子断層撮影法で利用される陽電子射出物質、非放射性常磁性金属イオンなどが挙げられるが、これらに限定されない。
【0108】
上記以外の好適な検査試薬の具体例として各種腫瘍細胞刺激リガンドがあるが、更にその具体例としては、成長因子(例えば、EGF、インシュリン、VEGFなど)、エストロゲンやエストロゲン複合物などのホルモンなどが挙げられる。
【0109】
本発明の方法および装置の抗固形腫瘍応用例またはそれ以外の抗癌応用例については、検査試薬の具体例として有効な製薬剤や細胞毒性化学療法薬があるが、更にそれらの具体例として、有効製薬剤は抗腫瘍単クローン抗体剤であるトラスツズマブ(ヘルセプチンまたは登録商標Herceptin)、セツキシマブ(エルビツクスまたは登録商標Erbitux)、ベバシズマブ(アバスチンまたは登録商標Avastin)、リツキシマブ(リツキサンまたは登録商標Rituxanもしくはマブテラまたは登録商標Mabthera)等と小型分子阻害剤であるゲフィチニブ(イレッサまたは登録商標Iressa)、エルロチニブ(タルセバまたは登録商標Tarceva)等を含んでおり、細胞毒性化学療法薬はタキサン系製剤(タクソテレまたは登録商標Taxotere)、代謝拮抗剤(フルオロウラシル)、アルキル化剤、白金剤、アントラサイクリン系物質等を含んでいる。上述の具体的な製薬剤は個別に使用されてもよいし、本明細書に開示されている別な製薬剤と組合わせて使用されてもよいし、または、それ以外の化合物と組合わせて使用されてもよい。
【0110】
検査試薬を投与した後で、検査試薬が1種類以上の生体マーカーの発現に影響を与えたか否かを判定することができるが、この場合、そのような発現の存在、不在、または、相対的程度は選択された製薬剤に対する細胞の感受性を示している。このような生体マーカーは、mRNA、マイクロRNA、cDNA、蛋白質、燐蛋白質、遺伝子情報翻訳後修飾蛋白質、修飾ヒストン、DNAパッケージング細胞などのような多様な体外生体マーカーを含んでいる。例えば、製薬剤に対する感受性に付随している初期反応遺伝子(例えば、FOSやJUNなど)については、生体マーカーはmRNAまたはcDNAとなるかもしれない。検査試薬が存在している場合における各種生体マーカーの組合わせの発現の存在、不在、または、発現の相対度数は、製薬剤などの選択された検査試薬に対する細胞の感受性を示している。
【0111】
<<F. 試料調製および試料安定化処理>>
本明細書に記載されて添付図面にも例示されているように、本発明を利用して処理される細胞は多数の方法で調製および安定化処理されて、そのような細胞に対して多様な細胞解析を実施することができるようにしている。例えば、、核酸解析、蛋白質解析、生細胞指標剤を利用した解析、または、これらの各種組合わせの解析ごとに細胞を調製することができる。
【0112】
核酸解析については、アール・エヌ・エイ・レイターやアール・エヌ・エイ・プロテクトセルリエイジェント(登録商標RNAlaterおよび登録商標RNA Protect Cell Reagent −キアゲン(Qiagen)社製)或いはエタノール等のような安定化試薬を細胞に添加するとよい。安定化処理済みの細胞は任意で溶解分離されるか、またそうでなければ、興味の対象である核酸が抽出される。抽出されて高純度化された核酸は、PCR技術などを利用して解析に付される。
【0113】
或る実施例においては、また、既に説明したように、本明細書に記載されている方法は更に別な解析に付す目的で核酸をもたらす。このような試料については、分散および任意の集積培養の処理に続いて、拡散を安定化または抽出(任意)し、高品質で相当量の核酸をもたらすことができる。例えば、具体例としては後段の実施例10ならびに図13および図14を参照のこと。これは、例えば、検査試薬に対して反応させた後で所望の細胞を溶解分離し、その次に、逆転写酵素とDNAプライマーを使ってcDNAを得るという方法で実施される。DNAプライマーの具体例としては、ポリAに相補的である非特異的プライマーである、例えば、オリゴ(dT)12-18の各プライマーや、興味の対象であるmRNA転写に相補的である特異的プライマーなどがある。当業者には分かることであるが、細胞は、化学的手段や機械的手段などの多様な方法を利用して溶解分離される。
【0114】
任意で、試薬を使って細胞を安定化することで生体マーカー情報を検出し、保存し、または、検出と保存の両方を行うことができるが、その手段として、例えば、逆転写酵素およびDNAプライマーを利用してcDNA転写を得て、下流分子解析のためのRNA、DNA、および、蛋白質を準備するとよい。
【0115】
蛋白質解析については、全細胞または溶解分離処理された細胞のいずれを使用してもよい。無傷の全細胞は固定化されてから、後段の表2に明記したもの等のような重合体を使って安定化され、硝子スライドなどのような隔離室に試料を付着させることができるようにする。このような試料は、例えば、免疫組織化学(IHC)解析などのような分析を受けることができる。細胞を溶解分離させる処理、または、それ以外の方法で破砕する処理はウエスターン・ブロット法などのような評価分析で利用することができ、安定化または固定化を必要としないことがある。
【0116】
病理学者による形態学的調査のスライド標本と免疫組織化学IHCによる蛋白質解析は、本明細書に記載されている方法の成果である。従って、細胞を調製するのに、任意で重合体を使って硝子スライド上に準備し、形態学的解析、免疫組織化学解析、または、その両方の解析に付すことができるようになる。例えば、表2に開示されている混合物は表3の具体的な培検計画案に従って使用することができる。ジェイ・エー・マクセム(J.A. Maksem)、ヴィー・ダンワダ(V. Dhanwada)ほか著(2006年刊)、「自動液体細胞学的試料検査を残留細胞懸濁液を利用した手動液体細胞学的方法でThinPrep(登録商標)による500事例に基づいて実施する(Testing Automated Liquid-Based Cytology Samples with a Manual Liquid-Based Cytology Method Using Residual Cell Suspensions from 500 ThinPrep Cases)」という題の細胞病理学診断(Diagnostic Cytopathology)34巻(6)、391-396掲載論文も同様に参照のこと。
【0117】
重合体溶液
アガロース 0.18グラム
ポリエチレングリコール(PEG) 4.8グラム
アルコール試薬 76.8ミリリットル
ポリL-リシン
(0.1%) 0.25ミリリットル
ノニデット(Nonidet)P40**** 0.05ミリリットル
合計 240ミリリットル
表2
【0118】

【0119】
生細胞指標剤解析は、細胞を生きたまま処理する方法のどの時点であれ分子指標剤(後段の各実施例に記載されているようなマイトトラッカー(登録商標MitoTracker)など)を添加する工程に関与しているようにしてもよい。生細胞指標剤をこのように添加する工程は、固定化処理工程より前に行われるべきであり、そうでなければ、細胞を死なせてしまうことになる。例えば、このような指標剤の添加時機は、細胞固定化処理工程より先ではあるが、細胞安定化処理工程についてはその前後のいずれの時点で添加されてもよい。
【0120】
或る実施例においては、細胞を安定化および固定化させるにあたり、その後で生体マーカーの分子解析および分子検出を行うことができるようにするのに好適であればどのような手段を利用してもよい。一般に、ホルマリンなどの架橋固定剤は好ましくないが、後続の解析の妨げとならない程度の少量であれば存在していても構わない。生体マーカーが特定の1種類または複数種類の遺伝子の発現である場合は、或る実施例においては、細胞は溶解分離されてから逆転写酵素および好適なプライマーと反応させられて、細胞中にmRNA転写のcDNA転写を生成する。これにより、mRNAと比較してcDNAが分解することは少なくなるので、後続の解析を容易にすることができる。
【0121】
或る実施例においては、1×104個またはそれより多数の細胞が処理されることにより、RNA、DNA、蛋白質、燐蛋白質、または、これらの各種組合わせのうちのいずれかまたは全てを安定化させている。
【0122】
或る実施例においては、細胞は処理後に固定されてもよい。好適であればどのような固定手段が採用されてもよいが、例えば、空気乾燥技術、アルコールのうちでもメタノールやエタノールなどのような低級アルカノールを含有している固定剤などの化合物を添加する手段、ホルマリンを添加する手段、RNase阻害剤を添加する手段、アガロースを添加する手段、ポリエチレングリコールを添加する手段、ポリL-リシンを添加する手段、1種類以上のキレート剤または1種類以上の抗酸化剤を添加する手段などを採用してもよい。或る実施例においては、固定剤は、アガロース、ポリエチレングリコール、オクチルフェノキシポリエチレングリコール、ポリL-リシン、試薬アルコール、および、水を含有している。
【0123】
本発明の方法の更に別な実施例は、例えば、選択された有効な製薬剤に対する細胞の感受性を判定する目的で、固形腫瘍ができている動物被検体またはヒト被検体から採取した固形腫瘍細胞などのような、被検体の固形組織細胞を調製する方法を含んでいる。或る具体的な方法は、(a)所望の細胞を含んでいる固形腫瘍を被検体から採取する工程と、(b)組織を分散させて(例えば、剪断力を用いて)個別の単一生細胞にし、個数にして100個以下の、例えば、10個から100個の生細胞からなる凝集塊にし、または、単一生細胞および生細胞凝集塊の両方に分散させる工程と、(c)例えば、生細胞から混入物質を除去することで試料を集積培養する工程と、(d)生細胞を分配して1分割量ずつの部分標本を隔離室に入れる工程と、(e)生細胞を1種類以上の検査試薬と反応させる工程と、(f)固定剤、安定剤(例えば、RNA、DNA、蛋白質、燐蛋白質、または、これらの各種組合わせを安定化させる薬剤)、固定剤と安定剤の両方を使って細胞を処理して腫瘍細胞を固定し、生体マーカーを固定して解析に付し、または、腫瘍細胞と生体マーカーの両方を固定して解析に付す工程とを含んでおり、その場合、腫瘍細胞、生体マーカー、または、その両方の固定は被検体から組織を除去してから4時間以内に自動方式または手動方式のいずれかで完了される。
【0124】
本発明のもう1つ別な実施例は細胞を検査する方法を提案しており、斯かる方法では、固形腫瘍細胞は哺乳動物(例えば、ヒト患者)から採取され、細胞の全部または一部を1種類以上の検査試薬に体外で反応させると、更にまた、細胞を安定化させるのに任意で、細胞DNA、細胞RNA、蛋白質、燐蛋白質、または、これらの各種組合わせなどの生体マーカー情報を保存することができる固定剤(例えば、重合体)を使うと、細胞の大半、例えば、少なくとも65%の細胞、より具体的には、少なくとも75%の細胞が生存しているが体外で自己複製することはない。このような生体マーカーは、当業者には周知の分子解析または本明細書に開示されている新規な生体外生体マーカー検査を利用することで検査されるとよい。
【0125】
後段の各実施例は本発明を更に例示しているが、本発明の範囲を制限するものと解釈するべきではない。
【実施例1】
【0126】
<1. 生細胞処理>
マイトトラッカー(米国カリフォルニア州カールスバッドに居所を置くインヴィトロジェン社製)などの生細胞分子指標剤を利用した生細胞処理の重要性は既に説明した。マイトトラッカーは、プラズマ膜をわたる受動拡散によって生細胞に適用されると、ミトコンドリアに集中して局在するようになる。生細胞はマイトトラッカー局在化を安定させるために固定化され、蛍光顕微鏡により解析される。目下利用できる生検処理法を利用している方法とは異なり、本発明による装置およびシステムは分子指標剤を用いた生細胞研究を可能にしている。これは図20および図21に例示されており、これらの図面では、指標剤が生細胞に適用された場合の、ミトコンドリアの特定の細胞質プラスマ局在化(粒状蛍光発光、図20Aおよび図21Aの左半分)が明瞭に立証されているが、先行技術の方法を利用して固定された細胞に指標剤が適用された場合には所望する情報を欠いていた(図20Bおよび図21Bの右半分)。
【実施例2】
【0127】
<2. MCF−7およびHCT−116の解離研究>
MCF−7(ヒトの乳癌細胞−ATCC番号HTB-22)およびHCT−116(ヒトの大腸癌細胞−ATCC番号CCL-247)を使って、半自動ピペット装置における細胞集団寸法、生存度、および、細胞活性化に及ぼされる剪断力の影響を検査した。簡単に説明すると、MCF−7細胞およびHCT−116細胞が培養組織中で80%の集密度まで増殖してから、ゴムヘラを使って静かに掻爬することによりプレートから取外してから増殖培地中に懸濁させ、通例の穿刺吸引採取試料中の細胞個数および細分化寸法と同程度にした。細胞懸濁液の1分割量の部分標本を22ゲージ針に4度にわたって通し、その際には自動ピペット装置(米国マサチューセッツ州ホリストンに居所を置くハーバード・ピペッタ・ハーバード・アパレイタス製(Harvard Pipetter, Harvard Apparatus))を使用し(1回の処理ごとに4.14ミリリットル/分の割合で吸引・注入される)、結局、100ダイン/平方センチメートルから800ダイン/平方センチメートルの範囲で壁剪断応力に晒されたが、その期間は1個の細胞につき、または、1個の凝集塊ごとに4(移行回数)×14ミリ秒/1回の移行=56ミリ秒であった。個々の細胞由来または個々の凝集塊由来の代表試料は硝子スライド上に細胞遠心分離処理され、95%エタノールで固定され、パパニコロウ染料で着色された。代表領域の顕微鏡写真を得た(倍率x200)。剪断力が増大するにつれて細胞集団寸法は減少する点に留意すること。これらの結果は図22に例示されている。
【実施例3】
【0128】
<3. 細胞集団寸法分布>
実施例2の方法を採用した後、細胞濃度および細胞寸法分布を測定する非流動画像方式細胞計数装置(米国マサチューセッツ州ローレンスに居所を置くネクセロム製(Nexcelom)のセロミター(登録商標Cellometer))を使用することにより平均細胞集団寸法を定量化した。100ダイン/平方センチメートルで、MCF−7細胞の平均集団寸法は97±3マイクロメートルであり、HCT細胞は51±6マイクロメートルであった(図15)。これらのデータは、生細胞の凝集塊を分散させるのに必要な再現可能な最適剪断力の範囲を提示している。
【実施例4】
【0129】
<4. 分散処理後の生存度解析>
実施例2の方法を利用した後で、半自動ピペット装置から相当の剪断力でトリパンブルー色素排除試験によって生存度が検査された。800ダイン/平方センチメートルよりも大きい剪断力は生細胞の操作および処理には厳し過ぎると思われるが結果的に生存度が40%を越えて減少したと結論づけられた。達成された結果を図表で描いたものとして図16を参照のこと。
【実施例5】
【0130】
<5. 分散処理後の活性化解析>
細胞活性化の機能的測定法として、定量RT-PCRによって判定されるFOS mRNA誘導法がある。FOSはEGFR経路に関与している初期反応遺伝子である。或る実験では、MCF−7細胞は6ウエルプレートにおける正常な増殖条件で80%の集密度まで増殖した。細胞を静かに掻爬してから、RNA抽出前に100ナノグラム/ミリリットルのEGFリガンド(シグマ受容体)を存在させて、または、同濃度のEGFリガンドを欠いたままでより長い培養時間(0分から45分)に亘ってより大きい剪断力(ハーバードピペッタ製装置により0ダイン/平方センチメートルから800ダイン/平方センチメートル)に晒した。30分から45分経過した時点でFOS mRNA誘導は最高潮に達し、約60分のうちに基底レベルに戻った。EGFリガンドを使った培養の結果としてFOS蛋白誘導は刺激により活発化した。ここで重要なのは、予備的な結果の示すところによると、半自動プラットフォームに生成される100ダイン/平方センチメートルから800ダイン/平方センチメートルの剪断力による分散処理の結果、EGF刺激と比べてそれほどの細胞活性化が生じることはない点である。得られた結果を図表で描いたものについては図17および図18を参照のこと。
【実施例6】
【0131】
<6. 装置>
図1は、組織の解離を遂行する機能、細胞計数装置の機能、遺伝子発現剤感受性検査の機能、および、解析に付すための試料固定の機能を統合するためのプラットフォームとして作用するような装置で使用される具体的カートリッジの概略図である。図1から図22は、本明細書に記載されている各特性の特定の実施例を例示している。当業者なら、本件の説明に関連づけて図面を思量すれば、各実施例が作用する態様が分かる。
【0132】
上述の装置は主要構成部材として以下のものを備えている。すなわち、装置に挿入することができるうえに手動処理の用途に付すことができる貯蔵カートリッジ1、斯かるカートリッジ1の上に搭載されて複数の小型容器が設けられた、例えば、96ウエルプレート型2、および、試料を初期受容し、試料を分散し、試料から混入物を除去するための複数の受容器3を備えている。受容器3は、図2に概略的に描かれているうえに本明細書中で既に説明されている複数の異なる機能を果たすことができる。カートリッジ1には標識4が取付けられており、斯かる標識4は試料を容易に識別することができるようにバーコード形式であってもよい。受容器3は各々が1個のウエルと内容物の生物学的拘禁を確保する封鎖部を備えており、針で刺し通すことができるが、針を抜取った時点で再封鎖される。組織試料は患者から採集されるが、通例は、細い針5を使った穿刺吸引生検法によって医者が採集し、医者は試料組織をカートリッジ1の受容器3内に置く。
【0133】
次に、カートリッジ1を装置に滑り込ませてから扉を閉じて装置を封鎖し、カートリッジ1は外部環境から生物学的に密封されるとともに、生物学的に危険な何らかの組織試料を放散することが無いように厳封される。代替の実施例においては、カートリッジは特定の試薬を保有しているプラットフォームであり、手動で処理に付すことができる。
【0134】
カートリッジ1には、組織試料の操作を遂行するのに使用される原材料を貯蔵および廃棄するための、1個以上のウエル6が設けられている。このような原材料の具体例として、針先端具および試薬が挙げられる。針先端具は開口および尖端が設けられたニードル部と、ニードル部の内側にあって開口および注射器と流体導通状態にある環帯部とから構成されている。本件の装置は自蔵式であるが、例外として、必要に応じてコードを通して電流が供給される。
【0135】
カートリッジ1は処理集成部を格納する受容器3を備えており、通例は、組織試料を混合する用途に付されるようにしてもよい。受容器3は緩衝生理食塩水の解離液が事前封入されており、任意で、解離溶液にプロテアーゼ系物質を使用するのを避けねばならないという抑制がある場合には、キレート剤、抗酸化剤、粘性修飾剤などを更に含有している。
【0136】
受容器3はウエルの密封カバー部材を含んでいる。この自蔵式のウエルと処理集成部との配置は人間の作業人員が生物危害に晒されるのを最小限に抑えている。係合用張出部が密封カバー部材から突出している。
【0137】
本発明の装置には作業部材が誂えてあり、カートリッジ1上の保管ウエル6から針先端具を選択的に持ち上げて針先端具を装着した注射器部材を操ることができるとともに、受容器の処理集成部などのような、装置に設けられている或る装具で作業することができるよう図っている。
【0138】
本発明の装置を使って初めて作業するにあたり、作業部材が針先端具を保管ウエル6から回収し、受容器3に関連する位置に移動させるが、受容器3はその内部に試料組織が医者によって既に置かれているうえに、緩衝液、キレート剤、および、抗酸化剤などのような解離溶液が事前に装填されており、針先端具で受容器3の封鎖部を刺し通して針先端具の尖端を均質な液状混合物の中に浸漬し、受容器3から試料の一部を針先端具の注射器の中に吸引してから針先端具の尖端を受容器3内部の所定位置まで移動させて、吸引した試料をその同じ受容器3かまたはもう1つ別な第2受容器3の中で分散させることで組織試料を解離させて、無傷の腫瘍細胞と混入物質とを含んでいる均質な溶液にする。このような工程は、組織試料を所定のレベルまで解離させるのに必要な回数だけ反復実施される。図3の、例えば、参照番号309を参照のこと。
【0139】
作業部材(または、手動操作に付される場合には、作業人員)はカートリッジの保管ウエル6から新しい針先端具を回収してから受容器3に関連する位置まで移動し、針先端部を使って選択された受容器3の封鎖部を刺し通し、針先端部の尖端を均質な液状混合物中に浸漬し、受容器3から試料の一部を針先端部の注射器の中に吸引し、針を受容器から抜取り、マトリクス状の受容器のうちの別な1個に関連する位置まで移動し、その受容器の封鎖部を針先端部を使って刺し通し、注射器から試料の一部を受容器3の中に入れる。図2を参照のこと。このマトリクス状の受容器3はその最下位置にある収蔵室の真上に樹脂ビーズ床が支持されており、その更に真上に装填室が設けられた構成になっている。樹脂ビーズの床には栓が装着されており、栓は樹脂ビーズ床の頂面から底面まで延在している。栓を構成している素材は、樹脂ビーズ床の頂面位置まできた針先端具による刺し通しを許容するとともに、針先端具が樹脂ビーズ床の底面を通り抜けて収蔵室内まで張出すのを許容するような素材である。図2を参照のこと。これに代わる具体例として、樹脂ビーズ床には導管が装着されており、導管は装填室の頂面付近から樹脂ビーズ床を突き抜けて収蔵室の底面付近まで延びている。作業時には、受容器内に置かれた試料液は樹脂ビーズ床より上位にあって、重力によって樹脂ビーズ床に給送されてその中に吸込まれ、樹脂ビーズ床が溶液から混入物を除去して収蔵室に回収する。導管の頂端は、収蔵室内に回収する前に樹脂ビーズ床をどの溶液といえども迂回することが無い態様で取付けられる。
【0140】
或る実施例においては、試料はその中に適正数の細胞が分散しているのを確保するように検査される。作業部材はカートリッジ保管ウエル6から針先端具を回収してから受容器に関連のある位置まで移動し、針先端具を使って受容器の封鎖部を刺し通し、針先端具の尖端を均質な液状混合物中に浸漬し、試料の所定の一部を受容器3から針先端具の注射器の中に吸引し、針先端具を受容器3から抜取り、細胞計数装置モジュールに関連する位置に移動し、試料の上記所定の一部を計数装置モジュール内に置く。針先端具は計数装置容器から抜取られ、カートリッジ上の処理容器に入れて処分される。
【0141】
計数装置モジュールは、カートリッジ上の受容器3のうちの1個であってもよいが、計数装置容器の格納室の内部に乾染料と一緒に梱包される。計数装置容器の内部では、格納室内に既に置かれている計数するべき試料部分が染料を溶かし、この染料が腫瘍細胞を着色している。所定の試料部分は漏斗状の計数装置管の中を通り抜けて落下し、任意で、細胞計数を目的としてスキャナーにより走査される。計数されるべき試料部分は格納ウエル内の計数装置管より下の位置に集積している。光学スキャナーが細胞個数を中継して表示器に伝えるが、表示器はその個数が良好な生検試料と言える所定計数寸法に合致しているか超過しているかを判定する。解析結果はディスプレイ装置に表示され、プリンターによって印字され、または、その両方が実施される。次に、解析結果が直ちに医者の手引きとなって更に別な生検が必要か否かを判断させる。試料が適正である場合には、患者は検査から放免される。
【0142】
細胞が分散処理されて混入物の除去が完了すると、細胞は1分割量ずつの部分標本にされて検査用マトリクス2、通例は、96ウエルプレート型の区画に置かれる。典型例として、ウエルは所望の媒体(緩衝生理食塩水溶液および検査試薬)の事前充填が済んでいる。作業部材がカートリッジからもう1本別な針を拾い上げて分散処理と混入物除去処理が済んだ所望量の細胞を受容器3から吸引し、一連の密封試料ウエル2セットに関連する位置まで移動し、連続して一個ずつウエルの封鎖部を次々に刺し通して所定量の試料部分を個々のウエルごとに注入してから針先端具を抜取ることを繰り返す。針先端部は処理容器6に入れて処分される。
【0143】
ウエル2には多様な投与量の多様な製薬剤が予備梱包されており、これら個々の投与量と個々の製薬剤に対する腫瘍細胞の感受性を検査することができるようにするのが好ましい。ウエルを維持する諸条件は当然のことながら生理学的条件に近似している。ウエル内の培地のpHは生理学的pHに近く、pH 6からpH 8であるのが好ましく、約pH 7からpH 7.8であるのが好ましく、pH 7.4が最も好ましい。生理学的体温の範囲は摂氏約30度から40度の間である。細胞は摂氏約35度から約37度の温度に維持されるのが好ましい。同様に、細胞を培養する酸素レベルは空気中の酸素濃度に比べて比較的低く、培地の酸素濃度は空気中の20%の酸素濃度ではなくむしろ、生理学的レベル(1%から6%)と同等であるとよい。培養時間が短い場合、一般に細胞に酸素供給することは必要ではない。
【0144】
多様な試薬ごとに所定の期間に亘って培養を行った後、ウエルは各々が、細胞を固定する固定剤と後続の解析処理のための指標剤とを使って処理される。このような処理は作業部材、未使用の針先端具、および、バイアルに入れた固定剤を利用して達成される。
【0145】
固形腫瘍細胞は、必要となるまで、当該技術分野で周知の何らかの方法で低温保存されるとよい。細胞は等張性溶液中に懸濁状態にされるとよいが、特定の低温保存剤を含有している細胞培養媒体中に浮遊させられるのが好ましい。このような低温保存剤の具体例としては、ジメチルスルホキシド(DMSO)やグリセロールなどがある。このような低温保存剤は5%から15%の濃度で使用され、8%から10%の濃度で使用されるのが好ましい。細胞は徐々に凍結されて、摂氏マイナス10度から摂氏マイナス150度の温度にされるが、摂氏マイナス20度から摂氏マイナス100度にするのが好ましく、摂氏マイナス150度にするのがより好ましい。
【0146】
しかしながら、前段までに記載されている本発明の装置および方法に、本発明の分野および範囲から外れることなく修正、追加、または、修正と追加を施すことができるのは明白である。例えば、受容器と光学スキャナーは、処理集成部の作業前に受容器から直接採取された試料に対して活用されてもよい。
【実施例7】
【0147】
<7. 解離研究>
MCF−7ヒト乳癌細胞(ATCC番号HTB-22)は組織培地において80%集密度まで増殖してから、ゴムヘラを使って静かに掻爬することによりプレートから取外され、増殖媒地中で懸濁状態にされた。1分割量の細胞懸濁液の部分標本を18ゲージ針に2度通され(1回通すごとに1ミリリットル/秒の割合で吸引・注入される)、172ダイン/平方センチメートルの壁剪断応力に晒される結果となり、1個の細胞または1個の凝集塊ごとに壁剪断応力に晒される総時間長は4(移行回数)×14ミリ秒/1回の移動=56ミリ秒であった。個々の細胞由来または個々の凝集塊由来の代表試料は硝子スライド上に細胞遠心分離処理され、95%エタノールで固定され、パパニコロウ染料で着色された。代表領域の顕微鏡写真を得た(倍率x200)。比較のために、転移乳癌があることが分かっている肥大リンパ節への超音波支援式穿刺吸引生検法(FNA)により、もう1つ別な画像を得た。この同じヒト試料に基づく画像は、無数のリンパ球を背景に数群の乳癌細胞を示していた。MCF−7細胞を掻爬してから、18ゲージ針(1インチ)に1ミリリットル/秒の割合で通すのを2回の吸引・注入サイクルまたは5回の吸引・注入サイクルで実施した。望ましくない条件では、溶解分離して細胞核が放出されるようにするには、試料C中において5回の吸引・注入サイクルで十分であることに留意するべきである。
【0148】
上述の実験では、MCF−7細胞に2回の吸引・注入サイクルを受けさせるというのは、エチレンジアミン四酢酸(EDTA)を欠いたまま掻爬したMCF−7単分子層を分散させる作業条件の予備鑑定を表したものである。このような実験条件が試料に加える総剪断応力はtw(4ttransit)=172dyne/cm2×0.056sec=9.6dyne・sec/cm2であった。
【実施例8】
【0149】
<8.EGFR遮断剤に対する感受性を知るための初期マーカーとしての相対FOS発現>
上皮成長因子受容体(EGFR)を標的とする少なくとも35種類の有効な癌治療薬が承認されており、或いは、臨床的試用に付されている。残念ながら、EGFR拮抗物質に対する腫瘍の感受性を予測する生体マーカーは、大半の癌種類について未知である。EGFR反応阻害の末梢効果としての初期反応遺伝子FOSの発現変化は評価することができ、更にまた、ヒト癌細胞株(A431、CAL27、HN11、HuCCT1、Hep2など)におけるゲフィチニブおよびエルロチニブの増殖抑制効果およびFOS修飾効果などの抗腫瘍効果に対する上述のFOS発現変化の関係が測定された。次に、これらの細胞株はマウスに異種移植することができ、ゲフィチニブ(A431およびHuCCT1)またはエルロチニブ(CAL27、HN11、および、Hep2)を使って14日間処理された。腫瘍に対する穿刺吸引生検は基本水準で治療から14日後にFOS査定を得る目的で実施された。これに加えて、固形腫瘍を有する患者にゲフィチニブを臨床試用することで得られた5対の腫瘍試料について上述のマーカー解析の実行可能性を試した。培地では、ゲフィチニブおよびエルロチニブは感受性のある細胞株A431、CAL27、および、HN11においてFOS mRNAレベルを減少させた。ゲフィチニブまたはエルロチニブは、EGFRに敏感なA431、CAL27、および、HN11の各腫瘍株についての生体内FOS発現増大を排除しているが、耐性菌については排除していない。簡単に述べると、FOS発現変化は器内モデルと生体内モデルの両方についてEGFR阻害物質が薬理学的に作用していることを反映している。例えば、エー・ジメノ(A. Jimeno)、ピー・クレザ(P. Kulesza)、イー・キンケイド(E. Kincaid)、エヌ・ブアラウド(N. Bouaroud)、エー・チャン(A. Chan)、エー・フォラスティエレ(A. Foratiere)、ジェイ・ブラーマー(J. Brahmer)、ディー・ピー・クラーク(D.P. Clark)、エム・イダルゴ(M. Hidalgo)共著、「抗上皮成長因子受容体効果のマーカーとしてのC-FOS査定(C-FOS Assessment as a Marker of Anti-Epidermal Growth Factor Receptor Effect)」という題の2006年刊行『癌研究(Cancer Research)』66号、2385-2390掲載論文を参照のこと。
【実施例9】
【0150】
<9. FNA法において即時であるが静かに分散させるための最適条件>
<<FNA法における乳癌細胞のアナログとしてのMCF−7細胞の選択>>
MCF−7ヒト乳癌細胞は、ホルモン依存乳癌の一モデルとして広く研究されている。この癌細胞は特徴づけが明確に行われたエストロゲン受容体(ER)陽性細胞株であるため、乳癌研究の有用な器内モデルとなっている。安定した上皮細胞株は、転移性疾患に罹った女性患者由来の胸膜滲出液から採取されたヒト乳癌細胞の一次培養から得られた(スーレ(Soule)著の論文、1973年)。それ以来、このMCF−7細胞株は、それに類似する多数の臨床特性の結果として数千回も引用された、最も広く研究された乳癌モデルとなったことには間違いない。ホルモン依存ER陽性乳癌と同様に、MCF−7細胞は初期的には、タモキシフェンやフルベストラントなどのような抗エストラゲン系物質に対して高感度である。MCF−7細胞株は、何度も予兆的臨床的試用の成果をあげた他の無数の乳癌モデルの起源となる親世代細胞株としても機能してきた。更に、MCF−7細胞株の誘導体は、第一線のホルモン治療に関与している抵抗のメカニズムに洞察を与えてきた。
【0151】
MCF−7ヒト乳癌細胞(ATCC番号HTB-22)は調製済み改良型最小必須培地(商品名Improved MEM、米国カリフォルニア州カールスバッドに居所を置くインヴィトロゲン製)、10%ウシ胎児の血清(米国ユタ州ローガンに居所を置くハイクローン(Hyclone)社製)、および、1%ペニシリン・ストレプトマイシン溶液(ペニシリン10,000 IUとストレプトマイシン10,000 IUずつ、インヴィトロジェン社製)の中で増殖した。80%の集密度に達した時に、細胞は一回だけ10ミリリットルのダルベッコ燐酸緩衝生理食塩水(DPBS)で洗浄されてから、ゴムヘラ細胞掻爬具を使って静かに掻爬してフラスコから除去される。細胞は10ミリリットルの増殖媒地中に懸濁状態にされてから1分割量ごとの複製部分標本に分配される。このような培検計画案は、ヒト乳癌穿刺吸引法で使用される腫瘍細胞凝集塊の代用となる非常に大型の凝集塊を生成するのに有効であった。第1部分標本(3ミリリットルの液中浮遊細胞)は画像解析装置で画像化され、コールター社製計数装置により寸法判定される。第1部分標本の初期寸法状態が計数された後で、試料はトリプシン処理されてから、全細胞が計数される。
【0152】
<<転移大腸癌FNAのアナログとしてのHCT−116大腸癌細胞株の選別>>
ヒト大腸癌細胞株HCT−116(ATCC番号CCL-247)は最初はヒト男性大腸腺癌に由来するものであったが、その後の研究で広く活用されてきた。形態学的には転移大腸癌に似ており、ras癌原遺伝子のコドン13の突然変異体などのヒト大腸癌に共通する遺伝子特性を示している。この癌細胞株は、製薬剤感受性ごとに選別されたヒト癌細胞株の米国国立癌研究所所有NCI-60パネルに含まれている。この癌細胞株については、広範囲なcDNAマイクロアレイ遺伝子発現データおよびこれと相関関係のある薬剤活性度データが利用できる(http://discover.nci.nih.gov/を参照のこと)。
【0153】
HCT−116細胞を10%のウシ胎児血清を含むマッコイ5a修飾培地で増殖させてから摂氏37度で尚且つ5%の二酸化炭素環境で保温培養した。培地は2・3日ごとに新しく取り替えられ、トリプシン・エチレンジアミン四酢酸(EDTA)溶液を使って約1:8の二次培養比で集密状態に達すると細胞を分割した。
【0154】
FOS着色法について説明する。すなわち、スライド標本を2%パラホルムアルデヒドおよび0.5%トリトンX-100(登録商標Triton X-100、組成式C14H22O(C2H4O)n)含有溶液中にて摂氏4度で15分間に亘って保温培養することにより、細胞凝集体を固定した。次に、スライド標本を燐酸緩衝生理食塩中に3%の割合のウシ血清アルブミンおよび0.5%の割合のトリトンX-100を含有する溶液にて洗浄してから、FOS蛋白に対するヒツジ多クローン性抗体(米国デラウエア州ウィルミントンに居所を置くケンブリッジ・リサーチ・インコーポレーティッド(Cambridge Research Inc.)社製)50マイクロリットルを1:20の希釈率で(PBS中に3%の割合のBSAおよび0.5%の割合のTritonを含有する溶液)、2時間に亘って保温培養した。続いて、ウシ血清アルブミンを3%、トリトンを0.5%の割合で含有する5ミリリットルの燐酸緩衝生理食塩水でスライドを3回洗浄した。スライドは各々がフルオレセインとロバの抗ヒツジIgG (H+L) の共役体染料液(米国オレゴン州に居所を置くモレキュラー・プローブズ・インコーポレーティッド(Molecular Probes Inc.)社製)5ミリリットル(1:20の希釈率)を使って1時間に亘って保温培養してから、燐酸緩衝生理食塩水で4度洗浄してから画像化した。
【0155】
<<トリパンブルー色素排除試験>>
この簡易検査は、細胞膜が無傷であれば細胞が色素を排除する能力を測定するものである。剪断応力の強度次第で、剪断力への細胞接触により細胞膜は過渡的に透過性を高め、または、細胞原形質膜を恒久的に破壊することができるようになる。分散実験後、細胞はハンク平衡塩溶液(HBSS)中に懸濁状態にされる。総量0.2ミリリットルの懸濁液を0.8ミリリットルの染料液(0.3ミリリットルのHBSS中に0.4%濃度の無菌トリパンブルー溶液(商品名Sigma T-8154)0.5ミリリットルを混合)に添加し、10分間に亘って保温培養してから、10マイクロリットルのこの溶液について血球計算装置を使って計数を行い、細胞の個数と死細胞の百分率を得た。
【0156】
<<細胞生死の染色判定試験>>
トリパンブルー色素排除支援は簡単かつ高精度ではあるが、蛍光染料使用の価値が検証されており、というのも、細胞の生存度と細胞の個体数は蛍光判定に付すほうが自動化も小型化も容易だからである。細胞生死の蛍光染色判定試験は2種類の染料を使用する。すなわち、カルセインアセトキシルメチル(カルセインAM)とエチジウムホモダイマー(EthD-1)である。カルセインAMは非蛍光性細胞透過性染料である。この染料は細胞内エステラーゼにより開烈して生細胞中で蛍光性を示す。エチジウムホモダイマー(EthD-1)はDNAと結合する一種の染色体計数染料であるが、生細胞に浸透することはなく、死細胞を検出するために使用することができる。標準キットがアクティブモーティフ(ActiveMotif)から購入できる。
【0157】
<<アポトーシスの検出>>
接触強度次第では、流体剪断力により細胞壊死またはアポトーシスを生じることがある。解離計画を実施してから半時間から1時間経過後に、固定処理していない細胞について何度かアポトーシスを判定するために、バイオチウム(Biotium)から購入できる細胞透過性ニュクヴュー488(商品名NucView 488)カスパーゼ3基質を使用した。カスパーゼ3は各種アポトーシスの共通マーカーである。ニュクヴュー488カスパーゼ3基質は蛍光生成DNA染料およびDEVD基質の細胞膜透過性共役物質である。細胞内カスパーゼ3によって染料を開裂することでDNA染料を放出するのと同時に細胞核を着色する。
【0158】
実験データAの遺伝子アルゴリズム(GA)に基づく細分化速度の判定を使用した目的は、実験の吸引・注入サイクルを1回実施した後ごとに得られた、t1、t2、t3、t4、および、t5それぞれの時間における時系列的な実験測定による寸法分布に基づいて寸法依存の細分化断片の核を回帰推定することであった。遺伝子アルゴリズムは、小進化(交錯進化、乱進化、適応度に左右される淘汰)の原理に従って、初期のランダムな個体数の核モデルを展開する。注射器を通して移行を1度行うたびごとに、寸法分布は非連続時間に何度か測定されて細分化された断片となる。所与の平均管内剪断率(Gavg)で得られたデータについて、式1(1組のk次数)を回帰推定するにあたり、検査対象の「染色体」の適応度の発達を利用したが、染色体は各々が進化可能なパラメータの集合[A(i,Gavg),y,g]を含んでおり、i-細胞から構成される凝集塊ごとにai=A*(Gavg)y(Rhyd)gの関係を満たしている。
【0159】
掻爬された単層のMCF−7および単層のHCT−116を無菌注射針の中で10ミリ秒から100秒までの多様な期間に亘って放物面剪断力場に当て(壁剪断応力は5ダイン/平方センチメートルから500ダイン/平方センチメートル)、分散特性を評価した。伸張性フローは間隙相互の離隔距離が100ミクロンから1000ミクロンの範囲である衝突フローにより検査された。細胞検査は生存度について実施された。寸法分布はコールター社製計数装置を使って得られた。細胞活性度はFOS免疫組織染色法を利用して測定されたが、初期反応遺伝子は高レベルの剪断力によって即時に細胞成分上昇発現が行われる。FOS誘導の結果として細胞核着色は強まり、細胞核計数処理に基づく百分率による活性度として評点が付与される。潜在的に重要な細胞表層蛋白質を破壊する可能性のあるプロテアーゼの使用を回避するという拘束条件を設けて、例えば、キレート剤、粘性修飾剤、各種細胞保護剤などを含有しているものなど、多様な緩衝剤が吟味された。
【0160】
MCF−7単層におけるFOS染色と生存度を査定し、掻爬した単層(穿刺吸引採集試料アナログ)について得られた査定結果と比較して、剪断破壊前の基底水準の活性法を確立した。或る程度までは、これは分散前の穿刺吸引法による試料獲得術中の活性法の模倣である。個々の細胞株ごとについて、判定するべき最も重要なパラメータは、試料を解離させるのに要する最小の剪断力接触強度(壁剪断応力)と最短の剪断力接触時間(針により移行させる累積時間)であった。1分割量(掻爬された細胞の0.2ミリリットルから3ミリリットルの懸濁液)の部分標本を15ゲージから21ゲージの針(長さ0.5インチから2インチ)に0.1ミリリットル/秒から5ミリリットル/秒の流量で通したが、その際にはコンピュータ制御によるハーバード社製の注射器ポンプを1サイクルから10サイクルで使用した。10ミリリットル容量の注射器を使った個別のサイクル(吸引・注入)を1サイクルと定義した。針は、自動液体処理システムの各種部品の注文製造業者であるポッパー・アンド・サンズ(Popper & Sons、http://www.popperandsons.com参照のこと)から入手できる。1サイクル終わるごとに、試料を画像化した。複数の異なるゲージの針、複数の異なる長さの針、複数の異なる流量などを採用することにより、壁剪断応力および応力接触させた累積時間は検査ごとに異なっているようにすることができた。壁剪断応力は流量Qに従って線形に高くなるが、半径の三乗に比例する。
【0161】
一般に、試料の解離状態を制御することで1凝集塊につき5個から10個の細胞を含んでいる態様で細胞凝集塊を採取するには、10ミリ秒から500ミリ秒の間の多様な期間に亘って10ダイン/平方センチメートルから150ダイン/平方センチメートルの層流壁剪断応力に晒すことで十分である。掻爬試料を信頼できる状態に分散させるには、一般に、2サイクルから3サイクルが最適である。FOS活性度および細胞生存度を調査するのについては、FOS発現を得るために15%未満の細胞核が陽性となるように掻爬単層を破砕する目的で、諸条件と剪断力により誘導されるFOS発現とを監視した。
【0162】
<<流出入効果>>
注射器(内部には実質的に細長い流れが存在できる)への試料の流入中またはそこからの試料の流出中における試料分散の役割を評価する実験を実施した。針のゲージと流量はいずれも同じであったが、針の長さをいろいろ変えて(0.5インチと1.0インチと2.0インチの対比)、更に、サイクル数をいろいろ変えて同一壁剪断応力に同一累積時間に亘って晒し、流出入事象の発生回数をいろいろ変えることで生成された多様な試料を生成することができるようにして、結果を比較した。一般に、試料の注射器への流入および流出が相当の解離を生じることは無い。
【0163】
個々のサイクルの吸引・注入を実施した後の解離状況の視覚的解析を行うために、試料を氷の上に置いて即時に細胞遠心分離処理に付した。まず、1試料ごとに卓上型遠心分離装置(ヘティッヒ(Hettich)社製のロティーナ46S(Rotina 46S)内で2000 rpmの回転速度で遠心分離処理することにより、顕微鏡解析用に細胞を調製してから、500マイクロリットルの平衡塩溶液(ノーモソル(Normosol))中に凝集細胞固形体を浮遊させた。ここで、細胞遠心分離装置(サーモシャンダン(ThermoShandon)社製のサイトスピン4(Cytospin 4)を750 rpmの回転速度で3分間使用して、硝子の顕微鏡用スライドに細胞を塗布した。直ちに95%エタノール中でスライド標本を固定し、パパニコロウ染料で着色した。アドービ・フォトショップ5.5版(Adobe Photoshop v. 5.5)およびディジタルカメラ(Kontron Elektronik Prog/Res/3012)を付帯させた光学顕微鏡(Olympus BX40)を使って、選択領域のディジタル画像を得た。細胞は粒子計数画像解析(画像解析ソフトNIH Image)に付され、解析結果を原初部分標本について取得された細胞計数結果と比較した。
【0164】
<<衝突フローシステム>>
針の端部を平坦面に向けることにより、衝突フローは信頼できる態様で得ることができる。沈水管から出る液体噴流は管の直径の数倍の距離を経ずして急速に減衰するせいで、間隙相互の離隔距離Sを針ゲージ(Ga)と比例させてS = k (内径) がk = 0.5から5となるように調整することが重要である。間隙相互の離隔距離は手動測微計を使って制御した。大きな径の針を使用した場合は、壁剪断応力は急速に降下した(表1を参照のこと)。小さいゲージの針(Ga = 10から14)を平坦底面壁に向けるとともに低流量(~0.1ミリリットル/秒)を採用することにより、管壁剪断応力は1ダイン/平方センチメートル未満に維持することができた。このような構成で、試料解離は衝突フローを制御することにより生じた。衝突フローにより細胞は極めて短時間(マイクロ秒単位)の間に細長い剪断力の炸裂を受けることができた。凝体と衝突する衝突フローが「非線形」である程度は大きくなり、分散を果たすための閾レベルが衝突フローの限界域に近くなる場合がそうである。穿刺吸引法における結着力の強い試料構造(間質組織)は衝突フローの後で標準的な管内フローに当てられることを必要とする場合がある。これは、容器の底面に関連する針位置を制御するためにステッパモーターを使用することにより、自動方式で容易に達成することができた。
【0165】
<<細胞活性化研究>>
細胞試料を破砕する流体条件を判断するための研究の最初の一区切りがついた後で、細胞膜の保全性について細胞凝集塊を解析し(トリパンブルー染色法および生死判定染色法)、細胞アポトーシスについて解析し(細胞透過性カスパーゼ3蛍光生成評価分析法)、更に、細胞活性度について解析した(FOS染色法)。明確な対照例として、MCF−7については細胞生存度の喪失の原因である諸条件は既に周知であった。掻爬された単層中で、細胞核の5%未満がFOS陽性である。FOS陽性の細胞核が15%未満であるというのが、掻爬単層を破砕して小型の凝集塊にする剪断条件である。アポトーシス調査については、細胞を分散させてから半時間から1時間に亘って保温培養することで、分散後のアポトーシス開始を評価することができた。
【0166】
<<緩衝剤の調整法>>
試料分散を向上させるとともに細胞活性化を最小限に抑えるように分散緩衝剤を調整することができる。エチレンジアミン四酢酸(EDTA)を使った細胞外カルシウムのキレート化により複数の細胞を一緒に保有している接合部の解体を容易にすることができた。エチレンジアミン四酢酸(5ミリモル、pH 7.4)に晒した後で再石灰化する処理それだけで単独の細胞刺激となることを検証した。掻爬単層試料の分散中に反応性酸素を生じた結果として細胞活性化を招くことがある。N-アセチル-L-システイン(NAC、5ミリモル)が細胞分散中のFOS蛋白誘導を低減した。最後に、0.2 %(w/v)のプルロニックF68は重合体添加物であるが、異なる細胞膜システム中における細胞膜相互作用による細胞保護作用については既に前段までに披露した。
【実施例10】
【0167】
<<10. 細胞の量>>
400ダイン/平方センチメートルの壁剪断応力を利用した先の実施例と同様に分散処理されたHCT−116細胞およびMCF−7細胞に対して、細胞保護剤を使って核酸を安定化した。キアゲン社の抽出技術を利用してDNAおよびRNAを抽出した。解析に付すのに適正なRNAレベルおよびDNAレベルを達成するのに必要な細胞個数を判定した。細胞から採取されたRNAを評価するのに、無欠RNA個体数評価法(RIN評価法)、光学密度260/280評価法、および、RNAの総マイクログラム量評価法を採用した。このような実験で確認できたこととして、例えば、DNA解析およびRNA解析には10万個を越える数の細胞の試料寸法が適切であることが挙げられる。
【0168】

このような結果は図13および図14においても図表で例示されている。
【実施例11】
【0169】
<<11. 細胞計数>>
先の実施例において分散された試料について(MCF−7およびHCT−116)、細胞計数を検証し、結像室に搬入される細胞懸濁液の1分割量として10マイクロリットルから100マイクロリットルが有効であるとの実証を得た。画像計数値を血球計算装置評点およびコールター製計数装置評点の両方と比較した。凝集塊の解析については、トリプシンおよび単一細胞計数法を利用した完璧な分散を果たすために試料を複数の部分集合に分割する方法を採用することで、画像処理アルゴリズムの有効性を実証した。コールター製計数装置を使って、振り分け機能を採用することで寸法分布を得ることができた。
【0170】
<<細胞核計数培検計画案および画像処理>>
細胞核を蛍光着色処理することの利点は、細胞核が特に大きく、単層培養細胞および懸濁液中浮遊細胞に混じっても容易に識別される分離した細胞物体である点である。細胞分離または細胞溶解分離を実施せずに単一工程で細胞計数を実施するのに有効な画像化方法では、染料は以下のような基準に適っているべきであることを検証した。すなわち、(1)固定化工程−洗浄工程−染色工程−洗浄工程という複雑な培検計画を必要とせずに細胞に適用することができなければならない、(2)低価格のダイオードまたはレーザーで利用できる波長で容易に励起されなければならない、(3)高い信号対バックグラウンド比を生じなければならない、(4)膜透過性SYTO-11およびSYTO-16(インヴィトロゲン社製)などのような即効性細胞染料を生じなければならない。紫外線染料(4',6-ジアミジノ-2-フェニリンドール(DAPI)、ヘキスト33342(Hoescht 33342)など)は上記基準の大半に適っているものの、紫外線源を必要とし、結像システムを小型化して経済効率を高める必要が生じた場合に、フェーズ2の損失となる。着脱自在チャンバー搭載スライド(ラブ・テク(商標Lab-Tek)、チャンバースライズ(商標Chamber Slides)、ヌンク(商品名Nunc)−1ウエルあたりの培養面積0.4平方センチメートル、作業容量マイクロリットル)における画像化処理の前に5分までの期間に亘り10ミリモルのSYTO-11(S7573、励起波長508 nm、蛍光波長527 nm)または10マイクロモルのSYTO-16(S7578、励起波長488 nm、蛍光波長527 nm)中で細胞を保温培養した。アドービ・フォトショップ(5.5版)およびディジタルカメラ(Kontron Elektronik Prog/Res/3012)を付帯させた光学顕微鏡(Olympus)を使ってディジタル画像を得た。目視検査と画像解析ソフト(NIH Image)の両方により画像に評点を付けて細胞核計数処理に付した。この評点を血球計算装置評点およびコールター製計数装置評点の両方と比較した。目標は即時的高精度細胞核計数培検計画案を開発することであり、ここでは、100マイクロリットルの細胞懸濁液を10マイクロリットルの染色溶液に添加してから、5分の保温培養の後に青色励起と緑色蛍光の発光により画像化処理を行った。上述のように選択された2種類の染料が不適当である場合は、SYTOシリーズ製品の中から幾つかの代用品が利用できる。同様に、透過性細胞核染料サイトラックオレンジ(CyTRAK Orange、バイオステイタス・リミティッド(Biostatus Ltd.)社製、励起波長488 nm、蛍光波長615 nm)が上述のような応用例に好適であることを実証した。
【0171】
小型凝集塊中の細胞核を高精度に計数する処理は、細胞単層中または単一細胞が浮遊する懸濁液中の細胞核を計数する処理よりも遥かに困難である。エッジ検出およびより複雑なバックグラウンドが原因で画像解析ソフトに誤差が生じる恐れがある。高精度と一貫性を確保するために、完全なトリプシン・エチレンジアミン四酢酸(EDTA)分散処理により得られた細胞計数値との比較を行うことで、どのような杜撰さが存在しているかを平均細胞集団寸法、細胞集団寸法分布、および、細胞集団の密度と画像面積の関数として測定した。必要ならば、シグナル範囲、バックグラウンド減算、閾値設定、オブジェクト検出、および、粒子計数を確定するために、未決定事項に寸法基準および強度基準を加えるとよい。
【0172】
上述の各実施例は本発明の考え得る実施形態を例示したものである。幾つかの実施例に言及しながら本発明を詳細に図示して説明してきたが、このような実施例は具体例として提示されてきたにすぎず、よって、限定するものではなく、本発明の真髄および範囲から外れることなく上述の実施例に多様な形式変更および細部修正を施すことができることが当業者には分かる。従って、本発明の外延および範囲は上述の具体的な実施例のいずれによっても制限されるべきではなく、添付の特許請求の範囲の各請求項およびそれらの均等物に従ってのみ限定されるべきである。本明細書で使用されている見出しはいずれも、編成のためにのみ提示されたものであって、特にそれと示唆していない限り、本明細書を分割したり何らかの意味を与えるものと解釈するべきではない。
【0173】
本明細書で引例に挙がっている文献は全て、ウエブサイト、雑誌掲載論文、論文要旨、公開済みまたは関連する米国特許出願または外国特許出願、交付済み特許または外国特許、それ以外の文献を含めていずれも、その各々の全体は本明細書で引例に挙げることにより本件の一部を構成しており、引例に挙がった文献に提示されているデータ、表、図面、および、テキストの全てを網羅するものとする。
【技術分野】
【0001】
本発明の実施例は、細胞、細胞凝集塊、または、固形腫瘍を分析する進歩した方法および装置に関するものである。このような方法および装置は、例えば、病理学の分野で有用であり、進歩した細胞処理および分析結果を提供することができる。
【背景技術】
【0002】
従来からの病理学的試料を大量処理するのに、細胞を殺傷することに関与したり試料処理時間が冗長である方法を採用してきた。このような方法は、治療の時点からかなり経てから実験室で実施されるのが一般的である。このような従来からの方法は、治療の時点で生細胞に対する動的生体マーカー法などのような生細胞検査を行うことができないうえに、治療の時点で迅速に試料処理したり分析結果生成を行うことができない。完全かつ即時取得された情報をこのように逸しているせいで、医者は適切な治療管理法を指定することができないか、或いは、少なくとも処理を遅延させてしまい、患者の生活の質に悪影響を及ぼすことになる。従来の処理を幾つかの進歩した実施例と対比させた一例を図9に示した。
【0003】
例えば、腫瘍学者は、治療の標準と特色づけられる、複数薬剤を各種組合わせて使用する方法とか、特定癌について承認を得ているという評判は得ていないがその特定の癌に有効であると実証されている多数の薬剤を使用する方法とかいった多様な治療選択肢を採用することができる。良好な治療成果を得る最も高い見込みを実現する要件として、患者に利用できる最適癌治療を施すこと、および、このような施療指定が診断後に極力迅速に行われることが挙げられる。
【0004】
或る種の癌はゲノムマーカーを利用して容易に同定することができ、癌は1種類または多数種類(通例は多数種類である)の正常な遺伝子が異常な発現をしたものであるという言い方が特徴をより適切に表していると思われるが、そのような癌の全てについて信頼できるゲノムマーカーが入手できるわけではない。癌を特定種類別に診断してから遺伝子発現に基づいて複数の異なる治療戦略の見込みのある効力を評価するのに目下利用できる診断試験には欠点があって、例えば、(1)斯かる試験は血液検査用に設計されたものであって、固形腫瘍を検査するのに適合させるのは容易ではないこと、(2)細胞解離処理などのような固形腫瘍試料の調製方法は、生細胞を処理したり、その後でマーカー発現を測定するのには好適とは言えない場合があること、(3)穿刺生検法などを利用して得られた小型試料は完全な分析を行うのに十分な組織として作用し得ないこと、(4)斯かる試験は生体外で細胞を培養する必要があるうえに、より長い培養期間を必要とし、患者から被験細胞を採取してから細胞を検査するまでに相当な遅延を見込む必要があり、または、これら全部を要件とするため、多様な外的影響がマーカー発現に及ぼされる潜在的可能性を生じてしまうこと、(5)斯かる試験は、発現を異常であると認識して特性を定めるのに重要である多数の遺伝子、多数の燐蛋白質、または、それ以外の多数のマーカーの発現を同時平行式に測定するのには不適となる場合があること、(6)斯かる試験は定量検査ではなく、或る蛋白質が存在していることまたは不在であることが複数遺伝子の相対発現レベルに反するものであると判定するのに原則的には免疫組織化学法に依存していること、(7)試薬および細胞処理条件が厳密に抑制されることなく、検査ごとに、更にまた、検査所ごとにかなりの差異を生じること、(8)斯かる試験は、RNAが不安定であるうえに患者から十分に新鮮な試料を採取するのが実際上困難であるせいで、RNAレベルの解析には不適切であること、(9)斯かる試験は、遺伝子発現解析を実施する前に、例えば、選択された試薬の存在下で、または、選択された試薬の不在時に細胞を固定する処理を含んでいる場合があること等の欠点がある。
【0005】
近年、マイクロアレイ遺伝子発現解析による多様な癌種類の分類に関する研究が公開されている(例えば、ガループ(Golub)ほか著の1999年刊行『サイエンス(Science)』286号531-537掲載論文、バタカルヤエ(Bhattacharjae)ほか著の2001年刊行『米国科学アカデミー(National Academy of Science, USA)会報』98号13790-13795掲載論文、チェンシャン(Chen-Hsiang)ほか著の2001年刊行『生物情報科学(Bioinformatics)』17号の別冊1のセクション316-322、ラマスウォミー(Ramaswamy)ほか著の2001年刊行『米国科学アカデミー会報』98号15149-15154掲載論文などを参照のこと)。遺伝子発現パターンに基づいて行ったヒトの乳癌の或る種の分類も報告されている(マーチン(Martin)ほか著の2000年刊行『癌研究(Cancer Research)』60号2232-2238掲載論文、ウエスト(West)ほか著の2001年刊行『米国科学アカデミー会報』98号11462-11467掲載論文、ソーリー(Sorlie)ほか著の2001年刊行『米国科学アカデミー会報』98号10869-10874掲載論文、ヤン(Yan)ほか著の2001年刊行『癌研究』61号8375-8380掲載論文を参照のこと)。しかしながら、上述の各研究はもっぱら多様な種類の癌についての既存の分類の改良と精査のし直しに主眼を置き、互いに異なる発現をした複数遺伝子の関係に新たな洞察を行ったものとは凡そ言い難い。このような研究は新たな発見を治療戦略と結びつけて癌治療の臨床的成果を進展させるものではないうえに、細胞の処理・解析の既存の技術を向上させ標準化するという問題に対処するものでもない。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】ガループ(Golub)ほか著、『サイエンス(Science)』286号531-537掲載論文、1999年刊
【非特許文献2】バタカルヤエ(Bhattacharjae)ほか著、『米国科学アカデミー(National Academy of Science, USA)会報』98号13790-13795掲載論文、2001年刊
【非特許文献3】チェンシャン(Chen-Hsiang)ほか著、『生物情報科学(Bioinformatics)』17号の別冊1のセクション316-322、2001年刊
【非特許文献4】ラマスウォミー(Ramaswamy)ほか著、『米国科学アカデミー会報』98号15149-15154掲載論文、2001年刊
【非特許文献5】マーチン(Martin)ほか著、『癌研究(Cancer Research)』60号2232-2238掲載論文、2000年刊
【非特許文献6】ウエスト(West)ほか著、『米国科学アカデミー会報』98号11462-11467掲載論文、2001年刊
【非特許文献7】ソーリー(Sorlie)ほか著、『米国科学アカデミー会報』98号10869-10874掲載論文、2001年刊
【非特許文献8】ヤン(Yan)ほか著、『癌研究』61号8375-8380掲載論文、2001年刊
【発明の概要】
【発明が解決しようとする課題】
【0007】
近年の分子生物学および生体化学は100種類を超える遺伝子とその活動の影響を受けた腫瘍細胞それぞれの動向、腫瘍細胞それぞれの分化状態、および、或る種の治療薬に対する腫瘍細胞それぞれの感度または耐性などを解明してきたが、このような遺伝子の状態を薬物治療に関わる臨床上の判断を定常的に行う目的で利用することは、2〜3の例外を除いてこれまで皆無であった。注目に値する一例外として、乳癌においてタモキシフェンなどのような抗エストロゲン剤を使った治療を施すにあたり患者の適否選別にエストロゲン受容体(ER)蛋白質発現を利用する方法がある。もう1つの例外的な具体例として、乳癌においてHer2拮抗薬ヘルセプチンを使うにあたり患者の適否選別にErbB2 (Her2) 蛋白質発現を利用する方法がある(ヘルセプチン(Herceptin)は米国カリフォルニア州サウスサンフランシスコのジェネンテク・インコーポレーティッド(Genentech, Inc.)登録商標である)。しかし、大半の癌について、遺伝子発現の病理は微妙さを増すことがあるうえに、多数遺伝子の発現パターンまたは特定の刺激に反応した遺伝子発現のパターンに関与することがある。
【0008】
癌治療への困難な取組みは依然として、特定治療管理を目標に掲げて腫瘍種類を病理学的に弁別することであり、更にまた、出来るだけ早期に最適治療を見極めて最適成果を得ることである。このため、多様な治療選択肢に対する患者の反応に関する予後、予報、または、その両方を同時に供与する検査が必要である。
【0009】
上述の各種欠点に対処するとともに組織試料を処理して調製する機能を単体の小型装置に統合して実施するにあたり、組織試料の生存力を維持して、組織試料が生存力を喪失する前に、または、生体外複製により培養されなくとも、同じ組織試料を刺激することができるようにする、同じ組織試料から得られた複数の互いに異なる生体マーカー反応を保存することができるようにする、または、同じ組織試料を刺激して尚且つ生体マーカー反応の保存も行うことができるようにするよく管理されて一貫性があるうえに効率的でもある幾つかの処理工程を採用した、固形腫瘍またはそれ以外の細胞凝集塊の生検材料調製装置および生検材料調製方法が必要である。
【課題を解決するための手段】
【0010】
本発明の実施例は、被検体から採取した細胞凝集塊を処理または調製して生組織試料にする方法を目的としている。この方法は、被検体から採取された生細胞凝集塊を水性溶液中に解離および分散させて生細胞凝集塊を含有している少なくとも1分割量の部分標本を第1隔離室内に入れる工程と、任意で、混入細胞を除去することにより標的細胞の残余の混入細胞に対する割合を増大させるようにこの部分標本を高純度化する工程と、任意で高純度化された生細胞を解析に付すために1個以上の第2隔離室内に分配する工程と、分配済みの細胞の細胞解析、分子解析、または、その両方の解析を行えるようにするために分配済みの細胞を安定させる工程とを含んでいるとよい。
【0011】
本発明はまた、或る実施例においては、固形腫瘍から採取した癌細胞を処理または調製する方法を目的としており、斯かる方法は固形腫瘍から得られた癌の生細胞を解離および分散させて少なくとも1分割量の部分試験標本を少なくとも1個の第1隔離室に入れる工程と、任意で混入物を除去するように癌の生細胞を高純度化する工程と、癌の生細胞を解析に付すために1個以上の第2隔離室に分配する工程と、分配済みの細胞の細胞解析、分子解析、または、その両方の解析を行えるようにするために分配済みの細胞を安定させる工程とを含んでいる。
【0012】
更に、本発明の或る実施例は細胞処理用のカートリッジを目的としている。例えば、複数の無菌室が設けられた、癌の生細胞を処理または調製する用途に付されるカートリッジにおいては、無菌室は互いに隔絶されているようにするとよい。他の実施例はまた、細胞を分散させる室、細胞を高純度化する室、および、隔離室である室などから構成された複数の小室が設けられているカートリッジを目的とする。
【0013】
本発明はまた、本発明のカートリッジと解析デバイスから構成されているシステムを目的としている。本発明のカートリッジを含んでいるキットも本発明に包含されている。
【図面の簡単な説明】
【0014】
【図1】図1は本発明のカートリッジの具体的な実施例を示した図である。
【図2】図2はカートリッジ内部に設けられて試料を受容して処理するための具体的な隔離室を例示した図である。
【図3】図3は本発明による具体的な解離プロセスを例示した図である。
【図4】図4は本発明のカートリッジのもう1つ別な実施例を示した図である。
【図5】図5は本発明のカートリッジに設置することができる硝子スライドホルダーの具体的実施例の縦断面図および頂面図である。
【図6】図6は本発明のカートリッジのもう1つ別な実施例の具体的特性を例示した図である。
【図7】図7は本発明のカートリッジの一実施例においてカートリッジの小室のうちの幾つかを互いから隔絶させることができるのを例示した図である。
【図8】図8は本発明のカートリッジのもう1つ別な実施例の具体的特性を例示した図である。
【図9】図9は従来の病理学的試料処理方法(左側)と本発明の具体的な処理方法(右側)との比較例を例示した図である。
【図10】図10は本発明の方法でRNA試料を生成した場合のほうがホルマリン固定・パラフィン埋設プロセスよりも無欠RNA個体数(RIN)が多いことを例示した図である。
【図11】図11は従来の腫瘍試料処理方法が生体マーカーを破損したことにより、利用できる細胞情報が低減する恐れがあることを例示した図である。
【図12】図12は穿刺吸引法(FNA)を利用した吸引法で始まる本発明の試料処理方法を例示した図である。
【図13】図13Aは無欠RNA個体数(RIN)評点を示したグラフであり、図13Bは生成RNAの量をマイクログラム(μg)単位で示したグラフであり、図13CはHCT-116細胞の細胞個数が変動している条件における260/280値を示したグラフである。
【図14】図14Aは無欠RNA個体数(RIN)評点を示したグラフであり、図14Bは生成RNAの量をマイクログラム(μg)単位で示したグラフであり、図14CはMCF-7 細胞の細胞個数が変動している条件における260/280値を示したグラフである。
【図15】図15はMCF-7細胞およびHCT-116細胞が分散してダイン/平方センチメートル(dyne/cm2)単位で変動した場合に細胞集団寸法に及ぼす影響を示したグラフである。
【図16】図16はMCF-7細胞およびHCT-116細胞が分散してダイン/平方センチメートル(dyne/cm2)単位で変動した場合に細胞生存力に及ぼす影響を示したグラフである。
【図17】図17はMCF-7細胞が分散して上皮細胞成長因子(EGF)刺激を受けたことによりFOS蛋白誘導レベルが変動するのを示したグラフである。
【図18】図18はHCT-116 細胞が分散して上皮細胞成長因子(EGF)刺激を受けたことによりFOS蛋白誘導レベルが変動するのを示したグラフである。
【図19】図19はMCF-7細胞およびHCT-116細胞において本発明の方法を利用して腫瘍細胞を集積培養したグラフである。
【図20A】図20Aは本発明の方法を利用して調製したMCF-7細胞に生細胞指標剤を導入した結果を示した図である。
【図20B】図20Bは3時間のホルマリン固定処置を利用して調製したMCF-7細胞に生細胞指標剤を導入した結果を示した図である。
【図21A】図21Aは本発明の方法を利用して調製したHCT-116細胞に生細胞指標剤を導入した結果を示した図である。
【図21B】図21Bは3時間のホルマリン固定処置を利用して調製したHCT-116細胞に生細胞指標剤を導入した結果を示した図である。
【図22】本明細書に記載されている解離技術を利用してMCF-7細胞およびHCT-116細胞を分散させた具体例を示した図である。
【発明を実施するための形態】
【0015】
本明細書に記載されている発明の実施例は、目標に掲げた各種治療と分子診断検査の開発利用を促進する自動自蔵式流体腫瘍細胞処理試験fシステムに関与しているが、これに限定されるものではない。本発明の実施例はまた、斯かるシステムを利用した方法であって、例えば、生細胞に対して生体外で実施することのできる進歩した病理学的処理方法を含んでいる。本発明はまた、本明細書に記載されているシステムおよび方法と併用するためのキットを目的としている。
【0016】
本発明は、固形細胞試料を体外で採集し、取扱い、処理するための、安全、効果的、高精度、正確、再生可能、廉価、コスト効率が良い、効率的、迅速、尚且つ、便利な方法および「カートリッジ式の」システムを提案している。このような方法およびカートリッジは、処理中も試料の生存力を維持して生体マーカーを無欠に保つことができるとともに、任意で、体外刺激により元の試料には存在していなかった各種燐蛋白質およびRNAなどのような生体マーカーを誘発するようにしてもよい。本発明は、完璧な診断細胞学実験室システムと生検後の管理された諸条件で完全無欠な試料と情報管理を提供するものであり、これにより或る検査から次の検査までの間の変化を最小限に抑え、生体混入の危険を最小限に抑え、尚且つ、試料調製プロセスそれ自体が生体マーカーの発現に及ぼす影響を最小限に抑えことができる。本発明の実施例を利用して、目標に掲げた腫瘍治療を容易にすることができるうえに、任意で、細胞計数機能、それ以外の関連解析、または、その両方を具体例とする組織試料の適性評価を行うこともできる。
【0017】
図9に例示されているように、従来の細胞処理技術は、組織処理前にホルマリン固定術を採用し、最終的には細胞をパラフィンに埋設する。この結果、図11に例示されているように、多数の潜在的な細胞情報が「喪失して」しまう。しかしながら、本明細書に記載されているとともに図9や図12などに描かれている進歩した方法は生細胞の自動処理、自動処理済みの生細胞の刺激、および、それに続く、本件後段に記載した各種方法を利用した細胞解析を行うことができる。
【0018】
当業者なら正しく認識することであるが、このような新規な装置、システム、キット、および、方法は臨床現場または研究現場で多数の利点を供することができる。例えば、これらを利用することで試料を遠隔の研究施設に発送する必要無しに、目の前にいる患者に直ちに生検処理を施すことができる。これらを利用することで生検処理をコスト効率の良い態様で標準化および自動化することもできる。本発明は、現行の病理学的処理が許容する以上に細胞についてより詳細な分子情報を提供することができ、これにより、任意で新規な体外における生体マーカー検査および診断検査を利用して、生検に付した細胞(例えば、癌細胞)をより細かく小分類することができるようにしている。本発明の各種利点は、それぞれ一緒に採択することで、治療の時点で迅速な診断を行えるようにするうえに、その後でより有効な患者ごとの固有治療管理計画を立てることを可能にする。
【0019】
本発明の装置、システム、および、方法のために利用される具体例のプロセス(限定するものではない)は、後段により詳細に説明されており、図12のフローチャートに例示されている。このプロセスは、図12に例示されている穿刺吸引(FNA)工程1201などのような方法で細胞凝集塊の試料を採取することで開始される。次に、試料は本明細書に記載されている新規な技術を利用して解離されてから、分散工程1203により複数の隔離室に分配される。試料が興味の対象である細胞とそうではない他の細胞とを混交して含有している場合は、任意で、混入物と興味の対象ではない細胞とを除去することにより、試料を高純度化して、試料中の興味の対象である全部の細胞を集積培養工程1205にまわしてもよい。次に、任意で、試料は体外刺激工程1207を受けるか、またそうでなければ、検査試薬と混合されてから、1分割量ずつの部分標本を新たな隔絶室に入れる工程1209にまわす。これら部分標本も、任意で、実施されるアッセイ次第で、体外刺激を受けるか、またそうでなければ、検査試薬と混合されるようにしてもよい。次に、これら部分標本は興味の対象となる特性について解析される。例えば、顕微鏡解析工程1211に備えて部分標本からスライドを準備するか、または、部分標本はそれぞれ1分割量ずつの細胞が核酸、RNA,および、DNAに溶解分離され、RNAは工程1213で、DNAは工程1215でそれぞれに解析される。解析結果は、穿刺吸引(FNA)の試料提供者である患者の治療管理の編成などの適切な行為を行うことができる研究者または臨床医に連絡される。更に、図11に例示されているように、本明細書に開示されている進歩した方法および装置により、従来の病理学的細胞処理技術中に「喪失され」ていた新情報を研究者または臨床医が得ることができるようになる。
【0020】
<1. 装置、システム、および、キット>
<<A. 装置>>
更に別な実施例では、本発明は、本明細書に記載されている生細胞の処理方法、生細胞の調製方法、または、その両方の方法などにおいて有用な装置またはプラットフォームを提案している。この装置はカートリッジとも称される。本発明の装置の幾つかの実施例が後段により詳細に説明され、図1から図8に描かれている。
【0021】
このようなカートリッジは1個以上の隔離室を備えている。隔離室は何らかの区画、区分、または、それら以外の実利的容器であって、生細胞の試料、固定済み細胞の試料、処理済み細胞の試料、安定化済み細胞の試料、または、それら全処理を完了した細胞の試料を保管することができる。具体例を挙げると、隔離室という用語の具体例としてはウエル、バイアル、管、スライド(例えば、硝子スライド)、プレートなどがあるが、これらに限定されるものではない。
【0022】
本発明の隔離室または区画は以下に列挙する機能のうちの1つ、複数、または、全部に好適である。すなわち、(1)隔壁またはそれ以外の方法により封鎖された小室に生体試料を受容する機能、(2)内蔵収納式注射針を保管する機能、(3)隔壁から取出しができる液体試薬を保管する機能、(4)隔壁内に廃棄物を受容・保管する機能、(5)液体剪断または機械剪断により試料を粉砕する機能、(6)細胞計数機能および細胞視覚化機能、(7)ビーズ分離機能、および、(8)固形樹脂含有機能のうちの1つ、幾つか、または、全部に好適である。
【0023】
カートリッジは各々がその用途次第で1個以上の隔離室を備えているようにするとよい。例えば、カートリッジには1個から約200個までの隔離室が設けられていてもよいし、1個から約100個までの隔離室が設けられていてもよいし、または、1個から約50個までの隔離室が設けられているようにしてもよい。或る実施例では隔離室の数は約24、約48、または、約96である。
【0024】
或る実施例においては、カートリッジには1個以上の第1隔離室と1個以上の第2隔離室が設けられている。カートリッジには細胞の試料を保有するための第1隔離室が設けられているようにしてもよい。このようなカートリッジは、分散された1分割量ずつの細胞試料の部分標本を保有する1個以上の第2隔離室を特徴としているようにしてもよい。或る実施例においては、第2隔離室は、分散された1分割量分の細胞の部分標本が添加される前に、そこに所定量の検査試薬を包含しているようにしてもよい。図2は、試料を受容して処理するためにあってもよい具体的な各種隔離室を例示している。
【0025】
或る実施例においては、本発明は、複数の区画(例えば、隔離室)が互いに分離して設けられているカートリッジを提案している。図7に例示されているように、区画は分離して設けられ、その内側の試料は複数の相互に異なる分析検査の用途に付すことができる。例えば、1区画がDNA解析のために回され、また別な区画はRNA解析のために回され、更にもう1つ別な区画は顕微鏡解析のため、更にもう1つの区画は免疫組織化学解析のために回されるようにしてもよい。或る実施例では、例えば、カートリッジに設けられた第2隔離室は第1隔離室とは別個に設けられていてもよい。
【0026】
本発明の装置は加熱部材を備えており、カートリッジの温度を摂氏約30度から40度まで、摂氏約36度から約38度まで、またはそれ以外の温度範囲の所望温度に維持することができる。
【0027】
本発明の装置は、装置内のカートリッジ、細胞試料源、または、その両方を識別するバーコードまたはそれ以外の手段を有しているようにしてもよい。カートリッジを識別するバーコードまたはそれ以外の手段を使って、試料識別、患者の安全、または、その両方を容易にすることができる。このような識別手段はコンピュータによるデータ保管システム、自動細胞処理システム、アッセイ、携帯用情報端末(PDA)、または、それらの各種組合わせと相互作用するようにしてもよい。バーコードが設けられたカートリッジの具体的実施例が図4に描かれている。
【0028】
例えば図2Fに描かれているように、装置の或る実施例には細胞計数機構が設けられていてもよい。このような機構は自動システムでも手動システムでも、いずれでもよい。例えば、細胞計数機構は血球計またはセロミター(登録商標Cellometer、ネクセロム・バイオサイエンシズ・エル・エル・シー(Nexcelom Biosciences, LLC)から購入可能)でもよいが、ディジタル計数装置または光学計数装置が使用される見込みである。当業者なら正しく認識することであるが、上記以外の細胞計数手段も当該技術で周知であり、本発明と併用するようにしてもよい。
【0029】
本発明のいずれの実施例のカートリッジであれ、1個以上のモジュールまたは1個以上の隔離室が設けられて、そこに樹脂、試薬、溶剤、それ以外の物質が保有されるようにしてもよい。モジュールは特定の目的で使用される1個の隔離室または1組の複数の隔離室のいずれであってもよい。例えば、多数の操作(例えば、溶解分離と染色など)が特定の検査に関与している場合は、その検査の「モジュール」の一部として2個以上の隔離室を利用してもよい。例えば、1個以上の隔離室が樹脂に核酸、蛋白質、天然重合体、合成重合体、小型分子などを付着させて保有しているようにしてもよい。1個以上の隔離室が緩衝剤、分子生物酵素、核酸または蛋白質などの生体分子、小分子化学物質などの液体を保有しているようにしてもよい。1個以上の隔離室がカートリッジ内可溶化処理用の乾燥試薬を保有しているようにしてもよいが、その場合、乾燥試薬の具体例としては核酸、蛋白質、天然重合体、合成重合体、小型分子などが挙げられる。
【0030】
或る実施例においては、カメラまたはそれ以外のディジタル結像装置がカートリッジの一部となっているか、または、カートリッジと併用される。従って、本発明のいずれの実施例のカートリッジであれ、10マイクロリットルから500マイクロリットルの間の量の試料に対して細胞視覚化とディジタル画像化による細胞計数処理を行うことができるようにした画像化モジュールを備えているようにしてもよいが(図2Fを参照のこと)、上述の量の試料は容積流動または毛細管作用によって画像化モジュール内に分配される。結像装置を利用して、例えば、蛋白質局在化データとなるような試料中の細胞成分などの試料写真を撮影するようにしてもよい。
【0031】
本発明のいずれの実施例のカートリッジであれ、直径が10ミクロンから500ミクロンである微細通路により細胞を通過させる流体モジュールが設けられて、10マイクロリットルから1000マイクロリットルの量を利用して100ダイン/平方センチメートルから800ダイン/平方センチメートルの壁剪断応力を生じるようにしてもよい。
【0032】
本発明のいずれの実施例のカートリッジであれ、免疫除去モジュールまたは免疫除去隔離室が設けられているようにしてもよい。このような免疫除去モジュールまたは免疫除去離室は磁気ビーズまたはそれ以外の方法を利用するとよい。例えば、磁気ビーズ製品はノルウエイのオスロに居所を置くダイナル・バイオテク(Dynal Biotech)から購入できる。このような実施例は方法解説部分でより詳細に説明している。
【0033】
本発明のいずれの実施例のカートリッジであれ、生体試料を含有する、または、生体試料を含有するように設計された1個以上のモジュールまたは1個以上の隔離室が設けらているようにしてもよく、斯かる生体試料の具体例として、穿刺吸引生検試料、コア生検試料、生体液試料(唾液、血液、精液、膣液など)、有機生物体由来の採取組織、細胞培養試料などがある。このようなモジュールは第1隔離室とも呼ばれ、例えば、図2の(A)および図4に描かれている。
【0034】
更に別な実施例においては、本発明は、本明細書に記載された方法および装置で使用するのに好適で、例えば、複数の個別の自蔵モジュールが設けられているようなカートリッジを提案しており、斯かるモジュールは細胞処理に好適な培地を保有しているとともに各々が隔壁またはそれ以外のシール機構によって封鎖されており、隔壁またはシール機構は針などの管による副側路形成や穿孔を行うことができるとともに管を取り出した際に再封鎖を行うことができる。或る実施例においては、液体試薬、生検試料、先鋭部材(すなわち、針)などを全部一括してカートリッジまたはカートリッジを封入した解析デバイスに投入したりそこから取出したりするのが十分可能なモジュールまたは隔離室が設けられており、この場合、解析デバイスは解析作業中の生物災害封じ込み作用を果たしている。モジュールには、細胞計数または細胞生存度アッセイなどの特殊検査や特殊活動を実施する試薬および装置を付随させた多数の隔離室が設けられている。上述の実施例は、例えば、図1、図2、図4、図6、図7、および、図8に描かれている。
【0035】
図5の参照番号501Bで示されているように、本発明のカートリッジは階段形状部501Aに複数スライドが積載される構成になっており、階段形状部のおかげで、これらスライドは細胞物質を収容した後で接近して取出すのに単に手動手段またはロボット手段を使って効率よく利用することができるようになる。図5は階段形状部501A、501Bを例示した断面図である。従って、更に別な実施例においては、本発明は、例えば硝子スライドなどのような多数の平坦な基板が階段状に配置されたホルダーを備えている装置を提案しており、斯かる装置においては、ホルダーは基板が左右上下に移動するのを抑制している。好適な基板としては、硝子スライドなどのような平坦な矩形板片、金属プレート、または、マイクロ流体装置などが挙げられるが、これらに限定されない。基板の厚みは0.1 mmから3 mm、縦横の寸法は2 cmから3 cmの幅に7 cmから9 cmの長さ、または、これら全部の条件を備えているとよい。当業者には分かることであるが、上記以外の基板または隔離室をカートリッジ上に同様の態様で配置してもよいが、そのような各種実施例も本件の範囲に含まれる。
【0036】
或る実施例においては、カートリッジ上のホルダーには底面部と上蓋部が設けられており、これら両部分は各々に階段が設けられて、複数の個別の基板を階段状に積載したものがホルダー内に設置され、または、ホルダーに相関的に位置決めされて、ホルダー内で、または、ホルダーに相関的に移動することがないように図っている。ホルダー内に保管されている間は、基板の遠位端は最も低い部位が積載部を越えた先まで突出している(図5の501Bを参照のこと)。この遠位端は機能上の特徴を印刷したもの、ウエル、または、刻印が1個以上設けられているようにしてもよい。特徴を印刷したものは、使用済み時または使用前に基板を識別するための付箋であってもよい。或る実施例では、ホルダーには上蓋が設けられており、基板の遠位端は露出状態になっており、上蓋の1個または複数個の隔壁を通り抜けて接近することができるようになっている。ホルダーはフレームの中に出し入れ自在であり、例えば、国際分子生物科学協会(SBS)推奨規格の設置面積を有するフレームへ出し入れ自在であるようにするとよい。任意で、ホルダーは底面に1個の小さな穴または複数の穴が設けられているようにしてもよい。
【0037】
図5は具体的なホルダーの頂面図である。スライドの積載部は、自動化用途または手動化用途に付すのに理想的なシステム構築をしている標準的な行列間隔設定に従って、上部から特定位置の認識が行えるようになっている。ホルダーが備えている上蓋には1個の基板ごとにその真上に隔壁が設けられており、真上から1個の基板ごとに個別の特定位置を割当てている。例えば、ホルダーにおいては、1個の基板ごとの識別できる特定位置の真上に1個のO字型リングまたはガスケットにより封鎖可能な密室が設けられているようにしてもよい。このようなO字型リングまたはガスケットにより封鎖可能な密室は所望に応じてどのような形状であってもよいが、例えば、円形、矩形、または、正方形であってもよい。
【0038】
所定の態様でホルダーと多数基板を設置することにより、ピペット、注射針、または、ピン型ツールを使って1ナノリットルから0.5ミリリットルまでの範囲の量の流体試料を基板に並列分配することができるようになる。或る実施例では、ホルダーは流体分配中に基板が左右方向または上下方向にずれるのを抑制しているとともに、流体分配中に基板が移動するのも抑制している。他の実施例においては、ホルダーにより基板は上下方向に回転するのは許容されるが、左右方向に移動するのを抑制されている。このような柔軟性により、多様な方法および多様なシステムを利用して個々の隔離室への並列流体搬入とそこからの並列流体搬出を自動または手動で行うことができるようになる。
【0039】
或る実施例においては、ホルダーの分解は上蓋の部分を取り外すことで行われ、底面部はホルダーの底面部に設けられた穴を突き抜けている突出位置に在るスタンドに載せて置くことができるようになっている。基板は本発明特有の態様でスタンド突出部に置かれた状態で差し出され、人の手で、または、ロボット型把握ツールにより連続して把握動作を行えるようになっている。これにより基板を連続して取り外すことができるようになり、例えば、最下位のスライドを真っ先に取り外して最後に最上位スライドを取出すことができるため、スライド上に堆積させた試料を基板が掠めて切り崩す事故を回避することにより、スライド標本式の細胞物質を安定して搬送することができるようになる。上述のホルダーの各種実施例を保有しているカートリッジの具体的な分解図が図6および図8に開示されている。
【0040】
流体試料は自動システムまたは手動のいずれで基板に分配されてもよい。或る実施例においては、流体サンプルは所定の順番で連続して基板に分配される。好適な流体試料として、各種の溶液、エマルジョン、懸濁液、重合体含有混合液などが挙げられるが、これらに限定されない。例えば、流体試料は各種の生物学的物質または化学物質であって、例えば、小型有機分子または小型無機分子、蛋白質、核酸、細胞、粒子、揮発性溶剤、不揮発性溶剤、重合体、定着剤などであればよいが、これらに限定されない。
【0041】
更に別な実施例においては、本発明は、本発明のカートリッジで有用となるウエルプレートを更に提案している。目下のところ、各構成部材(導通管、密封管、注射器、ピペット先端具など)を適所に固定することができるようにすることでプレートが斜交いまたは上下逆にされても構成部材が適所から脱落することがないようにしたウエルプレート技術が必要である。更に、ウエルプレート技術により、標準的な(デカルト空間内)ピペットツールを使用して固定済み構成部材を取外して使用してから元の固定位置に戻すのに、ピペットツールに取り付けられた先端具排出装置さえ必要とせずに行えるようになる。或る実施例では、本発明の狙いは、平坦面に多数のウエルが設けられているウエルプレートを製造するにあたり、ウエルプレート上の互いに隣接する2点の位置(「2重ウエル」と呼ぶ)がそれら2点の間に介在している空間によって接続されて、構成部材を左右方向に移動させることができるようにすることである。
【0042】
上述の構成部材は、導通管、密封管、隔壁が設けられた管、透明管、何らかの容器、注射器、針、刃、ピペット先端具などであればよい。或る実施例では、この構成部材は、固定機構を通り抜けるのに好適な厚みの正方形、円形、または、それ以外の形状の物質の剛性部材片を備えており、固定ウエルの固定機構の形状と一致している。
【0043】
2重ウエルプレートの或る実施例においては、2重ウエル(「固定ウエル」と称する)の互いに隣接し合う第1位置として複数の小型タブを含んでおり、これらタブにより各構成部材を適所に固定して移動できないようにし、とりわけ、プレートが上向きである場合に構成部材が上下方向に引き出されるのを阻止することができる。このような2重ウエルプレートには従属ガスケットを有している固定ウエルが設けられており、斯かるガスケットは、構成部材が固定ウエル内に固定されてガスケットが固定された構成部材の移動を阻止している間に限って一部が圧搾される。
【0044】
或る実施例においては、上述の構成部材はツール(例えば、ピペットまたは注射器)によって特定位置割当てができる「取付け部材」を備えており、この場合、取付け部材(例えば、ルアーロック)により構成部材は上記ツールと気密嵌合状態になることができる。上記ツールは固定ウエル内に固定されている構成部材の上に載せられてから構成部材を押下げることで更にガスケットを圧搾することができるが、これにより、構成部材を適所に置くことで2重ウエルの介在空間内で2重ウエルの第1位置(固定ウエル状態)から2重ウエルの第2位置(「解放ウエル」と称する状態)まで左右方向への移動を行えるようにすることができる。或る実施例においては、この構成部材はツールによって上下方向に移動させられると解放ウエルへの出入りを自由に行うことができる。ツールは構成部材を固定ウエルの十分内奥まで搬入することができ、ウエルプレートが表面に係留されるとツールがウエルプレートから垂直方向に離れる方向に移動することにより、構成部材を固定ウエル内に固定したままでツールから構成部材を切り離すことができる。
【0045】
上述のツールとプレートは各々がコンピュータ制御のガントリーシステム上に搭載されており、ツール、プレート、または、その両方がデカルト座標(x, y, z)空間内を移動することができるようにすることにより、ツールが構成部材を固定ウエルに搬入してから固定ウエル内に構成部材を放置し、固定ウエル位置で構成部材を乗せてから構成部材を解放ウエル位置まで移動させ、解放ウエルから構成部材を取出して、更に構成部材をウエルプレートから放免することができるようになる。このような装備によって、ツールが構成部材を解放ウエルに搬入してから、先端具排出装置により構成部材を解放ウエル内に放置することができるようにしてもよい。
【0046】
上述のツールとプレートを利用したコンピュータ制御のシステムの或るものは、角度運動(シータ軸中心)を採用する必要がないように構築されているため、構成部材がウエルプレートに存在したままでも、または、構成部材がウエルプレートから取外されていても、いずれの場合であれ、構成部材をウエルプレートに対して相関的に位置回転して配向し直しをするのを回避することができる。
【0047】
或る実施例においては、2重ウエルを利用して、試料から混入物を除去するように予め設計されている所定の経路を通って液体を流動させることができるようにしている。このような2重ウエルシステムは、例えば、図2においてはウエルCおよびウエルDとして例示されている。
【0048】
<<B. システム>>
本発明の狙いは、本明細書に記載されているカートリッジおよび方法を利用するシステムでもある。例えば、システムは本発明のカートリッジを個別的にまたはキットの一部として1個以上備えているとともに、カートリッジと相互作用して少なくとも1つの解析結果を得ることができるようにした解析デバイス(本明細書では解析装置とも称する)を備えている。例えば、斯かるシステムは治療中に使用して患者の医療診断を得ることができる。
【0049】
従って、本発明の或る実施例の狙いは複数の個別モジュール(例えば、複数の隔離室)が設けられたカートリッジにおいて各種操作を実施するための解析デバイスであり、この場合、解析デバイスは1個以上の注射器用の1個以上のホルダーを備えており、注射器は中空針を備えているとともにカートリッジが配置されているプラットフォームの真上で配向されて、針の尖点をカートリッジの個別モジュールに向けて当てるのにコンピュータ制御の運動制御によるデカルト座標システム(x, y, z)を採用することでカートリッジのモジュールから内容物を吸引したりモジュールに内容物を分配することができるように図っており、モジュールは各々に針で刺し通すことができる隔壁が設けられているが、そうでない限り、隔壁はモジュールの内容物を環境から隔絶している。これらカートリッジの或る実施例の態様が図1、図4、および、図8に描かれている。或る実施例においては、カートリッジによって調製された注射器またはツールをホルダーが持ち上げることができるようになっている。
【0050】
解析デバイスは、本発明のカートリッジを受容する手段を備えている。例えば、スロット、開口、穴、または、それ以外の、カートリッジを受容することができる領域を挙げることができる。或る実施例においては、カートリッジを受容手段内に設置完了すると、扉が閉まって受容手段を封鎖することにより、解析デバイス内にカートリッジを完全に封入する。このような扉閉鎖は手動で実施されてもよいし、自動であってもよい。このような完全密封実施態様が特に有用と言い得るのは、潜在的生物災害を撒き散らすのを防いでいる点、またそうでなくとも、研究室や臨床環境に放散させてしまうのを回避している点である。
【0051】
或る実施例においては、解析デバイスおよびカートリッジを利用するためのシステムは真空設備、空気供給設備、天然ガス設備を必要とせず利用もしないが、更に、試薬給送ライン(処理液流、分析用試薬流、および、廃棄物流)とそれぞれの付属ボトルも全く無用である。すなわち、デバイスは完全自蔵式である。
【0052】
このようなシステムで使用されるカートリッジ、或いは、単独で使用されるカートリッジも自蔵式であってもよい。これは、手動であれ自動システムを利用するのであれ、いずれにせよ、所望のアッセイを実施するのに必要なあらゆる必需ツール(例えば、ピペット先端具など)と試薬(例えば、検査試薬、顔料、または、それ以外の化合物)をカートリッジが事前装填した状態になっているということを意味する。例えば、カートリッジは癌療法のパネル(例えば、プレートに設けられたウエルなどの隔離室ごとに1療法ずつ)と試料を解離して複数のウエルに分散させるのに必要なあらゆるツールとを事前装填しているようにしてもよい。
【0053】
本発明のシステムはカートリッジのモジュールの特定位置を割当てることができる内部画像化機能を備えているようにしてもよい。このシステムを利用してデータを生成し、生成データをユーザーまたは他の装置に出力することができる。
【0054】
解析デバイスは、試料に対して検査が実施されている間も細胞生存力を保つための温熱培養に必要な各種構成部材を備えているようにしてもよい。このような解析デバイスの培養部は1個以上のカートリッジを保有しており、任意でカートリッジは所定の順序に配置される(例えば、試料採収時期に基づく時間順など)。
【0055】
前述の各種解析デバイスのいずれも、カートリッジのモジュールに試料識別子を付着させ、試料情報を伝達し、更には、通信ラインにより処理情報を他の装置に転送するかまたは検査を実施しているユーザーのために結果を表示することができる。
【0056】
<<C. キット>>
本発明はまた、本発明の装置を包含しているキットを目的としている。具体的なキットでは、本明細書に記載されている1個以上のカートリッジが1個の容器に梱包されている。キットは使用上の指示書きを印刷したもの、試薬、緩衝剤、分子指標剤、後段で説明するような1種類以上の検査試薬、ピペットまたは針などの解離または分配用のツール、および、後段で説明する方法を実施する際に有用となる上記以外の物品を更に含んでいるようにしてもよい。
【0057】
或る実施例においては、キットは当該技術で周知の方法を利用して殺菌されてから、無菌状態を保つ態様で梱包される。キットは個別キットとして販売されてもよいし、多数を一括梱包したセットとして販売されてもよい。キットはまた、包装物の中身を誰かにいじくられることがないように設計されるか、または、そのような事態が生じた場合に、それを表示する設計にされるか、いずれかの設計にされているとよい。
【0058】
キットは、本明細書に記載されているような、自動装置を使用するよりはむしろ手作業で利用することができる解析用カートリッジを包含しているようにしてもよい。この場合、検査を遂行する、または、カートリッジの特定目的を遂行するのに必要な試薬と器具がキットの一部として提供されるようにするとよい。斯かる器具としては、例えば、注射針やピペットなどがあるが、これらはカートリッジに事前装填されていてもよいし、或いは、カートリッジの外側に置かれて、キットの一部として提供されるようにしてもよい。他の実施例においては、器具はユーザーが準備するようにして、キットの一部に含まれていないようにしてもよい。同様に、キットと併用される検査試薬は、カートリッジの特定の隔離室内に事前装填されているようにしてもよいし、或いは、ユーザーの実用に適合するようにカートリッジの外側に梱包されているようにしてもよい。上述の各実施例によるキットは、1回きりの検査用の1個のカートリッジとして梱包されてもよいし、多数回の検査用に装填または準備された1個のカートリッジとして梱包されてもよいし、或いは、多数回の検査用の多数カートリッジとして梱包されてもよい。
【0059】
任意で、キットは、カートリッジやそれ以外の試薬などの必需品を適性に使用する指示書きを、本明細書に記載されているようなアッセイまたは方法の一部として包含していてもよい。例えば、キットはお知らせまたは印刷した指示書を含んでいるようにしてもよい。このような印刷した指示書は、医薬品または生体学製品の製造、使用、または、販売を管理指導する政府機関によって規定された形式を呈しているようにするとよいが、そのような通知は、本明細書に記載されているアッセイ、方法、および、装置から得られた情報を利用して扱うことができる症状を診断または治療するための人的管理について、製造、使用、または、販売を管理指導する政府機関の承諾を反映したものである。或る実施例においては、キットは、細胞を処理する目的でキットを使用する際の情報を提供する印刷物、或いは、細胞を処理する目的でキットを使用する際の情報を提供する事前記録媒体装置を更に含んでいるようにしてもよい。
【0060】
「印刷物」は、例えば、本、冊子、パンフレット、ちらし等のうちのいずれかであるとよい。印刷物は、本発明の方法に従って細胞を処理するための実験評価分析書、培検計画案、または、その両方を説明しているようにするとよい。考えられる様式として、段階的指示、箇条書きリスト、よくある質問(FAQ)リスト、図表などがあるが、これらに限定されない。更に、供与される情報は、写真、図画、または、これら以外の表象を利用した原文に典拠しない表現で例示されているようにしてもよい。
【0061】
「事前記録媒体装置」とは視覚媒体装置のことであり、例えば、ビデオテープカセット、DVD(ディジタルビデオディスク)、フィルムストリップ、35ミリ映画、または、それ以外の何らかの視覚媒体装置であるとよい。これに代わる例として、事前記録媒体装置は対話型ソフトウエアアプリケーションであってもよいが、その具体例として、CD−ROM(コンパクトディスク型リードオンリーメモリ)やフロッピー(登録商標)ディスクなどがある。これに代わる例として、事前記録媒体装置は、例えば、レコード、オーディオカセット、オーディオコンパクトディスクなどのようなオーディオ媒体装置であってもよい。事前記録媒体装置に保有されている情報は、本発明の方法に従って細胞を処理するための実験評価分析書、培検計画案、または、その両方を説明しているようにするとよい。
【0062】
<2. 方法>
本発明は細胞試料を処理する新規な方法を目的としており、特に、臨床現場または研究現場で使用することができる細胞凝集塊または固形腫瘍を処理する新規な方法を狙いとしている。このような方法は、被検体から得た癌の生細胞を水性溶液中に解離・分散させて少なくとも1分割量の部分検査標本にして第1隔離室に入れる工程を含んでおり、任意で、混入細胞を除去することにより標的細胞の残余の混入細胞に対する割合を増大させるようにこの部分標本を高純度化または操作する工程と、任意で高純度化された癌の生細胞を解析に付すために1個以上の第2隔離室内に分配する工程と、分配済みの生細胞を安定させることで分配済みの細胞の細胞解析、分子解析、または、その両方の解析を行えるようにする工程とを含んでいるとよい。或る実施例においては、安定化された分配済みの細胞は生細胞でもよいし死細胞でもよいが、これは所望の結果と興味の対象である細胞アッセイ次第である。
【0063】
本発明のまた別な実施例は、固形腫瘍から採取した癌細胞を処理または調製する方法を含んでおり、斯かる方法は固形腫瘍から得られた癌の生細胞を解離および分散させて少なくとも1分割量の部分試験標本を少なくとも1個の第1隔離室に入れる工程と、任意で、混入物を除去するように癌の生細胞を高純度化または操作する工程と、高純度化された癌の生細胞を解析に付すために1個以上の第2隔離室に分配する工程と、分配済みの細胞の細胞解析、分子解析、または、その両方の解析を行えるようにするために分配済みの細胞を安定させる工程とを含んでいる。
【0064】
本発明の方法は、生細胞を迅速に処理することができるようにする。細胞は生きた状態で最小限の細胞活性化または最小限の応力で処理される(例えば、環境応力、温度誘導応力、代謝応力、化学誘導応力など)。「最小限の細胞活性化または最小限の応力」という語は、刺激と比較して、細胞シグナリングのバックグラウンドノイズ変動量を最小限にすること、および、細胞応力経路の変化を最小限にすることと定義される。例えば、図17で分かるように、解離、分散、または、その両方処理の前後の細胞へのFOS蛋白(または、C-FOS)誘導を比較することで、FOSまたはそれ以外の早期反応遺伝子もしくは生体応力指標物質の誘導が最小限になる(3倍から5倍)になるのを、刺激を与えられた試料(上記物質が20倍から30倍増量する)と比較して示すことができる。
【0065】
本発明の方法のもう1つ別な利点は、元の試料中に存在する極めて少数の細胞を使用するだけでよいことである。例えば、或る実施例においては、処理された細胞凝集塊または固形腫瘍の総数は1×103個から1×107個の間である。
【0066】
本発明の方法はまた、迅速な試料処理を行えるようにする。或る実施例においては、分配済みの生細胞の安定化は、被検体から試料を得た後、約1時間以内、約2時間以内、約3時間以内、または、約4時間以内に完了する。このような驚くべき短い処理時間により細胞培養の必要性を排除しながら、細胞生存度は、例えば、約50%を越える、約60%を越える、約70%を越える、約75%を越える、約80%を越える、約85%を越える、約90%を越える、または、約95%を越える高い割合に維持することができる。或る実施例においては、細胞生存度の割合は約70%または約75%である。「約」という語は、例えば、百分率などのような数に関連づけて使用されている場合は、その数値プラスマイナス10%の増減幅を意味している。例えば、「約60%」という語は54%から66%の間を意味している。
【0067】
<<A. 試料採収>>
本明細書に記載されている各方法で使用される試料は多様な方法で得ることができる。試料は、哺乳類(例えば、ヒト)またはそれ以外の生きている有機生物体などのような被検体から採取された生細胞であればよい。具体的には、臨床現場で人間患者から解析を目的として採取された生検材料であって、最終的には、適切な臨床診断と治療方針を判断するのに役立てるために利用されるものであればよい。
【0068】
或る実施例の試料は、凝集状態であれ解離状態であれ、研究現場または臨床現場における興味の対象である何らかの群細胞または単一細胞であればよい。試料の具体例を挙げると、固形腫瘍は元より、トリプシンを使用するといったような、本明細書に記載されているものとは異なる手段を利用してリンパ腫または細胞塊を解離した個々の単一細胞でもよい。このような試料は既存の細胞株、異種移植片、または、臨床診断に付す目的とは異なる理由で検査される患者試料に由来するものとなる可能性がある。このような試料は解析に供されて、細胞と特定の検査試薬に対してそれぞれの細胞が示す反応とを更に特徴づけることができる。このような適用例は、新規な調製剤を識別したり既存の調製剤の投与を改善する目的で、薬品開発と分析評価法選別作業の一部として有用である。
【0069】
或る実施例においては、本明細書に記載されている方法は、どのような種類の解離細胞または解離腫瘍細胞とでも併用することができる。例えば、本発明の方法は癌種または肉腫を検査して処理することができる。本発明の方法を利用して検査することができる具体的な癌としては、大腸癌、膵臓癌、乳癌、卵巣癌、前立腺癌、扁平上皮細胞癌、子宮頸癌、肺癌、小細胞肺癌、腎臓癌、肝臓癌、脳腫瘍、皮膚癌、膀胱癌などが挙げられるが、これらに限定されない。このような各種癌はヒト、ヒト以外の哺乳類、または、ヒト以外の哺乳類(例えば、マウス)から除去されたヒト癌細胞の異種移植片に由来するものである。
【0070】
或る実施例においては、組織試料は固形腫瘍の一部、または、全腫瘍である。本発明で使用する腫瘍細胞を含んでいるこのような組織試料は、例えば、患者から生検材料を採取する等といったような、当該技術で周知の何らかの手段により得ることができる。本発明で採用することができる好適な生検法としては、切開生検、コア生検、パンチ生検、穿刺吸引生検のほかに、切除生検などが挙げられるが、これらに限定されない。或る実施例においては、生検材料は腫瘍の穿刺吸引術(FNA)によって採集される。
【0071】
穿刺吸引(FNA)生検は細い針を使って実施されるが、針は注射器に取り付けられている場合もあれば、単独で使用される場合もある。穿刺吸引生検すなわちFNAは、本発明においては、癌試料を得るために採用される。穿刺吸引生検は経皮(皮膚を貫通させる)生検法であってもよいし、或いはこれに代わる例として、気管支、食道、胃、または、腸などの器官の管腔を貫通させる生検法であってもよい。穿刺吸引生検は、通例は、ファインゲージ針(21ゲージまたはもっと細い針で、22ゲージまたは25ゲージなど)を使って達成される。穿刺領域がまず洗浄されてから、普通は、局所麻酔で麻痺状態にされる。針は興味の対象となる器官または組織の領域に穿刺される。針を刺した後、注射器を使って真空を設けるか、これに代わる例として、針の内部の毛細管作用のみを利用するようにしてもよいが、何度も針を刺し抜きする動作が実施される。採取される細胞は針の管腔内に入り込み、場合によっては、組織を刺し通した時に針の斜面の微細標本抜取り作用により針の円筒中心部に入り込む。通常は3個乃至6個の別個の試料が作られる。リンパ節や肝臓などの癌の転移部位は穿刺吸引生検のよい候補となる。穿刺吸引処置は、通例、超音波画像処理法またはコンピューター断層撮影法(CT)を採用して行われる。
【0072】
コアニードル生検(コア生検)は、小型の中空針で皮膚を貫いて器官の中に針を挿入することにより実施される。次いで、針は細胞層の内部に進入させられて、試料または標本を取出す。針は切断用先端部が設けられて組織の試料を除去するのを助ける設計になっている。コア生検は、組織試料を除去するのを支援するのに、バネを装填した銃型装置を使用して実施されることが多い。コア生検は、通例は、CT画像処理、超音波、または、マンモグラフィーなどの画像誘導下で実施される。針は手で刺すか、または、試料採取装置の支援で刺すか、いずれかの態様で行われる。十分な組織を得るために何度も挿入されることが多く、多数の試料が採取される。コア生検は、真空装置支援式の吸引法(真空支援生検)である場合がある。この方法により、1度しか針を挿入しないのに多数の試料を抜き取ることができる。コア生検とは異なり、真空支援式生検探針は、小さな皮膚の刺し傷から組織の中に1回のみ挿入される。試料採集用の針穴(開口)の回転を利用しながら、吸引支援を受けて多数試料が採取される。従って、コアニードル生検または真空支援式ニードル生検を本発明に採用することで、組織試料を採集することができる。
【0073】
内視鏡生検は、試料採集を目的として本発明に採用することができるありふれたタイプの生検法である。内視鏡生検は、試料採取器具と一緒に体内に挿入される内視鏡(体内を視認するための光ファイバーケーブル)によって行われる。内視鏡により、興味の対象である器官の内側の領域を直接視認することができるようになるうえに、試料の内部を貫いて延びている長いケーブルに取付けられた鉗子を使って少量の組織を採取し、または、切り取る。内視鏡生検は、例えば、胃腸管(消化管内視鏡検査)、膀胱(膀胱鏡検査)、腹腔(腹腔鏡検査)、関節腔(関節鏡検査)、胸部中間部(縦隔鏡検査)、気管および気管支系(咽頭鏡および気管支鏡検査)などに対して実施されるが、いずれも天然の肉体開口部または小さな外科手術切開部を通す。内視鏡超音波誘導式穿刺吸引生検法も肺、縦隔リンパ節、膵臓、肝臓などに対して、経食道アプローチ、経消化管アプローチ、経十二指腸アプローチなどの経路を利用して実施することもできる。
【0074】
癌試料を採集する目的で、表層生検が本発明に取り入れられてもよい。この技術は組織または器官の表面から試料抽出する、または、それらの表面を掻爬することで細胞を抜き取る処理に関与している。表層生検は皮膚の小片を抜き取る目的で実施されることが多い。
【0075】
<<B. 細胞の解離・分散>>
処理用に採取された試料は、細胞を互いから分離してから(凝集している場合は)分離した細胞を分散させて1分割量の部分標本ごとに本明細書に記載のカートリッジまたはそれ以外の好適な容器に入れる。このようなプロセスは、分散工程、計数工程、生存度評価検査、または、これらの各種組合わせを含んでいる多数の工程から構成されているとよい。
【0076】
外科手術で切除された腫瘍に由来する試料と比較した場合、本発明の方法で使用される試料は比較的少数の細胞(例えば、腫瘍細胞)しか含有していなくても済み、本明細書に開示されている各方法無しには、大半の現行の分子診断技術においてはこのような少量細胞しか含まない試料の利用が制限されてしまう場合がある。更に、固形腫瘍由来の穿刺吸引試料または他の方法を利用して採取された固形腫瘍細胞は極度に大きな塊の細胞(細胞数にして500個を越える)を含有していることがあり、多数の検査用隔離室に試料を均一に分配するのを阻害してしまう恐れがある。
【0077】
細胞を殺傷せずに、または、細胞内の応力反応経路を過度に活性化させてしまわずに、上述のような細胞を解離させて分散させる処理は、厳密な方法および厳密な技術を必要とする細心の注意を要するプロセスである。本件で採用されているように、解離手段は細胞を分離させたり細胞のほぼ均質な試料を供与する血用として、複数の細胞を含有している試料を分散させて多数の比較的均一な試料を生じることができるような態様を取っている。例えば、内皮細胞などのような付着依存性細胞においては、大動脈レベルの持続する一方向層流剪断力(10 dyne/cm2から25 dyne/cm2)は代謝の急変(プロスタシクリンおよび一酸化窒素NOの生成)を生じるばかりか、FOS mRNAおよびFOS蛋白質が1時間経過しないうちに上昇した状態での遺伝子発現の急変も生じることがある。これ以外の幾つかの細胞株で、例えば、CHOおよびHELAなどの細胞株も、一方向剪断応力に持続して晒された後にはFOS誘導を示す。このような研究は通例はフローチャンバーを配備して、数分間から数時間更に数日間に亘って細胞が剪断応力に晒されることで遺伝子表現型が変化するのを観る環境で実施される。例えば、エス・エル・ディアマンド(S.L. Diamond)、エス・ジー・エスキン(S.G. Eskin)、エル・ヴィー・マッキンタイア(L.V. McIntire)共著、「流体フローの刺激によるヒトの培養内皮細胞からの組織プラスミノゲン活性化因子分泌促進(Fluid Flow Stimulates Tissue Plasminogen Activator Secretion by Cultured Human Endothelial Cells)」という題の1989年3月17日刊行のサイエンス(Science)243 (4897)号1483-1485を参照のこと。流体剪断研究とは別に、機械的摂動(基板の伸展または誘導変形)が伸展活性イオンチャネルを活性化させることができるとともに、カルシウム流動化を生じることがある。摂動剪断応力は、通例、破裂する酸素気泡が膜を破壊することとの相互作用が特に細胞溶解反応的であるという点で、層流剪断応力に比べて好ましくない。プルロニックF68(登録商標Pluronic F68)またはウシ血清などのような添加剤は細胞保護性を示すが、細胞が気泡と結合するのを防ぐ界面活性剤効果により、作用は部分的にすぎない。
【0078】
本発明の驚嘆に値する発見は、所定量の層流剪断応力を利用すれば細胞には最小の応力反応しか誘発しない、または、応力反応を全く誘発しないことで細胞を殺傷せずに細胞の凝集を破断することができることである。このような解離作用は、例えば、細胞を所定寸法の針または管の中に引き入れてからウエル等の中に細胞を注入し、これを必要に応じて反復することにより実施される。層流剪断応力への露出時間を最小限に抑えることで、試料を流体機械的破壊処理に付している最中も細胞の剪断活性化を低減している。
【0079】
試料を解離させるための適性条件を予め考慮することで、必要な装備と培検計画案を認識することができるようになる。いかなる刹那であれ細胞系の凝集状態は、細胞個体数規模分布によって明確にされる。細胞系は、単一分散であってもよいし(例えば、単体または凝集塊がいずれも、例えば、全部20-mer以下の小さい量体数の細胞だけから構成されている)、或いは、凝集塊が複数の単体から構成されたものから単体と多様なk-merから構成されたものにまで及んでおり、kの値が大きく、例えば、20よりも大きい多重分散であってもよい。細胞培養株では、凝集塊は同型である。しかしながら、穿刺吸引法は、多数の細胞型を含んでいるという意味で異型である。時機を得て進化する凝集プロセスおよび細分化プロセスの数学は良好な発展を見た。複雑に応じて、個体数バランス等式の解を分析的に求めてもよいし(単純な同型凝集の場合)、解を数値的に求めてもよいし(複雑な同型凝集の場合)、或いは、モンテカルロシミュレーション法に従って求めてもよい(異型の凝集と細分化について)。穿刺吸引による細胞破壊については、基本プロセスは細分化断片の核Fによって必然的に決まるが、細分化断片の核Fは一般的なフロー場、細胞集団寸法、緩衝条件で決まる。細分化(1つの成分が、1個の粒子ごとに分断されて2個のより小さな粒子になる)を受ける各寸法ごとの個体数については、細分化バランスは次のように表すことができる。
【0080】

但し、

は時間tにおけるk-量体数の大きさに設定された粒子(または、k-mers)の濃度であり、

はk-mersの正味分割率であり、

はk-mersの分割時に生成されたi-mersの平均数である。従って、

で (i+j)-mersがi-mersとj-mersに分かれる正味の割合が求められる。細分化断片の核Fは管内フローにおいては空間に依存しており(管の壁の近辺では高く、管中央部ではゼロである)、尚且つ、細胞集団寸法の管直径に対する割合にも依存している。生検後に操作するにあたり、穿刺吸引採取試料は高度に希釈されることになるため(細胞容量/試料容量 << 1)、最小粒子が壁に向けて放射方向に移動することに関与する懸濁液中浮遊物の動力学は重要ではなくなる。凝集塊の細分化の範囲は二分裂から全くの粉砕(細胞凝集塊から得られた細胞単体の喪失)にまで及んでいる。細分化断片の核は穿刺吸引採取試料中の腫瘍凝集塊ゆえに周知なのではない。当業者には分かることであるが、剪断フローにおける細胞群の実験による細分化率は、平均剪断率Gavgと凝集塊の水力学的半径または衝突半径Rhydとに基づく冪法則の関係である。例えば、共通様式は次のとおりである。すなわち、

であり、Aとyは実験的に決まり、γ=2を満たしている。i-細胞の腫瘍凝集塊については、1個の細胞ごとにその半径がR0であれば、

であり、但し、Dfは分数寸法である(Dfは1.7から2.5)。
【0081】
穿刺吸引採取試料およびそれ以外の細胞凝集塊は複雑な物体であり、多数の細胞型と多様な細胞基質組成を有している場合がある。穿刺吸引採取試料の分断を考慮するにあたり、患者から得た大型組織試料を細分化して部分集団にすることは、主として、腫瘍細胞相互の接合を分断するという問題であり、第2に、腫瘍細胞とその下の基質層との間のインテグリン依存性癒着を破断するという問題である。
【0082】
例えば、穿刺吸引採取試料などのような生検試料を管の中で剪断誘導により解離させるとする。細胞を解離する方法の1つとして、剪断応力を利用することによる方法がある。上述のように、層流剪断応力が好ましい。層流剪断応力は管の内部で生成される。
【0083】
管内の剪断層流については(レイノルズ数 < 2100)、剪断応力は管壁の付近で最大となり、流体が単純に下流側に移動している管の中央部ではゼロである。壁剪断応力 twおよび推移時間ttransitは次のように定義することができる。すなわち、

であり、断面積A=πR2の管を通る容積流量Qについては

であるが、但し、

であり、この等式におけるQの単位はcm3/sであり、vavgの単位はcm/sであり、Aの単位はcm2である。管材の長さLを横断する平均推移時間は

を満たすようなvavg=L/ttransitに基づいて定められる。水の粘性は室温で0.01ポアズである。グリセロール、プルロニックF68、デキストラン、ポリエチレングリコール(PEG)などのような添加剤は全て液相の粘性を高める可能性がある。一定の流量と一定の幾何学的形状の元では、粘性を増すことで剪断力も上昇する。入口長さの効果は小径の管では相当に極限まで小さくなる。広く使用されている1インチ注射器の長さ、注射器ゲージ(G)、水の灌注緩衝(1センチポアズ)、壁剪断応力(dpc、ダイン/平方センチメートル)、および、推移時間が表1に列挙されている。
【0084】
【表1】

1mL/s(粘性=1 cP)の水緩衝で灌流された1インチ針について、針ゲージ、壁剪断応力(dpc、ダイン/平方センチメートル)、および、推移時間(msec)の関係
【0085】
管内の層流は適度な伸張性フローの一例である。管などの内部流で近傍平坦面に向かって当たる衝突フローの伸張性は高い。細胞懸濁液は、低剪断環境に入る前に管の出口付近を通るほんの短い瞬間に伸張力を受ける。伸張力の大きさは管直径、流量、および、平面からの距離によって容易に制御される。定常運動制御および微調整操作は10ミクロン以内の精度で距離を制御することができる。また、液体の針への流入または針からの流出は強く細長い流れを生じることができる。多様な長さと内径(ゲージ)を採用することにより、壁剪断応力に晒されたせいで生じた解離を針への流入または針からの流出が原因で生じた解離と区別することができる。
【0086】
必要と算定された力および装備に基づいて、祖h式試料の細胞を直径10ミクロンから500ミクロンの管に通し、この時に10マイクロリットルから2000マイクロリットルまでの間の容量を利用して100ダイン/平方センチメートルから800ダイン/平方センチメートルの壁剪断応力を生じるようにする。或る実施例では、細胞は22ゲージ針または18ゲージ針に通される。或る実施例では、細胞が晒される層流による壁剪断応力は約100ダイン/平方センチメートルから約800ダイン/平方センチメートル、約300ダイン/平方センチメートルから約500ダイン/平方センチメートル、または、約350ダイン/平方センチメートルから約450ダイン/平方センチメートルである。必要な力の量と細胞の種類に応じて、細胞が層流による壁剪断応力に晒される期間は約10ミリ秒から約500ミリ秒、もしくは、それよりも長くてもよい。
【0087】
或る実施例においては、媒体の粘性を調節して、適正な剪断力を供与している。
【0088】
解析に適した試料が生成されるまで、上述の解離工程を必要に応じて反復するとよい。或る実施例では、少なくとも約70%、約80%、約90%、または、約90%を越える細胞が分散により1個から100個の細胞を含んでいる凝集塊にされる。凝集塊は5個から100個の細胞群、10個から100個の細胞群、10個から25個の細胞群、または、5個から25個の細胞群であってもよい。凝集固まりは1凝集塊あたりの含有細胞の個数が15個よりも少なく、例えば、1個から10個の細胞を含有しているのが好ましい。
【0089】
解離工程はまた、解離を支援する化合物を添加する工程、または、細胞の応力反応の活性化を阻害する化合物を添加する工程を含んでいるようにしてもよい。例えば、解離工程の最中に以下に列挙するいずれかの物質を細胞に添加するとよく、すなわち、生理学的に容認できる抗酸化剤、ムコリチック剤、ジスルフィド結合を減じることができる、N-アセチル-L-システインまたはジチオトレイトール等のような薬剤、生理学的に容認できる、エチレンジアミン四酢酸(EDTA)等のようなキレート剤、1種類以上の膜組織を保護する界面活性剤、または、これらの各種組合わせを添加するとよいが、膜組織を保護する界面活性剤の具体例としては非イオン性界面活性剤があり、その具体例としては、ポリエチレングリコール、ポリエトキシレート型脂肪酸、エチレンオキシドブロック共重合体、プルロニックF68(BASF)などのようなプロピレンオキシドブロック共重合体などがある。
【0090】
分散工程は、例えば、約0.9 % w/vの塩化ナトリウムの無菌水溶液などのような血清が全く含まれていない等張性生理食塩水中に複数の細胞または細胞凝集塊を懸濁させる工程を含んでいるが、等張性生理食塩水は、任意で、生理学に容認できる緩衝剤や塩を更に含有していることもあり、例えば、ラクトリンゲル液、アセトリンゲル液、燐酸緩衝生理食塩水、トリス緩衝生理食塩水、ハンク平衡塩溶液、アール平衡塩溶液、標準的なクエン酸生理食塩水、ヘペス緩衝生理食塩水などを含有していることもある。
【0091】
当業者には分かることであるが、細胞解離プロセスは手作業で実施されてもよく、例えば、ピペットまたは針を使用して人が行うか、または、空気駆動式または流体駆動式の自動流体処理装置などの自動プロセスを利用して行ってもよい。手動解離プロセスと自動化入りプロセスのいずれも、本発明の多様な実施例が網羅している。
【0092】
或る実施例においては、組織試料が解離および分散されている間、細胞シグナル伝達路や応力反応経路など(これらに限定されない)の反応経路がリガンド刺激に比べて活性化していない状態にあるが、具体的には、EGF刺激に比べて分散処理がFOS発現を活性化しない。
【0093】
<<C. 試料の高純度化と集積培養>>
凝集塊状の細胞は多数の細胞型を含んでいることがあるが、そのような多数の細胞型のうちの極めて少数またはわずか1種類のみしか検査や解析の対象とならないことも多い。このような場合、細胞は解離処理に付されてより小型の複数の凝集塊、個々の単一細胞、または、その両方に離解されてから、それらの混合物を高純度化処理に付して、興味の対象ではない細胞などの混入物を除去することで試料を高純度化し、更に、元の混交細胞試料中に含まれている興味の対象である細胞の割合よりも高い割合で興味の対象である細胞を調製することにより、試料を集積培養する。本明細書中で使用されているような「高純度化」または「集積培養」という用語は、標的細胞(例えば、腫瘍細胞、それ以外の解析に付されている細胞など)の個体数の、高純度化や集積培養の処理に付して除去しておかなければ解析の妨げとなる恐れのある標的ではない細胞または細胞の各部分の個体数に対する割合を増大させることを意味している。
【0094】
例えば、固形腫瘍から採取された生検試料は、興味の対象である細胞(例えば、腫瘍細胞)と混入した正常な細胞成分(血液生成細胞、肝細胞、脈管構造細胞など)の両方を含有している細胞混合物から構成されている。具体的な実施例においては、混入成分を除去する方法としては培検計画案に応じて、混入成分に固有の抗体を利用する方法か、または、標的細胞に固有の抗体を利用する方法が取られる。抗体は、プレート壁面や磁気ビーズなどの可塑性ビーズまたは可塑材被膜ビーズなどの可塑性表面を具体例とする基板に直接結着されるか、または、第1抗体を認識する第2抗体により基板に間接結着されて、興味の対象である細胞から混入物質を除去することができる。
【0095】
<<D. 細胞分配>>
細胞の解離処理と任意の高純度化処理(必要な場合のみ実施)が完了すると、細胞の試料は、本発明のカートリッジ内の1個以上の隔離室(例えば、上述の1個以上の第2隔離室)またはそれ以外の何か好適な容器に分配される。
【0096】
興味の対象である細胞は、所望されれば、前項Bに記載されていたような各種技術を利用して分散されてから、1分割量ごとの部分標本に分配されて、検査試薬と反応させられ、他の解析・検査に回され、または、その両方が実施される。或る実施例においては、1分割量ごとの部分標本が特別に誂えたカートリッジのウエルのうちの幾つかまたは全部に分配される。部分標本は所望の検査試薬と反応させられるが、例えば、刺激により細胞増殖やシグナル伝達を促す1種類以上のリガンドが適用される。
【0097】
第2隔離室またはそれ以外の検査用基板に分配された部分標本は、必要な細胞の個数およびそれ以外の当業者には周知の実験条件次第で変容可能である。或る実施例では、検査用部分標本の1分割量は2ミリリットル未満であるが、200マイクロリットル未満であるか、または、1マイクロリットルから200マイクロリットルの間か、いずれかである。当業者には分かることであるが、この量は、検査用の懸濁液中に好適な数の細胞が獲得されたさえ、必要に応じて上述の具体的範囲とは異なる値であってもよい。
【0098】
或る実施例においては、1分割量ずつの検査用部分標本を受容している少なくとも1個の隔離室は対照試料と指定される。このような対照試料は細胞生存度および応力レベルごとに再度評価分析し直されてもよいし、細胞計数処理を受けるようにしてもよいし、更に別な添加剤か対照物質が加えられて、他の隔離室のデータ解析結果とプラスマイナスの対照を行うようにしてもよい。
【0099】
分配された細胞は、その細胞型に好適な何らかの培地中に懸濁状態にされる。例えば、分配された細胞の検査用部分標本は血清が全く含まれていない養分を最小限に抑えた培地内に置かれている。血清が全く含まれていない養分を最小限に抑えた培地とは、必須アミノ酸、塩(例えば、塩化カリウム、硫酸マグネシウム、塩化ナトリウム、燐酸二水素ナトリウムなど)、グルコース、各種ビタミン(例えば、葉酸、ニコチンアミド、リボフラビン、B-12など)、それ以外の、細胞を適切に処理したり解析するのに必要な成分などを含んでいる。血清が全く含まれていない好適な栄養培地の具体例としては、ダルベッコ・フォークト変法イーグル最小必須培地(DMEM)やRPMI培地などがある。
【0100】
或る実施例においては、検査用部分標本は、96ウエルプレートなどのような可塑性プレートのウエルに分配されるが、この場合のウエルの壁は、ポリエチレングリコール、デキストラン、アルギネート、シリコーンなどのような、生理学的に容認可能なヒドロゲルまたはオイルで被膜されている。
【0101】
<<E. 検査試薬および検査>>
検査用部分標本は多様な検査試薬と反応させられるが、カートリッジ内で実施されるか、または、1個以上の隔離室をカートリッジから分離させた後で実施されるか、いずれかである。本明細書における方法および装置の利点は、検査試薬が治療の時点で添加されてもよいこと、検査試薬がカートリッジの特定のウエルに事前装填されていてもよいこと、または、その両方を満たしていてもよいことである。これにより、体外生体マーカーの検査は生細胞を利用して、任意で治療の時点で行うことができるようになる。このような方法および装置を特定の検査試薬と併用することで試料を体外で操作し、新規な予測生体マーカーの開発を容易にし、特定の薬剤に対する細胞感度の監視および測定と当業者が認識する上記以外の用途を監視および測定することができるようになる。
【0102】
例えば、患者から採取した固形腫瘍の試料は解離され、分配されてから、治療の時点で目下利用できる癌治療法のパネルに対して検査が行われる。次に、試料は安定化処理され、必要なら固定処理され、または、安定化と固定化の両方の処理が行われてから、解析が実施される。検査試薬は各々についての結果次第で、個々の患者の腫瘍にどの治療が最も効果的であるかを治療の時点で医者が即時判断することができる。この個人ごとに誂えた衣料は幾多の恩恵を施すものであり、特に、迅速かつコスト効率のよい態様で標的癌の治療法と培検計画案を採用できるという恩恵がある。
【0103】
本発明の実施例は、少なくとも1種類の薬剤を投与することにより標的である体外生体マーカーまたは体外生体分子に測定可能な定量効果または定性効果を生じることにより、分配済みの細胞(例えば、癌細胞)を解析することを目標としている。定量効果または定性効果は細胞経路の活性化であってもよいし、細胞経路の抑制であってもよい。具体的な細胞経路として、代謝経路、複製経路、細胞シグナル発生経路、腫瘍形成シグナル発生経路、アポトーシス経路、血管新生誘導経路などがあるが、これらに限定されない。例えば、定量効果または定性効果とは、G蛋白質共役受容体、または、上皮細胞成長因子受容体(EGFR)などの受容体型チロシンキナーゼに対するアゴニスト的代用効果またはアンタゴニスト的拮抗効果、更に、下流経路に対するアゴニスト的代用効果またはアンタゴニスト的拮抗効果の測定値のことである。
【0104】
測定される定量効果または定性効果とは、即時型または遅延型の初期遺伝子系統のメンバーなどの遺伝子の発現レベルのことである。好適な即時型または遅延型の初期遺伝子系統メンバーの具体例として、FOS、JUN、DUSP 1-28などがあるが、これらに限定されない。
【0105】
検査試薬の存在または不在の効果も、遺伝子情報翻訳後修飾蛋白質、イオン、酵素などの体外生体マーカーを検出することにより判定することができる。
【0106】
好適な検査試薬は、次に列挙するもののうちの1種類または各種組合わせを含んでいる(それらに限定されないが)。すなわち、医薬品、化合物、細胞刺激剤、ポリペプチド、ポリヌクレオチド、抗体、Fab分屑、Fc分屑、RNA、miRNA、siRNA、燐蛋白質などのうちの1種類または各種組合わせを含んでいる。上述のように、試薬の投与の後に続いて、分散細胞または分配細胞の標的体外生体マーカーまたは標的体外生体分子に対する定量効果または定性効果の測定が行われる。
【0107】
或る解析方法について、検査試薬は検出可能な薬剤であるとよい。検出可能な薬剤は個別に使用してもよいし、或いは、もう1つ別な化合物(例えば、抗体と共役した検出可能な薬剤など)と共役状態またはそれ以外の結合状態になるようにして使用してもよい。好適な検出可能な薬剤の具体例として、酵素、蛍光物質、発光物質、生体発光物質、放射性物質、陽電子断層撮影法で利用される陽電子射出物質、非放射性常磁性金属イオンなどが挙げられるが、これらに限定されない。
【0108】
上記以外の好適な検査試薬の具体例として各種腫瘍細胞刺激リガンドがあるが、更にその具体例としては、成長因子(例えば、EGF、インシュリン、VEGFなど)、エストロゲンやエストロゲン複合物などのホルモンなどが挙げられる。
【0109】
本発明の方法および装置の抗固形腫瘍応用例またはそれ以外の抗癌応用例については、検査試薬の具体例として有効な製薬剤や細胞毒性化学療法薬があるが、更にそれらの具体例として、有効製薬剤は抗腫瘍単クローン抗体剤であるトラスツズマブ(ヘルセプチンまたは登録商標Herceptin)、セツキシマブ(エルビツクスまたは登録商標Erbitux)、ベバシズマブ(アバスチンまたは登録商標Avastin)、リツキシマブ(リツキサンまたは登録商標Rituxanもしくはマブテラまたは登録商標Mabthera)等と小型分子阻害剤であるゲフィチニブ(イレッサまたは登録商標Iressa)、エルロチニブ(タルセバまたは登録商標Tarceva)等を含んでおり、細胞毒性化学療法薬はタキサン系製剤(タクソテレまたは登録商標Taxotere)、代謝拮抗剤(フルオロウラシル)、アルキル化剤、白金剤、アントラサイクリン系物質等を含んでいる。上述の具体的な製薬剤は個別に使用されてもよいし、本明細書に開示されている別な製薬剤と組合わせて使用されてもよいし、または、それ以外の化合物と組合わせて使用されてもよい。
【0110】
検査試薬を投与した後で、検査試薬が1種類以上の生体マーカーの発現に影響を与えたか否かを判定することができるが、この場合、そのような発現の存在、不在、または、相対的程度は選択された製薬剤に対する細胞の感受性を示している。このような生体マーカーは、mRNA、マイクロRNA、cDNA、蛋白質、燐蛋白質、遺伝子情報翻訳後修飾蛋白質、修飾ヒストン、DNAパッケージング細胞などのような多様な体外生体マーカーを含んでいる。例えば、製薬剤に対する感受性に付随している初期反応遺伝子(例えば、FOSやJUNなど)については、生体マーカーはmRNAまたはcDNAとなるかもしれない。検査試薬が存在している場合における各種生体マーカーの組合わせの発現の存在、不在、または、発現の相対度数は、製薬剤などの選択された検査試薬に対する細胞の感受性を示している。
【0111】
<<F. 試料調製および試料安定化処理>>
本明細書に記載されて添付図面にも例示されているように、本発明を利用して処理される細胞は多数の方法で調製および安定化処理されて、そのような細胞に対して多様な細胞解析を実施することができるようにしている。例えば、、核酸解析、蛋白質解析、生細胞指標剤を利用した解析、または、これらの各種組合わせの解析ごとに細胞を調製することができる。
【0112】
核酸解析については、アール・エヌ・エイ・レイターやアール・エヌ・エイ・プロテクトセルリエイジェント(登録商標RNAlaterおよび登録商標RNA Protect Cell Reagent −キアゲン(Qiagen)社製)或いはエタノール等のような安定化試薬を細胞に添加するとよい。安定化処理済みの細胞は任意で溶解分離されるか、またそうでなければ、興味の対象である核酸が抽出される。抽出されて高純度化された核酸は、PCR技術などを利用して解析に付される。
【0113】
或る実施例においては、また、既に説明したように、本明細書に記載されている方法は更に別な解析に付す目的で核酸をもたらす。このような試料については、分散および任意の集積培養の処理に続いて、拡散を安定化または抽出(任意)し、高品質で相当量の核酸をもたらすことができる。例えば、具体例としては後段の実施例10ならびに図13および図14を参照のこと。これは、例えば、検査試薬に対して反応させた後で所望の細胞を溶解分離し、その次に、逆転写酵素とDNAプライマーを使ってcDNAを得るという方法で実施される。DNAプライマーの具体例としては、ポリAに相補的である非特異的プライマーである、例えば、オリゴ(dT)12-18の各プライマーや、興味の対象であるmRNA転写に相補的である特異的プライマーなどがある。当業者には分かることであるが、細胞は、化学的手段や機械的手段などの多様な方法を利用して溶解分離される。
【0114】
任意で、試薬を使って細胞を安定化することで生体マーカー情報を検出し、保存し、または、検出と保存の両方を行うことができるが、その手段として、例えば、逆転写酵素およびDNAプライマーを利用してcDNA転写を得て、下流分子解析のためのRNA、DNA、および、蛋白質を準備するとよい。
【0115】
蛋白質解析については、全細胞または溶解分離処理された細胞のいずれを使用してもよい。無傷の全細胞は固定化されてから、後段の表2に明記したもの等のような重合体を使って安定化され、硝子スライドなどのような隔離室に試料を付着させることができるようにする。このような試料は、例えば、免疫組織化学(IHC)解析などのような分析を受けることができる。細胞を溶解分離させる処理、または、それ以外の方法で破砕する処理はウエスターン・ブロット法などのような評価分析で利用することができ、安定化または固定化を必要としないことがある。
【0116】
病理学者による形態学的調査のスライド標本と免疫組織化学IHCによる蛋白質解析は、本明細書に記載されている方法の成果である。従って、細胞を調製するのに、任意で重合体を使って硝子スライド上に準備し、形態学的解析、免疫組織化学解析、または、その両方の解析に付すことができるようになる。例えば、表2に開示されている混合物は表3の具体的な培検計画案に従って使用することができる。ジェイ・エー・マクセム(J.A. Maksem)、ヴィー・ダンワダ(V. Dhanwada)ほか著(2006年刊)、「自動液体細胞学的試料検査を残留細胞懸濁液を利用した手動液体細胞学的方法でThinPrep(登録商標)による500事例に基づいて実施する(Testing Automated Liquid-Based Cytology Samples with a Manual Liquid-Based Cytology Method Using Residual Cell Suspensions from 500 ThinPrep Cases)」という題の細胞病理学診断(Diagnostic Cytopathology)34巻(6)、391-396掲載論文も同様に参照のこと。
【0117】
重合体溶液
アガロース 0.18グラム
ポリエチレングリコール(PEG) 4.8グラム
アルコール試薬 76.8ミリリットル
ポリL-リシン
(0.1%) 0.25ミリリットル
ノニデット(Nonidet)P40**** 0.05ミリリットル
合計 240ミリリットル
表2
【0118】

【0119】
生細胞指標剤解析は、細胞を生きたまま処理する方法のどの時点であれ分子指標剤(後段の各実施例に記載されているようなマイトトラッカー(登録商標MitoTracker)など)を添加する工程に関与しているようにしてもよい。生細胞指標剤をこのように添加する工程は、固定化処理工程より前に行われるべきであり、そうでなければ、細胞を死なせてしまうことになる。例えば、このような指標剤の添加時機は、細胞固定化処理工程より先ではあるが、細胞安定化処理工程についてはその前後のいずれの時点で添加されてもよい。
【0120】
或る実施例においては、細胞を安定化および固定化させるにあたり、その後で生体マーカーの分子解析および分子検出を行うことができるようにするのに好適であればどのような手段を利用してもよい。一般に、ホルマリンなどの架橋固定剤は好ましくないが、後続の解析の妨げとならない程度の少量であれば存在していても構わない。生体マーカーが特定の1種類または複数種類の遺伝子の発現である場合は、或る実施例においては、細胞は溶解分離されてから逆転写酵素および好適なプライマーと反応させられて、細胞中にmRNA転写のcDNA転写を生成する。これにより、mRNAと比較してcDNAが分解することは少なくなるので、後続の解析を容易にすることができる。
【0121】
或る実施例においては、1×104個またはそれより多数の細胞が処理されることにより、RNA、DNA、蛋白質、燐蛋白質、または、これらの各種組合わせのうちのいずれかまたは全てを安定化させている。
【0122】
或る実施例においては、細胞は処理後に固定されてもよい。好適であればどのような固定手段が採用されてもよいが、例えば、空気乾燥技術、アルコールのうちでもメタノールやエタノールなどのような低級アルカノールを含有している固定剤などの化合物を添加する手段、ホルマリンを添加する手段、RNase阻害剤を添加する手段、アガロースを添加する手段、ポリエチレングリコールを添加する手段、ポリL-リシンを添加する手段、1種類以上のキレート剤または1種類以上の抗酸化剤を添加する手段などを採用してもよい。或る実施例においては、固定剤は、アガロース、ポリエチレングリコール、オクチルフェノキシポリエチレングリコール、ポリL-リシン、試薬アルコール、および、水を含有している。
【0123】
本発明の方法の更に別な実施例は、例えば、選択された有効な製薬剤に対する細胞の感受性を判定する目的で、固形腫瘍ができている動物被検体またはヒト被検体から採取した固形腫瘍細胞などのような、被検体の固形組織細胞を調製する方法を含んでいる。或る具体的な方法は、(a)所望の細胞を含んでいる固形腫瘍を被検体から採取する工程と、(b)組織を分散させて(例えば、剪断力を用いて)個別の単一生細胞にし、個数にして100個以下の、例えば、10個から100個の生細胞からなる凝集塊にし、または、単一生細胞および生細胞凝集塊の両方に分散させる工程と、(c)例えば、生細胞から混入物質を除去することで試料を集積培養する工程と、(d)生細胞を分配して1分割量ずつの部分標本を隔離室に入れる工程と、(e)生細胞を1種類以上の検査試薬と反応させる工程と、(f)固定剤、安定剤(例えば、RNA、DNA、蛋白質、燐蛋白質、または、これらの各種組合わせを安定化させる薬剤)、固定剤と安定剤の両方を使って細胞を処理して腫瘍細胞を固定し、生体マーカーを固定して解析に付し、または、腫瘍細胞と生体マーカーの両方を固定して解析に付す工程とを含んでおり、その場合、腫瘍細胞、生体マーカー、または、その両方の固定は被検体から組織を除去してから4時間以内に自動方式または手動方式のいずれかで完了される。
【0124】
本発明のもう1つ別な実施例は細胞を検査する方法を提案しており、斯かる方法では、固形腫瘍細胞は哺乳動物(例えば、ヒト患者)から採取され、細胞の全部または一部を1種類以上の検査試薬に体外で反応させると、更にまた、細胞を安定化させるのに任意で、細胞DNA、細胞RNA、蛋白質、燐蛋白質、または、これらの各種組合わせなどの生体マーカー情報を保存することができる固定剤(例えば、重合体)を使うと、細胞の大半、例えば、少なくとも65%の細胞、より具体的には、少なくとも75%の細胞が生存しているが体外で自己複製することはない。このような生体マーカーは、当業者には周知の分子解析または本明細書に開示されている新規な生体外生体マーカー検査を利用することで検査されるとよい。
【0125】
後段の各実施例は本発明を更に例示しているが、本発明の範囲を制限するものと解釈するべきではない。
【実施例1】
【0126】
<1. 生細胞処理>
マイトトラッカー(米国カリフォルニア州カールスバッドに居所を置くインヴィトロジェン社製)などの生細胞分子指標剤を利用した生細胞処理の重要性は既に説明した。マイトトラッカーは、プラズマ膜をわたる受動拡散によって生細胞に適用されると、ミトコンドリアに集中して局在するようになる。生細胞はマイトトラッカー局在化を安定させるために固定化され、蛍光顕微鏡により解析される。目下利用できる生検処理法を利用している方法とは異なり、本発明による装置およびシステムは分子指標剤を用いた生細胞研究を可能にしている。これは図20および図21に例示されており、これらの図面では、指標剤が生細胞に適用された場合の、ミトコンドリアの特定の細胞質プラスマ局在化(粒状蛍光発光、図20Aおよび図21Aの左半分)が明瞭に立証されているが、先行技術の方法を利用して固定された細胞に指標剤が適用された場合には所望する情報を欠いていた(図20Bおよび図21Bの右半分)。
【実施例2】
【0127】
<2. MCF−7およびHCT−116の解離研究>
MCF−7(ヒトの乳癌細胞−ATCC番号HTB-22)およびHCT−116(ヒトの大腸癌細胞−ATCC番号CCL-247)を使って、半自動ピペット装置における細胞集団寸法、生存度、および、細胞活性化に及ぼされる剪断力の影響を検査した。簡単に説明すると、MCF−7細胞およびHCT−116細胞が培養組織中で80%の集密度まで増殖してから、ゴムヘラを使って静かに掻爬することによりプレートから取外してから増殖培地中に懸濁させ、通例の穿刺吸引採取試料中の細胞個数および細分化寸法と同程度にした。細胞懸濁液の1分割量の部分標本を22ゲージ針に4度にわたって通し、その際には自動ピペット装置(米国マサチューセッツ州ホリストンに居所を置くハーバード・ピペッタ・ハーバード・アパレイタス製(Harvard Pipetter, Harvard Apparatus))を使用し(1回の処理ごとに4.14ミリリットル/分の割合で吸引・注入される)、結局、100ダイン/平方センチメートルから800ダイン/平方センチメートルの範囲で壁剪断応力に晒されたが、その期間は1個の細胞につき、または、1個の凝集塊ごとに4(移行回数)×14ミリ秒/1回の移行=56ミリ秒であった。個々の細胞由来または個々の凝集塊由来の代表試料は硝子スライド上に細胞遠心分離処理され、95%エタノールで固定され、パパニコロウ染料で着色された。代表領域の顕微鏡写真を得た(倍率x200)。剪断力が増大するにつれて細胞集団寸法は減少する点に留意すること。これらの結果は図22に例示されている。
【実施例3】
【0128】
<3. 細胞集団寸法分布>
実施例2の方法を採用した後、細胞濃度および細胞寸法分布を測定する非流動画像方式細胞計数装置(米国マサチューセッツ州ローレンスに居所を置くネクセロム製(Nexcelom)のセロミター(登録商標Cellometer))を使用することにより平均細胞集団寸法を定量化した。100ダイン/平方センチメートルで、MCF−7細胞の平均集団寸法は97±3マイクロメートルであり、HCT細胞は51±6マイクロメートルであった(図15)。これらのデータは、生細胞の凝集塊を分散させるのに必要な再現可能な最適剪断力の範囲を提示している。
【実施例4】
【0129】
<4. 分散処理後の生存度解析>
実施例2の方法を利用した後で、半自動ピペット装置から相当の剪断力でトリパンブルー色素排除試験によって生存度が検査された。800ダイン/平方センチメートルよりも大きい剪断力は生細胞の操作および処理には厳し過ぎると思われるが結果的に生存度が40%を越えて減少したと結論づけられた。達成された結果を図表で描いたものとして図16を参照のこと。
【実施例5】
【0130】
<5. 分散処理後の活性化解析>
細胞活性化の機能的測定法として、定量RT-PCRによって判定されるFOS mRNA誘導法がある。FOSはEGFR経路に関与している初期反応遺伝子である。或る実験では、MCF−7細胞は6ウエルプレートにおける正常な増殖条件で80%の集密度まで増殖した。細胞を静かに掻爬してから、RNA抽出前に100ナノグラム/ミリリットルのEGFリガンド(シグマ受容体)を存在させて、または、同濃度のEGFリガンドを欠いたままでより長い培養時間(0分から45分)に亘ってより大きい剪断力(ハーバードピペッタ製装置により0ダイン/平方センチメートルから800ダイン/平方センチメートル)に晒した。30分から45分経過した時点でFOS mRNA誘導は最高潮に達し、約60分のうちに基底レベルに戻った。EGFリガンドを使った培養の結果としてFOS蛋白誘導は刺激により活発化した。ここで重要なのは、予備的な結果の示すところによると、半自動プラットフォームに生成される100ダイン/平方センチメートルから800ダイン/平方センチメートルの剪断力による分散処理の結果、EGF刺激と比べてそれほどの細胞活性化が生じることはない点である。得られた結果を図表で描いたものについては図17および図18を参照のこと。
【実施例6】
【0131】
<6. 装置>
図1は、組織の解離を遂行する機能、細胞計数装置の機能、遺伝子発現剤感受性検査の機能、および、解析に付すための試料固定の機能を統合するためのプラットフォームとして作用するような装置で使用される具体的カートリッジの概略図である。図1から図22は、本明細書に記載されている各特性の特定の実施例を例示している。当業者なら、本件の説明に関連づけて図面を思量すれば、各実施例が作用する態様が分かる。
【0132】
上述の装置は主要構成部材として以下のものを備えている。すなわち、装置に挿入することができるうえに手動処理の用途に付すことができる貯蔵カートリッジ1、斯かるカートリッジ1の上に搭載されて複数の小型容器が設けられた、例えば、96ウエルプレート型2、および、試料を初期受容し、試料を分散し、試料から混入物を除去するための複数の受容器3を備えている。受容器3は、図2に概略的に描かれているうえに本明細書中で既に説明されている複数の異なる機能を果たすことができる。カートリッジ1には標識4が取付けられており、斯かる標識4は試料を容易に識別することができるようにバーコード形式であってもよい。受容器3は各々が1個のウエルと内容物の生物学的拘禁を確保する封鎖部を備えており、針で刺し通すことができるが、針を抜取った時点で再封鎖される。組織試料は患者から採集されるが、通例は、細い針5を使った穿刺吸引生検法によって医者が採集し、医者は試料組織をカートリッジ1の受容器3内に置く。
【0133】
次に、カートリッジ1を装置に滑り込ませてから扉を閉じて装置を封鎖し、カートリッジ1は外部環境から生物学的に密封されるとともに、生物学的に危険な何らかの組織試料を放散することが無いように厳封される。代替の実施例においては、カートリッジは特定の試薬を保有しているプラットフォームであり、手動で処理に付すことができる。
【0134】
カートリッジ1には、組織試料の操作を遂行するのに使用される原材料を貯蔵および廃棄するための、1個以上のウエル6が設けられている。このような原材料の具体例として、針先端具および試薬が挙げられる。針先端具は開口および尖端が設けられたニードル部と、ニードル部の内側にあって開口および注射器と流体導通状態にある環帯部とから構成されている。本件の装置は自蔵式であるが、例外として、必要に応じてコードを通して電流が供給される。
【0135】
カートリッジ1は処理集成部を格納する受容器3を備えており、通例は、組織試料を混合する用途に付されるようにしてもよい。受容器3は緩衝生理食塩水の解離液が事前封入されており、任意で、解離溶液にプロテアーゼ系物質を使用するのを避けねばならないという抑制がある場合には、キレート剤、抗酸化剤、粘性修飾剤などを更に含有している。
【0136】
受容器3はウエルの密封カバー部材を含んでいる。この自蔵式のウエルと処理集成部との配置は人間の作業人員が生物危害に晒されるのを最小限に抑えている。係合用張出部が密封カバー部材から突出している。
【0137】
本発明の装置には作業部材が誂えてあり、カートリッジ1上の保管ウエル6から針先端具を選択的に持ち上げて針先端具を装着した注射器部材を操ることができるとともに、受容器の処理集成部などのような、装置に設けられている或る装具で作業することができるよう図っている。
【0138】
本発明の装置を使って初めて作業するにあたり、作業部材が針先端具を保管ウエル6から回収し、受容器3に関連する位置に移動させるが、受容器3はその内部に試料組織が医者によって既に置かれているうえに、緩衝液、キレート剤、および、抗酸化剤などのような解離溶液が事前に装填されており、針先端具で受容器3の封鎖部を刺し通して針先端具の尖端を均質な液状混合物の中に浸漬し、受容器3から試料の一部を針先端具の注射器の中に吸引してから針先端具の尖端を受容器3内部の所定位置まで移動させて、吸引した試料をその同じ受容器3かまたはもう1つ別な第2受容器3の中で分散させることで組織試料を解離させて、無傷の腫瘍細胞と混入物質とを含んでいる均質な溶液にする。このような工程は、組織試料を所定のレベルまで解離させるのに必要な回数だけ反復実施される。図3の、例えば、参照番号309を参照のこと。
【0139】
作業部材(または、手動操作に付される場合には、作業人員)はカートリッジの保管ウエル6から新しい針先端具を回収してから受容器3に関連する位置まで移動し、針先端部を使って選択された受容器3の封鎖部を刺し通し、針先端部の尖端を均質な液状混合物中に浸漬し、受容器3から試料の一部を針先端部の注射器の中に吸引し、針を受容器から抜取り、マトリクス状の受容器のうちの別な1個に関連する位置まで移動し、その受容器の封鎖部を針先端部を使って刺し通し、注射器から試料の一部を受容器3の中に入れる。図2を参照のこと。このマトリクス状の受容器3はその最下位置にある収蔵室の真上に樹脂ビーズ床が支持されており、その更に真上に装填室が設けられた構成になっている。樹脂ビーズの床には栓が装着されており、栓は樹脂ビーズ床の頂面から底面まで延在している。栓を構成している素材は、樹脂ビーズ床の頂面位置まできた針先端具による刺し通しを許容するとともに、針先端具が樹脂ビーズ床の底面を通り抜けて収蔵室内まで張出すのを許容するような素材である。図2を参照のこと。これに代わる具体例として、樹脂ビーズ床には導管が装着されており、導管は装填室の頂面付近から樹脂ビーズ床を突き抜けて収蔵室の底面付近まで延びている。作業時には、受容器内に置かれた試料液は樹脂ビーズ床より上位にあって、重力によって樹脂ビーズ床に給送されてその中に吸込まれ、樹脂ビーズ床が溶液から混入物を除去して収蔵室に回収する。導管の頂端は、収蔵室内に回収する前に樹脂ビーズ床をどの溶液といえども迂回することが無い態様で取付けられる。
【0140】
或る実施例においては、試料はその中に適正数の細胞が分散しているのを確保するように検査される。作業部材はカートリッジ保管ウエル6から針先端具を回収してから受容器に関連のある位置まで移動し、針先端具を使って受容器の封鎖部を刺し通し、針先端具の尖端を均質な液状混合物中に浸漬し、試料の所定の一部を受容器3から針先端具の注射器の中に吸引し、針先端具を受容器3から抜取り、細胞計数装置モジュールに関連する位置に移動し、試料の上記所定の一部を計数装置モジュール内に置く。針先端具は計数装置容器から抜取られ、カートリッジ上の処理容器に入れて処分される。
【0141】
計数装置モジュールは、カートリッジ上の受容器3のうちの1個であってもよいが、計数装置容器の格納室の内部に乾染料と一緒に梱包される。計数装置容器の内部では、格納室内に既に置かれている計数するべき試料部分が染料を溶かし、この染料が腫瘍細胞を着色している。所定の試料部分は漏斗状の計数装置管の中を通り抜けて落下し、任意で、細胞計数を目的としてスキャナーにより走査される。計数されるべき試料部分は格納ウエル内の計数装置管より下の位置に集積している。光学スキャナーが細胞個数を中継して表示器に伝えるが、表示器はその個数が良好な生検試料と言える所定計数寸法に合致しているか超過しているかを判定する。解析結果はディスプレイ装置に表示され、プリンターによって印字され、または、その両方が実施される。次に、解析結果が直ちに医者の手引きとなって更に別な生検が必要か否かを判断させる。試料が適正である場合には、患者は検査から放免される。
【0142】
細胞が分散処理されて混入物の除去が完了すると、細胞は1分割量ずつの部分標本にされて検査用マトリクス2、通例は、96ウエルプレート型の区画に置かれる。典型例として、ウエルは所望の媒体(緩衝生理食塩水溶液および検査試薬)の事前充填が済んでいる。作業部材がカートリッジからもう1本別な針を拾い上げて分散処理と混入物除去処理が済んだ所望量の細胞を受容器3から吸引し、一連の密封試料ウエル2セットに関連する位置まで移動し、連続して一個ずつウエルの封鎖部を次々に刺し通して所定量の試料部分を個々のウエルごとに注入してから針先端具を抜取ることを繰り返す。針先端部は処理容器6に入れて処分される。
【0143】
ウエル2には多様な投与量の多様な製薬剤が予備梱包されており、これら個々の投与量と個々の製薬剤に対する腫瘍細胞の感受性を検査することができるようにするのが好ましい。ウエルを維持する諸条件は当然のことながら生理学的条件に近似している。ウエル内の培地のpHは生理学的pHに近く、pH 6からpH 8であるのが好ましく、約pH 7からpH 7.8であるのが好ましく、pH 7.4が最も好ましい。生理学的体温の範囲は摂氏約30度から40度の間である。細胞は摂氏約35度から約37度の温度に維持されるのが好ましい。同様に、細胞を培養する酸素レベルは空気中の酸素濃度に比べて比較的低く、培地の酸素濃度は空気中の20%の酸素濃度ではなくむしろ、生理学的レベル(1%から6%)と同等であるとよい。培養時間が短い場合、一般に細胞に酸素供給することは必要ではない。
【0144】
多様な試薬ごとに所定の期間に亘って培養を行った後、ウエルは各々が、細胞を固定する固定剤と後続の解析処理のための指標剤とを使って処理される。このような処理は作業部材、未使用の針先端具、および、バイアルに入れた固定剤を利用して達成される。
【0145】
固形腫瘍細胞は、必要となるまで、当該技術分野で周知の何らかの方法で低温保存されるとよい。細胞は等張性溶液中に懸濁状態にされるとよいが、特定の低温保存剤を含有している細胞培養媒体中に浮遊させられるのが好ましい。このような低温保存剤の具体例としては、ジメチルスルホキシド(DMSO)やグリセロールなどがある。このような低温保存剤は5%から15%の濃度で使用され、8%から10%の濃度で使用されるのが好ましい。細胞は徐々に凍結されて、摂氏マイナス10度から摂氏マイナス150度の温度にされるが、摂氏マイナス20度から摂氏マイナス100度にするのが好ましく、摂氏マイナス150度にするのがより好ましい。
【0146】
しかしながら、前段までに記載されている本発明の装置および方法に、本発明の分野および範囲から外れることなく修正、追加、または、修正と追加を施すことができるのは明白である。例えば、受容器と光学スキャナーは、処理集成部の作業前に受容器から直接採取された試料に対して活用されてもよい。
【実施例7】
【0147】
<7. 解離研究>
MCF−7ヒト乳癌細胞(ATCC番号HTB-22)は組織培地において80%集密度まで増殖してから、ゴムヘラを使って静かに掻爬することによりプレートから取外され、増殖媒地中で懸濁状態にされた。1分割量の細胞懸濁液の部分標本を18ゲージ針に2度通され(1回通すごとに1ミリリットル/秒の割合で吸引・注入される)、172ダイン/平方センチメートルの壁剪断応力に晒される結果となり、1個の細胞または1個の凝集塊ごとに壁剪断応力に晒される総時間長は4(移行回数)×14ミリ秒/1回の移動=56ミリ秒であった。個々の細胞由来または個々の凝集塊由来の代表試料は硝子スライド上に細胞遠心分離処理され、95%エタノールで固定され、パパニコロウ染料で着色された。代表領域の顕微鏡写真を得た(倍率x200)。比較のために、転移乳癌があることが分かっている肥大リンパ節への超音波支援式穿刺吸引生検法(FNA)により、もう1つ別な画像を得た。この同じヒト試料に基づく画像は、無数のリンパ球を背景に数群の乳癌細胞を示していた。MCF−7細胞を掻爬してから、18ゲージ針(1インチ)に1ミリリットル/秒の割合で通すのを2回の吸引・注入サイクルまたは5回の吸引・注入サイクルで実施した。望ましくない条件では、溶解分離して細胞核が放出されるようにするには、試料C中において5回の吸引・注入サイクルで十分であることに留意するべきである。
【0148】
上述の実験では、MCF−7細胞に2回の吸引・注入サイクルを受けさせるというのは、エチレンジアミン四酢酸(EDTA)を欠いたまま掻爬したMCF−7単分子層を分散させる作業条件の予備鑑定を表したものである。このような実験条件が試料に加える総剪断応力はtw(4ttransit)=172dyne/cm2×0.056sec=9.6dyne・sec/cm2であった。
【実施例8】
【0149】
<8.EGFR遮断剤に対する感受性を知るための初期マーカーとしての相対FOS発現>
上皮成長因子受容体(EGFR)を標的とする少なくとも35種類の有効な癌治療薬が承認されており、或いは、臨床的試用に付されている。残念ながら、EGFR拮抗物質に対する腫瘍の感受性を予測する生体マーカーは、大半の癌種類について未知である。EGFR反応阻害の末梢効果としての初期反応遺伝子FOSの発現変化は評価することができ、更にまた、ヒト癌細胞株(A431、CAL27、HN11、HuCCT1、Hep2など)におけるゲフィチニブおよびエルロチニブの増殖抑制効果およびFOS修飾効果などの抗腫瘍効果に対する上述のFOS発現変化の関係が測定された。次に、これらの細胞株はマウスに異種移植することができ、ゲフィチニブ(A431およびHuCCT1)またはエルロチニブ(CAL27、HN11、および、Hep2)を使って14日間処理された。腫瘍に対する穿刺吸引生検は基本水準で治療から14日後にFOS査定を得る目的で実施された。これに加えて、固形腫瘍を有する患者にゲフィチニブを臨床試用することで得られた5対の腫瘍試料について上述のマーカー解析の実行可能性を試した。培地では、ゲフィチニブおよびエルロチニブは感受性のある細胞株A431、CAL27、および、HN11においてFOS mRNAレベルを減少させた。ゲフィチニブまたはエルロチニブは、EGFRに敏感なA431、CAL27、および、HN11の各腫瘍株についての生体内FOS発現増大を排除しているが、耐性菌については排除していない。簡単に述べると、FOS発現変化は器内モデルと生体内モデルの両方についてEGFR阻害物質が薬理学的に作用していることを反映している。例えば、エー・ジメノ(A. Jimeno)、ピー・クレザ(P. Kulesza)、イー・キンケイド(E. Kincaid)、エヌ・ブアラウド(N. Bouaroud)、エー・チャン(A. Chan)、エー・フォラスティエレ(A. Foratiere)、ジェイ・ブラーマー(J. Brahmer)、ディー・ピー・クラーク(D.P. Clark)、エム・イダルゴ(M. Hidalgo)共著、「抗上皮成長因子受容体効果のマーカーとしてのC-FOS査定(C-FOS Assessment as a Marker of Anti-Epidermal Growth Factor Receptor Effect)」という題の2006年刊行『癌研究(Cancer Research)』66号、2385-2390掲載論文を参照のこと。
【実施例9】
【0150】
<9. FNA法において即時であるが静かに分散させるための最適条件>
<<FNA法における乳癌細胞のアナログとしてのMCF−7細胞の選択>>
MCF−7ヒト乳癌細胞は、ホルモン依存乳癌の一モデルとして広く研究されている。この癌細胞は特徴づけが明確に行われたエストロゲン受容体(ER)陽性細胞株であるため、乳癌研究の有用な器内モデルとなっている。安定した上皮細胞株は、転移性疾患に罹った女性患者由来の胸膜滲出液から採取されたヒト乳癌細胞の一次培養から得られた(スーレ(Soule)著の論文、1973年)。それ以来、このMCF−7細胞株は、それに類似する多数の臨床特性の結果として数千回も引用された、最も広く研究された乳癌モデルとなったことには間違いない。ホルモン依存ER陽性乳癌と同様に、MCF−7細胞は初期的には、タモキシフェンやフルベストラントなどのような抗エストラゲン系物質に対して高感度である。MCF−7細胞株は、何度も予兆的臨床的試用の成果をあげた他の無数の乳癌モデルの起源となる親世代細胞株としても機能してきた。更に、MCF−7細胞株の誘導体は、第一線のホルモン治療に関与している抵抗のメカニズムに洞察を与えてきた。
【0151】
MCF−7ヒト乳癌細胞(ATCC番号HTB-22)は調製済み改良型最小必須培地(商品名Improved MEM、米国カリフォルニア州カールスバッドに居所を置くインヴィトロゲン製)、10%ウシ胎児の血清(米国ユタ州ローガンに居所を置くハイクローン(Hyclone)社製)、および、1%ペニシリン・ストレプトマイシン溶液(ペニシリン10,000 IUとストレプトマイシン10,000 IUずつ、インヴィトロジェン社製)の中で増殖した。80%の集密度に達した時に、細胞は一回だけ10ミリリットルのダルベッコ燐酸緩衝生理食塩水(DPBS)で洗浄されてから、ゴムヘラ細胞掻爬具を使って静かに掻爬してフラスコから除去される。細胞は10ミリリットルの増殖媒地中に懸濁状態にされてから1分割量ごとの複製部分標本に分配される。このような培検計画案は、ヒト乳癌穿刺吸引法で使用される腫瘍細胞凝集塊の代用となる非常に大型の凝集塊を生成するのに有効であった。第1部分標本(3ミリリットルの液中浮遊細胞)は画像解析装置で画像化され、コールター社製計数装置により寸法判定される。第1部分標本の初期寸法状態が計数された後で、試料はトリプシン処理されてから、全細胞が計数される。
【0152】
<<転移大腸癌FNAのアナログとしてのHCT−116大腸癌細胞株の選別>>
ヒト大腸癌細胞株HCT−116(ATCC番号CCL-247)は最初はヒト男性大腸腺癌に由来するものであったが、その後の研究で広く活用されてきた。形態学的には転移大腸癌に似ており、ras癌原遺伝子のコドン13の突然変異体などのヒト大腸癌に共通する遺伝子特性を示している。この癌細胞株は、製薬剤感受性ごとに選別されたヒト癌細胞株の米国国立癌研究所所有NCI-60パネルに含まれている。この癌細胞株については、広範囲なcDNAマイクロアレイ遺伝子発現データおよびこれと相関関係のある薬剤活性度データが利用できる(http://discover.nci.nih.gov/を参照のこと)。
【0153】
HCT−116細胞を10%のウシ胎児血清を含むマッコイ5a修飾培地で増殖させてから摂氏37度で尚且つ5%の二酸化炭素環境で保温培養した。培地は2・3日ごとに新しく取り替えられ、トリプシン・エチレンジアミン四酢酸(EDTA)溶液を使って約1:8の二次培養比で集密状態に達すると細胞を分割した。
【0154】
FOS着色法について説明する。すなわち、スライド標本を2%パラホルムアルデヒドおよび0.5%トリトンX-100(登録商標Triton X-100、組成式C14H22O(C2H4O)n)含有溶液中にて摂氏4度で15分間に亘って保温培養することにより、細胞凝集体を固定した。次に、スライド標本を燐酸緩衝生理食塩中に3%の割合のウシ血清アルブミンおよび0.5%の割合のトリトンX-100を含有する溶液にて洗浄してから、FOS蛋白に対するヒツジ多クローン性抗体(米国デラウエア州ウィルミントンに居所を置くケンブリッジ・リサーチ・インコーポレーティッド(Cambridge Research Inc.)社製)50マイクロリットルを1:20の希釈率で(PBS中に3%の割合のBSAおよび0.5%の割合のTritonを含有する溶液)、2時間に亘って保温培養した。続いて、ウシ血清アルブミンを3%、トリトンを0.5%の割合で含有する5ミリリットルの燐酸緩衝生理食塩水でスライドを3回洗浄した。スライドは各々がフルオレセインとロバの抗ヒツジIgG (H+L) の共役体染料液(米国オレゴン州に居所を置くモレキュラー・プローブズ・インコーポレーティッド(Molecular Probes Inc.)社製)5ミリリットル(1:20の希釈率)を使って1時間に亘って保温培養してから、燐酸緩衝生理食塩水で4度洗浄してから画像化した。
【0155】
<<トリパンブルー色素排除試験>>
この簡易検査は、細胞膜が無傷であれば細胞が色素を排除する能力を測定するものである。剪断応力の強度次第で、剪断力への細胞接触により細胞膜は過渡的に透過性を高め、または、細胞原形質膜を恒久的に破壊することができるようになる。分散実験後、細胞はハンク平衡塩溶液(HBSS)中に懸濁状態にされる。総量0.2ミリリットルの懸濁液を0.8ミリリットルの染料液(0.3ミリリットルのHBSS中に0.4%濃度の無菌トリパンブルー溶液(商品名Sigma T-8154)0.5ミリリットルを混合)に添加し、10分間に亘って保温培養してから、10マイクロリットルのこの溶液について血球計算装置を使って計数を行い、細胞の個数と死細胞の百分率を得た。
【0156】
<<細胞生死の染色判定試験>>
トリパンブルー色素排除支援は簡単かつ高精度ではあるが、蛍光染料使用の価値が検証されており、というのも、細胞の生存度と細胞の個体数は蛍光判定に付すほうが自動化も小型化も容易だからである。細胞生死の蛍光染色判定試験は2種類の染料を使用する。すなわち、カルセインアセトキシルメチル(カルセインAM)とエチジウムホモダイマー(EthD-1)である。カルセインAMは非蛍光性細胞透過性染料である。この染料は細胞内エステラーゼにより開烈して生細胞中で蛍光性を示す。エチジウムホモダイマー(EthD-1)はDNAと結合する一種の染色体計数染料であるが、生細胞に浸透することはなく、死細胞を検出するために使用することができる。標準キットがアクティブモーティフ(ActiveMotif)から購入できる。
【0157】
<<アポトーシスの検出>>
接触強度次第では、流体剪断力により細胞壊死またはアポトーシスを生じることがある。解離計画を実施してから半時間から1時間経過後に、固定処理していない細胞について何度かアポトーシスを判定するために、バイオチウム(Biotium)から購入できる細胞透過性ニュクヴュー488(商品名NucView 488)カスパーゼ3基質を使用した。カスパーゼ3は各種アポトーシスの共通マーカーである。ニュクヴュー488カスパーゼ3基質は蛍光生成DNA染料およびDEVD基質の細胞膜透過性共役物質である。細胞内カスパーゼ3によって染料を開裂することでDNA染料を放出するのと同時に細胞核を着色する。
【0158】
実験データAの遺伝子アルゴリズム(GA)に基づく細分化速度の判定を使用した目的は、実験の吸引・注入サイクルを1回実施した後ごとに得られた、t1、t2、t3、t4、および、t5それぞれの時間における時系列的な実験測定による寸法分布に基づいて寸法依存の細分化断片の核を回帰推定することであった。遺伝子アルゴリズムは、小進化(交錯進化、乱進化、適応度に左右される淘汰)の原理に従って、初期のランダムな個体数の核モデルを展開する。注射器を通して移行を1度行うたびごとに、寸法分布は非連続時間に何度か測定されて細分化された断片となる。所与の平均管内剪断率(Gavg)で得られたデータについて、式1(1組のk次数)を回帰推定するにあたり、検査対象の「染色体」の適応度の発達を利用したが、染色体は各々が進化可能なパラメータの集合[A(i,Gavg),y,g]を含んでおり、i-細胞から構成される凝集塊ごとにai=A*(Gavg)y(Rhyd)gの関係を満たしている。
【0159】
掻爬された単層のMCF−7および単層のHCT−116を無菌注射針の中で10ミリ秒から100秒までの多様な期間に亘って放物面剪断力場に当て(壁剪断応力は5ダイン/平方センチメートルから500ダイン/平方センチメートル)、分散特性を評価した。伸張性フローは間隙相互の離隔距離が100ミクロンから1000ミクロンの範囲である衝突フローにより検査された。細胞検査は生存度について実施された。寸法分布はコールター社製計数装置を使って得られた。細胞活性度はFOS免疫組織染色法を利用して測定されたが、初期反応遺伝子は高レベルの剪断力によって即時に細胞成分上昇発現が行われる。FOS誘導の結果として細胞核着色は強まり、細胞核計数処理に基づく百分率による活性度として評点が付与される。潜在的に重要な細胞表層蛋白質を破壊する可能性のあるプロテアーゼの使用を回避するという拘束条件を設けて、例えば、キレート剤、粘性修飾剤、各種細胞保護剤などを含有しているものなど、多様な緩衝剤が吟味された。
【0160】
MCF−7単層におけるFOS染色と生存度を査定し、掻爬した単層(穿刺吸引採集試料アナログ)について得られた査定結果と比較して、剪断破壊前の基底水準の活性法を確立した。或る程度までは、これは分散前の穿刺吸引法による試料獲得術中の活性法の模倣である。個々の細胞株ごとについて、判定するべき最も重要なパラメータは、試料を解離させるのに要する最小の剪断力接触強度(壁剪断応力)と最短の剪断力接触時間(針により移行させる累積時間)であった。1分割量(掻爬された細胞の0.2ミリリットルから3ミリリットルの懸濁液)の部分標本を15ゲージから21ゲージの針(長さ0.5インチから2インチ)に0.1ミリリットル/秒から5ミリリットル/秒の流量で通したが、その際にはコンピュータ制御によるハーバード社製の注射器ポンプを1サイクルから10サイクルで使用した。10ミリリットル容量の注射器を使った個別のサイクル(吸引・注入)を1サイクルと定義した。針は、自動液体処理システムの各種部品の注文製造業者であるポッパー・アンド・サンズ(Popper & Sons、http://www.popperandsons.com参照のこと)から入手できる。1サイクル終わるごとに、試料を画像化した。複数の異なるゲージの針、複数の異なる長さの針、複数の異なる流量などを採用することにより、壁剪断応力および応力接触させた累積時間は検査ごとに異なっているようにすることができた。壁剪断応力は流量Qに従って線形に高くなるが、半径の三乗に比例する。
【0161】
一般に、試料の解離状態を制御することで1凝集塊につき5個から10個の細胞を含んでいる態様で細胞凝集塊を採取するには、10ミリ秒から500ミリ秒の間の多様な期間に亘って10ダイン/平方センチメートルから150ダイン/平方センチメートルの層流壁剪断応力に晒すことで十分である。掻爬試料を信頼できる状態に分散させるには、一般に、2サイクルから3サイクルが最適である。FOS活性度および細胞生存度を調査するのについては、FOS発現を得るために15%未満の細胞核が陽性となるように掻爬単層を破砕する目的で、諸条件と剪断力により誘導されるFOS発現とを監視した。
【0162】
<<流出入効果>>
注射器(内部には実質的に細長い流れが存在できる)への試料の流入中またはそこからの試料の流出中における試料分散の役割を評価する実験を実施した。針のゲージと流量はいずれも同じであったが、針の長さをいろいろ変えて(0.5インチと1.0インチと2.0インチの対比)、更に、サイクル数をいろいろ変えて同一壁剪断応力に同一累積時間に亘って晒し、流出入事象の発生回数をいろいろ変えることで生成された多様な試料を生成することができるようにして、結果を比較した。一般に、試料の注射器への流入および流出が相当の解離を生じることは無い。
【0163】
個々のサイクルの吸引・注入を実施した後の解離状況の視覚的解析を行うために、試料を氷の上に置いて即時に細胞遠心分離処理に付した。まず、1試料ごとに卓上型遠心分離装置(ヘティッヒ(Hettich)社製のロティーナ46S(Rotina 46S)内で2000 rpmの回転速度で遠心分離処理することにより、顕微鏡解析用に細胞を調製してから、500マイクロリットルの平衡塩溶液(ノーモソル(Normosol))中に凝集細胞固形体を浮遊させた。ここで、細胞遠心分離装置(サーモシャンダン(ThermoShandon)社製のサイトスピン4(Cytospin 4)を750 rpmの回転速度で3分間使用して、硝子の顕微鏡用スライドに細胞を塗布した。直ちに95%エタノール中でスライド標本を固定し、パパニコロウ染料で着色した。アドービ・フォトショップ5.5版(Adobe Photoshop v. 5.5)およびディジタルカメラ(Kontron Elektronik Prog/Res/3012)を付帯させた光学顕微鏡(Olympus BX40)を使って、選択領域のディジタル画像を得た。細胞は粒子計数画像解析(画像解析ソフトNIH Image)に付され、解析結果を原初部分標本について取得された細胞計数結果と比較した。
【0164】
<<衝突フローシステム>>
針の端部を平坦面に向けることにより、衝突フローは信頼できる態様で得ることができる。沈水管から出る液体噴流は管の直径の数倍の距離を経ずして急速に減衰するせいで、間隙相互の離隔距離Sを針ゲージ(Ga)と比例させてS = k (内径) がk = 0.5から5となるように調整することが重要である。間隙相互の離隔距離は手動測微計を使って制御した。大きな径の針を使用した場合は、壁剪断応力は急速に降下した(表1を参照のこと)。小さいゲージの針(Ga = 10から14)を平坦底面壁に向けるとともに低流量(~0.1ミリリットル/秒)を採用することにより、管壁剪断応力は1ダイン/平方センチメートル未満に維持することができた。このような構成で、試料解離は衝突フローを制御することにより生じた。衝突フローにより細胞は極めて短時間(マイクロ秒単位)の間に細長い剪断力の炸裂を受けることができた。凝体と衝突する衝突フローが「非線形」である程度は大きくなり、分散を果たすための閾レベルが衝突フローの限界域に近くなる場合がそうである。穿刺吸引法における結着力の強い試料構造(間質組織)は衝突フローの後で標準的な管内フローに当てられることを必要とする場合がある。これは、容器の底面に関連する針位置を制御するためにステッパモーターを使用することにより、自動方式で容易に達成することができた。
【0165】
<<細胞活性化研究>>
細胞試料を破砕する流体条件を判断するための研究の最初の一区切りがついた後で、細胞膜の保全性について細胞凝集塊を解析し(トリパンブルー染色法および生死判定染色法)、細胞アポトーシスについて解析し(細胞透過性カスパーゼ3蛍光生成評価分析法)、更に、細胞活性度について解析した(FOS染色法)。明確な対照例として、MCF−7については細胞生存度の喪失の原因である諸条件は既に周知であった。掻爬された単層中で、細胞核の5%未満がFOS陽性である。FOS陽性の細胞核が15%未満であるというのが、掻爬単層を破砕して小型の凝集塊にする剪断条件である。アポトーシス調査については、細胞を分散させてから半時間から1時間に亘って保温培養することで、分散後のアポトーシス開始を評価することができた。
【0166】
<<緩衝剤の調整法>>
試料分散を向上させるとともに細胞活性化を最小限に抑えるように分散緩衝剤を調整することができる。エチレンジアミン四酢酸(EDTA)を使った細胞外カルシウムのキレート化により複数の細胞を一緒に保有している接合部の解体を容易にすることができた。エチレンジアミン四酢酸(5ミリモル、pH 7.4)に晒した後で再石灰化する処理それだけで単独の細胞刺激となることを検証した。掻爬単層試料の分散中に反応性酸素を生じた結果として細胞活性化を招くことがある。N-アセチル-L-システイン(NAC、5ミリモル)が細胞分散中のFOS蛋白誘導を低減した。最後に、0.2 %(w/v)のプルロニックF68は重合体添加物であるが、異なる細胞膜システム中における細胞膜相互作用による細胞保護作用については既に前段までに披露した。
【実施例10】
【0167】
<<10. 細胞の量>>
400ダイン/平方センチメートルの壁剪断応力を利用した先の実施例と同様に分散処理されたHCT−116細胞およびMCF−7細胞に対して、細胞保護剤を使って核酸を安定化した。キアゲン社の抽出技術を利用してDNAおよびRNAを抽出した。解析に付すのに適正なRNAレベルおよびDNAレベルを達成するのに必要な細胞個数を判定した。細胞から採取されたRNAを評価するのに、無欠RNA個体数評価法(RIN評価法)、光学密度260/280評価法、および、RNAの総マイクログラム量評価法を採用した。このような実験で確認できたこととして、例えば、DNA解析およびRNA解析には10万個を越える数の細胞の試料寸法が適切であることが挙げられる。
【0168】

このような結果は図13および図14においても図表で例示されている。
【実施例11】
【0169】
<<11. 細胞計数>>
先の実施例において分散された試料について(MCF−7およびHCT−116)、細胞計数を検証し、結像室に搬入される細胞懸濁液の1分割量として10マイクロリットルから100マイクロリットルが有効であるとの実証を得た。画像計数値を血球計算装置評点およびコールター製計数装置評点の両方と比較した。凝集塊の解析については、トリプシンおよび単一細胞計数法を利用した完璧な分散を果たすために試料を複数の部分集合に分割する方法を採用することで、画像処理アルゴリズムの有効性を実証した。コールター製計数装置を使って、振り分け機能を採用することで寸法分布を得ることができた。
【0170】
<<細胞核計数培検計画案および画像処理>>
細胞核を蛍光着色処理することの利点は、細胞核が特に大きく、単層培養細胞および懸濁液中浮遊細胞に混じっても容易に識別される分離した細胞物体である点である。細胞分離または細胞溶解分離を実施せずに単一工程で細胞計数を実施するのに有効な画像化方法では、染料は以下のような基準に適っているべきであることを検証した。すなわち、(1)固定化工程−洗浄工程−染色工程−洗浄工程という複雑な培検計画を必要とせずに細胞に適用することができなければならない、(2)低価格のダイオードまたはレーザーで利用できる波長で容易に励起されなければならない、(3)高い信号対バックグラウンド比を生じなければならない、(4)膜透過性SYTO-11およびSYTO-16(インヴィトロゲン社製)などのような即効性細胞染料を生じなければならない。紫外線染料(4',6-ジアミジノ-2-フェニリンドール(DAPI)、ヘキスト33342(Hoescht 33342)など)は上記基準の大半に適っているものの、紫外線源を必要とし、結像システムを小型化して経済効率を高める必要が生じた場合に、フェーズ2の損失となる。着脱自在チャンバー搭載スライド(ラブ・テク(商標Lab-Tek)、チャンバースライズ(商標Chamber Slides)、ヌンク(商品名Nunc)−1ウエルあたりの培養面積0.4平方センチメートル、作業容量マイクロリットル)における画像化処理の前に5分までの期間に亘り10ミリモルのSYTO-11(S7573、励起波長508 nm、蛍光波長527 nm)または10マイクロモルのSYTO-16(S7578、励起波長488 nm、蛍光波長527 nm)中で細胞を保温培養した。アドービ・フォトショップ(5.5版)およびディジタルカメラ(Kontron Elektronik Prog/Res/3012)を付帯させた光学顕微鏡(Olympus)を使ってディジタル画像を得た。目視検査と画像解析ソフト(NIH Image)の両方により画像に評点を付けて細胞核計数処理に付した。この評点を血球計算装置評点およびコールター製計数装置評点の両方と比較した。目標は即時的高精度細胞核計数培検計画案を開発することであり、ここでは、100マイクロリットルの細胞懸濁液を10マイクロリットルの染色溶液に添加してから、5分の保温培養の後に青色励起と緑色蛍光の発光により画像化処理を行った。上述のように選択された2種類の染料が不適当である場合は、SYTOシリーズ製品の中から幾つかの代用品が利用できる。同様に、透過性細胞核染料サイトラックオレンジ(CyTRAK Orange、バイオステイタス・リミティッド(Biostatus Ltd.)社製、励起波長488 nm、蛍光波長615 nm)が上述のような応用例に好適であることを実証した。
【0171】
小型凝集塊中の細胞核を高精度に計数する処理は、細胞単層中または単一細胞が浮遊する懸濁液中の細胞核を計数する処理よりも遥かに困難である。エッジ検出およびより複雑なバックグラウンドが原因で画像解析ソフトに誤差が生じる恐れがある。高精度と一貫性を確保するために、完全なトリプシン・エチレンジアミン四酢酸(EDTA)分散処理により得られた細胞計数値との比較を行うことで、どのような杜撰さが存在しているかを平均細胞集団寸法、細胞集団寸法分布、および、細胞集団の密度と画像面積の関数として測定した。必要ならば、シグナル範囲、バックグラウンド減算、閾値設定、オブジェクト検出、および、粒子計数を確定するために、未決定事項に寸法基準および強度基準を加えるとよい。
【0172】
上述の各実施例は本発明の考え得る実施形態を例示したものである。幾つかの実施例に言及しながら本発明を詳細に図示して説明してきたが、このような実施例は具体例として提示されてきたにすぎず、よって、限定するものではなく、本発明の真髄および範囲から外れることなく上述の実施例に多様な形式変更および細部修正を施すことができることが当業者には分かる。従って、本発明の外延および範囲は上述の具体的な実施例のいずれによっても制限されるべきではなく、添付の特許請求の範囲の各請求項およびそれらの均等物に従ってのみ限定されるべきである。本明細書で使用されている見出しはいずれも、編成のためにのみ提示されたものであって、特にそれと示唆していない限り、本明細書を分割したり何らかの意味を与えるものと解釈するべきではない。
【0173】
本明細書で引例に挙がっている文献は全て、ウエブサイト、雑誌掲載論文、論文要旨、公開済みまたは関連する米国特許出願または外国特許出願、交付済み特許または外国特許、それ以外の文献を含めていずれも、その各々の全体は本明細書で引例に挙げることにより本件の一部を構成しており、引例に挙がった文献に提示されているデータ、表、図面、および、テキストの全てを網羅するものとする。
【特許請求の範囲】
【請求項1】
被検体から採取した細胞凝集塊を処理または調製して生組織試料にする方法であって、
a.被検体から採取した生細胞凝集塊を水溶液中で解離および分散することで少なくとも1分割量の生細胞含有部分検査標本液を第1隔離室に入れる工程と、
b.任意で、混入細胞を除去することにより標的細胞の残余の異なる種類の混入細胞に対する割合を増大させるように前記1分割量の部分検査標本を高純度化する工程と、
c.前記任意で高純度化された生細胞を1個以上の第2隔離室に分配して解析に備える工程と、
d.前記分配された細胞を安定化させて、分配された細胞の細胞解析、分子解析、または、その両方の解析を行えるようにした工程とを含んでいる、方法。
【請求項2】
前記生細胞は所定量の機械的剪断応力を使って分散させられることを特徴とする、請求項1に記載の方法。
【請求項3】
前記細胞は最小限の細胞活性化または最小限の剪断応力で生きたままの状態で処理されることを特徴とする、請求項1に記載の方法。
【請求項4】
処理される前記細胞凝集塊の総個体数は約1000から10×106の間であることを特徴とする、請求項1に記載の方法。
【請求項5】
前記細胞凝集塊は被検体から固形腫瘍生検試料として採取された癌の生細胞であることを特徴とする、請求項1に記載の方法。
【請求項6】
前記試料は穿刺吸引技術を利用して採取されることを特徴とする、請求項5に記載の方法。
【請求項7】
分配された細胞を安定化させる前記工程は、被検体から前記試料を採取してから4時間以内に完了することを特徴とする、請求項5に記載の方法。
【請求項8】
少なくとも1種類の薬剤を投与することにより標的である1種類以上の体外生体マーカーまたは体外生体分子に測定可能な定量効果または定性効果を生じることにより、前記分散された細胞または分配された細胞を解析する工程を更に含んでいる、請求項5に記載の方法。
【請求項9】
前記定量効果または定性効果は、代謝経路、複製経路、細胞シグナル発生経路、腫瘍形成シグナル発生経路、アポトーシス経路、血管新生誘導経路などから構成されているグループから選択された細胞経路の活性化または抑制であることを特徴とする、請求項8に記載の方法。
【請求項10】
前記定量効果または定性効果は、G蛋白質共役受容体、または、受容体型チロシンキナーゼに対するアゴニスト的代用効果またはアンタゴニスト的拮抗効果の測定値のことであることを特徴とする、請求項8に記載の方法。
【請求項11】
前記受容体型チロシンキナーゼは上皮細胞成長因子受容体(EGFR)であることを特徴とする、請求項8に記載の方法。
【請求項12】
測定される前記定量効果または定性効果は、即時型または遅延型の初期遺伝子系統のメンバーから構成されているグループから選択された遺伝子の発現レベルのことであることを特徴とする、請求項8に記載の方法。
【請求項13】
前記体外生体マーカーは、イオン、酵素、脂質、遺伝子情報翻訳後修飾蛋白質などから構成されているグループから選択されることを特徴とする、請求項8に記載の方法。
【請求項14】
前記方法は、前記分散された細胞または分配された細胞に検査試薬を投与する工程を更に含んでおり、前記検査試薬は、医薬品、細胞刺激剤、ポリペプチド、ポリヌクレオチド、抗体、Fab分屑、Fc分屑、RNA、siRNA、燐蛋白質などから構成されているグループから選択され、前記方法は、検査試薬を投与する前記工程に続いて実施され、前記分散された細胞または分配された細胞の標的体外生体マーカーまたは標的体外生体分子に対する定量効果または定性効果を測定する工程を更に含んでいる、請求項5に記載の方法。
【請求項15】
前記検査試薬は、酵素、蛍光物質、発光物質、生体発光物質、放射性物質、陽電子断層撮影法で利用される陽電子射出物質、非放射性常磁性金属イオンなどから構成されているグループから選択された検出可能な薬剤を含んでいることを特徴とする、請求項5に記載の方法。
【請求項16】
前記高純度化された癌の生細胞が1個以上の隔離室に分配される前に、前記検査試薬は少なくとも1個の隔離室に事前装填されていることを特徴とする、請求項14に記載の方法。
【請求項17】
前記被検体はヒトを含む哺乳類であり、前記方法は治療の時点で実施されることを特徴とする、請求項5に記載の方法。
【請求項18】
前記第2隔離室は前記高純度化された細胞を個数にして約100万個未満包含していることを特徴とする、請求項5に記載の方法。
【請求項19】
前記細胞は約100ダイン/平方センチメートル(dyne/cm2)から約800ダイン/平方センチメートルの間の剪断力によって分散されることを特徴とする、請求項2に記載の方法。
【請求項20】
高純度化する前記工程は免疫除去工程を含んでいることを特徴とする、請求項1に記載の方法。
【請求項21】
硝子スライド上で前記分配された細胞の少なくとも一部を重合体中に固定する工程を更に含んでいる、請求項1に記載の方法。
【請求項22】
前記分配された細胞の一部に溶解分離剤を投与する工程を更に含んでいる、請求項1に記載の方法。
【請求項23】
固形腫瘍を処理または調製して癌細胞を採取する方法であって、
a.固形腫瘍を解離および分散することで少なくとも1分割量の癌の生細胞含有部分検査標本を第1隔離室に入れる工程と、
b.任意で、混入細胞を除去ように前記癌の生細胞を高純度化する工程と、
c.前記高純度化された癌の生細胞を1個以上の第2隔離室に分配して解析に備える工程と、
d.前記分配された細胞を安定化させて、分配された細胞の細胞解析、分子解析、または、その両方の解析を行えるようにした工程とを含んでいる、方法。
【請求項24】
前記分配する工程は手動で実施されるか、または、自動システムを使用して実施されることを特徴とする、請求項23に記載の方法。
【請求項25】
前記解離する工程は、固形腫瘍由来の癌細胞を含有している液体を所定寸法の針先端具またはピペット先端具に所定の力で吸引して通す工程を含んでいることを特徴とする、請求項23に記載の方法。
【請求項26】
前記分配された癌の生細胞は、前記分配する工程より前に前記液体中に存在していた生存適性を有する癌細胞の個体数と比較した場合、約75%を超過する生存度を示していることを特徴とする、請求項23に記載の方法。
【請求項27】
被検体から採取した癌の生細胞を処理または調製する際に使用するのに好適であり、複数の無菌小室が設けられているカートリッジであって、前記小室を互いから隔離状態にすることができることを特徴とする、カートリッジ。
【請求項28】
前記カートリッジ上の所定位置に少なくとも1個の着脱自在なバイアルを更に備えている、請求項27に記載のカートリッジ。
【請求項29】
複数の小室が設けられているカートリッジであって、前記複数の小室の具体例として、細胞を分散させる小室、細胞を高純度化する小室、隔離室として機能する小室などがあることを特徴とする、カートリッジ。
【請求項30】
前記複数の小室のうちの少なくとも1個は、前記カートリッジ上の所定位置に設けられた着脱自在はバイアルであることを特徴とする、請求項29に記載のカートリッジ。
【請求項31】
バーコードを更に備えている、請求項29に記載のカートリッジ。
【請求項32】
細胞計数機構を更に備えている、請求項29に記載のカートリッジ。
【請求項33】
前記複数の小室のうちの少なくとも1個は刺し通し可能な封鎖部により被覆されていることを特徴とする、請求項29に記載のカートリッジ。
【請求項34】
約1個から約96個のウエルが設けられている、請求項29に記載のカートリッジ。
【請求項35】
請求項29に記載のカートリッジおよび解析装置を備えており、癌の生細胞を処理するのに好適なシステム。
【請求項36】
治療の時点で解析判定結果を生じることを特徴とする、請求項35に記載のシステム。
【請求項37】
請求項29に記載のカートリッジを備えている検査キット。
【請求項38】
前記検査キットは治療の時点で使用されることを特徴とする、請求項37に記載の検査キット。
【請求項39】
前記検査キットは調査研究現場で使用されることを特徴とする、請求項37に記載の検査キット。
【請求項40】
使用説明書を更に備えている、請求項37に記載の検査キット。
【請求項1】
被検体から採取した細胞凝集塊を処理または調製して生組織試料にする方法であって、
a.被検体から採取した生細胞凝集塊を水溶液中で解離および分散することで少なくとも1分割量の生細胞含有部分検査標本液を第1隔離室に入れる工程と、
b.任意で、混入細胞を除去することにより標的細胞の残余の異なる種類の混入細胞に対する割合を増大させるように前記1分割量の部分検査標本を高純度化する工程と、
c.前記任意で高純度化された生細胞を1個以上の第2隔離室に分配して解析に備える工程と、
d.前記分配された細胞を安定化させて、分配された細胞の細胞解析、分子解析、または、その両方の解析を行えるようにした工程とを含んでいる、方法。
【請求項2】
前記生細胞は所定量の機械的剪断応力を使って分散させられることを特徴とする、請求項1に記載の方法。
【請求項3】
前記細胞は最小限の細胞活性化または最小限の剪断応力で生きたままの状態で処理されることを特徴とする、請求項1に記載の方法。
【請求項4】
処理される前記細胞凝集塊の総個体数は約1000から10×106の間であることを特徴とする、請求項1に記載の方法。
【請求項5】
前記細胞凝集塊は被検体から固形腫瘍生検試料として採取された癌の生細胞であることを特徴とする、請求項1に記載の方法。
【請求項6】
前記試料は穿刺吸引技術を利用して採取されることを特徴とする、請求項5に記載の方法。
【請求項7】
分配された細胞を安定化させる前記工程は、被検体から前記試料を採取してから4時間以内に完了することを特徴とする、請求項5に記載の方法。
【請求項8】
少なくとも1種類の薬剤を投与することにより標的である1種類以上の体外生体マーカーまたは体外生体分子に測定可能な定量効果または定性効果を生じることにより、前記分散された細胞または分配された細胞を解析する工程を更に含んでいる、請求項5に記載の方法。
【請求項9】
前記定量効果または定性効果は、代謝経路、複製経路、細胞シグナル発生経路、腫瘍形成シグナル発生経路、アポトーシス経路、血管新生誘導経路などから構成されているグループから選択された細胞経路の活性化または抑制であることを特徴とする、請求項8に記載の方法。
【請求項10】
前記定量効果または定性効果は、G蛋白質共役受容体、または、受容体型チロシンキナーゼに対するアゴニスト的代用効果またはアンタゴニスト的拮抗効果の測定値のことであることを特徴とする、請求項8に記載の方法。
【請求項11】
前記受容体型チロシンキナーゼは上皮細胞成長因子受容体(EGFR)であることを特徴とする、請求項8に記載の方法。
【請求項12】
測定される前記定量効果または定性効果は、即時型または遅延型の初期遺伝子系統のメンバーから構成されているグループから選択された遺伝子の発現レベルのことであることを特徴とする、請求項8に記載の方法。
【請求項13】
前記体外生体マーカーは、イオン、酵素、脂質、遺伝子情報翻訳後修飾蛋白質などから構成されているグループから選択されることを特徴とする、請求項8に記載の方法。
【請求項14】
前記方法は、前記分散された細胞または分配された細胞に検査試薬を投与する工程を更に含んでおり、前記検査試薬は、医薬品、細胞刺激剤、ポリペプチド、ポリヌクレオチド、抗体、Fab分屑、Fc分屑、RNA、siRNA、燐蛋白質などから構成されているグループから選択され、前記方法は、検査試薬を投与する前記工程に続いて実施され、前記分散された細胞または分配された細胞の標的体外生体マーカーまたは標的体外生体分子に対する定量効果または定性効果を測定する工程を更に含んでいる、請求項5に記載の方法。
【請求項15】
前記検査試薬は、酵素、蛍光物質、発光物質、生体発光物質、放射性物質、陽電子断層撮影法で利用される陽電子射出物質、非放射性常磁性金属イオンなどから構成されているグループから選択された検出可能な薬剤を含んでいることを特徴とする、請求項5に記載の方法。
【請求項16】
前記高純度化された癌の生細胞が1個以上の隔離室に分配される前に、前記検査試薬は少なくとも1個の隔離室に事前装填されていることを特徴とする、請求項14に記載の方法。
【請求項17】
前記被検体はヒトを含む哺乳類であり、前記方法は治療の時点で実施されることを特徴とする、請求項5に記載の方法。
【請求項18】
前記第2隔離室は前記高純度化された細胞を個数にして約100万個未満包含していることを特徴とする、請求項5に記載の方法。
【請求項19】
前記細胞は約100ダイン/平方センチメートル(dyne/cm2)から約800ダイン/平方センチメートルの間の剪断力によって分散されることを特徴とする、請求項2に記載の方法。
【請求項20】
高純度化する前記工程は免疫除去工程を含んでいることを特徴とする、請求項1に記載の方法。
【請求項21】
硝子スライド上で前記分配された細胞の少なくとも一部を重合体中に固定する工程を更に含んでいる、請求項1に記載の方法。
【請求項22】
前記分配された細胞の一部に溶解分離剤を投与する工程を更に含んでいる、請求項1に記載の方法。
【請求項23】
固形腫瘍を処理または調製して癌細胞を採取する方法であって、
a.固形腫瘍を解離および分散することで少なくとも1分割量の癌の生細胞含有部分検査標本を第1隔離室に入れる工程と、
b.任意で、混入細胞を除去ように前記癌の生細胞を高純度化する工程と、
c.前記高純度化された癌の生細胞を1個以上の第2隔離室に分配して解析に備える工程と、
d.前記分配された細胞を安定化させて、分配された細胞の細胞解析、分子解析、または、その両方の解析を行えるようにした工程とを含んでいる、方法。
【請求項24】
前記分配する工程は手動で実施されるか、または、自動システムを使用して実施されることを特徴とする、請求項23に記載の方法。
【請求項25】
前記解離する工程は、固形腫瘍由来の癌細胞を含有している液体を所定寸法の針先端具またはピペット先端具に所定の力で吸引して通す工程を含んでいることを特徴とする、請求項23に記載の方法。
【請求項26】
前記分配された癌の生細胞は、前記分配する工程より前に前記液体中に存在していた生存適性を有する癌細胞の個体数と比較した場合、約75%を超過する生存度を示していることを特徴とする、請求項23に記載の方法。
【請求項27】
被検体から採取した癌の生細胞を処理または調製する際に使用するのに好適であり、複数の無菌小室が設けられているカートリッジであって、前記小室を互いから隔離状態にすることができることを特徴とする、カートリッジ。
【請求項28】
前記カートリッジ上の所定位置に少なくとも1個の着脱自在なバイアルを更に備えている、請求項27に記載のカートリッジ。
【請求項29】
複数の小室が設けられているカートリッジであって、前記複数の小室の具体例として、細胞を分散させる小室、細胞を高純度化する小室、隔離室として機能する小室などがあることを特徴とする、カートリッジ。
【請求項30】
前記複数の小室のうちの少なくとも1個は、前記カートリッジ上の所定位置に設けられた着脱自在はバイアルであることを特徴とする、請求項29に記載のカートリッジ。
【請求項31】
バーコードを更に備えている、請求項29に記載のカートリッジ。
【請求項32】
細胞計数機構を更に備えている、請求項29に記載のカートリッジ。
【請求項33】
前記複数の小室のうちの少なくとも1個は刺し通し可能な封鎖部により被覆されていることを特徴とする、請求項29に記載のカートリッジ。
【請求項34】
約1個から約96個のウエルが設けられている、請求項29に記載のカートリッジ。
【請求項35】
請求項29に記載のカートリッジおよび解析装置を備えており、癌の生細胞を処理するのに好適なシステム。
【請求項36】
治療の時点で解析判定結果を生じることを特徴とする、請求項35に記載のシステム。
【請求項37】
請求項29に記載のカートリッジを備えている検査キット。
【請求項38】
前記検査キットは治療の時点で使用されることを特徴とする、請求項37に記載の検査キット。
【請求項39】
前記検査キットは調査研究現場で使用されることを特徴とする、請求項37に記載の検査キット。
【請求項40】
使用説明書を更に備えている、請求項37に記載の検査キット。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20A】


【図20B】


【図21A】


【図21B】


【図22】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20A】


【図20B】


【図21A】


【図21B】


【図22】


【公表番号】特表2011−501190(P2011−501190A)
【公表日】平成23年1月6日(2011.1.6)
【国際特許分類】
【出願番号】特願2010−531056(P2010−531056)
【出願日】平成20年10月24日(2008.10.24)
【国際出願番号】PCT/US2008/012148
【国際公開番号】WO2009/055052
【国際公開日】平成21年4月30日(2009.4.30)
【出願人】(510114734)バイオマーカー ストラテジーズ リミテッド ライアビリティ カンパニー (1)
【Fターム(参考)】
【公表日】平成23年1月6日(2011.1.6)
【国際特許分類】
【出願日】平成20年10月24日(2008.10.24)
【国際出願番号】PCT/US2008/012148
【国際公開番号】WO2009/055052
【国際公開日】平成21年4月30日(2009.4.30)
【出願人】(510114734)バイオマーカー ストラテジーズ リミテッド ライアビリティ カンパニー (1)
【Fターム(参考)】
[ Back to top ]

