細胞増殖因子産生促進剤
【課題】細胞増殖因子の産生を促進する、細胞増殖因子産生促進剤を提供する。
【解決手段】ニンジンの抽出物を有効成分とすることを特徴とする細胞増殖因子産生促進剤である。好適には、アンフィレグリンの産生を促進するする細胞増殖因子産生促進剤である。また、好適には、インヒビン又はアクチビンの産生を促進する細胞増殖因子産生促進剤である。また、好適には、PTGS2の産生を促進する細胞増殖因子産生促進剤である。
【解決手段】ニンジンの抽出物を有効成分とすることを特徴とする細胞増殖因子産生促進剤である。好適には、アンフィレグリンの産生を促進するする細胞増殖因子産生促進剤である。また、好適には、インヒビン又はアクチビンの産生を促進する細胞増殖因子産生促進剤である。また、好適には、PTGS2の産生を促進する細胞増殖因子産生促進剤である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、細胞増殖因子産生促進剤に関し、詳しくは、ニンジンの抽出物を有効成分とする、細胞増殖因子の産生を促進する細胞増殖因子産生促進剤に関する。
【背景技術】
【0002】
細胞増殖因子は、細胞増殖や細胞分化に関与する生体物質であり、主なものとして、トランスフォーミング増殖因子(TGF)、上皮増殖因子(EGF)、肝細胞増殖因子(HGF)が挙げられる。その多くはシグナル分子であり、標的細胞の特定の受容体(TGF受容体、EGF受容体、HGF受容体等)に結合して細胞増殖等を誘引する。近年、細胞増殖因子の制御による疾病や外傷の治療法が研究開発されている。
【0003】
アンフィレグリン(Amphiregulin)はTGF受容体とEGF受容体の両方に結合する増殖因子であり、表皮細胞の増殖を促進する効果や癌細胞の成長を阻害する効果が報告されている(非特許文献1)。アンフィレグリンを利用した疾病の治療法の例として、特許文献1には急性肝障害の治療にアンフィレグリンが有用であることが記載されている。また、特許文献2には、アンフィレグリンは包皮繊維芽細胞の増殖を誘導し創傷治癒に効果があることが記載されている。
【0004】
インヒビン(Inhibin)及びアクチビン(Actibin)はトランスフォーミング増殖因子に属する増殖因子である。インヒビンは、サブユニットであるインヒビンα(INHA)及びインヒビンβA(INHBA)又はβB(INHBB)からなる二量体タンパク質である。アクチビンは、インヒビンβA同士、インヒビンβB同士又はインヒビンβAとβBの組み合わせからなる二量体タンパク質である。アクチビンが卵胞刺激ホルモンの合成と分泌を促進する一方、インヒビンは卵胞刺激ホルモンの分泌を特異的に抑制する。その他にもアクチビンは、成長ホルモンや副腎皮質刺激ホルモンの合成と分泌や、胎盤および性腺ステロイドの合成等の種々の生物活性を有している。アクチビン及びインヒビンの制御による医療応用として、例えば、特許文献3には、アクチビン又はインヒビンの刺激因子を利用した創傷及び線維性障害の治癒を促進する医薬組成物が記載されている。
【0005】
プロスタグランジン(Prostaglandin)は、生体内ではアラキドン酸にPTGS2(Prostaglandin-endoperoxidesynthase 2)が作用して合成される生体物質であり、その様々な生理活性の一つとして肝細胞増殖因子の誘引作用が知られている。例えば、特許文献4には、プロスタグランジンを有効成分とする肝細胞増殖因子誘引剤が記載されており、脳血管障害、脳神経細胞障害、虚血性脳障害、痴呆症、糖尿病等に起因する中枢及び末梢の神経障害の予防薬あるいは治療薬として有効である旨が記載されている。また、特許文献5に記載されているように、プロスタグランジンが養毛育毛効果を有することも知られている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特表2008−506754号公報
【特許文献2】米国特許出願第5,115,096号公報
【特許文献3】特表平11−514373号公報
【特許文献4】特開平11−322612号公報
【特許文献5】特開平05−331025号公報
【非特許文献】
【0007】
【非特許文献1】Mol. Cell. Biol., 1990, 10, 1969-1981
【発明の概要】
【発明が解決しようとする課題】
【0008】
上記のように細胞増殖因子の制御による疾病や外傷の治療法が報告されている。しかしながら、細胞増殖因子の制御に限られることではないが、分子生物学的手法等により人工的に産生した分子を制御に用いる場合には、その人工的な産生に起因して生じた副産物を精製で除去しきれないことがあった。また、天然には存在しない副産物が生じてしまう恐れもあり、所望の効果の阻害や、予期し得ないような悪影響を及ぼしてしまう安全性におけるリスクがあった。
【0009】
そこで本発明の目的は、天然成分由来の細胞増殖因子産生促進剤を提供することにある。
【課題を解決するための手段】
【0010】
本発明者等は、上記課題を解決すべく鋭意検討した結果、生薬として知られているニンジンの抽出物が、細胞増殖因子の産生を促進しうることを見出し、本発明を完成するに至った。
【0011】
即ち、本発明の細胞増殖因子産生促進剤は、ニンジンの抽出物を有効成分とすることを特徴とするものである。
【0012】
本発明の細胞増殖因子産生促進剤は、アンフィレグリン(Amphiregulin)の産生を促進するものであることが好ましい。
【0013】
また、本発明の細胞増殖因子産生促進剤は、インヒビン(Inhibin)またはアクチビン(Actibin)の産生を促進するものであることが好ましい。
【0014】
また、本発明の細胞増殖因子産生促進剤は、前記細胞増殖因子として、サブユニットとしてインヒビンβAを有するインヒビンまたはアクチビンの産生を促進するものであることが好ましい。
【0015】
また、本発明の細胞増殖因子産生促進剤は、前記細胞増殖因子として、アクチビンAの産生を促進するものであることが好ましい。
【0016】
また、本発明の細胞増殖因子産生促進剤は、PTGS2(Prostaglandin-endoperoxidesynthase 2)の産生を促進するものであることが好ましい。
【0017】
また、本発明の細胞増殖因子産生促進剤は、育毛剤以外に用いられることが好ましい。
【0018】
また、本発明の細胞増殖因子産生促進剤は、前記ニンジンの抽出物がエタノール抽出物または含水エタノール抽出物であることが好ましい。
【発明の効果】
【0019】
本発明により、細胞増殖因子の産生を促進する、細胞増殖因子産生促進剤を提供することができる。また、生薬として既に広く利用されているニンジンの抽出物を有効成分とすることから、高い安全性を備えた細胞増殖因子産生促進剤を提供することができる。
【図面の簡単な説明】
【0020】
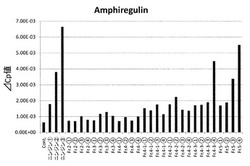
【図1】実施例のアンフィレグリンの産生促進試験の結果を表すグラフである。
【図2】実施例のインヒビンβAの産生促進試験の結果を表すグラフである。
【図3】実施例のPTGS2の産生促進試験の結果を表すグラフである。
【図4】実施例のマウスのアンフィレグリンの産生強度の経時的変化を表すグラフである。
【図5】実施例のマウスのインヒビンβAの産生強度の経時的変化を表すグラフである。
【図6】実施例のマウスのPTGS2の産生強度の経時的変化を表すグラフである。
【図7】実施例のヒト毛乳頭細胞の増殖促進試験の結果を表すグラフである。
【発明を実施するための形態】
【0021】
以下、本発明の実施形態につき詳細に説明する。
本発明は細胞増殖因子産生促進剤に関するものであり、特に、アンフィレグリン、インヒビン又はアクチビンの産生を促進し、また、PTGS2の産生を促進するものである。
【0022】
ニンジンとは、ウコギ科(Araliaceae)のオタネニンジン(Panax ginseng C.A.Meyer)のことであり、特に根の部位を用いるのが好ましい。ニンジンの抽出物(ニンジンエキス)は、滋養強壮剤として用いられている他、血行促進作用があることから、育毛剤として用いられているが、細胞増殖因子の産生促進に関する作用は全く知られていなかった。
【0023】
本発明で用いるニンジンの抽出物は、抽出方法は特に限定されず、公知の方法によりニンジンの成分を抽出したものを用いることができる。例えば、ニンジンを乾燥し、又は、乾燥することなく粉砕した後、常温又は加温下に、溶剤により抽出するか又はソックスレー抽出器等の抽出器具を用いて抽出することにより得られる各種溶媒抽出液、その希釈液、その濃縮液、あるいはその乾燥末が挙げられる。好ましくは溶媒抽出液である。
【0024】
ニンジンの抽出に使用される溶媒は特に限定されず、例えば、水、メタノール、エタノール等の低級アルコール、プロピレングリコール、1,3−ブチレングリコール等の液状多価アルコール、酢酸エチル等の低級アルキルエステル、ベンゼン、ヘキサン等の炭化水素、ジエチルエーテル、アセトン等の公知の溶媒が挙げられる。これらの溶媒は、1種を単独で用いてもよく、2種以上を組み合わせて用いてもよい。これらの中でも水、エタノール(無水エタノール)、プロピレングリコール、1,3−ブチレングリコール若しくはこれらの混液が好ましく、エタノール若しくはエタノールと水の混液である含水エタノールがより好ましく、65%エタノール水溶液が特に好ましい。なお、ニンジンの抽出は常法で行ない、得られたニンジン抽出物はそのまま用いてもよいが、さらに必要により濃縮、濾過等の処理をしたものを用いることができる。
【0025】
また、ニンジン抽出物を、メタノール/水で分配処理して得られた画分、酢酸エチル/水で分配処理して得られた画分、n−ブタノール/水で分配処理して得られた画分等や、ニンジン抽出物又は上記のような画分を、液体クロマトグラフィーにかけ得られた溶出画分等も使用できる。これらの分配処理は、組み合わせて行ってもよい。
【0026】
本発明の細胞増殖因子産生促進剤は、既に生薬として広く利用されているニンジン抽出物を有効成分とするものであり、優れた細胞増殖因子産生促進効果を有し、かつ安全性も高いので、剤型は限定されない。例えば、抽出物をそのまま使用してもよく、抽出物を精製したものを用いてもよい。また、適当な基剤、薬剤などと混合した皮膚外用剤や頭髪化粧料等の外用形態とすることができ、錠剤、カプセル剤、散剤、内服液、細粒剤、顆粒剤等の経口投与剤の形態となすこともできる。具体的には、ローション、乳液、軟膏、クリーム、しっぷ、ジェル、オイル、パック、シャンプー、リンス、トリートメント、ヘアートニック、ヘアーリキッド等の形態を採ることができる。さらに上記のような外用剤の他にも、例えば、石鹸、入浴剤といったものに配合して用いてもよい。
【0027】
ニンジン抽出物を適当な基剤等と混合した組成物として使用する場合ニンジンの配合量は、添加形態および投与形態によっても異なるが、外用剤では、全組成物中0.0001〜90質量%配合することが好ましく、0.001〜50質量%配合することがより好ましく、0.001〜10質量%配合することがさらに好ましい。また、経口投与剤の場合には、ニンジンの投与量が成人1日あたり0.001〜100gになるようにするのが好ましい。
【0028】
本発明の細胞増殖因子産生促進剤には、さらに必要に応じて、本発明の効果を損なわない範囲で、化粧品や医薬品等に一般に用いられている保湿剤、油性成分、界面活性剤、ビタミン類、蛋白分解酵素、増粘剤、防腐剤、粉体、酸化防止剤、紫外線吸収剤、乳化剤、アルコール類、色素、水性成分、脂肪酸類、香料、キレート剤、pH調整剤、精製水等の添加成分を配合することができる。
【0029】
保湿剤としては、例えば、グリセリン、プロピレングリコール、ポリエチレングリコール、1,3−ブチレングリコール等の多価アルコール、ソルビット、マンニット等の糖アルコール、ヒアルロン酸塩、コンドロイチン硫酸塩、キトサン等の水溶性高分子、尿素、乳酸ナトリウム、ピロリドンカルボン酸塩等が挙げられる。
【0030】
油性成分としては、例えば、大豆油、コメヌカ油、アボカド油、アーモンド油、オリーブ油、カカオ脂、ゴマ油、パーシック油、ヒマシ油、ヤシ油、ミンク油、牛脂、豚脂等の天然油脂、これらの天然油脂を水素添加して得られる硬化油及びミリスチン酸グリセリド、2−エチルヘキサン酸グリセリド等の合成グリセリド、ジグリセリド等の油脂類、ホホバ油、カルナウバロウ、鯨ロウ、ミツロウ、ラノリン等のロウ類、流動パラフィン、ワセリン、パラフィン、マイクロクリスタリンワックス、セレシン、スクワラン、プリスタン等の炭化水素類、ラウリン酸、ミリスチン酸、パルミチン酸、ステアリン酸、ベヘン酸、オレイン酸、リノール酸、リノレン酸、ラノリン酸、イソステアリン酸等の高級脂肪酸類、ラウリルアルコール、セチルアルコール、ステアリルアルコール、オレイルアルコール、コレステロール、2−ヘキシルデカノール、ホホバアルコール等の高級アルコール類、オクタン酸セチル、乳酸ミリスチル、乳酸セチル、ミリスチン酸ミリスチル、ミリスチン酸オクチルドデシル、ミリスチン酸イソプロピル、パルミチン酸イソプロピル、アジピン酸イソプロピル、ステアリン酸ブチル、オレイン酸デシル、イソステアリン酸コレステロール等のエステル類、精油類およびシリコーン油類が挙げられる。
【0031】
界面活性剤としては、例えば、グリセリン脂肪酸エステル、プロピレングリコール脂肪酸エステル、ソルビタン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、テトラオレイン酸ポリオキシエチレンソルビット、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンポリオキシプロピレンアルキルエーテル、ポリオキシエチレンアルキルフェニルエーテル、ポリオキシエチレン脂肪酸エステル、ポリエチレングリコール脂肪酸エステル、ポリオキシエチレンヒマシ油、ポリグリセリン脂肪酸エステル、脂肪酸モノグリセライド、ショ糖脂肪酸エステル、高級脂肪酸アルカノールアミド等の非イオン性界面活性剤、α−オレフィンスルホン酸ナトリウム、ラウリル硫酸ナトリウム、セチル硫酸ナトリウム、ポリオキシエチレンラウリル硫酸ナトリウム、スルホコハク酸ラウリル二ナトリウム、直鎖アルキルベンゼンスルホン酸塩、分岐鎖アルキルベンゼンスルホン酸塩、アルキル硫酸塩、アルケニル硫酸塩、エチレンオキサイド及び/又はプロピレンオキサイドを付加したアルキルエーテルカルボン酸塩又はアルケニルエーテルカルボン酸塩、α−スルホ脂肪酸エステル、アミノ酸型界面活性剤、リン酸エステル型界面活性剤、タウリン型界面活性剤、アマイドエーテルサルフェート型界面活性剤等の陰イオン性界面活性剤、カルボキシベタイン型、アミノカルボン酸、スルホベタイン型等の両性界面活性剤および4級アンモニウム塩等の陽イオン性界面活性剤が挙げられる。
【0032】
ビタミン類としては、例えば、ビタミンA、ビタミンB、ビタミンC、ビタミンD、ビタミンE、ビタミンF、ビタミンK、ビタミンP、ビタミンU、カルニチン、フェルラ酸、γ−オリザノール、リポ酸、オロット酸及びその誘導体等が挙げられる。蛋白分解酵素としては、例えば、ペプシン、トリプシン、キモトリプシン、カテプシン、パパイン、ブロメライン、フィシン及び細菌、酵母、カビ由来のプロテアーゼ等が挙げられる。
【0033】
増粘剤としては、例えば、カルボキシビニルポリマー、カルボキシメチルセルロース、ポリビニルアルコール、カラギーナン、ゼラチン、キサンタンガム、ポリアクリル酸塩等の水溶性高分子化合物、塩化ナトリウム、塩化カリウム等の無機塩が挙げられる。防腐剤としては、例えば、フェノキシエタノール、メチルパラベン、エチルパラベン、ブチルパラベン、安息香酸ナトリウム等が挙げられる。粉体としては、例えば、タルク、セリサイト、マイカ、カオリン、シリカ、ベントナイト、バーミキュライト、亜鉛華、雲母、雲母チタン、酸化チタン、酸化マグネシウム、酸化ジルコニウム、硫酸バリウム、ベンガラ、酸化鉄、群青等が挙げられる。その他の成分としては、香料、色素、殺菌剤等を挙げることができる。
【0034】
また、本発明の細胞増殖因子産生促進剤は、他の成分を併用せずにニンジン抽出物だけで用いてもよいが、さらに血行促進剤、局所刺激剤、角質溶解剤、抗脂漏剤、抗菌剤、抗炎症剤、毛包賦活剤、抗男性ホルモン剤等の他の成分と併用してもよい。
【0035】
本発明の細胞増殖因子産生促進剤は、ニンジン抽出物および任意成分を組み合わせて、常法に従って製造することができる。
【0036】
本発明の細胞増殖因子産生促進剤は、細胞増殖因子の産生を促進するが、細胞増殖因子としては、トランスフォーミング増殖因子(TGF)、上皮増殖因子(EGF)及びアンフィレグリンが好ましい。トランスフォーミング増殖因子としてはインヒビン及びアクチビンが好ましく、中でもインヒビンβAをサブユニットとして有するインヒビンまたはアクチビンであるインヒビンA、アクチビンA及びアクチビンABが更に好ましく、インヒビンβAのみをサブユニットとして有するアクチビンAが特に好ましい。
【0037】
本発明の細胞増殖因子産生促進剤は、プロスタグランジンを合成する酵素であるPTGS2(Prostaglandin-endoperoxide synthase 2)の産生を促進することもできる。プロスタグランジンはプロスタン酸骨格を有する有機カルボン酸であり、肝細胞増殖因子の誘引作用や養毛育毛効果が報告されている生体物質である。
【0038】
本願明細書の配列表の配列番号は、以下の配列を示す。
[配列番号:1]
実施例において発現強度の指標としたヒトGAPDHのmRNAの発現を確認するするために用いたプライマーの塩基配列を示す。
[配列番号:2]
実施例において発現強度の指標としたヒトGAPDHのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:3]
実施例においてヒトアンフィレグリンのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:4]
実施例においてヒトアンフィレグリンのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:5]
実施例においてヒトインヒビンβAのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:6]
実施例においてヒトインヒビンβAのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:7]
実施例においてヒトPTGS2のmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:8]
実施例においてヒトPTGS2のmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:9]
実施例において発現強度の指標としたマウスGAPDHのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:10]
実施例において発現強度の指標としたマウスGAPDHのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:11]
実施例においてマウスアンフィレグリンのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:12]
実施例においてマウスアンフィレグリンのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:13]
実施例においてマウスインヒビンβAのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:14]
実施例においてマウスインヒビンβAのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:15]
実施例においてマウスPTGS2のmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:16]
実施例においてマウスPTGS2のmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
【実施例】
【0039】
以下、実施例を用いて本発明をより詳細に説明するが、本発明は実施例により限定されるものではない。
【0040】
(被検試料溶液の調製)
ニンジンの根1kgを65%エタノール30Lに、50℃にて12時間浸漬した後、ろ過することによりニンジン抽出液を得た。
【0041】
希釈していないニンジン抽出液を濃縮して得られた約2.5gの固形物を約5mLの水に懸濁し、DIAION HP-20(三菱化学社製)を用いて、水−メタノール系で溶出し、メタノール0〜100%までの溶出液を順に6つに分画して、それぞれFr.1〜6とした。Fr.4に関しては、その一部をとり、1mLの0.1N NaOHに溶解させて室温にて30分間放置した後、1mLの0.1NHClを加えた。この溶液をDIAION HP-20を充填したカラムにチャージした後、水−メタノール系で溶出し、メタノール0〜100%までの溶出液を順に3つに分画して、それぞれFr.4-1,Fr.4-2, Fr.4-3とした。
【0042】
(産生促進試験)
ヒト毛乳頭細胞(DSファーマバイオメディカル(株))を、細胞濃度が約3×103細胞/100μLになるように、コントロール(0.05%FBS DMEM)、または、上記で得た被検試料溶液(ニンジン抽出液又は分画した各フラクション)を含有する0.05%FBS DMEMで調製して培養液とし、37℃で24時間培養した。培養後、CellAmp Direct RNA Prep kit(TAKARA Bio社製)を用いてTotal RNAを抽出し、Primescript RT Mastermix(TAKARA Bio社製)を用いてcDNAを合成した。アンフィレグリン(Amphiregulin)、インヒビンβA、及び、PTGS2について、合成したcDNAから、LightCycler480 Realtime PCR System(Roche Diagnostics社製)及びKAPA SYBR FAST qPCR Kit(KAPABIOSYSTEMS社製、増幅条件:初期変性として95℃・3分を1サイクル、95℃・10秒、60℃・20秒、72℃・1秒を45サイクル)を用いたリアルタイムPCR解析により、GAPDHのCp値との比較から求めたΔCp値をmRNAの発現強度とし、それぞれの産生促進効果を評価した。なお、ΔCp値は以下の計算式を用いて算出した。
ΔCp値=2^(A‐B)
A:GAPDHのCp値
B:ターゲット遺伝子のCp値
アンフィレグリン、インヒビンβA、及び、PTGS2の発現強度をそれぞれ下記表1〜3及び図1〜3に示す。図1〜3は表1〜3の発現強度をグラフ化したものである。前記リアルタイムPCR解析に用いたGAPDH、アンフィレグリン、インヒビンβA、及び、PTGS2のプライマーの塩基配列を配列表の配列番号1〜8に示す。
【0043】
下記表1〜3及び図1〜3において、ニンジン1、2及び3はニンジン抽出液を含有する0.05%FBS DMEMの結果を表しており、それぞれ、300倍、100倍及び30倍に希釈されたニンジン抽出液を含有する培養液の結果を表している。また、Fr.X-1、2、3及び4(Xはフラクション番号)は上記の各フラクションを含有する0.05%FBS DMEMの結果を表しており、それぞれ、各フラクションを乾燥して得た固形物を0.01、0.03、0.1及び0.3mg/mlの濃度で含有する培養液の結果を表している。
【0044】
【表1】

【0045】
【表2】

【0046】
【表3】

【0047】
(発現強度の経時的変化と毛周期との関連性評価)
C3Hマウスの背部の皮膚を生後0日から経時的に採取し、採取した皮膚からNucleoSpin Triprep kit(TAKARA Bio社製)を用いてTotal RNAを抽出し、Primescript RT Mastermix(TAKARA Bio社製)を用いてcDNAを合成した。アンフィレグリン、インヒビンβA、及び、PTGS2について、合成したcDNAから、LightCycler480 Realtime PCR System(Roche社製)及びKAPA SYBR FAST qPCR Kit(KAPABIOSYSTEMS社製、増幅条件:初期変性として95℃・3分を1サイクル、95℃・10秒、60℃・20秒、72℃・1秒を45サイクル)を用いたリアルタイムPCR解析により、GAPDHのCp値との比較から求めたΔCp値をmRNAの発現強度とした。なお、ΔCp値は以下の計算式を用いて算出した。
ΔCp値=2^(A‐B)
A:GAPDHのCp値
B:ターゲット遺伝子のCp値
アンフィレグリン、インヒビンβA、及び、PTGS2のmRNAの発現強度の生後0日からの経時的変化を下記図4〜6に示す。図4〜6の横軸は生後からの日数、縦軸はΔCp値を表す。なお、マウスの毛周期は、第一周期が約0〜18日、第二周期が約21〜36日である(Kobori T, et al., Medicine of Hair, 1987, 200-214)。前記リアルタイムPCR解析に用いたGAPDH、アンフィレグリン、インヒビンβA、及び、PTGS2のプライマーの塩基配列を配列表の配列番号9〜16に示す。
【0048】
(毛乳頭細胞の増殖促進試験)
ヒト毛乳頭細胞(DSファーマバイオメディカル(株))を、細胞濃度が約3×103細胞/100μLになるように、コントロール(10%FBS含有DMEM培地、または、0.05%FBS含有DMEM培地)、または、上記で得た被検試料溶液(ニンジン抽出液)を含有する0.05%FBS DMEMで調製して培養液とした。37℃で48時間培養した後、Cell counting kit 8(DOJINDO社製)を用いて、波長450nmの吸光度から増殖した細胞数を測定した。10%FBS含有DMEM培地で増殖した細胞数を100%、0.05%FBS含有DMEM培地で増殖した細胞数を0%として、ニンジン抽出液の毛乳頭細胞の増殖促進作用を評価した。結果を下記図7に示す。
【0049】
下記図7において、FBSは10%FBS含有DMEM培地を表している。SK2、3、4及び5はニンジン抽出液を含有する0.05%FBS DMEMの結果を表しており、それぞれ、各フラクションを乾燥して得た固形分を0.3、0.1、0.03及び0.01mg/mlの濃度で含有する培養液を表している。
【0050】
表1〜3及び図1〜3より、本発明の細胞増殖因子産生促進剤は、細胞増殖因子であるアンフィレグリン及びインヒビンβAの産生を、また、PTGS2の産生を促進できることがわかった。また、アンフィレグリンはフラクション4-3及び5、インヒビンβAはフラクション3、4-3及び5、また、PTGS2はフラクション4-3及び5の特定のフラクションに高い産生効果があることがわかった。インヒビンβAについて、これまでの毛乳頭細胞の解析から、インヒビンβA以外のサブユニットの遺伝子については発現が高くなっていなかったことから、アクチビンAの発現がより高まっていると考えられた。
【0051】
図4から、アンフィレグリンの発現強度の変化周期が毛周期と一致していることから、アンフィレグリンが毛包の発達や毛髪の成長に深く関与する因子であることが示唆された。また、図5及び図6から、インヒビンβA及びPTGS2についても、発現強度にばらつきが少しあるものの、発現強度の変化周期と毛周期とに幾分の関連性が見出され、毛包の発達や毛髪の成長への関与する因子であると推察された。
【0052】
図7から、アンフィレグリン、インヒビンβA及びPTGS2の産生促進効果を有する本発明の細胞増殖因子産生促進剤が、ヒト毛乳頭細胞の増殖を促進することが確認された。
【0053】
上記のように、本発明の細胞増殖因子産生促進剤は、細胞増殖因子の産生を促進することができる。本発明の細胞増殖因子産生促進剤は、その細胞増殖因子産生促進作用を利用して、例えば、上記したような疾病の治療の他にも、例えば、創傷治癒剤、肌荒れ改善剤、にきび治療薬としても利用可能である。
【技術分野】
【0001】
本発明は、細胞増殖因子産生促進剤に関し、詳しくは、ニンジンの抽出物を有効成分とする、細胞増殖因子の産生を促進する細胞増殖因子産生促進剤に関する。
【背景技術】
【0002】
細胞増殖因子は、細胞増殖や細胞分化に関与する生体物質であり、主なものとして、トランスフォーミング増殖因子(TGF)、上皮増殖因子(EGF)、肝細胞増殖因子(HGF)が挙げられる。その多くはシグナル分子であり、標的細胞の特定の受容体(TGF受容体、EGF受容体、HGF受容体等)に結合して細胞増殖等を誘引する。近年、細胞増殖因子の制御による疾病や外傷の治療法が研究開発されている。
【0003】
アンフィレグリン(Amphiregulin)はTGF受容体とEGF受容体の両方に結合する増殖因子であり、表皮細胞の増殖を促進する効果や癌細胞の成長を阻害する効果が報告されている(非特許文献1)。アンフィレグリンを利用した疾病の治療法の例として、特許文献1には急性肝障害の治療にアンフィレグリンが有用であることが記載されている。また、特許文献2には、アンフィレグリンは包皮繊維芽細胞の増殖を誘導し創傷治癒に効果があることが記載されている。
【0004】
インヒビン(Inhibin)及びアクチビン(Actibin)はトランスフォーミング増殖因子に属する増殖因子である。インヒビンは、サブユニットであるインヒビンα(INHA)及びインヒビンβA(INHBA)又はβB(INHBB)からなる二量体タンパク質である。アクチビンは、インヒビンβA同士、インヒビンβB同士又はインヒビンβAとβBの組み合わせからなる二量体タンパク質である。アクチビンが卵胞刺激ホルモンの合成と分泌を促進する一方、インヒビンは卵胞刺激ホルモンの分泌を特異的に抑制する。その他にもアクチビンは、成長ホルモンや副腎皮質刺激ホルモンの合成と分泌や、胎盤および性腺ステロイドの合成等の種々の生物活性を有している。アクチビン及びインヒビンの制御による医療応用として、例えば、特許文献3には、アクチビン又はインヒビンの刺激因子を利用した創傷及び線維性障害の治癒を促進する医薬組成物が記載されている。
【0005】
プロスタグランジン(Prostaglandin)は、生体内ではアラキドン酸にPTGS2(Prostaglandin-endoperoxidesynthase 2)が作用して合成される生体物質であり、その様々な生理活性の一つとして肝細胞増殖因子の誘引作用が知られている。例えば、特許文献4には、プロスタグランジンを有効成分とする肝細胞増殖因子誘引剤が記載されており、脳血管障害、脳神経細胞障害、虚血性脳障害、痴呆症、糖尿病等に起因する中枢及び末梢の神経障害の予防薬あるいは治療薬として有効である旨が記載されている。また、特許文献5に記載されているように、プロスタグランジンが養毛育毛効果を有することも知られている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特表2008−506754号公報
【特許文献2】米国特許出願第5,115,096号公報
【特許文献3】特表平11−514373号公報
【特許文献4】特開平11−322612号公報
【特許文献5】特開平05−331025号公報
【非特許文献】
【0007】
【非特許文献1】Mol. Cell. Biol., 1990, 10, 1969-1981
【発明の概要】
【発明が解決しようとする課題】
【0008】
上記のように細胞増殖因子の制御による疾病や外傷の治療法が報告されている。しかしながら、細胞増殖因子の制御に限られることではないが、分子生物学的手法等により人工的に産生した分子を制御に用いる場合には、その人工的な産生に起因して生じた副産物を精製で除去しきれないことがあった。また、天然には存在しない副産物が生じてしまう恐れもあり、所望の効果の阻害や、予期し得ないような悪影響を及ぼしてしまう安全性におけるリスクがあった。
【0009】
そこで本発明の目的は、天然成分由来の細胞増殖因子産生促進剤を提供することにある。
【課題を解決するための手段】
【0010】
本発明者等は、上記課題を解決すべく鋭意検討した結果、生薬として知られているニンジンの抽出物が、細胞増殖因子の産生を促進しうることを見出し、本発明を完成するに至った。
【0011】
即ち、本発明の細胞増殖因子産生促進剤は、ニンジンの抽出物を有効成分とすることを特徴とするものである。
【0012】
本発明の細胞増殖因子産生促進剤は、アンフィレグリン(Amphiregulin)の産生を促進するものであることが好ましい。
【0013】
また、本発明の細胞増殖因子産生促進剤は、インヒビン(Inhibin)またはアクチビン(Actibin)の産生を促進するものであることが好ましい。
【0014】
また、本発明の細胞増殖因子産生促進剤は、前記細胞増殖因子として、サブユニットとしてインヒビンβAを有するインヒビンまたはアクチビンの産生を促進するものであることが好ましい。
【0015】
また、本発明の細胞増殖因子産生促進剤は、前記細胞増殖因子として、アクチビンAの産生を促進するものであることが好ましい。
【0016】
また、本発明の細胞増殖因子産生促進剤は、PTGS2(Prostaglandin-endoperoxidesynthase 2)の産生を促進するものであることが好ましい。
【0017】
また、本発明の細胞増殖因子産生促進剤は、育毛剤以外に用いられることが好ましい。
【0018】
また、本発明の細胞増殖因子産生促進剤は、前記ニンジンの抽出物がエタノール抽出物または含水エタノール抽出物であることが好ましい。
【発明の効果】
【0019】
本発明により、細胞増殖因子の産生を促進する、細胞増殖因子産生促進剤を提供することができる。また、生薬として既に広く利用されているニンジンの抽出物を有効成分とすることから、高い安全性を備えた細胞増殖因子産生促進剤を提供することができる。
【図面の簡単な説明】
【0020】
【図1】実施例のアンフィレグリンの産生促進試験の結果を表すグラフである。
【図2】実施例のインヒビンβAの産生促進試験の結果を表すグラフである。
【図3】実施例のPTGS2の産生促進試験の結果を表すグラフである。
【図4】実施例のマウスのアンフィレグリンの産生強度の経時的変化を表すグラフである。
【図5】実施例のマウスのインヒビンβAの産生強度の経時的変化を表すグラフである。
【図6】実施例のマウスのPTGS2の産生強度の経時的変化を表すグラフである。
【図7】実施例のヒト毛乳頭細胞の増殖促進試験の結果を表すグラフである。
【発明を実施するための形態】
【0021】
以下、本発明の実施形態につき詳細に説明する。
本発明は細胞増殖因子産生促進剤に関するものであり、特に、アンフィレグリン、インヒビン又はアクチビンの産生を促進し、また、PTGS2の産生を促進するものである。
【0022】
ニンジンとは、ウコギ科(Araliaceae)のオタネニンジン(Panax ginseng C.A.Meyer)のことであり、特に根の部位を用いるのが好ましい。ニンジンの抽出物(ニンジンエキス)は、滋養強壮剤として用いられている他、血行促進作用があることから、育毛剤として用いられているが、細胞増殖因子の産生促進に関する作用は全く知られていなかった。
【0023】
本発明で用いるニンジンの抽出物は、抽出方法は特に限定されず、公知の方法によりニンジンの成分を抽出したものを用いることができる。例えば、ニンジンを乾燥し、又は、乾燥することなく粉砕した後、常温又は加温下に、溶剤により抽出するか又はソックスレー抽出器等の抽出器具を用いて抽出することにより得られる各種溶媒抽出液、その希釈液、その濃縮液、あるいはその乾燥末が挙げられる。好ましくは溶媒抽出液である。
【0024】
ニンジンの抽出に使用される溶媒は特に限定されず、例えば、水、メタノール、エタノール等の低級アルコール、プロピレングリコール、1,3−ブチレングリコール等の液状多価アルコール、酢酸エチル等の低級アルキルエステル、ベンゼン、ヘキサン等の炭化水素、ジエチルエーテル、アセトン等の公知の溶媒が挙げられる。これらの溶媒は、1種を単独で用いてもよく、2種以上を組み合わせて用いてもよい。これらの中でも水、エタノール(無水エタノール)、プロピレングリコール、1,3−ブチレングリコール若しくはこれらの混液が好ましく、エタノール若しくはエタノールと水の混液である含水エタノールがより好ましく、65%エタノール水溶液が特に好ましい。なお、ニンジンの抽出は常法で行ない、得られたニンジン抽出物はそのまま用いてもよいが、さらに必要により濃縮、濾過等の処理をしたものを用いることができる。
【0025】
また、ニンジン抽出物を、メタノール/水で分配処理して得られた画分、酢酸エチル/水で分配処理して得られた画分、n−ブタノール/水で分配処理して得られた画分等や、ニンジン抽出物又は上記のような画分を、液体クロマトグラフィーにかけ得られた溶出画分等も使用できる。これらの分配処理は、組み合わせて行ってもよい。
【0026】
本発明の細胞増殖因子産生促進剤は、既に生薬として広く利用されているニンジン抽出物を有効成分とするものであり、優れた細胞増殖因子産生促進効果を有し、かつ安全性も高いので、剤型は限定されない。例えば、抽出物をそのまま使用してもよく、抽出物を精製したものを用いてもよい。また、適当な基剤、薬剤などと混合した皮膚外用剤や頭髪化粧料等の外用形態とすることができ、錠剤、カプセル剤、散剤、内服液、細粒剤、顆粒剤等の経口投与剤の形態となすこともできる。具体的には、ローション、乳液、軟膏、クリーム、しっぷ、ジェル、オイル、パック、シャンプー、リンス、トリートメント、ヘアートニック、ヘアーリキッド等の形態を採ることができる。さらに上記のような外用剤の他にも、例えば、石鹸、入浴剤といったものに配合して用いてもよい。
【0027】
ニンジン抽出物を適当な基剤等と混合した組成物として使用する場合ニンジンの配合量は、添加形態および投与形態によっても異なるが、外用剤では、全組成物中0.0001〜90質量%配合することが好ましく、0.001〜50質量%配合することがより好ましく、0.001〜10質量%配合することがさらに好ましい。また、経口投与剤の場合には、ニンジンの投与量が成人1日あたり0.001〜100gになるようにするのが好ましい。
【0028】
本発明の細胞増殖因子産生促進剤には、さらに必要に応じて、本発明の効果を損なわない範囲で、化粧品や医薬品等に一般に用いられている保湿剤、油性成分、界面活性剤、ビタミン類、蛋白分解酵素、増粘剤、防腐剤、粉体、酸化防止剤、紫外線吸収剤、乳化剤、アルコール類、色素、水性成分、脂肪酸類、香料、キレート剤、pH調整剤、精製水等の添加成分を配合することができる。
【0029】
保湿剤としては、例えば、グリセリン、プロピレングリコール、ポリエチレングリコール、1,3−ブチレングリコール等の多価アルコール、ソルビット、マンニット等の糖アルコール、ヒアルロン酸塩、コンドロイチン硫酸塩、キトサン等の水溶性高分子、尿素、乳酸ナトリウム、ピロリドンカルボン酸塩等が挙げられる。
【0030】
油性成分としては、例えば、大豆油、コメヌカ油、アボカド油、アーモンド油、オリーブ油、カカオ脂、ゴマ油、パーシック油、ヒマシ油、ヤシ油、ミンク油、牛脂、豚脂等の天然油脂、これらの天然油脂を水素添加して得られる硬化油及びミリスチン酸グリセリド、2−エチルヘキサン酸グリセリド等の合成グリセリド、ジグリセリド等の油脂類、ホホバ油、カルナウバロウ、鯨ロウ、ミツロウ、ラノリン等のロウ類、流動パラフィン、ワセリン、パラフィン、マイクロクリスタリンワックス、セレシン、スクワラン、プリスタン等の炭化水素類、ラウリン酸、ミリスチン酸、パルミチン酸、ステアリン酸、ベヘン酸、オレイン酸、リノール酸、リノレン酸、ラノリン酸、イソステアリン酸等の高級脂肪酸類、ラウリルアルコール、セチルアルコール、ステアリルアルコール、オレイルアルコール、コレステロール、2−ヘキシルデカノール、ホホバアルコール等の高級アルコール類、オクタン酸セチル、乳酸ミリスチル、乳酸セチル、ミリスチン酸ミリスチル、ミリスチン酸オクチルドデシル、ミリスチン酸イソプロピル、パルミチン酸イソプロピル、アジピン酸イソプロピル、ステアリン酸ブチル、オレイン酸デシル、イソステアリン酸コレステロール等のエステル類、精油類およびシリコーン油類が挙げられる。
【0031】
界面活性剤としては、例えば、グリセリン脂肪酸エステル、プロピレングリコール脂肪酸エステル、ソルビタン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、テトラオレイン酸ポリオキシエチレンソルビット、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンポリオキシプロピレンアルキルエーテル、ポリオキシエチレンアルキルフェニルエーテル、ポリオキシエチレン脂肪酸エステル、ポリエチレングリコール脂肪酸エステル、ポリオキシエチレンヒマシ油、ポリグリセリン脂肪酸エステル、脂肪酸モノグリセライド、ショ糖脂肪酸エステル、高級脂肪酸アルカノールアミド等の非イオン性界面活性剤、α−オレフィンスルホン酸ナトリウム、ラウリル硫酸ナトリウム、セチル硫酸ナトリウム、ポリオキシエチレンラウリル硫酸ナトリウム、スルホコハク酸ラウリル二ナトリウム、直鎖アルキルベンゼンスルホン酸塩、分岐鎖アルキルベンゼンスルホン酸塩、アルキル硫酸塩、アルケニル硫酸塩、エチレンオキサイド及び/又はプロピレンオキサイドを付加したアルキルエーテルカルボン酸塩又はアルケニルエーテルカルボン酸塩、α−スルホ脂肪酸エステル、アミノ酸型界面活性剤、リン酸エステル型界面活性剤、タウリン型界面活性剤、アマイドエーテルサルフェート型界面活性剤等の陰イオン性界面活性剤、カルボキシベタイン型、アミノカルボン酸、スルホベタイン型等の両性界面活性剤および4級アンモニウム塩等の陽イオン性界面活性剤が挙げられる。
【0032】
ビタミン類としては、例えば、ビタミンA、ビタミンB、ビタミンC、ビタミンD、ビタミンE、ビタミンF、ビタミンK、ビタミンP、ビタミンU、カルニチン、フェルラ酸、γ−オリザノール、リポ酸、オロット酸及びその誘導体等が挙げられる。蛋白分解酵素としては、例えば、ペプシン、トリプシン、キモトリプシン、カテプシン、パパイン、ブロメライン、フィシン及び細菌、酵母、カビ由来のプロテアーゼ等が挙げられる。
【0033】
増粘剤としては、例えば、カルボキシビニルポリマー、カルボキシメチルセルロース、ポリビニルアルコール、カラギーナン、ゼラチン、キサンタンガム、ポリアクリル酸塩等の水溶性高分子化合物、塩化ナトリウム、塩化カリウム等の無機塩が挙げられる。防腐剤としては、例えば、フェノキシエタノール、メチルパラベン、エチルパラベン、ブチルパラベン、安息香酸ナトリウム等が挙げられる。粉体としては、例えば、タルク、セリサイト、マイカ、カオリン、シリカ、ベントナイト、バーミキュライト、亜鉛華、雲母、雲母チタン、酸化チタン、酸化マグネシウム、酸化ジルコニウム、硫酸バリウム、ベンガラ、酸化鉄、群青等が挙げられる。その他の成分としては、香料、色素、殺菌剤等を挙げることができる。
【0034】
また、本発明の細胞増殖因子産生促進剤は、他の成分を併用せずにニンジン抽出物だけで用いてもよいが、さらに血行促進剤、局所刺激剤、角質溶解剤、抗脂漏剤、抗菌剤、抗炎症剤、毛包賦活剤、抗男性ホルモン剤等の他の成分と併用してもよい。
【0035】
本発明の細胞増殖因子産生促進剤は、ニンジン抽出物および任意成分を組み合わせて、常法に従って製造することができる。
【0036】
本発明の細胞増殖因子産生促進剤は、細胞増殖因子の産生を促進するが、細胞増殖因子としては、トランスフォーミング増殖因子(TGF)、上皮増殖因子(EGF)及びアンフィレグリンが好ましい。トランスフォーミング増殖因子としてはインヒビン及びアクチビンが好ましく、中でもインヒビンβAをサブユニットとして有するインヒビンまたはアクチビンであるインヒビンA、アクチビンA及びアクチビンABが更に好ましく、インヒビンβAのみをサブユニットとして有するアクチビンAが特に好ましい。
【0037】
本発明の細胞増殖因子産生促進剤は、プロスタグランジンを合成する酵素であるPTGS2(Prostaglandin-endoperoxide synthase 2)の産生を促進することもできる。プロスタグランジンはプロスタン酸骨格を有する有機カルボン酸であり、肝細胞増殖因子の誘引作用や養毛育毛効果が報告されている生体物質である。
【0038】
本願明細書の配列表の配列番号は、以下の配列を示す。
[配列番号:1]
実施例において発現強度の指標としたヒトGAPDHのmRNAの発現を確認するするために用いたプライマーの塩基配列を示す。
[配列番号:2]
実施例において発現強度の指標としたヒトGAPDHのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:3]
実施例においてヒトアンフィレグリンのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:4]
実施例においてヒトアンフィレグリンのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:5]
実施例においてヒトインヒビンβAのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:6]
実施例においてヒトインヒビンβAのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:7]
実施例においてヒトPTGS2のmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:8]
実施例においてヒトPTGS2のmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:9]
実施例において発現強度の指標としたマウスGAPDHのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:10]
実施例において発現強度の指標としたマウスGAPDHのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:11]
実施例においてマウスアンフィレグリンのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:12]
実施例においてマウスアンフィレグリンのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:13]
実施例においてマウスインヒビンβAのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:14]
実施例においてマウスインヒビンβAのmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:15]
実施例においてマウスPTGS2のmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
[配列番号:16]
実施例においてマウスPTGS2のmRNAの発現を確認するために用いたプライマーの塩基配列を示す。
【実施例】
【0039】
以下、実施例を用いて本発明をより詳細に説明するが、本発明は実施例により限定されるものではない。
【0040】
(被検試料溶液の調製)
ニンジンの根1kgを65%エタノール30Lに、50℃にて12時間浸漬した後、ろ過することによりニンジン抽出液を得た。
【0041】
希釈していないニンジン抽出液を濃縮して得られた約2.5gの固形物を約5mLの水に懸濁し、DIAION HP-20(三菱化学社製)を用いて、水−メタノール系で溶出し、メタノール0〜100%までの溶出液を順に6つに分画して、それぞれFr.1〜6とした。Fr.4に関しては、その一部をとり、1mLの0.1N NaOHに溶解させて室温にて30分間放置した後、1mLの0.1NHClを加えた。この溶液をDIAION HP-20を充填したカラムにチャージした後、水−メタノール系で溶出し、メタノール0〜100%までの溶出液を順に3つに分画して、それぞれFr.4-1,Fr.4-2, Fr.4-3とした。
【0042】
(産生促進試験)
ヒト毛乳頭細胞(DSファーマバイオメディカル(株))を、細胞濃度が約3×103細胞/100μLになるように、コントロール(0.05%FBS DMEM)、または、上記で得た被検試料溶液(ニンジン抽出液又は分画した各フラクション)を含有する0.05%FBS DMEMで調製して培養液とし、37℃で24時間培養した。培養後、CellAmp Direct RNA Prep kit(TAKARA Bio社製)を用いてTotal RNAを抽出し、Primescript RT Mastermix(TAKARA Bio社製)を用いてcDNAを合成した。アンフィレグリン(Amphiregulin)、インヒビンβA、及び、PTGS2について、合成したcDNAから、LightCycler480 Realtime PCR System(Roche Diagnostics社製)及びKAPA SYBR FAST qPCR Kit(KAPABIOSYSTEMS社製、増幅条件:初期変性として95℃・3分を1サイクル、95℃・10秒、60℃・20秒、72℃・1秒を45サイクル)を用いたリアルタイムPCR解析により、GAPDHのCp値との比較から求めたΔCp値をmRNAの発現強度とし、それぞれの産生促進効果を評価した。なお、ΔCp値は以下の計算式を用いて算出した。
ΔCp値=2^(A‐B)
A:GAPDHのCp値
B:ターゲット遺伝子のCp値
アンフィレグリン、インヒビンβA、及び、PTGS2の発現強度をそれぞれ下記表1〜3及び図1〜3に示す。図1〜3は表1〜3の発現強度をグラフ化したものである。前記リアルタイムPCR解析に用いたGAPDH、アンフィレグリン、インヒビンβA、及び、PTGS2のプライマーの塩基配列を配列表の配列番号1〜8に示す。
【0043】
下記表1〜3及び図1〜3において、ニンジン1、2及び3はニンジン抽出液を含有する0.05%FBS DMEMの結果を表しており、それぞれ、300倍、100倍及び30倍に希釈されたニンジン抽出液を含有する培養液の結果を表している。また、Fr.X-1、2、3及び4(Xはフラクション番号)は上記の各フラクションを含有する0.05%FBS DMEMの結果を表しており、それぞれ、各フラクションを乾燥して得た固形物を0.01、0.03、0.1及び0.3mg/mlの濃度で含有する培養液の結果を表している。
【0044】
【表1】

【0045】
【表2】

【0046】
【表3】

【0047】
(発現強度の経時的変化と毛周期との関連性評価)
C3Hマウスの背部の皮膚を生後0日から経時的に採取し、採取した皮膚からNucleoSpin Triprep kit(TAKARA Bio社製)を用いてTotal RNAを抽出し、Primescript RT Mastermix(TAKARA Bio社製)を用いてcDNAを合成した。アンフィレグリン、インヒビンβA、及び、PTGS2について、合成したcDNAから、LightCycler480 Realtime PCR System(Roche社製)及びKAPA SYBR FAST qPCR Kit(KAPABIOSYSTEMS社製、増幅条件:初期変性として95℃・3分を1サイクル、95℃・10秒、60℃・20秒、72℃・1秒を45サイクル)を用いたリアルタイムPCR解析により、GAPDHのCp値との比較から求めたΔCp値をmRNAの発現強度とした。なお、ΔCp値は以下の計算式を用いて算出した。
ΔCp値=2^(A‐B)
A:GAPDHのCp値
B:ターゲット遺伝子のCp値
アンフィレグリン、インヒビンβA、及び、PTGS2のmRNAの発現強度の生後0日からの経時的変化を下記図4〜6に示す。図4〜6の横軸は生後からの日数、縦軸はΔCp値を表す。なお、マウスの毛周期は、第一周期が約0〜18日、第二周期が約21〜36日である(Kobori T, et al., Medicine of Hair, 1987, 200-214)。前記リアルタイムPCR解析に用いたGAPDH、アンフィレグリン、インヒビンβA、及び、PTGS2のプライマーの塩基配列を配列表の配列番号9〜16に示す。
【0048】
(毛乳頭細胞の増殖促進試験)
ヒト毛乳頭細胞(DSファーマバイオメディカル(株))を、細胞濃度が約3×103細胞/100μLになるように、コントロール(10%FBS含有DMEM培地、または、0.05%FBS含有DMEM培地)、または、上記で得た被検試料溶液(ニンジン抽出液)を含有する0.05%FBS DMEMで調製して培養液とした。37℃で48時間培養した後、Cell counting kit 8(DOJINDO社製)を用いて、波長450nmの吸光度から増殖した細胞数を測定した。10%FBS含有DMEM培地で増殖した細胞数を100%、0.05%FBS含有DMEM培地で増殖した細胞数を0%として、ニンジン抽出液の毛乳頭細胞の増殖促進作用を評価した。結果を下記図7に示す。
【0049】
下記図7において、FBSは10%FBS含有DMEM培地を表している。SK2、3、4及び5はニンジン抽出液を含有する0.05%FBS DMEMの結果を表しており、それぞれ、各フラクションを乾燥して得た固形分を0.3、0.1、0.03及び0.01mg/mlの濃度で含有する培養液を表している。
【0050】
表1〜3及び図1〜3より、本発明の細胞増殖因子産生促進剤は、細胞増殖因子であるアンフィレグリン及びインヒビンβAの産生を、また、PTGS2の産生を促進できることがわかった。また、アンフィレグリンはフラクション4-3及び5、インヒビンβAはフラクション3、4-3及び5、また、PTGS2はフラクション4-3及び5の特定のフラクションに高い産生効果があることがわかった。インヒビンβAについて、これまでの毛乳頭細胞の解析から、インヒビンβA以外のサブユニットの遺伝子については発現が高くなっていなかったことから、アクチビンAの発現がより高まっていると考えられた。
【0051】
図4から、アンフィレグリンの発現強度の変化周期が毛周期と一致していることから、アンフィレグリンが毛包の発達や毛髪の成長に深く関与する因子であることが示唆された。また、図5及び図6から、インヒビンβA及びPTGS2についても、発現強度にばらつきが少しあるものの、発現強度の変化周期と毛周期とに幾分の関連性が見出され、毛包の発達や毛髪の成長への関与する因子であると推察された。
【0052】
図7から、アンフィレグリン、インヒビンβA及びPTGS2の産生促進効果を有する本発明の細胞増殖因子産生促進剤が、ヒト毛乳頭細胞の増殖を促進することが確認された。
【0053】
上記のように、本発明の細胞増殖因子産生促進剤は、細胞増殖因子の産生を促進することができる。本発明の細胞増殖因子産生促進剤は、その細胞増殖因子産生促進作用を利用して、例えば、上記したような疾病の治療の他にも、例えば、創傷治癒剤、肌荒れ改善剤、にきび治療薬としても利用可能である。
【特許請求の範囲】
【請求項1】
ニンジンの抽出物を有効成分とすることを特徴とする細胞増殖因子産生促進剤。
【請求項2】
前記細胞増殖因子として、アンフィレグリン(Amphiregulin)の産生を促進する請求項1記載の細胞増殖因子産生促進剤。
【請求項3】
前記細胞増殖因子として、インヒビン(Inhibin)またはアクチビン(Actibin)の産生を促進する請求項1記載の細胞増殖因子産生促進剤。
【請求項4】
前記細胞増殖因子として、サブユニットとしてインヒビンβAを有するインヒビンまたはアクチビンの産生を促進する請求項3記載の細胞増殖因子産生促進剤。
【請求項5】
前記細胞増殖因子として、アクチビンAの産生を促進する請求項4記載の細胞増殖因子産生促進剤。
【請求項6】
PTGS2(Prostaglandin-endoperoxidesynthase 2)の産生を促進する請求項1〜5のいずれか一項記載の細胞増殖因子産生促進剤。
【請求項7】
育毛剤以外に用いられる請求項1〜6のいずれか一項記載の細胞増殖因子産生促進剤。
【請求項8】
前記ニンジンの抽出物がエタノール抽出物または含水エタノール抽出物である請求項1〜7のいずれか一項記載の細胞増殖因子産生促進剤。
【請求項1】
ニンジンの抽出物を有効成分とすることを特徴とする細胞増殖因子産生促進剤。
【請求項2】
前記細胞増殖因子として、アンフィレグリン(Amphiregulin)の産生を促進する請求項1記載の細胞増殖因子産生促進剤。
【請求項3】
前記細胞増殖因子として、インヒビン(Inhibin)またはアクチビン(Actibin)の産生を促進する請求項1記載の細胞増殖因子産生促進剤。
【請求項4】
前記細胞増殖因子として、サブユニットとしてインヒビンβAを有するインヒビンまたはアクチビンの産生を促進する請求項3記載の細胞増殖因子産生促進剤。
【請求項5】
前記細胞増殖因子として、アクチビンAの産生を促進する請求項4記載の細胞増殖因子産生促進剤。
【請求項6】
PTGS2(Prostaglandin-endoperoxidesynthase 2)の産生を促進する請求項1〜5のいずれか一項記載の細胞増殖因子産生促進剤。
【請求項7】
育毛剤以外に用いられる請求項1〜6のいずれか一項記載の細胞増殖因子産生促進剤。
【請求項8】
前記ニンジンの抽出物がエタノール抽出物または含水エタノール抽出物である請求項1〜7のいずれか一項記載の細胞増殖因子産生促進剤。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2013−40120(P2013−40120A)
【公開日】平成25年2月28日(2013.2.28)
【国際特許分類】
【出願番号】特願2011−177308(P2011−177308)
【出願日】平成23年8月12日(2011.8.12)
【出願人】(308040638)株式会社バスクリン (12)
【Fターム(参考)】
【公開日】平成25年2月28日(2013.2.28)
【国際特許分類】
【出願日】平成23年8月12日(2011.8.12)
【出願人】(308040638)株式会社バスクリン (12)
【Fターム(参考)】
[ Back to top ]

