細胞組織増加促進方法及び肌問題改善方法並びにこれらに用いるキット
【課題】自己由来の多血小板血漿(PRP)を美容形成の治療剤として用いる場面において、必ずしも高濃度の多血小板血漿(PRP)の調製が困難な場合であってもより安定した多血小板血漿(PRP)を用いた肌改善方法を提供すること。
【解決手段】患者の肌を改善する方法であって、患者から採血した血液を分離したものから多血小板血漿を精製する工程と、この精製した多血小板血漿と、予め精製された成長因子とを少なくとも含む注入液を混合して作成する工程と、前記注入液を前記患者の肌の問題が生じている箇所に注入する注入工程とを有することを特徴とする肌問題改善方法。なお肌問題の改善のみならず、広く細胞組織増加促進の目的に適用可能である。
【解決手段】患者の肌を改善する方法であって、患者から採血した血液を分離したものから多血小板血漿を精製する工程と、この精製した多血小板血漿と、予め精製された成長因子とを少なくとも含む注入液を混合して作成する工程と、前記注入液を前記患者の肌の問題が生じている箇所に注入する注入工程とを有することを特徴とする肌問題改善方法。なお肌問題の改善のみならず、広く細胞組織増加促進の目的に適用可能である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、美容形成、形成外科、皮膚科その他肌の問題を取り扱う分野において、組織再生を促進することにより患者の肌に関する問題を改善する方法、及びこれに用いる混合用キットに関する。
【背景技術】
【0002】
組織再生には、成長因子(Growth Factor:以下「GF」と表記することがある。)と呼ばれる、細胞の分化を実現することが可能なポリペプチド分子、または他の関連化学物質が大きく関与していることが知られている。成長因子は「増殖因子」とも呼ばれ、例えば、上皮成長因子(EGF)、トランスフォーミング成長因子−α(TGF−α)、トランスフォーミング成長因子−β(TGF−β)、ヒト内皮細胞成長因子(ECGF)、顆粒球マクロファージコロニー刺激因子(GM−CSF)、骨形成蛋白質(BMP)、神経成長因子(NGF)、血管内皮成長因子(VEGF)、インスリン様成長因子(IGF)、血小板由来増殖因子(PDGF)、血小板由来血管形成増殖因子(PDAF)、血小板由来上皮増殖因子(PDEGF)、塩基性線維芽細胞増殖因子(bFGF)などが挙げられる。
【0003】
損傷した組織が再生するにあたっては、ヒトの血液中の血小板に内在する成長因子(GF)が作用することが知られている。血小板は、骨髄中の巨核球(巨大核細胞)の細胞質が破砕したものであり、核を持っておらず、不定形略円盤状の形状を有する。血管が損傷すると、血小板は露出した内皮下組織に粘着し、血管外への血液の流出を防止する役割を果たす。
【0004】
上述の成長因子の多くは、血液成分中の血小板から放出されることが知られている。こうした背景から、創傷の治癒を促進するために多血小板血漿(Platelet Rich Plasma:以下「PRP」ということがある。)を使用する療法がある。多血小板血漿(PRP)とは、血小板が濃縮され豊富に含まれる血漿のことをいう。従来の多血小板血漿(PRP)の調製方法として例えば、採取した血液にクエン酸ナトリウム等の凝固防止剤を添加し、室温で所定時間放置した後、複数回の遠心分離に処理を行う。一回目の遠心分離(例えば約5,400rpm)によって2層に分離される。上層はPPP(Platelet Poor Plasma)と呼ばれる画分であり、下層には赤血球及びバフィーコートが含まれる。上層を除去したあと、更に赤血球が分離される条件(例えば約2,400rpm)で遠心分離処理を行う。その結果得られる、赤血球を実質的に含まない画分が多血小板血漿(PRP)として採取される。
【0005】
多血小板血漿(PRP)には、血小板由来増殖因子(PDGF)、血小板由来血管形成増殖因子(PDAF)、血小板由来上皮増殖因子(PDEGF)、トランスフォーミング増殖因子−β(TGF−β)などの様々な成長因子(GF)が含有されていることが知られており、この治癒力を組織再生に活用すべく、種々研究が行われている。
【0006】
ここで、一般の創傷治癒の過程において、血液の各成分、及びこれらから放出されるサイトカインの働きにつき説明する。一般的には出血・凝固期、炎症期、増殖期、再構築期といった時系列に沿って治癒は進展していく。
【0007】
出血・凝固期:血管が破綻し出血しているため、血小板が集まり止血する。血管は収縮し止血を助ける。これとともに、血小板からPDGF、EGFなどのサイトカインが放出される。
炎症期:白血球が創内に遊走し、身体の組織に侵入した細菌や異物を取り込むことにより感染予防に寄与する。白血球がマクロファージを遊走させ、マクロファージが創内に浸入し、壊死した組織などを除去する。
増殖期:マクロファージが各種増殖因子を放出する。また血管の新生や線維芽細胞の遊走・増殖、コラーゲンの産生が始まる。
再構築期:上皮細胞が表面を覆う。また線維芽細胞がコラーゲン、マトリックスなどを生成する。また毛細血管が増殖する。
【0008】
このように、血小板は、創傷箇所の物理的な止血作用において一定の役割を果たしている傍ら、これより放出される各種サイトカインの働きによってダメージを負った組織の再生を促進する働きを有していることが知られている。多血小板血漿(PRP)は、文字通り多量の血小板を含んだ分離血液の画分であることから、その中に含まれている血小板が活性化することにより放出される顆粒状の要素の中に、損傷した皮膚組織において足場を構築する物質と、ここで組織の再建をおこなう成長因子(GF)とが含まれており、これらの働きによって組織は復元する。
【0009】
このような、多血小板血漿(PRP)が有する組織復元能に着目した技術が、例えば下記に示す各特許文献において開示されている。特許文献1には、骨の再生に多血小板血漿(PRP)を含んでなる促進剤が開示されている。特許文献2には、筋肉及び/又は骨組織を再生するのに有用な、多血小板血漿を含む半合成の血小板ゲル及びその調製方法が開示されている。また特許文献3には、自己由来の多血小板血漿組成物を用い、哺乳動物での組織の血管新生を促進するための方法及びキットが提示されている。
【特許文献1】特開2003−55237
【特許文献2】特開2006−181365
【特許文献3】特開2006−232834
【発明の開示】
【発明が解決しようとする課題】
【0010】
しかしながら、特許文献1及び特許文献2のように、骨や筋肉の治療に多血小板血漿(PRP)を活用する例は記載されているものはあったが、美容形成の分野、特に皮膚、皮下、軟部組織の問題を改善する方法においてこれを活用することを具体的に開示するものは存在しなかった。特に、血小板ゲルやシーラントなど、患部に被覆させて使用する治療剤についての言及はあるものの、これらは特段外相を有さない肌問題の改善について適用することは難しく、問題を有する部位に直接多血小板血漿(PRP)を含む治療剤を注入する方法やそのための治療剤はなく、その出現が望まれていた。
【0011】
殊に、高齢化社会の進展とともに生活の質(QOL)が重視され、加齢に伴う肌の問題の改善方法が注目されている。また、美容治療においては安全性が高く、ノーダウンタイムあるいはミニマムダウンタイムであることが治療法として普及するための基礎的要件となっている。そのため、シワやタルミに関する治療に関しては、メスを入れてダウンタイムの発生するような治療よりは、ヒアルロン酸などフィラーによる治療が一般的となってきている。しかしながら、従来のフィラーを用いた治療は、治療終了時には改善するものの、永続性に乏しく、3ヶ月から半年でその効果が無くなってしまうのが欠点であった。
【0012】
その欠点を補うべく、BSEなどの感染の心配もない自己PRPを用いた肌改善の施術がシワ、タルミに対する治療に有効であることが認められてきており、近年美容領域の学会で発表されている。しかしながら、その原理や有効性に関しての基礎的研究がなされていないのが現状であった。さらに、従来のPRP治療は、ダウンタイムがほとんどなくシワやタルミを改善できるのが利点だが、個人の血液を用いる治療のため、肌改善効果の個人差が生じやすく、安定的な効果が期待できる肌改善方法が希求されている。
【0013】
加えて、確かに多血小板血漿(PRP)それ自体が成長因子(GF)を含んでおり、これに基づいて組織の再生が促進されるが、その効果を向上させるための技術の開示はなされていなかった。多血小板血漿(PRP)は、調製後の時間の経過とともにその効能が低下し、また凝固によってそもそも治療剤としての活用が困難になるという問題があるところ、特許文献3には、自己由来の多血小板血漿(PRP)を抗凝固剤やpH調整剤が一体となったキットが提案されている。これは自己由来の多血小板血漿(PRP)を処理するに際して求められる迅速性に寄与する技術ではあるが、多血小板血漿(PRP)の効能を向上させつつ迅速性を担保するという点については何らの言及もなされていない。
【0014】
更には、通常の多血小板血漿(PRP)を得るための遠心分離過程によって得られる多血小板血漿では必ずしも十分な肌改善、組織生成の効果が得られないケースもあることから、より効果の高い手法が求められていた。
【0015】
加えて、多血小板血漿(PRP)調製の方法にも優劣があり、高濃度の多血小板血漿(PRP)の画分を採取するためには、成分毎の精密な分離を行うことが可能な遠心分離機の存在が不可欠だが、かかる要求に応える性能を持ち合わせた遠心分離機は高価であり、美容形成を含め一般の治療現場において広く普及しているとはいえない。そのため、必ずしも濃度が高くない多血小板血漿(PRP)、具体的には既述の例におけるPPPもが混在した状態の多血小板血漿(PRP)を治療に用いなければならない場面もあり、この際高濃度の多血小板血漿(PRP)で期待しうる効能を得られるとは限らない。
【0016】
そこで本発明は、自己由来の多血小板血漿(PRP)を美容形成の治療剤として用いる場面において、必ずしも高濃度の多血小板血漿(PRP)の調製が困難な場合であってもより安定した多血小板血漿(PRP)を用いた細胞組織増加促進方法、及びこれを応用した肌改善方法を提供することを課題としている。
【0017】
出願人は、上記課題につき鋭意研究を行った結果、多血小板血漿(PRP)に成長因子(GF)を付加的に添加することにより、個人差のある多血小板血漿(PRP)の組織復元効果を補い、安定した効果を得られることを知見するに至った。加えて、多血小板血漿(PRP)の採取において、特定の遠心分離条件により遠心分離を行うことにより、従来に比して著しく効果の高い多血小板血漿(PRP)画分を得られることを知見するに至った。
【0018】
更には、得られた多血小板血漿(PRP)と成長因子(GF)とを混合して注入する現実の施術場面において、こうした処理を迅速に行うことができるようにするために、該治療に好適な混合用キットを案出するに至った。
【課題を解決するための手段】
【0019】
上記課題を解決すべく、本発明は下記のような構成を有する。
(1)細胞組織の増加を促進する方法であって、患者から採血した血液を分離したものから多血小板血漿を精製する工程と、前記精製された多血小板血漿と、予め精製された成長因子とを少なくとも含む注入液を作成する工程と、前記注入液を前期患者の要処方域に注入する工程とを含むことを特徴とする細胞組織増加促進方法(請求項1)。
(2)前記多血小板血漿は、白血球を多量に含むことを特徴とする(1)に記載の細胞組織増加促進方法(請求項2)。
(3)前記白血球を多量に含む多血小板血漿は、3,900個/μl以上の白血球を含むことを特徴とする(2)に記載の細胞組織増加促進方法(請求項3)。
(4)前記成長因子は、塩基性線維芽細胞成長因子(bFGF)であることを特徴とする(1)から(3)のいずれかに記載の細胞組織増加促進方法(請求項4)。
(5)上記記載の細胞組織増加促進方法を用いた肌問題改善方法であって、前記要処方域は前記患者の肌問題が生じている箇所であることを特徴とする肌問題改善方法(請求項5)。
(6)前記肌問題は、表皮、真皮、皮下組織及び軟部組織における乾燥、弾力の低下、欠損、減耗を含むことを特徴とする、(5)に記載の肌問題改善方法(請求項6)。
(7)上記記載の細胞組織増加促進方法又は肌問題改善方法に用いられる多血小板血漿と成長因子とを混合して注入するための混合注入キットであって、採血用試験管と、塩化カルシウムが予め封入された第一の真空試験管と、所定量の成長因子が予め封入された第二の真空試験管とを含むことを特徴とする混合注入キット(請求項7)。
(8)上記記載の細胞組織増加促進方法又は肌問題改善方法に用いられる多血小板血漿と成長因子とを混合して注入するための混合注入キットであって、採血用試験管と、塩化カルシウム及び所定量音成長因子が予め封入された真空試験管とを含むことを特徴とする混合注入キット(請求項8)。
【0020】
本発明の細胞組織増加促進方法によれば、多血小板血漿(PRP)の成分が一定でなくとも、補助的に成長因子(GF)を添加混合して注入することにより、より安定的な細胞組織増加の促進効果が期待できる。特に、自己由来の多血小板血漿(PRP)を用いる場合においては、例えば老齢者から採取する場合に必ずしも期待される治療効果が得られないことが予想される。これは加齢とともに細胞活性の低下が進み、老齢者の血小板から放出されるサイトカインの量が若年者のそれと必ずしも同様ではないためである。こうした場合であっても、成長因子(GF)を補助的に添加混合することにより、より優れた効果が期待できる。かかる細胞増加促進方法は、肌問題の改善においても、問題の生じている部位に直接注入することにより、効果が期待できる。
【0021】
特に、補助的に添加する成長因子(GF)としてbFGF(塩基性線維芽細胞増殖因子)を加えた際の改善効果が特に高いことが認められた。また、多血小板血漿(PRP)の抽出方法については、従来の遠心分離手法において得られる多血小板血漿の画分には白血球が殆ど含まれていなかった。ところが、肌問題の改善においては、上述の一般的創傷治癒過程における炎症期以降のステップを人為的に誘発させることが狙いであるところ、白血球(マクロファージ)の働きが重要である。そこで、所定の条件により得られる白血球含有多血小板血漿(White blood cell-containing platelet-rich plasma:以下「W−PRP」と表示することがある。)を投与することにより、肌問題の改善に著しく寄与することが認められた。
【0022】
ここで白血球含有多血小板血漿(W−PRP)の含有量としては、1μlあたり3,900個以上、好ましくは7,000個以上の白血球が含有されていることにより、顕著な肌問題改善効果が見られる。
【0023】
そして、これらの肌問題改善の為の措置は迅速に行われる要請があるところ、本発明の混合用キットによれば、採取した多血小板血漿(PRP)を所望の成長因子(GF)と即座に混合を行うことが可能であるため、治療が滞ることによる多血小板血漿(PRP)の不具合(凝固或いは失活)といった問題が生じることを防止することができる。予め成長因子(GF)が適切な量封入されていることにより、注入直前に添加量の計量等によって手間取ることがない。
【0024】
なお、本発明における「細胞組織増加促進」とは、本来存在した組織の欠損や減耗のみに限らず、生来的に矮小であった部位の増強など、例えば豊胸術や陰茎増大にも適用の余地がある。また本発明における「肌問題」とは、美容において施術の対象となりうる肌のトラブル、例えば肌のしわやたるみなど、主として老化によって生じる肌の乾燥や弾力の低下、皮脂細胞の萎縮や表情筋の過度の収縮や弛緩などによって起きる美観上の問題をいう。また美観上の問題に限らず、何等かの事故等による欠損、減耗或いは生来からの矮小などの問題も含まれる。
【0025】
なお、「bFGF」とは塩基性線維芽細胞増殖因子の意味であり、創傷治癒過程の増殖期において線維芽細胞を増殖させるとともに、再構築期に至る過程ではアポトーシスを促進することにより線維芽細胞の数を減らし、瘢痕を軽微化させることが知られている。創傷治療においては散布ないし噴霧投与されるのが一般的であるが、本発明ではこれを多血小板血漿(PRP)とともに注入投与する。
【発明を実施するための最良の形態】
【0026】
以下では、本発明の具体的な実施形態につき、図面を参照しつつ説明する。
【0027】
まず、PRP及びW−PRPの精製について説明する。PRPの調整には、1回遠心分離でPRPを精製可能な方法としてカスケードメディカル社製のPRP分離システムを用いた。これは、採血用試験管の中にポリエステル製のセパレータジェルが封入されているものであり、採血後遠心分離を行うことにより、比重差により所定の試験管内高さに定位する。採血量は9mlで、抗凝固剤にはTri-sodium citrate solutionが用いられている。遠心分離条件は一般的なPRP抽出手法である2600回転6分を含め、表1記載の通り、いくつかの方法を行った。遠心分離機はkubota 2410(ロータ半径14.5cm)を用いた。遠心分離後、フィルタ近くの層を1ml残して上清(platelet poor plasma:PPP)を除去した。残った液を混ぜてPRPを得た。なお下記遠心条件は、上述のPRP分離システムを用いた際の条件であり、2回遠心分離を行う場合、あるいはセパレータジェルの質に応じて適切な遠心条件は変化するものと思われる。
【0028】
【表1】

【0029】
<PRP、W-PRPの質の解析>
分離したPRPに対して、血小板(Pt)、白血球(WBC)、赤血球(RBC)、フィブリンモノマー複合体、bFGF、VEGF、IGF-1を測定した。bFGFの測定にはR&D System Inc. (MN. USA)社製、Human FGF basic Immunoassay キットを用いた。VEGFの測定には、R&D System Inc. (MN. USA)社製、Human VEGF Immunoassay Kitを用いた。IGF−1の測定には株式会社テイエフビ−(TFB,INC. Tokyo. Japan)社製試薬を用いてIRIAで測定した。また、ゲル化させて内容物をHE染色した。図1は、上記HE染色を施した(a)PRP(2600rpm/6min)、(b)W−PRP(1800rpm/10min)、(c)PPPの成分含有状況を示す写真である。(a)PRPではフィブリンネットワークに濃縮された血小板、多少の有核球(メインは白血球)を認めた。(b)W-PRPではフィブリンネットワークに濃縮された血小板、多くの有核球、若干の赤血球を認めた。(c)PPPではフィブリンネットワークのみ認めた。
【0030】
<PRP遠心条件に関して>
表2は、図1において示された各分画のうち、2600rpm/6minの分離条件で得られたPRP、1800rpm/10minの分離条件で得られたW−PRP、及びPPPの成分に関する分析結果である。まず、遠心分離の条件によってPRPに含まれる血小板や白血球が異なることが、前述のように分かった。従来言われている血小板が主体の効果をみるためには、2600回転6分の遠心分離条件がよく、それに白血球が混在するものの効果を見るためには、1800回転10分の遠心条件が望ましいと考え、両方の条件で検討を行った。2600回転6分の遠心分離条件では、血小板は約3倍に濃縮されており、白血球は0.7倍となっていた。1800回転10分では、血小板は5倍に濃縮されており、白血球は1.4倍に濃縮されていた。
【0031】
【表2】

【0032】
また、PRP, W-PRP, PPPの内容を分析したところ、PRPでは血小板の濃縮をメインに認めたが、W−PRPでは血小板とともに多数の白血球を認めた。また、bFGF、VEGFの放出量もW−PRPの方が多いことがわかった。またPPPには血小板、白血球ともにほとんど含まれていないことが示された。2600回転6分の遠心分離では従来のPRPが採取可能であり、1800回転10分の遠心分離では今回われわれが目的としている白血球含有率の高いW-PRPが採取できた。
【0033】
<PRP、W-PRPのヌードマウス耳介への注入実験>
つぎに、PRP、W-PRPの臨床効果を想定して、ヌードマウスの耳介にPRP、W-PRPを注入して組織学的検討をした。また、bFGFを添加することによってその効果を増大させることが出来るかを検討した。PRPの調整には、上述と同様の方法を用いた。活性化には10%塩化カルシウム(CaCl2)溶液を10分の1量添加した。得られたPRPをヌードマウスの耳介に0.2mlずつ、30G針で局所注入した。また、コントロールとして生食、PPP、さらにbFGFを添加したものに関しても検討した。bFGF添加量は、1、10、100μg/mlで行った。
【0034】
注入後2週目で組織学的に検討した。bFGF単独、bFGF+PPP、bFGF+PRPは、W−PRP+bFGF群と比較して優位な組織の増量を認めなかった。
【0035】
図2は、2週間後のヌードマウスの耳介の様子を示す写真を各条件毎に並べたものである。(a)はPRPを注入したもの、(b)はW−PRPを注入したもの、(c)はW−PRPにbFGF100μg/mlを添加して注入したもの、(d)はPPPを注入したもの、(e)は生理食塩水を注入したものである。外見上はPRP群、W−PRP群とW−PRP+bFGF群で耳介の肥厚を認めた。
【0036】
<組織学的検討>
図3は、局所注入2週後の耳介先端部位での耳介の横断切片をHE染色処理したものである。各写真の符号は図2におけるものと同一である。この所見では、PRP,W−PRP、W−PRP+100μg/ml bFGF群では、耳介の肥厚を認めた。とりわけ(c)のW−PRPにbFGFを添加したものでは他を凌駕する肥厚が認められた。耳介の肥厚の組織部位としては皮膚、皮下組織で著明であった。また、毛根の活性化も認められた。一方、PPPとコントロールとして生食を注入した群では、耳介の肥厚はほとんど認められなかった。
【0037】
図4は、耳介先端部から5mmの部位の厚さを比較した対比分析グラフである。各例を比較したところ、コントロール群やPPP群と比較し、PRP群、W−PRP群で肥厚傾向が認められた。またW−PRP+bFGF(10、100μg/ml)群では、有意に組織の肥厚が認められた。耳介の一番肥厚した部位の厚さの検討(図5)では、W−PRP群とbFGF添加W−PRP群で優位差のある耳介の肥厚が認められた。また、bFGF添加群では濃度依存性に耳介の肥厚が認められた。
【0038】
図6は、局所注入2週後の耳介先端部位での耳介の横断切片をαSMA染色処理したものである(各写真ごとの符号は図2及び図3と同一である)。また図7は各群におけるα陽性細胞の増加数をグラフ化したものである。αSMA染色の結果では、PPP群とコントロール群に比較し、PRP群、W−PRP群にαSMA陽性細胞数の増加傾向が認められた。また、W−PRP+bFGF(10、100μg/ml)群で優位なαSMA陽性細胞数の増加を認めた。図7は各群におけるαSMA陽性細胞数をグラフ化したものである。W−PRP+bFGF10群及びW−PRP+bFGF100群において顕著な効果が見られた。αSMA陽性細胞の増大により、組織を収縮させ、シワやたるみといった肌問題が改善されるという効果が期待される。
【0039】
以上のヌードマウス耳介への注入実験から、以下の結論が得られる。
(1)組織の増量には、PRPよりもW−PRPのほうが効果があることが認められた。
(2)組織の増量には、血小板のみならず、白血球の関与が重要であることが認められた。
(3)フィブリネット採血管を用いたW−PRPの作成には、1800回転、10分の遠心条件が最適であった。
(4)αSMA陽性細胞数は、PRP、W−PRP、bFGFを添加したW−PRPにおいて優位に増加していた。
【0040】
<肌問題の改善への適用>
以上の知見を、人間の肌のしわやたるみに対して適用する場面につき言及する。
人間の肌のしわやたるみの原因は、既述の通り老齢化に伴う肌の乾燥や皮下脂肪の減少、表情筋の過度の収縮や弛緩にあるといわれている。こうした問題を解決するために、老化した細胞の除去、新たな組織の産生が寄与する。一般的な創傷治癒過程における炎症期以降のステップを人為的に誘発することにより、肌組織が適切に増量するためのいわば材料が備わり、長期的な肌問題の改善に寄与するのである。
【0041】
しわやたるみに対してPRPを用いる場合、単なるPRPでは組織の増量は期待できず、W−PRPを用いる方がより優位な組織の増量が期待できる。これは、W−PRPに含まれている白血球がマクロファージを誘導し、さらにマクロファージが線維芽細胞を遊走、増殖させることが一因であると推測される。
【0042】
また組織の肥厚には筋線維芽細胞が関与していると考えられる。組織が肥厚することにより減少していた皮下組織が回復し、しわの改善に繋がるものである。また、潰瘍にPRPを用いるのと異なり、組織を構築しオーギュメンテーションを図るには、足場(scaffold)が必要であると考えられる。生体由来のスキャホールドとして、フィブリンや血小板糊によるネットワークの形成が重要であると考えられる。
【0043】
また、W-PRPに内在している白血球が周囲や流血中のマクロファージを注入部位に遊走させることも大切であると考えられる。マクロファージは、一般の創傷治癒において修復組織中に多数認められ、そのマクロファージは繊維芽細胞を遊走させて、その遊走してきた繊維芽細胞がコラーゲンを再生させると考えられるからである。つまり、W-PRPに含まれている白血球がマクロファージを誘導し、さらにマクロファージが線維芽細胞を遊走、増殖させることが一因であると推測されることから、従来の細胞移植の概念と異なり、サイトカインを放出する細胞を移植することによって、組織の修復に必要な細胞を生体自身から誘導するという新たな手法であるとも考えられる。これらの起序により、シワが改善するのではないかと考えられた。また、繊維芽細胞の中に出現する筋線維芽細胞組織を収縮させることによって、たるみを改善する効果があると考えられる。
【0044】
W-PRPにbFGFを添加することによって組織のさらなる増量が認められたことから、肌問題の改善にあっては、W-PRPはbFGFの徐放ドナーとしても有用であると思われる。ゼラチンなどを用いてbFGFを徐放させることでその働きを効果的にしようとの報告があるが、BSE問題もあり、ゼラチンをすぐに臨床で用いるのは難しい。外用剤としてのbFGF製剤を局所注入用に用いることに関しては、近年縫合創にbFGFを局所注射することによって創がきれいに治るとの報告や、ゼラチンを徐放ドナーとして局所注射することによってASOの患肢の血管新生の治療が可能であるとの報告からも、使用量を守れば問題ないと考えられる 。
【0045】
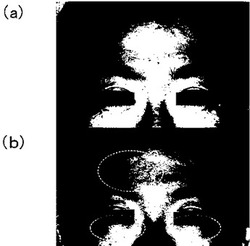
図8は、人体額部及び眼下部にW−PRPを注入したことの効果を示す図である。(a)は注入前、(b)は注入後7月経過時点の写真である。注入は、両下眼瞼及び右前額部(写真左側)について行った。写真からも明らかなように、注入を行った額部の隆起が生じており、陥没が改善されている。下眼瞼においても同様である。
【0046】
図9は、上記実験を行った人体をMRIにて撮影したものである。(a)の左はコントロールであり、右が注入を施したものである。(b)は当該部分の拡大図である。コントロール側では、骨の形態にそった陥凹が皮膚にまで認められるが、注入側では注入部位の皮膚、皮下組織(脂肪組織)、前頭筋の肥厚が認められ、皮膚の陥凹が消失していることが判る。
【0047】
<好適な混合注入キット>
次に、上記の肌問題改善方法に用いるW−PRPを迅速に抽出し、成長因子とともに注入するための混合注入キットについて説明する。図10(a)は、本発明を実施するにあたって好適な混合注入キット1を図示したものである。図10(b)に示すように、混合注入キット1は採血用試験管2、予め活性剤としての塩化カルシウム31が封入された第一の真空試験管3、及び予めbFGF41が封入された第二の真空試験管4を含んでいる。
【0048】
図11は、図10に示した混合注入キットを用いた肌問題改善方法の具体的ステップの一例を示したものである。まず、好適なシリンジを用い、肌問題を有する患者から採血用試験管2に採血する(図中ステップ(1)及び(2))。採血はすぐに遠心分離器にかけられる(ステップ(3))。この遠心分離にあたっては、上述のカスケードメディカル社製のPRP分離システムを用いることができる。所定の分離条件、例えば1800rpm/10minで遠沈させることにより上澄み部分をW−PRPとして抽出することができる(ステップ(4))。
【0049】
抽出したW−PRPは、直ちに第一の真空試験管3に移し替えられる。第一の真空試験管3には予め活性剤としての塩化カルシウムが封入されている。これをW−PRP混合後攪拌することにより、W−PRP内のサイトカインが活性化される(ステップ(5))。さらにこれを第二の真空試験管4へと移し変える(ステップ(6))。第二の真空試験管4には予めbFGFが封入されており、これと混合攪拌させた後、肌問題を有する患部に注入する。
【0050】
なお、塩化カルシウムとbFGFとを第一の真空試験管3と第二の真空試験管4とに分けて封入したのは、bFGFは粉体でないとその効能を維持することができないからである。このように、採血試験管2、第一の真空試験管3及び第二の真空試験管4がユニットとして備えられていることにより、迅速な処理が求められる肌問題改善の処置を速やかに行うことができ、肌問題の適切な改善に資する。
【0051】
なお、本実施例では混合注入キットに包含される構成要素として上記3種の試験管のみとしたが、これに限られず、例えば採血用のシリンジ、注入用のシリンジ及び注射針をキットに含めても良い。或いは、図示しないが、塩化カルシウムと所定量のbFGFとを一の真空試験管に封入してもよい。この場合bFGF効能を損なわないよう、塩化カルシウムも粉体のものを適用することが望ましい。
【図面の簡単な説明】
【0052】
【図1】各遠心分離条件毎の成分含有状況を示す写真である。
【図2】局所注入2週間後のヌードマウスの耳介の様子を示す写真を各条件毎に並べたものである。
【図3】局所注入2週後の耳介先端部位での耳介の横断切片をHE染色処理したものである。
【図4】耳介先端部から5mmの部位の厚さを比較した対比分析グラフである。
【図5】耳介の一番肥厚した部位の厚さを比較した対比分析グラフである。
【図6】局所注入2週後の耳介先端部位での耳介の横断切片をαSMA染色処理したものである。
【図7】各群におけるαSMA陽性細胞数をグラフ化したものである。
【図8】人体顔部への局所注入の前後を示す写真であり、(a)注入前の額部写真である。(b)注入後7月の額部写真である。
【図9】(a)局所注入を行った人体頭部の側面MRI画像(左は注入後7月、右はコントロール)である。(b)上記の注入部位の拡大図である。
【図10】本発明の一実施例である混合注入キットの構成を示した図である。
【図11】本発明の一実施例である混合注入キットを用いた肌問題改善の手順を図示したものである。
【符号の説明】
【0053】
1 混合注入キット
2 採血用試験管
3 第一の真空試験管
4 第二の真空試験管
31 塩化カルシウム
41 bFGF
【技術分野】
【0001】
本発明は、美容形成、形成外科、皮膚科その他肌の問題を取り扱う分野において、組織再生を促進することにより患者の肌に関する問題を改善する方法、及びこれに用いる混合用キットに関する。
【背景技術】
【0002】
組織再生には、成長因子(Growth Factor:以下「GF」と表記することがある。)と呼ばれる、細胞の分化を実現することが可能なポリペプチド分子、または他の関連化学物質が大きく関与していることが知られている。成長因子は「増殖因子」とも呼ばれ、例えば、上皮成長因子(EGF)、トランスフォーミング成長因子−α(TGF−α)、トランスフォーミング成長因子−β(TGF−β)、ヒト内皮細胞成長因子(ECGF)、顆粒球マクロファージコロニー刺激因子(GM−CSF)、骨形成蛋白質(BMP)、神経成長因子(NGF)、血管内皮成長因子(VEGF)、インスリン様成長因子(IGF)、血小板由来増殖因子(PDGF)、血小板由来血管形成増殖因子(PDAF)、血小板由来上皮増殖因子(PDEGF)、塩基性線維芽細胞増殖因子(bFGF)などが挙げられる。
【0003】
損傷した組織が再生するにあたっては、ヒトの血液中の血小板に内在する成長因子(GF)が作用することが知られている。血小板は、骨髄中の巨核球(巨大核細胞)の細胞質が破砕したものであり、核を持っておらず、不定形略円盤状の形状を有する。血管が損傷すると、血小板は露出した内皮下組織に粘着し、血管外への血液の流出を防止する役割を果たす。
【0004】
上述の成長因子の多くは、血液成分中の血小板から放出されることが知られている。こうした背景から、創傷の治癒を促進するために多血小板血漿(Platelet Rich Plasma:以下「PRP」ということがある。)を使用する療法がある。多血小板血漿(PRP)とは、血小板が濃縮され豊富に含まれる血漿のことをいう。従来の多血小板血漿(PRP)の調製方法として例えば、採取した血液にクエン酸ナトリウム等の凝固防止剤を添加し、室温で所定時間放置した後、複数回の遠心分離に処理を行う。一回目の遠心分離(例えば約5,400rpm)によって2層に分離される。上層はPPP(Platelet Poor Plasma)と呼ばれる画分であり、下層には赤血球及びバフィーコートが含まれる。上層を除去したあと、更に赤血球が分離される条件(例えば約2,400rpm)で遠心分離処理を行う。その結果得られる、赤血球を実質的に含まない画分が多血小板血漿(PRP)として採取される。
【0005】
多血小板血漿(PRP)には、血小板由来増殖因子(PDGF)、血小板由来血管形成増殖因子(PDAF)、血小板由来上皮増殖因子(PDEGF)、トランスフォーミング増殖因子−β(TGF−β)などの様々な成長因子(GF)が含有されていることが知られており、この治癒力を組織再生に活用すべく、種々研究が行われている。
【0006】
ここで、一般の創傷治癒の過程において、血液の各成分、及びこれらから放出されるサイトカインの働きにつき説明する。一般的には出血・凝固期、炎症期、増殖期、再構築期といった時系列に沿って治癒は進展していく。
【0007】
出血・凝固期:血管が破綻し出血しているため、血小板が集まり止血する。血管は収縮し止血を助ける。これとともに、血小板からPDGF、EGFなどのサイトカインが放出される。
炎症期:白血球が創内に遊走し、身体の組織に侵入した細菌や異物を取り込むことにより感染予防に寄与する。白血球がマクロファージを遊走させ、マクロファージが創内に浸入し、壊死した組織などを除去する。
増殖期:マクロファージが各種増殖因子を放出する。また血管の新生や線維芽細胞の遊走・増殖、コラーゲンの産生が始まる。
再構築期:上皮細胞が表面を覆う。また線維芽細胞がコラーゲン、マトリックスなどを生成する。また毛細血管が増殖する。
【0008】
このように、血小板は、創傷箇所の物理的な止血作用において一定の役割を果たしている傍ら、これより放出される各種サイトカインの働きによってダメージを負った組織の再生を促進する働きを有していることが知られている。多血小板血漿(PRP)は、文字通り多量の血小板を含んだ分離血液の画分であることから、その中に含まれている血小板が活性化することにより放出される顆粒状の要素の中に、損傷した皮膚組織において足場を構築する物質と、ここで組織の再建をおこなう成長因子(GF)とが含まれており、これらの働きによって組織は復元する。
【0009】
このような、多血小板血漿(PRP)が有する組織復元能に着目した技術が、例えば下記に示す各特許文献において開示されている。特許文献1には、骨の再生に多血小板血漿(PRP)を含んでなる促進剤が開示されている。特許文献2には、筋肉及び/又は骨組織を再生するのに有用な、多血小板血漿を含む半合成の血小板ゲル及びその調製方法が開示されている。また特許文献3には、自己由来の多血小板血漿組成物を用い、哺乳動物での組織の血管新生を促進するための方法及びキットが提示されている。
【特許文献1】特開2003−55237
【特許文献2】特開2006−181365
【特許文献3】特開2006−232834
【発明の開示】
【発明が解決しようとする課題】
【0010】
しかしながら、特許文献1及び特許文献2のように、骨や筋肉の治療に多血小板血漿(PRP)を活用する例は記載されているものはあったが、美容形成の分野、特に皮膚、皮下、軟部組織の問題を改善する方法においてこれを活用することを具体的に開示するものは存在しなかった。特に、血小板ゲルやシーラントなど、患部に被覆させて使用する治療剤についての言及はあるものの、これらは特段外相を有さない肌問題の改善について適用することは難しく、問題を有する部位に直接多血小板血漿(PRP)を含む治療剤を注入する方法やそのための治療剤はなく、その出現が望まれていた。
【0011】
殊に、高齢化社会の進展とともに生活の質(QOL)が重視され、加齢に伴う肌の問題の改善方法が注目されている。また、美容治療においては安全性が高く、ノーダウンタイムあるいはミニマムダウンタイムであることが治療法として普及するための基礎的要件となっている。そのため、シワやタルミに関する治療に関しては、メスを入れてダウンタイムの発生するような治療よりは、ヒアルロン酸などフィラーによる治療が一般的となってきている。しかしながら、従来のフィラーを用いた治療は、治療終了時には改善するものの、永続性に乏しく、3ヶ月から半年でその効果が無くなってしまうのが欠点であった。
【0012】
その欠点を補うべく、BSEなどの感染の心配もない自己PRPを用いた肌改善の施術がシワ、タルミに対する治療に有効であることが認められてきており、近年美容領域の学会で発表されている。しかしながら、その原理や有効性に関しての基礎的研究がなされていないのが現状であった。さらに、従来のPRP治療は、ダウンタイムがほとんどなくシワやタルミを改善できるのが利点だが、個人の血液を用いる治療のため、肌改善効果の個人差が生じやすく、安定的な効果が期待できる肌改善方法が希求されている。
【0013】
加えて、確かに多血小板血漿(PRP)それ自体が成長因子(GF)を含んでおり、これに基づいて組織の再生が促進されるが、その効果を向上させるための技術の開示はなされていなかった。多血小板血漿(PRP)は、調製後の時間の経過とともにその効能が低下し、また凝固によってそもそも治療剤としての活用が困難になるという問題があるところ、特許文献3には、自己由来の多血小板血漿(PRP)を抗凝固剤やpH調整剤が一体となったキットが提案されている。これは自己由来の多血小板血漿(PRP)を処理するに際して求められる迅速性に寄与する技術ではあるが、多血小板血漿(PRP)の効能を向上させつつ迅速性を担保するという点については何らの言及もなされていない。
【0014】
更には、通常の多血小板血漿(PRP)を得るための遠心分離過程によって得られる多血小板血漿では必ずしも十分な肌改善、組織生成の効果が得られないケースもあることから、より効果の高い手法が求められていた。
【0015】
加えて、多血小板血漿(PRP)調製の方法にも優劣があり、高濃度の多血小板血漿(PRP)の画分を採取するためには、成分毎の精密な分離を行うことが可能な遠心分離機の存在が不可欠だが、かかる要求に応える性能を持ち合わせた遠心分離機は高価であり、美容形成を含め一般の治療現場において広く普及しているとはいえない。そのため、必ずしも濃度が高くない多血小板血漿(PRP)、具体的には既述の例におけるPPPもが混在した状態の多血小板血漿(PRP)を治療に用いなければならない場面もあり、この際高濃度の多血小板血漿(PRP)で期待しうる効能を得られるとは限らない。
【0016】
そこで本発明は、自己由来の多血小板血漿(PRP)を美容形成の治療剤として用いる場面において、必ずしも高濃度の多血小板血漿(PRP)の調製が困難な場合であってもより安定した多血小板血漿(PRP)を用いた細胞組織増加促進方法、及びこれを応用した肌改善方法を提供することを課題としている。
【0017】
出願人は、上記課題につき鋭意研究を行った結果、多血小板血漿(PRP)に成長因子(GF)を付加的に添加することにより、個人差のある多血小板血漿(PRP)の組織復元効果を補い、安定した効果を得られることを知見するに至った。加えて、多血小板血漿(PRP)の採取において、特定の遠心分離条件により遠心分離を行うことにより、従来に比して著しく効果の高い多血小板血漿(PRP)画分を得られることを知見するに至った。
【0018】
更には、得られた多血小板血漿(PRP)と成長因子(GF)とを混合して注入する現実の施術場面において、こうした処理を迅速に行うことができるようにするために、該治療に好適な混合用キットを案出するに至った。
【課題を解決するための手段】
【0019】
上記課題を解決すべく、本発明は下記のような構成を有する。
(1)細胞組織の増加を促進する方法であって、患者から採血した血液を分離したものから多血小板血漿を精製する工程と、前記精製された多血小板血漿と、予め精製された成長因子とを少なくとも含む注入液を作成する工程と、前記注入液を前期患者の要処方域に注入する工程とを含むことを特徴とする細胞組織増加促進方法(請求項1)。
(2)前記多血小板血漿は、白血球を多量に含むことを特徴とする(1)に記載の細胞組織増加促進方法(請求項2)。
(3)前記白血球を多量に含む多血小板血漿は、3,900個/μl以上の白血球を含むことを特徴とする(2)に記載の細胞組織増加促進方法(請求項3)。
(4)前記成長因子は、塩基性線維芽細胞成長因子(bFGF)であることを特徴とする(1)から(3)のいずれかに記載の細胞組織増加促進方法(請求項4)。
(5)上記記載の細胞組織増加促進方法を用いた肌問題改善方法であって、前記要処方域は前記患者の肌問題が生じている箇所であることを特徴とする肌問題改善方法(請求項5)。
(6)前記肌問題は、表皮、真皮、皮下組織及び軟部組織における乾燥、弾力の低下、欠損、減耗を含むことを特徴とする、(5)に記載の肌問題改善方法(請求項6)。
(7)上記記載の細胞組織増加促進方法又は肌問題改善方法に用いられる多血小板血漿と成長因子とを混合して注入するための混合注入キットであって、採血用試験管と、塩化カルシウムが予め封入された第一の真空試験管と、所定量の成長因子が予め封入された第二の真空試験管とを含むことを特徴とする混合注入キット(請求項7)。
(8)上記記載の細胞組織増加促進方法又は肌問題改善方法に用いられる多血小板血漿と成長因子とを混合して注入するための混合注入キットであって、採血用試験管と、塩化カルシウム及び所定量音成長因子が予め封入された真空試験管とを含むことを特徴とする混合注入キット(請求項8)。
【0020】
本発明の細胞組織増加促進方法によれば、多血小板血漿(PRP)の成分が一定でなくとも、補助的に成長因子(GF)を添加混合して注入することにより、より安定的な細胞組織増加の促進効果が期待できる。特に、自己由来の多血小板血漿(PRP)を用いる場合においては、例えば老齢者から採取する場合に必ずしも期待される治療効果が得られないことが予想される。これは加齢とともに細胞活性の低下が進み、老齢者の血小板から放出されるサイトカインの量が若年者のそれと必ずしも同様ではないためである。こうした場合であっても、成長因子(GF)を補助的に添加混合することにより、より優れた効果が期待できる。かかる細胞増加促進方法は、肌問題の改善においても、問題の生じている部位に直接注入することにより、効果が期待できる。
【0021】
特に、補助的に添加する成長因子(GF)としてbFGF(塩基性線維芽細胞増殖因子)を加えた際の改善効果が特に高いことが認められた。また、多血小板血漿(PRP)の抽出方法については、従来の遠心分離手法において得られる多血小板血漿の画分には白血球が殆ど含まれていなかった。ところが、肌問題の改善においては、上述の一般的創傷治癒過程における炎症期以降のステップを人為的に誘発させることが狙いであるところ、白血球(マクロファージ)の働きが重要である。そこで、所定の条件により得られる白血球含有多血小板血漿(White blood cell-containing platelet-rich plasma:以下「W−PRP」と表示することがある。)を投与することにより、肌問題の改善に著しく寄与することが認められた。
【0022】
ここで白血球含有多血小板血漿(W−PRP)の含有量としては、1μlあたり3,900個以上、好ましくは7,000個以上の白血球が含有されていることにより、顕著な肌問題改善効果が見られる。
【0023】
そして、これらの肌問題改善の為の措置は迅速に行われる要請があるところ、本発明の混合用キットによれば、採取した多血小板血漿(PRP)を所望の成長因子(GF)と即座に混合を行うことが可能であるため、治療が滞ることによる多血小板血漿(PRP)の不具合(凝固或いは失活)といった問題が生じることを防止することができる。予め成長因子(GF)が適切な量封入されていることにより、注入直前に添加量の計量等によって手間取ることがない。
【0024】
なお、本発明における「細胞組織増加促進」とは、本来存在した組織の欠損や減耗のみに限らず、生来的に矮小であった部位の増強など、例えば豊胸術や陰茎増大にも適用の余地がある。また本発明における「肌問題」とは、美容において施術の対象となりうる肌のトラブル、例えば肌のしわやたるみなど、主として老化によって生じる肌の乾燥や弾力の低下、皮脂細胞の萎縮や表情筋の過度の収縮や弛緩などによって起きる美観上の問題をいう。また美観上の問題に限らず、何等かの事故等による欠損、減耗或いは生来からの矮小などの問題も含まれる。
【0025】
なお、「bFGF」とは塩基性線維芽細胞増殖因子の意味であり、創傷治癒過程の増殖期において線維芽細胞を増殖させるとともに、再構築期に至る過程ではアポトーシスを促進することにより線維芽細胞の数を減らし、瘢痕を軽微化させることが知られている。創傷治療においては散布ないし噴霧投与されるのが一般的であるが、本発明ではこれを多血小板血漿(PRP)とともに注入投与する。
【発明を実施するための最良の形態】
【0026】
以下では、本発明の具体的な実施形態につき、図面を参照しつつ説明する。
【0027】
まず、PRP及びW−PRPの精製について説明する。PRPの調整には、1回遠心分離でPRPを精製可能な方法としてカスケードメディカル社製のPRP分離システムを用いた。これは、採血用試験管の中にポリエステル製のセパレータジェルが封入されているものであり、採血後遠心分離を行うことにより、比重差により所定の試験管内高さに定位する。採血量は9mlで、抗凝固剤にはTri-sodium citrate solutionが用いられている。遠心分離条件は一般的なPRP抽出手法である2600回転6分を含め、表1記載の通り、いくつかの方法を行った。遠心分離機はkubota 2410(ロータ半径14.5cm)を用いた。遠心分離後、フィルタ近くの層を1ml残して上清(platelet poor plasma:PPP)を除去した。残った液を混ぜてPRPを得た。なお下記遠心条件は、上述のPRP分離システムを用いた際の条件であり、2回遠心分離を行う場合、あるいはセパレータジェルの質に応じて適切な遠心条件は変化するものと思われる。
【0028】
【表1】

【0029】
<PRP、W-PRPの質の解析>
分離したPRPに対して、血小板(Pt)、白血球(WBC)、赤血球(RBC)、フィブリンモノマー複合体、bFGF、VEGF、IGF-1を測定した。bFGFの測定にはR&D System Inc. (MN. USA)社製、Human FGF basic Immunoassay キットを用いた。VEGFの測定には、R&D System Inc. (MN. USA)社製、Human VEGF Immunoassay Kitを用いた。IGF−1の測定には株式会社テイエフビ−(TFB,INC. Tokyo. Japan)社製試薬を用いてIRIAで測定した。また、ゲル化させて内容物をHE染色した。図1は、上記HE染色を施した(a)PRP(2600rpm/6min)、(b)W−PRP(1800rpm/10min)、(c)PPPの成分含有状況を示す写真である。(a)PRPではフィブリンネットワークに濃縮された血小板、多少の有核球(メインは白血球)を認めた。(b)W-PRPではフィブリンネットワークに濃縮された血小板、多くの有核球、若干の赤血球を認めた。(c)PPPではフィブリンネットワークのみ認めた。
【0030】
<PRP遠心条件に関して>
表2は、図1において示された各分画のうち、2600rpm/6minの分離条件で得られたPRP、1800rpm/10minの分離条件で得られたW−PRP、及びPPPの成分に関する分析結果である。まず、遠心分離の条件によってPRPに含まれる血小板や白血球が異なることが、前述のように分かった。従来言われている血小板が主体の効果をみるためには、2600回転6分の遠心分離条件がよく、それに白血球が混在するものの効果を見るためには、1800回転10分の遠心条件が望ましいと考え、両方の条件で検討を行った。2600回転6分の遠心分離条件では、血小板は約3倍に濃縮されており、白血球は0.7倍となっていた。1800回転10分では、血小板は5倍に濃縮されており、白血球は1.4倍に濃縮されていた。
【0031】
【表2】

【0032】
また、PRP, W-PRP, PPPの内容を分析したところ、PRPでは血小板の濃縮をメインに認めたが、W−PRPでは血小板とともに多数の白血球を認めた。また、bFGF、VEGFの放出量もW−PRPの方が多いことがわかった。またPPPには血小板、白血球ともにほとんど含まれていないことが示された。2600回転6分の遠心分離では従来のPRPが採取可能であり、1800回転10分の遠心分離では今回われわれが目的としている白血球含有率の高いW-PRPが採取できた。
【0033】
<PRP、W-PRPのヌードマウス耳介への注入実験>
つぎに、PRP、W-PRPの臨床効果を想定して、ヌードマウスの耳介にPRP、W-PRPを注入して組織学的検討をした。また、bFGFを添加することによってその効果を増大させることが出来るかを検討した。PRPの調整には、上述と同様の方法を用いた。活性化には10%塩化カルシウム(CaCl2)溶液を10分の1量添加した。得られたPRPをヌードマウスの耳介に0.2mlずつ、30G針で局所注入した。また、コントロールとして生食、PPP、さらにbFGFを添加したものに関しても検討した。bFGF添加量は、1、10、100μg/mlで行った。
【0034】
注入後2週目で組織学的に検討した。bFGF単独、bFGF+PPP、bFGF+PRPは、W−PRP+bFGF群と比較して優位な組織の増量を認めなかった。
【0035】
図2は、2週間後のヌードマウスの耳介の様子を示す写真を各条件毎に並べたものである。(a)はPRPを注入したもの、(b)はW−PRPを注入したもの、(c)はW−PRPにbFGF100μg/mlを添加して注入したもの、(d)はPPPを注入したもの、(e)は生理食塩水を注入したものである。外見上はPRP群、W−PRP群とW−PRP+bFGF群で耳介の肥厚を認めた。
【0036】
<組織学的検討>
図3は、局所注入2週後の耳介先端部位での耳介の横断切片をHE染色処理したものである。各写真の符号は図2におけるものと同一である。この所見では、PRP,W−PRP、W−PRP+100μg/ml bFGF群では、耳介の肥厚を認めた。とりわけ(c)のW−PRPにbFGFを添加したものでは他を凌駕する肥厚が認められた。耳介の肥厚の組織部位としては皮膚、皮下組織で著明であった。また、毛根の活性化も認められた。一方、PPPとコントロールとして生食を注入した群では、耳介の肥厚はほとんど認められなかった。
【0037】
図4は、耳介先端部から5mmの部位の厚さを比較した対比分析グラフである。各例を比較したところ、コントロール群やPPP群と比較し、PRP群、W−PRP群で肥厚傾向が認められた。またW−PRP+bFGF(10、100μg/ml)群では、有意に組織の肥厚が認められた。耳介の一番肥厚した部位の厚さの検討(図5)では、W−PRP群とbFGF添加W−PRP群で優位差のある耳介の肥厚が認められた。また、bFGF添加群では濃度依存性に耳介の肥厚が認められた。
【0038】
図6は、局所注入2週後の耳介先端部位での耳介の横断切片をαSMA染色処理したものである(各写真ごとの符号は図2及び図3と同一である)。また図7は各群におけるα陽性細胞の増加数をグラフ化したものである。αSMA染色の結果では、PPP群とコントロール群に比較し、PRP群、W−PRP群にαSMA陽性細胞数の増加傾向が認められた。また、W−PRP+bFGF(10、100μg/ml)群で優位なαSMA陽性細胞数の増加を認めた。図7は各群におけるαSMA陽性細胞数をグラフ化したものである。W−PRP+bFGF10群及びW−PRP+bFGF100群において顕著な効果が見られた。αSMA陽性細胞の増大により、組織を収縮させ、シワやたるみといった肌問題が改善されるという効果が期待される。
【0039】
以上のヌードマウス耳介への注入実験から、以下の結論が得られる。
(1)組織の増量には、PRPよりもW−PRPのほうが効果があることが認められた。
(2)組織の増量には、血小板のみならず、白血球の関与が重要であることが認められた。
(3)フィブリネット採血管を用いたW−PRPの作成には、1800回転、10分の遠心条件が最適であった。
(4)αSMA陽性細胞数は、PRP、W−PRP、bFGFを添加したW−PRPにおいて優位に増加していた。
【0040】
<肌問題の改善への適用>
以上の知見を、人間の肌のしわやたるみに対して適用する場面につき言及する。
人間の肌のしわやたるみの原因は、既述の通り老齢化に伴う肌の乾燥や皮下脂肪の減少、表情筋の過度の収縮や弛緩にあるといわれている。こうした問題を解決するために、老化した細胞の除去、新たな組織の産生が寄与する。一般的な創傷治癒過程における炎症期以降のステップを人為的に誘発することにより、肌組織が適切に増量するためのいわば材料が備わり、長期的な肌問題の改善に寄与するのである。
【0041】
しわやたるみに対してPRPを用いる場合、単なるPRPでは組織の増量は期待できず、W−PRPを用いる方がより優位な組織の増量が期待できる。これは、W−PRPに含まれている白血球がマクロファージを誘導し、さらにマクロファージが線維芽細胞を遊走、増殖させることが一因であると推測される。
【0042】
また組織の肥厚には筋線維芽細胞が関与していると考えられる。組織が肥厚することにより減少していた皮下組織が回復し、しわの改善に繋がるものである。また、潰瘍にPRPを用いるのと異なり、組織を構築しオーギュメンテーションを図るには、足場(scaffold)が必要であると考えられる。生体由来のスキャホールドとして、フィブリンや血小板糊によるネットワークの形成が重要であると考えられる。
【0043】
また、W-PRPに内在している白血球が周囲や流血中のマクロファージを注入部位に遊走させることも大切であると考えられる。マクロファージは、一般の創傷治癒において修復組織中に多数認められ、そのマクロファージは繊維芽細胞を遊走させて、その遊走してきた繊維芽細胞がコラーゲンを再生させると考えられるからである。つまり、W-PRPに含まれている白血球がマクロファージを誘導し、さらにマクロファージが線維芽細胞を遊走、増殖させることが一因であると推測されることから、従来の細胞移植の概念と異なり、サイトカインを放出する細胞を移植することによって、組織の修復に必要な細胞を生体自身から誘導するという新たな手法であるとも考えられる。これらの起序により、シワが改善するのではないかと考えられた。また、繊維芽細胞の中に出現する筋線維芽細胞組織を収縮させることによって、たるみを改善する効果があると考えられる。
【0044】
W-PRPにbFGFを添加することによって組織のさらなる増量が認められたことから、肌問題の改善にあっては、W-PRPはbFGFの徐放ドナーとしても有用であると思われる。ゼラチンなどを用いてbFGFを徐放させることでその働きを効果的にしようとの報告があるが、BSE問題もあり、ゼラチンをすぐに臨床で用いるのは難しい。外用剤としてのbFGF製剤を局所注入用に用いることに関しては、近年縫合創にbFGFを局所注射することによって創がきれいに治るとの報告や、ゼラチンを徐放ドナーとして局所注射することによってASOの患肢の血管新生の治療が可能であるとの報告からも、使用量を守れば問題ないと考えられる 。
【0045】
図8は、人体額部及び眼下部にW−PRPを注入したことの効果を示す図である。(a)は注入前、(b)は注入後7月経過時点の写真である。注入は、両下眼瞼及び右前額部(写真左側)について行った。写真からも明らかなように、注入を行った額部の隆起が生じており、陥没が改善されている。下眼瞼においても同様である。
【0046】
図9は、上記実験を行った人体をMRIにて撮影したものである。(a)の左はコントロールであり、右が注入を施したものである。(b)は当該部分の拡大図である。コントロール側では、骨の形態にそった陥凹が皮膚にまで認められるが、注入側では注入部位の皮膚、皮下組織(脂肪組織)、前頭筋の肥厚が認められ、皮膚の陥凹が消失していることが判る。
【0047】
<好適な混合注入キット>
次に、上記の肌問題改善方法に用いるW−PRPを迅速に抽出し、成長因子とともに注入するための混合注入キットについて説明する。図10(a)は、本発明を実施するにあたって好適な混合注入キット1を図示したものである。図10(b)に示すように、混合注入キット1は採血用試験管2、予め活性剤としての塩化カルシウム31が封入された第一の真空試験管3、及び予めbFGF41が封入された第二の真空試験管4を含んでいる。
【0048】
図11は、図10に示した混合注入キットを用いた肌問題改善方法の具体的ステップの一例を示したものである。まず、好適なシリンジを用い、肌問題を有する患者から採血用試験管2に採血する(図中ステップ(1)及び(2))。採血はすぐに遠心分離器にかけられる(ステップ(3))。この遠心分離にあたっては、上述のカスケードメディカル社製のPRP分離システムを用いることができる。所定の分離条件、例えば1800rpm/10minで遠沈させることにより上澄み部分をW−PRPとして抽出することができる(ステップ(4))。
【0049】
抽出したW−PRPは、直ちに第一の真空試験管3に移し替えられる。第一の真空試験管3には予め活性剤としての塩化カルシウムが封入されている。これをW−PRP混合後攪拌することにより、W−PRP内のサイトカインが活性化される(ステップ(5))。さらにこれを第二の真空試験管4へと移し変える(ステップ(6))。第二の真空試験管4には予めbFGFが封入されており、これと混合攪拌させた後、肌問題を有する患部に注入する。
【0050】
なお、塩化カルシウムとbFGFとを第一の真空試験管3と第二の真空試験管4とに分けて封入したのは、bFGFは粉体でないとその効能を維持することができないからである。このように、採血試験管2、第一の真空試験管3及び第二の真空試験管4がユニットとして備えられていることにより、迅速な処理が求められる肌問題改善の処置を速やかに行うことができ、肌問題の適切な改善に資する。
【0051】
なお、本実施例では混合注入キットに包含される構成要素として上記3種の試験管のみとしたが、これに限られず、例えば採血用のシリンジ、注入用のシリンジ及び注射針をキットに含めても良い。或いは、図示しないが、塩化カルシウムと所定量のbFGFとを一の真空試験管に封入してもよい。この場合bFGF効能を損なわないよう、塩化カルシウムも粉体のものを適用することが望ましい。
【図面の簡単な説明】
【0052】
【図1】各遠心分離条件毎の成分含有状況を示す写真である。
【図2】局所注入2週間後のヌードマウスの耳介の様子を示す写真を各条件毎に並べたものである。
【図3】局所注入2週後の耳介先端部位での耳介の横断切片をHE染色処理したものである。
【図4】耳介先端部から5mmの部位の厚さを比較した対比分析グラフである。
【図5】耳介の一番肥厚した部位の厚さを比較した対比分析グラフである。
【図6】局所注入2週後の耳介先端部位での耳介の横断切片をαSMA染色処理したものである。
【図7】各群におけるαSMA陽性細胞数をグラフ化したものである。
【図8】人体顔部への局所注入の前後を示す写真であり、(a)注入前の額部写真である。(b)注入後7月の額部写真である。
【図9】(a)局所注入を行った人体頭部の側面MRI画像(左は注入後7月、右はコントロール)である。(b)上記の注入部位の拡大図である。
【図10】本発明の一実施例である混合注入キットの構成を示した図である。
【図11】本発明の一実施例である混合注入キットを用いた肌問題改善の手順を図示したものである。
【符号の説明】
【0053】
1 混合注入キット
2 採血用試験管
3 第一の真空試験管
4 第二の真空試験管
31 塩化カルシウム
41 bFGF
【特許請求の範囲】
【請求項1】
細胞組織の増加を促進する方法であって、
患者から採血した血液を分離したものから白血球を含有する多血小板血漿を精製する工程と、
前記精製された多血小板血漿と、予め精製された成長因子とを少なくとも含む注入液を作成する工程と、
前記注入液を前期患者の要処方域に注入する工程と
を含むことを特徴とする細胞組織増加促進方法。
【請求項2】
前記多血小板血漿は、白血球を多量に含むことを特徴とする、請求項1に記載の細胞組織増加促進方法。
【請求項3】
前記白血球を多量に含む多血小板血漿は、3,900個/μl以上の白血球を含むことを特徴とする、請求項2に記載の細胞組織増加促進方法。
【請求項4】
前記成長因子は、塩基性線維芽細胞成長因子(bFGF)であることを特徴とする、請求項2から請求項4のいずれかに記載の細胞組織増加促進方法。
【請求項5】
請求項1から請求項4に記載の細胞組織増加促進方法を用いた肌問題改善方法であって、
前記要処方域は前記患者の肌問題が生じている箇所であることを特徴とする肌問題改善方法。
【請求項6】
前記肌問題は、表皮、真皮、皮下組織及び軟部組織における乾燥、弾力の低下、欠損、減耗を含むことを特徴とする、請求項5に記載の肌問題改善方法。
【請求項7】
請求項1ないし請求項6のいずれかに記載の細胞組織増加促進方法又は肌問題改善方法に用いられる多血小板血漿と成長因子とを混合して注入するための混合注入キットであって、
採血用試験管と、
塩化カルシウムが予め封入された第一の真空試験管と、
所定量の成長因子が予め封入された第二の真空試験管と
を含むことを特徴とする混合注入キット。
【請求項8】
請求項1ないし請求項6のいずれかに記載の細胞組織増加促進方法又は肌問題改善方法に用いられる多血小板血漿と成長因子とを混合して注入するための混合注入キットであって、
採血用試験管と、
塩化カルシウム及び所定量音成長因子が予め封入された真空試験管と
を含むことを特徴とする混合注入キット。
【請求項1】
細胞組織の増加を促進する方法であって、
患者から採血した血液を分離したものから白血球を含有する多血小板血漿を精製する工程と、
前記精製された多血小板血漿と、予め精製された成長因子とを少なくとも含む注入液を作成する工程と、
前記注入液を前期患者の要処方域に注入する工程と
を含むことを特徴とする細胞組織増加促進方法。
【請求項2】
前記多血小板血漿は、白血球を多量に含むことを特徴とする、請求項1に記載の細胞組織増加促進方法。
【請求項3】
前記白血球を多量に含む多血小板血漿は、3,900個/μl以上の白血球を含むことを特徴とする、請求項2に記載の細胞組織増加促進方法。
【請求項4】
前記成長因子は、塩基性線維芽細胞成長因子(bFGF)であることを特徴とする、請求項2から請求項4のいずれかに記載の細胞組織増加促進方法。
【請求項5】
請求項1から請求項4に記載の細胞組織増加促進方法を用いた肌問題改善方法であって、
前記要処方域は前記患者の肌問題が生じている箇所であることを特徴とする肌問題改善方法。
【請求項6】
前記肌問題は、表皮、真皮、皮下組織及び軟部組織における乾燥、弾力の低下、欠損、減耗を含むことを特徴とする、請求項5に記載の肌問題改善方法。
【請求項7】
請求項1ないし請求項6のいずれかに記載の細胞組織増加促進方法又は肌問題改善方法に用いられる多血小板血漿と成長因子とを混合して注入するための混合注入キットであって、
採血用試験管と、
塩化カルシウムが予め封入された第一の真空試験管と、
所定量の成長因子が予め封入された第二の真空試験管と
を含むことを特徴とする混合注入キット。
【請求項8】
請求項1ないし請求項6のいずれかに記載の細胞組織増加促進方法又は肌問題改善方法に用いられる多血小板血漿と成長因子とを混合して注入するための混合注入キットであって、
採血用試験管と、
塩化カルシウム及び所定量音成長因子が予め封入された真空試験管と
を含むことを特徴とする混合注入キット。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【公開番号】特開2009−235004(P2009−235004A)
【公開日】平成21年10月15日(2009.10.15)
【国際特許分類】
【出願番号】特願2008−84595(P2008−84595)
【出願日】平成20年3月27日(2008.3.27)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 発行者名 :第16回日本形成外科学会基礎学術集会事務局 刊行物名 :第16回日本形成外科学会基礎学術集会プログラム・抄録集 発行年月日:平成19年10月11日
【出願人】(501345666)ジェイ・ヒューイット株式会社 (2)
【Fターム(参考)】
【公開日】平成21年10月15日(2009.10.15)
【国際特許分類】
【出願日】平成20年3月27日(2008.3.27)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 発行者名 :第16回日本形成外科学会基礎学術集会事務局 刊行物名 :第16回日本形成外科学会基礎学術集会プログラム・抄録集 発行年月日:平成19年10月11日
【出願人】(501345666)ジェイ・ヒューイット株式会社 (2)
【Fターム(参考)】
[ Back to top ]

