組成物及び前記組成物を用いた造影剤の製造方法
【課題】高密度に集積した粒子等を作製するため、疎水性溶媒に溶解しやすい親水性色素からなる組成物を提供すること。
【解決手段】スルホン酸基を有する親水性色素と疎水性溶媒とを有する組成物において、前記組成物がニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方を有することを特徴とする組成物。
【解決手段】スルホン酸基を有する親水性色素と疎水性溶媒とを有する組成物において、前記組成物がニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方を有することを特徴とする組成物。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、疎水性溶媒への溶解性を向上した、親水性色素を有する組成物及び前記組成物を用いた造影剤の製造方法に関する。
【背景技術】
【0002】
近年、非侵襲的に診断ができるイメージング方法として蛍光法や、光音響トモグラフィーが注目されている。光音響トモグラフィーは、光エネルギーを吸収した分子が放出する熱が起こす体積膨張により生じる音響波を検出する方法である。蛍光法や光音響トモグラフィーにおいて、観察対象部位の信号強度を増幅するために、色素を造影剤として用いることができる。この場合、生体に体外から排出しやすく、臨床検査に用いる際に安全性がより高い親水性色素を用いることが望まれる。インドシアニングリーン(Indocyanine Green、以下、ICGと略すことがある)は近赤外蛍光色素であるが、承認された医薬品であり、肝機能検査、循環機能検査、乳癌のセンチネルリンパ節の同定の診断に用いられている。すなわち、ICGは人体への投与における安全性が確認されており、光音響トモグラフィーの造影剤として用いられることが期待される親水性色素の1つである。
【0003】
一方、光音響トモグラフィーに用いる際に信号強度を有効に増幅するために、色素を粒子、ミセル、ポリマーミセル、リポソーム(総称して粒子等という)に集積することが望まれる。集積することにより、色素密度を上げて、照射エネルギーの吸収効率を上げると共に、特に色素が蛍光色素の場合は集積することで、消光を起こさせ、照射エネルギー中が蛍光発光に用いられることを防ぎ、より多くの熱エネルギーに変換するためである。
【0004】
非特許文献1には、ICGを親水性溶媒であるメタノールに溶解し、疎水性溶媒であるジクロロメタンと混合することで、Nanoemulsion法により、ICGをポリマーナノ粒子中に集積化した結果が報告されている。
【0005】
一方、非特許文献2には、ICGのテトラブチルアンモウニム塩を作製し、疎水性溶媒であるクロロホルムに溶解することで、Nanoemulsion法により、ICGをポリマーナノミセル中に集積化した結果が報告されている。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】Colloids and Surfaces B: Biointerfaces 75 (2010) 260−267
【非特許文献2】Journal of Biomedical Optics 131, 014025, 2008
【発明の概要】
【発明が解決しようとする課題】
【0007】
親水性色素は疎水性溶媒に難溶である。そのため、非特許文献1においては、ICGをジクロロメタンではなく、親水性溶媒であるメタノールに溶解させて、ジクロロメタンと混合して利用し粒子を作製している。
しかしながらこの手法では、ポリマー粒子作製時に親水性色素を含む材料を溶解させた有機溶媒を水に分散させる工程において、親水性色素が粒子外へ拡散し、粒子内へ色素を高濃度に集積することが困難である。
【0008】
また、非特許文献2においては、ICGが疎水性溶媒であるクロロホルムに溶解しないため、テトラブチルアンモウニム塩を用いて、ICGテトラブチルアンモウニム塩を作製し、クロロホルムに溶解させて粒子を作製している。
しかしながらこの手法では、親水性色素とテトラブチルアンモウニムからなる塩のクロロホルムへの溶解量が少なく、ミセル内へ親水性色素を高濃度に集積することが困難である。
【0009】
本発明者等は親水性色素を、高密度に集積した粒子等をエマルション法により作製するための組成物を提供すべく検討した。なお、本明細書中、エマルション法とは、親水性溶媒と疎水性溶媒を混和して、液・液分散状態とすることで粒子を形成する方法をさす。
【課題を解決するための手段】
【0010】
本発明は、スルホン酸基を有する親水性色素と疎水性溶媒とを有する組成物において、前記組成物がニコチン酸誘導体チアミン誘導体のうち少なくともいずれか一種を有することを特徴とする組成物に関する。
【発明の効果】
【0011】
本発明によれば、親水性色素の疎水性溶媒への溶解を可能にし、粒子等に親水性色素を高濃度に集積させることを可能にする。ICGのような親水性色素の疎水性溶媒の溶解性が向上することから、親水性色素の応用範囲を広げることが出来る。
【図面の簡単な説明】
【0012】
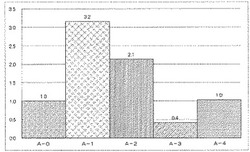
【図1】実施例A−1、A−2及び比較例A−0、A−3、A−4における親水性色素含有組成物のクロロホルム溶解性の評価結果である。
【図2】実施例B−1乃至B−2及び比較例B−0、B−5乃至B−7における親水性色素含有組成物のジクロロメタン溶解性の評価結果である。
【図3】実施例WBにおける、親水性色素含有組成物ジクロロメタン溶液の水へのICG移行量の評価結果である。
【図4】本実施形態に係る光イメージング用造影剤の製造方法の一例を説明するための図である。
【発明を実施するための形態】
【0013】
以下、本発明の実施形態について説明する。
【0014】
本発明の一の実施形態は、スルホン酸基を有する親水性色素、疎水性溶媒並びに、ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方を有する組成物に関する。
【0015】
本発明の一の実施形態では、ニコチン酸誘導体及び/またはチアミン誘導体を有することにより、スルホン酸基を有する親水性色素の疎水性溶媒への溶解度が高められる。この組成物を水と混和してエマルション法により粒子を形成した際、粒子内から水中へのスルホン酸基を有する色素の溶出量が抑制される。従って、本実施形態に係る組成物を用いれば、水中への、スルホン酸基を有する親水性色素の溶出の少ない粒子を作製することができ、蛍光法、及び光音響トモグラフィー等に有効に用いられる造影剤を調製できる。
本実施形態に係る組成物において、スルホン酸基を有する親水性色素の疎水性溶媒中の濃度は、0.01〜200mg/mL、好ましくは、0.1〜100mg/mLの範囲であることが好ましい。
また本実施形態に係る組成物は、光イメージング用造影剤製造用の組成物であることが好ましい。また、光音響イメージング用造影剤製造用の組成物であることがさらに好ましい。
【0016】
なお、スルホン酸基を有する親水性色素にニコチン酸誘導体及び/またはチアミン誘導体を添加することにより、スルホン酸基を有する親水性色素の疎水性溶媒への溶解度が高められる理由は以下のとおりであると考えられる。すなわち、ニコチン酸誘導体及び/またはチアミン誘導体がスルホン酸基を有する親水性色素の親水基に会合し、スルホン酸基を有する親水性色素が疎水性溶媒に溶解しやすくなるためと考えられる。特には、ニコチン酸誘導体ではピリジン環を含むニコチン酸骨格、チアミン誘導体はピリミジン環、あるいは、アミノ基の寄与が考えられる。なお、本発明におけるピリジン環を含むニコチン酸骨格とは、具体的には、ニコチン酸アミドからNH2を除いた構造を意味する。
【0017】
(スルホン酸基を有する親水性色素)
本実施形態においてスルホン酸基を有する親水性色素は、生体内で利用するにあたり、色素は生体から排出されやすい親水性色素が安全であり望ましい。また、本実施形態に係る組成物においては、ニコチン酸誘導体及び/またはチアミン誘導体が、スルホン酸基に会合して効果を奏すると考えられるため、とりわけスルホン酸基を有する親水性色素が好ましい。また、親水性色素は、生体内における光の吸収、拡散の影響が少ない「生体の窓」と呼ばれる600ナノメートル以上1300ナノメートル以下の波長に吸収を持つものが好ましい。以下、スルホン酸基を有する親水性色素を、単に、親水性色素と呼ぶことがある。
【0018】
前記親水性色素としては、例えば、アジン系色素、アクリジン系色素、トリフェニルメタン系色素、キサンテン系色素、ポルフィリン系色素、シアニン系色素、フタロシアニン系色素、スチリル系色素、ピリリウム系色素、アゾ系色素、キノン系色素、テトラサイクリン系色素、フラボン系色素、ポリエン系色素、BODIPY(登録商標)系色素、インジゴイド系色素を挙げることが出来る。
【0019】
前記シアニン系色素としては、例えば、インドシアニングリーン(ICG)、Alexa Fluor(登録商標)系色素(インビトロジェン社製)、Cy(登録商標)系色素(GE ヘルスケア バイオサイエンス社製)、IR−783 、IR−806、IR−820(シグマ アルドリッチ ジャパン株式会社製)、IRDye 800CW、IRDye 800RS(登録商標)(LI−COR社製)、ADS780WS、ADS795WS、ADS830WS、ADS832WS(American Dye Source社製)を挙げることが出来る。
【0020】
なお、本実施形態において、ICG(インドシアニングリーン)は下記の化学式1で示される構造、ただし、構造中、対イオンはNa+でなくともよく、例えばH+あるいはK+等であり得る。
【化1】

なお、上記のIR−820は下記の化学式2で示される。
【化2】

【0021】
前記インジゴイド系色素としては、例えば、インジゴカルミンを挙げることが出来る。
これらの親水性色素は、単独で使用してもよく、任意に混合して使用してもよい。
また、本実施形態において、パテントブルーなどの親水性色素を用いることもできる。
【0022】
(ニコチン酸誘導体)
本実施形態におけるニコチン酸誘導体は、ニコチン酸骨格を有していれば特に限定されないが、下記の一般式(I)で表されることが好ましい。
【化3】

式(I)において、Aは下記の式(a1)、式(a2)、式(a3)のいずれかである。式(a1)、式(a2)、式(a3)中の*は結合手を表し、*が式(I)のZと結合する。
【化4】

式(I)において、Zは下記の式(z1)、式(z2)、式(z3)のいずれかである。式(z1)、式(z2)、式(z3)中の*は結合手を表し、*が式(I)のAと結合する。式(z2)において、R1は水素原子、置換または無置換の炭素数1乃至10のアルキル基、ベンジル基のいずれかである。前記置換基はハロゲン原子、炭素数1乃至5のアルキル基、ヒドロキシル基、アミノ基のいずれかである。
【化5】

【化6】

【化7】

【0023】
本実施形態に係るニコチン酸誘導体が上記の式(I)で表される場合、スルホン酸基を有する親水性色素のスルホン酸基の負電荷と、ピリジン環の窒素原子と溶媒などに存在するプロトンとで形成されるNH+の正電荷が電荷をキャンセルすることで、該親水性色素が、疎水性溶媒に対して溶解しやすくなっていると考えられる。したがって、式(a1)、式(a2)、式(a3)のように、オルト、メタ、パラのいずれの位置に官能基が存在しても、式(I)で表されるニコチン酸誘導体とスルホン酸基を有する親水性色素の、疎水性溶媒に対する溶解性は、該親水性色素のみに比べて高いと考えられる。
【0024】
本実施形態におけるニコチン酸誘導体としては、ニコチン酸アミド、ニコチン酸ベンジルエステル、ニコチン酸、ニコチン酸メチル、ニコチン酸エチル、イソニコチン酸エチル、ニコチン酸トコフェロール等を挙げられる。これらのうち、ニコチン酸アミドまたはニコチン酸ベンジルエステルのうち少なくともいずれか一方であることが好ましい。
ニコチン酸誘導体は、単独で使用してもよく、任意に混合して使用してもよい。
【0025】
(チアミン誘導体)
本実施形態におけるチアミン誘導体は、特に限定されないが、下記の一般式(II)で表されることが好ましい。
【化8】

式(II)において、Bは下記の式(b)である。式(b)中の*1は結合手を表し、*1が式(II)のXと結合する。式(b)中の*2は結合手を表し、*2が式(II)のYと結合する。
【化9】

式(II)において、Xは下記の式(x1)、式(x2)、式(x3)のいずれかである。式(x1)、式(x2)、式(x3)中の*は結合手を表し、*が式(II)のBと結合する。式(x1)においてnは1乃至10のいずれかの整数である。式(x1)はハロゲン原子、炭素数1乃至5のアルキル基、ヒドロキシル基、アミノ基のいずれかで置換されていてもよい。式(x4)において、R2は、置換または無置換の炭素数1乃至10のアルキル基、置換または無置換のベンゼンのいずれかである。
【化10】

【化11】

【化12】

【化13】

式(II)において、Yは下記の式(y1)、式(y2)のいずれかである。式(y1)、式(y2)中の*は結合手を表し、*が式(II)のBと結合する。式(y2)において、R3は、置換または無置換の炭素数1乃至10のアルキル基、置換または無置換のベンゼンのいずれかである。
【化14】

【化15】

【0026】
チアミン誘導体としては、チアミンジスルフィド、プロスルチアミン、フルスルチアミン、ビスベンチアミン、スルブチアミン等が挙げられる。これらの中で、フルスルチアミン、プロスルチアミン、チアミンジスルフィドのうち少なくともいずれか一種であることが好ましい。
チアミン誘導体は、単独で使用してもよく、任意に混合して使用してもよい。
【0027】
また、ニコチン酸誘導体とチアミン誘導体を任意に混合して使用してもよい。
【0028】
(疎水性溶媒)
本実施形態に係る組成物は疎水性溶媒に対する溶解度の高いことを特徴とする。本実施形態において、疎水性溶媒は水に自由混合しない溶媒である。一方、水に自由混合する溶媒が親水性溶媒である。ここでいう自由混合とは、2つ以上の溶媒を混合したときに相分離などすることなく、均一に混じり合うことを意味する。
本実施形態における疎水性溶媒としては、ヘキサン、シクロへキサン、ヘプタン等の炭化水素類、ジメチルエーテル、ジエチルエーテル等のエーテル類、ジクロロメタン、クロロホルム、四塩化炭素、ジクロロエタン、トリクロロエタン等のハロゲン化炭化水素類、ベンゼン、トルエン等の芳香族炭化水素、酢酸エチル、酢酸ブチル等のエステル類が挙げられる。これらの中で、クロロホルム、ジクロロメタンのうち少なくともいずれか一方であることが好ましい。
疎水性溶媒は、単独で使用してもよく、任意に混合して使用してもよい。
【0029】
(組成物の作製方法)
本実施形態に係る組成物は、親水性色素と、ニコチン酸誘導体及び/またはチアミン誘導体を混合して得られるが、混合には公知の方法を利用することが出来、特に限定されない。
【0030】
本実施形態に係る組成物におけるニコチン酸誘導体及び/またはチアミン誘導体の量は、親水性色素に対して、0.1〜100.0倍モル、好ましくは、1.0倍〜20.0倍モルの範囲であることが好ましい。
【0031】
親水性色素と、ニコチン酸誘導体及び/またはチアミン誘導体との混合の際は、必要に応じ、溶媒を使用することが出来る。この際、溶媒として、ヘキサン、シクロへキサン、ヘプタン等の炭化水素類、アセトン、メチルエチルケトン等のケトン類、ジメチルエーテル、ジエチルエーテル、テトラヒドロフラン等のエーテル類、ジクロロメタン、クロロホルム、四塩化炭素、ジクロロエタン、トリクロロエタン等のハロゲン化炭化水素類、ベンゼン、トルエン等の芳香族炭化水素、エタノール、メタノール、イソプロパノール等のアルコール類、N,N−ジメチルホルムアミド、ジメチルスルホキシド等の非プロトン性極性溶媒類、酢酸エチル、酢酸ブチル等のエステル類、ピリジン誘導体、リン酸バッファー等の緩衝液、水、等を用いることができる。溶媒は、親水性色素並びに前記ニコチン酸誘導体及び/またはチアミン誘導体が溶解するものが好ましい。溶媒の使用量は、前記親水性色素の使用量、前記ニコチン酸誘導体及び/またはチアミン誘導体の使用量、混合条件等に応じて適宜定め得る。
【0032】
混合温度は、特に限定されないが、通常は−30℃から、溶媒を用いる場合は、使用する溶媒の沸点までの範囲の温度である。ただし、親水性色素、前記ニコチン酸誘導体及び/またはチアミン誘導体、並びに溶媒に合わせ、適宜最適な温度で混合を行うことが望ましい。混合時間は一概には言えないが、通常、1〜48時間の範囲であることが好ましい。
【0033】
混合溶液の溶媒は必要に応じて、常法である蒸留あるいはカラムクロマトグラフィー法を用いて取り除くことができるし、また、組成物が溶媒を含んでいてもよい。
【0034】
混合の際は、親水性色素を疎水性溶媒に分散させた後、ニコチン酸誘導体及び/またはチアミン誘導体を添加してもよいし、ニコチン酸誘導体及び/または、チアミン誘導体を疎水性溶媒に分散、または溶解させた後、親水性色素を添加してもよい。
【0035】
また、本実施形態に係る組成物は、必要に応じ、溶媒を含有、溶媒に分散、または、溶解させた状態であってもよい。
【0036】
<粒子化>
本実施形態に係る組成物は、水と混和した際に水への親水性色素の溶出量が少ない。従って、水に対してO/W型の液・液分散状態を形成する工程と、その後に有機溶剤相を固定する工程とによりICGを含有する粒子を形成する場合、親水性色素の利用率を高くすることができる。そのような有機溶剤相の固定工程としては、従来公知のものを用いることができる。一例を示すならば、本実施形態に係る組成物に対してこれに可溶な重合性モノマーあるいはプレポリマー、重合架橋剤等を添加し、得られた産物を水に液・液分散させた状態とした後、前記の重合性材料を重合反応することにより、有機溶剤相を固定し、粒子化することができる。ラジカル重合反応を進めるためには、低温用の熱重合開始剤や、酸化還元型ラジカル発生剤を好適に用いることができる。また別の例を示すならば、前記組成物にジカルボン酸塩化物を加えておき、これをジアミンの水溶液に液・液分散することにより、界面にてジカルボン酸とジアミンとからなる重縮合高分子膜を形成させて有機溶剤相を包含固定することができる。また、粒子化に際して界面活性剤を用いてもよい。このようにしてできた粒子は、蛍光法、及び光音響トモグラフィー等に有効に用いられる造影剤として用いることができる。
【0037】
<光イメージング用造影剤の製造方法>
本実施形態に係る光イメージング用造影剤の製造方法は、スルホン酸基を有する親水性色素と、疎水性溶媒と、ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方と、重合性モノマーあるいはプレポリマーとを有する組成物を用意する工程と、前記組成物と水を混合する混合工程と、前記混合工程の後に、前記重合性モノマーあるいは前記プレポリマーを重合する工程と、を有することを特徴とする。
本実施形態に係る光イメージング用造影剤の製造方法の一例について図3を用いて説明する。
まず、スルホン酸基を有する親水性色素101と、疎水性溶媒102と、ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方103と、重合性モノマーあるいはプレポリマー104とを有する組成物105を用意する。次に組成物105と、水106とを混合する。混合して得られた液体に超音波などを照射することにより、エマルションを得る。このとき得られたエマルションの分散質107は、上記の組成物105を有する。エマルションの分散質のうち、重合性モノマーあるいはプレポリマーを重合することで、光イメージング用造影剤108を得ることができる。
なお、重合性モノマーあるいはプレポリマーを重合する前に、エマルションの分散質から、疎水性溶媒を除去することが好ましい。疎水性溶媒を除去する方法としては、減圧する方法などが挙げられる。
【0038】
<光イメージング用造影剤>
本実施形態おける光イメージング用造影剤について説明する。本実施形態において光イメージングとは、光を照射することで、イメージング(画像化)することを意味する。すなわち、本実施形態に係る光イメージング用造影剤のスルホン酸基を有する親水性色素に光が照射されることで、音響波や蛍光などを発する。発せられた音響波を検出することで光音響イメージングをすることができ、発せられた蛍光を検出することで蛍光イメージングをすることができる。なお、光音響イメージングは、光音響トモグラフィー(断層撮影法)を含む概念である。
本実施形態に係る造影剤は、さらに、例えば生理食塩水、注射用蒸留水、リン酸緩衝生理食塩水(Phosphate buffered saline、以下PBSと略すことがある)などの分散媒を有していてもよい。また本実施形態に係る光イメージング用造影剤は、必要に応じて薬理上許容できる添加物を有していても良い。
本実施形態に係る光イメージング用造影剤は、上記の分散媒に予め分散させておいてもよいし、キットにしておき、生体内に投与する前に分散媒に分散させて使用してもよい。このように、本実施形態に係る光イメージング用造影剤は、光音響イメージング用造影剤や、蛍光イメージング用造影剤として利用することができる。
本実施形態に係る光イメージング用造影剤は、EPR(Enhanced Permeability and Retention)効果を利用することで、生体内に投与したときに、生体内の正常部位に比べて腫瘍部位により多く集積させることができる。その結果、複合体を生体内に投与した後、生体に光を照射して、生体からの音響波や蛍光を検出するときに、腫瘍部位から発せられる音響波や蛍光を正常部位から発せられる音響波や蛍光よりも大きくすることができる。従って、本実施形態に係る複合体は腫瘍部位を特異的に検出する光イメージング用造影剤として用いることができる。
【0039】
(重合性モノマーあるいはプレポリマー)
本実施形態において、重合性モノマーあるいはプレポリマーは上記の、スルホン酸基を有する親水性色素と疎水性溶媒とニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方とを有する組成物に可溶なものであれば特に限定されない。ここで、プレポリマーとは、重合性モノマーの重合または縮合反応を適当な所で止めた中間生成物のことであり、ポリマーとなる前段階にある状態のものを指す。
重合性モノマーとして例えば、スチレン、メタクリル酸、メタクリル酸ブチル、メタクリル酸ブチル−メタクリル酸メチル共重合体、乳酸、グリコール酸などを挙げることができる。
【0040】
(重合開始剤)
上記の重合性モノマーあるいはプレポリマーを重合させる重合開始剤としては、
従来から知られるものを使用できる。その具体例としては、アゾ系開始剤、パーオキサイド系開始剤、レドックス系開始剤、原子移動ラジカル開始剤、ニトロキサイド系開始剤等が挙げられる。特に、種類が豊富でモノマーの種類に合わせて適切なものを選ぶことができ、入手しやすく、安価であるアゾ系開始剤やパーオキサイド系開始剤を用いることが好ましい。
【0041】
(界面活性剤)
界面活性剤としては、例えば、ポリオキシエチレンアルキルエーテル、アルキル硫酸塩、リン脂質、ポリオキシエチレンソルビタン系脂肪酸エステル、ポリビニルアルコール、ポリオキシエチレンポリオキシプロピレングリコールを挙げることが出来る。
前記ポリオキシエチレンソルビタン系脂肪酸エステルとしては、Tween20、Tween40、Tween60、Tween80を挙げることが出来る。
前記リン脂質としては、アミノ基、NHS基、マレイミド、メトキシ基のいずれかの官能基とPEG鎖を有するホスファチジル系リン脂質を挙げることができる。
ホスファチジル系リン脂質としては、3−(N−succinimidyloxyglutaryl) aminopropyl, polyethyleneglycol−carbamyl distearoylphosphatidyl−ethanolamine(DSPE−PEG−NHS)、N−(3−maleimide−1−oxopropyl) aminopropyl polyethyleneglycol−carbamyl distearoylphosphatidyl−ethanolamine(DSPE−PEG−MAL)、N−(aminopropyl polyethyleneglycol)−carbamyl distearoylphosphatidyl−ethanolamine(DSPE−PEG−NH2)、N−(Carbonyl−methoxypolyethyleneglycol 2000)−1,2−distearoyl− sn−glycero−3−phosphoethanolamine, sodium salt(SUNBRIGHT DSPE−020CN)、N−(Carbonyl−methoxypolyethyleneglycol 5000)−1,2−distearoyl− sn−glycero−3−phosphoethanolamine, sodium salt(SUNBRIGHT DSPE−050CN)を挙げることができる。
ポリオキシエチレンポリオキシプロピレングリコールとしては、プルロニック(登録商標)F68、プルロニック(登録商標)F127を挙げることが出来る。
これらの界面活性剤は、単独で使用してもよく、任意に混合して使用してもよい。
【実施例】
【0042】
以下に、本発明の特徴をさらに明らかにするために実施例に沿って本発明を説明するが、本発明は、これらの実施例に限定されるものではなく、材料、組成条件等、同様な機能、効果を有する組成物が得られる範囲で自由に変えることが出来る。
【0043】
(実施例A―1)
ICG((財)日本公定書協会製)11mgをメタノール4mLに溶解させた。このICGに対して、20倍(モル比)のニコチン酸アミド34.7mgをメタノール4mLに溶解させた。この両メタノール溶液を混合し、15分攪拌した後、エバポレーターを用いて、メタノールを留去した。これにクロロホルム4mLを加えて攪拌した。さらに、超音波分散装置を用いて30秒間超音波照射を行った。孔径0.45マイクロメートルのフィルターを用いてろ過を行い、溶解した成分を回収した。回収された試料をA−1という。
【0044】
(実施例A−2、比較例A−3)
A−2、A−3は、実施例A−1で、ニコチン酸アミドを用いた代りに、ニコチン酸ベンジルエステル、ピリジンを用いた以外は、A−1と同様にして得られた。
【0045】
(比較例A−0)
比較対照であるA−0は、実施例A−1で、ニコチン酸アミドを用いない以外は、実施例A−1と同様にして得られた。
【0046】
(比較例A−4)
比較対照であるA−4は、ニコチン酸アミドを用いる代りに、非特許文献2で用いられている、テトラブチルアンモニウムヨージドを用い、それ以外は、A−1と同様に得られた。
【0047】
(実施例B−1、B−2)
B−1、B−2は、実施例A−1、A−2で、クロロホルムを用いる代りに、ジクロロメタンを用いた以外は、実施例A−1、A−2と同様に得られた。
【0048】
(比較例B−0)
比較対照であるB−0は、実施例B−1で、ニコチン酸アミドを用いない以外は、実施例B−1と同様に得られた。
【0049】
(比較例B−5)
比較対照であるB−5は、比較例B−0で、ジクロロメタンを用いる変わりに、ジクロロメタン:メタノール=3:1の混合溶液を用いた以外は、比較例B−0と同様に得られた。
【0050】
(比較例B−6)
比較対照であるB−6は、比較例B−0で、ジクロロメタンを用いる変わりに、ジクロロメタン:メタノール=1:1の混合溶液を用いた以外は、比較例B−0と同様に得られた。
【0051】
(比較例B−7)
比較対照であるB−7は、比較例B−0で、ジクロロメタンを用いる変わりに、ジクロロメタン:メタノール=1:3の混合溶液を用いた以外は、比較例B−0と同様に得られた。
【0052】
(実施例C−1、C−2、C−3)
C−1、C−2、C−3は、実施例A−1で、ニコチン酸アミドを用いた代りに、フルスルチアミン、プロスルチアミン、チアミンジスルフィドを用いた以外は、A−1と同様にして得られた。
【0053】
(溶解性評価)
上記実施例及び比較例で回収したA−0からA−4溶液を1000倍希釈して、常法に従い、UV−VIS−NIR測定を行った。550nmから950nmまでの吸光度を積算し、A−0で得られた値を1として規格化し、比較したものが図1である。
【0054】
色素と溶媒からなる対照組成物(A−0)と比較して、ニコチン酸アミドを用いた場合(A−1)は3.2倍、ニコチン酸ベンジルエステルを用いた場合(A−2)は2.1倍と、非常に良好な溶解性を示した。
【0055】
また、非特許文献2で用いられているテトラブチルアンモニウム塩を用いた場合(A−4)と比較しても、ニコチン酸アミドを用いた場合(A−1)は3.2倍、ニコチン酸ベンジルエステルを用いた場合(A−2)は2.1倍と、非常に良好な溶解性を示した。
【0056】
また、ピリジンを用いた場合(A−3)は、有効性が見られなかった。
【0057】
上記実施例及び比較例で回収したB−0からB−7溶液を1000倍希釈して、常法に従い、UV−VIS−NIR測定を行った。550nmから950nmまでの吸光度を積算し、比較例B−0の値を1として規格化し、比較したものが図2である。
【0058】
色素と溶媒からなる対照組成物(B−0)と比較して、ニコチン酸アミドを用いた場合(B−1)は10.4倍、ニコチン酸ベンジルエステルを用いた場合(B−2)は6.2倍と、非常に良好な溶解性を示した。
【0059】
また、B−0と比較して、メタノールを用いた場合(B−5、B−6,B−7)は6.3倍〜9.1倍とメタノールの添加量に応じて、非常に良好な溶解性を示した。
【0060】
上記実施例及び比較例で回収したC−1からC−3、A−0溶液を1000倍希釈して、常法に従い、UV−VIS−NIR測定を行った。550nmから950nmまでの吸光度を積算し、A−0で得られた値を1として規格化し比較した。
【0061】
色素と溶媒からなる対照組成物(A−0)と比較して、フルスルチアミンを用いた場合(C−1)は1.4倍、プロスルチアミンを用いた場合(C−2)は1.6倍と、チアミンジスルフィドを用いた場合(C−3)は1.9倍と、非常に良好な溶解性を示した。
【0062】
(実施例WB 疎水性溶媒から水への移行性評価)
上記実施例及び比較例で作製したB−0、B−1、B−2、B−5、B−6、B−7溶液0.5mLに、超純水1.5mL加えて、3秒間振盪した。5分間静置した後、水層を回収し、各々のサンプルを、WB−0、WB−1、WB−2、WB−5、WB−6、WB−7とした。
【0063】
常法に従い、UV−VIS−NIR測定を行った。550nmから950nmまでの吸光度を積算し、組成物WB−0、WB−1、WB−2、WB−5、WB−6、WB−7のICGの溶解量で規格化し、ICG同一量における水への移行量を算出した。サンプルB−0の移行量を1として規格化し、比較したものが図3である。
【0064】
メタノールを用いた場合(WB−5、WB−6、WB−7)は、疎水性溶媒から水への移行量が、WB−0と比較して、1.0倍〜2.9倍と大きな移行性を示した。
【0065】
一方、ニコチン酸アミド(WB−1)、ニコチン酸ベンジルエステルを用いた場合(WB−2)は、共に、疎水性溶媒から水への移行量は、WB−0と比較して、0.3倍、0.2倍と小さな値を示した。
【0066】
なお、実施例A、B、WBで用いた各試料の概略を表1に示す。
【0067】
【表1】

【符号の説明】
【0068】
101 スルホン酸基を有する親水性色素
102 疎水性溶媒
103 ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方
104 重合性モノマーあるいはプレポリマー
105 組成物
106 水
107 エマルションの分散質
108 光イメージング用造影剤
【技術分野】
【0001】
本発明は、疎水性溶媒への溶解性を向上した、親水性色素を有する組成物及び前記組成物を用いた造影剤の製造方法に関する。
【背景技術】
【0002】
近年、非侵襲的に診断ができるイメージング方法として蛍光法や、光音響トモグラフィーが注目されている。光音響トモグラフィーは、光エネルギーを吸収した分子が放出する熱が起こす体積膨張により生じる音響波を検出する方法である。蛍光法や光音響トモグラフィーにおいて、観察対象部位の信号強度を増幅するために、色素を造影剤として用いることができる。この場合、生体に体外から排出しやすく、臨床検査に用いる際に安全性がより高い親水性色素を用いることが望まれる。インドシアニングリーン(Indocyanine Green、以下、ICGと略すことがある)は近赤外蛍光色素であるが、承認された医薬品であり、肝機能検査、循環機能検査、乳癌のセンチネルリンパ節の同定の診断に用いられている。すなわち、ICGは人体への投与における安全性が確認されており、光音響トモグラフィーの造影剤として用いられることが期待される親水性色素の1つである。
【0003】
一方、光音響トモグラフィーに用いる際に信号強度を有効に増幅するために、色素を粒子、ミセル、ポリマーミセル、リポソーム(総称して粒子等という)に集積することが望まれる。集積することにより、色素密度を上げて、照射エネルギーの吸収効率を上げると共に、特に色素が蛍光色素の場合は集積することで、消光を起こさせ、照射エネルギー中が蛍光発光に用いられることを防ぎ、より多くの熱エネルギーに変換するためである。
【0004】
非特許文献1には、ICGを親水性溶媒であるメタノールに溶解し、疎水性溶媒であるジクロロメタンと混合することで、Nanoemulsion法により、ICGをポリマーナノ粒子中に集積化した結果が報告されている。
【0005】
一方、非特許文献2には、ICGのテトラブチルアンモウニム塩を作製し、疎水性溶媒であるクロロホルムに溶解することで、Nanoemulsion法により、ICGをポリマーナノミセル中に集積化した結果が報告されている。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】Colloids and Surfaces B: Biointerfaces 75 (2010) 260−267
【非特許文献2】Journal of Biomedical Optics 131, 014025, 2008
【発明の概要】
【発明が解決しようとする課題】
【0007】
親水性色素は疎水性溶媒に難溶である。そのため、非特許文献1においては、ICGをジクロロメタンではなく、親水性溶媒であるメタノールに溶解させて、ジクロロメタンと混合して利用し粒子を作製している。
しかしながらこの手法では、ポリマー粒子作製時に親水性色素を含む材料を溶解させた有機溶媒を水に分散させる工程において、親水性色素が粒子外へ拡散し、粒子内へ色素を高濃度に集積することが困難である。
【0008】
また、非特許文献2においては、ICGが疎水性溶媒であるクロロホルムに溶解しないため、テトラブチルアンモウニム塩を用いて、ICGテトラブチルアンモウニム塩を作製し、クロロホルムに溶解させて粒子を作製している。
しかしながらこの手法では、親水性色素とテトラブチルアンモウニムからなる塩のクロロホルムへの溶解量が少なく、ミセル内へ親水性色素を高濃度に集積することが困難である。
【0009】
本発明者等は親水性色素を、高密度に集積した粒子等をエマルション法により作製するための組成物を提供すべく検討した。なお、本明細書中、エマルション法とは、親水性溶媒と疎水性溶媒を混和して、液・液分散状態とすることで粒子を形成する方法をさす。
【課題を解決するための手段】
【0010】
本発明は、スルホン酸基を有する親水性色素と疎水性溶媒とを有する組成物において、前記組成物がニコチン酸誘導体チアミン誘導体のうち少なくともいずれか一種を有することを特徴とする組成物に関する。
【発明の効果】
【0011】
本発明によれば、親水性色素の疎水性溶媒への溶解を可能にし、粒子等に親水性色素を高濃度に集積させることを可能にする。ICGのような親水性色素の疎水性溶媒の溶解性が向上することから、親水性色素の応用範囲を広げることが出来る。
【図面の簡単な説明】
【0012】
【図1】実施例A−1、A−2及び比較例A−0、A−3、A−4における親水性色素含有組成物のクロロホルム溶解性の評価結果である。
【図2】実施例B−1乃至B−2及び比較例B−0、B−5乃至B−7における親水性色素含有組成物のジクロロメタン溶解性の評価結果である。
【図3】実施例WBにおける、親水性色素含有組成物ジクロロメタン溶液の水へのICG移行量の評価結果である。
【図4】本実施形態に係る光イメージング用造影剤の製造方法の一例を説明するための図である。
【発明を実施するための形態】
【0013】
以下、本発明の実施形態について説明する。
【0014】
本発明の一の実施形態は、スルホン酸基を有する親水性色素、疎水性溶媒並びに、ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方を有する組成物に関する。
【0015】
本発明の一の実施形態では、ニコチン酸誘導体及び/またはチアミン誘導体を有することにより、スルホン酸基を有する親水性色素の疎水性溶媒への溶解度が高められる。この組成物を水と混和してエマルション法により粒子を形成した際、粒子内から水中へのスルホン酸基を有する色素の溶出量が抑制される。従って、本実施形態に係る組成物を用いれば、水中への、スルホン酸基を有する親水性色素の溶出の少ない粒子を作製することができ、蛍光法、及び光音響トモグラフィー等に有効に用いられる造影剤を調製できる。
本実施形態に係る組成物において、スルホン酸基を有する親水性色素の疎水性溶媒中の濃度は、0.01〜200mg/mL、好ましくは、0.1〜100mg/mLの範囲であることが好ましい。
また本実施形態に係る組成物は、光イメージング用造影剤製造用の組成物であることが好ましい。また、光音響イメージング用造影剤製造用の組成物であることがさらに好ましい。
【0016】
なお、スルホン酸基を有する親水性色素にニコチン酸誘導体及び/またはチアミン誘導体を添加することにより、スルホン酸基を有する親水性色素の疎水性溶媒への溶解度が高められる理由は以下のとおりであると考えられる。すなわち、ニコチン酸誘導体及び/またはチアミン誘導体がスルホン酸基を有する親水性色素の親水基に会合し、スルホン酸基を有する親水性色素が疎水性溶媒に溶解しやすくなるためと考えられる。特には、ニコチン酸誘導体ではピリジン環を含むニコチン酸骨格、チアミン誘導体はピリミジン環、あるいは、アミノ基の寄与が考えられる。なお、本発明におけるピリジン環を含むニコチン酸骨格とは、具体的には、ニコチン酸アミドからNH2を除いた構造を意味する。
【0017】
(スルホン酸基を有する親水性色素)
本実施形態においてスルホン酸基を有する親水性色素は、生体内で利用するにあたり、色素は生体から排出されやすい親水性色素が安全であり望ましい。また、本実施形態に係る組成物においては、ニコチン酸誘導体及び/またはチアミン誘導体が、スルホン酸基に会合して効果を奏すると考えられるため、とりわけスルホン酸基を有する親水性色素が好ましい。また、親水性色素は、生体内における光の吸収、拡散の影響が少ない「生体の窓」と呼ばれる600ナノメートル以上1300ナノメートル以下の波長に吸収を持つものが好ましい。以下、スルホン酸基を有する親水性色素を、単に、親水性色素と呼ぶことがある。
【0018】
前記親水性色素としては、例えば、アジン系色素、アクリジン系色素、トリフェニルメタン系色素、キサンテン系色素、ポルフィリン系色素、シアニン系色素、フタロシアニン系色素、スチリル系色素、ピリリウム系色素、アゾ系色素、キノン系色素、テトラサイクリン系色素、フラボン系色素、ポリエン系色素、BODIPY(登録商標)系色素、インジゴイド系色素を挙げることが出来る。
【0019】
前記シアニン系色素としては、例えば、インドシアニングリーン(ICG)、Alexa Fluor(登録商標)系色素(インビトロジェン社製)、Cy(登録商標)系色素(GE ヘルスケア バイオサイエンス社製)、IR−783 、IR−806、IR−820(シグマ アルドリッチ ジャパン株式会社製)、IRDye 800CW、IRDye 800RS(登録商標)(LI−COR社製)、ADS780WS、ADS795WS、ADS830WS、ADS832WS(American Dye Source社製)を挙げることが出来る。
【0020】
なお、本実施形態において、ICG(インドシアニングリーン)は下記の化学式1で示される構造、ただし、構造中、対イオンはNa+でなくともよく、例えばH+あるいはK+等であり得る。
【化1】

なお、上記のIR−820は下記の化学式2で示される。
【化2】

【0021】
前記インジゴイド系色素としては、例えば、インジゴカルミンを挙げることが出来る。
これらの親水性色素は、単独で使用してもよく、任意に混合して使用してもよい。
また、本実施形態において、パテントブルーなどの親水性色素を用いることもできる。
【0022】
(ニコチン酸誘導体)
本実施形態におけるニコチン酸誘導体は、ニコチン酸骨格を有していれば特に限定されないが、下記の一般式(I)で表されることが好ましい。
【化3】

式(I)において、Aは下記の式(a1)、式(a2)、式(a3)のいずれかである。式(a1)、式(a2)、式(a3)中の*は結合手を表し、*が式(I)のZと結合する。
【化4】

式(I)において、Zは下記の式(z1)、式(z2)、式(z3)のいずれかである。式(z1)、式(z2)、式(z3)中の*は結合手を表し、*が式(I)のAと結合する。式(z2)において、R1は水素原子、置換または無置換の炭素数1乃至10のアルキル基、ベンジル基のいずれかである。前記置換基はハロゲン原子、炭素数1乃至5のアルキル基、ヒドロキシル基、アミノ基のいずれかである。
【化5】

【化6】

【化7】

【0023】
本実施形態に係るニコチン酸誘導体が上記の式(I)で表される場合、スルホン酸基を有する親水性色素のスルホン酸基の負電荷と、ピリジン環の窒素原子と溶媒などに存在するプロトンとで形成されるNH+の正電荷が電荷をキャンセルすることで、該親水性色素が、疎水性溶媒に対して溶解しやすくなっていると考えられる。したがって、式(a1)、式(a2)、式(a3)のように、オルト、メタ、パラのいずれの位置に官能基が存在しても、式(I)で表されるニコチン酸誘導体とスルホン酸基を有する親水性色素の、疎水性溶媒に対する溶解性は、該親水性色素のみに比べて高いと考えられる。
【0024】
本実施形態におけるニコチン酸誘導体としては、ニコチン酸アミド、ニコチン酸ベンジルエステル、ニコチン酸、ニコチン酸メチル、ニコチン酸エチル、イソニコチン酸エチル、ニコチン酸トコフェロール等を挙げられる。これらのうち、ニコチン酸アミドまたはニコチン酸ベンジルエステルのうち少なくともいずれか一方であることが好ましい。
ニコチン酸誘導体は、単独で使用してもよく、任意に混合して使用してもよい。
【0025】
(チアミン誘導体)
本実施形態におけるチアミン誘導体は、特に限定されないが、下記の一般式(II)で表されることが好ましい。
【化8】

式(II)において、Bは下記の式(b)である。式(b)中の*1は結合手を表し、*1が式(II)のXと結合する。式(b)中の*2は結合手を表し、*2が式(II)のYと結合する。
【化9】

式(II)において、Xは下記の式(x1)、式(x2)、式(x3)のいずれかである。式(x1)、式(x2)、式(x3)中の*は結合手を表し、*が式(II)のBと結合する。式(x1)においてnは1乃至10のいずれかの整数である。式(x1)はハロゲン原子、炭素数1乃至5のアルキル基、ヒドロキシル基、アミノ基のいずれかで置換されていてもよい。式(x4)において、R2は、置換または無置換の炭素数1乃至10のアルキル基、置換または無置換のベンゼンのいずれかである。
【化10】

【化11】

【化12】

【化13】

式(II)において、Yは下記の式(y1)、式(y2)のいずれかである。式(y1)、式(y2)中の*は結合手を表し、*が式(II)のBと結合する。式(y2)において、R3は、置換または無置換の炭素数1乃至10のアルキル基、置換または無置換のベンゼンのいずれかである。
【化14】

【化15】

【0026】
チアミン誘導体としては、チアミンジスルフィド、プロスルチアミン、フルスルチアミン、ビスベンチアミン、スルブチアミン等が挙げられる。これらの中で、フルスルチアミン、プロスルチアミン、チアミンジスルフィドのうち少なくともいずれか一種であることが好ましい。
チアミン誘導体は、単独で使用してもよく、任意に混合して使用してもよい。
【0027】
また、ニコチン酸誘導体とチアミン誘導体を任意に混合して使用してもよい。
【0028】
(疎水性溶媒)
本実施形態に係る組成物は疎水性溶媒に対する溶解度の高いことを特徴とする。本実施形態において、疎水性溶媒は水に自由混合しない溶媒である。一方、水に自由混合する溶媒が親水性溶媒である。ここでいう自由混合とは、2つ以上の溶媒を混合したときに相分離などすることなく、均一に混じり合うことを意味する。
本実施形態における疎水性溶媒としては、ヘキサン、シクロへキサン、ヘプタン等の炭化水素類、ジメチルエーテル、ジエチルエーテル等のエーテル類、ジクロロメタン、クロロホルム、四塩化炭素、ジクロロエタン、トリクロロエタン等のハロゲン化炭化水素類、ベンゼン、トルエン等の芳香族炭化水素、酢酸エチル、酢酸ブチル等のエステル類が挙げられる。これらの中で、クロロホルム、ジクロロメタンのうち少なくともいずれか一方であることが好ましい。
疎水性溶媒は、単独で使用してもよく、任意に混合して使用してもよい。
【0029】
(組成物の作製方法)
本実施形態に係る組成物は、親水性色素と、ニコチン酸誘導体及び/またはチアミン誘導体を混合して得られるが、混合には公知の方法を利用することが出来、特に限定されない。
【0030】
本実施形態に係る組成物におけるニコチン酸誘導体及び/またはチアミン誘導体の量は、親水性色素に対して、0.1〜100.0倍モル、好ましくは、1.0倍〜20.0倍モルの範囲であることが好ましい。
【0031】
親水性色素と、ニコチン酸誘導体及び/またはチアミン誘導体との混合の際は、必要に応じ、溶媒を使用することが出来る。この際、溶媒として、ヘキサン、シクロへキサン、ヘプタン等の炭化水素類、アセトン、メチルエチルケトン等のケトン類、ジメチルエーテル、ジエチルエーテル、テトラヒドロフラン等のエーテル類、ジクロロメタン、クロロホルム、四塩化炭素、ジクロロエタン、トリクロロエタン等のハロゲン化炭化水素類、ベンゼン、トルエン等の芳香族炭化水素、エタノール、メタノール、イソプロパノール等のアルコール類、N,N−ジメチルホルムアミド、ジメチルスルホキシド等の非プロトン性極性溶媒類、酢酸エチル、酢酸ブチル等のエステル類、ピリジン誘導体、リン酸バッファー等の緩衝液、水、等を用いることができる。溶媒は、親水性色素並びに前記ニコチン酸誘導体及び/またはチアミン誘導体が溶解するものが好ましい。溶媒の使用量は、前記親水性色素の使用量、前記ニコチン酸誘導体及び/またはチアミン誘導体の使用量、混合条件等に応じて適宜定め得る。
【0032】
混合温度は、特に限定されないが、通常は−30℃から、溶媒を用いる場合は、使用する溶媒の沸点までの範囲の温度である。ただし、親水性色素、前記ニコチン酸誘導体及び/またはチアミン誘導体、並びに溶媒に合わせ、適宜最適な温度で混合を行うことが望ましい。混合時間は一概には言えないが、通常、1〜48時間の範囲であることが好ましい。
【0033】
混合溶液の溶媒は必要に応じて、常法である蒸留あるいはカラムクロマトグラフィー法を用いて取り除くことができるし、また、組成物が溶媒を含んでいてもよい。
【0034】
混合の際は、親水性色素を疎水性溶媒に分散させた後、ニコチン酸誘導体及び/またはチアミン誘導体を添加してもよいし、ニコチン酸誘導体及び/または、チアミン誘導体を疎水性溶媒に分散、または溶解させた後、親水性色素を添加してもよい。
【0035】
また、本実施形態に係る組成物は、必要に応じ、溶媒を含有、溶媒に分散、または、溶解させた状態であってもよい。
【0036】
<粒子化>
本実施形態に係る組成物は、水と混和した際に水への親水性色素の溶出量が少ない。従って、水に対してO/W型の液・液分散状態を形成する工程と、その後に有機溶剤相を固定する工程とによりICGを含有する粒子を形成する場合、親水性色素の利用率を高くすることができる。そのような有機溶剤相の固定工程としては、従来公知のものを用いることができる。一例を示すならば、本実施形態に係る組成物に対してこれに可溶な重合性モノマーあるいはプレポリマー、重合架橋剤等を添加し、得られた産物を水に液・液分散させた状態とした後、前記の重合性材料を重合反応することにより、有機溶剤相を固定し、粒子化することができる。ラジカル重合反応を進めるためには、低温用の熱重合開始剤や、酸化還元型ラジカル発生剤を好適に用いることができる。また別の例を示すならば、前記組成物にジカルボン酸塩化物を加えておき、これをジアミンの水溶液に液・液分散することにより、界面にてジカルボン酸とジアミンとからなる重縮合高分子膜を形成させて有機溶剤相を包含固定することができる。また、粒子化に際して界面活性剤を用いてもよい。このようにしてできた粒子は、蛍光法、及び光音響トモグラフィー等に有効に用いられる造影剤として用いることができる。
【0037】
<光イメージング用造影剤の製造方法>
本実施形態に係る光イメージング用造影剤の製造方法は、スルホン酸基を有する親水性色素と、疎水性溶媒と、ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方と、重合性モノマーあるいはプレポリマーとを有する組成物を用意する工程と、前記組成物と水を混合する混合工程と、前記混合工程の後に、前記重合性モノマーあるいは前記プレポリマーを重合する工程と、を有することを特徴とする。
本実施形態に係る光イメージング用造影剤の製造方法の一例について図3を用いて説明する。
まず、スルホン酸基を有する親水性色素101と、疎水性溶媒102と、ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方103と、重合性モノマーあるいはプレポリマー104とを有する組成物105を用意する。次に組成物105と、水106とを混合する。混合して得られた液体に超音波などを照射することにより、エマルションを得る。このとき得られたエマルションの分散質107は、上記の組成物105を有する。エマルションの分散質のうち、重合性モノマーあるいはプレポリマーを重合することで、光イメージング用造影剤108を得ることができる。
なお、重合性モノマーあるいはプレポリマーを重合する前に、エマルションの分散質から、疎水性溶媒を除去することが好ましい。疎水性溶媒を除去する方法としては、減圧する方法などが挙げられる。
【0038】
<光イメージング用造影剤>
本実施形態おける光イメージング用造影剤について説明する。本実施形態において光イメージングとは、光を照射することで、イメージング(画像化)することを意味する。すなわち、本実施形態に係る光イメージング用造影剤のスルホン酸基を有する親水性色素に光が照射されることで、音響波や蛍光などを発する。発せられた音響波を検出することで光音響イメージングをすることができ、発せられた蛍光を検出することで蛍光イメージングをすることができる。なお、光音響イメージングは、光音響トモグラフィー(断層撮影法)を含む概念である。
本実施形態に係る造影剤は、さらに、例えば生理食塩水、注射用蒸留水、リン酸緩衝生理食塩水(Phosphate buffered saline、以下PBSと略すことがある)などの分散媒を有していてもよい。また本実施形態に係る光イメージング用造影剤は、必要に応じて薬理上許容できる添加物を有していても良い。
本実施形態に係る光イメージング用造影剤は、上記の分散媒に予め分散させておいてもよいし、キットにしておき、生体内に投与する前に分散媒に分散させて使用してもよい。このように、本実施形態に係る光イメージング用造影剤は、光音響イメージング用造影剤や、蛍光イメージング用造影剤として利用することができる。
本実施形態に係る光イメージング用造影剤は、EPR(Enhanced Permeability and Retention)効果を利用することで、生体内に投与したときに、生体内の正常部位に比べて腫瘍部位により多く集積させることができる。その結果、複合体を生体内に投与した後、生体に光を照射して、生体からの音響波や蛍光を検出するときに、腫瘍部位から発せられる音響波や蛍光を正常部位から発せられる音響波や蛍光よりも大きくすることができる。従って、本実施形態に係る複合体は腫瘍部位を特異的に検出する光イメージング用造影剤として用いることができる。
【0039】
(重合性モノマーあるいはプレポリマー)
本実施形態において、重合性モノマーあるいはプレポリマーは上記の、スルホン酸基を有する親水性色素と疎水性溶媒とニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方とを有する組成物に可溶なものであれば特に限定されない。ここで、プレポリマーとは、重合性モノマーの重合または縮合反応を適当な所で止めた中間生成物のことであり、ポリマーとなる前段階にある状態のものを指す。
重合性モノマーとして例えば、スチレン、メタクリル酸、メタクリル酸ブチル、メタクリル酸ブチル−メタクリル酸メチル共重合体、乳酸、グリコール酸などを挙げることができる。
【0040】
(重合開始剤)
上記の重合性モノマーあるいはプレポリマーを重合させる重合開始剤としては、
従来から知られるものを使用できる。その具体例としては、アゾ系開始剤、パーオキサイド系開始剤、レドックス系開始剤、原子移動ラジカル開始剤、ニトロキサイド系開始剤等が挙げられる。特に、種類が豊富でモノマーの種類に合わせて適切なものを選ぶことができ、入手しやすく、安価であるアゾ系開始剤やパーオキサイド系開始剤を用いることが好ましい。
【0041】
(界面活性剤)
界面活性剤としては、例えば、ポリオキシエチレンアルキルエーテル、アルキル硫酸塩、リン脂質、ポリオキシエチレンソルビタン系脂肪酸エステル、ポリビニルアルコール、ポリオキシエチレンポリオキシプロピレングリコールを挙げることが出来る。
前記ポリオキシエチレンソルビタン系脂肪酸エステルとしては、Tween20、Tween40、Tween60、Tween80を挙げることが出来る。
前記リン脂質としては、アミノ基、NHS基、マレイミド、メトキシ基のいずれかの官能基とPEG鎖を有するホスファチジル系リン脂質を挙げることができる。
ホスファチジル系リン脂質としては、3−(N−succinimidyloxyglutaryl) aminopropyl, polyethyleneglycol−carbamyl distearoylphosphatidyl−ethanolamine(DSPE−PEG−NHS)、N−(3−maleimide−1−oxopropyl) aminopropyl polyethyleneglycol−carbamyl distearoylphosphatidyl−ethanolamine(DSPE−PEG−MAL)、N−(aminopropyl polyethyleneglycol)−carbamyl distearoylphosphatidyl−ethanolamine(DSPE−PEG−NH2)、N−(Carbonyl−methoxypolyethyleneglycol 2000)−1,2−distearoyl− sn−glycero−3−phosphoethanolamine, sodium salt(SUNBRIGHT DSPE−020CN)、N−(Carbonyl−methoxypolyethyleneglycol 5000)−1,2−distearoyl− sn−glycero−3−phosphoethanolamine, sodium salt(SUNBRIGHT DSPE−050CN)を挙げることができる。
ポリオキシエチレンポリオキシプロピレングリコールとしては、プルロニック(登録商標)F68、プルロニック(登録商標)F127を挙げることが出来る。
これらの界面活性剤は、単独で使用してもよく、任意に混合して使用してもよい。
【実施例】
【0042】
以下に、本発明の特徴をさらに明らかにするために実施例に沿って本発明を説明するが、本発明は、これらの実施例に限定されるものではなく、材料、組成条件等、同様な機能、効果を有する組成物が得られる範囲で自由に変えることが出来る。
【0043】
(実施例A―1)
ICG((財)日本公定書協会製)11mgをメタノール4mLに溶解させた。このICGに対して、20倍(モル比)のニコチン酸アミド34.7mgをメタノール4mLに溶解させた。この両メタノール溶液を混合し、15分攪拌した後、エバポレーターを用いて、メタノールを留去した。これにクロロホルム4mLを加えて攪拌した。さらに、超音波分散装置を用いて30秒間超音波照射を行った。孔径0.45マイクロメートルのフィルターを用いてろ過を行い、溶解した成分を回収した。回収された試料をA−1という。
【0044】
(実施例A−2、比較例A−3)
A−2、A−3は、実施例A−1で、ニコチン酸アミドを用いた代りに、ニコチン酸ベンジルエステル、ピリジンを用いた以外は、A−1と同様にして得られた。
【0045】
(比較例A−0)
比較対照であるA−0は、実施例A−1で、ニコチン酸アミドを用いない以外は、実施例A−1と同様にして得られた。
【0046】
(比較例A−4)
比較対照であるA−4は、ニコチン酸アミドを用いる代りに、非特許文献2で用いられている、テトラブチルアンモニウムヨージドを用い、それ以外は、A−1と同様に得られた。
【0047】
(実施例B−1、B−2)
B−1、B−2は、実施例A−1、A−2で、クロロホルムを用いる代りに、ジクロロメタンを用いた以外は、実施例A−1、A−2と同様に得られた。
【0048】
(比較例B−0)
比較対照であるB−0は、実施例B−1で、ニコチン酸アミドを用いない以外は、実施例B−1と同様に得られた。
【0049】
(比較例B−5)
比較対照であるB−5は、比較例B−0で、ジクロロメタンを用いる変わりに、ジクロロメタン:メタノール=3:1の混合溶液を用いた以外は、比較例B−0と同様に得られた。
【0050】
(比較例B−6)
比較対照であるB−6は、比較例B−0で、ジクロロメタンを用いる変わりに、ジクロロメタン:メタノール=1:1の混合溶液を用いた以外は、比較例B−0と同様に得られた。
【0051】
(比較例B−7)
比較対照であるB−7は、比較例B−0で、ジクロロメタンを用いる変わりに、ジクロロメタン:メタノール=1:3の混合溶液を用いた以外は、比較例B−0と同様に得られた。
【0052】
(実施例C−1、C−2、C−3)
C−1、C−2、C−3は、実施例A−1で、ニコチン酸アミドを用いた代りに、フルスルチアミン、プロスルチアミン、チアミンジスルフィドを用いた以外は、A−1と同様にして得られた。
【0053】
(溶解性評価)
上記実施例及び比較例で回収したA−0からA−4溶液を1000倍希釈して、常法に従い、UV−VIS−NIR測定を行った。550nmから950nmまでの吸光度を積算し、A−0で得られた値を1として規格化し、比較したものが図1である。
【0054】
色素と溶媒からなる対照組成物(A−0)と比較して、ニコチン酸アミドを用いた場合(A−1)は3.2倍、ニコチン酸ベンジルエステルを用いた場合(A−2)は2.1倍と、非常に良好な溶解性を示した。
【0055】
また、非特許文献2で用いられているテトラブチルアンモニウム塩を用いた場合(A−4)と比較しても、ニコチン酸アミドを用いた場合(A−1)は3.2倍、ニコチン酸ベンジルエステルを用いた場合(A−2)は2.1倍と、非常に良好な溶解性を示した。
【0056】
また、ピリジンを用いた場合(A−3)は、有効性が見られなかった。
【0057】
上記実施例及び比較例で回収したB−0からB−7溶液を1000倍希釈して、常法に従い、UV−VIS−NIR測定を行った。550nmから950nmまでの吸光度を積算し、比較例B−0の値を1として規格化し、比較したものが図2である。
【0058】
色素と溶媒からなる対照組成物(B−0)と比較して、ニコチン酸アミドを用いた場合(B−1)は10.4倍、ニコチン酸ベンジルエステルを用いた場合(B−2)は6.2倍と、非常に良好な溶解性を示した。
【0059】
また、B−0と比較して、メタノールを用いた場合(B−5、B−6,B−7)は6.3倍〜9.1倍とメタノールの添加量に応じて、非常に良好な溶解性を示した。
【0060】
上記実施例及び比較例で回収したC−1からC−3、A−0溶液を1000倍希釈して、常法に従い、UV−VIS−NIR測定を行った。550nmから950nmまでの吸光度を積算し、A−0で得られた値を1として規格化し比較した。
【0061】
色素と溶媒からなる対照組成物(A−0)と比較して、フルスルチアミンを用いた場合(C−1)は1.4倍、プロスルチアミンを用いた場合(C−2)は1.6倍と、チアミンジスルフィドを用いた場合(C−3)は1.9倍と、非常に良好な溶解性を示した。
【0062】
(実施例WB 疎水性溶媒から水への移行性評価)
上記実施例及び比較例で作製したB−0、B−1、B−2、B−5、B−6、B−7溶液0.5mLに、超純水1.5mL加えて、3秒間振盪した。5分間静置した後、水層を回収し、各々のサンプルを、WB−0、WB−1、WB−2、WB−5、WB−6、WB−7とした。
【0063】
常法に従い、UV−VIS−NIR測定を行った。550nmから950nmまでの吸光度を積算し、組成物WB−0、WB−1、WB−2、WB−5、WB−6、WB−7のICGの溶解量で規格化し、ICG同一量における水への移行量を算出した。サンプルB−0の移行量を1として規格化し、比較したものが図3である。
【0064】
メタノールを用いた場合(WB−5、WB−6、WB−7)は、疎水性溶媒から水への移行量が、WB−0と比較して、1.0倍〜2.9倍と大きな移行性を示した。
【0065】
一方、ニコチン酸アミド(WB−1)、ニコチン酸ベンジルエステルを用いた場合(WB−2)は、共に、疎水性溶媒から水への移行量は、WB−0と比較して、0.3倍、0.2倍と小さな値を示した。
【0066】
なお、実施例A、B、WBで用いた各試料の概略を表1に示す。
【0067】
【表1】

【符号の説明】
【0068】
101 スルホン酸基を有する親水性色素
102 疎水性溶媒
103 ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方
104 重合性モノマーあるいはプレポリマー
105 組成物
106 水
107 エマルションの分散質
108 光イメージング用造影剤
【特許請求の範囲】
【請求項1】
スルホン酸基を有する親水性色素と疎水性溶媒とを有する組成物において、前記組成物がニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方を有することを特徴とする組成物。
【請求項2】
前記スルホン酸基を有する親水性色素が、インドシアニングリーンであることを特徴とする請求項1に記載の組成物。
【請求項3】
前記ニコチン酸誘導体が一般式(I)で表されることを特徴とする請求項1または2に記載の組成物。
【化1】

式(I)において、Aは下記の式(a1)、式(a2)、式(a3)のいずれかである。式(a1)、式(a2)、式(a3)中の*は結合手を表し、*が式(I)のZと結合する。
【化2】

式(I)において、Zは下記の式(z1)、式(z2)、式(z3)のいずれかである。式(z1)、式(z2)、式(z3)中の*は結合手を表し、*が式(I)のAと結合する。式(z2)において、R1は水素原子、置換または無置換の炭素数1乃至10のアルキル基、ベンジル基のいずれかである。前記置換基はハロゲン原子、炭素数1乃至5のアルキル基、ヒドロキシル基、アミノ基のいずれかである。
【化3】

【化4】

【化5】

【請求項4】
前記チアミン誘導体が一般式(II)で表されることを特徴とする請求項1または2に記載の組成物。
【化6】

式(II)において、Bは下記の式(b)である。式(b)中の*1は結合手を表し、*1が式(II)のXと結合する。式(b)中の*2は結合手を表し、*2が式(II)のYと結合する。
【化7】

式(II)において、Xは下記の式(x1)、式(x2)、式(x3)のいずれかである。式(x1)、式(x2)、式(x3)中の*は結合手を表し、*が式(II)のBと結合する。式(x1)においてnは1乃至10のいずれかの整数である。式(x1)はハロゲン原子、炭素数1乃至5のアルキル基、ヒドロキシル基、アミノ基のいずれかで置換されていてもよい。式(x4)において、R2は、置換または無置換の炭素数1乃至10のアルキル基、置換または無置換のベンゼンのいずれかである。
【化8】

【化9】

【化10】

【化11】

式(II)において、Yは下記の式(y1)、式(y2)のいずれかである。式(y1)、式(y2)中の*は結合手を表し、*が式(II)のBと結合する。式(y2)において、R3は、置換または無置換の炭素数1乃至10のアルキル基、置換または無置換のベンゼンのいずれかである。
【化12】

【化13】

【請求項5】
前記ニコチン酸誘導体が、ニコチン酸アミドまたはニコチン酸ベンジルエステルのうち少なくともいずれか一方であることを特徴とする請求項1乃至3のいずれか1項に記載の組成物。
【請求項6】
前記チアミン誘導体が、フルスルチアミン、プロスルチアミン、チアミンジスルフィドのうち少なくともいずれか一種であることを特徴とする請求項1または2または4のいずれか1項に記載の組成物。
【請求項7】
前記疎水性溶媒がクロロホルム、ジクロロメタンのうち少なくともいずれか一方であることを特徴とする請求項1乃至6のいずれか1項に記載の組成物。
【請求項8】
スルホン酸基を有する親水性色素と、疎水性溶媒と、ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方と、重合性モノマーあるいはプレポリマーとを有する組成物を用意する工程と、
前記組成物と水を混合する混合工程と、
前記混合工程の後に、前記重合性モノマーあるいは前記プレポリマーを重合する工程と、
を有することを特徴とする光イメージング用造影剤の製造方法。
【請求項1】
スルホン酸基を有する親水性色素と疎水性溶媒とを有する組成物において、前記組成物がニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方を有することを特徴とする組成物。
【請求項2】
前記スルホン酸基を有する親水性色素が、インドシアニングリーンであることを特徴とする請求項1に記載の組成物。
【請求項3】
前記ニコチン酸誘導体が一般式(I)で表されることを特徴とする請求項1または2に記載の組成物。
【化1】

式(I)において、Aは下記の式(a1)、式(a2)、式(a3)のいずれかである。式(a1)、式(a2)、式(a3)中の*は結合手を表し、*が式(I)のZと結合する。
【化2】

式(I)において、Zは下記の式(z1)、式(z2)、式(z3)のいずれかである。式(z1)、式(z2)、式(z3)中の*は結合手を表し、*が式(I)のAと結合する。式(z2)において、R1は水素原子、置換または無置換の炭素数1乃至10のアルキル基、ベンジル基のいずれかである。前記置換基はハロゲン原子、炭素数1乃至5のアルキル基、ヒドロキシル基、アミノ基のいずれかである。
【化3】

【化4】

【化5】

【請求項4】
前記チアミン誘導体が一般式(II)で表されることを特徴とする請求項1または2に記載の組成物。
【化6】

式(II)において、Bは下記の式(b)である。式(b)中の*1は結合手を表し、*1が式(II)のXと結合する。式(b)中の*2は結合手を表し、*2が式(II)のYと結合する。
【化7】

式(II)において、Xは下記の式(x1)、式(x2)、式(x3)のいずれかである。式(x1)、式(x2)、式(x3)中の*は結合手を表し、*が式(II)のBと結合する。式(x1)においてnは1乃至10のいずれかの整数である。式(x1)はハロゲン原子、炭素数1乃至5のアルキル基、ヒドロキシル基、アミノ基のいずれかで置換されていてもよい。式(x4)において、R2は、置換または無置換の炭素数1乃至10のアルキル基、置換または無置換のベンゼンのいずれかである。
【化8】

【化9】

【化10】

【化11】

式(II)において、Yは下記の式(y1)、式(y2)のいずれかである。式(y1)、式(y2)中の*は結合手を表し、*が式(II)のBと結合する。式(y2)において、R3は、置換または無置換の炭素数1乃至10のアルキル基、置換または無置換のベンゼンのいずれかである。
【化12】

【化13】

【請求項5】
前記ニコチン酸誘導体が、ニコチン酸アミドまたはニコチン酸ベンジルエステルのうち少なくともいずれか一方であることを特徴とする請求項1乃至3のいずれか1項に記載の組成物。
【請求項6】
前記チアミン誘導体が、フルスルチアミン、プロスルチアミン、チアミンジスルフィドのうち少なくともいずれか一種であることを特徴とする請求項1または2または4のいずれか1項に記載の組成物。
【請求項7】
前記疎水性溶媒がクロロホルム、ジクロロメタンのうち少なくともいずれか一方であることを特徴とする請求項1乃至6のいずれか1項に記載の組成物。
【請求項8】
スルホン酸基を有する親水性色素と、疎水性溶媒と、ニコチン酸誘導体、チアミン誘導体のうち少なくともいずれか一方と、重合性モノマーあるいはプレポリマーとを有する組成物を用意する工程と、
前記組成物と水を混合する混合工程と、
前記混合工程の後に、前記重合性モノマーあるいは前記プレポリマーを重合する工程と、
を有することを特徴とする光イメージング用造影剤の製造方法。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2012−67084(P2012−67084A)
【公開日】平成24年4月5日(2012.4.5)
【国際特許分類】
【出願番号】特願2011−177890(P2011−177890)
【出願日】平成23年8月16日(2011.8.16)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成18年度、文部科学省、「先端融合領域イノベーション創出拠点の形成(高次生体イメージング先端テクノハブ)」に係わる委託研究、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(000001007)キヤノン株式会社 (59,756)
【Fターム(参考)】
【公開日】平成24年4月5日(2012.4.5)
【国際特許分類】
【出願日】平成23年8月16日(2011.8.16)
【国等の委託研究の成果に係る記載事項】(出願人による申告)平成18年度、文部科学省、「先端融合領域イノベーション創出拠点の形成(高次生体イメージング先端テクノハブ)」に係わる委託研究、産業技術力強化法第19条の適用を受ける特許出願
【出願人】(000001007)キヤノン株式会社 (59,756)
【Fターム(参考)】
[ Back to top ]

