経口医薬製剤
薬理活性剤の投与に好適な耐乱用性経口製剤を提供する。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
薬理活性剤と、
・高粘度液体担体材料(HVLCM)、
・網状構造形成剤、
・レオロジー調整剤、
・親水性剤、及び
・溶媒、
を含む制御放出性担体系と、を含む経口医薬製剤。
【請求項2】
前記薬理活性剤が、オピオイド、中枢神経系(CNS)抑制剤、又はCNS刺激剤である、請求項1に記載の製剤。
【請求項3】
前記薬理活性剤が、遊離塩基形又はその製薬上許容される塩形のいずれかの、オキシコドン、オキシモルホン、ヒドロコドン、ヒドロモルフォンから選択される、請求項2に記載の製剤。
【請求項4】
前記薬理活性剤が、アンフェタミン、メチルフェニデート、及びそれらの製薬上許容される塩から選択される、請求項2に記載の製剤。
【請求項5】
前記制御放出性担体系が、粘度増強剤をさらに含む、請求項1〜4のいずれかに記載の製剤。
【請求項6】
前記粘度増強剤が、二酸化ケイ素である、請求項5に記載の製剤。
【請求項7】
薬理活性剤と、
・HVLCM、
・網状構造形成剤、
・第1の粘度増強剤、
・親水性溶媒、及び
・疎水性溶媒、
を含む制御放出性担体系と、を含む経口医薬製剤。
【請求項8】
前記薬理活性剤が、オピオイド、中枢神経系(CNS)抑制剤、又はCNS刺激剤である、請求項7に記載の製剤。
【請求項9】
前記薬理活性剤が、遊離塩基形又はその製薬上許容される塩形のいずれかの、オキシコドン、オキシモルホン、ヒドロコドン、ヒドロモルフォンから選択される、請求項8に記載の製剤。
【請求項10】
前記薬理活性剤が、アンフェタミン、メチルフェニデート、及びそれらの製薬上許容される塩から選択される、請求項10に記載の製剤。
【請求項11】
薬理活性剤と制御放出性担体系とを含む経口医薬製剤であって、
・該医薬製剤が耐乱用性であり、かつ
・該製剤が1日2回(BID)の投与に適している、
上記製剤。
【請求項12】
前記活性剤が、オキシコドン、オキシモルホン、ヒドロコドン、又はヒドロモルフォンである、請求項11に記載の製剤。
【請求項13】
前記オピオイドがオキシコドンである、請求項12に記載の製剤。
【請求項14】
前記活性剤が遊離塩基形で存在する、請求項11〜13のいずれかに記載の製剤。
【請求項15】
前記活性剤が塩形で存在する、請求項11〜13のいずれかに記載の製剤。
【請求項16】
前記制御放出性担体系が、さらに誤用又は乱用の低減された危険性を提供する、請求項11〜15のいずれかに記載の製剤。
【請求項17】
前記誤用又は乱用の低減された危険性が、前記製剤からの活性剤の低いin vitro溶媒抽出率により特徴付けられる、請求項16に記載の製剤。
【請求項18】
前記誤用又は乱用の低減された危険性が、被験者が前記製剤とアルコールとを同時摂取したときに前記製剤からの活性剤の吸収にいかなる有意な影響も及ぼさないことにより特徴付けられる、請求項16に記載の製剤。
【請求項19】
前記誤用又は乱用の低減された危険性が、被験者が前記製剤とアルコールとを同時摂取したときに前記製剤からの活性剤の吸収にいかなる有意な影響も及ぼさないことによりさらに特徴付けられる、請求項17に記載の製剤。
【請求項20】
前記製剤からの活性剤のin vivo吸収が、食物と共に製剤を投与したときに増強される、請求項11〜19のいずれかに記載の製剤。
【請求項21】
薬理活性剤と制御放出性担体系とを含む経口医薬製剤であって、
・該制御放出性担体系が、HVLCMと、網状構造形成剤と、レオロジー調整剤と、親水性剤と、を含み、かつ
・該製剤が耐乱用性である、
上記製剤。
【請求項22】
前記制御放出性担体系が、粘度増強剤をさらに含む、請求項21に記載の製剤。
【請求項23】
前記親水性剤が、第2の粘度増強剤としても機能する、請求項22に記載の製剤。
【請求項24】
前記親水性剤が、ヒドロキシエチルセルロース(HEC)である、請求項21〜23のいずれかに記載の製剤。
【請求項25】
前記HVLCMが、スクロースアセテートイソブチレート(SAIB)である、請求項21〜24のいずれかに記載の製剤。
【請求項26】
溶媒がさらに含まれる、請求項21〜25のいずれかに記載の製剤。
【請求項27】
前記溶媒が、トリアセチンである、請求項26に記載の製剤。
【請求項28】
前記粘度増強剤が、二酸化ケイ素である、請求項22に記載の製剤。
【請求項29】
前記網状構造形成剤が、セルロースアセテートブチレート(CAB)である、請求項21〜28のいずれかに記載の製剤。
【請求項30】
前記レオロジー調整剤が、イソプロピルミリステート(IPM)である、請求項21〜29のいずれかに記載の製剤。
【請求項31】
安定化剤がさらに含まれる、請求項21〜30のいずれかに記載の製剤。
【請求項32】
前記安定化剤が、ブチルヒドロキシルトルエン(BHT)である、請求項31に記載の製剤。
【請求項33】
前記薬理活性剤が、オピオイド、中枢神経系(CNS)抑制剤、又はCNS刺激剤である、請求項21〜32のいずれかに記載の製剤。
【請求項34】
前記薬理活性剤が、遊離塩基形又はその製薬上許容される塩形のいずれかの、オキシコドン、オキシモルホン、ヒドロコドン、ヒドロモルフォンから選択される、請求項33に記載の製剤。
【請求項35】
前記薬理活性剤が、アンフェタミン、メチルフェニデート、及びそれらの製薬上許容される塩から選択される、請求項33に記載の製剤。
【請求項1】
薬理活性剤と、
・高粘度液体担体材料(HVLCM)、
・網状構造形成剤、
・レオロジー調整剤、
・親水性剤、及び
・溶媒、
を含む制御放出性担体系と、を含む経口医薬製剤。
【請求項2】
前記薬理活性剤が、オピオイド、中枢神経系(CNS)抑制剤、又はCNS刺激剤である、請求項1に記載の製剤。
【請求項3】
前記薬理活性剤が、遊離塩基形又はその製薬上許容される塩形のいずれかの、オキシコドン、オキシモルホン、ヒドロコドン、ヒドロモルフォンから選択される、請求項2に記載の製剤。
【請求項4】
前記薬理活性剤が、アンフェタミン、メチルフェニデート、及びそれらの製薬上許容される塩から選択される、請求項2に記載の製剤。
【請求項5】
前記制御放出性担体系が、粘度増強剤をさらに含む、請求項1〜4のいずれかに記載の製剤。
【請求項6】
前記粘度増強剤が、二酸化ケイ素である、請求項5に記載の製剤。
【請求項7】
薬理活性剤と、
・HVLCM、
・網状構造形成剤、
・第1の粘度増強剤、
・親水性溶媒、及び
・疎水性溶媒、
を含む制御放出性担体系と、を含む経口医薬製剤。
【請求項8】
前記薬理活性剤が、オピオイド、中枢神経系(CNS)抑制剤、又はCNS刺激剤である、請求項7に記載の製剤。
【請求項9】
前記薬理活性剤が、遊離塩基形又はその製薬上許容される塩形のいずれかの、オキシコドン、オキシモルホン、ヒドロコドン、ヒドロモルフォンから選択される、請求項8に記載の製剤。
【請求項10】
前記薬理活性剤が、アンフェタミン、メチルフェニデート、及びそれらの製薬上許容される塩から選択される、請求項10に記載の製剤。
【請求項11】
薬理活性剤と制御放出性担体系とを含む経口医薬製剤であって、
・該医薬製剤が耐乱用性であり、かつ
・該製剤が1日2回(BID)の投与に適している、
上記製剤。
【請求項12】
前記活性剤が、オキシコドン、オキシモルホン、ヒドロコドン、又はヒドロモルフォンである、請求項11に記載の製剤。
【請求項13】
前記オピオイドがオキシコドンである、請求項12に記載の製剤。
【請求項14】
前記活性剤が遊離塩基形で存在する、請求項11〜13のいずれかに記載の製剤。
【請求項15】
前記活性剤が塩形で存在する、請求項11〜13のいずれかに記載の製剤。
【請求項16】
前記制御放出性担体系が、さらに誤用又は乱用の低減された危険性を提供する、請求項11〜15のいずれかに記載の製剤。
【請求項17】
前記誤用又は乱用の低減された危険性が、前記製剤からの活性剤の低いin vitro溶媒抽出率により特徴付けられる、請求項16に記載の製剤。
【請求項18】
前記誤用又は乱用の低減された危険性が、被験者が前記製剤とアルコールとを同時摂取したときに前記製剤からの活性剤の吸収にいかなる有意な影響も及ぼさないことにより特徴付けられる、請求項16に記載の製剤。
【請求項19】
前記誤用又は乱用の低減された危険性が、被験者が前記製剤とアルコールとを同時摂取したときに前記製剤からの活性剤の吸収にいかなる有意な影響も及ぼさないことによりさらに特徴付けられる、請求項17に記載の製剤。
【請求項20】
前記製剤からの活性剤のin vivo吸収が、食物と共に製剤を投与したときに増強される、請求項11〜19のいずれかに記載の製剤。
【請求項21】
薬理活性剤と制御放出性担体系とを含む経口医薬製剤であって、
・該制御放出性担体系が、HVLCMと、網状構造形成剤と、レオロジー調整剤と、親水性剤と、を含み、かつ
・該製剤が耐乱用性である、
上記製剤。
【請求項22】
前記制御放出性担体系が、粘度増強剤をさらに含む、請求項21に記載の製剤。
【請求項23】
前記親水性剤が、第2の粘度増強剤としても機能する、請求項22に記載の製剤。
【請求項24】
前記親水性剤が、ヒドロキシエチルセルロース(HEC)である、請求項21〜23のいずれかに記載の製剤。
【請求項25】
前記HVLCMが、スクロースアセテートイソブチレート(SAIB)である、請求項21〜24のいずれかに記載の製剤。
【請求項26】
溶媒がさらに含まれる、請求項21〜25のいずれかに記載の製剤。
【請求項27】
前記溶媒が、トリアセチンである、請求項26に記載の製剤。
【請求項28】
前記粘度増強剤が、二酸化ケイ素である、請求項22に記載の製剤。
【請求項29】
前記網状構造形成剤が、セルロースアセテートブチレート(CAB)である、請求項21〜28のいずれかに記載の製剤。
【請求項30】
前記レオロジー調整剤が、イソプロピルミリステート(IPM)である、請求項21〜29のいずれかに記載の製剤。
【請求項31】
安定化剤がさらに含まれる、請求項21〜30のいずれかに記載の製剤。
【請求項32】
前記安定化剤が、ブチルヒドロキシルトルエン(BHT)である、請求項31に記載の製剤。
【請求項33】
前記薬理活性剤が、オピオイド、中枢神経系(CNS)抑制剤、又はCNS刺激剤である、請求項21〜32のいずれかに記載の製剤。
【請求項34】
前記薬理活性剤が、遊離塩基形又はその製薬上許容される塩形のいずれかの、オキシコドン、オキシモルホン、ヒドロコドン、ヒドロモルフォンから選択される、請求項33に記載の製剤。
【請求項35】
前記薬理活性剤が、アンフェタミン、メチルフェニデート、及びそれらの製薬上許容される塩から選択される、請求項33に記載の製剤。
【図1A】


【図1B】


【図1C】


【図1D】


【図1E】


【図1F】


【図1G】


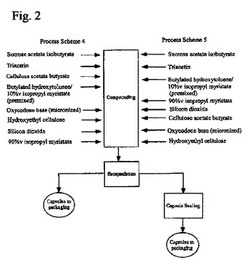
【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図6A】


【図6B】


【図6C】


【図7A】


【図7B】


【図7C】


【図8】


【図9A】


【図9B】


【図10A】


【図10B】


【図11】


【図12A】


【図12B】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】




【図1B】


【図1C】


【図1D】


【図1E】


【図1F】


【図1G】


【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図6A】


【図6B】


【図6C】


【図7A】


【図7B】


【図7C】


【図8】


【図9A】


【図9B】


【図10A】


【図10B】


【図11】


【図12A】


【図12B】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【公表番号】特表2011−506318(P2011−506318A)
【公表日】平成23年3月3日(2011.3.3)
【国際特許分類】
【出願番号】特願2010−536931(P2010−536931)
【出願日】平成20年12月5日(2008.12.5)
【国際出願番号】PCT/US2008/013381
【国際公開番号】WO2009/088414
【国際公開日】平成21年7月16日(2009.7.16)
【出願人】(508027589)デュレクト コーポレーション (14)
【Fターム(参考)】
【公表日】平成23年3月3日(2011.3.3)
【国際特許分類】
【出願日】平成20年12月5日(2008.12.5)
【国際出願番号】PCT/US2008/013381
【国際公開番号】WO2009/088414
【国際公開日】平成21年7月16日(2009.7.16)
【出願人】(508027589)デュレクト コーポレーション (14)
【Fターム(参考)】
[ Back to top ]

