経口吸収率を向上させるためのビスホスフォネートを含む薬剤学的組成物
生体内でイオン化し、水溶性が高くて生体脂質膜を通過できず、生物学的利用率が10%未満のビスホスフォネート系薬物から選ばれる1種以上の活性物質と、生体適合性水溶性キトサンから選ばれる1種以上を必須構成成分とする、ビスホスフォネート系薬物の経口吸収を改善させる薬剤学的組成物を提供する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、水で溶解可能な水溶性高分子キトサン及び/または低分子キトサン及び/またはキトサンモノマーを含有するビスホスフォネート系薬物の薬剤学的組成物に関し、極性が高いことから生体脂質膜を通過できず生物学的利用率が低い薬物の経口吸収率を向上させるための新規な薬剤学的組成物に関する。
【背景技術】
【0002】
現在開発中のビスホスフォネート系薬物などは、極性が極めて高くて生体脂質膜を透過できず、カルシウムなどの多価金属イオンと強い親和性を有して生体内でこれらと結合する際、不溶性複合体を形成することによって消化管で細胞膜を通じて吸収し難いと知られている(参考文献:Br.J.Cancer、71、Suppl.24、67、1995)。また、pH6〜8の小腸の内部でアニオン性を有するので、小腸における吸収も難しく、殆どの薬物が10%未満の吸収率を有し、特にアレンドロン酸ナトリウムの吸収率は1%未満であると報告されている(参考文献:Clin. Pharmacol. & Therapeutics、58(3)、288-209(1995))。
【0003】
従来から、高い極性のため胃腸(GI)生体脂質膜の吸収機作である自由拡散及び透過が行われなくて細胞間隙を通じた吸収も困難なことから、生体利用率が低いと知られたビスホスフォネート系薬物の吸収を増加させるための研究事例は一部報告されている。
【0004】
例えば、ビスホスフォネートを含む活性物質に脂肪酸を含む吸収促進剤を添加して経口吸収率を増加させる先行技術としては、アメリカ特許出願公開第2003/0091623号と国際公開第00/50012号公報があり、中鎖脂肪酸トリグリセリド(medium chain triglyceride)を吸収促進剤として用いた国際公開第99/18972号公報と双性イオン性(zwitterionic)リン脂質を用いた国際公開第01/76577号公報がある。これら先行技術は全て脂肪から由来する物質を使用して固形製剤を設計するため、多くの短所を抱えている。特に、脂肪酸と中鎖脂肪酸トリグリセリドは液状または半固形であり、活性物質より極めて多く使用すべきなので、実質的な製品化が難しく、双性リン脂質はそれ自体の低い安定性と腐敗の恐れのため、やはり製品化が困難である。
【0005】
アメリカ特許第6309663号には、親水性の表面活性剤と疎水性の表面活性剤を共に使用して吸収を増加させる方法が開示されている。この先行技術は、表面活性剤の極めて広範な範囲で、キトサン誘導体を包括的に要求するが、表面活性剤の存在それ自体が胃腸管に副作用効果の別な原因をもたらす。一方、本発明は表面活性剤を含まなくても胃腸障害改善に役に立つ。また、引例がキトサン本来の性質とは極めて異なるキトサン-EDTA及び/またはキトサン−EDTA−アンチパイン(antipain)複合体を使用したという点と、これらを酵素抑制剤として使用するという点において、本発明と明らかに区分される。
【0006】
自体開発した経口吸収促進剤を使用して経口吸収を増加させる方法が開示されている国際公開第02/070438号公報は、本発明で使用する水溶性キトサンとは相異なる吸収促進剤を使用している。この先行技術の合成された吸収促進剤は、生体適合性物質でなく、それ自体が有害な胃腸管副作用を持ち得ることから、当業界において通常の医薬品賦形剤と言えない。
【0007】
一方、国際公開第00/61111号公報は、吸収向上効果の立証なしに極めて広範な賦形剤の組成を、吸収改善組成物として請求している。ここで言及する賦形剤は、全ての界面活性剤;胆汁酸;脂肪酸及びそのけん化塩;中鎖脂肪酸グリセリド;オイル;エナミン(enamine);全てのキレート剤(chelating agent);フェノチアジン(phenothiazine);カルニチン又はペプチドの脂肪酸誘導体;アゾン、コンカナバリンA(concanavalin A)、ホスフェート及び誘導体、ジホスフェート及び誘導体;マイヤール反応(maillard reaction)の生成物;共重合体及び生分解性高分子を含む全高分子;キトサン及びキトサン誘導体;から選ばれる1種以上を使用すると開示されている。しかし、吸収改善の効果は、具体的な資料として提示された例がなく、ただ組成物だけが列挙されている。特に、本発明と関連するキトサンは、組成の例にも言及されていない。胃腸内環境が酸性であっても、実質的なヒトの胃腸内酸度はpH1から5まで広範なことから、キトサンが溶解されない可能性が高く、溶解されてもその速度が極めて遅くなる。ビスホスフォネートの主な吸収が経口服用後30分以内に発生することを考慮する際、一般的なキトサンの組成は溶解されないため、ビスホスフォネートの経口吸収にいずれの影響を及ぼさない。従って、本発明のキトサンが通常のキトサンではなく水でも迅速に可溶化するキトサンであるという点と、本発明の薬剤学的組成物が、水溶性キトサンを用いた即時放出の特徴を有するビスホスフォネートの薬剤学的組成物であるという点において明らかな違いがある。
【0008】
ヨーロッパ特許出願公開第1302201号は、経口吸収改善剤としてアミノアルキルメタクリレート共重合体に該当するEudragit Eと酸性物質を含有する組成物を開示している。この技術は、経口吸収改善のためにアクリレート誘導体であるEudragit Eを使用したが、本発明の水溶性キトサンはサッカライド構造であって相異なる。また、当業界で認知されているように、キトサンは生体適合性物質であり、胃腸管毒性を解消するのに役に立つ(参考文献:British Journal of Plastic Surgery、53、601-606(2000))という点において、胃腸管障害が酷いビスホスフォネート系薬物の薬剤学的組成物に最適である。
【0009】
一方、剤形の構造的特性を用いて活性物質の放出速度を物理的に制御することによって経口吸収率の向上を図った先行技術は次の通りである。
【0010】
アメリカ特許出願公開第2004/0176328号は、水溶性活性物質がその水溶性活性物質より低い融点を有する物質で封じ込められてカプセル化し、カプセル化した粒子が連続的な固相に担持される固形の剤形を開示している。アメリカ特許第6207197号は、活性物質を封じ込めた核粒、水不溶性重合体からなる制御放出層及び粘膜付着性陽イオン重合体からなる外郭層を、包含する胃滞留型微粒球を記載している。これら技術は、薬物とキトサンの相互作用による経口吸収率の上昇とは関係なく、活性物質をカプセル形態または微粒球形態に封じ込めた製剤を作って、これより薬物の放出速度を調節することによる生体利用率アップの目的があるという点において、本発明と異なる。また、これらは、持続的な放出効果を示す組成物である一方、本発明は、ビスホスフォネートの経口吸収率を実質的に向上させるために即時放出の薬剤学的組成物を提供するという点においても異なる。ビスホスフォネート系薬物の長時間胃腸滞留または持続的な放出は経口吸収率の変化を誘導することができるとしても、ビスホスフォネートと腸管粘膜の接触時間を延ばして食道及び胃腸での毒性が増加する短所を同時に有するので、適切な制御放出と言えない。
【発明の開示】
【発明が解決しようとする課題】
【0011】
本発明では、高い極性によって胃腸管の生体脂質膜の通過が困難なことから生体利用率が低く、通常高い単位量で投与されるビスホスフォネート系薬物であるアレンドロン酸ナトリウムに対して、水で溶解可能な水溶性高分子キトサン及び/または低分子キトサン及び/またはキトサンモノマーを適正比率で配合することによって、極性活性物質の経口吸収率を高めることを目的とする。
【0012】
また、経口吸収率を高めることによって相対的に高い単位で投与されていた活性物質の投与単位を下げることによって薬物が有する副作用を最小化させ、同時に、生体膜治療効果を有する水溶性キトサンを配合することによって胃腸毒性を最小化する、ビスホスフォネート系薬物の薬剤学的組成物を提供するところに、その目的がある。
【0013】
そして、これら組成物を使用して製剤化することによって、一般的に溶解速度が遅い重合体と結合して製剤化する場合問題となる遅い溶出を改善した剤形設計を、その目的とする。
【課題を解決するための手段】
【0014】
本発明は、生体内でイオン化し水溶性が高くて生体脂質膜を通過できず、生物学的利用率が10%未満のビスホスフォネート系薬物から選ばれる1種以上の活性物質と、生体適合性水溶性キトサンから選ばれる1種以上を必須構成成分にして、早い速度で崩壊させ最小60分以内に80%以上の活性物質を胃腸管系に放出することによって、ビスホスフォネート系薬物の経口吸収率を改善することを特徴とする、薬剤学的組成物を提供する。
【0015】
本発明の特徴は三つに大別される。第1に、極性活性物質(ビスホスフォネート系薬物)の陰イオン極性部位を水でも溶解可能な水溶性キトサンの陽イオン電荷部位で遮蔽することによって、相対的に薬物の陽イオン極性部位を露出させて細胞間隙を通じた吸収を容易にしたり、水溶性キトサン及び/または低分子キトサン及び/またはキトサンモノマーを使って薬物の極性を減少させ、薬物の疎水性を増加させることによって脂質膜を通じた自由拡散及び分配に有利な条件を誘導することによって、活性物質の生体脂質膜内部への搬送を容易にして、生物学的利用率を向上させている。第2に、活性物質の投与単位を減少するとともに、繊維芽細胞の増殖を刺激して傷治癒効果を有し、GI毒性を減少させることで知られている(参考文献:Biomaterials、20、2959-2966(2001) & Advanced Drug Delivery Review、52、105-115(2001))キトサン、特に水でも溶解可能な水溶性キトサンを使用することによって、既存ビスホスフォネート系薬物の製剤により示される食道及び胃腸関連毒性を減少させようとしている。本発明に適用される水溶性キトサンは水に対する溶解度が0.1%w/v以上であることが望ましく、さらに望ましくは水に対する溶解度が0.5%w/v以上のものである。
【0016】
最後に、水では溶解されず酸性条件下でだけ溶解される通常のキトサンで製剤化する場合、個体差によって溶解速度が遅れるか又は溶解自体が不完全なことから、薬物の一般的な吸収の60分以内、望ましくは30分以内に目的とする吸収効果を発揮できない短所がある。従って、通常のキトサンの代わりに、水で容易に溶解される水溶性キトサンを使うことによって、胃でも迅速に溶解される速崩性製剤を作って活性物質の迅速な溶出を誘導している。
【0017】
結局、本発明によって、経口吸収し難いビスホスフォネート系薬物に対してその経口吸収率を増加させることによって、薬物の少ない単位投与量でも骨吸収抑制作用を効率よく防止し、薬物から引き起こされる食道及び胃腸毒性を減らして、患者の適応性をよくすることができる、新たなビスホスフォネート系薬物の製剤の開発が可能になる。
【0018】
本発明の組成物は、ビスホスフォネート系薬物と生体適合性陽イオン性重合体である水溶性キトサン及び/または低分子キトサン及び/またはキトサンモノマーを必須とし、薬剤学的に許容される賦形剤をさらに含む。
【0019】
本発明のビスホスフォネート系薬物は、水溶性が高くて薬物の経口吸収が不可能な薬物であって、生物学的利用率30%未満、特に生物学的利用率10%未満の薬物を意味し、水に溶解する際、薬物の構造内に1個以上の陰イオン電荷及び/または陽イオン電荷を有する薬物である。そして、これらは水分配係数(Log P)が主に1.0以下であって、相対的にオイルに比べて水に対する親和力が高い特性を示す。このような活性物質としては、例えば、アレンドロネート(4−アミノ−1−ヒドロキシブチリデン−1、1−ビスホスホン酸)、シマドロネート(インカドロネート、1−(シクロヘプチルアミノ)メチリデン−1、1−ビスホスホン酸)、エチドロネート(1−ヒドロキシエチリデン−1、1−ビスホスホン酸)、チルドロネート(1−(4−クロロフェニルチオ)メチリデン−1、1−ビスホスホン酸)、ミノドロネート(1−ヒドロキシ−2−(イミダゾ[1、2−a]ピリジン−3−イル)エチリデン−1、1−ビスホスホン酸)、イバンドロネート(1−ヒドロキシ−3−(N−メチル−N−ペンチルアミノ)プロピリデン−1、1−ビスホスホン酸)、リセドロネート(1−ヒドロキシ−2−(3−ピリジル)エチリデン−1、1−ビスホスホン酸)、パミドロネート(3−アミノ−1−ヒドロキシプロピリデン−1、1−ビスホスホン酸)、ゾレドロネート(1−ヒドロキシ−3−(1−ピロリジニル)プロピリデン−1、1−ビスホスホン酸、1−ヒドロキシ−2−(1−イミダゾリル)エチリデン−1、1−ビスホスホン酸)、ネリドロネート(6−アミノ−1−ヒドロキシヘキシリデン−1、1−ビスホスホン酸)、オルパドロネート(ミルドロネート、N、N−ジメチル−3−アミノ−1−ヒドロキシプロピリデン−1、1−ビスホスホン酸)及びその可能な塩またはエステル誘導体及びその混合物がある。
【0020】
ビスホスフォネート系薬物は、骨組織からカルシウムの再吸収を強力に抑制して、破骨細胞の機能を低下させて、骨密度を緻密にできる、骨粗しょう症治療薬である。しかし、優れた薬効を有しているものの、生体内適用時色々の問題点を抱えている薬物として認識されている。経口吸収の面では、朝食の30分前に過量の水と共に服用してこそ薬物の吸収が起こり、その生体利用率も30%未満、特に10%未満である。最も代表的なビスホスフォネート系薬物であるアレンドロネートは生体利用率が0.7%未満と報告されている。特にカルシウムのような多価金属イオンと強く結合して、沈殿が発生し、食事や飲み物によっても薬物の生物学的利用率が半分以下に減少すると知られている。そして、用法では、錠剤を口腔内で溶かして服用する時は、深刻な口内炎または肝炎を引き起こす恐れがあり、正常に服用しても、長期服用時、患者の約36%で胸焼け(heartburn)または上腹部痛(epigastric pain)を起こしている。また食道疾患時には、重症な食道炎(severe esophagitis)または広範囲な食道炎(extensive esophagitis)を引き起こす場合があると使用説明書に記載されている。
【0021】
従って、ビスホスフォネート系薬物の最適な改良型薬剤(incrementally modified drugs(IMDs))は、生物学的利用率を向上させて、同じ効果を示す薬物の単位投与量を減らすことによって薬物自体が伴う副作用を最小化し、さらに胃腸管(GI)毒性を増加させないか、毒性を減少させうる生体適合性物質を含有する、薬剤学的組成物である。
【0022】
ビスホスフォネートは骨組織に分布された以後には、半減期が11.9年であって極めて長いので、胃腸管粘膜組織が再生される5日以上の間隔で投与されることが薬効を減少させず副作用を最小化する投与期間として認識されている。従って、アレンドロネートの場合、毎日10mgより、7日毎に70mgの経口投与単位容量が副作用を軽減できる方法である。しかしながら、これも生物学的利用率が1%に及ばないことを考慮すれば、生物学的利用率を増加させて、7日毎に70mgの単位を革新的に減少させることが、ビスホスフォネート系薬物の短所および問題点を改善する最も効率的な方法になり得る。
【0023】
生体適合性の物質でありビスホスフォネートの生物学的利用率を向上させることができる吸収担体としては、水溶性キトサンが適している。本発明の水溶性キトサンは、水で溶解可能な、高分子キトサン、分子量別混合キトサン、低分子キトサン、キトオリゴ糖、キトサンモノマー(グルコサミン)及びその混合物を包括する概念であり、キトサンと酸性物質が均質に配合された混合物を含む。本発明において使われる水溶性キトサンは、他の誘導体化過程や追加の酸性化過程を要らず、水でも極めて迅速に溶解される特性を有するが、キトサンのモノマーであるグルコサミンは水に対する溶解度が0.5w/v%以上であって極めて優れて、生体胃腸の酸度と関係なく一定した体内吸収率をアップすることができる特徴がある。
【0024】
本発明の水溶性キトサンはグルコサミンモノマーから成り、分子量によって水溶性高分子キトサンと低分子キトサン、キトサンモノマー(グルコサミン)とに大別される。水溶性高分子キトサンは、分子量10,000〜500,000の範囲が使用され、望ましくは100,000〜200,000の範囲が使用可能である。水溶性低分子キトサンは、キトオリゴ糖と同じ意味で混用される場合もあるが、分子量200〜10,000の範囲が使用され、望ましくは分子量500〜2,000の範囲が使用できる。そして、水溶性キトサンモノマーは、文字通りキトサンをモノマー単位まで分解して生成されるグルコサミン(キトサミン、2-アミノ-2-デオキシ-D-グルコース)を意味する。
【0025】
この水溶性キトサンは、キトサンが酸性物質と均質に配合された混合物であるか、キトサンモノマーであるグルコサミンが酸性物質とイオン的引力によって配列されたキトサンの酸性塩である。前記酸性物質として、塩酸、硫酸、硝酸などの無機酸または乳酸、酢酸、クエン酸、酒石酸、コハク酸などの有機酸から1種以上の酸性物質が使用でき、望ましくは塩酸が使用できるが、本発明はこれに限定されるものではない。前記において、キトサンが酸性物質と均質に配合された混合物とは、通常のキトサンが前記無機酸または有機酸と物理的に均質に混合された形態を意味する。前記でキトサンモノマーであるグルコサミンが酸性物質とイオン的引力によって配列されたキトサンの酸性塩とは、グルコサミンのアミン基が陽電荷を帯びて、無機酸または有機酸が陰電荷を帯びるので、陽電荷と陰電荷との間にイオン的に引力が働いてグルコサミンと酸性物質が規則的に配列された形態を意味する。この水溶性キトサンの具体的な製品としては韓国の(株)慈光のエチエフピーキトサン(HFP Chitosan)や(株)キトライフのFACOSなどがあるが、本発明はこれらに限定されるものではない。
【0026】
キトサン中のキトサンモノマーであるグルコサミンと無機酸または有機酸をモル比として1:0.1〜1:50、望ましくは1:0.5〜1:10で固相または液状に均質に混和した混合物、またはこれらを全て水に溶解してから再び乾燥して取得したキトサン粉末も本発明の水溶性キトサンの範疇に属する。また、通常のキトサンと無機酸または有機酸を全て水に溶解してから、これに有機溶媒を加えて析出させ、有機溶媒を除去したキトサン粉末も本発明の水溶性キトサンの範疇に属する。
【0027】
蟹、海老などの甲殻類及び昆虫類の外骨格や細胞壁の保護組織から得られるキチンという物質を脱アセチル化して得られる通常のキトサンも、グルコサミンを構成モノマーにしているが、本発明の水溶性キトサンと比較して、酸性物質を均質に持てず、酸性物質をモノマー構造内に有しない。したがって、pH3以下の酸性下でだけ溶解でき、水では全く溶解されず、酸性溶液でもその溶解速度が極めて遅く、本発明の効果である経口吸収率の向上を発揮できない。
【0028】
たとえ胃腸内環境が酸性であるとしても、実質的なヒトの胃腸内酸度はpH1〜5の広範なことから、通常のキトサンは溶解されない可能性が高く、溶解されてもその速度が極めて遅くなる。従って、通常のキトサンをもっては、生体内適用時に1時間以内の迅速な薬物吸収が適しているビスホスフォネート系薬物における、実質的な経口吸収率向上の効果が全く得られない。さらに溶解速度が遅い通常のキトサンは、かえって薬物の放出を阻害して、迅速な吸収が求められるビスホスフォネート系薬物の吸収を減少させる逆効果も発生する場合がある。
【0029】
全体として、本発明の薬剤学的組成物を製造するために、活性物質と水溶性キトサンを混合したり、薬剤学的に許容される賦形剤と共に混合することができる。活性物質に対して水溶性高分子キトサン及び/または低分子キトサン(キトオリゴ糖)及び/またはキトサンモノマーから選ばれる1種以上を、活性物質の重量を基準に、重量比として100:1〜1:100、望ましくは25:1〜1:25、さらに望ましくは10:1〜1:10で配合する。また、本発明の薬剤学的組成物は薬剤学的に認められる通常の方法として、混合(blending)及び練り混ぜ(kneading)、粉砕(grinding)、篩分け(sieving)、充填(filling)、圧縮(compressing)、凍結乾燥(lyophilization)、噴射乾燥(spray-drying)、流動乾燥(fluid-bed drying)、遠心分離造粒(centrifugal granulation)などを通じて製剤化できる。
【0030】
本発明の組成物は当業界で通常に使用されている薬剤学的に許容される賦形剤を、さらに含有することができる。薬剤学的に許容される賦形剤としては希釈剤(diluent)、結合剤(binder)、崩壊剤(disintegrant)、色素剤(coloring agent)、甘味剤(sweeting agent)、香料(Flavor)、保存剤(preservative)、潤滑剤(lubricant)などが使用可能であり、前述した機能を複合的に有する賦形剤を使用することもできる。希釈剤としては、ラクトース、デキストロース、微結晶セルロース、デンプンなどから選ばれた1種以上が使用可能であり、結合剤としては、ポリビニルピロリドン、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、ヒドロキシエチルセルロース、第二リン酸カルシウム、アルギン酸ナトリウムなどから選ばれた1種以上が、崩壊剤としては、クロスカメロースナトリウム、デンプングリコール酸ナトリウム、架橋化ポリビニルピロリドン、アルファ化デンプン、低置換度ヒドロキシプロピルセルロースなどから選ばれた1種以上が、色素剤としては、水溶性色素、タール色素などから選ばれる1種以上、甘味剤としては、デキストロース、ソルビトール、マンニトール、アスパルテーム、アセスルファム、クエン酸などから選ばれた1種以上、香料としては、オレンジ香粉末、ブドウ香粉末、イチゴ香粉末、ブルーベリー粉末などから選ばれた1種以上、保存剤としては、安息香酸、メチルパラベン、エチルパラベン、プロピルパラベンなどから選ばれた1種以上、潤滑剤としては、ステアリン酸マグネシウム、タルク、軽質無水珪酸、スクロース脂肪酸エステルなどから選ばれた1種以上が使用可能であるが、これらに限定されるものではない。このように形成されたビスホスフォネート系薬物と水溶性キトサンの組成物は、胃で迅速に崩壊され、1時間以内に、望ましくは30分以内に、製剤からビスホスフォネート系薬物を全て放出し、キトサンは迅速に溶解され、薬物の生体膜透過を促進するようになる。
【0031】
本発明の組成物は、水のない状態で、前述したような比率で、固相に均質に混合され、粉末剤や顆粒剤、錠剤、カプセル剤のような固形製剤に設計できる。また、本発明の組成物は、水と共に溶解され、シロップ剤、液剤のような液状製剤に設計でき、必要時、凍結乾燥を通じて、使用に際し懸濁または乳濁、溶解して投与することもできる。
【0032】
本発明の薬剤学的組成物は従来の組成物より経口吸収率が著しく増加するので、単位投与量を大幅に減らして使用することができる。例えば、活性成分がアレンドロン酸ナトリウムの場合、従来の単位投与量の最大1/100まで低減可能である。
【発明を実施するための最良の形態】
【0033】
以下、実施例を通じて本発明を具体的に説明する。但し、これら実施例は本発明の例示に過ぎず、本発明の範囲がこれらだけに限定されるものではない。
【0034】
実施例1〜3
実施例1〜3のため、活性物質(薬物)としてアレンドロン酸ナトリウム13.0mgをHBSS緩衝液(buffer)100mLに加え、水溶性高分子キトサン(HFP(登録商標)、(株)慈光)6.5mg、26.0mg、52.0mgをHBSS緩衝液100mLにそれぞれ加えて溶解させた。その後、アレンドロン酸溶液とそれぞれのキトサン溶液を同一量ずつ取って攪拌してから均質に混合した。
【0035】
実施例4
実施例4のため、活性物質としてアレンドロン酸ナトリウム13.0mgをHBSS緩衝液100mLに加え、水溶性低分子キトサン(FACOS(登録商標)、(株)キトライフ)52.0mgをHBSS緩衝液100mLに加えて溶解させた。その後、二つの溶液を同一量ずつ取って混合した後、よく混ざるように攪拌した。
【0036】
実施例5
実施例5のためには、活性物質としてアレンドロン酸ナトリウム13.0mgをHBSS緩衝液100mLに加え、キトサンモノマーである塩酸グルコサミン34.5mgをHBSS緩衝液100mLに加えて溶解させた。その後、二つの溶液を同一量ずつ取って混合した後、よく混ざるように攪拌した。
【0037】
比較例1及び2
比較例1のため、活性物質としてアレンドロン酸ナトリウム13.0mgをHBSS緩衝液200mLに加えて溶解させた。
【0038】
比較例2のためには、活性物質として アレンドロン酸ナトリウム13.0mgをHBSS緩衝液100mLに加え、従来の高分子キトサン52.0mgをHBSS緩衝液100mLに加えて懸濁させた。
【0039】
前述した実施例1〜5及び比較例1によって製造された溶液は、全て目視で透明に溶解されたが、比較例2で製造された溶液は、目視でも完全に溶解できず不透明な状態に懸濁させ、実験例に使用した。
【0040】
実験例1-7
実験例1〜7のため、実施例1〜5及び比較例1〜2で製造された水溶液ないし懸濁液を、2週培養されたCaco−2細胞の先端側(Apical side)に200μLずつ加え、基底側(basolateral side)にHEPES緩衝液1,000μLを入れた後、培養器中で2時間細胞を培養する。2時間後、細胞の先端及び基底側の両方から緩衝液を回収して、サンプルをFMOC−Clで前処理した後、高速液体クロマトグラフィー法で薬物の濃度を測定し、下記の数式1によって先端側から基底側への吸収度を測定した。
【0041】
透過度(%)=基底側の透過量(ng)/先端側の負荷量(ng)
【0042】
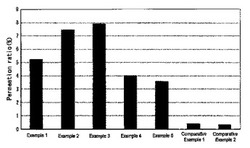
Caco−2細胞による透過度実験は、当業界で薬物の経口吸収率と経口を通じた吸収速度を評価するために施される典型的な実験モデルである。図1は、実験例1〜7において本発明の組成物のCaco−2細胞実験の2時間後のビスホスフォネート吸収度(%)を示すグラフである。ここで、実験例1〜5は、比較例1を使用した実験例6に比べて8〜20倍の著しい吸収率増加を示した。すなわち、本発明の組成物は、極性が高くて経口吸収が約1%未満に過ぎない活性物質に対して、経口吸収率を画期的に上昇させる結果をもたらすことが分かる。一方、比較例2を使用した実験例7の透過度は比較例1と類似している透過度を示して、通常のキトサンは水に溶けず薬物の吸収に全く影響を与えないと判断される。一方、溶解し易く生体活用性が高く開発された水溶性高分子キトサン(HFP)及び低分子キトサン、キトサンモノマーは、アレンドロン酸ナトリウムの細胞透過に影響を与えることによって、経口投与時吸収率を画期的に上昇させる結果をもたらすことが分かる。
【0043】
実施例6〜8
実施例6〜8のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、水溶性高分子キトサン(HFP(登録商標))2.51g、7.53g、20.08gをそれぞれ混合し、これに薬剤学的に許容される賦形剤のうち通常の崩壊剤として、デンプングリコール酸ナトリウムを重量比として5%加えて、均一に混合した。これを圧縮強打し、粉砕した後、18メッシュ篩で選別して顆粒を形成させた。それぞれの顆粒に崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%、潤滑剤としてべヘン酸グリセリルを重量比として3%加えた後、総重量が70gになるように微結晶セルロースを適量加えて最終混合した。前述したように形成された最終混合物を、打錠機を用いて活性成分がアレンドロン酸として20mg含有するように打錠して、それぞれの錠剤を製造した。
【0044】
実施例9
実施例9のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、水溶性低分子キトサン(FACOS(登録商標))20.08gを混合し、これに薬剤学的に許容される賦形剤のうち通常の崩壊剤として、デンプングリコール酸ナトリウムを重量比として5%加えて、均一に混合した。これを無水エタノールで練り混ぜ、乾燥した後、18メッシュ篩で選別して顆粒を形成させた。形成された顆粒に、崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%、潤滑剤としてべヘン酸グリセリルを重量比として3%加えた後、総重量が70gになるように微結晶セルロースを適量加えて最終混合した。前述したように形成された最終混合物を、打錠機を用いて活性成分がアレンドロン酸として20mg含有するように打錠して、それぞれの錠剤を製造した。
【0045】
実施例10
実施例10のため、活性物質であるアレンドロン酸ナトリウム5.02gに対してキトサンモノマーである塩酸グルコサミン13.3gを混合し、これに薬剤学的に許容される賦形剤のうち通常の崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%加えて、均一に混合した。これを水で練り混ぜ、乾燥した後、18メッシュ篩で選別して顆粒を形成させた。形成された顆粒に、崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%、潤滑剤としてべヘン酸グリセリルを重量比として3%加えた後、総重量が70gになるように微結晶セルロースを適量加えて最終混合した。前述したように形成された最終混合物を、打錠機を用いて活性成分がアレンドロン酸として20mg含有するように打錠して、それぞれの錠剤を製造した。
【0046】
実施例11〜13
実施例11〜13のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、水溶性高分子キトサン2.51g、7.53g、20.08gをそれぞれ混合し、これに実施例6〜8と同様な方式で顆粒を製造し、最終混合した。前述したように形成された最終混合物をカプセル充填機を用いて活性成分がアレンドロン酸として20mg含有するようにそれぞれのカプセル剤を製造した。
【0047】
実施例14
実施例14のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、低分子水溶性低分子キトサン20.08gを混合し、これに実施例9と同様な方式で顆粒を製造し、最終混合した。前述したように形成された最終混合物をカプセル充填機を用いて活性成分がアレンドロン酸として20mg含有するようにカプセル剤を製造した。
【0048】
実施例15
実施例15のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、キトサンモノマーである塩酸グルコサミン13.3gを混合し、これに実施例10と同様な方式で顆粒を製造し、最終混合した。前述したように形成された最終混合物を充填機を用いて活性成分がアレンドロン酸として20mg含有するようにそれぞれのカプセル剤を製造した。
【0049】
実施例16
実施例16のため、活性物質としてアレンドロン酸ナトリウム1.0gと水溶性高分子キトサン (HFP(登録商標)) 4.0gを、水200mLに加えて目視で透明になるまで攪拌溶解した。製造された溶液に、アセスルパム(acesulfam)50mgとクエン酸20mg、オレンジエッセンス適量を加えて経口用液剤を製造した。
【0050】
実施例17
実施例17のため、活性物質としてアレンドロン酸ナトリウム1.0gと水溶性低分子キトサン(FACOS(登録商標))4.0gを、水200mLに加えて目視で透明になるまで攪拌した。製造された溶液にアセスルパム50mg、クエン酸20mg、オレンジエッセンス適量を加えて経口用液剤を製造した。
【0051】
実施例18及び19
実施例18ないし19のため、活性物質であるアレンドロン酸ナトリウム 5.02gとキトサン20.08gに対して、有機酸としてグルタミン酸10.04g、クエン酸10.04gのうち1種をそれぞれ混合し、これに薬剤学的に許容される賦形剤のうち通常の崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%加え、均一に混合した。これを無水エタノールで練り混ぜ乾燥し、圧縮強打して粉砕した後、18メッシュ篩で選別して顆粒を形成させた。それぞれの顆粒に崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%、潤滑剤としてべヘン酸グリセリルを重量比として3%加えた後、総重量が70gになるように微細結晶セルロースを適量加えて最終混合した。前述したように形成された最終顆粒を、打錠機を用いて活性成分がアレンドロン酸として20mg含有するように打錠してそれぞれの錠剤を製造した。
【0052】
実験例8 〜12
実験例8〜12のため、37℃、50rpmの条件で作動される溶出機を使用して、実施例6〜10で製造された錠剤を使って、下記の数式2によって水におけるそれぞれの溶出率を測定した。
【0053】
溶出率(%)=(At×標準採取量(mg)×9×標準純度(%))/(As×91.37)
At: 溶出時間当たり試験液のピーク面積
As: 溶出時間当たり標準液のピーク面積
【0054】
図2は、実験例8〜12において本発明の組成物で製造された錠剤の経時的な溶出率(%)を示すグラフである。ここで、実験例8〜12において全て、溶出開始60分以内に80%以上の高い溶出率を示した。すなわち、本発明の製剤は、水と共に経口的に投与される時、1時間以内に殆どの薬物が製剤から放出され、水によく溶解できず薬物の放出を遅らせる従来のキトサンとは違って、薬物の吸収率向上に寄与することが分かる。
【産業上の利用可能性】
【0055】
本発明は、生体内でイオン化し水溶性が高く、生体脂質膜を通過できず、生物学的利用率が10%未満のビスホスフォネート系薬物から選ばれる1種以上の活性物質と、生体適合性水溶性キトサンから選ばれる1種以上を必須構成成分とする薬剤学的組成物であって、本発明では、高容量で投与されていたビスホスフォネート系薬物の経口吸収を改善して、薬物の副作用を最小化することによって、薬物に対する患者の適応性を高めることができる。
【0056】
本発明の好ましい態様を例示的な目的で開示してきたが、当業者であれば、添付の請求項に開示されているような本発明の精神及び範囲を逸脱することなく、様々な変更、追加及び代用が可能であることを理解されるであろう。
【図面の簡単な説明】
【0057】
本発明の上記および他の目的、特徴及びその他の利点は、添付図面を参照して、詳細な説明より明らかに理解されるであろう。
【図1】図1は、実験例1〜7で測定した活性薬物のCaco−2細胞への透過度(%)を示すグラフである。
【図2】図2は、実験例8〜12において本発明の組成物で製造された錠剤の経時的な溶出率(%)を測定した結果を示したグラフである。
【技術分野】
【0001】
本発明は、水で溶解可能な水溶性高分子キトサン及び/または低分子キトサン及び/またはキトサンモノマーを含有するビスホスフォネート系薬物の薬剤学的組成物に関し、極性が高いことから生体脂質膜を通過できず生物学的利用率が低い薬物の経口吸収率を向上させるための新規な薬剤学的組成物に関する。
【背景技術】
【0002】
現在開発中のビスホスフォネート系薬物などは、極性が極めて高くて生体脂質膜を透過できず、カルシウムなどの多価金属イオンと強い親和性を有して生体内でこれらと結合する際、不溶性複合体を形成することによって消化管で細胞膜を通じて吸収し難いと知られている(参考文献:Br.J.Cancer、71、Suppl.24、67、1995)。また、pH6〜8の小腸の内部でアニオン性を有するので、小腸における吸収も難しく、殆どの薬物が10%未満の吸収率を有し、特にアレンドロン酸ナトリウムの吸収率は1%未満であると報告されている(参考文献:Clin. Pharmacol. & Therapeutics、58(3)、288-209(1995))。
【0003】
従来から、高い極性のため胃腸(GI)生体脂質膜の吸収機作である自由拡散及び透過が行われなくて細胞間隙を通じた吸収も困難なことから、生体利用率が低いと知られたビスホスフォネート系薬物の吸収を増加させるための研究事例は一部報告されている。
【0004】
例えば、ビスホスフォネートを含む活性物質に脂肪酸を含む吸収促進剤を添加して経口吸収率を増加させる先行技術としては、アメリカ特許出願公開第2003/0091623号と国際公開第00/50012号公報があり、中鎖脂肪酸トリグリセリド(medium chain triglyceride)を吸収促進剤として用いた国際公開第99/18972号公報と双性イオン性(zwitterionic)リン脂質を用いた国際公開第01/76577号公報がある。これら先行技術は全て脂肪から由来する物質を使用して固形製剤を設計するため、多くの短所を抱えている。特に、脂肪酸と中鎖脂肪酸トリグリセリドは液状または半固形であり、活性物質より極めて多く使用すべきなので、実質的な製品化が難しく、双性リン脂質はそれ自体の低い安定性と腐敗の恐れのため、やはり製品化が困難である。
【0005】
アメリカ特許第6309663号には、親水性の表面活性剤と疎水性の表面活性剤を共に使用して吸収を増加させる方法が開示されている。この先行技術は、表面活性剤の極めて広範な範囲で、キトサン誘導体を包括的に要求するが、表面活性剤の存在それ自体が胃腸管に副作用効果の別な原因をもたらす。一方、本発明は表面活性剤を含まなくても胃腸障害改善に役に立つ。また、引例がキトサン本来の性質とは極めて異なるキトサン-EDTA及び/またはキトサン−EDTA−アンチパイン(antipain)複合体を使用したという点と、これらを酵素抑制剤として使用するという点において、本発明と明らかに区分される。
【0006】
自体開発した経口吸収促進剤を使用して経口吸収を増加させる方法が開示されている国際公開第02/070438号公報は、本発明で使用する水溶性キトサンとは相異なる吸収促進剤を使用している。この先行技術の合成された吸収促進剤は、生体適合性物質でなく、それ自体が有害な胃腸管副作用を持ち得ることから、当業界において通常の医薬品賦形剤と言えない。
【0007】
一方、国際公開第00/61111号公報は、吸収向上効果の立証なしに極めて広範な賦形剤の組成を、吸収改善組成物として請求している。ここで言及する賦形剤は、全ての界面活性剤;胆汁酸;脂肪酸及びそのけん化塩;中鎖脂肪酸グリセリド;オイル;エナミン(enamine);全てのキレート剤(chelating agent);フェノチアジン(phenothiazine);カルニチン又はペプチドの脂肪酸誘導体;アゾン、コンカナバリンA(concanavalin A)、ホスフェート及び誘導体、ジホスフェート及び誘導体;マイヤール反応(maillard reaction)の生成物;共重合体及び生分解性高分子を含む全高分子;キトサン及びキトサン誘導体;から選ばれる1種以上を使用すると開示されている。しかし、吸収改善の効果は、具体的な資料として提示された例がなく、ただ組成物だけが列挙されている。特に、本発明と関連するキトサンは、組成の例にも言及されていない。胃腸内環境が酸性であっても、実質的なヒトの胃腸内酸度はpH1から5まで広範なことから、キトサンが溶解されない可能性が高く、溶解されてもその速度が極めて遅くなる。ビスホスフォネートの主な吸収が経口服用後30分以内に発生することを考慮する際、一般的なキトサンの組成は溶解されないため、ビスホスフォネートの経口吸収にいずれの影響を及ぼさない。従って、本発明のキトサンが通常のキトサンではなく水でも迅速に可溶化するキトサンであるという点と、本発明の薬剤学的組成物が、水溶性キトサンを用いた即時放出の特徴を有するビスホスフォネートの薬剤学的組成物であるという点において明らかな違いがある。
【0008】
ヨーロッパ特許出願公開第1302201号は、経口吸収改善剤としてアミノアルキルメタクリレート共重合体に該当するEudragit Eと酸性物質を含有する組成物を開示している。この技術は、経口吸収改善のためにアクリレート誘導体であるEudragit Eを使用したが、本発明の水溶性キトサンはサッカライド構造であって相異なる。また、当業界で認知されているように、キトサンは生体適合性物質であり、胃腸管毒性を解消するのに役に立つ(参考文献:British Journal of Plastic Surgery、53、601-606(2000))という点において、胃腸管障害が酷いビスホスフォネート系薬物の薬剤学的組成物に最適である。
【0009】
一方、剤形の構造的特性を用いて活性物質の放出速度を物理的に制御することによって経口吸収率の向上を図った先行技術は次の通りである。
【0010】
アメリカ特許出願公開第2004/0176328号は、水溶性活性物質がその水溶性活性物質より低い融点を有する物質で封じ込められてカプセル化し、カプセル化した粒子が連続的な固相に担持される固形の剤形を開示している。アメリカ特許第6207197号は、活性物質を封じ込めた核粒、水不溶性重合体からなる制御放出層及び粘膜付着性陽イオン重合体からなる外郭層を、包含する胃滞留型微粒球を記載している。これら技術は、薬物とキトサンの相互作用による経口吸収率の上昇とは関係なく、活性物質をカプセル形態または微粒球形態に封じ込めた製剤を作って、これより薬物の放出速度を調節することによる生体利用率アップの目的があるという点において、本発明と異なる。また、これらは、持続的な放出効果を示す組成物である一方、本発明は、ビスホスフォネートの経口吸収率を実質的に向上させるために即時放出の薬剤学的組成物を提供するという点においても異なる。ビスホスフォネート系薬物の長時間胃腸滞留または持続的な放出は経口吸収率の変化を誘導することができるとしても、ビスホスフォネートと腸管粘膜の接触時間を延ばして食道及び胃腸での毒性が増加する短所を同時に有するので、適切な制御放出と言えない。
【発明の開示】
【発明が解決しようとする課題】
【0011】
本発明では、高い極性によって胃腸管の生体脂質膜の通過が困難なことから生体利用率が低く、通常高い単位量で投与されるビスホスフォネート系薬物であるアレンドロン酸ナトリウムに対して、水で溶解可能な水溶性高分子キトサン及び/または低分子キトサン及び/またはキトサンモノマーを適正比率で配合することによって、極性活性物質の経口吸収率を高めることを目的とする。
【0012】
また、経口吸収率を高めることによって相対的に高い単位で投与されていた活性物質の投与単位を下げることによって薬物が有する副作用を最小化させ、同時に、生体膜治療効果を有する水溶性キトサンを配合することによって胃腸毒性を最小化する、ビスホスフォネート系薬物の薬剤学的組成物を提供するところに、その目的がある。
【0013】
そして、これら組成物を使用して製剤化することによって、一般的に溶解速度が遅い重合体と結合して製剤化する場合問題となる遅い溶出を改善した剤形設計を、その目的とする。
【課題を解決するための手段】
【0014】
本発明は、生体内でイオン化し水溶性が高くて生体脂質膜を通過できず、生物学的利用率が10%未満のビスホスフォネート系薬物から選ばれる1種以上の活性物質と、生体適合性水溶性キトサンから選ばれる1種以上を必須構成成分にして、早い速度で崩壊させ最小60分以内に80%以上の活性物質を胃腸管系に放出することによって、ビスホスフォネート系薬物の経口吸収率を改善することを特徴とする、薬剤学的組成物を提供する。
【0015】
本発明の特徴は三つに大別される。第1に、極性活性物質(ビスホスフォネート系薬物)の陰イオン極性部位を水でも溶解可能な水溶性キトサンの陽イオン電荷部位で遮蔽することによって、相対的に薬物の陽イオン極性部位を露出させて細胞間隙を通じた吸収を容易にしたり、水溶性キトサン及び/または低分子キトサン及び/またはキトサンモノマーを使って薬物の極性を減少させ、薬物の疎水性を増加させることによって脂質膜を通じた自由拡散及び分配に有利な条件を誘導することによって、活性物質の生体脂質膜内部への搬送を容易にして、生物学的利用率を向上させている。第2に、活性物質の投与単位を減少するとともに、繊維芽細胞の増殖を刺激して傷治癒効果を有し、GI毒性を減少させることで知られている(参考文献:Biomaterials、20、2959-2966(2001) & Advanced Drug Delivery Review、52、105-115(2001))キトサン、特に水でも溶解可能な水溶性キトサンを使用することによって、既存ビスホスフォネート系薬物の製剤により示される食道及び胃腸関連毒性を減少させようとしている。本発明に適用される水溶性キトサンは水に対する溶解度が0.1%w/v以上であることが望ましく、さらに望ましくは水に対する溶解度が0.5%w/v以上のものである。
【0016】
最後に、水では溶解されず酸性条件下でだけ溶解される通常のキトサンで製剤化する場合、個体差によって溶解速度が遅れるか又は溶解自体が不完全なことから、薬物の一般的な吸収の60分以内、望ましくは30分以内に目的とする吸収効果を発揮できない短所がある。従って、通常のキトサンの代わりに、水で容易に溶解される水溶性キトサンを使うことによって、胃でも迅速に溶解される速崩性製剤を作って活性物質の迅速な溶出を誘導している。
【0017】
結局、本発明によって、経口吸収し難いビスホスフォネート系薬物に対してその経口吸収率を増加させることによって、薬物の少ない単位投与量でも骨吸収抑制作用を効率よく防止し、薬物から引き起こされる食道及び胃腸毒性を減らして、患者の適応性をよくすることができる、新たなビスホスフォネート系薬物の製剤の開発が可能になる。
【0018】
本発明の組成物は、ビスホスフォネート系薬物と生体適合性陽イオン性重合体である水溶性キトサン及び/または低分子キトサン及び/またはキトサンモノマーを必須とし、薬剤学的に許容される賦形剤をさらに含む。
【0019】
本発明のビスホスフォネート系薬物は、水溶性が高くて薬物の経口吸収が不可能な薬物であって、生物学的利用率30%未満、特に生物学的利用率10%未満の薬物を意味し、水に溶解する際、薬物の構造内に1個以上の陰イオン電荷及び/または陽イオン電荷を有する薬物である。そして、これらは水分配係数(Log P)が主に1.0以下であって、相対的にオイルに比べて水に対する親和力が高い特性を示す。このような活性物質としては、例えば、アレンドロネート(4−アミノ−1−ヒドロキシブチリデン−1、1−ビスホスホン酸)、シマドロネート(インカドロネート、1−(シクロヘプチルアミノ)メチリデン−1、1−ビスホスホン酸)、エチドロネート(1−ヒドロキシエチリデン−1、1−ビスホスホン酸)、チルドロネート(1−(4−クロロフェニルチオ)メチリデン−1、1−ビスホスホン酸)、ミノドロネート(1−ヒドロキシ−2−(イミダゾ[1、2−a]ピリジン−3−イル)エチリデン−1、1−ビスホスホン酸)、イバンドロネート(1−ヒドロキシ−3−(N−メチル−N−ペンチルアミノ)プロピリデン−1、1−ビスホスホン酸)、リセドロネート(1−ヒドロキシ−2−(3−ピリジル)エチリデン−1、1−ビスホスホン酸)、パミドロネート(3−アミノ−1−ヒドロキシプロピリデン−1、1−ビスホスホン酸)、ゾレドロネート(1−ヒドロキシ−3−(1−ピロリジニル)プロピリデン−1、1−ビスホスホン酸、1−ヒドロキシ−2−(1−イミダゾリル)エチリデン−1、1−ビスホスホン酸)、ネリドロネート(6−アミノ−1−ヒドロキシヘキシリデン−1、1−ビスホスホン酸)、オルパドロネート(ミルドロネート、N、N−ジメチル−3−アミノ−1−ヒドロキシプロピリデン−1、1−ビスホスホン酸)及びその可能な塩またはエステル誘導体及びその混合物がある。
【0020】
ビスホスフォネート系薬物は、骨組織からカルシウムの再吸収を強力に抑制して、破骨細胞の機能を低下させて、骨密度を緻密にできる、骨粗しょう症治療薬である。しかし、優れた薬効を有しているものの、生体内適用時色々の問題点を抱えている薬物として認識されている。経口吸収の面では、朝食の30分前に過量の水と共に服用してこそ薬物の吸収が起こり、その生体利用率も30%未満、特に10%未満である。最も代表的なビスホスフォネート系薬物であるアレンドロネートは生体利用率が0.7%未満と報告されている。特にカルシウムのような多価金属イオンと強く結合して、沈殿が発生し、食事や飲み物によっても薬物の生物学的利用率が半分以下に減少すると知られている。そして、用法では、錠剤を口腔内で溶かして服用する時は、深刻な口内炎または肝炎を引き起こす恐れがあり、正常に服用しても、長期服用時、患者の約36%で胸焼け(heartburn)または上腹部痛(epigastric pain)を起こしている。また食道疾患時には、重症な食道炎(severe esophagitis)または広範囲な食道炎(extensive esophagitis)を引き起こす場合があると使用説明書に記載されている。
【0021】
従って、ビスホスフォネート系薬物の最適な改良型薬剤(incrementally modified drugs(IMDs))は、生物学的利用率を向上させて、同じ効果を示す薬物の単位投与量を減らすことによって薬物自体が伴う副作用を最小化し、さらに胃腸管(GI)毒性を増加させないか、毒性を減少させうる生体適合性物質を含有する、薬剤学的組成物である。
【0022】
ビスホスフォネートは骨組織に分布された以後には、半減期が11.9年であって極めて長いので、胃腸管粘膜組織が再生される5日以上の間隔で投与されることが薬効を減少させず副作用を最小化する投与期間として認識されている。従って、アレンドロネートの場合、毎日10mgより、7日毎に70mgの経口投与単位容量が副作用を軽減できる方法である。しかしながら、これも生物学的利用率が1%に及ばないことを考慮すれば、生物学的利用率を増加させて、7日毎に70mgの単位を革新的に減少させることが、ビスホスフォネート系薬物の短所および問題点を改善する最も効率的な方法になり得る。
【0023】
生体適合性の物質でありビスホスフォネートの生物学的利用率を向上させることができる吸収担体としては、水溶性キトサンが適している。本発明の水溶性キトサンは、水で溶解可能な、高分子キトサン、分子量別混合キトサン、低分子キトサン、キトオリゴ糖、キトサンモノマー(グルコサミン)及びその混合物を包括する概念であり、キトサンと酸性物質が均質に配合された混合物を含む。本発明において使われる水溶性キトサンは、他の誘導体化過程や追加の酸性化過程を要らず、水でも極めて迅速に溶解される特性を有するが、キトサンのモノマーであるグルコサミンは水に対する溶解度が0.5w/v%以上であって極めて優れて、生体胃腸の酸度と関係なく一定した体内吸収率をアップすることができる特徴がある。
【0024】
本発明の水溶性キトサンはグルコサミンモノマーから成り、分子量によって水溶性高分子キトサンと低分子キトサン、キトサンモノマー(グルコサミン)とに大別される。水溶性高分子キトサンは、分子量10,000〜500,000の範囲が使用され、望ましくは100,000〜200,000の範囲が使用可能である。水溶性低分子キトサンは、キトオリゴ糖と同じ意味で混用される場合もあるが、分子量200〜10,000の範囲が使用され、望ましくは分子量500〜2,000の範囲が使用できる。そして、水溶性キトサンモノマーは、文字通りキトサンをモノマー単位まで分解して生成されるグルコサミン(キトサミン、2-アミノ-2-デオキシ-D-グルコース)を意味する。
【0025】
この水溶性キトサンは、キトサンが酸性物質と均質に配合された混合物であるか、キトサンモノマーであるグルコサミンが酸性物質とイオン的引力によって配列されたキトサンの酸性塩である。前記酸性物質として、塩酸、硫酸、硝酸などの無機酸または乳酸、酢酸、クエン酸、酒石酸、コハク酸などの有機酸から1種以上の酸性物質が使用でき、望ましくは塩酸が使用できるが、本発明はこれに限定されるものではない。前記において、キトサンが酸性物質と均質に配合された混合物とは、通常のキトサンが前記無機酸または有機酸と物理的に均質に混合された形態を意味する。前記でキトサンモノマーであるグルコサミンが酸性物質とイオン的引力によって配列されたキトサンの酸性塩とは、グルコサミンのアミン基が陽電荷を帯びて、無機酸または有機酸が陰電荷を帯びるので、陽電荷と陰電荷との間にイオン的に引力が働いてグルコサミンと酸性物質が規則的に配列された形態を意味する。この水溶性キトサンの具体的な製品としては韓国の(株)慈光のエチエフピーキトサン(HFP Chitosan)や(株)キトライフのFACOSなどがあるが、本発明はこれらに限定されるものではない。
【0026】
キトサン中のキトサンモノマーであるグルコサミンと無機酸または有機酸をモル比として1:0.1〜1:50、望ましくは1:0.5〜1:10で固相または液状に均質に混和した混合物、またはこれらを全て水に溶解してから再び乾燥して取得したキトサン粉末も本発明の水溶性キトサンの範疇に属する。また、通常のキトサンと無機酸または有機酸を全て水に溶解してから、これに有機溶媒を加えて析出させ、有機溶媒を除去したキトサン粉末も本発明の水溶性キトサンの範疇に属する。
【0027】
蟹、海老などの甲殻類及び昆虫類の外骨格や細胞壁の保護組織から得られるキチンという物質を脱アセチル化して得られる通常のキトサンも、グルコサミンを構成モノマーにしているが、本発明の水溶性キトサンと比較して、酸性物質を均質に持てず、酸性物質をモノマー構造内に有しない。したがって、pH3以下の酸性下でだけ溶解でき、水では全く溶解されず、酸性溶液でもその溶解速度が極めて遅く、本発明の効果である経口吸収率の向上を発揮できない。
【0028】
たとえ胃腸内環境が酸性であるとしても、実質的なヒトの胃腸内酸度はpH1〜5の広範なことから、通常のキトサンは溶解されない可能性が高く、溶解されてもその速度が極めて遅くなる。従って、通常のキトサンをもっては、生体内適用時に1時間以内の迅速な薬物吸収が適しているビスホスフォネート系薬物における、実質的な経口吸収率向上の効果が全く得られない。さらに溶解速度が遅い通常のキトサンは、かえって薬物の放出を阻害して、迅速な吸収が求められるビスホスフォネート系薬物の吸収を減少させる逆効果も発生する場合がある。
【0029】
全体として、本発明の薬剤学的組成物を製造するために、活性物質と水溶性キトサンを混合したり、薬剤学的に許容される賦形剤と共に混合することができる。活性物質に対して水溶性高分子キトサン及び/または低分子キトサン(キトオリゴ糖)及び/またはキトサンモノマーから選ばれる1種以上を、活性物質の重量を基準に、重量比として100:1〜1:100、望ましくは25:1〜1:25、さらに望ましくは10:1〜1:10で配合する。また、本発明の薬剤学的組成物は薬剤学的に認められる通常の方法として、混合(blending)及び練り混ぜ(kneading)、粉砕(grinding)、篩分け(sieving)、充填(filling)、圧縮(compressing)、凍結乾燥(lyophilization)、噴射乾燥(spray-drying)、流動乾燥(fluid-bed drying)、遠心分離造粒(centrifugal granulation)などを通じて製剤化できる。
【0030】
本発明の組成物は当業界で通常に使用されている薬剤学的に許容される賦形剤を、さらに含有することができる。薬剤学的に許容される賦形剤としては希釈剤(diluent)、結合剤(binder)、崩壊剤(disintegrant)、色素剤(coloring agent)、甘味剤(sweeting agent)、香料(Flavor)、保存剤(preservative)、潤滑剤(lubricant)などが使用可能であり、前述した機能を複合的に有する賦形剤を使用することもできる。希釈剤としては、ラクトース、デキストロース、微結晶セルロース、デンプンなどから選ばれた1種以上が使用可能であり、結合剤としては、ポリビニルピロリドン、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、ヒドロキシエチルセルロース、第二リン酸カルシウム、アルギン酸ナトリウムなどから選ばれた1種以上が、崩壊剤としては、クロスカメロースナトリウム、デンプングリコール酸ナトリウム、架橋化ポリビニルピロリドン、アルファ化デンプン、低置換度ヒドロキシプロピルセルロースなどから選ばれた1種以上が、色素剤としては、水溶性色素、タール色素などから選ばれる1種以上、甘味剤としては、デキストロース、ソルビトール、マンニトール、アスパルテーム、アセスルファム、クエン酸などから選ばれた1種以上、香料としては、オレンジ香粉末、ブドウ香粉末、イチゴ香粉末、ブルーベリー粉末などから選ばれた1種以上、保存剤としては、安息香酸、メチルパラベン、エチルパラベン、プロピルパラベンなどから選ばれた1種以上、潤滑剤としては、ステアリン酸マグネシウム、タルク、軽質無水珪酸、スクロース脂肪酸エステルなどから選ばれた1種以上が使用可能であるが、これらに限定されるものではない。このように形成されたビスホスフォネート系薬物と水溶性キトサンの組成物は、胃で迅速に崩壊され、1時間以内に、望ましくは30分以内に、製剤からビスホスフォネート系薬物を全て放出し、キトサンは迅速に溶解され、薬物の生体膜透過を促進するようになる。
【0031】
本発明の組成物は、水のない状態で、前述したような比率で、固相に均質に混合され、粉末剤や顆粒剤、錠剤、カプセル剤のような固形製剤に設計できる。また、本発明の組成物は、水と共に溶解され、シロップ剤、液剤のような液状製剤に設計でき、必要時、凍結乾燥を通じて、使用に際し懸濁または乳濁、溶解して投与することもできる。
【0032】
本発明の薬剤学的組成物は従来の組成物より経口吸収率が著しく増加するので、単位投与量を大幅に減らして使用することができる。例えば、活性成分がアレンドロン酸ナトリウムの場合、従来の単位投与量の最大1/100まで低減可能である。
【発明を実施するための最良の形態】
【0033】
以下、実施例を通じて本発明を具体的に説明する。但し、これら実施例は本発明の例示に過ぎず、本発明の範囲がこれらだけに限定されるものではない。
【0034】
実施例1〜3
実施例1〜3のため、活性物質(薬物)としてアレンドロン酸ナトリウム13.0mgをHBSS緩衝液(buffer)100mLに加え、水溶性高分子キトサン(HFP(登録商標)、(株)慈光)6.5mg、26.0mg、52.0mgをHBSS緩衝液100mLにそれぞれ加えて溶解させた。その後、アレンドロン酸溶液とそれぞれのキトサン溶液を同一量ずつ取って攪拌してから均質に混合した。
【0035】
実施例4
実施例4のため、活性物質としてアレンドロン酸ナトリウム13.0mgをHBSS緩衝液100mLに加え、水溶性低分子キトサン(FACOS(登録商標)、(株)キトライフ)52.0mgをHBSS緩衝液100mLに加えて溶解させた。その後、二つの溶液を同一量ずつ取って混合した後、よく混ざるように攪拌した。
【0036】
実施例5
実施例5のためには、活性物質としてアレンドロン酸ナトリウム13.0mgをHBSS緩衝液100mLに加え、キトサンモノマーである塩酸グルコサミン34.5mgをHBSS緩衝液100mLに加えて溶解させた。その後、二つの溶液を同一量ずつ取って混合した後、よく混ざるように攪拌した。
【0037】
比較例1及び2
比較例1のため、活性物質としてアレンドロン酸ナトリウム13.0mgをHBSS緩衝液200mLに加えて溶解させた。
【0038】
比較例2のためには、活性物質として アレンドロン酸ナトリウム13.0mgをHBSS緩衝液100mLに加え、従来の高分子キトサン52.0mgをHBSS緩衝液100mLに加えて懸濁させた。
【0039】
前述した実施例1〜5及び比較例1によって製造された溶液は、全て目視で透明に溶解されたが、比較例2で製造された溶液は、目視でも完全に溶解できず不透明な状態に懸濁させ、実験例に使用した。
【0040】
実験例1-7
実験例1〜7のため、実施例1〜5及び比較例1〜2で製造された水溶液ないし懸濁液を、2週培養されたCaco−2細胞の先端側(Apical side)に200μLずつ加え、基底側(basolateral side)にHEPES緩衝液1,000μLを入れた後、培養器中で2時間細胞を培養する。2時間後、細胞の先端及び基底側の両方から緩衝液を回収して、サンプルをFMOC−Clで前処理した後、高速液体クロマトグラフィー法で薬物の濃度を測定し、下記の数式1によって先端側から基底側への吸収度を測定した。
【0041】
透過度(%)=基底側の透過量(ng)/先端側の負荷量(ng)
【0042】
Caco−2細胞による透過度実験は、当業界で薬物の経口吸収率と経口を通じた吸収速度を評価するために施される典型的な実験モデルである。図1は、実験例1〜7において本発明の組成物のCaco−2細胞実験の2時間後のビスホスフォネート吸収度(%)を示すグラフである。ここで、実験例1〜5は、比較例1を使用した実験例6に比べて8〜20倍の著しい吸収率増加を示した。すなわち、本発明の組成物は、極性が高くて経口吸収が約1%未満に過ぎない活性物質に対して、経口吸収率を画期的に上昇させる結果をもたらすことが分かる。一方、比較例2を使用した実験例7の透過度は比較例1と類似している透過度を示して、通常のキトサンは水に溶けず薬物の吸収に全く影響を与えないと判断される。一方、溶解し易く生体活用性が高く開発された水溶性高分子キトサン(HFP)及び低分子キトサン、キトサンモノマーは、アレンドロン酸ナトリウムの細胞透過に影響を与えることによって、経口投与時吸収率を画期的に上昇させる結果をもたらすことが分かる。
【0043】
実施例6〜8
実施例6〜8のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、水溶性高分子キトサン(HFP(登録商標))2.51g、7.53g、20.08gをそれぞれ混合し、これに薬剤学的に許容される賦形剤のうち通常の崩壊剤として、デンプングリコール酸ナトリウムを重量比として5%加えて、均一に混合した。これを圧縮強打し、粉砕した後、18メッシュ篩で選別して顆粒を形成させた。それぞれの顆粒に崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%、潤滑剤としてべヘン酸グリセリルを重量比として3%加えた後、総重量が70gになるように微結晶セルロースを適量加えて最終混合した。前述したように形成された最終混合物を、打錠機を用いて活性成分がアレンドロン酸として20mg含有するように打錠して、それぞれの錠剤を製造した。
【0044】
実施例9
実施例9のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、水溶性低分子キトサン(FACOS(登録商標))20.08gを混合し、これに薬剤学的に許容される賦形剤のうち通常の崩壊剤として、デンプングリコール酸ナトリウムを重量比として5%加えて、均一に混合した。これを無水エタノールで練り混ぜ、乾燥した後、18メッシュ篩で選別して顆粒を形成させた。形成された顆粒に、崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%、潤滑剤としてべヘン酸グリセリルを重量比として3%加えた後、総重量が70gになるように微結晶セルロースを適量加えて最終混合した。前述したように形成された最終混合物を、打錠機を用いて活性成分がアレンドロン酸として20mg含有するように打錠して、それぞれの錠剤を製造した。
【0045】
実施例10
実施例10のため、活性物質であるアレンドロン酸ナトリウム5.02gに対してキトサンモノマーである塩酸グルコサミン13.3gを混合し、これに薬剤学的に許容される賦形剤のうち通常の崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%加えて、均一に混合した。これを水で練り混ぜ、乾燥した後、18メッシュ篩で選別して顆粒を形成させた。形成された顆粒に、崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%、潤滑剤としてべヘン酸グリセリルを重量比として3%加えた後、総重量が70gになるように微結晶セルロースを適量加えて最終混合した。前述したように形成された最終混合物を、打錠機を用いて活性成分がアレンドロン酸として20mg含有するように打錠して、それぞれの錠剤を製造した。
【0046】
実施例11〜13
実施例11〜13のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、水溶性高分子キトサン2.51g、7.53g、20.08gをそれぞれ混合し、これに実施例6〜8と同様な方式で顆粒を製造し、最終混合した。前述したように形成された最終混合物をカプセル充填機を用いて活性成分がアレンドロン酸として20mg含有するようにそれぞれのカプセル剤を製造した。
【0047】
実施例14
実施例14のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、低分子水溶性低分子キトサン20.08gを混合し、これに実施例9と同様な方式で顆粒を製造し、最終混合した。前述したように形成された最終混合物をカプセル充填機を用いて活性成分がアレンドロン酸として20mg含有するようにカプセル剤を製造した。
【0048】
実施例15
実施例15のため、活性物質であるアレンドロン酸ナトリウム5.02gに対して、キトサンモノマーである塩酸グルコサミン13.3gを混合し、これに実施例10と同様な方式で顆粒を製造し、最終混合した。前述したように形成された最終混合物を充填機を用いて活性成分がアレンドロン酸として20mg含有するようにそれぞれのカプセル剤を製造した。
【0049】
実施例16
実施例16のため、活性物質としてアレンドロン酸ナトリウム1.0gと水溶性高分子キトサン (HFP(登録商標)) 4.0gを、水200mLに加えて目視で透明になるまで攪拌溶解した。製造された溶液に、アセスルパム(acesulfam)50mgとクエン酸20mg、オレンジエッセンス適量を加えて経口用液剤を製造した。
【0050】
実施例17
実施例17のため、活性物質としてアレンドロン酸ナトリウム1.0gと水溶性低分子キトサン(FACOS(登録商標))4.0gを、水200mLに加えて目視で透明になるまで攪拌した。製造された溶液にアセスルパム50mg、クエン酸20mg、オレンジエッセンス適量を加えて経口用液剤を製造した。
【0051】
実施例18及び19
実施例18ないし19のため、活性物質であるアレンドロン酸ナトリウム 5.02gとキトサン20.08gに対して、有機酸としてグルタミン酸10.04g、クエン酸10.04gのうち1種をそれぞれ混合し、これに薬剤学的に許容される賦形剤のうち通常の崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%加え、均一に混合した。これを無水エタノールで練り混ぜ乾燥し、圧縮強打して粉砕した後、18メッシュ篩で選別して顆粒を形成させた。それぞれの顆粒に崩壊剤としてデンプングリコール酸ナトリウムを重量比として5%、潤滑剤としてべヘン酸グリセリルを重量比として3%加えた後、総重量が70gになるように微細結晶セルロースを適量加えて最終混合した。前述したように形成された最終顆粒を、打錠機を用いて活性成分がアレンドロン酸として20mg含有するように打錠してそれぞれの錠剤を製造した。
【0052】
実験例8 〜12
実験例8〜12のため、37℃、50rpmの条件で作動される溶出機を使用して、実施例6〜10で製造された錠剤を使って、下記の数式2によって水におけるそれぞれの溶出率を測定した。
【0053】
溶出率(%)=(At×標準採取量(mg)×9×標準純度(%))/(As×91.37)
At: 溶出時間当たり試験液のピーク面積
As: 溶出時間当たり標準液のピーク面積
【0054】
図2は、実験例8〜12において本発明の組成物で製造された錠剤の経時的な溶出率(%)を示すグラフである。ここで、実験例8〜12において全て、溶出開始60分以内に80%以上の高い溶出率を示した。すなわち、本発明の製剤は、水と共に経口的に投与される時、1時間以内に殆どの薬物が製剤から放出され、水によく溶解できず薬物の放出を遅らせる従来のキトサンとは違って、薬物の吸収率向上に寄与することが分かる。
【産業上の利用可能性】
【0055】
本発明は、生体内でイオン化し水溶性が高く、生体脂質膜を通過できず、生物学的利用率が10%未満のビスホスフォネート系薬物から選ばれる1種以上の活性物質と、生体適合性水溶性キトサンから選ばれる1種以上を必須構成成分とする薬剤学的組成物であって、本発明では、高容量で投与されていたビスホスフォネート系薬物の経口吸収を改善して、薬物の副作用を最小化することによって、薬物に対する患者の適応性を高めることができる。
【0056】
本発明の好ましい態様を例示的な目的で開示してきたが、当業者であれば、添付の請求項に開示されているような本発明の精神及び範囲を逸脱することなく、様々な変更、追加及び代用が可能であることを理解されるであろう。
【図面の簡単な説明】
【0057】
本発明の上記および他の目的、特徴及びその他の利点は、添付図面を参照して、詳細な説明より明らかに理解されるであろう。
【図1】図1は、実験例1〜7で測定した活性薬物のCaco−2細胞への透過度(%)を示すグラフである。
【図2】図2は、実験例8〜12において本発明の組成物で製造された錠剤の経時的な溶出率(%)を測定した結果を示したグラフである。
【特許請求の範囲】
【請求項1】
ビスホスフォネート系薬物から選ばれる1種以上の活性物質と水に対する溶解度が0.1%w/v以上の水溶性キトサンから選ばれる1種以上を、重量比として25:1〜1:25含有することを特徴とする、ビスホスフォネート系薬物の経口吸収率を改善した薬剤学的組成物。
【請求項2】
前記ビスホスフォネート系薬物と水溶性キトサンが重量比として、10:1〜1:10で配合されることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項3】
前記水溶性キトサンが、水に対する溶解度が0.5%w/v以上であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項4】
前記水溶性キトサンが、分子量10,000〜500,000範囲の高分子キトサン、分子量200〜10,000範囲の低分子キトサン、グルコサミン及びその混合物から選ばれる1種以上であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項5】
前記水溶性キトサンが、キトサンと酸性物質との均質に配合された混合物であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項6】
前記水溶性キトサンが、キトサンのモノマーであるグルコサミンが酸性物質とイオン的引力により配列された、キトサンの酸性塩であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項7】
前記ビスホスフォネート系薬物が、アレンドロネート、シマドロネート(インカドロネート)、エチドロネート、チルドロネート、イバンドロネート、リセドロネート、パミドロネート、ゾレドロネート、ネリドロネート、オルパドロネート(ミルドロネート)、ミノドロネート及びその可能な塩又はエステル誘導体から、選ばれる1種以上であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項8】
前記ビスホスフォネート系薬物が、アレンドロン酸ナトリウムであることを特徴とする、請求項1〜7のいずれか1項に記載の薬剤学的組成物。
【請求項9】
組成物の剤形が、粉末剤、顆粒剤、錠剤、カプセル剤、シロップ剤、液剤、服用時懸濁剤又は乳濁剤、及び溶解して使用される凍結乾燥物から選ばれる1種であることを特徴とする、請求項1〜7のいずれか1項に記載の薬剤学的組成物。
【請求項1】
ビスホスフォネート系薬物から選ばれる1種以上の活性物質と水に対する溶解度が0.1%w/v以上の水溶性キトサンから選ばれる1種以上を、重量比として25:1〜1:25含有することを特徴とする、ビスホスフォネート系薬物の経口吸収率を改善した薬剤学的組成物。
【請求項2】
前記ビスホスフォネート系薬物と水溶性キトサンが重量比として、10:1〜1:10で配合されることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項3】
前記水溶性キトサンが、水に対する溶解度が0.5%w/v以上であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項4】
前記水溶性キトサンが、分子量10,000〜500,000範囲の高分子キトサン、分子量200〜10,000範囲の低分子キトサン、グルコサミン及びその混合物から選ばれる1種以上であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項5】
前記水溶性キトサンが、キトサンと酸性物質との均質に配合された混合物であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項6】
前記水溶性キトサンが、キトサンのモノマーであるグルコサミンが酸性物質とイオン的引力により配列された、キトサンの酸性塩であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項7】
前記ビスホスフォネート系薬物が、アレンドロネート、シマドロネート(インカドロネート)、エチドロネート、チルドロネート、イバンドロネート、リセドロネート、パミドロネート、ゾレドロネート、ネリドロネート、オルパドロネート(ミルドロネート)、ミノドロネート及びその可能な塩又はエステル誘導体から、選ばれる1種以上であることを特徴とする、請求項1に記載の薬剤学的組成物。
【請求項8】
前記ビスホスフォネート系薬物が、アレンドロン酸ナトリウムであることを特徴とする、請求項1〜7のいずれか1項に記載の薬剤学的組成物。
【請求項9】
組成物の剤形が、粉末剤、顆粒剤、錠剤、カプセル剤、シロップ剤、液剤、服用時懸濁剤又は乳濁剤、及び溶解して使用される凍結乾燥物から選ばれる1種であることを特徴とする、請求項1〜7のいずれか1項に記載の薬剤学的組成物。
【図1】


【図2】




【図2】


【公表番号】特表2008−528575(P2008−528575A)
【公表日】平成20年7月31日(2008.7.31)
【国際特許分類】
【出願番号】特願2007−553025(P2007−553025)
【出願日】平成18年1月3日(2006.1.3)
【国際出願番号】PCT/KR2006/000013
【国際公開番号】WO2006/080780
【国際公開日】平成18年8月3日(2006.8.3)
【出願人】(502153215)チョン・クン・ダン・ファーマシューティカル・コーポレーション (6)
【Fターム(参考)】
【公表日】平成20年7月31日(2008.7.31)
【国際特許分類】
【出願日】平成18年1月3日(2006.1.3)
【国際出願番号】PCT/KR2006/000013
【国際公開番号】WO2006/080780
【国際公開日】平成18年8月3日(2006.8.3)
【出願人】(502153215)チョン・クン・ダン・ファーマシューティカル・コーポレーション (6)
【Fターム(参考)】
[ Back to top ]

