肝障害モデル動物、及びそれを用いた肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法
【課題】従来技術に比してコスト的に遥かに有利であり、倫理的な問題が少ないにもかかわらず、簡便、正確で、有用性の高いin vivo評価系が構築できる新規な肝障害モデル動物とその作製方法を提供することであり、また、その肝障害モデル動物を用いることで、従来のモデル動物では事実上不可能であった、ヒト等の哺乳類の肝障害治療薬や肝機能改善若しくは予防機能を持つ食品素材を、in vivo評価系でありながら、網羅的・スクリーニング的に探索できる方法を提供すること。
【解決手段】完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その脂肪体及び/又は腸管に治療可能な障害が与えられているものであることを特徴とする肝障害モデル動物、及び、上記の肝障害モデル動物を用いることを特徴とする、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法。
【解決手段】完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その脂肪体及び/又は腸管に治療可能な障害が与えられているものであることを特徴とする肝障害モデル動物、及び、上記の肝障害モデル動物を用いることを特徴とする、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、哺乳類の肝障害を改善又は予防するために用いられる、肝障害モデル動物、その作製方法、それを用いた肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法に関するものである。
【背景技術】
【0002】
ヒト等の哺乳類の肝障害について改善効果又は予防効果のある、薬剤若しくは食品素材を開発するために、肝障害モデル動物を用いて被検薬剤や被検食品素材の効果を検証することは必須の検討項目となっている。
【0003】
代表的な肝障害モデルとしては、ラットやマウスに四塩化炭素を投与して急性又は慢性肝障害を起こさせるもの、あるいはアミノ酸の一種であるd−ガラクトサミンをラットに投与して肝障害を起こさせるもの等がある。後者の場合、マウスを用いた場合では肝障害が起こらないことが知られており、ラットのみ肝障害モデル動物として用いることができる。
【0004】
このように、用いる動物と「急性又は慢性肝障害を起こさせる化合物」によって肝障害の発生の有無が異なるため、化合物処理による肝障害の発生を一義的に予測することはできず、選択される動物とその処理結果との関係は単純なものとはなっていない。
【0005】
これらの肝障害モデルを利用して治療薬の効果を検討した具体的な例として、ラットのガラクトサミン肝障害モデル、又は、四塩化炭素肝障害モデルに及ぼす各種タンパク質の投与効果を、モデル動物血液中の肝臓逸脱酵素であるGOT、GPT(ALT)及びLDH活性を指標として検討した例(非特許文献1)や、四塩化炭素誘発慢性肝障害ラットを用いて、五味子リグナン中の有効成分が肝再生に及ぼす効果を検討した例(非特許文献2)等がある。
【0006】
肝障害モデル動物に対する個体レベルの影響・効果を指標として、肝障害改善効果又は肝障害予防効果が期待される薬剤や食品素材を探索することは、in vitroの系では見ることのできない薬剤や食品素材の「吸収」「代謝」「排泄」等の体内動態を反映したものとなるため、実際の治療効果を反映した有用性の高いものであることは明らかである。
【0007】
しかしながら、モデル動物を用いたin vivo評価系は有用性の高い評価系であるものの、肝障害改善作用や肝障害予防作用が期待される薬剤や食品素材には、無機物、有機物、ペプチド、タンパク質、天然物、漢方薬素材等、多方面・多種類の候補があるため、それらを網羅的・スクリーニング的に探索するには多くの問題点があった。
【0008】
すなわち、マウスやラットを肝障害モデル動物として用いる評価系は、被検対象の少ない最終段階の評価系としては適しているものの、多種類で多量処理が要求されるスクリーニング段階では、コストや操作性に問題があるだけでなく、倫理上の問題も大きい。そのため、スクリーニング用の評価系として見た場合、マウスやラットを用いる評価系は事実上用いることができないのが現状である。
【0009】
そこで、本発明者は、特にスクリーニング段階でマウスやラットに代替し得る病態モデル動物として、完全変態型昆虫の幼虫の1種であるカイコガの幼虫(以下、「カイコ」と略記する)に着目した。病態モデル動物として、カイコを用いることができるならば、安価で倫理上の問題も少ないからである。そして、自然免疫機構のみを有するカイコが獲得免疫機構を有するヒト等に感染する病原微生物に対する治療薬開発のための評価系と成り得ることを見出し報告した(特許文献1及び特許文献2)。
【0010】
しかしながら、上記の結果は、動物全身が関与する免疫応答機構と病原微生物との関係において、カイコ等の自然免疫機構のみを有する完全変態型昆虫の幼虫が、異なる免疫機構を有するヒト等の哺乳類を対象とした感染治療薬の効果を評価できるモデル動物となり得ることを示したものであって、哺乳類の特定臓器の障害を治療対象とした場合に、そのモデル動物となり得ることを示したものではなかった。
【0011】
カイコ等の完全変態型昆虫の幼虫は、マウスやラットのように人と同じ肝臓という臓器を持つものではなく、これまで肝障害モデル動物として用いることができるか否かについて、何らの検討も行われてこなかった。
【0012】
例えば、マウスやラット等に肝障害を起こさせる化合物を、完全変態型昆虫の幼虫に投与した場合、完全変態型昆虫の幼虫のどの部分が障害を受けるのか、障害の程度を定量的で正確な方法で評価できるのか、というような事項につき、何らの検討もされていなかった。すなわち、肝障害モデル動物として、完全変態型昆虫の幼虫を用いることができるかどうかについては、これまでなんら明らかにされてこなかった。
【0013】
従って、肝障害に対する新たな治療薬や食品等が強く望まれているにもかかわらず、それらを探索するための、コスト的な問題や倫理的問題が少なく、正確で有用な結果を与える肝障害モデル動物やそれを用いた治療薬等のスクリーニング方法は事実上ないのが現状であった。
【0014】
【特許文献1】WO2001/086287号公報
【特許文献2】WO2005/116269号公報
【非特許文献1】江頭祐嘉合他、日本栄養・食糧学会誌,48(4),291-297(1995)
【非特許文献2】竹田茂文他、日本薬理学会雑誌,90(1),51-65(1987)
【発明の開示】
【発明が解決しようとする課題】
【0015】
本発明は、上記背景技術に鑑みてなされたものであり、その課題は、従来技術に比してコスト的に遥かに有利であり、倫理的な問題が少ないにもかかわらず、簡便、正確で、有用性の高いin vivo評価系が構築できる新規な肝障害モデル動物とその作製方法を提供することにある。
【0016】
また、その肝障害モデル動物を用いることで、従来のモデル動物では事実上不可能であった、ヒト等の哺乳類の肝障害治療薬や肝機能改善若しくは予防機能を持つ食品素材を、in vivo評価系でありながら、網羅的・スクリーニング的に探索できる方法を提供することにある。
【課題を解決するための手段】
【0017】
本発明者は、上記課題を解決するため、昆虫類中でも完全変態型昆虫の幼虫に着目した。そして、完全変態型昆虫の幼虫は、ヒト、マウス、ラット等の哺乳類に肝障害を発症させる化合物を適切に投与することによって、哺乳類の肝細胞に特異的に存在するアラニン・アミノトランスフェラーゼ(以下、「ALT」と略記する)の活性(以下、「ALT活性」と略記する)が、完全変態型昆虫の幼虫の体液でも上昇することを見出した。
【0018】
また、その際に、完全変態型昆虫の幼虫の脂肪体組織及び/又は腸管に障害を生じていること、脂肪体及び/又は腸管が、化合物の代謝に関しては哺乳類の肝臓に相当する機能を有していると考えられること、ALT活性を測定すること、脂肪体組織と腸管組織の観察、個体死の判定によって障害の程度を正確に評価することができること、更に、ヒト等の肝障害を改善する薬剤を投与することで、上記酵素活性値の上昇が対照群と比較して明確に低下したり抑制されたりすること等を見出し、本発明を完成するに至った。
【0019】
すなわち、本発明は、完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その脂肪体及び/又は腸管に治療可能な障害が与えられているものであることを特徴とする肝障害モデル動物を提供することにある。
【0020】
また、本発明は、桑の葉又は桑の葉抽出物を実質的に含まない餌で育てたカイコの幼虫に、その脂肪体及び/又は腸管に治療可能な障害を与える化合物を投与する工程を含むことを特徴とする肝障害モデル動物の作製方法を提供することにある。
【0021】
また、本発明は、上記の肝障害モデル動物を用いることを特徴とする、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法を提供することにある。
【0022】
また、本発明は、哺乳類の肝障害を改善する薬剤又は食品素材のスクリーニング方法であって、
(a)完全変態型昆虫の幼虫に化合物を投与することによって、その脂肪体及び/又は腸管に治療可能な障害を与える工程、
(b)(a)工程中又は(a)工程後の完全変態型昆虫の幼虫に、被検薬剤又は被検食品素材を、注入又は食餌させることによって投与する工程、
(c)脂肪体及び/又は腸管の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法を提供することにある。
【0023】
また、本発明は、哺乳類の肝障害を予防する薬剤又は食品素材のスクリーニング方法であって、
(d)被検薬剤又は被検食品素材を、完全変態型昆虫の幼虫に注入又は食餌させることによって投与する工程、
(e)(d)工程中又は(d)工程後の完全変態型昆虫の幼虫に化合物を投与することによって、脂肪体及び/又は腸管に治療可能な障害を与える工程、
(f)脂肪体及び/又は腸管の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法を提供することにある。
【発明の効果】
【0024】
本発明によれば、肝障害の改善若しくは予防作用のある薬剤又は食品素材を多種多様な被検対象物から網羅的・スクリーニング的にピックアップできると共に従来のマウスやラットをモデル動物として用いた場合と同様のin vivoでの薬理評価を可能とする新規な肝障害モデル動物とその作製方法を提供することができ、またその新規な肝障害モデル動物を用いた、肝障害の改善若しくは予防作用に有用性の高い薬剤又は食品素材のスクリーニング方法を提供することができる。
【発明を実施するための最良の形態】
【0025】
以下、本発明について説明するが、本発明は以下の実施の形態に限定されるものではなく、発明の範囲内で任意に変形して実施することができる。
【0026】
本発明は、完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その脂肪体及び/又は腸管(以下、単に「脂肪体等」と略記する場合がある)に治療可能な障害が与えられているものであることを特徴とする肝障害モデル動物に関する。
【0027】
<1>完全変態型昆虫の幼虫
完全変態型昆虫とは、卵、幼虫、蛹、成虫の成長過程を経る昆虫をいう。完全変態型昆虫としては、例えば、鱗翅目(チョウ、ガ等)、双翅目(ハエ等)、膜翅目(ハチ、アリ等)、甲虫目(カブトムシ等)等に属する昆虫が挙げられる。下記の(5)〜(7)の要件を満たすため、完全変態型昆虫の幼虫(以下、単に「幼虫」と略記する場合がある)が本発明には用いられる。
【0028】
本発明においては、その脂肪体及び/又は腸管に治療可能な障害を与える化合物の投与や、「被検薬剤又は被検食品素材(以下、単に「被検薬剤等」と略記する場合がある)」の投与が容易であるため、イモムシ形態のものが好ましい。その点、鱗翅目又は甲虫目に属する昆虫の幼虫が適しており、中でもカイコガの幼虫(以下、「カイコ」と略記する)は、下記の(1)〜(7)の全てを満たすので、特に好適に用いることができる。
【0029】
(1)入手が容易である。
(2)飼育する方法が既に確立されており、更に飼育に利便性がある。
(3)ヒト等の哺乳類の内臓・器官と類似する性質が、これまでの研究である程度分かっている。
(4)遺伝系統が確立されており、遺伝的均一性の維持ができている。
(5)比較的大型で、動きが緩慢であり、実質上無毛なので、定量的に扱いやすい。
(6)狭いスペースで多数の個体を飼育でき、倫理的な問題も少ない。
(7)齢や体重を揃える等、同じ状態の個体を揃えることが容易である。
【0030】
これに対し、カマキリやバッタ等に代表される不完全変態昆虫は最初から成虫と同様の形態をしており、動きも活発であることから、投与が容易ではないため、完全変態型昆虫の幼虫と比べると不利な点が多い。
【0031】
本発明において、上記完全変態型昆虫の幼虫は、実質的に無毛であり、定量的な化合物の投与を可能とする大きさを有するものであることが好ましい。
【0032】
ここで、「実質的に無毛」とは、明らかに体毛を有する時期があっても、化合物や被検物質等の投与に使用する時期には少なくとも投与になんら支障がない無視できる短い体毛となっているという意味である。
【0033】
また、「定量的な化合物の投与を可能とする大きさ」とは、文字通り、肝障害モデル動物作製のための化合物の投与を行うことができる大きさを意味し、幼虫の種類、幼虫がずんぐりしているか細長いか等の形態、用いる注射器やシリンジの種類、その投与方法等により変動するものであるため、幼虫の具体的な大きさにより限定されるものではない。しかしながら、化合物の投与や被検物質等の投与、脂肪体、腸管等の臓器の取り出し、体液の採取の容易さ等の点から、体長は1cm以上であることがより好ましく、1.5cm以上15cm以下であることが特に好ましく、2cm以上10cm以下であることが更に好ましい。
【0034】
本発明においては、上記幼虫の大きさや齢数は、幼虫の種類、幼虫の形態、操作上の観点等から選択されればよく特に限定はないが、例えばカイコ等の場合、3齢以上の幼虫を用いることが好ましい。4齢〜5齢の幼虫がより好ましく、5齢の幼虫が特に好ましい。
【0035】
5齢幼虫は最終齢の幼虫であるため、体長が7cm程度と特に大きく、型も揃っていて体重もほぼ一定しているので、化合物や被検薬剤等の投与とその評価に適している。また、被検薬剤等を食餌させることによって投与する場合、食餌行動が旺盛であるため、食餌行動を阻害しない被検薬剤等であれば、餌に混ぜて食餌させた場合にその効果が現れ易い等の利点を有している。
【0036】
具体的な体重自体に制限はないが、5齢のカイコを用いた場合の体重と体重の幅は、5齢1日目の平均体重が2gであることを考慮し、好ましくは1.6g〜2.5g、より好ましくは1.7g〜2.4g、特に好ましくは1.8〜2.2g、最も好ましくは1.9〜2.1gである。更に、体重の幅が小さくなれば、より精密な結果が得られることはいうまでもない。
【0037】
本発明にカイコを用いる場合には、その品種は特に限定されない。これらは受精卵から育てて用いてもよいし、必要な齢の幼虫を入手してもよい。カイコガの受精卵やカイコの入手先としては、愛媛蚕種、上田蚕種等がある。
【0038】
<2>肝障害モデル動物の作製
本発明の肝障害モデル動物は、完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その「脂肪体及び/又は腸管」(脂肪体等)に治療可能な障害が与えられているものである。「肝障害モデル動物」とは、ヒト等の哺乳類の肝障害に関して知見を得るためのモデル動物という意味である。
【0039】
本発明において、完全変態型昆虫の幼虫に化合物を投与することによって、完全変態型昆虫の幼虫の脂肪体等に治療可能な障害を与えられることが新たに見いだされた。そして、この治療可能な障害が与えられた完全変態型昆虫の幼虫が、ヒト等の哺乳類の肝障害に関して知見を得るためのモデル動物となり得ることが新たに見いだされた。
【0040】
脂肪体等に治療可能な障害を与える化合物としては特に限定はなく、有機化合物であっても無機化合物であってもよい。ヒト等の哺乳類に肝障害を与えることが分かっているものが多い点等から有機物が好ましい。
【0041】
例えば、四塩化炭素は、哺乳類において、肝臓のシトクロームP450 2E1によって代謝され、トリクロロメチルラジカルとなり肝細胞に損傷を与えることが知られている。また、ラット等で肝障害モデル動物を作製する際に好適に用いられる、エチルアルコール、d−ガラクトサミン、リポポリサッカライド(LPS)、d−ガラクトサミン等も、完全変態型昆虫の幼虫の脂肪体等に治療可能な障害を与える可能性がある。
【0042】
完全変態型昆虫の幼虫の脂肪体等に治療可能な障害を与える化合物としては、有機物の中でも、塩素置換炭化水素類がより好ましい。かかる塩素置換炭化水素類としては特に限定はないが、例えば、モノクロロベンゼン、ジクロロベンゼン、トリクロロベンゼン、モノクロロメタン、ジクロロメタン、トリクロロメタン、四塩化炭素、モノクロロエチレン、ジクロロエチレン、トリクロロエチレン、1,1,1−トリクロロエタン、1,1,2−トリクロロエタン等が挙げられる。なかでも、塩素置換脂肪族炭化水素類が特に好ましく、そのうち、四塩化炭素が、上記したように、哺乳類の肝臓で代謝され、トリクロロメチルラジカルとなり肝細胞に損傷を与えることが詳しく研究されている等の理由で更に好ましい。
【0043】
本発明においては、肝障害モデル動物の有する「哺乳類の肝障害に相当する障害」、すなわち、脂肪体等に与えられた障害が治療可能であることが必須である。治療可能でなければ、被検薬剤等が有する、肝障害を改善する効果又は肝障害を予防する効果を見いだし得ない。従って、化合物の「脂肪体等に与える障害の強さ」を調節して、被検薬剤等のスクリーニングが可能な障害を与えるようにする必要がある。
【0044】
治療可能な障害を与えるには、投与する化合物の種類を決めたり、該化合物の投与量を決めたりする。化合物の投与量は、オリーブ油等の植物油;脂肪酸グリセリドであるパナセート(登録商標)等で、該化合物の投与液中の含有量を調整することが好ましい。投与液中の該化合物の濃度としては、適度な「治療可能な障害」を与えられれば特に限定はなく、また、化合物の種類(飽和度や比活性)によって異なるが、0.1〜70質量%が好ましく、1〜40質量%が好ましく、3〜30質量%が特に好ましい。
【0045】
5齢のカイコを例にとれば、1頭のカイコに対して、オリーブ油等の植物油で、好ましくは5質量%〜30質量%、より好ましくは10〜20質量%、特に好ましくは15質量%〜20質量%に希釈した、四塩化炭素等の塩素置換脂肪族炭化水素類を投与することが好ましい。希釈液の投与量は、5〜100μLが好ましく、10〜50μLがより好ましく、20〜30μLが特に好ましい。四塩化炭素量としては、カイコの体重1g当たり、好ましくは0.5mg〜5mg、より好ましくは1〜3mg、特に好ましくは1.8mg〜2.5mgが、脂肪体等に治療可能な障害を与える点で好ましい。
【0046】
なお、上記の濃度や投与量は、後述する被検薬剤等も同時に投与する場合であっても、化合物のみを投与する場合であっても(化合物を被検薬剤等より先に投与する場合であっても後に投与する場合であっても)、ほぼ同様である。投与の方法や投与部位は特に限定はないが、マイクロシリンジ等で、経口から消化管内への注入、又は、体内への注射によることが好ましい。カイコは開放血管系なので、腹脚から体腔内に注射することが特に好ましい。
【0047】
投与後、約6時間〜約24時間でALT活性が上昇する。化合物の種類、濃度、投与量等を調整することによって、ALT活性の上昇を可逆的にすることができ、すなわち、脂肪体及び/又は腸管に治療可能な障害を与えることができ、それができたために、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法が可能な「障害を有する肝障害モデル動物」ができた。
【0048】
多過ぎる化合物(例えば、5齢のカイコに、30質量%以上の四塩化炭素を25μL以上)を投与した場合には、障害の程度が強すぎるために、ALT活性の上昇は不可逆的となる場合があり、40質量%より多いと、ほとんどが不可逆的となる。この場合の障害は治療不可能な障害と考えられ、哺乳類で肝障害を改善する効果があることが知られている被検薬剤等で処理しても、カイコのALT活性は低下しないので、肝障害モデル動物として使用することができない場合がある。また、5質量%より低い濃度では、ALT活性の上昇が、被検薬剤等の効果を見るには小さ過ぎるかほとんど認められないので、肝障害モデル動物となり得ない場合がある。
【0049】
更に、上記適正投与量範囲であっても、ALT活性の上昇度には、試験毎に若干の変動が認められるので、より確実に被検薬剤等の肝障害改善又は予防効果の評価を行うためには、15質量%、20質量%等、1回の試験につき2種類以上の化合物濃度を設定して試験をすることが好ましい。
【0050】
また、投与時期は、被検薬剤等の肝障害改善の評価を行う場合は、例えば、5齢幼虫1日目に餌を与えた後、1日経過後更に6時間の絶食期間(この間で摂食した餌はほぼ消化される)を置いてから四塩化炭素等の化合物の投与を行い、被検薬剤等の肝障害予防の評価を行う場合は、例えば、被検薬剤等を投与してから、約24時間経過後に、四塩化炭素等の化合物の投与を行う等の方法を例示することができる。
【0051】
対照群は、希釈溶媒にオリーブ油等の植物油を用いた場合はその希釈溶媒を、化合物単独で投与した場合は、生理食塩水である0.9%食塩水を、化合物投与群と同量を同じタイミングで投与することが好ましい。
【0052】
肝障害モデル動物の作製に際して完全変態型昆虫の幼虫に与える餌は特に限定はないが、哺乳類の肝障害を改善又は予防する薬剤等のスクリーニングに大きな支障をきたさない餌が好ましい。また、完全変態型昆虫の幼虫において、ALT活性の上昇を抑制する物質が含まれていない餌が好ましい。例えば、完全変態型昆虫の幼虫がカイコの場合、「桑の葉又は桑の葉抽出物」(以下、単に「桑の葉等」と略記する)が実質的に含まれていない餌で育てたカイコが好ましい。カイコの5齢幼虫を肝障害モデル動物にする場合、「桑の葉等を実質的に含まない餌」は、カイコの種類によって飼育当初から使用してもよいし、3〜4齢幼虫となってから使用してもよい。また、例えば、完全変態型昆虫の幼虫がアゲハ蝶類の幼虫の場合、ミカン、サンショウ等のミカン科の植物の葉若しくは葉の抽出物が実質的に含まれていない餌で育てたアゲハ蝶類の幼虫が好ましい。
【0053】
ここで「実質的に含まれない場合」とは、例えば「桑の葉等」の場合、桑の葉等を全く含んでいない場合だけでなく、桑の葉等を含んでいるがALT活性に影響を与えない程度の含有量である場合やALT活性に影響を与える成分以外の桑の葉等を含んでいる場合も含まれる。
【0054】
通常、カイコに与える餌は桑の葉等を含む餌が用いられる。しかしながら、桑の葉等をカイコに摂取させた場合には、好ましい肝障害モデル動物とならない場合があることが確認された。すなわち、現象的には、桑の葉等を摂取したカイコは、ALT活性の上昇が認められないため、実際上、被検薬剤等の肝障害改善又は予防の効果をモニターすることがし難い状態となる場合がある。
【0055】
カイコの場合、餌は好ましくは、Silkmate 2S(日本農産工業)、又は、200g当り、例えば、ソルビー600(日清コスモフーズ)18g、大豆油(Wako)1.8mL、β−シトステロール(Sigma)0.12g、クエン酸(Wako)0.18g、アスコルビン酸(関東化学)1.2g、ソルビン酸(Wako)0.12g、無機塩混合物(カヤノ)1.8g、グルコース(nacalai)6g、でんぷん(Wako)18g、Vitamin mix[ビオチン(nacalai)480μg、葉酸(Wako)480μg、チアミンHCl(Wako)4.8mg、リボフラビン(Wako)4.8mg、ピリドキシンHCl(Wako)7.2mg、ニコチン酸(Wako)24mg、パトチン酸Ca(Wako)360mg、コリンCa(Wako)360mg、イノシトール(Wako)480mg、蒸留水24mL]4.8mL、寒天3.0g、蒸留水144mLを含む餌等である。
【0056】
桑の葉等には、特定の哺乳類を用いた検討により、肝障害改善又は予防の効果があることが報告されていることから、カイコにおいても、哺乳類と同様の桑の葉等の効果により、ALT活性が上昇しなかったと考えることができる。つまり、桑の葉等を含む餌による上記現象は、本発明の肝障害モデル動物によって、哺乳類において肝障害改善又は予防の効果のある被検薬剤等がスクリーニングできることを、具体例によって明確に示したものとなっている。
【0057】
また、完全変態型昆虫の幼虫に被検薬剤等を投与する場合は、餌を与えてから約1日経過後、更に被検薬剤等投与前に、好ましくは5〜7時間の絶食時間をおき、腸管内容物を消化させるようにすることが望ましい。腸管内容物が残っていると、真の体重からのバラツキが生じ、体重を元に決定される被検薬剤等の投与量にバラツキが生じ、結果的にALT活性のバラツキとなって現れる場合がある。
【0058】
本発明の場合、多くの個体数を用意することができるので、絶食時間を取った後の体重を測定し、一定体重内の個体を選別して用いることで、被検薬剤等の投与量をほぼ揃えることが可能である。
【0059】
<3>「肝障害を改善する薬剤又は食品素材のスクリーニング方法」における「肝障害モデル動物に対する被検薬剤等の投与」
本発明の一つの形態は、哺乳類の肝障害を改善する薬剤又は食品素材のスクリーニング方法であって、
(a)完全変態型昆虫の幼虫に化合物を投与することによって、その脂肪体等に治療可能な障害を与える工程、
(b)(a)工程中又は(a)工程後の完全変態型昆虫の幼虫に、被検薬剤等を注入又は食餌させることによって投与する工程、
(c)脂肪体等の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法である。
【0060】
被検薬剤等の肝障害改善の効果を評価する場合、化合物投与と同時又は化合物投与後に、被検薬剤等を投与することによって行う。被検薬剤等の投与は、注入又は食餌させることによって行うことが好ましい。「注入」とは、強制的に投与することをいい、経口から消化管内への注入、又は、体内への注射が含まれる。体内への注射の方法や注射部位は特に限定はないが、カイコは開放血管系なので、腹脚から体腔内に注射することが特に好ましい。
【0061】
化合物投与と同時に被検薬剤等を投与する方法は、得られた結果の相互比較を行うに際し、投与後の変動要因を少なくすることができる利点がある。しかしながら、被検薬剤等の種類やその投与方法によって、化合物投与から時間をおいて評価する必要がある場合には、個々の事情に応じて被検薬剤等の投与時期を設定すればよい。その場合、その投与時点における肝障害モデル動物のALT活性を確認しておくことが好ましい。
【0062】
被検薬剤等の投与量は、投与する物質、その状態、投与方法等の種々の要因により変動するものと考えられるので、ある程度の試行錯誤が必要である。しかしながら、被検薬剤等と同様の性状を有し、肝障害改善効果のあることが判っている薬剤や食品素材等がある場合には、それらによる結果を参考として投与量を決定する等の方法が好ましい。例えば、下記するNALCと同様の効果が期待される被検薬剤等を試験する場合の投与量は、NALCの場合を参考として、例えば、濃度0.1M〜0.4Mを、50μLが目安となる。
【0063】
被検薬剤等の投与量は、上記の事情があるため特に限定はないが、完全変態型昆虫の幼虫1g当たり、1〜20μmol/gが好ましく、2.5〜10μmol/gが特に好ましい。
【0064】
本発明において、被検薬剤等と比較するための陽性コントロールとして用いる薬剤や食品素材は特に限定はないが、四塩化炭素等の塩素置換炭化水素類による障害が活性酸素によるものであることを考慮すれば、例えば、抗酸化剤であることが好ましく、このうち、N−アセチルL−システイン(「NALC」と略記する)であることが特に好ましい。
【0065】
上記陽性コントロールとしてのNALCの投与量は、通常、四塩化炭素等の塩素置換炭化水素類の投与量に応じて変えなければならないが、2.5〜10μmol/gが、ALT活性の上昇を抑制することが確認されている等の理由で好ましい。上記範囲より多い投与量では、NALC自体による障害が発生し易くなる場合があり、更に多い場合は死亡する場合がある。
【0066】
<4>「肝障害を予防する薬剤又は食品素材のスクリーニング方法」における「肝障害モデル動物に対する被検薬剤等の投与」
本発明の一つの形態は、哺乳類の肝障害を予防する薬剤又は食品素材のスクリーニング方法であって、
(d)被検薬剤等を、完全変態型昆虫の幼虫に注入又は食餌させることによって投与する工程、
(e)(d)工程中又は(d)工程後の完全変態型昆虫の幼虫に化合物を投与することによって、脂肪体等に治療可能な障害を与える工程、
(f)脂肪体等の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法である。
【0067】
被検薬剤等の肝障害予防の効果を評価する場合、被検薬剤等の投与と同時又は被検薬剤等の投与後に、化合物を投与することによって行うことが好ましい。被検薬剤等の投与は、肝障害改善の評価を行う場合と同じく、注入又は食餌させることによって行うことが好ましい。
【0068】
注入させることによる投与の場合は、上記肝障害改善の評価を行う場合に順ずる方法で行えばよい。注入による投与の場合に、被検薬剤等の投与の回数を1回とするか、複数回とするかは、薬剤としての投与か、食品素材としての投与か等、評価の目的等に応じて選択することが好ましい。
【0069】
食餌させることによって投与を行う場合、予め被検薬剤等を混ぜた餌を、被検薬剤等を混ぜない餌と比較して問題なく摂取するかどうかを確認しておくことが好ましい。食餌させることによって投与する方法は、特に、食品素材、食品抽出物、天然物抽出物、タンパク質、繊維質、アミノ酸、ペプチド、無機物等の評価に有用である。
【0070】
被検薬剤等の最終投与後、絶食期間を置いた後に化合物を投与することも特に好ましい。絶食期間は、得られたデータ等に応じて適宜変更すべきであることはいうまでもないが、5〜7時間が好ましい。
【0071】
また、被検薬剤等を食餌によって投与した場合の化合物の投与時期、すなわち被検薬剤等の投与期間は、被検薬剤等投与開始1〜5日(5齢幼虫の期間内)が好ましいが、完全変態型昆虫の幼虫の状態に応じて適宜調整することができる。被検薬剤等の肝障害予防の評価を行う場合、被検薬剤等の投与方法や投与期間、投与量等による効果の表れ方の振れが肝障害改善の評価を行う場合より大きいと考えられるからである。
【0072】
被検薬剤等の肝障害予防の評価を行う場合に関するデータとして、桑の葉を餌として摂食したカイコは、四塩化炭素を投与してもALT活性が全く上昇しなかった(図4参照)。桑の葉はマウスやラット等を用いた検討により肝障害改善効果があることが報告されているので、桑の葉を上記肝障害予防効果の確認としての被検薬剤等と考えた場合、ALT活性が上昇しなかったことは、本発明が、肝障害予防効果を有する被検薬剤等のスクリーニングに用いることができることを示したものと考えることができる。
【0073】
<5>脂肪体等の障害の程度の評価
前記(c)及び上記(f)中の、「脂肪体等の障害の程度を評価する工程」は、完全変態型昆虫の幼虫の、体液中のALT活性の測定、脂肪体等の組織の観察、又は、個体死の判定を含むものである。以下に説明する。
【0074】
(A)ALT活性の測定
<ALT活性測定用試料の調製>
ALT活性測定用試料は、例えば、完全変態型昆虫の幼虫の体液を採取後、過塩素酸等と混合してタンパク質を沈殿・遠心分離することによって調製される。以下、これによって調製された試料を「体液抽出液」と略記する場合がある。
【0075】
<ALT活性の測定方法>
ALT活性の測定は、体液抽出液を検体として、例えば、文献「Methods for the measurement of catalytic concentrations of enzymes. (1980) Clinica. Chimica. Acta. 105, 147-154」に記載されている方法に従って行う。
【0076】
<完全変態型昆虫の幼虫の脂肪体等に発現するALT活性と哺乳類の肝臓に発現するALT活性との相関の検討>
本発明の一形態は、上記肝障害モデル動物を用いることを特徴とする、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法を提供するものである。本発明前までは、カイコにおいて四塩化炭素等による障害付与処理を行った後に、カイコ体液抽出液を検体として、哺乳類の肝臓に特異的に発現するALT活性を評価した例はなかったが、本発明により、カイコにおいても、脂肪体等の障害のマーカーとしてALT活性を用いることができることが明らかとなった。
【0077】
通常状態におけるカイコ体液中のALT活性と脂肪体中のALT活性とを比較したところ、脂肪体中のALT活性は、体液中のALT活性の100倍以上であること(なお、マウスの場合は肝臓中と血中で150倍程度)が判明し、ALTがカイコ脂肪体中に多く存在している酵素であることが確認された。
【0078】
哺乳類の場合、ALTは肝細胞に特異的に存在する酵素であるが、カイコにおいてALTは、前記したように、一般的に肝臓に相当するといわれている脂肪体に多く存在し、また腸管にも存在する。このことは、「カイコにおける脂肪体等の障害とALT活性との関係」が、「哺乳類における肝障害とALT活性との関係」と類似していることを示している。カイコの場合、脂肪体及び/又は腸管(脂肪体等)が、薬物分解等の哺乳類における肝臓に相当する機能を担っている可能性が高いものと考えられる。すなわち、カイコにおけるALT活性は、脂肪体等の障害の程度を反映したものであるが、機能的には哺乳類における肝障害の程度を反映したものであると考えられる。
【0079】
(B)脂肪体等の組織の観察
塩素置換炭化水素類等の化合物や被検薬剤等を投与した完全変態型昆虫の幼虫の脂肪体等は、完全変態型昆虫の幼虫から摘出後に組織切片として脂肪体試料又は腸管試料を調製し、組織における障害の有無や障害の程度を確認する。その際、例えば、ヘマトキシン・エオジン染色法等の染色法を使用することが好ましい。
【0080】
(C)完全変態型昆虫の幼虫の個体死の判定
個体死は弛緩の有無を目視で判定することによって判断する。個体が瀕死か否かの判定も、上記「個体死の判定」に含まれる。
【0081】
上記(c)(f)脂肪体及び/又は腸管の障害の程度を評価する工程における、(A)完全変態型昆虫の幼虫の体液中のALT活性の測定、(B)脂肪体及び/又は腸管の組織の観察、(C)個体死の判定は、陰性コントロール、陽性コントロール、化合物投与群、化合物及び被検薬剤等投与群、被検薬剤等投与群等を対象とする。
【0082】
<6>効果
本発明の肝障害モデル動物は、マウスやラット等のモデル動物では実質的に不可能であった肝障害の改善又は予防効果のある薬剤若しくは食品素材を、多種多様な被検薬剤等から、網羅的・スクリーニング的にピックアップできるとともに、上記薬剤又は食品素材の「吸収」「代謝」「排泄」等の体内動態を反映したin vivoでの効果を反映できる評価系を構築することが可能である。
【0083】
従って、スクリーニングの段階から実用性の高い肝障害の改善又は予防効果のある「薬剤若しくは食品素材」をピックアップすることができるので、上記薬剤や食品素材の開発の効率化と促進を図ることができる。
【実施例】
【0084】
以下に、実施例、試験例を挙げて本発明を更に具体的に説明するが、本発明は、その要旨を超えない限りこれらの実施例に限定されるものではない。
【0085】
実施例1
[肝障害モデル動物の作製と評価]
<カイコの種類・飼育条件>
カイコ(Hu Yo x Tsukuba・Ne)受精卵は、日本農産工業から購入した。27℃に設定したインキュベーター(サンヨー社製)で、桑の葉等を含まない人工餌であるシルクメイト2S(日本農産工業)を与え、5齢まで育てた。飼育容器としては、2齢までは、角型2号シャーレ(栄研器材社製)を用い、それ以降は、使い捨てのプラスチック製フードパック(フードパックFD大深、中央化学株式会社製)を用いた。以下に述べる各検討には、別途記載がない限り、5齢1日目に餌を与えた後、1日経過した(5齢2日目)カイコを用い、投与前、6時間の絶食期間を設けた。また、各検討には、絶食期間後の体重が1.8g〜2.2gの範囲のカイコを選別して用いた。
【0086】
<四塩化炭素の投与によるカイコの脂肪体等への障害付与処理>
上記絶食期間経過後のカイコの第5体節の模様部に、オリーブオイルで10質量%に希釈した四塩化炭素溶液25μLを注射により投与した。同様に、オリーブオイルのみ25μLを注射により投与した。
【0087】
<障害付与処理したカイコのALT活性の測定>
四塩化炭素溶液又はオリーブオイル投与後、1時間、3時間、5時間、24時間、48時間経過後にそれぞれ体液を採取し、10倍量の1%β−MEと混合してタンパク質を沈殿・遠心分離し、ALT活性測定用の体液抽出液とした。
【0088】
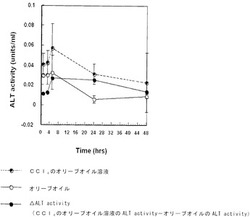
<肝障害モデル動物の示すALT活性の経時変化例>
上記ALT活性を測定した結果を図1に示す。四塩化炭素投与によるALT活性(四塩化炭素投与による真のALT活性値。図1中の「△ALT activity」(四塩化炭素のオリーブオイル溶液によるALT活性値からオリーブオイルのみによるALT活性値を引いた値))は、四塩化炭素投与後5時間で上昇し、四塩化炭素投与後5時間から24時間の間は一定値となっていた。また、四塩化炭素投与後48時間でALT活性は、ほぼ四塩化炭素投与時の値まで低下した。
【0089】
このことは、四塩化炭素溶液付与により惹起されたカイコ体内の障害が、哺乳類の肝臓における障害と同様の障害(哺乳類の肝臓と同様の機能を有する部位の障害)であり、少なくとも四塩化炭素投与後5時間から24時間の間、上記障害が与えられたカイコが作製されたことを示している。
【0090】
また、四塩化炭素投与後24時間経過後にはALT活性が低下し、48時間では元の水準に戻っていることから、カイコの上記障害は、治療できない不可逆的な障害ではなく治療可能な障害である。以上より、実施例1で作製された肝障害モデル動物は、哺乳類の肝障害を改善又は予防する効果を示す被検薬剤等(被検薬剤又は被検食品素材)のスクリーニングに適用可能なものであることが確認された。
【0091】
実施例2
[肝障害モデル動物の肝障害改善例1]
(NALCの投与によるALT活性低下の検討)
<N−アセチルL−システイン(NALC)投与例>
上記肝障害モデル動物が実際に哺乳類の肝障害改善又は予防効果を示す被検薬剤等のスクリーニングに適用可能か否かを検討する目的で以下の検討を行った。
【0092】
10質量%の四塩化炭素のオリーブオイル溶液を25μLカイコに注射し、6時間後のALT活性を確認する場合において、四塩化炭素溶液投与と同時に、0.1MのNALCの0.9%NaCl溶液を50μL投与したときに、ALT活性が低下するか否か(ALT活性の上昇が抑制されるか否か)について検討を行った。得られた結果を図2に示す。
【0093】
NALCを投与したカイコのALT活性は、検討した11頭のカイコ全てで低い値を示した。一方、NALCを投与しなかったカイコのALT活性は、11頭のカイコの中で5頭のカイコで高いALT活性を示した。また、高いALT活性を示した5頭のカイコ中3頭は弛緩が見られ個体死が確認された。
【0094】
これより、四塩化炭素による障害が活性酸素によるものであることを考慮すれば、抗酸化剤であるNALCを投与することにより、ALT活性の上昇が抑制されたことは、前記肝障害モデル動物を用いて、哺乳類の肝障害を改善又は予防する「薬剤若しくは食品素材」のスクリーニングができることを示している。
【0095】
実施例3
[肝障害モデル動物の肝障害改善例2]
(桑の葉抽出物の投与によるALT活性低下の検討)
実施例2において、「NALCの0.9%NaCl溶液50μL」に代えて「桑の葉抽出物の水溶液50μL」を用いた以外は、実施例2と同様に評価したところ、ALT活性の上昇が抑制される傾向が認められた(図4の左半分、○で示した人工餌摂取のデータ参照)。すなわち、図4の左から4列目のプロットによると、5例中全例において、ALT活性の上昇の抑制が認められた。
【0096】
すなわち、四塩化炭素投与により障害を与えられたカイコの治療効果が認められた。このことは、前記肝障害モデル動物を用いて、哺乳類の肝障害を改善又は予防する「薬剤若しくは食品素材」のスクリーニングが可能であることを示している。
【0097】
実施例4
[肝障害モデル動物の作製例1]
(四塩化炭素の濃度がALT活性又はその抑制に与える影響の検討)
濃度の異なる2種類の四塩化炭素溶液(15質量%と20質量%)25μLを、それぞれ注射を用いてカイコに投与し、24時間後のALT活性を確認した。四塩化炭素溶液投与と同時に、50μLの0.4MのNALCの0.9%NaCl溶液を投与した場合としない場合とを比較した。得られた結果を図3に示す。
【0098】
図3中の「P(t−test)」は、t検定におけるP−valueであり、帰無仮説を「NALC投与と非投与でALT活性に差がない」としたときの有意確率である。通常、Pが0.05以下なら、帰無仮説は棄却されて両分布(NALC投与と非投与のALT活性値の分布)には有意差があるとされる。15質量%と20質量%の何れも、Pは0.05以下であったことから、NALC投与による効果が認められた。
【0099】
更に詳しく見ると、15質量%四塩化炭素投与群は、検討した7例全てでALT活性は上昇したが、7例全てが一定値まで大きく上昇はしなかった。また、NALC投与によるALT活性の抑制については、ALT活性が7例全てで一定値まで明確に下がっていた。一方、20質量%四塩化炭素投与群は、検討した7例全てでALT活性が一定値まで明確に上昇したが、NALC投与によるALT活性の抑制は、15質量%四塩化炭素投与群に比べてややばらけた結果となった。
【0100】
同様に、5質量%四塩化炭素投与群でも評価した結果、全ての例でALT活性は上昇し、NALC投与によってALT活性が低くなった。しかし、四塩化炭素によるALT活性の上昇度が2.3倍(10質量%の場合は11倍)と小さかった。
【0101】
前記「肝障害モデル動物の肝障害改善例1」の四塩化炭素濃度10質量%でも良好な結果が得られたことも考慮すると、四塩化炭素濃度は、より好ましくは10〜20質量%、特に好ましくは15〜20質量%であることが分かった。また、四塩化炭素の濃度は15質量%と20質量%等、1回の試験につき少なくとも2種類の濃度で検討することが望ましいことが分かった。
【0102】
実施例5
[肝障害モデル動物の作製例2]
(桑の葉等の食餌の肝障害モデル動物に与える影響の検討)
実施例3において、桑の葉等(桑の葉又は桑の葉抽出物)を注射によって投与したカイコに四塩化炭素投与により障害を与えた場合、ALT活性の上昇が抑制される傾向が認められた。そこで改めて、桑の葉等が肝障害モデル動物の作製に与える影響について以下の検討を行った。
【0103】
<肝障害モデル動物の作製条件>
桑の葉等を含まない人工餌を与えた前記カイコ(以下、「人工餌摂食カイコ」と略記する)及び桑の葉を与えたカイコ(以下、「桑の葉摂食カイコ」と略記する)に、10質量%の四塩化炭素のオリーブオイル溶液を25μL注射し、24時間後のALT活性を測定した。
【0104】
0.1MのNALCオリーブオイル溶液50μLを、四塩化炭素投与と同時に投与したものを肝障害改善又は予防効果の陽性対照とした。また、オリーブオイルのみを注射したものを陰性対照とした。
【0105】
<桑の葉抽出物の投与>
桑の葉抽出物の水溶液50μLを、10質量%の四塩化炭素のオリーブオイル溶液25μLの注射と同時に注射した。
【0106】
人工餌摂食カイコは、実施例1とほぼ同様の結果を示した。すなわち、10質量%の四塩化炭素投与により、7例中4例において、ALT活性の上昇が認められた。また、陽性対照である0.1MのNALCの投与により、7例中全例において、ALT活性の上昇の抑制が認められた。また、桑の葉抽出物を投与した場合でも、5例中全例において、ALT活性の上昇の抑制が認められた(図4の○プロット参照)。
【0107】
10質量%の四塩化炭素投与前に桑の葉を食餌によって摂取されたカイコ(桑の葉摂食カイコ)は、24時間経過後に四塩化炭素を投与しても、6例全例において、ALT活性の明確な上昇は認められなかった。NALC投与群、桑の葉抽出物投与群も同様であった。従って、桑の葉摂食カイコを被検薬剤等の肝障害改善又は予防効果の評価に用いることは実質的にできないことが明らかとなった。
【0108】
通常、カイコの餌には桑の葉を含む餌が用いられるが、そのような餌を摂取したカイコを、肝障害改善効果や肝障害予防効果を有する被検薬剤等のスクリーニングのための肝障害モデル動物として用いることは好ましくないことが確認された。このことはカイコを用いて肝障害モデル動物を作製し、それによって肝障害改善効果や肝障害予防効果を有する被検薬剤等のスクリーニング方法を構築する上で非常に重要なポイントであり、本発明によって新たに見出されたことである。
【産業上の利用可能性】
【0109】
本発明の肝障害モデル動物は、従来の肝障害モデル動物では不可能であった被検薬剤等のスクリーニング段階でのin vivoでの効果を反映できる評価系を構築できるため、従来に比して非常に効率的に肝障害改善効果や肝障害予防効果を有する薬剤又は食品素材の研究開発を行うことができる。また、従来の方法ではピックアップできなかった「in vitroで効果が弱く、in vivoで有効な効果を発揮する薬剤又は食品素材」をピックアップすることが可能なため、これまでにない新たな肝障害改善・予防効果を有する「薬剤若しくは食品素材」を見出すために利用することが可能である。そのため、薬剤や食品素材の検討に広く利用されるものである。
【図面の簡単な説明】
【0110】
【図1】本発明の肝障害モデル動物におけるALT活性の経時変化の一例を示す図である。
【図2】本発明の肝障害モデル動物において、NALC投与によるALT活性の上昇の抑制を示す図である。
【図3】ALT活性の上昇、NALC投与によるALT活性の上昇の抑制の程度が、化合物(四塩化炭素)の濃度によってどれだけ影響を受けるかを検討した結果を示す図である。
【図4】本発明の肝障害モデル動物において、桑の葉抽出物投与によるALT活性の上昇の抑制を示す図であり、また、カイコに人工餌を摂取させた場合と桑の葉を摂取させた場合とについて、ALT活性の上昇とその抑制の程度を検討した結果を示す図である。
【技術分野】
【0001】
本発明は、哺乳類の肝障害を改善又は予防するために用いられる、肝障害モデル動物、その作製方法、それを用いた肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法に関するものである。
【背景技術】
【0002】
ヒト等の哺乳類の肝障害について改善効果又は予防効果のある、薬剤若しくは食品素材を開発するために、肝障害モデル動物を用いて被検薬剤や被検食品素材の効果を検証することは必須の検討項目となっている。
【0003】
代表的な肝障害モデルとしては、ラットやマウスに四塩化炭素を投与して急性又は慢性肝障害を起こさせるもの、あるいはアミノ酸の一種であるd−ガラクトサミンをラットに投与して肝障害を起こさせるもの等がある。後者の場合、マウスを用いた場合では肝障害が起こらないことが知られており、ラットのみ肝障害モデル動物として用いることができる。
【0004】
このように、用いる動物と「急性又は慢性肝障害を起こさせる化合物」によって肝障害の発生の有無が異なるため、化合物処理による肝障害の発生を一義的に予測することはできず、選択される動物とその処理結果との関係は単純なものとはなっていない。
【0005】
これらの肝障害モデルを利用して治療薬の効果を検討した具体的な例として、ラットのガラクトサミン肝障害モデル、又は、四塩化炭素肝障害モデルに及ぼす各種タンパク質の投与効果を、モデル動物血液中の肝臓逸脱酵素であるGOT、GPT(ALT)及びLDH活性を指標として検討した例(非特許文献1)や、四塩化炭素誘発慢性肝障害ラットを用いて、五味子リグナン中の有効成分が肝再生に及ぼす効果を検討した例(非特許文献2)等がある。
【0006】
肝障害モデル動物に対する個体レベルの影響・効果を指標として、肝障害改善効果又は肝障害予防効果が期待される薬剤や食品素材を探索することは、in vitroの系では見ることのできない薬剤や食品素材の「吸収」「代謝」「排泄」等の体内動態を反映したものとなるため、実際の治療効果を反映した有用性の高いものであることは明らかである。
【0007】
しかしながら、モデル動物を用いたin vivo評価系は有用性の高い評価系であるものの、肝障害改善作用や肝障害予防作用が期待される薬剤や食品素材には、無機物、有機物、ペプチド、タンパク質、天然物、漢方薬素材等、多方面・多種類の候補があるため、それらを網羅的・スクリーニング的に探索するには多くの問題点があった。
【0008】
すなわち、マウスやラットを肝障害モデル動物として用いる評価系は、被検対象の少ない最終段階の評価系としては適しているものの、多種類で多量処理が要求されるスクリーニング段階では、コストや操作性に問題があるだけでなく、倫理上の問題も大きい。そのため、スクリーニング用の評価系として見た場合、マウスやラットを用いる評価系は事実上用いることができないのが現状である。
【0009】
そこで、本発明者は、特にスクリーニング段階でマウスやラットに代替し得る病態モデル動物として、完全変態型昆虫の幼虫の1種であるカイコガの幼虫(以下、「カイコ」と略記する)に着目した。病態モデル動物として、カイコを用いることができるならば、安価で倫理上の問題も少ないからである。そして、自然免疫機構のみを有するカイコが獲得免疫機構を有するヒト等に感染する病原微生物に対する治療薬開発のための評価系と成り得ることを見出し報告した(特許文献1及び特許文献2)。
【0010】
しかしながら、上記の結果は、動物全身が関与する免疫応答機構と病原微生物との関係において、カイコ等の自然免疫機構のみを有する完全変態型昆虫の幼虫が、異なる免疫機構を有するヒト等の哺乳類を対象とした感染治療薬の効果を評価できるモデル動物となり得ることを示したものであって、哺乳類の特定臓器の障害を治療対象とした場合に、そのモデル動物となり得ることを示したものではなかった。
【0011】
カイコ等の完全変態型昆虫の幼虫は、マウスやラットのように人と同じ肝臓という臓器を持つものではなく、これまで肝障害モデル動物として用いることができるか否かについて、何らの検討も行われてこなかった。
【0012】
例えば、マウスやラット等に肝障害を起こさせる化合物を、完全変態型昆虫の幼虫に投与した場合、完全変態型昆虫の幼虫のどの部分が障害を受けるのか、障害の程度を定量的で正確な方法で評価できるのか、というような事項につき、何らの検討もされていなかった。すなわち、肝障害モデル動物として、完全変態型昆虫の幼虫を用いることができるかどうかについては、これまでなんら明らかにされてこなかった。
【0013】
従って、肝障害に対する新たな治療薬や食品等が強く望まれているにもかかわらず、それらを探索するための、コスト的な問題や倫理的問題が少なく、正確で有用な結果を与える肝障害モデル動物やそれを用いた治療薬等のスクリーニング方法は事実上ないのが現状であった。
【0014】
【特許文献1】WO2001/086287号公報
【特許文献2】WO2005/116269号公報
【非特許文献1】江頭祐嘉合他、日本栄養・食糧学会誌,48(4),291-297(1995)
【非特許文献2】竹田茂文他、日本薬理学会雑誌,90(1),51-65(1987)
【発明の開示】
【発明が解決しようとする課題】
【0015】
本発明は、上記背景技術に鑑みてなされたものであり、その課題は、従来技術に比してコスト的に遥かに有利であり、倫理的な問題が少ないにもかかわらず、簡便、正確で、有用性の高いin vivo評価系が構築できる新規な肝障害モデル動物とその作製方法を提供することにある。
【0016】
また、その肝障害モデル動物を用いることで、従来のモデル動物では事実上不可能であった、ヒト等の哺乳類の肝障害治療薬や肝機能改善若しくは予防機能を持つ食品素材を、in vivo評価系でありながら、網羅的・スクリーニング的に探索できる方法を提供することにある。
【課題を解決するための手段】
【0017】
本発明者は、上記課題を解決するため、昆虫類中でも完全変態型昆虫の幼虫に着目した。そして、完全変態型昆虫の幼虫は、ヒト、マウス、ラット等の哺乳類に肝障害を発症させる化合物を適切に投与することによって、哺乳類の肝細胞に特異的に存在するアラニン・アミノトランスフェラーゼ(以下、「ALT」と略記する)の活性(以下、「ALT活性」と略記する)が、完全変態型昆虫の幼虫の体液でも上昇することを見出した。
【0018】
また、その際に、完全変態型昆虫の幼虫の脂肪体組織及び/又は腸管に障害を生じていること、脂肪体及び/又は腸管が、化合物の代謝に関しては哺乳類の肝臓に相当する機能を有していると考えられること、ALT活性を測定すること、脂肪体組織と腸管組織の観察、個体死の判定によって障害の程度を正確に評価することができること、更に、ヒト等の肝障害を改善する薬剤を投与することで、上記酵素活性値の上昇が対照群と比較して明確に低下したり抑制されたりすること等を見出し、本発明を完成するに至った。
【0019】
すなわち、本発明は、完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その脂肪体及び/又は腸管に治療可能な障害が与えられているものであることを特徴とする肝障害モデル動物を提供することにある。
【0020】
また、本発明は、桑の葉又は桑の葉抽出物を実質的に含まない餌で育てたカイコの幼虫に、その脂肪体及び/又は腸管に治療可能な障害を与える化合物を投与する工程を含むことを特徴とする肝障害モデル動物の作製方法を提供することにある。
【0021】
また、本発明は、上記の肝障害モデル動物を用いることを特徴とする、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法を提供することにある。
【0022】
また、本発明は、哺乳類の肝障害を改善する薬剤又は食品素材のスクリーニング方法であって、
(a)完全変態型昆虫の幼虫に化合物を投与することによって、その脂肪体及び/又は腸管に治療可能な障害を与える工程、
(b)(a)工程中又は(a)工程後の完全変態型昆虫の幼虫に、被検薬剤又は被検食品素材を、注入又は食餌させることによって投与する工程、
(c)脂肪体及び/又は腸管の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法を提供することにある。
【0023】
また、本発明は、哺乳類の肝障害を予防する薬剤又は食品素材のスクリーニング方法であって、
(d)被検薬剤又は被検食品素材を、完全変態型昆虫の幼虫に注入又は食餌させることによって投与する工程、
(e)(d)工程中又は(d)工程後の完全変態型昆虫の幼虫に化合物を投与することによって、脂肪体及び/又は腸管に治療可能な障害を与える工程、
(f)脂肪体及び/又は腸管の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法を提供することにある。
【発明の効果】
【0024】
本発明によれば、肝障害の改善若しくは予防作用のある薬剤又は食品素材を多種多様な被検対象物から網羅的・スクリーニング的にピックアップできると共に従来のマウスやラットをモデル動物として用いた場合と同様のin vivoでの薬理評価を可能とする新規な肝障害モデル動物とその作製方法を提供することができ、またその新規な肝障害モデル動物を用いた、肝障害の改善若しくは予防作用に有用性の高い薬剤又は食品素材のスクリーニング方法を提供することができる。
【発明を実施するための最良の形態】
【0025】
以下、本発明について説明するが、本発明は以下の実施の形態に限定されるものではなく、発明の範囲内で任意に変形して実施することができる。
【0026】
本発明は、完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その脂肪体及び/又は腸管(以下、単に「脂肪体等」と略記する場合がある)に治療可能な障害が与えられているものであることを特徴とする肝障害モデル動物に関する。
【0027】
<1>完全変態型昆虫の幼虫
完全変態型昆虫とは、卵、幼虫、蛹、成虫の成長過程を経る昆虫をいう。完全変態型昆虫としては、例えば、鱗翅目(チョウ、ガ等)、双翅目(ハエ等)、膜翅目(ハチ、アリ等)、甲虫目(カブトムシ等)等に属する昆虫が挙げられる。下記の(5)〜(7)の要件を満たすため、完全変態型昆虫の幼虫(以下、単に「幼虫」と略記する場合がある)が本発明には用いられる。
【0028】
本発明においては、その脂肪体及び/又は腸管に治療可能な障害を与える化合物の投与や、「被検薬剤又は被検食品素材(以下、単に「被検薬剤等」と略記する場合がある)」の投与が容易であるため、イモムシ形態のものが好ましい。その点、鱗翅目又は甲虫目に属する昆虫の幼虫が適しており、中でもカイコガの幼虫(以下、「カイコ」と略記する)は、下記の(1)〜(7)の全てを満たすので、特に好適に用いることができる。
【0029】
(1)入手が容易である。
(2)飼育する方法が既に確立されており、更に飼育に利便性がある。
(3)ヒト等の哺乳類の内臓・器官と類似する性質が、これまでの研究である程度分かっている。
(4)遺伝系統が確立されており、遺伝的均一性の維持ができている。
(5)比較的大型で、動きが緩慢であり、実質上無毛なので、定量的に扱いやすい。
(6)狭いスペースで多数の個体を飼育でき、倫理的な問題も少ない。
(7)齢や体重を揃える等、同じ状態の個体を揃えることが容易である。
【0030】
これに対し、カマキリやバッタ等に代表される不完全変態昆虫は最初から成虫と同様の形態をしており、動きも活発であることから、投与が容易ではないため、完全変態型昆虫の幼虫と比べると不利な点が多い。
【0031】
本発明において、上記完全変態型昆虫の幼虫は、実質的に無毛であり、定量的な化合物の投与を可能とする大きさを有するものであることが好ましい。
【0032】
ここで、「実質的に無毛」とは、明らかに体毛を有する時期があっても、化合物や被検物質等の投与に使用する時期には少なくとも投与になんら支障がない無視できる短い体毛となっているという意味である。
【0033】
また、「定量的な化合物の投与を可能とする大きさ」とは、文字通り、肝障害モデル動物作製のための化合物の投与を行うことができる大きさを意味し、幼虫の種類、幼虫がずんぐりしているか細長いか等の形態、用いる注射器やシリンジの種類、その投与方法等により変動するものであるため、幼虫の具体的な大きさにより限定されるものではない。しかしながら、化合物の投与や被検物質等の投与、脂肪体、腸管等の臓器の取り出し、体液の採取の容易さ等の点から、体長は1cm以上であることがより好ましく、1.5cm以上15cm以下であることが特に好ましく、2cm以上10cm以下であることが更に好ましい。
【0034】
本発明においては、上記幼虫の大きさや齢数は、幼虫の種類、幼虫の形態、操作上の観点等から選択されればよく特に限定はないが、例えばカイコ等の場合、3齢以上の幼虫を用いることが好ましい。4齢〜5齢の幼虫がより好ましく、5齢の幼虫が特に好ましい。
【0035】
5齢幼虫は最終齢の幼虫であるため、体長が7cm程度と特に大きく、型も揃っていて体重もほぼ一定しているので、化合物や被検薬剤等の投与とその評価に適している。また、被検薬剤等を食餌させることによって投与する場合、食餌行動が旺盛であるため、食餌行動を阻害しない被検薬剤等であれば、餌に混ぜて食餌させた場合にその効果が現れ易い等の利点を有している。
【0036】
具体的な体重自体に制限はないが、5齢のカイコを用いた場合の体重と体重の幅は、5齢1日目の平均体重が2gであることを考慮し、好ましくは1.6g〜2.5g、より好ましくは1.7g〜2.4g、特に好ましくは1.8〜2.2g、最も好ましくは1.9〜2.1gである。更に、体重の幅が小さくなれば、より精密な結果が得られることはいうまでもない。
【0037】
本発明にカイコを用いる場合には、その品種は特に限定されない。これらは受精卵から育てて用いてもよいし、必要な齢の幼虫を入手してもよい。カイコガの受精卵やカイコの入手先としては、愛媛蚕種、上田蚕種等がある。
【0038】
<2>肝障害モデル動物の作製
本発明の肝障害モデル動物は、完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その「脂肪体及び/又は腸管」(脂肪体等)に治療可能な障害が与えられているものである。「肝障害モデル動物」とは、ヒト等の哺乳類の肝障害に関して知見を得るためのモデル動物という意味である。
【0039】
本発明において、完全変態型昆虫の幼虫に化合物を投与することによって、完全変態型昆虫の幼虫の脂肪体等に治療可能な障害を与えられることが新たに見いだされた。そして、この治療可能な障害が与えられた完全変態型昆虫の幼虫が、ヒト等の哺乳類の肝障害に関して知見を得るためのモデル動物となり得ることが新たに見いだされた。
【0040】
脂肪体等に治療可能な障害を与える化合物としては特に限定はなく、有機化合物であっても無機化合物であってもよい。ヒト等の哺乳類に肝障害を与えることが分かっているものが多い点等から有機物が好ましい。
【0041】
例えば、四塩化炭素は、哺乳類において、肝臓のシトクロームP450 2E1によって代謝され、トリクロロメチルラジカルとなり肝細胞に損傷を与えることが知られている。また、ラット等で肝障害モデル動物を作製する際に好適に用いられる、エチルアルコール、d−ガラクトサミン、リポポリサッカライド(LPS)、d−ガラクトサミン等も、完全変態型昆虫の幼虫の脂肪体等に治療可能な障害を与える可能性がある。
【0042】
完全変態型昆虫の幼虫の脂肪体等に治療可能な障害を与える化合物としては、有機物の中でも、塩素置換炭化水素類がより好ましい。かかる塩素置換炭化水素類としては特に限定はないが、例えば、モノクロロベンゼン、ジクロロベンゼン、トリクロロベンゼン、モノクロロメタン、ジクロロメタン、トリクロロメタン、四塩化炭素、モノクロロエチレン、ジクロロエチレン、トリクロロエチレン、1,1,1−トリクロロエタン、1,1,2−トリクロロエタン等が挙げられる。なかでも、塩素置換脂肪族炭化水素類が特に好ましく、そのうち、四塩化炭素が、上記したように、哺乳類の肝臓で代謝され、トリクロロメチルラジカルとなり肝細胞に損傷を与えることが詳しく研究されている等の理由で更に好ましい。
【0043】
本発明においては、肝障害モデル動物の有する「哺乳類の肝障害に相当する障害」、すなわち、脂肪体等に与えられた障害が治療可能であることが必須である。治療可能でなければ、被検薬剤等が有する、肝障害を改善する効果又は肝障害を予防する効果を見いだし得ない。従って、化合物の「脂肪体等に与える障害の強さ」を調節して、被検薬剤等のスクリーニングが可能な障害を与えるようにする必要がある。
【0044】
治療可能な障害を与えるには、投与する化合物の種類を決めたり、該化合物の投与量を決めたりする。化合物の投与量は、オリーブ油等の植物油;脂肪酸グリセリドであるパナセート(登録商標)等で、該化合物の投与液中の含有量を調整することが好ましい。投与液中の該化合物の濃度としては、適度な「治療可能な障害」を与えられれば特に限定はなく、また、化合物の種類(飽和度や比活性)によって異なるが、0.1〜70質量%が好ましく、1〜40質量%が好ましく、3〜30質量%が特に好ましい。
【0045】
5齢のカイコを例にとれば、1頭のカイコに対して、オリーブ油等の植物油で、好ましくは5質量%〜30質量%、より好ましくは10〜20質量%、特に好ましくは15質量%〜20質量%に希釈した、四塩化炭素等の塩素置換脂肪族炭化水素類を投与することが好ましい。希釈液の投与量は、5〜100μLが好ましく、10〜50μLがより好ましく、20〜30μLが特に好ましい。四塩化炭素量としては、カイコの体重1g当たり、好ましくは0.5mg〜5mg、より好ましくは1〜3mg、特に好ましくは1.8mg〜2.5mgが、脂肪体等に治療可能な障害を与える点で好ましい。
【0046】
なお、上記の濃度や投与量は、後述する被検薬剤等も同時に投与する場合であっても、化合物のみを投与する場合であっても(化合物を被検薬剤等より先に投与する場合であっても後に投与する場合であっても)、ほぼ同様である。投与の方法や投与部位は特に限定はないが、マイクロシリンジ等で、経口から消化管内への注入、又は、体内への注射によることが好ましい。カイコは開放血管系なので、腹脚から体腔内に注射することが特に好ましい。
【0047】
投与後、約6時間〜約24時間でALT活性が上昇する。化合物の種類、濃度、投与量等を調整することによって、ALT活性の上昇を可逆的にすることができ、すなわち、脂肪体及び/又は腸管に治療可能な障害を与えることができ、それができたために、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法が可能な「障害を有する肝障害モデル動物」ができた。
【0048】
多過ぎる化合物(例えば、5齢のカイコに、30質量%以上の四塩化炭素を25μL以上)を投与した場合には、障害の程度が強すぎるために、ALT活性の上昇は不可逆的となる場合があり、40質量%より多いと、ほとんどが不可逆的となる。この場合の障害は治療不可能な障害と考えられ、哺乳類で肝障害を改善する効果があることが知られている被検薬剤等で処理しても、カイコのALT活性は低下しないので、肝障害モデル動物として使用することができない場合がある。また、5質量%より低い濃度では、ALT活性の上昇が、被検薬剤等の効果を見るには小さ過ぎるかほとんど認められないので、肝障害モデル動物となり得ない場合がある。
【0049】
更に、上記適正投与量範囲であっても、ALT活性の上昇度には、試験毎に若干の変動が認められるので、より確実に被検薬剤等の肝障害改善又は予防効果の評価を行うためには、15質量%、20質量%等、1回の試験につき2種類以上の化合物濃度を設定して試験をすることが好ましい。
【0050】
また、投与時期は、被検薬剤等の肝障害改善の評価を行う場合は、例えば、5齢幼虫1日目に餌を与えた後、1日経過後更に6時間の絶食期間(この間で摂食した餌はほぼ消化される)を置いてから四塩化炭素等の化合物の投与を行い、被検薬剤等の肝障害予防の評価を行う場合は、例えば、被検薬剤等を投与してから、約24時間経過後に、四塩化炭素等の化合物の投与を行う等の方法を例示することができる。
【0051】
対照群は、希釈溶媒にオリーブ油等の植物油を用いた場合はその希釈溶媒を、化合物単独で投与した場合は、生理食塩水である0.9%食塩水を、化合物投与群と同量を同じタイミングで投与することが好ましい。
【0052】
肝障害モデル動物の作製に際して完全変態型昆虫の幼虫に与える餌は特に限定はないが、哺乳類の肝障害を改善又は予防する薬剤等のスクリーニングに大きな支障をきたさない餌が好ましい。また、完全変態型昆虫の幼虫において、ALT活性の上昇を抑制する物質が含まれていない餌が好ましい。例えば、完全変態型昆虫の幼虫がカイコの場合、「桑の葉又は桑の葉抽出物」(以下、単に「桑の葉等」と略記する)が実質的に含まれていない餌で育てたカイコが好ましい。カイコの5齢幼虫を肝障害モデル動物にする場合、「桑の葉等を実質的に含まない餌」は、カイコの種類によって飼育当初から使用してもよいし、3〜4齢幼虫となってから使用してもよい。また、例えば、完全変態型昆虫の幼虫がアゲハ蝶類の幼虫の場合、ミカン、サンショウ等のミカン科の植物の葉若しくは葉の抽出物が実質的に含まれていない餌で育てたアゲハ蝶類の幼虫が好ましい。
【0053】
ここで「実質的に含まれない場合」とは、例えば「桑の葉等」の場合、桑の葉等を全く含んでいない場合だけでなく、桑の葉等を含んでいるがALT活性に影響を与えない程度の含有量である場合やALT活性に影響を与える成分以外の桑の葉等を含んでいる場合も含まれる。
【0054】
通常、カイコに与える餌は桑の葉等を含む餌が用いられる。しかしながら、桑の葉等をカイコに摂取させた場合には、好ましい肝障害モデル動物とならない場合があることが確認された。すなわち、現象的には、桑の葉等を摂取したカイコは、ALT活性の上昇が認められないため、実際上、被検薬剤等の肝障害改善又は予防の効果をモニターすることがし難い状態となる場合がある。
【0055】
カイコの場合、餌は好ましくは、Silkmate 2S(日本農産工業)、又は、200g当り、例えば、ソルビー600(日清コスモフーズ)18g、大豆油(Wako)1.8mL、β−シトステロール(Sigma)0.12g、クエン酸(Wako)0.18g、アスコルビン酸(関東化学)1.2g、ソルビン酸(Wako)0.12g、無機塩混合物(カヤノ)1.8g、グルコース(nacalai)6g、でんぷん(Wako)18g、Vitamin mix[ビオチン(nacalai)480μg、葉酸(Wako)480μg、チアミンHCl(Wako)4.8mg、リボフラビン(Wako)4.8mg、ピリドキシンHCl(Wako)7.2mg、ニコチン酸(Wako)24mg、パトチン酸Ca(Wako)360mg、コリンCa(Wako)360mg、イノシトール(Wako)480mg、蒸留水24mL]4.8mL、寒天3.0g、蒸留水144mLを含む餌等である。
【0056】
桑の葉等には、特定の哺乳類を用いた検討により、肝障害改善又は予防の効果があることが報告されていることから、カイコにおいても、哺乳類と同様の桑の葉等の効果により、ALT活性が上昇しなかったと考えることができる。つまり、桑の葉等を含む餌による上記現象は、本発明の肝障害モデル動物によって、哺乳類において肝障害改善又は予防の効果のある被検薬剤等がスクリーニングできることを、具体例によって明確に示したものとなっている。
【0057】
また、完全変態型昆虫の幼虫に被検薬剤等を投与する場合は、餌を与えてから約1日経過後、更に被検薬剤等投与前に、好ましくは5〜7時間の絶食時間をおき、腸管内容物を消化させるようにすることが望ましい。腸管内容物が残っていると、真の体重からのバラツキが生じ、体重を元に決定される被検薬剤等の投与量にバラツキが生じ、結果的にALT活性のバラツキとなって現れる場合がある。
【0058】
本発明の場合、多くの個体数を用意することができるので、絶食時間を取った後の体重を測定し、一定体重内の個体を選別して用いることで、被検薬剤等の投与量をほぼ揃えることが可能である。
【0059】
<3>「肝障害を改善する薬剤又は食品素材のスクリーニング方法」における「肝障害モデル動物に対する被検薬剤等の投与」
本発明の一つの形態は、哺乳類の肝障害を改善する薬剤又は食品素材のスクリーニング方法であって、
(a)完全変態型昆虫の幼虫に化合物を投与することによって、その脂肪体等に治療可能な障害を与える工程、
(b)(a)工程中又は(a)工程後の完全変態型昆虫の幼虫に、被検薬剤等を注入又は食餌させることによって投与する工程、
(c)脂肪体等の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法である。
【0060】
被検薬剤等の肝障害改善の効果を評価する場合、化合物投与と同時又は化合物投与後に、被検薬剤等を投与することによって行う。被検薬剤等の投与は、注入又は食餌させることによって行うことが好ましい。「注入」とは、強制的に投与することをいい、経口から消化管内への注入、又は、体内への注射が含まれる。体内への注射の方法や注射部位は特に限定はないが、カイコは開放血管系なので、腹脚から体腔内に注射することが特に好ましい。
【0061】
化合物投与と同時に被検薬剤等を投与する方法は、得られた結果の相互比較を行うに際し、投与後の変動要因を少なくすることができる利点がある。しかしながら、被検薬剤等の種類やその投与方法によって、化合物投与から時間をおいて評価する必要がある場合には、個々の事情に応じて被検薬剤等の投与時期を設定すればよい。その場合、その投与時点における肝障害モデル動物のALT活性を確認しておくことが好ましい。
【0062】
被検薬剤等の投与量は、投与する物質、その状態、投与方法等の種々の要因により変動するものと考えられるので、ある程度の試行錯誤が必要である。しかしながら、被検薬剤等と同様の性状を有し、肝障害改善効果のあることが判っている薬剤や食品素材等がある場合には、それらによる結果を参考として投与量を決定する等の方法が好ましい。例えば、下記するNALCと同様の効果が期待される被検薬剤等を試験する場合の投与量は、NALCの場合を参考として、例えば、濃度0.1M〜0.4Mを、50μLが目安となる。
【0063】
被検薬剤等の投与量は、上記の事情があるため特に限定はないが、完全変態型昆虫の幼虫1g当たり、1〜20μmol/gが好ましく、2.5〜10μmol/gが特に好ましい。
【0064】
本発明において、被検薬剤等と比較するための陽性コントロールとして用いる薬剤や食品素材は特に限定はないが、四塩化炭素等の塩素置換炭化水素類による障害が活性酸素によるものであることを考慮すれば、例えば、抗酸化剤であることが好ましく、このうち、N−アセチルL−システイン(「NALC」と略記する)であることが特に好ましい。
【0065】
上記陽性コントロールとしてのNALCの投与量は、通常、四塩化炭素等の塩素置換炭化水素類の投与量に応じて変えなければならないが、2.5〜10μmol/gが、ALT活性の上昇を抑制することが確認されている等の理由で好ましい。上記範囲より多い投与量では、NALC自体による障害が発生し易くなる場合があり、更に多い場合は死亡する場合がある。
【0066】
<4>「肝障害を予防する薬剤又は食品素材のスクリーニング方法」における「肝障害モデル動物に対する被検薬剤等の投与」
本発明の一つの形態は、哺乳類の肝障害を予防する薬剤又は食品素材のスクリーニング方法であって、
(d)被検薬剤等を、完全変態型昆虫の幼虫に注入又は食餌させることによって投与する工程、
(e)(d)工程中又は(d)工程後の完全変態型昆虫の幼虫に化合物を投与することによって、脂肪体等に治療可能な障害を与える工程、
(f)脂肪体等の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法である。
【0067】
被検薬剤等の肝障害予防の効果を評価する場合、被検薬剤等の投与と同時又は被検薬剤等の投与後に、化合物を投与することによって行うことが好ましい。被検薬剤等の投与は、肝障害改善の評価を行う場合と同じく、注入又は食餌させることによって行うことが好ましい。
【0068】
注入させることによる投与の場合は、上記肝障害改善の評価を行う場合に順ずる方法で行えばよい。注入による投与の場合に、被検薬剤等の投与の回数を1回とするか、複数回とするかは、薬剤としての投与か、食品素材としての投与か等、評価の目的等に応じて選択することが好ましい。
【0069】
食餌させることによって投与を行う場合、予め被検薬剤等を混ぜた餌を、被検薬剤等を混ぜない餌と比較して問題なく摂取するかどうかを確認しておくことが好ましい。食餌させることによって投与する方法は、特に、食品素材、食品抽出物、天然物抽出物、タンパク質、繊維質、アミノ酸、ペプチド、無機物等の評価に有用である。
【0070】
被検薬剤等の最終投与後、絶食期間を置いた後に化合物を投与することも特に好ましい。絶食期間は、得られたデータ等に応じて適宜変更すべきであることはいうまでもないが、5〜7時間が好ましい。
【0071】
また、被検薬剤等を食餌によって投与した場合の化合物の投与時期、すなわち被検薬剤等の投与期間は、被検薬剤等投与開始1〜5日(5齢幼虫の期間内)が好ましいが、完全変態型昆虫の幼虫の状態に応じて適宜調整することができる。被検薬剤等の肝障害予防の評価を行う場合、被検薬剤等の投与方法や投与期間、投与量等による効果の表れ方の振れが肝障害改善の評価を行う場合より大きいと考えられるからである。
【0072】
被検薬剤等の肝障害予防の評価を行う場合に関するデータとして、桑の葉を餌として摂食したカイコは、四塩化炭素を投与してもALT活性が全く上昇しなかった(図4参照)。桑の葉はマウスやラット等を用いた検討により肝障害改善効果があることが報告されているので、桑の葉を上記肝障害予防効果の確認としての被検薬剤等と考えた場合、ALT活性が上昇しなかったことは、本発明が、肝障害予防効果を有する被検薬剤等のスクリーニングに用いることができることを示したものと考えることができる。
【0073】
<5>脂肪体等の障害の程度の評価
前記(c)及び上記(f)中の、「脂肪体等の障害の程度を評価する工程」は、完全変態型昆虫の幼虫の、体液中のALT活性の測定、脂肪体等の組織の観察、又は、個体死の判定を含むものである。以下に説明する。
【0074】
(A)ALT活性の測定
<ALT活性測定用試料の調製>
ALT活性測定用試料は、例えば、完全変態型昆虫の幼虫の体液を採取後、過塩素酸等と混合してタンパク質を沈殿・遠心分離することによって調製される。以下、これによって調製された試料を「体液抽出液」と略記する場合がある。
【0075】
<ALT活性の測定方法>
ALT活性の測定は、体液抽出液を検体として、例えば、文献「Methods for the measurement of catalytic concentrations of enzymes. (1980) Clinica. Chimica. Acta. 105, 147-154」に記載されている方法に従って行う。
【0076】
<完全変態型昆虫の幼虫の脂肪体等に発現するALT活性と哺乳類の肝臓に発現するALT活性との相関の検討>
本発明の一形態は、上記肝障害モデル動物を用いることを特徴とする、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法を提供するものである。本発明前までは、カイコにおいて四塩化炭素等による障害付与処理を行った後に、カイコ体液抽出液を検体として、哺乳類の肝臓に特異的に発現するALT活性を評価した例はなかったが、本発明により、カイコにおいても、脂肪体等の障害のマーカーとしてALT活性を用いることができることが明らかとなった。
【0077】
通常状態におけるカイコ体液中のALT活性と脂肪体中のALT活性とを比較したところ、脂肪体中のALT活性は、体液中のALT活性の100倍以上であること(なお、マウスの場合は肝臓中と血中で150倍程度)が判明し、ALTがカイコ脂肪体中に多く存在している酵素であることが確認された。
【0078】
哺乳類の場合、ALTは肝細胞に特異的に存在する酵素であるが、カイコにおいてALTは、前記したように、一般的に肝臓に相当するといわれている脂肪体に多く存在し、また腸管にも存在する。このことは、「カイコにおける脂肪体等の障害とALT活性との関係」が、「哺乳類における肝障害とALT活性との関係」と類似していることを示している。カイコの場合、脂肪体及び/又は腸管(脂肪体等)が、薬物分解等の哺乳類における肝臓に相当する機能を担っている可能性が高いものと考えられる。すなわち、カイコにおけるALT活性は、脂肪体等の障害の程度を反映したものであるが、機能的には哺乳類における肝障害の程度を反映したものであると考えられる。
【0079】
(B)脂肪体等の組織の観察
塩素置換炭化水素類等の化合物や被検薬剤等を投与した完全変態型昆虫の幼虫の脂肪体等は、完全変態型昆虫の幼虫から摘出後に組織切片として脂肪体試料又は腸管試料を調製し、組織における障害の有無や障害の程度を確認する。その際、例えば、ヘマトキシン・エオジン染色法等の染色法を使用することが好ましい。
【0080】
(C)完全変態型昆虫の幼虫の個体死の判定
個体死は弛緩の有無を目視で判定することによって判断する。個体が瀕死か否かの判定も、上記「個体死の判定」に含まれる。
【0081】
上記(c)(f)脂肪体及び/又は腸管の障害の程度を評価する工程における、(A)完全変態型昆虫の幼虫の体液中のALT活性の測定、(B)脂肪体及び/又は腸管の組織の観察、(C)個体死の判定は、陰性コントロール、陽性コントロール、化合物投与群、化合物及び被検薬剤等投与群、被検薬剤等投与群等を対象とする。
【0082】
<6>効果
本発明の肝障害モデル動物は、マウスやラット等のモデル動物では実質的に不可能であった肝障害の改善又は予防効果のある薬剤若しくは食品素材を、多種多様な被検薬剤等から、網羅的・スクリーニング的にピックアップできるとともに、上記薬剤又は食品素材の「吸収」「代謝」「排泄」等の体内動態を反映したin vivoでの効果を反映できる評価系を構築することが可能である。
【0083】
従って、スクリーニングの段階から実用性の高い肝障害の改善又は予防効果のある「薬剤若しくは食品素材」をピックアップすることができるので、上記薬剤や食品素材の開発の効率化と促進を図ることができる。
【実施例】
【0084】
以下に、実施例、試験例を挙げて本発明を更に具体的に説明するが、本発明は、その要旨を超えない限りこれらの実施例に限定されるものではない。
【0085】
実施例1
[肝障害モデル動物の作製と評価]
<カイコの種類・飼育条件>
カイコ(Hu Yo x Tsukuba・Ne)受精卵は、日本農産工業から購入した。27℃に設定したインキュベーター(サンヨー社製)で、桑の葉等を含まない人工餌であるシルクメイト2S(日本農産工業)を与え、5齢まで育てた。飼育容器としては、2齢までは、角型2号シャーレ(栄研器材社製)を用い、それ以降は、使い捨てのプラスチック製フードパック(フードパックFD大深、中央化学株式会社製)を用いた。以下に述べる各検討には、別途記載がない限り、5齢1日目に餌を与えた後、1日経過した(5齢2日目)カイコを用い、投与前、6時間の絶食期間を設けた。また、各検討には、絶食期間後の体重が1.8g〜2.2gの範囲のカイコを選別して用いた。
【0086】
<四塩化炭素の投与によるカイコの脂肪体等への障害付与処理>
上記絶食期間経過後のカイコの第5体節の模様部に、オリーブオイルで10質量%に希釈した四塩化炭素溶液25μLを注射により投与した。同様に、オリーブオイルのみ25μLを注射により投与した。
【0087】
<障害付与処理したカイコのALT活性の測定>
四塩化炭素溶液又はオリーブオイル投与後、1時間、3時間、5時間、24時間、48時間経過後にそれぞれ体液を採取し、10倍量の1%β−MEと混合してタンパク質を沈殿・遠心分離し、ALT活性測定用の体液抽出液とした。
【0088】
<肝障害モデル動物の示すALT活性の経時変化例>
上記ALT活性を測定した結果を図1に示す。四塩化炭素投与によるALT活性(四塩化炭素投与による真のALT活性値。図1中の「△ALT activity」(四塩化炭素のオリーブオイル溶液によるALT活性値からオリーブオイルのみによるALT活性値を引いた値))は、四塩化炭素投与後5時間で上昇し、四塩化炭素投与後5時間から24時間の間は一定値となっていた。また、四塩化炭素投与後48時間でALT活性は、ほぼ四塩化炭素投与時の値まで低下した。
【0089】
このことは、四塩化炭素溶液付与により惹起されたカイコ体内の障害が、哺乳類の肝臓における障害と同様の障害(哺乳類の肝臓と同様の機能を有する部位の障害)であり、少なくとも四塩化炭素投与後5時間から24時間の間、上記障害が与えられたカイコが作製されたことを示している。
【0090】
また、四塩化炭素投与後24時間経過後にはALT活性が低下し、48時間では元の水準に戻っていることから、カイコの上記障害は、治療できない不可逆的な障害ではなく治療可能な障害である。以上より、実施例1で作製された肝障害モデル動物は、哺乳類の肝障害を改善又は予防する効果を示す被検薬剤等(被検薬剤又は被検食品素材)のスクリーニングに適用可能なものであることが確認された。
【0091】
実施例2
[肝障害モデル動物の肝障害改善例1]
(NALCの投与によるALT活性低下の検討)
<N−アセチルL−システイン(NALC)投与例>
上記肝障害モデル動物が実際に哺乳類の肝障害改善又は予防効果を示す被検薬剤等のスクリーニングに適用可能か否かを検討する目的で以下の検討を行った。
【0092】
10質量%の四塩化炭素のオリーブオイル溶液を25μLカイコに注射し、6時間後のALT活性を確認する場合において、四塩化炭素溶液投与と同時に、0.1MのNALCの0.9%NaCl溶液を50μL投与したときに、ALT活性が低下するか否か(ALT活性の上昇が抑制されるか否か)について検討を行った。得られた結果を図2に示す。
【0093】
NALCを投与したカイコのALT活性は、検討した11頭のカイコ全てで低い値を示した。一方、NALCを投与しなかったカイコのALT活性は、11頭のカイコの中で5頭のカイコで高いALT活性を示した。また、高いALT活性を示した5頭のカイコ中3頭は弛緩が見られ個体死が確認された。
【0094】
これより、四塩化炭素による障害が活性酸素によるものであることを考慮すれば、抗酸化剤であるNALCを投与することにより、ALT活性の上昇が抑制されたことは、前記肝障害モデル動物を用いて、哺乳類の肝障害を改善又は予防する「薬剤若しくは食品素材」のスクリーニングができることを示している。
【0095】
実施例3
[肝障害モデル動物の肝障害改善例2]
(桑の葉抽出物の投与によるALT活性低下の検討)
実施例2において、「NALCの0.9%NaCl溶液50μL」に代えて「桑の葉抽出物の水溶液50μL」を用いた以外は、実施例2と同様に評価したところ、ALT活性の上昇が抑制される傾向が認められた(図4の左半分、○で示した人工餌摂取のデータ参照)。すなわち、図4の左から4列目のプロットによると、5例中全例において、ALT活性の上昇の抑制が認められた。
【0096】
すなわち、四塩化炭素投与により障害を与えられたカイコの治療効果が認められた。このことは、前記肝障害モデル動物を用いて、哺乳類の肝障害を改善又は予防する「薬剤若しくは食品素材」のスクリーニングが可能であることを示している。
【0097】
実施例4
[肝障害モデル動物の作製例1]
(四塩化炭素の濃度がALT活性又はその抑制に与える影響の検討)
濃度の異なる2種類の四塩化炭素溶液(15質量%と20質量%)25μLを、それぞれ注射を用いてカイコに投与し、24時間後のALT活性を確認した。四塩化炭素溶液投与と同時に、50μLの0.4MのNALCの0.9%NaCl溶液を投与した場合としない場合とを比較した。得られた結果を図3に示す。
【0098】
図3中の「P(t−test)」は、t検定におけるP−valueであり、帰無仮説を「NALC投与と非投与でALT活性に差がない」としたときの有意確率である。通常、Pが0.05以下なら、帰無仮説は棄却されて両分布(NALC投与と非投与のALT活性値の分布)には有意差があるとされる。15質量%と20質量%の何れも、Pは0.05以下であったことから、NALC投与による効果が認められた。
【0099】
更に詳しく見ると、15質量%四塩化炭素投与群は、検討した7例全てでALT活性は上昇したが、7例全てが一定値まで大きく上昇はしなかった。また、NALC投与によるALT活性の抑制については、ALT活性が7例全てで一定値まで明確に下がっていた。一方、20質量%四塩化炭素投与群は、検討した7例全てでALT活性が一定値まで明確に上昇したが、NALC投与によるALT活性の抑制は、15質量%四塩化炭素投与群に比べてややばらけた結果となった。
【0100】
同様に、5質量%四塩化炭素投与群でも評価した結果、全ての例でALT活性は上昇し、NALC投与によってALT活性が低くなった。しかし、四塩化炭素によるALT活性の上昇度が2.3倍(10質量%の場合は11倍)と小さかった。
【0101】
前記「肝障害モデル動物の肝障害改善例1」の四塩化炭素濃度10質量%でも良好な結果が得られたことも考慮すると、四塩化炭素濃度は、より好ましくは10〜20質量%、特に好ましくは15〜20質量%であることが分かった。また、四塩化炭素の濃度は15質量%と20質量%等、1回の試験につき少なくとも2種類の濃度で検討することが望ましいことが分かった。
【0102】
実施例5
[肝障害モデル動物の作製例2]
(桑の葉等の食餌の肝障害モデル動物に与える影響の検討)
実施例3において、桑の葉等(桑の葉又は桑の葉抽出物)を注射によって投与したカイコに四塩化炭素投与により障害を与えた場合、ALT活性の上昇が抑制される傾向が認められた。そこで改めて、桑の葉等が肝障害モデル動物の作製に与える影響について以下の検討を行った。
【0103】
<肝障害モデル動物の作製条件>
桑の葉等を含まない人工餌を与えた前記カイコ(以下、「人工餌摂食カイコ」と略記する)及び桑の葉を与えたカイコ(以下、「桑の葉摂食カイコ」と略記する)に、10質量%の四塩化炭素のオリーブオイル溶液を25μL注射し、24時間後のALT活性を測定した。
【0104】
0.1MのNALCオリーブオイル溶液50μLを、四塩化炭素投与と同時に投与したものを肝障害改善又は予防効果の陽性対照とした。また、オリーブオイルのみを注射したものを陰性対照とした。
【0105】
<桑の葉抽出物の投与>
桑の葉抽出物の水溶液50μLを、10質量%の四塩化炭素のオリーブオイル溶液25μLの注射と同時に注射した。
【0106】
人工餌摂食カイコは、実施例1とほぼ同様の結果を示した。すなわち、10質量%の四塩化炭素投与により、7例中4例において、ALT活性の上昇が認められた。また、陽性対照である0.1MのNALCの投与により、7例中全例において、ALT活性の上昇の抑制が認められた。また、桑の葉抽出物を投与した場合でも、5例中全例において、ALT活性の上昇の抑制が認められた(図4の○プロット参照)。
【0107】
10質量%の四塩化炭素投与前に桑の葉を食餌によって摂取されたカイコ(桑の葉摂食カイコ)は、24時間経過後に四塩化炭素を投与しても、6例全例において、ALT活性の明確な上昇は認められなかった。NALC投与群、桑の葉抽出物投与群も同様であった。従って、桑の葉摂食カイコを被検薬剤等の肝障害改善又は予防効果の評価に用いることは実質的にできないことが明らかとなった。
【0108】
通常、カイコの餌には桑の葉を含む餌が用いられるが、そのような餌を摂取したカイコを、肝障害改善効果や肝障害予防効果を有する被検薬剤等のスクリーニングのための肝障害モデル動物として用いることは好ましくないことが確認された。このことはカイコを用いて肝障害モデル動物を作製し、それによって肝障害改善効果や肝障害予防効果を有する被検薬剤等のスクリーニング方法を構築する上で非常に重要なポイントであり、本発明によって新たに見出されたことである。
【産業上の利用可能性】
【0109】
本発明の肝障害モデル動物は、従来の肝障害モデル動物では不可能であった被検薬剤等のスクリーニング段階でのin vivoでの効果を反映できる評価系を構築できるため、従来に比して非常に効率的に肝障害改善効果や肝障害予防効果を有する薬剤又は食品素材の研究開発を行うことができる。また、従来の方法ではピックアップできなかった「in vitroで効果が弱く、in vivoで有効な効果を発揮する薬剤又は食品素材」をピックアップすることが可能なため、これまでにない新たな肝障害改善・予防効果を有する「薬剤若しくは食品素材」を見出すために利用することが可能である。そのため、薬剤や食品素材の検討に広く利用されるものである。
【図面の簡単な説明】
【0110】
【図1】本発明の肝障害モデル動物におけるALT活性の経時変化の一例を示す図である。
【図2】本発明の肝障害モデル動物において、NALC投与によるALT活性の上昇の抑制を示す図である。
【図3】ALT活性の上昇、NALC投与によるALT活性の上昇の抑制の程度が、化合物(四塩化炭素)の濃度によってどれだけ影響を受けるかを検討した結果を示す図である。
【図4】本発明の肝障害モデル動物において、桑の葉抽出物投与によるALT活性の上昇の抑制を示す図であり、また、カイコに人工餌を摂取させた場合と桑の葉を摂取させた場合とについて、ALT活性の上昇とその抑制の程度を検討した結果を示す図である。
【特許請求の範囲】
【請求項1】
完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その脂肪体及び/又は腸管に治療可能な障害が与えられているものであることを特徴とする肝障害モデル動物。
【請求項2】
上記完全変態型昆虫の幼虫が、実質的に無毛であり、定量的な化合物の投与を可能とする大きさを有するものである請求項1記載の肝障害モデル動物。
【請求項3】
上記完全変態型昆虫の幼虫が、桑の葉又は桑の葉抽出物を実質的に含まない餌で育てたカイコである請求項1又は請求項2に記載の肝障害モデル動物。
【請求項4】
上記脂肪体及び/又は腸管に治療可能な障害を与える化合物が、塩素置換炭化水素類である請求項1ないし請求項3の何れかの請求項に記載の肝障害モデル動物。
【請求項5】
桑の葉又は桑の葉抽出物を実質的に含まない餌で育てたカイコの幼虫に、その脂肪体及び/又は腸管に治療可能な障害を与える化合物を投与する工程を含むことを特徴とする肝障害モデル動物の作製方法。
【請求項6】
脂肪体及び/又は腸管に治療可能な障害を与える化合物が塩素置換炭化水素類である請求項5に記載の肝障害モデル動物の作製方法。
【請求項7】
請求項1ないし請求項4の何れかの請求項に記載の肝障害モデル動物を用いることを特徴とする、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法。
【請求項8】
哺乳類の肝障害を改善する薬剤又は食品素材のスクリーニング方法であって、
(a)完全変態型昆虫の幼虫に化合物を投与することによって、その脂肪体及び/又は腸管に治療可能な障害を与える工程、
(b)(a)工程中又は(a)工程後の完全変態型昆虫の幼虫に、被検薬剤又は被検食品素材を、注入又は食餌させることによって投与する工程、
(c)脂肪体及び/又は腸管の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法。
【請求項9】
哺乳類の肝障害を予防する薬剤又は食品素材のスクリーニング方法であって、
(d)被検薬剤又は被検食品素材を、完全変態型昆虫の幼虫に注入又は食餌させることによって投与する工程、
(e)(d)工程中又は(d)工程後の完全変態型昆虫の幼虫に化合物を投与することによって、脂肪体及び/又は腸管に治療可能な障害を与える工程、
(f)脂肪体及び/又は腸管の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法。
【請求項10】
上記完全変態型昆虫の幼虫が、実質的に無毛であり、定量的な化合物の投与を可能とする大きさを有するものである請求項8又は請求項9に記載のスクリーニング方法。
【請求項11】
上記完全変態型昆虫の幼虫が、桑の葉又は桑の葉抽出物を実質的に含まない餌で育てたカイコである請求項8ないし請求項10の何れかの請求項に記載のスクリーニング方法。
【請求項12】
上記脂肪体及び/又は腸管に治療可能な障害を与える化合物が、塩素置換炭化水素類である請求項8ないし請求項11の何れかの請求項に記載のスクリーニング方法。
【請求項13】
上記(c)(f)脂肪体及び/又は腸管の障害の程度を評価する工程が、体液中のアラニン・アミノトランスフェラーゼ(ALT)活性の測定、脂肪体及び/又は腸管の組織の観察、又は、個体死の判定を含むものである請求項8ないし請求項12の何れかの請求項に記載のスクリーニング方法。
【請求項1】
完全変態型昆虫の幼虫であって、化合物を投与されたことによって、その脂肪体及び/又は腸管に治療可能な障害が与えられているものであることを特徴とする肝障害モデル動物。
【請求項2】
上記完全変態型昆虫の幼虫が、実質的に無毛であり、定量的な化合物の投与を可能とする大きさを有するものである請求項1記載の肝障害モデル動物。
【請求項3】
上記完全変態型昆虫の幼虫が、桑の葉又は桑の葉抽出物を実質的に含まない餌で育てたカイコである請求項1又は請求項2に記載の肝障害モデル動物。
【請求項4】
上記脂肪体及び/又は腸管に治療可能な障害を与える化合物が、塩素置換炭化水素類である請求項1ないし請求項3の何れかの請求項に記載の肝障害モデル動物。
【請求項5】
桑の葉又は桑の葉抽出物を実質的に含まない餌で育てたカイコの幼虫に、その脂肪体及び/又は腸管に治療可能な障害を与える化合物を投与する工程を含むことを特徴とする肝障害モデル動物の作製方法。
【請求項6】
脂肪体及び/又は腸管に治療可能な障害を与える化合物が塩素置換炭化水素類である請求項5に記載の肝障害モデル動物の作製方法。
【請求項7】
請求項1ないし請求項4の何れかの請求項に記載の肝障害モデル動物を用いることを特徴とする、哺乳類の肝障害を改善又は予防する、薬剤若しくは食品素材のスクリーニング方法。
【請求項8】
哺乳類の肝障害を改善する薬剤又は食品素材のスクリーニング方法であって、
(a)完全変態型昆虫の幼虫に化合物を投与することによって、その脂肪体及び/又は腸管に治療可能な障害を与える工程、
(b)(a)工程中又は(a)工程後の完全変態型昆虫の幼虫に、被検薬剤又は被検食品素材を、注入又は食餌させることによって投与する工程、
(c)脂肪体及び/又は腸管の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法。
【請求項9】
哺乳類の肝障害を予防する薬剤又は食品素材のスクリーニング方法であって、
(d)被検薬剤又は被検食品素材を、完全変態型昆虫の幼虫に注入又は食餌させることによって投与する工程、
(e)(d)工程中又は(d)工程後の完全変態型昆虫の幼虫に化合物を投与することによって、脂肪体及び/又は腸管に治療可能な障害を与える工程、
(f)脂肪体及び/又は腸管の障害の程度を評価する工程、
を有することを特徴とするスクリーニング方法。
【請求項10】
上記完全変態型昆虫の幼虫が、実質的に無毛であり、定量的な化合物の投与を可能とする大きさを有するものである請求項8又は請求項9に記載のスクリーニング方法。
【請求項11】
上記完全変態型昆虫の幼虫が、桑の葉又は桑の葉抽出物を実質的に含まない餌で育てたカイコである請求項8ないし請求項10の何れかの請求項に記載のスクリーニング方法。
【請求項12】
上記脂肪体及び/又は腸管に治療可能な障害を与える化合物が、塩素置換炭化水素類である請求項8ないし請求項11の何れかの請求項に記載のスクリーニング方法。
【請求項13】
上記(c)(f)脂肪体及び/又は腸管の障害の程度を評価する工程が、体液中のアラニン・アミノトランスフェラーゼ(ALT)活性の測定、脂肪体及び/又は腸管の組織の観察、又は、個体死の判定を含むものである請求項8ないし請求項12の何れかの請求項に記載のスクリーニング方法。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2010−75096(P2010−75096A)
【公開日】平成22年4月8日(2010.4.8)
【国際特許分類】
【出願番号】特願2008−246986(P2008−246986)
【出願日】平成20年9月25日(2008.9.25)
【出願人】(501481492)株式会社ゲノム創薬研究所 (25)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【Fターム(参考)】
【公開日】平成22年4月8日(2010.4.8)
【国際特許分類】
【出願日】平成20年9月25日(2008.9.25)
【出願人】(501481492)株式会社ゲノム創薬研究所 (25)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【Fターム(参考)】
[ Back to top ]

