脂肪滴・セルライト抑制装置および脂質抑制効果増強薬、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC製剤
【課題】プロビタミンC剤と高周波温熱装置を組み合わせることにより、脂肪滴抑制効果・セルライト抑制の大幅な向上を可能ならしめるとともに温熱による細胞死の最小限の抑制を図り、かつ被施術者にとって温熱による苦痛を感じることが無く穏やかな温熱処理を行うことができる脂肪滴・セルライト抑制装置を提供するとともに、脂質抑制効果増強薬を提供する。
【解決手段】 セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱向けの上記プロビタミンC剤および/またはビタミンCを含有することを特徴とする脂質抑制効果増強薬である。
【解決手段】 セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱向けの上記プロビタミンC剤および/またはビタミンCを含有することを特徴とする脂質抑制効果増強薬である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は高周波温熱による細胞死の最小限抑制、好ましくは97%以上の細胞生存率をもたらす安全性の高いセルライト/脂質代謝の改善を図ることができる脂肪滴・セルライト抑制装置およびに脂質抑制効果増強薬、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC製剤に関する。
【背景技術】
【0002】
従来、脂肪滴に係わる組織や細胞の好ましくない発現とその影響を抑制することのできる新しい組成物とその薬剤に関するものが知られている。
【先行技術文献】
【特許文献】
【0003】
従来、脂肪滴形成抑制剤として、水酸化フラーレン類および有機化合物により修飾もしくは包接されたフラーレン複合体のうち1種以上を有効成分として含有していることを特徴とする脂肪滴形成抑制剤(請求項1)の発明がある(特許文献1:特開2008−222645)。
同文献1には、請求項2以下に次の通り記載されている。水酸化フラーレン類は、水酸基を1分子当り30以上40以下で結合しているフラーレンまたはその誘導体であることを特徴とする請求項1に記載の脂肪滴形成抑制剤(請求項2)。フラーレン複合体は、フラーレンおよびフラーレン誘導体のうちの1種以上と、有機オリゴマー、有機ポリマー、シクロデキストリンおよびクラウンエーテルとその類縁化合物のうちの1種以上の有機化合物との複合体であることを特徴とする請求項1に記載の脂肪滴形成抑制剤(請求項3)。γ−シクロデキストリンにより1.5〜2.0mol/mol比で包接されているフラーレン複合体であることを特徴とする請求項3に記載の脂肪滴形成抑制剤(請求項4)。請求項1から4のうちのいずれかの抑制剤からなることを特徴とする脂肪滴由来の細胞傷害の防御剤(請求項5)。請求項1から4のうちのいずれかの抑制剤からなることを特徴とする脂肪細胞分化抑制剤(請求項6)。
【0004】
【特許文献1】特開2008−222645公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
上記特許文献1は、従来のレチノイドに代わり得る高活性の脂肪滴形成の抑制が実現され、これによって、脂肪滴由来の細胞傷害の発生が効果的に防御され、脂肪細胞そのものの分化が抑制されることになる旨の記載がされ、スキンケア、化粧品、皮膚活性剤等として有用である旨の記載がされている。
しかし、脂肪滴形成抑制剤を配合したスキンケア、化粧品等が市販されたとしてもこれだけでは脂肪滴形成抑制やセルライト抑制に十分な効果が期待できるものであるとは言えない。
【0006】
また、従来の高周波温熱機器では、被施術者が温熱に耐えられる範囲での高い温度設定をすることでより温熱効果が得られるとされていたが被施術者にとっては温熱による苦痛は避けがたいものであった。
【0007】
さらに、温熱が脂肪滴・セルライト(皮膚表面凸凹脂肪塊)を抑制するらしいことは、従来は経験的に漠然と知られているに過ぎなかったが、その具体的な温熱条件も解明されてこなかったし、その解明のために人体それ自体で解析することは、統計学的に充分に多数の症例数を確保することも困難な上に、対照群と試験群との間で人体特性条件を同一に揃えることも容易ではなく、さらに、その人体においてセルライトや脂肪滴の増減を解析することも精度と感度の観点から困難であった。
【0008】
本発明は上記の点に鑑みてなされたもので、その目的とするところは、プロビタミンC剤(体内に吸収された後、化学変化を起こしてビタミンCになるものをいう。前駆体ともいう。)と高周波温熱装置を組み合わせることにより、脂肪滴抑制効果・セルライト抑制の大幅な向上を可能ならしめるとともに温熱による細胞死の最小限の抑制を図り、かつ被施術者にとって温熱による苦痛を感じることが無く穏やかな温熱処理を行うことができる脂肪滴・セルライト抑制装置および脂質抑制効果増強薬、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC製剤を提供することにある。
【課題を解決するための手段】
【0009】
本発明に係る脂肪滴・セルライト抑制装置は、プロビタミンC剤の標的体部への投与手段と、被施術部位に当接するためのエレクトロードと、該エレクトロードに当接する被施術対象体の背後に設置する戻し電極であるレジスティブを備え、かつ0.45MHzの高周波の下で、温度37〜41℃の範囲の温度調節部を備えるとともに1回当たりの温熱処理時間を1分〜30分に設定する温熱処理時間調節部を備え、合計で6時間〜1週間のインターバルを置いた温熱投与手段を備えたことを特徴とする。
【0010】
上記プロビタミンC剤は、アスコルビン酸−2−0−フォスフェート・アスコルビン酸−2−0−α−D−グルコシド・アスコルビン酸−2−0−フォスフェート−6−0−パルミチン酸エステル・アスコルビン酸−2−0−フォスフェート−6−0−(2−ヘキシルデカン酸)エステル・アスコルビン酸−2,3,5,6−0−(2’−ヘキシルデカン酸)テトラエステル、アスコルビン酸−6−0−パルミチン酸エステル、アスコルビン酸−6−0−ステアリン酸エステルからなる群から選ばれた一つまたは二つ以上を用いることを特徴とする。
【0011】
本発明に係る脂肪抑制効果増強薬は、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱向けの上記プロビタミンC剤および/またはビタミンCを含有することを特徴とする。特に、ビタミンCの場合にあっては、水素添加大豆レシチン・コレステロールから構成され、超音波装置・エクストルーダから調整されたリポソームによってアスコルビン酸のまま包含する皮膚浸透性が増強されたビタミンCであることを特徴とする。
【0012】
本発明に係るセルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC剤および/ビタミンC製剤は、上記プロビタミンC剤および/またはビタミンCを温熱処理においても分解せずに保持させる温熱安定化剤を含有することを特徴とする。
【0013】
本発明に係るセルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向け上記プロビタミンC剤および/ビタミンC製剤は、温熱安定化剤として、マニトール、コーンスターチ、キチン・キトサンからなる群から選ばれた一つ以上の物質を含有することを特徴とする。
【発明の効果】
【0014】
温熱が脂肪滴・セルライト(皮膚表面凸凹脂肪塊)を抑制するらしいことは、従来は経験的に漠然と知られているに過ぎなかったが、その具体的な温熱条件も解明されてこなかったし、その解明のために人体それ自体で解析することは、統計学的に充分に多数の症例数を確保することも困難な上に、対照群と試験群との間で人体特性条件を同一に揃えることも容易ではなく、さらに、その人体においてセルライトや脂肪滴の増減を解析することも精度と感度の観点から困難であった。
【0015】
本発明は、脂肪滴やセルライトの形成に関する中心的役割を果たす前駆脂肪細胞および/または脂肪細胞を用い、さらには、これら前駆脂肪細胞および/または脂肪細胞を組み込んだ3次元ヒト皮膚組織モデル、加えて、ヒト皮膚摘出組織片、および、ユカタン産ミニ豚皮膚摘出組織片などを用いて、各々、同一の皮膚特性条件の下に、試験群と比較対照群を操作し、統計学的に充分に多数の適用例を解析して、脂肪滴とセルライトを抑制する最適条件を求めた上で、その範囲前後に絞って臨床上の最適条件を求めた。
【0016】
その結果、温熱処理装置の単独使用よりも、温熱に加えて、各種プロビタミンC剤を併用したことにより、相乗効果として、脂肪滴とセルライトの抑制が顕著になることが判明した。
また、温熱を一定期間のインターバルを置いて温熱処理する手段と、各温熱処理手段の適用に際して本発明で見いだした特定プロビタミンC剤を特定濃度で標的体部に投与する併用手段が脂肪滴・セルライト抑制に著効を示すことが本発明によって見いだされた。
【0017】
さらに、本発明に係る脂肪抑制効果増強薬は、上記プロビタミンC剤および/またはビタミンCを含有するので、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱向け治療に有効に機能することとなる。
【0018】
さらにまた、本発明に係るセルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC剤および/ビタミンC製剤は、上記プロビタミンC剤および/またはビタミンCを温熱処理においても分解せずに保持させる温熱安定化剤として寄与することができる。
【0019】
そして、本発明の上記プロビタミンC剤および/ビタミンC製剤は、温熱安定化剤として、マニトール、コーンスターチ、キチン・キトサンからなる群から選ばれた一つ以上の物質を含有することによりセルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けとして好適である。
【図面の簡単な説明】
【0020】
【図1】ユカタン産ミニ豚皮膚摘出組織片を用いてプロビタミンC剤と高周波温熱装置の併用による脂肪滴・セルライト抑制装置を示す斜視図である。
【図2】図1のプロビタミンC剤を投与した試験片A、B、Cに本発明に係る温熱処理装置を用いて41℃の温度条件下で5分間、高周波温熱を投与した場合を示す状態図である。
【図3】APS投与量に対する脂肪滴蓄積量の変化を示す状態図である。
【図4】脂肪滴の顕微鏡写真で、左上写真はプロビタミンC剤及び温熱処理装置を無投与の場合を示し、右上写真は0.03%濃度のAPSのみを投与した場合を示し、左下写真はAPSは無投与で温熱処理装置のみを適用した場合を示し、右下写真は0.03%濃度のAPS及び温熱処理装置を適用した場合の脂肪滴の状態を示す。
【図5】30,000個の細胞群を2日放置後、APS投与と温熱処理装置を適用し、6時間後に温熱処理装置のみを適用し、18時間後にAPS投与と温熱処理装置を適用する操作を繰り返して、顕微鏡写真撮影の条件とした説明図である。
【図6】脂肪滴蓄積量の相対比を示す顕微鏡写真である。
【図7】図8の顕微鏡写真を撮影するための試験片の顕微鏡写真撮影の条件とした説明図である。
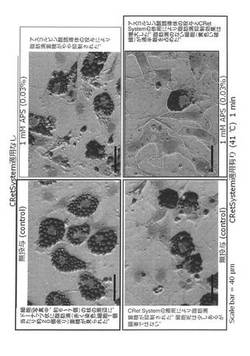
【図8】0.03%濃度のAPSを投与せず温熱処理装置の適用もしない場合及びいずれか一方を採用した場合及び併用した場合の脂肪滴の状態を示す顕微鏡写真である。
【図9】キャパシティブエレクトリックトランスファーシステムの電流の動きを示す説明図である。
【図10】非対称電極間で加えられたエネルギー分配を示す説明図である。
【図11】MD530のインディバCRet Systemの背面図である。
【図12】MD530のインディバCRet Systemの正面図である。
【図13】MD530のインディバCRet System前面に表示されるコントロール類の表示部の説明図である。
【発明を実施するための形態】
【実施例1】
【0021】
脂肪細胞/前駆脂肪細胞での脂肪滴・セルライト抑制と細胞死防御についてについて実施した。
間葉系前駆脂肪細胞OP9を培養し通常培地からインスリン含有KSR培地に置換すると、脂肪細胞への分化が開始されるが、この時に本発明のCapacitive−Resistive Electric−Transfer装置((株)インディバ・ジャパン製品:MD530) (CRet System )の身体温熱装置を使用してLevel 5, Indicator 5, 20 secに該当する電気特性を設定した。室温26.5℃から41℃にシフトアップするが、その後に、同装置のLevel 2〜3に設定した。脂肪細胞は41℃で1 min保持した。この時に、プロビタミンC剤としてアスコルビン酸−2−O−フォスフェート ナトリウム塩(APS) を1 mM (300 ppm, 0.03wt%)の濃度で投与して一日12時間おきに2回反復して3日間実施する試験区と無投与の比較対照区とを比較した。
細胞内の脂肪滴は、オイルレッドオー色素で染色した後に10%メタノール水溶液でリンスしてリンス廃液が530 nmでの吸光度がゼロと成る3〜5回まで徹底的にリンスして、細胞外や細胞表面のオイルレッドオー色素を消滅させた後に、位相差顕微鏡で撮影すると共に、細胞内のオイルレッドオー色素を抽出して530 nmで吸光プレ−トリーダーと分光光度計で細胞内脂肪滴を定量した。細胞死と細胞生存は、各々、プロピジウムヨーダイドとカルセインアミノメトキシエステルで染色し、その蛍光度を蛍光プレートリーダーで評価した。
【0022】
本発明で使用するMD530は0.45MHzの高周波温熱機器であり、施術箇所への循環を通じて人体細胞の深部加温を行う。キャパシティブ用エレクトロードとレジスティブ用エレクトロードを使用し、深部加温を行う。キャパシティブモードを採用する場合、ステンレス製のエレクロロードの円形盤の表面は人の肌に直接触れないようにプラスチックで表面をコーティングしている。エレクトロードは、細胞に高周波エネルギーを透過するコンデンサーの役割をし、施術部位を加温する。透過された高周波エネルギーは、板型戻し電極に向って透過される。他方、レジスティブモードでは、直接、施術箇所に置かれたRES用エレクトロード(ステンレス製)を通して人体細胞へ高周波電流を流す。この電流は戻し電極に電導する。高周波エネルギーが細胞内に透過されたとき、細胞が抵抗体となり組織の温度を集中的に上昇させ、深部加温が行われる。本機器では、被施術者に流れる電流の強さ、被施術者に加えられる皮相電力(キャパシティブモード)、アクティブパワー(レジスティブモード)及びエレクトロードと被施術者の抵抗を測定し、モニタリングができる。
【0023】
図11はMD530のインディバCRet Systemの背面図で、1は電源スイッチ、2はヒューズホルダー、3は電源ソケット、4はアース用ジャック、5は冷却ファン、6は仕様ラベルをそれぞれ示す。図12はMD530の正面図で、7はLCD画面、8はキーパッド、9はキャパシティブ用出力、10は戻し電極用出力、11はレジスティブ用出力をそれぞれ示す。図13はMD530の前面に表示されるコントロール類の表示部の説明図で、12はスタンバイインジケータランプ、13はON/OFFキー、14はメニューキー、15はキャパシティブモードキー、レジスティブモードキー、17はリセットキー、18はスタート/ストップキー、19は時間増キー、時間減キー、21は出力増/減ダイヤルノブをそれぞれ示す。
【0024】
キャパシティブモードの出力に対するインピーダンスは、皮膚組織上に置かれたエレクトロードのインピーダンス(1,000オーム)に相応するように計算されている。この方法により多容量のエネルギーの透過を実現できる。エレクトロードを通じての組織への循環高周波エネルギーの行方は、図9に示す。MD530からのエネルギーは、金属軸Aを通してBの先端(エレクトロードの最下部)へ伝わる。そのエネルギーは,Cの絶縁体部分により組織と隔てられるため低下し、エレクトロード全表面、容量的に組織に伝達される。組織Dは、合計で1,000オームとなる複数の無限大の抵抗を定着させ、そのコンデンサーの性質により第二のプレートのような働きをする。図9の点線Eが第二のプレートとして定義され、コンデンサーとしての働きがなされる。1,000オーム相当の抵抗は、実際はB点とE点の間で発生し、その部分で温度上昇が起こり、その強深度は、本機器のパワー(レベル調整に対応)・エレクトロードの大きさ・施術部位の組織の特質・施術時間により決まる。特に本発明では、被施術者が被施術者にとって温熱による苦痛を感じることが無く穏やかな温熱処理、すなわち37〜41℃の範囲の温度設定により温熱処理を行うことができる点にある。
【0025】
上記の条件下において、その結果を以下に示す。
(1)脂肪細胞への分化誘導処理によって、細胞の核の周辺に、ドーナッツ状に脂肪滴(赤く染色;細胞1個当たり約20個余り)蓄積が見られた。細胞生存率は99.3±0.4%だった。
(2)41℃でのCRet温熱装置は、プロビタミンC剤なしでも脂肪滴蓄積量を22%減少した。CRet System温熱装置の適用により脂肪滴蓄積が抑制された。細胞死は0.8±0.2%と少しあるが顕著ではなかった。
【0026】
(3)プロビタミンC剤(アスコルビン酸誘導体)APS(アスコルビン酸−2−O−フォスフェート ナトリウム塩)の300 ppm (0.03wt%, 1 mM)の濃度での上記温熱装置を適用しない場合での37℃での投与は、細胞核の周辺に脂肪滴蓄積が見られたが、脂肪滴蓄積を20%抑制した。APSまたはCRet温熱装置(1 min)適用による細胞死は0.1±0.0%と少し見られたが、無視しうるレベルであった。
【0027】
(4)APSの300 ppm投与とCRet System温熱装置の併用は、脂肪滴蓄積を54%抑制した。アスコルビン酸誘導体APSの投与とCRet System温熱装置の併用により脂肪滴抑制効果は大幅に増大した。脂肪滴のない細胞が過半数を占めた。細胞核の周辺に脂肪滴が蓄積されたが、APS投与で細胞全体に脂肪滴蓄積が抑制され、この抑制は、CRet System温熱装置の併用で一層増大した。細胞生存率は99.0±0.6%を維持した。APSから変換されたビタミンCが脂肪燃焼促進剤カルニチンを合成する酵素トリメチルリシン ジオキゲナーゼ&γ−ブチロベタイン ジオキシゲナーゼを促進すると共に、CRet System温熱装置による脂肪滴流動化&分散化が奏功したことを示唆するものである。
【0028】
(5)従来法として、通常の身体温熱装置で42,43,44,45℃の温度4点で各々60分間の処理による温熱単独を行なう比較対照例を試験した結果、脂肪滴抑制は、各温度で、8.9,11.6,10.4,5.2%の抑制であり、細胞死が各々、18.1±4.7,27.0±5.9,41.3±11.0,61.8±5.5%だった。過酷な温熱装置の単独使用は細胞傷害と細胞生存の指標であるサクシネートデヒドロゲナーゼを主体とするミトコンドリア脱水素酵素の活性低下をもたらすと共に、透過型電子顕微鏡による細胞形態では、活発な細胞代謝の指標となるマイクロビラスの消失、細胞膜の破綻、シュリンキッジ(細胞萎縮)、ピクノーシス(核凝縮)、カリオレキシス(核断片化)が認められた。これらは従来の過酷な温熱装置の適用が細胞死を広範囲に惹起させるという犠牲の下に施行されていた可能性を示唆するものである。
【実施例2】
【0029】
前駆脂肪細胞を組み込んだ3次元ヒト皮膚組織モデルでの脂肪滴・セルライト抑制と細胞死防御について実施した。
ヒト皮膚繊維芽細胞OUMS−36を含むI型コラーゲンから構成される真皮、その上にIV型コラーゲン・ラミニン・エンタクチン・フィブロネクチンを含有するマトリゲルから構成される基底膜、さらにその上に、間葉系前駆脂肪細胞OP9を添加することを特徴とし、その上に、ヒト皮膚角化細胞HaCaTから構成される表皮を各々重層し、最後にエアーリフトによって角層を形成させて取得される脂肪滴形成量評価向けの3次元ヒト皮膚組織モデルを作製し、実施例1と同様な試験を行ない、脂肪滴・セルライト抑制と細胞死防御を評価し、併せて、皮膚組織片をクライオスタットで4μm厚の超薄切片を調製してオイルレッドオー色素で脂肪滴を染色した皮膚組織の断面構造において、断面積に占める脂肪滴の面積の割合をNIH−ImageとImage−Jソフトウェアで解析した。細胞死レベルはヘマトキシリンーエオシン染色によって、変質細胞の細胞総数に占める比率から、評価した。さらに、皮膚表面の凹凸形状も走査型電子顕微鏡で撮影した。皮膚表面の凹凸形状はシリコーンゴムを用いたレプリカを作製して凸凹度をラインヒストグラム化してセルライト度を評価した。
【0030】
この結果、比較例として、41℃でのCRet System温熱装置の単独適用(常温からのシフトアップ34sec、設定温度到達後の温度平行時間5min、常温へ低下するシフトダウン3min14sec:以下、これらを単に「5min適用」と呼ぶ)は、プロビタミンC剤なしでも脂肪滴蓄積量を22.4±3.7%減少させた。CRet System温熱装置の単独適用による脂肪滴蓄積抑制効果が有意に示された。
もう一つの比較例として、プロビタミンC剤(アスコルビン酸誘導体)APS(アスコルビン酸−2−O−フォスフェート ナトリウム塩)の300ppm(0.03wt%)の濃度での上記温熱装置を適用しない場合での37℃での投与は、細胞核の周辺に脂肪滴蓄積が見られたが、脂肪滴蓄積を16.1±2.9%抑制した。APS単独投与またはCRet System温熱装置(5min適用)単独適用による細胞死は各々0.1±0.0%、2.2±0.3%と無視しうるレベルまたは僅少レベルであった。
【0031】
一方、本発明では、APSの300 ppm投与とCRet System温熱装置の併用、または、温熱安定化剤としてマニトール500ppm、コーンスターチ800ppm、イカ筋(中骨)キトサン(キトサン成分83〜97%、キチン成分3〜17%;β型キチンを出発材料にして脱アセチル反応などの処理で調製したキチン・キトサン)350ppmを添加したAPSの300ppm投与とCRet System温熱装置の併用、は、脂肪滴蓄積を54.7±4.6%、または、73.3±5.8%抑制した。アスコルビン酸誘導体APSの投与とCRet温熱装置(5min適用)の併用により脂肪滴抑制効果は増大し、さらに、温熱安定化剤の添加によってこの効果が促進された。これら本発明例ではいずれも脂肪滴のほぼ検出されない細胞が過半数を占めた。細胞核の周辺に脂肪滴が蓄積されたが、APS投与で細胞全体に脂肪滴蓄積が抑制され、この抑制は、CRet System温熱装置の併用で一層増大し、さらに温熱安定化剤によって顕著になったことになる。細胞死率も各々0.3±0.0%と0.2±0.0%と無視しうるレベルだった。
【実施例3】
【0032】
改変ブロノフ拡散チェンバーに組み込んだインフォームドコンセントを提出した48歳の日本人女性の耳后下の皮膚摘出組織片での脂肪滴・セルライト抑制と細胞死防御について実施例2と同様に実施した。
脂肪滴抑制試験の終了後に当該チェンバーより単離した皮膚組織片をクライオスタットで4μm厚の超薄切片を調製し、実施例2と同様に脂肪滴・セルライト抑制と細胞死防御を評価した。
【0033】
この結果、比較例として、41℃でのCRet System温熱装置の単独適用(常温からのシフトアップ33sec、設定温度到達後の温度平行時間5min、常温へ低下するシフトダウン3min27sec:以下、これらを単に「5min適用」と呼ぶ)は、プロビタミンC剤なしでも脂肪滴蓄積量を19.1±2.9%減少させた。CRet温熱装置の単独適用による脂肪滴蓄積抑制効果が有意に示された。
もう一つの比較例として、プロビタミンC剤(アスコルビン酸誘導体)APS(アスコルビン酸−2−O−フォスフェートナトリウム塩)の300ppm(0.03wt%)の濃度での上記温熱装置を適用しない場合での37℃での投与は、細胞核の周辺に脂肪滴蓄積が見られたが、脂肪滴蓄積を12.0±3.5%抑制した。APS投与またはAPSなしのCRet System温熱装置(5min適用)単独適用による細胞死は各々2.0±0.4%または6.9±0.8%と無視しうるレベルまたは僅少レベルであった。
【0034】
一方、本発明では、APSの300ppm投与とCRet System温熱装置の併用、または、温熱安定化剤としてマニトール500ppm、コーンスターチ800ppm、イカ筋(中骨)キトサン(キトサン成分83〜97%、キチン成分3〜17%;β型キチンを出発材料にして脱アセチル反応などの処理で調製したキチン・キトサン)350ppmを添加したAPSの300ppm投与とCRet System温熱装置の併用は、各々54.8±12.6%または70.4±6.3%脂肪滴蓄積を抑制した。脂肪滴抑制効果はプロビタミンCのAPSの投与とCRet System温熱装置(5min適用)の併用により明確となり、さらに温熱安定化剤を併用すると脂肪滴抑制効果は顕著になった。脂肪滴のほぼ検出されない細胞が過半数を占めた。細胞核の周辺に脂肪滴が蓄積されたが、APS投与で細胞全体に脂肪滴蓄積が抑制され、この抑制は、CRet System温熱装置の併用で一層増大したことになり温熱安定化剤による促進効果も認められた。細胞死率も各々1.1±0.2%または1.7±0.2%と無視しうるレベルだった。
【実施例4】
【0035】
臨床試験での脂肪塊・セルライトはインフォームドコンセントを得た健康な26〜56歳の日本人女性24名をあらかじめ大腿最太部後側と臀部最厚部先端での皮下脂肪率をMRIで評価し、当該部の皮膚表面形状は、セルライト皮表凹凸度として、スキンキャスト皮表形状レプリカ法で評価した。
この試験前の皮下脂肪率とセルライト皮表度および平均年齢に偏りがないように24名を8名ずつ3群に分けて、毎週3回、各回、A群は、温熱安定化剤なしのAPS300ppmを太腿と臀部に1mL/cm2で塗布しCRet System温熱装置を各々10分間と15分間適用し、本発明のB群は、温熱安定化剤としてマニトール500ppm、コーンスターチ800ppm、イカ筋(中骨)キトサン(キトサン成分83〜97%、キチン成分3〜17%;β型キチンを出発材料にして脱アセチル反応などの処理で調製したキチン・キトサン)350ppmを添加したAPS300ppmを同様に塗布してCRet Systemも同様に適用し、比較対照のC群は、CRet System適用のみとして、各3週間継続して試験した。MRI画像データは0−Gaugeソフトウェアを用いて内臓脂肪との境界線をも識別し皮下脂肪を自動判別して脂肪面積を算出する計測アルゴリズムで高精度に解析した。セルライト皮表凹凸度は、太腿・臀部の各当該部を各々10cm平方、15cm平方でスキンキャストで皮表形状を複製し、キメ・シワの小(上下)振幅を平坦化してセルライトの中〜大(上下)振幅を計測対象としてImage−jソフトウェアで解析した。
【0036】
この結果、皮下脂肪面積率は、被験者8名の平均で試験前の数値を基準にして試験後に各々、A群は84.5±7.4%、B群は68.9±4.0%、C群は92.5±6.2%であり、セルライト皮表凸凹度は、A群は73.1±4.8%、B群は44.5±2.0%、C群は88.9±9.3%と3群いずれも試験前に比較して、皮下脂肪もセルライト形状も両方とも低下し、A・B・C3群とも改善効果が有意に認められたことになるが、このうち、C群に比較してA群の改善効果が大きく、プロビタミンC剤のAPSによる併用効果が優れていることを示すと共に、A群に比較してB群は皮下脂肪もセルライト形状も両方ともより顕著な改善効果が認められ、APSの温熱に対する安定化剤の添加効果が著明なことが検証された。
【産業上の利用可能性】
【0037】
本発明はエステティック美容業界及び皮膚科医療等の分野あるいは医療装置・美容装置産業等に多大の貢献することができる。
【符号の説明】
【0038】
A 金属軸
B エレクトロード
C 絶縁体部分
E 第二のプレート
9 キャパシティブ用出力
10 戻し電極用出力
11 レジスティブ用出力
15 キャパシティブモードキー
16 レジスティブモードキー
19 時間増キー
20 時間減キー
【技術分野】
【0001】
本発明は高周波温熱による細胞死の最小限抑制、好ましくは97%以上の細胞生存率をもたらす安全性の高いセルライト/脂質代謝の改善を図ることができる脂肪滴・セルライト抑制装置およびに脂質抑制効果増強薬、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC製剤に関する。
【背景技術】
【0002】
従来、脂肪滴に係わる組織や細胞の好ましくない発現とその影響を抑制することのできる新しい組成物とその薬剤に関するものが知られている。
【先行技術文献】
【特許文献】
【0003】
従来、脂肪滴形成抑制剤として、水酸化フラーレン類および有機化合物により修飾もしくは包接されたフラーレン複合体のうち1種以上を有効成分として含有していることを特徴とする脂肪滴形成抑制剤(請求項1)の発明がある(特許文献1:特開2008−222645)。
同文献1には、請求項2以下に次の通り記載されている。水酸化フラーレン類は、水酸基を1分子当り30以上40以下で結合しているフラーレンまたはその誘導体であることを特徴とする請求項1に記載の脂肪滴形成抑制剤(請求項2)。フラーレン複合体は、フラーレンおよびフラーレン誘導体のうちの1種以上と、有機オリゴマー、有機ポリマー、シクロデキストリンおよびクラウンエーテルとその類縁化合物のうちの1種以上の有機化合物との複合体であることを特徴とする請求項1に記載の脂肪滴形成抑制剤(請求項3)。γ−シクロデキストリンにより1.5〜2.0mol/mol比で包接されているフラーレン複合体であることを特徴とする請求項3に記載の脂肪滴形成抑制剤(請求項4)。請求項1から4のうちのいずれかの抑制剤からなることを特徴とする脂肪滴由来の細胞傷害の防御剤(請求項5)。請求項1から4のうちのいずれかの抑制剤からなることを特徴とする脂肪細胞分化抑制剤(請求項6)。
【0004】
【特許文献1】特開2008−222645公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
上記特許文献1は、従来のレチノイドに代わり得る高活性の脂肪滴形成の抑制が実現され、これによって、脂肪滴由来の細胞傷害の発生が効果的に防御され、脂肪細胞そのものの分化が抑制されることになる旨の記載がされ、スキンケア、化粧品、皮膚活性剤等として有用である旨の記載がされている。
しかし、脂肪滴形成抑制剤を配合したスキンケア、化粧品等が市販されたとしてもこれだけでは脂肪滴形成抑制やセルライト抑制に十分な効果が期待できるものであるとは言えない。
【0006】
また、従来の高周波温熱機器では、被施術者が温熱に耐えられる範囲での高い温度設定をすることでより温熱効果が得られるとされていたが被施術者にとっては温熱による苦痛は避けがたいものであった。
【0007】
さらに、温熱が脂肪滴・セルライト(皮膚表面凸凹脂肪塊)を抑制するらしいことは、従来は経験的に漠然と知られているに過ぎなかったが、その具体的な温熱条件も解明されてこなかったし、その解明のために人体それ自体で解析することは、統計学的に充分に多数の症例数を確保することも困難な上に、対照群と試験群との間で人体特性条件を同一に揃えることも容易ではなく、さらに、その人体においてセルライトや脂肪滴の増減を解析することも精度と感度の観点から困難であった。
【0008】
本発明は上記の点に鑑みてなされたもので、その目的とするところは、プロビタミンC剤(体内に吸収された後、化学変化を起こしてビタミンCになるものをいう。前駆体ともいう。)と高周波温熱装置を組み合わせることにより、脂肪滴抑制効果・セルライト抑制の大幅な向上を可能ならしめるとともに温熱による細胞死の最小限の抑制を図り、かつ被施術者にとって温熱による苦痛を感じることが無く穏やかな温熱処理を行うことができる脂肪滴・セルライト抑制装置および脂質抑制効果増強薬、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC製剤を提供することにある。
【課題を解決するための手段】
【0009】
本発明に係る脂肪滴・セルライト抑制装置は、プロビタミンC剤の標的体部への投与手段と、被施術部位に当接するためのエレクトロードと、該エレクトロードに当接する被施術対象体の背後に設置する戻し電極であるレジスティブを備え、かつ0.45MHzの高周波の下で、温度37〜41℃の範囲の温度調節部を備えるとともに1回当たりの温熱処理時間を1分〜30分に設定する温熱処理時間調節部を備え、合計で6時間〜1週間のインターバルを置いた温熱投与手段を備えたことを特徴とする。
【0010】
上記プロビタミンC剤は、アスコルビン酸−2−0−フォスフェート・アスコルビン酸−2−0−α−D−グルコシド・アスコルビン酸−2−0−フォスフェート−6−0−パルミチン酸エステル・アスコルビン酸−2−0−フォスフェート−6−0−(2−ヘキシルデカン酸)エステル・アスコルビン酸−2,3,5,6−0−(2’−ヘキシルデカン酸)テトラエステル、アスコルビン酸−6−0−パルミチン酸エステル、アスコルビン酸−6−0−ステアリン酸エステルからなる群から選ばれた一つまたは二つ以上を用いることを特徴とする。
【0011】
本発明に係る脂肪抑制効果増強薬は、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱向けの上記プロビタミンC剤および/またはビタミンCを含有することを特徴とする。特に、ビタミンCの場合にあっては、水素添加大豆レシチン・コレステロールから構成され、超音波装置・エクストルーダから調整されたリポソームによってアスコルビン酸のまま包含する皮膚浸透性が増強されたビタミンCであることを特徴とする。
【0012】
本発明に係るセルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC剤および/ビタミンC製剤は、上記プロビタミンC剤および/またはビタミンCを温熱処理においても分解せずに保持させる温熱安定化剤を含有することを特徴とする。
【0013】
本発明に係るセルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向け上記プロビタミンC剤および/ビタミンC製剤は、温熱安定化剤として、マニトール、コーンスターチ、キチン・キトサンからなる群から選ばれた一つ以上の物質を含有することを特徴とする。
【発明の効果】
【0014】
温熱が脂肪滴・セルライト(皮膚表面凸凹脂肪塊)を抑制するらしいことは、従来は経験的に漠然と知られているに過ぎなかったが、その具体的な温熱条件も解明されてこなかったし、その解明のために人体それ自体で解析することは、統計学的に充分に多数の症例数を確保することも困難な上に、対照群と試験群との間で人体特性条件を同一に揃えることも容易ではなく、さらに、その人体においてセルライトや脂肪滴の増減を解析することも精度と感度の観点から困難であった。
【0015】
本発明は、脂肪滴やセルライトの形成に関する中心的役割を果たす前駆脂肪細胞および/または脂肪細胞を用い、さらには、これら前駆脂肪細胞および/または脂肪細胞を組み込んだ3次元ヒト皮膚組織モデル、加えて、ヒト皮膚摘出組織片、および、ユカタン産ミニ豚皮膚摘出組織片などを用いて、各々、同一の皮膚特性条件の下に、試験群と比較対照群を操作し、統計学的に充分に多数の適用例を解析して、脂肪滴とセルライトを抑制する最適条件を求めた上で、その範囲前後に絞って臨床上の最適条件を求めた。
【0016】
その結果、温熱処理装置の単独使用よりも、温熱に加えて、各種プロビタミンC剤を併用したことにより、相乗効果として、脂肪滴とセルライトの抑制が顕著になることが判明した。
また、温熱を一定期間のインターバルを置いて温熱処理する手段と、各温熱処理手段の適用に際して本発明で見いだした特定プロビタミンC剤を特定濃度で標的体部に投与する併用手段が脂肪滴・セルライト抑制に著効を示すことが本発明によって見いだされた。
【0017】
さらに、本発明に係る脂肪抑制効果増強薬は、上記プロビタミンC剤および/またはビタミンCを含有するので、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱向け治療に有効に機能することとなる。
【0018】
さらにまた、本発明に係るセルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けプロビタミンC剤および/ビタミンC製剤は、上記プロビタミンC剤および/またはビタミンCを温熱処理においても分解せずに保持させる温熱安定化剤として寄与することができる。
【0019】
そして、本発明の上記プロビタミンC剤および/ビタミンC製剤は、温熱安定化剤として、マニトール、コーンスターチ、キチン・キトサンからなる群から選ばれた一つ以上の物質を含有することによりセルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けとして好適である。
【図面の簡単な説明】
【0020】
【図1】ユカタン産ミニ豚皮膚摘出組織片を用いてプロビタミンC剤と高周波温熱装置の併用による脂肪滴・セルライト抑制装置を示す斜視図である。
【図2】図1のプロビタミンC剤を投与した試験片A、B、Cに本発明に係る温熱処理装置を用いて41℃の温度条件下で5分間、高周波温熱を投与した場合を示す状態図である。
【図3】APS投与量に対する脂肪滴蓄積量の変化を示す状態図である。
【図4】脂肪滴の顕微鏡写真で、左上写真はプロビタミンC剤及び温熱処理装置を無投与の場合を示し、右上写真は0.03%濃度のAPSのみを投与した場合を示し、左下写真はAPSは無投与で温熱処理装置のみを適用した場合を示し、右下写真は0.03%濃度のAPS及び温熱処理装置を適用した場合の脂肪滴の状態を示す。
【図5】30,000個の細胞群を2日放置後、APS投与と温熱処理装置を適用し、6時間後に温熱処理装置のみを適用し、18時間後にAPS投与と温熱処理装置を適用する操作を繰り返して、顕微鏡写真撮影の条件とした説明図である。
【図6】脂肪滴蓄積量の相対比を示す顕微鏡写真である。
【図7】図8の顕微鏡写真を撮影するための試験片の顕微鏡写真撮影の条件とした説明図である。
【図8】0.03%濃度のAPSを投与せず温熱処理装置の適用もしない場合及びいずれか一方を採用した場合及び併用した場合の脂肪滴の状態を示す顕微鏡写真である。
【図9】キャパシティブエレクトリックトランスファーシステムの電流の動きを示す説明図である。
【図10】非対称電極間で加えられたエネルギー分配を示す説明図である。
【図11】MD530のインディバCRet Systemの背面図である。
【図12】MD530のインディバCRet Systemの正面図である。
【図13】MD530のインディバCRet System前面に表示されるコントロール類の表示部の説明図である。
【発明を実施するための形態】
【実施例1】
【0021】
脂肪細胞/前駆脂肪細胞での脂肪滴・セルライト抑制と細胞死防御についてについて実施した。
間葉系前駆脂肪細胞OP9を培養し通常培地からインスリン含有KSR培地に置換すると、脂肪細胞への分化が開始されるが、この時に本発明のCapacitive−Resistive Electric−Transfer装置((株)インディバ・ジャパン製品:MD530) (CRet System )の身体温熱装置を使用してLevel 5, Indicator 5, 20 secに該当する電気特性を設定した。室温26.5℃から41℃にシフトアップするが、その後に、同装置のLevel 2〜3に設定した。脂肪細胞は41℃で1 min保持した。この時に、プロビタミンC剤としてアスコルビン酸−2−O−フォスフェート ナトリウム塩(APS) を1 mM (300 ppm, 0.03wt%)の濃度で投与して一日12時間おきに2回反復して3日間実施する試験区と無投与の比較対照区とを比較した。
細胞内の脂肪滴は、オイルレッドオー色素で染色した後に10%メタノール水溶液でリンスしてリンス廃液が530 nmでの吸光度がゼロと成る3〜5回まで徹底的にリンスして、細胞外や細胞表面のオイルレッドオー色素を消滅させた後に、位相差顕微鏡で撮影すると共に、細胞内のオイルレッドオー色素を抽出して530 nmで吸光プレ−トリーダーと分光光度計で細胞内脂肪滴を定量した。細胞死と細胞生存は、各々、プロピジウムヨーダイドとカルセインアミノメトキシエステルで染色し、その蛍光度を蛍光プレートリーダーで評価した。
【0022】
本発明で使用するMD530は0.45MHzの高周波温熱機器であり、施術箇所への循環を通じて人体細胞の深部加温を行う。キャパシティブ用エレクトロードとレジスティブ用エレクトロードを使用し、深部加温を行う。キャパシティブモードを採用する場合、ステンレス製のエレクロロードの円形盤の表面は人の肌に直接触れないようにプラスチックで表面をコーティングしている。エレクトロードは、細胞に高周波エネルギーを透過するコンデンサーの役割をし、施術部位を加温する。透過された高周波エネルギーは、板型戻し電極に向って透過される。他方、レジスティブモードでは、直接、施術箇所に置かれたRES用エレクトロード(ステンレス製)を通して人体細胞へ高周波電流を流す。この電流は戻し電極に電導する。高周波エネルギーが細胞内に透過されたとき、細胞が抵抗体となり組織の温度を集中的に上昇させ、深部加温が行われる。本機器では、被施術者に流れる電流の強さ、被施術者に加えられる皮相電力(キャパシティブモード)、アクティブパワー(レジスティブモード)及びエレクトロードと被施術者の抵抗を測定し、モニタリングができる。
【0023】
図11はMD530のインディバCRet Systemの背面図で、1は電源スイッチ、2はヒューズホルダー、3は電源ソケット、4はアース用ジャック、5は冷却ファン、6は仕様ラベルをそれぞれ示す。図12はMD530の正面図で、7はLCD画面、8はキーパッド、9はキャパシティブ用出力、10は戻し電極用出力、11はレジスティブ用出力をそれぞれ示す。図13はMD530の前面に表示されるコントロール類の表示部の説明図で、12はスタンバイインジケータランプ、13はON/OFFキー、14はメニューキー、15はキャパシティブモードキー、レジスティブモードキー、17はリセットキー、18はスタート/ストップキー、19は時間増キー、時間減キー、21は出力増/減ダイヤルノブをそれぞれ示す。
【0024】
キャパシティブモードの出力に対するインピーダンスは、皮膚組織上に置かれたエレクトロードのインピーダンス(1,000オーム)に相応するように計算されている。この方法により多容量のエネルギーの透過を実現できる。エレクトロードを通じての組織への循環高周波エネルギーの行方は、図9に示す。MD530からのエネルギーは、金属軸Aを通してBの先端(エレクトロードの最下部)へ伝わる。そのエネルギーは,Cの絶縁体部分により組織と隔てられるため低下し、エレクトロード全表面、容量的に組織に伝達される。組織Dは、合計で1,000オームとなる複数の無限大の抵抗を定着させ、そのコンデンサーの性質により第二のプレートのような働きをする。図9の点線Eが第二のプレートとして定義され、コンデンサーとしての働きがなされる。1,000オーム相当の抵抗は、実際はB点とE点の間で発生し、その部分で温度上昇が起こり、その強深度は、本機器のパワー(レベル調整に対応)・エレクトロードの大きさ・施術部位の組織の特質・施術時間により決まる。特に本発明では、被施術者が被施術者にとって温熱による苦痛を感じることが無く穏やかな温熱処理、すなわち37〜41℃の範囲の温度設定により温熱処理を行うことができる点にある。
【0025】
上記の条件下において、その結果を以下に示す。
(1)脂肪細胞への分化誘導処理によって、細胞の核の周辺に、ドーナッツ状に脂肪滴(赤く染色;細胞1個当たり約20個余り)蓄積が見られた。細胞生存率は99.3±0.4%だった。
(2)41℃でのCRet温熱装置は、プロビタミンC剤なしでも脂肪滴蓄積量を22%減少した。CRet System温熱装置の適用により脂肪滴蓄積が抑制された。細胞死は0.8±0.2%と少しあるが顕著ではなかった。
【0026】
(3)プロビタミンC剤(アスコルビン酸誘導体)APS(アスコルビン酸−2−O−フォスフェート ナトリウム塩)の300 ppm (0.03wt%, 1 mM)の濃度での上記温熱装置を適用しない場合での37℃での投与は、細胞核の周辺に脂肪滴蓄積が見られたが、脂肪滴蓄積を20%抑制した。APSまたはCRet温熱装置(1 min)適用による細胞死は0.1±0.0%と少し見られたが、無視しうるレベルであった。
【0027】
(4)APSの300 ppm投与とCRet System温熱装置の併用は、脂肪滴蓄積を54%抑制した。アスコルビン酸誘導体APSの投与とCRet System温熱装置の併用により脂肪滴抑制効果は大幅に増大した。脂肪滴のない細胞が過半数を占めた。細胞核の周辺に脂肪滴が蓄積されたが、APS投与で細胞全体に脂肪滴蓄積が抑制され、この抑制は、CRet System温熱装置の併用で一層増大した。細胞生存率は99.0±0.6%を維持した。APSから変換されたビタミンCが脂肪燃焼促進剤カルニチンを合成する酵素トリメチルリシン ジオキゲナーゼ&γ−ブチロベタイン ジオキシゲナーゼを促進すると共に、CRet System温熱装置による脂肪滴流動化&分散化が奏功したことを示唆するものである。
【0028】
(5)従来法として、通常の身体温熱装置で42,43,44,45℃の温度4点で各々60分間の処理による温熱単独を行なう比較対照例を試験した結果、脂肪滴抑制は、各温度で、8.9,11.6,10.4,5.2%の抑制であり、細胞死が各々、18.1±4.7,27.0±5.9,41.3±11.0,61.8±5.5%だった。過酷な温熱装置の単独使用は細胞傷害と細胞生存の指標であるサクシネートデヒドロゲナーゼを主体とするミトコンドリア脱水素酵素の活性低下をもたらすと共に、透過型電子顕微鏡による細胞形態では、活発な細胞代謝の指標となるマイクロビラスの消失、細胞膜の破綻、シュリンキッジ(細胞萎縮)、ピクノーシス(核凝縮)、カリオレキシス(核断片化)が認められた。これらは従来の過酷な温熱装置の適用が細胞死を広範囲に惹起させるという犠牲の下に施行されていた可能性を示唆するものである。
【実施例2】
【0029】
前駆脂肪細胞を組み込んだ3次元ヒト皮膚組織モデルでの脂肪滴・セルライト抑制と細胞死防御について実施した。
ヒト皮膚繊維芽細胞OUMS−36を含むI型コラーゲンから構成される真皮、その上にIV型コラーゲン・ラミニン・エンタクチン・フィブロネクチンを含有するマトリゲルから構成される基底膜、さらにその上に、間葉系前駆脂肪細胞OP9を添加することを特徴とし、その上に、ヒト皮膚角化細胞HaCaTから構成される表皮を各々重層し、最後にエアーリフトによって角層を形成させて取得される脂肪滴形成量評価向けの3次元ヒト皮膚組織モデルを作製し、実施例1と同様な試験を行ない、脂肪滴・セルライト抑制と細胞死防御を評価し、併せて、皮膚組織片をクライオスタットで4μm厚の超薄切片を調製してオイルレッドオー色素で脂肪滴を染色した皮膚組織の断面構造において、断面積に占める脂肪滴の面積の割合をNIH−ImageとImage−Jソフトウェアで解析した。細胞死レベルはヘマトキシリンーエオシン染色によって、変質細胞の細胞総数に占める比率から、評価した。さらに、皮膚表面の凹凸形状も走査型電子顕微鏡で撮影した。皮膚表面の凹凸形状はシリコーンゴムを用いたレプリカを作製して凸凹度をラインヒストグラム化してセルライト度を評価した。
【0030】
この結果、比較例として、41℃でのCRet System温熱装置の単独適用(常温からのシフトアップ34sec、設定温度到達後の温度平行時間5min、常温へ低下するシフトダウン3min14sec:以下、これらを単に「5min適用」と呼ぶ)は、プロビタミンC剤なしでも脂肪滴蓄積量を22.4±3.7%減少させた。CRet System温熱装置の単独適用による脂肪滴蓄積抑制効果が有意に示された。
もう一つの比較例として、プロビタミンC剤(アスコルビン酸誘導体)APS(アスコルビン酸−2−O−フォスフェート ナトリウム塩)の300ppm(0.03wt%)の濃度での上記温熱装置を適用しない場合での37℃での投与は、細胞核の周辺に脂肪滴蓄積が見られたが、脂肪滴蓄積を16.1±2.9%抑制した。APS単独投与またはCRet System温熱装置(5min適用)単独適用による細胞死は各々0.1±0.0%、2.2±0.3%と無視しうるレベルまたは僅少レベルであった。
【0031】
一方、本発明では、APSの300 ppm投与とCRet System温熱装置の併用、または、温熱安定化剤としてマニトール500ppm、コーンスターチ800ppm、イカ筋(中骨)キトサン(キトサン成分83〜97%、キチン成分3〜17%;β型キチンを出発材料にして脱アセチル反応などの処理で調製したキチン・キトサン)350ppmを添加したAPSの300ppm投与とCRet System温熱装置の併用、は、脂肪滴蓄積を54.7±4.6%、または、73.3±5.8%抑制した。アスコルビン酸誘導体APSの投与とCRet温熱装置(5min適用)の併用により脂肪滴抑制効果は増大し、さらに、温熱安定化剤の添加によってこの効果が促進された。これら本発明例ではいずれも脂肪滴のほぼ検出されない細胞が過半数を占めた。細胞核の周辺に脂肪滴が蓄積されたが、APS投与で細胞全体に脂肪滴蓄積が抑制され、この抑制は、CRet System温熱装置の併用で一層増大し、さらに温熱安定化剤によって顕著になったことになる。細胞死率も各々0.3±0.0%と0.2±0.0%と無視しうるレベルだった。
【実施例3】
【0032】
改変ブロノフ拡散チェンバーに組み込んだインフォームドコンセントを提出した48歳の日本人女性の耳后下の皮膚摘出組織片での脂肪滴・セルライト抑制と細胞死防御について実施例2と同様に実施した。
脂肪滴抑制試験の終了後に当該チェンバーより単離した皮膚組織片をクライオスタットで4μm厚の超薄切片を調製し、実施例2と同様に脂肪滴・セルライト抑制と細胞死防御を評価した。
【0033】
この結果、比較例として、41℃でのCRet System温熱装置の単独適用(常温からのシフトアップ33sec、設定温度到達後の温度平行時間5min、常温へ低下するシフトダウン3min27sec:以下、これらを単に「5min適用」と呼ぶ)は、プロビタミンC剤なしでも脂肪滴蓄積量を19.1±2.9%減少させた。CRet温熱装置の単独適用による脂肪滴蓄積抑制効果が有意に示された。
もう一つの比較例として、プロビタミンC剤(アスコルビン酸誘導体)APS(アスコルビン酸−2−O−フォスフェートナトリウム塩)の300ppm(0.03wt%)の濃度での上記温熱装置を適用しない場合での37℃での投与は、細胞核の周辺に脂肪滴蓄積が見られたが、脂肪滴蓄積を12.0±3.5%抑制した。APS投与またはAPSなしのCRet System温熱装置(5min適用)単独適用による細胞死は各々2.0±0.4%または6.9±0.8%と無視しうるレベルまたは僅少レベルであった。
【0034】
一方、本発明では、APSの300ppm投与とCRet System温熱装置の併用、または、温熱安定化剤としてマニトール500ppm、コーンスターチ800ppm、イカ筋(中骨)キトサン(キトサン成分83〜97%、キチン成分3〜17%;β型キチンを出発材料にして脱アセチル反応などの処理で調製したキチン・キトサン)350ppmを添加したAPSの300ppm投与とCRet System温熱装置の併用は、各々54.8±12.6%または70.4±6.3%脂肪滴蓄積を抑制した。脂肪滴抑制効果はプロビタミンCのAPSの投与とCRet System温熱装置(5min適用)の併用により明確となり、さらに温熱安定化剤を併用すると脂肪滴抑制効果は顕著になった。脂肪滴のほぼ検出されない細胞が過半数を占めた。細胞核の周辺に脂肪滴が蓄積されたが、APS投与で細胞全体に脂肪滴蓄積が抑制され、この抑制は、CRet System温熱装置の併用で一層増大したことになり温熱安定化剤による促進効果も認められた。細胞死率も各々1.1±0.2%または1.7±0.2%と無視しうるレベルだった。
【実施例4】
【0035】
臨床試験での脂肪塊・セルライトはインフォームドコンセントを得た健康な26〜56歳の日本人女性24名をあらかじめ大腿最太部後側と臀部最厚部先端での皮下脂肪率をMRIで評価し、当該部の皮膚表面形状は、セルライト皮表凹凸度として、スキンキャスト皮表形状レプリカ法で評価した。
この試験前の皮下脂肪率とセルライト皮表度および平均年齢に偏りがないように24名を8名ずつ3群に分けて、毎週3回、各回、A群は、温熱安定化剤なしのAPS300ppmを太腿と臀部に1mL/cm2で塗布しCRet System温熱装置を各々10分間と15分間適用し、本発明のB群は、温熱安定化剤としてマニトール500ppm、コーンスターチ800ppm、イカ筋(中骨)キトサン(キトサン成分83〜97%、キチン成分3〜17%;β型キチンを出発材料にして脱アセチル反応などの処理で調製したキチン・キトサン)350ppmを添加したAPS300ppmを同様に塗布してCRet Systemも同様に適用し、比較対照のC群は、CRet System適用のみとして、各3週間継続して試験した。MRI画像データは0−Gaugeソフトウェアを用いて内臓脂肪との境界線をも識別し皮下脂肪を自動判別して脂肪面積を算出する計測アルゴリズムで高精度に解析した。セルライト皮表凹凸度は、太腿・臀部の各当該部を各々10cm平方、15cm平方でスキンキャストで皮表形状を複製し、キメ・シワの小(上下)振幅を平坦化してセルライトの中〜大(上下)振幅を計測対象としてImage−jソフトウェアで解析した。
【0036】
この結果、皮下脂肪面積率は、被験者8名の平均で試験前の数値を基準にして試験後に各々、A群は84.5±7.4%、B群は68.9±4.0%、C群は92.5±6.2%であり、セルライト皮表凸凹度は、A群は73.1±4.8%、B群は44.5±2.0%、C群は88.9±9.3%と3群いずれも試験前に比較して、皮下脂肪もセルライト形状も両方とも低下し、A・B・C3群とも改善効果が有意に認められたことになるが、このうち、C群に比較してA群の改善効果が大きく、プロビタミンC剤のAPSによる併用効果が優れていることを示すと共に、A群に比較してB群は皮下脂肪もセルライト形状も両方ともより顕著な改善効果が認められ、APSの温熱に対する安定化剤の添加効果が著明なことが検証された。
【産業上の利用可能性】
【0037】
本発明はエステティック美容業界及び皮膚科医療等の分野あるいは医療装置・美容装置産業等に多大の貢献することができる。
【符号の説明】
【0038】
A 金属軸
B エレクトロード
C 絶縁体部分
E 第二のプレート
9 キャパシティブ用出力
10 戻し電極用出力
11 レジスティブ用出力
15 キャパシティブモードキー
16 レジスティブモードキー
19 時間増キー
20 時間減キー
【特許請求の範囲】
【請求項1】
セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱向けの上記プロビタミンC剤および/またはビタミンCを含有することを特徴とする脂質抑制効果増強薬。
【請求項2】
上記プロビタミンC剤および/またはビタミンCは、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けとして温熱処理においても分解せずに保持させる温熱安定化剤を含有することを特徴とする請求項3記載の脂質抑制効果増強薬。
【請求項3】
上記温熱安定化剤は、マニトール、コーンスターチ、キチン・キトサンからなる群から選ばれた一つ以上の物質を含有することを特徴とする請求項3又は4記載の脂質抑制効果増強薬。
【請求項4】
上記ビタミンCは、水素添加大豆レシチン・コレステロールから構成され、超音波装置・エクストルーダから調整されたリポソームによってアスコルビン酸のまま包含する皮膚浸透性が増強されたビタミンCであることを特徴とする請求項3、4又は5記載の脂質抑制効果増強薬。
【請求項1】
セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱向けの上記プロビタミンC剤および/またはビタミンCを含有することを特徴とする脂質抑制効果増強薬。
【請求項2】
上記プロビタミンC剤および/またはビタミンCは、セルライト予防治療・脂肪滴抑制・脂質代謝改善用の温熱療法向けとして温熱処理においても分解せずに保持させる温熱安定化剤を含有することを特徴とする請求項3記載の脂質抑制効果増強薬。
【請求項3】
上記温熱安定化剤は、マニトール、コーンスターチ、キチン・キトサンからなる群から選ばれた一つ以上の物質を含有することを特徴とする請求項3又は4記載の脂質抑制効果増強薬。
【請求項4】
上記ビタミンCは、水素添加大豆レシチン・コレステロールから構成され、超音波装置・エクストルーダから調整されたリポソームによってアスコルビン酸のまま包含する皮膚浸透性が増強されたビタミンCであることを特徴とする請求項3、4又は5記載の脂質抑制効果増強薬。
【図1】


【図2】


【図3】


【図5】


【図7】


【図9】


【図10】


【図4】


【図6】


【図8】


【図11】


【図12】


【図13】




【図2】


【図3】


【図5】


【図7】


【図9】


【図10】


【図4】


【図6】


【図8】


【図11】


【図12】


【図13】


【公開番号】特開2013−23496(P2013−23496A)
【公開日】平成25年2月4日(2013.2.4)
【国際特許分類】
【出願番号】特願2011−216741(P2011−216741)
【出願日】平成23年9月30日(2011.9.30)
【分割の表示】特願2011−162509(P2011−162509)の分割
【原出願日】平成23年7月25日(2011.7.25)
【出願人】(503321703)株式会社インディバ・ジャパン (3)
【Fターム(参考)】
【公開日】平成25年2月4日(2013.2.4)
【国際特許分類】
【出願日】平成23年9月30日(2011.9.30)
【分割の表示】特願2011−162509(P2011−162509)の分割
【原出願日】平成23年7月25日(2011.7.25)
【出願人】(503321703)株式会社インディバ・ジャパン (3)
【Fターム(参考)】
[ Back to top ]

