脳保護剤
【課題】脳の保護作用を有する剤を提供する。
【解決手段】小麦の末粉抽出物を有効成分とする脳保護剤。
【解決手段】小麦の末粉抽出物を有効成分とする脳保護剤。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、虚血性疾患に伴う脳障害を予防する剤に関する。
【背景技術】
【0002】
脳梗塞などによる虚血性神経細胞死は、虚血巣中心部においてオルガネラの膨化や核の凝集など病理学的に無秩序な典型的な壊死の状態を示すことから、脳虚血に陥った細胞における壊死(Necrosis)による神経細胞死であるとされてきた。しかし、軽度の脳虚血時には壊死とは全く異なった病理像を呈することから(非特許文献1:Brain Res. Mol., 29, pp.1-14, 1995;)、これらの神経細胞では、壊死に加えてアポトーシスが誘発されていると考えらるようになった(非特許文献2:Science, 281, pp.1302-1304, 1998)。
【0003】
アポトーシスは、細胞死へのスイッチがオンになってから一連のシグナルカスケードが進行し、細胞死の実行分子であるカスパーゼが活性化され、最終的に細胞が死に至ると考えられている。新生児期の低酸素脳症にもカスパーゼの活性化を介するアポトーシスの関与が示唆されている(非特許文献3:J. Clin. Invest., 101, pp.1992-1999, 1998)。 また、損傷脳領域と神経線維連絡を持つ遠隔部位領域の神経細胞が二次的に細胞死に至ることが知られており、これにもアポトーシスが深く関与していることが判明している。
【0004】
脳虚血によるアポトーシスは、虚血壊死(コア部分)の辺縁部(ペナンブラ領域)において壊死より少し遅れて出現することが認められている。従って、脳虚血時のアポトーシスに起因する脳細胞死を抑制するための治療開始時間(治療タイムウインドー)は、壊死に比べて許容度が大きく、発症後数時間を経て薬剤を投与してもアポトーシスに起因する細胞死を抑制できる可能性がある。また、このことによって、アポトーシスに陥る運命にある細胞を保護して生存細胞数を増やすことができ、さらに遠隔部位領域における二次的な変性を阻止して神経機能後遺障害を軽減できる可能性がある。
【0005】
このような観点から特許文献1(特開2000−344663号公報)には、2-フェニル-1,2-ベンゾイソセレナゾール-3(2H)-オン(一般名エプセレン)がアポトーシスに起因する脳細胞死を抑制することから、脳虚血に伴う脳障害を予防する剤として使用可能であることが記載されている。また最近では虚血性の障害の治療剤として天然物由来の脳保護剤やアポトーシス抑制剤が注目されている。特許文献2(特開平6−172200号公報)にはラクトフェリン由来のペプチド、特許文献3(特開2002−265359号公報)にはお茶由来のテアニン、特許文献4(特開2008−266177号公報)には担子菌や子嚢菌抽出物、特許文献5(特開2009−292747号公報)には紫芋発酵液など天然物由来の脳保護剤が開示されている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2000−344663号公報
【特許文献2】特開平6−172200号公報
【特許文献3】特開2002−265359号公報
【特許文献4】特開2008−266177号公報
【特許文献5】特開2009−292747号公報
【非特許文献】
【0007】
【非特許文献1】Brain Res. Mol., 29, pp.1-14, 1995;
【非特許文献2】Science, 281, pp.1302-1304, 1998
【非特許文献3】J. Clin. Invest., 101, pp.1992-1999, 1998
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明は、脳の保護作用を有する剤を提供することを課題とする。またこの剤を含有する飲食品を提供することを課題とする。
【課題を解決するための手段】
【0009】
本発明者らは小麦末粉に着目して試験した結果、小麦末粉の抽出物に虚血によって引き起こされるアポトーシス発生の抑制作用があることを知見したことに基づき、本発明を提案する。
【0010】
すなわち、本発明は、
(1)小麦末粉の抽出物を有効成分とする脳保護剤。
(2)脳保護が虚血性脳障害による予防用である(1)記載の脳保護剤。
(3)脳保護が虚血に由来して発生するアポトーシス抑制によるものである(1)又は(2)記載の脳保護剤。
(4)経口剤である(1)〜(3)のいずれかに記載の脳保護剤
(5)(1)〜(4)のいずれかに記載の脳保護剤を含有する飲食品
【発明の効果】
【0011】
本発明は、虚血によって発生するアポトーシスを抑制し、脳保護作用を有する剤を提供することができる。また虚血性の脳障害を予防する飲食品を提供することができる。
【図面の簡単な説明】
【0012】
【図1】小麦末粉の水抽出物によるヒト神経芽細胞腫由来SH-SY5Y細胞に対するアポトーシス抑制効果を示すグラフ。
【図2】人工的に脳虚血を発生させたマウス脳の梗塞状態を観察した画像を示す。
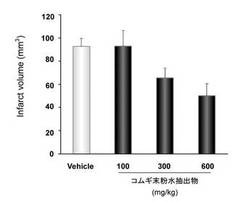
【図3】脳梗塞画像を画像解析し、小麦末粉が濃度依存性で梗塞を抑制していることを示すグラフ。
【図4】脳梗塞モデルの脳断面画像を示す。本画像では梗塞部位が白く映し出されている。
【発明を実施するための形態】
【0013】
本発明の脳保護剤は小麦末粉の抽出物を有効成分とする。
【0014】
小麦粉を分類するには大きく分けて2つの方法がある。ひとつは、タイプ(種類)による分類で、もうひとつはグレード(等級)によるものでる。グレードによる分類は、原料の小麦粒の形態に由来する。本発明に用いる末粉はグレードによる分類である。
同じ小麦粒の胚乳部分でも、中心部は灰分が少なく、色が白く、またたんぱく質の量も少なくなる傾向がある。製粉工程で、主にこの中心部分からとれる粉を分類して上級粉と呼ぶ。上級粉は、灰分が低く、乳白色または淡黄色の冴えた色をしている。逆に、表皮近くからとれる下級粉は、たんぱく質も多くなり、色がくすんで茶褐色を帯びてくる。一般に、灰分値が0.3〜0.35%のものは特等粉、0.35〜0.45%のものは1等粉、0.45〜0.65%のものは2等粉、0.7〜1.0%のものは3等粉、そして1.2〜2.0%のものを末粉(すえこ)と分類している。また小麦粒の外皮はふすまとして別に篩い分けられる末粉は通常食用には適さないため、ふすまとあわせて動物用飼料としたり、工業用の糊原料とされたりする。本発明はこの末粉を原料としている。
【0015】
小麦末粉から本発明の剤を調製するためには、末粉を水で抽出する。以降「末粉」として記載した場合は、小麦末粉を意味する。
末粉は飼料用として市販されているものでよいが、製粉直後のものが脂質分の酸化がなく好ましい。
【0016】
末粉1重量部に対して水5〜10重量部を加え、攪拌しながら、0.5〜1時間室温抽出する。抽出時間を短縮するためには、超音波振動を与えるなど物理的な振動を加え、水溶性成分を抽出する。小規模な抽出操作であれば、末粉1重量部に対して水5重量部を加え攪拌分散させた後、超音波処理を3〜10分行うことで有効成分が水に溶出してくる。
ついで、遠心分離あるいはフィルター濾過で固液分離を行い、ロ液又は上清を回収する。回収した上清又はロ液は乾燥処理を行い粉末化する。乾燥処理は通常の液体を乾燥する方法であれば噴霧乾燥やドラムドライヤー、凍結乾燥などどのような方法でも適用できるが、活性を低下させないためには可能な限り低温で乾燥させることが好ましい。
【0017】
本発明の脳保護剤は、上記の方法で得られた乾燥物を更に粉砕し、超微細粒子とすることもできる。
本発明品の脳保護剤は、常法によって、粉末、顆粒、錠剤、カプセル剤として製品化することができる。また、水や果汁に溶解して液状、ゼリー状の飲料として製品化することもできる。更に、各種飲食品に添加して利用することもできる。
このような飲食品としては、特に限定されない。
本発明の脳保護剤の有効投与量は、経口摂取において成人1日当り1〜10gである。
以下実施例を示し、本発明をさらに説明する。
【実施例】
【0018】
<試験例1>
1.酸化ストレスによる神経細胞のアポトーシス予防試験
A.試験材料および方法
(1)使用細胞及び培養方法
DSファーマバイオメディカル株式会社より購入したヒト神経芽細胞腫由来SH-SY5Y細胞(継代数X+18)を使用した。通常培養用培地はD-MEM/Ham's F-12(和光純薬工業株式会社)に不活化したウシ胎児血清(ライフテクノロジーズジャパン株式会社)15%、非必須アミノ酸(Sigma)1%、ペニシリン(SIGMA)50000 U、ストレプトマイシン(明治製菓)0。05 pot。を添加して使用した。通常培養においては、10cmシャーレに細胞を播種し、80-90%コンフルエント時に0.05%トリプシン-EDTA溶液で細胞を剥離して継代を行った。培養は37℃、5%二酸化炭素、95%空気存在下で行った。
【0019】
(2)プレート播種
継代したSH-SY5Y細胞(継代数X+19〜25)を96wellプレート(96well マイクロテストプレート;FALCON(日本ベクトン・ディッキンソン株式会社))上に1.0〜1.5×105 cells / mLで播種し、一晩培養した。
【0020】
(3)試薬調製
6-Hydroxydopamineの調製
酸化ストレス誘因物質として6-Hydroxydopamine(6-OHDA)を用いた。6-OHDAを150mMになるよう蒸留水で調製し、最終濃度150μMになるよう培地に添加した。
【0021】
末粉抽出物の調製
日本製粉株式会社製の末粉を用いた。
末粉1gに対して水5mLを添加し、3分超音波処理を行った。遠心機で1000rpm×10分遠心後、上清を回収し、凍結乾燥を行い乾燥物を得た。以下水抽出物と呼ぶ。
【0022】
抽出物を3、10、30および100mg/mLになるよう蒸留水で調製し、それぞれ最終濃度が3、10、30および100μg/mLになるよう培地(通常培養培地6-OHDAを添加したもの)に添加した。
【0023】
(4)MTTアッセイ
MTT試薬の調製
3-[4、5-dimethylthiazol-2-yl]-2、5-diphenyltetrazolium bromide(MTT)をPBS(-)で5mg/mLになるよう調製し、0.45μmフィルター(アデバンテック東洋株式会社)で濾過したものをMTT溶液とした。MTT溶液は分注し、使用まで-20℃保存とした。使用時は、500μg/mLになるよう通常培養培地に添加した(MTT培地)。
【0024】
MTTアッセイ
6-OHDAおよび被験物質添加から15時間後、MTTアッセイを行った。
6-OHDAおよび被験物質添加培地からMTT培地に交換して3時間インキュベートした後、培地を除去し、dimethyl sulfoxideを添加した。沈殿したホルマザンを溶解させた後、570nmの吸光度を測定した。
【0025】
B.結果
測定結果を図1に示す。末粉水抽出物を6-OHDA 150μMと同時に添加した結果、末粉水抽出物は用量依存的に6-OHDAの酸化ストレスによるアポトーシスを抑制することが分かった。特に10μg/mL以上の濃度としたとき顕著なアポトーシス抑制効果が確認できた。
【0026】
<試験例2>
1.人工的脳梗塞モデルを用いた脳保護効果の確認試験
人工的に脳血流を遮断して脳梗塞モデルを作成して本発明の脳保護作用を確認した。
A.試験方法
(1)脳保護剤の調製と投与
試験例1で用いた抽出物を連続的に経口投与して脳保護効果を確認した。
試験用の脳保護剤は、あらかじめ1日分ずつ規定量を秤量・分注し、投与日および群を記載して-20℃に保存した。投与液の調製は用時調製とし、転倒混和にて、10、30、60mg/mLになるように溶解した。
【0027】
(2)試験動物
マウス,Slc:ddY,雄60匹を用いた。
入荷時:4週齢
手術・解剖時:7週齢
入荷時に種、系統、週齢、動物数及び性別を確認し、一般状態および外観を観察するとともに体重を測定した。馴化期間は7日間とした。
体重をもとに、各群に差がないよう群分けを行った。
【0028】
(3)試験系の環境条件
飼育環境
設定温度:25℃(許容範囲23〜27℃)、設定湿度:60%(許容範囲40〜80%)、照明:午前7時点灯、午後7時消灯の12時間に維持された福岡大学薬学部 動物飼育室で動物を飼育した。動物は、プラスチックケージを用いて、1ケージあたり5匹で飼育した。
飼料
固形飼料(CE-2、日本クレア株式会社)を給餌器に入れて自由に摂取させた。.
飲料水
フィルターで洗浄した水道水を給水瓶より自由に摂取させた。
【0029】
(4)投与方法・投与経路
胃ゾンデを用いた強制経口投与とした。また1日1回14日間投与した。投与液量は、最も近い測定体重値から換算して、10mL/kgで算出した。
【0030】
群構成および投与量
投与量(mg/kg) 使用動物数
対照群 0 15
100mg/kg群 100 15
300mg/kg群 300 15
600mg/kg群 600 15
【0031】
(5)脳梗塞モデルの作成
8-0ナイロンモノフィラメント(Ethilon; Ethicon, NJ, USA)を11mmの長さに切り、先端から4mmをシリコン樹脂(Xantopren; Bayer Dental, Osaka, Japan)でコーティングしたものを塞栓子として作成した。これを以下の手法でマウスに挿入して脳梗塞モデルを作成した。
手術方法
マウスに2% halothane吸入より麻酔を導入し、続いて1% halothane吸入によって麻酔を維持し手術台上に固定した。マウスの頚部の中央を切開し、左側総頸動脈と外頸動脈を結紮した。総頸動脈を切開し、塞栓子が中大脳動脈(MCA)の起始部に到達するように内頸動脈と外頸動脈の分岐部から内頸動脈を経由して9mm挿入した。再灌流は、塞栓子を手前に引き抜くことによって行った。MCA閉塞時間は4時間を負荷し、24時間後に行動観察(Neurological score)および2,3,5,-Triphenyltetrazolium chloride(TTC)染色を行い、梗塞巣体積の変化を測定した。
【0032】
(6)行動観察(Neurological score)
MCA閉塞4時間後再灌流を行い、その梗塞巣の変化を観察するためMCA閉塞24時間後に、脳梗塞のスコア付を行った。スコア付は以下の通り。
Score (0-5)
0: 運動機能に影響なし
1: 胴体の屈曲、前肢のlifting
2: 正常な姿勢でのcircling行動
3: 明らかな姿勢の異常でのcircling行動
4: Rolling行動
5: 自発的な行動がなく、体が傾く状態
【0033】
(7)TTC染色および画像解析
行動観察の後、マウスの頚椎を脱臼して、ただちに断頭した。取り出した脳を冷えた生理食塩水でよく冷し、アクリル製スライサー(マウス用Sagittal type スライス厚2mm;株式会社ニューロサイエンス;Fig. 3)を用いて、大脳皮質を含む脳の前額断スライスを2mm間隔で作製した。2%2,3,5,-triphenyltetrazolium chloride(シグマアルドリッチジャパン株式会社)を生理食塩水で作製し、切片を溶液中で37℃、30分間インキュベートした。
その後、スライドガラス上に並べ、デジタルスチルカメラ(MVC-FD91, SONY)で撮影した。梗塞巣体積は。割面の写真から梗塞総面積を画像解析ソフト(NIH Image 1.63)で測定し算出した。
【0034】
B.結果
図2に示すとおり、行動観察(Neurological score)の結果、用量依存的に脳梗塞に伴う障害発生が抑制された。4時間目までの行動は比較的活発であったが、末粉抽出物投与量に応じて、行動が活発であった。末粉抽出物600mg/Kg投与群ではNeurological scoreは2以下と良好であり、本発明の脳保護剤の効果が行動上も確認された。また24時間後の行動はいずれも悪化していたが、無投与群と比較して投与群の行動スコアは低く、脳梗塞の進行が抑制されていることが推測された。
また図3、図4に示すとおり脳梗塞巣の画像解析の結果用量依存的に脳梗塞巣の減少が認められた。特に600mg/Kg投与群では、脳梗塞部位は対照(無投与)群と比較して顕著であった。これは上記の行動観察の結果とよく対応していた。
以上の結果から本発明の脳保護剤は虚血性の脳梗塞による脳の障害を予防することが明らかとなった。
【技術分野】
【0001】
本発明は、虚血性疾患に伴う脳障害を予防する剤に関する。
【背景技術】
【0002】
脳梗塞などによる虚血性神経細胞死は、虚血巣中心部においてオルガネラの膨化や核の凝集など病理学的に無秩序な典型的な壊死の状態を示すことから、脳虚血に陥った細胞における壊死(Necrosis)による神経細胞死であるとされてきた。しかし、軽度の脳虚血時には壊死とは全く異なった病理像を呈することから(非特許文献1:Brain Res. Mol., 29, pp.1-14, 1995;)、これらの神経細胞では、壊死に加えてアポトーシスが誘発されていると考えらるようになった(非特許文献2:Science, 281, pp.1302-1304, 1998)。
【0003】
アポトーシスは、細胞死へのスイッチがオンになってから一連のシグナルカスケードが進行し、細胞死の実行分子であるカスパーゼが活性化され、最終的に細胞が死に至ると考えられている。新生児期の低酸素脳症にもカスパーゼの活性化を介するアポトーシスの関与が示唆されている(非特許文献3:J. Clin. Invest., 101, pp.1992-1999, 1998)。 また、損傷脳領域と神経線維連絡を持つ遠隔部位領域の神経細胞が二次的に細胞死に至ることが知られており、これにもアポトーシスが深く関与していることが判明している。
【0004】
脳虚血によるアポトーシスは、虚血壊死(コア部分)の辺縁部(ペナンブラ領域)において壊死より少し遅れて出現することが認められている。従って、脳虚血時のアポトーシスに起因する脳細胞死を抑制するための治療開始時間(治療タイムウインドー)は、壊死に比べて許容度が大きく、発症後数時間を経て薬剤を投与してもアポトーシスに起因する細胞死を抑制できる可能性がある。また、このことによって、アポトーシスに陥る運命にある細胞を保護して生存細胞数を増やすことができ、さらに遠隔部位領域における二次的な変性を阻止して神経機能後遺障害を軽減できる可能性がある。
【0005】
このような観点から特許文献1(特開2000−344663号公報)には、2-フェニル-1,2-ベンゾイソセレナゾール-3(2H)-オン(一般名エプセレン)がアポトーシスに起因する脳細胞死を抑制することから、脳虚血に伴う脳障害を予防する剤として使用可能であることが記載されている。また最近では虚血性の障害の治療剤として天然物由来の脳保護剤やアポトーシス抑制剤が注目されている。特許文献2(特開平6−172200号公報)にはラクトフェリン由来のペプチド、特許文献3(特開2002−265359号公報)にはお茶由来のテアニン、特許文献4(特開2008−266177号公報)には担子菌や子嚢菌抽出物、特許文献5(特開2009−292747号公報)には紫芋発酵液など天然物由来の脳保護剤が開示されている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2000−344663号公報
【特許文献2】特開平6−172200号公報
【特許文献3】特開2002−265359号公報
【特許文献4】特開2008−266177号公報
【特許文献5】特開2009−292747号公報
【非特許文献】
【0007】
【非特許文献1】Brain Res. Mol., 29, pp.1-14, 1995;
【非特許文献2】Science, 281, pp.1302-1304, 1998
【非特許文献3】J. Clin. Invest., 101, pp.1992-1999, 1998
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明は、脳の保護作用を有する剤を提供することを課題とする。またこの剤を含有する飲食品を提供することを課題とする。
【課題を解決するための手段】
【0009】
本発明者らは小麦末粉に着目して試験した結果、小麦末粉の抽出物に虚血によって引き起こされるアポトーシス発生の抑制作用があることを知見したことに基づき、本発明を提案する。
【0010】
すなわち、本発明は、
(1)小麦末粉の抽出物を有効成分とする脳保護剤。
(2)脳保護が虚血性脳障害による予防用である(1)記載の脳保護剤。
(3)脳保護が虚血に由来して発生するアポトーシス抑制によるものである(1)又は(2)記載の脳保護剤。
(4)経口剤である(1)〜(3)のいずれかに記載の脳保護剤
(5)(1)〜(4)のいずれかに記載の脳保護剤を含有する飲食品
【発明の効果】
【0011】
本発明は、虚血によって発生するアポトーシスを抑制し、脳保護作用を有する剤を提供することができる。また虚血性の脳障害を予防する飲食品を提供することができる。
【図面の簡単な説明】
【0012】
【図1】小麦末粉の水抽出物によるヒト神経芽細胞腫由来SH-SY5Y細胞に対するアポトーシス抑制効果を示すグラフ。
【図2】人工的に脳虚血を発生させたマウス脳の梗塞状態を観察した画像を示す。
【図3】脳梗塞画像を画像解析し、小麦末粉が濃度依存性で梗塞を抑制していることを示すグラフ。
【図4】脳梗塞モデルの脳断面画像を示す。本画像では梗塞部位が白く映し出されている。
【発明を実施するための形態】
【0013】
本発明の脳保護剤は小麦末粉の抽出物を有効成分とする。
【0014】
小麦粉を分類するには大きく分けて2つの方法がある。ひとつは、タイプ(種類)による分類で、もうひとつはグレード(等級)によるものでる。グレードによる分類は、原料の小麦粒の形態に由来する。本発明に用いる末粉はグレードによる分類である。
同じ小麦粒の胚乳部分でも、中心部は灰分が少なく、色が白く、またたんぱく質の量も少なくなる傾向がある。製粉工程で、主にこの中心部分からとれる粉を分類して上級粉と呼ぶ。上級粉は、灰分が低く、乳白色または淡黄色の冴えた色をしている。逆に、表皮近くからとれる下級粉は、たんぱく質も多くなり、色がくすんで茶褐色を帯びてくる。一般に、灰分値が0.3〜0.35%のものは特等粉、0.35〜0.45%のものは1等粉、0.45〜0.65%のものは2等粉、0.7〜1.0%のものは3等粉、そして1.2〜2.0%のものを末粉(すえこ)と分類している。また小麦粒の外皮はふすまとして別に篩い分けられる末粉は通常食用には適さないため、ふすまとあわせて動物用飼料としたり、工業用の糊原料とされたりする。本発明はこの末粉を原料としている。
【0015】
小麦末粉から本発明の剤を調製するためには、末粉を水で抽出する。以降「末粉」として記載した場合は、小麦末粉を意味する。
末粉は飼料用として市販されているものでよいが、製粉直後のものが脂質分の酸化がなく好ましい。
【0016】
末粉1重量部に対して水5〜10重量部を加え、攪拌しながら、0.5〜1時間室温抽出する。抽出時間を短縮するためには、超音波振動を与えるなど物理的な振動を加え、水溶性成分を抽出する。小規模な抽出操作であれば、末粉1重量部に対して水5重量部を加え攪拌分散させた後、超音波処理を3〜10分行うことで有効成分が水に溶出してくる。
ついで、遠心分離あるいはフィルター濾過で固液分離を行い、ロ液又は上清を回収する。回収した上清又はロ液は乾燥処理を行い粉末化する。乾燥処理は通常の液体を乾燥する方法であれば噴霧乾燥やドラムドライヤー、凍結乾燥などどのような方法でも適用できるが、活性を低下させないためには可能な限り低温で乾燥させることが好ましい。
【0017】
本発明の脳保護剤は、上記の方法で得られた乾燥物を更に粉砕し、超微細粒子とすることもできる。
本発明品の脳保護剤は、常法によって、粉末、顆粒、錠剤、カプセル剤として製品化することができる。また、水や果汁に溶解して液状、ゼリー状の飲料として製品化することもできる。更に、各種飲食品に添加して利用することもできる。
このような飲食品としては、特に限定されない。
本発明の脳保護剤の有効投与量は、経口摂取において成人1日当り1〜10gである。
以下実施例を示し、本発明をさらに説明する。
【実施例】
【0018】
<試験例1>
1.酸化ストレスによる神経細胞のアポトーシス予防試験
A.試験材料および方法
(1)使用細胞及び培養方法
DSファーマバイオメディカル株式会社より購入したヒト神経芽細胞腫由来SH-SY5Y細胞(継代数X+18)を使用した。通常培養用培地はD-MEM/Ham's F-12(和光純薬工業株式会社)に不活化したウシ胎児血清(ライフテクノロジーズジャパン株式会社)15%、非必須アミノ酸(Sigma)1%、ペニシリン(SIGMA)50000 U、ストレプトマイシン(明治製菓)0。05 pot。を添加して使用した。通常培養においては、10cmシャーレに細胞を播種し、80-90%コンフルエント時に0.05%トリプシン-EDTA溶液で細胞を剥離して継代を行った。培養は37℃、5%二酸化炭素、95%空気存在下で行った。
【0019】
(2)プレート播種
継代したSH-SY5Y細胞(継代数X+19〜25)を96wellプレート(96well マイクロテストプレート;FALCON(日本ベクトン・ディッキンソン株式会社))上に1.0〜1.5×105 cells / mLで播種し、一晩培養した。
【0020】
(3)試薬調製
6-Hydroxydopamineの調製
酸化ストレス誘因物質として6-Hydroxydopamine(6-OHDA)を用いた。6-OHDAを150mMになるよう蒸留水で調製し、最終濃度150μMになるよう培地に添加した。
【0021】
末粉抽出物の調製
日本製粉株式会社製の末粉を用いた。
末粉1gに対して水5mLを添加し、3分超音波処理を行った。遠心機で1000rpm×10分遠心後、上清を回収し、凍結乾燥を行い乾燥物を得た。以下水抽出物と呼ぶ。
【0022】
抽出物を3、10、30および100mg/mLになるよう蒸留水で調製し、それぞれ最終濃度が3、10、30および100μg/mLになるよう培地(通常培養培地6-OHDAを添加したもの)に添加した。
【0023】
(4)MTTアッセイ
MTT試薬の調製
3-[4、5-dimethylthiazol-2-yl]-2、5-diphenyltetrazolium bromide(MTT)をPBS(-)で5mg/mLになるよう調製し、0.45μmフィルター(アデバンテック東洋株式会社)で濾過したものをMTT溶液とした。MTT溶液は分注し、使用まで-20℃保存とした。使用時は、500μg/mLになるよう通常培養培地に添加した(MTT培地)。
【0024】
MTTアッセイ
6-OHDAおよび被験物質添加から15時間後、MTTアッセイを行った。
6-OHDAおよび被験物質添加培地からMTT培地に交換して3時間インキュベートした後、培地を除去し、dimethyl sulfoxideを添加した。沈殿したホルマザンを溶解させた後、570nmの吸光度を測定した。
【0025】
B.結果
測定結果を図1に示す。末粉水抽出物を6-OHDA 150μMと同時に添加した結果、末粉水抽出物は用量依存的に6-OHDAの酸化ストレスによるアポトーシスを抑制することが分かった。特に10μg/mL以上の濃度としたとき顕著なアポトーシス抑制効果が確認できた。
【0026】
<試験例2>
1.人工的脳梗塞モデルを用いた脳保護効果の確認試験
人工的に脳血流を遮断して脳梗塞モデルを作成して本発明の脳保護作用を確認した。
A.試験方法
(1)脳保護剤の調製と投与
試験例1で用いた抽出物を連続的に経口投与して脳保護効果を確認した。
試験用の脳保護剤は、あらかじめ1日分ずつ規定量を秤量・分注し、投与日および群を記載して-20℃に保存した。投与液の調製は用時調製とし、転倒混和にて、10、30、60mg/mLになるように溶解した。
【0027】
(2)試験動物
マウス,Slc:ddY,雄60匹を用いた。
入荷時:4週齢
手術・解剖時:7週齢
入荷時に種、系統、週齢、動物数及び性別を確認し、一般状態および外観を観察するとともに体重を測定した。馴化期間は7日間とした。
体重をもとに、各群に差がないよう群分けを行った。
【0028】
(3)試験系の環境条件
飼育環境
設定温度:25℃(許容範囲23〜27℃)、設定湿度:60%(許容範囲40〜80%)、照明:午前7時点灯、午後7時消灯の12時間に維持された福岡大学薬学部 動物飼育室で動物を飼育した。動物は、プラスチックケージを用いて、1ケージあたり5匹で飼育した。
飼料
固形飼料(CE-2、日本クレア株式会社)を給餌器に入れて自由に摂取させた。.
飲料水
フィルターで洗浄した水道水を給水瓶より自由に摂取させた。
【0029】
(4)投与方法・投与経路
胃ゾンデを用いた強制経口投与とした。また1日1回14日間投与した。投与液量は、最も近い測定体重値から換算して、10mL/kgで算出した。
【0030】
群構成および投与量
投与量(mg/kg) 使用動物数
対照群 0 15
100mg/kg群 100 15
300mg/kg群 300 15
600mg/kg群 600 15
【0031】
(5)脳梗塞モデルの作成
8-0ナイロンモノフィラメント(Ethilon; Ethicon, NJ, USA)を11mmの長さに切り、先端から4mmをシリコン樹脂(Xantopren; Bayer Dental, Osaka, Japan)でコーティングしたものを塞栓子として作成した。これを以下の手法でマウスに挿入して脳梗塞モデルを作成した。
手術方法
マウスに2% halothane吸入より麻酔を導入し、続いて1% halothane吸入によって麻酔を維持し手術台上に固定した。マウスの頚部の中央を切開し、左側総頸動脈と外頸動脈を結紮した。総頸動脈を切開し、塞栓子が中大脳動脈(MCA)の起始部に到達するように内頸動脈と外頸動脈の分岐部から内頸動脈を経由して9mm挿入した。再灌流は、塞栓子を手前に引き抜くことによって行った。MCA閉塞時間は4時間を負荷し、24時間後に行動観察(Neurological score)および2,3,5,-Triphenyltetrazolium chloride(TTC)染色を行い、梗塞巣体積の変化を測定した。
【0032】
(6)行動観察(Neurological score)
MCA閉塞4時間後再灌流を行い、その梗塞巣の変化を観察するためMCA閉塞24時間後に、脳梗塞のスコア付を行った。スコア付は以下の通り。
Score (0-5)
0: 運動機能に影響なし
1: 胴体の屈曲、前肢のlifting
2: 正常な姿勢でのcircling行動
3: 明らかな姿勢の異常でのcircling行動
4: Rolling行動
5: 自発的な行動がなく、体が傾く状態
【0033】
(7)TTC染色および画像解析
行動観察の後、マウスの頚椎を脱臼して、ただちに断頭した。取り出した脳を冷えた生理食塩水でよく冷し、アクリル製スライサー(マウス用Sagittal type スライス厚2mm;株式会社ニューロサイエンス;Fig. 3)を用いて、大脳皮質を含む脳の前額断スライスを2mm間隔で作製した。2%2,3,5,-triphenyltetrazolium chloride(シグマアルドリッチジャパン株式会社)を生理食塩水で作製し、切片を溶液中で37℃、30分間インキュベートした。
その後、スライドガラス上に並べ、デジタルスチルカメラ(MVC-FD91, SONY)で撮影した。梗塞巣体積は。割面の写真から梗塞総面積を画像解析ソフト(NIH Image 1.63)で測定し算出した。
【0034】
B.結果
図2に示すとおり、行動観察(Neurological score)の結果、用量依存的に脳梗塞に伴う障害発生が抑制された。4時間目までの行動は比較的活発であったが、末粉抽出物投与量に応じて、行動が活発であった。末粉抽出物600mg/Kg投与群ではNeurological scoreは2以下と良好であり、本発明の脳保護剤の効果が行動上も確認された。また24時間後の行動はいずれも悪化していたが、無投与群と比較して投与群の行動スコアは低く、脳梗塞の進行が抑制されていることが推測された。
また図3、図4に示すとおり脳梗塞巣の画像解析の結果用量依存的に脳梗塞巣の減少が認められた。特に600mg/Kg投与群では、脳梗塞部位は対照(無投与)群と比較して顕著であった。これは上記の行動観察の結果とよく対応していた。
以上の結果から本発明の脳保護剤は虚血性の脳梗塞による脳の障害を予防することが明らかとなった。
【特許請求の範囲】
【請求項1】
小麦末粉の抽出物を有効成分とする脳保護剤。
【請求項2】
脳保護が虚血性脳障害による予防用である請求項1記載の脳保護剤。
【請求項3】
脳保護が虚血に由来して発生するアポトーシス抑制によるものである請求項1又は請求項2記載の脳保護剤。
【請求項4】
経口剤である請求項1〜請求項3のいずれかに記載の脳保護剤
【請求項5】
請求項1〜請求項4のいずれかに記載の脳保護剤を含有する飲食品
【請求項1】
小麦末粉の抽出物を有効成分とする脳保護剤。
【請求項2】
脳保護が虚血性脳障害による予防用である請求項1記載の脳保護剤。
【請求項3】
脳保護が虚血に由来して発生するアポトーシス抑制によるものである請求項1又は請求項2記載の脳保護剤。
【請求項4】
経口剤である請求項1〜請求項3のいずれかに記載の脳保護剤
【請求項5】
請求項1〜請求項4のいずれかに記載の脳保護剤を含有する飲食品
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2013−71911(P2013−71911A)
【公開日】平成25年4月22日(2013.4.22)
【国際特許分類】
【出願番号】特願2011−212422(P2011−212422)
【出願日】平成23年9月28日(2011.9.28)
【出願人】(593106918)株式会社ファンケル (310)
【Fターム(参考)】
【公開日】平成25年4月22日(2013.4.22)
【国際特許分類】
【出願日】平成23年9月28日(2011.9.28)
【出願人】(593106918)株式会社ファンケル (310)
【Fターム(参考)】
[ Back to top ]

