脳活動測定装置
【課題】ニューロン活動異常部位の3次元識別化及びその処理時間の短縮化を実現する。
【解決手段】頭部の複数のセンサからの脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx、y又はz方向の電流成分を求め、その時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求めて全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し、各周波数バンク毎に隣接する平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから被験者のZスコアを求め、指定された水平面上の格子点に対応するを等高線マップ化する。
【解決手段】頭部の複数のセンサからの脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx、y又はz方向の電流成分を求め、その時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求めて全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し、各周波数バンク毎に隣接する平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから被験者のZスコアを求め、指定された水平面上の格子点に対応するを等高線マップ化する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は脳活動測定装置に関し、特に老人性痴呆障害等の脳疾患を判定するために脳活動状態を測定する装置に関するものである。
【背景技術】
【0002】
脳疾患、特に90歳では30%近くが認知症になっているという統計もあり、これからの高齢化社会にとって大きな問題になりつつある。
【0003】
これに伴い、このような認知障害をできるだけ早期に発見し、重度の認知状態に至る前にその治療を行うことが望まれているが、この認知症の判定装置としては、本発明者らが、被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個の脳電位センサと、各脳電位センサの出力信号中のアルファ波成分を数値データに変換して、各サンプリング時点についての双極子度を求め、該双極子度のピーク発生時点における等価双極子による脳電位と該測定脳電位との二乗誤差の一定時間範囲内の平均値およびバリアンスを各脳電位センサについて求め、これらの平均値又はバリアンスの頭皮上又はこれに対応する脳表面上の分布に関する等高線マップを作成する演算装置と、該等高線マップを出力する出力装置とを備えた脳活動測定装置、を既に提案している(例えば特許文献1参照。)。
【0004】
上記の特許文献1では、脳内のどこかにニューロン機能の低下が存在することを、アルファ波の脳電位分布を解析することにより検出しているため、下記の問題点がある。
イ) アルファ波をほとんど示さない人がかなり(10〜15%)の数に上る。
ロ) 開眼状態ではアルファ波は抑制されて非常に不安定である。
ハ) アルファ波は感性状態に大きく影響される。
ニ) アルファ波のみによる脳機能低下度計測は、脳機能低下部位を特定することができない。
【0005】
このように、特許文献1は、あくまでアルファ波に基づいた測定を行っているため、ニューロン機能低下部位を検出せず、脳疾患の度合が不明であり、また各種の治療によってどの部分のニューロン機能が回復したのかが不明である点に問題がある。
【0006】
そこで、本発明者らは先に、アルファ波に制限されること無く、脳疾患の度合と、ニューロン機能の低下/回復部分を明確に示すことができる脳活動測定装置を開発した(例えば特許文献2参照。)。
【0007】
すなわち、この時点で本発明者らは、大脳皮質内のニューロン機能が低下すると、ニューロン活動が不安定になることを発見した。この影響は局所的な脳電位パワーのゆらぎとして現れる(T.Musha, T.Asada, F.Yamashita, T.Kinoshita, H.Matsuda, M.Uno, Z.Chen and W.R.Shankle, "A new EEG method for estimating cortical neuronal impairment that is sensitive to early stage Alzheimer’s disease," Clinical Neurophysiology, 113 (2002) 1052-1058)。この性質はアルファ波に限らず、これより広い脳電位の周波数全域(例えば2〜40Hz)に及ぶことを確認した。
【0008】
これに基づいて開発された脳活動測定装置は、被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサと、各センサから出力された脳電位のアルファ波の周波数より広い所定周波数帯域を更に一定周波数幅を持った所定個数の周波数バンクに分割し、分割した各周波数バンクのデータを時間軸上で所定時間幅のセグメントに分割し、各セグメントについて求めた規格化パワーバリアンス(Normalized Power Variance:以下、単にNPVと称することがある。)間の平均値と、所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値及び標準偏差とから該被験者のZスコアを求め、全周波数バンクに亘る各脳電位センサについての該Zスコアの平均値を脳表面上にマップ化する演算装置とを備え、以てニューロンの局所的な機能低下マップを作成するものであった。
【0009】
このマップは、被験者の脳活動が正常者からどの位ズレているか、すなわちニューロン活動の「異常性」を示すため、被験者のZスコアを算出する。異常性には2種類あって、Zスコア>0であると、ニューロン活動のゆらぎが正常者集団よりも大きく、「不安定」となっていることを示し、これに対してZスコア<0であると、ニューロン活動が正常者集団よりも「不活発」となっていることを示すことができる。
【0010】
このようにして、瞬き等のアーチファクトおよび商用交流電源からの誘導を避けるために、2Hz〜40Hzの脳電位全てを対象にしたので、アルファ波より周波数領域を拡大でき、開眼・閉眼に拘わらずに適用できることになる。
【0011】
さらに、各種の脳疾患に関する標準テンプレートを臨床的に作成しておけば、それらの疾患に関する鑑別診断を行うことが出来、さらに、それぞれの脳疾患に対する治療効果の詳細をもこのマップの変化から知ることが出来るものであった。
【先行技術文献】
【特許文献】
【0012】
【特許文献1】特許第3581361号
【特許文献2】特許第4145344号
【発明の開示】
【発明が解決しようとする課題】
【0013】
しかしながら、上記の特許文献2では、下記のような問題点があった。
1)Zスコアは脳表面にマップ化されるだけであるので、ニューロン異常活動の脳表面からの深さだけが異なっている脳疾患の識別が困難である。
2)規格化パワーバリアンス(NPV)を計算する際に、頭皮上の各センサ(チャンネル)から得られる脳電位、すなわち脳電位の時系列データを高速フーリエ変換(FFT)によって周波数バンクに分け、それを逆高速フーリエ変換(IFFT)して時系列データに戻してからNPVを計算していたため、FFT演算と逆FFT演算の双方を実行することに伴って演算回数が過大になり、遅延時間が発生していた。従って、インターネット経由でサーバーによって集中的にデータ処理が行われるような場合には、システムの利用者数の増大によって回線の渋滞が予想され、以って信号処理が大幅に遅れてしまうことになる。
【0014】
従って、本発明は、ニューロン活動異常部位の3次元識別化及びその処理時間の短縮化を実現した脳活動測定装置を提供することを目的とする。
【課題を解決するための手段】
【0015】
本発明者は、セグメント毎に計算するNPVの値の統計的な変動が大きく、セグメントについて平均した後でも、信号対雑音比が1程度になり、この原因がセグメント毎にNPVを求めていることに原因があることを突き止めた。
【0016】
従って、本発明に係る脳活動測定装置は、被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサと、各センサから出力された脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx方向又は y方向又は z方向の電流成分或いは該電流成分の合成した電流の大きさを求め;各電流成分又は電流の大きさを時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求め、各フーリエ係数について全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し;各周波数バンク毎に該隣接するフーリエ係数の絶対値の二乗の平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての該規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のZスコアを求めるか、又は該正常者集団を基準とする代わりに該被験者の全格子点から得られる規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のYスコアを求め;指定された水平面上の格子点に対応する該ZスコアまたはYスコアを等高線マップ化する演算装置と、を備えたことを特徴とする。
【0017】
上記の所定周波数範囲は例えば2〜40Hzであり、該相互に隣接する複数が2個で0.78Hzの周波数帯域を含み、該セグメント幅は例えば2.56秒である。
【0018】
さらに本発明では、上記のセンサーを端末装置に設け、上記の演算装置を計算センターに設けると共に該端末装置と該計算センターとを通信回線を介して接続し、脳電位に関するデータが該計算センターにデータベースとして収集・蓄積され、該端末装置からは該データベースが参照できるようにすることができる。
【0019】
さらに本発明では、被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサから出力された脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx方向又は y方向又は z方向の電流成分或いは該電流成分の合成した電流の大きさを求め;各電流成分又は電流の大きさを時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求め、各フーリエ係数について全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し;各周波数バンク毎に該隣接するフーリエ係数の絶対値の二乗の平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての該規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のZスコアを求めるか、又は該正常者集団を基準とする代わりに該被験者の全格子点から得られる規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のYスコアを求め;指定された水平面上の格子点に対応する該ZスコアまたはYスコアを等高線マップ化する手順をコンピュータに実行させるためのプログラム、及びこのプログラムを記録したコンピュータ読み取り可能な記録媒体が提供される。
【発明の効果】
【0020】
本発明では、ニューロン活動の異常部位を脳内部に表示できるので、脳疾患診断を安価・非侵襲・高感度・高信頼度で実現できる。そのために中小の医療機関に普及することが期待される。このことは予防のために早期発見を必要とするアルツハイマー病の抑制手段にもなり、最近増加して来た鬱病や発達障害児の診断およびそのモニターとしても利用できるので、その社会的な役割は大きい。
【図面の簡単な説明】
【0021】
【図1】本発明に係る脳活動測定装置の構成実施例[1]を示したブロック図である。
【図2】本発明に係る脳活動測定装置の構成実施例[2]を示したブロック図である。
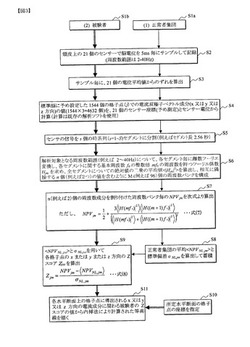
【図3】本発明に係る脳活動測定装置の動作実施例IとしてZスコアをマップ表示化する手順を示したフロチャート図である。
【図4】図3に示すフローチャートに対応してより分かり易く示したフロチャート図である。
【図5】本発明に係る脳活動測定装置の各動作実施例において使用する脳内格子点の配置例を示した図である。
【図6】本発明に係る脳活動測定装置の動作実施例1で得られる或る水平面上の各格子点におけるx方向電流成分のZスコアの等高線マップ図である。
【図7】本発明に係る脳活動測定装置の動作実施例1で得られる或る水平面上の各格子点におけるy方向電流成分のZスコアの等高線マップ図である。
【図8】本発明に係る脳活動測定装置の動作実施例1で得られる或る水平面上の各格子点におけるz方向電流成分のZスコアの等高線マップ図である。
【図9】本発明に係る脳活動測定装置の動作実施例2で得られる或る水平面上の各格子点におけるx、y、z方向電流成分を合成した電流の大きさについて求めたZスコアをマップ表示化する手順を示したフロチャート図である。
【図10】本発明に係る脳活動測定装置の動作実施例2で得られる或る水平面上の各格子点におけるx、y、z方向電流成分を合成した電流の大きさについて求めたZスコアの等高線マップ図である。
【図11】本発明に係る脳活動測定装置の動作実施例3としてYスコアをマップ表示化する手順を示したフロチャート図である。
【発明を実施するための最良の形態】
【0022】
*構成実施例:図1及び図2
図1は、本発明に係る脳活動測定装置の構成実施例[1]示したものである。この構成例では、まず、頭部1に例えば21個前後の脳電位センサ又は脳磁センサ(電極とも称するが、以下、センサで総称することがある。)21〜221(以下、符号2で総称することがある)を装着して脳内神経活動に基づく脳電位を測定するか、或いは、予めこれらのセンサを配置したキャップ又はヘルメットを被る。なお、この場合のセンサ2は、International 10-20 standardによって決められた位置に配置するとともに、基準電位として、例えば右耳朶にもセンサ(図示せず)を装着する。
【0023】
センサ2で測定された脳電位は増幅器3及びマルチプレクサ4を介してアナログ/ディジタル変換器(A/D)5に供給され、ディジタル化された測定脳電位)データは入力インタフェース(I/F)15を介してコンピュータ10に供給される。なお、入力インタフェース15では該データをそのまま通過させてもよいし、或いは予め指定した周波数帯域(例えばアルファ波の周波数より広い所定の周波数帯域)を持つ成分のみをディジタル・フィルタリング処理を行ってから出力してもよい。
【0024】
コンピュータ10内では、CPU11がバス12を介してROM13、RAM14、入力インタフェース15、及び出力インタフェース16に接続されている。上記ROM13は読取専用の記憶媒体であり、RAM14は、キーボード24及びA/D変換器5からの脳電位データを演算時に記憶するメモリである。
【0025】
また、入力インタフェース15には、プログラム等を格納した外部記憶装置25が接続され、出力インタフェース16にはコンピュータ10の演算結果を表示するCRT等の表示装置31と、この表示装置31に表示されるデータや波形を記憶するプリンタ32が出力装置として接続されている。なお、外部記憶装置25は用いずに、全てROM13にプログラム等を予め格納しておいてもよい。
【0026】
ここで、上記の脳電位データは、図2の構成実施例例[2]に示すように、データ転送端末装置として動作する臨床現場のコンピュータ10のインタフェース17から、インターネット等の通信回線41を経由して演算装置としての計算センター42に送り、ここで解析した結果を再び通信回線41を経由してコンピュータ10に送り返し、CRT31又はプリンタ32などの出力装置において出力し、医師が診断の材料とするように構成してもよい。この場合は、サーバ装置、プログラムと記録媒体は計算センター42に装備され、サーバ装置等で脳電位、すなわち脳電位に関するデータを収集・蓄積し、特定の脳疾患に関するデータが蓄積される。コンピュータ10からはデータベース化された特定の脳疾患ごとのデータが参照できる。
【0027】
以下、ニューロン異常性表示マップの生成と異常性識別の動作実施例を図3〜図11を参照して説明する。
*動作実施例1:或る水平面上の各格子点におけるx方向(又はy方向又はz方向)電流成分のZスコアの等高線マップ表示例(図3〜図8)
上述の構成例における動作例1を、図3及びこれに対応して別の角度で示した図4のフローチャートに沿って以下に説明する。なお、頭部1に示されたセンサ群2を配置した後、図示しない電源を投入してコンピュータ10を初期状態に設定しておく。また、頭部1に載置した21個のセンサ21〜221から脳内神経活動に基づく脳電位の測定を一定のサンプリング時間間隔で行う。
(1)正常者集団のデータベースの作成(実線矢印ルート)
ステップS1a, S2:
まず、既存の認知機能を評価するためのミニ・メンタル・ステート検査(MMSE)法や画像検査によるMRI(Magnetic Resonance Imaging)やSPECT(Single Photon Emission Computing Tomography)測定等で予め一定人数の正常者集団を決めておき、一人づつセンサ2から脳電位(頭皮上電位)を測定する。
【0028】
この場合、各センサ21〜221の電位信号は5ms毎にサンプリングする。周波数範囲は、バンドパスフィルタ処理により、α波の周波数帯域より広い一定の周波数帯域(例えば2〜40Hz)とする。
【0029】
ステップS3:
サンプル毎に21個の脳電位平均がゼロになるように各測定値から定数を引いておくことにより、21個の脳電位平均値からのずれを算出する。
【0030】
ステップS4:
図5(1)~(3)に示すように、標準脳に予め設定した1544個の格子点(j)を設定する。これは、予め3層の頭蓋モデル(標準脳を「頭蓋骨」、「脳脊髄液層」、「脳組織」の3つの幾何学的領域に分け、それらの導電率を1/80:3:1とする)を構成しておき、標準頭部モデル内に、1cm間隔の立方格子を組み立て、その位置座標を決定すると格子点の数は1544個になる。そして各格子点での電流双極子(以下単に電流と言う)ベクトル成分(x又はy又はz方向)の値(1544×3=4632個)を、予め測定した21個のセンサー座標とセンサ21〜221の測定脳電位から計算する。
【0031】
このように頭皮上の電位分布から脳内の起電力の3次元的な分布を計算する方法はsLORETA, eLORETA (Low ResolutionBrain Electromagnetic Tomography)として,
そのアルゴリズムが公開されている。
【0032】
このLORETAの出力データの処理は、全格子点jで1544個×3 (x,y,z)=4632回実行される。
【0033】
ステップS5:
センサ(チャンネル)の信号時系列を時間軸上でs(例えばs=70)個のセグメントに分割する。この場合のセグメント長は2.56秒(=5ms×512)である。
ステップS6:
解析対象となる周波数範囲(例えば2〜40Hz)について、各セグメント毎に離散フーリエ変換し(ステップS6a)、各セグメントに関する基本周波数f0の整数倍mf0の周波数を持つフーリエ係数Hjmを求め(同)、全セグメントに亘っての絶対値の二乗の平均値<|Hjm|2>を算出し(ステップS6b)、相互に隣接するn個(例えば2つ)の値を含むようにM (例えば96)個の周波数バンクを構成する(ステップS6c)。
【0034】
例えば上記の如くサンプリング周波数200Hz(5ms)、2.56秒のセグメント長とすると、離散化された周波数は基本周波数f0 (=1/2.56=0.39 Hz)の整数倍となり、最低周波数のバンク#1には6f0=2.34Hzと7f0=2.73Hz、その次のバンクには7f0と8f0が入り、最高周波数のバンク#96には101f0 =39.41Hzと102f0=39.8Hzが分配され、全部で96の周波数バンクに分割される。
【0035】
ステップS7:
上記のとおり2個づつ周波数成分を割り付けた各周波数バンク#1〜#96について、各格子点jと各周波数バンクm(本例ではmは“6”から始まり、周波数バンク#1がm=6に対応する)を指定したときの規格化パワーバリアンスNPVjmを算出してRAM14に格納する。このNPVjmの算出過程は次の通りである。
【0036】
長さT secの一つセグメントがN 個のデータサンプルを含む、xn 、n= 0 ~ N - 1をフーリエ展開する。フーリエ係数をHmとする。周波数はmf0 でf0 = 1/Tは基本周波数。
【0037】
【数1】

【0038】
ここで
【0039】
【数2】

【0040】
式(1)において、周波数成分を2個だけ、つまりmf0 と (m+1)f0 のみを残すと、 n番目のサンプルデータは次のようになる。
【0041】
【数3】

【0042】
cc は複素共役項の意味である。すべてのセグメントに亘って平均すると
【0043】
【数4】

【0044】
同様にして
【0045】
【数5】

【0046】
一方、NPVは下式で表される。
【0047】
【数6】

【0048】
したがって、式(4)及び(5)を式(6)に代入すると、次式(7)を得る。
【0049】
【数7】

【0050】
ステップS8:
上記のステップS1a〜S7を全ての正常者に対して繰り返すことにより、正常者集団についての群平均<NPV NL,jm>と群の内部での標準偏差σNL,jmを計算し、その結果をデータベースとしてRAM14に格納する。
(2)被験者のZスコアマップの作成(二重実線矢印ルート)
ステップS1b:
被験者に装着したセンサ2からの脳電位を測定する。
【0051】
ステップS2〜S7:
上記の正常者集団の場合と同様にステップS2〜S7を実行して、被験者の規格化パワーバリアンスNPVjmを算出する。
【0052】
ステップS9:
被験者のZスコアを、被験者の規格化パワーバリアンスNPVjmと正常者集団の平均規格化パワーバリアンス<NPV NL,jm>と標準偏差σNL,jmとから次式に従って求める。
【0053】
【数8】

【0054】
ステップS10:
頭部の標準モデルについて、指定された格子点を含むように1 cm間隔の水平断面の形状と格子点の座標を指定する。
【0055】
ステップS11:
各水平断面上の格子点に導出されるx方向又はy方向又はz方向の電流に関わる被験者のZスコアの値から内挿法により計算された等高線を描く。
【0056】
x方向の等高線が図6に示されており、y方向の等高線が図7に、そしてz方向の等高線が図8に示されている。いずれも脳の水平面をスライスしたときの垂直方向の位置をzで示している。
【0057】
この等高線の判断は、画像図において白くなればなるほどZスコアのプラスの値が大きくなり、黒くなればなるほどZスコアのマイナス値が大きくなってニューロンの異常部位であることを示す。
【0058】
すなわち、Zスコアがマイナスの値を取るのは規格化パワーバリアンスNPVjが正常者集団の格子点jに関する平均値<NPVj>よりも小さい値を取る場合である。つまり被験者の格子点のパワー変動が正常者の対応する格子点jのパワーゆらぎよりも小さいことを意味しており、正常者よりもニューロン活動が不活発になっているという異常性を表している。
【0059】
逆に、Zスコアのプラスの値は、ニューロン活動のゆらぎが正常者集団よりも大きく「不安定」となっているという異常性を表わしている。そして、絶対値が大きければ大きい程異常性を示す。
<計算処理の高速化の説明>
各セグメントが、図4のステップS6cに示すように2つのフーリエ係数Hf1, Hf2だけを含む場合に、セグメント毎のNPVは、式(7)で示す如く計算される。この場合にはこれら2つのフーリエ係数を逆フーリエ変換により時系列に変化する場合に比べて計算時間は約1%に短縮される。
【0060】
本発明の場合、周波数バンクが2個の周波数成分(フーリエ係数の絶対値の二乗のセグメント間平均値)を含む場合には、5分間の時系列データは約117個のセグメントに分割され、フーリエ係数から直接にNPV値が算出できるため、逆FFT演算を行わなくて良く、FFT演算回数は117回となり、上記の特許文献2の場合、NPV計算はFFT演算後、逆FFT演算を行う必要があるので、特許文献2に比べて著しく演算処理時間が短縮されることになる。
【0061】
さらに本発明では、フーリエ係数の絶対値の二乗値が70個のセグメントに亘って平均化されてから、それを用いてNPVが計算されるので、NPVの中に含まれている相対的な統計的なノイズは(117)−0.5倍、つまり10%に縮小される。一方で、フーリエ係数の持つ相対的なノイズは、上記の式(7)から、フーリエ係数に内在する相対ノイズの8倍であるから、NPVに内在する相対ノイズは、フーリエ係数に内在するノイズの2×8=16倍にも達することとなり、ノイズ削減効果も大きい。
*動作実施例2:或る水平面上の各格子点におけるx方向とy方向とz方向の合成電流の大きさのZスコアの等高線マップ表示例(図9及び図10)
本実施例と上記の動作実施例1との違いは、図3のフローチャートにおけるステップS4が、図9ではステップS4aに置き換わっている点である。
【0062】
すなわち、実施例1の場合には、各水平断面上の格子点に導出されるx方向又はy方向又はz方向の電流成分に関わる被験者のZスコアの値から図6〜図8に示す等高線マップを得たが、本実施例2の場合には、各格子点におけるx方向とy方向とz方向の合成電流の大きさからZスコアを求めて等高線マップを表示した点が異なっている。従って、図4の出力データの処理は1544回である。その他は実施例1と同様である。
*動作実施例3:或る水平面上の各格子点におけるx方向(又はy方向又はz方向)電流成分のYスコアの等高線マップ表示例(図11)
本実施例と上記の動作実施例1との違いは、図3のフローチャートにおけるステップS9が、図11ではステップS9aに置き換わっている点である。
【0063】
すなわち、実施例1の場合には、各水平断面上の格子点に導出されるx方向又はy方向又はz方向の電流成分に関わる被験者のZスコアの値から図6〜図8に示す等高線マップを得たが、本実施例3の場合には、各格子点におけるx方向又はy方向又はz方向の電流成分に関わる被験者の「Yスコア」を求めて等高線マップを生成する点が異なっている。その他は実施例1と同様である。ただし、生成される等高線マップ自体は実施例1の等高線マップとは異なるが、ここでは図示を省略した。
【0064】
この実施例におけるYスコアYjmとは、各格子点におけるNPVjmの平均値<NPV ,jm>と標準偏差σjmとから次式の如く算出されるものである。
【0065】
【数9】

【0066】
*動作実施例4:或る水平面上の各格子点におけるx方向とy方向とz方向の合成電流の大きさのYスコアの等高線マップ表示例(図示せず)
本実施例と上記の動作実施例2との違いは、図9のフローチャートにおけるZスコアの生成ステップS9の変わりに被験者の「Yスコア」を求めて等高線マップを生成する点が異なっているのみである。その等高線マップは、ここでは図示を省略した。
【0067】
なお、本発明は、上記実施例によって限定されるものではなく、特許請求の範囲の記載に基づき、当業者によって種々の変更が可能であり、脳疾患としての鬱病等に対しても適用可能なことは明らかである。
【符号の説明】
【0068】
1 被験者の頭部
2, 21〜221 脳電位(脳磁)センサ
3 増幅器
4 マルチプレクサ
5 A/D変換器
10 コンピュータ
11 CPU
13 ROM
14 RAM
15, 16, 17 インタフェース
24 キーボード
25 外部記憶装置
31 CRT
32 プリンタ
41 通信回線
42 計算センター
図中、同一符号は同一又は相当部分を示す。
【技術分野】
【0001】
本発明は脳活動測定装置に関し、特に老人性痴呆障害等の脳疾患を判定するために脳活動状態を測定する装置に関するものである。
【背景技術】
【0002】
脳疾患、特に90歳では30%近くが認知症になっているという統計もあり、これからの高齢化社会にとって大きな問題になりつつある。
【0003】
これに伴い、このような認知障害をできるだけ早期に発見し、重度の認知状態に至る前にその治療を行うことが望まれているが、この認知症の判定装置としては、本発明者らが、被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個の脳電位センサと、各脳電位センサの出力信号中のアルファ波成分を数値データに変換して、各サンプリング時点についての双極子度を求め、該双極子度のピーク発生時点における等価双極子による脳電位と該測定脳電位との二乗誤差の一定時間範囲内の平均値およびバリアンスを各脳電位センサについて求め、これらの平均値又はバリアンスの頭皮上又はこれに対応する脳表面上の分布に関する等高線マップを作成する演算装置と、該等高線マップを出力する出力装置とを備えた脳活動測定装置、を既に提案している(例えば特許文献1参照。)。
【0004】
上記の特許文献1では、脳内のどこかにニューロン機能の低下が存在することを、アルファ波の脳電位分布を解析することにより検出しているため、下記の問題点がある。
イ) アルファ波をほとんど示さない人がかなり(10〜15%)の数に上る。
ロ) 開眼状態ではアルファ波は抑制されて非常に不安定である。
ハ) アルファ波は感性状態に大きく影響される。
ニ) アルファ波のみによる脳機能低下度計測は、脳機能低下部位を特定することができない。
【0005】
このように、特許文献1は、あくまでアルファ波に基づいた測定を行っているため、ニューロン機能低下部位を検出せず、脳疾患の度合が不明であり、また各種の治療によってどの部分のニューロン機能が回復したのかが不明である点に問題がある。
【0006】
そこで、本発明者らは先に、アルファ波に制限されること無く、脳疾患の度合と、ニューロン機能の低下/回復部分を明確に示すことができる脳活動測定装置を開発した(例えば特許文献2参照。)。
【0007】
すなわち、この時点で本発明者らは、大脳皮質内のニューロン機能が低下すると、ニューロン活動が不安定になることを発見した。この影響は局所的な脳電位パワーのゆらぎとして現れる(T.Musha, T.Asada, F.Yamashita, T.Kinoshita, H.Matsuda, M.Uno, Z.Chen and W.R.Shankle, "A new EEG method for estimating cortical neuronal impairment that is sensitive to early stage Alzheimer’s disease," Clinical Neurophysiology, 113 (2002) 1052-1058)。この性質はアルファ波に限らず、これより広い脳電位の周波数全域(例えば2〜40Hz)に及ぶことを確認した。
【0008】
これに基づいて開発された脳活動測定装置は、被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサと、各センサから出力された脳電位のアルファ波の周波数より広い所定周波数帯域を更に一定周波数幅を持った所定個数の周波数バンクに分割し、分割した各周波数バンクのデータを時間軸上で所定時間幅のセグメントに分割し、各セグメントについて求めた規格化パワーバリアンス(Normalized Power Variance:以下、単にNPVと称することがある。)間の平均値と、所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値及び標準偏差とから該被験者のZスコアを求め、全周波数バンクに亘る各脳電位センサについての該Zスコアの平均値を脳表面上にマップ化する演算装置とを備え、以てニューロンの局所的な機能低下マップを作成するものであった。
【0009】
このマップは、被験者の脳活動が正常者からどの位ズレているか、すなわちニューロン活動の「異常性」を示すため、被験者のZスコアを算出する。異常性には2種類あって、Zスコア>0であると、ニューロン活動のゆらぎが正常者集団よりも大きく、「不安定」となっていることを示し、これに対してZスコア<0であると、ニューロン活動が正常者集団よりも「不活発」となっていることを示すことができる。
【0010】
このようにして、瞬き等のアーチファクトおよび商用交流電源からの誘導を避けるために、2Hz〜40Hzの脳電位全てを対象にしたので、アルファ波より周波数領域を拡大でき、開眼・閉眼に拘わらずに適用できることになる。
【0011】
さらに、各種の脳疾患に関する標準テンプレートを臨床的に作成しておけば、それらの疾患に関する鑑別診断を行うことが出来、さらに、それぞれの脳疾患に対する治療効果の詳細をもこのマップの変化から知ることが出来るものであった。
【先行技術文献】
【特許文献】
【0012】
【特許文献1】特許第3581361号
【特許文献2】特許第4145344号
【発明の開示】
【発明が解決しようとする課題】
【0013】
しかしながら、上記の特許文献2では、下記のような問題点があった。
1)Zスコアは脳表面にマップ化されるだけであるので、ニューロン異常活動の脳表面からの深さだけが異なっている脳疾患の識別が困難である。
2)規格化パワーバリアンス(NPV)を計算する際に、頭皮上の各センサ(チャンネル)から得られる脳電位、すなわち脳電位の時系列データを高速フーリエ変換(FFT)によって周波数バンクに分け、それを逆高速フーリエ変換(IFFT)して時系列データに戻してからNPVを計算していたため、FFT演算と逆FFT演算の双方を実行することに伴って演算回数が過大になり、遅延時間が発生していた。従って、インターネット経由でサーバーによって集中的にデータ処理が行われるような場合には、システムの利用者数の増大によって回線の渋滞が予想され、以って信号処理が大幅に遅れてしまうことになる。
【0014】
従って、本発明は、ニューロン活動異常部位の3次元識別化及びその処理時間の短縮化を実現した脳活動測定装置を提供することを目的とする。
【課題を解決するための手段】
【0015】
本発明者は、セグメント毎に計算するNPVの値の統計的な変動が大きく、セグメントについて平均した後でも、信号対雑音比が1程度になり、この原因がセグメント毎にNPVを求めていることに原因があることを突き止めた。
【0016】
従って、本発明に係る脳活動測定装置は、被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサと、各センサから出力された脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx方向又は y方向又は z方向の電流成分或いは該電流成分の合成した電流の大きさを求め;各電流成分又は電流の大きさを時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求め、各フーリエ係数について全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し;各周波数バンク毎に該隣接するフーリエ係数の絶対値の二乗の平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての該規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のZスコアを求めるか、又は該正常者集団を基準とする代わりに該被験者の全格子点から得られる規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のYスコアを求め;指定された水平面上の格子点に対応する該ZスコアまたはYスコアを等高線マップ化する演算装置と、を備えたことを特徴とする。
【0017】
上記の所定周波数範囲は例えば2〜40Hzであり、該相互に隣接する複数が2個で0.78Hzの周波数帯域を含み、該セグメント幅は例えば2.56秒である。
【0018】
さらに本発明では、上記のセンサーを端末装置に設け、上記の演算装置を計算センターに設けると共に該端末装置と該計算センターとを通信回線を介して接続し、脳電位に関するデータが該計算センターにデータベースとして収集・蓄積され、該端末装置からは該データベースが参照できるようにすることができる。
【0019】
さらに本発明では、被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサから出力された脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx方向又は y方向又は z方向の電流成分或いは該電流成分の合成した電流の大きさを求め;各電流成分又は電流の大きさを時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求め、各フーリエ係数について全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し;各周波数バンク毎に該隣接するフーリエ係数の絶対値の二乗の平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての該規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のZスコアを求めるか、又は該正常者集団を基準とする代わりに該被験者の全格子点から得られる規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のYスコアを求め;指定された水平面上の格子点に対応する該ZスコアまたはYスコアを等高線マップ化する手順をコンピュータに実行させるためのプログラム、及びこのプログラムを記録したコンピュータ読み取り可能な記録媒体が提供される。
【発明の効果】
【0020】
本発明では、ニューロン活動の異常部位を脳内部に表示できるので、脳疾患診断を安価・非侵襲・高感度・高信頼度で実現できる。そのために中小の医療機関に普及することが期待される。このことは予防のために早期発見を必要とするアルツハイマー病の抑制手段にもなり、最近増加して来た鬱病や発達障害児の診断およびそのモニターとしても利用できるので、その社会的な役割は大きい。
【図面の簡単な説明】
【0021】
【図1】本発明に係る脳活動測定装置の構成実施例[1]を示したブロック図である。
【図2】本発明に係る脳活動測定装置の構成実施例[2]を示したブロック図である。
【図3】本発明に係る脳活動測定装置の動作実施例IとしてZスコアをマップ表示化する手順を示したフロチャート図である。
【図4】図3に示すフローチャートに対応してより分かり易く示したフロチャート図である。
【図5】本発明に係る脳活動測定装置の各動作実施例において使用する脳内格子点の配置例を示した図である。
【図6】本発明に係る脳活動測定装置の動作実施例1で得られる或る水平面上の各格子点におけるx方向電流成分のZスコアの等高線マップ図である。
【図7】本発明に係る脳活動測定装置の動作実施例1で得られる或る水平面上の各格子点におけるy方向電流成分のZスコアの等高線マップ図である。
【図8】本発明に係る脳活動測定装置の動作実施例1で得られる或る水平面上の各格子点におけるz方向電流成分のZスコアの等高線マップ図である。
【図9】本発明に係る脳活動測定装置の動作実施例2で得られる或る水平面上の各格子点におけるx、y、z方向電流成分を合成した電流の大きさについて求めたZスコアをマップ表示化する手順を示したフロチャート図である。
【図10】本発明に係る脳活動測定装置の動作実施例2で得られる或る水平面上の各格子点におけるx、y、z方向電流成分を合成した電流の大きさについて求めたZスコアの等高線マップ図である。
【図11】本発明に係る脳活動測定装置の動作実施例3としてYスコアをマップ表示化する手順を示したフロチャート図である。
【発明を実施するための最良の形態】
【0022】
*構成実施例:図1及び図2
図1は、本発明に係る脳活動測定装置の構成実施例[1]示したものである。この構成例では、まず、頭部1に例えば21個前後の脳電位センサ又は脳磁センサ(電極とも称するが、以下、センサで総称することがある。)21〜221(以下、符号2で総称することがある)を装着して脳内神経活動に基づく脳電位を測定するか、或いは、予めこれらのセンサを配置したキャップ又はヘルメットを被る。なお、この場合のセンサ2は、International 10-20 standardによって決められた位置に配置するとともに、基準電位として、例えば右耳朶にもセンサ(図示せず)を装着する。
【0023】
センサ2で測定された脳電位は増幅器3及びマルチプレクサ4を介してアナログ/ディジタル変換器(A/D)5に供給され、ディジタル化された測定脳電位)データは入力インタフェース(I/F)15を介してコンピュータ10に供給される。なお、入力インタフェース15では該データをそのまま通過させてもよいし、或いは予め指定した周波数帯域(例えばアルファ波の周波数より広い所定の周波数帯域)を持つ成分のみをディジタル・フィルタリング処理を行ってから出力してもよい。
【0024】
コンピュータ10内では、CPU11がバス12を介してROM13、RAM14、入力インタフェース15、及び出力インタフェース16に接続されている。上記ROM13は読取専用の記憶媒体であり、RAM14は、キーボード24及びA/D変換器5からの脳電位データを演算時に記憶するメモリである。
【0025】
また、入力インタフェース15には、プログラム等を格納した外部記憶装置25が接続され、出力インタフェース16にはコンピュータ10の演算結果を表示するCRT等の表示装置31と、この表示装置31に表示されるデータや波形を記憶するプリンタ32が出力装置として接続されている。なお、外部記憶装置25は用いずに、全てROM13にプログラム等を予め格納しておいてもよい。
【0026】
ここで、上記の脳電位データは、図2の構成実施例例[2]に示すように、データ転送端末装置として動作する臨床現場のコンピュータ10のインタフェース17から、インターネット等の通信回線41を経由して演算装置としての計算センター42に送り、ここで解析した結果を再び通信回線41を経由してコンピュータ10に送り返し、CRT31又はプリンタ32などの出力装置において出力し、医師が診断の材料とするように構成してもよい。この場合は、サーバ装置、プログラムと記録媒体は計算センター42に装備され、サーバ装置等で脳電位、すなわち脳電位に関するデータを収集・蓄積し、特定の脳疾患に関するデータが蓄積される。コンピュータ10からはデータベース化された特定の脳疾患ごとのデータが参照できる。
【0027】
以下、ニューロン異常性表示マップの生成と異常性識別の動作実施例を図3〜図11を参照して説明する。
*動作実施例1:或る水平面上の各格子点におけるx方向(又はy方向又はz方向)電流成分のZスコアの等高線マップ表示例(図3〜図8)
上述の構成例における動作例1を、図3及びこれに対応して別の角度で示した図4のフローチャートに沿って以下に説明する。なお、頭部1に示されたセンサ群2を配置した後、図示しない電源を投入してコンピュータ10を初期状態に設定しておく。また、頭部1に載置した21個のセンサ21〜221から脳内神経活動に基づく脳電位の測定を一定のサンプリング時間間隔で行う。
(1)正常者集団のデータベースの作成(実線矢印ルート)
ステップS1a, S2:
まず、既存の認知機能を評価するためのミニ・メンタル・ステート検査(MMSE)法や画像検査によるMRI(Magnetic Resonance Imaging)やSPECT(Single Photon Emission Computing Tomography)測定等で予め一定人数の正常者集団を決めておき、一人づつセンサ2から脳電位(頭皮上電位)を測定する。
【0028】
この場合、各センサ21〜221の電位信号は5ms毎にサンプリングする。周波数範囲は、バンドパスフィルタ処理により、α波の周波数帯域より広い一定の周波数帯域(例えば2〜40Hz)とする。
【0029】
ステップS3:
サンプル毎に21個の脳電位平均がゼロになるように各測定値から定数を引いておくことにより、21個の脳電位平均値からのずれを算出する。
【0030】
ステップS4:
図5(1)~(3)に示すように、標準脳に予め設定した1544個の格子点(j)を設定する。これは、予め3層の頭蓋モデル(標準脳を「頭蓋骨」、「脳脊髄液層」、「脳組織」の3つの幾何学的領域に分け、それらの導電率を1/80:3:1とする)を構成しておき、標準頭部モデル内に、1cm間隔の立方格子を組み立て、その位置座標を決定すると格子点の数は1544個になる。そして各格子点での電流双極子(以下単に電流と言う)ベクトル成分(x又はy又はz方向)の値(1544×3=4632個)を、予め測定した21個のセンサー座標とセンサ21〜221の測定脳電位から計算する。
【0031】
このように頭皮上の電位分布から脳内の起電力の3次元的な分布を計算する方法はsLORETA, eLORETA (Low ResolutionBrain Electromagnetic Tomography)として,
そのアルゴリズムが公開されている。
【0032】
このLORETAの出力データの処理は、全格子点jで1544個×3 (x,y,z)=4632回実行される。
【0033】
ステップS5:
センサ(チャンネル)の信号時系列を時間軸上でs(例えばs=70)個のセグメントに分割する。この場合のセグメント長は2.56秒(=5ms×512)である。
ステップS6:
解析対象となる周波数範囲(例えば2〜40Hz)について、各セグメント毎に離散フーリエ変換し(ステップS6a)、各セグメントに関する基本周波数f0の整数倍mf0の周波数を持つフーリエ係数Hjmを求め(同)、全セグメントに亘っての絶対値の二乗の平均値<|Hjm|2>を算出し(ステップS6b)、相互に隣接するn個(例えば2つ)の値を含むようにM (例えば96)個の周波数バンクを構成する(ステップS6c)。
【0034】
例えば上記の如くサンプリング周波数200Hz(5ms)、2.56秒のセグメント長とすると、離散化された周波数は基本周波数f0 (=1/2.56=0.39 Hz)の整数倍となり、最低周波数のバンク#1には6f0=2.34Hzと7f0=2.73Hz、その次のバンクには7f0と8f0が入り、最高周波数のバンク#96には101f0 =39.41Hzと102f0=39.8Hzが分配され、全部で96の周波数バンクに分割される。
【0035】
ステップS7:
上記のとおり2個づつ周波数成分を割り付けた各周波数バンク#1〜#96について、各格子点jと各周波数バンクm(本例ではmは“6”から始まり、周波数バンク#1がm=6に対応する)を指定したときの規格化パワーバリアンスNPVjmを算出してRAM14に格納する。このNPVjmの算出過程は次の通りである。
【0036】
長さT secの一つセグメントがN 個のデータサンプルを含む、xn 、n= 0 ~ N - 1をフーリエ展開する。フーリエ係数をHmとする。周波数はmf0 でf0 = 1/Tは基本周波数。
【0037】
【数1】

【0038】
ここで
【0039】
【数2】

【0040】
式(1)において、周波数成分を2個だけ、つまりmf0 と (m+1)f0 のみを残すと、 n番目のサンプルデータは次のようになる。
【0041】
【数3】

【0042】
cc は複素共役項の意味である。すべてのセグメントに亘って平均すると
【0043】
【数4】

【0044】
同様にして
【0045】
【数5】

【0046】
一方、NPVは下式で表される。
【0047】
【数6】

【0048】
したがって、式(4)及び(5)を式(6)に代入すると、次式(7)を得る。
【0049】
【数7】

【0050】
ステップS8:
上記のステップS1a〜S7を全ての正常者に対して繰り返すことにより、正常者集団についての群平均<NPV NL,jm>と群の内部での標準偏差σNL,jmを計算し、その結果をデータベースとしてRAM14に格納する。
(2)被験者のZスコアマップの作成(二重実線矢印ルート)
ステップS1b:
被験者に装着したセンサ2からの脳電位を測定する。
【0051】
ステップS2〜S7:
上記の正常者集団の場合と同様にステップS2〜S7を実行して、被験者の規格化パワーバリアンスNPVjmを算出する。
【0052】
ステップS9:
被験者のZスコアを、被験者の規格化パワーバリアンスNPVjmと正常者集団の平均規格化パワーバリアンス<NPV NL,jm>と標準偏差σNL,jmとから次式に従って求める。
【0053】
【数8】

【0054】
ステップS10:
頭部の標準モデルについて、指定された格子点を含むように1 cm間隔の水平断面の形状と格子点の座標を指定する。
【0055】
ステップS11:
各水平断面上の格子点に導出されるx方向又はy方向又はz方向の電流に関わる被験者のZスコアの値から内挿法により計算された等高線を描く。
【0056】
x方向の等高線が図6に示されており、y方向の等高線が図7に、そしてz方向の等高線が図8に示されている。いずれも脳の水平面をスライスしたときの垂直方向の位置をzで示している。
【0057】
この等高線の判断は、画像図において白くなればなるほどZスコアのプラスの値が大きくなり、黒くなればなるほどZスコアのマイナス値が大きくなってニューロンの異常部位であることを示す。
【0058】
すなわち、Zスコアがマイナスの値を取るのは規格化パワーバリアンスNPVjが正常者集団の格子点jに関する平均値<NPVj>よりも小さい値を取る場合である。つまり被験者の格子点のパワー変動が正常者の対応する格子点jのパワーゆらぎよりも小さいことを意味しており、正常者よりもニューロン活動が不活発になっているという異常性を表している。
【0059】
逆に、Zスコアのプラスの値は、ニューロン活動のゆらぎが正常者集団よりも大きく「不安定」となっているという異常性を表わしている。そして、絶対値が大きければ大きい程異常性を示す。
<計算処理の高速化の説明>
各セグメントが、図4のステップS6cに示すように2つのフーリエ係数Hf1, Hf2だけを含む場合に、セグメント毎のNPVは、式(7)で示す如く計算される。この場合にはこれら2つのフーリエ係数を逆フーリエ変換により時系列に変化する場合に比べて計算時間は約1%に短縮される。
【0060】
本発明の場合、周波数バンクが2個の周波数成分(フーリエ係数の絶対値の二乗のセグメント間平均値)を含む場合には、5分間の時系列データは約117個のセグメントに分割され、フーリエ係数から直接にNPV値が算出できるため、逆FFT演算を行わなくて良く、FFT演算回数は117回となり、上記の特許文献2の場合、NPV計算はFFT演算後、逆FFT演算を行う必要があるので、特許文献2に比べて著しく演算処理時間が短縮されることになる。
【0061】
さらに本発明では、フーリエ係数の絶対値の二乗値が70個のセグメントに亘って平均化されてから、それを用いてNPVが計算されるので、NPVの中に含まれている相対的な統計的なノイズは(117)−0.5倍、つまり10%に縮小される。一方で、フーリエ係数の持つ相対的なノイズは、上記の式(7)から、フーリエ係数に内在する相対ノイズの8倍であるから、NPVに内在する相対ノイズは、フーリエ係数に内在するノイズの2×8=16倍にも達することとなり、ノイズ削減効果も大きい。
*動作実施例2:或る水平面上の各格子点におけるx方向とy方向とz方向の合成電流の大きさのZスコアの等高線マップ表示例(図9及び図10)
本実施例と上記の動作実施例1との違いは、図3のフローチャートにおけるステップS4が、図9ではステップS4aに置き換わっている点である。
【0062】
すなわち、実施例1の場合には、各水平断面上の格子点に導出されるx方向又はy方向又はz方向の電流成分に関わる被験者のZスコアの値から図6〜図8に示す等高線マップを得たが、本実施例2の場合には、各格子点におけるx方向とy方向とz方向の合成電流の大きさからZスコアを求めて等高線マップを表示した点が異なっている。従って、図4の出力データの処理は1544回である。その他は実施例1と同様である。
*動作実施例3:或る水平面上の各格子点におけるx方向(又はy方向又はz方向)電流成分のYスコアの等高線マップ表示例(図11)
本実施例と上記の動作実施例1との違いは、図3のフローチャートにおけるステップS9が、図11ではステップS9aに置き換わっている点である。
【0063】
すなわち、実施例1の場合には、各水平断面上の格子点に導出されるx方向又はy方向又はz方向の電流成分に関わる被験者のZスコアの値から図6〜図8に示す等高線マップを得たが、本実施例3の場合には、各格子点におけるx方向又はy方向又はz方向の電流成分に関わる被験者の「Yスコア」を求めて等高線マップを生成する点が異なっている。その他は実施例1と同様である。ただし、生成される等高線マップ自体は実施例1の等高線マップとは異なるが、ここでは図示を省略した。
【0064】
この実施例におけるYスコアYjmとは、各格子点におけるNPVjmの平均値<NPV ,jm>と標準偏差σjmとから次式の如く算出されるものである。
【0065】
【数9】

【0066】
*動作実施例4:或る水平面上の各格子点におけるx方向とy方向とz方向の合成電流の大きさのYスコアの等高線マップ表示例(図示せず)
本実施例と上記の動作実施例2との違いは、図9のフローチャートにおけるZスコアの生成ステップS9の変わりに被験者の「Yスコア」を求めて等高線マップを生成する点が異なっているのみである。その等高線マップは、ここでは図示を省略した。
【0067】
なお、本発明は、上記実施例によって限定されるものではなく、特許請求の範囲の記載に基づき、当業者によって種々の変更が可能であり、脳疾患としての鬱病等に対しても適用可能なことは明らかである。
【符号の説明】
【0068】
1 被験者の頭部
2, 21〜221 脳電位(脳磁)センサ
3 増幅器
4 マルチプレクサ
5 A/D変換器
10 コンピュータ
11 CPU
13 ROM
14 RAM
15, 16, 17 インタフェース
24 キーボード
25 外部記憶装置
31 CRT
32 プリンタ
41 通信回線
42 計算センター
図中、同一符号は同一又は相当部分を示す。
【特許請求の範囲】
【請求項1】
被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサと、
各センサから出力された脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx方向又は y方向又は z方向の電流成分或いは該電流成分の合成した電流の大きさを求め;各電流成分又は電流の大きさを時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求め、各フーリエ係数について全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し;各周波数バンク毎に該隣接するフーリエ係数の絶対値の二乗の平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての該規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のZスコアを求めるか、又は該正常者集団を基準とする代わりに該被験者の全格子点から得られる規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のYスコアを求め;指定された水平面上の格子点に対応する該ZスコアまたはYスコアを等高線マップ化する演算装置と、
を備えたことを特徴とする脳活動測定装置。
【請求項2】
請求項1において、
該所定周波数範囲が2〜40Hzであり、該相互に隣接する複数が2個で0.78Hzの周波数帯域を含み、該セグメント幅が2.56秒であることを特徴とした脳活動測定装置。
【請求項3】
請求項1において、
該センサを端末装置に設け、該演算装置を計算センターに設けると共に該端末装置と該計算センターとを通信回線を介して接続し、脳電位に関するデータが該計算センターにデータベースとして収集・蓄積され、該端末装置からは該データベースが参照できるようにしたことを特徴とした脳活動測定装置。
【請求項4】
被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサから出力された脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx方向又は y方向又は z方向の電流成分或いは該電流成分の合成した電流の大きさを求め;各電流成分又は電流の大きさを時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求め、各フーリエ係数について全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し;各周波数バンク毎に該隣接するフーリエ係数の絶対値の二乗の平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての該規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のZスコアを求めるか、又は該正常者集団を基準とする代わりに該被験者の全格子点から得られる規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のYスコアを求め;指定された水平面上の格子点に対応する該ZスコアまたはYスコアを等高線マップ化する手順をコンピュータに実行させるためのプログラム。
【請求項5】
請求項4に記載のプログラムを記録したことを特徴とするコンピュータ読み取り可能な記録媒体。
【請求項1】
被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサと、
各センサから出力された脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx方向又は y方向又は z方向の電流成分或いは該電流成分の合成した電流の大きさを求め;各電流成分又は電流の大きさを時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求め、各フーリエ係数について全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し;各周波数バンク毎に該隣接するフーリエ係数の絶対値の二乗の平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての該規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のZスコアを求めるか、又は該正常者集団を基準とする代わりに該被験者の全格子点から得られる規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のYスコアを求め;指定された水平面上の格子点に対応する該ZスコアまたはYスコアを等高線マップ化する演算装置と、
を備えたことを特徴とする脳活動測定装置。
【請求項2】
請求項1において、
該所定周波数範囲が2〜40Hzであり、該相互に隣接する複数が2個で0.78Hzの周波数帯域を含み、該セグメント幅が2.56秒であることを特徴とした脳活動測定装置。
【請求項3】
請求項1において、
該センサを端末装置に設け、該演算装置を計算センターに設けると共に該端末装置と該計算センターとを通信回線を介して接続し、脳電位に関するデータが該計算センターにデータベースとして収集・蓄積され、該端末装置からは該データベースが参照できるようにしたことを特徴とした脳活動測定装置。
【請求項4】
被験者の頭部に取り付けられて該被験者の脳電位を測定する複数個のセンサから出力された脳電位と予め標準脳に設定した格子点の所定座標と各センサの所定座標とから該格子点で推定されるx方向又は y方向又は z方向の電流成分或いは該電流成分の合成した電流の大きさを求め;各電流成分又は電流の大きさを時間軸上で所定時間幅のセグメントに分割し、所定周波数範囲内で各セグメント毎にフーリエ変換してフーリエ係数を求め、各フーリエ係数について全セグメントに亘っての絶対値の二乗の平均値を求め、この中から相互に隣接する複数の該平均値を含むように周波数バンクに分割し;各周波数バンク毎に該隣接するフーリエ係数の絶対値の二乗の平均値を用いて規格化パワーバリアンスを求めるとともに全周波数バンクに亘っての該規格化パワーバリアンスの平均値を求め;所定の正常者集団について同様にして予め求めた規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のZスコアを求めるか、又は該正常者集団を基準とする代わりに該被験者の全格子点から得られる規格化パワーバリアンス間の平均値とその標準偏差とから該被験者のYスコアを求め;指定された水平面上の格子点に対応する該ZスコアまたはYスコアを等高線マップ化する手順をコンピュータに実行させるためのプログラム。
【請求項5】
請求項4に記載のプログラムを記録したことを特徴とするコンピュータ読み取り可能な記録媒体。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【公開番号】特開2012−235842(P2012−235842A)
【公開日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願番号】特願2011−105608(P2011−105608)
【出願日】平成23年5月10日(2011.5.10)
【出願人】(594056340)株式会社脳機能研究所 (11)
【Fターム(参考)】
【公開日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願日】平成23年5月10日(2011.5.10)
【出願人】(594056340)株式会社脳機能研究所 (11)
【Fターム(参考)】
[ Back to top ]

