腫瘍特異性を有するリポソーム
【課題】腫瘍細胞に特異的かつ効率的に吸着・摂取されるようなドラッグデリバリーシステム(DDS)製剤を提供すること。
【解決手段】シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター、抗腫瘍効果を示す薬物が封入された該薬物導入用ベクターを含有する癌治療用組成物、標識物質が封入された該薬物導入用ベクターを含有する腫瘍細胞標識用化組成物、抗腫瘍効果を示す薬物が封入された該薬物導入用ベクターを投与することを特徴とする癌治療方法、および標識物質が封入された該薬物導入用ベクターを投与することを特徴とする腫瘍細胞標識化方法。
【解決手段】シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター、抗腫瘍効果を示す薬物が封入された該薬物導入用ベクターを含有する癌治療用組成物、標識物質が封入された該薬物導入用ベクターを含有する腫瘍細胞標識用化組成物、抗腫瘍効果を示す薬物が封入された該薬物導入用ベクターを投与することを特徴とする癌治療方法、および標識物質が封入された該薬物導入用ベクターを投与することを特徴とする腫瘍細胞標識化方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、腫瘍細胞内への薬物導入用ベクターに関する。より詳しくは、本発明は、シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクターに関する。さらに本発明は、薬物が封入された上記ベクターに関する。また本発明は、抗腫瘍効果を示す薬物が封入された上記ベクターを含有する癌治療用組成物、および、標識物質が封入された上記ベクターを含有する腫瘍細胞標識化用組成物に関する。さらにまた本発明は、抗腫瘍効果を示す薬物が封入された上記ベクターを投与することを特徴とする癌治療方法、および、標識物質が封入された上記ベクターを投与することを特徴とする腫瘍細胞標識化方法に関する。
【背景技術】
【0002】
薬物を効果的かつ集中的に、標的とする患部、すなわち臓器や組織、細胞、病原体などに送達する薬物投与に関する技術、いわゆるドラッグデリバリーシステム(以下、DDSと略称することがある)の開発が盛んに行われている。DDSは、薬物の投与方法や投与形態を工夫することにより体内での薬物動態を制御し、それにより薬物の標的部位への選択的送達を可能とする。その結果、薬物による最適の治療効果、さらに薬物による副作用の軽減を達成することができる。各種のDDS製剤が開発されているが、中でもリポソームは有用な(DDS)製剤として注目されている。
【0003】
リポソームは、生体の細胞膜を構成しているリン脂質を基本とする脂質二重層からなる閉鎖型小胞体であり、水溶性や脂溶性の薬物を封入することができる。したがって、リポソームは、生体適合性が高く、また、体内では封入された薬物を分解酵素などから保護しながら輸送できるため、DDSにおける薬物輸送体として有用である。一方、リポソームは肝臓や脾臓を中心とする細網内皮系組織(RES)の貪食細胞により捕捉され易く、その結果肝臓や脾臓に蓄積し易く、また、生体から排出され易いという問題点がある。
【0004】
近年、リポソームのDDS製剤としての有用性を高めた機能性リポソームが開発されている。例えば、標的とする組織や細胞へのターゲティング機能(標的到達特異性)を高めるために、リガンドや抗体により修飾したリポソームが開発されている。また、リポソームの一般的性質、例えば封入物のもれ、凝集、およびRESでの捕捉などの性質を改良するために、リポソームの表面を水溶性高分子ポリエチレングリコール(以下、PEGと略称することがある。)などの、親水性ポリマーで修飾することにより、RESに捕捉されにくく、血中に長時間循環滞留する特性を有するリポソームが開発されている(非特許文献1)。PEG修飾リポソームは、ステルスリポソームと呼ばれている。ドキソルビシンを封入したPEG修飾リポソームは、DOXIL登録商標という商品名で上市され、悪性腫瘍の治療に使用されている。また、PEG修飾リポソームは化学療法剤を封入するだけでなく、ポルフィリン誘導体による光化学療法、ボロン化合物による中性子捕捉療法への応用研究が進められている。
【0005】
一方、リポソームの細胞質内への導入効率を高めるために、膜融合能を有するウイルスとリポソームとを融合させて作製した細胞内物質導入ベクターが開発されている(特許文献1)。ウイルスとリポソームとを融合させて作製した細胞内物質導入ベクターは、内部にリポソーム由来の内空を有し、脂質二重層の外側にはウイルスエンベロープと同じタンパク質を有している。そのため、このようなリポソームは、その内空に封入された薬物をウイルスと同等の高い効率で細胞内に導入することができる。このようなベクターとして、例えばセンダイウイルス(Hemagglutinating Virus of Japan)や水疱性口内炎ウイルス(Vesicular Stomatitis Vius)とリポソームとを融合させてなるベクターが報告されている(非特許文献2および特許文献1)。水疱性口内炎ウイルス、またはその部分をリポソームと融合させたベクターは、生理的条件下でも赤血球溶血作用を示さず、安全に使用できるように良好な安定性と優れた細胞内物質導入率を示すことが報告されている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開平11-187873号公報。
【非特許文献】
【0007】
【非特許文献1】クリバノフ(Klibanov A.L.)ら、「フェブス レターズ(FEBS Letters)」、1990年、第268巻、p.235-237。
【非特許文献2】ナカガワ(Nakagawa T.)ら、「ドラッグ デリバリー システム(Drug Delivery System)」、1996年、第11巻、p.411-417。
【発明の概要】
【発明が解決しようとする課題】
【0008】
現在、癌治療に有効なDDSを含め、DDSの開発が盛んに行われているが、腫瘍細胞に特異的かつ効率的に吸着・摂取されるようなシステムの開発には至っていない。
【0009】
DDS製剤として有用とされているリポソームも、それ自体の腫瘍標的性は低い。そのため、EPR(Enhanced Permeability Retention)効果や、腫瘍関連抗原に対する抗体の修飾、腫瘍関連抗原の封入による腫瘍免疫の誘導などにより腫瘍標的性を高めている。EPR効果や腫瘍免疫の誘導は二次的効果であり、また、効果的な腫瘍関連抗原は研究段階にあるため、腫瘍標的性はなお低く、その向上が求められている。また、上記リポソームは、臨床応用を検討した際に、非腫瘍細胞へも薬物導入効果が高いことが観察され、重大な副作用を惹き起こす可能性があるため、腫瘍標的性を改善する必要がある。
【0010】
本発明の課題は、腫瘍細胞に特異的かつ効率的に吸着・摂取されるようなDDS製剤を提供することである。
【課題を解決するための手段】
【0011】
本発明者らは、上記目的を達成すべく、腫瘍溶解ウイルス(Oncolytic virus)に着目し、鋭意研究を行った。本発明者らが研究を行ってきたレオウイルス科レオウイルスおよびトガウイルス科アルファウイルス属シンドビスウイルスは腫瘍に特異的に感染(吸着)し、腫瘍特異的に増殖する。特にシンドビスウイルスは非常に多くの種類の腫瘍細胞、例えば悪性黒色腫、悪性リンパ腫、扁平上皮癌、および腺癌などに感染する。これらウイルスの腫瘍細胞への感染(吸着)は腫瘍細胞膜上のレセプターを介して行われることが知られており、数種類のレセプターが同定されている。このため、これらのレセプターと結合するリガンドを用いれば癌特異的なDDSの開発が可能になると考えた。
【0012】
そして、シンドビスウイルスと融合させたリポソームが、腫瘍細胞に特異的かつ効率的に吸着・摂取されること、および抗腫瘍効果を示す薬物を封入した該リポソームが、該薬物を封入した通常のリポソームと比較して腫瘍細胞に対する高い細胞障害性を示すことを見出し、本発明を達成した。
【0013】
即ち、本発明は以下に関する。
1.シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター。
2.シンドビスウイルスのE1タンパク質およびE2タンパク質を実質的に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター。
3.シンドビスウイルスをショ糖密度勾配遠心処理してE1タンパク質およびE2タンパク質分画を得、これを構成成分としてリポソームとした、腫瘍細胞内への薬物導入用ベクター。
4.リポソームがポリエチレングリコールにより修飾されたリポソームである前記1.から3.のいずれかの腫瘍細胞内への薬物導入用ベクター。
5.ポリエチレングリコールが、平均分子量1,000〜5,000のポリエチレングリコールである前記4.の腫瘍細胞内への薬物導入用ベクター。
6.薬物が封入された前記1.から5.のいずれかの腫瘍細胞内への薬物導入用ベクター。
7.薬物が抗腫瘍効果を示す薬物である前記6.の腫瘍細胞内への薬物導入用ベクター。
8.抗腫瘍効果を示す薬物がシスプラチンである前記7.の腫瘍細胞内への薬物導入用ベクター。
9.薬物が標識物質である前記6.の腫瘍細胞内への薬物導入用ベクター。
10.前記1.から5.のいずれかの腫瘍細胞内への薬物導入用ベクターの、癌治療用組成物の製造における使用。
11.前記7.または8.の腫瘍細胞内への薬物導入用ベクターを有効成分として含有する癌治療用組成物。
12.前記7.または8.の薬物導入用ベクターを投与することを特徴とする癌治療方法。
13.前記1.から5.のいずれかの腫瘍細胞内への薬物導入用ベクターの、腫瘍細胞標識化用組成物の製造における使用。
14.前記9.の薬物導入用ベクターを含有する腫瘍細胞標識化用組成物。
15.前記9.の薬物導入用ベクターを投与することを特徴とする腫瘍細胞標識化方法。
【発明の効果】
【0014】
本発明によれば、シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター、並びに、該ベクターを含有する癌治療用組成物および腫瘍細胞標識化用組成物を提供できる。
【0015】
本発明に係る薬物導入用ベクターは、腫瘍細胞に特異的に吸着するため、封入された薬物を腫瘍細胞特異的に輸送することができる。そのため、封入された薬物の正常細胞に対する副作用が軽減される。
【0016】
また、シンドビスウイルスは、蚊の媒介によりヒトに感染するが、軽微な発熱を惹き起こすだけの低病原性ウイルスであり、全身投与もできることから、その成分を用いた製剤は副作用が少なく、かつ全身投与が可能な安全で有用な薬剤であると考えられる。
【0017】
このように本発明は、腫瘍細胞に特異的かつ効率的に吸着・摂取され、高い腫瘍細胞障害性を示す一方、副作用の軽減されたDDS製剤を提供するものであり、癌治療分野において有用である。
【図面の簡単な説明】
【0018】
【図1】グリーン蛍光タンパク質(GFP)発現シンドビスウイルス(図中、GFP-SIN (+))を静脈注射した担癌ヌードマウスにおいて、腫瘍特異的な該ウイルスの分布が観察されたことを説明する図である。腫瘍(Tumor)において高いGFP蛍光が観察されたが、脳(Brain)、心臓(Heart)、肺(Lung)、肝臓(Liver)、腎臓(Kidney)、精巣(Intestine)で観察されたGFP蛍光は、GFPのみを静脈注射した担癌ヌードマウスのものと同程度であった。(実施例1)
【図2】シスプラチンを封入したシンドビスウイルス(SIN)ハイブリッドリポソームが、正常生理食塩水(NS)を封入したSINハイブリッドリポソームやシスプラチン若しくはNSを封入した非SINハイブリッドリポソームと比較して、腫瘍細胞株(HSC-2、HSC-3、RERF-LC-AI)に対して高い細胞傷害性を示したことを説明する図である。一方、正常線維芽細胞(Fibroblast)に対する細胞傷害性効果に大きな差異は無かった。図中、シスプラチンを封入したSINハイブリッドリポソームはSIN liposome cisplatinと表示する。また、NSを封入したSINハイブリッドリポソーム、シスプラチン若しくはNSを封入した非SINハイブリッドリポソームは、それぞれSIN liposome NS、liposome cisplatin、liposome NSと表示する。(実施例1)
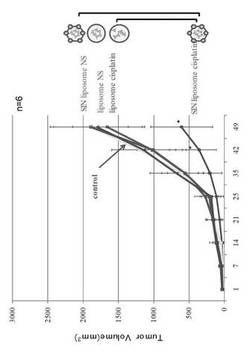
【図3】シスプラチンを封入したシンドビスウイルス(SIN)ハイブリッドリポソームを注入したマウスでは急速な腫瘍退縮が観察されたことを説明する図である。一方、正常生理食塩水(NS)を封入したSINハイブリッドリポソームまたはシスプラチン若しくはNSを封入したSINハイブリッドリポソームを注入したマウスでは大きな腫瘍(1500〜2000 mm3)が形成された。横軸はリポソーム注入後の日数を、縦軸は腫瘍体積(Tumor Volume)を示す。図中、シスプラチンを封入したSINハイブリッドリポソームはSIN liposome cisplatinと表示する(●)。また、NSを封入したSINハイブリッドリポソーム、シスプラチン若しくはNSを封入した非SINハイブリッドリポソームは、それぞれSIN liposome NS、liposome cisplatin、liposomeNSと表示する(□、■、△)。(実施例1)
【発明を実施するための形態】
【0019】
本発明は、シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクターに関する。本薬物導入用ベクターは腫瘍細胞特異性が高く、該ベクターに封入した薬物を腫瘍細胞に特異的かつ効率的に輸送できるという特徴を有し、さらに該薬物による正常細胞への副作用が軽減されるという利点を併せ持つ。
【0020】
腫瘍細胞内への薬物導入用ベクターとは、腫瘍細胞内に薬物を輸送するための運搬体を意味する。
【0021】
シンドビスウイルスはエンベロープを有する正二十面体様構造の一本鎖(+)RNAウイルスである。その感染は蚊によって媒介され、脊椎動物に感染するが、ヒトでは軽い風邪症状を引き起こすのみの低病原性ウイルスである。
【0022】
シンドビスウイルスは、腫瘍溶解ウイルス(Oncolytic virus)として知られ、非常に多くの種類の腫瘍細胞、例えば悪性黒色腫、悪性リンパ腫、扁平上皮癌、および腺癌などに感染し、腫瘍細胞特異的に増殖する。また、シンドビスウイルスによる、子宮頸癌細胞および卵巣癌細胞の治療の可能性が報告されている(ウンノ(Unno Y.)ら、「キャンサー セラピー(Cancer Therapy)」、2005年、第11巻、第12号、p.4553-4560)。腫瘍溶解ウイルス(Oncolytic virus)とは、腫瘍細胞特異的に結合、吸着して腫瘍細胞内部に侵入し、腫瘍細胞内で複製して腫瘍細胞のみを殺滅する能力をもつウイルスをいう。腫瘍細胞特異的とは、正常細胞と比較して腫瘍細胞に選択的に作用し、正常細胞にはほとんど作用しないことを意味する。
【0023】
エンベロープを有するウイルスの標的細胞への感染には、一般的にエンベロープに存在するエンベロープタンパク質が関与することが知られている。エンベロープは、一部のウイルスが有する脂質二重膜構造であり、ウイルス粒子の最も外側に位置しており、ウイルスの基本構造となるウイルスゲノムを含むカプシドを覆っている。エンベロープは、ウイルスが感染細胞内で増殖し、細胞外に出る際に細胞膜あるいは核膜などの生体膜を被ったまま出芽することによって獲得されるものである。このため、基本的には宿主細胞の脂質二重膜に由来するものであるが、この他にウイルス遺伝子にコードされているそのウイルス独自のタンパク質を生体膜に発現した後で該生体膜と一緒にウイルス粒子に取り込み、エンベロープタンパク質としてウイルス粒子表面に発現させている。エンベロープタンパク質は、糖タンパク質であり、スパイクとも呼ばれ、エンベロープ上に突出して存在する。エンベロープタンパク質には、そのウイルスの標的細胞への吸着・侵入において標的細胞側が持つレセプターに結合する機能や、宿主の生体防御機能を回避する機能など、さまざまな機能を持つものが知られており、ウイルスの感染に重要な役割を果たしている。標的細胞の細胞膜に由来するエンベロープを有するウイルスの多くでは、エンベロープタンパク質が標的細胞側のレセプターに結合した後、ウイルスのエンベロープと細胞膜とが膜融合することにより、エンベロープに内包されていたウイルスゲノムを含むカプシドが標的細胞内に送達される。
【0024】
シンドビスウイルスはE1タンパク質およびE2タンパク質と呼ばれるエンベロープタンパク質を有することが知られており、これらE1タンパク質およびE2タンパク質が、標的細胞への特異的吸着に関与していると考えられる。
【0025】
したがって、シンドビスウイルスの一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクターとして、好ましくはシンドビスウイルスのエンベロープタンパク質を実質的に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター、さらに好ましくはシンドビスウイルスのE1タンパク質およびE2タンパク質を実質的に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクターを例示できる。ここで、「エンベロープタンパク質を実質的に含む」とは、エンベロープタンパク質を含む限り、シンドビスウイルス由来のその他のタンパク質、例えばコアタンパク質が含まれていてもよいことを意味する。また、「E1タンパク質およびE2タンパク質を実質的に含む」とは、E1タンパク質およびE2タンパク質を含む限り、シンドビスウイルス由来のその他のタンパク質、例えばE1タンパク質およびE2タンパク質以外のエンベロープタンパク質やコアタンパク質が含まれていてもよいことを意味する。
【0026】
シンドビスウイルスまたはその一部分を構成成分に含むリポソームを、本明細書ではシンドビスウイルスハイブリッドリポソームと称することがある。
【0027】
シンドビスウイルスハイブリッドリポソームの製造は、シンドビスウイルスまたはその一部分とリポソームとを自体公知の方法で融合させることにより実施できる。シンドビスウイルスまたはその一部分とリポソームとを融合させるとは、シンドビスウイルスまたはその一部分とリポソーム膜の脂質とが同一の膜を構成し、かつ、シンドビスウイルスまたはその一部分に含まれるタンパク質の構造や機能がリポソーム膜中でもウイルス粒子中に存在したときと同等に示されるように処理することをいう。
【0028】
その製造において、シンドビスウイルスは不活化して使用する。シンドビスウイルスの調製は、自体公知の感染可能な細胞に感染させ増殖させることにより実施でき、その不活化は、自体公知の方法、例えば紫外線照射や界面活性剤処理により実施できる。
【0029】
具体的には、不活化シンドビスウイルスとリポソームとを混合し、激しく振騰させながら37℃でインキュベーションすることにより、シンドビスウイルスハイブリッドリポソームを製造することができる。インキュベーションの時間は、一般的に6時間〜1時間、好ましくは3〜1時間、より好ましくは2時間である。また、シンドビスウイルスのE1タンパク質およびE2タンパク質を実質的に含むリポソームは、シンドビスウイルスをショ糖密度勾配遠心処理してE1タンパク質およびE2タンパク質分画を得、これを構成成分としてリポソームとすることにより製造することができる。
【0030】
リポソームの製造は、自体公知のリポソーム調製法を使用して実施できる。リポソームは、その構造から、多重層小胞(multilamellar vesicles、MLV)と単一層小胞(unilamellar vesicles)に分類される。単一層小胞はさらに直径により、直径20-100nmの小単一層小胞(small unilamellar vesicles、SUV)、直径100-1000nmの大単一層小胞(large unilamellar vesicles、LUV)、直径5000-100000nmの巨大単一層小胞(giant unilamellar vesicles、GUV)に分けられる。MLVの調製はボルテックス処理法で実施できる。SUVの調製法としては、超音波処理法、エタノール注入法、界面活性剤除去法、押出し法等が知られている。LUVの調整法としては、逆相蒸発法、エタノール注入法、凍結融解法、押出し法等が知られている。また、GUVの調整法としては、静置水和法、電気的形成法、有機溶媒透析法、凍結融解塩透析法等が知られている。MLVは、一般に安定で高分子物質の保持効率もよいが、大きさが不均一で多重層であるため、封入薬剤の細胞への導入効率が低い。しかし、MLVは超音波処理後にインキュベーションするアニーリング法により、SUV、さらにLUVに変化させることができる。SUVは大きさが均一であるが、高分子物質を保持しにくく、比較的不安定である。LUVは、蛋白質やDNAなどの保持効率がよいが、大きさが不均一である。このようにリポソームの調製には多数の方法が知られており、封入する薬物や用途に応じて適当なリポソームを選択し、該リポソームに適当な調製法を採用すればよい。
【0031】
リポソームは、多重層小胞であっても、単一層小胞であってもよいが、単一層小胞であることが好ましい。大きさも特に限定されないが、直径10μm〜0.1μm、好ましくは3μm〜0.1μm、さらに好ましくは0.5μm〜0.1μmであることが適当である。
【0032】
リポソームの構成成分としては、一般に、リン脂質、コレステロール類、窒素脂質等が使用されるが、特にリン脂質が好適に使用される。
【0033】
脂質としては、リン脂質、糖脂質、ステロール、および飽和または不飽和の脂肪酸などを例示できる。リン脂質の具体例としては、ホスファチジルコリン、ホスファチジルセリン、ホスファチジルグリセロール、ホスファチジルイノシトール、ホスファチジルエタノールアミン、ホスファチジン酸、カルジオリピン、スフィンゴミエリン、卵黄レシチン、大豆レシチン、リゾレシチン等の天然リン脂質、あるいはこれらを常法によって水素添加したものなどを挙げることができる。糖脂質の具体例としては、スルホキシリボシルグリセリド、ジグリコシルジグリセリド、ジガラクトシルジグリセリド、ガラクトシルジグリセリド、およびグリコシルジグリセリドなどのグリセロ糖脂質や、ガラクトシルセレブロシド、ラクトシルセレブロシド、およびガングリオシなどのスフィンゴ糖脂質などを挙げることができる。ステロールの具体例としては、コレステロール、コレステロールコハク酸、コレスタノール、ラノステロール、ジヒドロラノステロール、デスモステロール、およびジヒドロコレステロールなどの動物由来のステロール、スチグマステロール、シトステロール、カンペステロール、およびブラシカステロールなどの植物由来のステロール(フィトステロール)、並びにチモステロール、エルゴステロールなどの微生物由来のステロールを挙げることができる。飽和または不飽和の脂肪酸の具体例としては、 パルミチン酸、オレイン酸、ステアリン酸、アラキドン酸、およびミリスチン酸などの炭素数12〜20の飽和または不飽和の脂肪酸。を挙げることができる。これらの脂質は単独で使用することができるが、二種以上を組み合わせて使用することもできる。
【0034】
リポソームの構成成分としてさらに、脂質膜を物理的または化学的に安定させたり、脂質膜の流動性を調節したりするために、膜安定化剤を含有させることができる。膜安定化剤としては、ステロール、グリセリンまたはその脂肪酸エステルなどを例示できる。ステロールとしては、上記同様の具体例を挙げることができ、グリセリンの脂肪酸エステルとしては、例えば、トリオレイン、トリオクタノイン等を挙げることができる。
【0035】
また、脂質膜の酸化を防止するために抗酸化剤を含有させることができる。抗酸化剤としては、トコフェロール、没食子酸プロピル、パルミチン酸アスコルビル、ブチル化ヒドロキシトルエンなどを例示できる。
【0036】
さらに、脂質膜に正荷電又は負荷電を付与するために荷電物質を含有させることができる。正荷電を付与する荷電物質としては、ステアリルアミンおよびオレイルアミンなどの飽和または不飽和脂肪族アミンや、ジオレオイルトリメチルアンモニウムプロパンなどの飽和または不飽和カチオン性合成脂質などを例示できる。負電荷を付与する荷電物質としては、ジセチルホスフェート、コレステリルヘミスクシネート、ホスファチジルセリン、ホスファチジルイノシトール、ホスファチジン酸などを例示できる。
【0037】
より具体的なリポソームとして、卵黄ホスファチジルコリン、コレステロール、およびホスファチジルセリンをモル比4:5:1で混合し、脱水再水和法により製造したリポソームを例示できる(実施例1参照)。
【0038】
リポソームは、その外表面を親水性ポリマーで修飾することができる。このような修飾により、リポソームのRESへの捕捉を回避することができ、リポソームの血中循環滞留時間を長くすることができるため、腫瘍細胞内への薬剤輸送をより効率的に行うことができる。親水性ポリマーとして、ポリエチレングリコール、ポリメチルエチレングリコール、ポリヒドロキシプロピレングリコール、ポリプロピレングリコール、ポリメチルプロピレングリコール、およびポリヒドロキシプロピレンオキシドが例示できる。特に好ましくはポリエチレングリコールである。シンドビスウイルスハイブリッドリポソームの形成において、リポソーム膜に融合されたウイルスタンパク質がポリエチレングリコールにより埋没しないように、使用するポリエチレングリコールの分子量を選択することが好ましい。ポリエチレングリコールの平均分子量として、好ましくは1,000〜5,000、より好ましくは1,000〜3,000、さらに好ましくは2000が適当である。このようなポリエチレングリコールとして、例えば、PEG-DSPE(1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-[Methoxy(Polyethyleneglycol)-2000])を例示できる。
【0039】
シンドビスウイルスハイブリッドリポソームへの薬物の封入は、通常、シンドビスウイルスまたはその一部とリポソームとの融合の前に、リポソームの製造工程において実施する。すなわち、リポソームに所望の薬物を封入し、その後、薬物が封入されたリポソームとシンドビスウイルスまたはその一部とを融合することにより実施する。リポソームへの薬物の封入は、自体公知の方法で実施できる。例えばリポソーム製造用原料、例えば脂質の混合物から薄膜を作製し、該薄膜を所望の薬物を含有する溶液にけん濁して混合することにより、薬物のリポソームへの封入を実施できる。混合後に、必要に応じて超音波処理などを施しても良い。より具体的には、例えば、リン脂質をクロロホルムなどの有機溶媒に溶解した溶液に、目所望の薬物を溶媒に溶解した溶液を加えた後、溶媒を留去し、これにリン酸緩衝液を加え、振とう、超音波処理および遠心処理した後、上清をろ過処理して回収することにより行い得る。
【0040】
封入する薬物は、特に制限はないが、その具体例としては、抗腫瘍効果を示す薬物や核酸などを挙げることができる。抗腫瘍効果とは、腫瘍の増殖を抑制して減弱させる作用、腫瘍の浸潤を抑制して減弱させる作用、および腫瘍を殺滅する作用のいずれも意味する。抗腫瘍効果を示す薬物は、癌治療の目的に用いられている薬剤であればいずれでもよく、シスプラチンやオキサリプラチンなどのプラチナ製剤、シクロホスファミドやダカルバジンなどのアルキル化剤、フルオロウラシルやテガフールなどの代謝拮抗剤、イリノテカンやパクリタキセルなどの植物アルカロイド、アクチノマイシンDやドキソルビシンなどの抗癌性抗生物質、アナストロゾールやタモキシフェンなどのホルモン剤、およびインターフェロンなどの生物学的応答調節剤を挙げることができる。核酸としては、所望のタンパクをコードした核酸、所望のタンパクの発現を抑制することのできる核酸、例えばアンチセンス核酸、siRNAやshRNAなどの短鎖二本鎖RNA、自殺遺伝子、アポトーシス誘導遺伝子などを挙げることができる。
【0041】
封入する薬物としてその他、癌の光化学療法に使用されるポルフィリン誘導体などの光増感剤を好適に例示できる。光化学療法は生体に光増感剤を投与後にレーザー光を照射した部位のみで薬剤が活性化を受けるため、副作用が少ないという利点を有する。光増感剤は腫瘍蓄積性が低いという問題を有するが、本願の薬物導入用ベクターに封入して使用することにより、腫瘍蓄積性が増加し、高い治療効果を得られる。
【0042】
封入する薬物としてその他、腫瘍細胞を標識化するための標識物質を好適に例示できる。標識物質として、例えば、テクネチウム99mなどのγ線を放出する核種を含む化合物を挙げることができる。このような化合物はイメージング剤と呼ばれ、腫瘍に蓄積させてγ線を検出することにより、腫瘍の検出を実施できる。本願の薬物薬物導入用ベクターに封入して使用することにより、腫瘍特異的にイメージング剤を蓄積させることができるため、腫瘍の検出を精度高く行うことができ、また、正常組織への副作用も少ない。さらに、転移癌の検出も可能である。標識物質としてその他、蛍光物質を挙げることができる。
【0043】
封入する薬物は、一種類であってよく、また二種類以上を組み合わせて封入することができる。封入する薬物の量は、特に限定されず、その有効性により適宜変更することができる。
【0044】
本発明に係る薬物薬物導入用ベクターは、腫瘍細胞特異性が高く、該ベクターに封入した薬物を腫瘍細胞に特異的かつ効率的に輸送できるという特徴を有する。そのため薬物導入用ベクターは、食道癌、肺癌、乳癌、胃癌、結腸・直腸癌、膵臓癌、肝臓癌、腎癌、膀胱癌、および子宮癌などの固形癌、腹水癌や胸水癌などの浮遊癌、白血病やリンパ腫などの造血系癌などの広範な癌に適用できる。
【0045】
本発明においては、抗腫瘍効果を示す薬物や核酸などの癌治療用薬物を封入した上記薬物導入用ベクターを有効成分として含有する癌治療用組成物を提供できる。癌治療用組成物は、薬物導入用ベクターのほかに、薬学的に許容される担体を含む。薬学的に許容される担体としては、薬学的に許容される担体としては、例えば、水、医薬的に許容される有機溶剤、コラーゲン、ポリビニルアルコール、ポリビニルピロリドン、カルボキシビニルポリマー、アルギン酸ナトリウム、水溶性デキストラン、カルボキシメチルスターチナトリウム、ペクチン、キサンタンガム、アラビアゴム、カゼイン、ゼラチン、寒天、グリセリン、プロピレングリコール、ポリエチレングリコール、ワセリン、パラフィン、ステアリルアルコール、ステアリン酸、ヒト血清アルブミン、マンニトール、ソルビトール、ラクトースを例示できる。これらは、本薬剤の剤形に応じて適宜1種類または2種類以上を組み合わせて使用される。その他、安定化剤、殺菌剤、緩衝剤、等張化剤、およびpH調整剤等を適宜使用することもできる。安定化剤は、例えばヒト血清アルブミンや通常のL−アミノ酸、糖類、セルロース誘導体を例示できる。L−アミノ酸は、特に限定はなく、例えばグリシン、システイン、グルタミン酸等のいずれでもよい。糖類も特に限定はなく、例えばグルコース、マンノース、ガラクトース、果糖等の単糖類、マンニトール、イノシトール、キシリトール等の糖アルコール、ショ糖、マルトース、乳糖等の二糖類、デキストラン、ヒドロキシプロピルスターチ、コンドロイチン硫酸、ヒアルロン酸等の多糖類等およびそれらの誘導体等のいずれでもよい。セルロース誘導体も特に限定はなく、メチルセルロース、エチルセルロース、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、カルボキシメチルセルロースナトリウム等のいずれでもよい。緩衝剤は、ホウ酸、リン酸、酢酸、クエン酸、ε−アミノカプロン酸、グルタミン酸および/またはそれらに対応する塩(例えばそれらのナトリウム塩、カリウム塩、カルシウム塩、マグネシウム塩等のアルカリ金属塩やアルカリ土類金属塩)を例示できる。等張化剤は、塩化ナトリウム、塩化カリウム、糖類、グリセリンを例示できる。
【0046】
本発明においては、腫瘍細胞を標識化するための標識物質を封入した上記薬物導入用ベクターを有効成分として含有する腫瘍細胞標識化用組成物を提供できる。腫瘍細胞標識化用組成物は、薬物導入用ベクターのほかに、薬学的に許容される担体を含むことができる。
【0047】
本発明に係る癌治療用組成物および腫瘍細胞標識化用組成物は、ボーラス注射または連続注入により非経口的に投与することができる。投与経路は、静脈や動脈などに投与するか、または腫瘍組織に直接投与することができる。腫瘍溶解ウイルス(Oncolytic virus)は、腫瘍特異的に吸着・進入することが知られており、例えばシンドビスウイルスは、感染により軽微な発熱を惹き起こすだけの低病原性ウイルスであり、全身投与もできることから、その成分を用いた製剤は副作用が少なく、かつ全身投与が可能な安全で有用な薬剤であると考えられる。
【0048】
本発明に係る組成物の用量範囲は特に限定されず、薬物導入用ベクターに封入した薬物の有効性、投与形態、投与経路、対象の性質(体重、年齢、病状および他の医薬の使用の有無等)、および担当医師の判断等に応じて適宜選択される。
【0049】
本発明においては、抗腫瘍効果を示す薬物や核酸などの癌治療用薬物を封入した上記薬物導入用ベクターや、該薬物導入用ベクターを含有する医薬組成物を、癌疾患を有する対象に投与することを特徴とする癌治療方法を提供する。
【0050】
本発明においては、腫瘍細胞を標識化するための標識物質を封入した上記薬物導入用ベクターや、該薬物導入用ベクターを含有する組成物を、対象に投与することを特徴とする腫瘍細胞標識化方法を提供する。本腫瘍細胞標識化方法により腫瘍細胞特異的に標識物質が蓄積するため、蓄積した標識物質を測定することにより、腫瘍細胞検出を実施できる。したがって、本腫瘍細胞標識化方法は、腫瘍細胞検出方法に使用でき、さらに癌疾患の診断、および、癌転移の診断に使用できる。
【0051】
以下、実施例を示して本発明をより具体的に説明するが、本発明は以下に示す実施例によって何ら限定されるものではない。
【実施例1】
【0052】
シンドビスウイルスとリポソームとを融合させたハイブリッドリポソームを作製し、該ハイブリッドリポソームの腫瘍細胞への吸着特異性および封入薬物の輸送能、並びに抗癌剤を封入した該ハイブリッドリポソームのインビトロおよびインビボでの細胞障害性を検討した。以下、シンドビスウイルスとリポソームとを融合させたハイブリッドリポソームをSIMハイブリッドリポソームと称し、シンドビスウイルスと融合させていないリポソームを非SIMハイブリッドリポソームと称することがある。
【0053】
[材料および方法]
【0054】
シスプラチン(cis-diammineplatinum(II) dichloride,Pt(NH3)2Cl2)、コレステロール(以下、CHと略称することがある。)、ホスファチジルセリン(以下、PSと略称することがある。)、およびFITC-4KD(Fluoresceinisothiocyanate-4KD)はシグマケミカル(Sigma Chemical)社より購入した。正常生理食塩水(以下、NSと略称することがある。)は株式会社大塚製薬工場より購入した。卵黄ホスファチジルコリン(以下、EPCと略称することがある。99%。)およびホスファチジルエタノールアミン(PE)のポリエチレングリコール誘導体(PEG-DSPE2K、以下、PEPと略称することがある:PEGの平均分子量は2000である。)は日本油脂から得た。ヒト肺癌細胞株RERF-LC-AI、口腔癌細胞株HSC-2およびHSC-3、Vero細胞、並びに正常線維芽細胞は、10% ウシ胎仔血清(FCS)並びに50ユニット/mlのペニシリンおよびストレプトマイシンを含むダルベッコ変法イーグル培地(DMEM)中で培養した。初代培養ヒト角化細胞(Normal Human Keratinocyte、NHKと略称することがある。)は正常ヒト表皮角化細胞培地KGM中で培養した。N-(リサアミンローダミンBスルフォニル)-ホスファチジルエタノールアミン(以下、N-Rh-PEと略称することがある)、NED-PE、オレゴングリーンはインビトロージェン(Invitrogen)社より購入した。
【0055】
本発明において使用した野生型シンドビスウイルスAR339は、国立感染研究所(日本)より提供されたものである。ウイルスは、初代ニワトリ胚線維芽細胞中で増殖させ、次いでベロ細胞中で数回継代した。このウイルスを研究用ストックとして使用した。GFP発現組換えシンドビスウイルスTR339-GFP/2A(以下、GFP-SINと称する。)は、cDNAクローンpTR339-GFP/2Aから由来した。該cDNAクローンをXhoIによる消化で直線化し、そしてランオフ転写産物をSP6 RNAポリメラーゼを使用して産生した。RNA転写産物は、次いでC33A細胞に電気穿孔法で導入し、そして導入後48時間目にウイルスを含む成育培地を回収し、−80℃で凍結した。 AR339およびTR339-GFP/2Aは、10% FCSを含むDMEM中で37℃、5% CO2の条件下で維持されたC33A細胞中で増殖させ、ウイルス力価を単層のBHK-21細胞を使用するプラークアッセイにより測定した。
【0056】
シンドビスウイルスのインビボ分布およびターゲティング試験を、次に説明するように実施した。まず、C33A腫瘍担癌マウスに、 1x106 pfuのGFP-SINを含む100μLのDMEMを、頸静脈から注入した。腫瘍におけるGFP発現を注入後12時間ごとに調べた。GFP発現の測定は、GFP用反射照明蛍光ユニット(SZX-RFL2-GFP)を備えたオリンパス蛍光ステレオ顕微鏡(モデルSZX7)をハママツORCA-ER冷却CCDカメラと連結して使用することにより実施した。所定の間隔で、腫瘍部位および種々の臓器を切り離して秤量し、腫瘍内のシンドビスウイルスの蓄積を測定した。腫瘍および臓器を切り離した後、それらを秤量してはさみで細切し、4.31% スルホサリチル酸の1mlを含むガラスホモジェナイザーに入れた。種々の臓器由来の溶解物中のGFPカウントは、プレートリーダー(Wallac 1420 ARVOsx MultilabelCounter, Perkin-Elmer社製)で測定した蛍光により評価した。
【0057】
ウイルスの精製を次に説明するように実施した。ウイルスを含有する培地を、20% ショ糖を含む2ml容量の緩衝液上に重層した。ウイルス粒子は、Ti42ローター(Beckman社製)で50000gで2時間遠心処理することにより、回収した培地から沈澱させた。沈澱物は、100μl GTEN緩衝液(200mM グリシン、50mM Tris、100mM NaCl、1mM エチレンジアミン四酢酸(EDTA)、pH7.5にHCLで調製)に溶解した。ウイルスは、45分間の紫外線照射により不活化した。不活化したウイルスは複製できないが、ウイルスの吸着能および融合能は変わらずに残っている。
【0058】
リポソームの調製は、脱水再水和法により実施した。簡潔にいえば、EPC、コレステロール、およびPSをモル比4:5:1で含む脂質混合物を、クロロホルムを含む溶液にけん濁し、そして、クロロホルムを除去するために50℃でロータリーエバポレータにより留去した。リポソーム膜を標識化するために、N-Rh-PEまたはオレゴングリーン-DHPEを混合物に加えた。薄層(film)をNSまたは5mM シスプラチンで水和させた。その後、孔サイズ0.4μmのポリカーボネートフィルター (Nuclepore社製)を二重に重ねて(two stacked)、加圧エクストルーダー(Lipex Biomembranes社製)を用い、エクストルージョンを10回行った。PEG修飾リポソーム(pegylated liposome)の調製のために、リポソームをPEG-DSPEと混合し、激しく振騰させながら48℃で30分間インキュベーションした。
【0059】
シンドビスウイルスハイブリッドリポソーム(SINハイブリッドリポソーム)の調製は、PEG修飾リポソームを紫外線不活化シンドビスウイルスと混合し、激しく振騰させながら37℃で2時間インキュベーションすることにより実施した。
【0060】
細胞結合および薬物送達のインビトロにおける検討を、次のように実施した。まず、癌細胞を細胞数2×105で直径35mmの培養シャーレ播種して培養した。24時間後、FITC‐デキストランを封入したSINハイブリッドローダミン標識化リポソームをDMEM中で希釈し、培養シャーレにウエル当たり総脂質0.3mgの濃度で添加した。37℃で1時間インキュベーション後、細胞をリン酸緩衝生理食塩水(PBS、pH7.4)で3回洗浄し、結合していないリポソームを除去した。結合した蛍光リポソームをオリンパスフロロビュー コンフォーカルレーザースキャンニング顕微鏡(オリンパス社製)で可視化した。
【0061】
抗癌剤を封入したリポソームの細胞傷害性の検討のために、シスプラチンをSINハイブリッドリポソームまたは非SINハイブリッドリポソームに導入した。癌細胞は細胞数1×103/wellで96ウエルプレートに播種した。24時間後、シスプラチン若しくはNSを含むSINハイブリッドリポソーム、またはシスプラチン若しくはNSを含む非SINハイブリッドリポソームをDMEM中で総脂質0.3mg/mlの濃度に希釈し、100μl/wellを8ウエルに添加し、そしてプレートを5% CO2雰囲気下で37℃にて48時間インキュベーションした。異なる処理後の細胞生存率をMTTアッセイを使用して測定した。細胞生存率は対照に対する割合として算出した。
【0062】
リポソームのインビボ治療効果を次に説明するように検討した。まず、RERF-LC-AI細胞を回収し、培地に5×107/mLの濃度でけん濁した。異種移植(xenograft)腫瘍を、100μlのFCS不含培養培地中の5×106腫瘍細胞を6週齢のメスBALB/c nu/nuマウスの背部皮膚に皮下注射することにより確立した。腫瘍容積が約100 mm3になった時点で治療を開始した。シスプラチン若しくはNSを含むSINハイブリッドリポソーム、またはシスプラチン若しくはNSを含む非SINハイブリッドリポソームを、総脂質0.4 mmol/kgで週1回、7週間にわたって頸静脈から注入した。腫瘍容積(mm3)は、式0.873×a×b×cにより算出し、ここでaは最長直径、bは最短直径、およびcは高さである。マウスの体重はモニターし記録した。
【0063】
[結果]
【0064】
シンドビスウイルスの生体内分布を検討した結果、GFP発現シンドビスウイルス(GFP-SIN)を静脈注射した担癌ヌードマウスにおいて、GFP-SINの腫瘍特異的な分布(spread)が認められた(図1)。具体的には、GFP-SINは、GFP-SINを静脈注射された担癌ヌードマウスの腫瘍から調製した溶解物中に特異的に認められた(図1)。当該マウスの他の臓器にはGFP-SINの感染はほとんど認められなかった。
【0065】
次に、SINハイブリッドリポソームを作製して吸着能と内容物移送能を評価した。具体的には、腫瘍細胞(口腔癌、肺癌、抗癌剤耐性株)および正常細胞をFITC‐デキストランを封入したローダミン標識化SINハイブリッドリポソームまたはローダミン標識化非SINハイブリッドリポソームとインキュベーションし、そして共焦点顕微鏡で観察した。ローダミン標識化非SINハイブリッドリポソームでインキュベーションした細胞中では、わずかな蛍光しか観察されなかったのに対し、ローダミン標識化SINハイブリッドリポソームで細胞を処理した時には細胞膜上には多数のローダミン蛍光が、そして、細胞質内にはFITCが検出された。一方、正常細胞株へのリポソームの特異的吸着や封入された薬物の移送の程度は低かった。
【0066】
このように、腫瘍細胞株では、SINハイブリッドリポソームの特異的な吸着、および封入された薬物の移送が観察され、SINハイブリッドリポソームが腫瘍ターゲッティング薬物輸送用担体として有用であることが示唆された。
【0067】
SINハイブリッドリポソームの薬物輸送能を試験するために、リポソームへ抗癌剤を封入して、癌細胞株(口腔癌、肺癌、抗癌剤耐性株)と正常細胞株への抗癌剤の効果を検討した。具体的には、SINハイブリッドリポソームのインビトロでの細胞傷害性を、NSを封入したSINハイブリッドリポソームとシスプラチン若しくはNSを封入した非SINハイブリッドリポソームの細胞傷害性と比較検討した。シスプラチンを封入したSINハイブリッドリポソームは、腫瘍細胞に対して、他のリポソームと比較して有意に高い細胞傷害活性を48時間インキュベーション試験で示した(図2)。
【0068】
このように、SINハイブリッドリポソームが腫瘍細胞へのシスプラチン輸送に有効であることがインビトロ試験において判明した。
【0069】
抗癌剤を封入したこのリポソームを担癌マウスに血中投与してインビボ腫瘍ターゲティング効果を検討した。具体的には、100 mm3の定着腫瘍(established tumor)を担持するマウスをランダムに4群に分けた。シスプラチンを封入したSINハイブリッドリポソームを注入したマウスは急速な腫瘍退縮を示した。これに対し、NSを封入したSINハイブリッドリポソームまたはシスプラチン若しくはNSを封入したSINハイブリッドリポソームを注入したマウスは大きな腫瘍(1500〜2000mm3)を形成し、最終的に49日目に安楽死させた(図3)。
【0070】
このように、SINハイブリッドリポソームを使用することにより、インビボでも抗癌剤の効果を腫瘍特異的に得られることが判明した。この結果は、SINハイブリッドリポソームがインビボにおいても封入された薬物を腫瘍特異的に輸送することを示唆する。
【産業上の利用可能性】
【0071】
本発明によれば、腫瘍細胞に特異的に薬物を輸送することができるため、癌治療において副作用の軽減された高い効果を得ることができる。このように、本発明は医薬開発分野において極めて有用な発明である。
【技術分野】
【0001】
本発明は、腫瘍細胞内への薬物導入用ベクターに関する。より詳しくは、本発明は、シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクターに関する。さらに本発明は、薬物が封入された上記ベクターに関する。また本発明は、抗腫瘍効果を示す薬物が封入された上記ベクターを含有する癌治療用組成物、および、標識物質が封入された上記ベクターを含有する腫瘍細胞標識化用組成物に関する。さらにまた本発明は、抗腫瘍効果を示す薬物が封入された上記ベクターを投与することを特徴とする癌治療方法、および、標識物質が封入された上記ベクターを投与することを特徴とする腫瘍細胞標識化方法に関する。
【背景技術】
【0002】
薬物を効果的かつ集中的に、標的とする患部、すなわち臓器や組織、細胞、病原体などに送達する薬物投与に関する技術、いわゆるドラッグデリバリーシステム(以下、DDSと略称することがある)の開発が盛んに行われている。DDSは、薬物の投与方法や投与形態を工夫することにより体内での薬物動態を制御し、それにより薬物の標的部位への選択的送達を可能とする。その結果、薬物による最適の治療効果、さらに薬物による副作用の軽減を達成することができる。各種のDDS製剤が開発されているが、中でもリポソームは有用な(DDS)製剤として注目されている。
【0003】
リポソームは、生体の細胞膜を構成しているリン脂質を基本とする脂質二重層からなる閉鎖型小胞体であり、水溶性や脂溶性の薬物を封入することができる。したがって、リポソームは、生体適合性が高く、また、体内では封入された薬物を分解酵素などから保護しながら輸送できるため、DDSにおける薬物輸送体として有用である。一方、リポソームは肝臓や脾臓を中心とする細網内皮系組織(RES)の貪食細胞により捕捉され易く、その結果肝臓や脾臓に蓄積し易く、また、生体から排出され易いという問題点がある。
【0004】
近年、リポソームのDDS製剤としての有用性を高めた機能性リポソームが開発されている。例えば、標的とする組織や細胞へのターゲティング機能(標的到達特異性)を高めるために、リガンドや抗体により修飾したリポソームが開発されている。また、リポソームの一般的性質、例えば封入物のもれ、凝集、およびRESでの捕捉などの性質を改良するために、リポソームの表面を水溶性高分子ポリエチレングリコール(以下、PEGと略称することがある。)などの、親水性ポリマーで修飾することにより、RESに捕捉されにくく、血中に長時間循環滞留する特性を有するリポソームが開発されている(非特許文献1)。PEG修飾リポソームは、ステルスリポソームと呼ばれている。ドキソルビシンを封入したPEG修飾リポソームは、DOXIL登録商標という商品名で上市され、悪性腫瘍の治療に使用されている。また、PEG修飾リポソームは化学療法剤を封入するだけでなく、ポルフィリン誘導体による光化学療法、ボロン化合物による中性子捕捉療法への応用研究が進められている。
【0005】
一方、リポソームの細胞質内への導入効率を高めるために、膜融合能を有するウイルスとリポソームとを融合させて作製した細胞内物質導入ベクターが開発されている(特許文献1)。ウイルスとリポソームとを融合させて作製した細胞内物質導入ベクターは、内部にリポソーム由来の内空を有し、脂質二重層の外側にはウイルスエンベロープと同じタンパク質を有している。そのため、このようなリポソームは、その内空に封入された薬物をウイルスと同等の高い効率で細胞内に導入することができる。このようなベクターとして、例えばセンダイウイルス(Hemagglutinating Virus of Japan)や水疱性口内炎ウイルス(Vesicular Stomatitis Vius)とリポソームとを融合させてなるベクターが報告されている(非特許文献2および特許文献1)。水疱性口内炎ウイルス、またはその部分をリポソームと融合させたベクターは、生理的条件下でも赤血球溶血作用を示さず、安全に使用できるように良好な安定性と優れた細胞内物質導入率を示すことが報告されている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開平11-187873号公報。
【非特許文献】
【0007】
【非特許文献1】クリバノフ(Klibanov A.L.)ら、「フェブス レターズ(FEBS Letters)」、1990年、第268巻、p.235-237。
【非特許文献2】ナカガワ(Nakagawa T.)ら、「ドラッグ デリバリー システム(Drug Delivery System)」、1996年、第11巻、p.411-417。
【発明の概要】
【発明が解決しようとする課題】
【0008】
現在、癌治療に有効なDDSを含め、DDSの開発が盛んに行われているが、腫瘍細胞に特異的かつ効率的に吸着・摂取されるようなシステムの開発には至っていない。
【0009】
DDS製剤として有用とされているリポソームも、それ自体の腫瘍標的性は低い。そのため、EPR(Enhanced Permeability Retention)効果や、腫瘍関連抗原に対する抗体の修飾、腫瘍関連抗原の封入による腫瘍免疫の誘導などにより腫瘍標的性を高めている。EPR効果や腫瘍免疫の誘導は二次的効果であり、また、効果的な腫瘍関連抗原は研究段階にあるため、腫瘍標的性はなお低く、その向上が求められている。また、上記リポソームは、臨床応用を検討した際に、非腫瘍細胞へも薬物導入効果が高いことが観察され、重大な副作用を惹き起こす可能性があるため、腫瘍標的性を改善する必要がある。
【0010】
本発明の課題は、腫瘍細胞に特異的かつ効率的に吸着・摂取されるようなDDS製剤を提供することである。
【課題を解決するための手段】
【0011】
本発明者らは、上記目的を達成すべく、腫瘍溶解ウイルス(Oncolytic virus)に着目し、鋭意研究を行った。本発明者らが研究を行ってきたレオウイルス科レオウイルスおよびトガウイルス科アルファウイルス属シンドビスウイルスは腫瘍に特異的に感染(吸着)し、腫瘍特異的に増殖する。特にシンドビスウイルスは非常に多くの種類の腫瘍細胞、例えば悪性黒色腫、悪性リンパ腫、扁平上皮癌、および腺癌などに感染する。これらウイルスの腫瘍細胞への感染(吸着)は腫瘍細胞膜上のレセプターを介して行われることが知られており、数種類のレセプターが同定されている。このため、これらのレセプターと結合するリガンドを用いれば癌特異的なDDSの開発が可能になると考えた。
【0012】
そして、シンドビスウイルスと融合させたリポソームが、腫瘍細胞に特異的かつ効率的に吸着・摂取されること、および抗腫瘍効果を示す薬物を封入した該リポソームが、該薬物を封入した通常のリポソームと比較して腫瘍細胞に対する高い細胞障害性を示すことを見出し、本発明を達成した。
【0013】
即ち、本発明は以下に関する。
1.シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター。
2.シンドビスウイルスのE1タンパク質およびE2タンパク質を実質的に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター。
3.シンドビスウイルスをショ糖密度勾配遠心処理してE1タンパク質およびE2タンパク質分画を得、これを構成成分としてリポソームとした、腫瘍細胞内への薬物導入用ベクター。
4.リポソームがポリエチレングリコールにより修飾されたリポソームである前記1.から3.のいずれかの腫瘍細胞内への薬物導入用ベクター。
5.ポリエチレングリコールが、平均分子量1,000〜5,000のポリエチレングリコールである前記4.の腫瘍細胞内への薬物導入用ベクター。
6.薬物が封入された前記1.から5.のいずれかの腫瘍細胞内への薬物導入用ベクター。
7.薬物が抗腫瘍効果を示す薬物である前記6.の腫瘍細胞内への薬物導入用ベクター。
8.抗腫瘍効果を示す薬物がシスプラチンである前記7.の腫瘍細胞内への薬物導入用ベクター。
9.薬物が標識物質である前記6.の腫瘍細胞内への薬物導入用ベクター。
10.前記1.から5.のいずれかの腫瘍細胞内への薬物導入用ベクターの、癌治療用組成物の製造における使用。
11.前記7.または8.の腫瘍細胞内への薬物導入用ベクターを有効成分として含有する癌治療用組成物。
12.前記7.または8.の薬物導入用ベクターを投与することを特徴とする癌治療方法。
13.前記1.から5.のいずれかの腫瘍細胞内への薬物導入用ベクターの、腫瘍細胞標識化用組成物の製造における使用。
14.前記9.の薬物導入用ベクターを含有する腫瘍細胞標識化用組成物。
15.前記9.の薬物導入用ベクターを投与することを特徴とする腫瘍細胞標識化方法。
【発明の効果】
【0014】
本発明によれば、シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター、並びに、該ベクターを含有する癌治療用組成物および腫瘍細胞標識化用組成物を提供できる。
【0015】
本発明に係る薬物導入用ベクターは、腫瘍細胞に特異的に吸着するため、封入された薬物を腫瘍細胞特異的に輸送することができる。そのため、封入された薬物の正常細胞に対する副作用が軽減される。
【0016】
また、シンドビスウイルスは、蚊の媒介によりヒトに感染するが、軽微な発熱を惹き起こすだけの低病原性ウイルスであり、全身投与もできることから、その成分を用いた製剤は副作用が少なく、かつ全身投与が可能な安全で有用な薬剤であると考えられる。
【0017】
このように本発明は、腫瘍細胞に特異的かつ効率的に吸着・摂取され、高い腫瘍細胞障害性を示す一方、副作用の軽減されたDDS製剤を提供するものであり、癌治療分野において有用である。
【図面の簡単な説明】
【0018】
【図1】グリーン蛍光タンパク質(GFP)発現シンドビスウイルス(図中、GFP-SIN (+))を静脈注射した担癌ヌードマウスにおいて、腫瘍特異的な該ウイルスの分布が観察されたことを説明する図である。腫瘍(Tumor)において高いGFP蛍光が観察されたが、脳(Brain)、心臓(Heart)、肺(Lung)、肝臓(Liver)、腎臓(Kidney)、精巣(Intestine)で観察されたGFP蛍光は、GFPのみを静脈注射した担癌ヌードマウスのものと同程度であった。(実施例1)
【図2】シスプラチンを封入したシンドビスウイルス(SIN)ハイブリッドリポソームが、正常生理食塩水(NS)を封入したSINハイブリッドリポソームやシスプラチン若しくはNSを封入した非SINハイブリッドリポソームと比較して、腫瘍細胞株(HSC-2、HSC-3、RERF-LC-AI)に対して高い細胞傷害性を示したことを説明する図である。一方、正常線維芽細胞(Fibroblast)に対する細胞傷害性効果に大きな差異は無かった。図中、シスプラチンを封入したSINハイブリッドリポソームはSIN liposome cisplatinと表示する。また、NSを封入したSINハイブリッドリポソーム、シスプラチン若しくはNSを封入した非SINハイブリッドリポソームは、それぞれSIN liposome NS、liposome cisplatin、liposome NSと表示する。(実施例1)
【図3】シスプラチンを封入したシンドビスウイルス(SIN)ハイブリッドリポソームを注入したマウスでは急速な腫瘍退縮が観察されたことを説明する図である。一方、正常生理食塩水(NS)を封入したSINハイブリッドリポソームまたはシスプラチン若しくはNSを封入したSINハイブリッドリポソームを注入したマウスでは大きな腫瘍(1500〜2000 mm3)が形成された。横軸はリポソーム注入後の日数を、縦軸は腫瘍体積(Tumor Volume)を示す。図中、シスプラチンを封入したSINハイブリッドリポソームはSIN liposome cisplatinと表示する(●)。また、NSを封入したSINハイブリッドリポソーム、シスプラチン若しくはNSを封入した非SINハイブリッドリポソームは、それぞれSIN liposome NS、liposome cisplatin、liposomeNSと表示する(□、■、△)。(実施例1)
【発明を実施するための形態】
【0019】
本発明は、シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクターに関する。本薬物導入用ベクターは腫瘍細胞特異性が高く、該ベクターに封入した薬物を腫瘍細胞に特異的かつ効率的に輸送できるという特徴を有し、さらに該薬物による正常細胞への副作用が軽減されるという利点を併せ持つ。
【0020】
腫瘍細胞内への薬物導入用ベクターとは、腫瘍細胞内に薬物を輸送するための運搬体を意味する。
【0021】
シンドビスウイルスはエンベロープを有する正二十面体様構造の一本鎖(+)RNAウイルスである。その感染は蚊によって媒介され、脊椎動物に感染するが、ヒトでは軽い風邪症状を引き起こすのみの低病原性ウイルスである。
【0022】
シンドビスウイルスは、腫瘍溶解ウイルス(Oncolytic virus)として知られ、非常に多くの種類の腫瘍細胞、例えば悪性黒色腫、悪性リンパ腫、扁平上皮癌、および腺癌などに感染し、腫瘍細胞特異的に増殖する。また、シンドビスウイルスによる、子宮頸癌細胞および卵巣癌細胞の治療の可能性が報告されている(ウンノ(Unno Y.)ら、「キャンサー セラピー(Cancer Therapy)」、2005年、第11巻、第12号、p.4553-4560)。腫瘍溶解ウイルス(Oncolytic virus)とは、腫瘍細胞特異的に結合、吸着して腫瘍細胞内部に侵入し、腫瘍細胞内で複製して腫瘍細胞のみを殺滅する能力をもつウイルスをいう。腫瘍細胞特異的とは、正常細胞と比較して腫瘍細胞に選択的に作用し、正常細胞にはほとんど作用しないことを意味する。
【0023】
エンベロープを有するウイルスの標的細胞への感染には、一般的にエンベロープに存在するエンベロープタンパク質が関与することが知られている。エンベロープは、一部のウイルスが有する脂質二重膜構造であり、ウイルス粒子の最も外側に位置しており、ウイルスの基本構造となるウイルスゲノムを含むカプシドを覆っている。エンベロープは、ウイルスが感染細胞内で増殖し、細胞外に出る際に細胞膜あるいは核膜などの生体膜を被ったまま出芽することによって獲得されるものである。このため、基本的には宿主細胞の脂質二重膜に由来するものであるが、この他にウイルス遺伝子にコードされているそのウイルス独自のタンパク質を生体膜に発現した後で該生体膜と一緒にウイルス粒子に取り込み、エンベロープタンパク質としてウイルス粒子表面に発現させている。エンベロープタンパク質は、糖タンパク質であり、スパイクとも呼ばれ、エンベロープ上に突出して存在する。エンベロープタンパク質には、そのウイルスの標的細胞への吸着・侵入において標的細胞側が持つレセプターに結合する機能や、宿主の生体防御機能を回避する機能など、さまざまな機能を持つものが知られており、ウイルスの感染に重要な役割を果たしている。標的細胞の細胞膜に由来するエンベロープを有するウイルスの多くでは、エンベロープタンパク質が標的細胞側のレセプターに結合した後、ウイルスのエンベロープと細胞膜とが膜融合することにより、エンベロープに内包されていたウイルスゲノムを含むカプシドが標的細胞内に送達される。
【0024】
シンドビスウイルスはE1タンパク質およびE2タンパク質と呼ばれるエンベロープタンパク質を有することが知られており、これらE1タンパク質およびE2タンパク質が、標的細胞への特異的吸着に関与していると考えられる。
【0025】
したがって、シンドビスウイルスの一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクターとして、好ましくはシンドビスウイルスのエンベロープタンパク質を実質的に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター、さらに好ましくはシンドビスウイルスのE1タンパク質およびE2タンパク質を実質的に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクターを例示できる。ここで、「エンベロープタンパク質を実質的に含む」とは、エンベロープタンパク質を含む限り、シンドビスウイルス由来のその他のタンパク質、例えばコアタンパク質が含まれていてもよいことを意味する。また、「E1タンパク質およびE2タンパク質を実質的に含む」とは、E1タンパク質およびE2タンパク質を含む限り、シンドビスウイルス由来のその他のタンパク質、例えばE1タンパク質およびE2タンパク質以外のエンベロープタンパク質やコアタンパク質が含まれていてもよいことを意味する。
【0026】
シンドビスウイルスまたはその一部分を構成成分に含むリポソームを、本明細書ではシンドビスウイルスハイブリッドリポソームと称することがある。
【0027】
シンドビスウイルスハイブリッドリポソームの製造は、シンドビスウイルスまたはその一部分とリポソームとを自体公知の方法で融合させることにより実施できる。シンドビスウイルスまたはその一部分とリポソームとを融合させるとは、シンドビスウイルスまたはその一部分とリポソーム膜の脂質とが同一の膜を構成し、かつ、シンドビスウイルスまたはその一部分に含まれるタンパク質の構造や機能がリポソーム膜中でもウイルス粒子中に存在したときと同等に示されるように処理することをいう。
【0028】
その製造において、シンドビスウイルスは不活化して使用する。シンドビスウイルスの調製は、自体公知の感染可能な細胞に感染させ増殖させることにより実施でき、その不活化は、自体公知の方法、例えば紫外線照射や界面活性剤処理により実施できる。
【0029】
具体的には、不活化シンドビスウイルスとリポソームとを混合し、激しく振騰させながら37℃でインキュベーションすることにより、シンドビスウイルスハイブリッドリポソームを製造することができる。インキュベーションの時間は、一般的に6時間〜1時間、好ましくは3〜1時間、より好ましくは2時間である。また、シンドビスウイルスのE1タンパク質およびE2タンパク質を実質的に含むリポソームは、シンドビスウイルスをショ糖密度勾配遠心処理してE1タンパク質およびE2タンパク質分画を得、これを構成成分としてリポソームとすることにより製造することができる。
【0030】
リポソームの製造は、自体公知のリポソーム調製法を使用して実施できる。リポソームは、その構造から、多重層小胞(multilamellar vesicles、MLV)と単一層小胞(unilamellar vesicles)に分類される。単一層小胞はさらに直径により、直径20-100nmの小単一層小胞(small unilamellar vesicles、SUV)、直径100-1000nmの大単一層小胞(large unilamellar vesicles、LUV)、直径5000-100000nmの巨大単一層小胞(giant unilamellar vesicles、GUV)に分けられる。MLVの調製はボルテックス処理法で実施できる。SUVの調製法としては、超音波処理法、エタノール注入法、界面活性剤除去法、押出し法等が知られている。LUVの調整法としては、逆相蒸発法、エタノール注入法、凍結融解法、押出し法等が知られている。また、GUVの調整法としては、静置水和法、電気的形成法、有機溶媒透析法、凍結融解塩透析法等が知られている。MLVは、一般に安定で高分子物質の保持効率もよいが、大きさが不均一で多重層であるため、封入薬剤の細胞への導入効率が低い。しかし、MLVは超音波処理後にインキュベーションするアニーリング法により、SUV、さらにLUVに変化させることができる。SUVは大きさが均一であるが、高分子物質を保持しにくく、比較的不安定である。LUVは、蛋白質やDNAなどの保持効率がよいが、大きさが不均一である。このようにリポソームの調製には多数の方法が知られており、封入する薬物や用途に応じて適当なリポソームを選択し、該リポソームに適当な調製法を採用すればよい。
【0031】
リポソームは、多重層小胞であっても、単一層小胞であってもよいが、単一層小胞であることが好ましい。大きさも特に限定されないが、直径10μm〜0.1μm、好ましくは3μm〜0.1μm、さらに好ましくは0.5μm〜0.1μmであることが適当である。
【0032】
リポソームの構成成分としては、一般に、リン脂質、コレステロール類、窒素脂質等が使用されるが、特にリン脂質が好適に使用される。
【0033】
脂質としては、リン脂質、糖脂質、ステロール、および飽和または不飽和の脂肪酸などを例示できる。リン脂質の具体例としては、ホスファチジルコリン、ホスファチジルセリン、ホスファチジルグリセロール、ホスファチジルイノシトール、ホスファチジルエタノールアミン、ホスファチジン酸、カルジオリピン、スフィンゴミエリン、卵黄レシチン、大豆レシチン、リゾレシチン等の天然リン脂質、あるいはこれらを常法によって水素添加したものなどを挙げることができる。糖脂質の具体例としては、スルホキシリボシルグリセリド、ジグリコシルジグリセリド、ジガラクトシルジグリセリド、ガラクトシルジグリセリド、およびグリコシルジグリセリドなどのグリセロ糖脂質や、ガラクトシルセレブロシド、ラクトシルセレブロシド、およびガングリオシなどのスフィンゴ糖脂質などを挙げることができる。ステロールの具体例としては、コレステロール、コレステロールコハク酸、コレスタノール、ラノステロール、ジヒドロラノステロール、デスモステロール、およびジヒドロコレステロールなどの動物由来のステロール、スチグマステロール、シトステロール、カンペステロール、およびブラシカステロールなどの植物由来のステロール(フィトステロール)、並びにチモステロール、エルゴステロールなどの微生物由来のステロールを挙げることができる。飽和または不飽和の脂肪酸の具体例としては、 パルミチン酸、オレイン酸、ステアリン酸、アラキドン酸、およびミリスチン酸などの炭素数12〜20の飽和または不飽和の脂肪酸。を挙げることができる。これらの脂質は単独で使用することができるが、二種以上を組み合わせて使用することもできる。
【0034】
リポソームの構成成分としてさらに、脂質膜を物理的または化学的に安定させたり、脂質膜の流動性を調節したりするために、膜安定化剤を含有させることができる。膜安定化剤としては、ステロール、グリセリンまたはその脂肪酸エステルなどを例示できる。ステロールとしては、上記同様の具体例を挙げることができ、グリセリンの脂肪酸エステルとしては、例えば、トリオレイン、トリオクタノイン等を挙げることができる。
【0035】
また、脂質膜の酸化を防止するために抗酸化剤を含有させることができる。抗酸化剤としては、トコフェロール、没食子酸プロピル、パルミチン酸アスコルビル、ブチル化ヒドロキシトルエンなどを例示できる。
【0036】
さらに、脂質膜に正荷電又は負荷電を付与するために荷電物質を含有させることができる。正荷電を付与する荷電物質としては、ステアリルアミンおよびオレイルアミンなどの飽和または不飽和脂肪族アミンや、ジオレオイルトリメチルアンモニウムプロパンなどの飽和または不飽和カチオン性合成脂質などを例示できる。負電荷を付与する荷電物質としては、ジセチルホスフェート、コレステリルヘミスクシネート、ホスファチジルセリン、ホスファチジルイノシトール、ホスファチジン酸などを例示できる。
【0037】
より具体的なリポソームとして、卵黄ホスファチジルコリン、コレステロール、およびホスファチジルセリンをモル比4:5:1で混合し、脱水再水和法により製造したリポソームを例示できる(実施例1参照)。
【0038】
リポソームは、その外表面を親水性ポリマーで修飾することができる。このような修飾により、リポソームのRESへの捕捉を回避することができ、リポソームの血中循環滞留時間を長くすることができるため、腫瘍細胞内への薬剤輸送をより効率的に行うことができる。親水性ポリマーとして、ポリエチレングリコール、ポリメチルエチレングリコール、ポリヒドロキシプロピレングリコール、ポリプロピレングリコール、ポリメチルプロピレングリコール、およびポリヒドロキシプロピレンオキシドが例示できる。特に好ましくはポリエチレングリコールである。シンドビスウイルスハイブリッドリポソームの形成において、リポソーム膜に融合されたウイルスタンパク質がポリエチレングリコールにより埋没しないように、使用するポリエチレングリコールの分子量を選択することが好ましい。ポリエチレングリコールの平均分子量として、好ましくは1,000〜5,000、より好ましくは1,000〜3,000、さらに好ましくは2000が適当である。このようなポリエチレングリコールとして、例えば、PEG-DSPE(1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-[Methoxy(Polyethyleneglycol)-2000])を例示できる。
【0039】
シンドビスウイルスハイブリッドリポソームへの薬物の封入は、通常、シンドビスウイルスまたはその一部とリポソームとの融合の前に、リポソームの製造工程において実施する。すなわち、リポソームに所望の薬物を封入し、その後、薬物が封入されたリポソームとシンドビスウイルスまたはその一部とを融合することにより実施する。リポソームへの薬物の封入は、自体公知の方法で実施できる。例えばリポソーム製造用原料、例えば脂質の混合物から薄膜を作製し、該薄膜を所望の薬物を含有する溶液にけん濁して混合することにより、薬物のリポソームへの封入を実施できる。混合後に、必要に応じて超音波処理などを施しても良い。より具体的には、例えば、リン脂質をクロロホルムなどの有機溶媒に溶解した溶液に、目所望の薬物を溶媒に溶解した溶液を加えた後、溶媒を留去し、これにリン酸緩衝液を加え、振とう、超音波処理および遠心処理した後、上清をろ過処理して回収することにより行い得る。
【0040】
封入する薬物は、特に制限はないが、その具体例としては、抗腫瘍効果を示す薬物や核酸などを挙げることができる。抗腫瘍効果とは、腫瘍の増殖を抑制して減弱させる作用、腫瘍の浸潤を抑制して減弱させる作用、および腫瘍を殺滅する作用のいずれも意味する。抗腫瘍効果を示す薬物は、癌治療の目的に用いられている薬剤であればいずれでもよく、シスプラチンやオキサリプラチンなどのプラチナ製剤、シクロホスファミドやダカルバジンなどのアルキル化剤、フルオロウラシルやテガフールなどの代謝拮抗剤、イリノテカンやパクリタキセルなどの植物アルカロイド、アクチノマイシンDやドキソルビシンなどの抗癌性抗生物質、アナストロゾールやタモキシフェンなどのホルモン剤、およびインターフェロンなどの生物学的応答調節剤を挙げることができる。核酸としては、所望のタンパクをコードした核酸、所望のタンパクの発現を抑制することのできる核酸、例えばアンチセンス核酸、siRNAやshRNAなどの短鎖二本鎖RNA、自殺遺伝子、アポトーシス誘導遺伝子などを挙げることができる。
【0041】
封入する薬物としてその他、癌の光化学療法に使用されるポルフィリン誘導体などの光増感剤を好適に例示できる。光化学療法は生体に光増感剤を投与後にレーザー光を照射した部位のみで薬剤が活性化を受けるため、副作用が少ないという利点を有する。光増感剤は腫瘍蓄積性が低いという問題を有するが、本願の薬物導入用ベクターに封入して使用することにより、腫瘍蓄積性が増加し、高い治療効果を得られる。
【0042】
封入する薬物としてその他、腫瘍細胞を標識化するための標識物質を好適に例示できる。標識物質として、例えば、テクネチウム99mなどのγ線を放出する核種を含む化合物を挙げることができる。このような化合物はイメージング剤と呼ばれ、腫瘍に蓄積させてγ線を検出することにより、腫瘍の検出を実施できる。本願の薬物薬物導入用ベクターに封入して使用することにより、腫瘍特異的にイメージング剤を蓄積させることができるため、腫瘍の検出を精度高く行うことができ、また、正常組織への副作用も少ない。さらに、転移癌の検出も可能である。標識物質としてその他、蛍光物質を挙げることができる。
【0043】
封入する薬物は、一種類であってよく、また二種類以上を組み合わせて封入することができる。封入する薬物の量は、特に限定されず、その有効性により適宜変更することができる。
【0044】
本発明に係る薬物薬物導入用ベクターは、腫瘍細胞特異性が高く、該ベクターに封入した薬物を腫瘍細胞に特異的かつ効率的に輸送できるという特徴を有する。そのため薬物導入用ベクターは、食道癌、肺癌、乳癌、胃癌、結腸・直腸癌、膵臓癌、肝臓癌、腎癌、膀胱癌、および子宮癌などの固形癌、腹水癌や胸水癌などの浮遊癌、白血病やリンパ腫などの造血系癌などの広範な癌に適用できる。
【0045】
本発明においては、抗腫瘍効果を示す薬物や核酸などの癌治療用薬物を封入した上記薬物導入用ベクターを有効成分として含有する癌治療用組成物を提供できる。癌治療用組成物は、薬物導入用ベクターのほかに、薬学的に許容される担体を含む。薬学的に許容される担体としては、薬学的に許容される担体としては、例えば、水、医薬的に許容される有機溶剤、コラーゲン、ポリビニルアルコール、ポリビニルピロリドン、カルボキシビニルポリマー、アルギン酸ナトリウム、水溶性デキストラン、カルボキシメチルスターチナトリウム、ペクチン、キサンタンガム、アラビアゴム、カゼイン、ゼラチン、寒天、グリセリン、プロピレングリコール、ポリエチレングリコール、ワセリン、パラフィン、ステアリルアルコール、ステアリン酸、ヒト血清アルブミン、マンニトール、ソルビトール、ラクトースを例示できる。これらは、本薬剤の剤形に応じて適宜1種類または2種類以上を組み合わせて使用される。その他、安定化剤、殺菌剤、緩衝剤、等張化剤、およびpH調整剤等を適宜使用することもできる。安定化剤は、例えばヒト血清アルブミンや通常のL−アミノ酸、糖類、セルロース誘導体を例示できる。L−アミノ酸は、特に限定はなく、例えばグリシン、システイン、グルタミン酸等のいずれでもよい。糖類も特に限定はなく、例えばグルコース、マンノース、ガラクトース、果糖等の単糖類、マンニトール、イノシトール、キシリトール等の糖アルコール、ショ糖、マルトース、乳糖等の二糖類、デキストラン、ヒドロキシプロピルスターチ、コンドロイチン硫酸、ヒアルロン酸等の多糖類等およびそれらの誘導体等のいずれでもよい。セルロース誘導体も特に限定はなく、メチルセルロース、エチルセルロース、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、カルボキシメチルセルロースナトリウム等のいずれでもよい。緩衝剤は、ホウ酸、リン酸、酢酸、クエン酸、ε−アミノカプロン酸、グルタミン酸および/またはそれらに対応する塩(例えばそれらのナトリウム塩、カリウム塩、カルシウム塩、マグネシウム塩等のアルカリ金属塩やアルカリ土類金属塩)を例示できる。等張化剤は、塩化ナトリウム、塩化カリウム、糖類、グリセリンを例示できる。
【0046】
本発明においては、腫瘍細胞を標識化するための標識物質を封入した上記薬物導入用ベクターを有効成分として含有する腫瘍細胞標識化用組成物を提供できる。腫瘍細胞標識化用組成物は、薬物導入用ベクターのほかに、薬学的に許容される担体を含むことができる。
【0047】
本発明に係る癌治療用組成物および腫瘍細胞標識化用組成物は、ボーラス注射または連続注入により非経口的に投与することができる。投与経路は、静脈や動脈などに投与するか、または腫瘍組織に直接投与することができる。腫瘍溶解ウイルス(Oncolytic virus)は、腫瘍特異的に吸着・進入することが知られており、例えばシンドビスウイルスは、感染により軽微な発熱を惹き起こすだけの低病原性ウイルスであり、全身投与もできることから、その成分を用いた製剤は副作用が少なく、かつ全身投与が可能な安全で有用な薬剤であると考えられる。
【0048】
本発明に係る組成物の用量範囲は特に限定されず、薬物導入用ベクターに封入した薬物の有効性、投与形態、投与経路、対象の性質(体重、年齢、病状および他の医薬の使用の有無等)、および担当医師の判断等に応じて適宜選択される。
【0049】
本発明においては、抗腫瘍効果を示す薬物や核酸などの癌治療用薬物を封入した上記薬物導入用ベクターや、該薬物導入用ベクターを含有する医薬組成物を、癌疾患を有する対象に投与することを特徴とする癌治療方法を提供する。
【0050】
本発明においては、腫瘍細胞を標識化するための標識物質を封入した上記薬物導入用ベクターや、該薬物導入用ベクターを含有する組成物を、対象に投与することを特徴とする腫瘍細胞標識化方法を提供する。本腫瘍細胞標識化方法により腫瘍細胞特異的に標識物質が蓄積するため、蓄積した標識物質を測定することにより、腫瘍細胞検出を実施できる。したがって、本腫瘍細胞標識化方法は、腫瘍細胞検出方法に使用でき、さらに癌疾患の診断、および、癌転移の診断に使用できる。
【0051】
以下、実施例を示して本発明をより具体的に説明するが、本発明は以下に示す実施例によって何ら限定されるものではない。
【実施例1】
【0052】
シンドビスウイルスとリポソームとを融合させたハイブリッドリポソームを作製し、該ハイブリッドリポソームの腫瘍細胞への吸着特異性および封入薬物の輸送能、並びに抗癌剤を封入した該ハイブリッドリポソームのインビトロおよびインビボでの細胞障害性を検討した。以下、シンドビスウイルスとリポソームとを融合させたハイブリッドリポソームをSIMハイブリッドリポソームと称し、シンドビスウイルスと融合させていないリポソームを非SIMハイブリッドリポソームと称することがある。
【0053】
[材料および方法]
【0054】
シスプラチン(cis-diammineplatinum(II) dichloride,Pt(NH3)2Cl2)、コレステロール(以下、CHと略称することがある。)、ホスファチジルセリン(以下、PSと略称することがある。)、およびFITC-4KD(Fluoresceinisothiocyanate-4KD)はシグマケミカル(Sigma Chemical)社より購入した。正常生理食塩水(以下、NSと略称することがある。)は株式会社大塚製薬工場より購入した。卵黄ホスファチジルコリン(以下、EPCと略称することがある。99%。)およびホスファチジルエタノールアミン(PE)のポリエチレングリコール誘導体(PEG-DSPE2K、以下、PEPと略称することがある:PEGの平均分子量は2000である。)は日本油脂から得た。ヒト肺癌細胞株RERF-LC-AI、口腔癌細胞株HSC-2およびHSC-3、Vero細胞、並びに正常線維芽細胞は、10% ウシ胎仔血清(FCS)並びに50ユニット/mlのペニシリンおよびストレプトマイシンを含むダルベッコ変法イーグル培地(DMEM)中で培養した。初代培養ヒト角化細胞(Normal Human Keratinocyte、NHKと略称することがある。)は正常ヒト表皮角化細胞培地KGM中で培養した。N-(リサアミンローダミンBスルフォニル)-ホスファチジルエタノールアミン(以下、N-Rh-PEと略称することがある)、NED-PE、オレゴングリーンはインビトロージェン(Invitrogen)社より購入した。
【0055】
本発明において使用した野生型シンドビスウイルスAR339は、国立感染研究所(日本)より提供されたものである。ウイルスは、初代ニワトリ胚線維芽細胞中で増殖させ、次いでベロ細胞中で数回継代した。このウイルスを研究用ストックとして使用した。GFP発現組換えシンドビスウイルスTR339-GFP/2A(以下、GFP-SINと称する。)は、cDNAクローンpTR339-GFP/2Aから由来した。該cDNAクローンをXhoIによる消化で直線化し、そしてランオフ転写産物をSP6 RNAポリメラーゼを使用して産生した。RNA転写産物は、次いでC33A細胞に電気穿孔法で導入し、そして導入後48時間目にウイルスを含む成育培地を回収し、−80℃で凍結した。 AR339およびTR339-GFP/2Aは、10% FCSを含むDMEM中で37℃、5% CO2の条件下で維持されたC33A細胞中で増殖させ、ウイルス力価を単層のBHK-21細胞を使用するプラークアッセイにより測定した。
【0056】
シンドビスウイルスのインビボ分布およびターゲティング試験を、次に説明するように実施した。まず、C33A腫瘍担癌マウスに、 1x106 pfuのGFP-SINを含む100μLのDMEMを、頸静脈から注入した。腫瘍におけるGFP発現を注入後12時間ごとに調べた。GFP発現の測定は、GFP用反射照明蛍光ユニット(SZX-RFL2-GFP)を備えたオリンパス蛍光ステレオ顕微鏡(モデルSZX7)をハママツORCA-ER冷却CCDカメラと連結して使用することにより実施した。所定の間隔で、腫瘍部位および種々の臓器を切り離して秤量し、腫瘍内のシンドビスウイルスの蓄積を測定した。腫瘍および臓器を切り離した後、それらを秤量してはさみで細切し、4.31% スルホサリチル酸の1mlを含むガラスホモジェナイザーに入れた。種々の臓器由来の溶解物中のGFPカウントは、プレートリーダー(Wallac 1420 ARVOsx MultilabelCounter, Perkin-Elmer社製)で測定した蛍光により評価した。
【0057】
ウイルスの精製を次に説明するように実施した。ウイルスを含有する培地を、20% ショ糖を含む2ml容量の緩衝液上に重層した。ウイルス粒子は、Ti42ローター(Beckman社製)で50000gで2時間遠心処理することにより、回収した培地から沈澱させた。沈澱物は、100μl GTEN緩衝液(200mM グリシン、50mM Tris、100mM NaCl、1mM エチレンジアミン四酢酸(EDTA)、pH7.5にHCLで調製)に溶解した。ウイルスは、45分間の紫外線照射により不活化した。不活化したウイルスは複製できないが、ウイルスの吸着能および融合能は変わらずに残っている。
【0058】
リポソームの調製は、脱水再水和法により実施した。簡潔にいえば、EPC、コレステロール、およびPSをモル比4:5:1で含む脂質混合物を、クロロホルムを含む溶液にけん濁し、そして、クロロホルムを除去するために50℃でロータリーエバポレータにより留去した。リポソーム膜を標識化するために、N-Rh-PEまたはオレゴングリーン-DHPEを混合物に加えた。薄層(film)をNSまたは5mM シスプラチンで水和させた。その後、孔サイズ0.4μmのポリカーボネートフィルター (Nuclepore社製)を二重に重ねて(two stacked)、加圧エクストルーダー(Lipex Biomembranes社製)を用い、エクストルージョンを10回行った。PEG修飾リポソーム(pegylated liposome)の調製のために、リポソームをPEG-DSPEと混合し、激しく振騰させながら48℃で30分間インキュベーションした。
【0059】
シンドビスウイルスハイブリッドリポソーム(SINハイブリッドリポソーム)の調製は、PEG修飾リポソームを紫外線不活化シンドビスウイルスと混合し、激しく振騰させながら37℃で2時間インキュベーションすることにより実施した。
【0060】
細胞結合および薬物送達のインビトロにおける検討を、次のように実施した。まず、癌細胞を細胞数2×105で直径35mmの培養シャーレ播種して培養した。24時間後、FITC‐デキストランを封入したSINハイブリッドローダミン標識化リポソームをDMEM中で希釈し、培養シャーレにウエル当たり総脂質0.3mgの濃度で添加した。37℃で1時間インキュベーション後、細胞をリン酸緩衝生理食塩水(PBS、pH7.4)で3回洗浄し、結合していないリポソームを除去した。結合した蛍光リポソームをオリンパスフロロビュー コンフォーカルレーザースキャンニング顕微鏡(オリンパス社製)で可視化した。
【0061】
抗癌剤を封入したリポソームの細胞傷害性の検討のために、シスプラチンをSINハイブリッドリポソームまたは非SINハイブリッドリポソームに導入した。癌細胞は細胞数1×103/wellで96ウエルプレートに播種した。24時間後、シスプラチン若しくはNSを含むSINハイブリッドリポソーム、またはシスプラチン若しくはNSを含む非SINハイブリッドリポソームをDMEM中で総脂質0.3mg/mlの濃度に希釈し、100μl/wellを8ウエルに添加し、そしてプレートを5% CO2雰囲気下で37℃にて48時間インキュベーションした。異なる処理後の細胞生存率をMTTアッセイを使用して測定した。細胞生存率は対照に対する割合として算出した。
【0062】
リポソームのインビボ治療効果を次に説明するように検討した。まず、RERF-LC-AI細胞を回収し、培地に5×107/mLの濃度でけん濁した。異種移植(xenograft)腫瘍を、100μlのFCS不含培養培地中の5×106腫瘍細胞を6週齢のメスBALB/c nu/nuマウスの背部皮膚に皮下注射することにより確立した。腫瘍容積が約100 mm3になった時点で治療を開始した。シスプラチン若しくはNSを含むSINハイブリッドリポソーム、またはシスプラチン若しくはNSを含む非SINハイブリッドリポソームを、総脂質0.4 mmol/kgで週1回、7週間にわたって頸静脈から注入した。腫瘍容積(mm3)は、式0.873×a×b×cにより算出し、ここでaは最長直径、bは最短直径、およびcは高さである。マウスの体重はモニターし記録した。
【0063】
[結果]
【0064】
シンドビスウイルスの生体内分布を検討した結果、GFP発現シンドビスウイルス(GFP-SIN)を静脈注射した担癌ヌードマウスにおいて、GFP-SINの腫瘍特異的な分布(spread)が認められた(図1)。具体的には、GFP-SINは、GFP-SINを静脈注射された担癌ヌードマウスの腫瘍から調製した溶解物中に特異的に認められた(図1)。当該マウスの他の臓器にはGFP-SINの感染はほとんど認められなかった。
【0065】
次に、SINハイブリッドリポソームを作製して吸着能と内容物移送能を評価した。具体的には、腫瘍細胞(口腔癌、肺癌、抗癌剤耐性株)および正常細胞をFITC‐デキストランを封入したローダミン標識化SINハイブリッドリポソームまたはローダミン標識化非SINハイブリッドリポソームとインキュベーションし、そして共焦点顕微鏡で観察した。ローダミン標識化非SINハイブリッドリポソームでインキュベーションした細胞中では、わずかな蛍光しか観察されなかったのに対し、ローダミン標識化SINハイブリッドリポソームで細胞を処理した時には細胞膜上には多数のローダミン蛍光が、そして、細胞質内にはFITCが検出された。一方、正常細胞株へのリポソームの特異的吸着や封入された薬物の移送の程度は低かった。
【0066】
このように、腫瘍細胞株では、SINハイブリッドリポソームの特異的な吸着、および封入された薬物の移送が観察され、SINハイブリッドリポソームが腫瘍ターゲッティング薬物輸送用担体として有用であることが示唆された。
【0067】
SINハイブリッドリポソームの薬物輸送能を試験するために、リポソームへ抗癌剤を封入して、癌細胞株(口腔癌、肺癌、抗癌剤耐性株)と正常細胞株への抗癌剤の効果を検討した。具体的には、SINハイブリッドリポソームのインビトロでの細胞傷害性を、NSを封入したSINハイブリッドリポソームとシスプラチン若しくはNSを封入した非SINハイブリッドリポソームの細胞傷害性と比較検討した。シスプラチンを封入したSINハイブリッドリポソームは、腫瘍細胞に対して、他のリポソームと比較して有意に高い細胞傷害活性を48時間インキュベーション試験で示した(図2)。
【0068】
このように、SINハイブリッドリポソームが腫瘍細胞へのシスプラチン輸送に有効であることがインビトロ試験において判明した。
【0069】
抗癌剤を封入したこのリポソームを担癌マウスに血中投与してインビボ腫瘍ターゲティング効果を検討した。具体的には、100 mm3の定着腫瘍(established tumor)を担持するマウスをランダムに4群に分けた。シスプラチンを封入したSINハイブリッドリポソームを注入したマウスは急速な腫瘍退縮を示した。これに対し、NSを封入したSINハイブリッドリポソームまたはシスプラチン若しくはNSを封入したSINハイブリッドリポソームを注入したマウスは大きな腫瘍(1500〜2000mm3)を形成し、最終的に49日目に安楽死させた(図3)。
【0070】
このように、SINハイブリッドリポソームを使用することにより、インビボでも抗癌剤の効果を腫瘍特異的に得られることが判明した。この結果は、SINハイブリッドリポソームがインビボにおいても封入された薬物を腫瘍特異的に輸送することを示唆する。
【産業上の利用可能性】
【0071】
本発明によれば、腫瘍細胞に特異的に薬物を輸送することができるため、癌治療において副作用の軽減された高い効果を得ることができる。このように、本発明は医薬開発分野において極めて有用な発明である。
【特許請求の範囲】
【請求項1】
シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター。
【請求項2】
シンドビスウイルスのE1タンパク質およびE2タンパク質を実質的に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター。
【請求項3】
シンドビスウイルスをショ糖密度勾配遠心処理してE1タンパク質およびE2タンパク質分画を得、これを構成成分としてリポソームとした、腫瘍細胞内への薬物導入用ベクター。
【請求項4】
リポソームがポリエチレングリコールにより修飾されたリポソームである請求項1から3のいずれか1項に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項5】
ポリエチレングリコールが、平均分子量1,000〜5,000のポリエチレングリコールである請求項4に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項6】
薬物が封入された請求項1から5のいずれか1項に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項7】
薬物が抗腫瘍効果を示す薬物である請求項6に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項8】
抗腫瘍効果を示す薬物がシスプラチンである請求項7に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項9】
薬物が標識物質である請求項6に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項10】
請求項1から5のいずれか1項に記載の腫瘍細胞内への薬物導入用ベクターの、癌治療用組成物の製造における使用。
【請求項11】
請求項7または8に記載の腫瘍細胞内への薬物導入用ベクターを有効成分として含有する癌治療用組成物。
【請求項12】
請求項7または8に記載の薬物導入用ベクターを投与することを特徴とする癌治療方法。
【請求項13】
請求項1から5のいずれか1項に記載の腫瘍細胞内への薬物導入用ベクターの、腫瘍細胞標識化用組成物の製造における使用。
【請求項14】
請求項9に記載の薬物導入用ベクターを含有する腫瘍細胞標識化用組成物。
【請求項15】
請求項9に記載の薬物導入用ベクターを投与することを特徴とする腫瘍細胞標識化方法。
【請求項1】
シンドビスウイルスまたはその一部分を構成成分に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター。
【請求項2】
シンドビスウイルスのE1タンパク質およびE2タンパク質を実質的に含むリポソームからなる、腫瘍細胞内への薬物導入用ベクター。
【請求項3】
シンドビスウイルスをショ糖密度勾配遠心処理してE1タンパク質およびE2タンパク質分画を得、これを構成成分としてリポソームとした、腫瘍細胞内への薬物導入用ベクター。
【請求項4】
リポソームがポリエチレングリコールにより修飾されたリポソームである請求項1から3のいずれか1項に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項5】
ポリエチレングリコールが、平均分子量1,000〜5,000のポリエチレングリコールである請求項4に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項6】
薬物が封入された請求項1から5のいずれか1項に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項7】
薬物が抗腫瘍効果を示す薬物である請求項6に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項8】
抗腫瘍効果を示す薬物がシスプラチンである請求項7に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項9】
薬物が標識物質である請求項6に記載の腫瘍細胞内への薬物導入用ベクター。
【請求項10】
請求項1から5のいずれか1項に記載の腫瘍細胞内への薬物導入用ベクターの、癌治療用組成物の製造における使用。
【請求項11】
請求項7または8に記載の腫瘍細胞内への薬物導入用ベクターを有効成分として含有する癌治療用組成物。
【請求項12】
請求項7または8に記載の薬物導入用ベクターを投与することを特徴とする癌治療方法。
【請求項13】
請求項1から5のいずれか1項に記載の腫瘍細胞内への薬物導入用ベクターの、腫瘍細胞標識化用組成物の製造における使用。
【請求項14】
請求項9に記載の薬物導入用ベクターを含有する腫瘍細胞標識化用組成物。
【請求項15】
請求項9に記載の薬物導入用ベクターを投与することを特徴とする腫瘍細胞標識化方法。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2011−211996(P2011−211996A)
【公開日】平成23年10月27日(2011.10.27)
【国際特許分類】
【出願番号】特願2010−86071(P2010−86071)
【出願日】平成22年4月2日(2010.4.2)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成21年10月3日、日本癌学会主催、第68回 日本癌学会学術総会において発表及び、平成21年10月14日、http://www.oraloncology.com/article/S1368−8375(09)00908−7を通じて発表
【出願人】(304021831)国立大学法人 千葉大学 (601)
【Fターム(参考)】
【公開日】平成23年10月27日(2011.10.27)
【国際特許分類】
【出願日】平成22年4月2日(2010.4.2)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成21年10月3日、日本癌学会主催、第68回 日本癌学会学術総会において発表及び、平成21年10月14日、http://www.oraloncology.com/article/S1368−8375(09)00908−7を通じて発表
【出願人】(304021831)国立大学法人 千葉大学 (601)
【Fターム(参考)】
[ Back to top ]

