膵臓癌に関連するマイクロRNA発現プロファイル
【課題】膵臓癌を確実かつ正確に診断する方法、あるいは膵臓癌の素因について個体をスクリーニングする方法を提供する。
【解決手段】被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法が提供される。本方法は、被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手順を含む。生体試料におけるmiR遺伝子産物のレベルが対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかが示される。
【解決手段】被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法が提供される。本方法は、被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手順を含む。生体試料におけるmiR遺伝子産物のレベルが対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかが示される。
【発明の詳細な説明】
【背景技術】
【0001】
政府の支援に関する声明
本発明は、アメリカ合衆国のNational Institute of Healthによるグラント番号CA107435によって少なくとも部分的にサポートされる。The Ohio State UniversityのTissue Procurement Shared Resourceは、National Cancer InstituteのグラントP30 CA16058によって資金援助される。米国合衆国政府は、本発明において一定の権利を有する。
【0002】
関連出願への相互参照
本願は、2006年3月2日に出願された米国仮特許出願第60/778,271号に基づく。米国仮特許出願第60/778,271号の利益は、本明細書によって特許請求され、そしてその開示は本明細書中に参考として援用される。
【0003】
背景
膵臓癌は、米国の癌関連の死亡で4番目の主要原因である。この5年間の年間死亡率は約3万人であり、毎年診断される新症例の数とほとんど同じである。膵臓癌の予後はすべての癌の中で最悪であり、死亡率/発現率の比は0.99である。米国の膵臓癌の発現率は、10万人当たり約9人である。これらの思わしくない数字は、発現率と死亡率とが増加傾向にあることを反映しており、検出法および診断法の進歩が見られないことや、治療計画における進展が不十分であることに起因する。
【0004】
マイクロRNA(miRNA)は、広範囲にわたる種のゲノムにおいて同定されている短い非コードRNAである。miRNAは、1993年に最初にシノラディス・エレガンスにおいて発見され、その後すべての多細胞生物で発見された。miRNAは、遺伝子発現の負の調節因子であり、タンパク質コードmRNAの3’非翻訳領域内の配列との塩基対の不完全な相互作用によって主に機能すると考えられる。2006年までに326種のmiRNAがヒトにおいて発見された。これらのmiRNAのそれぞれの役割は知られていないが、特定のmiRNAは、脂肪細胞の分化や、卵母細胞の成熟、多能性細胞状態の維持、インスリン分泌の調節などの多様な細胞過程の調節に関わっていた。
【0005】
miRNAの発現の変化と癌との間の関係を示唆する直接的エビデンスおよび間接的エビデンスが増加している。これらには、慢性リンパ性白血病におけるmiR‐15aおよびmiR‐16‐1、結腸直腸癌におけるmiR‐143およびmiR‐145、肺癌におけるlet‐7、びまん性大細胞型B細胞リンパ腫におけるmiR‐155が含まれる。発現プロファイリングによって、乳癌や、膠芽細胞腫、甲状腺乳頭癌など、いくつかのmiRNAの特異的な発現を伴う他の癌が同定されてきた。5種のmiRNAをコードするポリシストロンがヒトB細胞リンパ腫で増幅され、c‐mycとのポリシストロンの強制的発現は腫瘍形成性であったが、このことはこのmiRNAの群が腫瘍遺伝子として機能することを示唆する。
【0006】
膵臓癌を確実かつ正確に診断する方法、あるいは膵臓癌の素因について個体をスクリーニングする方法が必要とされる。また、膵臓癌の治療方法も非常に望まれる。
【発明の概要】
【課題を解決するための手段】
【0007】
要旨
本発明は、膵臓腺癌において発現が変化するmiRNAの同定に一部基づく。
【0008】
従って、本発明は、被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法を包含する。本方法は、被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手順を含む。生体試料におけるmiR遺伝子産物のレベルが対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかが示される。
【0009】
特定の実施形態において、発現が変化したmiR遺伝子産物は、以下の群から選択される:MIR‐034b、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐130a‐P、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐192、MIR‐200a‐P、MIR‐204、MIR‐210、MIR‐299‐P、MIR‐302d、MIR‐337、MIR‐371、MIR‐378、MIR‐383、MIR‐422b、MIR‐423、MIR‐375、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MlR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせ。
【0010】
一実施形態において、生体試料における遺伝子産物のレベルは、対照試料におけるその対応するmiR遺伝子産物のレベルよりも低い。このような過小発現の遺伝子産物には、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR188b‐P、MIR‐204、MIR‐299‐P、MIR‐337、MIR‐371、MIR‐383、MIR‐375およびそれらの組み合わせが含まれる。
【0011】
別の実施形態において、生体試料におけるmiR遺伝子産物のレベルは、対照試料におけるその対応するmiR遺伝子産物のレベルよりも高い。このような過剰発現のmiR遺伝子産物には、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせが含まれる。
【0012】
本発明はまた、被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性
があるのかを診断する別の方法も提供する。本方法は、(a)被験体の膵臓由来の試験試料を提供する手順であって、前記試験試料が複数のmiR遺伝子産物を含む、手順;(b)試験試料におけるmiR遺伝子産物の発現レベルを検定して、試験試料のmiR発現プロファイルを得る手順;(c)試験試料のmiR発現プロファイルを、対照試料から作成された対応するmiR発現プロファイルと比較する手順を含む。試験試料のmiR発現プロファイルと対照試料のmiR発現プロファイルとの差によって、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかが示される。
【0013】
一実施形態において、複数のmiR遺伝子産物は、細胞内のmiR遺伝子の補体全長の実質部分に相当する。他の実施形態において、複数のmiR遺伝子産物は、細胞内のmiR補体全長な補体の約95%、90%、80%、70%または60%に相当する。
【0014】
別の実施形態において、複数のmiR遺伝子産物は、MIR‐139、MIR096‐P、MIR‐375、let‐7b、let‐7d、let‐7f‐1、let‐7i、MIR‐155、MIR‐181a、MIR‐212、MIR‐301、MIR‐007‐1およびMIR‐021からなる群から選択される1つ以上のmiR遺伝子産物を含む。
【0015】
前記miR遺伝子産物のレベルは、当該技術分野で周知の種々の技法を使用して測定することができる。これらの技法には、増幅に基づく検定、ハイブリダイゼーションに基づく検定およびマイクロアレイ分析が含まれる。他の実施形態において、miR遺伝子産物のレベルは、試料中の対応するmiR遺伝子コピーを測定することによって判定できる。
【0016】
被験体から得られる生体試料は、膵組織、膵腫瘍または膵臓細胞を含んでよい。また、生体試料は膵液を含むこともできる。
【0017】
本発明はまた、膵臓癌に羅患しているか、もしくは膵臓癌を発症する危険性がある被験体における膵臓癌を診断するためのキットも企図する。このようなキットは、(a)被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手段、および(b)生体試料におけるmiR遺伝子産物のレベルを、対照試料における対応するmiR遺伝子産物のレベルと比較する手段を含む。生体試料におけるmiR遺伝子産物のレベルと、対照試料における対応するmiR遺伝子産物のレベルとの間で検出された差は、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかであることを示す。
【0018】
本発明はまた、膵臓癌を発症する危険性がある被験体をスクリーニングする方法も提供する。このような方法は、被験体の膵臓から得た生体試料中の膵臓癌に関連した、少なくとも1つのmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルを評価する手順であって、生体試料におけるmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルが、対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、被験体に膵臓癌を発症する危険性があることが示される、手順を含む。
【0019】
一実施形態において、生体試料は、正常であるか、もしくは前癌性の疑いがあるかのいずれかの膵組織を含む。
【0020】
本発明はまた、対照細胞よりも多くのmiR遺伝子産物を含む膵臓癌細胞を有する被験体における膵臓癌の進行を抑制する方法も提供する。このような方法は、膵臓癌細胞内のmiR遺伝子産物の量を減少させることができる有効量の阻害剤分子を被験体に投与する手順を含む。
【0021】
いくつかの実施形態において、阻害剤分子は、アップレギュレートされたmiR遺伝子産物の転写後のサイレンシングを引き起こすか、もしくはアップレギュレートされたmiR遺伝子産物の成熟を阻害する。いくつかの実施形態において、阻害剤分子は、前記アップレギュレートされたmiR遺伝子産物のアンチセンスオリゴヌクレオチド、リボザイム、低分子干渉RNA(siRNA)、またはアップレギュレートされたmiR遺伝子産物についてコードする遺伝子とともに3重らせんを形成することができる分子である。いくつかの実施形態において、阻害剤化合物は、miR遺伝子産物プロモーターのメチル化を引き起こし、それによってmiR遺伝子の発現が低下する。
【0022】
一実施形態において、阻害剤分子は、送達剤とともに裸のRNAとして投与される。別の実施形態において、阻害剤分子は、阻害剤分子をコードする核酸として投与される。
【0023】
本発明はまた、対照細胞よりも少ないmiR遺伝子産物を含む膵臓癌細胞を有する被験体における膵臓癌の進行を抑制する方法も提供する。このような方法は、miR遺伝子産物に対応する有効量の単離されたmiR遺伝子産物を被験体に投与する手順を含む。
【0024】
一実施形態において、単離されたmiR遺伝子産物は、機能性成熟型miRである。他の実施形態において、単離されたmiR遺伝子産物は、ヘアピンのループ部を含むmiR前駆体ヘアピン配列を含むオリゴヌクレオチド、またはヘアピンを有さない2本鎖のmiR前駆体を含むオリゴヌクレオチドである。
【0025】
一実施形態において、単離された遺伝子産物は、送達剤とともに裸のRNAとして投与される。別の実施形態において、単離された遺伝子産物は、単離されたmiR遺伝子産物をコードする核酸として投与される。
【0026】
別の方法においては、癌の進行は、ダウンレギュレートされたmiR遺伝子産物のプロモーター領域の低メチル化を引き起こす化合物の投与によって抑制される。
【0027】
本発明はまた、少なくとも1つの過小発現のmiR遺伝子産物を示す被験体における膵臓癌を治療するための薬学的組成物も提供する。いくつかの実施形態において、薬学的組成物は、過小発現のmiR遺伝子産物に対応する単離されたmiR遺伝子産物と薬学的に許容される担体とを含む。他の実施形態において、薬学的組成物は、過小発現のmiR遺伝子産物をコードする少なくとも1つの核酸と薬学的に許容される担体とを含む。
【0028】
本発明はまた、少なくとも1つの過剰発現のmiR遺伝子産物を示す被験体における膵臓癌を治療するための薬学的組成物も提供する。薬学的化合物は、過剰発現のmiR遺伝子産物に特異的な少なくとも1つのmiR遺伝子阻害剤化合物と薬学的に許容される担体とを含む。
【0029】
本発明はまた、被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する方法も提供する。このような方法は、(a)対照細胞に比べてアップレギュレートされたmiR遺伝子産物を有する癌細胞を含む被験体の膵臓から第1の試験試料を得る手順;(b)被験体に治療レジメンを施す手順;(d)ある期間後に被験体の膵臓から第2の試験試料を得る手順;および(e)第1および第2の試験試料におけるアップレギュレートされたmiR遺伝子産物のレベルを比較する手順を含む。第2の試験試料におけるアップレギュレートされたmiR遺伝子産物レベルが第1の試験試料よりも低いことによって、その治療レジメンが被験体における膵臓癌の進行抑制に効果的であることが示される。
【0030】
本発明で検討される別の方法においては、被験体における膵臓癌の進行の抑制に対する治療レジメンの有効性は、(a)対照細胞に比べてアップレギュレートされたmiR遺伝
子産物を有する癌細胞を含む被験体の膵臓から第1の試験試料を得る手順;(b)被験体に治療レジメンを施す手順;(d)ある期間後に被験体の膵臓から第2の試験試料を得る手順;および(e)第1および第2の試験試料におけるアップレギュレートされたmiR遺伝子産物のレベルを比較する手順によって評価される。第2の試験試料におけるアップレギュレートされたmiR遺伝子産物レベルが第1の試験試料よりも低いことによって、その治療レジメンが被験体における膵臓癌の進行抑制に効果的であることが示される。
【0031】
本発明はまた、膵臓癌用抗癌剤を同定する方法も提供する。本方法は、(a)膵臓癌細胞を含む生体試料において過剰発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;(b)生体試料に試験剤を接触させる手順;(c)生体試料のmiR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順であって、miR遺伝子産物の試験後の発現レベルが低下することによって、試験剤が膵臓癌の抗癌性を有することが示される、手順を含む。
【0032】
本発明はまた、膵臓癌用抗癌剤を同定する方法も提供する。本方法は、(a)膵臓癌細胞を含む生体試料において過小発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;(b)生体試料に試験剤を接触させる手順;(c)手順(b)の後に生体試料のmiR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順であって、miR遺伝子産物の試験後の発現レベルが上昇することによって、試験剤が膵臓癌の抗癌性を有することが示される、手順を含む。
本発明はまた、以下の項目を提供する。
(項目1)
被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法であって、前記被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手順であって、前記生体試料における前記miR遺伝子産物のレベルが対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、前記被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかであることが示される、手順を含む、方法。
(項目2)
前記miR遺伝子産物が、MIR‐034b、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐130a‐P、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐192、MIR‐200a‐P、MIR‐204、MIR‐210、MIR‐299‐P、MIR‐302d、MIR‐337、MIR‐371、MIR‐378、MIR‐383、MIR‐422b、MIR‐423、MIR‐375、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MlR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせからなる群から選択される、項目1に記載の方法。
(項目3)
前記miR遺伝子産物が、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐098、MIR‐099a、MIR‐100、MIR‐125b‐1、MIR‐126、MIR‐132、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐218‐1,2,、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐331‐P、MIR‐345、MIR‐376およびそれらの組み合わせからなる群から選択される、項目2に記載の方法。
(項目4)
前記生体試料におけるmiR遺伝子産物のレベルが、前記対照試料におけるその対応するmiR遺伝子産物のレベルよりも低い、項目1に記載の方法。
(項目5)
前記miR遺伝子産物が、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐204、MIR‐299‐P、MIR‐337、MIR‐371、MIR‐383、MIR‐375およびそれらの組み合わせからなる群から選択される、項目4に記載の方法。
(項目6)
前記miR遺伝子産物がMIR‐139である、項目5に記載の方法。
(項目7)
前記miR遺伝子産物がMIR‐096‐Pである、項目5に記載の方法。
(項目8)
前記miR遺伝子産物がMIR‐375である、項目5に記載の方法。
(項目9)
前記生体試料における前記miR遺伝子産物のレベルが、前記対照試料におけるその対応するmiR遺伝子産物のレベルよりも高い、項目1に記載の方法。
(項目10)
前記miR遺伝子産物が、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目11)
前記miR遺伝子産物が、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐030d、MIR‐098、MIR‐099a、MIR‐100、MIR‐125b‐1、MIR‐126、MIR‐132、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐331‐P、MIR‐345、M
IR‐376およびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目12)
前記miR遺伝子産物が、let‐7b;let‐7d;let‐7f;let‐7i、MIR‐015a;MIR‐015b;MIR‐016‐1;MIR‐021;MlR‐023a、MIR‐024、MIR‐100;MIR‐125b;MIR‐132、MIR‐155、MIR‐181a、MIR‐181c;MIR‐212;MIR‐221;MIR‐301;MIR‐376aおよびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目13)
前記miR遺伝子産物が、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐015b、MIR‐019b‐1‐P、MIR‐098、MIR‐128a、MIR‐136、MIR‐152、MIR‐155、MIR‐181a、MIR‐196a‐2、MIR‐212、MIR‐215、MIR‐218‐1、MIR‐218‐2、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐424およびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目14)
前記miR遺伝子産物が、let‐7b、let‐7d、let‐7f‐1、let‐7i、MIR‐155、MIR‐181a、MIR‐212、MIR‐301およびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目15)
前記miR遺伝子産物がMIR‐155である、項目9に記載の方法。
(項目16)
前記miR遺伝子産物がMIR‐007‐1である、項目9に記載の方法。
(項目17)
前記miR遺伝子産物がMIR‐021である、項目9に記載の方法。
(項目18)
被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法であって、
(a)前記被験体の膵臓由来の試験試料を提供する手順であって、前記試験試料が複数のmiR遺伝子産物を含む、手順;
(b)前記試験試料における前記miR遺伝子産物の発現レベルを検定して、前記試験試料のmiR発現プロファイルを得る手順;
(c)前記試験試料の前記miR発現プロファイルを、対照試料から作成された対応するmiR発現プロファイルと比較する手順であって、前記試験試料の前記miR発現プロファイルと前記対照試料の前記miR発現プロファイルとの差によって、前記被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかが示される、手順
を含む、方法。
(項目19)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の実質部分に相当する、項目18に記載の方法。
(項目20)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約95%に相当する、項目18に記載の方法。
(項目21)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約90%に相当する、項目18に記載の方法。
(項目22)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約80%に相当する、項目18に記載の方法。
(項目23)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約70%に相当する、項目18に記載の方法。
(項目24)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約60%に相当する、項目18に記載の方法。
(項目25)
前記複数のmiR遺伝子産物が、MIR‐139、MIR096‐P、MIR‐375、let‐7b、let‐7d、let‐7f‐1、let‐7i、MIR‐155、MIR‐181a、MIR‐212、MIR‐301、MIR‐007‐1、MIR‐021およびそれらの組み合わせからなる群から選択される1つ以上のmiR遺伝子産物を含む、項目18に記載の方法。
(項目26)
前記対照試料が正常膵組織から得られる、項目1〜25に記載の方法。
(項目27)
前記試験試料が、癌または前癌性であることが疑われる膵臓の領域から得られる、項目1〜25に記載の方法。
(項目28)
前記miR遺伝子産物がmiRNA前駆体である、項目1〜25に記載の方法。
(項目29)
前記miR遺伝子産物が成熟型miRNAである、項目1〜25に記載の方法。
(項目30)
前記miR遺伝子産物のレベルが、増幅に基づく検定を使用して測定される、項目1〜29に記載の方法。
(項目31)
前記増幅に基づく検定が、ポリメラーゼ連鎖反応(PCR)、逆転写酵素ポリメラーゼ連鎖反応(RT‐PCR)、定量的RT‐PCR、リアルタイム定量的RT‐PCRおよびin situ PCRからなる群から選択される、項目30に記載の方法。
(項目32)
前記miR遺伝子産物のレベルが、ハイブリダイゼーションに基づく検定を使用して測定される、項目1〜29に記載の方法。
(項目33)
前記ハイブリダイゼーションに基づく検定が、ノーザンブロット解析、in situハイブリダイゼーション、溶液ハイブリダイゼーション、リボヌクレアーゼ防御検定、RNAマイクロアレイ分析ならびにDNAまたはcDNAマイクロアレイ分析からなる群から選択される、項目32に記載の方法。
(項目34)
前記miR遺伝子産物のレベルが、前記試料における前記対応するmiR遺伝子コピーを測定することによって判定される、項目1〜29に記載の方法。
(項目35)
前記生体試料が膵組織、膵腫瘍または膵臓細胞を含む、項目1〜34に記載の方法。
(項目36)
前記生体試料が膵液の試料を含む、項目1〜34に記載の方法。
(項目37)
膵臓癌に羅患しているか、もしくは膵臓癌を発症する危険性がある被験体における膵臓癌を診断するためのキットであって、
(a)前記被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手段、および
(b)前記生体試料における前記miR遺伝子産物のレベルを、対照試料における対応するmiR遺伝子産物のレベルと比較する手段
を含み、
前記生体試料における前記miR遺伝子産物のレベルと、前記対照試料における前記対応するmiR遺伝子産物のレベルとの間で検出された差によって、前記被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかであることが示される、
キット。
(項目38)
膵臓癌を発症する危険性がある被験体をスクリーニングする方法であって、前記被験体の膵臓から得た生体試料中の膵臓癌に関連した、少なくとも1つのmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルを評価する手順であって、前記生体試料におけるmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルが、対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、前記被験体に膵臓癌を発症する危険性があることが示される、手順を含む、方法。
(項目39)
前記生体試料が、正常であるか、もしくは前癌性の疑いがある膵組織を含む、項目38に記載の方法。
(項目40)
対照細胞よりも多くのmiR遺伝子産物を含む膵臓癌細胞を有する被験体における膵臓癌の進行を抑制する方法であって、前記膵臓癌細胞内の前記miR遺伝子産物の量を減少させることができる有効量の阻害剤分子を前記被験体に投与する手順を含む、方法。
(項目41)
前記miR遺伝子産物が、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目42)
前記miR遺伝子産物が、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐030d、MIR‐098、MIR‐099a、MIR‐100、MIR‐125b‐1、MIR‐126、MIR‐132、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐331‐P、MIR‐345、MIR‐376およびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目43)
前記miR遺伝子産物が、let‐7b;let‐7d;let‐7f;let‐7i、MIR‐015a;MIR‐015b;MIR‐016‐1;MIR‐021;MlR
‐023a、MIR‐024、MIR‐100;MIR‐125b;MIR‐132、MIR‐155、MIR‐181a、MIR‐181c;MIR‐212;MIR‐221;MIR‐301;MIR‐376aおよびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目44)
miR遺伝子産物が、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐015b、MIR‐019b‐1‐P、MIR‐098、MIR‐128a、MIR‐136、MIR‐152、MIR‐155、MIR‐181a、MIR‐196a‐2、MIR‐212、MIR‐215、MIR‐218‐1、MIR‐218‐2、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐424およびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目45)
前記miR遺伝子産物が、let‐7b、let‐7d、let‐7f‐1、let‐7i、MIR‐155、MIR‐181a、MIR‐212、MIR‐301およびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目46)
前記miR遺伝子産物がMIR‐155である、項目40に記載の方法。
(項目47)
前記miR遺伝子産物がMIR‐007‐1である、項目40に記載の方法。
(項目48)
前記miR遺伝子産物がMIR‐021である、項目40に記載の方法。
(項目49)
前記miR遺伝子産物が成熟型miRである、項目40〜48に記載の方法。
(項目50)
前記阻害剤分子が前記miR遺伝子産物の転写後のサイレンシングを引き起こす、項目40〜48に記載の方法。
(項目51)
前記阻害剤分子が前記miR遺伝子産物の成熟を阻害する、項目40〜48に記載の方法。
(項目52)
前記阻害剤分子が前記miR遺伝子産物のアンチセンスオリゴヌクレオチドである、項目40〜48に記載の方法。
(項目53)
前記阻害剤分子が低分子干渉RNA(siRNA)である、項目40〜48に記載の方法。
(項目54)
前記阻害剤分子が、前記miR遺伝子産物についてコードする遺伝子とともに3重らせんを形成することができる分子である、項目40〜48に記載の方法。
(項目55)
前記阻害剤分子がリボザイムである、項目40〜48に記載の方法。
(項目56)
前記阻害剤分子が送達剤とともに裸のRNAとして投与される、項目40〜54に記載の方法。
(項目57)
前記阻害剤分子が、前記阻害剤分子をコードする核酸として投与される、項目40〜54に記載の方法。
(項目58)
対照細胞よりも少ないmiR遺伝子産物を含む膵臓癌細胞を有する被験体における膵臓癌の進行を抑制する方法であって、前記miR遺伝子産物に対応する有効量の単離された
miR遺伝子産物を前記被験体に投与する手順を含む、方法。
(項目59)
前記miR遺伝子産物が、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐204、MIR‐299‐P、MIR‐337、MIR‐371、MIR‐383、MIR‐375およびそれらの組み合わせからなる群から選択される、項目58に記載の方法。
(項目60)
前記miR遺伝子産物がMIR‐139である、項目58に記載の方法。
(項目61)
前記miR遺伝子産物がMIR‐096‐Pである、項目58に記載の方法。
(項目62)
前記miR遺伝子産物がMIR‐375である、項目58に記載の方法。
(項目63)
前記単離されたmiR遺伝子産物が前記機能性成熟型miRである、項目58〜62に記載の方法。
(項目64)
前記単離されたmiR遺伝子産物が、ヘアピンのループ部を含むmiR前駆体ヘアピン配列を含むオリゴヌクレオチドである、項目58〜62に記載の方法。
(項目65)
前記単離されたmiR遺伝子産物が、前記ヘアピンを有さない2本鎖のmiR前駆体を含むオリゴヌクレオチドである、項目58〜62に記載の方法。
(項目66)
前記単離された遺伝子産物が送達剤とともに裸のRNAとして投与される、項目58〜62に記載の方法。
(項目67)
前記単離された遺伝子産物が、前記単離されたmiR遺伝子産物をコードする核酸として投与される、項目58〜62に記載の方法。
(項目68)
前記核酸が組換えプラスミドまたは組換えウイルスベクターである、項目67に記載の方法。
(項目69)
項目40〜57に記載の阻害剤分子と薬学的に許容される担体とを含む、被験体における膵臓癌を治療するための薬学的組成物。
(項目70)
項目58〜66に記載の単離されたmiR遺伝子産物と薬学的に許容される担体とを含む、被験体における膵臓癌を治療するための薬学的組成物。
(項目71)
項目67〜68に記載の単離されたmiR遺伝子産物をコードする核酸と薬学的に許容される担体とを含む、被験体における膵臓癌を治療するための薬学的組成物。
(項目72)
被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する方法であって、
(a)対照細胞に比べてアップレギュレートされたmiR遺伝子産物を有する癌細胞を含む前記被験体の膵臓から第1の試験試料を得る手順;
(b)前記被験体に前記治療レジメンを施す手順;
(d)ある期間後に前記被験体の膵臓から第2の試験試料を得る手順;ならびに
(e)前記第1および前記第2の試験試料における前記アップレギュレートされたmiR遺伝子産物のレベルを比較する手順であって、前記第2の試験試料における前記アップレギュレートされたmiR遺伝子産物レベルが前記第1の試験試料よりも低いことによって、前記治療レジメンが前記被験体における膵臓癌の進行抑制に効果的であることが示さ
れる、手順
を含む、方法。
(項目73)
被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する方法であって、
(a)対照細胞に比べてダウンレギュレートされたmiR遺伝子産物を有する癌細胞を含む前記被験体の膵臓から第1の試験試料を得る手順;
(b)前記被験体に前記治療レジメンを施す手順;
(d)ある期間後に前記被験体の膵臓から第2の試験試料を得る手順;および
(e)前記第1および前記第2の試験試料における前記ダウンレギュレートされたmiR遺伝子産物のレベルを比較する手順であって、前記第2の試験試料における前記ダウンレギュレートされたmiR遺伝子産物レベルが前記第1の試験試料よりも高いことによって、前記治療レジメンが前記被験体における膵臓癌の進行抑制に効果的であることが示される、手順
を含む、方法。
(項目74)
膵臓癌用抗癌剤を同定する方法であって、
(a)膵臓癌細胞を含む生体試料において過剰発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;
(b)前記生体試料に試験剤を接触させる手順;
(c)手順(b)の後に前記生体試料における前記miR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および
(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順であって、前記miR遺伝子産物の前記試験後の発現レベルが低下することによって、前記試験剤が膵臓癌の抗癌性を有することが示される、手順
を含む、方法。
(項目75)
膵臓癌用抗癌剤を同定する方法であって、
(a)膵臓癌細胞を含む生体試料において過小発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;
(b)前記生体試料に試験剤を接触させる手順;
(c)手順(b)の後に前記生体試料における前記miR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および
(d)前記miR遺伝子産物の前記試験後の発現レベルを前記試験前の発現レベルと比較する手順であって、前記miR遺伝子産物の前記試験後の発現レベルが上昇することによって、前記試験剤が膵臓癌の抗癌性を有することが示される、手順
を含む、方法。
【図面の簡単な説明】
【0033】
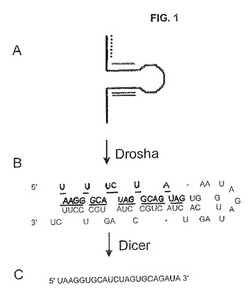
【図1】miRNAプロセッシングおよびプライマー設計。ヒトmiR‐18などのmiRNAは、核酵素のDroshaによってプロセッシングされる(A)大きな一次前駆体(pri‐miRNA)として転写され、(B)推定で62ntの前駆体miRNA(pre‐miRNA)を作製する。pri‐miRNAとpre‐miRNAの両方ともヘアピン構造を含む。pre‐miRNAの下線部分は、リボヌクレアーゼのDicerによってpre‐miRNAからプロセッシングされる(C)22ntの成熟型miRNAの配列を表す。単線は前方プライマーを示し、2重線は後方プライマーを示し;破線はpri‐miRNAだけを増幅するために後方(黒)プライマーとともに使用されるセンスプライマーを示す。
【図2−1】ヒトmiR遺伝子産物配列の表。前記配列はmiRNA前駆体を表し、前駆体配列内の下線が引かれた配列は成熟型miRNAを表す。すべての配列は5’側から3’側の方向に示す。
【図2−2】ヒトmiR遺伝子産物配列の表。
【図2−3】ヒトmiR遺伝子産物配列の表。
【図2−4】ヒトmiR遺伝子産物配列の表。
【図2−5】ヒトmiR遺伝子産物配列の表。
【図2−6】ヒトmiR遺伝子産物配列の表。
【図2−7】ヒトmiR遺伝子産物配列の表。
【図2−8】ヒトmiR遺伝子産物配列の表。
【図2−9】ヒトmiR遺伝子産物配列の表。
【図2−10】ヒトmiR遺伝子産物配列の表。
【図2−11】ヒトmiR遺伝子産物配列の表。
【図2−12】ヒトmiR遺伝子産物配列の表。
【図2−13】ヒトmiR遺伝子産物配列の表。
【図2−14】ヒトmiR遺伝子産物配列の表。
【図3−1】臨床データおよび腫瘍病理。
【図3−2】臨床データおよび腫瘍病理。
【図4−1】ヒトmiRNA前駆体を増幅するために使用されるPCRプライマー。miRNA一次前駆体配列へのp,プライマー。その他すべてのプライマーは、miRNAを一次前駆体と前駆体の両方に存在するヘアピンにハイブリダイズする。
【図4−2】ヒトmiRNA前駆体を増幅するために使用されるPCRプライマー。miRNA一次前駆体配列へのp,プライマー。その他すべてのプライマーは、miRNAを一次前駆体と前駆体の両方に存在するヘアピンにハイブリダイズする。
【図4−3】ヒトmiRNA前駆体を増幅するために使用されるPCRプライマー。miRNA一次前駆体配列へのp,プライマー。その他すべてのプライマーは、miRNAを一次前駆体と前駆体の両方に存在するヘアピンにハイブリダイズする。
【図4−4】ヒトmiRNA前駆体を増幅するために使用されるPCRプライマー。miRNA一次前駆体配列へのp,プライマー。その他すべてのプライマーは、miRNAを一次前駆体と前駆体の両方に存在するヘアピンにハイブリダイズする。
【図5】膵組織内の18S rRNAの発現。18S rRNA内部コントロールの発現は、膵腫瘍、隣接する良性組織、正常な膵臓、慢性膵炎および膵臓癌の細胞株に認められる。本明細書に記載されるリアルタイムPCRを使用して判定される18S rRNA発現は、2‐CTとして示される。破線は平均値。
【図6】膵臓試料におけるmiRNA前駆体の発現のヒートマップ。A.201のmiRNA前駆体の相対的発現がリアルタイムPCRによって判定され;データは、Δ CTとして示される。管理されない階層的クラスタリングを、すべてのデータセットのサブセットにおいて実施した;データはフィルタリングされない。1に等しい発現値の中央値は黒色で;発現増加は赤色で;発現低下は緑色で;検知されない発現は灰色で示される。B.47の試料におけるmiRNA前駆体の発現パターンの階層的クラスター分析の結果を表す樹状図。試料は、原発性膵腫瘍(黄色、N=28)、正常膵組織(青、N=6)、慢性膵炎(オレンジ、N=4)および膵臓癌細胞株(トルコ玉色、N=9)を含む。
【図7】膵臓試料におけるmiRNA前駆体の発現。A.各miRNA前駆体の相対的発現がリアルタイムPCRによって判定され;データは、Δ CTとして示される。ANOVA多群比較試験によって判定される群(腫瘍、慢性膵炎、細胞株および正常組織)の中で異なって発現する(P<0.001)108の遺伝子のサブセットにおいて、管理されない階層的クラスタリングを実施した。1に等しい発現値の中央値は黒色で;発現増加は赤色で;発現低下は緑色で;検知されない発現は灰色で示される。B.47の試料におけるmiRNA前駆体の発現パターンの階層的クラスター分析の結果を表す樹状図。試料は、原発性膵腫瘍(N=28)、隣接する良性組織(N=15)、正常膵組織(N=6)、慢性膵炎(N=4)および膵臓癌細胞株(N=9)を含む。
【図8】立体的な発現地形図が該当なし7に示すフィルタリングされたmiRNA前駆体の発現データから作成された。各山は、個々の試料(腫瘍、隣接する良性、慢性的膵炎、正常な膵臓または膵臓癌細胞株)を表す。個々の山は、互いの類似性または差に基づいて小さな群に分かれる。着色された点は試料のタイプを表し、腫瘍は黄色;隣接する良性組織は青色;正常膵組織は黒色;慢性膵炎はオレンジ色;および膵臓癌細胞株はトルコ玉色である。試料の対をつなぐ線は、平均相関が閾値(>0.8)を超えるmiRNAの発現の非常に類似したパターンを有するそれらの試料を示す。
【図9】トレーニングデータおよび試験データについて推定された確率。6個の正常膵臓試料と膵腫瘍であることが知られている試料の内の18個とを含むすべてのトレーニングデータが正確に分類される(A)。15個の隣接する良性試料の内の11個と膵腫瘍であることが知られている10個の試料が試験群(B)に正確に分類される。試料は、真実のクラス(A)と予測されたクラス(B)とで分けられる。
【図10−1】上位69番目までは膵臓腺癌におけるmiRNA前駆体を異常に発現した。
【図10−2】上位69番目までは膵臓腺癌におけるmiRNA前駆体を異常に発現した。
【図10−3】上位69番目までは膵臓腺癌におけるmiRNA前駆体を異常に発現した。
【図11】マイクロRNAの発現についての膵臓癌の組織学的解析および分子解析。パネルA(400×)は、膵臓腺癌のヘマトキシリン‐エオジン分析を示す。正常な膵臓腺(小さな矢印)には、癌(大きな矢印)の不十分に形成された腺が侵入している。対応するcDNAのin situ増幅後のmiR‐221の連続切片の分析によって、腫瘍細胞の内の多くが標的配列を含むことが示され;細胞質の局在化が示される(矢印、パネルB‐400×およびそれ以上の倍率、パネルC‐1000×;シグナルは、ファストレッドで対比染色された陰性細胞を有するNBT/BCIPにより青色)。シグナルは、プライマーの除外またはHPV特異的プライマー(パネルD、400×)による置き換えのいずれかによって消失した。隣接する連続切片もまた、cDNA(E、F)のin situ増幅後に腫瘍細胞の内の多くがmiR‐376aを発現することを示した。パネルE(400×)は、陽性の腫瘍細胞(大きな矢印)と、線維形成の領域における陰性の間質細胞(小さな矢印)とを示すが、一方でパネルF(400×)は、陰性の良性の膵腺房(小さな矢印)に隣接する陽性の腫瘍細胞(大きな矢印)を示す。
【図12】ノーザンブロット法によるmiRNA発現。miR‐100、miR‐375、miR‐155およびU6RNAの発現は、膵臓癌(T)、隣接する良性組織(B)または正常膵臓(N)の組織標本において判定された。ブロットはストリップされ、次いで再プローブされた。
【図13】成熟型および前駆体miRNA発現のバリデーション。
【図14】前駆体および成熟型miRNAレベルのバリデーション。8つのmiRNAの発現が、6つの正常膵臓標本、10の隣接する良性組織および16の膵臓腺癌において確認された。miRNA前駆体の相対的発現(開いた棒)がmiRNA前駆体に対するリアルタイムPCR検定を使用して判定され、一方で成熟型miRNAの相対的発現(閉じた棒)が成熟型miRNAに対するリアルタイムPCR検定を使用して判定された。miRNA発現における平均差は、膵臓(黒色)と腫瘍(赤色)の間で有意(P<0.01(スチューデントのt検定))であった。A、let7i;B、miR‐221;C、miR‐100;D、miR‐301;E、miR‐21;F、miR‐181a,c(前駆体)およびmiR‐181a(成熟型);G、miR‐125b‐1(前駆体)およびmiR‐125b(成熟型);H、miR‐212。
【図15】膵臓試料における成熟型miRNA発現のヒートマップ。A.9つの膵臓癌の腫瘍と膵疾患のない6人のドナーからの膵臓とのリアルタイムPCRを使用して測定された184の成熟型miRNAの相対的発現。データはΔCTとして示される。管理されない階層的クラスタリングを、すべてのデータセットのサブセットにおいて実施した;データはフィルタリングされない。1に等しい発現値の中央値は黒色で;発現増加は赤色で;発現低下は緑色で;検知されない発現は灰色で示される。B.15の試料におけるmiRNA前駆体の発現パターンの階層的クラスター分析の結果を表す樹状図。
【図16】膵臓腺癌における異常発現した成熟型miRNA。
【図17】miR‐21の発現増加が腫瘍に局在化されることを示す、正常膵臓の部分(A)および膵臓癌(B)に適用したin situ RT‐PCR検定。成熟型miR‐21は、正常膵臓管よりも顕微解剖された腫瘍組織において実質的に増加した(C)。成熟型miR‐21の発現は、腫瘍において増加した(D)。また、成熟型miR‐21発現は、正常膵臓細胞株よりも、7つの膵臓癌細胞株すべてにおいて増加した(E)。
【発明を実施するための形態】
【0034】
詳細な説明
本発明は、膵臓腺癌(以下、「膵臓癌」)の被験体から得られた生体試料における発現が特定の対照試料に比べて変化した特定のマイクロRNA遺伝子産物の同定に一部基づく。本発明は、被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法を包含する。本発明はまた、膵臓癌を発症する危険性があると考えられる被験体をスクリーニングする方法、膵臓癌の進行を抑制することによって膵臓癌を治療する方法、ならびにこのような治療に使用することができる薬学的化合物も提供する。また、膵臓癌を抑制する治療レジメンの有効性を判定する方法、および膵臓癌用抗癌剤を同定する方法も提供される。本発明はまた、上述の方法の実施に適切な各種キットも包含する。
【0035】
本発明を、より詳細な例を参照して説明する。これらの例は、当業者が本発明を作製および使用することができる方法を例示するものであって、特許請求の範囲に列挙されないいかなる限界も課すことなく、本発明の使用可能性および最良の形態を提供するために本明細書に記載するものである。
【0036】
本明細書で言及されるすべての刊行物、特許出願、特許、インターネットウェブページおよび他の参考文献は、全体が参考として本明細書で明示的に援用される。援用される参考文献の用語の定義が本教示内容で定められる定義と異なると思われる場合は、本教示内容で定められる定義が優先される。
【0037】
特に明記しない限り、本明細書および特許請求の範囲で使用される成分、反応条件などの量を表すすべての数値は、すべての例で「約」という用語によって修飾されると理解されるものとする。従って、そうでないことが示されない限り、以下の明細書および添付の特許請求の範囲に記載される数値パラメータは、本発明によって得られることが求められる所望の性質によって異なる場合がある近似値である。各数値パラメータは、少なくとも、そして特許請求の範囲に均等論の適用を限定しようとするものとしてではなく、有効桁数および通常の丸め方法を考慮して解釈されなければならない。
【0038】
本発明の幅広い適用範囲を示す数値範囲およびパラメータは、近似値であるが、具体例に記載される数値は可能な限り正確に報告している。しかし、いずれの数値も、それぞれの試験測定値に認められる標準偏差から必然的に生じる特定の誤差を本質的に含んでいる。本明細書全体にわたって定められるすべての数値範囲は、このようなより広い数値範囲内に含まれるすべてのより狭い数値範囲を、あたかもこのようなより狭い数値範囲がすべて本明細書で明示的に記載されているかのように包含する。
【0039】
以下の紹介は、本明細書で使用される用語の理解に有用である。以下の理論に拘束されることなく該当なし1を参照すると、マイクロRNA(または「miRNA」)は、単一
のまたはクラスター形成されたmiRNA前駆体に転写されるmiR遺伝子によってコードされると考えられる。
【0040】
本明細書で交換可能に使用される「miR遺伝子産物」、「マイクロRNA」または「miRNA」は、miR遺伝子からのプロセッシングされていないまたはプロセッシングされたRNA転写物を指す。プロセッシングされていないmiR遺伝子転写物はまた、「miRNA前駆体」とも称される。図1に示す通り、これらのmiRNA前駆体は、段階的なプロセッシングによってmiRNAの成熟形に変わる。このプロセッシングは、まず(A)大きな一次前駆体または「pri‐miRNA」を産生し、これが次いで核酵素のDroshaによってプロセッシングされ、(B)推定前駆体または「pre‐miRNA」を産生すると考えられる。pre‐miRNAは、通常50〜90ヌクレオチド(nt)を、具体的には60〜80ntを有する。本明細書で使用される「miRNA前駆体」または「プロセッシングされていない」miRNAという用語は、pri‐miRNAおよびpre‐miRNAの両方を示し該当なし1における分子Aおよび/またはBを指す。活性の19〜25nt成熟型miRNAは、リボヌクレアーゼのDicerによってpre‐miRNAからプロセッシングされる。図1におけるpre‐miRNA配列の下線部分は、「プロセッシングされた」miR遺伝子転写物とも称される成熟型miRNAの配列を表し該当なし1の分子Cとして示される。
【0041】
活性または成熟型のmiRNA分子は、天然のプロセッシング経路を介して(例えば、無傷細胞や細胞溶解液を使用して)または合成プロセッシング経路によって(例えば、単離されたDicerやArgonaut、RNAアーゼIIIなどの単離されたプロセッシング酵素を使用して)miRNA前駆体から得ることができる。但し、活性の19〜25個のヌクレオチドRNA分子はまた、miR前駆体からプロセッシングされることなく、生物学的または化学的な合成によって直接産生できることが理解される。
【0042】
さらに図1を参照すると、pri‐miRNA分子およびpre‐miRNA分子はいずれも特徴的な「ヘアピン配列」を有している。この配列は、前半部分が少なくとも部分的にその後半部分に対して相補的であるオリゴヌクレオチド配列であって、それによりその半分の部分をそれ自体の上に折り畳み、「ヘアピン構造」を形成する。ヘアピン構造は該当なし1に示す通り、通常は、相補配列または部分的相補配列からなる「幹」部分、および幹部分の2つの相補鎖の間に位置する領域である「ループ」部分で構成される。
【0043】
本明細書で使用される「miR遺伝子発現」という用語は、miR遺伝子からmiR遺伝子産物を産生することを指し、成熟型miRNA遺伝子産物にmiR前駆体をプロセッシングすることを包含する。
【0044】
標的miR遺伝子産物のレベルは、被験体から得られる生体試料において測定される。例えば、生体試料は、膵臓癌を有することが疑われる被験体から切除することができる。このような生体試料は、前癌性または癌であることが疑われる膵臓の領域から得られる組織または細胞の生検材料を含んでよい。あるいは、生体試料は、膵臓の刺激後に抽出される膵液を含んでよい。別の例では、血液試料を被験体から採取することができる。膵液試料の使用については、例えば、内容が本明細書で援用される、Fukushima,N.,et al.,(2003),Cancer Biol Ther.2:78‐83;Rosty,C. et al.(2002),Hematol Oncol Clin
North Am.16:37‐52;Matsubayashi,H.,et al.,(2005),Clinical Cancer Research 11:573‐583;およびGrφnburg,M.,et al.,(2004)Journal
of Proteome Research,3(5),1042‐1055に記載の通り、当該技術分野で既知である。対応する対照試料は、被験体の影響を受けていない膵
組織から、すなわち正常被験体または正常被験体群から得ることができる。次いで、対照試料は、被験体の試料において特定のmiR遺伝子から産生されたmiR遺伝子産物のレベルを、対照試料由来の対応するmiR遺伝子産物レベルと比較できるように、被験体由来の試験試料とともにプロセッシングされる。
【0045】
本明細書で使用される「被験体」という用語は、生体試料がmiR遺伝子産物を含むいずれの動物をも包含する。動物は哺乳類であってよく、イヌやネコなどの愛玩動物;ウシや、ウマ、ヒツジなどの家畜;ラットや、マウス、ウサギなどの実験動物;およびサルやヒトなどの霊長類を包含してよい。一実施形態において、哺乳類はヒトまたはマウスである。
【0046】
対照試料における対応するmiR遺伝子産物のレベルに比べた、被験体から得られる試料におけるmiR遺伝子産物のレベルの変化(すなわち上昇または低下)によって、被験体において膵臓癌が存在することが示される。いくつかの実施形態において、試験試料における標的miR遺伝子産物のレベルは、対照試料における対応するmiR遺伝子産物のレベルよりも高い(すなわち、miR遺伝子産物の発現が「アップレギュレート」されるか、またはmiR遺伝子産物が「過剰発現」する)。本明細書で使用される通り、被験体由来の試験試料のmiR遺伝子産物の量が対照試料における同じ遺伝子産物の量よりも多い場合、miR遺伝子産物の発現は「アップレギュレート」される。
【0047】
いくつかの実施形態において、アップレギュレートされたmiR遺伝子産物は、以下の1つ以上を含む:let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424。
【0048】
他の実施形態において、試験試料における標的miR遺伝子産物のレベルは、対照試料における対応するmiR遺伝子産物のレベルよりも低い(すなわち、miR遺伝子産物の発現が「ダウンレギュレート」されるか、またはmiR遺伝子産物が「過小発現」する)。本明細書で使用される通り、被験体由来の試験試料におけるmiR遺伝子産物の量が対照試料における同じ遺伝子産物の量よりも少ない場合、miR遺伝子の発現は「ダウンレギュレート」される。対照試料における相対的なmiR遺伝子の発現は、1つ以上のRNA発現基準に対して判定することができる。これらの基準は、例えば、正常な対照群についてすでに得られたmiR遺伝子発現の平均レベルを含んでよい。
【0049】
いくつかの実施形態において、ダウンレギュレートされたmiR遺伝子産物は、以下の1つ以上を含む:MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐204、MIR‐299‐P、MIR‐337、MIR‐371、MIR‐383、MIR‐375。
【0050】
複数のmiR遺伝子産物が膵臓癌と関連していることから、膵臓癌は、列挙したmiR遺伝子産物のいずれか1つを評価することによって、または測定の際に膵臓癌の症状を示
す列挙したmiR遺伝子産物のいずれかの組み合わせを評価することによって、診断することができると理解される。いくつかの例においては、膵臓腺癌に固有に関連するmiR遺伝子産物が評価される。
【0051】
膵臓癌に関連するmiR遺伝子産物のレベルの変化は、被験体の細胞における形質転換されたまたは腫瘍性の表現型の発現の前または発現の初期段階に検出することができる。そのため、本発明はまた、膵臓癌を発症する危険性がある被験体をスクリーニングする方法であって、被験体の膵臓から得た生体試料において膵臓癌に関連する少なくとも1つのmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルを評価する手順を含む、方法も提供する。従って、生体試料におけるmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルが、対照試料における対応するmiR遺伝子産物のレベルに比べて変化することは、被験体に膵臓癌を発症する危険性があることを示す。このようなスクリーニングのために使用される生体試料は、正常であるかまたは前癌性であることが疑われるかのいずれかの膵組織を含んでよい。膵臓癌に関連する1つ以上のmiR遺伝子産物のレベルが変化した被験体は、さらなるモニタリングおよび試験の候補者である。このようなさらなる試験は、組織試料の組織学的検査または当該技術分野の範囲内に含まれる他の技法を含んでよい。
【0052】
本明細書で使用される「標的ヌクレオチド配列」または「標的ヌクレオチド」という用語は、検出されることが求められるポリヌクレオチド配列を指す。標的ヌクレオチド配列は、DNA(例えばcDNAまたはゲノムDNA)、RNA、ヌクレオチド類似体を使用して生成されたDNAまたはRNAの類似体、ならびにそれらの誘導体、フラグメントおよび同族体を含むものとして意図される。
【0053】
試料におけるmiR遺伝子産物のレベルは、生体試料におけるRNA発現レベルを検出するのに適切ないずれかの技法を使用して測定することができる。生体試料におけるRNA発現レベルを判定するのに適切な技法には、増幅に基づく検定やハイブリダイゼーションに基づく検定が含まれる。
【0054】
増幅に基づく検定では、増幅反応(例えば、ポリメラーゼ連鎖反応またはPCR)における鋳型として、miR遺伝子産物の核酸配列またはmiR遺伝子を使用する。miR遺伝子転写物の相対数はまた、miR遺伝子転写物の逆転写の後、ポリメラーゼ連鎖反応(RT‐PCR)によって逆転写された転写物の増幅によって判定することもできる。miR遺伝子転写物のレベルは、内部標準、例えば同じ試料内に存在する「ハウスキーピング」遺伝子由来のmRNAのレベルと比較して定量化することができる。内部標準として使用するのに適切な「ハウスキーピング」遺伝子には、例えば、18S rRNA、ミオシン、またはグリセルアルデヒド‐3‐リン酸脱水素酵素(G3PDH)が含まれる。定量的増幅では、増幅産物の量が、元の試料における鋳型の量と比例する。TaqManプローブを使用するリアルタイム定量的PCRまたはRT‐PCRの方法は、当該技術分野で周知であり、例えば、Heid et al.1996,Real time quantitative PCR,Genome Res.,10:986‐994;およびGibson et al.,1996,A novel method for real time quantitative RT‐PCR,Genome Res.10:995‐1001に記載されている。癌と相関するすべての既知のmiR遺伝子の転写物の発現レベルを判定することができる定量的リアルタイムRT‐PCR法は、全体が参考として本明細書で援用される、Jiang,J.,et al.(2005),Nucleic Acids Res.33,5394‐5403;Schmittgen T.D.,et al.(2004),Nucleic Acids Res.32,E43;および2005年2月24日出願の米国仮出願第60/656,109号に記載されている。miRNA検出のための増幅に基づく検定の他の例は、当該技術分野で周知であ
り、例えば、全体が参考として本明細書で援用される、米国特許出願第2006/0078924号の説明を参照されたい。
【0055】
ハイブリダイゼーションに基づく検定はまた、試料におけるmiR遺伝子産物のレベルを検出するために使用することもできる。これらの検定には、例えば、ノーザンブロット解析、in situハイブリダイゼーション、溶液ハイブリダイゼーション、およびRNアーゼ保護検定(Ma YJ,et al.(1996)RNase protection assay,Methods,10273‐8)が含まれ、当業者に周知である。
【0056】
本明細書で使用される「ハイブリダイゼーション」という用語は、2重らせん、3重らせんまたは他の高次構造の形成をもたらす核酸同士の相補的塩基対合相互作用を指し、本明細書において「アニーリング」と交換可能に使用される。通常、一次相互反応は、ワトソン/クリックおよびフーグスティーン型水素結合によって塩基特異的(例えばA/TおよびG/C)である。また、塩基スタッキングおよび疎水性相互作用はまた、2重らせんの安定性にも寄与する可能性がある。相補的および実質的に相補的な標的配列に対する検出用プローブおよびプライマーをハイブリダイズさせる条件は、例えば、Nucleic
Acid Hybridization,A Practical Approach,B. Hames and S. Higgins,eds.,IRL Press,Washington,D.C.(1985)などに記載される通り、周知である。一般的に、このようなアニーリングが起こるかどうかは、とりわけ、ポリヌクレオチドおよび相補形の長さ、pH、温度、1価および2価の陽イオンの存在、ハイブリダイズ領域におけるGヌクレオチドとCヌクレオチドの割合、培地の粘度、ならびに変性剤の存在に影響される。このような変数は、ハイブリダイゼーションに必要な時間に影響を及ぼす。従って、好ましいアニーリング条件は特定の用途により異なる。しかし、このような条件は、過度の実験を行うことなく当業者により慣例的に判定することができる。相補性は完全である必要がなく、標的配列と本教示内容の1本鎖核酸との間のハイブリダイゼーションの最小限の妨げとなる塩基対ミスマッチが少数存在する可能性があることが理解されるであろう。しかし、塩基対ミスマッチの数が、最小限のストリンジェントな条件下でもハイブリダイゼーションが行われないほどに多い場合、配列は一般的に相補的な標的配列でない。従って、本明細書における相補性とは、プローブまたはプライマーが、本教示内容の目的を達成するために選択された反応条件下でハイブリダイズする上で、標的配列に対して十分に相補的であることを意味する。
【0057】
生体試料における特定の遺伝子のRNA転写物のレベルを判定するのに適切な技法は、ノーザンブロット法である。例えば、トータル細胞RNAは、核酸抽出緩衝剤の存在下でホモジナイゼーションを行った後、遠心分離することによって細胞から精製することができる。核酸を析出させた後、DNAをDNアーゼによる処理と析出とによって除去する。次いでRNA分子を、標準的技法に従ってアガロースゲル上のゲル電気泳動によって分離し、ニトロセルロースフィルターに移す。次いでRNAを加熱によってフィルター上に固定する。特異的RNAの検出および定量化は、当該のRNAに相補的な適切に標識されたDNAまたはRNAプローブを使用して達成される。例えば、開示内容全体が参考として本明細書で援用される、Molecular Cloning:A Laboratory Manual,J.Sambrook et al.,eds.,2nd edition,Cold Spring Harbor Laboratory Press,1989,Chapter 7を参照されたい。
【0058】
特定のmiR遺伝子産物のノーザンブロットハイブリダイゼーションに適切なプローブは該当なし2で示される核酸配列、あるいは、例えば、(http://www.sanger.ac.uk/Software/Rfarn/mirna/index.sht
ml)(Griffiths‐Jones,S.,The micro‐RNA Registry.Nucleic Acids Res,2004.32(1):p.D109‐11)におけるmiRNAレジストリにおいて入手可能な既知のmiRNA種の公表された配列から産生することができる。標識DNAおよびRNAプローブの調製方法、ならびに標的ヌクレオチド配列にこれらをハイブリダイズする条件は、当該技術分野で既知であり、例えば、開示内容が参考として本明細書で援用される、Molecular Cloning:A Laboratory Manual,J.Sambrook et
al.,eds.,2nd edition,Cold Spring Harbor
Laboratory Press,1989,Chapters 10 and 11に記載されている。
【0059】
RNA転写物のレベルの判定は、ノーザンおよび他のRNAハイブリダイゼーション法のほかに、in situハイブリダイゼーション法を使用して達成することができる。この技法は、必要とする細胞がノーザンブロット法よりも少なく、顕微鏡カバーガラスまたはスライド上に細胞全体を置いて、放射性プローブまたは他の標識核酸(例えば、cDNAまたはRNA)プローブを含む溶液で細胞の核酸含有量を調べる手順を伴う。この技法は、被験体由来の組織生検試料の解析に特に適している。in situハイブリダイゼーション法の実施については、開示内容全体が参考として本明細書で援用される、米国特許第5,427,916号に詳述されている。上記の通り、特定のmiR遺伝子産物のin situハイブリダイゼーションに適切なプローブは、図2で示される核酸配列から産生することができる。
【0060】
試料における複数のmiR遺伝子産物の発現レベルを同時に測定するのに適切な技法は、高処理のマイクロアレイに基づく方法である。このような技法を使用して、例えば、癌と相関するすべての既知のmiR遺伝子の転写物の発現レベルを判定する場合がある。このような方法は、1組のmiR遺伝子に特異的な1組のプローブオリゴヌクレオチドを含むマイクロチップフォーマット(すなわち、マイクロアレイ)において、オリゴライブラリーを作成する手順を伴う。このようなマイクロアレイを使用して、生体試料における複数のマイクロRNAの発現レベルは、RNAを逆転写して1組の標的オリゴヌクレオチドを生成し、それらの標的オリゴヌクレオチドをマイクロアレイ上のプローブオリゴヌクレオチドにハイブリダイズして、ハイブリダイゼーションプロファイルまたは発現プロファイルを作成することにより、判定される。次いで、試験試料のハイブリダイゼーションプロファイルを対照試料のハイブリダイゼーションプロファイルと比較し、どのマイクロRNAにおいて膵臓癌または前癌性の細胞における発現レベルが変化したのかを判定することができる。一例として、オリゴライブラリーは、ヒトゲノム由来のすべての既知のmiRに対応するプローブを含む。マイクロアレイは、miRNAが発見されるにつれてさらなるmiRNAを含むように拡大される場合がある。このアレイは、各miRNAに対して2種類異の異なるオリゴヌクレオチドプローブを含み、1つは成熟型miRの活性配列を含むプローブであり、もう1つはmiR前駆体に特異的なプローブである。このアレイはまた、ハイブリダイゼーションの厳密性条件のために対照を含む場合もある。miRNAsを検出するためのマイクロアレイ法の例は、内容が参考として本明細書で援用される、米国特許出願第2005/0277139号に記載されている。
【0061】
miR遺伝子産物のレベルはまた、miR遺伝子産物をコードするmiR遺伝子のコピー数を検出する検定を使用して判定することもできる。腫瘍において増幅を受けたmiR遺伝子の存在は、miR遺伝子のコピー数、すなわちmiR遺伝子産物をコードする細胞内のDNA配列の数を判定することによって評価される。一般的に、正常2倍体細胞は、特定の常染色体遺伝子のコピーを2つ有する。しかし、コピー数は、例えば癌細胞において、遺伝子増幅または複製によって増加させることもできれば、欠失によって減少させることもできる。特定の遺伝子のコピー数を評価する方法は、当該技術分野で周知であり、
とりわけ、ハイブリダイゼーションに基づく検定および増幅に基づく検定を含む。
【0062】
いくつかのハイブリダイゼーションに基づく検定のいずれを使用しても、生体試料の細胞におけるmiR遺伝子のコピー数を検出することができる。このような方法の1つがサザンブロット分析であり(Ausubel,et al.,Eds.,Current Protocols in Molecular Biology,Greene Publishing and Wiley‐Interscience,New York,1995;Sambrook et al.,Molecular Cloning,A Laboratory Manual 2d Ed.を参照)、この分析において、ゲノムDNAは通常断片化され、電気泳動により分離され、膜に転写された後、miR遺伝子特異的プローブにハイブリダイズされる。標的領域のプローブのハイブリダイゼーションシグナルの強度と、同じゲノムにおける正常な非増幅、単一コピーゲノムDNAの領域の対照プローブのシグナルとの比較によって、使用する特異的なプローブに対応する相対的miR遺伝子コピー数の推定値が得られる。対照よりもシグナルが増加していれば、増幅の存在が示される。
【0063】
試料中のmiR遺伝子のコピー数を判定する方法は、例えば、蛍光in situハイブリダイゼーション(FISH)などのin situハイブリダイゼーションである(Angerer,1987 Meth.Enzymol.,152:649を参照)。一般的に、in situハイブリダイゼーションは、以下の主な手順を含む:(1)解析する組織または生体構造の固定;(2)標的DNAのアクセシビリティの向上および非特異的結合の減少のための生体構造のプレハイブリダイゼーション処理;(3)生体構造内または組織内の核酸への核酸混合物のハイブリダイゼーション;(4)ハイブリダイゼーション非結合していない核酸フラグメントを除去するハイブリダイゼーション後洗浄、および(5)ハイブリダイズされた核酸フラグメントの検出。このような用途で使用されるプローブは、通常、例えば、放射性同位体または蛍光レポーターによって標識される。適切なプローブは、例えば約50、100または200ヌクレオチドから約1000以上のヌクレオチドと十分に長く、ストリンジェントの条件下で標的核酸による特異的なハイブリダイゼーションを可能にする。
【0064】
DNAコピーの数を判定するための別の代替の方法は、比較ゲノムハイブリダイゼーション(CGH)である。比較ゲノムハイブリダイゼーション法では、核酸の「試験」回収物が第1の標識によって標識され、第2の回収物(例えば、正常細胞または組織由来のもの)は第2の標識によって標識される。核酸のハイブリダイゼーションの比率は、アレイにおける各ファイバーに結合する第1および第2の標識の比率によって判定される。例えば、試験回収物における遺伝子増幅による2つの標識からのシグナルの比率の差が検出され、この比率によって、使用される特異的プローブに対応するmiR遺伝子コピー数の測定値が得られる。DNAコピー数の変化の細胞遺伝学的表現はCGHによって作成することができ、これにより、特異的に標識された試験および参照ゲノムDNAに由来する染色体の長さに沿って蛍光比が得られる。
【0065】
本発明の方法による使用に適したハイブリダイゼーションプロトコルは、例えば、Albertson(1984)EMBO J.3:1227‐1234;Pinkel(1988)Proc.Natl.Acad.Sci.USA,85:9138‐9142;EPO Pub.No.430:402;Methods in Molecular Biology,Vol.33:In Situ Hybridization Protocols,Choo,ed.,Humana Press,Totowa,N.J.(1994)に記載されている。
【0066】
また、増幅に基づく検定を使用して、miR遺伝子のコピー数を測定することもできる
。このような検定において、対応するmiR核酸配列は、増幅反応(例えば、PCR)の鋳型の役割を果たす。定量的増幅では、増幅産物の量が元の試料における鋳型の量に比例する。適切な対照に対する比較により、上で考察した原理に従って、使用される特異的プローブに対応するmiR遺伝子のコピー数の指標が得られる。TaqManプローブを使用したリアルタイム定量的PCRの方法は、当該技術分野で周知である。リアルタイム定量的PCRの詳細なプロトコルは、例えば、Heid et al.,1996,Real time quantitative PCR.Genome Res.,10:986‐994に示されている。
【0067】
また、TaqManに基づく検定を使用して、miRポリヌクレオチドを定量化することもできる。TaqManに基づく検定では、5’蛍光色素および3’消光剤を含む蛍光発生オリゴヌクレオチドプローブが使用される。このプローブはPCR産物にハイブリダイズするが、3’末端における遮断剤によりそれ自体は伸長することができない。次のサイクルでPCR産物が増幅されると、ポリメラーゼ(例えば、AmpliTaq)の5’ヌクレアーゼ活性は、TaqManプローブの開裂をもたらす。この開裂によって、5’蛍光色素と3’消光剤とが分離し、それによって増幅の機能として蛍光が増大する(例えば、http://www2.perkin‐elmer.comを参照)。
【0068】
適切な増幅方法の他の例には、リガーゼ連鎖反応(LCR)(Wu and Wallace,Genomics,4:560,1989;Landegren et al.,Science,241:1077,1988;およびBarringer et al.,Gene,89:117,1990)、転写増幅(Kwoh et al.,Proc.Natl.Acad.Sci.USA,86:1173,1989)、自立配列複製(Guatelli et al.,Proc Nat Acad Sci,USA 87:1874,1990)、ドットPCR、およびリンカーアダプターPCRが含まれるが、これらに限定されない。
【0069】
DNAコピー数を判定する1つの効果的な方法は、マイクロアレイに基づくプラットフォームを使用する。マイクロアレイ技術は、高分解能が得られるため、使用される場合がある。例えば、伝統的なCGHのマッピング分解能は一般的に20Mbと限られているのに対して、マイクロアレイに基づくCGHでは、特異的に標識された試験および参照ゲノムDNAの蛍光比によって、遺伝子座ごとのDNAコピー数の変化の指標が得られ、それによりマッピング分解能の向上が達成される。各種のマイクロアレイ方法の詳細については、文献に記載されている。例えば、米国特許第6,232,068号;Pollack
et al.,Nat.Genet.,23(1):41‐6,(1999)などを参照されたい。
【0070】
本明細書で使用される「プローブオリゴヌクレオチド」とは、標的オリゴヌクレオチドにハイブリダイズすることができるオリゴヌクレオチドを指す。「標的オリゴヌクレオチド」とは、(例えばハイブリダイゼーションを介して)検出する分子または配列を指す。「miR特異的プローブオリゴヌクレオチド」または「miRに特異的なプローブオリゴヌクレオチド」とは、特異的miR遺伝子産物に、または特異的なmiR遺伝子産物の逆転写物にハイブリダイズするように選択された配列を有するプローブオリゴヌクレオチドを意味する。
【0071】
特定の試料の「発現プロファイル」または「ハイブリダイゼーションプロファイル」は、本質的には試料の状態のフィンガープリントであり、2つの状態にはいずれかの特定の遺伝子が同じように発現されている場合があり、いくつかの遺伝子の評価によって、細胞の状態に固有の遺伝子発現プロファイルの作成が同時に可能となる。すなわち、正常組織は、膵臓癌組織、膵炎組織、あるいは癌組織に隣接した被験体の膵臓の非癌性部位から得
られる「良性組織」と区別される場合がある。異なる状態の膵組織の発現プロファイルを比較することによって、これらの状態のそれぞれにおいてどの遺伝子が重要であるのか(遺伝子のアップレギュレーションおよびダウンレギュレーションの両方を含む)に関する情報が得られる。この情報の使用は、膵臓癌組織または正常膵組織に特異的に発現される配列の同定、ならびに異なる予後の転帰をもたらす特異な発現によって、いくつかの方法で可能となる。例えば、特定の治療レジメンは、(例えば、特定の患者の長期の予後を改善するように化学療法薬が作用するかどうかを判定するために)評価される場合がある。同様に、診断は、患者の試料を既知の発現プロファイルと比較することにより実施または確認される場合がある。さらに、これらの遺伝子発現プロファイル(または個体遺伝子)によって、膵臓癌発現プロファイルを抑制するかもしくは予後不良プロファイルを予後良好プロファイルに変える候補薬のスクリーニングが可能となる。
【0072】
従って、検出するmiR遺伝子産物の標的ヌクレオチド配列は、(a)成熟型miRNAの一部またはすべての配列;(b)miRNA前駆体の一部またはすべてのヘアピン配列;または(c)pri‐miRNAの一部またはすべての配列;(d)配列(a)〜(c)の補体;または(f)配列(a)〜(d)に実質的に同一である配列、であってよい。(図1を参照)。実質的に同一の核酸は、標的配列に対して80%、85%、90%、95%、97%、98%または99%超の配列同一性を有する。
【0073】
本発明の一例において、miR遺伝子産物のレベルは、ヒト膵組織または膵臓細胞の生検材料におけるmiRNA前駆体を測定することによって検出される。201の測定されたmiR遺伝子産物の配列を、図2に示す。本明細書における核酸配列はすべて、5’側から3’側の方向で得られる。さらに、遺伝子はイタリック体で表し、遺伝子産物は通常体で表す。例えば、mir‐17は遺伝子であり、miR‐17は遺伝子産物である。ヒトmiRNA前駆体を増幅するために使用されるプライマーを、図4に示す。
【0074】
別の例において、miR遺伝子産物のレベルは、ヒト膵臓癌または良性組織の生検材料における成熟型miRNAを測定することによって検出される。測定された成熟型miR遺伝子産物の配列を、図13および図16に示す。
【0075】
別の例において、活性の成熟型miRNAiの発現は、ノーザンブロット法を使用して評価される。
【0076】
別の例において、逆転写in situ PCRを使用して膵臓腫瘍細胞に対して最も特異的に発現したmiRNAの内の3つを局在化させる。
【0077】
また、膵臓癌に罹患しているか、もしくは膵臓癌を発症する危険性があることが疑われる被験体の膵臓癌を診断するためのキットも検討される。このようなキットは、(a)被験体の膵臓に由来する生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手段、および(b)生体試料におけるmiR遺伝子産物のレベルを、対照試料における対応するmiR遺伝子産物のレベルと比較する手段を含む。従って、生体試料におけるmiR遺伝子産物のレベルと、対照試料における対応するmiR遺伝子産物のレベルとの間で検出された差によって、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれが示される。
【0078】
被験体が膵臓癌に羅患しているのか、もしくは膵臓癌を発症する危険性があるのかの診断に加えて、本発明は、膵臓癌特異的miR遺伝子産物の発現が変化した被験体を治療する方法を検討する。いかなる理論によっても縛られることを望まないが、細胞内の1つ以上のmiR遺伝子産物のレベルの変化は、癌の形成を生じる可能性があるこれらのmiRに対する1つ以上の標的の調節解除をもたらす可能性がある。そのため、(例えば、癌細
胞においてアップレギュレートされたmiR遺伝子産物のレベルを低下させることにより、および/または癌細胞においてダウンレギュレートされたmiR遺伝子産物のレベルを上昇させることにより)癌特異的miR遺伝子産物のレベルを変化させることによって、膵臓癌の治療を成功させることができる。
【0079】
従って、本発明は、被験体における膵臓癌を治療する方法であって、少なくとも1つの膵臓癌特異的miR遺伝子産物が、被験体の癌細胞において調節解除(例えば、ダウンレギュレート、アップレギュレート)される、方法を包含する。miR遺伝子産物が膵臓癌細胞においてダウンレギュレートされる場合、本方法は、被験体における癌の進行が抑制されるように有効量のmiR遺伝子産物を投与する手順を含む。miR遺伝子産物が癌細胞においてアップレギュレートされる場合、本方法は、被験体における癌の進行が抑制されるように、アップレギュレートされたmiR遺伝子の発現を抑制するための有効量の少なくとも1つの化合物(本明細書において、miR遺伝子発現抑制化合物と称される)を被験体に投与する手順を含む。
【0080】
癌の「進行の抑制」または癌の「治療」という用語は、癌の形成、発現または成長の阻止または緩慢化、ならびに侵襲および/または転移を包含する癌症状の消失または軽減を意味する。このような治療は、癌細胞のさらなる分化をもたらすことを含む。
【0081】
本明細書で使用される通り、単離されたmiR遺伝子産物の「有効量」とは、膵臓癌を患っている被験体における癌の進行を抑制するのに十分な量のことである。当業者は、因子(例えば、被験体のサイズおよび重量;疾患の浸透度;被験体の年齢、健康および性別;投与経路;投与が局所的であるか全身性であるか)を考慮することによって、特定の被験体に投与するmiR遺伝子産物の有効量を容易に判定することができる。
【0082】
例えば、単離されたmiR遺伝子産物の有効量は、治療する腫瘤の近似の重量に基づいてよい。腫瘤の近似の重量は、腫瘤の近似の体積を算出することによって判定することができるが、ここで1立方センチメートルの体積はおよそ1グラムに相当する。腫瘤の重量に基づく単離されたmiR遺伝子産物の有効量は、腫瘤1グラム当たり約10〜500マイクログラムであってよい。特定の実施形態において、腫瘤は、腫瘤1グラム当たり少なくとも約10マイクログラム、腫瘤1グラム当たり少なくとも約60マイクログラム、または腫瘤1グラム当たり少なくとも約100マイクログラムであってよい。
【0083】
単離されたmiR遺伝子産物の有効量はまた、治療する被験体の近似または推定の体重に基づいてもよい。本明細書に記載の通り、このような有効量は、非経口的または経腸的に投与することができる。
【0084】
当業者はまた、特定の被験体に単離されたmiR遺伝子産物を投与するための適切な投与計画を容易に判定することもできる。例えば、miR遺伝子産物は、被験体に1回投与することができる(例えば、単回注射または沈殿として)。あるいは、miR遺伝子産物は、数日から数カ月の期間、特に約3日間から約28日間、とりわけ約7日間から約10日間、1日1回または1日2回、被験体に投与することができる。特定の投与計画において、miR遺伝子産物は、1日1回、7日間投与される。投与計画が反復投与を含む場合、被験体に投与されるmiR遺伝子産物の有効量は、すべての投与計画を通じて投与される遺伝子産物の総量を含んでよいものと理解される。
【0085】
本明細書で使用される、「単離」されたmiR遺伝子産物は、合成されたものか、もしくは人の介入によって自然状態から変化または取り出されたものである。例えば、合成のmiR遺伝子産物、あるいはその自然状態の共存材料から部分的または完全に分離されたmiR遺伝子産物は、「単離」されたと判断される。単離されたmiR遺伝子産物は、実
質的に精製された形態で存在することができるか、もしくはmiR遺伝子産物が送達された細胞内に存在することができる。
【0086】
単離された遺伝子産物は、機能性成熟型miR遺伝子産物を含むオリゴヌクレオチド、ヘアピンのループ部を含むmiR前駆体の短いヘアピンを含むオリゴヌクレオチド、ヘアピンを有さない2本鎖のmiR前駆体、またはこのような分子を発現するベクターであってよい。従って、慎重に細胞内に送達または発現されるmiR遺伝子産物は、「単離」されたmiR遺伝子産物と判断される。また、miR前駆体分子から細胞内部で産生されたmiR遺伝子産物は、「単離」された分子であると判断される。
【0087】
いくつかの態様において、単離されたmiR遺伝子産物は、以下の内の1つ以上を含む:MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐204、M1R‐299‐P、MIR‐337、MR‐371、MIR‐383、MIR‐375。
【0088】
単離されたmiR遺伝子産物は、多くの標準的技法を使用して得ることができる。例えば、miR遺伝子産物は、当該技術分野で既知である方法を使用して、化学的に合成することができるか、もしくは組み換えにより産生することができる。一実施形態において、miR遺伝子産物は、適切に保護されたリボヌクレオシドホスホラミダイトおよび従来のDNA/RNAシンセサイザを使用して化学的に合成される。合成のRNA分子または合成試薬の商品製造業者には、例えば、Proligo(ドイツ、ハンブルグ)、Dharmacon Research(米国コロラド州ラファイエット)や、Pierce Chemical(Perbio Scienceの一部門、米国イリノイ州ロックフォード)、Glen Research(米国バージニア州スターリング)、ChemGenes(米国マサチューセッツ州アシュランド)、Cruachem(英国グラスゴー)が含まれる。
【0089】
単離されたmiR遺伝子産物は、裸のRNAとして、送達剤とともに投与することができる。あるいは、miR遺伝子産物は、任意の適切なプロモーターを使用して組換え環状または直鎖状DNAプラスミドから発現させることができる。プラスミドからRNAを発現するための適切なプロモーターには、例えば、U6またはH1 RNA pol IIIプロモーター配列やサイトメガロウイルスプロモーターが含まれる。他の適切なプロモーターの選択は、当該技術分野の範囲内に含まれる。また、本発明の組換えプラスミドは、癌細胞におけるmiR遺伝子産物の発現のための誘導性または調節可能なプロモーターを含むこともできる。
【0090】
組換えプラスミドから発現されたmiR遺伝子産物は、標準的技法によって培養細胞発現系から単離することができる。また、組換えプラスミドから発現するmiR遺伝子産物は、癌細胞に送達することができるか、もしくは癌細胞において直接発現することができる。癌細胞にmiR遺伝子産物を送達する組換えプラスミドの使用については、以下でさらに詳細に考察する。
【0091】
miR遺伝子産物は、別々の組換えプラスミドから発現させることができるか、もしくは同じ組換えプラスミドから発現させることができる。一実施形態において、miR遺伝子産物は単一のプラスミドからRNA前駆体分子として発現し、前駆体分子は、癌細胞の中に残存するプロセッシング系を包含するがこれに限らない適切なプロセッシング系によって、機能性成熟型miR遺伝子産物にプロセッシングされる。他の適切なプロセッシング系には、例えば、in vitroショウジョウバエ細胞可溶化物系(例えば、開示内容全体が参考として本明細書で援用される、米国特許出願第2002/0086356号(Tuschl et al.)に記載)や、大腸菌RNAseIII系、(例えば、開
示内容全体が参考として本明細書で援用される、米国特許出願第2004/00141号(Yang et al.)に記載)が含まれる。
【0092】
miR遺伝子産物の発現に適切なプラスミドの選択、遺伝子産物を発現するためのプラスミド内に核酸配列を挿入する方法、および対象の細胞に組換えプラスミドを送達する方法は、当該技術分野の範囲内に含まれる。例えば、開示内容全体が参考として本明細書で援用される、Zeng et al.(2002),Molecular Cell 9:1327‐1333;Tuschl(2002),Nat.Biotechnol,20:446‐448;Brummelkamp et al.(2002),Science 296:550‐553;Miyagishi et al.(2002),Nat.Biotechnol.20:497‐500;Paddison et al.(2002),Genes Dev.16:948‐958;Lee et al.(2002),Nat.Biotechnol.20:500‐505;およびPaul et
al.(2002),Nat.Biotechnol.20:505‐508を参照されたい。
【0093】
一実施形態において、miR遺伝子産物を発現するプラスミドは、CMV中間体初期プロモーターのコントロール下にあるmiR前駆体RNAをコードする配列を含む。本明細書で使用される、プロモーターの「コントロール下」とは、プロモーターがmiR遺伝子産物コード配列の転写を開始することができるようにmiR遺伝子産物をコードする核酸配列がプロモーターに機能的に結合することを意味する。
【0094】
また、miR遺伝子産物は、組換えウイルスベクターから発現させることもできる。miR遺伝子産物は、2種の別々の組換えウイルスベクターから、あるいは同じウイルスベクターから発現させることができると考えられる。組換えウイルスベクターから発現させるRNAは、標準的技法によって培養細胞発現系から単離すること、あるいは癌細胞において直接発現させることのいずれかが可能である。癌細胞にmiR遺伝子産物を送達する組換えウイルスベクターの使用については、以下でさらに詳細に考察する。
【0095】
本発明の組換えウイルスベクターは、miR遺伝子産物をコードする配列ならびにRNA配列を発現するための任意の適切なプロモーターを含む。適切なプロモーターには、例えば、U6またはH1 RNA pol IIIプロモーター配列やサイトメガロウイルスプロモーターが含まれる。他の適切なプロモーターの選択は、当該技術分野の範囲内に含まれる。また、本発明の組換えウイルスベクターは、癌細胞におけるmiR遺伝子産物の発現のための誘導性または調節可能なプロモーターを含むこともできる。
【0096】
miR遺伝子産物のためのコード配列を収容することができるいずれのウイルスベクター(例えば、アデノウイルス(AV)に由来するベクター;アデノ関連ウイルス(AAV);レトロウイルス(例えば、レンチウイルス(LV)、ラブドウイルス、マウス白血病ウイルス);ヘルペスウイルスなど)も使用することができる。ウイルスベクターの向性は、エンベロープタンパク質または他のウイルス由来の他の表面抗原でベクターを偽型にすることによって、あるいは必要に応じて種々のウイルスキャプシドタンパク質を置換することによって変化させることができる。
【0097】
例えば、本発明のベクターは、水疱性口内炎ウイルス(VSV)や、狂犬病ウイルス、エボラウイルス、モコラウイルスなどに由来する表面タンパク質によって偽型にされてよい。本発明のAAVベクターは、異なるキャプシドタンパク質血清型を発現するためのベクターを設計することによって異なる細胞を標的とすることができる。例えば、血清2型ゲノムにおける血清2型キャプシドを発現するAAVベクターは、AAV2/2と称される。AAV2/2ベクター内のこの血清2型キャプシド遺伝子を血清5型キャプシド遺伝
子で置換してAAV2/5ベクターを作製することができる。異なるキャプシドタンパク質血清型を発現するAAVベクターを作製するための技法は、当該技術分野の範囲内に含まれる。例えば、開示内容全体が参考として本明細書で援用される、Rabinowitz,J.E.et al.,(2002),J.Virol.76:791‐801を参照されたい。
【0098】
本発明の使用に適する組換えウイルスベクターの選択、ベクター内にRNAを発現させるための核酸配列を挿入する方法、対象の細胞にウイルスベクターを送達する方法、および発現したRNA産物の回収は、当該技術分野の範囲内に含まれる。例えば、開示内容全体が参考として本明細書で援用される、Dornburg(1995),Gene Therap.2:301‐310;Eglitis(1988),Biotechniques 6:608‐614;Miller(1990),Hum.Gene Therap.1:5‐14;およびAnderson(1998),Nature 392:25‐30を参照されたい。
【0099】
適切なウイルスベクターは、AVおよびAAVに由来するものである。miR遺伝子産物を発現するための適切なAVベクター、組換えAVベクターを作製する方法、および標的細胞内にベクターを送達する方法は、開示内容全体が参考として本明細書で援用される、Xia et al.(2002),Nat.Biotech.20:1006‐1010に記載されている。miR遺伝子産物を発現するための適切なAAVベクター、組換えAAVベクターを作製する方法、および標的細胞にベクターを送達する方法は、開示内容全体が参考として本明細書で援用される、Samulski et al.(1987),J.Virol.61:3096‐3101;Fisher et al.(1996),J.Virol,70:520‐532;Samulski et al.(1989),J.Virol.63:3822‐3826;米国特許第5,252,479号;米国特許第5,139,941号;国際特許出願第WO94/13788号;国際特許出願第WO93/24641号に記載されている。一実施形態において、miR遺伝子産物は、CMV中間体初期プロモーターを含む単一の組換えAAVベクターから発現する。
【0100】
一実施形態において、本発明の組換えAAVウイルス性ベクターは、ヒトU6RNAプロモーターのコントロール下でpolyT終止配列と機能的に結合してmiR前駆体RNAをコードする核酸配列を含む。本明細書で使用される「polyT終止配列と機能的に結合して」は、センス鎖またはアンチセンス鎖をコードする核酸配列が5’側の方向のpolyT終止シグナルに直接隣接していることを意味する。ベクターからのmiR配列の転写中に、polyT終止シグナルは、転写を終了させるために作用する。
【0101】
膵臓癌のmiRNA発現レベルを変化させる別の方法は、例えばmiRNA遺伝子のプロモーターの高メチル化や低メチル化などの後成的事象によるものである。プロモーターの高メチル化はmiRNA遺伝子の発現の低下につながり、プロモーターの低メチル化はmiRNA遺伝子の発現の増大につながる。(Jones PA,Baylin SB.The fundamental role of epigenetic events in cancer.Nat Rev Genet.3:415‐28(2005))。そのため、癌の進行を抑制する別の方法は、ダウンレギュレートされたmiR遺伝子産物のプロモーター領域の低メチル化をもたらす化合物の投与である。
【0102】
また、本発明の治療方法の他の実施形態において、miR発現を抑制する有効量の少なくとも1つの化合物を被験体に投与することができる。本明細書で使用される、「miR発現の抑制」とは、投与後のmiR遺伝子産物の活性の成熟形態の産生が、投与前に産生した量よりも少ないことを意味する。当業者は、例えば、診断法について上記で考察したmiR転写物レベルを判定するための技法を使用して、miR発現が癌細胞において抑制
されたかどうかを容易に判定することができる。抑制は、遺伝子発現のレベル(すなわち、miR遺伝子産物をコードするmiR遺伝子の転写を抑制することによる)またはプロセッシングのレベル(例えば、成熟型の活性miRへのmiR前駆体のプロセッシングを抑制することによる)で生じる可能性がある。
【0103】
本明細書で使用される、miR発現を抑制する化合物の「有効量」とは、膵臓癌を患う被験体の癌の進行を抑制するのに十分な量である。当業者は、因子(例えば、被験体のサイズおよび重量;疾患の浸透度;被験体の年齢、健康および性別;投与経路;投与が局所的であるか全身性であるか)を考慮することによって、特定の被験体に投与するmiR発現抑制化合物の有効量を容易に判定することができる。
【0104】
例えば、発現抑制化合物の有効量は、治療する腫瘤の近似の重量に基づくてよい。腫瘤の近似の重量は、腫瘤の近似の体積を算出することによって判定することができるが、ここで1立方センチメートルの体積はおよそ1グラムに相当する。腫瘤の重量に基づく有効量は、腫瘤1グラム当たり約10〜500マイクログラムであってよく、腫瘤1グラム当たり少なくとも約10マイクログラム、腫瘤1グラム当たり少なくとも約60マイクログラム、および腫瘤1グラム当たり少なくとも約100マイクログラムであってよい。
【0105】
miR発現を抑制する化合物の有効量はまた、治療する被験体の近似または推定の体重に基づいてもよい。とりわけ、本明細書に記載の通り、このような有効量は非経口的または経腸的に投与することができる。例えば、被験体に投与される発現抑制化合物の有効量は、体重1kg当たり約5〜3000マイクログラム、体重1kg当たり約700〜1000マイクログラムであってもよければ、あるいは体重1kg当たり約1000マイクログラムを超えてもよい。
【0106】
当業者はまた、特定の被験体にmiR発現を抑制する化合物を投与するための適切な投与計画を容易に判定することもできる。例えば、発現抑制化合物は、被験体に1回投与することができる(例えば、単回注射または沈殿として)。あるいは、発現抑制化合物は、数日から数カ月の期間、特に約3日間から約28日間、とりわけ約7日間から約10日間、1日1回または1日2回、被験体に投与することができる。特定の投与計画において、発現抑制化合物は、1日1回、7日間投与される。投与計画が反復投与を含む場合、被験体に投与される発現抑制化合物の有効量は、すべての投与計画を通じて投与される化合物の総量を含んでよいものと理解される。
【0107】
いくつかの態様において、レベルが低下する可能性があるmiR遺伝子産物は、以下の内の1つ以上を含む:let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MlR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424。
【0108】
miR遺伝子発現を抑制するための適切な化合物には、2本鎖RNA(例えば短い干渉RNAまたは低分子干渉RNA「siRNA」)、アンチセンス核酸、リボザイムなどの
酵素RNA分子、または3重らせんをmiR遺伝子により形成することができる分子が含まれる。抑制化合物の別の種類は、miR遺伝子産物プロモーターの高メチル化を引き起こし、それによりmiR遺伝子の発現を低下させる。これらの化合物のそれぞれは、特定のmiR遺伝子産物を標的として、miR遺伝子産物を破壊するか、miR遺伝子産物の破壊を誘導するか、さもなければmiR遺伝子産物のレベルを低下させることができる。
【0109】
例えば、特定のmiR遺伝子の発現は、miR遺伝子産物の少なくとも一部と少なくとも90%、例えば少なくとも95%、少なくとも98%、少なくとも99%または100%の配列相同性を有する単離された2本鎖RNA(「dsRNA」)分子でmiR遺伝子のRNA干渉を誘導することによって抑制することができる。特定の一実施形態において、dsRNA分子は、「短い干渉RNAまたは低分子干渉RNA」または「siRNA」である。
【0110】
本方法において有用なsiRNAは、約17〜約29ヌクレオチドの長さ、あるいは約19〜約25ヌクレオチドの長さの短い2本鎖RNAを含む。siRNAは、標準的ワトソン‐クリック塩基対合相互作用(以下「塩基対」)によって共にアニール化されたセンスRNAストランドおよび相補型アンチセンスRNAストランドを含む。センス鎖は、標的miR遺伝子産物の中に含まれる核酸配列と実質的に同一である核酸配列を含む。
【0111】
本明細書で使用される、標的mRNAの範囲内に含まれる標的配列に「実質的に同一」であるsiRNA内の核酸配列は、標的配列と同一である核酸配列であるか、もしくは標的配列とは1個または2個のヌクレオチドが異なる核酸配列である。siRNAのセンス鎖およびアンチセンス鎖は、2つの相補型1本鎖RNA分子を含んでよいか、もしくは2つの相補的部分が塩基対を形成しかつ1本鎖「ヘアピン」領域が共有結合した単一の分子を含んでよい。
【0112】
siRNAはまた、1個以上のヌクレオチドの付加、欠失、置換および/または変化によって天然のRNAとは異なる変化したRNAであってもよい。このような変化には、例えばsiRNAの末端やsiRNAの1個以上の内部ヌクレオチドへの非ヌクレオチド材料の付加、siRNAをヌクレアーゼ分解に抵抗性とする修飾、またはデオキシリボヌクレオチドによるsiRNAにおける1個以上のヌクレオチドの置換が含まれる場合がある。
【0113】
また、siRNAは、特定の「薬物のような」性質を含むように設計することもできる。このような修飾には、安定のための化学修飾や送達のためのコレステロール抱合が含まれる。このような修飾によってsiRNAに対してより良好な薬理学的性質が付与され、このような修飾を使用して、薬理活性siRNAは、幅広い生体分布を達成することができ、in vivoにおける大部分の組織内でmiRNAの効率的なサイレンシングを達成することができる。
【0114】
また、siRNAの一方または両方のストランドは、3’オーバーハングを含んでよい。本明細書で使用される「3’オーバーハング」とは、2重らせんRNAストランドの3’末端から伸長する少なくとも1つの不対ヌクレオチドを指す。従って、特定の実施形態において、siRNAは、1〜約6個のヌクレオチド(リボヌクレオチドまたはデオキシリボヌクレオチドを含む)の長さ、1〜約5個のヌクレオチドの長さ、1〜約4個のヌクレオチドの長さ、または約2〜約4個のヌクレオチドの長さの少なくとも1つの3’オーバーハングを含む。一実施形態において、3’オーバーハングは、siRNAの両ストランドに存在しており、かつ2個のヌクレオチドの長さである。例えば、siRNAの各ストランドは、ジチミジル酸(「TT」)またはジウリジル酸(「uu」)の3’オーバーハングを含んでよい。
【0115】
siRNAは、単離されたmiR遺伝子産物について上記で記載した通り、化学的または生物学的に産生することができるか、もしくは組換えプラスミドまたはウイルスベクターから発現させることができる。dsRNAまたはsiRNA分子を産生および試験するための例示的な方法は、開示内容全体が参考として本明細書で援用される、米国特許出願第2002/0173478号(Gewirtz)および米国特許出願第2004/0018176号(Reich et al.)に記載されている。in vivoでmiRNAを非発現化するために設計される治療上有効なsiRNAを合成および確認する方法は、内容全体が参考として本明細書で援用される、Krutzfeldt J, et al.(2005),Silencing of microRNAs in vivo
with’antagomirs,’Nature 438(7068):685‐9に記載されている。
【0116】
また、特定のmiR遺伝子の発現は、アンチセンス核酸によって抑制することもできる。本明細書で使用される場合、「アンチセンス核酸」とは、標的RNAの活性を変えるRNA‐RNAまたはRNA‐DNAまたはRNA‐ペプチド核酸相互作用によって標的RNAに結合する核酸分子を指す。本方法の使用に適したアンチセンス核酸は、一般的にmiR遺伝子産物内の連続した核酸配列に相補的な核酸配列を含む1本鎖核酸(例えばRNA、DNA、RNA‐DNAキメラ、PNA)である。アンチセンス核酸は、miR遺伝子産物内の連続した核酸配列に対して50〜100%相補的、75〜100%相補的、または95〜100%相補的な核酸配列を含んでよい。いかなる理論によっても縛られることを望まないが、アンチセンス核酸は、miR遺伝子産物/アンチセンス核酸2本鎖を消化するRNアーゼHまたは別の細胞ヌクレアーゼを活性化すると考えられる。
【0117】
例えば、真核生物においては、RNAポリメラーゼは、構造遺伝子の転写を触媒してmRNAを産生する。DNA分子は、RNA転写物が好ましいmRNAの配列に相補的な配列を有するRNAポリメラーゼ鋳型を含むように設計することができる。RNA転写物は、「アンチセンスRNA」と称される。アンチセンスRNA分子は、mRNA発現を抑制することができる(例えば、Rylova et al.,Cancer Res,62(3):801‐8,2002;Shim et al.,Int. J.Cancer,94(1):6‐15,2001)。
【0118】
あるいは、第1の核酸分子に対して、相補配列であるかもしくは第1の分子の相補配列またはその一部に相同である配列で作製される第2のDNA分子または第2のキメラ核酸分子は、第1の分子の「アンチセンスDNAまたはDNAデコイまたはデコイ分子」と称される。「デコイ分子」という用語はまた、DNAまたはPNA(ペプチド核酸)を含み(Mischiati et al.,Int.J.Mol.Med.,9(6):633‐9,2002)、かつ調節タンパク質のための結合部位や転写因子のための結合部位などのタンパク質結合部位の配列を含む核分子(1本鎖であっても2本鎖であってもよい)を包含する。アンチセンス核酸分子の応用は、アンチセンスDNAおよびデコイDNA分子を包含し、当該技術分野で既知である(例えば、開示内容全体が参考として本明細書で援用される、Morishita et al.,Ann.NY Acad.Sci.,947:294‐301,2001;Andratschke et al.,Anticancer Res,21:(5)3541‐3550,2001)。
【0119】
また、アンチセンス核酸は、核酸主鎖あるいは糖および塩基部分(またはそれらの等価物)に修飾を含んで標的特異性、ヌクレアーゼ耐性、送達性または分子の有効性に関するその他の性質を向上させることができる。このような修飾は、コレステロール部分、アクリジンなどの2本鎖インターカレータ、または1つ以上のヌクレアーゼ耐性群を含む。
【0120】
アンチセンス核酸は、単離されたmiR遺伝子産物について上記で記載した通り、化学的または生物学的に産生することができるか、もしくは組換えプラスミドまたはウイルスベクターから発現させることができる。産生および試験するための例示的な方法は、当該技術分野の範囲内に含まれ;例えば、開示内容全体が参考として本明細書で援用される、Stein and Cheng(1993),Science 261:1004;および米国特許第5,849,902号(Woolf et al.)を参照されたい。
【0121】
特定のmiR遺伝子の発現はまた、酵素核酸によって抑制することもできる。本明細書で使用される「酵素核酸」とは、miR遺伝子産物の連続した核酸配列に相補性を有し、具体的にはmiR遺伝子産物を開裂することが可能な基質結合領域を含む核酸を指す。酵素核酸基質結合領域は、miR遺伝子産物における連続した核酸配列に対して、例えば50〜100%相補的、75〜100%相補的、または95〜100%相補的であってよい。酵素核酸はまた、塩基、糖および/またはリン酸基に修飾を含むこともできる。本発明の方法で使用される酵素拡散の例にはリボザイムがある。
【0122】
リボザイムは、RNAの特異的開裂を触媒することができる酵素RNA分子である。概要は、Rossi,Current Biology,4:469‐471(1994)で示される。リボザイムの作用機序は、相補型標的RNAに対するリボザイム分子の配列特異的ハイブリダイゼーションと、その後のエンドヌクレアーゼによる開裂を含む。リボザイム分子の組成物は、標的遺伝子mRNAに相補的な1つ以上の配列を含む必要があり、かつmRNA開裂の原因となる周知の触媒配列を含む必要がある(米国特許第5,093,246号)。
【0123】
いずれの可能性のあるRNA標的中の特異的なリボザイム開裂部位も、GUA、GUUおよびGUCという配列を含むリボザイム開裂部位に対する対象の分子をスキャンすることによって先ず同定される。一度同定されると、開裂部位を含むmiR遺伝子の領域に対応する約15〜20リボヌクレオチドの短いRNA配列は、オリゴヌクレオチド配列を不適切にする可能性がある、例えば二次構造などの予想される構造特性について評価することができる。候補配列の適合性もまた、相補的オリゴヌクレオチドとのハイブリダイゼーションの容易さを、リボヌクレアーゼ防御検定を使用して評価することができる。
【0124】
酵素核酸は、単離されたmiR遺伝子産物について上記で記載した通り、化学的または生物学的に産生することができるか、もしくは組換えプラスミドまたはウイルスベクターから発現させることができる。dsRNAまたはsiRNA分子を産生および試験するための例示的な方法は、開示内容全体が参考として本明細書で援用される、Werner and Uhlenbeck(1995),Nucl.Acids Res.23:2092‐96;Hammann et al.,(1999),Antisense and Nucleic Acid Drug Dev.9:25‐31;および米国特許第4,987,071号(Cech et al.)に記載されている。
【0125】
3重らせん形成分子は、標的miR遺伝子活性のレベルを低下させる際に使用することができる。3本鎖立体配座(3重らせん)において共に会合することができ、それにより標的遺伝子の翻訳を阻害するために使用することができる核酸分子は、デオキシヌクレオチドから構成される1重らせんでなければならない。これらのオリゴヌクレオチドの塩基組成は、一般的に2本鎖の一方の鎖上のプリンまたはピリミジンのいずれかの相当大きなストレッチを必要とするフーグスティーン型塩基対合則により3重らせんの形成を促進するように設計される必要がある。ヌクレオチド配列はピリミジンに基づくことができ、それによって、生成する3重らせんの3本の会合した鎖を横切るTATおよびCGCトリプレットが生じるのである。ピリミジン富化分子は、2本鎖のうちの1本鎖のプリン富化領域に対し、この鎖と平行方向の塩基相補性を提供する。加えて、プリンに富んだ核酸分子
、例えばG残基のストレッチを有するものを選択することができる。これらの分子が、GC対に富んだDNA2本鎖と3重らせんを形成するのである。この場合、プリン残基の大半は、標的2本鎖の内の1本鎖に位置し、3本鎖中の3本の鎖を横切るGGCトリプレットを生成させる。あるいは、いわゆる「スイッチバック」核酸分子を作製することにより、3重らせん形成のために標的とされる可能性のある配列を増加させることができる。スイッチバック分子は、交互に5’‐3’、3’‐5’様式で合成され、その結果、それらは2本鎖の最初の1本の鎖と塩基対合し、次いでもう一方の鎖と塩基対合することになり、2本鎖分子の一方の鎖上のプリンまたはピリミジンのいずれかの相当大きなストレッチの必要性がなくなる。
【0126】
膵臓癌のmiRNA発現レベルを変化させる別の方法は、例えばmiRNA遺伝子のプロモーターの高メチル化や低メチル化などの後成的事象によるものである。プロモーターの高メチル化はmiRNA遺伝子の発現の低下につながり、プロモーターの低メチル化はmiRNA遺伝子の発現の増大につながる。(Jones PA,Baylin SB.The fundamental role of epigenetic events in cancer.Nat Rev Genet.3:415‐28(2005))。
【0127】
少なくとも1つのmiR遺伝子産物またはmiR発現を抑制するために少なくとも1つの化合物を投与することで、被験体の膵臓癌の進行が抑制される。miR遺伝子産物またはmiR遺伝子発現を抑制する化合物の投与後に被験体におけるかかる細胞の数が一定のままであるかもしくは減少する場合に、癌細胞増殖の抑制が推定される。このような細胞の絶対数は増加するが、腫瘍成長の速度が減少する場合に、癌細胞の増殖の抑制が推定される。
【0128】
被験体の身体内の癌細胞の数は、直接測定するか、もしくは原発性腫瘤または転移性腫瘤のサイズから推定することによって判定することができる。例えば、被験体における癌細胞の数は、免疫組織学的方法、フローサイトメトリー、または癌細胞の特徴的な表面マーカーを検出するように設計された他の技法によって測定することができる。
【0129】
腫瘤のサイズは、直接的な目視観測によって、あるいはX線や、磁気共鳴映像法、超音波検査、シンチグラフィーなどの画像診断法によって確認することができる。当該技術分野で既知であるように、腫瘤のサイズを確認するために使用される画像診断法は、コントラスト剤の有無にかかわらず使用することができる。腫瘤のサイズはまた、物理的手段(例えば、組織塊の触診あるいはキャリパーなどの計器による組織塊の測定)によって確認することもできる。
【0130】
miR遺伝子産物またはmiR遺伝子発現抑制化合物は、被験体の癌細胞へのこれらの化合物の送達に適切ないずれの手段によっても被験体に投与することができる。例えば、miR遺伝子産物またはmiR発現抑制化合物は、これらの化合物またはこれらの化合物をコードする配列を含む核酸によって被験体の細胞をトランスフェクションさせるための適切な方法によって投与することができる。一実施形態において、細胞は、少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物をコードする配列を含むプラスミドまたはウイルスベクターによってトランスフェクションされる。
【0131】
真核細胞のトランスフェクション方法は、当該技術分野で周知であり、細胞の核または前核への核酸の直接注入;エレクトロポレーション;リポソーム転移または疎水性材料によって仲介される転移;レセプター仲介核酸送達、バイオバリスティックまたは粒子加速;リン酸カルシウム沈殿およびウイルスベクターによって仲介されるトランスフェクションを包含する。
【0132】
例えば、細胞は、リポソーム型転移化合物(例えば、DOTAP(N‐[1‐(2,3‐ジオレオイロキシ)プロピル]‐N,N,N‐トリメチルアンモニウムメチルスルフェイト、Boehringer‐Mannheim)または等価物(例えばLIPOFECTIN))によってトランスフェクションすることができる。使用する核酸の量は、本発明の診療に重大な意味を持たず;許容される結果は、細胞105個当たり0.1〜100マイクログラムの核酸で達成される場合がある。例えば、細胞105個当たり3マイクログラムのDOTAPにおいて約0.5マイクログラムのプラスミドベクターの比を使用することができる。
【0133】
一実施形態において、膵臓癌細胞は、被験体から単離され、ダウンレギュレートされたmiR遺伝子産物をコードする核酸によってトランスフェクションされ、被験体に再導入される。
【0134】
また、miR遺伝子産物またはmiR遺伝子発現抑制化合物は、任意の適切な経腸または非経口投与経路によって被験体に投与することができる。本方法に適切な経腸投与経路には、例えば、経口送達や、直腸送達、鼻腔内送達が含まれる。適切な非経口投与経路には、例えば、血管内投与(例えば静脈内ボーラス注射や、静脈内注入、動脈内ボーラス注射、動脈内注入、血管系へのカテーテル滴下注入);組織周囲および組織内注射(例えば、腫瘍周囲および腫瘍内注射や、網膜内注射、網膜下注射);皮下注射または沈殿(皮下注入(例えば浸透ポンプによって)など);例えばカテーテルまたは他の配置装置(例えば、網膜ペレットや、坐剤や、多孔性、非多孔性またはゼラチン状材料を含むインプラント)による対象の組織に対する直接塗布;および吸入が含まれる。適切な投与経路は、腫瘍への注射、注入および直接注入である。
【0135】
本方法において、miR遺伝子産物またはmiR遺伝子産物発現抑制化合物は、送達試薬とともに裸のRNA、もしくはmiR遺伝子産物または発現抑制化合物を発現する配列を含む核酸(例えば組換えプラスミドまたはウイルスベクター)のいずれかとして被験体に投与することができる。適切な送達試薬には、例えば、Mirus Transit TKO疎水性試薬や;リポフェクチン;リポフェクタミン;セルフェクチン;ポリ陽イオン(例えばポリリジン)、リポソームが含まれる。
【0136】
miR遺伝子産物またはmiR遺伝子発現抑制化合物を発現する配列を含む組換えプラスミドおよびウイルスベクター、ならびに癌細胞にこのようなプラスミドおよびベクターを送達するための技法は、本明細書において考察される。
【0137】
一実施形態において、リポソームを使用して、miR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む核酸)が被験体に送達される。リポソームはまた、遺伝子産物または核酸の血中半減期を延長させることができる。本発明に使用される適切なリポソームは、一般的に中性または負に荷電したリン脂質やステロール(例えばコレステロール)を含む標準的ベシクル形成脂質から形成されることができる。脂質の選択は、一般的に、因子(例えば所望のリポソームのサイズや、血流におけるリポソームの半減期)を考慮して導かれる。例えば、開示内容全体が参考として本明細書で援用される、Szoka et al.(1980),Ann.Rev.Biophys.Bioeng.9:467;ならびに米国特許第4,235,871号、第4,501,728号、第4,837,028号および第5,019,369号に記載の通り、リポソームを調製するための種々の方法が知られている。
【0138】
本方法に使用されるリポソームは、リポソームを癌細胞に標的とするリガンド分子を含んでよい。癌細胞に一般的なレセプターと結合するリガンド(例えば、腫瘍細胞抗原と結
合するモノクローナル抗体)が適切である。
【0139】
本方法に使用されるリポソームはまた、単核マクロファージ系(「MMS」)および細網内皮系(「RES」)によるクリアランスを回避するように修飾することができる。そのように修飾されたリポソームは、表面上にオプソニン化抑制部分を有するか、もしくはリポソーム構造内に組み込まれる。いくつかの実施形態において、本発明のリポソームは、オプソニン化抑制部分およびリガンドの両方を含んでよい。
【0140】
本発明のリポソームの調製に使用されるオプソニン化抑制部分は、通常は、リポソーム膜に結合する大きな親水性ポリマーである。本明細書で使用される場合、オプソニン化抑制部分がリポソーム膜に「結合」するとは、例えば膜自体への脂溶性アンカーの挿入または膜脂質の活性基への直接の結合によって化学的または物理的に膜に結合させる場合のことである。開示内容全体が参考として本明細書で援用される米国特許第4,920,016号に記載されている通り、これらのオプソニン化抑制親水性ポリマーは、MMSおよびRESによるリポソームの取り込みを著しく減少させる保護表面層を形成する。
【0141】
リポソームの修飾に適切なオプソニン化抑制部分は、約500〜約40,000ダルトン、または約2,000〜約20,000ダルトンの数平均分子量を有する水溶性ポリマーを含む。このようなポリマーには、ポリエチレングリコール(PEG)またはポリプロピレングリコール(PPG)誘導体;例えば、メトキシPEGまたはPPGやステアリン酸PEGまたはPPG;合成ポリマー(例えばポリアクリルアミドやポリN‐ビニルピロリドン);直鎖状、分岐状またはデンドリマーのポリアミドアミン;ポリアクリル酸;ポリアルコール(例えば、カルボキシル基またはアミノ基が化学的に結合するポリビニルアルコールやポリキシリトール)ならびにガングリオシド(例えばガングリオシドGM1)が含まれる。また、PEG、メトキシPEGまたはメトキシPPGのコポリマーまたはそれらの誘導体も適切である。さらに、オプソニン化抑制ポリマーは、PEGのブロックコポリマーならびにポリアミノ酸、ポリサッカリド、ポリアミドアミン、ポリエチレンアミン、ポリヌクレオチドのいずれかであってよい。オプソニン化抑制ポリマーはまた、アミノ酸またはカルボン酸(例えば、ガラクツロン酸、グルクロン酸、マンヌロン酸、ヒアルロン酸、ペクチン酸、ノイラミン酸、アルギン酸)、カラギーナンを含む天然のポリサッカリド;アミノ化されたポリサッカリドまたはオリゴサッカリド(直鎖状または分岐状);あるいはカルボキシ化されたポリサッカリドまたはオリゴサッカリド(例えば、カルボキシル基と結合を生じる炭酸の誘導体と反応したもの)であってもよい。オプソニン化抑制部分は、PEG、PPGまたはそれらの誘導体であってよい。PEGまたはPEG誘導体で修飾されるリポソームは、「ポリエチレングリコール化されたリポソーム」と称される場合がある。
【0142】
オプソニン化抑制部分は、数多くの周知の技法の内のいずれか1つによって、リポソーム膜に結合させることができる。例えば、PEGのN‐ヒドロキシスクシンイミドエステルは、ホスファチジルエタノールアミン脂溶性アンカーに結合させることができ、次いで膜に結合させることができる。同様に、デキストランポリマーは、Na(CN)BH3と混合溶媒(例えば、60℃で30:12の比のテトラヒドロフランと水)を使用して還元的アミノ化によってステアリルアミン脂溶性アンカーで誘導体化することができる。
【0143】
オプソニン化抑制部分によって修飾されるリポソームは、無修飾リポソームより非常に長く血行の中にとどまる。このために、このようなリポソームは「ステルス」リポソームと称されることがある。ステルスリポソームは、多孔性または「漏出性」微小血管系によって供給された組織内に蓄積することが知られている。従って、このような微小血管系の欠損(例えば固形腫瘍)を特徴とする組織は、これらのリポソームを効率的に蓄積する。Gabizon,et al.(1988),Proc.Natl.Acad.Sci.
,U.S.A.,18:6949‐53を参照されたい。さらに、RESによる取り込みの減少は、肝臓および脾臓におけるリポソームの著しい蓄積を防止することによってステルスリポソームの毒性を低下させる。従って、オプソニン化抑制部分によって修飾されるリポソームは、腫瘍細胞へのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む核酸)の送達に非常に適している。
【0144】
miR遺伝子産物またはmiR遺伝子発現抑制化合物は、当該技術分野で既知の技法に従って、被験体への投与前に、「医薬品」と称されることがある薬学的組成物として調製することができる。従って、本発明は、膵臓癌を治療するための薬学的組成物を包含する。一実施形態において、薬学的組成物は、少なくとも1つの単離されたmiR遺伝子産物および薬学的に許容される担体を含む。特定の実施形態において、miR遺伝子産物は、適切な対照細胞よりも膵臓癌細胞における発現レベルが低下したmiR遺伝子産物に相当する。
【0145】
他の実施形態において、本発明の薬学的組成物は、少なくとも1つのmiR発現抑制化合物を含む。特定の実施形態において、少なくとも1つのmiR遺伝子発現抑制化合物は、対照細胞よりも膵臓癌細胞において発現が大きいmiR遺伝子に特異的である。
【0146】
本発明の薬学的組成物は、少なくとも無菌であり、かつ発熱物質がないことを特徴とする。本明細書で使用される場合、薬学的「組成物」または「製剤」は、ヒトおよび獣医学的使用のための製剤を包含する。本発明の薬学的組成物を調製する方法は、開示内容全体が参考として本明細書で援用される、Remington’s Pharmaceutical Science,17th ed.,Mack Publishing Company,Easton,Pa.(1985)に記載の通り、当該技術分野の範囲内に含まれる。
【0147】
本薬学的製剤は、薬学的に許容される担体と混合された少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)(例えば0.1〜90重量%)またはその生理的に許容される塩を含む。また、本発明の薬学的製剤は、リポソームおよび薬学的に許容される担体によってカプセル化された少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)を含んでよい。
【0148】
特に適切な薬学的に許容される担体は、水、緩衝用水、生理食塩液、0.4%生理食塩水、0.3%グリシン、ヒアルロン酸などである。
【0149】
本発明の薬学的組成物は、ヌクレアーゼによる分解に対して抵抗性である少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)を含んでよい。当業者は、例えば2’位で修飾される1つ以上のリボヌクレオチドをmiR遺伝子産物内に組み込むことによって、ヌクレアーゼ抵抗性である核酸を容易に合成することができる。適切な2’修飾リボヌクレオチドには、フルオロ、アミノ、アルキル、アルコキシおよびO‐アリルで2’位が修飾されたものが含まれる。
【0150】
本発明の薬学的組成物はまた、従来の薬学的賦形剤および/または添加剤を含んでもよい。適切な薬学的賦形剤には、安定剤、抗酸化剤、モル浸透圧調整剤、緩衝剤、およびpH調整剤が含まれる。適切な添加剤には、例えば、生理的に生体適合性の緩衝剤(例えば塩酸トロメタミン)、キレート剤(例えば、DTPAやDTPA‐ビスアミド)またはカルシウムキレート錯体(例えば、カルシウムDTPA、CaNaDTPA‐ビスアミド)の添加剤、あるいたは場合により、カルシウムまたはナトリウム塩(例えば、塩酸カルシ
ウム、アスコルビン酸カルシウム、グルコン酸カルシウム、乳酸カルシウム)の添加剤が含まれる。本発明の薬学的組成物は、液体形態で使用するためにパッケージすることができるか、もしくは凍結乾燥することができる。
【0151】
本発明の固体の薬学的組成物としては、従来の無毒性で固体の薬学的に許容される担体(例えば、マンニトール、ラクトース、デンプン、ステアリン酸マグネシウム、ナトリウムサッカリン、滑石、セルロース、グルコース、スクロース、炭酸マグネシウムなどの医薬品グレード)を使用することができる。
【0152】
例えば、経口投与のための固体の薬学的組成物は、上記に掲載された担体および賦形剤のいずれか、ならびに10〜95%、好ましくは25%〜75%の少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)を含んでよい。エアゾール(吸入)投与のための薬学的組成物は、0.01〜20重量%、好ましくは1%〜10重量%の、上記の通りのリポソームおよび噴射剤の中にカプセル化した少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)を含んでよい。また、例えば鼻腔内送達のためのレシチンなどの担体を所望により含んでよい。
【0153】
本発明はまた、被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する方法も提供する。本方法は、(a)対照細胞に比べてアップレギュレートされたmiR遺伝子産物を有する癌細胞を含む被験体の膵臓から第1の試験試料を得る手順;(b)被験体に治療レジメンを施す手順;(d)ある期間後に被験体の膵臓から第2の試験試料を得る手順;および(e)第1および第2の試験試料におけるアップレギュレートされたmiR遺伝子産物のレベルを比較する手順を含む。第2の試験試料におけるアップレギュレートされたmiR遺伝子産物レベルが第1の試験試料よりも低いことによって、その治療レジメンが被験体における膵臓癌の進行抑制に効果的であることが示される。
【0154】
被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する他の方法は、(a)対照細胞に比べてダウンレギュレートされたmiR遺伝子産物を有する癌細胞を含む被験体の膵臓から第1の試験試料を得る手順;(b)被験体に治療レジメンを施す手順;(d)ある期間後に被験体の膵臓から第2の試験試料を得る手順;および(e)第1および第2の試験試料におけるダウンレギュレートされたmiR遺伝子産物のレベルを比較する手順を含む。第2の試験試料におけるダウンレギュレートされたmiR遺伝子産物レベルが第1の試験試料よりも高いことによって、その治療レジメンが被験体における膵臓癌の進行抑制に効果的であることが示される。
【0155】
本発明はまた、膵臓癌用抗癌剤を同定する方法も包含する。本方法は、(a)膵臓癌細胞を含む生体試料において過剰発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;(b)生体試料に試験剤を接触させる手順;(c)手順(b)の後に生体試料におけるmiR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順を含む。過剰発現したmiR遺伝子産物の試験後の発現レベルが低下することによって、試験剤が膵臓癌の抗癌性を有することが示される。
【0156】
別の実施形態において、膵臓癌用抗癌剤を同定する方法は、(a)膵臓癌細胞を含む生体試料において過小発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;(b)前記生体試料に試験剤を接触させる手順;(c)手順(b)の後に生体試料におけるmiR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについての
データを作成する手順;および(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順であって、過小発現したmiR遺伝子産物の試験後の発現レベルが上昇することによって、試験剤が膵臓癌の抗癌性を有することが示される、手順を含む。
【0157】
適切な剤としては薬物(例えば低分子、ペプチド)や生体高分子(例えばタンパク質、核酸)が含まれるが、これらに限定されるものではない。剤は、組み換えにより、合成的に作製することができるか、もしくは天然の原料から単離(すなわち、精製)することができる。このような剤を細胞に与える各種方法(例えばトランスフェクション)は、当該技術分野で周知であり、このような方法のいくつかは上に記載されている。少なくとも1つのmiR遺伝子産物の発現を検出する方法(例えばノーザンブロット法や、in situハイブリダイゼーション、RT‐PCR、発現プロファイリング)は、当該技術分野で周知である。これらの方法のいくつかもまた、上に記載されている。
【0158】
以下では、本発明を以下の非限定的な実施例で例示する。
【実施例】
【0159】
(実施例1) 膵臓癌を正常組織または膵炎組織と区別するマイクロRNA発現サインの同定
リアルタイム定量的PCR検定を使用して、ヒト膵臓癌(腺癌)、良性対組織、正常な膵臓、慢性膵炎および膵臓癌細胞株の臨床検査材料における200超のmiRNA前駆体の発現を測定した。膵臓癌を正常かつ良性の膵臓と区別した固有のmiRNAサインを同定した。リアルタイム定量的RT‐PCRのために使用される方法は、開示内容全体が参考として本明細書で援用される、Jiang,J.,et al.(2005),Nucleic Acids Res 33:5394‐5403;Schmittgen T.D.,et al.(2004),Nucleic Acids Res 32:E43;および2005年2月24日出願の米国仮出願第60/656,109号に詳述されている。また、実験手順および結果は、開示内容全体が参考として本明細書で援用される、Lee et al.,(2006)Int.J.Cancer 120:1046‐1054に報告されている。
【0160】
材料および方法
組織の入手:この研究において解析された組織試料は、オクラホマ大学ヘルスサイエンスセンターおよびオハイオ州立大学で膵臓の一部の切除のための外科手術を受けた患者に由来するものであった。試料の採集は、施設の施設内倫理委員会の方針および慣行に適合したものであった。外科的な検体の切除と同時に、研究員は直ちにその組織を外科病理検査室に移した。病理部は、検体のグロス分析を実施し、研究のために、癌と思われる膵組織および正常と思われる膵組織を選んだ。各試料をクライオバイアル内に配置し、液体窒素中で急速冷凍し、解析を行うまで‐150℃で保存した。次に、外科的な検体を提供する研究所によって次病理学的解析を行い、それにより研究のために採取された試料の組織変化を確認した。RNA解析を実施した研究機関によって、隣接する良性組織にセカンドレベルの精度管理を行った。組織のスライドを、RNAが単離された組織に直接隣接する凍結組織の切片から準備した。これらのスライドを、良性組織が膵臓腫瘍細胞を含むかどうかを判定するために、本発明者等(W.L.F.)の内の1人が検査した。残りの腫瘍を含む良性組織については、この研究に含めなかった。検体に関する臨床データを付録の表1に示す。
【0161】
細胞株:以下の膵臓腫瘍細胞株を、American Type Tissue Collection(米国バージニア州マナッサス)から購入した。Panc‐1、HS766T、MIA PaCa‐2、HPAF‐II、BxPC‐3、Mpanc‐96、P
L45、Panc03.27およびPanc10.05。細胞株を、標準条件を使用して、10%FBSまたは他の最適化された完全培地を含むRPMI1640培地中で培養した。
【0162】
miRNA前駆体発現プロファイリング:トータルRNAを、1mLのTrizol(Invitrogen、米国カリフォルニア州カールズバッド)中で細胞株または組織から単離した。まず、凍結組織(約10mg)をステンレス鋼乳鉢および乳棒で微粉状にした。正常膵臓由来のトータルRNAは、Ambion(米国テキサス州オースティン)、BD Biosciences(米国カリフォルニア州マウンテンビュー)およびStratagene(米国カリフォルニア州ラ・ホーヤ)から購入した。正常組織のすべてのドナーは、膵疾患以外の合併症で死亡した(図3)。RNAの完全性を、Agilent
2100 Bioanalyzer(Agilent Technologies、米国カリフォルニア州パロアルト)を使用して評価した。RNA完全性番号(RIN)は、Imbeaud,S.,et al.(2005),Nucleic Acids Res 33,e56におけるプロトコルに従って、Agilent 2100エキスパートソフトウェアのRINアルゴリズムを使用して判定された。RIN≧4のRNA試料をこの研究に含めた(図3)。しばらくRNAをRNアーゼフリーのDNAase Iで処理し、222のmiRNA前駆体と18S rRNAとに対する遺伝子特異的プライマーを使用してcDNAを1μgのトータルRNAから合成した。222のmiRNA前駆体の発現は、リアルタイム定量的PCR検定を使用して測定した。cDNAの各試料中の各miRNA前駆体遺伝子について重複PCRを行った。平均CTを重複PCRから判定した。相対的遺伝子発現を2‐(CTmiRNA‐CT18S rRNA)として算出した。相対的遺伝子発現には、データの提示を単純化するために、106を乗算した。生の相対的miRNA前駆体発現データを図4に示す。
【0163】
統計:201の遺伝子発現値(対照遺伝子発現に比べたもの)についてのΔCTデータの平均中心を求め、以下の方法を使用して解析した。フィルタリングされていないデータの発現パターンを、試料の管理されない階層的クラスタリングと、平均連結法およびユークリッド距離に基づく遺伝子の管理されない階層的クラスタリングとを使用して評価した(Eisen MB, et al.(1998),Proc Natl Acad Sci USA 95:14863‐8;Saeed AI,et al.(2003),Biotechniques 34:374‐8)。試料群間に特異に発現する遺伝子を判定するため、そのデータは、p<0.01(10,000無作為順列)の多群の順列に基づくANOVA検定(ウェルチの近似法)および多重検定補正(maxTのWestfall‐Young手順ダウン補正)を使用して差の有意性においてフィルタリングを行った。特異に発現した遺伝子の発現パターンを比較するため、フィルタリングされたデータを、試料の階層的クラスタリングと、平均連結法およびユークリッド距離に基づく遺伝子の階層的クラスタリングとを使用して解析した。
【0164】
フィルタリングされたデータのさらなるクラスター分析を、発現地形図を使用して行った(Kim,et al.(2001),Science,293:2087‐92)。その地形図は、そのデータにおいて固有の主要なクラスターの3次元の概観を提供する。試料は、各エレメントの配置が、miRNA前駆体発現データを使用して算出されたユークリッド距離に基づく多くの最近傍によって影響される、二次元のグリッドに最初にマップされた。第3次元は二次元のグリッド上の点の密度によって判定され、その値は表面として投影されるが、より高いピークは、非常に類似したエレメントのより大きな数を示す。試料の各組間の平均相関もまた算出した。閾値(0.8)超の平均相関を有する試料の各組は、2つの試料を結ぶ線によって発現地形図に示される。これにより、miRNA発現の高相関パターンを有する試料のサブセットの視覚化が可能になる。特定のクラスターからの試料を表すピークは、各ピークの上で着色してコードされた球体によって標識され
た。
【0165】
管理された装置の学習アルゴリズムを、フィルタリングされていないmiRNA発現データに基づいて、試料の分類のために適用した。各miRNAの予測スコアは、訓練、テイクワンアウトクロス確認および試験手順に基づくマイクロアレイアルゴリズムの予測分析(PAM)(Tibshirani R, et al.(2002),Proc Natl Acad Sci USA 99:6567‐72)を使用した発現データの2つのクラスの比較(正常対腫瘍)に基づいて算出した。訓練セットと試験セットとへの試料の分割は、データを無作為に訓練セットと試験セットとに分割する(通常、訓練には2/3。試験には1/3)一般的に認められたアプローチを使用して行う。この研究では、腫瘍試料を、訓練のために約75%に、試験のために25%に無作為に分割した。正常例の数がわずかだった(N=6)ため、正常例は訓練セットのみに含めた。わずかな数の慢性膵炎試料(N=4)は、PAM分析に含めなかった。2つのレベルの精度管理を行っていかなる腫瘍細胞を含む隣接良性組織も除去しつつ、RNAを、顕微解剖した組織ではなく組織全体から抽出した。従って、本発明者等は、いくつかの腫瘍細胞が隣接良性組織を汚染したという可能性を完全に除外することができず、腫瘍に隣接した組織から得られるこれらの良性試料において早期の前癌性変化が発現したのかどうかは不明である。そのため、真の正常例および腫瘍例についてのクラシファイアを訓練するために、良性試料を訓練セットから除外した。良性例については、試験セットにおいて使用した。
【0166】
結果
内部コントロール遺伝子のバリデーション:膵組織はリボヌクレアーゼが豊富であり、RNA単離時には自己分解の可能性を低下させるように注意する必要がある。膵組織から単離されるRNAの完全性を確認するため、約100ngの各RNA試料を、Agilent 2100 Bioanalyzerを使用して検定した。52の組織において、RIN≧4(中央値7.6、範囲4.3〜9.6、(図3))であった。
【0167】
試料のそれぞれにおけるmiRNA前駆体の発現を、リアルタイムPCRを使用して判定し、内部コントロール遺伝子に正規化した。対応量のトータルRNAを各RT反応物に添加し、各種試料(すなわち腫瘍、正常および良性)における平均発現を比較することによって18S rRNAを内部コントロールとして確認した。平均18S rRNA発現においては、腫瘍試料と正常膵臓の間に統計学的有意差がみられなかった(p=0.116、図5)。ここで判定された腫瘍および正常組織における18S rRNA発現は、膵組織についてすでに報告されたもの(Rubie C,et al.,(2005)Mol Cell Probes 19:101‐9)と一致していた。腫瘍群と正常群と良性群との間に18S rRNA発現の有意差がなかったことから、18S rRNAは、その研究の内部コントロール遺伝子として選ばれた。
【0168】
膵組織におけるmiRNA前駆体プロファイリング:2005年4月に見出された222のmiRNAを表す201のmiRNA前駆体の発現を、28の腫瘍、15の隣接良性組織、4つの慢性膵炎検体、6つの正常膵臓組織、および9つの膵臓癌細胞株において測定した。試料の管理されない階層的クラスタリングを、腫瘍、正常膵臓、膵炎および膵臓癌細胞株についてのフィルタリングされていないデータのすべてのセットにおいて実施した。ヒートマップは、201のmiRNA前駆体のみのフィルタリングされていない発現データにより試料が正常な膵臓、腫瘍、慢性膵炎および細胞株のクラスターに十分に分類されることを示す(図6)。
【0169】
同一の膵臓癌患者に由来する15の隣接良性組織のmiRNA発現は、正常膵臓、膵炎、膵腫瘍および癌細胞株とともに含まれていた。miRNA前駆体発現データを、多群ANOVAを使用してフィルタリングした。遺伝子発現データは本質的にノイズが多いため
、データの統計学的フィルタリングは、発現データの前処理の必要な手順であると慣習的に判断される。試料および遺伝子の階層的クラスタリングは、結果として生じた112のmiRNAについて実施した。フィルタリングされたデータの階層的クラスタリングによって、本発明者等は、結果として生じた4つの試料クラスターにおける異なる発現パターンを有するmiRNAの主要な群を同定することができた(図7)。1つのクラスターは、細胞株のみを含んでいた。別のクラスターは、6つのすべての正常膵臓および15の良性組織の内の9つを含んでいた。3番目のクラスターは、4つの慢性膵炎検体および1つの良性組織を含んでいた。最後に、大きなクラスターは、28の腫瘍の内の28および5つの良性組織を含んでいた(図7)。
【0170】
また、フィルタリングされたデータを、発現地形図として知られている種々のクラスタリング法を使用して解析した。地形図から、発現データは、試料の5つの主な群に分けられた(図8)。階層的クラスタリングのように、地形図では、正常膵臓、細胞株、膵臓腺癌および慢性膵炎から試料群が分けられる。この分析は、試料のクラスターのそれぞれが発現地形図上の異なる領域を占めることを示しており、従って、試料の4群のそれぞれがmiRNA発現の異なるパターンを有しており、正常試料と腫瘍試料とを識別するマイクロRNAのサブセットを明らかにする可能性を示唆するものであるというさらなる証拠を提供する。大部分の隣接良性組織は正常と腫瘍とに分類されるが、腫瘍によってクラスター形成されたそれらの良性試料もまた、地形図上の腫瘍で分類される(図8)。地形図のさらなる特徴としては、すべてのmiRNA発現値の平均相関を、試料の各組間で算出した。0.8の閾値を越えるそれらの相関は、miRNA発現パターンが類似した試料の組を結ぶ線として示される。これにより、miRNA発現の高く相関しているパターンを有する試料のサブセットを視覚化することが可能になる。4つの主な群それぞれの中の試料が結ばれるが(すなわち、平均相関>0.8)、腫瘍試料の一部と相関する2つの膵炎試料を除いて群の間に結線はなかった(図8)。
【0171】
異なる膵臓組織の中の遺伝子発現プロファイルの比較を使用して、間質および細胞増殖(例えば細胞株)の寄与を排除し、膵腫瘍において発現する遺伝子を同定した。図7のmiRNA発現データにおけるこのような解析を実施する試みは、癌細胞株における発現が一様に高く、かつ膵炎試料における発現が一様に低かったため、成功しなかった。しかし、多くの腫瘍関連の可能性があるmiRNAは、細胞株および/または腫瘍においては増加したが、正常または膵炎においては増加しないことが同定された(図7)。
【0172】
マイクロアレイアルゴリズムの予測分析(PAM)によるデータ解析:PAM分類アルゴリズムを使用して、miRNA発現データによってどのクラスに試料が適合するのか(腫瘍または正常)を予測することができ、かつ膵臓腺癌に関連した最も重要で、特異に発現したmiRNAを判定することができた。201のpre‐miRNAに関するフィルタリングされていないデータを、Tibshirani R,et al.(2002),Proc Natl Acad Sci USA 99,6567‐72に記載された方法に従って、PAMアルゴリズムにより解析した。75%超の欠測値を有する3つの遺伝子は、補完アルゴリズムの起こり得るアーチファクトを阻止するために分析から除外した。PAM訓練およびクロス確認を、6つの正常膵臓および18の膵腫瘍を使用して実施した。PAMによって、正常および腫瘍試料の100%が正確に分類された(図9A)。PAM試験を、10の腫瘍試料および15の隣接良性試料について実施した。PAMによって、試験された腫瘍試料の100%および試験された15の良性試料の内の11が正確に分類された(図9B)。PAMによって選択された通りの膵臓腺癌において特異に発現した上位68番目までにランクされたmiRNAを図10に示す。PAMによって選択された通りの膵臓腺癌において特異に発現した上位20番目までにランクされたmiRNAを表1に示す。
【0173】
【表1】

【0174】
考察
以下では、膵管腺癌において初めての詳細なmiRNA発現プロファイリング研究の結果を報告する。発現プロファイリングによって、膵管腺癌において異常に発現する多数のmiRNAが同定された。
【0175】
miRNAは、標的mRNAの3’非翻訳領域内の保存配列への結合後の遺伝子発現の負の調節因子として主に機能すると考えられる。miRNAの生物学的役割については、鋭意研究が行われているが、発生のタイミングおよび分化を調節することによって転写因子と類似の方法で細胞内運命を規定かつ維持すると考えられる。発育経路の変化が膵臓癌の発生において重大な役割を果たすことから、miRNA発現の変化は、膵臓腺癌の発生にとって重要な要因である場合がある。
【0176】
miRNA発現プロファイリングによって、腫瘍として、28の組織の内の28が正確に同定された(図9)。全6つの正常膵臓が正しく予測され、15の隣接良性組織の内の11が正常組織として分類された(図9)。ここで示されるデータによって、miRNA発現プロファイリングが特定の癌についての固有の分子サインを作成することができることが示される。
【0177】
腫瘍と正常組織との間に遺伝子発現の差をもたらすと考えられる3つの因子は、正常な腺房、間質および腫瘍細胞である。本発明者等は、RT in situ PCRによって、スクリーニングにおいて同定された特異に発現したmiRNAの内の上位3つが腫瘍細胞に局在していることを確認した(図11)。良性の組織の一部は、正常な膵臓とクラスターを形成することができなかった(図7)。2つのレベルの精度管理を行って腫瘍細胞を汚染したという可能性を低下させたものの、RNAが組織全体から単離されたが、顕微解剖組織からは単離されなかったことから、いくつかの腫瘍細胞が良性組織に存在して
いた可能性がある。別の可能性としては、それらの試料が腫瘍に隣接する組織から得られるので、良性組織の一部に前癌性の変化がすでに発現していたというものである。この考え方を支持するものとしては、大部分の良性試料(および慢性膵炎も)が発現地形図において正常膵臓と腫瘍との間にあるという事実がある(図8)。この観察は、miRNA発現プロファイリングによって、これらの良性組織において起きた前癌性の変化を検出できるということを示す。
【0178】
膵臓癌において特異に発現したmiRNAの一部は、他の癌において異常に発現した。これらには、miR‐155(本研究およびびまん性大細胞型B細胞リンパ腫において増加した);miR‐21(本研究ならびに膠芽細胞腫、乳癌および甲状腺乳頭癌において増加した);miR‐221(膵臓癌、膠芽細胞腫および甲状腺癌において増加した)が含まれる。miR‐221は、X染色体上のmiR‐222から約700bpに位置し;両miR‐221およびmiR‐222は、キットに結合してそれを調節すると予測される。miR‐222前駆体は、上位20位までの特異に発現したmiRNAの中になかったが、PCRによる成熟型miR‐222の次の分析は、miR‐221に類似のレベルで膵臓癌においてmiR‐222が増加したことを示した(データ未掲載)。従って、上述のmiRNAの調節解除は、癌全般に固有であってよい。他の癌において特異に発現したmiRNAは、膵臓癌と同程度には調節解除されなかった。肺癌において減少するlet‐7ファミリーは、ここでは増加した。miR‐17‐92ポリシストロン(miR‐17、‐18、‐19a、‐19b‐1および‐92‐1をコードする)の発現は、リンパ腫および結腸直腸癌において増加したが、膵臓癌においては有意な変化はなかった。本発明者等は、膵臓癌において多くのmiRNA(例えば、本発明者等の知る限りでは他の癌において報告のないmiR‐376aや、miR‐212、miR‐301、miR‐181a)の調節解除を報告する。また、ここで報告された大部分の調節解除されたmiRNAは、正常な膵臓よりも腫瘍の発現が増加したことを示すという事実も興味深い。miR‐375やmiR‐139などの多少のmiRNAは、膵臓癌における発現が低下した(表1、図12〜13)。miR‐375は、膵臓からクローニングされ、膵島細胞特異的であると考えられる(Poy MN,et al.(2004)Nature,432:226‐30)。
【0179】
(実施例2) 膵臓癌組織における成熟型miRNA発現のノーザンブロット法
実施例1において使用されたリアルタイムPCR検定によって、miRNA前駆体が定量化されるが、活性の成熟型miRNAは定量化されない。リアルタイムPCR分析において使用したのと同一のRNAについてノーザンブロット法を実施して、成熟型miRNAが前駆体miRNAと相関したかを確認した。
【0180】
3つの正常膵臓および4組の腫瘍/隣接良性組織に由来する成熟型miR‐100、mir‐375およびmiR‐155の発現レベルは、PCRによるmiRNA前駆体のレベルに近似していた(図12)。miR‐100およびmiR‐155は、上位20位までの特異に発現するmiRNAの中にあった(表1)。miR‐375は、膵臓癌における発現が低下した数少ないmiRNAの内の1つであったため、ノーザンブロット法によって確認した。miR‐375は上位20位までのmiRNAの中になかったが(表1)、前駆体および成熟型miR‐375の両方の発現は、リアルタイムPCRにより、膵臓癌において有意に減少した(p<1×10‐5)。良性および腫瘍対組織におけるmiRNA発現は、すべての例において一貫して増減したが、このことによって、腫瘍と良性との間のmiRNA発現における差は、個々の患者の組織の差によるものであって、群の平均発現の差によるものではないことを示している。
【0181】
ノーザンブロット法:ノーザンブロット法を、Lau NC,et al.(2001),Science 294:858‐62およびSchmittgen TD,et
al.(2004),Nucleic Acids Res 32:E43に既述したように実施した。成熟型miRNAに対する逆相補鎖のDNAオリゴヌクレオチドをプローブとして使用した。ブロットを首尾よくストリップし、3回まで再プローブした。
【0182】
(実施例3) 膵臓癌組織における成熟型miRNAのリアルタイムPCR
実施例1に記載されたリアルタイムPCRデータを、市販されるリアルタイムPCR検定を使用して確認し、成熟型miRNAを増幅および定量化した。成熟型miRNA発現は、PAMから、上位28位までの異常に発現したmiRNAについて確認した。以下の組織に由来するcDNAを検定した:6つの正常膵臓、16の膵臓腺癌およびPAMから正常であると予測された10の隣接良性組織。
【0183】
成熟型miRNA発現は、miRNA前駆体と高度に相関していた(図13および14)。本発明者等の知る限り、これは、感受性リアルタイムPCR検定によって判定される前駆体および成熟型miRNAの両方の発現の最初の発現である。これらの成熟型miRNAについての相対発現値が3log(0.1〜100)にわたったが、腫瘍と正常組織との間の特異な発現における傾向は存続した(図14)ことは興味深い。このことにより、miRNAは異なる発現レベルで腫瘍および正常膵臓において機能するものの、特異な発現が癌と正常組織との間で維持されることが示唆される。
【0184】
成熟型miRNAのリアルタイムPCR。成熟型miRNAを定量化する検定(すなわち、TaqMan(登録商標)マイクロRNA検定、Applied Biosystems、米国カリフォルニア州フォスターシティー)を、1つの変更を伴ってChen,C.,et al.(2005),Nucleic Acids Res 33:el79に記載された通りに実施した。28の異なるアンチセンスループRTプライマーを含む5×カクテルを、Speed Vacにおいて2×原液を濃縮することによって調製した。100ナノグラムのトータルRNAを80℃で5分間加熱し、次いで10μMの18S rRNAアンチセンスプライマーとともに60℃で5分間インキュベートし、その後室温に冷却した。次いで3マイクロリットルの5×ループプライマー混合物を添加し、cDNAを作製した。これにより、28のmiRNA cDNAと18S rRNA内部コントロールのライブラリーの作成が可能になった。リアルタイムPCR(10μLの全体の反応)を、記載された通りにcDNAの1μLの1:50希釈溶液を使用して行った。cDNAの各試料における各成熟型miRNA遺伝子について重複PCRを行った。平均CTを、重複PCRから判定した。上記の通りに遺伝子発現を18S rRNAに比べて算出し、データ提示を単純化するために106を乗算した。
【0185】
(実施例4) 膵臓腫瘍細胞におけるmiRNA前駆体のRT in situ PCR
細胞型miRNA発現を、RT in situ PCRを使用して検討した。miR‐221、miR‐376aおよびmiR‐301は、上位で特異に発現したmiRNA(表1)の中のものであり、かつ正常膵臓および膵炎よりも腫瘍および細胞株において発現が増加したことから、in situ PCRのために選択した(図7)。本発明者等は特にmiR‐376aの細胞型発現に関心があったが、それは、Poy M.N.,et al.(2004),Nature 432,226‐30において膵細胞からクローニングされたためであった。本発明者等の結果から、miR‐221およびmiR‐376aは、腫瘍細胞に局在したが、良性膵腺房または間質細胞(図11)または良性の管(図示せず)には局在しなかったことが示された。また、miR‐301は、腫瘍に局在した(データ未掲載)。
【0186】
RT in situ PCR: RT in situ PCRプロトコルを、Nuovo GJ,et al.(1999),Proc Natl Acad Sci U
SA 96,12754‐9に既述したように実施した。概略説明すると、最適プロテアーゼ消化時間は、レポーターヌクレオチドジゴキシゲニンdUTPの非特異的組み込みを使用して判定した。最適プロテアーゼ消化の後、RNアーゼフリーのDNアーゼ(1試料当たり10U、Boehringer Mannheim、米国インディアナ州インディアナポリス)における一晩のインキュベーションとrTth系およびジゴキシゲニンdUTPを使用したワンステップRT/PCRとを行った。色素原は、ニトロブルーテトラゾリウムおよび対比染色としてヌクレアファストレッドを有するブロモクロロインドリルホスフェート(NBT/BCIP)であった。miR‐221、miR‐301およびmiR‐376aの前駆体に対するプライマー配列は、実施例1におけるプロファイリングのために使用されたものと同様であった。陰性対照においては、プライマーの除外および無関係な(ヒトパピローマウイルスに特異的な)プライマーによる置換が行われたが、それはこのウイルスが膵組織に感染しないためであった。RT in situ PCRは、保存状態のホルマリン固定パラフィン包埋試料1050005A2(T)において行った(図3)。
【0187】
(実施例5) 膵臓特異的miRNAおよび膵臓濃縮miRNAの同定
正常な膵臓組織に特異的であるか、あるいは正常な膵臓組織において濃縮されるかのいずれかのmiRNAを同定するために、184の成熟型miRNAの発現を、22の正常なヒト組織におけるリアルタイムPCRを使用して測定した。これらの組織には、脂肪、膀胱、脳、子宮頚部、大腸、食道、心臓、腎臓、肝臓、肺、骨格筋、卵巣、膵臓、胎盤、前立腺、脾臓、小腸、気管、胸腺、甲状腺、精巣、および正常なB細胞が含まれる。膵臓特異的miRNAは、膵臓においては高発現で、他の21の正常組織においては発現がほとんど検出されないmiRNAと定義された。膵臓濃縮miRNAは、膵臓組織における発現が他の21の組織の平均よりも10倍以上のmiRNAと定義された。膵臓濃縮miRNAは、他の組織の一部に存在してもよい。膵臓特異的miRNAには、miR‐216やmiR‐217が含まれる。膵臓濃縮miRNAには、miR‐7、miR‐148aおよびmiR‐375が含まれる。
【0188】
【表2】

【0189】
(実施例6) 膵臓組織における成熟型miRNAのプロファイリング
膵臓癌において特異に発現するmiRNAを同定するために、9つの膵臓癌腫瘍と、膵
疾患のない6人のドナーからの膵臓とにおけるリアルタイムPCRを使用して、184の成熟型miRNAの発現を測定した。成熟型miRNAは、市販されるリアルタイムPCR検定(TaqMan(登録商標)マイクロRNA検定、Applied Biosystems、米国カリフォルニア州フォスターシティー)を使用して測定した。この検定は、実施例3で説明した通りに実施された。リアルタイムPCRデータは、ヒートマップとして示され、管理されない階層的クラスタリングを使用して解析された(図15)。多少のmiRNAの発現が15の試料のすべてにおいて検知されず、これらのmiRNAはヒートマップに含めなかった。多くの成熟型miRNAは、正常膵臓よりも膵臓腫瘍における発現が増加した。ヒートマップはまた、成熟型miRNA発現プロファイルによって、膵臓腫瘍と正常とを区別することが、その両者が樹状図の分かれた分枝として出現するために可能になることを示す。正常に比べた腫瘍における成熟型miRNA発現の倍率変化およびp値を、図16に示す。
【0190】
(実施例7) 膵臓癌細胞においてmiR‐21の発現が増加
いくつかの方法を使用して、成熟型miR‐21の発現は、膵臓腺癌細胞に局在し、膵臓の腺房、間質および他の非癌細胞には局在しなかったことを示した。(図17)in situ RT‐PCRは、正常膵臓の切片(A)および膵臓癌(B)に適用され、miR‐21の発現増加が腫瘍に局在することを示した。膵管腺癌および正常な(非癌)膵臓管を、レーザー顕微解剖を使用していくつかの検体から単離した。RNAを顕微解剖組織から単離し、次いで18S rRNA内部コントロールと同様に成熟型miR‐21をリアルタイムPCRによって定量化した。成熟型miR‐21は、正常膵臓管(C)よりも顕微解剖腫瘍組織において実質的に増加した。前に記載された通りに成熟型miRNAの市販されるリアルタイムPCR検定を使用して、膵臓腫瘍の9つの検体および6つの正常膵臓検体において、成熟型miR‐21を検定した。成熟型miR‐21発現は、腫瘍(D)において増加した。成熟型miR‐21発現を、2つの正常膵臓上皮細胞株および転移癌に由来する3つと原発性膵臓癌に由来する4つとを含む7つのヒト膵臓癌細胞株におけるリアルタイムPCRによって定量化した。成熟型miR‐21発現は、正常膵臓細胞株(E)よりも7つの膵臓癌細胞株のすべてにおいて増加した。
【背景技術】
【0001】
政府の支援に関する声明
本発明は、アメリカ合衆国のNational Institute of Healthによるグラント番号CA107435によって少なくとも部分的にサポートされる。The Ohio State UniversityのTissue Procurement Shared Resourceは、National Cancer InstituteのグラントP30 CA16058によって資金援助される。米国合衆国政府は、本発明において一定の権利を有する。
【0002】
関連出願への相互参照
本願は、2006年3月2日に出願された米国仮特許出願第60/778,271号に基づく。米国仮特許出願第60/778,271号の利益は、本明細書によって特許請求され、そしてその開示は本明細書中に参考として援用される。
【0003】
背景
膵臓癌は、米国の癌関連の死亡で4番目の主要原因である。この5年間の年間死亡率は約3万人であり、毎年診断される新症例の数とほとんど同じである。膵臓癌の予後はすべての癌の中で最悪であり、死亡率/発現率の比は0.99である。米国の膵臓癌の発現率は、10万人当たり約9人である。これらの思わしくない数字は、発現率と死亡率とが増加傾向にあることを反映しており、検出法および診断法の進歩が見られないことや、治療計画における進展が不十分であることに起因する。
【0004】
マイクロRNA(miRNA)は、広範囲にわたる種のゲノムにおいて同定されている短い非コードRNAである。miRNAは、1993年に最初にシノラディス・エレガンスにおいて発見され、その後すべての多細胞生物で発見された。miRNAは、遺伝子発現の負の調節因子であり、タンパク質コードmRNAの3’非翻訳領域内の配列との塩基対の不完全な相互作用によって主に機能すると考えられる。2006年までに326種のmiRNAがヒトにおいて発見された。これらのmiRNAのそれぞれの役割は知られていないが、特定のmiRNAは、脂肪細胞の分化や、卵母細胞の成熟、多能性細胞状態の維持、インスリン分泌の調節などの多様な細胞過程の調節に関わっていた。
【0005】
miRNAの発現の変化と癌との間の関係を示唆する直接的エビデンスおよび間接的エビデンスが増加している。これらには、慢性リンパ性白血病におけるmiR‐15aおよびmiR‐16‐1、結腸直腸癌におけるmiR‐143およびmiR‐145、肺癌におけるlet‐7、びまん性大細胞型B細胞リンパ腫におけるmiR‐155が含まれる。発現プロファイリングによって、乳癌や、膠芽細胞腫、甲状腺乳頭癌など、いくつかのmiRNAの特異的な発現を伴う他の癌が同定されてきた。5種のmiRNAをコードするポリシストロンがヒトB細胞リンパ腫で増幅され、c‐mycとのポリシストロンの強制的発現は腫瘍形成性であったが、このことはこのmiRNAの群が腫瘍遺伝子として機能することを示唆する。
【0006】
膵臓癌を確実かつ正確に診断する方法、あるいは膵臓癌の素因について個体をスクリーニングする方法が必要とされる。また、膵臓癌の治療方法も非常に望まれる。
【発明の概要】
【課題を解決するための手段】
【0007】
要旨
本発明は、膵臓腺癌において発現が変化するmiRNAの同定に一部基づく。
【0008】
従って、本発明は、被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法を包含する。本方法は、被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手順を含む。生体試料におけるmiR遺伝子産物のレベルが対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかが示される。
【0009】
特定の実施形態において、発現が変化したmiR遺伝子産物は、以下の群から選択される:MIR‐034b、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐130a‐P、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐192、MIR‐200a‐P、MIR‐204、MIR‐210、MIR‐299‐P、MIR‐302d、MIR‐337、MIR‐371、MIR‐378、MIR‐383、MIR‐422b、MIR‐423、MIR‐375、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MlR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせ。
【0010】
一実施形態において、生体試料における遺伝子産物のレベルは、対照試料におけるその対応するmiR遺伝子産物のレベルよりも低い。このような過小発現の遺伝子産物には、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR188b‐P、MIR‐204、MIR‐299‐P、MIR‐337、MIR‐371、MIR‐383、MIR‐375およびそれらの組み合わせが含まれる。
【0011】
別の実施形態において、生体試料におけるmiR遺伝子産物のレベルは、対照試料におけるその対応するmiR遺伝子産物のレベルよりも高い。このような過剰発現のmiR遺伝子産物には、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせが含まれる。
【0012】
本発明はまた、被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性
があるのかを診断する別の方法も提供する。本方法は、(a)被験体の膵臓由来の試験試料を提供する手順であって、前記試験試料が複数のmiR遺伝子産物を含む、手順;(b)試験試料におけるmiR遺伝子産物の発現レベルを検定して、試験試料のmiR発現プロファイルを得る手順;(c)試験試料のmiR発現プロファイルを、対照試料から作成された対応するmiR発現プロファイルと比較する手順を含む。試験試料のmiR発現プロファイルと対照試料のmiR発現プロファイルとの差によって、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかが示される。
【0013】
一実施形態において、複数のmiR遺伝子産物は、細胞内のmiR遺伝子の補体全長の実質部分に相当する。他の実施形態において、複数のmiR遺伝子産物は、細胞内のmiR補体全長な補体の約95%、90%、80%、70%または60%に相当する。
【0014】
別の実施形態において、複数のmiR遺伝子産物は、MIR‐139、MIR096‐P、MIR‐375、let‐7b、let‐7d、let‐7f‐1、let‐7i、MIR‐155、MIR‐181a、MIR‐212、MIR‐301、MIR‐007‐1およびMIR‐021からなる群から選択される1つ以上のmiR遺伝子産物を含む。
【0015】
前記miR遺伝子産物のレベルは、当該技術分野で周知の種々の技法を使用して測定することができる。これらの技法には、増幅に基づく検定、ハイブリダイゼーションに基づく検定およびマイクロアレイ分析が含まれる。他の実施形態において、miR遺伝子産物のレベルは、試料中の対応するmiR遺伝子コピーを測定することによって判定できる。
【0016】
被験体から得られる生体試料は、膵組織、膵腫瘍または膵臓細胞を含んでよい。また、生体試料は膵液を含むこともできる。
【0017】
本発明はまた、膵臓癌に羅患しているか、もしくは膵臓癌を発症する危険性がある被験体における膵臓癌を診断するためのキットも企図する。このようなキットは、(a)被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手段、および(b)生体試料におけるmiR遺伝子産物のレベルを、対照試料における対応するmiR遺伝子産物のレベルと比較する手段を含む。生体試料におけるmiR遺伝子産物のレベルと、対照試料における対応するmiR遺伝子産物のレベルとの間で検出された差は、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかであることを示す。
【0018】
本発明はまた、膵臓癌を発症する危険性がある被験体をスクリーニングする方法も提供する。このような方法は、被験体の膵臓から得た生体試料中の膵臓癌に関連した、少なくとも1つのmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルを評価する手順であって、生体試料におけるmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルが、対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、被験体に膵臓癌を発症する危険性があることが示される、手順を含む。
【0019】
一実施形態において、生体試料は、正常であるか、もしくは前癌性の疑いがあるかのいずれかの膵組織を含む。
【0020】
本発明はまた、対照細胞よりも多くのmiR遺伝子産物を含む膵臓癌細胞を有する被験体における膵臓癌の進行を抑制する方法も提供する。このような方法は、膵臓癌細胞内のmiR遺伝子産物の量を減少させることができる有効量の阻害剤分子を被験体に投与する手順を含む。
【0021】
いくつかの実施形態において、阻害剤分子は、アップレギュレートされたmiR遺伝子産物の転写後のサイレンシングを引き起こすか、もしくはアップレギュレートされたmiR遺伝子産物の成熟を阻害する。いくつかの実施形態において、阻害剤分子は、前記アップレギュレートされたmiR遺伝子産物のアンチセンスオリゴヌクレオチド、リボザイム、低分子干渉RNA(siRNA)、またはアップレギュレートされたmiR遺伝子産物についてコードする遺伝子とともに3重らせんを形成することができる分子である。いくつかの実施形態において、阻害剤化合物は、miR遺伝子産物プロモーターのメチル化を引き起こし、それによってmiR遺伝子の発現が低下する。
【0022】
一実施形態において、阻害剤分子は、送達剤とともに裸のRNAとして投与される。別の実施形態において、阻害剤分子は、阻害剤分子をコードする核酸として投与される。
【0023】
本発明はまた、対照細胞よりも少ないmiR遺伝子産物を含む膵臓癌細胞を有する被験体における膵臓癌の進行を抑制する方法も提供する。このような方法は、miR遺伝子産物に対応する有効量の単離されたmiR遺伝子産物を被験体に投与する手順を含む。
【0024】
一実施形態において、単離されたmiR遺伝子産物は、機能性成熟型miRである。他の実施形態において、単離されたmiR遺伝子産物は、ヘアピンのループ部を含むmiR前駆体ヘアピン配列を含むオリゴヌクレオチド、またはヘアピンを有さない2本鎖のmiR前駆体を含むオリゴヌクレオチドである。
【0025】
一実施形態において、単離された遺伝子産物は、送達剤とともに裸のRNAとして投与される。別の実施形態において、単離された遺伝子産物は、単離されたmiR遺伝子産物をコードする核酸として投与される。
【0026】
別の方法においては、癌の進行は、ダウンレギュレートされたmiR遺伝子産物のプロモーター領域の低メチル化を引き起こす化合物の投与によって抑制される。
【0027】
本発明はまた、少なくとも1つの過小発現のmiR遺伝子産物を示す被験体における膵臓癌を治療するための薬学的組成物も提供する。いくつかの実施形態において、薬学的組成物は、過小発現のmiR遺伝子産物に対応する単離されたmiR遺伝子産物と薬学的に許容される担体とを含む。他の実施形態において、薬学的組成物は、過小発現のmiR遺伝子産物をコードする少なくとも1つの核酸と薬学的に許容される担体とを含む。
【0028】
本発明はまた、少なくとも1つの過剰発現のmiR遺伝子産物を示す被験体における膵臓癌を治療するための薬学的組成物も提供する。薬学的化合物は、過剰発現のmiR遺伝子産物に特異的な少なくとも1つのmiR遺伝子阻害剤化合物と薬学的に許容される担体とを含む。
【0029】
本発明はまた、被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する方法も提供する。このような方法は、(a)対照細胞に比べてアップレギュレートされたmiR遺伝子産物を有する癌細胞を含む被験体の膵臓から第1の試験試料を得る手順;(b)被験体に治療レジメンを施す手順;(d)ある期間後に被験体の膵臓から第2の試験試料を得る手順;および(e)第1および第2の試験試料におけるアップレギュレートされたmiR遺伝子産物のレベルを比較する手順を含む。第2の試験試料におけるアップレギュレートされたmiR遺伝子産物レベルが第1の試験試料よりも低いことによって、その治療レジメンが被験体における膵臓癌の進行抑制に効果的であることが示される。
【0030】
本発明で検討される別の方法においては、被験体における膵臓癌の進行の抑制に対する治療レジメンの有効性は、(a)対照細胞に比べてアップレギュレートされたmiR遺伝
子産物を有する癌細胞を含む被験体の膵臓から第1の試験試料を得る手順;(b)被験体に治療レジメンを施す手順;(d)ある期間後に被験体の膵臓から第2の試験試料を得る手順;および(e)第1および第2の試験試料におけるアップレギュレートされたmiR遺伝子産物のレベルを比較する手順によって評価される。第2の試験試料におけるアップレギュレートされたmiR遺伝子産物レベルが第1の試験試料よりも低いことによって、その治療レジメンが被験体における膵臓癌の進行抑制に効果的であることが示される。
【0031】
本発明はまた、膵臓癌用抗癌剤を同定する方法も提供する。本方法は、(a)膵臓癌細胞を含む生体試料において過剰発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;(b)生体試料に試験剤を接触させる手順;(c)生体試料のmiR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順であって、miR遺伝子産物の試験後の発現レベルが低下することによって、試験剤が膵臓癌の抗癌性を有することが示される、手順を含む。
【0032】
本発明はまた、膵臓癌用抗癌剤を同定する方法も提供する。本方法は、(a)膵臓癌細胞を含む生体試料において過小発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;(b)生体試料に試験剤を接触させる手順;(c)手順(b)の後に生体試料のmiR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順であって、miR遺伝子産物の試験後の発現レベルが上昇することによって、試験剤が膵臓癌の抗癌性を有することが示される、手順を含む。
本発明はまた、以下の項目を提供する。
(項目1)
被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法であって、前記被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手順であって、前記生体試料における前記miR遺伝子産物のレベルが対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、前記被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかであることが示される、手順を含む、方法。
(項目2)
前記miR遺伝子産物が、MIR‐034b、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐130a‐P、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐192、MIR‐200a‐P、MIR‐204、MIR‐210、MIR‐299‐P、MIR‐302d、MIR‐337、MIR‐371、MIR‐378、MIR‐383、MIR‐422b、MIR‐423、MIR‐375、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MlR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせからなる群から選択される、項目1に記載の方法。
(項目3)
前記miR遺伝子産物が、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐098、MIR‐099a、MIR‐100、MIR‐125b‐1、MIR‐126、MIR‐132、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐218‐1,2,、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐331‐P、MIR‐345、MIR‐376およびそれらの組み合わせからなる群から選択される、項目2に記載の方法。
(項目4)
前記生体試料におけるmiR遺伝子産物のレベルが、前記対照試料におけるその対応するmiR遺伝子産物のレベルよりも低い、項目1に記載の方法。
(項目5)
前記miR遺伝子産物が、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐204、MIR‐299‐P、MIR‐337、MIR‐371、MIR‐383、MIR‐375およびそれらの組み合わせからなる群から選択される、項目4に記載の方法。
(項目6)
前記miR遺伝子産物がMIR‐139である、項目5に記載の方法。
(項目7)
前記miR遺伝子産物がMIR‐096‐Pである、項目5に記載の方法。
(項目8)
前記miR遺伝子産物がMIR‐375である、項目5に記載の方法。
(項目9)
前記生体試料における前記miR遺伝子産物のレベルが、前記対照試料におけるその対応するmiR遺伝子産物のレベルよりも高い、項目1に記載の方法。
(項目10)
前記miR遺伝子産物が、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目11)
前記miR遺伝子産物が、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐030d、MIR‐098、MIR‐099a、MIR‐100、MIR‐125b‐1、MIR‐126、MIR‐132、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐331‐P、MIR‐345、M
IR‐376およびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目12)
前記miR遺伝子産物が、let‐7b;let‐7d;let‐7f;let‐7i、MIR‐015a;MIR‐015b;MIR‐016‐1;MIR‐021;MlR‐023a、MIR‐024、MIR‐100;MIR‐125b;MIR‐132、MIR‐155、MIR‐181a、MIR‐181c;MIR‐212;MIR‐221;MIR‐301;MIR‐376aおよびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目13)
前記miR遺伝子産物が、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐015b、MIR‐019b‐1‐P、MIR‐098、MIR‐128a、MIR‐136、MIR‐152、MIR‐155、MIR‐181a、MIR‐196a‐2、MIR‐212、MIR‐215、MIR‐218‐1、MIR‐218‐2、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐424およびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目14)
前記miR遺伝子産物が、let‐7b、let‐7d、let‐7f‐1、let‐7i、MIR‐155、MIR‐181a、MIR‐212、MIR‐301およびそれらの組み合わせからなる群から選択される、項目9に記載の方法。
(項目15)
前記miR遺伝子産物がMIR‐155である、項目9に記載の方法。
(項目16)
前記miR遺伝子産物がMIR‐007‐1である、項目9に記載の方法。
(項目17)
前記miR遺伝子産物がMIR‐021である、項目9に記載の方法。
(項目18)
被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法であって、
(a)前記被験体の膵臓由来の試験試料を提供する手順であって、前記試験試料が複数のmiR遺伝子産物を含む、手順;
(b)前記試験試料における前記miR遺伝子産物の発現レベルを検定して、前記試験試料のmiR発現プロファイルを得る手順;
(c)前記試験試料の前記miR発現プロファイルを、対照試料から作成された対応するmiR発現プロファイルと比較する手順であって、前記試験試料の前記miR発現プロファイルと前記対照試料の前記miR発現プロファイルとの差によって、前記被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかが示される、手順
を含む、方法。
(項目19)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の実質部分に相当する、項目18に記載の方法。
(項目20)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約95%に相当する、項目18に記載の方法。
(項目21)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約90%に相当する、項目18に記載の方法。
(項目22)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約80%に相当する、項目18に記載の方法。
(項目23)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約70%に相当する、項目18に記載の方法。
(項目24)
前記複数のmiR遺伝子産物が、細胞内のmiR遺伝子の補体全長の約60%に相当する、項目18に記載の方法。
(項目25)
前記複数のmiR遺伝子産物が、MIR‐139、MIR096‐P、MIR‐375、let‐7b、let‐7d、let‐7f‐1、let‐7i、MIR‐155、MIR‐181a、MIR‐212、MIR‐301、MIR‐007‐1、MIR‐021およびそれらの組み合わせからなる群から選択される1つ以上のmiR遺伝子産物を含む、項目18に記載の方法。
(項目26)
前記対照試料が正常膵組織から得られる、項目1〜25に記載の方法。
(項目27)
前記試験試料が、癌または前癌性であることが疑われる膵臓の領域から得られる、項目1〜25に記載の方法。
(項目28)
前記miR遺伝子産物がmiRNA前駆体である、項目1〜25に記載の方法。
(項目29)
前記miR遺伝子産物が成熟型miRNAである、項目1〜25に記載の方法。
(項目30)
前記miR遺伝子産物のレベルが、増幅に基づく検定を使用して測定される、項目1〜29に記載の方法。
(項目31)
前記増幅に基づく検定が、ポリメラーゼ連鎖反応(PCR)、逆転写酵素ポリメラーゼ連鎖反応(RT‐PCR)、定量的RT‐PCR、リアルタイム定量的RT‐PCRおよびin situ PCRからなる群から選択される、項目30に記載の方法。
(項目32)
前記miR遺伝子産物のレベルが、ハイブリダイゼーションに基づく検定を使用して測定される、項目1〜29に記載の方法。
(項目33)
前記ハイブリダイゼーションに基づく検定が、ノーザンブロット解析、in situハイブリダイゼーション、溶液ハイブリダイゼーション、リボヌクレアーゼ防御検定、RNAマイクロアレイ分析ならびにDNAまたはcDNAマイクロアレイ分析からなる群から選択される、項目32に記載の方法。
(項目34)
前記miR遺伝子産物のレベルが、前記試料における前記対応するmiR遺伝子コピーを測定することによって判定される、項目1〜29に記載の方法。
(項目35)
前記生体試料が膵組織、膵腫瘍または膵臓細胞を含む、項目1〜34に記載の方法。
(項目36)
前記生体試料が膵液の試料を含む、項目1〜34に記載の方法。
(項目37)
膵臓癌に羅患しているか、もしくは膵臓癌を発症する危険性がある被験体における膵臓癌を診断するためのキットであって、
(a)前記被験体の膵臓由来の生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手段、および
(b)前記生体試料における前記miR遺伝子産物のレベルを、対照試料における対応するmiR遺伝子産物のレベルと比較する手段
を含み、
前記生体試料における前記miR遺伝子産物のレベルと、前記対照試料における前記対応するmiR遺伝子産物のレベルとの間で検出された差によって、前記被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれかであることが示される、
キット。
(項目38)
膵臓癌を発症する危険性がある被験体をスクリーニングする方法であって、前記被験体の膵臓から得た生体試料中の膵臓癌に関連した、少なくとも1つのmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルを評価する手順であって、前記生体試料におけるmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルが、対照試料における対応するmiR遺伝子産物のレベルに比べて変化することによって、前記被験体に膵臓癌を発症する危険性があることが示される、手順を含む、方法。
(項目39)
前記生体試料が、正常であるか、もしくは前癌性の疑いがある膵組織を含む、項目38に記載の方法。
(項目40)
対照細胞よりも多くのmiR遺伝子産物を含む膵臓癌細胞を有する被験体における膵臓癌の進行を抑制する方法であって、前記膵臓癌細胞内の前記miR遺伝子産物の量を減少させることができる有効量の阻害剤分子を前記被験体に投与する手順を含む、方法。
(項目41)
前記miR遺伝子産物が、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424およびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目42)
前記miR遺伝子産物が、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐030d、MIR‐098、MIR‐099a、MIR‐100、MIR‐125b‐1、MIR‐126、MIR‐132、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐331‐P、MIR‐345、MIR‐376およびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目43)
前記miR遺伝子産物が、let‐7b;let‐7d;let‐7f;let‐7i、MIR‐015a;MIR‐015b;MIR‐016‐1;MIR‐021;MlR
‐023a、MIR‐024、MIR‐100;MIR‐125b;MIR‐132、MIR‐155、MIR‐181a、MIR‐181c;MIR‐212;MIR‐221;MIR‐301;MIR‐376aおよびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目44)
miR遺伝子産物が、let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐015b、MIR‐019b‐1‐P、MIR‐098、MIR‐128a、MIR‐136、MIR‐152、MIR‐155、MIR‐181a、MIR‐196a‐2、MIR‐212、MIR‐215、MIR‐218‐1、MIR‐218‐2、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐424およびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目45)
前記miR遺伝子産物が、let‐7b、let‐7d、let‐7f‐1、let‐7i、MIR‐155、MIR‐181a、MIR‐212、MIR‐301およびそれらの組み合わせからなる群から選択される、項目40に記載の方法。
(項目46)
前記miR遺伝子産物がMIR‐155である、項目40に記載の方法。
(項目47)
前記miR遺伝子産物がMIR‐007‐1である、項目40に記載の方法。
(項目48)
前記miR遺伝子産物がMIR‐021である、項目40に記載の方法。
(項目49)
前記miR遺伝子産物が成熟型miRである、項目40〜48に記載の方法。
(項目50)
前記阻害剤分子が前記miR遺伝子産物の転写後のサイレンシングを引き起こす、項目40〜48に記載の方法。
(項目51)
前記阻害剤分子が前記miR遺伝子産物の成熟を阻害する、項目40〜48に記載の方法。
(項目52)
前記阻害剤分子が前記miR遺伝子産物のアンチセンスオリゴヌクレオチドである、項目40〜48に記載の方法。
(項目53)
前記阻害剤分子が低分子干渉RNA(siRNA)である、項目40〜48に記載の方法。
(項目54)
前記阻害剤分子が、前記miR遺伝子産物についてコードする遺伝子とともに3重らせんを形成することができる分子である、項目40〜48に記載の方法。
(項目55)
前記阻害剤分子がリボザイムである、項目40〜48に記載の方法。
(項目56)
前記阻害剤分子が送達剤とともに裸のRNAとして投与される、項目40〜54に記載の方法。
(項目57)
前記阻害剤分子が、前記阻害剤分子をコードする核酸として投与される、項目40〜54に記載の方法。
(項目58)
対照細胞よりも少ないmiR遺伝子産物を含む膵臓癌細胞を有する被験体における膵臓癌の進行を抑制する方法であって、前記miR遺伝子産物に対応する有効量の単離された
miR遺伝子産物を前記被験体に投与する手順を含む、方法。
(項目59)
前記miR遺伝子産物が、MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐204、MIR‐299‐P、MIR‐337、MIR‐371、MIR‐383、MIR‐375およびそれらの組み合わせからなる群から選択される、項目58に記載の方法。
(項目60)
前記miR遺伝子産物がMIR‐139である、項目58に記載の方法。
(項目61)
前記miR遺伝子産物がMIR‐096‐Pである、項目58に記載の方法。
(項目62)
前記miR遺伝子産物がMIR‐375である、項目58に記載の方法。
(項目63)
前記単離されたmiR遺伝子産物が前記機能性成熟型miRである、項目58〜62に記載の方法。
(項目64)
前記単離されたmiR遺伝子産物が、ヘアピンのループ部を含むmiR前駆体ヘアピン配列を含むオリゴヌクレオチドである、項目58〜62に記載の方法。
(項目65)
前記単離されたmiR遺伝子産物が、前記ヘアピンを有さない2本鎖のmiR前駆体を含むオリゴヌクレオチドである、項目58〜62に記載の方法。
(項目66)
前記単離された遺伝子産物が送達剤とともに裸のRNAとして投与される、項目58〜62に記載の方法。
(項目67)
前記単離された遺伝子産物が、前記単離されたmiR遺伝子産物をコードする核酸として投与される、項目58〜62に記載の方法。
(項目68)
前記核酸が組換えプラスミドまたは組換えウイルスベクターである、項目67に記載の方法。
(項目69)
項目40〜57に記載の阻害剤分子と薬学的に許容される担体とを含む、被験体における膵臓癌を治療するための薬学的組成物。
(項目70)
項目58〜66に記載の単離されたmiR遺伝子産物と薬学的に許容される担体とを含む、被験体における膵臓癌を治療するための薬学的組成物。
(項目71)
項目67〜68に記載の単離されたmiR遺伝子産物をコードする核酸と薬学的に許容される担体とを含む、被験体における膵臓癌を治療するための薬学的組成物。
(項目72)
被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する方法であって、
(a)対照細胞に比べてアップレギュレートされたmiR遺伝子産物を有する癌細胞を含む前記被験体の膵臓から第1の試験試料を得る手順;
(b)前記被験体に前記治療レジメンを施す手順;
(d)ある期間後に前記被験体の膵臓から第2の試験試料を得る手順;ならびに
(e)前記第1および前記第2の試験試料における前記アップレギュレートされたmiR遺伝子産物のレベルを比較する手順であって、前記第2の試験試料における前記アップレギュレートされたmiR遺伝子産物レベルが前記第1の試験試料よりも低いことによって、前記治療レジメンが前記被験体における膵臓癌の進行抑制に効果的であることが示さ
れる、手順
を含む、方法。
(項目73)
被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する方法であって、
(a)対照細胞に比べてダウンレギュレートされたmiR遺伝子産物を有する癌細胞を含む前記被験体の膵臓から第1の試験試料を得る手順;
(b)前記被験体に前記治療レジメンを施す手順;
(d)ある期間後に前記被験体の膵臓から第2の試験試料を得る手順;および
(e)前記第1および前記第2の試験試料における前記ダウンレギュレートされたmiR遺伝子産物のレベルを比較する手順であって、前記第2の試験試料における前記ダウンレギュレートされたmiR遺伝子産物レベルが前記第1の試験試料よりも高いことによって、前記治療レジメンが前記被験体における膵臓癌の進行抑制に効果的であることが示される、手順
を含む、方法。
(項目74)
膵臓癌用抗癌剤を同定する方法であって、
(a)膵臓癌細胞を含む生体試料において過剰発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;
(b)前記生体試料に試験剤を接触させる手順;
(c)手順(b)の後に前記生体試料における前記miR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および
(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順であって、前記miR遺伝子産物の前記試験後の発現レベルが低下することによって、前記試験剤が膵臓癌の抗癌性を有することが示される、手順
を含む、方法。
(項目75)
膵臓癌用抗癌剤を同定する方法であって、
(a)膵臓癌細胞を含む生体試料において過小発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;
(b)前記生体試料に試験剤を接触させる手順;
(c)手順(b)の後に前記生体試料における前記miR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および
(d)前記miR遺伝子産物の前記試験後の発現レベルを前記試験前の発現レベルと比較する手順であって、前記miR遺伝子産物の前記試験後の発現レベルが上昇することによって、前記試験剤が膵臓癌の抗癌性を有することが示される、手順
を含む、方法。
【図面の簡単な説明】
【0033】
【図1】miRNAプロセッシングおよびプライマー設計。ヒトmiR‐18などのmiRNAは、核酵素のDroshaによってプロセッシングされる(A)大きな一次前駆体(pri‐miRNA)として転写され、(B)推定で62ntの前駆体miRNA(pre‐miRNA)を作製する。pri‐miRNAとpre‐miRNAの両方ともヘアピン構造を含む。pre‐miRNAの下線部分は、リボヌクレアーゼのDicerによってpre‐miRNAからプロセッシングされる(C)22ntの成熟型miRNAの配列を表す。単線は前方プライマーを示し、2重線は後方プライマーを示し;破線はpri‐miRNAだけを増幅するために後方(黒)プライマーとともに使用されるセンスプライマーを示す。
【図2−1】ヒトmiR遺伝子産物配列の表。前記配列はmiRNA前駆体を表し、前駆体配列内の下線が引かれた配列は成熟型miRNAを表す。すべての配列は5’側から3’側の方向に示す。
【図2−2】ヒトmiR遺伝子産物配列の表。
【図2−3】ヒトmiR遺伝子産物配列の表。
【図2−4】ヒトmiR遺伝子産物配列の表。
【図2−5】ヒトmiR遺伝子産物配列の表。
【図2−6】ヒトmiR遺伝子産物配列の表。
【図2−7】ヒトmiR遺伝子産物配列の表。
【図2−8】ヒトmiR遺伝子産物配列の表。
【図2−9】ヒトmiR遺伝子産物配列の表。
【図2−10】ヒトmiR遺伝子産物配列の表。
【図2−11】ヒトmiR遺伝子産物配列の表。
【図2−12】ヒトmiR遺伝子産物配列の表。
【図2−13】ヒトmiR遺伝子産物配列の表。
【図2−14】ヒトmiR遺伝子産物配列の表。
【図3−1】臨床データおよび腫瘍病理。
【図3−2】臨床データおよび腫瘍病理。
【図4−1】ヒトmiRNA前駆体を増幅するために使用されるPCRプライマー。miRNA一次前駆体配列へのp,プライマー。その他すべてのプライマーは、miRNAを一次前駆体と前駆体の両方に存在するヘアピンにハイブリダイズする。
【図4−2】ヒトmiRNA前駆体を増幅するために使用されるPCRプライマー。miRNA一次前駆体配列へのp,プライマー。その他すべてのプライマーは、miRNAを一次前駆体と前駆体の両方に存在するヘアピンにハイブリダイズする。
【図4−3】ヒトmiRNA前駆体を増幅するために使用されるPCRプライマー。miRNA一次前駆体配列へのp,プライマー。その他すべてのプライマーは、miRNAを一次前駆体と前駆体の両方に存在するヘアピンにハイブリダイズする。
【図4−4】ヒトmiRNA前駆体を増幅するために使用されるPCRプライマー。miRNA一次前駆体配列へのp,プライマー。その他すべてのプライマーは、miRNAを一次前駆体と前駆体の両方に存在するヘアピンにハイブリダイズする。
【図5】膵組織内の18S rRNAの発現。18S rRNA内部コントロールの発現は、膵腫瘍、隣接する良性組織、正常な膵臓、慢性膵炎および膵臓癌の細胞株に認められる。本明細書に記載されるリアルタイムPCRを使用して判定される18S rRNA発現は、2‐CTとして示される。破線は平均値。
【図6】膵臓試料におけるmiRNA前駆体の発現のヒートマップ。A.201のmiRNA前駆体の相対的発現がリアルタイムPCRによって判定され;データは、Δ CTとして示される。管理されない階層的クラスタリングを、すべてのデータセットのサブセットにおいて実施した;データはフィルタリングされない。1に等しい発現値の中央値は黒色で;発現増加は赤色で;発現低下は緑色で;検知されない発現は灰色で示される。B.47の試料におけるmiRNA前駆体の発現パターンの階層的クラスター分析の結果を表す樹状図。試料は、原発性膵腫瘍(黄色、N=28)、正常膵組織(青、N=6)、慢性膵炎(オレンジ、N=4)および膵臓癌細胞株(トルコ玉色、N=9)を含む。
【図7】膵臓試料におけるmiRNA前駆体の発現。A.各miRNA前駆体の相対的発現がリアルタイムPCRによって判定され;データは、Δ CTとして示される。ANOVA多群比較試験によって判定される群(腫瘍、慢性膵炎、細胞株および正常組織)の中で異なって発現する(P<0.001)108の遺伝子のサブセットにおいて、管理されない階層的クラスタリングを実施した。1に等しい発現値の中央値は黒色で;発現増加は赤色で;発現低下は緑色で;検知されない発現は灰色で示される。B.47の試料におけるmiRNA前駆体の発現パターンの階層的クラスター分析の結果を表す樹状図。試料は、原発性膵腫瘍(N=28)、隣接する良性組織(N=15)、正常膵組織(N=6)、慢性膵炎(N=4)および膵臓癌細胞株(N=9)を含む。
【図8】立体的な発現地形図が該当なし7に示すフィルタリングされたmiRNA前駆体の発現データから作成された。各山は、個々の試料(腫瘍、隣接する良性、慢性的膵炎、正常な膵臓または膵臓癌細胞株)を表す。個々の山は、互いの類似性または差に基づいて小さな群に分かれる。着色された点は試料のタイプを表し、腫瘍は黄色;隣接する良性組織は青色;正常膵組織は黒色;慢性膵炎はオレンジ色;および膵臓癌細胞株はトルコ玉色である。試料の対をつなぐ線は、平均相関が閾値(>0.8)を超えるmiRNAの発現の非常に類似したパターンを有するそれらの試料を示す。
【図9】トレーニングデータおよび試験データについて推定された確率。6個の正常膵臓試料と膵腫瘍であることが知られている試料の内の18個とを含むすべてのトレーニングデータが正確に分類される(A)。15個の隣接する良性試料の内の11個と膵腫瘍であることが知られている10個の試料が試験群(B)に正確に分類される。試料は、真実のクラス(A)と予測されたクラス(B)とで分けられる。
【図10−1】上位69番目までは膵臓腺癌におけるmiRNA前駆体を異常に発現した。
【図10−2】上位69番目までは膵臓腺癌におけるmiRNA前駆体を異常に発現した。
【図10−3】上位69番目までは膵臓腺癌におけるmiRNA前駆体を異常に発現した。
【図11】マイクロRNAの発現についての膵臓癌の組織学的解析および分子解析。パネルA(400×)は、膵臓腺癌のヘマトキシリン‐エオジン分析を示す。正常な膵臓腺(小さな矢印)には、癌(大きな矢印)の不十分に形成された腺が侵入している。対応するcDNAのin situ増幅後のmiR‐221の連続切片の分析によって、腫瘍細胞の内の多くが標的配列を含むことが示され;細胞質の局在化が示される(矢印、パネルB‐400×およびそれ以上の倍率、パネルC‐1000×;シグナルは、ファストレッドで対比染色された陰性細胞を有するNBT/BCIPにより青色)。シグナルは、プライマーの除外またはHPV特異的プライマー(パネルD、400×)による置き換えのいずれかによって消失した。隣接する連続切片もまた、cDNA(E、F)のin situ増幅後に腫瘍細胞の内の多くがmiR‐376aを発現することを示した。パネルE(400×)は、陽性の腫瘍細胞(大きな矢印)と、線維形成の領域における陰性の間質細胞(小さな矢印)とを示すが、一方でパネルF(400×)は、陰性の良性の膵腺房(小さな矢印)に隣接する陽性の腫瘍細胞(大きな矢印)を示す。
【図12】ノーザンブロット法によるmiRNA発現。miR‐100、miR‐375、miR‐155およびU6RNAの発現は、膵臓癌(T)、隣接する良性組織(B)または正常膵臓(N)の組織標本において判定された。ブロットはストリップされ、次いで再プローブされた。
【図13】成熟型および前駆体miRNA発現のバリデーション。
【図14】前駆体および成熟型miRNAレベルのバリデーション。8つのmiRNAの発現が、6つの正常膵臓標本、10の隣接する良性組織および16の膵臓腺癌において確認された。miRNA前駆体の相対的発現(開いた棒)がmiRNA前駆体に対するリアルタイムPCR検定を使用して判定され、一方で成熟型miRNAの相対的発現(閉じた棒)が成熟型miRNAに対するリアルタイムPCR検定を使用して判定された。miRNA発現における平均差は、膵臓(黒色)と腫瘍(赤色)の間で有意(P<0.01(スチューデントのt検定))であった。A、let7i;B、miR‐221;C、miR‐100;D、miR‐301;E、miR‐21;F、miR‐181a,c(前駆体)およびmiR‐181a(成熟型);G、miR‐125b‐1(前駆体)およびmiR‐125b(成熟型);H、miR‐212。
【図15】膵臓試料における成熟型miRNA発現のヒートマップ。A.9つの膵臓癌の腫瘍と膵疾患のない6人のドナーからの膵臓とのリアルタイムPCRを使用して測定された184の成熟型miRNAの相対的発現。データはΔCTとして示される。管理されない階層的クラスタリングを、すべてのデータセットのサブセットにおいて実施した;データはフィルタリングされない。1に等しい発現値の中央値は黒色で;発現増加は赤色で;発現低下は緑色で;検知されない発現は灰色で示される。B.15の試料におけるmiRNA前駆体の発現パターンの階層的クラスター分析の結果を表す樹状図。
【図16】膵臓腺癌における異常発現した成熟型miRNA。
【図17】miR‐21の発現増加が腫瘍に局在化されることを示す、正常膵臓の部分(A)および膵臓癌(B)に適用したin situ RT‐PCR検定。成熟型miR‐21は、正常膵臓管よりも顕微解剖された腫瘍組織において実質的に増加した(C)。成熟型miR‐21の発現は、腫瘍において増加した(D)。また、成熟型miR‐21発現は、正常膵臓細胞株よりも、7つの膵臓癌細胞株すべてにおいて増加した(E)。
【発明を実施するための形態】
【0034】
詳細な説明
本発明は、膵臓腺癌(以下、「膵臓癌」)の被験体から得られた生体試料における発現が特定の対照試料に比べて変化した特定のマイクロRNA遺伝子産物の同定に一部基づく。本発明は、被験体が膵臓癌に罹患しているのか、もしくは膵臓癌を発症する危険性があるのかを診断する方法を包含する。本発明はまた、膵臓癌を発症する危険性があると考えられる被験体をスクリーニングする方法、膵臓癌の進行を抑制することによって膵臓癌を治療する方法、ならびにこのような治療に使用することができる薬学的化合物も提供する。また、膵臓癌を抑制する治療レジメンの有効性を判定する方法、および膵臓癌用抗癌剤を同定する方法も提供される。本発明はまた、上述の方法の実施に適切な各種キットも包含する。
【0035】
本発明を、より詳細な例を参照して説明する。これらの例は、当業者が本発明を作製および使用することができる方法を例示するものであって、特許請求の範囲に列挙されないいかなる限界も課すことなく、本発明の使用可能性および最良の形態を提供するために本明細書に記載するものである。
【0036】
本明細書で言及されるすべての刊行物、特許出願、特許、インターネットウェブページおよび他の参考文献は、全体が参考として本明細書で明示的に援用される。援用される参考文献の用語の定義が本教示内容で定められる定義と異なると思われる場合は、本教示内容で定められる定義が優先される。
【0037】
特に明記しない限り、本明細書および特許請求の範囲で使用される成分、反応条件などの量を表すすべての数値は、すべての例で「約」という用語によって修飾されると理解されるものとする。従って、そうでないことが示されない限り、以下の明細書および添付の特許請求の範囲に記載される数値パラメータは、本発明によって得られることが求められる所望の性質によって異なる場合がある近似値である。各数値パラメータは、少なくとも、そして特許請求の範囲に均等論の適用を限定しようとするものとしてではなく、有効桁数および通常の丸め方法を考慮して解釈されなければならない。
【0038】
本発明の幅広い適用範囲を示す数値範囲およびパラメータは、近似値であるが、具体例に記載される数値は可能な限り正確に報告している。しかし、いずれの数値も、それぞれの試験測定値に認められる標準偏差から必然的に生じる特定の誤差を本質的に含んでいる。本明細書全体にわたって定められるすべての数値範囲は、このようなより広い数値範囲内に含まれるすべてのより狭い数値範囲を、あたかもこのようなより狭い数値範囲がすべて本明細書で明示的に記載されているかのように包含する。
【0039】
以下の紹介は、本明細書で使用される用語の理解に有用である。以下の理論に拘束されることなく該当なし1を参照すると、マイクロRNA(または「miRNA」)は、単一
のまたはクラスター形成されたmiRNA前駆体に転写されるmiR遺伝子によってコードされると考えられる。
【0040】
本明細書で交換可能に使用される「miR遺伝子産物」、「マイクロRNA」または「miRNA」は、miR遺伝子からのプロセッシングされていないまたはプロセッシングされたRNA転写物を指す。プロセッシングされていないmiR遺伝子転写物はまた、「miRNA前駆体」とも称される。図1に示す通り、これらのmiRNA前駆体は、段階的なプロセッシングによってmiRNAの成熟形に変わる。このプロセッシングは、まず(A)大きな一次前駆体または「pri‐miRNA」を産生し、これが次いで核酵素のDroshaによってプロセッシングされ、(B)推定前駆体または「pre‐miRNA」を産生すると考えられる。pre‐miRNAは、通常50〜90ヌクレオチド(nt)を、具体的には60〜80ntを有する。本明細書で使用される「miRNA前駆体」または「プロセッシングされていない」miRNAという用語は、pri‐miRNAおよびpre‐miRNAの両方を示し該当なし1における分子Aおよび/またはBを指す。活性の19〜25nt成熟型miRNAは、リボヌクレアーゼのDicerによってpre‐miRNAからプロセッシングされる。図1におけるpre‐miRNA配列の下線部分は、「プロセッシングされた」miR遺伝子転写物とも称される成熟型miRNAの配列を表し該当なし1の分子Cとして示される。
【0041】
活性または成熟型のmiRNA分子は、天然のプロセッシング経路を介して(例えば、無傷細胞や細胞溶解液を使用して)または合成プロセッシング経路によって(例えば、単離されたDicerやArgonaut、RNAアーゼIIIなどの単離されたプロセッシング酵素を使用して)miRNA前駆体から得ることができる。但し、活性の19〜25個のヌクレオチドRNA分子はまた、miR前駆体からプロセッシングされることなく、生物学的または化学的な合成によって直接産生できることが理解される。
【0042】
さらに図1を参照すると、pri‐miRNA分子およびpre‐miRNA分子はいずれも特徴的な「ヘアピン配列」を有している。この配列は、前半部分が少なくとも部分的にその後半部分に対して相補的であるオリゴヌクレオチド配列であって、それによりその半分の部分をそれ自体の上に折り畳み、「ヘアピン構造」を形成する。ヘアピン構造は該当なし1に示す通り、通常は、相補配列または部分的相補配列からなる「幹」部分、および幹部分の2つの相補鎖の間に位置する領域である「ループ」部分で構成される。
【0043】
本明細書で使用される「miR遺伝子発現」という用語は、miR遺伝子からmiR遺伝子産物を産生することを指し、成熟型miRNA遺伝子産物にmiR前駆体をプロセッシングすることを包含する。
【0044】
標的miR遺伝子産物のレベルは、被験体から得られる生体試料において測定される。例えば、生体試料は、膵臓癌を有することが疑われる被験体から切除することができる。このような生体試料は、前癌性または癌であることが疑われる膵臓の領域から得られる組織または細胞の生検材料を含んでよい。あるいは、生体試料は、膵臓の刺激後に抽出される膵液を含んでよい。別の例では、血液試料を被験体から採取することができる。膵液試料の使用については、例えば、内容が本明細書で援用される、Fukushima,N.,et al.,(2003),Cancer Biol Ther.2:78‐83;Rosty,C. et al.(2002),Hematol Oncol Clin
North Am.16:37‐52;Matsubayashi,H.,et al.,(2005),Clinical Cancer Research 11:573‐583;およびGrφnburg,M.,et al.,(2004)Journal
of Proteome Research,3(5),1042‐1055に記載の通り、当該技術分野で既知である。対応する対照試料は、被験体の影響を受けていない膵
組織から、すなわち正常被験体または正常被験体群から得ることができる。次いで、対照試料は、被験体の試料において特定のmiR遺伝子から産生されたmiR遺伝子産物のレベルを、対照試料由来の対応するmiR遺伝子産物レベルと比較できるように、被験体由来の試験試料とともにプロセッシングされる。
【0045】
本明細書で使用される「被験体」という用語は、生体試料がmiR遺伝子産物を含むいずれの動物をも包含する。動物は哺乳類であってよく、イヌやネコなどの愛玩動物;ウシや、ウマ、ヒツジなどの家畜;ラットや、マウス、ウサギなどの実験動物;およびサルやヒトなどの霊長類を包含してよい。一実施形態において、哺乳類はヒトまたはマウスである。
【0046】
対照試料における対応するmiR遺伝子産物のレベルに比べた、被験体から得られる試料におけるmiR遺伝子産物のレベルの変化(すなわち上昇または低下)によって、被験体において膵臓癌が存在することが示される。いくつかの実施形態において、試験試料における標的miR遺伝子産物のレベルは、対照試料における対応するmiR遺伝子産物のレベルよりも高い(すなわち、miR遺伝子産物の発現が「アップレギュレート」されるか、またはmiR遺伝子産物が「過剰発現」する)。本明細書で使用される通り、被験体由来の試験試料のmiR遺伝子産物の量が対照試料における同じ遺伝子産物の量よりも多い場合、miR遺伝子産物の発現は「アップレギュレート」される。
【0047】
いくつかの実施形態において、アップレギュレートされたmiR遺伝子産物は、以下の1つ以上を含む:let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MIR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424。
【0048】
他の実施形態において、試験試料における標的miR遺伝子産物のレベルは、対照試料における対応するmiR遺伝子産物のレベルよりも低い(すなわち、miR遺伝子産物の発現が「ダウンレギュレート」されるか、またはmiR遺伝子産物が「過小発現」する)。本明細書で使用される通り、被験体由来の試験試料におけるmiR遺伝子産物の量が対照試料における同じ遺伝子産物の量よりも少ない場合、miR遺伝子の発現は「ダウンレギュレート」される。対照試料における相対的なmiR遺伝子の発現は、1つ以上のRNA発現基準に対して判定することができる。これらの基準は、例えば、正常な対照群についてすでに得られたmiR遺伝子発現の平均レベルを含んでよい。
【0049】
いくつかの実施形態において、ダウンレギュレートされたmiR遺伝子産物は、以下の1つ以上を含む:MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐204、MIR‐299‐P、MIR‐337、MIR‐371、MIR‐383、MIR‐375。
【0050】
複数のmiR遺伝子産物が膵臓癌と関連していることから、膵臓癌は、列挙したmiR遺伝子産物のいずれか1つを評価することによって、または測定の際に膵臓癌の症状を示
す列挙したmiR遺伝子産物のいずれかの組み合わせを評価することによって、診断することができると理解される。いくつかの例においては、膵臓腺癌に固有に関連するmiR遺伝子産物が評価される。
【0051】
膵臓癌に関連するmiR遺伝子産物のレベルの変化は、被験体の細胞における形質転換されたまたは腫瘍性の表現型の発現の前または発現の初期段階に検出することができる。そのため、本発明はまた、膵臓癌を発症する危険性がある被験体をスクリーニングする方法であって、被験体の膵臓から得た生体試料において膵臓癌に関連する少なくとも1つのmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルを評価する手順を含む、方法も提供する。従って、生体試料におけるmiR遺伝子産物またはmiR遺伝子産物の組み合わせのレベルが、対照試料における対応するmiR遺伝子産物のレベルに比べて変化することは、被験体に膵臓癌を発症する危険性があることを示す。このようなスクリーニングのために使用される生体試料は、正常であるかまたは前癌性であることが疑われるかのいずれかの膵組織を含んでよい。膵臓癌に関連する1つ以上のmiR遺伝子産物のレベルが変化した被験体は、さらなるモニタリングおよび試験の候補者である。このようなさらなる試験は、組織試料の組織学的検査または当該技術分野の範囲内に含まれる他の技法を含んでよい。
【0052】
本明細書で使用される「標的ヌクレオチド配列」または「標的ヌクレオチド」という用語は、検出されることが求められるポリヌクレオチド配列を指す。標的ヌクレオチド配列は、DNA(例えばcDNAまたはゲノムDNA)、RNA、ヌクレオチド類似体を使用して生成されたDNAまたはRNAの類似体、ならびにそれらの誘導体、フラグメントおよび同族体を含むものとして意図される。
【0053】
試料におけるmiR遺伝子産物のレベルは、生体試料におけるRNA発現レベルを検出するのに適切ないずれかの技法を使用して測定することができる。生体試料におけるRNA発現レベルを判定するのに適切な技法には、増幅に基づく検定やハイブリダイゼーションに基づく検定が含まれる。
【0054】
増幅に基づく検定では、増幅反応(例えば、ポリメラーゼ連鎖反応またはPCR)における鋳型として、miR遺伝子産物の核酸配列またはmiR遺伝子を使用する。miR遺伝子転写物の相対数はまた、miR遺伝子転写物の逆転写の後、ポリメラーゼ連鎖反応(RT‐PCR)によって逆転写された転写物の増幅によって判定することもできる。miR遺伝子転写物のレベルは、内部標準、例えば同じ試料内に存在する「ハウスキーピング」遺伝子由来のmRNAのレベルと比較して定量化することができる。内部標準として使用するのに適切な「ハウスキーピング」遺伝子には、例えば、18S rRNA、ミオシン、またはグリセルアルデヒド‐3‐リン酸脱水素酵素(G3PDH)が含まれる。定量的増幅では、増幅産物の量が、元の試料における鋳型の量と比例する。TaqManプローブを使用するリアルタイム定量的PCRまたはRT‐PCRの方法は、当該技術分野で周知であり、例えば、Heid et al.1996,Real time quantitative PCR,Genome Res.,10:986‐994;およびGibson et al.,1996,A novel method for real time quantitative RT‐PCR,Genome Res.10:995‐1001に記載されている。癌と相関するすべての既知のmiR遺伝子の転写物の発現レベルを判定することができる定量的リアルタイムRT‐PCR法は、全体が参考として本明細書で援用される、Jiang,J.,et al.(2005),Nucleic Acids Res.33,5394‐5403;Schmittgen T.D.,et al.(2004),Nucleic Acids Res.32,E43;および2005年2月24日出願の米国仮出願第60/656,109号に記載されている。miRNA検出のための増幅に基づく検定の他の例は、当該技術分野で周知であ
り、例えば、全体が参考として本明細書で援用される、米国特許出願第2006/0078924号の説明を参照されたい。
【0055】
ハイブリダイゼーションに基づく検定はまた、試料におけるmiR遺伝子産物のレベルを検出するために使用することもできる。これらの検定には、例えば、ノーザンブロット解析、in situハイブリダイゼーション、溶液ハイブリダイゼーション、およびRNアーゼ保護検定(Ma YJ,et al.(1996)RNase protection assay,Methods,10273‐8)が含まれ、当業者に周知である。
【0056】
本明細書で使用される「ハイブリダイゼーション」という用語は、2重らせん、3重らせんまたは他の高次構造の形成をもたらす核酸同士の相補的塩基対合相互作用を指し、本明細書において「アニーリング」と交換可能に使用される。通常、一次相互反応は、ワトソン/クリックおよびフーグスティーン型水素結合によって塩基特異的(例えばA/TおよびG/C)である。また、塩基スタッキングおよび疎水性相互作用はまた、2重らせんの安定性にも寄与する可能性がある。相補的および実質的に相補的な標的配列に対する検出用プローブおよびプライマーをハイブリダイズさせる条件は、例えば、Nucleic
Acid Hybridization,A Practical Approach,B. Hames and S. Higgins,eds.,IRL Press,Washington,D.C.(1985)などに記載される通り、周知である。一般的に、このようなアニーリングが起こるかどうかは、とりわけ、ポリヌクレオチドおよび相補形の長さ、pH、温度、1価および2価の陽イオンの存在、ハイブリダイズ領域におけるGヌクレオチドとCヌクレオチドの割合、培地の粘度、ならびに変性剤の存在に影響される。このような変数は、ハイブリダイゼーションに必要な時間に影響を及ぼす。従って、好ましいアニーリング条件は特定の用途により異なる。しかし、このような条件は、過度の実験を行うことなく当業者により慣例的に判定することができる。相補性は完全である必要がなく、標的配列と本教示内容の1本鎖核酸との間のハイブリダイゼーションの最小限の妨げとなる塩基対ミスマッチが少数存在する可能性があることが理解されるであろう。しかし、塩基対ミスマッチの数が、最小限のストリンジェントな条件下でもハイブリダイゼーションが行われないほどに多い場合、配列は一般的に相補的な標的配列でない。従って、本明細書における相補性とは、プローブまたはプライマーが、本教示内容の目的を達成するために選択された反応条件下でハイブリダイズする上で、標的配列に対して十分に相補的であることを意味する。
【0057】
生体試料における特定の遺伝子のRNA転写物のレベルを判定するのに適切な技法は、ノーザンブロット法である。例えば、トータル細胞RNAは、核酸抽出緩衝剤の存在下でホモジナイゼーションを行った後、遠心分離することによって細胞から精製することができる。核酸を析出させた後、DNAをDNアーゼによる処理と析出とによって除去する。次いでRNA分子を、標準的技法に従ってアガロースゲル上のゲル電気泳動によって分離し、ニトロセルロースフィルターに移す。次いでRNAを加熱によってフィルター上に固定する。特異的RNAの検出および定量化は、当該のRNAに相補的な適切に標識されたDNAまたはRNAプローブを使用して達成される。例えば、開示内容全体が参考として本明細書で援用される、Molecular Cloning:A Laboratory Manual,J.Sambrook et al.,eds.,2nd edition,Cold Spring Harbor Laboratory Press,1989,Chapter 7を参照されたい。
【0058】
特定のmiR遺伝子産物のノーザンブロットハイブリダイゼーションに適切なプローブは該当なし2で示される核酸配列、あるいは、例えば、(http://www.sanger.ac.uk/Software/Rfarn/mirna/index.sht
ml)(Griffiths‐Jones,S.,The micro‐RNA Registry.Nucleic Acids Res,2004.32(1):p.D109‐11)におけるmiRNAレジストリにおいて入手可能な既知のmiRNA種の公表された配列から産生することができる。標識DNAおよびRNAプローブの調製方法、ならびに標的ヌクレオチド配列にこれらをハイブリダイズする条件は、当該技術分野で既知であり、例えば、開示内容が参考として本明細書で援用される、Molecular Cloning:A Laboratory Manual,J.Sambrook et
al.,eds.,2nd edition,Cold Spring Harbor
Laboratory Press,1989,Chapters 10 and 11に記載されている。
【0059】
RNA転写物のレベルの判定は、ノーザンおよび他のRNAハイブリダイゼーション法のほかに、in situハイブリダイゼーション法を使用して達成することができる。この技法は、必要とする細胞がノーザンブロット法よりも少なく、顕微鏡カバーガラスまたはスライド上に細胞全体を置いて、放射性プローブまたは他の標識核酸(例えば、cDNAまたはRNA)プローブを含む溶液で細胞の核酸含有量を調べる手順を伴う。この技法は、被験体由来の組織生検試料の解析に特に適している。in situハイブリダイゼーション法の実施については、開示内容全体が参考として本明細書で援用される、米国特許第5,427,916号に詳述されている。上記の通り、特定のmiR遺伝子産物のin situハイブリダイゼーションに適切なプローブは、図2で示される核酸配列から産生することができる。
【0060】
試料における複数のmiR遺伝子産物の発現レベルを同時に測定するのに適切な技法は、高処理のマイクロアレイに基づく方法である。このような技法を使用して、例えば、癌と相関するすべての既知のmiR遺伝子の転写物の発現レベルを判定する場合がある。このような方法は、1組のmiR遺伝子に特異的な1組のプローブオリゴヌクレオチドを含むマイクロチップフォーマット(すなわち、マイクロアレイ)において、オリゴライブラリーを作成する手順を伴う。このようなマイクロアレイを使用して、生体試料における複数のマイクロRNAの発現レベルは、RNAを逆転写して1組の標的オリゴヌクレオチドを生成し、それらの標的オリゴヌクレオチドをマイクロアレイ上のプローブオリゴヌクレオチドにハイブリダイズして、ハイブリダイゼーションプロファイルまたは発現プロファイルを作成することにより、判定される。次いで、試験試料のハイブリダイゼーションプロファイルを対照試料のハイブリダイゼーションプロファイルと比較し、どのマイクロRNAにおいて膵臓癌または前癌性の細胞における発現レベルが変化したのかを判定することができる。一例として、オリゴライブラリーは、ヒトゲノム由来のすべての既知のmiRに対応するプローブを含む。マイクロアレイは、miRNAが発見されるにつれてさらなるmiRNAを含むように拡大される場合がある。このアレイは、各miRNAに対して2種類異の異なるオリゴヌクレオチドプローブを含み、1つは成熟型miRの活性配列を含むプローブであり、もう1つはmiR前駆体に特異的なプローブである。このアレイはまた、ハイブリダイゼーションの厳密性条件のために対照を含む場合もある。miRNAsを検出するためのマイクロアレイ法の例は、内容が参考として本明細書で援用される、米国特許出願第2005/0277139号に記載されている。
【0061】
miR遺伝子産物のレベルはまた、miR遺伝子産物をコードするmiR遺伝子のコピー数を検出する検定を使用して判定することもできる。腫瘍において増幅を受けたmiR遺伝子の存在は、miR遺伝子のコピー数、すなわちmiR遺伝子産物をコードする細胞内のDNA配列の数を判定することによって評価される。一般的に、正常2倍体細胞は、特定の常染色体遺伝子のコピーを2つ有する。しかし、コピー数は、例えば癌細胞において、遺伝子増幅または複製によって増加させることもできれば、欠失によって減少させることもできる。特定の遺伝子のコピー数を評価する方法は、当該技術分野で周知であり、
とりわけ、ハイブリダイゼーションに基づく検定および増幅に基づく検定を含む。
【0062】
いくつかのハイブリダイゼーションに基づく検定のいずれを使用しても、生体試料の細胞におけるmiR遺伝子のコピー数を検出することができる。このような方法の1つがサザンブロット分析であり(Ausubel,et al.,Eds.,Current Protocols in Molecular Biology,Greene Publishing and Wiley‐Interscience,New York,1995;Sambrook et al.,Molecular Cloning,A Laboratory Manual 2d Ed.を参照)、この分析において、ゲノムDNAは通常断片化され、電気泳動により分離され、膜に転写された後、miR遺伝子特異的プローブにハイブリダイズされる。標的領域のプローブのハイブリダイゼーションシグナルの強度と、同じゲノムにおける正常な非増幅、単一コピーゲノムDNAの領域の対照プローブのシグナルとの比較によって、使用する特異的なプローブに対応する相対的miR遺伝子コピー数の推定値が得られる。対照よりもシグナルが増加していれば、増幅の存在が示される。
【0063】
試料中のmiR遺伝子のコピー数を判定する方法は、例えば、蛍光in situハイブリダイゼーション(FISH)などのin situハイブリダイゼーションである(Angerer,1987 Meth.Enzymol.,152:649を参照)。一般的に、in situハイブリダイゼーションは、以下の主な手順を含む:(1)解析する組織または生体構造の固定;(2)標的DNAのアクセシビリティの向上および非特異的結合の減少のための生体構造のプレハイブリダイゼーション処理;(3)生体構造内または組織内の核酸への核酸混合物のハイブリダイゼーション;(4)ハイブリダイゼーション非結合していない核酸フラグメントを除去するハイブリダイゼーション後洗浄、および(5)ハイブリダイズされた核酸フラグメントの検出。このような用途で使用されるプローブは、通常、例えば、放射性同位体または蛍光レポーターによって標識される。適切なプローブは、例えば約50、100または200ヌクレオチドから約1000以上のヌクレオチドと十分に長く、ストリンジェントの条件下で標的核酸による特異的なハイブリダイゼーションを可能にする。
【0064】
DNAコピーの数を判定するための別の代替の方法は、比較ゲノムハイブリダイゼーション(CGH)である。比較ゲノムハイブリダイゼーション法では、核酸の「試験」回収物が第1の標識によって標識され、第2の回収物(例えば、正常細胞または組織由来のもの)は第2の標識によって標識される。核酸のハイブリダイゼーションの比率は、アレイにおける各ファイバーに結合する第1および第2の標識の比率によって判定される。例えば、試験回収物における遺伝子増幅による2つの標識からのシグナルの比率の差が検出され、この比率によって、使用される特異的プローブに対応するmiR遺伝子コピー数の測定値が得られる。DNAコピー数の変化の細胞遺伝学的表現はCGHによって作成することができ、これにより、特異的に標識された試験および参照ゲノムDNAに由来する染色体の長さに沿って蛍光比が得られる。
【0065】
本発明の方法による使用に適したハイブリダイゼーションプロトコルは、例えば、Albertson(1984)EMBO J.3:1227‐1234;Pinkel(1988)Proc.Natl.Acad.Sci.USA,85:9138‐9142;EPO Pub.No.430:402;Methods in Molecular Biology,Vol.33:In Situ Hybridization Protocols,Choo,ed.,Humana Press,Totowa,N.J.(1994)に記載されている。
【0066】
また、増幅に基づく検定を使用して、miR遺伝子のコピー数を測定することもできる
。このような検定において、対応するmiR核酸配列は、増幅反応(例えば、PCR)の鋳型の役割を果たす。定量的増幅では、増幅産物の量が元の試料における鋳型の量に比例する。適切な対照に対する比較により、上で考察した原理に従って、使用される特異的プローブに対応するmiR遺伝子のコピー数の指標が得られる。TaqManプローブを使用したリアルタイム定量的PCRの方法は、当該技術分野で周知である。リアルタイム定量的PCRの詳細なプロトコルは、例えば、Heid et al.,1996,Real time quantitative PCR.Genome Res.,10:986‐994に示されている。
【0067】
また、TaqManに基づく検定を使用して、miRポリヌクレオチドを定量化することもできる。TaqManに基づく検定では、5’蛍光色素および3’消光剤を含む蛍光発生オリゴヌクレオチドプローブが使用される。このプローブはPCR産物にハイブリダイズするが、3’末端における遮断剤によりそれ自体は伸長することができない。次のサイクルでPCR産物が増幅されると、ポリメラーゼ(例えば、AmpliTaq)の5’ヌクレアーゼ活性は、TaqManプローブの開裂をもたらす。この開裂によって、5’蛍光色素と3’消光剤とが分離し、それによって増幅の機能として蛍光が増大する(例えば、http://www2.perkin‐elmer.comを参照)。
【0068】
適切な増幅方法の他の例には、リガーゼ連鎖反応(LCR)(Wu and Wallace,Genomics,4:560,1989;Landegren et al.,Science,241:1077,1988;およびBarringer et al.,Gene,89:117,1990)、転写増幅(Kwoh et al.,Proc.Natl.Acad.Sci.USA,86:1173,1989)、自立配列複製(Guatelli et al.,Proc Nat Acad Sci,USA 87:1874,1990)、ドットPCR、およびリンカーアダプターPCRが含まれるが、これらに限定されない。
【0069】
DNAコピー数を判定する1つの効果的な方法は、マイクロアレイに基づくプラットフォームを使用する。マイクロアレイ技術は、高分解能が得られるため、使用される場合がある。例えば、伝統的なCGHのマッピング分解能は一般的に20Mbと限られているのに対して、マイクロアレイに基づくCGHでは、特異的に標識された試験および参照ゲノムDNAの蛍光比によって、遺伝子座ごとのDNAコピー数の変化の指標が得られ、それによりマッピング分解能の向上が達成される。各種のマイクロアレイ方法の詳細については、文献に記載されている。例えば、米国特許第6,232,068号;Pollack
et al.,Nat.Genet.,23(1):41‐6,(1999)などを参照されたい。
【0070】
本明細書で使用される「プローブオリゴヌクレオチド」とは、標的オリゴヌクレオチドにハイブリダイズすることができるオリゴヌクレオチドを指す。「標的オリゴヌクレオチド」とは、(例えばハイブリダイゼーションを介して)検出する分子または配列を指す。「miR特異的プローブオリゴヌクレオチド」または「miRに特異的なプローブオリゴヌクレオチド」とは、特異的miR遺伝子産物に、または特異的なmiR遺伝子産物の逆転写物にハイブリダイズするように選択された配列を有するプローブオリゴヌクレオチドを意味する。
【0071】
特定の試料の「発現プロファイル」または「ハイブリダイゼーションプロファイル」は、本質的には試料の状態のフィンガープリントであり、2つの状態にはいずれかの特定の遺伝子が同じように発現されている場合があり、いくつかの遺伝子の評価によって、細胞の状態に固有の遺伝子発現プロファイルの作成が同時に可能となる。すなわち、正常組織は、膵臓癌組織、膵炎組織、あるいは癌組織に隣接した被験体の膵臓の非癌性部位から得
られる「良性組織」と区別される場合がある。異なる状態の膵組織の発現プロファイルを比較することによって、これらの状態のそれぞれにおいてどの遺伝子が重要であるのか(遺伝子のアップレギュレーションおよびダウンレギュレーションの両方を含む)に関する情報が得られる。この情報の使用は、膵臓癌組織または正常膵組織に特異的に発現される配列の同定、ならびに異なる予後の転帰をもたらす特異な発現によって、いくつかの方法で可能となる。例えば、特定の治療レジメンは、(例えば、特定の患者の長期の予後を改善するように化学療法薬が作用するかどうかを判定するために)評価される場合がある。同様に、診断は、患者の試料を既知の発現プロファイルと比較することにより実施または確認される場合がある。さらに、これらの遺伝子発現プロファイル(または個体遺伝子)によって、膵臓癌発現プロファイルを抑制するかもしくは予後不良プロファイルを予後良好プロファイルに変える候補薬のスクリーニングが可能となる。
【0072】
従って、検出するmiR遺伝子産物の標的ヌクレオチド配列は、(a)成熟型miRNAの一部またはすべての配列;(b)miRNA前駆体の一部またはすべてのヘアピン配列;または(c)pri‐miRNAの一部またはすべての配列;(d)配列(a)〜(c)の補体;または(f)配列(a)〜(d)に実質的に同一である配列、であってよい。(図1を参照)。実質的に同一の核酸は、標的配列に対して80%、85%、90%、95%、97%、98%または99%超の配列同一性を有する。
【0073】
本発明の一例において、miR遺伝子産物のレベルは、ヒト膵組織または膵臓細胞の生検材料におけるmiRNA前駆体を測定することによって検出される。201の測定されたmiR遺伝子産物の配列を、図2に示す。本明細書における核酸配列はすべて、5’側から3’側の方向で得られる。さらに、遺伝子はイタリック体で表し、遺伝子産物は通常体で表す。例えば、mir‐17は遺伝子であり、miR‐17は遺伝子産物である。ヒトmiRNA前駆体を増幅するために使用されるプライマーを、図4に示す。
【0074】
別の例において、miR遺伝子産物のレベルは、ヒト膵臓癌または良性組織の生検材料における成熟型miRNAを測定することによって検出される。測定された成熟型miR遺伝子産物の配列を、図13および図16に示す。
【0075】
別の例において、活性の成熟型miRNAiの発現は、ノーザンブロット法を使用して評価される。
【0076】
別の例において、逆転写in situ PCRを使用して膵臓腫瘍細胞に対して最も特異的に発現したmiRNAの内の3つを局在化させる。
【0077】
また、膵臓癌に罹患しているか、もしくは膵臓癌を発症する危険性があることが疑われる被験体の膵臓癌を診断するためのキットも検討される。このようなキットは、(a)被験体の膵臓に由来する生体試料における少なくとも1つのmiR遺伝子産物のレベルを測定する手段、および(b)生体試料におけるmiR遺伝子産物のレベルを、対照試料における対応するmiR遺伝子産物のレベルと比較する手段を含む。従って、生体試料におけるmiR遺伝子産物のレベルと、対照試料における対応するmiR遺伝子産物のレベルとの間で検出された差によって、被験体が膵臓癌に羅患していることか、もしくは膵臓癌を発症する危険性があることのいずれが示される。
【0078】
被験体が膵臓癌に羅患しているのか、もしくは膵臓癌を発症する危険性があるのかの診断に加えて、本発明は、膵臓癌特異的miR遺伝子産物の発現が変化した被験体を治療する方法を検討する。いかなる理論によっても縛られることを望まないが、細胞内の1つ以上のmiR遺伝子産物のレベルの変化は、癌の形成を生じる可能性があるこれらのmiRに対する1つ以上の標的の調節解除をもたらす可能性がある。そのため、(例えば、癌細
胞においてアップレギュレートされたmiR遺伝子産物のレベルを低下させることにより、および/または癌細胞においてダウンレギュレートされたmiR遺伝子産物のレベルを上昇させることにより)癌特異的miR遺伝子産物のレベルを変化させることによって、膵臓癌の治療を成功させることができる。
【0079】
従って、本発明は、被験体における膵臓癌を治療する方法であって、少なくとも1つの膵臓癌特異的miR遺伝子産物が、被験体の癌細胞において調節解除(例えば、ダウンレギュレート、アップレギュレート)される、方法を包含する。miR遺伝子産物が膵臓癌細胞においてダウンレギュレートされる場合、本方法は、被験体における癌の進行が抑制されるように有効量のmiR遺伝子産物を投与する手順を含む。miR遺伝子産物が癌細胞においてアップレギュレートされる場合、本方法は、被験体における癌の進行が抑制されるように、アップレギュレートされたmiR遺伝子の発現を抑制するための有効量の少なくとも1つの化合物(本明細書において、miR遺伝子発現抑制化合物と称される)を被験体に投与する手順を含む。
【0080】
癌の「進行の抑制」または癌の「治療」という用語は、癌の形成、発現または成長の阻止または緩慢化、ならびに侵襲および/または転移を包含する癌症状の消失または軽減を意味する。このような治療は、癌細胞のさらなる分化をもたらすことを含む。
【0081】
本明細書で使用される通り、単離されたmiR遺伝子産物の「有効量」とは、膵臓癌を患っている被験体における癌の進行を抑制するのに十分な量のことである。当業者は、因子(例えば、被験体のサイズおよび重量;疾患の浸透度;被験体の年齢、健康および性別;投与経路;投与が局所的であるか全身性であるか)を考慮することによって、特定の被験体に投与するmiR遺伝子産物の有効量を容易に判定することができる。
【0082】
例えば、単離されたmiR遺伝子産物の有効量は、治療する腫瘤の近似の重量に基づいてよい。腫瘤の近似の重量は、腫瘤の近似の体積を算出することによって判定することができるが、ここで1立方センチメートルの体積はおよそ1グラムに相当する。腫瘤の重量に基づく単離されたmiR遺伝子産物の有効量は、腫瘤1グラム当たり約10〜500マイクログラムであってよい。特定の実施形態において、腫瘤は、腫瘤1グラム当たり少なくとも約10マイクログラム、腫瘤1グラム当たり少なくとも約60マイクログラム、または腫瘤1グラム当たり少なくとも約100マイクログラムであってよい。
【0083】
単離されたmiR遺伝子産物の有効量はまた、治療する被験体の近似または推定の体重に基づいてもよい。本明細書に記載の通り、このような有効量は、非経口的または経腸的に投与することができる。
【0084】
当業者はまた、特定の被験体に単離されたmiR遺伝子産物を投与するための適切な投与計画を容易に判定することもできる。例えば、miR遺伝子産物は、被験体に1回投与することができる(例えば、単回注射または沈殿として)。あるいは、miR遺伝子産物は、数日から数カ月の期間、特に約3日間から約28日間、とりわけ約7日間から約10日間、1日1回または1日2回、被験体に投与することができる。特定の投与計画において、miR遺伝子産物は、1日1回、7日間投与される。投与計画が反復投与を含む場合、被験体に投与されるmiR遺伝子産物の有効量は、すべての投与計画を通じて投与される遺伝子産物の総量を含んでよいものと理解される。
【0085】
本明細書で使用される、「単離」されたmiR遺伝子産物は、合成されたものか、もしくは人の介入によって自然状態から変化または取り出されたものである。例えば、合成のmiR遺伝子産物、あるいはその自然状態の共存材料から部分的または完全に分離されたmiR遺伝子産物は、「単離」されたと判断される。単離されたmiR遺伝子産物は、実
質的に精製された形態で存在することができるか、もしくはmiR遺伝子産物が送達された細胞内に存在することができる。
【0086】
単離された遺伝子産物は、機能性成熟型miR遺伝子産物を含むオリゴヌクレオチド、ヘアピンのループ部を含むmiR前駆体の短いヘアピンを含むオリゴヌクレオチド、ヘアピンを有さない2本鎖のmiR前駆体、またはこのような分子を発現するベクターであってよい。従って、慎重に細胞内に送達または発現されるmiR遺伝子産物は、「単離」されたmiR遺伝子産物と判断される。また、miR前駆体分子から細胞内部で産生されたmiR遺伝子産物は、「単離」された分子であると判断される。
【0087】
いくつかの態様において、単離されたmiR遺伝子産物は、以下の内の1つ以上を含む:MIR‐092‐2‐P、MIR‐096‐P、MIR‐129‐2、MIR‐133b、MIR‐139、MIR‐188b‐P、MIR‐204、M1R‐299‐P、MIR‐337、MR‐371、MIR‐383、MIR‐375。
【0088】
単離されたmiR遺伝子産物は、多くの標準的技法を使用して得ることができる。例えば、miR遺伝子産物は、当該技術分野で既知である方法を使用して、化学的に合成することができるか、もしくは組み換えにより産生することができる。一実施形態において、miR遺伝子産物は、適切に保護されたリボヌクレオシドホスホラミダイトおよび従来のDNA/RNAシンセサイザを使用して化学的に合成される。合成のRNA分子または合成試薬の商品製造業者には、例えば、Proligo(ドイツ、ハンブルグ)、Dharmacon Research(米国コロラド州ラファイエット)や、Pierce Chemical(Perbio Scienceの一部門、米国イリノイ州ロックフォード)、Glen Research(米国バージニア州スターリング)、ChemGenes(米国マサチューセッツ州アシュランド)、Cruachem(英国グラスゴー)が含まれる。
【0089】
単離されたmiR遺伝子産物は、裸のRNAとして、送達剤とともに投与することができる。あるいは、miR遺伝子産物は、任意の適切なプロモーターを使用して組換え環状または直鎖状DNAプラスミドから発現させることができる。プラスミドからRNAを発現するための適切なプロモーターには、例えば、U6またはH1 RNA pol IIIプロモーター配列やサイトメガロウイルスプロモーターが含まれる。他の適切なプロモーターの選択は、当該技術分野の範囲内に含まれる。また、本発明の組換えプラスミドは、癌細胞におけるmiR遺伝子産物の発現のための誘導性または調節可能なプロモーターを含むこともできる。
【0090】
組換えプラスミドから発現されたmiR遺伝子産物は、標準的技法によって培養細胞発現系から単離することができる。また、組換えプラスミドから発現するmiR遺伝子産物は、癌細胞に送達することができるか、もしくは癌細胞において直接発現することができる。癌細胞にmiR遺伝子産物を送達する組換えプラスミドの使用については、以下でさらに詳細に考察する。
【0091】
miR遺伝子産物は、別々の組換えプラスミドから発現させることができるか、もしくは同じ組換えプラスミドから発現させることができる。一実施形態において、miR遺伝子産物は単一のプラスミドからRNA前駆体分子として発現し、前駆体分子は、癌細胞の中に残存するプロセッシング系を包含するがこれに限らない適切なプロセッシング系によって、機能性成熟型miR遺伝子産物にプロセッシングされる。他の適切なプロセッシング系には、例えば、in vitroショウジョウバエ細胞可溶化物系(例えば、開示内容全体が参考として本明細書で援用される、米国特許出願第2002/0086356号(Tuschl et al.)に記載)や、大腸菌RNAseIII系、(例えば、開
示内容全体が参考として本明細書で援用される、米国特許出願第2004/00141号(Yang et al.)に記載)が含まれる。
【0092】
miR遺伝子産物の発現に適切なプラスミドの選択、遺伝子産物を発現するためのプラスミド内に核酸配列を挿入する方法、および対象の細胞に組換えプラスミドを送達する方法は、当該技術分野の範囲内に含まれる。例えば、開示内容全体が参考として本明細書で援用される、Zeng et al.(2002),Molecular Cell 9:1327‐1333;Tuschl(2002),Nat.Biotechnol,20:446‐448;Brummelkamp et al.(2002),Science 296:550‐553;Miyagishi et al.(2002),Nat.Biotechnol.20:497‐500;Paddison et al.(2002),Genes Dev.16:948‐958;Lee et al.(2002),Nat.Biotechnol.20:500‐505;およびPaul et
al.(2002),Nat.Biotechnol.20:505‐508を参照されたい。
【0093】
一実施形態において、miR遺伝子産物を発現するプラスミドは、CMV中間体初期プロモーターのコントロール下にあるmiR前駆体RNAをコードする配列を含む。本明細書で使用される、プロモーターの「コントロール下」とは、プロモーターがmiR遺伝子産物コード配列の転写を開始することができるようにmiR遺伝子産物をコードする核酸配列がプロモーターに機能的に結合することを意味する。
【0094】
また、miR遺伝子産物は、組換えウイルスベクターから発現させることもできる。miR遺伝子産物は、2種の別々の組換えウイルスベクターから、あるいは同じウイルスベクターから発現させることができると考えられる。組換えウイルスベクターから発現させるRNAは、標準的技法によって培養細胞発現系から単離すること、あるいは癌細胞において直接発現させることのいずれかが可能である。癌細胞にmiR遺伝子産物を送達する組換えウイルスベクターの使用については、以下でさらに詳細に考察する。
【0095】
本発明の組換えウイルスベクターは、miR遺伝子産物をコードする配列ならびにRNA配列を発現するための任意の適切なプロモーターを含む。適切なプロモーターには、例えば、U6またはH1 RNA pol IIIプロモーター配列やサイトメガロウイルスプロモーターが含まれる。他の適切なプロモーターの選択は、当該技術分野の範囲内に含まれる。また、本発明の組換えウイルスベクターは、癌細胞におけるmiR遺伝子産物の発現のための誘導性または調節可能なプロモーターを含むこともできる。
【0096】
miR遺伝子産物のためのコード配列を収容することができるいずれのウイルスベクター(例えば、アデノウイルス(AV)に由来するベクター;アデノ関連ウイルス(AAV);レトロウイルス(例えば、レンチウイルス(LV)、ラブドウイルス、マウス白血病ウイルス);ヘルペスウイルスなど)も使用することができる。ウイルスベクターの向性は、エンベロープタンパク質または他のウイルス由来の他の表面抗原でベクターを偽型にすることによって、あるいは必要に応じて種々のウイルスキャプシドタンパク質を置換することによって変化させることができる。
【0097】
例えば、本発明のベクターは、水疱性口内炎ウイルス(VSV)や、狂犬病ウイルス、エボラウイルス、モコラウイルスなどに由来する表面タンパク質によって偽型にされてよい。本発明のAAVベクターは、異なるキャプシドタンパク質血清型を発現するためのベクターを設計することによって異なる細胞を標的とすることができる。例えば、血清2型ゲノムにおける血清2型キャプシドを発現するAAVベクターは、AAV2/2と称される。AAV2/2ベクター内のこの血清2型キャプシド遺伝子を血清5型キャプシド遺伝
子で置換してAAV2/5ベクターを作製することができる。異なるキャプシドタンパク質血清型を発現するAAVベクターを作製するための技法は、当該技術分野の範囲内に含まれる。例えば、開示内容全体が参考として本明細書で援用される、Rabinowitz,J.E.et al.,(2002),J.Virol.76:791‐801を参照されたい。
【0098】
本発明の使用に適する組換えウイルスベクターの選択、ベクター内にRNAを発現させるための核酸配列を挿入する方法、対象の細胞にウイルスベクターを送達する方法、および発現したRNA産物の回収は、当該技術分野の範囲内に含まれる。例えば、開示内容全体が参考として本明細書で援用される、Dornburg(1995),Gene Therap.2:301‐310;Eglitis(1988),Biotechniques 6:608‐614;Miller(1990),Hum.Gene Therap.1:5‐14;およびAnderson(1998),Nature 392:25‐30を参照されたい。
【0099】
適切なウイルスベクターは、AVおよびAAVに由来するものである。miR遺伝子産物を発現するための適切なAVベクター、組換えAVベクターを作製する方法、および標的細胞内にベクターを送達する方法は、開示内容全体が参考として本明細書で援用される、Xia et al.(2002),Nat.Biotech.20:1006‐1010に記載されている。miR遺伝子産物を発現するための適切なAAVベクター、組換えAAVベクターを作製する方法、および標的細胞にベクターを送達する方法は、開示内容全体が参考として本明細書で援用される、Samulski et al.(1987),J.Virol.61:3096‐3101;Fisher et al.(1996),J.Virol,70:520‐532;Samulski et al.(1989),J.Virol.63:3822‐3826;米国特許第5,252,479号;米国特許第5,139,941号;国際特許出願第WO94/13788号;国際特許出願第WO93/24641号に記載されている。一実施形態において、miR遺伝子産物は、CMV中間体初期プロモーターを含む単一の組換えAAVベクターから発現する。
【0100】
一実施形態において、本発明の組換えAAVウイルス性ベクターは、ヒトU6RNAプロモーターのコントロール下でpolyT終止配列と機能的に結合してmiR前駆体RNAをコードする核酸配列を含む。本明細書で使用される「polyT終止配列と機能的に結合して」は、センス鎖またはアンチセンス鎖をコードする核酸配列が5’側の方向のpolyT終止シグナルに直接隣接していることを意味する。ベクターからのmiR配列の転写中に、polyT終止シグナルは、転写を終了させるために作用する。
【0101】
膵臓癌のmiRNA発現レベルを変化させる別の方法は、例えばmiRNA遺伝子のプロモーターの高メチル化や低メチル化などの後成的事象によるものである。プロモーターの高メチル化はmiRNA遺伝子の発現の低下につながり、プロモーターの低メチル化はmiRNA遺伝子の発現の増大につながる。(Jones PA,Baylin SB.The fundamental role of epigenetic events in cancer.Nat Rev Genet.3:415‐28(2005))。そのため、癌の進行を抑制する別の方法は、ダウンレギュレートされたmiR遺伝子産物のプロモーター領域の低メチル化をもたらす化合物の投与である。
【0102】
また、本発明の治療方法の他の実施形態において、miR発現を抑制する有効量の少なくとも1つの化合物を被験体に投与することができる。本明細書で使用される、「miR発現の抑制」とは、投与後のmiR遺伝子産物の活性の成熟形態の産生が、投与前に産生した量よりも少ないことを意味する。当業者は、例えば、診断法について上記で考察したmiR転写物レベルを判定するための技法を使用して、miR発現が癌細胞において抑制
されたかどうかを容易に判定することができる。抑制は、遺伝子発現のレベル(すなわち、miR遺伝子産物をコードするmiR遺伝子の転写を抑制することによる)またはプロセッシングのレベル(例えば、成熟型の活性miRへのmiR前駆体のプロセッシングを抑制することによる)で生じる可能性がある。
【0103】
本明細書で使用される、miR発現を抑制する化合物の「有効量」とは、膵臓癌を患う被験体の癌の進行を抑制するのに十分な量である。当業者は、因子(例えば、被験体のサイズおよび重量;疾患の浸透度;被験体の年齢、健康および性別;投与経路;投与が局所的であるか全身性であるか)を考慮することによって、特定の被験体に投与するmiR発現抑制化合物の有効量を容易に判定することができる。
【0104】
例えば、発現抑制化合物の有効量は、治療する腫瘤の近似の重量に基づくてよい。腫瘤の近似の重量は、腫瘤の近似の体積を算出することによって判定することができるが、ここで1立方センチメートルの体積はおよそ1グラムに相当する。腫瘤の重量に基づく有効量は、腫瘤1グラム当たり約10〜500マイクログラムであってよく、腫瘤1グラム当たり少なくとも約10マイクログラム、腫瘤1グラム当たり少なくとも約60マイクログラム、および腫瘤1グラム当たり少なくとも約100マイクログラムであってよい。
【0105】
miR発現を抑制する化合物の有効量はまた、治療する被験体の近似または推定の体重に基づいてもよい。とりわけ、本明細書に記載の通り、このような有効量は非経口的または経腸的に投与することができる。例えば、被験体に投与される発現抑制化合物の有効量は、体重1kg当たり約5〜3000マイクログラム、体重1kg当たり約700〜1000マイクログラムであってもよければ、あるいは体重1kg当たり約1000マイクログラムを超えてもよい。
【0106】
当業者はまた、特定の被験体にmiR発現を抑制する化合物を投与するための適切な投与計画を容易に判定することもできる。例えば、発現抑制化合物は、被験体に1回投与することができる(例えば、単回注射または沈殿として)。あるいは、発現抑制化合物は、数日から数カ月の期間、特に約3日間から約28日間、とりわけ約7日間から約10日間、1日1回または1日2回、被験体に投与することができる。特定の投与計画において、発現抑制化合物は、1日1回、7日間投与される。投与計画が反復投与を含む場合、被験体に投与される発現抑制化合物の有効量は、すべての投与計画を通じて投与される化合物の総量を含んでよいものと理解される。
【0107】
いくつかの態様において、レベルが低下する可能性があるmiR遺伝子産物は、以下の内の1つ以上を含む:let‐7a‐2‐P、let‐7b、let‐7c、let‐7d、let‐7f‐1、let‐7i、MIR‐001‐2、MIR‐007‐1、MIR‐015a、MIR‐015b、MIR‐016‐1、MIR‐019b‐1‐P、MIR‐021、MIR‐023a、MIR‐024‐1,2、MIR‐027a,b、MIR‐029a,c、MIR‐030d、MIR‐032、MIR‐092‐1、MIR‐098、MlR‐099a、MIR‐100、MIR‐107、MIR‐125b‐1、MIR‐126、MIR‐128a、MIR‐132、MIR‐136、MIR‐142‐P、MIR‐145‐P、MIR‐152、MIR‐155、MIR‐181a,c、MIR‐196a‐2、MIR‐212、MIR‐213、MIR‐215、MIR‐218‐1,2、MIR‐221、MIR‐222‐P、MIR‐301、MIR‐328、MIR‐331‐P、MIR‐345、MIR‐367、MIR‐376、MIR‐424。
【0108】
miR遺伝子発現を抑制するための適切な化合物には、2本鎖RNA(例えば短い干渉RNAまたは低分子干渉RNA「siRNA」)、アンチセンス核酸、リボザイムなどの
酵素RNA分子、または3重らせんをmiR遺伝子により形成することができる分子が含まれる。抑制化合物の別の種類は、miR遺伝子産物プロモーターの高メチル化を引き起こし、それによりmiR遺伝子の発現を低下させる。これらの化合物のそれぞれは、特定のmiR遺伝子産物を標的として、miR遺伝子産物を破壊するか、miR遺伝子産物の破壊を誘導するか、さもなければmiR遺伝子産物のレベルを低下させることができる。
【0109】
例えば、特定のmiR遺伝子の発現は、miR遺伝子産物の少なくとも一部と少なくとも90%、例えば少なくとも95%、少なくとも98%、少なくとも99%または100%の配列相同性を有する単離された2本鎖RNA(「dsRNA」)分子でmiR遺伝子のRNA干渉を誘導することによって抑制することができる。特定の一実施形態において、dsRNA分子は、「短い干渉RNAまたは低分子干渉RNA」または「siRNA」である。
【0110】
本方法において有用なsiRNAは、約17〜約29ヌクレオチドの長さ、あるいは約19〜約25ヌクレオチドの長さの短い2本鎖RNAを含む。siRNAは、標準的ワトソン‐クリック塩基対合相互作用(以下「塩基対」)によって共にアニール化されたセンスRNAストランドおよび相補型アンチセンスRNAストランドを含む。センス鎖は、標的miR遺伝子産物の中に含まれる核酸配列と実質的に同一である核酸配列を含む。
【0111】
本明細書で使用される、標的mRNAの範囲内に含まれる標的配列に「実質的に同一」であるsiRNA内の核酸配列は、標的配列と同一である核酸配列であるか、もしくは標的配列とは1個または2個のヌクレオチドが異なる核酸配列である。siRNAのセンス鎖およびアンチセンス鎖は、2つの相補型1本鎖RNA分子を含んでよいか、もしくは2つの相補的部分が塩基対を形成しかつ1本鎖「ヘアピン」領域が共有結合した単一の分子を含んでよい。
【0112】
siRNAはまた、1個以上のヌクレオチドの付加、欠失、置換および/または変化によって天然のRNAとは異なる変化したRNAであってもよい。このような変化には、例えばsiRNAの末端やsiRNAの1個以上の内部ヌクレオチドへの非ヌクレオチド材料の付加、siRNAをヌクレアーゼ分解に抵抗性とする修飾、またはデオキシリボヌクレオチドによるsiRNAにおける1個以上のヌクレオチドの置換が含まれる場合がある。
【0113】
また、siRNAは、特定の「薬物のような」性質を含むように設計することもできる。このような修飾には、安定のための化学修飾や送達のためのコレステロール抱合が含まれる。このような修飾によってsiRNAに対してより良好な薬理学的性質が付与され、このような修飾を使用して、薬理活性siRNAは、幅広い生体分布を達成することができ、in vivoにおける大部分の組織内でmiRNAの効率的なサイレンシングを達成することができる。
【0114】
また、siRNAの一方または両方のストランドは、3’オーバーハングを含んでよい。本明細書で使用される「3’オーバーハング」とは、2重らせんRNAストランドの3’末端から伸長する少なくとも1つの不対ヌクレオチドを指す。従って、特定の実施形態において、siRNAは、1〜約6個のヌクレオチド(リボヌクレオチドまたはデオキシリボヌクレオチドを含む)の長さ、1〜約5個のヌクレオチドの長さ、1〜約4個のヌクレオチドの長さ、または約2〜約4個のヌクレオチドの長さの少なくとも1つの3’オーバーハングを含む。一実施形態において、3’オーバーハングは、siRNAの両ストランドに存在しており、かつ2個のヌクレオチドの長さである。例えば、siRNAの各ストランドは、ジチミジル酸(「TT」)またはジウリジル酸(「uu」)の3’オーバーハングを含んでよい。
【0115】
siRNAは、単離されたmiR遺伝子産物について上記で記載した通り、化学的または生物学的に産生することができるか、もしくは組換えプラスミドまたはウイルスベクターから発現させることができる。dsRNAまたはsiRNA分子を産生および試験するための例示的な方法は、開示内容全体が参考として本明細書で援用される、米国特許出願第2002/0173478号(Gewirtz)および米国特許出願第2004/0018176号(Reich et al.)に記載されている。in vivoでmiRNAを非発現化するために設計される治療上有効なsiRNAを合成および確認する方法は、内容全体が参考として本明細書で援用される、Krutzfeldt J, et al.(2005),Silencing of microRNAs in vivo
with’antagomirs,’Nature 438(7068):685‐9に記載されている。
【0116】
また、特定のmiR遺伝子の発現は、アンチセンス核酸によって抑制することもできる。本明細書で使用される場合、「アンチセンス核酸」とは、標的RNAの活性を変えるRNA‐RNAまたはRNA‐DNAまたはRNA‐ペプチド核酸相互作用によって標的RNAに結合する核酸分子を指す。本方法の使用に適したアンチセンス核酸は、一般的にmiR遺伝子産物内の連続した核酸配列に相補的な核酸配列を含む1本鎖核酸(例えばRNA、DNA、RNA‐DNAキメラ、PNA)である。アンチセンス核酸は、miR遺伝子産物内の連続した核酸配列に対して50〜100%相補的、75〜100%相補的、または95〜100%相補的な核酸配列を含んでよい。いかなる理論によっても縛られることを望まないが、アンチセンス核酸は、miR遺伝子産物/アンチセンス核酸2本鎖を消化するRNアーゼHまたは別の細胞ヌクレアーゼを活性化すると考えられる。
【0117】
例えば、真核生物においては、RNAポリメラーゼは、構造遺伝子の転写を触媒してmRNAを産生する。DNA分子は、RNA転写物が好ましいmRNAの配列に相補的な配列を有するRNAポリメラーゼ鋳型を含むように設計することができる。RNA転写物は、「アンチセンスRNA」と称される。アンチセンスRNA分子は、mRNA発現を抑制することができる(例えば、Rylova et al.,Cancer Res,62(3):801‐8,2002;Shim et al.,Int. J.Cancer,94(1):6‐15,2001)。
【0118】
あるいは、第1の核酸分子に対して、相補配列であるかもしくは第1の分子の相補配列またはその一部に相同である配列で作製される第2のDNA分子または第2のキメラ核酸分子は、第1の分子の「アンチセンスDNAまたはDNAデコイまたはデコイ分子」と称される。「デコイ分子」という用語はまた、DNAまたはPNA(ペプチド核酸)を含み(Mischiati et al.,Int.J.Mol.Med.,9(6):633‐9,2002)、かつ調節タンパク質のための結合部位や転写因子のための結合部位などのタンパク質結合部位の配列を含む核分子(1本鎖であっても2本鎖であってもよい)を包含する。アンチセンス核酸分子の応用は、アンチセンスDNAおよびデコイDNA分子を包含し、当該技術分野で既知である(例えば、開示内容全体が参考として本明細書で援用される、Morishita et al.,Ann.NY Acad.Sci.,947:294‐301,2001;Andratschke et al.,Anticancer Res,21:(5)3541‐3550,2001)。
【0119】
また、アンチセンス核酸は、核酸主鎖あるいは糖および塩基部分(またはそれらの等価物)に修飾を含んで標的特異性、ヌクレアーゼ耐性、送達性または分子の有効性に関するその他の性質を向上させることができる。このような修飾は、コレステロール部分、アクリジンなどの2本鎖インターカレータ、または1つ以上のヌクレアーゼ耐性群を含む。
【0120】
アンチセンス核酸は、単離されたmiR遺伝子産物について上記で記載した通り、化学的または生物学的に産生することができるか、もしくは組換えプラスミドまたはウイルスベクターから発現させることができる。産生および試験するための例示的な方法は、当該技術分野の範囲内に含まれ;例えば、開示内容全体が参考として本明細書で援用される、Stein and Cheng(1993),Science 261:1004;および米国特許第5,849,902号(Woolf et al.)を参照されたい。
【0121】
特定のmiR遺伝子の発現はまた、酵素核酸によって抑制することもできる。本明細書で使用される「酵素核酸」とは、miR遺伝子産物の連続した核酸配列に相補性を有し、具体的にはmiR遺伝子産物を開裂することが可能な基質結合領域を含む核酸を指す。酵素核酸基質結合領域は、miR遺伝子産物における連続した核酸配列に対して、例えば50〜100%相補的、75〜100%相補的、または95〜100%相補的であってよい。酵素核酸はまた、塩基、糖および/またはリン酸基に修飾を含むこともできる。本発明の方法で使用される酵素拡散の例にはリボザイムがある。
【0122】
リボザイムは、RNAの特異的開裂を触媒することができる酵素RNA分子である。概要は、Rossi,Current Biology,4:469‐471(1994)で示される。リボザイムの作用機序は、相補型標的RNAに対するリボザイム分子の配列特異的ハイブリダイゼーションと、その後のエンドヌクレアーゼによる開裂を含む。リボザイム分子の組成物は、標的遺伝子mRNAに相補的な1つ以上の配列を含む必要があり、かつmRNA開裂の原因となる周知の触媒配列を含む必要がある(米国特許第5,093,246号)。
【0123】
いずれの可能性のあるRNA標的中の特異的なリボザイム開裂部位も、GUA、GUUおよびGUCという配列を含むリボザイム開裂部位に対する対象の分子をスキャンすることによって先ず同定される。一度同定されると、開裂部位を含むmiR遺伝子の領域に対応する約15〜20リボヌクレオチドの短いRNA配列は、オリゴヌクレオチド配列を不適切にする可能性がある、例えば二次構造などの予想される構造特性について評価することができる。候補配列の適合性もまた、相補的オリゴヌクレオチドとのハイブリダイゼーションの容易さを、リボヌクレアーゼ防御検定を使用して評価することができる。
【0124】
酵素核酸は、単離されたmiR遺伝子産物について上記で記載した通り、化学的または生物学的に産生することができるか、もしくは組換えプラスミドまたはウイルスベクターから発現させることができる。dsRNAまたはsiRNA分子を産生および試験するための例示的な方法は、開示内容全体が参考として本明細書で援用される、Werner and Uhlenbeck(1995),Nucl.Acids Res.23:2092‐96;Hammann et al.,(1999),Antisense and Nucleic Acid Drug Dev.9:25‐31;および米国特許第4,987,071号(Cech et al.)に記載されている。
【0125】
3重らせん形成分子は、標的miR遺伝子活性のレベルを低下させる際に使用することができる。3本鎖立体配座(3重らせん)において共に会合することができ、それにより標的遺伝子の翻訳を阻害するために使用することができる核酸分子は、デオキシヌクレオチドから構成される1重らせんでなければならない。これらのオリゴヌクレオチドの塩基組成は、一般的に2本鎖の一方の鎖上のプリンまたはピリミジンのいずれかの相当大きなストレッチを必要とするフーグスティーン型塩基対合則により3重らせんの形成を促進するように設計される必要がある。ヌクレオチド配列はピリミジンに基づくことができ、それによって、生成する3重らせんの3本の会合した鎖を横切るTATおよびCGCトリプレットが生じるのである。ピリミジン富化分子は、2本鎖のうちの1本鎖のプリン富化領域に対し、この鎖と平行方向の塩基相補性を提供する。加えて、プリンに富んだ核酸分子
、例えばG残基のストレッチを有するものを選択することができる。これらの分子が、GC対に富んだDNA2本鎖と3重らせんを形成するのである。この場合、プリン残基の大半は、標的2本鎖の内の1本鎖に位置し、3本鎖中の3本の鎖を横切るGGCトリプレットを生成させる。あるいは、いわゆる「スイッチバック」核酸分子を作製することにより、3重らせん形成のために標的とされる可能性のある配列を増加させることができる。スイッチバック分子は、交互に5’‐3’、3’‐5’様式で合成され、その結果、それらは2本鎖の最初の1本の鎖と塩基対合し、次いでもう一方の鎖と塩基対合することになり、2本鎖分子の一方の鎖上のプリンまたはピリミジンのいずれかの相当大きなストレッチの必要性がなくなる。
【0126】
膵臓癌のmiRNA発現レベルを変化させる別の方法は、例えばmiRNA遺伝子のプロモーターの高メチル化や低メチル化などの後成的事象によるものである。プロモーターの高メチル化はmiRNA遺伝子の発現の低下につながり、プロモーターの低メチル化はmiRNA遺伝子の発現の増大につながる。(Jones PA,Baylin SB.The fundamental role of epigenetic events in cancer.Nat Rev Genet.3:415‐28(2005))。
【0127】
少なくとも1つのmiR遺伝子産物またはmiR発現を抑制するために少なくとも1つの化合物を投与することで、被験体の膵臓癌の進行が抑制される。miR遺伝子産物またはmiR遺伝子発現を抑制する化合物の投与後に被験体におけるかかる細胞の数が一定のままであるかもしくは減少する場合に、癌細胞増殖の抑制が推定される。このような細胞の絶対数は増加するが、腫瘍成長の速度が減少する場合に、癌細胞の増殖の抑制が推定される。
【0128】
被験体の身体内の癌細胞の数は、直接測定するか、もしくは原発性腫瘤または転移性腫瘤のサイズから推定することによって判定することができる。例えば、被験体における癌細胞の数は、免疫組織学的方法、フローサイトメトリー、または癌細胞の特徴的な表面マーカーを検出するように設計された他の技法によって測定することができる。
【0129】
腫瘤のサイズは、直接的な目視観測によって、あるいはX線や、磁気共鳴映像法、超音波検査、シンチグラフィーなどの画像診断法によって確認することができる。当該技術分野で既知であるように、腫瘤のサイズを確認するために使用される画像診断法は、コントラスト剤の有無にかかわらず使用することができる。腫瘤のサイズはまた、物理的手段(例えば、組織塊の触診あるいはキャリパーなどの計器による組織塊の測定)によって確認することもできる。
【0130】
miR遺伝子産物またはmiR遺伝子発現抑制化合物は、被験体の癌細胞へのこれらの化合物の送達に適切ないずれの手段によっても被験体に投与することができる。例えば、miR遺伝子産物またはmiR発現抑制化合物は、これらの化合物またはこれらの化合物をコードする配列を含む核酸によって被験体の細胞をトランスフェクションさせるための適切な方法によって投与することができる。一実施形態において、細胞は、少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物をコードする配列を含むプラスミドまたはウイルスベクターによってトランスフェクションされる。
【0131】
真核細胞のトランスフェクション方法は、当該技術分野で周知であり、細胞の核または前核への核酸の直接注入;エレクトロポレーション;リポソーム転移または疎水性材料によって仲介される転移;レセプター仲介核酸送達、バイオバリスティックまたは粒子加速;リン酸カルシウム沈殿およびウイルスベクターによって仲介されるトランスフェクションを包含する。
【0132】
例えば、細胞は、リポソーム型転移化合物(例えば、DOTAP(N‐[1‐(2,3‐ジオレオイロキシ)プロピル]‐N,N,N‐トリメチルアンモニウムメチルスルフェイト、Boehringer‐Mannheim)または等価物(例えばLIPOFECTIN))によってトランスフェクションすることができる。使用する核酸の量は、本発明の診療に重大な意味を持たず;許容される結果は、細胞105個当たり0.1〜100マイクログラムの核酸で達成される場合がある。例えば、細胞105個当たり3マイクログラムのDOTAPにおいて約0.5マイクログラムのプラスミドベクターの比を使用することができる。
【0133】
一実施形態において、膵臓癌細胞は、被験体から単離され、ダウンレギュレートされたmiR遺伝子産物をコードする核酸によってトランスフェクションされ、被験体に再導入される。
【0134】
また、miR遺伝子産物またはmiR遺伝子発現抑制化合物は、任意の適切な経腸または非経口投与経路によって被験体に投与することができる。本方法に適切な経腸投与経路には、例えば、経口送達や、直腸送達、鼻腔内送達が含まれる。適切な非経口投与経路には、例えば、血管内投与(例えば静脈内ボーラス注射や、静脈内注入、動脈内ボーラス注射、動脈内注入、血管系へのカテーテル滴下注入);組織周囲および組織内注射(例えば、腫瘍周囲および腫瘍内注射や、網膜内注射、網膜下注射);皮下注射または沈殿(皮下注入(例えば浸透ポンプによって)など);例えばカテーテルまたは他の配置装置(例えば、網膜ペレットや、坐剤や、多孔性、非多孔性またはゼラチン状材料を含むインプラント)による対象の組織に対する直接塗布;および吸入が含まれる。適切な投与経路は、腫瘍への注射、注入および直接注入である。
【0135】
本方法において、miR遺伝子産物またはmiR遺伝子産物発現抑制化合物は、送達試薬とともに裸のRNA、もしくはmiR遺伝子産物または発現抑制化合物を発現する配列を含む核酸(例えば組換えプラスミドまたはウイルスベクター)のいずれかとして被験体に投与することができる。適切な送達試薬には、例えば、Mirus Transit TKO疎水性試薬や;リポフェクチン;リポフェクタミン;セルフェクチン;ポリ陽イオン(例えばポリリジン)、リポソームが含まれる。
【0136】
miR遺伝子産物またはmiR遺伝子発現抑制化合物を発現する配列を含む組換えプラスミドおよびウイルスベクター、ならびに癌細胞にこのようなプラスミドおよびベクターを送達するための技法は、本明細書において考察される。
【0137】
一実施形態において、リポソームを使用して、miR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む核酸)が被験体に送達される。リポソームはまた、遺伝子産物または核酸の血中半減期を延長させることができる。本発明に使用される適切なリポソームは、一般的に中性または負に荷電したリン脂質やステロール(例えばコレステロール)を含む標準的ベシクル形成脂質から形成されることができる。脂質の選択は、一般的に、因子(例えば所望のリポソームのサイズや、血流におけるリポソームの半減期)を考慮して導かれる。例えば、開示内容全体が参考として本明細書で援用される、Szoka et al.(1980),Ann.Rev.Biophys.Bioeng.9:467;ならびに米国特許第4,235,871号、第4,501,728号、第4,837,028号および第5,019,369号に記載の通り、リポソームを調製するための種々の方法が知られている。
【0138】
本方法に使用されるリポソームは、リポソームを癌細胞に標的とするリガンド分子を含んでよい。癌細胞に一般的なレセプターと結合するリガンド(例えば、腫瘍細胞抗原と結
合するモノクローナル抗体)が適切である。
【0139】
本方法に使用されるリポソームはまた、単核マクロファージ系(「MMS」)および細網内皮系(「RES」)によるクリアランスを回避するように修飾することができる。そのように修飾されたリポソームは、表面上にオプソニン化抑制部分を有するか、もしくはリポソーム構造内に組み込まれる。いくつかの実施形態において、本発明のリポソームは、オプソニン化抑制部分およびリガンドの両方を含んでよい。
【0140】
本発明のリポソームの調製に使用されるオプソニン化抑制部分は、通常は、リポソーム膜に結合する大きな親水性ポリマーである。本明細書で使用される場合、オプソニン化抑制部分がリポソーム膜に「結合」するとは、例えば膜自体への脂溶性アンカーの挿入または膜脂質の活性基への直接の結合によって化学的または物理的に膜に結合させる場合のことである。開示内容全体が参考として本明細書で援用される米国特許第4,920,016号に記載されている通り、これらのオプソニン化抑制親水性ポリマーは、MMSおよびRESによるリポソームの取り込みを著しく減少させる保護表面層を形成する。
【0141】
リポソームの修飾に適切なオプソニン化抑制部分は、約500〜約40,000ダルトン、または約2,000〜約20,000ダルトンの数平均分子量を有する水溶性ポリマーを含む。このようなポリマーには、ポリエチレングリコール(PEG)またはポリプロピレングリコール(PPG)誘導体;例えば、メトキシPEGまたはPPGやステアリン酸PEGまたはPPG;合成ポリマー(例えばポリアクリルアミドやポリN‐ビニルピロリドン);直鎖状、分岐状またはデンドリマーのポリアミドアミン;ポリアクリル酸;ポリアルコール(例えば、カルボキシル基またはアミノ基が化学的に結合するポリビニルアルコールやポリキシリトール)ならびにガングリオシド(例えばガングリオシドGM1)が含まれる。また、PEG、メトキシPEGまたはメトキシPPGのコポリマーまたはそれらの誘導体も適切である。さらに、オプソニン化抑制ポリマーは、PEGのブロックコポリマーならびにポリアミノ酸、ポリサッカリド、ポリアミドアミン、ポリエチレンアミン、ポリヌクレオチドのいずれかであってよい。オプソニン化抑制ポリマーはまた、アミノ酸またはカルボン酸(例えば、ガラクツロン酸、グルクロン酸、マンヌロン酸、ヒアルロン酸、ペクチン酸、ノイラミン酸、アルギン酸)、カラギーナンを含む天然のポリサッカリド;アミノ化されたポリサッカリドまたはオリゴサッカリド(直鎖状または分岐状);あるいはカルボキシ化されたポリサッカリドまたはオリゴサッカリド(例えば、カルボキシル基と結合を生じる炭酸の誘導体と反応したもの)であってもよい。オプソニン化抑制部分は、PEG、PPGまたはそれらの誘導体であってよい。PEGまたはPEG誘導体で修飾されるリポソームは、「ポリエチレングリコール化されたリポソーム」と称される場合がある。
【0142】
オプソニン化抑制部分は、数多くの周知の技法の内のいずれか1つによって、リポソーム膜に結合させることができる。例えば、PEGのN‐ヒドロキシスクシンイミドエステルは、ホスファチジルエタノールアミン脂溶性アンカーに結合させることができ、次いで膜に結合させることができる。同様に、デキストランポリマーは、Na(CN)BH3と混合溶媒(例えば、60℃で30:12の比のテトラヒドロフランと水)を使用して還元的アミノ化によってステアリルアミン脂溶性アンカーで誘導体化することができる。
【0143】
オプソニン化抑制部分によって修飾されるリポソームは、無修飾リポソームより非常に長く血行の中にとどまる。このために、このようなリポソームは「ステルス」リポソームと称されることがある。ステルスリポソームは、多孔性または「漏出性」微小血管系によって供給された組織内に蓄積することが知られている。従って、このような微小血管系の欠損(例えば固形腫瘍)を特徴とする組織は、これらのリポソームを効率的に蓄積する。Gabizon,et al.(1988),Proc.Natl.Acad.Sci.
,U.S.A.,18:6949‐53を参照されたい。さらに、RESによる取り込みの減少は、肝臓および脾臓におけるリポソームの著しい蓄積を防止することによってステルスリポソームの毒性を低下させる。従って、オプソニン化抑制部分によって修飾されるリポソームは、腫瘍細胞へのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む核酸)の送達に非常に適している。
【0144】
miR遺伝子産物またはmiR遺伝子発現抑制化合物は、当該技術分野で既知の技法に従って、被験体への投与前に、「医薬品」と称されることがある薬学的組成物として調製することができる。従って、本発明は、膵臓癌を治療するための薬学的組成物を包含する。一実施形態において、薬学的組成物は、少なくとも1つの単離されたmiR遺伝子産物および薬学的に許容される担体を含む。特定の実施形態において、miR遺伝子産物は、適切な対照細胞よりも膵臓癌細胞における発現レベルが低下したmiR遺伝子産物に相当する。
【0145】
他の実施形態において、本発明の薬学的組成物は、少なくとも1つのmiR発現抑制化合物を含む。特定の実施形態において、少なくとも1つのmiR遺伝子発現抑制化合物は、対照細胞よりも膵臓癌細胞において発現が大きいmiR遺伝子に特異的である。
【0146】
本発明の薬学的組成物は、少なくとも無菌であり、かつ発熱物質がないことを特徴とする。本明細書で使用される場合、薬学的「組成物」または「製剤」は、ヒトおよび獣医学的使用のための製剤を包含する。本発明の薬学的組成物を調製する方法は、開示内容全体が参考として本明細書で援用される、Remington’s Pharmaceutical Science,17th ed.,Mack Publishing Company,Easton,Pa.(1985)に記載の通り、当該技術分野の範囲内に含まれる。
【0147】
本薬学的製剤は、薬学的に許容される担体と混合された少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)(例えば0.1〜90重量%)またはその生理的に許容される塩を含む。また、本発明の薬学的製剤は、リポソームおよび薬学的に許容される担体によってカプセル化された少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)を含んでよい。
【0148】
特に適切な薬学的に許容される担体は、水、緩衝用水、生理食塩液、0.4%生理食塩水、0.3%グリシン、ヒアルロン酸などである。
【0149】
本発明の薬学的組成物は、ヌクレアーゼによる分解に対して抵抗性である少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)を含んでよい。当業者は、例えば2’位で修飾される1つ以上のリボヌクレオチドをmiR遺伝子産物内に組み込むことによって、ヌクレアーゼ抵抗性である核酸を容易に合成することができる。適切な2’修飾リボヌクレオチドには、フルオロ、アミノ、アルキル、アルコキシおよびO‐アリルで2’位が修飾されたものが含まれる。
【0150】
本発明の薬学的組成物はまた、従来の薬学的賦形剤および/または添加剤を含んでもよい。適切な薬学的賦形剤には、安定剤、抗酸化剤、モル浸透圧調整剤、緩衝剤、およびpH調整剤が含まれる。適切な添加剤には、例えば、生理的に生体適合性の緩衝剤(例えば塩酸トロメタミン)、キレート剤(例えば、DTPAやDTPA‐ビスアミド)またはカルシウムキレート錯体(例えば、カルシウムDTPA、CaNaDTPA‐ビスアミド)の添加剤、あるいたは場合により、カルシウムまたはナトリウム塩(例えば、塩酸カルシ
ウム、アスコルビン酸カルシウム、グルコン酸カルシウム、乳酸カルシウム)の添加剤が含まれる。本発明の薬学的組成物は、液体形態で使用するためにパッケージすることができるか、もしくは凍結乾燥することができる。
【0151】
本発明の固体の薬学的組成物としては、従来の無毒性で固体の薬学的に許容される担体(例えば、マンニトール、ラクトース、デンプン、ステアリン酸マグネシウム、ナトリウムサッカリン、滑石、セルロース、グルコース、スクロース、炭酸マグネシウムなどの医薬品グレード)を使用することができる。
【0152】
例えば、経口投与のための固体の薬学的組成物は、上記に掲載された担体および賦形剤のいずれか、ならびに10〜95%、好ましくは25%〜75%の少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)を含んでよい。エアゾール(吸入)投与のための薬学的組成物は、0.01〜20重量%、好ましくは1%〜10重量%の、上記の通りのリポソームおよび噴射剤の中にカプセル化した少なくとも1つのmiR遺伝子産物またはmiR遺伝子発現抑制化合物(またはそれらをコードする配列を含む少なくとも1つの核酸)を含んでよい。また、例えば鼻腔内送達のためのレシチンなどの担体を所望により含んでよい。
【0153】
本発明はまた、被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する方法も提供する。本方法は、(a)対照細胞に比べてアップレギュレートされたmiR遺伝子産物を有する癌細胞を含む被験体の膵臓から第1の試験試料を得る手順;(b)被験体に治療レジメンを施す手順;(d)ある期間後に被験体の膵臓から第2の試験試料を得る手順;および(e)第1および第2の試験試料におけるアップレギュレートされたmiR遺伝子産物のレベルを比較する手順を含む。第2の試験試料におけるアップレギュレートされたmiR遺伝子産物レベルが第1の試験試料よりも低いことによって、その治療レジメンが被験体における膵臓癌の進行抑制に効果的であることが示される。
【0154】
被験体における膵臓癌の進行を抑制する治療レジメンの有効性を判定する他の方法は、(a)対照細胞に比べてダウンレギュレートされたmiR遺伝子産物を有する癌細胞を含む被験体の膵臓から第1の試験試料を得る手順;(b)被験体に治療レジメンを施す手順;(d)ある期間後に被験体の膵臓から第2の試験試料を得る手順;および(e)第1および第2の試験試料におけるダウンレギュレートされたmiR遺伝子産物のレベルを比較する手順を含む。第2の試験試料におけるダウンレギュレートされたmiR遺伝子産物レベルが第1の試験試料よりも高いことによって、その治療レジメンが被験体における膵臓癌の進行抑制に効果的であることが示される。
【0155】
本発明はまた、膵臓癌用抗癌剤を同定する方法も包含する。本方法は、(a)膵臓癌細胞を含む生体試料において過剰発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;(b)生体試料に試験剤を接触させる手順;(c)手順(b)の後に生体試料におけるmiR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについてのデータを作成する手順;および(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順を含む。過剰発現したmiR遺伝子産物の試験後の発現レベルが低下することによって、試験剤が膵臓癌の抗癌性を有することが示される。
【0156】
別の実施形態において、膵臓癌用抗癌剤を同定する方法は、(a)膵臓癌細胞を含む生体試料において過小発現する少なくとも1つのmiR遺伝子産物の発現レベルを測定し、これにより前記miR遺伝子産物の試験前の発現レベルについてのデータを作成する手順;(b)前記生体試料に試験剤を接触させる手順;(c)手順(b)の後に生体試料におけるmiR遺伝子産物の発現レベルを測定し、これにより試験後の発現レベルについての
データを作成する手順;および(d)前記miR遺伝子産物の試験後の発現レベルを試験前の発現レベルと比較する手順であって、過小発現したmiR遺伝子産物の試験後の発現レベルが上昇することによって、試験剤が膵臓癌の抗癌性を有することが示される、手順を含む。
【0157】
適切な剤としては薬物(例えば低分子、ペプチド)や生体高分子(例えばタンパク質、核酸)が含まれるが、これらに限定されるものではない。剤は、組み換えにより、合成的に作製することができるか、もしくは天然の原料から単離(すなわち、精製)することができる。このような剤を細胞に与える各種方法(例えばトランスフェクション)は、当該技術分野で周知であり、このような方法のいくつかは上に記載されている。少なくとも1つのmiR遺伝子産物の発現を検出する方法(例えばノーザンブロット法や、in situハイブリダイゼーション、RT‐PCR、発現プロファイリング)は、当該技術分野で周知である。これらの方法のいくつかもまた、上に記載されている。
【0158】
以下では、本発明を以下の非限定的な実施例で例示する。
【実施例】
【0159】
(実施例1) 膵臓癌を正常組織または膵炎組織と区別するマイクロRNA発現サインの同定
リアルタイム定量的PCR検定を使用して、ヒト膵臓癌(腺癌)、良性対組織、正常な膵臓、慢性膵炎および膵臓癌細胞株の臨床検査材料における200超のmiRNA前駆体の発現を測定した。膵臓癌を正常かつ良性の膵臓と区別した固有のmiRNAサインを同定した。リアルタイム定量的RT‐PCRのために使用される方法は、開示内容全体が参考として本明細書で援用される、Jiang,J.,et al.(2005),Nucleic Acids Res 33:5394‐5403;Schmittgen T.D.,et al.(2004),Nucleic Acids Res 32:E43;および2005年2月24日出願の米国仮出願第60/656,109号に詳述されている。また、実験手順および結果は、開示内容全体が参考として本明細書で援用される、Lee et al.,(2006)Int.J.Cancer 120:1046‐1054に報告されている。
【0160】
材料および方法
組織の入手:この研究において解析された組織試料は、オクラホマ大学ヘルスサイエンスセンターおよびオハイオ州立大学で膵臓の一部の切除のための外科手術を受けた患者に由来するものであった。試料の採集は、施設の施設内倫理委員会の方針および慣行に適合したものであった。外科的な検体の切除と同時に、研究員は直ちにその組織を外科病理検査室に移した。病理部は、検体のグロス分析を実施し、研究のために、癌と思われる膵組織および正常と思われる膵組織を選んだ。各試料をクライオバイアル内に配置し、液体窒素中で急速冷凍し、解析を行うまで‐150℃で保存した。次に、外科的な検体を提供する研究所によって次病理学的解析を行い、それにより研究のために採取された試料の組織変化を確認した。RNA解析を実施した研究機関によって、隣接する良性組織にセカンドレベルの精度管理を行った。組織のスライドを、RNAが単離された組織に直接隣接する凍結組織の切片から準備した。これらのスライドを、良性組織が膵臓腫瘍細胞を含むかどうかを判定するために、本発明者等(W.L.F.)の内の1人が検査した。残りの腫瘍を含む良性組織については、この研究に含めなかった。検体に関する臨床データを付録の表1に示す。
【0161】
細胞株:以下の膵臓腫瘍細胞株を、American Type Tissue Collection(米国バージニア州マナッサス)から購入した。Panc‐1、HS766T、MIA PaCa‐2、HPAF‐II、BxPC‐3、Mpanc‐96、P
L45、Panc03.27およびPanc10.05。細胞株を、標準条件を使用して、10%FBSまたは他の最適化された完全培地を含むRPMI1640培地中で培養した。
【0162】
miRNA前駆体発現プロファイリング:トータルRNAを、1mLのTrizol(Invitrogen、米国カリフォルニア州カールズバッド)中で細胞株または組織から単離した。まず、凍結組織(約10mg)をステンレス鋼乳鉢および乳棒で微粉状にした。正常膵臓由来のトータルRNAは、Ambion(米国テキサス州オースティン)、BD Biosciences(米国カリフォルニア州マウンテンビュー)およびStratagene(米国カリフォルニア州ラ・ホーヤ)から購入した。正常組織のすべてのドナーは、膵疾患以外の合併症で死亡した(図3)。RNAの完全性を、Agilent
2100 Bioanalyzer(Agilent Technologies、米国カリフォルニア州パロアルト)を使用して評価した。RNA完全性番号(RIN)は、Imbeaud,S.,et al.(2005),Nucleic Acids Res 33,e56におけるプロトコルに従って、Agilent 2100エキスパートソフトウェアのRINアルゴリズムを使用して判定された。RIN≧4のRNA試料をこの研究に含めた(図3)。しばらくRNAをRNアーゼフリーのDNAase Iで処理し、222のmiRNA前駆体と18S rRNAとに対する遺伝子特異的プライマーを使用してcDNAを1μgのトータルRNAから合成した。222のmiRNA前駆体の発現は、リアルタイム定量的PCR検定を使用して測定した。cDNAの各試料中の各miRNA前駆体遺伝子について重複PCRを行った。平均CTを重複PCRから判定した。相対的遺伝子発現を2‐(CTmiRNA‐CT18S rRNA)として算出した。相対的遺伝子発現には、データの提示を単純化するために、106を乗算した。生の相対的miRNA前駆体発現データを図4に示す。
【0163】
統計:201の遺伝子発現値(対照遺伝子発現に比べたもの)についてのΔCTデータの平均中心を求め、以下の方法を使用して解析した。フィルタリングされていないデータの発現パターンを、試料の管理されない階層的クラスタリングと、平均連結法およびユークリッド距離に基づく遺伝子の管理されない階層的クラスタリングとを使用して評価した(Eisen MB, et al.(1998),Proc Natl Acad Sci USA 95:14863‐8;Saeed AI,et al.(2003),Biotechniques 34:374‐8)。試料群間に特異に発現する遺伝子を判定するため、そのデータは、p<0.01(10,000無作為順列)の多群の順列に基づくANOVA検定(ウェルチの近似法)および多重検定補正(maxTのWestfall‐Young手順ダウン補正)を使用して差の有意性においてフィルタリングを行った。特異に発現した遺伝子の発現パターンを比較するため、フィルタリングされたデータを、試料の階層的クラスタリングと、平均連結法およびユークリッド距離に基づく遺伝子の階層的クラスタリングとを使用して解析した。
【0164】
フィルタリングされたデータのさらなるクラスター分析を、発現地形図を使用して行った(Kim,et al.(2001),Science,293:2087‐92)。その地形図は、そのデータにおいて固有の主要なクラスターの3次元の概観を提供する。試料は、各エレメントの配置が、miRNA前駆体発現データを使用して算出されたユークリッド距離に基づく多くの最近傍によって影響される、二次元のグリッドに最初にマップされた。第3次元は二次元のグリッド上の点の密度によって判定され、その値は表面として投影されるが、より高いピークは、非常に類似したエレメントのより大きな数を示す。試料の各組間の平均相関もまた算出した。閾値(0.8)超の平均相関を有する試料の各組は、2つの試料を結ぶ線によって発現地形図に示される。これにより、miRNA発現の高相関パターンを有する試料のサブセットの視覚化が可能になる。特定のクラスターからの試料を表すピークは、各ピークの上で着色してコードされた球体によって標識され
た。
【0165】
管理された装置の学習アルゴリズムを、フィルタリングされていないmiRNA発現データに基づいて、試料の分類のために適用した。各miRNAの予測スコアは、訓練、テイクワンアウトクロス確認および試験手順に基づくマイクロアレイアルゴリズムの予測分析(PAM)(Tibshirani R, et al.(2002),Proc Natl Acad Sci USA 99:6567‐72)を使用した発現データの2つのクラスの比較(正常対腫瘍)に基づいて算出した。訓練セットと試験セットとへの試料の分割は、データを無作為に訓練セットと試験セットとに分割する(通常、訓練には2/3。試験には1/3)一般的に認められたアプローチを使用して行う。この研究では、腫瘍試料を、訓練のために約75%に、試験のために25%に無作為に分割した。正常例の数がわずかだった(N=6)ため、正常例は訓練セットのみに含めた。わずかな数の慢性膵炎試料(N=4)は、PAM分析に含めなかった。2つのレベルの精度管理を行っていかなる腫瘍細胞を含む隣接良性組織も除去しつつ、RNAを、顕微解剖した組織ではなく組織全体から抽出した。従って、本発明者等は、いくつかの腫瘍細胞が隣接良性組織を汚染したという可能性を完全に除外することができず、腫瘍に隣接した組織から得られるこれらの良性試料において早期の前癌性変化が発現したのかどうかは不明である。そのため、真の正常例および腫瘍例についてのクラシファイアを訓練するために、良性試料を訓練セットから除外した。良性例については、試験セットにおいて使用した。
【0166】
結果
内部コントロール遺伝子のバリデーション:膵組織はリボヌクレアーゼが豊富であり、RNA単離時には自己分解の可能性を低下させるように注意する必要がある。膵組織から単離されるRNAの完全性を確認するため、約100ngの各RNA試料を、Agilent 2100 Bioanalyzerを使用して検定した。52の組織において、RIN≧4(中央値7.6、範囲4.3〜9.6、(図3))であった。
【0167】
試料のそれぞれにおけるmiRNA前駆体の発現を、リアルタイムPCRを使用して判定し、内部コントロール遺伝子に正規化した。対応量のトータルRNAを各RT反応物に添加し、各種試料(すなわち腫瘍、正常および良性)における平均発現を比較することによって18S rRNAを内部コントロールとして確認した。平均18S rRNA発現においては、腫瘍試料と正常膵臓の間に統計学的有意差がみられなかった(p=0.116、図5)。ここで判定された腫瘍および正常組織における18S rRNA発現は、膵組織についてすでに報告されたもの(Rubie C,et al.,(2005)Mol Cell Probes 19:101‐9)と一致していた。腫瘍群と正常群と良性群との間に18S rRNA発現の有意差がなかったことから、18S rRNAは、その研究の内部コントロール遺伝子として選ばれた。
【0168】
膵組織におけるmiRNA前駆体プロファイリング:2005年4月に見出された222のmiRNAを表す201のmiRNA前駆体の発現を、28の腫瘍、15の隣接良性組織、4つの慢性膵炎検体、6つの正常膵臓組織、および9つの膵臓癌細胞株において測定した。試料の管理されない階層的クラスタリングを、腫瘍、正常膵臓、膵炎および膵臓癌細胞株についてのフィルタリングされていないデータのすべてのセットにおいて実施した。ヒートマップは、201のmiRNA前駆体のみのフィルタリングされていない発現データにより試料が正常な膵臓、腫瘍、慢性膵炎および細胞株のクラスターに十分に分類されることを示す(図6)。
【0169】
同一の膵臓癌患者に由来する15の隣接良性組織のmiRNA発現は、正常膵臓、膵炎、膵腫瘍および癌細胞株とともに含まれていた。miRNA前駆体発現データを、多群ANOVAを使用してフィルタリングした。遺伝子発現データは本質的にノイズが多いため
、データの統計学的フィルタリングは、発現データの前処理の必要な手順であると慣習的に判断される。試料および遺伝子の階層的クラスタリングは、結果として生じた112のmiRNAについて実施した。フィルタリングされたデータの階層的クラスタリングによって、本発明者等は、結果として生じた4つの試料クラスターにおける異なる発現パターンを有するmiRNAの主要な群を同定することができた(図7)。1つのクラスターは、細胞株のみを含んでいた。別のクラスターは、6つのすべての正常膵臓および15の良性組織の内の9つを含んでいた。3番目のクラスターは、4つの慢性膵炎検体および1つの良性組織を含んでいた。最後に、大きなクラスターは、28の腫瘍の内の28および5つの良性組織を含んでいた(図7)。
【0170】
また、フィルタリングされたデータを、発現地形図として知られている種々のクラスタリング法を使用して解析した。地形図から、発現データは、試料の5つの主な群に分けられた(図8)。階層的クラスタリングのように、地形図では、正常膵臓、細胞株、膵臓腺癌および慢性膵炎から試料群が分けられる。この分析は、試料のクラスターのそれぞれが発現地形図上の異なる領域を占めることを示しており、従って、試料の4群のそれぞれがmiRNA発現の異なるパターンを有しており、正常試料と腫瘍試料とを識別するマイクロRNAのサブセットを明らかにする可能性を示唆するものであるというさらなる証拠を提供する。大部分の隣接良性組織は正常と腫瘍とに分類されるが、腫瘍によってクラスター形成されたそれらの良性試料もまた、地形図上の腫瘍で分類される(図8)。地形図のさらなる特徴としては、すべてのmiRNA発現値の平均相関を、試料の各組間で算出した。0.8の閾値を越えるそれらの相関は、miRNA発現パターンが類似した試料の組を結ぶ線として示される。これにより、miRNA発現の高く相関しているパターンを有する試料のサブセットを視覚化することが可能になる。4つの主な群それぞれの中の試料が結ばれるが(すなわち、平均相関>0.8)、腫瘍試料の一部と相関する2つの膵炎試料を除いて群の間に結線はなかった(図8)。
【0171】
異なる膵臓組織の中の遺伝子発現プロファイルの比較を使用して、間質および細胞増殖(例えば細胞株)の寄与を排除し、膵腫瘍において発現する遺伝子を同定した。図7のmiRNA発現データにおけるこのような解析を実施する試みは、癌細胞株における発現が一様に高く、かつ膵炎試料における発現が一様に低かったため、成功しなかった。しかし、多くの腫瘍関連の可能性があるmiRNAは、細胞株および/または腫瘍においては増加したが、正常または膵炎においては増加しないことが同定された(図7)。
【0172】
マイクロアレイアルゴリズムの予測分析(PAM)によるデータ解析:PAM分類アルゴリズムを使用して、miRNA発現データによってどのクラスに試料が適合するのか(腫瘍または正常)を予測することができ、かつ膵臓腺癌に関連した最も重要で、特異に発現したmiRNAを判定することができた。201のpre‐miRNAに関するフィルタリングされていないデータを、Tibshirani R,et al.(2002),Proc Natl Acad Sci USA 99,6567‐72に記載された方法に従って、PAMアルゴリズムにより解析した。75%超の欠測値を有する3つの遺伝子は、補完アルゴリズムの起こり得るアーチファクトを阻止するために分析から除外した。PAM訓練およびクロス確認を、6つの正常膵臓および18の膵腫瘍を使用して実施した。PAMによって、正常および腫瘍試料の100%が正確に分類された(図9A)。PAM試験を、10の腫瘍試料および15の隣接良性試料について実施した。PAMによって、試験された腫瘍試料の100%および試験された15の良性試料の内の11が正確に分類された(図9B)。PAMによって選択された通りの膵臓腺癌において特異に発現した上位68番目までにランクされたmiRNAを図10に示す。PAMによって選択された通りの膵臓腺癌において特異に発現した上位20番目までにランクされたmiRNAを表1に示す。
【0173】
【表1】

【0174】
考察
以下では、膵管腺癌において初めての詳細なmiRNA発現プロファイリング研究の結果を報告する。発現プロファイリングによって、膵管腺癌において異常に発現する多数のmiRNAが同定された。
【0175】
miRNAは、標的mRNAの3’非翻訳領域内の保存配列への結合後の遺伝子発現の負の調節因子として主に機能すると考えられる。miRNAの生物学的役割については、鋭意研究が行われているが、発生のタイミングおよび分化を調節することによって転写因子と類似の方法で細胞内運命を規定かつ維持すると考えられる。発育経路の変化が膵臓癌の発生において重大な役割を果たすことから、miRNA発現の変化は、膵臓腺癌の発生にとって重要な要因である場合がある。
【0176】
miRNA発現プロファイリングによって、腫瘍として、28の組織の内の28が正確に同定された(図9)。全6つの正常膵臓が正しく予測され、15の隣接良性組織の内の11が正常組織として分類された(図9)。ここで示されるデータによって、miRNA発現プロファイリングが特定の癌についての固有の分子サインを作成することができることが示される。
【0177】
腫瘍と正常組織との間に遺伝子発現の差をもたらすと考えられる3つの因子は、正常な腺房、間質および腫瘍細胞である。本発明者等は、RT in situ PCRによって、スクリーニングにおいて同定された特異に発現したmiRNAの内の上位3つが腫瘍細胞に局在していることを確認した(図11)。良性の組織の一部は、正常な膵臓とクラスターを形成することができなかった(図7)。2つのレベルの精度管理を行って腫瘍細胞を汚染したという可能性を低下させたものの、RNAが組織全体から単離されたが、顕微解剖組織からは単離されなかったことから、いくつかの腫瘍細胞が良性組織に存在して
いた可能性がある。別の可能性としては、それらの試料が腫瘍に隣接する組織から得られるので、良性組織の一部に前癌性の変化がすでに発現していたというものである。この考え方を支持するものとしては、大部分の良性試料(および慢性膵炎も)が発現地形図において正常膵臓と腫瘍との間にあるという事実がある(図8)。この観察は、miRNA発現プロファイリングによって、これらの良性組織において起きた前癌性の変化を検出できるということを示す。
【0178】
膵臓癌において特異に発現したmiRNAの一部は、他の癌において異常に発現した。これらには、miR‐155(本研究およびびまん性大細胞型B細胞リンパ腫において増加した);miR‐21(本研究ならびに膠芽細胞腫、乳癌および甲状腺乳頭癌において増加した);miR‐221(膵臓癌、膠芽細胞腫および甲状腺癌において増加した)が含まれる。miR‐221は、X染色体上のmiR‐222から約700bpに位置し;両miR‐221およびmiR‐222は、キットに結合してそれを調節すると予測される。miR‐222前駆体は、上位20位までの特異に発現したmiRNAの中になかったが、PCRによる成熟型miR‐222の次の分析は、miR‐221に類似のレベルで膵臓癌においてmiR‐222が増加したことを示した(データ未掲載)。従って、上述のmiRNAの調節解除は、癌全般に固有であってよい。他の癌において特異に発現したmiRNAは、膵臓癌と同程度には調節解除されなかった。肺癌において減少するlet‐7ファミリーは、ここでは増加した。miR‐17‐92ポリシストロン(miR‐17、‐18、‐19a、‐19b‐1および‐92‐1をコードする)の発現は、リンパ腫および結腸直腸癌において増加したが、膵臓癌においては有意な変化はなかった。本発明者等は、膵臓癌において多くのmiRNA(例えば、本発明者等の知る限りでは他の癌において報告のないmiR‐376aや、miR‐212、miR‐301、miR‐181a)の調節解除を報告する。また、ここで報告された大部分の調節解除されたmiRNAは、正常な膵臓よりも腫瘍の発現が増加したことを示すという事実も興味深い。miR‐375やmiR‐139などの多少のmiRNAは、膵臓癌における発現が低下した(表1、図12〜13)。miR‐375は、膵臓からクローニングされ、膵島細胞特異的であると考えられる(Poy MN,et al.(2004)Nature,432:226‐30)。
【0179】
(実施例2) 膵臓癌組織における成熟型miRNA発現のノーザンブロット法
実施例1において使用されたリアルタイムPCR検定によって、miRNA前駆体が定量化されるが、活性の成熟型miRNAは定量化されない。リアルタイムPCR分析において使用したのと同一のRNAについてノーザンブロット法を実施して、成熟型miRNAが前駆体miRNAと相関したかを確認した。
【0180】
3つの正常膵臓および4組の腫瘍/隣接良性組織に由来する成熟型miR‐100、mir‐375およびmiR‐155の発現レベルは、PCRによるmiRNA前駆体のレベルに近似していた(図12)。miR‐100およびmiR‐155は、上位20位までの特異に発現するmiRNAの中にあった(表1)。miR‐375は、膵臓癌における発現が低下した数少ないmiRNAの内の1つであったため、ノーザンブロット法によって確認した。miR‐375は上位20位までのmiRNAの中になかったが(表1)、前駆体および成熟型miR‐375の両方の発現は、リアルタイムPCRにより、膵臓癌において有意に減少した(p<1×10‐5)。良性および腫瘍対組織におけるmiRNA発現は、すべての例において一貫して増減したが、このことによって、腫瘍と良性との間のmiRNA発現における差は、個々の患者の組織の差によるものであって、群の平均発現の差によるものではないことを示している。
【0181】
ノーザンブロット法:ノーザンブロット法を、Lau NC,et al.(2001),Science 294:858‐62およびSchmittgen TD,et
al.(2004),Nucleic Acids Res 32:E43に既述したように実施した。成熟型miRNAに対する逆相補鎖のDNAオリゴヌクレオチドをプローブとして使用した。ブロットを首尾よくストリップし、3回まで再プローブした。
【0182】
(実施例3) 膵臓癌組織における成熟型miRNAのリアルタイムPCR
実施例1に記載されたリアルタイムPCRデータを、市販されるリアルタイムPCR検定を使用して確認し、成熟型miRNAを増幅および定量化した。成熟型miRNA発現は、PAMから、上位28位までの異常に発現したmiRNAについて確認した。以下の組織に由来するcDNAを検定した:6つの正常膵臓、16の膵臓腺癌およびPAMから正常であると予測された10の隣接良性組織。
【0183】
成熟型miRNA発現は、miRNA前駆体と高度に相関していた(図13および14)。本発明者等の知る限り、これは、感受性リアルタイムPCR検定によって判定される前駆体および成熟型miRNAの両方の発現の最初の発現である。これらの成熟型miRNAについての相対発現値が3log(0.1〜100)にわたったが、腫瘍と正常組織との間の特異な発現における傾向は存続した(図14)ことは興味深い。このことにより、miRNAは異なる発現レベルで腫瘍および正常膵臓において機能するものの、特異な発現が癌と正常組織との間で維持されることが示唆される。
【0184】
成熟型miRNAのリアルタイムPCR。成熟型miRNAを定量化する検定(すなわち、TaqMan(登録商標)マイクロRNA検定、Applied Biosystems、米国カリフォルニア州フォスターシティー)を、1つの変更を伴ってChen,C.,et al.(2005),Nucleic Acids Res 33:el79に記載された通りに実施した。28の異なるアンチセンスループRTプライマーを含む5×カクテルを、Speed Vacにおいて2×原液を濃縮することによって調製した。100ナノグラムのトータルRNAを80℃で5分間加熱し、次いで10μMの18S rRNAアンチセンスプライマーとともに60℃で5分間インキュベートし、その後室温に冷却した。次いで3マイクロリットルの5×ループプライマー混合物を添加し、cDNAを作製した。これにより、28のmiRNA cDNAと18S rRNA内部コントロールのライブラリーの作成が可能になった。リアルタイムPCR(10μLの全体の反応)を、記載された通りにcDNAの1μLの1:50希釈溶液を使用して行った。cDNAの各試料における各成熟型miRNA遺伝子について重複PCRを行った。平均CTを、重複PCRから判定した。上記の通りに遺伝子発現を18S rRNAに比べて算出し、データ提示を単純化するために106を乗算した。
【0185】
(実施例4) 膵臓腫瘍細胞におけるmiRNA前駆体のRT in situ PCR
細胞型miRNA発現を、RT in situ PCRを使用して検討した。miR‐221、miR‐376aおよびmiR‐301は、上位で特異に発現したmiRNA(表1)の中のものであり、かつ正常膵臓および膵炎よりも腫瘍および細胞株において発現が増加したことから、in situ PCRのために選択した(図7)。本発明者等は特にmiR‐376aの細胞型発現に関心があったが、それは、Poy M.N.,et al.(2004),Nature 432,226‐30において膵細胞からクローニングされたためであった。本発明者等の結果から、miR‐221およびmiR‐376aは、腫瘍細胞に局在したが、良性膵腺房または間質細胞(図11)または良性の管(図示せず)には局在しなかったことが示された。また、miR‐301は、腫瘍に局在した(データ未掲載)。
【0186】
RT in situ PCR: RT in situ PCRプロトコルを、Nuovo GJ,et al.(1999),Proc Natl Acad Sci U
SA 96,12754‐9に既述したように実施した。概略説明すると、最適プロテアーゼ消化時間は、レポーターヌクレオチドジゴキシゲニンdUTPの非特異的組み込みを使用して判定した。最適プロテアーゼ消化の後、RNアーゼフリーのDNアーゼ(1試料当たり10U、Boehringer Mannheim、米国インディアナ州インディアナポリス)における一晩のインキュベーションとrTth系およびジゴキシゲニンdUTPを使用したワンステップRT/PCRとを行った。色素原は、ニトロブルーテトラゾリウムおよび対比染色としてヌクレアファストレッドを有するブロモクロロインドリルホスフェート(NBT/BCIP)であった。miR‐221、miR‐301およびmiR‐376aの前駆体に対するプライマー配列は、実施例1におけるプロファイリングのために使用されたものと同様であった。陰性対照においては、プライマーの除外および無関係な(ヒトパピローマウイルスに特異的な)プライマーによる置換が行われたが、それはこのウイルスが膵組織に感染しないためであった。RT in situ PCRは、保存状態のホルマリン固定パラフィン包埋試料1050005A2(T)において行った(図3)。
【0187】
(実施例5) 膵臓特異的miRNAおよび膵臓濃縮miRNAの同定
正常な膵臓組織に特異的であるか、あるいは正常な膵臓組織において濃縮されるかのいずれかのmiRNAを同定するために、184の成熟型miRNAの発現を、22の正常なヒト組織におけるリアルタイムPCRを使用して測定した。これらの組織には、脂肪、膀胱、脳、子宮頚部、大腸、食道、心臓、腎臓、肝臓、肺、骨格筋、卵巣、膵臓、胎盤、前立腺、脾臓、小腸、気管、胸腺、甲状腺、精巣、および正常なB細胞が含まれる。膵臓特異的miRNAは、膵臓においては高発現で、他の21の正常組織においては発現がほとんど検出されないmiRNAと定義された。膵臓濃縮miRNAは、膵臓組織における発現が他の21の組織の平均よりも10倍以上のmiRNAと定義された。膵臓濃縮miRNAは、他の組織の一部に存在してもよい。膵臓特異的miRNAには、miR‐216やmiR‐217が含まれる。膵臓濃縮miRNAには、miR‐7、miR‐148aおよびmiR‐375が含まれる。
【0188】
【表2】

【0189】
(実施例6) 膵臓組織における成熟型miRNAのプロファイリング
膵臓癌において特異に発現するmiRNAを同定するために、9つの膵臓癌腫瘍と、膵
疾患のない6人のドナーからの膵臓とにおけるリアルタイムPCRを使用して、184の成熟型miRNAの発現を測定した。成熟型miRNAは、市販されるリアルタイムPCR検定(TaqMan(登録商標)マイクロRNA検定、Applied Biosystems、米国カリフォルニア州フォスターシティー)を使用して測定した。この検定は、実施例3で説明した通りに実施された。リアルタイムPCRデータは、ヒートマップとして示され、管理されない階層的クラスタリングを使用して解析された(図15)。多少のmiRNAの発現が15の試料のすべてにおいて検知されず、これらのmiRNAはヒートマップに含めなかった。多くの成熟型miRNAは、正常膵臓よりも膵臓腫瘍における発現が増加した。ヒートマップはまた、成熟型miRNA発現プロファイルによって、膵臓腫瘍と正常とを区別することが、その両者が樹状図の分かれた分枝として出現するために可能になることを示す。正常に比べた腫瘍における成熟型miRNA発現の倍率変化およびp値を、図16に示す。
【0190】
(実施例7) 膵臓癌細胞においてmiR‐21の発現が増加
いくつかの方法を使用して、成熟型miR‐21の発現は、膵臓腺癌細胞に局在し、膵臓の腺房、間質および他の非癌細胞には局在しなかったことを示した。(図17)in situ RT‐PCRは、正常膵臓の切片(A)および膵臓癌(B)に適用され、miR‐21の発現増加が腫瘍に局在することを示した。膵管腺癌および正常な(非癌)膵臓管を、レーザー顕微解剖を使用していくつかの検体から単離した。RNAを顕微解剖組織から単離し、次いで18S rRNA内部コントロールと同様に成熟型miR‐21をリアルタイムPCRによって定量化した。成熟型miR‐21は、正常膵臓管(C)よりも顕微解剖腫瘍組織において実質的に増加した。前に記載された通りに成熟型miRNAの市販されるリアルタイムPCR検定を使用して、膵臓腫瘍の9つの検体および6つの正常膵臓検体において、成熟型miR‐21を検定した。成熟型miR‐21発現は、腫瘍(D)において増加した。成熟型miR‐21発現を、2つの正常膵臓上皮細胞株および転移癌に由来する3つと原発性膵臓癌に由来する4つとを含む7つのヒト膵臓癌細胞株におけるリアルタイムPCRによって定量化した。成熟型miR‐21発現は、正常膵臓細胞株(E)よりも7つの膵臓癌細胞株のすべてにおいて増加した。
【特許請求の範囲】
【請求項1】
明細書中に記載の発明。
【請求項1】
明細書中に記載の発明。
【図1】


【図2−1】


【図2−2】


【図2−3】


【図2−4】


【図2−5】


【図2−6】


【図2−7】


【図2−8】


【図2−9】


【図2−10】


【図2−11】


【図2−12】


【図2−13】


【図2−14】


【図3−1】


【図3−2】


【図4−1】


【図4−2】


【図4−3】


【図4−4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10−1】


【図10−2】


【図10−3】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】




【図2−1】


【図2−2】


【図2−3】


【図2−4】


【図2−5】


【図2−6】


【図2−7】


【図2−8】


【図2−9】


【図2−10】


【図2−11】


【図2−12】


【図2−13】


【図2−14】


【図3−1】


【図3−2】


【図4−1】


【図4−2】


【図4−3】


【図4−4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10−1】


【図10−2】


【図10−3】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【公開番号】特開2013−81483(P2013−81483A)
【公開日】平成25年5月9日(2013.5.9)
【国際特許分類】
【外国語出願】
【出願番号】特願2013−23199(P2013−23199)
【出願日】平成25年2月8日(2013.2.8)
【分割の表示】特願2012−188756(P2012−188756)の分割
【原出願日】平成19年3月2日(2007.3.2)
【出願人】(502042458)ザ オハイオ ステイト ユニバーシティ (4)
【Fターム(参考)】
【公開日】平成25年5月9日(2013.5.9)
【国際特許分類】
【出願番号】特願2013−23199(P2013−23199)
【出願日】平成25年2月8日(2013.2.8)
【分割の表示】特願2012−188756(P2012−188756)の分割
【原出願日】平成19年3月2日(2007.3.2)
【出願人】(502042458)ザ オハイオ ステイト ユニバーシティ (4)
【Fターム(参考)】
[ Back to top ]

