臨床分析装置においてスループットを改善する方法
【課題】患者サンプル液を吸引してスライド検査要素へ分注するために使用されるチップ内で患者サンプル特性と分析物の両方又はいずれかを検出するための装置及び方法を提供すること。
【解決手段】まだチップ内にある間に、光を通さない囲い内で近赤外及び近可視放射線を使用してチップを透過度に関して走査し、液体の吸光スペクトルを検出することによって、分光光度分析が液体で行われる。その後又はその前に、分光光度検定を行われていない分析物を検定するために液体が乾式スライド検査要素に分注され、こうして、スループットを向上させる。
【解決手段】まだチップ内にある間に、光を通さない囲い内で近赤外及び近可視放射線を使用してチップを透過度に関して走査し、液体の吸光スペクトルを検出することによって、分光光度分析が液体で行われる。その後又はその前に、分光光度検定を行われていない分析物を検定するために液体が乾式スライド検査要素に分注され、こうして、スループットを向上させる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、血液サンプルを従来通り乾式又は湿式検定法で検査する前に分光光度分析を血液サンプルに関して行うことができるようにする、古い装置の新しい使用法及び新規の分注ステーションに関する。
【背景技術】
【0002】
一般に、分光測光法分析は内容物を決定するために多くの液体に適用される。かかる分析は、近赤外放射線で行われるのであれば、近赤外放射線の標的分析物と他の物質とを差別化する能力のため、特に有効となる。
分光測光法分析はヘモグロビン、アルブミン、脂質、及び他の多数の血清構成成分を確認することが可能であることは、例えば非特許文献1から明らかである。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】欧州特許出願公開第185330号明細書
【特許文献2】米国特許第3992158号明細書
【特許文献3】米国特許第5441895号明細書
【特許文献4】カナダ特許第2019511号明細書
【特許文献5】米国特許第4340390号明細書
【非特許文献】
【0004】
【非特許文献1】臨床化学(Clin.Chem.)第38巻第1623〜1631頁(1992年)
【非特許文献2】分析化学(Anal.Chem.)第59巻第17号第1007A〜1017A頁(1987年9月)
【非特許文献3】分析化学第66巻第15号第795A〜804A頁(1994年8月)
【発明の概要】
【発明が解決しようとする課題】
【0005】
しかしながら、血液サンプルの内容物又は特性を決定するために、かかる分析を血液サンプルに適用する際には問題が存在する。例えば、血液サンプルが最初に、すなわち、1次患者収集容器に取られるので、この分析を血液サンプルに適用するのは困難とされてきた。これらの容器は通常様々な寸法のチューブであり、細胞相から液体血清又は血漿を分離するために遠心分離処理を施されてきた。したがって、このようなチューブは、a)患者識別ラベルを有し、b)血清の様々な予測不能な場所が分析され、c)大量(ミリリットル)のサンプルを必要とする。様々な位置に関しては、細胞相から液体相を分離するために使用されるゲルバリアが液体相の代わりに走査されると、不正確な評価となるのは間違いない。
【0006】
したがって、予測不能な高さの液体のチューブを取り扱うときには、余計な露出をさせ且つ余計な時間をかけて2次チューブに小分けすること、又は、例えば、特許文献1について図3に示されるようにチューブの中身をLED走査することによって、液体相がどこにあるかを確認することが実際的とされてきた。このような必要条件は付加的な装置費用及び処理の遅延を生じさせる。このことは、患者ラベルを通して分光測光法的に走査することの難しさと合わさって、1次収集容器のこのような走査を問題があって高価なものとさせている。
【0007】
他方で、乾式スライド検査要素を使用して標的物質の検査を行う従来の臨床分析装置は、インキュベーションを必要とするのであれば、標的物質の検定を行うためには、通常は少なくとも5分を必要とする。これらのインキュベーション時間がある場合には、毎時1000検査を大きく越すスループットを得ることが困難となる。このような分析装置におけるより高いスループットを可能にする方法が切に必要とされる。
【0008】
このように、本発明の前には、全血から分離される血清又は血漿のような生物学的液体の分光光度走査をする安価で簡単な方法、すなわち、どんな容器が使用されているかに関係なく液体の位置を見つける必要性を除去し、識別ラベルを透過させて走査する必要性をさらに除去する方法を提供する必要性が存在した。さらに、標的物質を検定する分析装置における検査のスループットを向上させる必要性がある。
【課題を解決するための手段】
【0009】
本発明により、分注ステーションと、患者サンプルにおいて標的物質を検出するための少なくとも1つの検査ステーションとを備える臨床分析装置において、前記分注ステーションが、
吸引器プローブと、
1次収集容器から生物学的サンプル液を収集し、収集されたサンプル液の少なくとも一部を検査要素上へ又はその中へ分注するために、前記プローブに取り付けられるチップと、
前記プローブ及び前記チップ内に部分的な圧力又は部分的な真空を生じさせるための手段とを備え、
a)前記プローブに取り付けられるチップの1つに生物学的液体を吸引するステップと、
b)前記生物学的液体がチップ内にあり、チップがプローブに取り付けられている間に、近赤外及び近可視放射線波長の光に複数の波長でチップを透過させることによって、生物学的液体中の1つ又はそれ以上の標的物質を検出し、生物学的液体中の1つ又はそれ以上の標的物質の濃度と透過した光を相関させることによって、チップを透過した光の一部分を複数の波長で分光光度分析を行うステップとを含み、この相関させるステップは吸光度の1次導関数の値を波長の関数として計算するステップを含み、
c)チップから生物学的液体の一部を検査要素へ分注するステップと、
d)前記1つ又はそれ以上の標的物質以外の標的物質に関して、前記検査ステーションで生物学的液体を加えた検査要素を検査するステップとをさらに含み、前記1つ又はそれ以上の標的物質を前記検査ステーションで検査するのに必要とされなくなった時間の量によって、スループットを増加させる、臨床分析装置においてスループットを改善する方法が提供される。
【図面の簡単な説明】
【0010】
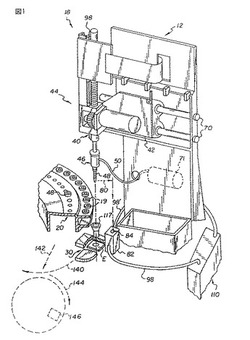
【図1】従来の分析装置の残りの部分における図2(A)及び(B)の走査ロックの位置を示す、分析装置の吸引器プローブの部分等角図である。
【図2】本発明の2つの代替実施態様を示す、装置の中間断面における代替部分立面図である。
【図3】チップが挿入されるときにパルス状の上方圧力が発生することと、チップが取り除かれるときにチップの端部で吸引が発生することとの両方を防止する空気孔を示す、部分的に中間断面で切り取られた図2(A)の検査ステーション82の等角図である。
【図4】本発明の他の代替実施態様の部分等角図である。
【図5】チップ48Aの位置を定めるための機構を示す、図4の構造の一部分の断面平面図である。
【図6】本発明によって分光測光法で走査及び分析された検査サンプルのヘモグロビンの水準に関する回帰プロットである。
【図7】本発明によって分光測光法で走査及び分析された検査サンプルのヘモグロビンの水準に関する回帰プロットである。
【図8】本発明によって分光測光法で走査及び分析された検査サンプルの脂肪血の水準に関する回帰プロットである。
【図9】本発明によって分光測光法で走査及び分析された検査サンプルの脂肪血の水準に関する回帰プロットである。
【図10】本発明によって分光測光法で走査及び分析された検査サンプルの黄疸性の水準に関する回帰プロットである。
【図11】本発明によって分光測光法で走査及び分析された検査サンプルの黄疸性の水準に関する回帰プロットである。
【図12】黄疸、ヘモグロビン、及び脂質のそれぞれのサンプルを示す、本発明によって検出されたスペクトル透過のプロットである。
【図13】図2(A)と類似である、光を通さない囲いの代替実施態様の部分立面図である。
【図14】図2(A)と類似である、光を通さない囲いの代替実施態様の部分立面図である。
【図15】本発明によって分光測光法で走査及び分析された検査サンプルのビリルビンの水準に関する回帰プロットである。
【図16】本発明によって分光測光法で走査及び分析された検査サンプルのビリルビンの水準に関する回帰プロットである。
【図17】図15及び図16と類似である、ヘモグロビンの分析に関する回帰プロットである。
【図18】図15及び図16と類似である、ヘモグロビンの分析に関する回帰プロットである。
【発明を実施するための形態】
【0011】
本発明が好適な実施態様に関して以下で説明され、これらの実施態様においては、好適な(従来の)半透明の使い捨てチップが、血清又は血漿の患者サンプル品質を表す標的に関して分析を行うために、好適な(従来の)分析装置吸引器と、光ファイバを使用している通路によって分光光度計に接続されている好適な光を通さない囲いとで使用されている。しかしながら、さらに、本発明は、標的が十分なNIR及び近可視放射吸収を有する限り、使用される半透明又は透明なチップ、吸引器、液体、又は光を通さない囲いのタイプ、分光光度計への光の通路及びそこからの光の通路となる光学装置、及び検出される標的物質にかかわらず使用される。すなわち、標的物質は、従来の分析装置においてスライド検査要素上で濃度に関して検査されるありきたりの物質、例えば、アルブミン又はぶどう糖であってもよい。液体は全血、尿、又は大脳髄液でもよい。液体は好適には試薬に制限されない。さらに、チップは使い捨てではなくて継続使用するものでよく、光を通さない囲いへ、次に検出ステーションへ光を集めるために、光ファイバの代わりに開レンズシステムが使用されてもよい。
【0012】
本発明と共に使用される分光光度計は以下においては示されず又詳細に関しても説明されていない。その理由は、分光光度計が十分なスペクトル精度を持つ近赤外及び近可視光線領域で放射される放射線を発生させ、透過を介して検出するものであれば、分光光度計はどんなものでも有効であるからである。本願で使用される「近赤外及び近可視」は400nmと2500nmの間の放射線を意味し、最も好ましくは475nmと1075nmの間の放射線を意味する。これらの波長は、使い捨てチップの十分なスペクトル透過並びに標的分析物からの十分なスペクトル吸収を示すので、有利となる。475nmは本発明によってビリルビン検出に特に有効であると考えられている。所望のスペクトル透過を許容する有効なチップ用材料は使い捨てチップを製造するのに一般的に使用されているもの(ポリプロピレン又はポリエチレン)である。
【0013】
さらに本願で使用される「分光光度法(又は分光測光法)」は或る範囲の波長に対するスペクトル応答を捕捉して、その範囲の各波長に関する応答を相関させる方法を意味する。比較として、「測光法」は特定の波長のみに対する反応を相関させる光放射線の分析を意味する。したがって、「分光光度計」はこの分光光度分析を行う装置である。
【0014】
また、本願で使用される「1次患者収集容器」は、患者の生物学的液体、普通は血液が、ラベルを貼られて最初に入れられ、検査のために所望のサンプル液を準備するための処理を施される容器を意味する。全血の場合には、このような処理は、液体血清又は血漿が普通はゲル分離バリアで血球からなる細胞相から分離される相分離を含んでいる。
【0015】
さらに、本願で使用される「検査要素」は少なくとも1つの試薬が予め供給されている任意の容器を意味し、この容器は、例えば特許文献2に記載されているようないわゆる乾式スライド検査要素、あるいは、特許文献3に記載されているような1つ又はそれ以上の抗体で予備被覆された窪み又は試薬を添加されている被覆されていない窪みを有するカップ又はウェルのようなものである。
【0016】
また、本願で使用される「光を通さない」は、検出される光のわずか10%が外部の周囲光によるものとなるような量まで周囲光を排除する効果があることを意味する。
さらにまた、本願で使用される「黄疸がある」は高水準のビリルビン及び/又はビリベルジンがサンプル中に存在する状態を意味する。
【0017】
近赤外及び近可視放射線の生物学的液体の透過量を標的物質の濃度と相関させる際に必要とされる数学的分析に関する詳細は説明されていない。その理由は、このような数学的分析は、特許文献4、非特許文献1の論説、及び、非特許文献2及び非特許文献3の指導論説から明らかであるように公知となっているからである。
【0018】
図1は最新の発明を利用している従来の分析装置12を示している。従来は、分注ステーション18を利用して、トレイ20に複数の1次収集容器19からなる供給物から吸引器プローブ46に取り付けられている使い捨てチップ48へ、例えば血清又は血漿といった生物学的液体のサンプルを吸引によって収集する。続いて、サンプル液が、図示されていないスライド検査要素供給源から獲得されてスライド分配器30に保持されているスライド検査要素Eへ分注される。プローブ46を具備する分注器40の制御は支持ロッド70に取り付けられている垂直方向駆動装置44及び可動台42のような機構によってなされ、このような機構は全て例えば特許文献5に記載されている。任意の種類の従来のポンプ71が部分的な真空又は部分的な圧力をチップ48内に生じさせるための手段として使用される。
【0019】
本発明の1つの態様によれば、単に容器19から液体を吸引によって収集して、続いてスライド検査要素Eへ分注する以外に、新規の方法でのチップ48の使用がなされる。吸引されたサンプル液を搬送するチップ48が、分注のためにホルダ117へ置かれる前に、検査ステーション82へ図1の矢印80の方向に移動される。図2(A)、(B)と図3により明確に示されるように、検査ステーション82は、チップ48を受容する寸法に形成されている空洞84を有する光を通さない効果を有する囲いである走査ブロックを備える。好適には、空洞84は、図3の上部部分86と、上部部分86より小さい内径の下部部分88と、上部部分と下部部分の間の境界の棚部90と、棚部90の空気孔92と、上部部分から離れる方向へ下部部分から延びる円錐状出口孔94と、分光光度計の部分へ向かう及びそこから来る光ファイバ98、98’を受容するのに適した2つの通路96とを備える。出口孔94がチップ48の出口孔部分の形状、よって、この好適なチップ48の場合には円錐状形状と概略合う形状に形成されている。オプションの空気チューブ100がチップから流体をポンプ効果で汲み出す可能性を低減させるために出口孔94に接続される。もし空気チューブが不透明であれば、オプションで、空気チューブはチップへの光の漏れを無くす手助けとなる。
【0020】
図1に示されるように、光ファイバ98、98’が、光源110と、結合されて単一の装置110になっている検出器とを備える従来の分光光度計に接続される。
最大に効果が発揮される場合、検査ステーション82は、本願で定義されている、光を通さない効果があり、検出器へ通過する光は光ファイバ98からチップ48を通って透過される光の少なくとも90%となる。これが達成されることができる方法が幾つかある。
【0021】
第一に、図2(A)に示されるように、拡大されている上部部分111のための支持肩として働き、よって、拡大されている上部部分111よりは高い位置へは行かない上部表面90を有し、チップ48との間に0.5mmの側部隙間があるブロック83を備える検査ステーション82の場合には、発生する光の漏れが、NIR及び近可視放射線が光ファイバ98によって伝送されるときに使用されるのと同じ周囲光条件で(ファイバー98が光を伝送していない状態で)空読み取りを行うことによって補正される。次に、空読み取りがサンプル読み取り及び基準読み取りから引き算される。
【0022】
あるいはまた、引き算される空読み取りが利用されるべきではなく、側部隙間がまだ上述されたのと同じであれば、同じ光不透過性が、図2(B)に示されるように、ブロック83の高さを少なくともチップ48の上部部分111の上部表面113の高さまで延長することによって達成されることができる。
肩表面90へのチップ48の着座は効果的なシールとなるので、好適には、チップ48が挿入及び引き抜かれるときには上部部分86と下部部分88の間である種の空気抜きがなされる。これが図3の空気孔92の機能である。この空気孔は、気泡がチップの液体へ無理に押し通されて、液体の光走査を妨害する可能性がないように、チップが検査ステーション82へ挿入されるときに生じる圧力の増加を解放させる。同様に、光を走査された後で、チップ48が引き抜かれるときに、空気孔92は真空が生じるのを防止するが、この真空はサンプル液の一部をチップ48から吸引することがあり、次のチップ及びサンプルにとって検査ステーション82を汚染する。
【0023】
光ファイバ98及び98’の間の空洞部分88内にチップ48を中心合わせする際にさらなる補助をするために、図3に示されるように、通路96の上の空洞部分88の底部の近くに複数の位置決め突起140を配置することができる。
使用においては、チップ48が、ホルダ116への挿入の前に検査ステーション82へ挿入される。検査ステーション82にある間に、上で定義されたNIR及び近可視波長の光線がチップ及び液体を通過させられ、透過した放射線が分光光度計110で分光光度分析されるようにする。次に、検出器によって生み出される信号が標的物質の濃度との相関関係を算定させられる。標的物質の好適な組は、サンプル特性を測定するもの、詳細には、以下の例で示されるようなヘモグロビン、脂質、ビリルビン(BR)、及びビリベルジン(BV)からなるグループから選択されるものである。しかしながら、吸収スペクトルによって分光光度検出が可能な標的物質はいずれも、本発明によって相関関係を算定されて検出されることができる。さらに詳細には、従来はスライド検査要素Eで行われてきた或る検定が以下で説明されるようにチップを通して分光測光法で行われることができる。
【0024】
その後で、チップが引き抜かれて、ホルダ116に挿入され、この時点で、公知であるようにサンプル液の分析物の濃度を確認するために、サンプル液が従来通り1つ又はそれ以上の試薬を含んでいるスライド検査要素Eに分注される。
容易に明らかとなるように、本発明で使用されるチップ48はNIR及び近可視放射線、最も好適には475nmから1200nmである放射線を透過させることができ、ラベル貼付が1次容器19においてしか行われないので、好適にはラベルがない。この目的に有効な材料はポリプロピレン及びポリエチレンを含む。
【0025】
検査ステーション82が使い捨てチップ用空洞及び光ファイバ用孔のみを有する固体ブロックとして構成される必要はなく、チップが同じところまで降下させられる必要もない。その代わりに、検査ステーション82の側壁が開閉され、図4(A)及び図5に示されるように、チップの通り抜けを可能とさせるスロットを具備することができる。前に説明された部分と類似の部分は同じ参照番号を付されており、この参照番号に区別するための接尾記号「A」が添付されている。
【0026】
したがって、検査ステーション82Aはある距離離されて配置されている2つの固定されている対向部分109、112を備える。各部分は対向する面116、116’を有し、この面がその間にスロット115を画定する。面116、116’の上部表面117は案内レール及びチップ48Aの上部部分111Aのための台座となる。部分109は、図示されていない光源から部分109を通る光ファイバ98Aを有し、一方、部分112は、面116に分光光度計へ接続されているセンサ114を有し、分光光度計は部分112に設けられている又は部分112と接続されている。
【0027】
部分109及び112の対向する面はある距離だけ間隔を空けたスリット115を画定し、このスリット115は使い捨てチップ48Aが矢印120で示されるように滑り抜けることを可能にする。これらの対向する面がチップ48Aの滑り抜けのために一定の距離だけ離間されることができる。
部分109及び112は、矢印120で示されるチップ48Aの通過のために、垂直方向孔84に関して上で説明されたアスペクト比よりもかなり小さいアスペクト比のスロットをつくり出すので、分光光度測定のためにはスロット115を閉じた方がよい。このために、矢印136及び138で示されるように、閉鎖位置(不図示)へ旋回されたときにスロット115を閉鎖するに十分な幅の旋回する扉130、132が参照番号134で示される部分で部分109の両端部へ蝶番式に取り付けられている。(扉132が簡単化のためだけに仮想線で示されている)。扉を旋回するために、好適には蝶番134のピントルが従来のモータ136の回転駆動軸(不図示)に付設されている又は取り付けられている。
【0028】
あるいはまた、扉130及び132が、空洞84に関して上述された垂直アスペクト比に等しい水平方向アスペクト比を有するようにスロット115を長くすることによって、省略されることができる。
図5に示される光ファイバ98A及び検出器114のところでチップ48Aの矢印120で示されるような横方向の運動を精度良く止める補助をするために、好適には、ばね付勢されている移動止め210が面116に設けられ、この移動止め210は反対側の面116’にある固定されている突起212と協動する。読み取り後、矢印120の方向にスロット115からチップ48Aを移動させるときには、移動止め210がチップによって面116へ押し付けられる。前出の実施態様において述べられたように、チップ48Aは使用されるNIR及び近可視波長を透過させる。
【0029】
あるいはまた、図4(B)に示される部分112Bが光の漏れをふさぐために板122Bに可動に取り付けられることができる。前に説明された部分に類似の部分は同じ参照番号を付されており、この参照番号に区別するための接尾記号「B」が添付されている。したがって、検査ステーション82Bは、面116B及び116’Bと共にU字形状スロットを形成する板122Bを備え、このU字形状スロットはチップ48Bが上部表面117Bに支持されると同時に矢印120Bで示されるように滑り抜けることを可能にさせる。光ファイバ98Bは静止部分130Bを通して光を伝送し、静止面116Bのセンサ114Bは図示されていない分光光度計へ光を伝送する。
【0030】
板122Bと面116B及び116’BからなるU字形状スロットを通して起こり得る光の漏れをふさぐために、部分112Bが板122Bを滑動するように取り付けられ、ラック162及びドライブピニオン164によって矢印168に駆動され、スロットを開放又は閉鎖する。閉鎖されると、面116B及びチップ48Bが部分112B内の空間172を占有し、壁部分169がスロット115Bを閉鎖する。
【0031】
患者サンプルの特性に関する検査に加えて、NIR及び近可視波長を使用して分光光度分析が可能である標的物質はいずれも、患者サンプルがチップ48Aにある間に分光光度計110によって分析されることができる。これらの標的物質は数あるなかでヘモグロビン、アルブミン、ぶどう糖を含む。チップ内のこれらの標的物質を検査することによって、必ずではないが、実際には、サンプルがスライド検査要素Eに置かれたときに、好適には、分析装置はそれらの標的物質に関するさらなるそれ以上の検定を抜かす。チップを通した分光光度検出はスライド検査要素Eで行われる個別の各検定での4秒と比較して、分析される標的物質全てで4秒しか必要としないので、このことは分析装置の全体スループット大幅に向上させる。「結果を出す時間」がさらにチップを通しての分光光度分析によって劇的に改善され、スライド検査要素の場合の5分と比較してチップを通しての場合には4秒となる。
【0032】
向上されたスループットの例として、以下がジョンソン&ジョンソン・クリニカルダイガノスティックス(Johnson&Johnson Clinical Diagnostics)から商標「VITROS950」分析装置で販売されているような分析装置で達成され得る利点の推定である。この推定は、スライド検査要素へのサンプル液の分注は分析における制限ステップであることと、分注ステップは吸引に8秒、検査要素への分注して検査要素をVITROS950(商標)分析装置の分配器ヘ装填するのに4秒などを必要とすることと、本発明によって比色定量分析がチップ内で行われることのみを仮定している。
【0033】
行われるべき化学的性質の混合比が電位差検査0、比色検査7、示差(rate)検査0であれば、本発明を用いない場合には、スループットは毎時300検査要素である。本発明を用いた場合には、スループットは毎時2100検査となることが示され、これは7倍の増加である。他方で比色検査5のみ、示差検査2又は電位差検査2のいずれかが行われるのであれば、本発明を用いない場合のスループットは毎時420検査で、本発明を用いた場合は毎時1050検査となり、2.5倍の増加である。さらにまた、7つ化学的性質の混合比が比色検査3のみ、電位差検査4で行われるとすれば、本発明を行うことによって得られるスループットの増加はない(両方の場合とも毎時525検査である)。
【0034】
好適には、チップ内にある間のかかる分析物のこのような検査がサンプル液のある種の温度制御と共に行われる。このことは、検査ステーション82において温度を制御することによって行われることを必要とするだけでなく、図1の容器19内のサンプル液を加熱する又は冷却することによって行われることができる又はサンプル液がチップ48等にある間に加熱又は冷却することによって行われることができるが、検査ステーション82では加熱又は冷却は行われない。
【0035】
しかしながら、スライド検査要素Eの使用を必要とする検定が依然として幾つかある。工程が図1に略図的に示されている。チップ48がホルダ117に挿入され、患者サンプルの一部がスライド検査要素Eに分注される。その後、分配器30が、検査要素Eが矢印142にインキュベータ(不図示)へ直線的に移送される位置へ矢印140に回転され、インキュベータ内で検査要素Eが、検査ステーション146において読み取られる又は検出されるまで矢印144へ回転されるが、以上全ては、公知であり、従来のものである。検査ステーション146は、チップ48、48Aと共に使用される分光光度計110とは対照的に、従来通り比色検出器又は電位差検出器を備える。
【0036】
上述されたように、好適には、検査ステーション146で行われる検査はチップを通して行われる検査を抜かすけれども、チップ内で行われる検査の精度の「確認」をするために、かかる分光測光法検定を検査ステーション146で繰り返すことも可能である。
検査の順番を逆にすることも考えられる、すなわち、NIR及び近可視波長でチップを通した測定を行う前に、サンプル液の一部を上述されたように検査スライドに置くこともできる。
【0037】
本発明を説明するために、以下の非消耗的検査を行う。
図2の装置が使用され、この装置においては、以前は「エクタケム(Ektachem)」使い捨てチップとして知られていた商標「ビトロス(Vitros)」でジョンソン&ジョンソン・クリニカルダイガノスティックス社から販売されている使い捨てチップが使用された。光ファイバは0.2mmシングルファイバであり、これによってファイバ98及び98’を介して検査ステーション82を「TC2000」二重光線同期分光光度計へ接続しており、この分光光度計はCMEテレメトリクス(Telemetrix)から販売している検出器112としてタングステン−ハロゲン白熱電球光源110を使用している線形ダイオード配列検出器を使用している。580nmから1100nmまでの放射線のみを検出できるようにするために、検出器112では回折格子が使用された。(分光光度計の基準光線部分は明確化のために省略されている)。チップ48に吸引される液体の量は液体の高さが図2の通過矢印200の完全に上となるように50μLとした。実証された30μLのみを検査することが必要とされる。
【0038】
検査される液体は、第一に較正液として、ヘモグロビンと、ファルマシア(Pharamacia)社から販売されているイントラリピド(Intralipid)(商標)(自然発生乳状脂粒を擬態する脂肪乳液)と、ビリベルジンとを含む既知量の液体を無作為に組合わせたものであり、これらの液体全てが人血清基質に加えられている。
【0039】
以下の表1は添加後の血清中のHb、IL、及びBVを示している。「Hb」はヘモグロビンを、「IL」はイントラリピド(商標)を、「BV」はビリベルジンを、「BR」はビリルビンを意味する。
【0040】
【表1】

【0041】
同様に準備された21種の液体の第二の組み合わせは表2の構成成分を有するように準備され、未知のものとして取り扱われた。
【0042】
【表2】

【0043】
液体の第一の組み合わせが、従来の分光光度手法を用いる較正アルゴリズムを作り出すために上述されたように放射線照射され、この測定で検出されたHbの値が回帰グラフを得るために図6のように実際の値に対してグラフに記入された。種々の較正アルゴリズムが有効であり、例えば、一次及び二次導関数によって式を選択する。以下の等式は単に例示的なものである。
1)Hb(g/L)=C1 (dA600 /dλ600 )−C2 (dA663 /dλ663 )−C3
2)IL(g/L)=C4 (dA874 /dλ874 )+C5
3)BV(mg/dL)=C6 (dA724 /dλ724 )−C(dA803 /dλ803 )+C8
ここで、A600 は600nmにおける吸光度、λ600 は600nmの波長、その他のA及びλの値に関しても同じであり、(dAi /dλi )は波長に対する吸光度の1次導関数、C1 、…C9 は好適には以下の値を有する定数である。
【0044】
C1 =15.892 C5 =0.244
C2 =15.882 C6 =98.068
C3 =0.21 C7 =122.732
C4 =252.155 C8 =0.0685
図6の場合の回帰相関係数R2 は0.991であった。
【0045】
次に、液体の第二の組み合わせが上述のように放射線照射され、液体の第一の組み合わせから導かれた図6の較正アルゴリズムを使用して、予測値が図7のように既知の結果に対してグラフに記入された。0.982というR2 の値は優秀である。この精度は、スライド検査要素における検査に代わって、この結果を未知のサンプル内のHbの臨床検定に信頼して適用することを可能にするのに適したものである。
【0046】
同様に、上述されたように検出されたスペクトルの数値がILに関して評価された。較正の結果は図8に示されており、予測の結果が図9に示されている。この場合のR2 はそれぞれ0.9941と0.9878である。
また、記述されたスペクトルが評価されたが、今度の分析はBVに関するものであった。図10は較正の結果を示しており、図11はR2 の値が示されるようなものである予測の結果を示している。
【0047】
新しい、第三の液体の組み合わせがビリルビンの検出に関して本発明を説明するために用意され、その組み合わせの較正液の形式は以下の表のように構成された。
【0048】
【表3】

【0049】
この検査に使用された較正アルゴリズムは以下のようなものであった。
4)BR(mg/dL)=C9 (dA495 /dλ495 )+C10(dA512 /dλ512 )+C11(dA578 /dλ578 )−C12
定数は以下のようになった。
C9 =−24.878
C10=201.61
C11=44.98
C12=6.475
液体の第四の組み合わせがビリルビンの値の予測に関する確認のために同様に用意され、その組み合わせは以下の表のように構成された。
【0050】
【表4】

【0051】
スペクトルが前出の例と同じように評価された。図15は較正の結果を示し、図16はR2 の値が示されるようなものである予測の結果を示している。
4つの実験(Hb、IL、BV、及びBR)全てに関して、その結果は優れた相関を示し、その結果はスライド検査要素での検査に代わって使用するに十分であり、これらのいずれもが所望の検定と見なされるべきものである。いずれにしても、これらの結果は明らかに生物学的液体のサンプルの特性を確認することを可能にし、そのサンプルが許容可能な特性の範囲の外側にあると判定されたなら不合格とすることができるようにする。
【0052】
用いることができる他の較正アルゴリズムの例として、ILに関して以下のものが上式#2の代替式となる。
2’)IL(g/L)=C13(dA999 /dλ999 )+C14(dA1051/dλ1051)−C15
ここで、C13=166.068、C14=92.352、C15=0.693である。この較正アルゴリズムが上述の第一及び第二の液体の組み合わせに関して用いられると、R2 は較正に関して0.988となり、予測に関して0.984となる。(実際のプロットは示されていない)。
【0053】
再び図7に関して、上述されたヘモグロビンの存在を確認するための方法が、5g/Lまででは、直線性、すなわち測定の正確性を示したことが明らかとなる。5g/Lを越えると、データは「真値」から離れていく傾向がある。このことは図17において最も明確に示されている。したがって、もし5g/Lより多くの量が含有されているようであれば、別な組み合わせのアルゴリズムの方が好ましい。
【0054】
より詳細には、全範囲を網羅するために2つの異なるアルゴリズムが使用されるのであれば、真の曲線とのより優れた追従性が達成され、これらのアルゴリズムが重なり部分で連続的なデータを示すように選択される。好適には、3g/Lから上で用いられるアルゴリズムはg/L単位のヘモグロビン濃度の自然対数である。最も好適には、3g/Lから35g/Lまででは、用いられるアルゴリズムは以下の形態である。
【0055】
【数1】

【0056】
ここで、C16、C17、C18の詳細な例はC16=−17.38、C17=+9.96+C18=+0.37である。
3g/L以下には、上で示された式1)に類似の型の様々なアルゴリズムが有効である。3g/Lより上で式5)とかみ合うために、非常に好適な式は以下の式となる。
1’)Hb(g/L)=C19(dA593 /dλ593 )+C20(dA608 /dλ608 )+C21
ここで、C19は好適には−66.689、C20は好適には81.081、C21は好適には−0.25である。
【0057】
図17に示されるヘモグロビンの水準が3g/L以上及び3g/L以下に上述の新しいアルゴリズム5)及び1’)を用いて再計算されたときに、図18のプロットが結果として得られた。このプロットは、予測された値が図17のデータ点で得られるものよりも45°の「真」の直線により近くなることを示している。
【0058】
図18のデータは10g/Lまでしか延びていないが、希釈なしステップを用いることによって、式5)及び式1’)がヘモグロビンの値に関しては35g/Lまで有効となることが示された。
図12は、実際にNIR及び近可視スペクトルにおける吸光度の一次導関数の値が、有効波長において、IL、BV、又はHb構成成分が存在するサンプルの独立した検出を可能にするのに十分に分離していることを示すプロットである。すなわち、曲線200はそれらの構成成分のいずれも有さないサンプル、曲線202は1.79g/LのHbのみを有するサンプル、曲線204は2.38g/LのILのみを有するサンプル、曲線206は3.95mg/dLのBVのみを有するサンプルである。したがって、Hbは主としてNIRの580〜605nmの領域に寄与し、ILは896〜1051nmの領域、好適には896〜939nmに寄与し、BVは680〜750nmの領域に寄与する。
【0059】
さらに別の実施態様においては、チップが従来のチップから変更されていないが、図13の吸収スペクトルが受光される前に、分光光度計によって1本より多くのNIR及び近可視放射線のチップを通した通過が達成される。前述された部分が同じ参照番号によって参照されており、この参照番号に区別するための接尾語「D」が添付されている。
【0060】
したがって、光ファイバ98Dから放射しているNIR及び近可視放射線による放射線照射が処理用光ファイバ98’Dによって受光されるように、チップ48Dが前述のように空洞84Dにはめ込まれる。しかしながら、前出の実施態様と異なり、受光用光ファイバ98’Dは発光用光ファイバ98Dと直接に向かい合ってもいなければ、「第一通過」放射線を受光する位置にもない。代わりに、少なくとも1対の、好適には3対の鏡(230、232;240、242;250、252)が、鏡と同じ回数だけ放射線にチップ48Dを再度通過させるように配置される。(3対からなる6枚の鏡は放射線に6回チップを透過させる)。
【0061】
さらに別の実施態様においては、光ファイバ98、98’(又は上で開示された他の型の光ファイバ)はNIR及び近可視光にチップの最も厚い部分のみを通過させる必要はない。その代わりに、光がより狭い首部分を透過させることができる。(前に説明された部分と同様の部分は同じ参照番号を冠しており、区別のための接尾語「E」が添付されている)。
【0062】
したがって、図14の照射用光ファイバ98Eがチップ48Eの円錐状首部分300を放射線照射するように検査ステーション82Eのブロックに配置されており、この首部分は本体部分224Eの直径「d」と比較して直径が小さくなっていく。次に、チップを通って受光用光ファイバ98’Eへ透過させられる光はサンプルのずっと狭い部分を通過する。検出される分析物が高密度のものである又は当のNIR及び近可視波長に対して高吸光係数を有しているのであれば、これが所望される。最も極端な場合には、光ファイバ98E及び98’Eが、チップ48Eの最も狭い部分304を通して読み取る仮想位置302まで下に移動される。
【0063】
あるいはまた、チップのより狭い部分をNIR及び近可視放射線が通過することが、前出の実施態様を用いて、単に検査ステーション82内でチップ(及びプローブ)を十分に持ち上げてNIR放射線で照射することによっても達成され得る。さらに好適には、ステップの順番は、図2(A)(B)、図4(A)(B)のいずれかに示されるようなNIR及び近可視放射線放射源を含む光を通さない囲いに、チップが着座するまでチップを下降させるステップ、放射源から放射されるNIR及び近可視放射線でチップ及びその中身を走査するステップ、もし中身が所定の閾値を上回る密度を有するなら、その後、放射源がチップのより狭い部分を走査するように配置されるまで囲いの中でチップを持ち上げるステップという順番となる。
【0064】
分析装置における標的物質の検定のスループットを向上させることが本発明の有利な特徴である。
さらに別な有利な特徴は、分光測光法での分析にインキュベーション時間が必要とされないことから、結果がより短い時間で得られることである。
【符号の説明】
【0065】
12 分析装置
18 分注ステーション
19 1次収集容器
46 吸引器プローブ
48 チップ
71 ポンプ
82 検査ステーション
【技術分野】
【0001】
本発明は、血液サンプルを従来通り乾式又は湿式検定法で検査する前に分光光度分析を血液サンプルに関して行うことができるようにする、古い装置の新しい使用法及び新規の分注ステーションに関する。
【背景技術】
【0002】
一般に、分光測光法分析は内容物を決定するために多くの液体に適用される。かかる分析は、近赤外放射線で行われるのであれば、近赤外放射線の標的分析物と他の物質とを差別化する能力のため、特に有効となる。
分光測光法分析はヘモグロビン、アルブミン、脂質、及び他の多数の血清構成成分を確認することが可能であることは、例えば非特許文献1から明らかである。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】欧州特許出願公開第185330号明細書
【特許文献2】米国特許第3992158号明細書
【特許文献3】米国特許第5441895号明細書
【特許文献4】カナダ特許第2019511号明細書
【特許文献5】米国特許第4340390号明細書
【非特許文献】
【0004】
【非特許文献1】臨床化学(Clin.Chem.)第38巻第1623〜1631頁(1992年)
【非特許文献2】分析化学(Anal.Chem.)第59巻第17号第1007A〜1017A頁(1987年9月)
【非特許文献3】分析化学第66巻第15号第795A〜804A頁(1994年8月)
【発明の概要】
【発明が解決しようとする課題】
【0005】
しかしながら、血液サンプルの内容物又は特性を決定するために、かかる分析を血液サンプルに適用する際には問題が存在する。例えば、血液サンプルが最初に、すなわち、1次患者収集容器に取られるので、この分析を血液サンプルに適用するのは困難とされてきた。これらの容器は通常様々な寸法のチューブであり、細胞相から液体血清又は血漿を分離するために遠心分離処理を施されてきた。したがって、このようなチューブは、a)患者識別ラベルを有し、b)血清の様々な予測不能な場所が分析され、c)大量(ミリリットル)のサンプルを必要とする。様々な位置に関しては、細胞相から液体相を分離するために使用されるゲルバリアが液体相の代わりに走査されると、不正確な評価となるのは間違いない。
【0006】
したがって、予測不能な高さの液体のチューブを取り扱うときには、余計な露出をさせ且つ余計な時間をかけて2次チューブに小分けすること、又は、例えば、特許文献1について図3に示されるようにチューブの中身をLED走査することによって、液体相がどこにあるかを確認することが実際的とされてきた。このような必要条件は付加的な装置費用及び処理の遅延を生じさせる。このことは、患者ラベルを通して分光測光法的に走査することの難しさと合わさって、1次収集容器のこのような走査を問題があって高価なものとさせている。
【0007】
他方で、乾式スライド検査要素を使用して標的物質の検査を行う従来の臨床分析装置は、インキュベーションを必要とするのであれば、標的物質の検定を行うためには、通常は少なくとも5分を必要とする。これらのインキュベーション時間がある場合には、毎時1000検査を大きく越すスループットを得ることが困難となる。このような分析装置におけるより高いスループットを可能にする方法が切に必要とされる。
【0008】
このように、本発明の前には、全血から分離される血清又は血漿のような生物学的液体の分光光度走査をする安価で簡単な方法、すなわち、どんな容器が使用されているかに関係なく液体の位置を見つける必要性を除去し、識別ラベルを透過させて走査する必要性をさらに除去する方法を提供する必要性が存在した。さらに、標的物質を検定する分析装置における検査のスループットを向上させる必要性がある。
【課題を解決するための手段】
【0009】
本発明により、分注ステーションと、患者サンプルにおいて標的物質を検出するための少なくとも1つの検査ステーションとを備える臨床分析装置において、前記分注ステーションが、
吸引器プローブと、
1次収集容器から生物学的サンプル液を収集し、収集されたサンプル液の少なくとも一部を検査要素上へ又はその中へ分注するために、前記プローブに取り付けられるチップと、
前記プローブ及び前記チップ内に部分的な圧力又は部分的な真空を生じさせるための手段とを備え、
a)前記プローブに取り付けられるチップの1つに生物学的液体を吸引するステップと、
b)前記生物学的液体がチップ内にあり、チップがプローブに取り付けられている間に、近赤外及び近可視放射線波長の光に複数の波長でチップを透過させることによって、生物学的液体中の1つ又はそれ以上の標的物質を検出し、生物学的液体中の1つ又はそれ以上の標的物質の濃度と透過した光を相関させることによって、チップを透過した光の一部分を複数の波長で分光光度分析を行うステップとを含み、この相関させるステップは吸光度の1次導関数の値を波長の関数として計算するステップを含み、
c)チップから生物学的液体の一部を検査要素へ分注するステップと、
d)前記1つ又はそれ以上の標的物質以外の標的物質に関して、前記検査ステーションで生物学的液体を加えた検査要素を検査するステップとをさらに含み、前記1つ又はそれ以上の標的物質を前記検査ステーションで検査するのに必要とされなくなった時間の量によって、スループットを増加させる、臨床分析装置においてスループットを改善する方法が提供される。
【図面の簡単な説明】
【0010】
【図1】従来の分析装置の残りの部分における図2(A)及び(B)の走査ロックの位置を示す、分析装置の吸引器プローブの部分等角図である。
【図2】本発明の2つの代替実施態様を示す、装置の中間断面における代替部分立面図である。
【図3】チップが挿入されるときにパルス状の上方圧力が発生することと、チップが取り除かれるときにチップの端部で吸引が発生することとの両方を防止する空気孔を示す、部分的に中間断面で切り取られた図2(A)の検査ステーション82の等角図である。
【図4】本発明の他の代替実施態様の部分等角図である。
【図5】チップ48Aの位置を定めるための機構を示す、図4の構造の一部分の断面平面図である。
【図6】本発明によって分光測光法で走査及び分析された検査サンプルのヘモグロビンの水準に関する回帰プロットである。
【図7】本発明によって分光測光法で走査及び分析された検査サンプルのヘモグロビンの水準に関する回帰プロットである。
【図8】本発明によって分光測光法で走査及び分析された検査サンプルの脂肪血の水準に関する回帰プロットである。
【図9】本発明によって分光測光法で走査及び分析された検査サンプルの脂肪血の水準に関する回帰プロットである。
【図10】本発明によって分光測光法で走査及び分析された検査サンプルの黄疸性の水準に関する回帰プロットである。
【図11】本発明によって分光測光法で走査及び分析された検査サンプルの黄疸性の水準に関する回帰プロットである。
【図12】黄疸、ヘモグロビン、及び脂質のそれぞれのサンプルを示す、本発明によって検出されたスペクトル透過のプロットである。
【図13】図2(A)と類似である、光を通さない囲いの代替実施態様の部分立面図である。
【図14】図2(A)と類似である、光を通さない囲いの代替実施態様の部分立面図である。
【図15】本発明によって分光測光法で走査及び分析された検査サンプルのビリルビンの水準に関する回帰プロットである。
【図16】本発明によって分光測光法で走査及び分析された検査サンプルのビリルビンの水準に関する回帰プロットである。
【図17】図15及び図16と類似である、ヘモグロビンの分析に関する回帰プロットである。
【図18】図15及び図16と類似である、ヘモグロビンの分析に関する回帰プロットである。
【発明を実施するための形態】
【0011】
本発明が好適な実施態様に関して以下で説明され、これらの実施態様においては、好適な(従来の)半透明の使い捨てチップが、血清又は血漿の患者サンプル品質を表す標的に関して分析を行うために、好適な(従来の)分析装置吸引器と、光ファイバを使用している通路によって分光光度計に接続されている好適な光を通さない囲いとで使用されている。しかしながら、さらに、本発明は、標的が十分なNIR及び近可視放射吸収を有する限り、使用される半透明又は透明なチップ、吸引器、液体、又は光を通さない囲いのタイプ、分光光度計への光の通路及びそこからの光の通路となる光学装置、及び検出される標的物質にかかわらず使用される。すなわち、標的物質は、従来の分析装置においてスライド検査要素上で濃度に関して検査されるありきたりの物質、例えば、アルブミン又はぶどう糖であってもよい。液体は全血、尿、又は大脳髄液でもよい。液体は好適には試薬に制限されない。さらに、チップは使い捨てではなくて継続使用するものでよく、光を通さない囲いへ、次に検出ステーションへ光を集めるために、光ファイバの代わりに開レンズシステムが使用されてもよい。
【0012】
本発明と共に使用される分光光度計は以下においては示されず又詳細に関しても説明されていない。その理由は、分光光度計が十分なスペクトル精度を持つ近赤外及び近可視光線領域で放射される放射線を発生させ、透過を介して検出するものであれば、分光光度計はどんなものでも有効であるからである。本願で使用される「近赤外及び近可視」は400nmと2500nmの間の放射線を意味し、最も好ましくは475nmと1075nmの間の放射線を意味する。これらの波長は、使い捨てチップの十分なスペクトル透過並びに標的分析物からの十分なスペクトル吸収を示すので、有利となる。475nmは本発明によってビリルビン検出に特に有効であると考えられている。所望のスペクトル透過を許容する有効なチップ用材料は使い捨てチップを製造するのに一般的に使用されているもの(ポリプロピレン又はポリエチレン)である。
【0013】
さらに本願で使用される「分光光度法(又は分光測光法)」は或る範囲の波長に対するスペクトル応答を捕捉して、その範囲の各波長に関する応答を相関させる方法を意味する。比較として、「測光法」は特定の波長のみに対する反応を相関させる光放射線の分析を意味する。したがって、「分光光度計」はこの分光光度分析を行う装置である。
【0014】
また、本願で使用される「1次患者収集容器」は、患者の生物学的液体、普通は血液が、ラベルを貼られて最初に入れられ、検査のために所望のサンプル液を準備するための処理を施される容器を意味する。全血の場合には、このような処理は、液体血清又は血漿が普通はゲル分離バリアで血球からなる細胞相から分離される相分離を含んでいる。
【0015】
さらに、本願で使用される「検査要素」は少なくとも1つの試薬が予め供給されている任意の容器を意味し、この容器は、例えば特許文献2に記載されているようないわゆる乾式スライド検査要素、あるいは、特許文献3に記載されているような1つ又はそれ以上の抗体で予備被覆された窪み又は試薬を添加されている被覆されていない窪みを有するカップ又はウェルのようなものである。
【0016】
また、本願で使用される「光を通さない」は、検出される光のわずか10%が外部の周囲光によるものとなるような量まで周囲光を排除する効果があることを意味する。
さらにまた、本願で使用される「黄疸がある」は高水準のビリルビン及び/又はビリベルジンがサンプル中に存在する状態を意味する。
【0017】
近赤外及び近可視放射線の生物学的液体の透過量を標的物質の濃度と相関させる際に必要とされる数学的分析に関する詳細は説明されていない。その理由は、このような数学的分析は、特許文献4、非特許文献1の論説、及び、非特許文献2及び非特許文献3の指導論説から明らかであるように公知となっているからである。
【0018】
図1は最新の発明を利用している従来の分析装置12を示している。従来は、分注ステーション18を利用して、トレイ20に複数の1次収集容器19からなる供給物から吸引器プローブ46に取り付けられている使い捨てチップ48へ、例えば血清又は血漿といった生物学的液体のサンプルを吸引によって収集する。続いて、サンプル液が、図示されていないスライド検査要素供給源から獲得されてスライド分配器30に保持されているスライド検査要素Eへ分注される。プローブ46を具備する分注器40の制御は支持ロッド70に取り付けられている垂直方向駆動装置44及び可動台42のような機構によってなされ、このような機構は全て例えば特許文献5に記載されている。任意の種類の従来のポンプ71が部分的な真空又は部分的な圧力をチップ48内に生じさせるための手段として使用される。
【0019】
本発明の1つの態様によれば、単に容器19から液体を吸引によって収集して、続いてスライド検査要素Eへ分注する以外に、新規の方法でのチップ48の使用がなされる。吸引されたサンプル液を搬送するチップ48が、分注のためにホルダ117へ置かれる前に、検査ステーション82へ図1の矢印80の方向に移動される。図2(A)、(B)と図3により明確に示されるように、検査ステーション82は、チップ48を受容する寸法に形成されている空洞84を有する光を通さない効果を有する囲いである走査ブロックを備える。好適には、空洞84は、図3の上部部分86と、上部部分86より小さい内径の下部部分88と、上部部分と下部部分の間の境界の棚部90と、棚部90の空気孔92と、上部部分から離れる方向へ下部部分から延びる円錐状出口孔94と、分光光度計の部分へ向かう及びそこから来る光ファイバ98、98’を受容するのに適した2つの通路96とを備える。出口孔94がチップ48の出口孔部分の形状、よって、この好適なチップ48の場合には円錐状形状と概略合う形状に形成されている。オプションの空気チューブ100がチップから流体をポンプ効果で汲み出す可能性を低減させるために出口孔94に接続される。もし空気チューブが不透明であれば、オプションで、空気チューブはチップへの光の漏れを無くす手助けとなる。
【0020】
図1に示されるように、光ファイバ98、98’が、光源110と、結合されて単一の装置110になっている検出器とを備える従来の分光光度計に接続される。
最大に効果が発揮される場合、検査ステーション82は、本願で定義されている、光を通さない効果があり、検出器へ通過する光は光ファイバ98からチップ48を通って透過される光の少なくとも90%となる。これが達成されることができる方法が幾つかある。
【0021】
第一に、図2(A)に示されるように、拡大されている上部部分111のための支持肩として働き、よって、拡大されている上部部分111よりは高い位置へは行かない上部表面90を有し、チップ48との間に0.5mmの側部隙間があるブロック83を備える検査ステーション82の場合には、発生する光の漏れが、NIR及び近可視放射線が光ファイバ98によって伝送されるときに使用されるのと同じ周囲光条件で(ファイバー98が光を伝送していない状態で)空読み取りを行うことによって補正される。次に、空読み取りがサンプル読み取り及び基準読み取りから引き算される。
【0022】
あるいはまた、引き算される空読み取りが利用されるべきではなく、側部隙間がまだ上述されたのと同じであれば、同じ光不透過性が、図2(B)に示されるように、ブロック83の高さを少なくともチップ48の上部部分111の上部表面113の高さまで延長することによって達成されることができる。
肩表面90へのチップ48の着座は効果的なシールとなるので、好適には、チップ48が挿入及び引き抜かれるときには上部部分86と下部部分88の間である種の空気抜きがなされる。これが図3の空気孔92の機能である。この空気孔は、気泡がチップの液体へ無理に押し通されて、液体の光走査を妨害する可能性がないように、チップが検査ステーション82へ挿入されるときに生じる圧力の増加を解放させる。同様に、光を走査された後で、チップ48が引き抜かれるときに、空気孔92は真空が生じるのを防止するが、この真空はサンプル液の一部をチップ48から吸引することがあり、次のチップ及びサンプルにとって検査ステーション82を汚染する。
【0023】
光ファイバ98及び98’の間の空洞部分88内にチップ48を中心合わせする際にさらなる補助をするために、図3に示されるように、通路96の上の空洞部分88の底部の近くに複数の位置決め突起140を配置することができる。
使用においては、チップ48が、ホルダ116への挿入の前に検査ステーション82へ挿入される。検査ステーション82にある間に、上で定義されたNIR及び近可視波長の光線がチップ及び液体を通過させられ、透過した放射線が分光光度計110で分光光度分析されるようにする。次に、検出器によって生み出される信号が標的物質の濃度との相関関係を算定させられる。標的物質の好適な組は、サンプル特性を測定するもの、詳細には、以下の例で示されるようなヘモグロビン、脂質、ビリルビン(BR)、及びビリベルジン(BV)からなるグループから選択されるものである。しかしながら、吸収スペクトルによって分光光度検出が可能な標的物質はいずれも、本発明によって相関関係を算定されて検出されることができる。さらに詳細には、従来はスライド検査要素Eで行われてきた或る検定が以下で説明されるようにチップを通して分光測光法で行われることができる。
【0024】
その後で、チップが引き抜かれて、ホルダ116に挿入され、この時点で、公知であるようにサンプル液の分析物の濃度を確認するために、サンプル液が従来通り1つ又はそれ以上の試薬を含んでいるスライド検査要素Eに分注される。
容易に明らかとなるように、本発明で使用されるチップ48はNIR及び近可視放射線、最も好適には475nmから1200nmである放射線を透過させることができ、ラベル貼付が1次容器19においてしか行われないので、好適にはラベルがない。この目的に有効な材料はポリプロピレン及びポリエチレンを含む。
【0025】
検査ステーション82が使い捨てチップ用空洞及び光ファイバ用孔のみを有する固体ブロックとして構成される必要はなく、チップが同じところまで降下させられる必要もない。その代わりに、検査ステーション82の側壁が開閉され、図4(A)及び図5に示されるように、チップの通り抜けを可能とさせるスロットを具備することができる。前に説明された部分と類似の部分は同じ参照番号を付されており、この参照番号に区別するための接尾記号「A」が添付されている。
【0026】
したがって、検査ステーション82Aはある距離離されて配置されている2つの固定されている対向部分109、112を備える。各部分は対向する面116、116’を有し、この面がその間にスロット115を画定する。面116、116’の上部表面117は案内レール及びチップ48Aの上部部分111Aのための台座となる。部分109は、図示されていない光源から部分109を通る光ファイバ98Aを有し、一方、部分112は、面116に分光光度計へ接続されているセンサ114を有し、分光光度計は部分112に設けられている又は部分112と接続されている。
【0027】
部分109及び112の対向する面はある距離だけ間隔を空けたスリット115を画定し、このスリット115は使い捨てチップ48Aが矢印120で示されるように滑り抜けることを可能にする。これらの対向する面がチップ48Aの滑り抜けのために一定の距離だけ離間されることができる。
部分109及び112は、矢印120で示されるチップ48Aの通過のために、垂直方向孔84に関して上で説明されたアスペクト比よりもかなり小さいアスペクト比のスロットをつくり出すので、分光光度測定のためにはスロット115を閉じた方がよい。このために、矢印136及び138で示されるように、閉鎖位置(不図示)へ旋回されたときにスロット115を閉鎖するに十分な幅の旋回する扉130、132が参照番号134で示される部分で部分109の両端部へ蝶番式に取り付けられている。(扉132が簡単化のためだけに仮想線で示されている)。扉を旋回するために、好適には蝶番134のピントルが従来のモータ136の回転駆動軸(不図示)に付設されている又は取り付けられている。
【0028】
あるいはまた、扉130及び132が、空洞84に関して上述された垂直アスペクト比に等しい水平方向アスペクト比を有するようにスロット115を長くすることによって、省略されることができる。
図5に示される光ファイバ98A及び検出器114のところでチップ48Aの矢印120で示されるような横方向の運動を精度良く止める補助をするために、好適には、ばね付勢されている移動止め210が面116に設けられ、この移動止め210は反対側の面116’にある固定されている突起212と協動する。読み取り後、矢印120の方向にスロット115からチップ48Aを移動させるときには、移動止め210がチップによって面116へ押し付けられる。前出の実施態様において述べられたように、チップ48Aは使用されるNIR及び近可視波長を透過させる。
【0029】
あるいはまた、図4(B)に示される部分112Bが光の漏れをふさぐために板122Bに可動に取り付けられることができる。前に説明された部分に類似の部分は同じ参照番号を付されており、この参照番号に区別するための接尾記号「B」が添付されている。したがって、検査ステーション82Bは、面116B及び116’Bと共にU字形状スロットを形成する板122Bを備え、このU字形状スロットはチップ48Bが上部表面117Bに支持されると同時に矢印120Bで示されるように滑り抜けることを可能にさせる。光ファイバ98Bは静止部分130Bを通して光を伝送し、静止面116Bのセンサ114Bは図示されていない分光光度計へ光を伝送する。
【0030】
板122Bと面116B及び116’BからなるU字形状スロットを通して起こり得る光の漏れをふさぐために、部分112Bが板122Bを滑動するように取り付けられ、ラック162及びドライブピニオン164によって矢印168に駆動され、スロットを開放又は閉鎖する。閉鎖されると、面116B及びチップ48Bが部分112B内の空間172を占有し、壁部分169がスロット115Bを閉鎖する。
【0031】
患者サンプルの特性に関する検査に加えて、NIR及び近可視波長を使用して分光光度分析が可能である標的物質はいずれも、患者サンプルがチップ48Aにある間に分光光度計110によって分析されることができる。これらの標的物質は数あるなかでヘモグロビン、アルブミン、ぶどう糖を含む。チップ内のこれらの標的物質を検査することによって、必ずではないが、実際には、サンプルがスライド検査要素Eに置かれたときに、好適には、分析装置はそれらの標的物質に関するさらなるそれ以上の検定を抜かす。チップを通した分光光度検出はスライド検査要素Eで行われる個別の各検定での4秒と比較して、分析される標的物質全てで4秒しか必要としないので、このことは分析装置の全体スループット大幅に向上させる。「結果を出す時間」がさらにチップを通しての分光光度分析によって劇的に改善され、スライド検査要素の場合の5分と比較してチップを通しての場合には4秒となる。
【0032】
向上されたスループットの例として、以下がジョンソン&ジョンソン・クリニカルダイガノスティックス(Johnson&Johnson Clinical Diagnostics)から商標「VITROS950」分析装置で販売されているような分析装置で達成され得る利点の推定である。この推定は、スライド検査要素へのサンプル液の分注は分析における制限ステップであることと、分注ステップは吸引に8秒、検査要素への分注して検査要素をVITROS950(商標)分析装置の分配器ヘ装填するのに4秒などを必要とすることと、本発明によって比色定量分析がチップ内で行われることのみを仮定している。
【0033】
行われるべき化学的性質の混合比が電位差検査0、比色検査7、示差(rate)検査0であれば、本発明を用いない場合には、スループットは毎時300検査要素である。本発明を用いた場合には、スループットは毎時2100検査となることが示され、これは7倍の増加である。他方で比色検査5のみ、示差検査2又は電位差検査2のいずれかが行われるのであれば、本発明を用いない場合のスループットは毎時420検査で、本発明を用いた場合は毎時1050検査となり、2.5倍の増加である。さらにまた、7つ化学的性質の混合比が比色検査3のみ、電位差検査4で行われるとすれば、本発明を行うことによって得られるスループットの増加はない(両方の場合とも毎時525検査である)。
【0034】
好適には、チップ内にある間のかかる分析物のこのような検査がサンプル液のある種の温度制御と共に行われる。このことは、検査ステーション82において温度を制御することによって行われることを必要とするだけでなく、図1の容器19内のサンプル液を加熱する又は冷却することによって行われることができる又はサンプル液がチップ48等にある間に加熱又は冷却することによって行われることができるが、検査ステーション82では加熱又は冷却は行われない。
【0035】
しかしながら、スライド検査要素Eの使用を必要とする検定が依然として幾つかある。工程が図1に略図的に示されている。チップ48がホルダ117に挿入され、患者サンプルの一部がスライド検査要素Eに分注される。その後、分配器30が、検査要素Eが矢印142にインキュベータ(不図示)へ直線的に移送される位置へ矢印140に回転され、インキュベータ内で検査要素Eが、検査ステーション146において読み取られる又は検出されるまで矢印144へ回転されるが、以上全ては、公知であり、従来のものである。検査ステーション146は、チップ48、48Aと共に使用される分光光度計110とは対照的に、従来通り比色検出器又は電位差検出器を備える。
【0036】
上述されたように、好適には、検査ステーション146で行われる検査はチップを通して行われる検査を抜かすけれども、チップ内で行われる検査の精度の「確認」をするために、かかる分光測光法検定を検査ステーション146で繰り返すことも可能である。
検査の順番を逆にすることも考えられる、すなわち、NIR及び近可視波長でチップを通した測定を行う前に、サンプル液の一部を上述されたように検査スライドに置くこともできる。
【0037】
本発明を説明するために、以下の非消耗的検査を行う。
図2の装置が使用され、この装置においては、以前は「エクタケム(Ektachem)」使い捨てチップとして知られていた商標「ビトロス(Vitros)」でジョンソン&ジョンソン・クリニカルダイガノスティックス社から販売されている使い捨てチップが使用された。光ファイバは0.2mmシングルファイバであり、これによってファイバ98及び98’を介して検査ステーション82を「TC2000」二重光線同期分光光度計へ接続しており、この分光光度計はCMEテレメトリクス(Telemetrix)から販売している検出器112としてタングステン−ハロゲン白熱電球光源110を使用している線形ダイオード配列検出器を使用している。580nmから1100nmまでの放射線のみを検出できるようにするために、検出器112では回折格子が使用された。(分光光度計の基準光線部分は明確化のために省略されている)。チップ48に吸引される液体の量は液体の高さが図2の通過矢印200の完全に上となるように50μLとした。実証された30μLのみを検査することが必要とされる。
【0038】
検査される液体は、第一に較正液として、ヘモグロビンと、ファルマシア(Pharamacia)社から販売されているイントラリピド(Intralipid)(商標)(自然発生乳状脂粒を擬態する脂肪乳液)と、ビリベルジンとを含む既知量の液体を無作為に組合わせたものであり、これらの液体全てが人血清基質に加えられている。
【0039】
以下の表1は添加後の血清中のHb、IL、及びBVを示している。「Hb」はヘモグロビンを、「IL」はイントラリピド(商標)を、「BV」はビリベルジンを、「BR」はビリルビンを意味する。
【0040】
【表1】

【0041】
同様に準備された21種の液体の第二の組み合わせは表2の構成成分を有するように準備され、未知のものとして取り扱われた。
【0042】
【表2】

【0043】
液体の第一の組み合わせが、従来の分光光度手法を用いる較正アルゴリズムを作り出すために上述されたように放射線照射され、この測定で検出されたHbの値が回帰グラフを得るために図6のように実際の値に対してグラフに記入された。種々の較正アルゴリズムが有効であり、例えば、一次及び二次導関数によって式を選択する。以下の等式は単に例示的なものである。
1)Hb(g/L)=C1 (dA600 /dλ600 )−C2 (dA663 /dλ663 )−C3
2)IL(g/L)=C4 (dA874 /dλ874 )+C5
3)BV(mg/dL)=C6 (dA724 /dλ724 )−C(dA803 /dλ803 )+C8
ここで、A600 は600nmにおける吸光度、λ600 は600nmの波長、その他のA及びλの値に関しても同じであり、(dAi /dλi )は波長に対する吸光度の1次導関数、C1 、…C9 は好適には以下の値を有する定数である。
【0044】
C1 =15.892 C5 =0.244
C2 =15.882 C6 =98.068
C3 =0.21 C7 =122.732
C4 =252.155 C8 =0.0685
図6の場合の回帰相関係数R2 は0.991であった。
【0045】
次に、液体の第二の組み合わせが上述のように放射線照射され、液体の第一の組み合わせから導かれた図6の較正アルゴリズムを使用して、予測値が図7のように既知の結果に対してグラフに記入された。0.982というR2 の値は優秀である。この精度は、スライド検査要素における検査に代わって、この結果を未知のサンプル内のHbの臨床検定に信頼して適用することを可能にするのに適したものである。
【0046】
同様に、上述されたように検出されたスペクトルの数値がILに関して評価された。較正の結果は図8に示されており、予測の結果が図9に示されている。この場合のR2 はそれぞれ0.9941と0.9878である。
また、記述されたスペクトルが評価されたが、今度の分析はBVに関するものであった。図10は較正の結果を示しており、図11はR2 の値が示されるようなものである予測の結果を示している。
【0047】
新しい、第三の液体の組み合わせがビリルビンの検出に関して本発明を説明するために用意され、その組み合わせの較正液の形式は以下の表のように構成された。
【0048】
【表3】

【0049】
この検査に使用された較正アルゴリズムは以下のようなものであった。
4)BR(mg/dL)=C9 (dA495 /dλ495 )+C10(dA512 /dλ512 )+C11(dA578 /dλ578 )−C12
定数は以下のようになった。
C9 =−24.878
C10=201.61
C11=44.98
C12=6.475
液体の第四の組み合わせがビリルビンの値の予測に関する確認のために同様に用意され、その組み合わせは以下の表のように構成された。
【0050】
【表4】

【0051】
スペクトルが前出の例と同じように評価された。図15は較正の結果を示し、図16はR2 の値が示されるようなものである予測の結果を示している。
4つの実験(Hb、IL、BV、及びBR)全てに関して、その結果は優れた相関を示し、その結果はスライド検査要素での検査に代わって使用するに十分であり、これらのいずれもが所望の検定と見なされるべきものである。いずれにしても、これらの結果は明らかに生物学的液体のサンプルの特性を確認することを可能にし、そのサンプルが許容可能な特性の範囲の外側にあると判定されたなら不合格とすることができるようにする。
【0052】
用いることができる他の較正アルゴリズムの例として、ILに関して以下のものが上式#2の代替式となる。
2’)IL(g/L)=C13(dA999 /dλ999 )+C14(dA1051/dλ1051)−C15
ここで、C13=166.068、C14=92.352、C15=0.693である。この較正アルゴリズムが上述の第一及び第二の液体の組み合わせに関して用いられると、R2 は較正に関して0.988となり、予測に関して0.984となる。(実際のプロットは示されていない)。
【0053】
再び図7に関して、上述されたヘモグロビンの存在を確認するための方法が、5g/Lまででは、直線性、すなわち測定の正確性を示したことが明らかとなる。5g/Lを越えると、データは「真値」から離れていく傾向がある。このことは図17において最も明確に示されている。したがって、もし5g/Lより多くの量が含有されているようであれば、別な組み合わせのアルゴリズムの方が好ましい。
【0054】
より詳細には、全範囲を網羅するために2つの異なるアルゴリズムが使用されるのであれば、真の曲線とのより優れた追従性が達成され、これらのアルゴリズムが重なり部分で連続的なデータを示すように選択される。好適には、3g/Lから上で用いられるアルゴリズムはg/L単位のヘモグロビン濃度の自然対数である。最も好適には、3g/Lから35g/Lまででは、用いられるアルゴリズムは以下の形態である。
【0055】
【数1】

【0056】
ここで、C16、C17、C18の詳細な例はC16=−17.38、C17=+9.96+C18=+0.37である。
3g/L以下には、上で示された式1)に類似の型の様々なアルゴリズムが有効である。3g/Lより上で式5)とかみ合うために、非常に好適な式は以下の式となる。
1’)Hb(g/L)=C19(dA593 /dλ593 )+C20(dA608 /dλ608 )+C21
ここで、C19は好適には−66.689、C20は好適には81.081、C21は好適には−0.25である。
【0057】
図17に示されるヘモグロビンの水準が3g/L以上及び3g/L以下に上述の新しいアルゴリズム5)及び1’)を用いて再計算されたときに、図18のプロットが結果として得られた。このプロットは、予測された値が図17のデータ点で得られるものよりも45°の「真」の直線により近くなることを示している。
【0058】
図18のデータは10g/Lまでしか延びていないが、希釈なしステップを用いることによって、式5)及び式1’)がヘモグロビンの値に関しては35g/Lまで有効となることが示された。
図12は、実際にNIR及び近可視スペクトルにおける吸光度の一次導関数の値が、有効波長において、IL、BV、又はHb構成成分が存在するサンプルの独立した検出を可能にするのに十分に分離していることを示すプロットである。すなわち、曲線200はそれらの構成成分のいずれも有さないサンプル、曲線202は1.79g/LのHbのみを有するサンプル、曲線204は2.38g/LのILのみを有するサンプル、曲線206は3.95mg/dLのBVのみを有するサンプルである。したがって、Hbは主としてNIRの580〜605nmの領域に寄与し、ILは896〜1051nmの領域、好適には896〜939nmに寄与し、BVは680〜750nmの領域に寄与する。
【0059】
さらに別の実施態様においては、チップが従来のチップから変更されていないが、図13の吸収スペクトルが受光される前に、分光光度計によって1本より多くのNIR及び近可視放射線のチップを通した通過が達成される。前述された部分が同じ参照番号によって参照されており、この参照番号に区別するための接尾語「D」が添付されている。
【0060】
したがって、光ファイバ98Dから放射しているNIR及び近可視放射線による放射線照射が処理用光ファイバ98’Dによって受光されるように、チップ48Dが前述のように空洞84Dにはめ込まれる。しかしながら、前出の実施態様と異なり、受光用光ファイバ98’Dは発光用光ファイバ98Dと直接に向かい合ってもいなければ、「第一通過」放射線を受光する位置にもない。代わりに、少なくとも1対の、好適には3対の鏡(230、232;240、242;250、252)が、鏡と同じ回数だけ放射線にチップ48Dを再度通過させるように配置される。(3対からなる6枚の鏡は放射線に6回チップを透過させる)。
【0061】
さらに別の実施態様においては、光ファイバ98、98’(又は上で開示された他の型の光ファイバ)はNIR及び近可視光にチップの最も厚い部分のみを通過させる必要はない。その代わりに、光がより狭い首部分を透過させることができる。(前に説明された部分と同様の部分は同じ参照番号を冠しており、区別のための接尾語「E」が添付されている)。
【0062】
したがって、図14の照射用光ファイバ98Eがチップ48Eの円錐状首部分300を放射線照射するように検査ステーション82Eのブロックに配置されており、この首部分は本体部分224Eの直径「d」と比較して直径が小さくなっていく。次に、チップを通って受光用光ファイバ98’Eへ透過させられる光はサンプルのずっと狭い部分を通過する。検出される分析物が高密度のものである又は当のNIR及び近可視波長に対して高吸光係数を有しているのであれば、これが所望される。最も極端な場合には、光ファイバ98E及び98’Eが、チップ48Eの最も狭い部分304を通して読み取る仮想位置302まで下に移動される。
【0063】
あるいはまた、チップのより狭い部分をNIR及び近可視放射線が通過することが、前出の実施態様を用いて、単に検査ステーション82内でチップ(及びプローブ)を十分に持ち上げてNIR放射線で照射することによっても達成され得る。さらに好適には、ステップの順番は、図2(A)(B)、図4(A)(B)のいずれかに示されるようなNIR及び近可視放射線放射源を含む光を通さない囲いに、チップが着座するまでチップを下降させるステップ、放射源から放射されるNIR及び近可視放射線でチップ及びその中身を走査するステップ、もし中身が所定の閾値を上回る密度を有するなら、その後、放射源がチップのより狭い部分を走査するように配置されるまで囲いの中でチップを持ち上げるステップという順番となる。
【0064】
分析装置における標的物質の検定のスループットを向上させることが本発明の有利な特徴である。
さらに別な有利な特徴は、分光測光法での分析にインキュベーション時間が必要とされないことから、結果がより短い時間で得られることである。
【符号の説明】
【0065】
12 分析装置
18 分注ステーション
19 1次収集容器
46 吸引器プローブ
48 チップ
71 ポンプ
82 検査ステーション
【特許請求の範囲】
【請求項1】
分注ステーションと、患者サンプル中の標的物質を検出するための少なくとも一つの検査ステーションとを備える臨床分析装置においてスループットを改善する方法であって、
前記分注ステーションが、
吸引器プローブと、
一次収集容器から生物学的サンプル液を収集し、収集されたサンプル液の少なくとも一部を検査要素上へ又はその中へ分注するために、前記プローブに取り付けられるチップと、
前記プローブ及び前記チップ内に部分的な圧力又は部分的な真空を生じさせるための手段と、
を備え、前記方法が、
a)前記プローブに取り付けられるチップの一つに生物学的液体を吸引するステップと、
b)前記生物学的液体が前記チップ内にあり且つ前記チップが前記プローブに取り付けられている間に、近赤外及び近可視放射線波長の光に複数の波長でチップを透過させることによって、前記生物学的液体中の一つ又はそれ以上の標的物質を検出し、前記生物学的液体中の一つ又はそれ以上の標的物質の濃度と透過した光とを相関させることによって、前記チップを透過した光の一部分を複数の波長で分光光度分析を行うステップであって、前記相関が吸光度の一次導関数の値を波長の関数として計算することを含むステップと、
c)分光光度分析を行うステップに先立って、前記チップから前記生物学的液体の一部を検査要素へ分注するステップと、
d)前記一つ又はそれ以上の標的物質以外の標的物質に関して、前記検査ステーションで前記生物学的液体を加えた前記検査要素を検査するステップと、
を含み、前記一つ又はそれ以上の標的物質を前記前記検査ステーションで検査するのに必要とされなくなった時間量によってスループットを増加させ、
前記相関させるステップが、0から約3g/Lで用いられる一つの較正アルゴリズムと3g/L以上で用いられる他の較正アルゴリズムとの二つの較正アルゴリズムを使用して全範囲を網羅するようになっている、臨床分析装置においてスループットを改善する方法。
【請求項2】
前記他の較正アルゴリズムは、波長に関する吸光度の第一次導関数の値からヘモグロビン濃度の自然対数を求める、請求項1に記載の臨床分析装置においてスループットを改善する方法。
【請求項3】
前記二つの較正アルゴリズムは、
0から約3g/Lの範囲におけるヘモグロビン濃度についての式、
Hb(g/L)=−66.689(dA593/dλ593)+81.081(dA608/dλ608)−0.25、
3g/L以上の範囲におけるヘモグロビン濃度についての式、
Hb(g/L)=e[-17.38(dA593/dλ593)+9.96(dA608/dλ608)+0.37]
からなる、請求項2に記載の臨床分析装置においてスループットを改善する方法。
【請求項1】
分注ステーションと、患者サンプル中の標的物質を検出するための少なくとも一つの検査ステーションとを備える臨床分析装置においてスループットを改善する方法であって、
前記分注ステーションが、
吸引器プローブと、
一次収集容器から生物学的サンプル液を収集し、収集されたサンプル液の少なくとも一部を検査要素上へ又はその中へ分注するために、前記プローブに取り付けられるチップと、
前記プローブ及び前記チップ内に部分的な圧力又は部分的な真空を生じさせるための手段と、
を備え、前記方法が、
a)前記プローブに取り付けられるチップの一つに生物学的液体を吸引するステップと、
b)前記生物学的液体が前記チップ内にあり且つ前記チップが前記プローブに取り付けられている間に、近赤外及び近可視放射線波長の光に複数の波長でチップを透過させることによって、前記生物学的液体中の一つ又はそれ以上の標的物質を検出し、前記生物学的液体中の一つ又はそれ以上の標的物質の濃度と透過した光とを相関させることによって、前記チップを透過した光の一部分を複数の波長で分光光度分析を行うステップであって、前記相関が吸光度の一次導関数の値を波長の関数として計算することを含むステップと、
c)分光光度分析を行うステップに先立って、前記チップから前記生物学的液体の一部を検査要素へ分注するステップと、
d)前記一つ又はそれ以上の標的物質以外の標的物質に関して、前記検査ステーションで前記生物学的液体を加えた前記検査要素を検査するステップと、
を含み、前記一つ又はそれ以上の標的物質を前記前記検査ステーションで検査するのに必要とされなくなった時間量によってスループットを増加させ、
前記相関させるステップが、0から約3g/Lで用いられる一つの較正アルゴリズムと3g/L以上で用いられる他の較正アルゴリズムとの二つの較正アルゴリズムを使用して全範囲を網羅するようになっている、臨床分析装置においてスループットを改善する方法。
【請求項2】
前記他の較正アルゴリズムは、波長に関する吸光度の第一次導関数の値からヘモグロビン濃度の自然対数を求める、請求項1に記載の臨床分析装置においてスループットを改善する方法。
【請求項3】
前記二つの較正アルゴリズムは、
0から約3g/Lの範囲におけるヘモグロビン濃度についての式、
Hb(g/L)=−66.689(dA593/dλ593)+81.081(dA608/dλ608)−0.25、
3g/L以上の範囲におけるヘモグロビン濃度についての式、
Hb(g/L)=e[-17.38(dA593/dλ593)+9.96(dA608/dλ608)+0.37]
からなる、請求項2に記載の臨床分析装置においてスループットを改善する方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【公開番号】特開2009−204620(P2009−204620A)
【公開日】平成21年9月10日(2009.9.10)
【国際特許分類】
【外国語出願】
【出願番号】特願2009−133345(P2009−133345)
【出願日】平成21年6月2日(2009.6.2)
【分割の表示】特願平10−250775の分割
【原出願日】平成10年9月4日(1998.9.4)
【出願人】(594199337)オルソ−クリニカル ダイアグノスティクス,インコーポレイティド (14)
【Fターム(参考)】
【公開日】平成21年9月10日(2009.9.10)
【国際特許分類】
【出願番号】特願2009−133345(P2009−133345)
【出願日】平成21年6月2日(2009.6.2)
【分割の表示】特願平10−250775の分割
【原出願日】平成10年9月4日(1998.9.4)
【出願人】(594199337)オルソ−クリニカル ダイアグノスティクス,インコーポレイティド (14)
【Fターム(参考)】
[ Back to top ]

