自動分析装置
【課題】検査ステージの設置スペース、構成を最小限に抑えながら、検査カートリッジを用いた効率的な連続検査を可能とする。
【解決手段】複数の検査カートリッジ10がセット可能なカートリッジ受部1を有し、セットステージST内の検査初期位置ST1に順次移送選択するカートリッジ選択手段2と、カートリッジ選択手段2にて検査初期位置ST1に移送選択された検査前検査カートリッジ10を検査ステージKTに直線的に搬入すると共に検査後検査カートリッジ10をセットステージSTに直線的に搬出するカートリッジ搬送手段3と、カートリッジ搬送手段3にて搬入された検査ステージKT内の検査カートリッジ10に対し当該検査カートリッジ10の検体、試薬を反応セルに分注する検体試薬分注手段4と、検体試薬分注手段4にて分注された反応セル11c内の検体と試薬との反応を測定する測定手段5とを備える。
【解決手段】複数の検査カートリッジ10がセット可能なカートリッジ受部1を有し、セットステージST内の検査初期位置ST1に順次移送選択するカートリッジ選択手段2と、カートリッジ選択手段2にて検査初期位置ST1に移送選択された検査前検査カートリッジ10を検査ステージKTに直線的に搬入すると共に検査後検査カートリッジ10をセットステージSTに直線的に搬出するカートリッジ搬送手段3と、カートリッジ搬送手段3にて搬入された検査ステージKT内の検査カートリッジ10に対し当該検査カートリッジ10の検体、試薬を反応セルに分注する検体試薬分注手段4と、検体試薬分注手段4にて分注された反応セル11c内の検体と試薬との反応を測定する測定手段5とを備える。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、血液などの検体と試薬との反応を分析する自動分析装置に係り、特に、複数の検査カートリッジを自動的に分析する態様に有効な自動分析装置の改良に関する。
【背景技術】
【0002】
従来この種の自動分析装置としては、血液などの検体が収容される検体セル、試薬が収容される試薬セル及び検体、試薬が反応させられる反応セルが含まれる検査カートリッジ(カートリッジ容器)を用い、検査カートリッジの検体と試薬との反応を自動分析する方式が既に提供されている(例えば特許文献1参照)。
ところで、この種の自動分析装置にあっては、複数の検査カートリッジを自動的に分析したいという要請がある。このような要請に基づいて、複数の検査カートリッジを所定方向に配列すると共に、コンベアにて順次検査カートリッジを搬送し、各作業ステージにて検体試薬分注機構による検体、試薬の分注を行い、測定装置による測定を行うものである。
【0003】
【特許文献1】特許第2731613号公報(実施例,図1,図3)
【発明の開示】
【発明が解決しようとする課題】
【0004】
しかしながら、この種の特許文献1記載の先行技術にあっては、検査ステージ内に検査カートリッジ搬送用のコンベアを配設し、かつ、各作業ステージを設けているため、検査ステージの設置スペースが増大すると共にその構成が複雑になるという懸念がある。
本発明は、以上の技術的課題を解決するためになされたものであって、検査ステージの設置スペース、構成を最小限に抑えながら、検査カートリッジを用いた効率的な連続検査を可能とする自動分析装置を提供するものである。
【課題を解決するための手段】
【0005】
すなわち、本発明は、図1(a)(b)に示すように、検体が収容される検体セル11a、試薬が収容される試薬セル11b及び検体、試薬が反応させられる反応セル11cが含まれる検査カートリッジ10を用い、夫々の検体に対応する複数の検査カートリッジ10をセットした後、検査カートリッジ10毎に検体と試薬との反応を自動分析する自動分析装置において、セットステージST内に複数の検査カートリッジ10が所定の配列方向に沿って予めセットされるカートリッジ受部1を有し、このセットステージST内の検査初期位置ST1に順次移送選択するカートリッジ選択手段2と、セットステージSTに隣接する検査ステージKTに設けられ、カートリッジ選択手段2にて検査初期位置ST1に移送選択された検査前の検査カートリッジ10を検査ステージKTに直線的に搬入すると共に検査後の検査カートリッジ10を検査ステージKTからセットステージSTに直線的に搬出するカートリッジ搬送手段3と、このカートリッジ搬送手段3にて搬入された検査ステージKT内の検査カートリッジ10に対し当該検査カートリッジ10の検体、試薬を反応セルに分注する検体試薬分注手段4と、この検体試薬分注手段4にて分注された反応セル11c内の検体と試薬との反応を測定する測定手段5とを備えたことを特徴とするものである。
尚、図1(a)(b)は本発明が適用される自動分析装置の代表的態様を模式的に示したものであり、本発明の態様が図1(a)(b)に示す態様に限定されるものではない。
【0006】
このような技術的手段において、検査カートリッジ10の形態は直線的なものに限られず例えば試薬セル等を二列配置する態様なども含む。また、規定したセル11の数も適宜選定してよいし、他の機能部(例えば他のセルや着脱自在なノズルチップの保持部等)を備えていてもよい。
また、本件は、複数の検査カートリッジ10を連続的に自動分析することを主として想定していることから、カートリッジ受部1は複数の検査カートリッジ10が保持可能であることを要する。但し、カートリッジ受部1に一つの検査カートリッジ10をセットして使用することは差し支えない。
更に、検査初期位置ST1は通常は一つであるが複数設けても差し支えない。但し、複数設けた態様にあっては、検査ステージKT側のカートリッジ搬送手段3,検体試薬分注手段4及び測定手段5を複数設け、夫々の検査初期位置ST1に設定された検査カートリッジ10に対する検査を並列的に行うことが好ましい。
【0007】
また、カートリッジ搬送手段3は直線的に検査カートリッジ10を搬入、搬出するものであればよく、回転方式などは含まない。このため、検査ステージKTの設置スペースを必要最小限に抑えることができる。
更に、検体試薬分注手段4は検体、試薬の分注を共通のデバイスで構築してもよいし、別体のデバイスで構築してもよい。また、後述するように、着脱自在なノズルチップ15を用いる態様に限られるものではなく、ノズルチップ15を用いずに洗浄手段にて検体試薬分注手段を洗浄するようにしてもよい。更に、本件の検体には希釈したものも含まれる。
更にまた、測定手段5は予め決められた反応を一義的に測定するものであってもよいし、複数種の反応を測定するものであってもよい。ここで、測定手段5の代表的態様としては、反応セル11cに所定の波長の光を照射する発光素子と、反応セル11cを挟んで発光素子と対向する部位に配設される受光素子とを備えたものが挙げられる。
【0008】
また、検査カートリッジ10の好ましい態様としては、各セル11が直線的に配列されている態様が挙げられる。本態様によれば、カートリッジ搬送手段3,検体試薬分注手段4の動きを直線的な軌跡にすることができ、構成を簡略化できる。
更に、検査カートリッジ10の好ましい態様としては、カートリッジ受部1に沿って案内挿入され、カートリッジ本体には誤った方向からの挿入時に前記カートリッジ本体に衝合するストッパを具備させるようにすればよい。本態様によれば、検査カートリッジ10の逆向きでの挿入を有効に防止可能である点で好ましい。
また、カートリッジ選択手段2の好ましい態様としては、複数の検査カートリッジ10がセットされるカートリッ受部1全体を移送せるものが挙げられる。この場合、検査カートリッジ10の検査初期位置ST1への選択動作を簡略化できる点で好ましい。
更に、カートリッジ選択手段2の好ましい態様としては、一つの検査初期位置ST1に各検査カートリッジ10を順次移送選択するものが挙げられる。この場合、一つの検査初期位置ST1に対して一つの検査ステージKTを構築すればよく、検査ステージKTを簡略化することが可能である。
【0009】
また、カートリッジ搬送手段3の好ましい態様としては、カートリッジ選択手段2による検査カートリッジ10の移送動作を許容し、検査初期位置ST1に位置する検査カートリッジ10の被係合片14に対して係合可能な係合片を備えているものが挙げられる。本態様によれば、カートリッジ選択手段2による検査カートリッジ10の移送動作中に、カートリッジ選択手段2とカートリッジ搬送手段3との間で干渉し合うことがなく、カーリッジ搬送手段3を一時退避させるなどの機構が不要である点で好ましい。
更に、検体試薬分注手段5の代表的態様としては、検査カートリッジ10毎に着脱自在なノズルチップ15を使用するものが挙げられる。本態様によれば、着脱自在なノズルチップ15を使用することで、検体試薬分注手段4を洗浄する工程を省略することが可能になる点で好ましい。
更にまた、測定手段5の好ましい態様としては、検査カートリッジ10の検査項目に対応して測定条件を可変にするものが挙げられる。本態様によれば、複数の検査項目に簡単に対応することができる点で好ましく、例えば光学式の測定手段5にあっては、波長の異なる光源を複数具備させる(回転板に複数設置、光源基板を差し替えるなど)方式が好ましい。
【0010】
また、検査ステージKTの好ましい態様としては、カートリッジ搬送手段3にて検査ステージKTに搬入された検査カートリッジ10の少なくとも反応セル11cを所定の恒温環境温度に保つ恒温槽6が設けられている態様が挙げられる。本態様によれば、反応セル11cでの検体と試薬との反応を同じ条件下で測定することが可能である点で好ましい。
更に、検査ステージKTの好ましい態様としては、恒温槽6に加え、更に、測定手段5が動作する前に恒温環境温度よりも高い温度で検査カートリッジ10のセル11の少なくとも一部を予め加温する補助加温手段7が設けられている態様が挙げられる。本態様によれば、恒温条件に至るまでの時間を短縮することができ、その分、検体試薬分注手段4による分注処理、測定手段5による測定処理を迅速に開始することが可能である点で好ましい。
ここで、補助加温手段7による加温対象範囲は、検査カートリッジ10のセル11の少なくとも一部であればよく、例えば試薬セル11bの全部若しくは一部だけでもよいし、あるいは、検体セル11a内に希釈液などが予め収容されている場合には検体セル11aであってもよいし、あるいは、反応セル11cについて検体や試薬を分注する前若しくは後に補助加温するようにしてもよいし、これらを適宜組合せたり、全てのセル11を補助加温対象にしてもよい。尚、補助加温手段7による補助加温範囲は一定で差し支えないが、例えば補助加温範囲を複数に分割しておき、必要に応じて補助加温範囲を可変設定するようにしてもよい。
【0011】
更にまた、恒温槽6を備えている態様において、測定手段5の好ましい態様としては、測定手段5による測定条件が恒温槽の恒温環境条件から外れたときに、温度条件に基づいて測定結果が補正可能な温度補正手段を備えている態様がある。この場合、恒温槽6による恒温環境条件に満たなくても、温度補正手段により測定結果を補正することができることから、測定処理の開始時間を速めることができる。
ここで、温度補正手段の代表的態様としては、検査カートリッジ10の表面に対して非接触配置される非接触型温度センサからの温度情報に基づいて温度補正するものが挙げられる。この場合において、非接触型温度センサは例えば恒温槽6に取り付けられるが、これに限られるものではなく、適宜箇所に設けて差し支えない。
また、検体試薬分注手段4がノズルチップ15を使用する方式にあっては、検査カートリッジ10としては、ノズルチップ15を着脱自在に保持するチップ保持部12を有する態様が好ましい。この場合、チップ保持12には新規なノズルチップ15を保持してもよいし、使用済みのノズルチップ15を保持させ、検査済みの検査カートリッジ10と共に廃棄するようにしてもよい。
更に、着脱自在なノズルチップ方式の好ましい態様としては、検査カートリッジ10はセル11の全部若しくは一部を穿孔可能なシール13にて密封し、検体試薬分注手段4のノズルチップ15にて検体、試薬の分注動作前にセル11に対応するシール13に孔を穿設可能とするものであることが好ましい。
【発明の効果】
【0012】
本発明によれば、複数の検査カートリッジがセットされるセットステージと、セットステージと隣接して設けられ且つセットステージの複数の検査カートリッジを順次搬入しながら検査を進める検査ステージとを備え、検査カートリッジを引き込み検査する方式を採用したので、検査ステージの設置スペース、構成を最小限に抑えながら、効率的な連続検査を実現することができる。
【発明を実施するための最良の形態】
【0013】
以下、添付図面に示す実施の形態に基づいてこの発明を詳細に説明する。
◎実施の形態1
<全体構成>
図2は本発明が適用された自動分析装置の実施の形態1の外観を示す説明図である。
同図において、自動分析装置20は、装置筐体21の前面側(ユーザーの操作側)に開閉可能な扉22を有すると共に、この扉22の開口部の上方には操作部23(スタートボタン24,操作ボタン25、表示ディスプレイ26を具備)を有し、ユーザーが前記扉22を開放した状態で装置筐体21内に検査すべき検体が分注された複数(例えば3つ)の検査カートリッジ200をセットし、しかる後、スタートボタン24を操作することにより、複数の検査カートリッジ200の検体について順次自動分析するものである。
【0014】
本実施の形態において、自動分析装置20は、図2〜図5に示すように、装置筐体21内に、検査カートリッジ200がセットされるセットステージSTと、このセットステージSTに隣接して設けられ且つ検査カートリッジ200の検体について分析検査する検査ステージKTと、各検査カートリッジ200の検査結果を印刷するプリンタ部27とを備えている。
セットステージSTは、装置筐体21のベースフレーム28上に装置筐体21の幅方向(X方向)に沿って移動するXテーブル30を配設し、このXテーブル30上に検査カートリッジ200が保持可能なカートリッジラック40を設け、予め決められた検査初期位置ST1に検査カートリッジ200を順次移動させるものである。
ここで、Xテーブル30としてはX方向に延びる固定台31又はガイドレールに沿って可動台32を摺動自在に設けたものが用いられる。また、Xテーブル30の位置規制については図示外の位置センサを用いた公知の手法や、パルスモータ等の駆動モータを用いた位置制御にて行われる。
また、検査ステージKTは、セットステージSTの検査初期位置ST1に移動設定された検査カートリッジ200をX方向と直交するY方向に沿って検査ステージKT側に戻し可能に引き込むカートリッジ引き込み機構50と、検査カートリッジ200に対して検体、試薬を分注する検体試薬分注機構70と、検査カートリッジ200の少なくとも一部(後述する反応セルに相当)を恒温条件に保つ恒温槽80と、この恒温槽80とは別に設けられ且つ検査カートリッジ200を恒温条件よりも高い温度にて補助的に加温する補助加温装置90と、恒温槽80の内部に設けられて検査カートリッジ200の反応セルに分注された検体と試薬との反応を測定する測定装置100とを備えている。
【0015】
<検査カートリッジ>
次に、検査カートリッジ200について説明する。
本実施の形態において、検査カートリッジ200は、図6(a)〜(c)に示すように、例えばポリプロピレン等の合成樹脂にて成形され且つY方向に沿って直線状に延びるカートリッジ本体201を有し、このカートリッジ本体201には有底の複数のセル202を一体的に且つ直線的に配列したものである。
本実施の形態において、セル202は、カートリッジ本体201の挿入方向端から離間した側から順に、検体が収容される一つの検体セル203と、試薬が収容可能な複数(例えば3つ)の試薬セル204〜206と、検体と試薬とが分注されて反応させられる一つの反応セル207とを備えている。尚、例えば検体セル203や反応セル207が複数設けられるなど適宜選定できることは勿論である。
【0016】
特に、本実施の形態では、セル202のうち、反応セル207は略矩形筒状断面を有する容器であり、セル外壁面がX方向に直交する平面として構成されているのに対し、他のセル202、具体的には検体セル203、試薬セル204〜206は円筒状断面を有する形状として構成されている。また、本実施の形態では、複数の試薬セル204〜206の
うち、一つの試薬セル204は未使用で、他の二つの試薬セル205,206にR1,R2の試薬(図7参照)が所定量予め分注されている。一方、本実施の形態では、検体セル203には希釈液W(図7参照)が所定量予め分注されている。
【0017】
更に、本実施の形態では、カートリッジ本体201の挿入方向端から離間した側には検体セル202に隣接してチップ保持孔208が貫通した状態で開設されており、このチップ保持孔208には検体試薬分注機構70に着脱自在に装着可能なノズルチップ210が上方から離脱可能に係止保持されている。
そして更に、カートリッジ本体201の挿入方向端とは反対側には把持部211が突出形成されており、この把持部211の裏面には指押さえ212が突出形成されている。
一方、カートリッジ本体201の挿入方向端側には下側に開口したU字状の被係合片213が形成されている。
【0018】
更に、本実施の形態では、カートリッジ本体201の各セル202(203〜207)の開口縁には上方に突出する突縁214が設けられており、各セル202(203〜207)の開口はシール215にて上方から被覆されている。このとき、各セル202の突縁214がシール215に接触するため、各セル202は突縁214を介して完全に密封状態で仕切られることになり、セル202内の試薬や希釈液が他のセルに流入する懸念は有効に回避される。
また、セル202の一部、例えば検体セル203及び試薬セル204はX方向に対して非対称形状になっており、少なくとも片側にフランジ部216が形成される一方、前記他方側のフランジ部216の一部に切欠217が設けられている。
【0019】
<採血具>
また、本実施の形態では、図7に示すように、検査カートリッジ200の検体セル203には採血具230で採取した血液からなる検体が分注されるようになっている。
本実施の形態において、採血具230は、図7及び図8に示すように、両端が開口する筒状のポリプロピレン等の透明若しくは半透明の合成樹脂製の本体パイプ231と、この本体パイプ231の一端に連通可能に接続され且つ本体パイプ231の一端から突出配置されると共に毛管現象(毛細管現象)にて血液240が採取可能なガラス管又はポリエチレンテレレート等の透明若しくは半透明の合成樹脂製の毛管パイプ232と、本体パイプ231の他端に連通可能に接続され且つ本体パイプ231の他端から突出配置されると共に弾性材(例えばシリコーンゴム)にて潰れ変形可能に構成される弾性パイプ233とを備えている。
【0020】
そして、本実施の形態において、毛管パイプ232は本体パイプ231の一端開口縁に毛管ホルダ234を介して嵌合保持されている。
この毛管ホルダ234は透明若しくは半透明の材料である例えばシリコーンゴム等の弾性材料からなる円柱部材の中央に毛管パイプ232が挿通可能な挿通孔を有するものであり、毛管パイプ232は毛管ホルダ234の挿通孔の両端から突出するように毛管ホルダ234の挿通孔縁にて圧入固定され、毛管ホルダ234に対して交差配置された状態でサブユニット化されている。そして、毛管ホルダ234は本体パイプ231の一端開口縁に圧入固定されている。尚、毛管パイプ232、毛管ホルダ234は必要に応じて接着固定するようにしてもよい。
そして、毛管パイプ232は本体パイプ231の内部に毛管ホルダ234から突出寸法mだけ突出配置されると共に、本体パイプ231の外部に毛管ホルダ234から突出寸法hだけ突出配置されている。
本実施の形態では、突出寸法mは1.0mm以上確保されており、本体パイプ231内のうち、毛管パイプ232と毛管ホルダ234との間に溝部235が形成されている。
また、突出寸法hは3.0mm以上、好ましくは10.0mm以上確保されており、毛管パイプ232の先端に接する血液240が本体パイプ231の端部に付着しないように配慮されている。
【0021】
次に、本実施の形態に係る採血具の使用方法について説明する。
先ず、採血時について説明すると、図8(a)に示すように、採血作業者は人体の一部に針などで疵をつけることで僅かに出血させ、採血具230の本体パイプ231を把持した状態で出血した血液240部分に対して採血具230を略直交配置すると共に、血液240部分に採血具230の毛管パイプ232の先端を接触させるようにすればよい。
この状態において、毛管パイプ232内には毛管現象により血液240が吸引保持され、ついには毛管パイプ232内全体に血液240が充填保持される。
次いで、採血具230を用いて採血した血液240を吐出する場合には、図8(b)に示すように、弾性パイプ233を押し潰すことにより、本体パイプ231内に正圧を作用させ、もって、毛管パイプ232内の血液240を所定部位に吐出させるようにすればよい。
この状態において、毛管パイプ232内の血液240を全て吐出するようにすれば、毛管パイプ232の容量に対応した所定量の血液240が得られる。
【0022】
本実施の形態に係る採血具230を用いて当該採血具230で採取した血液を検査カートリッジ200に分注するには、例えば検査カートリッジ200の検体セル203に対応するシール215に例えばノズルチップや専用の穿孔具を用いて孔を開け、しかる後、シール215の孔を通じて検体セル203内に採血具230の毛管パイプ232を挿入し、この状態で、採血具230の弾性パイプ233を押し潰し、毛管パイプ232内の血液240を検体セル203内に吐出するようにすればよい。
このとき、仮に、採血時に毛管パイプ232から溢れた血液240が毛管パイプ232と毛管ホルダ234との間の溝部235に溜まっていたとしても、当該血液残留物240’が検体セル203に逆流することはなく、毛管パイプ232内の血液240のみが検体セル203に定量供給される。
【0023】
<カートリッジラック>
また、本実施の形態では、カートリッジラック40は、図5及び図9(a)(b)に示すように、複数(本例では3つ)の検査カートリッジ200が保持可能な複数のラックホルダ41を有している。このラックホルダ41は、一対のホルダ脚42間にX方向に直交するY方向に延びるスリット43を設け、このスリット縁部を支持面44としたものであり、この支持面44に検査カートリッジ200のカートリッジ本体201の幅方向両側縁部を支持するようになっている。更に、一対のホルダ脚42の一方には検査カートリッジ200の切欠217(図6参照)に対応してストッパ45が設けられており、カートリッジラック40への検査カートリッジ200の挿入方向が逆になった状況下では、前記検査カートリッジ200のフランジ部216が前記ストッパ45に衝合し、検査カートリッジ200が誤った挿入方向からカートリッジラック40にセットされないように配慮されている。
【0024】
<カートリッジ引き込み機構>
更に、カートリッジ引き込み機構50は、図10〜図12に示すように、Y方向に延びる引き込み軌道51を有し、この引き込み軌道51に沿って移動自在なYテーブル(可動ユニット)52を設け、このYテーブル52にはセットステージST側に延びる係止アーム53を設けると共に、この係止アーム53の先端には上方に突出する係止片54を設け、この係止片54が検査カートリッジ200の被係合片213に係脱自在に係合するようになっている。
特に、本実施の形態では、検査カートリッジ200の被係合片213はX方向に貫通する凹部218を有しており、Xテーブル30の移動に伴って検査カートリッジ200の被係合片213とカートリッジ引き込み機構50の係止片54とが相互に干渉することはなく、Xテーブル30が適宜位置に移動し、検査初期位置ST1に移動設定された検査カートリッジ200は、その被係合片213がカートリッジ引き込み機構50の係止片54と係合する位置関係になるようになっている。
【0025】
また、Yテーブル(可動ユニット)52の駆動系及び位置停止機構を図13〜図15に示す。
同図において、このYテーブル52の駆動系は、例えば図13〜図15(a)に示すように、装置筐体21に固定された支持ブラケット21aに駆動モータ55及びモータドライバ56を固定設置し、駆動モータ55からの駆動力を駆動力伝達機構57を介してYテーブル52に伝達し、引き込み軌道51に沿ってYテーブル52を進退動するようになっている。
ここで、駆動力伝達機構57としては適宜選定して差し支えないが、例えばYテーブル52の移動方向に沿って循環回転する移動ベルト57aをプーリ57b,57c間に掛け渡すと共に、この移動ベルト57aに前記係止アーム53の一端部を固定する一方、前記駆動モータ55からの駆動力を図示外の駆動プーリを介して駆動ベルト57dに伝達し、この駆動ベルト57dからの駆動力をプーリ57bを介して移動ベルト57aに伝達し、この移動ベルト57aを進退動させることによりYテーブル52を進退動させるものが挙げられる。
尚、Yテーブル52の駆動系として、駆動モータ55,モータドライバ56を固定的に配設しているが、Yテーブル52にこれらを搭載して自走式に構成してもよいことは勿論である。
更に、Yテーブル(可動ユニット)52の位置停止機構は、例えば図15(b)に示すように、支持ブラケット21aの所定部位には例えばフォトカプラなどからなる位置決めセンサ61,62を配設する一方、Yテーブル52には進退方向に延びるセンサ板63を取付け、このセンサ板63に位置合せ用のセンサスリット64を所定ピッチ毎に開設し、位置決めセンサ61,62にてセンサ板63の所定位置を検出することにより、Yテーブル52の進退位置を規制し、検査カートリッジ200の引き込み位置を制御するようになっている。
【0026】
<検体試薬分注装置>
また、図4に示す検体試薬分注機構70としては検体、試薬を分注するものであれば公知のものを適宜選定して差し支えないが、例えば図16(a)に示すように、X方向、Y方向に直交するZ方向に沿って進退移動する昇降台71を有し、この昇降台71にシリンジポンプ72に連通するノズルチャック73を取付け、このノズルチャック73にノズルチップ210を着脱自在に取り付けるようにしたものが用いられる。
本実施の形態では、検体試薬分注機構70は、図16(b)に示すように、カートリッジ引き込み機構50にて所定位置まで検査カートリッジ200を引き込み、検体試薬分注機構70の分注位置に検査カートリッジ200の分注対象セル202を配置した後、シリンジポンプ72を負圧若しくは正圧に切り替えることにより、検査カートリッジ200内の所定のセル202(検体セル203,試薬セル205,206)から検体、試薬を所定量吸引保持し、測定対象である反応セル207内に所定量の検体、試薬を吐出するものである。
【0027】
このとき、検体試薬分注機構70は検体又は試薬を個別に吸引して吐出する方式を採用してもよいし、あるいは、ノズルチップ210内で空気層を介在させることにより、検体と試薬、あるいは、複数の試薬を同時に吸引保持した後、吐出するようにしてもよいことは勿論である。
尚、本実施の形態では、検体試薬分注機構70は検体、試薬の分注動作をともに兼用する態様になっているが、夫々別に設けるようにしてもよい。また、本実施の形態では、廃棄可能なノズルチップ210を用いているが、これに限られるものではなく、ノズルチップ210を用いないで、専用ノズルを洗浄しながら使用する方式を採用してもよいことは勿論である。
【0028】
<穿孔装置>
本実施の形態では、検査カートリッジ200は、各セル202がシール215で被覆されているため、検体試薬分注機構70にて検体、試薬の分注動作を行う前に、検体試薬分注機構70のノズルチップ210が挿入可能となるように、シール215に対し挿入用の孔を穿つことが行われる。
このような要請下において、本実施の形態では、検体試薬分注機構70を穿孔装置として兼用する手法が採用されている。
つまり、穿孔動作時には、検体試薬分注機構70は、図16(c)に示すように、検査カートリッジ200の各セル202のうち使用可能なセル202(検体セル203,試薬セル205,206,反応セル207)に対応するシール215を目がけてノズルチップ210を穿孔具として用い、シール215に孔を穿つものである。
【0029】
本実施の形態において、穿孔装置として兼用される検体試薬分注機構70はシール215に対して孔を穿つものであれば、孔の穿ち方など適宜選定して差し支えないが、本実施の形態では、使用するセル202に対応するシール215部分に夫々複数の孔を穿つようになっている。詳細は後述する。
尚、本実施の形態では、検体試薬分注機構70にて穿孔装置を兼用するようにしているが、必ずしもノズルチップ210を穿孔具として利用する態様に限られるものではなく、例えば検体試薬分注機構70の昇降台71の一部に穿孔具を取付け、この穿孔具を利用して検査カートリッジ200のシール215に孔を穿つようにしてもよい。また、検体試薬分注機構70とは全く別に専用の穿孔装置を配設し、この穿孔装置にて検査カーリッジ200のシール215に孔を穿つようにしても差し支えない。
【0030】
<温度調整機構>
また、本実施の形態において、検査ステージKTには、図11及び図17〜図21に示すように、温度調整機構として恒温槽80及び補助加温装置90が設けられている。
恒温槽80は検査カートリッジ200の引き込み位置を挟むように両側から配設されており、セットステージST寄りの片側の一部が切り欠かれた非対称形状になっている。
そして、前記切り欠かれた部位には恒温槽80に代わって補助加温装置90が配設されている。尚、本実施の形態にあっては、恒温槽80の一部に補助加温装置90が設けられているが、これに限られるものではなく、恒温槽80内に補助加温装置90を組み込むようにしても差し支えない。
【0031】
―恒温槽―
本実施の形態において、恒温槽80は、図17〜図19に示すように、例えばアルミニウム製の恒温ブロック81にて周囲が覆われており、この恒温ブロック81の底面にヒータ(例えばシリコンラバーヒータ)82を取り付けると共に、恒温ブロック81の一部に例えばサーミスタからなる温度センサ83(図20参照)を設け、この温度センサ83からの温度情報をモニタリングすることにより所定の恒温条件(例えば37℃)に保つようにヒータ82をオンオフ制御するようになっている。
ここで、温度センサ83の配設位置は適宜選定して差し支えないが、例えば後述する測定装置100の近傍に配設するようにすれば測定装置100による測定ステージの環境温度を直接的に検出することになる分、恒温槽80の温度調整がより正確に行われる。
尚、恒温槽80内には必要に応じて断熱材を設け、恒温槽80内からの不必要な熱放出を抑えるように設計することが好ましい。
【0032】
―補助加温装置―
また、補助加温装置90は、図17,図18及び図21に示すように、装置筐体21のベースフレーム28上に支持ブラケット93を取付け、この支持ブラケット93に例えばアルミニウム製の加温ブロック91を揺動アーム92を介して揺動自在に支持する一方、加温ブロック91には検査カートリッジ200の各セル202(検体セル203,試薬セル204〜206,反応セル207)に対応した複数(本例では5つ)の凹所94を設け、カートリッジ引き込み機構50にて引き込まれた検査カートリッジ200の各セル202を片側から覆うことが可能な構造になっている。
ここで、加温ブロック91の背面にはヒータ95が設けられると共に、加温ブロック91の一部には例えばサーミスタからなる温度センサ96が設けられ、加温ブロック91が恒温条件より高い所定温度(例えば70℃)に加温されるようになっている。また、ヒータ95としては一定の発熱量のものでよいが、勿論発熱量調整可能なものでもよい。尚、本例ではヒータ95は主電源スイッチがオンされた時点で作動するようになっている。
【0033】
更に、本実施の形態では、加温ブロック91はその揺動アーム92を電磁ソレノイド等の駆動アクチュエータ97にて揺動自在とすることにより、図17(a)(b)及び図21(a)に示すように、検査カートリッジ200が引き込まれる位置から離間した退避位置に傾斜姿勢にて保持されると共に、図18(a)(b)及び図21(b)に示すように、検査カートリッジ200が引き込まれる位置に近接した加温位置に略直立した姿勢にて保持される。
尚、本実施の形態では、加温ブロック91は加温位置と退避位置との間で揺動するようになっているが、例えば駆動アクチュエータ97を多段シフト可能に構成し、加温ブロック91の揺動位置を多段階に調整することにより、被加温対象セルとの間の隙間寸法をパラメータとして加温ブロック91による加温量を可変設定するようにしてもよい。本態様によれば、加温ブロック91自体の発熱量が一定であっても、加温ブロック91による加温量を容易に調整することができる。勿論、加温ブロック91自体の発熱量を調整可能な態様にあっては、特に加温ブロック91の揺動位置を変化させなくても、加温ブロック91による加温量を変更することは可能である。
【0034】
更に、本実施の形態において、補助加温装置90は検査カートリッジ200の試薬セル205(試薬R1を収容)に対向した恒温槽80には例えばサーモパイルからなる非接触型温度センサ98が設けられており、この非接触型温度センサ98は検査カートリッジ200の試薬セル205の表面温度を非接触状態にて検出するようになっている。そして、駆動アクチュエータ97は非接触型温度センサ98にて検出された試薬セル205の表面温度をパラメータとしてオンオフ制御されるようになっており、試薬セル205の表面温度が目標温度(例えば恒温条件である37℃に相当)に到達しない条件下では駆動アクチュエータ97がオン動作する一方、試薬セル205の表面温度が目標温度に到達した条件下では駆動アクチュエータ97はその作動を停止するようになっている。
【0035】
また、本実施の形態では、加温目標温度を一定に設定して差し支えないが、環境温度の影響(例えばノズルチップ210の温度条件により分注した試薬R1などの温度が変化するという影響)を低減するという観点からすれば、例えば検査ステージKTの任意の箇所に恒温槽80以外の環境温度が計測可能な図示外の計測器(例えばサーミスタ等)を設け、この計測器からの温度情報に基づいて加温目標温度を変化させ、加温ブロック91による加温量を決定するようにしてもよい。例えば環境温度が基準温度である場合の加温目標温度を基準値(例えば37℃)とし、環境温度が基準温度を超える場合には加温目標温度を基準値よりも減少させ、逆に、環境温度が基準温度未満である場合には加温目標温度を増加させるようにすればよい。
【0036】
<測定装置>
また、本実施の形態では、図19、図20(a)に示すように、検査カートリッジ200の引き込み方向先端側の恒温槽80内に測定装置100が配設されている。この測定装置100は、所定の測定ステージMTを挟んで配設される例えば赤外線LEDからなる発光素子101と、測定ステージMTを挟んで前記発光素子101に対向する部位に配設される例えばフォトディテクタからなる受光素子102とを備えている。尚、符号103は発光素子101からの拡散光を検出するフォトディテクタからなる受光素子であり、受光素子102,103間の差分を検出可能としている。
そして、本実施の形態では、測定ステージMTは、図20(b)に示すように、検査カートリッジ200の反応セル207が配置されるようになっており、測定装置100は、測定ステージMTにて検査カートリッジ200の反応セル207内の検体と試薬との反応を測定するようになっている。
【0037】
<制御系>
図22は自動分析装置の制御系を示す。
同図において、符号110はマイクロコンピュータからなる制御装置であり、この制御装置110は、主電源スイッチ、各種動作センサ(スタートボタン等の操作部、位置センサ等)、各種温度センサからの情報を取り込み、各種ヒータによる温度制御処理(恒温槽80、補助加温装置90の温度制御処理など)111を行い、各種動作源による動作制御処理(Xテーブル駆動制御処理、検査カートリッジの引き込み制御処理、検体試薬分注制御処理、測定制御処理など)112を行い、更に、プリンタ部による印刷制御処理113を行うものである。
【0038】
<自動分析装置の作動>
次に、本実施の形態に係る自動分析装置の作動について説明する。
この自動分析装置を使用するに当たって、
(1)検査カートリッジのセット操作
(2)測定シーケンスの実行操作
を行うようにすればよい。
【0039】
―検査カートリッジのセット操作―
先ず、ユーザーは、図2及び図3に示すように、自動分析装置20の扉22を開放した後、自動分析装置20のセットステージSTのカートリッジラック40に検査に必要な複数の検査カートリッジ200をユーザー操作側から見て右側から順にセットすることが必要である。
このとき、セットすべき検査カートリッジ200に対する準備として、採血分注、並びに、ノズルチップ210のセットを行うことが必要である。
例えば図7に示すように、検査カートリッジ200の各検体セル203(本例では希釈液W内蔵)には夫々採血具230にて採血された血液を所定量分注する。
また、図6に示すように、検査カートリッジ200のチップ保持孔208にはノズルチップ210を上方から挿入保持させるようにすればよい。
【0040】
また、図9に示すように、カートリッジラック40に対して検査カートリッジ200は所定方向にセットされることが必要であるが、ユーザーは、カートリッジラック40のラックホルダ41のスリット43に沿って検査カートリッジ200を所定位置まで挿入させるようにすればよい。
このとき、仮に、検査カートリッジ200の挿入方向が逆方向である場合には、検査カートリッジ200の挿入動作が阻止されるようになっている。つまり、誤った方向から検査カートリッジ200を挿入しようとすると、カートリッジラック40のストッパ45に検査カートリッジ200のフランジ部216が衝合し、検査カートリッジ200の挿入方向への移動が阻止される。一方、検査カートリッジ200が正規の方向から挿入される場合には、カートリッジラック40のストッパ45に対応した検査カートリッジ200のフランジ部216に切欠217が設けられているため、検査カートリッジ200はカートリッジラック40のストッパ45に阻止されることなく挿入される。このため、カートリッジラック40に対して検査カートリッジ200は正規の方向から必ず挿入セットされる。
【0041】
―測定シーケンスの実行―
検査カートリッジ200のセット操作が終了した後、自動分析装置20の扉22を閉じ、しかる後、操作部23のスタートボタン24を操作すれば、測定シーケンスが自動的に実行される。
(1)検査カートリッジの装着確認
自動分析装置20のスタートボタン24を操作すると、先ず検査カートリッジ200の装着確認動作が行われる。
これは、カートリッジラック40の初期位置のうち、ユーザー操作側から見て右端のラックホルダ41の奥側に対応した部位に非接触型位置センサ(図示せず)からなる存在確認センサを設け、制御装置110は存在確認センサにて検査カートリッジ200の存在が確認された条件下でXテーブル30を移動開始させる。尚、存在確認センサにて検査カートリッジ200の存在が確認されない場合には、検査カートリッジ200が装着されていないことを表示ディスプレイ26に表示する等の警告を行い、ユーザーに注意を喚起する。
【0042】
(2)検査カートリッジの検査初期位置設定
この後、制御装置110は、図4に示すように、Xテーブル30を移動させ、最初の検査対象である検査カートリッジ200(本例ではユーザー側から見て右端にある検査カートリッジに相当)を検査初期位置ST1に設定する。
この状態において、例えば図25に示すように、検査初期位置ST1に対応した上部にバーコードリーダー等のマークリーダー120を配設すると共に、検査カートリッジ200に設けられたシール215の表面には検査カートリッジ200を特定するためのハーコード等のマーク(図示せず)を設け、これにより、検査対象となる検査カートリッジ200を確認した後、検査カートリッジ200の引き込み動作に移行する。尚、バーコード等のマークを付す箇所はシール215の表面に限られるものではなく、例えば検査カートリッジ200のカートリッジ本体201の適宜箇所にシール215とは別に設けるようにしてもよいことは勿論である。
【0043】
(3)検査カートリッジの引き込み動作(図25参照)
次いで、図25に示すように、カートリッジ引き込み機構50により検査初期位置ST1に設定された検査カートリッジ200を検査ステージKT側に引き込む。
本実施の形態では、カートリッジ引き込み機構50は、検査カートリッジ200の反応セル207が測定装置100の測定ステージMTに停止するように、検査カートリッジ200を引き込む。
尚、制御装置110は、主電源スイッチがオンされた時に恒温槽80のヒータ82を作動させ、恒温槽80内を所定温度(例えば37℃)になるように恒温制御している。
【0044】
(4)反応セルの状態確認動作(図23(a)参照)
検査カートリッジ200の反応セル207が測定装置100の測定ステージMTに位置決めされた段階で、制御装置110は、測定装置100にて反応セル207の状態を測定し、異常(反応セル表面の汚れや検査カートリッジの排出忘れ等)
の有無を確認する。
【0045】
(5)ノズルチップの有無確認動作(図23(a),図26,図27参照)
次いで、制御装置110は、検体試薬分注機構70をZ軸方向で移動させ、検体試薬分注機構70に検査カートリッジ200に保持されているノズルチップ210を装着させる。このとき、検体試薬分注機構70のZ軸軌道に沿った部位に非接触型位置センサからなる存在確認センサ121を配設し、この存在確認センサ121にてノズルチップ210の装着状態を確認する。尚、ノズルチップ210の装着状態が不良であることが検出された場合には、例えば表示ディスプレイ26に警告表示を行う。
【0046】
(6)空気孔開け動作
次いで、制御装置110は、図28に示すように、検体試薬分注機構70を穿孔装置として働かせ、カートリッジ引き込み機構50にて検査カートリッジ200を適宜進退させながら、検体試薬分注機構70を利用した穿孔装置にて検査カートリッジ200のシール215に空気孔を穿つように制御する。
本実施の形態では、空気孔開け動作は、図29(a)に示すように、検査カートリッジ200の使用セル202(検体セル203,試薬セル205,206,反応セル207)に対応するシール215部分に夫々複数(本例では2つ)の空気孔131,132を穿つものである。
ここで、空気孔131,132の大きさとしては、例えば1〜2mm程度でよく、ノズルチップ210の外径変化を考慮し、その挿入深さを決定するようにすればよい。
特に、本実施の形態では、各空気孔131,132は対応する使用セル202(検体セル203,試薬セル205,206,反応セル207)の開口中心133を挟んだ位置、例えば略点対称となる位置に開けられている。
尚、検査カートリッジ200の検体セル203に対応するシール215部分には検体分注時に孔135が開けられているが、ユーザー操作によりどの位置に孔を開けたか不確かであるため、本実施の形態では、検体セル203に対応したシール215部分についても、他のセルと同様に、複数の空気孔131,132を穿つように検体試薬分注機構70を利用した穿孔装置を制御する方式が採用されている。
【0047】
このように、使用セル202のシール215部分に複数の空気孔131,132を開けると、例えば図29(b)に示すように、穿孔具としてのノズルチップ210が一方の空気孔131を塞ぐように挿入されたとしても、他方の空気孔132が大気開放されているため、ノズルチップ210の挿入により使用セル202内の圧力が不必要に高くなり、ノズルチップ210による検体、試薬の吸引動作や、吐出動作が不安定になることはない。
また、穿孔具としてのノズルチップ210が使用セル202のシール215部分の開口中心133近傍に挿入されるような場合には、複数の空気孔131,132の存在により、使用セル202のシール215部分が容易に破砕され、大気開放された状態でノズルチップ210が使用セル202内に挿入される。
【0048】
特に、本実施の形態では、複数の空気孔131,132が使用セル202の開口中心133を挟んだ位置に開設されているため、検体、試薬分注時において、ノズルチップ210の挿入位置が比較的ラフであるとしても、ノズルチップ210による穿孔動作時にシール215が確実に破砕される。この点、例えば複数の空気孔131,132が使用セル202の開口中心133に対して片側に偏倚して開設されている態様にあっては、検体、試薬分注時において、シール215部分のうち空気孔131,132が開設されていない側にノズルチップ210が挿入される際に若干破砕し難いという懸念はあるものの、複数の空気孔131,132が存在する以上、一つの空気孔の場合よりも破砕し易い点で好ましい。
【0049】
ここで、比較の形態として、事前に空気孔を開設しない態様にあっては、検体、試薬分注時にノズルチップ210にてシール215を破砕し且つ使用セル202内にノズルチップ210を挿入すると、ノズルチップ210にて開けた孔が塞がれてしまうため、使用セル202内が密封状態になり易く、検体、試薬の分注動作が不安定になり易い。
また、一つの空気孔を開設する態様にあっては、一つの空気孔をノズルチップ210で塞ぐと、使用セル202内が密封になり易い虞れがあり、また、空気孔から離れたシール215部分にノズルチップ210を挿入する際には前記空気孔がノズルチップ210によるシール215部分の破砕を助長する作用が働き難いという懸念もある。このため、このような態様で使用する場合には、シール215素材として破砕し易いものを使用する等の工夫をすることが好ましい。
【0050】
(7)試薬R1の温度測定(図23(b)参照)
上述した空気孔開け動作が終了すると、制御装置110は、図30に示すように、検査カートリッジ200の試薬セル205(R1内蔵)が恒温槽80の非接触型温度センサ98に対応した位置になるように、カートリッジ引き込み機構50にて検査カートリッジ200を移動させる。
この状態において、制御装置110は、非接触型温度センサ98にて試薬セル205の表面温度(試薬R1の温度に相当)を検出し、この情報を取り込む。
【0051】
(8)試薬R1加温動作(図23(b)参照)
制御装置110は、非接触型温度センサ98からの検出温度に基づいて、非接触型温度センサ98の検出温度が加温目標温度(恒温槽80の恒温条件温度:例えば37℃)になるまで補助加温装置90による加温動作を行う。
この補助加温装置90による加温動作は、ヒータ95及び温度センサ96により、高温条件温度(例えば37℃)よりも高い温度(例えば70℃)になるように加温された加温ブロック91を駆動アクチュエータ97のオン動作にて加温位置に回動させ、非接触型温度センサ98の温度情報をモニタリングしながら、試薬R1(試薬セル205の表面温度)の温度が目標温度(恒温条件温度)に至るまで加温する。
このとき、ヒータ95は温度センサ96にて加温ブロック91が恒温条件温度(例えば37℃)よりも高い温度(例えば70℃)になるように加熱されているため、加温ブロック91による加温量は十分に大きく、その分、試薬R1の温度上昇率は、恒温槽80だけで加温される態様に比べて速い。
【0052】
特に、本実施の形態では、補助加温装置90の加温ブロック91は検査カートリッジ200の各セル202(検体セル203,試薬セル204〜206,反応セル207)に対応した凹所94を有し、各セル202を加温することが可能になるため、試薬セル205内の試薬R1のみならず、試薬セル206内の試薬R2、検体セル203内の検体、更には、反応セル207自体も補助的に加温される。
また、ノズルチップ210は補助加温されないので、後述するように、試薬R1を吸引するときに、ノズルチップ210の温度の影響を受けて試薬R1の温度が低下する懸念がある。
このような状況を有効に解消するには、自動分析装置20内の外気取り入れ付近に例えばサーミスタ等の環境温度センサを設け、環境温度に応じて加温目標温度を変化させるようにすることが好ましい。
例えば環境温度と加温目標温度との関係を以下のように設定することが挙げられる。
環境温度(℃) 加温目標温度(℃)
15 40
25 37
35 36
【0053】
(9)試薬R1吸引動作(図23(c)参照)
試薬R1が目標温度(恒温条件温度)に到達すると、制御装置110は、検体試薬分注機構70の分注位置に試薬セル205(試薬R1内蔵)が位置するようにカートリッジ引き込み機構50にて検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70のノズルチップ210にて試薬セル205のシール215部分を突き破り、試薬セル205内の試薬R1にノズルチップ210を浸漬させ、しかる後、試薬R1を所定量吸引する。
このとき、ノズルチップ210は試薬セル205のシール215部分を簡単に破砕することができ、しかも、ノズルチップ210が試薬セル205内に浸入したとしても、試薬セル205内が密封状態になる懸念はないため、ノズルチップ210による試薬R1の吸引動作は安定的に行われる。
【0054】
(10)試薬R1吐出動作(図23(d)参照)
この後、制御装置110は、検体試薬分注機構70にて試薬セル205からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて反応セル207が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70のノズルチップ210にて反応セル207のシール215部分を突き破り、反応セル207内にノズルチップ210を挿入させた後に、反応セル207内に試薬R1を所定量吐出させる。
【0055】
(11)検体撹拌動作(図24(a)参照)
次いで、制御装置110は、検体試薬分注機構70にて反応セル207からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて検体セル203が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70のノズルチップ210にて検体セル203のシール215部分を突き破り、検体セル203内にノズルチップ210を挿入させた後に、検体セル203内の検体を撹拌するようにする。
この検体撹拌動作は、例えば検体セル203内において検体に対してノズルチップ210を浸漬させ、検体の吸引、吐出を複数回行うことにより検体を撹拌する手法が採用されている。特に、ノズルチップ210を上下動させる動作を組合せ、下位置で吸引、上位置で吐出させるようにすれば、検体の撹拌動作をより促進させることができる点で好ましい。
【0056】
(12)検体バースト動作(図24(c)参照)
検体セル203内の検体の撹拌動作後、図24(c)の測定位置に所定時間放置し、検体をバーストさせる。これにより、検体内の血球が均一に分散することになり、検体の均質化を確保することが可能である。
(13)検体吸引動作(図24(a)参照)
しかる後、制御装置110は、検体試薬分注機構70のノズルチップ210を検体セル203内の検体に浸漬させ、所定量検体を吸引するようにする。
【0057】
(14)検体吐出動作(図23(d)参照)
この後、制御装置110は、検体試薬分注機構70にて検体セル203からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて反応セル207が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70にて反応セル207内にノズルチップ210を挿入させた後に、反応セル207内に検体を所定量吐出させる。
【0058】
(15)検体撹拌動作(図23(d)参照)
次いで、制御装置110は、検体試薬分注機構70のノズルチップ210にて反応セル207内の検体と試薬R1とを撹拌するようにする。
この場合の撹拌動作は、例えば反応セル207内において検体及び試薬R1に対してノズルチップ210を浸漬させ、吸引、吐出を複数回行うことにより両者を撹拌するものである。尚、撹拌動作をより促進させるためにノズルチップ210を必要に応じて上下動させてもよいことは勿論である。
【0059】
(16)試薬R2吸引動作(図24(b)参照)
この後、制御装置110は、検体試薬分注機構70にて反応セル207からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて試薬セル206(試薬R2内蔵)が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70のノズルチップ210にて試薬セル206のシール215部分を突き破り、検体試薬分注機構70にて試薬セル206内にノズルチップ210を挿入させた後に、試薬セル206内の試薬R2を所定量吸引するようにする。
【0060】
(17)試薬R2吐出動作(図23(d)参照)
この後、制御装置110は、検体試薬分注機構70にて試薬セル206からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて反応セル207が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70にて反応セル207内にノズルチップ210を挿入させた後に、反応セル207内に試薬R2を所定量吐出させる。
(18)試薬R2撹拌動作(図23(d)参照)
次いで、制御装置110は、検体試薬分注機構70のノズルチップ210にて反応セル207内の検体、試薬R1及び試薬R2を撹拌するようにする。
この場合の撹拌動作は、例えば反応セル207内において検体、試薬R1及び試薬R2に対してノズルチップ210を浸漬させ、吸引、吐出を複数回行うことにより全体的に撹拌するものである。尚、撹拌動作をより促進させるためにノズルチップ210を必要に応じて上下動させてもよいことは勿論である。
【0061】
(19)ノズルチップ排出動作
この後、制御装置110は、検体試薬分注機構70のノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて検査カートリッジ200のチップ保持孔208が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、図31に示すように、検査カートリッジ200のチップ保持孔208に検体試薬分注機構70のノズルチップ210を上方から挿入させ、検体試薬分注機構70のノズルチャック73(図16参照)によるノズルチップ210の保持状態を解除することにより、検査カートリッジ200の元の位置に廃棄すべきノズルチップ210を戻すようにする。
このノズルチップ210の排出動作は、反応セル207内の検体、試薬の反応が未だ不安定である時間帯を利用して行うため、自動分析装置20の処理能力にはほとんど影響しない。
【0062】
(20)測定動作(図24(c)参照)
そして、制御装置110は、図31に示すように、検査カートリッジ200の反応セル207が測定ステージMTに位置するように、カートリッジ引き込み機構50にて検査カートリッジ200を移動させる。
この後、制御装置110は、反応セル207が測定ステージMTに到達した状態で測定装置100による測定を所定時間(例えば1分〜5分)行う。
このとき、測定装置100は、発光素子101からの光を反応セル207内の検体と試薬との混合液に透過させ、その光変化を受光素子102にて検出すると共に、発光素子101自体の光変化を受光素子103にて検出し、反応セル207内の検体と試薬との反応変化を経時的に測定する。
【0063】
また、試薬R1の吸引、吐出の分注動作、試薬R2の吸引、吐出の分注動作、反応セル207内の撹拌等では、反応セル207は恒温槽80外に配置されるため、自動分析装置20内の環境温度の影響を受けて反応セル207内の温度が下がる懸念がある。このような状況をより正確に考慮する場合には、例えば自動分析装置20内の外気取り入れ付近に例えばサーミスタ等の環境温度センサを設け、環境温度に応じて恒温槽80の温度補正を行うようにしてもよい。
【0064】
(21)検査カートリッジ排出動作
この後、制御装置110は、図32に示すように、カートリッジ引き込み機構50にて検査済みの検査カートリッジ200をセットステージST側に戻すようにする。
(22)結果印刷動作
また、制御装置110は、測定装置100による測定結果をプリンタ部27にて印刷する。
この段階にて一つの検査カートリッジ200に対する所定の測定シーケンスが終了する。
【0065】
この後、制御装置110は、セットステージSTに未処理の検査カートリッジ200が存在することを確認の上、各検査カートリッジ200に対して一連の測定シーケンスを実行する。
具体的には、制御装置110は、例えば図3及び図4に示すように、カートリッジラック40の次のラックホルダ41に位置する検査カートリッジ200を検査初期位置ST1に設定した後、一連の測定シーケンスを行い、更に、次の検査カートリッジ200を検査初期位置ST1に設定した後に一連の測定シーケンスを実行する。
そして、全ての検査カートリッジ200について一連の測定シーケンスが終了すると、制御装置110は、表示ディスプレイ26に全検査が終了した旨の検査終了表示を行う。
この後、ユーザーは、自動分析装置20の扉22を開放し、カートリッジラック40から検査済みの検査カートリッジ200を廃棄すべきノズルチップ210と共に取り出し、廃棄するようにすればよい。
【0066】
◎実施の形態2
図33は本発明に係る自動分析装置の実施の形態2の要部を示す説明図である。
同図において、自動分析装置の基本的構成は実施の形態1と略同様であるが、測定装置100の構成が実施の形態1と異なっている。
つまり、本実施の形態では、測定装置100は、測定ステージMTを挟んで発光素子101と受光素子102とを対向配置した態様であるが、発光素子101が検査項目に応じて交換可能に構成されている。
この種の発光デバイスとしては、波長特性の異なる複数の発光素子101(101a〜101c)が夫々含まれる複数の光源ボード141〜143を予め用意しておき、検査項目に応じてボード装着部145に必要な光源ボード141〜143のいずれかを抜き差し可能に装着し、各光源ボード141〜143のいずれかに対応する発光素子101を使用するものが挙げられる。
【0067】
また、この種の測定装置100としては、図33に示す態様に限られるものではなく、例えば図34に示すように、回転プレート150に複数の発光素子101(101a〜101c)を所定の円弧軌跡上に配列し、検査項目に応じて回転プレート150を適宜位置に回転させ、所定の発光素子101を使用するものが挙げられる。尚、回転プレート150ではなく、図示外の直線プレートに複数の発光素子を配列し、検査項目に応じて必要な発光素子を使用するようにしても差し支えない。
【0068】
◎実施の形態3
図35〜図39は本発明に係る自動分析装置の実施の形態3の要部を示す説明図である。
同図において、自動分析装置の基本的構成は実施の形態1と略同様であるが、ノズルチップ210の廃棄方式が実施の形態1と異なるものになっている。尚、実施の形態1と略同様な構成要素については実施の形態1と同様な符号を付してここではその詳細な説明を省略する。
本実施の形態においては、セットステージSTは、例えば図35(1)に示すように、実施の形態1と同様に、Xテーブル30上に複数(例えば3つ)の検査カートリッジ200が保持可能なカートリッジラック40を設けているが、実施の形態1と異なり、カートリッジラック40に隣接した部位にノズルチップ210の廃棄ラック160を設け、この廃棄ラック160にはノズルチップ専用の廃棄カートリッジ170を検査カートリッジ200と略平行に且つY方向に対して進退自在に設けたものである。
ここで、廃棄カートリッジ170は、廃棄ラック160に摺動自在に保持されるカートリッジ本体171を有し、このカートリッジ本体171に廃棄用のノズルチップ210が保持可能な複数(例えば3つ)のチップ保持部172〜174を開設したものである。
【0069】
次に、本実施の形態に係る検査カートリッジ200及びノズルチップ210の動作過程について説明する。
先ず、図35(1)はカートリッジラック40に各検査カートリッジ200が保持されており、一つの検査カートリッジ200が検査初期位置ST1に位置する状態を示す。
この後、図35(2)に示すように、検査初期位置ST1に位置する検査カートリッジ200がカートリッジ引き込み機構50にて検査ステージKT側に引き込まれ、検査カートリッジ200が図示外の補助加温装置にて補助的に加温される。
更に、図36(3)に示すように、図示外の検体試薬分注機構にノズルチップ210が装着される。
しかる後、図36(4)に示すように、カートリッジ引き込み機構50にて検査カートリッジ200が適宜移動させられ、検体試薬分注機構による検体、試薬の分注動作、測定装置100による測定動作が行われる。
【0070】
そして、測定装置100による測定が終了すると、図37(5)に示すように、カートリッジ引き込み機構50が検査済みの検査カートリッジ200をセットステージSTのカートリッジラック40に戻す。
このとき、ノズルチップ210は図示外の検体試薬分注機構に装着されたままである。
この後、図37(6)に示すように、Xテーブル30が矢印方向に移動し、廃棄ラック160に保持されている廃棄カートリッジ170が検査初期位置ST1に設定される。
この後、図38(7)に示すように、カートリッジ引き込み機構50が廃棄カートリッジ170を検査ステージKT側に引き込み、検体試薬分注機構の分注位置に廃棄カートリッジ170のチップ保持部172が位置するように廃棄カートリッジ170を移動する。
【0071】
そして、図38(8)に示すように、検体試薬分注機構は、装着されたノズルチップ210の装着状態を解除した後、廃棄カートリッジ170のチップ保持部172にノズルチップ210を挿入保持させる。
この後、図39(9)に示すように、カートリッジ引き込み機構50が廃棄カートリッジ170をセットステージST側に戻す。
更に、残りの検査カートリッジ200についても同様な測定シーケンスが行われ、その測定シーケンスで用いられた各ノズルチップ210は夫々廃棄カートリッジ170のチップ保持部173,174に保持される。
そして、自動分析装置の全検査が終了した時点で、検査済みの検査カートリッジ200並びに廃棄カートリッジ170に保持された複数のノズルチップ210が夫々廃棄される。
【0072】
実施の形態1,3はいずれも廃棄用のノズルチップ210をセットステージST側に戻した後に廃棄するようにしているが、例えば検査ステージKT側で別途廃棄ステージを設け、その廃棄ステージに廃棄用のノズルチップ210を廃棄する等適宜選定して差し支えない。
【0073】
◎実施の形態4
図40は本発明に係る自動分析装置の実施の形態4の要部を示す説明図である。
同図において、自動分析装置20の基本的構成は、実施の形態1と略同様であるが、実施の形態1と異なり、検査ステージKTには補助加温装置90を設けることなく、恒温槽80のみを備えており、恒温条件温度(例えば37℃)に達する前に検査カートリッジ200の反応セル207内の液反応を測定開始するようにしたものである。尚、実施の形態1と同様な構成要素については実施の形態1と同様な符号を付してここではその詳細な説明を省略する。
本実施の形態では、恒温槽80は、図40及び図41に示すように、検査カートリッジ200が収容可能で少なくとも測定ステージMTが恒温条件温度(例えば37℃)に保たれる恒温ブロック81を有し、この恒温ブロック81は測定装置100(発光素子101,受光素子102,103)部分を両側から覆うばかりでなく、実施の形態1の補助加温装置90の設置箇所に対応した部位をも両側にて覆うようになっている。
また、本実施の形態では、恒温槽80には実施の形態1と同様な非接触型温度センサ98が配設されているが、この非接触型温度センサ98は、検査カートリッジ200の反応セル207内の初期液温データT0、所定時間(例えば3分)経過後の反応セル207内の液温データT1を測定し、後述する制御装置110にデータ入力するようになっている。
【0074】
また、本実施の形態において、自動分析装置の制御系を図42に示す。
同図において、符号110はマイクロコンピュータからなる制御装置であり、この制御装置110は、主電源スイッチ、各種動作スイッチ(スタートボタン等の操作部、位置センサ等)、各種温度センサからの情報を取り込み、温度補正テーブル115を参照しながら反応セル207内の液に対する温度制御処理111(恒温槽80のヒータ83による温度制御処理)を行い、各種動作源による動作制御処理(Xテーブル駆動制御処理、検査カートリッジの引き込み制御処理、検体試薬分注制御処理、測定制御処理など)112を行い、更に、プリンタ部による印刷制御処理113を行うものである。
特に、本実施の形態において、温度補正テーブル115は、反応セル207内の初期液温データT0、反応セル内の所定時間(例えば3分)経過後の測定開始時の液温データT1とに基づく温度補正係数k(T0,T1)などの補正情報を保有し、制御装置110は、非接触温度センサ98からの入力データに基づいて温度補整テーブル115を検索し、対応する温度補正係数k(T0,T1)などの補正情報を選定し、測定装置100による測定結果について恒温条件温度(例えば37℃)で反応したであろう状態に補正するようになっている。
ここで、温度補正テーブル115内の補正情報としては予め実測されたデータに基づいて演算決定されたものが用いられる。
【0075】
従って、本実施の形態によれば、実施の形態1と同様に、検査カートリッジ200のセット操作を行った後、スタートボタンを操作することにより以下のような測定シーケンスが実行される。
(1)検査カートリッジの装着確認
(2)検査カートリッジの検査初期位置設定
(3)検査カートリッジの引き込み動作
(4)反応セルの状態確認動作
(5)ノズルチップの有無確認動作
(6)空気孔開け動作
(7)試薬R1の温度測定
ここまでは実施の形態1と略同様であるので、その詳細については省略する。
但し、試薬R1の温度測定の結果は試薬セル205表面に対する温度計測であるが、本実施の形態ではこれを反応セル207内の初期液温データT0とし、制御装置110に取り込む。尚、反応セル207内に試薬R1を吐出した後の液温を初期液温データT0としてもよいことは勿論である。
【0076】
この後、以下の動作へと移行する。
(8)試薬R1吸引動作
(9)試薬R1吐出動作
(10)検体撹拌動作
(11)検体バースト動作
(12)検体吸引動作
(13)検体吐出動作
(14)検体撹拌動作
(15)試薬R2吸引動作
(16)試薬R2吐出動作
(17)試薬R2撹拌動作
(8)〜(17)までは実施の形態1と略同様であるので、その詳細は省略する。
【0077】
(18)反応セル内の液温測定
反応セル207内の初期液温データT0の測定から所定時間(例えば3分)経過後の液温データを測定開始時の液温データT1を測定し、制御装置110に取り込む。
(19)ノズルチップ排出動作
(20)測定動作
(21)検査カートリッジ排出動作
(19)〜(21)は実施の形態1と略同様であるので、ここではその詳細な説明を省略する。
(22)結果印刷動作
測定動作終了後、制御装置110は、非接触型温度センサ98からの温度データT0,T1に基づいて温度補正テーブル115にて温度補正係数k(T0,T1)等の補正情報を決定し、この補正情報に基づいて測定結果を恒温条件での測定結果になるように補正し、この補正結果を印刷する。尚、補正前の測定結果自体を参考データとして印刷するようにしてもよいことは勿論である。
【実施例】
【0078】
◎実施例1
実施の形態1に係る自動分析装置を実施例とし、検査ステージKTに検査カートリッジ200を引き込んだ後、補助加温装置90及び恒温槽80を使用し、試薬セル205が恒温条件温度(本例では37℃)に到達するまでの時間を測定したところ、図43に示す‘プレヒート有’の結果が得られた。また、比較例として、補助加温装置90を用いないで恒温槽80のみで試薬セル205が恒温条件温度(本例では37℃)に到達するまでの時間を測定したところ、図43に示す‘プレヒート無’の結果が得られた。但し、実施例、比較例共に環境温度が23℃である条件下で行った。
図43によれば、実施例では、恒温条件温度に到達するまでの時間が30秒弱であるのに対し、比較例では、恒温条件温度に到達するまでの時間が約5分程度かかり、補助加温装置90により検査カートリッジ200の温度を早期に恒温条件温度に調整することが可能になり、仮に、検体が冷蔵庫などに保管され、また、検査カートリッジ200が恒温条件温度よりも低い環境下に置かれていたとしても、恒温条件の下で、検査カートリッジ200に対する測定時間を短縮可能であることが理解される。
【0079】
◎実施例2
実施の形態4に係る自動分析装置を実施例2とし、検査カートリッジ200の反応セル207内の液温立ち上がり状態、並びに、反応セル207内の所定時間(例えば3分)経過後の液温を測定し、モニタリングする。
これらの結果を図44,図45に示す。
図44は反応セル207内の液温立ち上がり状態をモニタリングしたものである。
同図においては、液温初期温度T0を15℃、20℃、25℃、30℃の4通りについて液温立ち上がり状態を測定し、恒温条件温度(例えば37℃)に到達するまでの時間tを計測したところ、以下のような結果が得られた。
液温初期温度T0 恒温条件温度到達時間t
15℃ 5分 2秒
20℃ 4分26秒
25℃ 3分51秒
30℃ 3分10秒
これらの結果からすれば、液温初期温度T0が高いと恒温条件温度に達する時間は短く、逆に低いと恒温条件温度に達する時間が長くなるという相関関係が把握される。
【0080】
また、図45は反応セル207内の液温立ち上がり状態のうち、所定時間(例えば3分)経過後の液温を測定したところ、以下のような結果が得られた。
液温初期温度T0 所定時間経過後の液温T1
15℃ 34.2℃
20℃ 35.4℃
25℃ 36.2℃
30℃ 36.8℃
これらの結果からすれば、液温初期温度T0が高い程、定時間経過後の液温T1は恒温条件温度(例えば37℃)に接近した状態に至ることが理解される。
このため、仮に、恒温条件温度に達しない状態で所定時間(例えば3分)経過後に測定装置100による測定を開始したとしても、各温度条件において、恒温条件を満たしていない状況での反応時間、恒温条件を満たした状況での反応時間を把握することは可能である。このとき、恒温条件を満たしていない状況での反応が恒温条件を満たしている状況に対する影響度合を補正情報として予め保有しておけば、恒温条件を満たしていない状況での反応に対する測定結果を有効に補正することは可能である。
それゆえ、仮に、恒温条件温度に達しない状態で所定時間経過後に測定装置100による測定を開始したとしても、所定の温度補正処理を行うことで測定結果を補正することが可能になり、測定装置100による測定開始時間を速めることができる。
【産業上の利用可能性】
【0081】
本発明は、複数の検査カートリッジを連続検査する際に有効であるが、より簡略化した自動分析装置技術として、カートリッジ受部に一つの検査カートリッジをセットし、この検査カートリッジを検査ステージ側に引き込み、各種検査を行った後に再びカートリッジ受部に戻すような方式に構築することも可能である。
【図面の簡単な説明】
【0082】
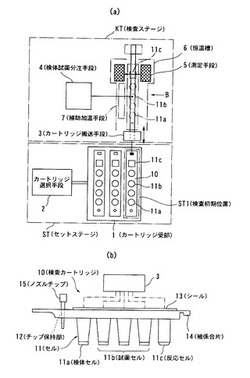
【図1】(a)は本発明に係る自動分析装置の概要を示す説明図、(b)は(a)中B方向から見た検査カートリッジの一例を示す模式図である。
【図2】本発明に係る自動分析装置の実施の形態1の外観を示す説明図である。
【図3】実施の形態1に係る自動分析装置の内部構造の概要を示す説明図である。
【図4】実施の形態1に係る自動分析装置の平面模式図である。
【図5】検査カートリッジのセット、引き込み動作に伴う機構を示す説明図である。
【図6】(a)は実施の形態で用いられる検査カートリッジの構成を示す斜視説明図、(b)はその正面説明図、(c)は同図(b)中C方向から見た矢視図である。
【図7】検査カートリッジへの検体の分注方法の一例を示す説明図である。
【図8】検体としての血液を採取する採血具の一例を示し、(a)は採血時の状態、(b)は採取した血液を吐出する際の状態を示す説明図である。
【図9】(a)はカートリッジラックの正面説明図、(b)はその側面説明図である。
【図10】実施の形態で用いられるカートリッジ引き込み機構の一例を示す説明図である。
【図11】図10の平面説明図である。
【図12】図10の側面説明図である。
【図13】実施の形態で用いられるカートリッジ引き込み機構の駆動系を示す説明図である。
【図14】図13の側面説明図である。
【図15】(a)はカートリッジ引き込み機構の動作過程を示す説明図、(b)はカートリッジ引き込み機構の位置規制例を示す説明図である。
【図16】実施の形態で用いられる検体試薬分注機構の一例であり、(a)はノズルチップ装着時の状態を示す説明図、(b)は検体試薬分注時の状態を示す説明図、(c)は穿孔装置を兼用する際の状態を示す説明図である。
【図17】実施の形態で用いられる検査ステージの測定周辺部に設けられる温度調整機構の構成例を示す説明図であり、(a)は補助加温装置が退避位置に位置する状態での全体斜視図、(b)は同図(a)中B方向から見た矢視図である。
【図18】実施の形態で用いられる検査ステージの測定周辺部に設けられる温度調整機構の構成例を示す説明図であり、(a)は補助加温装置が加温位置に位置する状態での全体斜視図、(b)は同図(a)中B方向から見た矢視図である。
【図19】(a)は実施の形態で用いられる恒温槽の斜視説明図、(b)はその側面説明図である。
【図20】(a)は図19(b)中A−A線断面説明図、(b)は測定ステージに検査カートレッジの反応セルがセットされた状態を示す説明図である。
【図21】(a)は実施の形態で用いられる補助加温装置の退避状態を示す説明図、(b)は同補助加温装置の加温状態を示す説明図である。
【図22】実施の形態1で用いられる制御系を示す説明図である。
【図23】(a)〜(d)は実施の形態1に係る自動分析装置の動作過程を示す説明図(1)である。
【図24】(a)〜(c)は実施の形態1に係る自動分析装置の動作過程を示す説明図(2)である。
【図25】実施の形態1で用いられる自動分析装置のバーコード読取動作過程を模式的に示す説明図である。
【図26】実施の形態1で用いられる自動分析装置のノズルチップの有無確認動作過程(1)を模式的に示す説明図である。
【図27】実施の形態1で用いられる自動分析装置のノズルチップの有無確認動作過程(2)を模式的に示す説明図である。
【図28】実施の形態1で用いられる自動分析装置の空気孔開け動作過程を模式的に示す説明図である。
【図29】(a)は図28の空気孔開け動作過程の詳細を示す説明図、(b)は空気孔開けの利点を示す説明図である。
【図30】実施の形態1で用いられる自動分析装置のプレヒート過程、試薬、検体分注動作過程を模式的に示す説明図である。
【図31】実施の形態1で用いられる自動分析装置のノズルチップ排出動作、測定動作過程を模式的に示す説明図である。
【図32】実施の形態1で用いられる自動分析装置の検査カートリッジ排出動作過程を模式的に示す説明図である。
【図33】実施の形態2に係る自動分析装置で用いられる測定装置を示す説明図である。
【図34】実施の形態2で用いられる測定装置の変形形態を示す説明図である。
【図35】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(1)(2)を示す説明図である。
【図36】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(3)(4)を示す説明図である。
【図37】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(5)(6)を示す説明図である。
【図38】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(7)(8)を示す説明図である。
【図39】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(9)を示す説明図である。
【図40】実施の形態4に係る自動分析装置の概要を示す図4に相当する説明図である。
【図41】実施の形態4で用いられる自動分析装置の検査ステージの要部を示す説明図である。
【図42】実施の形態4に係る自動分析装置の制御系を示す説明図である。
【図43】実施例1に係る自動分析装置の性能を示す説明図である。
【図44】実施例2に係る自動分析装置の性能(反応セル内の液温立ち上がり性能)を示す説明図である。
【図45】実施例2に係る自動分析装置の性能(反応セル内液温モニタリング)を示す説明図である。
【符号の説明】
【0083】
1…カートリッジ受部,2…カートリッジ選択手段,3…カートリッジ搬送手段,4…検体試薬分注手段,5…測定手段,6…恒温槽,7…補助加温手段,10…検査カートリッジ,11…セル,11a…検体セル,11b…試薬セル,11c…反応セル,12…チップ保持部,13…シール,15…ノズルチップ,ST…セットステージ,ST1…検査初期位置,KT…検査ステージ
【技術分野】
【0001】
本発明は、血液などの検体と試薬との反応を分析する自動分析装置に係り、特に、複数の検査カートリッジを自動的に分析する態様に有効な自動分析装置の改良に関する。
【背景技術】
【0002】
従来この種の自動分析装置としては、血液などの検体が収容される検体セル、試薬が収容される試薬セル及び検体、試薬が反応させられる反応セルが含まれる検査カートリッジ(カートリッジ容器)を用い、検査カートリッジの検体と試薬との反応を自動分析する方式が既に提供されている(例えば特許文献1参照)。
ところで、この種の自動分析装置にあっては、複数の検査カートリッジを自動的に分析したいという要請がある。このような要請に基づいて、複数の検査カートリッジを所定方向に配列すると共に、コンベアにて順次検査カートリッジを搬送し、各作業ステージにて検体試薬分注機構による検体、試薬の分注を行い、測定装置による測定を行うものである。
【0003】
【特許文献1】特許第2731613号公報(実施例,図1,図3)
【発明の開示】
【発明が解決しようとする課題】
【0004】
しかしながら、この種の特許文献1記載の先行技術にあっては、検査ステージ内に検査カートリッジ搬送用のコンベアを配設し、かつ、各作業ステージを設けているため、検査ステージの設置スペースが増大すると共にその構成が複雑になるという懸念がある。
本発明は、以上の技術的課題を解決するためになされたものであって、検査ステージの設置スペース、構成を最小限に抑えながら、検査カートリッジを用いた効率的な連続検査を可能とする自動分析装置を提供するものである。
【課題を解決するための手段】
【0005】
すなわち、本発明は、図1(a)(b)に示すように、検体が収容される検体セル11a、試薬が収容される試薬セル11b及び検体、試薬が反応させられる反応セル11cが含まれる検査カートリッジ10を用い、夫々の検体に対応する複数の検査カートリッジ10をセットした後、検査カートリッジ10毎に検体と試薬との反応を自動分析する自動分析装置において、セットステージST内に複数の検査カートリッジ10が所定の配列方向に沿って予めセットされるカートリッジ受部1を有し、このセットステージST内の検査初期位置ST1に順次移送選択するカートリッジ選択手段2と、セットステージSTに隣接する検査ステージKTに設けられ、カートリッジ選択手段2にて検査初期位置ST1に移送選択された検査前の検査カートリッジ10を検査ステージKTに直線的に搬入すると共に検査後の検査カートリッジ10を検査ステージKTからセットステージSTに直線的に搬出するカートリッジ搬送手段3と、このカートリッジ搬送手段3にて搬入された検査ステージKT内の検査カートリッジ10に対し当該検査カートリッジ10の検体、試薬を反応セルに分注する検体試薬分注手段4と、この検体試薬分注手段4にて分注された反応セル11c内の検体と試薬との反応を測定する測定手段5とを備えたことを特徴とするものである。
尚、図1(a)(b)は本発明が適用される自動分析装置の代表的態様を模式的に示したものであり、本発明の態様が図1(a)(b)に示す態様に限定されるものではない。
【0006】
このような技術的手段において、検査カートリッジ10の形態は直線的なものに限られず例えば試薬セル等を二列配置する態様なども含む。また、規定したセル11の数も適宜選定してよいし、他の機能部(例えば他のセルや着脱自在なノズルチップの保持部等)を備えていてもよい。
また、本件は、複数の検査カートリッジ10を連続的に自動分析することを主として想定していることから、カートリッジ受部1は複数の検査カートリッジ10が保持可能であることを要する。但し、カートリッジ受部1に一つの検査カートリッジ10をセットして使用することは差し支えない。
更に、検査初期位置ST1は通常は一つであるが複数設けても差し支えない。但し、複数設けた態様にあっては、検査ステージKT側のカートリッジ搬送手段3,検体試薬分注手段4及び測定手段5を複数設け、夫々の検査初期位置ST1に設定された検査カートリッジ10に対する検査を並列的に行うことが好ましい。
【0007】
また、カートリッジ搬送手段3は直線的に検査カートリッジ10を搬入、搬出するものであればよく、回転方式などは含まない。このため、検査ステージKTの設置スペースを必要最小限に抑えることができる。
更に、検体試薬分注手段4は検体、試薬の分注を共通のデバイスで構築してもよいし、別体のデバイスで構築してもよい。また、後述するように、着脱自在なノズルチップ15を用いる態様に限られるものではなく、ノズルチップ15を用いずに洗浄手段にて検体試薬分注手段を洗浄するようにしてもよい。更に、本件の検体には希釈したものも含まれる。
更にまた、測定手段5は予め決められた反応を一義的に測定するものであってもよいし、複数種の反応を測定するものであってもよい。ここで、測定手段5の代表的態様としては、反応セル11cに所定の波長の光を照射する発光素子と、反応セル11cを挟んで発光素子と対向する部位に配設される受光素子とを備えたものが挙げられる。
【0008】
また、検査カートリッジ10の好ましい態様としては、各セル11が直線的に配列されている態様が挙げられる。本態様によれば、カートリッジ搬送手段3,検体試薬分注手段4の動きを直線的な軌跡にすることができ、構成を簡略化できる。
更に、検査カートリッジ10の好ましい態様としては、カートリッジ受部1に沿って案内挿入され、カートリッジ本体には誤った方向からの挿入時に前記カートリッジ本体に衝合するストッパを具備させるようにすればよい。本態様によれば、検査カートリッジ10の逆向きでの挿入を有効に防止可能である点で好ましい。
また、カートリッジ選択手段2の好ましい態様としては、複数の検査カートリッジ10がセットされるカートリッ受部1全体を移送せるものが挙げられる。この場合、検査カートリッジ10の検査初期位置ST1への選択動作を簡略化できる点で好ましい。
更に、カートリッジ選択手段2の好ましい態様としては、一つの検査初期位置ST1に各検査カートリッジ10を順次移送選択するものが挙げられる。この場合、一つの検査初期位置ST1に対して一つの検査ステージKTを構築すればよく、検査ステージKTを簡略化することが可能である。
【0009】
また、カートリッジ搬送手段3の好ましい態様としては、カートリッジ選択手段2による検査カートリッジ10の移送動作を許容し、検査初期位置ST1に位置する検査カートリッジ10の被係合片14に対して係合可能な係合片を備えているものが挙げられる。本態様によれば、カートリッジ選択手段2による検査カートリッジ10の移送動作中に、カートリッジ選択手段2とカートリッジ搬送手段3との間で干渉し合うことがなく、カーリッジ搬送手段3を一時退避させるなどの機構が不要である点で好ましい。
更に、検体試薬分注手段5の代表的態様としては、検査カートリッジ10毎に着脱自在なノズルチップ15を使用するものが挙げられる。本態様によれば、着脱自在なノズルチップ15を使用することで、検体試薬分注手段4を洗浄する工程を省略することが可能になる点で好ましい。
更にまた、測定手段5の好ましい態様としては、検査カートリッジ10の検査項目に対応して測定条件を可変にするものが挙げられる。本態様によれば、複数の検査項目に簡単に対応することができる点で好ましく、例えば光学式の測定手段5にあっては、波長の異なる光源を複数具備させる(回転板に複数設置、光源基板を差し替えるなど)方式が好ましい。
【0010】
また、検査ステージKTの好ましい態様としては、カートリッジ搬送手段3にて検査ステージKTに搬入された検査カートリッジ10の少なくとも反応セル11cを所定の恒温環境温度に保つ恒温槽6が設けられている態様が挙げられる。本態様によれば、反応セル11cでの検体と試薬との反応を同じ条件下で測定することが可能である点で好ましい。
更に、検査ステージKTの好ましい態様としては、恒温槽6に加え、更に、測定手段5が動作する前に恒温環境温度よりも高い温度で検査カートリッジ10のセル11の少なくとも一部を予め加温する補助加温手段7が設けられている態様が挙げられる。本態様によれば、恒温条件に至るまでの時間を短縮することができ、その分、検体試薬分注手段4による分注処理、測定手段5による測定処理を迅速に開始することが可能である点で好ましい。
ここで、補助加温手段7による加温対象範囲は、検査カートリッジ10のセル11の少なくとも一部であればよく、例えば試薬セル11bの全部若しくは一部だけでもよいし、あるいは、検体セル11a内に希釈液などが予め収容されている場合には検体セル11aであってもよいし、あるいは、反応セル11cについて検体や試薬を分注する前若しくは後に補助加温するようにしてもよいし、これらを適宜組合せたり、全てのセル11を補助加温対象にしてもよい。尚、補助加温手段7による補助加温範囲は一定で差し支えないが、例えば補助加温範囲を複数に分割しておき、必要に応じて補助加温範囲を可変設定するようにしてもよい。
【0011】
更にまた、恒温槽6を備えている態様において、測定手段5の好ましい態様としては、測定手段5による測定条件が恒温槽の恒温環境条件から外れたときに、温度条件に基づいて測定結果が補正可能な温度補正手段を備えている態様がある。この場合、恒温槽6による恒温環境条件に満たなくても、温度補正手段により測定結果を補正することができることから、測定処理の開始時間を速めることができる。
ここで、温度補正手段の代表的態様としては、検査カートリッジ10の表面に対して非接触配置される非接触型温度センサからの温度情報に基づいて温度補正するものが挙げられる。この場合において、非接触型温度センサは例えば恒温槽6に取り付けられるが、これに限られるものではなく、適宜箇所に設けて差し支えない。
また、検体試薬分注手段4がノズルチップ15を使用する方式にあっては、検査カートリッジ10としては、ノズルチップ15を着脱自在に保持するチップ保持部12を有する態様が好ましい。この場合、チップ保持12には新規なノズルチップ15を保持してもよいし、使用済みのノズルチップ15を保持させ、検査済みの検査カートリッジ10と共に廃棄するようにしてもよい。
更に、着脱自在なノズルチップ方式の好ましい態様としては、検査カートリッジ10はセル11の全部若しくは一部を穿孔可能なシール13にて密封し、検体試薬分注手段4のノズルチップ15にて検体、試薬の分注動作前にセル11に対応するシール13に孔を穿設可能とするものであることが好ましい。
【発明の効果】
【0012】
本発明によれば、複数の検査カートリッジがセットされるセットステージと、セットステージと隣接して設けられ且つセットステージの複数の検査カートリッジを順次搬入しながら検査を進める検査ステージとを備え、検査カートリッジを引き込み検査する方式を採用したので、検査ステージの設置スペース、構成を最小限に抑えながら、効率的な連続検査を実現することができる。
【発明を実施するための最良の形態】
【0013】
以下、添付図面に示す実施の形態に基づいてこの発明を詳細に説明する。
◎実施の形態1
<全体構成>
図2は本発明が適用された自動分析装置の実施の形態1の外観を示す説明図である。
同図において、自動分析装置20は、装置筐体21の前面側(ユーザーの操作側)に開閉可能な扉22を有すると共に、この扉22の開口部の上方には操作部23(スタートボタン24,操作ボタン25、表示ディスプレイ26を具備)を有し、ユーザーが前記扉22を開放した状態で装置筐体21内に検査すべき検体が分注された複数(例えば3つ)の検査カートリッジ200をセットし、しかる後、スタートボタン24を操作することにより、複数の検査カートリッジ200の検体について順次自動分析するものである。
【0014】
本実施の形態において、自動分析装置20は、図2〜図5に示すように、装置筐体21内に、検査カートリッジ200がセットされるセットステージSTと、このセットステージSTに隣接して設けられ且つ検査カートリッジ200の検体について分析検査する検査ステージKTと、各検査カートリッジ200の検査結果を印刷するプリンタ部27とを備えている。
セットステージSTは、装置筐体21のベースフレーム28上に装置筐体21の幅方向(X方向)に沿って移動するXテーブル30を配設し、このXテーブル30上に検査カートリッジ200が保持可能なカートリッジラック40を設け、予め決められた検査初期位置ST1に検査カートリッジ200を順次移動させるものである。
ここで、Xテーブル30としてはX方向に延びる固定台31又はガイドレールに沿って可動台32を摺動自在に設けたものが用いられる。また、Xテーブル30の位置規制については図示外の位置センサを用いた公知の手法や、パルスモータ等の駆動モータを用いた位置制御にて行われる。
また、検査ステージKTは、セットステージSTの検査初期位置ST1に移動設定された検査カートリッジ200をX方向と直交するY方向に沿って検査ステージKT側に戻し可能に引き込むカートリッジ引き込み機構50と、検査カートリッジ200に対して検体、試薬を分注する検体試薬分注機構70と、検査カートリッジ200の少なくとも一部(後述する反応セルに相当)を恒温条件に保つ恒温槽80と、この恒温槽80とは別に設けられ且つ検査カートリッジ200を恒温条件よりも高い温度にて補助的に加温する補助加温装置90と、恒温槽80の内部に設けられて検査カートリッジ200の反応セルに分注された検体と試薬との反応を測定する測定装置100とを備えている。
【0015】
<検査カートリッジ>
次に、検査カートリッジ200について説明する。
本実施の形態において、検査カートリッジ200は、図6(a)〜(c)に示すように、例えばポリプロピレン等の合成樹脂にて成形され且つY方向に沿って直線状に延びるカートリッジ本体201を有し、このカートリッジ本体201には有底の複数のセル202を一体的に且つ直線的に配列したものである。
本実施の形態において、セル202は、カートリッジ本体201の挿入方向端から離間した側から順に、検体が収容される一つの検体セル203と、試薬が収容可能な複数(例えば3つ)の試薬セル204〜206と、検体と試薬とが分注されて反応させられる一つの反応セル207とを備えている。尚、例えば検体セル203や反応セル207が複数設けられるなど適宜選定できることは勿論である。
【0016】
特に、本実施の形態では、セル202のうち、反応セル207は略矩形筒状断面を有する容器であり、セル外壁面がX方向に直交する平面として構成されているのに対し、他のセル202、具体的には検体セル203、試薬セル204〜206は円筒状断面を有する形状として構成されている。また、本実施の形態では、複数の試薬セル204〜206の
うち、一つの試薬セル204は未使用で、他の二つの試薬セル205,206にR1,R2の試薬(図7参照)が所定量予め分注されている。一方、本実施の形態では、検体セル203には希釈液W(図7参照)が所定量予め分注されている。
【0017】
更に、本実施の形態では、カートリッジ本体201の挿入方向端から離間した側には検体セル202に隣接してチップ保持孔208が貫通した状態で開設されており、このチップ保持孔208には検体試薬分注機構70に着脱自在に装着可能なノズルチップ210が上方から離脱可能に係止保持されている。
そして更に、カートリッジ本体201の挿入方向端とは反対側には把持部211が突出形成されており、この把持部211の裏面には指押さえ212が突出形成されている。
一方、カートリッジ本体201の挿入方向端側には下側に開口したU字状の被係合片213が形成されている。
【0018】
更に、本実施の形態では、カートリッジ本体201の各セル202(203〜207)の開口縁には上方に突出する突縁214が設けられており、各セル202(203〜207)の開口はシール215にて上方から被覆されている。このとき、各セル202の突縁214がシール215に接触するため、各セル202は突縁214を介して完全に密封状態で仕切られることになり、セル202内の試薬や希釈液が他のセルに流入する懸念は有効に回避される。
また、セル202の一部、例えば検体セル203及び試薬セル204はX方向に対して非対称形状になっており、少なくとも片側にフランジ部216が形成される一方、前記他方側のフランジ部216の一部に切欠217が設けられている。
【0019】
<採血具>
また、本実施の形態では、図7に示すように、検査カートリッジ200の検体セル203には採血具230で採取した血液からなる検体が分注されるようになっている。
本実施の形態において、採血具230は、図7及び図8に示すように、両端が開口する筒状のポリプロピレン等の透明若しくは半透明の合成樹脂製の本体パイプ231と、この本体パイプ231の一端に連通可能に接続され且つ本体パイプ231の一端から突出配置されると共に毛管現象(毛細管現象)にて血液240が採取可能なガラス管又はポリエチレンテレレート等の透明若しくは半透明の合成樹脂製の毛管パイプ232と、本体パイプ231の他端に連通可能に接続され且つ本体パイプ231の他端から突出配置されると共に弾性材(例えばシリコーンゴム)にて潰れ変形可能に構成される弾性パイプ233とを備えている。
【0020】
そして、本実施の形態において、毛管パイプ232は本体パイプ231の一端開口縁に毛管ホルダ234を介して嵌合保持されている。
この毛管ホルダ234は透明若しくは半透明の材料である例えばシリコーンゴム等の弾性材料からなる円柱部材の中央に毛管パイプ232が挿通可能な挿通孔を有するものであり、毛管パイプ232は毛管ホルダ234の挿通孔の両端から突出するように毛管ホルダ234の挿通孔縁にて圧入固定され、毛管ホルダ234に対して交差配置された状態でサブユニット化されている。そして、毛管ホルダ234は本体パイプ231の一端開口縁に圧入固定されている。尚、毛管パイプ232、毛管ホルダ234は必要に応じて接着固定するようにしてもよい。
そして、毛管パイプ232は本体パイプ231の内部に毛管ホルダ234から突出寸法mだけ突出配置されると共に、本体パイプ231の外部に毛管ホルダ234から突出寸法hだけ突出配置されている。
本実施の形態では、突出寸法mは1.0mm以上確保されており、本体パイプ231内のうち、毛管パイプ232と毛管ホルダ234との間に溝部235が形成されている。
また、突出寸法hは3.0mm以上、好ましくは10.0mm以上確保されており、毛管パイプ232の先端に接する血液240が本体パイプ231の端部に付着しないように配慮されている。
【0021】
次に、本実施の形態に係る採血具の使用方法について説明する。
先ず、採血時について説明すると、図8(a)に示すように、採血作業者は人体の一部に針などで疵をつけることで僅かに出血させ、採血具230の本体パイプ231を把持した状態で出血した血液240部分に対して採血具230を略直交配置すると共に、血液240部分に採血具230の毛管パイプ232の先端を接触させるようにすればよい。
この状態において、毛管パイプ232内には毛管現象により血液240が吸引保持され、ついには毛管パイプ232内全体に血液240が充填保持される。
次いで、採血具230を用いて採血した血液240を吐出する場合には、図8(b)に示すように、弾性パイプ233を押し潰すことにより、本体パイプ231内に正圧を作用させ、もって、毛管パイプ232内の血液240を所定部位に吐出させるようにすればよい。
この状態において、毛管パイプ232内の血液240を全て吐出するようにすれば、毛管パイプ232の容量に対応した所定量の血液240が得られる。
【0022】
本実施の形態に係る採血具230を用いて当該採血具230で採取した血液を検査カートリッジ200に分注するには、例えば検査カートリッジ200の検体セル203に対応するシール215に例えばノズルチップや専用の穿孔具を用いて孔を開け、しかる後、シール215の孔を通じて検体セル203内に採血具230の毛管パイプ232を挿入し、この状態で、採血具230の弾性パイプ233を押し潰し、毛管パイプ232内の血液240を検体セル203内に吐出するようにすればよい。
このとき、仮に、採血時に毛管パイプ232から溢れた血液240が毛管パイプ232と毛管ホルダ234との間の溝部235に溜まっていたとしても、当該血液残留物240’が検体セル203に逆流することはなく、毛管パイプ232内の血液240のみが検体セル203に定量供給される。
【0023】
<カートリッジラック>
また、本実施の形態では、カートリッジラック40は、図5及び図9(a)(b)に示すように、複数(本例では3つ)の検査カートリッジ200が保持可能な複数のラックホルダ41を有している。このラックホルダ41は、一対のホルダ脚42間にX方向に直交するY方向に延びるスリット43を設け、このスリット縁部を支持面44としたものであり、この支持面44に検査カートリッジ200のカートリッジ本体201の幅方向両側縁部を支持するようになっている。更に、一対のホルダ脚42の一方には検査カートリッジ200の切欠217(図6参照)に対応してストッパ45が設けられており、カートリッジラック40への検査カートリッジ200の挿入方向が逆になった状況下では、前記検査カートリッジ200のフランジ部216が前記ストッパ45に衝合し、検査カートリッジ200が誤った挿入方向からカートリッジラック40にセットされないように配慮されている。
【0024】
<カートリッジ引き込み機構>
更に、カートリッジ引き込み機構50は、図10〜図12に示すように、Y方向に延びる引き込み軌道51を有し、この引き込み軌道51に沿って移動自在なYテーブル(可動ユニット)52を設け、このYテーブル52にはセットステージST側に延びる係止アーム53を設けると共に、この係止アーム53の先端には上方に突出する係止片54を設け、この係止片54が検査カートリッジ200の被係合片213に係脱自在に係合するようになっている。
特に、本実施の形態では、検査カートリッジ200の被係合片213はX方向に貫通する凹部218を有しており、Xテーブル30の移動に伴って検査カートリッジ200の被係合片213とカートリッジ引き込み機構50の係止片54とが相互に干渉することはなく、Xテーブル30が適宜位置に移動し、検査初期位置ST1に移動設定された検査カートリッジ200は、その被係合片213がカートリッジ引き込み機構50の係止片54と係合する位置関係になるようになっている。
【0025】
また、Yテーブル(可動ユニット)52の駆動系及び位置停止機構を図13〜図15に示す。
同図において、このYテーブル52の駆動系は、例えば図13〜図15(a)に示すように、装置筐体21に固定された支持ブラケット21aに駆動モータ55及びモータドライバ56を固定設置し、駆動モータ55からの駆動力を駆動力伝達機構57を介してYテーブル52に伝達し、引き込み軌道51に沿ってYテーブル52を進退動するようになっている。
ここで、駆動力伝達機構57としては適宜選定して差し支えないが、例えばYテーブル52の移動方向に沿って循環回転する移動ベルト57aをプーリ57b,57c間に掛け渡すと共に、この移動ベルト57aに前記係止アーム53の一端部を固定する一方、前記駆動モータ55からの駆動力を図示外の駆動プーリを介して駆動ベルト57dに伝達し、この駆動ベルト57dからの駆動力をプーリ57bを介して移動ベルト57aに伝達し、この移動ベルト57aを進退動させることによりYテーブル52を進退動させるものが挙げられる。
尚、Yテーブル52の駆動系として、駆動モータ55,モータドライバ56を固定的に配設しているが、Yテーブル52にこれらを搭載して自走式に構成してもよいことは勿論である。
更に、Yテーブル(可動ユニット)52の位置停止機構は、例えば図15(b)に示すように、支持ブラケット21aの所定部位には例えばフォトカプラなどからなる位置決めセンサ61,62を配設する一方、Yテーブル52には進退方向に延びるセンサ板63を取付け、このセンサ板63に位置合せ用のセンサスリット64を所定ピッチ毎に開設し、位置決めセンサ61,62にてセンサ板63の所定位置を検出することにより、Yテーブル52の進退位置を規制し、検査カートリッジ200の引き込み位置を制御するようになっている。
【0026】
<検体試薬分注装置>
また、図4に示す検体試薬分注機構70としては検体、試薬を分注するものであれば公知のものを適宜選定して差し支えないが、例えば図16(a)に示すように、X方向、Y方向に直交するZ方向に沿って進退移動する昇降台71を有し、この昇降台71にシリンジポンプ72に連通するノズルチャック73を取付け、このノズルチャック73にノズルチップ210を着脱自在に取り付けるようにしたものが用いられる。
本実施の形態では、検体試薬分注機構70は、図16(b)に示すように、カートリッジ引き込み機構50にて所定位置まで検査カートリッジ200を引き込み、検体試薬分注機構70の分注位置に検査カートリッジ200の分注対象セル202を配置した後、シリンジポンプ72を負圧若しくは正圧に切り替えることにより、検査カートリッジ200内の所定のセル202(検体セル203,試薬セル205,206)から検体、試薬を所定量吸引保持し、測定対象である反応セル207内に所定量の検体、試薬を吐出するものである。
【0027】
このとき、検体試薬分注機構70は検体又は試薬を個別に吸引して吐出する方式を採用してもよいし、あるいは、ノズルチップ210内で空気層を介在させることにより、検体と試薬、あるいは、複数の試薬を同時に吸引保持した後、吐出するようにしてもよいことは勿論である。
尚、本実施の形態では、検体試薬分注機構70は検体、試薬の分注動作をともに兼用する態様になっているが、夫々別に設けるようにしてもよい。また、本実施の形態では、廃棄可能なノズルチップ210を用いているが、これに限られるものではなく、ノズルチップ210を用いないで、専用ノズルを洗浄しながら使用する方式を採用してもよいことは勿論である。
【0028】
<穿孔装置>
本実施の形態では、検査カートリッジ200は、各セル202がシール215で被覆されているため、検体試薬分注機構70にて検体、試薬の分注動作を行う前に、検体試薬分注機構70のノズルチップ210が挿入可能となるように、シール215に対し挿入用の孔を穿つことが行われる。
このような要請下において、本実施の形態では、検体試薬分注機構70を穿孔装置として兼用する手法が採用されている。
つまり、穿孔動作時には、検体試薬分注機構70は、図16(c)に示すように、検査カートリッジ200の各セル202のうち使用可能なセル202(検体セル203,試薬セル205,206,反応セル207)に対応するシール215を目がけてノズルチップ210を穿孔具として用い、シール215に孔を穿つものである。
【0029】
本実施の形態において、穿孔装置として兼用される検体試薬分注機構70はシール215に対して孔を穿つものであれば、孔の穿ち方など適宜選定して差し支えないが、本実施の形態では、使用するセル202に対応するシール215部分に夫々複数の孔を穿つようになっている。詳細は後述する。
尚、本実施の形態では、検体試薬分注機構70にて穿孔装置を兼用するようにしているが、必ずしもノズルチップ210を穿孔具として利用する態様に限られるものではなく、例えば検体試薬分注機構70の昇降台71の一部に穿孔具を取付け、この穿孔具を利用して検査カートリッジ200のシール215に孔を穿つようにしてもよい。また、検体試薬分注機構70とは全く別に専用の穿孔装置を配設し、この穿孔装置にて検査カーリッジ200のシール215に孔を穿つようにしても差し支えない。
【0030】
<温度調整機構>
また、本実施の形態において、検査ステージKTには、図11及び図17〜図21に示すように、温度調整機構として恒温槽80及び補助加温装置90が設けられている。
恒温槽80は検査カートリッジ200の引き込み位置を挟むように両側から配設されており、セットステージST寄りの片側の一部が切り欠かれた非対称形状になっている。
そして、前記切り欠かれた部位には恒温槽80に代わって補助加温装置90が配設されている。尚、本実施の形態にあっては、恒温槽80の一部に補助加温装置90が設けられているが、これに限られるものではなく、恒温槽80内に補助加温装置90を組み込むようにしても差し支えない。
【0031】
―恒温槽―
本実施の形態において、恒温槽80は、図17〜図19に示すように、例えばアルミニウム製の恒温ブロック81にて周囲が覆われており、この恒温ブロック81の底面にヒータ(例えばシリコンラバーヒータ)82を取り付けると共に、恒温ブロック81の一部に例えばサーミスタからなる温度センサ83(図20参照)を設け、この温度センサ83からの温度情報をモニタリングすることにより所定の恒温条件(例えば37℃)に保つようにヒータ82をオンオフ制御するようになっている。
ここで、温度センサ83の配設位置は適宜選定して差し支えないが、例えば後述する測定装置100の近傍に配設するようにすれば測定装置100による測定ステージの環境温度を直接的に検出することになる分、恒温槽80の温度調整がより正確に行われる。
尚、恒温槽80内には必要に応じて断熱材を設け、恒温槽80内からの不必要な熱放出を抑えるように設計することが好ましい。
【0032】
―補助加温装置―
また、補助加温装置90は、図17,図18及び図21に示すように、装置筐体21のベースフレーム28上に支持ブラケット93を取付け、この支持ブラケット93に例えばアルミニウム製の加温ブロック91を揺動アーム92を介して揺動自在に支持する一方、加温ブロック91には検査カートリッジ200の各セル202(検体セル203,試薬セル204〜206,反応セル207)に対応した複数(本例では5つ)の凹所94を設け、カートリッジ引き込み機構50にて引き込まれた検査カートリッジ200の各セル202を片側から覆うことが可能な構造になっている。
ここで、加温ブロック91の背面にはヒータ95が設けられると共に、加温ブロック91の一部には例えばサーミスタからなる温度センサ96が設けられ、加温ブロック91が恒温条件より高い所定温度(例えば70℃)に加温されるようになっている。また、ヒータ95としては一定の発熱量のものでよいが、勿論発熱量調整可能なものでもよい。尚、本例ではヒータ95は主電源スイッチがオンされた時点で作動するようになっている。
【0033】
更に、本実施の形態では、加温ブロック91はその揺動アーム92を電磁ソレノイド等の駆動アクチュエータ97にて揺動自在とすることにより、図17(a)(b)及び図21(a)に示すように、検査カートリッジ200が引き込まれる位置から離間した退避位置に傾斜姿勢にて保持されると共に、図18(a)(b)及び図21(b)に示すように、検査カートリッジ200が引き込まれる位置に近接した加温位置に略直立した姿勢にて保持される。
尚、本実施の形態では、加温ブロック91は加温位置と退避位置との間で揺動するようになっているが、例えば駆動アクチュエータ97を多段シフト可能に構成し、加温ブロック91の揺動位置を多段階に調整することにより、被加温対象セルとの間の隙間寸法をパラメータとして加温ブロック91による加温量を可変設定するようにしてもよい。本態様によれば、加温ブロック91自体の発熱量が一定であっても、加温ブロック91による加温量を容易に調整することができる。勿論、加温ブロック91自体の発熱量を調整可能な態様にあっては、特に加温ブロック91の揺動位置を変化させなくても、加温ブロック91による加温量を変更することは可能である。
【0034】
更に、本実施の形態において、補助加温装置90は検査カートリッジ200の試薬セル205(試薬R1を収容)に対向した恒温槽80には例えばサーモパイルからなる非接触型温度センサ98が設けられており、この非接触型温度センサ98は検査カートリッジ200の試薬セル205の表面温度を非接触状態にて検出するようになっている。そして、駆動アクチュエータ97は非接触型温度センサ98にて検出された試薬セル205の表面温度をパラメータとしてオンオフ制御されるようになっており、試薬セル205の表面温度が目標温度(例えば恒温条件である37℃に相当)に到達しない条件下では駆動アクチュエータ97がオン動作する一方、試薬セル205の表面温度が目標温度に到達した条件下では駆動アクチュエータ97はその作動を停止するようになっている。
【0035】
また、本実施の形態では、加温目標温度を一定に設定して差し支えないが、環境温度の影響(例えばノズルチップ210の温度条件により分注した試薬R1などの温度が変化するという影響)を低減するという観点からすれば、例えば検査ステージKTの任意の箇所に恒温槽80以外の環境温度が計測可能な図示外の計測器(例えばサーミスタ等)を設け、この計測器からの温度情報に基づいて加温目標温度を変化させ、加温ブロック91による加温量を決定するようにしてもよい。例えば環境温度が基準温度である場合の加温目標温度を基準値(例えば37℃)とし、環境温度が基準温度を超える場合には加温目標温度を基準値よりも減少させ、逆に、環境温度が基準温度未満である場合には加温目標温度を増加させるようにすればよい。
【0036】
<測定装置>
また、本実施の形態では、図19、図20(a)に示すように、検査カートリッジ200の引き込み方向先端側の恒温槽80内に測定装置100が配設されている。この測定装置100は、所定の測定ステージMTを挟んで配設される例えば赤外線LEDからなる発光素子101と、測定ステージMTを挟んで前記発光素子101に対向する部位に配設される例えばフォトディテクタからなる受光素子102とを備えている。尚、符号103は発光素子101からの拡散光を検出するフォトディテクタからなる受光素子であり、受光素子102,103間の差分を検出可能としている。
そして、本実施の形態では、測定ステージMTは、図20(b)に示すように、検査カートリッジ200の反応セル207が配置されるようになっており、測定装置100は、測定ステージMTにて検査カートリッジ200の反応セル207内の検体と試薬との反応を測定するようになっている。
【0037】
<制御系>
図22は自動分析装置の制御系を示す。
同図において、符号110はマイクロコンピュータからなる制御装置であり、この制御装置110は、主電源スイッチ、各種動作センサ(スタートボタン等の操作部、位置センサ等)、各種温度センサからの情報を取り込み、各種ヒータによる温度制御処理(恒温槽80、補助加温装置90の温度制御処理など)111を行い、各種動作源による動作制御処理(Xテーブル駆動制御処理、検査カートリッジの引き込み制御処理、検体試薬分注制御処理、測定制御処理など)112を行い、更に、プリンタ部による印刷制御処理113を行うものである。
【0038】
<自動分析装置の作動>
次に、本実施の形態に係る自動分析装置の作動について説明する。
この自動分析装置を使用するに当たって、
(1)検査カートリッジのセット操作
(2)測定シーケンスの実行操作
を行うようにすればよい。
【0039】
―検査カートリッジのセット操作―
先ず、ユーザーは、図2及び図3に示すように、自動分析装置20の扉22を開放した後、自動分析装置20のセットステージSTのカートリッジラック40に検査に必要な複数の検査カートリッジ200をユーザー操作側から見て右側から順にセットすることが必要である。
このとき、セットすべき検査カートリッジ200に対する準備として、採血分注、並びに、ノズルチップ210のセットを行うことが必要である。
例えば図7に示すように、検査カートリッジ200の各検体セル203(本例では希釈液W内蔵)には夫々採血具230にて採血された血液を所定量分注する。
また、図6に示すように、検査カートリッジ200のチップ保持孔208にはノズルチップ210を上方から挿入保持させるようにすればよい。
【0040】
また、図9に示すように、カートリッジラック40に対して検査カートリッジ200は所定方向にセットされることが必要であるが、ユーザーは、カートリッジラック40のラックホルダ41のスリット43に沿って検査カートリッジ200を所定位置まで挿入させるようにすればよい。
このとき、仮に、検査カートリッジ200の挿入方向が逆方向である場合には、検査カートリッジ200の挿入動作が阻止されるようになっている。つまり、誤った方向から検査カートリッジ200を挿入しようとすると、カートリッジラック40のストッパ45に検査カートリッジ200のフランジ部216が衝合し、検査カートリッジ200の挿入方向への移動が阻止される。一方、検査カートリッジ200が正規の方向から挿入される場合には、カートリッジラック40のストッパ45に対応した検査カートリッジ200のフランジ部216に切欠217が設けられているため、検査カートリッジ200はカートリッジラック40のストッパ45に阻止されることなく挿入される。このため、カートリッジラック40に対して検査カートリッジ200は正規の方向から必ず挿入セットされる。
【0041】
―測定シーケンスの実行―
検査カートリッジ200のセット操作が終了した後、自動分析装置20の扉22を閉じ、しかる後、操作部23のスタートボタン24を操作すれば、測定シーケンスが自動的に実行される。
(1)検査カートリッジの装着確認
自動分析装置20のスタートボタン24を操作すると、先ず検査カートリッジ200の装着確認動作が行われる。
これは、カートリッジラック40の初期位置のうち、ユーザー操作側から見て右端のラックホルダ41の奥側に対応した部位に非接触型位置センサ(図示せず)からなる存在確認センサを設け、制御装置110は存在確認センサにて検査カートリッジ200の存在が確認された条件下でXテーブル30を移動開始させる。尚、存在確認センサにて検査カートリッジ200の存在が確認されない場合には、検査カートリッジ200が装着されていないことを表示ディスプレイ26に表示する等の警告を行い、ユーザーに注意を喚起する。
【0042】
(2)検査カートリッジの検査初期位置設定
この後、制御装置110は、図4に示すように、Xテーブル30を移動させ、最初の検査対象である検査カートリッジ200(本例ではユーザー側から見て右端にある検査カートリッジに相当)を検査初期位置ST1に設定する。
この状態において、例えば図25に示すように、検査初期位置ST1に対応した上部にバーコードリーダー等のマークリーダー120を配設すると共に、検査カートリッジ200に設けられたシール215の表面には検査カートリッジ200を特定するためのハーコード等のマーク(図示せず)を設け、これにより、検査対象となる検査カートリッジ200を確認した後、検査カートリッジ200の引き込み動作に移行する。尚、バーコード等のマークを付す箇所はシール215の表面に限られるものではなく、例えば検査カートリッジ200のカートリッジ本体201の適宜箇所にシール215とは別に設けるようにしてもよいことは勿論である。
【0043】
(3)検査カートリッジの引き込み動作(図25参照)
次いで、図25に示すように、カートリッジ引き込み機構50により検査初期位置ST1に設定された検査カートリッジ200を検査ステージKT側に引き込む。
本実施の形態では、カートリッジ引き込み機構50は、検査カートリッジ200の反応セル207が測定装置100の測定ステージMTに停止するように、検査カートリッジ200を引き込む。
尚、制御装置110は、主電源スイッチがオンされた時に恒温槽80のヒータ82を作動させ、恒温槽80内を所定温度(例えば37℃)になるように恒温制御している。
【0044】
(4)反応セルの状態確認動作(図23(a)参照)
検査カートリッジ200の反応セル207が測定装置100の測定ステージMTに位置決めされた段階で、制御装置110は、測定装置100にて反応セル207の状態を測定し、異常(反応セル表面の汚れや検査カートリッジの排出忘れ等)
の有無を確認する。
【0045】
(5)ノズルチップの有無確認動作(図23(a),図26,図27参照)
次いで、制御装置110は、検体試薬分注機構70をZ軸方向で移動させ、検体試薬分注機構70に検査カートリッジ200に保持されているノズルチップ210を装着させる。このとき、検体試薬分注機構70のZ軸軌道に沿った部位に非接触型位置センサからなる存在確認センサ121を配設し、この存在確認センサ121にてノズルチップ210の装着状態を確認する。尚、ノズルチップ210の装着状態が不良であることが検出された場合には、例えば表示ディスプレイ26に警告表示を行う。
【0046】
(6)空気孔開け動作
次いで、制御装置110は、図28に示すように、検体試薬分注機構70を穿孔装置として働かせ、カートリッジ引き込み機構50にて検査カートリッジ200を適宜進退させながら、検体試薬分注機構70を利用した穿孔装置にて検査カートリッジ200のシール215に空気孔を穿つように制御する。
本実施の形態では、空気孔開け動作は、図29(a)に示すように、検査カートリッジ200の使用セル202(検体セル203,試薬セル205,206,反応セル207)に対応するシール215部分に夫々複数(本例では2つ)の空気孔131,132を穿つものである。
ここで、空気孔131,132の大きさとしては、例えば1〜2mm程度でよく、ノズルチップ210の外径変化を考慮し、その挿入深さを決定するようにすればよい。
特に、本実施の形態では、各空気孔131,132は対応する使用セル202(検体セル203,試薬セル205,206,反応セル207)の開口中心133を挟んだ位置、例えば略点対称となる位置に開けられている。
尚、検査カートリッジ200の検体セル203に対応するシール215部分には検体分注時に孔135が開けられているが、ユーザー操作によりどの位置に孔を開けたか不確かであるため、本実施の形態では、検体セル203に対応したシール215部分についても、他のセルと同様に、複数の空気孔131,132を穿つように検体試薬分注機構70を利用した穿孔装置を制御する方式が採用されている。
【0047】
このように、使用セル202のシール215部分に複数の空気孔131,132を開けると、例えば図29(b)に示すように、穿孔具としてのノズルチップ210が一方の空気孔131を塞ぐように挿入されたとしても、他方の空気孔132が大気開放されているため、ノズルチップ210の挿入により使用セル202内の圧力が不必要に高くなり、ノズルチップ210による検体、試薬の吸引動作や、吐出動作が不安定になることはない。
また、穿孔具としてのノズルチップ210が使用セル202のシール215部分の開口中心133近傍に挿入されるような場合には、複数の空気孔131,132の存在により、使用セル202のシール215部分が容易に破砕され、大気開放された状態でノズルチップ210が使用セル202内に挿入される。
【0048】
特に、本実施の形態では、複数の空気孔131,132が使用セル202の開口中心133を挟んだ位置に開設されているため、検体、試薬分注時において、ノズルチップ210の挿入位置が比較的ラフであるとしても、ノズルチップ210による穿孔動作時にシール215が確実に破砕される。この点、例えば複数の空気孔131,132が使用セル202の開口中心133に対して片側に偏倚して開設されている態様にあっては、検体、試薬分注時において、シール215部分のうち空気孔131,132が開設されていない側にノズルチップ210が挿入される際に若干破砕し難いという懸念はあるものの、複数の空気孔131,132が存在する以上、一つの空気孔の場合よりも破砕し易い点で好ましい。
【0049】
ここで、比較の形態として、事前に空気孔を開設しない態様にあっては、検体、試薬分注時にノズルチップ210にてシール215を破砕し且つ使用セル202内にノズルチップ210を挿入すると、ノズルチップ210にて開けた孔が塞がれてしまうため、使用セル202内が密封状態になり易く、検体、試薬の分注動作が不安定になり易い。
また、一つの空気孔を開設する態様にあっては、一つの空気孔をノズルチップ210で塞ぐと、使用セル202内が密封になり易い虞れがあり、また、空気孔から離れたシール215部分にノズルチップ210を挿入する際には前記空気孔がノズルチップ210によるシール215部分の破砕を助長する作用が働き難いという懸念もある。このため、このような態様で使用する場合には、シール215素材として破砕し易いものを使用する等の工夫をすることが好ましい。
【0050】
(7)試薬R1の温度測定(図23(b)参照)
上述した空気孔開け動作が終了すると、制御装置110は、図30に示すように、検査カートリッジ200の試薬セル205(R1内蔵)が恒温槽80の非接触型温度センサ98に対応した位置になるように、カートリッジ引き込み機構50にて検査カートリッジ200を移動させる。
この状態において、制御装置110は、非接触型温度センサ98にて試薬セル205の表面温度(試薬R1の温度に相当)を検出し、この情報を取り込む。
【0051】
(8)試薬R1加温動作(図23(b)参照)
制御装置110は、非接触型温度センサ98からの検出温度に基づいて、非接触型温度センサ98の検出温度が加温目標温度(恒温槽80の恒温条件温度:例えば37℃)になるまで補助加温装置90による加温動作を行う。
この補助加温装置90による加温動作は、ヒータ95及び温度センサ96により、高温条件温度(例えば37℃)よりも高い温度(例えば70℃)になるように加温された加温ブロック91を駆動アクチュエータ97のオン動作にて加温位置に回動させ、非接触型温度センサ98の温度情報をモニタリングしながら、試薬R1(試薬セル205の表面温度)の温度が目標温度(恒温条件温度)に至るまで加温する。
このとき、ヒータ95は温度センサ96にて加温ブロック91が恒温条件温度(例えば37℃)よりも高い温度(例えば70℃)になるように加熱されているため、加温ブロック91による加温量は十分に大きく、その分、試薬R1の温度上昇率は、恒温槽80だけで加温される態様に比べて速い。
【0052】
特に、本実施の形態では、補助加温装置90の加温ブロック91は検査カートリッジ200の各セル202(検体セル203,試薬セル204〜206,反応セル207)に対応した凹所94を有し、各セル202を加温することが可能になるため、試薬セル205内の試薬R1のみならず、試薬セル206内の試薬R2、検体セル203内の検体、更には、反応セル207自体も補助的に加温される。
また、ノズルチップ210は補助加温されないので、後述するように、試薬R1を吸引するときに、ノズルチップ210の温度の影響を受けて試薬R1の温度が低下する懸念がある。
このような状況を有効に解消するには、自動分析装置20内の外気取り入れ付近に例えばサーミスタ等の環境温度センサを設け、環境温度に応じて加温目標温度を変化させるようにすることが好ましい。
例えば環境温度と加温目標温度との関係を以下のように設定することが挙げられる。
環境温度(℃) 加温目標温度(℃)
15 40
25 37
35 36
【0053】
(9)試薬R1吸引動作(図23(c)参照)
試薬R1が目標温度(恒温条件温度)に到達すると、制御装置110は、検体試薬分注機構70の分注位置に試薬セル205(試薬R1内蔵)が位置するようにカートリッジ引き込み機構50にて検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70のノズルチップ210にて試薬セル205のシール215部分を突き破り、試薬セル205内の試薬R1にノズルチップ210を浸漬させ、しかる後、試薬R1を所定量吸引する。
このとき、ノズルチップ210は試薬セル205のシール215部分を簡単に破砕することができ、しかも、ノズルチップ210が試薬セル205内に浸入したとしても、試薬セル205内が密封状態になる懸念はないため、ノズルチップ210による試薬R1の吸引動作は安定的に行われる。
【0054】
(10)試薬R1吐出動作(図23(d)参照)
この後、制御装置110は、検体試薬分注機構70にて試薬セル205からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて反応セル207が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70のノズルチップ210にて反応セル207のシール215部分を突き破り、反応セル207内にノズルチップ210を挿入させた後に、反応セル207内に試薬R1を所定量吐出させる。
【0055】
(11)検体撹拌動作(図24(a)参照)
次いで、制御装置110は、検体試薬分注機構70にて反応セル207からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて検体セル203が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70のノズルチップ210にて検体セル203のシール215部分を突き破り、検体セル203内にノズルチップ210を挿入させた後に、検体セル203内の検体を撹拌するようにする。
この検体撹拌動作は、例えば検体セル203内において検体に対してノズルチップ210を浸漬させ、検体の吸引、吐出を複数回行うことにより検体を撹拌する手法が採用されている。特に、ノズルチップ210を上下動させる動作を組合せ、下位置で吸引、上位置で吐出させるようにすれば、検体の撹拌動作をより促進させることができる点で好ましい。
【0056】
(12)検体バースト動作(図24(c)参照)
検体セル203内の検体の撹拌動作後、図24(c)の測定位置に所定時間放置し、検体をバーストさせる。これにより、検体内の血球が均一に分散することになり、検体の均質化を確保することが可能である。
(13)検体吸引動作(図24(a)参照)
しかる後、制御装置110は、検体試薬分注機構70のノズルチップ210を検体セル203内の検体に浸漬させ、所定量検体を吸引するようにする。
【0057】
(14)検体吐出動作(図23(d)参照)
この後、制御装置110は、検体試薬分注機構70にて検体セル203からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて反応セル207が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70にて反応セル207内にノズルチップ210を挿入させた後に、反応セル207内に検体を所定量吐出させる。
【0058】
(15)検体撹拌動作(図23(d)参照)
次いで、制御装置110は、検体試薬分注機構70のノズルチップ210にて反応セル207内の検体と試薬R1とを撹拌するようにする。
この場合の撹拌動作は、例えば反応セル207内において検体及び試薬R1に対してノズルチップ210を浸漬させ、吸引、吐出を複数回行うことにより両者を撹拌するものである。尚、撹拌動作をより促進させるためにノズルチップ210を必要に応じて上下動させてもよいことは勿論である。
【0059】
(16)試薬R2吸引動作(図24(b)参照)
この後、制御装置110は、検体試薬分注機構70にて反応セル207からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて試薬セル206(試薬R2内蔵)が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70のノズルチップ210にて試薬セル206のシール215部分を突き破り、検体試薬分注機構70にて試薬セル206内にノズルチップ210を挿入させた後に、試薬セル206内の試薬R2を所定量吸引するようにする。
【0060】
(17)試薬R2吐出動作(図23(d)参照)
この後、制御装置110は、検体試薬分注機構70にて試薬セル206からノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて反応セル207が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、検体試薬分注機構70にて反応セル207内にノズルチップ210を挿入させた後に、反応セル207内に試薬R2を所定量吐出させる。
(18)試薬R2撹拌動作(図23(d)参照)
次いで、制御装置110は、検体試薬分注機構70のノズルチップ210にて反応セル207内の検体、試薬R1及び試薬R2を撹拌するようにする。
この場合の撹拌動作は、例えば反応セル207内において検体、試薬R1及び試薬R2に対してノズルチップ210を浸漬させ、吸引、吐出を複数回行うことにより全体的に撹拌するものである。尚、撹拌動作をより促進させるためにノズルチップ210を必要に応じて上下動させてもよいことは勿論である。
【0061】
(19)ノズルチップ排出動作
この後、制御装置110は、検体試薬分注機構70のノズルチップ210を上昇させた後に待機し、カートリッジ引き込み機構50にて検査カートリッジ200のチップ保持孔208が分注位置に位置するように検査カートリッジ200を移動させる。
この状態において、制御装置110は、図31に示すように、検査カートリッジ200のチップ保持孔208に検体試薬分注機構70のノズルチップ210を上方から挿入させ、検体試薬分注機構70のノズルチャック73(図16参照)によるノズルチップ210の保持状態を解除することにより、検査カートリッジ200の元の位置に廃棄すべきノズルチップ210を戻すようにする。
このノズルチップ210の排出動作は、反応セル207内の検体、試薬の反応が未だ不安定である時間帯を利用して行うため、自動分析装置20の処理能力にはほとんど影響しない。
【0062】
(20)測定動作(図24(c)参照)
そして、制御装置110は、図31に示すように、検査カートリッジ200の反応セル207が測定ステージMTに位置するように、カートリッジ引き込み機構50にて検査カートリッジ200を移動させる。
この後、制御装置110は、反応セル207が測定ステージMTに到達した状態で測定装置100による測定を所定時間(例えば1分〜5分)行う。
このとき、測定装置100は、発光素子101からの光を反応セル207内の検体と試薬との混合液に透過させ、その光変化を受光素子102にて検出すると共に、発光素子101自体の光変化を受光素子103にて検出し、反応セル207内の検体と試薬との反応変化を経時的に測定する。
【0063】
また、試薬R1の吸引、吐出の分注動作、試薬R2の吸引、吐出の分注動作、反応セル207内の撹拌等では、反応セル207は恒温槽80外に配置されるため、自動分析装置20内の環境温度の影響を受けて反応セル207内の温度が下がる懸念がある。このような状況をより正確に考慮する場合には、例えば自動分析装置20内の外気取り入れ付近に例えばサーミスタ等の環境温度センサを設け、環境温度に応じて恒温槽80の温度補正を行うようにしてもよい。
【0064】
(21)検査カートリッジ排出動作
この後、制御装置110は、図32に示すように、カートリッジ引き込み機構50にて検査済みの検査カートリッジ200をセットステージST側に戻すようにする。
(22)結果印刷動作
また、制御装置110は、測定装置100による測定結果をプリンタ部27にて印刷する。
この段階にて一つの検査カートリッジ200に対する所定の測定シーケンスが終了する。
【0065】
この後、制御装置110は、セットステージSTに未処理の検査カートリッジ200が存在することを確認の上、各検査カートリッジ200に対して一連の測定シーケンスを実行する。
具体的には、制御装置110は、例えば図3及び図4に示すように、カートリッジラック40の次のラックホルダ41に位置する検査カートリッジ200を検査初期位置ST1に設定した後、一連の測定シーケンスを行い、更に、次の検査カートリッジ200を検査初期位置ST1に設定した後に一連の測定シーケンスを実行する。
そして、全ての検査カートリッジ200について一連の測定シーケンスが終了すると、制御装置110は、表示ディスプレイ26に全検査が終了した旨の検査終了表示を行う。
この後、ユーザーは、自動分析装置20の扉22を開放し、カートリッジラック40から検査済みの検査カートリッジ200を廃棄すべきノズルチップ210と共に取り出し、廃棄するようにすればよい。
【0066】
◎実施の形態2
図33は本発明に係る自動分析装置の実施の形態2の要部を示す説明図である。
同図において、自動分析装置の基本的構成は実施の形態1と略同様であるが、測定装置100の構成が実施の形態1と異なっている。
つまり、本実施の形態では、測定装置100は、測定ステージMTを挟んで発光素子101と受光素子102とを対向配置した態様であるが、発光素子101が検査項目に応じて交換可能に構成されている。
この種の発光デバイスとしては、波長特性の異なる複数の発光素子101(101a〜101c)が夫々含まれる複数の光源ボード141〜143を予め用意しておき、検査項目に応じてボード装着部145に必要な光源ボード141〜143のいずれかを抜き差し可能に装着し、各光源ボード141〜143のいずれかに対応する発光素子101を使用するものが挙げられる。
【0067】
また、この種の測定装置100としては、図33に示す態様に限られるものではなく、例えば図34に示すように、回転プレート150に複数の発光素子101(101a〜101c)を所定の円弧軌跡上に配列し、検査項目に応じて回転プレート150を適宜位置に回転させ、所定の発光素子101を使用するものが挙げられる。尚、回転プレート150ではなく、図示外の直線プレートに複数の発光素子を配列し、検査項目に応じて必要な発光素子を使用するようにしても差し支えない。
【0068】
◎実施の形態3
図35〜図39は本発明に係る自動分析装置の実施の形態3の要部を示す説明図である。
同図において、自動分析装置の基本的構成は実施の形態1と略同様であるが、ノズルチップ210の廃棄方式が実施の形態1と異なるものになっている。尚、実施の形態1と略同様な構成要素については実施の形態1と同様な符号を付してここではその詳細な説明を省略する。
本実施の形態においては、セットステージSTは、例えば図35(1)に示すように、実施の形態1と同様に、Xテーブル30上に複数(例えば3つ)の検査カートリッジ200が保持可能なカートリッジラック40を設けているが、実施の形態1と異なり、カートリッジラック40に隣接した部位にノズルチップ210の廃棄ラック160を設け、この廃棄ラック160にはノズルチップ専用の廃棄カートリッジ170を検査カートリッジ200と略平行に且つY方向に対して進退自在に設けたものである。
ここで、廃棄カートリッジ170は、廃棄ラック160に摺動自在に保持されるカートリッジ本体171を有し、このカートリッジ本体171に廃棄用のノズルチップ210が保持可能な複数(例えば3つ)のチップ保持部172〜174を開設したものである。
【0069】
次に、本実施の形態に係る検査カートリッジ200及びノズルチップ210の動作過程について説明する。
先ず、図35(1)はカートリッジラック40に各検査カートリッジ200が保持されており、一つの検査カートリッジ200が検査初期位置ST1に位置する状態を示す。
この後、図35(2)に示すように、検査初期位置ST1に位置する検査カートリッジ200がカートリッジ引き込み機構50にて検査ステージKT側に引き込まれ、検査カートリッジ200が図示外の補助加温装置にて補助的に加温される。
更に、図36(3)に示すように、図示外の検体試薬分注機構にノズルチップ210が装着される。
しかる後、図36(4)に示すように、カートリッジ引き込み機構50にて検査カートリッジ200が適宜移動させられ、検体試薬分注機構による検体、試薬の分注動作、測定装置100による測定動作が行われる。
【0070】
そして、測定装置100による測定が終了すると、図37(5)に示すように、カートリッジ引き込み機構50が検査済みの検査カートリッジ200をセットステージSTのカートリッジラック40に戻す。
このとき、ノズルチップ210は図示外の検体試薬分注機構に装着されたままである。
この後、図37(6)に示すように、Xテーブル30が矢印方向に移動し、廃棄ラック160に保持されている廃棄カートリッジ170が検査初期位置ST1に設定される。
この後、図38(7)に示すように、カートリッジ引き込み機構50が廃棄カートリッジ170を検査ステージKT側に引き込み、検体試薬分注機構の分注位置に廃棄カートリッジ170のチップ保持部172が位置するように廃棄カートリッジ170を移動する。
【0071】
そして、図38(8)に示すように、検体試薬分注機構は、装着されたノズルチップ210の装着状態を解除した後、廃棄カートリッジ170のチップ保持部172にノズルチップ210を挿入保持させる。
この後、図39(9)に示すように、カートリッジ引き込み機構50が廃棄カートリッジ170をセットステージST側に戻す。
更に、残りの検査カートリッジ200についても同様な測定シーケンスが行われ、その測定シーケンスで用いられた各ノズルチップ210は夫々廃棄カートリッジ170のチップ保持部173,174に保持される。
そして、自動分析装置の全検査が終了した時点で、検査済みの検査カートリッジ200並びに廃棄カートリッジ170に保持された複数のノズルチップ210が夫々廃棄される。
【0072】
実施の形態1,3はいずれも廃棄用のノズルチップ210をセットステージST側に戻した後に廃棄するようにしているが、例えば検査ステージKT側で別途廃棄ステージを設け、その廃棄ステージに廃棄用のノズルチップ210を廃棄する等適宜選定して差し支えない。
【0073】
◎実施の形態4
図40は本発明に係る自動分析装置の実施の形態4の要部を示す説明図である。
同図において、自動分析装置20の基本的構成は、実施の形態1と略同様であるが、実施の形態1と異なり、検査ステージKTには補助加温装置90を設けることなく、恒温槽80のみを備えており、恒温条件温度(例えば37℃)に達する前に検査カートリッジ200の反応セル207内の液反応を測定開始するようにしたものである。尚、実施の形態1と同様な構成要素については実施の形態1と同様な符号を付してここではその詳細な説明を省略する。
本実施の形態では、恒温槽80は、図40及び図41に示すように、検査カートリッジ200が収容可能で少なくとも測定ステージMTが恒温条件温度(例えば37℃)に保たれる恒温ブロック81を有し、この恒温ブロック81は測定装置100(発光素子101,受光素子102,103)部分を両側から覆うばかりでなく、実施の形態1の補助加温装置90の設置箇所に対応した部位をも両側にて覆うようになっている。
また、本実施の形態では、恒温槽80には実施の形態1と同様な非接触型温度センサ98が配設されているが、この非接触型温度センサ98は、検査カートリッジ200の反応セル207内の初期液温データT0、所定時間(例えば3分)経過後の反応セル207内の液温データT1を測定し、後述する制御装置110にデータ入力するようになっている。
【0074】
また、本実施の形態において、自動分析装置の制御系を図42に示す。
同図において、符号110はマイクロコンピュータからなる制御装置であり、この制御装置110は、主電源スイッチ、各種動作スイッチ(スタートボタン等の操作部、位置センサ等)、各種温度センサからの情報を取り込み、温度補正テーブル115を参照しながら反応セル207内の液に対する温度制御処理111(恒温槽80のヒータ83による温度制御処理)を行い、各種動作源による動作制御処理(Xテーブル駆動制御処理、検査カートリッジの引き込み制御処理、検体試薬分注制御処理、測定制御処理など)112を行い、更に、プリンタ部による印刷制御処理113を行うものである。
特に、本実施の形態において、温度補正テーブル115は、反応セル207内の初期液温データT0、反応セル内の所定時間(例えば3分)経過後の測定開始時の液温データT1とに基づく温度補正係数k(T0,T1)などの補正情報を保有し、制御装置110は、非接触温度センサ98からの入力データに基づいて温度補整テーブル115を検索し、対応する温度補正係数k(T0,T1)などの補正情報を選定し、測定装置100による測定結果について恒温条件温度(例えば37℃)で反応したであろう状態に補正するようになっている。
ここで、温度補正テーブル115内の補正情報としては予め実測されたデータに基づいて演算決定されたものが用いられる。
【0075】
従って、本実施の形態によれば、実施の形態1と同様に、検査カートリッジ200のセット操作を行った後、スタートボタンを操作することにより以下のような測定シーケンスが実行される。
(1)検査カートリッジの装着確認
(2)検査カートリッジの検査初期位置設定
(3)検査カートリッジの引き込み動作
(4)反応セルの状態確認動作
(5)ノズルチップの有無確認動作
(6)空気孔開け動作
(7)試薬R1の温度測定
ここまでは実施の形態1と略同様であるので、その詳細については省略する。
但し、試薬R1の温度測定の結果は試薬セル205表面に対する温度計測であるが、本実施の形態ではこれを反応セル207内の初期液温データT0とし、制御装置110に取り込む。尚、反応セル207内に試薬R1を吐出した後の液温を初期液温データT0としてもよいことは勿論である。
【0076】
この後、以下の動作へと移行する。
(8)試薬R1吸引動作
(9)試薬R1吐出動作
(10)検体撹拌動作
(11)検体バースト動作
(12)検体吸引動作
(13)検体吐出動作
(14)検体撹拌動作
(15)試薬R2吸引動作
(16)試薬R2吐出動作
(17)試薬R2撹拌動作
(8)〜(17)までは実施の形態1と略同様であるので、その詳細は省略する。
【0077】
(18)反応セル内の液温測定
反応セル207内の初期液温データT0の測定から所定時間(例えば3分)経過後の液温データを測定開始時の液温データT1を測定し、制御装置110に取り込む。
(19)ノズルチップ排出動作
(20)測定動作
(21)検査カートリッジ排出動作
(19)〜(21)は実施の形態1と略同様であるので、ここではその詳細な説明を省略する。
(22)結果印刷動作
測定動作終了後、制御装置110は、非接触型温度センサ98からの温度データT0,T1に基づいて温度補正テーブル115にて温度補正係数k(T0,T1)等の補正情報を決定し、この補正情報に基づいて測定結果を恒温条件での測定結果になるように補正し、この補正結果を印刷する。尚、補正前の測定結果自体を参考データとして印刷するようにしてもよいことは勿論である。
【実施例】
【0078】
◎実施例1
実施の形態1に係る自動分析装置を実施例とし、検査ステージKTに検査カートリッジ200を引き込んだ後、補助加温装置90及び恒温槽80を使用し、試薬セル205が恒温条件温度(本例では37℃)に到達するまでの時間を測定したところ、図43に示す‘プレヒート有’の結果が得られた。また、比較例として、補助加温装置90を用いないで恒温槽80のみで試薬セル205が恒温条件温度(本例では37℃)に到達するまでの時間を測定したところ、図43に示す‘プレヒート無’の結果が得られた。但し、実施例、比較例共に環境温度が23℃である条件下で行った。
図43によれば、実施例では、恒温条件温度に到達するまでの時間が30秒弱であるのに対し、比較例では、恒温条件温度に到達するまでの時間が約5分程度かかり、補助加温装置90により検査カートリッジ200の温度を早期に恒温条件温度に調整することが可能になり、仮に、検体が冷蔵庫などに保管され、また、検査カートリッジ200が恒温条件温度よりも低い環境下に置かれていたとしても、恒温条件の下で、検査カートリッジ200に対する測定時間を短縮可能であることが理解される。
【0079】
◎実施例2
実施の形態4に係る自動分析装置を実施例2とし、検査カートリッジ200の反応セル207内の液温立ち上がり状態、並びに、反応セル207内の所定時間(例えば3分)経過後の液温を測定し、モニタリングする。
これらの結果を図44,図45に示す。
図44は反応セル207内の液温立ち上がり状態をモニタリングしたものである。
同図においては、液温初期温度T0を15℃、20℃、25℃、30℃の4通りについて液温立ち上がり状態を測定し、恒温条件温度(例えば37℃)に到達するまでの時間tを計測したところ、以下のような結果が得られた。
液温初期温度T0 恒温条件温度到達時間t
15℃ 5分 2秒
20℃ 4分26秒
25℃ 3分51秒
30℃ 3分10秒
これらの結果からすれば、液温初期温度T0が高いと恒温条件温度に達する時間は短く、逆に低いと恒温条件温度に達する時間が長くなるという相関関係が把握される。
【0080】
また、図45は反応セル207内の液温立ち上がり状態のうち、所定時間(例えば3分)経過後の液温を測定したところ、以下のような結果が得られた。
液温初期温度T0 所定時間経過後の液温T1
15℃ 34.2℃
20℃ 35.4℃
25℃ 36.2℃
30℃ 36.8℃
これらの結果からすれば、液温初期温度T0が高い程、定時間経過後の液温T1は恒温条件温度(例えば37℃)に接近した状態に至ることが理解される。
このため、仮に、恒温条件温度に達しない状態で所定時間(例えば3分)経過後に測定装置100による測定を開始したとしても、各温度条件において、恒温条件を満たしていない状況での反応時間、恒温条件を満たした状況での反応時間を把握することは可能である。このとき、恒温条件を満たしていない状況での反応が恒温条件を満たしている状況に対する影響度合を補正情報として予め保有しておけば、恒温条件を満たしていない状況での反応に対する測定結果を有効に補正することは可能である。
それゆえ、仮に、恒温条件温度に達しない状態で所定時間経過後に測定装置100による測定を開始したとしても、所定の温度補正処理を行うことで測定結果を補正することが可能になり、測定装置100による測定開始時間を速めることができる。
【産業上の利用可能性】
【0081】
本発明は、複数の検査カートリッジを連続検査する際に有効であるが、より簡略化した自動分析装置技術として、カートリッジ受部に一つの検査カートリッジをセットし、この検査カートリッジを検査ステージ側に引き込み、各種検査を行った後に再びカートリッジ受部に戻すような方式に構築することも可能である。
【図面の簡単な説明】
【0082】
【図1】(a)は本発明に係る自動分析装置の概要を示す説明図、(b)は(a)中B方向から見た検査カートリッジの一例を示す模式図である。
【図2】本発明に係る自動分析装置の実施の形態1の外観を示す説明図である。
【図3】実施の形態1に係る自動分析装置の内部構造の概要を示す説明図である。
【図4】実施の形態1に係る自動分析装置の平面模式図である。
【図5】検査カートリッジのセット、引き込み動作に伴う機構を示す説明図である。
【図6】(a)は実施の形態で用いられる検査カートリッジの構成を示す斜視説明図、(b)はその正面説明図、(c)は同図(b)中C方向から見た矢視図である。
【図7】検査カートリッジへの検体の分注方法の一例を示す説明図である。
【図8】検体としての血液を採取する採血具の一例を示し、(a)は採血時の状態、(b)は採取した血液を吐出する際の状態を示す説明図である。
【図9】(a)はカートリッジラックの正面説明図、(b)はその側面説明図である。
【図10】実施の形態で用いられるカートリッジ引き込み機構の一例を示す説明図である。
【図11】図10の平面説明図である。
【図12】図10の側面説明図である。
【図13】実施の形態で用いられるカートリッジ引き込み機構の駆動系を示す説明図である。
【図14】図13の側面説明図である。
【図15】(a)はカートリッジ引き込み機構の動作過程を示す説明図、(b)はカートリッジ引き込み機構の位置規制例を示す説明図である。
【図16】実施の形態で用いられる検体試薬分注機構の一例であり、(a)はノズルチップ装着時の状態を示す説明図、(b)は検体試薬分注時の状態を示す説明図、(c)は穿孔装置を兼用する際の状態を示す説明図である。
【図17】実施の形態で用いられる検査ステージの測定周辺部に設けられる温度調整機構の構成例を示す説明図であり、(a)は補助加温装置が退避位置に位置する状態での全体斜視図、(b)は同図(a)中B方向から見た矢視図である。
【図18】実施の形態で用いられる検査ステージの測定周辺部に設けられる温度調整機構の構成例を示す説明図であり、(a)は補助加温装置が加温位置に位置する状態での全体斜視図、(b)は同図(a)中B方向から見た矢視図である。
【図19】(a)は実施の形態で用いられる恒温槽の斜視説明図、(b)はその側面説明図である。
【図20】(a)は図19(b)中A−A線断面説明図、(b)は測定ステージに検査カートレッジの反応セルがセットされた状態を示す説明図である。
【図21】(a)は実施の形態で用いられる補助加温装置の退避状態を示す説明図、(b)は同補助加温装置の加温状態を示す説明図である。
【図22】実施の形態1で用いられる制御系を示す説明図である。
【図23】(a)〜(d)は実施の形態1に係る自動分析装置の動作過程を示す説明図(1)である。
【図24】(a)〜(c)は実施の形態1に係る自動分析装置の動作過程を示す説明図(2)である。
【図25】実施の形態1で用いられる自動分析装置のバーコード読取動作過程を模式的に示す説明図である。
【図26】実施の形態1で用いられる自動分析装置のノズルチップの有無確認動作過程(1)を模式的に示す説明図である。
【図27】実施の形態1で用いられる自動分析装置のノズルチップの有無確認動作過程(2)を模式的に示す説明図である。
【図28】実施の形態1で用いられる自動分析装置の空気孔開け動作過程を模式的に示す説明図である。
【図29】(a)は図28の空気孔開け動作過程の詳細を示す説明図、(b)は空気孔開けの利点を示す説明図である。
【図30】実施の形態1で用いられる自動分析装置のプレヒート過程、試薬、検体分注動作過程を模式的に示す説明図である。
【図31】実施の形態1で用いられる自動分析装置のノズルチップ排出動作、測定動作過程を模式的に示す説明図である。
【図32】実施の形態1で用いられる自動分析装置の検査カートリッジ排出動作過程を模式的に示す説明図である。
【図33】実施の形態2に係る自動分析装置で用いられる測定装置を示す説明図である。
【図34】実施の形態2で用いられる測定装置の変形形態を示す説明図である。
【図35】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(1)(2)を示す説明図である。
【図36】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(3)(4)を示す説明図である。
【図37】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(5)(6)を示す説明図である。
【図38】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(7)(8)を示す説明図である。
【図39】実施の形態3に係る自動分析装置で用いられるチップ廃棄システム(9)を示す説明図である。
【図40】実施の形態4に係る自動分析装置の概要を示す図4に相当する説明図である。
【図41】実施の形態4で用いられる自動分析装置の検査ステージの要部を示す説明図である。
【図42】実施の形態4に係る自動分析装置の制御系を示す説明図である。
【図43】実施例1に係る自動分析装置の性能を示す説明図である。
【図44】実施例2に係る自動分析装置の性能(反応セル内の液温立ち上がり性能)を示す説明図である。
【図45】実施例2に係る自動分析装置の性能(反応セル内液温モニタリング)を示す説明図である。
【符号の説明】
【0083】
1…カートリッジ受部,2…カートリッジ選択手段,3…カートリッジ搬送手段,4…検体試薬分注手段,5…測定手段,6…恒温槽,7…補助加温手段,10…検査カートリッジ,11…セル,11a…検体セル,11b…試薬セル,11c…反応セル,12…チップ保持部,13…シール,15…ノズルチップ,ST…セットステージ,ST1…検査初期位置,KT…検査ステージ
【特許請求の範囲】
【請求項1】
検体が収容される検体セル、試薬が収容される試薬セル及び検体、試薬が反応させられる反応セルが含まれる検査カートリッジを用い、夫々の検体に対応する複数の検査カートリッジをセットした後、検査カートリッジ毎に検体と試薬との反応を自動分析する自動分析装置において、
セットステージ内に複数の検査カートリッジが所定の配列方向に沿って予めセットされるカートリッジ受部を有し、このセットステージ内の検査初期位置に順次移送選択するカートリッジ選択手段と、
セットステージに隣接する検査ステージに設けられ、カートリッジ選択手段にて検査初期位置に移送選択された検査前の検査カートリッジを検査ステージに直線的に搬入すると共に検査後の検査カートリッジを検査ステージからセットステージに直線的に搬出するカートリッジ搬送手段と、
このカートリッジ搬送手段にて搬入された検査ステージ内の検査カートリッジに対し当該検査カートリッジの検体、試薬を反応セルに分注する検体試薬分注手段と、
この検体試薬分注手段にて分注された反応セル内の検体と試薬との反応を測定する測定手段とを備えたことを特徴とする自動分析装置。
【請求項2】
請求項1記載の自動分析装置において、
検査カートリッジは各セルが直線的に配列されている態様であることを特徴とする自動分析装置。
【請求項3】
請求項1記載の自動分析装置において、
検査カートリッジは、カートリッジ受部に沿って案内挿入され、カートリッジ本体には誤った方向からの挿入時に前記カートリッジ本体に衝合するストッパを具備させたことを特徴とする自動分析装置。
【請求項4】
請求項1記載の自動分析装置において、
カートリッジ選択手段は、複数の検査カートリッジがセットされるカートリッジ受部全体を移送させるものであることを特徴とする自動分析装置。
【請求項5】
請求項1記載の自動分析装置において、
カートリッジ選択手段は、一つの検査初期位置に各検査カートリッジを順次移送選択するものであることを特徴とする自動分析装置。
【請求項6】
請求項1記載の自動分析装置において、
カートリッジ搬送手段は、カートリッジ選択手段による検査カートリッジの移送動作を許容し、検査初期位置に位置する検査カートリッジの被係合片に対して係合可能な係合片を備えていることを特徴とする自動分析装置。
【請求項7】
請求項1記載の自動分析装置において、
検体試薬分注手段は、検査カートリッジ毎に着脱自在なノズルチップを使用するものであることを特徴とする自動分析装置。
【請求項8】
請求項1記載の自動分析装置において、
測定手段は、検査カートリッジの検査項目に対応して測定条件を可変にするものであることを特徴とする自動分析装置。
【請求項9】
請求項1記載の自動分析装置において、
検査ステージには、カートリッジ搬送手段にて検査ステージに搬入された検査カートリッジの少なくとも反応セルを所定の恒温環境温度に保つ恒温槽が設けられていることを特徴とする自動分析装置。
【請求項10】
請求項9記載の自動分析装置において、
検査ステージには、更に、測定手段が動作する前に恒温環境温度よりも高い温度で検査カートリッジのセルの少なくとも一部を予め加温する補助加温手段が設けられていることを特徴とする自動分析装置。
【請求項11】
請求項9記載の自動分析装置において、
測定手段は、測定手段による測定条件が恒温槽の恒温環境条件から外れたときに、温度条件に基づいて測定結果が補正可能な温度補正手段を備えていることを特徴とする自動分析装置。
【請求項12】
請求項11記載の自動分析装置において、
温度補正手段は、検査カートリッジの表面に対して非接触配置される非接触型温度センサからの温度情報に基づいて温度補正するものであることを特徴とする自動分析装置。
【請求項13】
請求項12記載の自動分析装置において、
非接触型温度センサは恒温槽に取り付けたものであることを特徴とする自動分析装置。
【請求項14】
請求項7記載の自動分析装置において、
検査カートリッジは、ノズルチップを着脱可能に保持するチップ保持部を有することを特徴とする自動分析装置。
【請求項15】
請求項7記載の自動分析装置において、
検査カートリッジは、セルの全部若しくは一部を穿孔可能なシールにて密封し、検体試薬分注手段のノズルチップにて検体、試薬の分注動作前にセルに対応するシールに孔を穿設可能としたことを特徴とする自動分析装置。
【請求項1】
検体が収容される検体セル、試薬が収容される試薬セル及び検体、試薬が反応させられる反応セルが含まれる検査カートリッジを用い、夫々の検体に対応する複数の検査カートリッジをセットした後、検査カートリッジ毎に検体と試薬との反応を自動分析する自動分析装置において、
セットステージ内に複数の検査カートリッジが所定の配列方向に沿って予めセットされるカートリッジ受部を有し、このセットステージ内の検査初期位置に順次移送選択するカートリッジ選択手段と、
セットステージに隣接する検査ステージに設けられ、カートリッジ選択手段にて検査初期位置に移送選択された検査前の検査カートリッジを検査ステージに直線的に搬入すると共に検査後の検査カートリッジを検査ステージからセットステージに直線的に搬出するカートリッジ搬送手段と、
このカートリッジ搬送手段にて搬入された検査ステージ内の検査カートリッジに対し当該検査カートリッジの検体、試薬を反応セルに分注する検体試薬分注手段と、
この検体試薬分注手段にて分注された反応セル内の検体と試薬との反応を測定する測定手段とを備えたことを特徴とする自動分析装置。
【請求項2】
請求項1記載の自動分析装置において、
検査カートリッジは各セルが直線的に配列されている態様であることを特徴とする自動分析装置。
【請求項3】
請求項1記載の自動分析装置において、
検査カートリッジは、カートリッジ受部に沿って案内挿入され、カートリッジ本体には誤った方向からの挿入時に前記カートリッジ本体に衝合するストッパを具備させたことを特徴とする自動分析装置。
【請求項4】
請求項1記載の自動分析装置において、
カートリッジ選択手段は、複数の検査カートリッジがセットされるカートリッジ受部全体を移送させるものであることを特徴とする自動分析装置。
【請求項5】
請求項1記載の自動分析装置において、
カートリッジ選択手段は、一つの検査初期位置に各検査カートリッジを順次移送選択するものであることを特徴とする自動分析装置。
【請求項6】
請求項1記載の自動分析装置において、
カートリッジ搬送手段は、カートリッジ選択手段による検査カートリッジの移送動作を許容し、検査初期位置に位置する検査カートリッジの被係合片に対して係合可能な係合片を備えていることを特徴とする自動分析装置。
【請求項7】
請求項1記載の自動分析装置において、
検体試薬分注手段は、検査カートリッジ毎に着脱自在なノズルチップを使用するものであることを特徴とする自動分析装置。
【請求項8】
請求項1記載の自動分析装置において、
測定手段は、検査カートリッジの検査項目に対応して測定条件を可変にするものであることを特徴とする自動分析装置。
【請求項9】
請求項1記載の自動分析装置において、
検査ステージには、カートリッジ搬送手段にて検査ステージに搬入された検査カートリッジの少なくとも反応セルを所定の恒温環境温度に保つ恒温槽が設けられていることを特徴とする自動分析装置。
【請求項10】
請求項9記載の自動分析装置において、
検査ステージには、更に、測定手段が動作する前に恒温環境温度よりも高い温度で検査カートリッジのセルの少なくとも一部を予め加温する補助加温手段が設けられていることを特徴とする自動分析装置。
【請求項11】
請求項9記載の自動分析装置において、
測定手段は、測定手段による測定条件が恒温槽の恒温環境条件から外れたときに、温度条件に基づいて測定結果が補正可能な温度補正手段を備えていることを特徴とする自動分析装置。
【請求項12】
請求項11記載の自動分析装置において、
温度補正手段は、検査カートリッジの表面に対して非接触配置される非接触型温度センサからの温度情報に基づいて温度補正するものであることを特徴とする自動分析装置。
【請求項13】
請求項12記載の自動分析装置において、
非接触型温度センサは恒温槽に取り付けたものであることを特徴とする自動分析装置。
【請求項14】
請求項7記載の自動分析装置において、
検査カートリッジは、ノズルチップを着脱可能に保持するチップ保持部を有することを特徴とする自動分析装置。
【請求項15】
請求項7記載の自動分析装置において、
検査カートリッジは、セルの全部若しくは一部を穿孔可能なシールにて密封し、検体試薬分注手段のノズルチップにて検体、試薬の分注動作前にセルに対応するシールに孔を穿設可能としたことを特徴とする自動分析装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】


【公開番号】特開2008−14636(P2008−14636A)
【公開日】平成20年1月24日(2008.1.24)
【国際特許分類】
【出願番号】特願2006−182845(P2006−182845)
【出願日】平成18年6月30日(2006.6.30)
【出願人】(501315762)株式会社サカエ (18)
【出願人】(591249884)トネックス株式会社 (4)
【Fターム(参考)】
【公開日】平成20年1月24日(2008.1.24)
【国際特許分類】
【出願日】平成18年6月30日(2006.6.30)
【出願人】(501315762)株式会社サカエ (18)
【出願人】(591249884)トネックス株式会社 (4)
【Fターム(参考)】
[ Back to top ]

