自動分析装置
【課題】異物が混入した分析結果を的確に判定できる自動分析装置を提供すること。
【解決手段】血液を含む検体と試薬とを分注して反応させるウェルWを複数有するマイクロプレート20を用いて、各ウェルW内の反応の有無を撮像して分析を行う自動分析装置1において、複数の検査項目にそれぞれ対応する複数のウェルW内を撮像して得られた複数の撮像画像を用いて各画像の測光パラメータを算出して、撮像画像による測定結果が陰性であるか否かを検査項目ごとに判断し、検体の特性情報を分析する分析部33と、検体の特性情報と測定結果とを対応付けて記憶する記憶部37と、分析部が陰性であると判断した測定結果の測光パラメータを抽出する抽出部34と、抽出部34が抽出した測光パラメータの最大値と最小値との差を算出し、算出した差を用いて測定結果が有効であるか否かを判定し、判定の結果を対応する検体の特性情報に付加する判定処理部311とを備えた。
【解決手段】血液を含む検体と試薬とを分注して反応させるウェルWを複数有するマイクロプレート20を用いて、各ウェルW内の反応の有無を撮像して分析を行う自動分析装置1において、複数の検査項目にそれぞれ対応する複数のウェルW内を撮像して得られた複数の撮像画像を用いて各画像の測光パラメータを算出して、撮像画像による測定結果が陰性であるか否かを検査項目ごとに判断し、検体の特性情報を分析する分析部33と、検体の特性情報と測定結果とを対応付けて記憶する記憶部37と、分析部が陰性であると判断した測定結果の測光パラメータを抽出する抽出部34と、抽出部34が抽出した測光パラメータの最大値と最小値との差を算出し、算出した差を用いて測定結果が有効であるか否かを判定し、判定の結果を対応する検体の特性情報に付加する判定処理部311とを備えた。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、免疫学的凝集反応を行なう自動分析装置に関するものである。
【背景技術】
【0002】
従来、血液や体液などの検体の成分を分析する際には、ウェルと呼ばれる複数の反応容器がマトリックス状に配設されて成るマイクロプレートが用いられる。マイクロプレートの各ウェルには、分析対象の物質を含む検体、および分析対象の物質と抗原抗体反応を起こす物質を含む反応試薬が分注される。そして、この分注から所定時間経過した後、ウェル内で生じた凝集反応の有無をCCDカメラ等の撮像手段によって撮像し、この撮像によって得た画像データを用いて検体の成分の分析を行う。
【0003】
ところで、上述した分析は、反応物を撮像した撮像データ(撮像画像)から陰性・陽性の判定を行うため、異物の混入が分析結果に大きく影響する。反応結果を正確に確認するうえで、特に、異物が含まれていない反応物に対して分析処理を行うことが重要となる。この要望に対して、異物の混入を防止するため、分注配管内の圧力を圧力センサで検知し、容器をCCDカメラで撮像して吸引量・分注量の確認を行なう確認方法が開示されている(例えば、特許文献1参照)。
【0004】
【特許文献1】特開2000−193670号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかしながら、特許文献1に示した確認方法において、固形物(ゲル状を含む)等の異物が分注対象の液体に含まれている場合、CCDカメラで撮像されたものは、分注された体積を確認するものであって、内容物を確認することは困難であった。また、圧力センサで検知する圧力変化においても、特に、血液凝集反応に用いられる血液中の異物であるフィブリンは、その大きさや粘性によっては検知できない場合があった。このように、特許文献1に示す確認方法では、異物によってはエラー処理されずに反応処理が行われ、検体と試薬との反応結果に影響を及ぼすおそれがあった。
【0006】
本発明は、上記に鑑みてなされたものであって、異物が混入した分析結果を的確に判定できる自動分析装置を提供することを目的とする。
【課題を解決するための手段】
【0007】
上述した課題を解決し、目的を達成するために、本発明は、血液を含む検体と試薬とを分注して反応させる反応容器を複数有する基板を用いて、各反応容器内を撮像し、該反応容器内の反応の有無をもとに検体の分析を行う自動分析装置において、複数の検査項目にそれぞれ対応する複数の反応容器内を撮像して得られた複数の撮像画像を用いて各画像の測光パラメータを算出し、前記測光パラメータをもとに、前記反応容器内で反応がない場合を陰性として、前記撮像画像による測定結果が陰性であるか否かを検査項目ごとに判断し、検体の特性情報を分析する分析部と、前記検体の特性情報と前記測定結果とを対応付けて記憶する記憶部と、前記分析部が陰性であると判断した前記測定結果の前記測光パラメータを抽出する抽出部と、前記抽出部が抽出した前記測光パラメータの最大値と最小値との差を算出し、該算出した差を用いて前記測定結果が有効であるか否かを判定し、該判定の結果を対応する前記検体の特性情報に付加する判定処理部と、を備えたことを特徴とする。
【0008】
また、本発明にかかる自動分析装置は、上記の発明において、前記測光パラメータは、P/C、SPCおよびLIAからなる群から少なくとも2つ選択され、前記判定処理部は、前記測光パラメータのうち少なくとも1つの測光パラメータの前記差が所定範囲外である場合に、前記測定結果が無効であると判定することを特徴とする。
【0009】
また、本発明にかかる自動分析装置は、上記の発明において、前記測光パラメータは、P/C、SPCおよびLIAからなる群から少なくとも1つ選択され、前記判定処理部は、全ての測光パラメータの前記差が所定範囲外である場合に、前記測定結果が無効であると判定することを特徴とする。
【0010】
また、本発明にかかる自動分析装置は、上記の発明において、前記複数の検査項目に応じて使用する試薬のうちの1つは、必ず陰性を示す参照試薬であることを特徴とする。
【0011】
また、本発明にかかる自動分析装置は、上記の発明において、前記判定処理部によって前記測定結果が無効であると判定された場合に、当該測定結果が無効である旨を出力する出力部をさらに備えたことを特徴とする。
【発明の効果】
【0012】
本発明によれば、撮像データから得られる測光パラメータの最大値と最小値との差を閾値と比較することで測定結果が有効であるか否かを判定するようにしたので、信頼性のある測定結果を得ることができるという効果を奏する。
【図面の簡単な説明】
【0013】
【図1】図1は、本発明の実施の形態にかかる自動分析装置の概略構成を示す模式図である。
【図2】図2は、本発明の実施の形態にかかるABO式血液型の各試薬の陰性(−)および陽性(+)の組み合わせを示す図である。
【図3】図3は、本発明の実施の形態にかかるRho(D)血液型の陰性および陽性の組み合わせを示す図である。
【図4】図4は、本発明の実施の形態にかかるSPC,P/C,LIAの各測光パラメータの閾値の一例を示す図である。
【図5】図5は、図4に示すSPC,P/C,LIAの各測光パラメータの閾値と陰性および陽性の判定との関係を示す図である。
【図6】図6は、本発明の実施の形態にかかるフィブリンが混入した場合の各測光パラメータの測定値および判定と、正常時の測光パラメータの測定値および判定とを示す図である。
【図7】図7は、本発明の実施の形態にかかる測光レンジと閾値とを示す図である。
【図8】図8は、本発明の実施の形態にかかる分析処理を示すフローチャートである。
【図9】図9は、本発明の実施の形態にかかる分析処理の変形例を示すフローチャートである。
【図10】図10は、本発明の実施の形態にかかるポップアップ画面の一例を示す図である。
【発明を実施するための形態】
【0014】
以下、図面を参照して、この発明の実施の形態である分析装置について説明する。なお、この実施の形態によりこの発明が限定されるものではない。また、図面の記載において、同一部分には同一の符号を付している。
【0015】
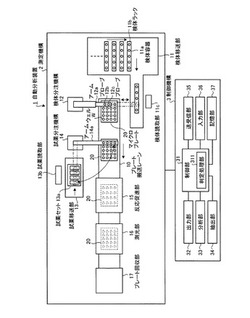
図1は、本実施の形態にかかる分析装置の構成を示す模式図である。図1に示すように、本実施の形態にかかる自動分析装置1は、分析対象である検体および試薬を、マイクロプレート20の所定のウェルWにそれぞれ分注し、ウェルW内で生じる反応を光学的に測定する測定機構2と、測定機構2を含む自動分析装置1全体の制御を行うとともに測定機構2における測定結果の分析を行う制御機構3とを備える。自動分析装置1は、これらの二つの機構が連携することによって複数の検体の免疫学的な分析を自動的に行う。なお、マイクロプレート20は、アクリル等の透明な材料によって構成したプレートで、その表面に開口したウェルWと称する孔を多数有する。ウェルWは、検体と試薬とを収容して反応させる反応容器で、傾斜面が形成された孔であり、マイクロプレート20の表面にマトリクス状に配列されている。
【0016】
測定機構2は、大別してプレート搬送レーン10、検体移送部11、検体分注機構12、試薬移送部13、試薬分注機構14、反応促進部15、測光部16およびプレート回収部17を備える。また、制御機構3は、制御部31、出力部32、分析部33、抽出部34、送受信部35、入力部36および記憶部37を備える。測定機構2および制御機構3が備えるこれらの各部は、制御部31に電気的に接続されている。
【0017】
プレート搬送レーン10は、マイクロプレート20における各ウェルWへの検体や試薬の分注、ウェルW内の液体の反応促進および測光を行うためにマイクロプレート20を所定の位置まで搬送する。このプレート搬送レーン10は、制御部31の制御のもと、図示しない駆動機構が駆動することによって、たとえば図1中の矢印に示すように左方向にマイクロプレート20を搬送する。
【0018】
検体移送部11は、検体を収容した複数の検体容器11aを保持し、図中の矢印方向に順次移送される複数の検体ラック11bを備える。検体容器11aに収容された検体は、検体の提供者から採取した血液に抗凝固剤を加え遠心分離を行い、上澄み液となる血漿と、堆積物となる血球(赤血球)粒子とに分離したものである。検体移送部11上の所定位置に移送された検体容器11a内の検体は、検体分注機構12によって、プレート搬送レーン10上に配列して搬送されるマイクロプレート20の所定のウェルWに分注される。
【0019】
検体容器11aの側面部には、検体容器11aに収容された検体に関する検体情報が記録された記録媒体が付されている。記録媒体は、符号化された各種の情報を表示しており、光学的に読み取られる。検体情報は、たとえば、検体を提供した患者の氏名、性別、年齢、分析項目などがある。
【0020】
検体移送部11の対応箇所には、この記録媒体を光学的に読み取る検体読取部11cが設けられている。検体読取部11cは、記録媒体に対して赤外光または可視光を発し、記録媒体からの反射光を処理することによって、記録媒体の情報を読み取る。また、検体読取部11cは、記録媒体を撮像処理し、撮像処理によって得られた画像情報を解読して、記録媒体の情報を取得してもよい。検体読取部11cは、この検体読取部11cの前を通過する際に、検体容器11aに付された記録媒体の情報を読み取る。
【0021】
検体分注機構12は、検体の吸引および吐出を行うプローブ12b,12cが先端部に取り付けられたアーム12aと、図示しない吸排シリンジまたは圧電素子を用いた吸排機構とを備える。検体分注機構12は、上述した検体移送部11上の所定位置に移送された検体容器11aの中からプローブ12b,12cによって検体を吸引し、アーム12aを図中、上下方向に移動させ、各ウェルWに検体を吐出して分注を行う。なお、プローブ12bは、検体容器11a内の血清を吸引および吐出し、プローブ12cは、検体容器11a内の血球粒子を吸引および吐出する。
【0022】
試薬移送部13は、マイクロプレート20中における各ウェルWに分注される試薬がそれぞれ収容された試薬セット13aを試薬分注機構14による試薬吸引位置まで移送する。試薬セット13aには、各種の分析項目に応じて所要の試薬がそれぞれ所定量収容され、1セットの試薬セット13aに含まれる各試薬は、所定回数の分注に対応する場合のほか、一度の分注に対応する場合もある。試薬移送部13は、所定回数の分注処理が終了した試薬セット13aを回収し、次に分注対象となる試薬セット13aを試薬吸引位置まで移送する。
【0023】
試薬セット13aの側面部には、試薬セット13aに収容された各試薬に関する試薬情報が記録された記録媒体が付されている。記録媒体は、符号化された各種の情報を表示しており、光学的に読み取られる。試薬移送部13の対応箇所には、この記録媒体を光学的に読み取る試薬読取部13bが設けられている。試薬読取部13bは、記録媒体に対して赤外光または可視光を発し、記録媒体からの反射光を処理することによって、記録媒体の情報を読み取る。また、試薬読取部13bは、記録媒体を撮像処理し、撮像処理によって得られた画像情報を解読して、記録媒体の情報を取得してもよい。
【0024】
試薬分注機構14は、試薬の吸引および吐出を行うプローブが先端部に取り付けられたアーム14aを備える。アーム14aは、鉛直方向への昇降および自身の基端部を通過する鉛直線を中心軸とする回転を自在に行う。試薬分注機構14は、図示しない吸排シリンジまたは圧電素子を用いた吸排機構を備える。試薬分注機構14は、試薬移送部13上の所定位置に移動された試薬セット13a内の試薬を対応する各プローブによって吸引し、アーム14aを図中反時計回りに旋回させ、プレート搬送レーン10上の所定位置に搬送されたマイクロプレート20の各ウェルWに対応する各試薬を吐出して分注を行う。
【0025】
反応促進部15は、マイクロプレート20に分注された検体および試薬の反応を促進し、抗原抗体反応を行わせ、マイクロプレート20の各ウェルW底面に凝集パターンを形成させる。反応促進部15は、たとえば、マイクロプレート20を振動させてウェルW内の検体および試薬を攪拌する。また、反応促進部15は、たとえば、分析方法の内容に対応させた所定時間の間、マイクロプレート20を静置し、血球粒子の自然沈降などを促進する。また、反応促進部15は、たとえば、所定の磁場を印加することによってウェルW内に存在する微粒子を操作する。
【0026】
測光部16は、反応促進部15において形成された凝集パターンを測光検出する。測光部16は、たとえばCCDカメラによって構成され、マイクロプレート20の各ウェルWを上方から撮像し、各ウェルWに形成された凝集パターンを撮像した画像情報を出力する。また、測光部16は、マイクロプレート20の各ウェルWに所定の光を照射する発光部と各ウェルW内の検液に発生する光を受光する受光部とを備え、検液に発生した光の輝度を測光結果として出力してもよい。
【0027】
プレート回収部17は、測光部16による測光処理が終了したマイクロプレート20を回収する。回収されたマイクロプレート20は、図示しない洗浄部によって、各ウェルWの混合液の吸引および排出、洗浄液の注入および吸引によって洗浄される。洗浄されたマイクロプレート20は再利用される。なお、検査内容によっては1回の測定終了後にマイクロプレート20が廃棄される場合もある。
【0028】
つぎに、制御機構3について説明する。制御部31は、CPU等を用いて構成され、自動分析装置1の各部の処理および動作を制御する。制御部31は、これらの各構成部位に入出力される情報について所定の入出力制御を行い、かつ、この情報に対して所定の情報処理を行う。また、制御部31は、判定処理部311を有する。判定処理部311は、抽出された測定結果の測光パラメータをもとに、測定結果の有効性を判定する。
【0029】
出力部32は、ディスプレイ、プリンタ、スピーカー等を用いて構成され、分析部33が生成した分析情報を含む諸情報を出力する。また、抽出部34によって抽出された画像データを画面に出力する。
【0030】
分析部33は、測光部16によって測定された測光結果をもとに抗原抗体反応を分析する。なお、分析部33は、測光部16が画像情報を出力する場合、測光部16によって出力された画像情報を処理し、検体の輝度に応じた測光値を取得する。また、分析部33は、凝集反応の陰性、陽性の判定に用いる、SPC(中心部の像のエッジの明瞭さ)、P(周辺領域の明るさ)、C(中心領域の明るさ)、LIA(中心部の像の面積)等を用いて測光パラメータを算出し、記憶部37に記憶されているSPC,P/C,LIAの各測光パラメータの閾値と比較する。なお、SPC,P/Cの測光パラメータは、0〜99の値で求められ、LIAの測光パラメータは0〜999の値で求められる。算出した測光パラメータの数値と、測光パラメータの閾値とを比較して、検査項目ごとに+(陽性)、−(陰性)、不明(陽性と陰性の間であってどちらとも判定できない場合)に判定可能である。ここで、測光パラメータP/Cは、PをCで除算した後、10倍した値をP/Cの測光パラメータとして用いる。
【0031】
抽出部34は、分析部33において陰性であると判断された測定結果がある場合に、記憶部37または図示しない一時記憶領域から当該測定結果に対応する測光パラメータを抽出する。抽出した測光パラメータは、判定処理部311に出力される。
【0032】
送受信部35は、図示しない通信ネットワークを介して所定の形式にしたがった情報の送受信を行うインターフェースとしての機能を有する。入力部36は、キーボード、マウス、マイクロフォン等を用いて構成され、検体の分析に必要な諸情報や分析動作の指示情報等を外部から取得する。また、画面に表示するための抽出項目を制御部31に出力する。
【0033】
記憶部37は、情報を磁気的に記憶するハードディスクと、分析装置1が処理を実行する際にその処理にかかわる各種プログラムをハードディスクからロードして電気的に記憶するメモリとを用いて構成される。また、記憶部37は、検体ごとに、特性情報としての項目判定と項目判定に用いられた測光パラメータとを関連付けて記憶する。なお、記憶部37は、CD−ROM、DVD−ROM、PCカード等の記憶媒体に記憶された情報を読み取ることができる補助記憶装置を備えてもよい。
【0034】
以上のように構成された自動分析装置1では、順次搬送される複数のマイクロプレート20に対して、検体分注機構12が検体容器11a中の検体を分注し、試薬分注機構14が試薬セット13a中の各試薬を分注した後、測光部16が検体と試薬とを反応させた状態の反応像の撮像を行い、この撮像データから分析部33が分析することで、検体の凝集反応分析等が自動的に行われる。
【0035】
ここで、分析部33が行なうABO式血液型およびRho(D)血液型の項目判定について、図2,3を参照して説明する。図2は、本発明の実施の形態にかかるABO式血液型の各試薬の陰性(−)および陽性(+)の組み合わせを示す図であり、図3は、本発明の実施の形態にかかるRho(D)血液型の陰性および陽性の組み合わせを示す図である。分析部33は、図2,3にそれぞれ示す各試薬の陰性および陽性の結果を組み合わせることによって、検体の特性情報としてのABO式血液型およびRho(D)血液型の各項目判定を決定する。本実施の形態における項目判定において、ABO式血液型は、図2に示す関係性をもとに、抗A抗体(抗A)、抗B抗体(抗B)、A血球(Acell)、B血球(Bcell)に対する凝集反応を総合して判定され、Rho(D)血液型は、図3に示す関係性をもとに、抗D抗体(抗D)と対照(Ref)との凝集反応を総合して判定される。ここで、ABO式血液型の判定は、抗A抗体および抗B抗体のみでも判定可能である。
【0036】
なお、試薬判定結果における陰性および陽性の判定は、上述したSPC,P/C,LIAの各測光パラメータの閾値と比較することによって導出される。図4は、本発明の実施の形態にかかるSPC,P/C,LIAの各測光パラメータの閾値の一例を示す図であり、図5は、図4に示すSPC,P/C,LIAの各測光パラメータの閾値と陰性および陽性の判定との関係を示す図である。
【0037】
図4に示す定性判定用閾値の一例において、SPC,P/C,LIAの各測定パラメータは、陽性判定に対応する閾値と、陰性判定に対応する閾値とを有する。SPCは、陽性判定の判定基準値(Low)として10、陰性判定の判定基準値(High)として20に設定されている。また、P/Cは、陰性判定の判定基準値((−)limit)として20、陽性判定の判定基準値((+)limit)として30に設定される。LIAは、陰性判定の判定基準値((−)limit)として100、陽性判定の判定基準値((+)limit)として400に設定される。なお、refは、リファレンス(参照試薬)であり、反応性成分を含まない生理食塩水を試薬として検体とを混合し、反応像を確認する。リファレンスは、必ず陰性の反応像を形成し、種々の検査項目の測定結果との比較にもなる。
【0038】
分析部33は、定性判定用閾値の設定によって、算出した測光パラメータの値をもとに、図5に示す各判定の領域を参照して、各試薬(検査項目)の測光パラメータが陰性であるか否かを判断する。つまり、分析部33は、測光パラメータSPCにおいて、得られた測光パラメータSPCの値が、陽性判定基準値(Low)である10未満の場合は判定結果を陽性と判断し、陰性判定基準値(High)である20を越えた場合は陰性と判断する。また、測光パラメータSPCの値が10〜20の場合は判定不能(図5、?)であると判断する。
【0039】
一方、分析部33は、測光パラメータP/Cにおいて、得られた測光パラメータP/Cの値が、陽性判定基準値30未満の場合は陽性と判断し、陰性判定基準値20を超えた場合は陰性と判断する。また、測光パラメータP/Cの値が、両判定基準値にはさまれた20〜30の場合は陽性とも陰性とも判定可能であり(図5、+or−)、他の測光パラメータの判定結果から試薬判定結果を決定する。測光パラメータLIAはP/Cと同様、測光パラメータLIAの値が、陽性判定基準値400未満の場合は陽性と判断され、陰性判定基準値100を超えた場合は陰性と判断され、両判定基準値にはさまれた100〜400の場合は陽性とも陰性とも判定可能であり(図5、+or−)、他の測光パラメータの判定結果から試薬判定結果を決定する。なお、各測光パラメータの定性判定用閾値の設定および試薬判定方法は、上記に限定されるものではない。
【0040】
分析部33は、試薬に対応する各測光パラメータの陰性または陽性を決定した後、SPC,P/C,LIAの各測定パラメータの判定が同一である場合に、その判定が試薬判定結果として決定する。ここで、SPC,P/C,LIAの判定のうち、1つでも判定が異なる場合は、判定不可として試薬判定結果が決定される。なお、各測光パラメータに優先度を設け、優先度の高い測光パラメータの判定を判定結果として試薬判定結果を決定するようにしてもよい。
【0041】
上述した流れで得られた試薬判定結果を用いて、図2,3に示した組み合わせを参照して各項目判定結果が決定される。なお、不規則抗体等、他の試験においても同様の流れで陰性・陽性が決定することができる。
【0042】
つづいて、分注された検体に異物が混入した場合、たとえば、検体中にフィブリンが析出した場合の項目判定結果の有効性について、図6,7,8を参照して説明する。フィブリンは、フィブリノーゲンとして血漿中に溶解し、プロテアーゼおよびカルシウムの作用によってフィブリン・ポリマーを形成し、血液凝固に関わっている。血液分析においては、このフィブリンによる血液の凝固を防止するために抗凝固剤が添加されるが、経時変化によるフィブリンの析出や抗凝固剤の混合不足による血餅が発生し、析出したフィブリンや血餅が反応容器に混入し、撮像されることによって検査結果の誤判定を起こすことがあった。
【0043】
図6は、本発明の実施の形態にかかるフィブリンが混入した場合の各測光パラメータの測定値および判定と、正常時の測光パラメータの測定値および判定とを示す図である。検体は、同一の検体を使用し、一方の検体にフィブリンが混入している状態(分注異常)で反応処理・分析処理を行った。図6に示すように、各試薬(検査項目)に対して、それぞれ測光パラメータの数値が算出され、その数値をもとに陰性または陽性の判定が決定されている。
【0044】
ここで、抗A(抗A抗体)において、フィブリン吸引時の判定と正常分注時の判定が異なっている。このため、本来A型と判定されるべき項目判定が、O型と誤判定され、輸血時等に事故を起こしてしまうおそれがある。これは、本来血球が凝集して陽性と判定されるところを、血餅または析出したフィブリンの像が撮像され、各測光パラメータの算出時に血餅または析出したフィブリンの像を非凝集像として誤認識してしまうために起こる。本実施の形態では、この誤認識を判定し、測定結果の有効性を判断する。
【0045】
有効性の判断は、図6に示す測光レンジを算出し、図7に示す閾値と比較することによって決定される。図7は、本発明の実施の形態にかかる測光レンジと閾値とを示す図である。測光レンジは、同一検体を分析した各試薬の中で陰性と判定された試薬の各測光パラメータの数値から最大値と最小値との差を算出した値である。たとえば、分注異常(フィブリン吸引時)のLIAでは、最大値が抗Aの869、最小値が抗Bの390となり、その差を算出した479が測光値レンジとなる。また、正常分注時のLIAでは、最大値が抗Bの689、最小値がrefの679となり、測光値レンジは10となる。このようにして求められる測光値レンジに対して図7に示す閾値を設けることで、判定に用いられる各パラメータに信頼性があるか否かを判断し、判定が有効性を有するか否かを決定する。
【0046】
図7において、フィブリン吸引時のP/CおよびSPCの測定値レンジがP/Cレンジで11、SPCレンジで6となっている一方、正常時のP/Cレンジ、SPCレンジは、ともに1となっている。また、LIAレンジにおいても、フィブリン吸引時は479と各試薬間で幅広い値をとっているのに対して正常時は10と低い値となっている。この測光値レンジの差に閾値を設けることで、判定の有効性を判断する。なお、閾値は、任意に設定が可能であり、無効と判定すべき閾値を検査項目や検体種によって変更することができる。
【0047】
つぎに、上述した分析処理の流れにについて図8を参照して説明する。図8は、自動分析装置1が行なう分析処理を示すフローチャートである。制御部31は、測光部16から撮像データを取得すると(ステップS102)、分析部33に取得した撮像データから測光パラメータを算出して(ステップS104)、各試薬に対する陰性・陽性判定(ステップS106)およびステップS106の判定結果から項目判定(特性情報)を決定するよう指示する(ステップS108)。
【0048】
項目判定(特性情報)決定後、制御部31は、リファレンスを除く試薬で陰性であると決定された試薬判定があるか否かを確認する(ステップS110)。ここで、陰性であると決定された試薬がある場合(ステップS110:Yes)、制御部31は、抽出部34に対象の測光パラメータを抽出するよう指示する(ステップS112)。測光パラメータを抽出後、制御部31は、抽出された測光パラメータを判定処理部311に出力し、測光値レンジを算出させる(ステップS114)。
【0049】
測光レンジの算出後、判定処理部311は、各測光パラメータの測光値レンジが、閾値未満であるか否か判断する(ステップS116〜120)。まず、判定処理部311は、測光パラメータLIAの測光値レンジ(LIAレンジ)が閾値未満であるか否かを判定する(ステップS116)。ここで、LIAレンジが閾値未満である場合(ステップS116:Yes)、判定処理部311は、ステップS118に移行して測光パラメータP/Cの測光値レンジ(P/Cレンジ)が閾値未満であるか否かを判定する。P/Cレンジにおいても閾値未満である場合(ステップS118:Yes)、判定処理部311は、ステップS120に移行して、測光パラメータSPCの測光値レンジ(SPCレンジ)が閾値未満であるか否かを判定する。SPCレンジが閾値未満である場合(ステップS120:Yes)、判定処理部311は、測光パラメータの各レンジが閾値未満であるため、項目判定は有効であると判定し、制御部31に有効である旨の情報を出力する。制御部31は、有効である旨の情報の入力によってステップS124に移行する。ステップS124において、制御部31は、次の分析対象の測定結果がある場合(ステップS124:Yes)、ステップS102に移行して上述した処理を繰り返し、測定結果がない場合(ステップS124:No)、作業を終了する。
【0050】
一方、ステップS116〜S120のいずれかにおいて各測光値レンジが閾値以上であった場合(ステップS116,S118,S120:No)、判定処理部311は、測光パラメータの数値に異常があると判定し、異常値である旨の判定結果情報を項目判定(特性情報)に付加する(ステップS122)。制御部31は、判定結果情報を付加した旨の情報を受け取ると、ステップS124に移行する。
【0051】
また、ステップS110において、陰性であると決定された試薬判定がない場合(ステップS110:No)、制御部31は、ステップS124に移行する。
【0052】
上述した処理によって、画像データから得られる測光パラメータが有効であるか否かを判定して項目判定(特性情報)の有効性を判断することによって、得られたデータの信頼性を向上させることが可能となる。
【0053】
なお、図8に示すフローチャートは、3つのパラメータLIA,P/C,SPCのうち1つでも閾値を越えるものがあれば異常値と判定されたが、3つのパラメータすべてが閾値を超えた場合に異常であると判定するようにしてもよい。図9は、本発明の実施の形態にかかる分析処理の変形例を示すフローチャートである。
【0054】
図8に示すフローチャートと同様に、制御部31は、測光部16から撮像データを取得すると(ステップS202)、分析部33に取得した撮像データから測光パラメータを算出して(ステップS204)、各試薬に対する陰性・陽性判定(ステップS206)およびステップS206の判定結果から項目判定(特性情報)を決定するよう指示する(ステップS208)。
【0055】
項目判定(特性情報)決定後、制御部31は、リファレンスを除く試薬で陰性であると決定された試薬判定があるか否かを確認する(ステップS210)。ここで、陰性であると決定された試薬判定がある場合(ステップS210:Yes)、制御部31は、抽出部34に対象の測光パラメータを抽出するよう指示する(ステップS212)。測光パラメータを抽出後、制御部31は、抽出された測光パラメータを判定処理部311に出力し、測光値レンジを算出させる(ステップS214)。
【0056】
測光レンジの算出後、判定処理部311は、各測光パラメータの測光値レンジが、閾値以上であるか否か判断する(ステップS216〜220)。まず、判定処理部311は、測光パラメータLIAの測光値レンジ(LIAレンジ)が閾値以上であるか否かを判定する(ステップS216)。ここで、LIAレンジが閾値以上である場合(ステップS216:Yes)、判定処理部311は、ステップS218に移行して測光パラメータP/Cの測光値レンジ(P/Cレンジ)が閾値以上であるか否かを判定する。P/Cレンジにおいても閾値以上である場合(ステップS218:Yes)、判定処理部311は、ステップS220に移行して、測光パラメータSPCの測光値レンジ(SPCレンジ)が閾値以上であるか否かを判定する。SPCレンジが閾値以上である場合(ステップS220:Yes)、判定処理部311は、測光パラメータの各レンジが閾値以上であるため、測光パラメータが異常値であって、項目判定は無効であると判定し、項目判定(特性情報)に異常値である旨の情報を付加して、制御部31に出力する(ステップS222)。制御部31は、無効である旨の情報を受けると、ステップS224に移行する。ステップS224において、制御部31は、次の分析対象の測定結果がある場合(ステップS224:Yes)、ステップS202に移行して上述した処理を繰り返し、測定結果がない場合(ステップS224:No)、作業を終了する。
【0057】
一方、ステップS216〜S220のいずれかにおいて各測光値レンジが閾値未満であった場合(ステップS216,S218,S220:No)、判定処理部311は、測光パラメータの数値は有効であると判定し、測光パラメータが有効である旨の情報を制御部31に出力する。制御部31は、判定結果情報を付加した旨の情報を受け取ると、ステップS224に移行する。また、ステップS210において、陰性であると決定された試薬判定がない場合(ステップS210:No)、制御部31は、ステップS224に移行する。
【0058】
上述した分析処理によって、各測光パラメータの測光値レンジすべてが閾値を越えた場合に異常値であると判定することが可能となる。
【0059】
なお、本実施の形態では、ステップS110,S210において、リファレンスを除く陰性判定結果を検索するとしたが、リファレンスを含めた複数の陰性判定結果があるか否かを検索するようにしてもよい。本来、リファレンスは必ず陰性となるため、リファレンスで陽性と判定された場合は、フィブリンの析出や血餅以外の要因によるものであるため、別途確認が必要である。
【0060】
また、閾値との比較を行なう測光パラメータの順序は、如何なる順序でもよい。検体種または試薬に対する各測光パラメータの性質によって任意に順序の変更が可能である。
【0061】
ここで、測光パラメータが異常値であると判定され、項目判定(特性情報)に異常値である旨の情報が付加された項目判定結果の表示は、出力部32がモニタ等に項目判定結果を表示する際に、対応する項目判定および/または試薬判定および/または測光パラメータ部分を網掛けで表示してもよく、判定にかかる文字および数値の色を変えて表示してもよい。
【0062】
また、測光パラメータが異常であると判定された測光パラメータがある場合に、出力部32がメッセージを表示するようにしてもよい。図10は、本発明の実施の形態にかかるポップアップ画面の一例を示す図である。図10に示すポップアップ画面W1のように、分析情報として検体IDと測定結果が異常である旨のメッセージとを出力部32がモニタ等に表示するようにしてもよい。
【0063】
なお、表示のタイミングは、異常であると判定したときに表示してもよく、操作者が判定結果を確認した際に表示するようにしてもよい。さらに、操作者がメッセージを確認してOKボタンB1を押下した場合に、ポップアップ画面W1を終了するように設定してもよいし、OKボタンB1が押下された場合に、測定結果を確認する画面が自動的に表示されるように設定してもよい。
【0064】
上述した実施の形態にかかる自動分析装置によって、異物の混入によって誤判定された測定結果を的確に抽出して確認することが可能となる。なお、フィブリンの他、検体中(撮像画像中)に異物が混入した場合でも対応できる。本実施の形態にかかる分析処理によれば、撮像画像の変化によって有効か否かの判定が可能なため、測光パラメータの数値を比較することで無効となる測定結果を的確に抽出することができる。
【0065】
ここで、図8,9に示すフローチャートにおいて、閾値と比較する測光パラメータを、異物の混入により最も顕著に測定値が変化する測光パラメータのみ、たとえば、LIAの測光値レンジを閾値と比較するようにしてもよく、任意に選択した2つの測光パラメータ、たとえば、LIAとP/Cとの各測光値レンジを閾値と比較するようにしてもよい。本発明に用いられる測光パラメータは、試薬の特性または検体の性質により任意に選択可能である。
【産業上の利用可能性】
【0066】
以上のように、本発明にかかる自動分析装置は、誤判定された測定結果を抽出する場合に有用であり、特に、画像から分析される分析処理に適している。
【符号の説明】
【0067】
1 自動分析装置
2 測定機構
3 制御機構
10 プレート搬送レーン
11 検体移送部
11a 検体容器
11b 検体ラック
11c 検体読取部
12 検体分注機構
12a,14a アーム
12b,12c プローブ
13 試薬移送部
13a 試薬セット
13b 試薬読取部
14 試薬分注機構
15 反応促進部
16 測光部
17 プレート回収部
20 マイクロプレート
31 制御部
311 判定処理部
32 出力部
33 分析部
34 抽出部
35 送受信部
36 入力部
37 記憶部
【技術分野】
【0001】
本発明は、免疫学的凝集反応を行なう自動分析装置に関するものである。
【背景技術】
【0002】
従来、血液や体液などの検体の成分を分析する際には、ウェルと呼ばれる複数の反応容器がマトリックス状に配設されて成るマイクロプレートが用いられる。マイクロプレートの各ウェルには、分析対象の物質を含む検体、および分析対象の物質と抗原抗体反応を起こす物質を含む反応試薬が分注される。そして、この分注から所定時間経過した後、ウェル内で生じた凝集反応の有無をCCDカメラ等の撮像手段によって撮像し、この撮像によって得た画像データを用いて検体の成分の分析を行う。
【0003】
ところで、上述した分析は、反応物を撮像した撮像データ(撮像画像)から陰性・陽性の判定を行うため、異物の混入が分析結果に大きく影響する。反応結果を正確に確認するうえで、特に、異物が含まれていない反応物に対して分析処理を行うことが重要となる。この要望に対して、異物の混入を防止するため、分注配管内の圧力を圧力センサで検知し、容器をCCDカメラで撮像して吸引量・分注量の確認を行なう確認方法が開示されている(例えば、特許文献1参照)。
【0004】
【特許文献1】特開2000−193670号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかしながら、特許文献1に示した確認方法において、固形物(ゲル状を含む)等の異物が分注対象の液体に含まれている場合、CCDカメラで撮像されたものは、分注された体積を確認するものであって、内容物を確認することは困難であった。また、圧力センサで検知する圧力変化においても、特に、血液凝集反応に用いられる血液中の異物であるフィブリンは、その大きさや粘性によっては検知できない場合があった。このように、特許文献1に示す確認方法では、異物によってはエラー処理されずに反応処理が行われ、検体と試薬との反応結果に影響を及ぼすおそれがあった。
【0006】
本発明は、上記に鑑みてなされたものであって、異物が混入した分析結果を的確に判定できる自動分析装置を提供することを目的とする。
【課題を解決するための手段】
【0007】
上述した課題を解決し、目的を達成するために、本発明は、血液を含む検体と試薬とを分注して反応させる反応容器を複数有する基板を用いて、各反応容器内を撮像し、該反応容器内の反応の有無をもとに検体の分析を行う自動分析装置において、複数の検査項目にそれぞれ対応する複数の反応容器内を撮像して得られた複数の撮像画像を用いて各画像の測光パラメータを算出し、前記測光パラメータをもとに、前記反応容器内で反応がない場合を陰性として、前記撮像画像による測定結果が陰性であるか否かを検査項目ごとに判断し、検体の特性情報を分析する分析部と、前記検体の特性情報と前記測定結果とを対応付けて記憶する記憶部と、前記分析部が陰性であると判断した前記測定結果の前記測光パラメータを抽出する抽出部と、前記抽出部が抽出した前記測光パラメータの最大値と最小値との差を算出し、該算出した差を用いて前記測定結果が有効であるか否かを判定し、該判定の結果を対応する前記検体の特性情報に付加する判定処理部と、を備えたことを特徴とする。
【0008】
また、本発明にかかる自動分析装置は、上記の発明において、前記測光パラメータは、P/C、SPCおよびLIAからなる群から少なくとも2つ選択され、前記判定処理部は、前記測光パラメータのうち少なくとも1つの測光パラメータの前記差が所定範囲外である場合に、前記測定結果が無効であると判定することを特徴とする。
【0009】
また、本発明にかかる自動分析装置は、上記の発明において、前記測光パラメータは、P/C、SPCおよびLIAからなる群から少なくとも1つ選択され、前記判定処理部は、全ての測光パラメータの前記差が所定範囲外である場合に、前記測定結果が無効であると判定することを特徴とする。
【0010】
また、本発明にかかる自動分析装置は、上記の発明において、前記複数の検査項目に応じて使用する試薬のうちの1つは、必ず陰性を示す参照試薬であることを特徴とする。
【0011】
また、本発明にかかる自動分析装置は、上記の発明において、前記判定処理部によって前記測定結果が無効であると判定された場合に、当該測定結果が無効である旨を出力する出力部をさらに備えたことを特徴とする。
【発明の効果】
【0012】
本発明によれば、撮像データから得られる測光パラメータの最大値と最小値との差を閾値と比較することで測定結果が有効であるか否かを判定するようにしたので、信頼性のある測定結果を得ることができるという効果を奏する。
【図面の簡単な説明】
【0013】
【図1】図1は、本発明の実施の形態にかかる自動分析装置の概略構成を示す模式図である。
【図2】図2は、本発明の実施の形態にかかるABO式血液型の各試薬の陰性(−)および陽性(+)の組み合わせを示す図である。
【図3】図3は、本発明の実施の形態にかかるRho(D)血液型の陰性および陽性の組み合わせを示す図である。
【図4】図4は、本発明の実施の形態にかかるSPC,P/C,LIAの各測光パラメータの閾値の一例を示す図である。
【図5】図5は、図4に示すSPC,P/C,LIAの各測光パラメータの閾値と陰性および陽性の判定との関係を示す図である。
【図6】図6は、本発明の実施の形態にかかるフィブリンが混入した場合の各測光パラメータの測定値および判定と、正常時の測光パラメータの測定値および判定とを示す図である。
【図7】図7は、本発明の実施の形態にかかる測光レンジと閾値とを示す図である。
【図8】図8は、本発明の実施の形態にかかる分析処理を示すフローチャートである。
【図9】図9は、本発明の実施の形態にかかる分析処理の変形例を示すフローチャートである。
【図10】図10は、本発明の実施の形態にかかるポップアップ画面の一例を示す図である。
【発明を実施するための形態】
【0014】
以下、図面を参照して、この発明の実施の形態である分析装置について説明する。なお、この実施の形態によりこの発明が限定されるものではない。また、図面の記載において、同一部分には同一の符号を付している。
【0015】
図1は、本実施の形態にかかる分析装置の構成を示す模式図である。図1に示すように、本実施の形態にかかる自動分析装置1は、分析対象である検体および試薬を、マイクロプレート20の所定のウェルWにそれぞれ分注し、ウェルW内で生じる反応を光学的に測定する測定機構2と、測定機構2を含む自動分析装置1全体の制御を行うとともに測定機構2における測定結果の分析を行う制御機構3とを備える。自動分析装置1は、これらの二つの機構が連携することによって複数の検体の免疫学的な分析を自動的に行う。なお、マイクロプレート20は、アクリル等の透明な材料によって構成したプレートで、その表面に開口したウェルWと称する孔を多数有する。ウェルWは、検体と試薬とを収容して反応させる反応容器で、傾斜面が形成された孔であり、マイクロプレート20の表面にマトリクス状に配列されている。
【0016】
測定機構2は、大別してプレート搬送レーン10、検体移送部11、検体分注機構12、試薬移送部13、試薬分注機構14、反応促進部15、測光部16およびプレート回収部17を備える。また、制御機構3は、制御部31、出力部32、分析部33、抽出部34、送受信部35、入力部36および記憶部37を備える。測定機構2および制御機構3が備えるこれらの各部は、制御部31に電気的に接続されている。
【0017】
プレート搬送レーン10は、マイクロプレート20における各ウェルWへの検体や試薬の分注、ウェルW内の液体の反応促進および測光を行うためにマイクロプレート20を所定の位置まで搬送する。このプレート搬送レーン10は、制御部31の制御のもと、図示しない駆動機構が駆動することによって、たとえば図1中の矢印に示すように左方向にマイクロプレート20を搬送する。
【0018】
検体移送部11は、検体を収容した複数の検体容器11aを保持し、図中の矢印方向に順次移送される複数の検体ラック11bを備える。検体容器11aに収容された検体は、検体の提供者から採取した血液に抗凝固剤を加え遠心分離を行い、上澄み液となる血漿と、堆積物となる血球(赤血球)粒子とに分離したものである。検体移送部11上の所定位置に移送された検体容器11a内の検体は、検体分注機構12によって、プレート搬送レーン10上に配列して搬送されるマイクロプレート20の所定のウェルWに分注される。
【0019】
検体容器11aの側面部には、検体容器11aに収容された検体に関する検体情報が記録された記録媒体が付されている。記録媒体は、符号化された各種の情報を表示しており、光学的に読み取られる。検体情報は、たとえば、検体を提供した患者の氏名、性別、年齢、分析項目などがある。
【0020】
検体移送部11の対応箇所には、この記録媒体を光学的に読み取る検体読取部11cが設けられている。検体読取部11cは、記録媒体に対して赤外光または可視光を発し、記録媒体からの反射光を処理することによって、記録媒体の情報を読み取る。また、検体読取部11cは、記録媒体を撮像処理し、撮像処理によって得られた画像情報を解読して、記録媒体の情報を取得してもよい。検体読取部11cは、この検体読取部11cの前を通過する際に、検体容器11aに付された記録媒体の情報を読み取る。
【0021】
検体分注機構12は、検体の吸引および吐出を行うプローブ12b,12cが先端部に取り付けられたアーム12aと、図示しない吸排シリンジまたは圧電素子を用いた吸排機構とを備える。検体分注機構12は、上述した検体移送部11上の所定位置に移送された検体容器11aの中からプローブ12b,12cによって検体を吸引し、アーム12aを図中、上下方向に移動させ、各ウェルWに検体を吐出して分注を行う。なお、プローブ12bは、検体容器11a内の血清を吸引および吐出し、プローブ12cは、検体容器11a内の血球粒子を吸引および吐出する。
【0022】
試薬移送部13は、マイクロプレート20中における各ウェルWに分注される試薬がそれぞれ収容された試薬セット13aを試薬分注機構14による試薬吸引位置まで移送する。試薬セット13aには、各種の分析項目に応じて所要の試薬がそれぞれ所定量収容され、1セットの試薬セット13aに含まれる各試薬は、所定回数の分注に対応する場合のほか、一度の分注に対応する場合もある。試薬移送部13は、所定回数の分注処理が終了した試薬セット13aを回収し、次に分注対象となる試薬セット13aを試薬吸引位置まで移送する。
【0023】
試薬セット13aの側面部には、試薬セット13aに収容された各試薬に関する試薬情報が記録された記録媒体が付されている。記録媒体は、符号化された各種の情報を表示しており、光学的に読み取られる。試薬移送部13の対応箇所には、この記録媒体を光学的に読み取る試薬読取部13bが設けられている。試薬読取部13bは、記録媒体に対して赤外光または可視光を発し、記録媒体からの反射光を処理することによって、記録媒体の情報を読み取る。また、試薬読取部13bは、記録媒体を撮像処理し、撮像処理によって得られた画像情報を解読して、記録媒体の情報を取得してもよい。
【0024】
試薬分注機構14は、試薬の吸引および吐出を行うプローブが先端部に取り付けられたアーム14aを備える。アーム14aは、鉛直方向への昇降および自身の基端部を通過する鉛直線を中心軸とする回転を自在に行う。試薬分注機構14は、図示しない吸排シリンジまたは圧電素子を用いた吸排機構を備える。試薬分注機構14は、試薬移送部13上の所定位置に移動された試薬セット13a内の試薬を対応する各プローブによって吸引し、アーム14aを図中反時計回りに旋回させ、プレート搬送レーン10上の所定位置に搬送されたマイクロプレート20の各ウェルWに対応する各試薬を吐出して分注を行う。
【0025】
反応促進部15は、マイクロプレート20に分注された検体および試薬の反応を促進し、抗原抗体反応を行わせ、マイクロプレート20の各ウェルW底面に凝集パターンを形成させる。反応促進部15は、たとえば、マイクロプレート20を振動させてウェルW内の検体および試薬を攪拌する。また、反応促進部15は、たとえば、分析方法の内容に対応させた所定時間の間、マイクロプレート20を静置し、血球粒子の自然沈降などを促進する。また、反応促進部15は、たとえば、所定の磁場を印加することによってウェルW内に存在する微粒子を操作する。
【0026】
測光部16は、反応促進部15において形成された凝集パターンを測光検出する。測光部16は、たとえばCCDカメラによって構成され、マイクロプレート20の各ウェルWを上方から撮像し、各ウェルWに形成された凝集パターンを撮像した画像情報を出力する。また、測光部16は、マイクロプレート20の各ウェルWに所定の光を照射する発光部と各ウェルW内の検液に発生する光を受光する受光部とを備え、検液に発生した光の輝度を測光結果として出力してもよい。
【0027】
プレート回収部17は、測光部16による測光処理が終了したマイクロプレート20を回収する。回収されたマイクロプレート20は、図示しない洗浄部によって、各ウェルWの混合液の吸引および排出、洗浄液の注入および吸引によって洗浄される。洗浄されたマイクロプレート20は再利用される。なお、検査内容によっては1回の測定終了後にマイクロプレート20が廃棄される場合もある。
【0028】
つぎに、制御機構3について説明する。制御部31は、CPU等を用いて構成され、自動分析装置1の各部の処理および動作を制御する。制御部31は、これらの各構成部位に入出力される情報について所定の入出力制御を行い、かつ、この情報に対して所定の情報処理を行う。また、制御部31は、判定処理部311を有する。判定処理部311は、抽出された測定結果の測光パラメータをもとに、測定結果の有効性を判定する。
【0029】
出力部32は、ディスプレイ、プリンタ、スピーカー等を用いて構成され、分析部33が生成した分析情報を含む諸情報を出力する。また、抽出部34によって抽出された画像データを画面に出力する。
【0030】
分析部33は、測光部16によって測定された測光結果をもとに抗原抗体反応を分析する。なお、分析部33は、測光部16が画像情報を出力する場合、測光部16によって出力された画像情報を処理し、検体の輝度に応じた測光値を取得する。また、分析部33は、凝集反応の陰性、陽性の判定に用いる、SPC(中心部の像のエッジの明瞭さ)、P(周辺領域の明るさ)、C(中心領域の明るさ)、LIA(中心部の像の面積)等を用いて測光パラメータを算出し、記憶部37に記憶されているSPC,P/C,LIAの各測光パラメータの閾値と比較する。なお、SPC,P/Cの測光パラメータは、0〜99の値で求められ、LIAの測光パラメータは0〜999の値で求められる。算出した測光パラメータの数値と、測光パラメータの閾値とを比較して、検査項目ごとに+(陽性)、−(陰性)、不明(陽性と陰性の間であってどちらとも判定できない場合)に判定可能である。ここで、測光パラメータP/Cは、PをCで除算した後、10倍した値をP/Cの測光パラメータとして用いる。
【0031】
抽出部34は、分析部33において陰性であると判断された測定結果がある場合に、記憶部37または図示しない一時記憶領域から当該測定結果に対応する測光パラメータを抽出する。抽出した測光パラメータは、判定処理部311に出力される。
【0032】
送受信部35は、図示しない通信ネットワークを介して所定の形式にしたがった情報の送受信を行うインターフェースとしての機能を有する。入力部36は、キーボード、マウス、マイクロフォン等を用いて構成され、検体の分析に必要な諸情報や分析動作の指示情報等を外部から取得する。また、画面に表示するための抽出項目を制御部31に出力する。
【0033】
記憶部37は、情報を磁気的に記憶するハードディスクと、分析装置1が処理を実行する際にその処理にかかわる各種プログラムをハードディスクからロードして電気的に記憶するメモリとを用いて構成される。また、記憶部37は、検体ごとに、特性情報としての項目判定と項目判定に用いられた測光パラメータとを関連付けて記憶する。なお、記憶部37は、CD−ROM、DVD−ROM、PCカード等の記憶媒体に記憶された情報を読み取ることができる補助記憶装置を備えてもよい。
【0034】
以上のように構成された自動分析装置1では、順次搬送される複数のマイクロプレート20に対して、検体分注機構12が検体容器11a中の検体を分注し、試薬分注機構14が試薬セット13a中の各試薬を分注した後、測光部16が検体と試薬とを反応させた状態の反応像の撮像を行い、この撮像データから分析部33が分析することで、検体の凝集反応分析等が自動的に行われる。
【0035】
ここで、分析部33が行なうABO式血液型およびRho(D)血液型の項目判定について、図2,3を参照して説明する。図2は、本発明の実施の形態にかかるABO式血液型の各試薬の陰性(−)および陽性(+)の組み合わせを示す図であり、図3は、本発明の実施の形態にかかるRho(D)血液型の陰性および陽性の組み合わせを示す図である。分析部33は、図2,3にそれぞれ示す各試薬の陰性および陽性の結果を組み合わせることによって、検体の特性情報としてのABO式血液型およびRho(D)血液型の各項目判定を決定する。本実施の形態における項目判定において、ABO式血液型は、図2に示す関係性をもとに、抗A抗体(抗A)、抗B抗体(抗B)、A血球(Acell)、B血球(Bcell)に対する凝集反応を総合して判定され、Rho(D)血液型は、図3に示す関係性をもとに、抗D抗体(抗D)と対照(Ref)との凝集反応を総合して判定される。ここで、ABO式血液型の判定は、抗A抗体および抗B抗体のみでも判定可能である。
【0036】
なお、試薬判定結果における陰性および陽性の判定は、上述したSPC,P/C,LIAの各測光パラメータの閾値と比較することによって導出される。図4は、本発明の実施の形態にかかるSPC,P/C,LIAの各測光パラメータの閾値の一例を示す図であり、図5は、図4に示すSPC,P/C,LIAの各測光パラメータの閾値と陰性および陽性の判定との関係を示す図である。
【0037】
図4に示す定性判定用閾値の一例において、SPC,P/C,LIAの各測定パラメータは、陽性判定に対応する閾値と、陰性判定に対応する閾値とを有する。SPCは、陽性判定の判定基準値(Low)として10、陰性判定の判定基準値(High)として20に設定されている。また、P/Cは、陰性判定の判定基準値((−)limit)として20、陽性判定の判定基準値((+)limit)として30に設定される。LIAは、陰性判定の判定基準値((−)limit)として100、陽性判定の判定基準値((+)limit)として400に設定される。なお、refは、リファレンス(参照試薬)であり、反応性成分を含まない生理食塩水を試薬として検体とを混合し、反応像を確認する。リファレンスは、必ず陰性の反応像を形成し、種々の検査項目の測定結果との比較にもなる。
【0038】
分析部33は、定性判定用閾値の設定によって、算出した測光パラメータの値をもとに、図5に示す各判定の領域を参照して、各試薬(検査項目)の測光パラメータが陰性であるか否かを判断する。つまり、分析部33は、測光パラメータSPCにおいて、得られた測光パラメータSPCの値が、陽性判定基準値(Low)である10未満の場合は判定結果を陽性と判断し、陰性判定基準値(High)である20を越えた場合は陰性と判断する。また、測光パラメータSPCの値が10〜20の場合は判定不能(図5、?)であると判断する。
【0039】
一方、分析部33は、測光パラメータP/Cにおいて、得られた測光パラメータP/Cの値が、陽性判定基準値30未満の場合は陽性と判断し、陰性判定基準値20を超えた場合は陰性と判断する。また、測光パラメータP/Cの値が、両判定基準値にはさまれた20〜30の場合は陽性とも陰性とも判定可能であり(図5、+or−)、他の測光パラメータの判定結果から試薬判定結果を決定する。測光パラメータLIAはP/Cと同様、測光パラメータLIAの値が、陽性判定基準値400未満の場合は陽性と判断され、陰性判定基準値100を超えた場合は陰性と判断され、両判定基準値にはさまれた100〜400の場合は陽性とも陰性とも判定可能であり(図5、+or−)、他の測光パラメータの判定結果から試薬判定結果を決定する。なお、各測光パラメータの定性判定用閾値の設定および試薬判定方法は、上記に限定されるものではない。
【0040】
分析部33は、試薬に対応する各測光パラメータの陰性または陽性を決定した後、SPC,P/C,LIAの各測定パラメータの判定が同一である場合に、その判定が試薬判定結果として決定する。ここで、SPC,P/C,LIAの判定のうち、1つでも判定が異なる場合は、判定不可として試薬判定結果が決定される。なお、各測光パラメータに優先度を設け、優先度の高い測光パラメータの判定を判定結果として試薬判定結果を決定するようにしてもよい。
【0041】
上述した流れで得られた試薬判定結果を用いて、図2,3に示した組み合わせを参照して各項目判定結果が決定される。なお、不規則抗体等、他の試験においても同様の流れで陰性・陽性が決定することができる。
【0042】
つづいて、分注された検体に異物が混入した場合、たとえば、検体中にフィブリンが析出した場合の項目判定結果の有効性について、図6,7,8を参照して説明する。フィブリンは、フィブリノーゲンとして血漿中に溶解し、プロテアーゼおよびカルシウムの作用によってフィブリン・ポリマーを形成し、血液凝固に関わっている。血液分析においては、このフィブリンによる血液の凝固を防止するために抗凝固剤が添加されるが、経時変化によるフィブリンの析出や抗凝固剤の混合不足による血餅が発生し、析出したフィブリンや血餅が反応容器に混入し、撮像されることによって検査結果の誤判定を起こすことがあった。
【0043】
図6は、本発明の実施の形態にかかるフィブリンが混入した場合の各測光パラメータの測定値および判定と、正常時の測光パラメータの測定値および判定とを示す図である。検体は、同一の検体を使用し、一方の検体にフィブリンが混入している状態(分注異常)で反応処理・分析処理を行った。図6に示すように、各試薬(検査項目)に対して、それぞれ測光パラメータの数値が算出され、その数値をもとに陰性または陽性の判定が決定されている。
【0044】
ここで、抗A(抗A抗体)において、フィブリン吸引時の判定と正常分注時の判定が異なっている。このため、本来A型と判定されるべき項目判定が、O型と誤判定され、輸血時等に事故を起こしてしまうおそれがある。これは、本来血球が凝集して陽性と判定されるところを、血餅または析出したフィブリンの像が撮像され、各測光パラメータの算出時に血餅または析出したフィブリンの像を非凝集像として誤認識してしまうために起こる。本実施の形態では、この誤認識を判定し、測定結果の有効性を判断する。
【0045】
有効性の判断は、図6に示す測光レンジを算出し、図7に示す閾値と比較することによって決定される。図7は、本発明の実施の形態にかかる測光レンジと閾値とを示す図である。測光レンジは、同一検体を分析した各試薬の中で陰性と判定された試薬の各測光パラメータの数値から最大値と最小値との差を算出した値である。たとえば、分注異常(フィブリン吸引時)のLIAでは、最大値が抗Aの869、最小値が抗Bの390となり、その差を算出した479が測光値レンジとなる。また、正常分注時のLIAでは、最大値が抗Bの689、最小値がrefの679となり、測光値レンジは10となる。このようにして求められる測光値レンジに対して図7に示す閾値を設けることで、判定に用いられる各パラメータに信頼性があるか否かを判断し、判定が有効性を有するか否かを決定する。
【0046】
図7において、フィブリン吸引時のP/CおよびSPCの測定値レンジがP/Cレンジで11、SPCレンジで6となっている一方、正常時のP/Cレンジ、SPCレンジは、ともに1となっている。また、LIAレンジにおいても、フィブリン吸引時は479と各試薬間で幅広い値をとっているのに対して正常時は10と低い値となっている。この測光値レンジの差に閾値を設けることで、判定の有効性を判断する。なお、閾値は、任意に設定が可能であり、無効と判定すべき閾値を検査項目や検体種によって変更することができる。
【0047】
つぎに、上述した分析処理の流れにについて図8を参照して説明する。図8は、自動分析装置1が行なう分析処理を示すフローチャートである。制御部31は、測光部16から撮像データを取得すると(ステップS102)、分析部33に取得した撮像データから測光パラメータを算出して(ステップS104)、各試薬に対する陰性・陽性判定(ステップS106)およびステップS106の判定結果から項目判定(特性情報)を決定するよう指示する(ステップS108)。
【0048】
項目判定(特性情報)決定後、制御部31は、リファレンスを除く試薬で陰性であると決定された試薬判定があるか否かを確認する(ステップS110)。ここで、陰性であると決定された試薬がある場合(ステップS110:Yes)、制御部31は、抽出部34に対象の測光パラメータを抽出するよう指示する(ステップS112)。測光パラメータを抽出後、制御部31は、抽出された測光パラメータを判定処理部311に出力し、測光値レンジを算出させる(ステップS114)。
【0049】
測光レンジの算出後、判定処理部311は、各測光パラメータの測光値レンジが、閾値未満であるか否か判断する(ステップS116〜120)。まず、判定処理部311は、測光パラメータLIAの測光値レンジ(LIAレンジ)が閾値未満であるか否かを判定する(ステップS116)。ここで、LIAレンジが閾値未満である場合(ステップS116:Yes)、判定処理部311は、ステップS118に移行して測光パラメータP/Cの測光値レンジ(P/Cレンジ)が閾値未満であるか否かを判定する。P/Cレンジにおいても閾値未満である場合(ステップS118:Yes)、判定処理部311は、ステップS120に移行して、測光パラメータSPCの測光値レンジ(SPCレンジ)が閾値未満であるか否かを判定する。SPCレンジが閾値未満である場合(ステップS120:Yes)、判定処理部311は、測光パラメータの各レンジが閾値未満であるため、項目判定は有効であると判定し、制御部31に有効である旨の情報を出力する。制御部31は、有効である旨の情報の入力によってステップS124に移行する。ステップS124において、制御部31は、次の分析対象の測定結果がある場合(ステップS124:Yes)、ステップS102に移行して上述した処理を繰り返し、測定結果がない場合(ステップS124:No)、作業を終了する。
【0050】
一方、ステップS116〜S120のいずれかにおいて各測光値レンジが閾値以上であった場合(ステップS116,S118,S120:No)、判定処理部311は、測光パラメータの数値に異常があると判定し、異常値である旨の判定結果情報を項目判定(特性情報)に付加する(ステップS122)。制御部31は、判定結果情報を付加した旨の情報を受け取ると、ステップS124に移行する。
【0051】
また、ステップS110において、陰性であると決定された試薬判定がない場合(ステップS110:No)、制御部31は、ステップS124に移行する。
【0052】
上述した処理によって、画像データから得られる測光パラメータが有効であるか否かを判定して項目判定(特性情報)の有効性を判断することによって、得られたデータの信頼性を向上させることが可能となる。
【0053】
なお、図8に示すフローチャートは、3つのパラメータLIA,P/C,SPCのうち1つでも閾値を越えるものがあれば異常値と判定されたが、3つのパラメータすべてが閾値を超えた場合に異常であると判定するようにしてもよい。図9は、本発明の実施の形態にかかる分析処理の変形例を示すフローチャートである。
【0054】
図8に示すフローチャートと同様に、制御部31は、測光部16から撮像データを取得すると(ステップS202)、分析部33に取得した撮像データから測光パラメータを算出して(ステップS204)、各試薬に対する陰性・陽性判定(ステップS206)およびステップS206の判定結果から項目判定(特性情報)を決定するよう指示する(ステップS208)。
【0055】
項目判定(特性情報)決定後、制御部31は、リファレンスを除く試薬で陰性であると決定された試薬判定があるか否かを確認する(ステップS210)。ここで、陰性であると決定された試薬判定がある場合(ステップS210:Yes)、制御部31は、抽出部34に対象の測光パラメータを抽出するよう指示する(ステップS212)。測光パラメータを抽出後、制御部31は、抽出された測光パラメータを判定処理部311に出力し、測光値レンジを算出させる(ステップS214)。
【0056】
測光レンジの算出後、判定処理部311は、各測光パラメータの測光値レンジが、閾値以上であるか否か判断する(ステップS216〜220)。まず、判定処理部311は、測光パラメータLIAの測光値レンジ(LIAレンジ)が閾値以上であるか否かを判定する(ステップS216)。ここで、LIAレンジが閾値以上である場合(ステップS216:Yes)、判定処理部311は、ステップS218に移行して測光パラメータP/Cの測光値レンジ(P/Cレンジ)が閾値以上であるか否かを判定する。P/Cレンジにおいても閾値以上である場合(ステップS218:Yes)、判定処理部311は、ステップS220に移行して、測光パラメータSPCの測光値レンジ(SPCレンジ)が閾値以上であるか否かを判定する。SPCレンジが閾値以上である場合(ステップS220:Yes)、判定処理部311は、測光パラメータの各レンジが閾値以上であるため、測光パラメータが異常値であって、項目判定は無効であると判定し、項目判定(特性情報)に異常値である旨の情報を付加して、制御部31に出力する(ステップS222)。制御部31は、無効である旨の情報を受けると、ステップS224に移行する。ステップS224において、制御部31は、次の分析対象の測定結果がある場合(ステップS224:Yes)、ステップS202に移行して上述した処理を繰り返し、測定結果がない場合(ステップS224:No)、作業を終了する。
【0057】
一方、ステップS216〜S220のいずれかにおいて各測光値レンジが閾値未満であった場合(ステップS216,S218,S220:No)、判定処理部311は、測光パラメータの数値は有効であると判定し、測光パラメータが有効である旨の情報を制御部31に出力する。制御部31は、判定結果情報を付加した旨の情報を受け取ると、ステップS224に移行する。また、ステップS210において、陰性であると決定された試薬判定がない場合(ステップS210:No)、制御部31は、ステップS224に移行する。
【0058】
上述した分析処理によって、各測光パラメータの測光値レンジすべてが閾値を越えた場合に異常値であると判定することが可能となる。
【0059】
なお、本実施の形態では、ステップS110,S210において、リファレンスを除く陰性判定結果を検索するとしたが、リファレンスを含めた複数の陰性判定結果があるか否かを検索するようにしてもよい。本来、リファレンスは必ず陰性となるため、リファレンスで陽性と判定された場合は、フィブリンの析出や血餅以外の要因によるものであるため、別途確認が必要である。
【0060】
また、閾値との比較を行なう測光パラメータの順序は、如何なる順序でもよい。検体種または試薬に対する各測光パラメータの性質によって任意に順序の変更が可能である。
【0061】
ここで、測光パラメータが異常値であると判定され、項目判定(特性情報)に異常値である旨の情報が付加された項目判定結果の表示は、出力部32がモニタ等に項目判定結果を表示する際に、対応する項目判定および/または試薬判定および/または測光パラメータ部分を網掛けで表示してもよく、判定にかかる文字および数値の色を変えて表示してもよい。
【0062】
また、測光パラメータが異常であると判定された測光パラメータがある場合に、出力部32がメッセージを表示するようにしてもよい。図10は、本発明の実施の形態にかかるポップアップ画面の一例を示す図である。図10に示すポップアップ画面W1のように、分析情報として検体IDと測定結果が異常である旨のメッセージとを出力部32がモニタ等に表示するようにしてもよい。
【0063】
なお、表示のタイミングは、異常であると判定したときに表示してもよく、操作者が判定結果を確認した際に表示するようにしてもよい。さらに、操作者がメッセージを確認してOKボタンB1を押下した場合に、ポップアップ画面W1を終了するように設定してもよいし、OKボタンB1が押下された場合に、測定結果を確認する画面が自動的に表示されるように設定してもよい。
【0064】
上述した実施の形態にかかる自動分析装置によって、異物の混入によって誤判定された測定結果を的確に抽出して確認することが可能となる。なお、フィブリンの他、検体中(撮像画像中)に異物が混入した場合でも対応できる。本実施の形態にかかる分析処理によれば、撮像画像の変化によって有効か否かの判定が可能なため、測光パラメータの数値を比較することで無効となる測定結果を的確に抽出することができる。
【0065】
ここで、図8,9に示すフローチャートにおいて、閾値と比較する測光パラメータを、異物の混入により最も顕著に測定値が変化する測光パラメータのみ、たとえば、LIAの測光値レンジを閾値と比較するようにしてもよく、任意に選択した2つの測光パラメータ、たとえば、LIAとP/Cとの各測光値レンジを閾値と比較するようにしてもよい。本発明に用いられる測光パラメータは、試薬の特性または検体の性質により任意に選択可能である。
【産業上の利用可能性】
【0066】
以上のように、本発明にかかる自動分析装置は、誤判定された測定結果を抽出する場合に有用であり、特に、画像から分析される分析処理に適している。
【符号の説明】
【0067】
1 自動分析装置
2 測定機構
3 制御機構
10 プレート搬送レーン
11 検体移送部
11a 検体容器
11b 検体ラック
11c 検体読取部
12 検体分注機構
12a,14a アーム
12b,12c プローブ
13 試薬移送部
13a 試薬セット
13b 試薬読取部
14 試薬分注機構
15 反応促進部
16 測光部
17 プレート回収部
20 マイクロプレート
31 制御部
311 判定処理部
32 出力部
33 分析部
34 抽出部
35 送受信部
36 入力部
37 記憶部
【特許請求の範囲】
【請求項1】
血液を含む検体と試薬とを分注して反応させる反応容器を複数有する基板を用いて、各反応容器内を撮像し、該反応容器内の反応の有無をもとに検体の分析を行う自動分析装置において、
複数の検査項目にそれぞれ対応する複数の反応容器内を撮像して得られた複数の撮像画像を用いて各画像の測光パラメータを算出し、前記測光パラメータをもとに、前記反応容器内で反応がない場合を陰性として、前記撮像画像による測定結果が陰性であるか否かを検査項目ごとに判断し、検体の特性情報を分析する分析部と、
前記検体の特性情報と前記測定結果とを対応付けて記憶する記憶部と、
前記分析部が陰性であると判断した前記測定結果の前記測光パラメータを抽出する抽出部と、
前記抽出部が抽出した前記測光パラメータの最大値と最小値との差を算出し、該算出した差を用いて前記測定結果が有効であるか否かを判定し、該判定の結果を対応する前記検体の特性情報に付加する判定処理部と、
を備えたことを特徴とする自動分析装置。
【請求項2】
前記測光パラメータは、P/C、SPCおよびLIAからなる群から少なくとも2つ選択され、
前記判定処理部は、前記測光パラメータのうち少なくとも1つの測光パラメータの前記差が所定範囲外である場合に、前記測定結果が無効であると判定することを特徴とする請求項1に記載の自動分析装置。
【請求項3】
前記測光パラメータは、P/C、SPCおよびLIAからなる群から少なくとも1つ選択され、
前記判定処理部は、全ての測光パラメータの前記差が所定範囲外である場合に、前記測定結果が無効であると判定することを特徴とする請求項1に記載の自動分析装置。
【請求項4】
前記複数の検査項目に応じて使用する試薬のうちの1つは、必ず陰性を示す参照試薬であることを特徴とする請求項1〜3のいずれか一つに記載の自動分析装置。
【請求項5】
前記判定処理部によって前記測定結果が無効であると判定された場合に、当該測定結果が無効である旨を出力する出力部をさらに備えたことを特徴とする請求項1〜4のいずれか一つに記載の自動分析装置。
【請求項1】
血液を含む検体と試薬とを分注して反応させる反応容器を複数有する基板を用いて、各反応容器内を撮像し、該反応容器内の反応の有無をもとに検体の分析を行う自動分析装置において、
複数の検査項目にそれぞれ対応する複数の反応容器内を撮像して得られた複数の撮像画像を用いて各画像の測光パラメータを算出し、前記測光パラメータをもとに、前記反応容器内で反応がない場合を陰性として、前記撮像画像による測定結果が陰性であるか否かを検査項目ごとに判断し、検体の特性情報を分析する分析部と、
前記検体の特性情報と前記測定結果とを対応付けて記憶する記憶部と、
前記分析部が陰性であると判断した前記測定結果の前記測光パラメータを抽出する抽出部と、
前記抽出部が抽出した前記測光パラメータの最大値と最小値との差を算出し、該算出した差を用いて前記測定結果が有効であるか否かを判定し、該判定の結果を対応する前記検体の特性情報に付加する判定処理部と、
を備えたことを特徴とする自動分析装置。
【請求項2】
前記測光パラメータは、P/C、SPCおよびLIAからなる群から少なくとも2つ選択され、
前記判定処理部は、前記測光パラメータのうち少なくとも1つの測光パラメータの前記差が所定範囲外である場合に、前記測定結果が無効であると判定することを特徴とする請求項1に記載の自動分析装置。
【請求項3】
前記測光パラメータは、P/C、SPCおよびLIAからなる群から少なくとも1つ選択され、
前記判定処理部は、全ての測光パラメータの前記差が所定範囲外である場合に、前記測定結果が無効であると判定することを特徴とする請求項1に記載の自動分析装置。
【請求項4】
前記複数の検査項目に応じて使用する試薬のうちの1つは、必ず陰性を示す参照試薬であることを特徴とする請求項1〜3のいずれか一つに記載の自動分析装置。
【請求項5】
前記判定処理部によって前記測定結果が無効であると判定された場合に、当該測定結果が無効である旨を出力する出力部をさらに備えたことを特徴とする請求項1〜4のいずれか一つに記載の自動分析装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【公開番号】特開2011−112501(P2011−112501A)
【公開日】平成23年6月9日(2011.6.9)
【国際特許分類】
【出願番号】特願2009−269039(P2009−269039)
【出願日】平成21年11月26日(2009.11.26)
【出願人】(510005889)ベックマン コールター, インコーポレイテッド (174)
【Fターム(参考)】
【公開日】平成23年6月9日(2011.6.9)
【国際特許分類】
【出願日】平成21年11月26日(2009.11.26)
【出願人】(510005889)ベックマン コールター, インコーポレイテッド (174)
【Fターム(参考)】
[ Back to top ]

