自由エネルギー差予測方法及びシミュレーション装置
【課題】 本発明の課題は、溶媒中での高分子化合物と化合物の結合に関する自由エネルギー差の計算を高速化することを目的とする。
【解決手段】 上記課題は、コンピュータが化合物間の自由エネルギー差を予測する自由エネルギー差予測方法であって、該コンピュータが、記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定し、第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間することを特徴とする自由エネルギー差予測方法により達成される。
【解決手段】 上記課題は、コンピュータが化合物間の自由エネルギー差を予測する自由エネルギー差予測方法であって、該コンピュータが、記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定し、第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間することを特徴とする自由エネルギー差予測方法により達成される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、溶媒中の高分子化合物と候補化合物の結合に関する自由エネルギー差の計算を高速化することに関する。
【背景技術】
【0002】
従来より、分子シミュレーションを用いて分子設計を行うことがなされている。分子シミュレーションの主要な問題はその計算量であり、計算量を効率的に行い高速化する工夫がなされている。
【0003】
例えば、基底関数として少なくとも2階以上の導関数にまで連続なものを採用し、当該レベルにおいて格子点のペア(又は粒子のペア)のいずれかの格子点(又は粒子)も、1段階上位であってより粗いレベルの格子の格子点に重なっている場合には、ひとつ上位レベルでのペアのエネルギーが必ず当該レベルの正しいエネルギー値と一致するようした上位レベルの格子点に対する電荷決定方法等が提案されている。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2007−80044号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
計算機を用いた薬の開発(計算創薬)では、依然として、その計算時間及び計算機資源が実験と比べて高価である。そのため、実験では得られないミクロスコピックな現象の理解を行うためでしかなく、現在、実験に比肩しうるデータを出そうとすると、一試薬あたり320CPUで5日間の計算量が必要であり容易ではないと言った問題がある。
【課題を解決するための手段】
【0006】
開示の技術は、コンピュータが化合物間の自由エネルギー差を予測する自由エネルギー差予測方法であって、該コンピュータが、記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定し、第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間することを特徴とする自由エネルギー差予測方法のように構成される。
【0007】
また、上記課題を解決するための手段として、コンピュータによって実現されるシミュレーション装置、コンピュータに上記処理を実行させるための自由エネルギー差予測プログラム、及び、その自由エネルギー差予測プログラムを記録した記録媒体とすることもできる。
【発明の効果】
【0008】
開示の技術では、溶媒中の高分子化合物と候補化合物の結合に関する自由エネルギー差の計算を高速化することができる。
【図面の簡単な説明】
【0009】
【図1】結合強度を説明するための図である。
【図2】第2エネルギー差を説明するための図である。
【図3】λ間隔の結合強度と計算量との関係を示すグラフ図である。
【図4】微分値を用いて結合強度と計算量との関係を示す図である。
【図5】本実施例に係る、分割した領域毎の計算方法を説明するための図である。
【図6】創薬シミュレータのハードウェア構成を示すブロック図である。
【図7】本実施例に係る創薬シミュレータの機能構成例を示す図である。
【図8】創薬シミュレータによって行われる結合強度を求めるためのシミュレーションを説明するためのフローチャート図である。
【図9】計算精度の対比を示す図である。
【発明を実施するための形態】
【0010】
以下、本発明の実施の形態を図面に基づいて説明する。先ず、標的タンパク質に対する医薬候補化合物の結合強度について、図1及び図2で説明する。標的タンパク質とは、疾患に関与する体内機能物質であり、候補化合物とは標的タンパク質に対して結合の強い化合物であり、結合することによって標的タンパク質の機能が阻害されると考えられ医薬品となりうる化合物である。
【0011】
図1は、結合強度を説明するための図である。図1において、水5内(溶媒中)で標的タンパク質3と候補化合物4とが分離している非結合状態2aと、水5内で標的タンパク質3と候補化合物4とが結合している結合状態2bとが示される。標的タンパク質3と候補化合物4との結合強度ΔGは、非結合状態2aと結合状態2bとの相対自由エネルギー差(以下、単にエネルギー差と言う)で表される。
【0012】
結合強度ΔGは、更に、第1エネルギー差ΔG1と第2エネルギー差ΔG2との加算によって得られる。第1エネルギー差ΔG1は、非結合状態2aと、水5内の候補化合物4が真空6に取り出された状態2cとの部分エネルギー差を示す。第2エネルギー差ΔG2は、結合状態2bと状態2cとの部分エネルギー差を示す。
【0013】
創薬シミュレータ100によって結合強度をシミュレーション(MD:Molecular Dynamics)する医薬品候補は、予め絞り込まれた凡そ100の候補化合物であるが、一つの医薬品候補に対して、第1エネルギー差ΔG1のシミュレーション時間が1日程であるのに対して、第2エネルギー差ΔG2の値が収束するまでのシミュレーション時間は凡そ2週間を要する。
【0014】
図2は、第2エネルギー差を説明するための図である。図2において、λは、0(ゼロ)のときに結合状態2bを示し、1のときに状態2cを示す結合定数である。候補化合物4とその周囲の原子との相互作用の強度を表す指標であり、λが0のときには生来の相互作用であり、λが1のときには、相互作用がない状態を表している。0≦λ≦1の範囲におけるλ0からλnまでのλ間隔でエネルギー差Δg(λi,i+1)kcal/mol(i=0、1、・・・、n−1)を算出し、下記に示すように、合計した値が第2エネルギー差ΔG2となる。
【0015】
【数1】

【0016】
図3は、λ間隔の結合強度と計算量との関係を示すグラフ図である。図3中、横軸にλを示し、左縦軸にはλ間隔のエネルギー差Δg(λi,i+1)を示し、右縦軸には計算量を示す。また、丸印8aが各λ間隔で収束したエネルギー差Δgを示し、破線8bが計算量を示す。
【0017】
図3において、λの値が凡そ0.6より小さい、つまり、結合状態2bに近い場合には、標的タンパク質3と候補化合物4間のエネルギー変化が少なく収束し易いため凡そ1日の計算量で済む。一方、より非結合状態2aに近づいたλの値が凡そ0.7から0.9の領域7では、エネルギー差Δgが大きく変化するため、必要な精度を得るためには緻密にλ間隔をとる必要があり、また、収束時間も要する等により、計算時間が非常に長くなる。
【0018】
そこで、発明者は、図3に示すλ間隔の結合強度に関して、微分値Δg/Δλで結合強度を表すことにより、特異点のない滑らかなプロットを得ることができ、また、λ=1では正確に0になることに着目した。
【0019】
図4は、微分値を用いて結合強度と計算量との関係を示す図である。図4中、横軸にλを示し、左縦軸にはλ間隔のエネルギー差Δgの微分値Δg(λi,i+1)/Δλi,i+1を示し、右縦軸には計算量を示す。
【0020】
図4を参照すると、丸印8'aがλ間隔のエネルギー差Δgの微分値Δg/Δλを示し、特異点のない滑らかなプロットであることが分かる。また、λ=1では正確に0となっている。この微分値0(ゼロ)を超える領域において、計算量が急激に増大することが分かる。この計算量が急激に増大する領域が、計算値が収束し難い領域である。
【0021】
従って、本実施例では、この微分値を用いてλの領域を3つに分け、計算値が収束し難い領域7'の値を前後の領域から予測する。
【0022】
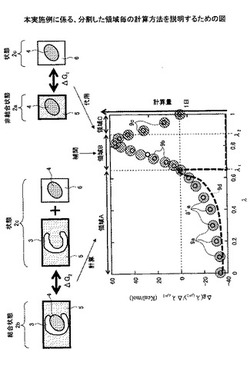
図5は、本実施例に係る、分割した領域毎の計算方法を説明するための図である。図5中、横軸及び縦軸は図4と同様であるのでその説明を省略する。図5において、微分値が0(ゼロ)となるλの値をλ1とし、微分値がピークとなった後に所定値以下となるλの値をλ2とする。本実施例では、λが0からエネルギー差Δgの微分値が0(ゼロ)となるλ1までの領域A(0≦λ≦λ1)と、エネルギー差Δgの微分値が0(ゼロ)より大、かつ、ピーク後に所定値以下となるλ2までの領域B(λ1<λ<λ2)と、エネルギー差Δgの微分値がピーク後に所定値以下となるλ2からλが1までの領域C(λ2≦λ≦1)とに分割する。
【0023】
領域A内では、結合状態2bと状態2c間の第2エネルギー差ΔG2を計算する。領域C内では、予め計算しておいた非結合状態2aと状態2c間の第1エネルギー差ΔG1を代用する。第1エネルギー差ΔG1は、この領域C内において、第2エネルギー差ΔG2と略同様の値を示すからである。領域B内では、領域Aと領域Cの値から3次元スプライン関数等を用いて近似して補間する。
【0024】
本実施例では、最初の候補化合物については全領域を通してλ間隔でシミュレーションを行い、λ間隔のエネルギー差Δgの微分値Δg/Δλを取得する。丸印8'aは、全領域を通してλ間隔でシミュレーションを行った結果(第2エネルギー差ΔG2)を示している。
【0025】
次の候補化合物から、領域A、B、及びCに応じた計算を行う。影付き丸印9aは、領域A内の第2エネルギー差ΔG2を示す。影付き丸印9cは、代用したこの候補化合物の非結合状態2aと状態2c間の第1エネルギー差ΔG1を示す。影付き丸印9bは、領域Aと領域Bの値から3次元スプライン関数等を用いて補間した値を示している。
【0026】
このようにして、標的タンパク質に対する候補化合物の結合強度予測を行う創薬シミュレータは、図6に示すようなハードウェア構成を有する。図6は、創薬シミュレータのハードウェア構成を示すブロック図である。
【0027】
図6において、創薬シミュレータ100は、コンピュータによって制御される端末であって、CPU(Central Processing Unit)11と、メモリユニット12と、表示ユニット13と、出力ユニット14と、入力ユニット15と、通信ユニット16と、記憶装置17と、ドライバ18とを有し 、システムバスBに接続される。
【0028】
CPU11は、メモリユニット12に格納されたプログラムに従って創薬シミュレータ100を制御する。メモリユニット12には、RAM(Random Access Memory)及びROM(Read-Only Memory)等が用いられ、CPU11にて実行されるプログラム、CPU11での処理に必要なデータ、CPU11での処理にて得られたデータ等を格納する。また、メモリユニット12の一部の領域が、CPU11での処理に利用されるワークエリアとして割り付けられている。
【0029】
表示ユニット13は、CPU11の制御のもとに必要な各種情報を表示する。出力ユニット14は、プリンタ等を有し、利用者からの指示に応じて各種情報を出力するために用いられる。入力ユニット15は、マウス、キーボード等を有し、利用者が創薬シミュレータ100が処理を行なうための必要な各種情報を入力するために用いられる。通信ユニット16は、例えばインターネット、LAN(Local Area Network)等に接続し、外部装置との間の通信制御をするための装置である。記憶装置17には、例えば、ハードディスクユニットが用いられ、各種処理を実行するプログラム等のデータを格納する。
【0030】
創薬シミュレータ100によって行われる処理を実現するプログラムは、例えば、CD−ROM(Compact Disc Read-Only Memory)等の記憶媒体19によって創薬シミュレータ100に提供される。即ち、プログラムが保存された記憶媒体19がドライバ18にセットされると、ドライバ18が記憶媒体19からプログラムを読み出し、その読み出されたプログラムがシステムバスBを介して記憶装置17にインストールされる。そして、プログラムが起動されると、記憶装置17にインストールされたプログラムに従ってCPU11がその処理を開始する。尚、プログラムを格納する媒体としてCD−ROMに限定するものではなく、コンピュータが読み取り可能な媒体であればよい。コンピュータ読取可能な記憶媒体として、CD−ROMの他に、DVDディスク、USBメモリ等の可搬型記録媒体、フラッシュメモリ等の半導体メモリであっても良い。
【0031】
また、創薬シミュレータ100によって行われる処理を実現するプログラムが、通信ユニット16を介して外部装置から提供されてもよい。
【0032】
本実施例に係る創薬シミュレータ100は、図7に示すような機能構成を有する。図7は、本実施例に係る創薬シミュレータの機能構成例を示す図である。図7において、創薬シミュレータ100は、分子構造入力部31と、第1エネルギー差計算部32と、第2エネルギー差計算部33と、領域分割部34と、領域A計算部35と、領域C代用部36と、領域B補間部37と、結合強度計算部38とを有する。各部31〜38は、CPU11が対応するプログラムを実行することによって実現される。
【0033】
また、創薬シミュレータ100は、標的タンパク質データ40と、候補化合物リスト41と、Δg1リスト42と、Δg1微分値リスト42−2と、Δg2リスト43と、Δg2参照値44と、境界λデータ45と、結合強度データ46とを記憶部50に記憶する。記憶部50は、メモリユニット12又は/及び記憶装置17の一部に相当する。
【0034】
分子構造入力部31は、利用者が創薬シミュレータ100へ標的タンパク質及び候補化合物の分子構造を入力すると、標的タンパク質の分子構造を示す標的タンパク質データ40を記憶部50に記憶すると共に、候補化合物の識別情報毎に入力された候補化合物の分子構造を示す候補化合物リスト41を記憶部50に記憶する処理部である。
【0035】
第1エネルギー差計算部32は、候補化合物リスト41を参照して、各候補化合物の分子構造と標的タンパク質データ40で示される標的タンパク質の高分子構造とに基づいて、λ間隔毎に第1エネルギー差Δg1を計算する処理部である。λ間隔毎の第1エネルギー差Δg1は、候補化合物の識別情報に対応させて、記憶部50内のΔg1リスト42に記憶される。
【0036】
第2エネルギー差計算部33は、最初の候補化合物の分子構造と標的タンパク質データ40とに基づいて、領域A、B、Cの全領域に対してλ間隔毎の第2エネルギー差Δg2を計算する処理部である。計算されたλ間隔毎の第2エネルギー差Δg2は、最初の候補化合物の識別情報に対応付けて記憶部50内のΔg2リスト43に格納される。また、第2エネルギー差計算部33は、最初の候補化合物の第2エネルギー差Δg2の微分値をλ間隔毎に計算してΔg2参照値44として記憶部50に記憶する。
【0037】
領域分割部34は、Δg2参照値43を参照して、微分値が0(ゼロ)となるλ1及びλ2を特定し、λ1及びλ2を示す境界λデータ45を記憶部50に記憶する。
【0038】
領域A計算部35は、候補化合物リスト41を参照して得られる最初の候補化合物以外の候補化合物毎の分子構造と標的タンパク質データ40とに基づいて、0≦λ≦λ1の領域Aの第2エネルギー差Δg2を計算する処理部である。計算された第2エネルギー差Δg2は、候補化合物の識別情報に対応付けて領域Aのλ間隔毎に記憶部50内のΔg2リスト43に追加して格納される。また、領域A計算部35は、領域A内の第2エネルギー差Δg2の微分値をλ間隔毎に計算してΔg2微分値リスト43−2に格納する。
【0039】
領域C代用部36は、第1エネルギー差計算部32によって計算された候補化合物と標的タンパク質データ40との領域Cにおける第1エネルギー差Δg1を、Δg1リスト42から取得して代用する処理部である。Δg1リスト42から取得した第1エネルギー差Δg1は、候補化合物の識別情報に対応させて領域Cのλ間隔毎にΔg2リストに追加して格納される。また、領域C代用部36は、領域C内の第1エネルギー差Δg1の微分値をλ間隔毎に計算してΔg1微分値リスト42−2に格納する。
【0040】
領域B補間部37は、Δg2微分値リスト43−2から領域Aのλ間隔毎の第2エネルギー差Δg2の微分値と、Δg1微分値リスト42−2から領域Cのλ間隔毎の第1エネルギー差Δg1の微分値とを参照し、領域B内の第2エネルギー差Δg2の微分値を3次元スプライン関数等を用いて補間する処理部である。領域B補間部37は、領域Bの境界となるλ1とλ2の時の微分値から領域B内を予測して補間する。
【0041】
また、領域B補間部37は、補間した領域B内の第2エネルギー差Δg2の微分値から、領域Bのλ間隔毎に第2エネルギー差Δg2を逆算して(微分値に対応するλ間隔を乗算して)、候補化合物の識別情報に対応付けて領域Bのλ間隔毎に記憶部50内のΔg2リスト43に追加して格納する。
【0042】
結合強度計算部38は、候補化合物毎に、Δg1リスト42を参照してλ間隔毎の第1エネルギー差Δg1の合計値を計算することによって第1エネルギー差ΔG1を求め、また、Δg2リスト43を参照してλ間隔毎の第2エネルギー差Δg2の合計値を計算することによって第2エネルギー差ΔG2を求め、更に、第1エネルギー差ΔG1と第2エネルギー差ΔG2とを合算して結合強度を計算する処理部である。合算することによって求めた結合強度は、候補化合物の識別情報に対応させて結合強度データ46として記憶部50に格納される。候補化合物リスト41の全ての候補化合物に対して結合強度が算出された際には、利用者の要求に応じて、結合強度データ46を結合強度の強さ順等でソートし、表示ユニット13に表示させるようにしてもよい。
【0043】
図8は、創薬シミュレータによって行われる結合強度を求めるためのシミュレーションを説明するためのフローチャート図である。図8において、創薬シミュレータ100内では、第1エネルギー差計算部32は、記憶部50に格納されている標的タンパク質データ40から標的タンパク質の高分子構造を読み込み、候補化合物リスト41から候補化合物の分子構造を1つ読み込み(ステップS11)、λ間隔毎に第1エネルギー差Δg1を計算する(ステップS12)。第1エネルギー差計算部32は、計算したλ間隔毎の第1エネルギー差Δg1を、候補化合物の識別情報に対応させて、記憶部50内のΔg1リスト42に記憶する。
【0044】
そして、最初の候補化合物であるか否かが判断される(ステップS13)。候補化合物リスト41の先頭に格納されている候補化合物であるか否かをチェックすることによって最初の候補化合物であるか否かを判断できる。最初の候補化合物である場合には、第2エネルギー差計算部33が、最初の候補化合物の分子構造と標的タンパク質データ40とに基づいて、領域A、B、Cの全領域に対してλ間隔毎の第2エネルギー差Δg2を計算する(ステップS14)。第2エネルギー差計算部33は、計算したλ間隔毎の第2エネルギー差Δg2を、最初の候補化合物の識別情報に対応付けて記憶部50内のΔg2リスト43に出力する。また、第2エネルギー差計算部33は、最初の候補化合物の全領域における各第2エネルギー差Δg2の微分値を計算して、計算したλ間隔毎の第2エネルギー差Δg2の微分値を示すΔg2参照値44を記憶部50に格納する。
【0045】
次に、領域分割部34は、記憶部50に格納されているΔg2参照値43を参照して、λ間隔毎の第2エネルギー差Δg2の微分値のうち0(ゼロ)となるλ1及びλ2を特定し、λ1及びλ2を示す境界λデータ45を記憶部50に格納する(ステップS15)。
【0046】
一方、ステップS13において、最初の候補化合物でないと判断した場合には、領域A計算部35によって、第1エネルギー差計算部32が候補化合物リスト41から読み込んだ候補化合物の分子構造と標的タンパク質データ40で示される標的タンパク質の高分子構造とに基づいて、領域Aの第2エネルギー差Δg2をλ間隔毎に計算する(ステップS18)。領域A計算部35は、境界λデータ45からλ1を取得して0≦λ≦λ1の領域Aを特定し、特定した領域A内でλ間隔毎に第2エネルギー差Δg2を計算し、候補化合物の識別情報に対応付けて領域Aのλ間隔毎に記憶部50内のΔg2リスト43に追加して格納する。
【0047】
また、領域A計算部35は、領域A内の第2エネルギー差Δg2の微分値をλ間隔毎に計算して領域Aのλ間隔毎に第2エネルギー差Δg2の微分値をΔg2微分値リスト43−2に格納する。
【0048】
次に、領域C代用部36は、第1エネルギー差計算部32によって計算された候補化合物と標的タンパク質データ40との領域Cにおける第1エネルギー差Δg1を、Δg1リスト42から取得して代用する(ステップS19)。領域C代用部36は、境界λデータ45からλ2を取得してλ2≦λ≦1の領域Cを特定し、特定した領域C内でλ間隔毎の第1エネルギー差Δg1をΔg1リスト42から取得する。取得したλ間隔毎の第1エネルギー差Δg1は、候補化合物の識別情報に対応させてΔG2リスト43に格納される。
【0049】
また、領域C代用部36は、Δg1リスト42から取得したλ間隔毎の第1エネルギー差Δg1の微分値を計算して領域Cのλ間隔毎にΔg1微分値リスト42−2に格納する。
【0050】
領域Aと領域Cにおける微分値を取得した後、領域B補間部37は、領域Aのλ1に対応する第2エネルギー差Δg2の微分値を参照し、領域Cのλ2に対応する第2エネルギー差Δg2の微分値を参照することによって、領域B内の第2エネルギー差Δg2の微分値を3次元スプライン関数等を用いて補間する(ステップS20)。
【0051】
領域B補間部37は、補間した領域B内の第2エネルギー差Δg2の微分値から、領域Bのλ間隔毎に第2エネルギー差Δg2を逆算して、候補化合物の識別情報に対応付けて領域Bのλ間隔毎に記憶部50内のΔg2リスト43に追加して格納する。
【0052】
最初の候補化合物に対して全領域で第2エネルギー差Δg2を計算して領域を分割した後、又は、最初の候補化合物以外の候補化合物に対して分割した領域A、B、C毎の処理をした後、結合強度計算部38は、Δg1リスト42を参照してλ間隔毎の第1エネルギー差Δg1の合計値を計算することによって第1エネルギー差ΔG1を求め、また、Δg2リスト43を参照してλ間隔毎の第2エネルギー差Δg2の合計値を計算することによって第2エネルギー差ΔG2を求め、更に、第1エネルギー差ΔG1と第2エネルギー差ΔG2とを合算して結合強度を計算する(ステップS16)。結合強度計算部38は、求めた結合強度を候補化合物の識別情報に対応させて記憶部50内の結合強度データ46に追加して格納する。
【0053】
そして、候補化合物リスト41の全ての候補化合物に対して処理を終了したか否かを判断する(ステップS17)。終了した場合、創薬シミュレータ100による結合強度を求めるためのシミュレーションを終了する。
【0054】
ステップS17において、全ての候補化合物に対して処理を終了していないと判断した場合、創薬シミュレータ100は、候補化合物リスト41の次の候補化合物の結合強度を求めるためにステップS11へ戻る。
【0055】
上述したように、本実施例に係る創薬シミュレータ100では、最初の候補化合物以外の候補化合物に対しては、ステップS18、S19、及びS20での処理60を行うため、全ての候補化合物に対して処理負荷の大きいλ間隔毎の第2エネルギー差Δg2を計算することがないため、シミュレーション処理に要する時間を大幅に短縮することができる。
【0056】
例えば、100個の候補化合物が処理対象であった場合、最初の候補化合物に対しては、ステップS14での全領域に対してλ間隔毎の第2エネルギー差Δg2を計算するものの、残り99の候補化合物に対しては、処理60における領域毎の対応となる。従って、図5の破線9dで例示されるように、領域B及び領域Cに対してλ間隔毎の第2エネルギー差Δg2を計算するシミュレーションを不要とすることができる。
【0057】
本実施例が適用されない(ステップS15及び処理60が無い)場合には、一つの候補化合物に対して凡そ1日を要するステップS12によるλ間隔毎の第1エネルギー差Δg1を計算するためのシミュレーションを100通り行うと、
1日×100通り= 100日
必要となる。また、一つの候補化合物に対して凡そ15日を要するステップS14によるλ間隔毎の第2エネルギー差Δg2を計算するためのシミュレーションを100通り行うと、
15日×100通り=1500日
必要となる。従って、合計(100日+1500日)で1600日を要する。
【0058】
一方、本実施例が適用された(ステップS15及び処理60を含めて実行した)場合には、ステップS12によるシミュレーションの所要日数は100日と同様であるが、ステップS14によるシミュレーションは、最初の候補化合物のみであるので、
15日× 1通り= 15日
となり、凡そ1日を要する処理60は残りの99個の候補化合物に対して行われ、
1日× 99通り= 99日
必要となる。従って、合計(100日+15日+99日)で214日を要する。本実施例が適用されない場合と比べて、大幅に処理日数を削減できることが分かる。
【0059】
図9は、計算精度の対比を示す図である。図9では、標的タンパク質と候補化合物間との各候補化合物A、B、C、及びDについて、実験値、本実施例が適用されていない場合の計算値A、及び本実施例を適用した場合の計算値Bを示している。結合強度は、相対自由エネルギー差(kcal/mol)で表される。
【0060】
実験値と計算値Aとの相関係数Rは0.95であったのに対して、実験値と本実施例を適用した場合の計算値Bとの相関係数Rは0.98となり、より精度が改善していることが分かる。本実施例に係る創薬シミュレータ100によるシミュレーションによって、溶媒中の標的タンパク質と薬剤候補化合物との自由エネルギー差計算を高速化することができる。また、他の高分子化合物と候補化合物との自由エネルギー差計算においても同様に高速化が可能である。
【0061】
上述したように、本実施例によれば、結合定数λをパラメータにして2つの状態(非結合状態2a及び結合状態2b)を定義し、2つの状態間の自由エネルギー差を各Δλi間のΔGiの和として求める際に、計算値の収束の遅い領域(領域B)を3次元スプライン関数で補間する。従って、処理日数を削減すると共に、計算精度をより改善させることができる。
【0062】
本実施例は、タンパク質、DNA(Deoxyribo Nucleic Acid)、RNA(Ribo Nucleic Acid)、有機化合物などが溶媒中で相互に非共有結合を行う場合の自由エネルギー差をシミュレーションで予測するために必要な計算機資源を減少させることができる。
【0063】
本発明は、具体的に開示された実施例に限定されるものではなく、特許請求の範囲から逸脱することなく、種々の変形や変更が可能である。
【0064】
以上の実施例を含む実施形態に関し、更に以下の付記を開示する。
(付記1)
コンピュータが化合物間の自由エネルギー差を予測する自由エネルギー差予測方法であって、該コンピュータが、
記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域(領域B)を特定し、
第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する
ことを特徴とする自由エネルギー差予測方法。
(付記2)
前記コンピュータが、
前記変化領域の前領域において、前記結合定数の値毎に前記結合状態に係る部分自由エネルギー差を計算し、
前記記憶部に格納される、前記結合定数の値毎に前記第2候補化合物の溶媒中からの分離に係る部分自由エネルギー差を参照することによって、前記変化領域の後領域に対して、該溶媒中からの分離に係る部分自由エネルギー差を代用する
ことを特徴とする付記1記載の自由エネルギー差予測方法。
(付記3)
前記コンピュータが、
前記記憶部に格納される前記溶媒中からの分離に係る部分自由エネルギー差を参照して該部分自由エネルギー差の合算値を計算し、前記前領域、前記変化領域、及び前記後領域の前記結合状態に係る部分自由エネルギー差の合算値を計算し、該2つの合算値を加算することによって、前記標的化合物と前記第2候補化合物間の相対自由エネルギー差を計算することを特徴とする付記2記載の自由エネルギー差予測方法。
(付記4)
前記コンピュータが、前記前後領域について求めた前記部分自由エネルギー差の微分値に基づいて、前記近似関数を用いて前記変化領域の前記結合状態に係る部分自由エネルギー差を補間し、該補間した微分値から逆算することによって該変化領域の前記結合状態に係る部分自由エネルギー差を求めることを特徴とする付記1乃至3のいずれか一項記載の自由エネルギー差予測方法。
(付記5)
化合物間の自由エネルギー差を予測するシミュレーション装置であって、
標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を記憶した記憶部と、
前記記憶部に格納される前記部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定する特定手段と、
第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する補間手段と
を有することを特徴とするシミュレーション装置。
(付記6)
記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域(領域B)を特定し、
前記第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する、
処理をコンピュータに実行させることを特徴とする自由エネルギー差予測プログラム。
(付記7)
記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定し、
前記第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する、
処理をコンピュータに実行させるための自由エネルギー差予測プログラムを記憶したコンピュータ読取可能な記憶媒体。
【符号の説明】
【0065】
2a 非結合状態
2b 結合状態
2c 状態
3 標的タンパク質
4 候補化合物
5 水
6 真空
11 CPU
12 メモリユニット
13 表示ユニット
14 出力ユニット
15 入力ユニット
16 通信ユニット
17 記憶装置
18 ドライバ
19 記憶媒体
31 分子構造入力部
32 第1エネルギー差計算部
33 第2エネルギー差計算部
34 領域分割部
35 領域A計算部
36 領域C代用部
37 領域B補間部
38 結合強度計算部
40 標的タンパク質データ
41 候補化合物リスト
42 Δg1リスト
42−2 Δg1微分値リスト
43 Δg2リスト
43−2 Δg2微分値リスト
44 Δg2参照値(微分値)
45 境界λデータ
46 結合強度データ
50 記憶部
100 創薬シミュレータ
【技術分野】
【0001】
本発明は、溶媒中の高分子化合物と候補化合物の結合に関する自由エネルギー差の計算を高速化することに関する。
【背景技術】
【0002】
従来より、分子シミュレーションを用いて分子設計を行うことがなされている。分子シミュレーションの主要な問題はその計算量であり、計算量を効率的に行い高速化する工夫がなされている。
【0003】
例えば、基底関数として少なくとも2階以上の導関数にまで連続なものを採用し、当該レベルにおいて格子点のペア(又は粒子のペア)のいずれかの格子点(又は粒子)も、1段階上位であってより粗いレベルの格子の格子点に重なっている場合には、ひとつ上位レベルでのペアのエネルギーが必ず当該レベルの正しいエネルギー値と一致するようした上位レベルの格子点に対する電荷決定方法等が提案されている。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2007−80044号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
計算機を用いた薬の開発(計算創薬)では、依然として、その計算時間及び計算機資源が実験と比べて高価である。そのため、実験では得られないミクロスコピックな現象の理解を行うためでしかなく、現在、実験に比肩しうるデータを出そうとすると、一試薬あたり320CPUで5日間の計算量が必要であり容易ではないと言った問題がある。
【課題を解決するための手段】
【0006】
開示の技術は、コンピュータが化合物間の自由エネルギー差を予測する自由エネルギー差予測方法であって、該コンピュータが、記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定し、第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間することを特徴とする自由エネルギー差予測方法のように構成される。
【0007】
また、上記課題を解決するための手段として、コンピュータによって実現されるシミュレーション装置、コンピュータに上記処理を実行させるための自由エネルギー差予測プログラム、及び、その自由エネルギー差予測プログラムを記録した記録媒体とすることもできる。
【発明の効果】
【0008】
開示の技術では、溶媒中の高分子化合物と候補化合物の結合に関する自由エネルギー差の計算を高速化することができる。
【図面の簡単な説明】
【0009】
【図1】結合強度を説明するための図である。
【図2】第2エネルギー差を説明するための図である。
【図3】λ間隔の結合強度と計算量との関係を示すグラフ図である。
【図4】微分値を用いて結合強度と計算量との関係を示す図である。
【図5】本実施例に係る、分割した領域毎の計算方法を説明するための図である。
【図6】創薬シミュレータのハードウェア構成を示すブロック図である。
【図7】本実施例に係る創薬シミュレータの機能構成例を示す図である。
【図8】創薬シミュレータによって行われる結合強度を求めるためのシミュレーションを説明するためのフローチャート図である。
【図9】計算精度の対比を示す図である。
【発明を実施するための形態】
【0010】
以下、本発明の実施の形態を図面に基づいて説明する。先ず、標的タンパク質に対する医薬候補化合物の結合強度について、図1及び図2で説明する。標的タンパク質とは、疾患に関与する体内機能物質であり、候補化合物とは標的タンパク質に対して結合の強い化合物であり、結合することによって標的タンパク質の機能が阻害されると考えられ医薬品となりうる化合物である。
【0011】
図1は、結合強度を説明するための図である。図1において、水5内(溶媒中)で標的タンパク質3と候補化合物4とが分離している非結合状態2aと、水5内で標的タンパク質3と候補化合物4とが結合している結合状態2bとが示される。標的タンパク質3と候補化合物4との結合強度ΔGは、非結合状態2aと結合状態2bとの相対自由エネルギー差(以下、単にエネルギー差と言う)で表される。
【0012】
結合強度ΔGは、更に、第1エネルギー差ΔG1と第2エネルギー差ΔG2との加算によって得られる。第1エネルギー差ΔG1は、非結合状態2aと、水5内の候補化合物4が真空6に取り出された状態2cとの部分エネルギー差を示す。第2エネルギー差ΔG2は、結合状態2bと状態2cとの部分エネルギー差を示す。
【0013】
創薬シミュレータ100によって結合強度をシミュレーション(MD:Molecular Dynamics)する医薬品候補は、予め絞り込まれた凡そ100の候補化合物であるが、一つの医薬品候補に対して、第1エネルギー差ΔG1のシミュレーション時間が1日程であるのに対して、第2エネルギー差ΔG2の値が収束するまでのシミュレーション時間は凡そ2週間を要する。
【0014】
図2は、第2エネルギー差を説明するための図である。図2において、λは、0(ゼロ)のときに結合状態2bを示し、1のときに状態2cを示す結合定数である。候補化合物4とその周囲の原子との相互作用の強度を表す指標であり、λが0のときには生来の相互作用であり、λが1のときには、相互作用がない状態を表している。0≦λ≦1の範囲におけるλ0からλnまでのλ間隔でエネルギー差Δg(λi,i+1)kcal/mol(i=0、1、・・・、n−1)を算出し、下記に示すように、合計した値が第2エネルギー差ΔG2となる。
【0015】
【数1】

【0016】
図3は、λ間隔の結合強度と計算量との関係を示すグラフ図である。図3中、横軸にλを示し、左縦軸にはλ間隔のエネルギー差Δg(λi,i+1)を示し、右縦軸には計算量を示す。また、丸印8aが各λ間隔で収束したエネルギー差Δgを示し、破線8bが計算量を示す。
【0017】
図3において、λの値が凡そ0.6より小さい、つまり、結合状態2bに近い場合には、標的タンパク質3と候補化合物4間のエネルギー変化が少なく収束し易いため凡そ1日の計算量で済む。一方、より非結合状態2aに近づいたλの値が凡そ0.7から0.9の領域7では、エネルギー差Δgが大きく変化するため、必要な精度を得るためには緻密にλ間隔をとる必要があり、また、収束時間も要する等により、計算時間が非常に長くなる。
【0018】
そこで、発明者は、図3に示すλ間隔の結合強度に関して、微分値Δg/Δλで結合強度を表すことにより、特異点のない滑らかなプロットを得ることができ、また、λ=1では正確に0になることに着目した。
【0019】
図4は、微分値を用いて結合強度と計算量との関係を示す図である。図4中、横軸にλを示し、左縦軸にはλ間隔のエネルギー差Δgの微分値Δg(λi,i+1)/Δλi,i+1を示し、右縦軸には計算量を示す。
【0020】
図4を参照すると、丸印8'aがλ間隔のエネルギー差Δgの微分値Δg/Δλを示し、特異点のない滑らかなプロットであることが分かる。また、λ=1では正確に0となっている。この微分値0(ゼロ)を超える領域において、計算量が急激に増大することが分かる。この計算量が急激に増大する領域が、計算値が収束し難い領域である。
【0021】
従って、本実施例では、この微分値を用いてλの領域を3つに分け、計算値が収束し難い領域7'の値を前後の領域から予測する。
【0022】
図5は、本実施例に係る、分割した領域毎の計算方法を説明するための図である。図5中、横軸及び縦軸は図4と同様であるのでその説明を省略する。図5において、微分値が0(ゼロ)となるλの値をλ1とし、微分値がピークとなった後に所定値以下となるλの値をλ2とする。本実施例では、λが0からエネルギー差Δgの微分値が0(ゼロ)となるλ1までの領域A(0≦λ≦λ1)と、エネルギー差Δgの微分値が0(ゼロ)より大、かつ、ピーク後に所定値以下となるλ2までの領域B(λ1<λ<λ2)と、エネルギー差Δgの微分値がピーク後に所定値以下となるλ2からλが1までの領域C(λ2≦λ≦1)とに分割する。
【0023】
領域A内では、結合状態2bと状態2c間の第2エネルギー差ΔG2を計算する。領域C内では、予め計算しておいた非結合状態2aと状態2c間の第1エネルギー差ΔG1を代用する。第1エネルギー差ΔG1は、この領域C内において、第2エネルギー差ΔG2と略同様の値を示すからである。領域B内では、領域Aと領域Cの値から3次元スプライン関数等を用いて近似して補間する。
【0024】
本実施例では、最初の候補化合物については全領域を通してλ間隔でシミュレーションを行い、λ間隔のエネルギー差Δgの微分値Δg/Δλを取得する。丸印8'aは、全領域を通してλ間隔でシミュレーションを行った結果(第2エネルギー差ΔG2)を示している。
【0025】
次の候補化合物から、領域A、B、及びCに応じた計算を行う。影付き丸印9aは、領域A内の第2エネルギー差ΔG2を示す。影付き丸印9cは、代用したこの候補化合物の非結合状態2aと状態2c間の第1エネルギー差ΔG1を示す。影付き丸印9bは、領域Aと領域Bの値から3次元スプライン関数等を用いて補間した値を示している。
【0026】
このようにして、標的タンパク質に対する候補化合物の結合強度予測を行う創薬シミュレータは、図6に示すようなハードウェア構成を有する。図6は、創薬シミュレータのハードウェア構成を示すブロック図である。
【0027】
図6において、創薬シミュレータ100は、コンピュータによって制御される端末であって、CPU(Central Processing Unit)11と、メモリユニット12と、表示ユニット13と、出力ユニット14と、入力ユニット15と、通信ユニット16と、記憶装置17と、ドライバ18とを有し 、システムバスBに接続される。
【0028】
CPU11は、メモリユニット12に格納されたプログラムに従って創薬シミュレータ100を制御する。メモリユニット12には、RAM(Random Access Memory)及びROM(Read-Only Memory)等が用いられ、CPU11にて実行されるプログラム、CPU11での処理に必要なデータ、CPU11での処理にて得られたデータ等を格納する。また、メモリユニット12の一部の領域が、CPU11での処理に利用されるワークエリアとして割り付けられている。
【0029】
表示ユニット13は、CPU11の制御のもとに必要な各種情報を表示する。出力ユニット14は、プリンタ等を有し、利用者からの指示に応じて各種情報を出力するために用いられる。入力ユニット15は、マウス、キーボード等を有し、利用者が創薬シミュレータ100が処理を行なうための必要な各種情報を入力するために用いられる。通信ユニット16は、例えばインターネット、LAN(Local Area Network)等に接続し、外部装置との間の通信制御をするための装置である。記憶装置17には、例えば、ハードディスクユニットが用いられ、各種処理を実行するプログラム等のデータを格納する。
【0030】
創薬シミュレータ100によって行われる処理を実現するプログラムは、例えば、CD−ROM(Compact Disc Read-Only Memory)等の記憶媒体19によって創薬シミュレータ100に提供される。即ち、プログラムが保存された記憶媒体19がドライバ18にセットされると、ドライバ18が記憶媒体19からプログラムを読み出し、その読み出されたプログラムがシステムバスBを介して記憶装置17にインストールされる。そして、プログラムが起動されると、記憶装置17にインストールされたプログラムに従ってCPU11がその処理を開始する。尚、プログラムを格納する媒体としてCD−ROMに限定するものではなく、コンピュータが読み取り可能な媒体であればよい。コンピュータ読取可能な記憶媒体として、CD−ROMの他に、DVDディスク、USBメモリ等の可搬型記録媒体、フラッシュメモリ等の半導体メモリであっても良い。
【0031】
また、創薬シミュレータ100によって行われる処理を実現するプログラムが、通信ユニット16を介して外部装置から提供されてもよい。
【0032】
本実施例に係る創薬シミュレータ100は、図7に示すような機能構成を有する。図7は、本実施例に係る創薬シミュレータの機能構成例を示す図である。図7において、創薬シミュレータ100は、分子構造入力部31と、第1エネルギー差計算部32と、第2エネルギー差計算部33と、領域分割部34と、領域A計算部35と、領域C代用部36と、領域B補間部37と、結合強度計算部38とを有する。各部31〜38は、CPU11が対応するプログラムを実行することによって実現される。
【0033】
また、創薬シミュレータ100は、標的タンパク質データ40と、候補化合物リスト41と、Δg1リスト42と、Δg1微分値リスト42−2と、Δg2リスト43と、Δg2参照値44と、境界λデータ45と、結合強度データ46とを記憶部50に記憶する。記憶部50は、メモリユニット12又は/及び記憶装置17の一部に相当する。
【0034】
分子構造入力部31は、利用者が創薬シミュレータ100へ標的タンパク質及び候補化合物の分子構造を入力すると、標的タンパク質の分子構造を示す標的タンパク質データ40を記憶部50に記憶すると共に、候補化合物の識別情報毎に入力された候補化合物の分子構造を示す候補化合物リスト41を記憶部50に記憶する処理部である。
【0035】
第1エネルギー差計算部32は、候補化合物リスト41を参照して、各候補化合物の分子構造と標的タンパク質データ40で示される標的タンパク質の高分子構造とに基づいて、λ間隔毎に第1エネルギー差Δg1を計算する処理部である。λ間隔毎の第1エネルギー差Δg1は、候補化合物の識別情報に対応させて、記憶部50内のΔg1リスト42に記憶される。
【0036】
第2エネルギー差計算部33は、最初の候補化合物の分子構造と標的タンパク質データ40とに基づいて、領域A、B、Cの全領域に対してλ間隔毎の第2エネルギー差Δg2を計算する処理部である。計算されたλ間隔毎の第2エネルギー差Δg2は、最初の候補化合物の識別情報に対応付けて記憶部50内のΔg2リスト43に格納される。また、第2エネルギー差計算部33は、最初の候補化合物の第2エネルギー差Δg2の微分値をλ間隔毎に計算してΔg2参照値44として記憶部50に記憶する。
【0037】
領域分割部34は、Δg2参照値43を参照して、微分値が0(ゼロ)となるλ1及びλ2を特定し、λ1及びλ2を示す境界λデータ45を記憶部50に記憶する。
【0038】
領域A計算部35は、候補化合物リスト41を参照して得られる最初の候補化合物以外の候補化合物毎の分子構造と標的タンパク質データ40とに基づいて、0≦λ≦λ1の領域Aの第2エネルギー差Δg2を計算する処理部である。計算された第2エネルギー差Δg2は、候補化合物の識別情報に対応付けて領域Aのλ間隔毎に記憶部50内のΔg2リスト43に追加して格納される。また、領域A計算部35は、領域A内の第2エネルギー差Δg2の微分値をλ間隔毎に計算してΔg2微分値リスト43−2に格納する。
【0039】
領域C代用部36は、第1エネルギー差計算部32によって計算された候補化合物と標的タンパク質データ40との領域Cにおける第1エネルギー差Δg1を、Δg1リスト42から取得して代用する処理部である。Δg1リスト42から取得した第1エネルギー差Δg1は、候補化合物の識別情報に対応させて領域Cのλ間隔毎にΔg2リストに追加して格納される。また、領域C代用部36は、領域C内の第1エネルギー差Δg1の微分値をλ間隔毎に計算してΔg1微分値リスト42−2に格納する。
【0040】
領域B補間部37は、Δg2微分値リスト43−2から領域Aのλ間隔毎の第2エネルギー差Δg2の微分値と、Δg1微分値リスト42−2から領域Cのλ間隔毎の第1エネルギー差Δg1の微分値とを参照し、領域B内の第2エネルギー差Δg2の微分値を3次元スプライン関数等を用いて補間する処理部である。領域B補間部37は、領域Bの境界となるλ1とλ2の時の微分値から領域B内を予測して補間する。
【0041】
また、領域B補間部37は、補間した領域B内の第2エネルギー差Δg2の微分値から、領域Bのλ間隔毎に第2エネルギー差Δg2を逆算して(微分値に対応するλ間隔を乗算して)、候補化合物の識別情報に対応付けて領域Bのλ間隔毎に記憶部50内のΔg2リスト43に追加して格納する。
【0042】
結合強度計算部38は、候補化合物毎に、Δg1リスト42を参照してλ間隔毎の第1エネルギー差Δg1の合計値を計算することによって第1エネルギー差ΔG1を求め、また、Δg2リスト43を参照してλ間隔毎の第2エネルギー差Δg2の合計値を計算することによって第2エネルギー差ΔG2を求め、更に、第1エネルギー差ΔG1と第2エネルギー差ΔG2とを合算して結合強度を計算する処理部である。合算することによって求めた結合強度は、候補化合物の識別情報に対応させて結合強度データ46として記憶部50に格納される。候補化合物リスト41の全ての候補化合物に対して結合強度が算出された際には、利用者の要求に応じて、結合強度データ46を結合強度の強さ順等でソートし、表示ユニット13に表示させるようにしてもよい。
【0043】
図8は、創薬シミュレータによって行われる結合強度を求めるためのシミュレーションを説明するためのフローチャート図である。図8において、創薬シミュレータ100内では、第1エネルギー差計算部32は、記憶部50に格納されている標的タンパク質データ40から標的タンパク質の高分子構造を読み込み、候補化合物リスト41から候補化合物の分子構造を1つ読み込み(ステップS11)、λ間隔毎に第1エネルギー差Δg1を計算する(ステップS12)。第1エネルギー差計算部32は、計算したλ間隔毎の第1エネルギー差Δg1を、候補化合物の識別情報に対応させて、記憶部50内のΔg1リスト42に記憶する。
【0044】
そして、最初の候補化合物であるか否かが判断される(ステップS13)。候補化合物リスト41の先頭に格納されている候補化合物であるか否かをチェックすることによって最初の候補化合物であるか否かを判断できる。最初の候補化合物である場合には、第2エネルギー差計算部33が、最初の候補化合物の分子構造と標的タンパク質データ40とに基づいて、領域A、B、Cの全領域に対してλ間隔毎の第2エネルギー差Δg2を計算する(ステップS14)。第2エネルギー差計算部33は、計算したλ間隔毎の第2エネルギー差Δg2を、最初の候補化合物の識別情報に対応付けて記憶部50内のΔg2リスト43に出力する。また、第2エネルギー差計算部33は、最初の候補化合物の全領域における各第2エネルギー差Δg2の微分値を計算して、計算したλ間隔毎の第2エネルギー差Δg2の微分値を示すΔg2参照値44を記憶部50に格納する。
【0045】
次に、領域分割部34は、記憶部50に格納されているΔg2参照値43を参照して、λ間隔毎の第2エネルギー差Δg2の微分値のうち0(ゼロ)となるλ1及びλ2を特定し、λ1及びλ2を示す境界λデータ45を記憶部50に格納する(ステップS15)。
【0046】
一方、ステップS13において、最初の候補化合物でないと判断した場合には、領域A計算部35によって、第1エネルギー差計算部32が候補化合物リスト41から読み込んだ候補化合物の分子構造と標的タンパク質データ40で示される標的タンパク質の高分子構造とに基づいて、領域Aの第2エネルギー差Δg2をλ間隔毎に計算する(ステップS18)。領域A計算部35は、境界λデータ45からλ1を取得して0≦λ≦λ1の領域Aを特定し、特定した領域A内でλ間隔毎に第2エネルギー差Δg2を計算し、候補化合物の識別情報に対応付けて領域Aのλ間隔毎に記憶部50内のΔg2リスト43に追加して格納する。
【0047】
また、領域A計算部35は、領域A内の第2エネルギー差Δg2の微分値をλ間隔毎に計算して領域Aのλ間隔毎に第2エネルギー差Δg2の微分値をΔg2微分値リスト43−2に格納する。
【0048】
次に、領域C代用部36は、第1エネルギー差計算部32によって計算された候補化合物と標的タンパク質データ40との領域Cにおける第1エネルギー差Δg1を、Δg1リスト42から取得して代用する(ステップS19)。領域C代用部36は、境界λデータ45からλ2を取得してλ2≦λ≦1の領域Cを特定し、特定した領域C内でλ間隔毎の第1エネルギー差Δg1をΔg1リスト42から取得する。取得したλ間隔毎の第1エネルギー差Δg1は、候補化合物の識別情報に対応させてΔG2リスト43に格納される。
【0049】
また、領域C代用部36は、Δg1リスト42から取得したλ間隔毎の第1エネルギー差Δg1の微分値を計算して領域Cのλ間隔毎にΔg1微分値リスト42−2に格納する。
【0050】
領域Aと領域Cにおける微分値を取得した後、領域B補間部37は、領域Aのλ1に対応する第2エネルギー差Δg2の微分値を参照し、領域Cのλ2に対応する第2エネルギー差Δg2の微分値を参照することによって、領域B内の第2エネルギー差Δg2の微分値を3次元スプライン関数等を用いて補間する(ステップS20)。
【0051】
領域B補間部37は、補間した領域B内の第2エネルギー差Δg2の微分値から、領域Bのλ間隔毎に第2エネルギー差Δg2を逆算して、候補化合物の識別情報に対応付けて領域Bのλ間隔毎に記憶部50内のΔg2リスト43に追加して格納する。
【0052】
最初の候補化合物に対して全領域で第2エネルギー差Δg2を計算して領域を分割した後、又は、最初の候補化合物以外の候補化合物に対して分割した領域A、B、C毎の処理をした後、結合強度計算部38は、Δg1リスト42を参照してλ間隔毎の第1エネルギー差Δg1の合計値を計算することによって第1エネルギー差ΔG1を求め、また、Δg2リスト43を参照してλ間隔毎の第2エネルギー差Δg2の合計値を計算することによって第2エネルギー差ΔG2を求め、更に、第1エネルギー差ΔG1と第2エネルギー差ΔG2とを合算して結合強度を計算する(ステップS16)。結合強度計算部38は、求めた結合強度を候補化合物の識別情報に対応させて記憶部50内の結合強度データ46に追加して格納する。
【0053】
そして、候補化合物リスト41の全ての候補化合物に対して処理を終了したか否かを判断する(ステップS17)。終了した場合、創薬シミュレータ100による結合強度を求めるためのシミュレーションを終了する。
【0054】
ステップS17において、全ての候補化合物に対して処理を終了していないと判断した場合、創薬シミュレータ100は、候補化合物リスト41の次の候補化合物の結合強度を求めるためにステップS11へ戻る。
【0055】
上述したように、本実施例に係る創薬シミュレータ100では、最初の候補化合物以外の候補化合物に対しては、ステップS18、S19、及びS20での処理60を行うため、全ての候補化合物に対して処理負荷の大きいλ間隔毎の第2エネルギー差Δg2を計算することがないため、シミュレーション処理に要する時間を大幅に短縮することができる。
【0056】
例えば、100個の候補化合物が処理対象であった場合、最初の候補化合物に対しては、ステップS14での全領域に対してλ間隔毎の第2エネルギー差Δg2を計算するものの、残り99の候補化合物に対しては、処理60における領域毎の対応となる。従って、図5の破線9dで例示されるように、領域B及び領域Cに対してλ間隔毎の第2エネルギー差Δg2を計算するシミュレーションを不要とすることができる。
【0057】
本実施例が適用されない(ステップS15及び処理60が無い)場合には、一つの候補化合物に対して凡そ1日を要するステップS12によるλ間隔毎の第1エネルギー差Δg1を計算するためのシミュレーションを100通り行うと、
1日×100通り= 100日
必要となる。また、一つの候補化合物に対して凡そ15日を要するステップS14によるλ間隔毎の第2エネルギー差Δg2を計算するためのシミュレーションを100通り行うと、
15日×100通り=1500日
必要となる。従って、合計(100日+1500日)で1600日を要する。
【0058】
一方、本実施例が適用された(ステップS15及び処理60を含めて実行した)場合には、ステップS12によるシミュレーションの所要日数は100日と同様であるが、ステップS14によるシミュレーションは、最初の候補化合物のみであるので、
15日× 1通り= 15日
となり、凡そ1日を要する処理60は残りの99個の候補化合物に対して行われ、
1日× 99通り= 99日
必要となる。従って、合計(100日+15日+99日)で214日を要する。本実施例が適用されない場合と比べて、大幅に処理日数を削減できることが分かる。
【0059】
図9は、計算精度の対比を示す図である。図9では、標的タンパク質と候補化合物間との各候補化合物A、B、C、及びDについて、実験値、本実施例が適用されていない場合の計算値A、及び本実施例を適用した場合の計算値Bを示している。結合強度は、相対自由エネルギー差(kcal/mol)で表される。
【0060】
実験値と計算値Aとの相関係数Rは0.95であったのに対して、実験値と本実施例を適用した場合の計算値Bとの相関係数Rは0.98となり、より精度が改善していることが分かる。本実施例に係る創薬シミュレータ100によるシミュレーションによって、溶媒中の標的タンパク質と薬剤候補化合物との自由エネルギー差計算を高速化することができる。また、他の高分子化合物と候補化合物との自由エネルギー差計算においても同様に高速化が可能である。
【0061】
上述したように、本実施例によれば、結合定数λをパラメータにして2つの状態(非結合状態2a及び結合状態2b)を定義し、2つの状態間の自由エネルギー差を各Δλi間のΔGiの和として求める際に、計算値の収束の遅い領域(領域B)を3次元スプライン関数で補間する。従って、処理日数を削減すると共に、計算精度をより改善させることができる。
【0062】
本実施例は、タンパク質、DNA(Deoxyribo Nucleic Acid)、RNA(Ribo Nucleic Acid)、有機化合物などが溶媒中で相互に非共有結合を行う場合の自由エネルギー差をシミュレーションで予測するために必要な計算機資源を減少させることができる。
【0063】
本発明は、具体的に開示された実施例に限定されるものではなく、特許請求の範囲から逸脱することなく、種々の変形や変更が可能である。
【0064】
以上の実施例を含む実施形態に関し、更に以下の付記を開示する。
(付記1)
コンピュータが化合物間の自由エネルギー差を予測する自由エネルギー差予測方法であって、該コンピュータが、
記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域(領域B)を特定し、
第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する
ことを特徴とする自由エネルギー差予測方法。
(付記2)
前記コンピュータが、
前記変化領域の前領域において、前記結合定数の値毎に前記結合状態に係る部分自由エネルギー差を計算し、
前記記憶部に格納される、前記結合定数の値毎に前記第2候補化合物の溶媒中からの分離に係る部分自由エネルギー差を参照することによって、前記変化領域の後領域に対して、該溶媒中からの分離に係る部分自由エネルギー差を代用する
ことを特徴とする付記1記載の自由エネルギー差予測方法。
(付記3)
前記コンピュータが、
前記記憶部に格納される前記溶媒中からの分離に係る部分自由エネルギー差を参照して該部分自由エネルギー差の合算値を計算し、前記前領域、前記変化領域、及び前記後領域の前記結合状態に係る部分自由エネルギー差の合算値を計算し、該2つの合算値を加算することによって、前記標的化合物と前記第2候補化合物間の相対自由エネルギー差を計算することを特徴とする付記2記載の自由エネルギー差予測方法。
(付記4)
前記コンピュータが、前記前後領域について求めた前記部分自由エネルギー差の微分値に基づいて、前記近似関数を用いて前記変化領域の前記結合状態に係る部分自由エネルギー差を補間し、該補間した微分値から逆算することによって該変化領域の前記結合状態に係る部分自由エネルギー差を求めることを特徴とする付記1乃至3のいずれか一項記載の自由エネルギー差予測方法。
(付記5)
化合物間の自由エネルギー差を予測するシミュレーション装置であって、
標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を記憶した記憶部と、
前記記憶部に格納される前記部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定する特定手段と、
第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する補間手段と
を有することを特徴とするシミュレーション装置。
(付記6)
記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域(領域B)を特定し、
前記第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する、
処理をコンピュータに実行させることを特徴とする自由エネルギー差予測プログラム。
(付記7)
記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定し、
前記第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する、
処理をコンピュータに実行させるための自由エネルギー差予測プログラムを記憶したコンピュータ読取可能な記憶媒体。
【符号の説明】
【0065】
2a 非結合状態
2b 結合状態
2c 状態
3 標的タンパク質
4 候補化合物
5 水
6 真空
11 CPU
12 メモリユニット
13 表示ユニット
14 出力ユニット
15 入力ユニット
16 通信ユニット
17 記憶装置
18 ドライバ
19 記憶媒体
31 分子構造入力部
32 第1エネルギー差計算部
33 第2エネルギー差計算部
34 領域分割部
35 領域A計算部
36 領域C代用部
37 領域B補間部
38 結合強度計算部
40 標的タンパク質データ
41 候補化合物リスト
42 Δg1リスト
42−2 Δg1微分値リスト
43 Δg2リスト
43−2 Δg2微分値リスト
44 Δg2参照値(微分値)
45 境界λデータ
46 結合強度データ
50 記憶部
100 創薬シミュレータ
【特許請求の範囲】
【請求項1】
コンピュータが化合物間の自由エネルギー差を予測する自由エネルギー差予測方法であって、該コンピュータが、
記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定し、
第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する
ことを特徴とする自由エネルギー差予測方法。
【請求項2】
前記コンピュータが、
前記変化領域の前領域において、前記結合定数の値毎に前記結合状態に係る部分自由エネルギー差を計算し、
前記記憶部に格納される、前記結合定数の値毎に前記第2候補化合物の溶媒中からの分離に係る部分自由エネルギー差を参照することによって、前記変化領域の後領域に対して、該溶媒中からの分離に係る部分自由エネルギー差を代用する
ことを特徴とする請求項1記載の自由エネルギー差予測方法。
【請求項3】
前記コンピュータが、
前記記憶部に格納される前記溶媒中からの分離に係る部分自由エネルギー差を参照して該部分自由エネルギー差の合算値を計算し、前記前領域、前記変化領域、及び前記後領域の前記結合状態に係る部分自由エネルギー差の合算値を計算し、該2つの合算値を加算することによって、前記標的化合物と前記第2候補化合物間の相対自由エネルギー差を計算することを特徴とする請求項2記載の自由エネルギー差予測方法。
【請求項4】
前記コンピュータが、前記前後領域について求めた前記部分自由エネルギー差の微分値に基づいて、前記近似関数を用いて前記変化領域の前記結合状態に係る部分自由エネルギー差を補間し、該補間した微分値から逆算することによって該変化領域の前記結合状態に係る部分自由エネルギー差を求めることを特徴とする請求項1乃至3のいずれか一項記載の自由エネルギー差予測方法。
【請求項5】
化合物間の自由エネルギー差を予測するシミュレーション装置であって、
標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を記憶した記憶部と、
前記記憶部に格納される前記部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定する特定手段と、
第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する補間手段と
を有することを特徴とするシミュレーション装置。
【請求項1】
コンピュータが化合物間の自由エネルギー差を予測する自由エネルギー差予測方法であって、該コンピュータが、
記憶部に格納される、標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定し、
第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する
ことを特徴とする自由エネルギー差予測方法。
【請求項2】
前記コンピュータが、
前記変化領域の前領域において、前記結合定数の値毎に前記結合状態に係る部分自由エネルギー差を計算し、
前記記憶部に格納される、前記結合定数の値毎に前記第2候補化合物の溶媒中からの分離に係る部分自由エネルギー差を参照することによって、前記変化領域の後領域に対して、該溶媒中からの分離に係る部分自由エネルギー差を代用する
ことを特徴とする請求項1記載の自由エネルギー差予測方法。
【請求項3】
前記コンピュータが、
前記記憶部に格納される前記溶媒中からの分離に係る部分自由エネルギー差を参照して該部分自由エネルギー差の合算値を計算し、前記前領域、前記変化領域、及び前記後領域の前記結合状態に係る部分自由エネルギー差の合算値を計算し、該2つの合算値を加算することによって、前記標的化合物と前記第2候補化合物間の相対自由エネルギー差を計算することを特徴とする請求項2記載の自由エネルギー差予測方法。
【請求項4】
前記コンピュータが、前記前後領域について求めた前記部分自由エネルギー差の微分値に基づいて、前記近似関数を用いて前記変化領域の前記結合状態に係る部分自由エネルギー差を補間し、該補間した微分値から逆算することによって該変化領域の前記結合状態に係る部分自由エネルギー差を求めることを特徴とする請求項1乃至3のいずれか一項記載の自由エネルギー差予測方法。
【請求項5】
化合物間の自由エネルギー差を予測するシミュレーション装置であって、
標的化合物と該標的化合物と結合する第1候補化合物間の結合状態を指定する結合定数の値毎の部分自由エネルギー差を記憶した記憶部と、
前記記憶部に格納される前記部分自由エネルギー差を参照することによって、前記結合定数の領域から前記部分自由エネルギー差が所定変化値以上となる変化領域を特定する特定手段と、
第2候補化合物の前記変化領域の前記部分自由エネルギー差を、前記前後領域について求めた前記部分自由エネルギー差に基づいて、近似関数を用いて補間する補間手段と
を有することを特徴とするシミュレーション装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2012−190423(P2012−190423A)
【公開日】平成24年10月4日(2012.10.4)
【国際特許分類】
【出願番号】特願2011−55828(P2011−55828)
【出願日】平成23年3月14日(2011.3.14)
【出願人】(000005223)富士通株式会社 (25,993)
【Fターム(参考)】
【公開日】平成24年10月4日(2012.10.4)
【国際特許分類】
【出願日】平成23年3月14日(2011.3.14)
【出願人】(000005223)富士通株式会社 (25,993)
【Fターム(参考)】
[ Back to top ]

