薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法
【課題】目的成分の採取量に個人差が生じず、また、モニタリング場所の材質に左右されることなく目的成分を正確に且つ安全に採取でき、モニタリング場所での薬剤による汚染状態を正確に且つ定量的にモニタリング可能な薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法を提供する。
【解決手段】シート状部材10を用意し、基材100側を上向きして検査対象場所80にシート状部材10を設置するステップと、基材100の表面に検体を捕捉するステップと、捕捉した検体に水又は有機溶媒を加え、この溶液に超音波を付与又は該溶液を振とうさせることにより、検体を前記溶液中に溶解抽出させて抽出液を得るステップと、抽出液中の検体成分を所定の分析手段を用いて分析し、基材に残留する検体の情報を得るステップを含む。
【解決手段】シート状部材10を用意し、基材100側を上向きして検査対象場所80にシート状部材10を設置するステップと、基材100の表面に検体を捕捉するステップと、捕捉した検体に水又は有機溶媒を加え、この溶液に超音波を付与又は該溶液を振とうさせることにより、検体を前記溶液中に溶解抽出させて抽出液を得るステップと、抽出液中の検体成分を所定の分析手段を用いて分析し、基材に残留する検体の情報を得るステップを含む。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法に関する。
【背景技術】
【0002】
薬剤の一種である抗がん剤は、悪性腫瘍(がん)の化学療法に用いられる薬剤である。抗がん剤は、がん細胞内の遺伝子に致命的な障害を及ぼす、或いは細胞分裂を阻害することによりがん細胞に対して効力を発揮する。その反面、抗がん剤は変異原性、催奇形性及び発がん性が証明されているものが多く、正常細胞にも影響を及ぼす。
【0003】
抗がん剤を取り扱う医療従事者には、調製時や投与時及び廃棄の際に抗がん剤を吸入したり、抗がん剤が皮膚に付着したりするリスクがある。また、付着した抗がん剤が手、靴底を媒介して拡散し、医療従事者のみならず病棟全体が汚染される虞がある。特に、抗がん剤の主要な投与剤形である注射剤は、アンプル、バイアルの取り扱い時にエアロゾル粒子の吸入、注射針の誤刺、バイアル、アンプルの汚染表面の接触等の被曝リスクが報告されている。
【0004】
抗がん剤を取り扱う医療従事者を被曝や環境汚染から守るため、日本病院薬剤師会は1991年に抗がん剤の取扱いに関するガイドラインを策定した(2005年、2007年及び2009年に改定。)。このガイドラインには、防護服、マスク及び手袋の着用や、薬剤の調製や投与の手順の改善、安全キャビネットの導入等、医療従事者が日常業務で抗がん剤を取扱う際に、医療従事者自身が被曝しないのはもちろんのこと、医療環境を汚染させないために、日常業務で注意すべきことが述べられている。一方、米国薬局方総則第797章では、抗がん剤による汚染状態を定期的にモニタリングすることを推奨しているが、日本国内においてはまだそのような推奨事項はなく、医療機関ごとに抗がん剤を取扱う環境が異なっているのが現状である。
【0005】
医療従事者自身の被曝や医療環境の汚染を防止するためには、医療従事者の保護対策やガイドラインを遵守する一方で、定期的に抗がん剤による汚染状態のモニタリングを行い、日常業務における抗がん剤の取扱いを継続的に見直すことが肝要である。
【0006】
そこで、従来、一定面積内に残留している抗がん剤の残留量をモニタリングする方法として、拭き取り法(以下、「スワブ法」と称する。)と呼ばれる検査方法が医療機関において実施されている(例えば、非特許文献1参照。)。
【先行技術文献】
【非特許文献】
【0007】
【非特許文献1】株式会社EXコントロールジャパン、“拭き取り検査の方法(抜粋)”、[online]、インターネット<URL: http:// www.exposurecontrol.jp/pdf/inspectingcommissions.pdf>
【発明の概要】
【発明が解決しようとする課題】
【0008】
非特許文献1に記載されているスワブ法を説明する。先ず、70cm×70cmの一定面積の被検面に例えば、水酸化ナトリウム等の薬剤を散布する。次に、綿又はガーゼ等の拭き取り部材で被検面を強く拭き取り、該被検面に付着している抗がん剤を薬剤とともに物理的に採取する。その後、当該拭き取り部材から目的成分の抗がん剤を抽出するために前処理を施し、質量分析法等の所定の分析手段によって測定する。
【0009】
非特許文献1に記載されているスワブ法の一般的な問題点として、拭き取り操作は医療に従事する現場の作業者により実施されることが一般的であり、被検面を拭き取る際、拭き取り部材で被検面を押し付ける強さが検査者によって異なる虞があるため、採取される目的成分の量に個人差が出やすいと言われている。また、拭き取り部材で被検面を拭き取る際、取り扱いに注意すべき水酸化ナトリウム等の薬剤を用いるので安全上好ましくない。
【0010】
他方、抗がん剤による汚染状態をモニタリングするには、抗がん剤の調製や投与にかかわる場所で実施する必要がある。具体的には、薬剤調整室へ搬入するトレー、薬剤調整室入口の床、安全キャビネット前の床面、安全キャビネット内、机、点滴ラインをセットする作業台、該作業台前の床面、病室内の点滴台下の床面、ナースステーション等である。これらの場所の被検面の材質は金属面、コンクリート面、タイル面等、様々である。
【0011】
しかしながら、従来のスワブ法は上述の問題点に加えて、仮に採取場所が同じであっても異なる材質の被検面から拭き取り部材で目的成分を拭き取ろうとすると、目的成分を正確に採取することが困難であり(正味の目的成分を採取できない。)、測定の信頼性に乏しいという問題がある。
【0012】
さらに、スワブ法は、モニタリング場所において過去からの抗がん剤の総蓄積量が把握できるのみであり、ある時点から例えば1週間や1ヶ月間等、検査者が意図する期間内に蓄積した抗がん剤の量がどれだけであるかを把握できない。
【0013】
モニタリング場所の被検面を何らかの方法で清浄化し、一定期間経過後に該被検面に存在している抗がん剤を拭き取ることにより対応することも考えられるが、上述したようにスワブ法は、目的成分が正確に採取することが困難であるという根本的な問題を有するため、ある時点から一定期間経過後の被験面に存在する抗がん剤の量をモニタリングすることは容易ではない。このように、従来のスワブ法は、抗がん剤による汚染状態を定量的にモニタリングするのに適切な方法ではなかった。
【0014】
そこで、本発明者等は、上述のスワブ法の問題を解決すべく鋭意検討を重ねた結果、清浄なシート状部材をモニタリング場所に設置し、表面に付着した抗がん剤を採取することで、検査者によって目的成分の採取量に個人差が生じず、また、モニタリング場所の環境や条件に左右されることなく目的成分を正確に且つ安全に採取できることを知見した。そして、採取された抗がん剤を所定の分析手段を用いて分析して該抗がん剤の情報を得ることにより、モニタリング場所での抗がん剤による汚染状態を正確に且つ定量的にモニタリングできることを見出して本発明に至ったのである。
【0015】
したがって、本発明は、このような問題点を解決することを課題としてなされたものであり、その目的とするところは、目的成分の採取量に個人差が生じず、また、モニタリング場所の材質に左右されることなく目的成分を正確に且つ安全に採取でき、モニタリング場所での薬剤による汚染状態を正確に且つ定量的にモニタリング可能な薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法を提供することにある。また、本発明の他の目的は、ある時点から一定期間経過後に蓄積した薬剤の量を容易にモニタリングできる薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法を提供することである。
【課題を解決するための手段】
【0016】
本発明の薬剤の汚染状態検査具は、シート状部材と、開口部から収容物を内部に収容した後、前記開口部を封止する封止部を備えた検体採取容器とを少なくとも含み、開口を閉じることにより内部を略密閉状態とする鞄内にこれらを収容してなる。
【0017】
本発明の薬剤の汚染状態検査具を用いた薬剤の汚染状態検査方法は、シート状部材を用意し、検査対象場所に当該シート状部材を設置するステップと、シート状部材の表面に検体を捕捉するステップと、基材の表面に検体を捕捉するステップと、捕捉した検体に水又は有機溶媒を加え、この溶液に超音波を付与又は該溶液を振とうさせることにより、検体を前記溶液中に溶解抽出させて抽出液を得るステップと、抽出液中の検体成分を所定の分析手段を用いて分析し、基材に残留する検体の情報を得るステップを含んでいる。
【発明の効果】
【0018】
本発明によれば、目的成分の採取量に個人差が生じず、また、モニタリング場所の環境や条件に左右されることなく目的成分を正確に且つ安全に採取でき、モニタリング場所での薬剤による汚染状態を正確に且つ定量的にモニタリング可能な薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法を提供することができるという効果を奏する。また、本発明は、ある時点から一定期間経過後に蓄積した薬剤の量を容易にモニタリングできるという効果を奏する。
【図面の簡単な説明】
【0019】
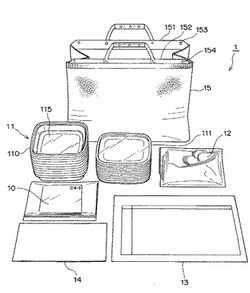
【図1】本実施の形態に係る検査キットの全体を示した斜視図である。
【図2】透明樹脂シートを説明する平面図である。
【図3】透明樹脂シートから剥離フィルムを剥がす状態を説明する斜視図である。
【図4】透明樹脂シートを所定の場所に設置(貼り付けた)した状態を示す斜視図である。
【図5】検体を採取した透明樹脂シート収容容器に収容する状態を説明する斜視図である。
【図6】検体を採取した透明樹脂シート収容容器に密閉収容した状態を説明する斜視図である。
【図7】記録用紙を示した平面図である。
【図8】検体(収容容器に収容)を検査部門に配送する状態を示した斜視図である。
【図9】検査キットを用いたモニタリング実験の実験結果を示した平面図である。
【発明を実施するための形態】
【0020】
以下、本発明の実施の形態に係る薬剤の汚染状態検査具(以下、単に「検査キット」と称する。)、及び該検査キットを用いた薬剤の汚染状態検査方法について、添付図面に従って説明する。なお、以下の説明では、方向や位置を表す用語(例えば、「表面」、「裏面」、「上部」、「下部」等)を便宜上用いるが、これらは発明の理解を容易にするためであり、それらの用語の意味によって本発明の技術的範囲が限定されるものではない。また、以下の説明は、本質的に例示に過ぎず、本発明、その適用物或いはその用途を制限することを意図するものではない。
【0021】
なお、本発明の「薬剤」の概念は、誤った投与、被曝や環境汚染により人体の健康状態を阻害し、死亡を含む深刻な影響をもたらし得る化学物質を含む。具体的には、国際がん研究機構(IARC:International Agency for Research on Cancer)がGroup1(ヒトに対する発がん性が認められる。)、Group2A(ヒトに対する発がん性が恐らくある。)、Group2B(ヒトに対する発がん性が疑われる。)に分類している化学物質のほか、麻薬、覚せい剤、向精神薬等の法規制薬物、例えばジクロロジフェニルトリクロロエタン(DDT)等の殺虫剤や、殺菌剤、殺鼠剤、除草剤、忌避剤、誘引剤等の農薬である。
【0022】
上述の薬剤のうち、Group1に属する化学物質としては、シクロホスファミド、メルファラン、タモキシフェン、エトポシドとシスプラチンとブレオマイシンの併用剤、ホルムアルデヒド等が含まれる。Group2Aに属する化学物質としては、シスプラチン、エトポシド、ロムスチン、アドリアマイシン等が含まれる。Group2Bに属する化学物質としては、ブレオマイシン、ダウノマイシン、メチルチオウラシル、マイトマイシンC、プロピルチオウラシル、ナフタレン等が含まれる。その他、上記Group1、2A及び2Bに属さない抗がん剤のイホスファミドも含まれる。なお、以下の実施の形態では、薬剤のうち、シクロホスファミド及びイホスファミドの抗がん剤を例示して説明する。
【0023】
[検査キット]
図1に示すように、本実施の形態の検査キット1は、透明樹脂シート(シート状部材)10と、収容容器(検体採取容器)11と、手袋12と、記録用紙13と、宅配便送り状14のほか、図示しない検体採取方法説明書を含む。透明樹脂シート10、収容容器11及び手袋12は例えば、各10セットずつ用意されている。そして、これらが運搬用の鞄15に収納されている。
【0024】
透明樹脂シート10は、抗がん剤の調製や投与にかかわる場所において抗がん剤の汚染状態をモニタリングするため、当該透明樹脂シート10を所定の場所に設置し、調製や投与を通じてエアロゾルや液滴、或いは粉末となって空気中に拡散した抗がん剤(以下、単に「検体」と称する。)や、飛散した検体が手、靴底等を媒介して拡散したものを清浄な透明樹脂シート10の表面に捕捉するものである。
【0025】
透明樹脂シート10は例えば、10cm×10cmの正方形で、厚みが0.3mmのポリエチレンテレフタレート(Polyethylene terephthalate)の樹脂フィルムで形成されている。図2に示すように、透明樹脂シート10は基材100に粘着層101が積層された二層構造のシート状部材である。粘着層101における基材100側とは反対側の面には、剥離フィルム102が被覆されている。
【0026】
図2(a)に示すように、基材100の表面(非粘着)であって、該基材100の上部右隅位置には、検体を示すサンプルID103が印刷されている。図2(b)示すように、剥離フィルム102には、上部左角の一部がカットされた切欠き104が形成されている。これは、手袋12を着用した検査者が基材100から剥離フィルム102を剥離する作業を円滑にするためである。
【0027】
また、図示するように、サンプルID103と対応する位置であって、剥離フィルム102の上部左隅位置には丸型のシール105が貼り付けられている。これは、基材100と剥離フィルム102を明確に区別することにより、透明樹脂シート10を使用する際に基材100が誤って廃棄されることを防止するためである。
【0028】
本実施の形態の透明樹脂シート10は、基材100の一方の片面に粘着層101を有するものであるが、本発明のシート状部材において、粘着層を有しない基材100のみのシート状部材であってもよいし、また、例えば、第1の基材の両面(表面と裏面)に粘着層を有し、一方の粘着層に剥離フィルムが被覆され、他方の粘着層に第2の基材が被服されている多層構造のシート状部材であってもよい。この多層構造のシート状部材を用いて検体を採取する手順は後述する。また、透明樹脂シート10の形状は正方形に限らず、短辺と長辺を有する矩形状のものや、三角形、四辺形等を含む多角形状のもの、或いは円形状のものであっても構わない。その大きさも設置する場所に応じて適宜変更可能である。
【0029】
また、本実施の形態では、シート状部材としてポリエチレンテレフタレートで形成した透明樹脂シート10を例示しているが、これに限定するものではない。ポリエチレンテレフタレートに代わる材質としては、ポリテトラフルオロエチレン(polytetrafluoroethylene:PTFE)や表面が滑らかに加工されたステンレス製の薄板等が検体を好適に捕捉できることが発明者らの実験で確認されている。しかし、ステンレス製の薄板は曲面の床に設置するには不向きであり、しかも重い。また、ポリテトラフルオロエチレンは腰が強く、曲面の床に設置するのは不向きである。これらのことを考慮すると、本発明のシート状部材としては、重量が軽くて適度な柔軟性を有するポリエチレンテレフタレート製の透明樹脂シートが好適である。なお、本発明のシート状部材は、必ずしも透明である必要はなく、所定の場所に設置したときに視認できるよう着色が施されていてもよい。
【0030】
図1に戻り、収容容器11は、検体を捕捉した透明樹脂シート10を密閉収容するための略箱状の収容容器である。図示するように、収容容器11は、収容物(この場合、透明樹脂シート10)を出し入れするための開口が形成された容器本体110と、該開口を塞ぐように着脱可能に嵌合する蓋体111からなる。容器本体110は例えば、ポリプロピレンで形成され、蓋体111は例えば、スチロール樹脂で形成されている。
【0031】
図5及び図6を参照すると、収容容器11は容器本体110の底部115が平坦に形成されている。この平坦に形成された底部115に透明樹脂シート10を戴置する。また、蓋体111の周縁部には係止片117が形成され、容器本体110の周縁部に該係止片117を係止するための図示しない溝(封止部)が形成されている。これにより、容器本体110に蓋体111を嵌合させた際に係止片117が溝に係合し、容器本体110から蓋体111が外れないようにロックできる。なお、容器本体110から蓋体111を外す場合は、ロック解除機構118を手で摘まんで外方へ引き出すことにより上記溝が破壊され、蓋体111を外すことができる。
【0032】
収容容器11の形態は、底部115に透明樹脂シート10を水平に戴置でき、蓋締めの際に容器本体110から蓋体111が簡単に外れない構造であればどのような形態の収容容器でも十分に目的を達成できる。材質についても、樹脂製に限らず例えば、アルミニウムやステンレス製の収容容器であってもよい。また、例えば、ポリプロピレンからなる透明のシ−ト材を外表面に用いて水が入らないように水封構造の袋状に形成し、開口部から透明樹脂シート10を内部に挿入した後、該開口部を気密的に閉塞するZiploc(登録商標:ジップロック)等のプラスチックファスナ−(封止部)が設けられた収容容器(検体採取容器)であってもよい。
【0033】
手袋12は、検査者の手指に検体が付着するのを防止するとともに検査者の手指の付着物や汗、油等が透明樹脂シート10に付着するのを防止するものである。このため、手袋12は医療従事者用として市販されているものが好ましい。
【0034】
図1及び図7に示すように、記録用紙13は検体の採取に関して必要事項を記録する記録媒体である。具体的には、サンプルIDの番号、透明樹脂シート10を設置した場所(サンプリング場所)、汚染源として対象とする薬剤名、透明樹脂シート10を設置した日付、及び透明樹脂シート10を回収した日付の各項目を表形式にした所謂チェックシートである。
【0035】
図1に戻り、鞄15は例えば、発泡ポリエチレンのシートと、一方の面にアルミ蒸着層を有するプラスチックフィルムとをラミネートした材料を、接着又は縫製により袋状に形成するとともに、該袋の開口の側縁部に一対のマチ部151,152が設けられた公知の保冷バッグである。図示するように、マチ部151には複数の突起153が形成されている。突起153の対向する位置であって、マチ部152には複数の孔154が形成されている。マチ部151,152を突合せるとともに、突起153を孔154に差し込むことで、鞄15が略密閉状態となる。
【0036】
鞄15の形態は、外側から収容物が視認されず、且つ開口を閉じることにより内部が略密閉できるものであればどのような形態の鞄であってもよい。なお、宅配便送り状14については説明を省略する。
【0037】
次に、本実施の形態の検査キットを用いた薬剤の汚染状態検査方法について説明する。
【0038】
[検体の採取]
先ず、検査者は、鞄15から手袋12を取り出し、該手袋12を両手に着用する。次に、図3に示すようにサンプルID103が印刷されている透明樹脂シート10(基材100)の上部右隅位置を指で掴み、もう一方の指で剥離フィルム102の切欠き104を掴んで該剥離フィルム102を基材100から剥ぎ取り、剥ぎ取った剥離フィルム102を廃棄する。
【0039】
続いて、透明樹脂シート10を抗がん剤の調製や投与にかかわる所定の場所80に設置する。具体的には図4に示すように、基材100のサンプルID103が印刷されている側を上向きにして(粘着層101側を下向きにして)所定の場所80に該基材100を直接貼り付ける。なお、上述した多層構造のシート状部材を所定の場所80に設置するときは、剥離フィルムを第1の基材から剥ぎ取り、第2の基材を上向きにして設置面に直接貼り付け、該第2の基材の表面に検体を捕捉する。
【0040】
この所定の場所80は、[発明の概要]でも説明したように、薬剤調整室へ搬入するトレー、薬剤調整室入口の床、安全キャビネット前の床面、安全キャビネット内、机、点滴ラインをセットする作業台、該作業台前の床面、病室内の点滴台下の床面、ナースステーション等である。基材100を貼り付ける面は、金属面、コンクリート面、タイル面等それぞれ材質が異なり、それらの面形状も曲面や凹凸面等、様々であるが、本実施の形態の透明樹脂シート10は、貼り付け場所の材質に制約を受けることなくどのような場所にも容易に貼り付けることができる。
【0041】
所定の場所80への基材100の貼り付けが完了すると、一定期間そのままの状態で放置する。この期間は検査者が意図的に設定する例えば、1週間や1ヶ月間等の一定期間である。つまり、基材100を貼り付けた日から該基材100を回収するまでの期間において基材100の表面に捕捉した検体の量を測定するのである。なお、基材100の貼り付け時に着用した手袋12は廃棄される。
【0042】
検査者は、基材100の上部右隅位置に印刷されているサンプルID103の番号、基材100を貼り付けた場所(サンプリング場所)、汚染源として対象とする薬剤名「シクロホスファミド」、「イホスファミド」の選択、及び基材100を所定の場所80に貼り付けた日付を記録用紙13に記録する(図7参照。)。
【0043】
上記一定期間経過後、検査者は手袋12を両手に着用した後、所定の場所80に貼り付けられている基材100を剥がし、基材100のサンプルID103が印刷されている側を上向きにして(粘着層101側を下向きにして)容器本体110の底部115に該基材100を直接貼り付ける(図5参照。)。続いて、容器本体110に蓋体111を嵌合させて基材100を収容容器11内に密閉収容する(図6参照。)。そして、基材100を所定の場所80から剥がして回収した日付を記録用紙13に記録する(図7参照。)。なお、基材100の回収時に着用した手袋12は廃棄される。
【0044】
なお、上述した多層構造のシート状部材を回収するときは、所定の場所80から第1の基材を剥ぎ取るとともに、該第1の基材から第2の基材を剥がし、該第2の基材を上述したZiploc(登録商標:ジップロック)式のプラスチックファスナ−(封止部)が設けられた収容容器に密閉収容してもよい。
【0045】
上述の作業が終わると、図8に示すように、基材100を密閉収容した収容容器11と記録用紙13を鞄15内に収容した後、該鞄15のマチ部151,152を突合せて鞄15を略密閉状態にし、鞄15の側面に宅配便送り状14を貼り付けてこれを検査部門に配送する。本実施の形態では、検査者が宅配便送り状14を鞄15に貼り付けて該鞄15(検体)を宅配便にて検査部門に配送する例を説明したが、これに限定するものではなく、検査者が鞄15(検体)を検査部門に直接持ち込んでもよい。
【0046】
このように、本実施の形態の検査キット1は、従来技術のように検体を拭き取って採取するのではなく、清浄な基材100の表面に検体を捕捉させるだけであるので、検体を安全に採取できるとともに、検体による汚染状態を正確に把握できる。また、検査者によって採取される目的成分の量にばらつきが生じない。採取される目的成分の量が正確であるため、検査者が意図的に設定した一定期間に拡散した検体の汚染状態も正確に把握できる。
【0047】
[検体の抽出方法と抽出された検体の残留量の分析方法]
ここからは、基材100の表面に付着している検体の抽出方法と、抽出した検体量がどれだけであったかの分析方法について説明する。以下の分析例では、検体としてシクロホスファミドを例示して説明する。
【0048】
なお、以下に説明する検体の抽出方法、及び抽出された検体量の分析方法については、発明者らの事前の実験において、特異性、直線性、検出限界、回収率(真度)が評価され、全ての評価項目において評価基準に適合していることが確認されている。
【0049】
ここで、特異性とは、他の影響を受けないで特異的に、それのみを測定する方法である。直線性とは、一定の濃度範囲において分析対象物(検体)の濃度(含有量)と測定結果が比例関係にあることを示す能力である。検出限界とは、文字どおり分析対象物(検体)の検出可能な最低の量である。回収率(真度)とは、十分多数の試験結果から得られた平均値と承認された標準値との一致の程度のことである。このように、これから説明する検体の抽出方法、及び抽出された検体量の分析方法は、バリデート(妥当性が確認)された方法で実施されている。
【0050】
1.試料溶液の調製
基材100を密閉収容した収容容器11について、ロック解除機構118を手で摘まんで外方へ引き出し、容器本体110から蓋体111を外す(つまり、図5に示した状態にする。)。続いて、この容器本体110に10mLの純水を加えた後、超音波発信器を作動させて該水溶液に超音波振動を5分間付与する。これにより、基材100に付着した検体(シクロホスファミド)が純水に溶解し、均一な試料溶液が得られる。なお、超音波発信器に代えて、例えば卓上振とう器により容器本体110を振とうさせることにより均一な水溶液を得ることもできる。水溶液中にゴミ等の不溶性の物質が含まれている場合は、検体を吸着しない例えば、ポリテトラフルオロエチレン(polytetrafluoroethylene:PTFE)製のフィルタで該水溶液をろ過してもよい。本調製方法は、例えば、粘着層を有しない基材100のみのシート状部材の表面に捕捉した検体、又は多層構造のシート状部材の第2の基材の表面に捕捉した検体を抽出するのに特に好ましい。
【0051】
上述のように本実施の形態に係る検体の抽出は、検体が付着している基材100に純水を加えて水溶液を作り、該水溶液に超音波を付与、又は該水溶液を振とうさせることにより検体が均一に溶解した水溶液を機械的に得るようにしている。このため、検体が均一に溶解した水溶液の抽出に熟練を要することはなく、誰でも簡単に該水溶液の抽出が可能である。
【0052】
上述の検体の抽出方法に代えて、以下のような方法も可能である。先ず、70%エタノール(消毒用エタノール)1mLを湿潤させた3cm×3cmの日局脱脂綿(第1の脱脂綿)と、溶液を湿潤させない3cm×3cmの日局脱脂綿(第2の脱脂綿)を用意し、前者の脱脂綿で検体が付着している基材100の表面を拭き取った後、後者の脱脂綿で再度基材100の表面を拭き取る。次に、拭き取り後の2つの脱脂綿を遠心沈殿管(容器)に入れ、当該遠心沈殿管に9mLの純水を加え、これをミキサーに装着して10分間激しく振り混ぜることにより試料溶液を得る。
【0053】
2.ブランク溶液の調製
未使用の容器本体110の底部115に未使用の基材100を貼り付け、この容器本体110に10mLの純水を加えた後、超音波発信器を作動させて該水溶液に超音波振動を5分間付与することにより、ブランク溶液を得る。なお、超音波発信器に代えて、例えば卓上振とう器により容器本体110を振とうさせることによりブランク溶液を得ることもできる。
【0054】
ブランク溶液の調製についても上述した試料溶液の調製と同様に、70%エタノール(消毒用エタノール)1mLを湿潤させた3cm×3cmの日局脱脂綿と、溶液を湿潤させない3cm×3cmの日局脱脂綿を用意し、前者の脱脂綿で未使用の基材100の表面を拭き取った後、後者の脱脂綿で再度基材100の表面を拭き取る。次に、拭き取り後の2つの脱脂綿を遠心沈殿管に入れ、当該遠心沈殿管に9mLの純水を加え、これをミキサーに装着して10分間激しく振り混ぜることによりブランク溶液を得てもよい。
【0055】
3.標準溶液の調製
シクロホスファミド標準品約22mgを精密に量り、これをメタノールで溶かして正確に200mLとし、シクロホスファミド標準原液とする。シクロホスファミド標準原液2mLを正確に量り、水を加えて正確に200mLとする。この液2.5mLを正確に量り、水を加えて正確に100mLとする。この液2mLを正確に量り、水を加えて正確に100mLとし、標準溶液とする(シクロホスファミド:0.5ng/mL)。
【0056】
4.検体の残留量の分析方法
上述の試料溶液及び標準溶液を5μLにつき、これらを下記の装置条件で高速液体クロマトグラフ質量分析法により試験を行い、それぞれの溶液のシクロホスファミドのピーク面積AT及びASを測定する。高速液体クロマトグラフ質量分析法は、試料の分離分析に優れる高速液体クロマトグラフ(HPLC)と、試料について高感度な分析及び構造解析に優れる質量分析計(MS)を接続した装置を用い、液体クロマトグラフで分離した成分をイオン化して質量分析計に導き、そこで質量レベルで分けて目的成分を検出する分析方法である。本実施の形態では、LC部にUPLC(Ultra Performance LC)を、MS部にタンデム4極型質量分析計を搭載した液体クロマトグラフ・タンデム型質量分析計(LC/MS/MS)を用いている。得られたピーク面積AT及びASを[数1]に代入して検体(シクロホスファミド)の残留量を算出する。
【0057】
[UPLC条件]
装置:ACQUITY UPLC(Waters社製)
カラム:ACQUITY UPLC HSS T3, 1.8μm,内径2.1mm,長さ50mm
カラム温度:40℃
注入量:5μL
サンプルクーラー:10℃
表1にグラジエント条件を示した。
【0058】
[表1]

【0059】
[MS/MS条件]
検出器:ZEVO TQ MS(Waters社製)
イオン化モード:ESI+
測定条件:MRMモード
シクロホスファミドにおける216.13(m/Z)のプレカーサーイオンの分解によって生じる105.86(m/Z)のプロダクトイオンをターゲットとした。
【0060】
[数1]
検体の残留量(ng)=Ws1×P/100×261.09/279.1×AT/AS×1/4,000,000×1,000,000
ここで、Ws1:シクロホスファミド標準品の標取量(mg)
P:含量
261.09/279.1:シクロホスファミド無水物表示量/シクロホスファミド一水和物表示量
1/4,000,000:希釈倍率,1,000,000:単位換算係数(mg→ng)
【0061】
なお、本分析例では、検体としてシクロホスファミドを例示して説明しているが、検体が例えばイホスファミドの場合は、以下のように実施する。先ず、イホスファミドが0.25ng/mの標準溶液を調製する。検体の分析の際は、液体クロマトグラフで分離したイホスファミドの成分をイオン化して質量分析計に導き、イホスファミドにおける216.13(m/Z)のプレカーサーイオンの分解によって生じる91.87(m/Z)のプロダクトイオンをターゲットとしてイホスファミドのピーク面積AT及びASを測定する。そして、得られたピーク面積AT及びASを[数2]に代入して検体(イホスファミド)の残留量を算出する。
【0062】
[数2]
検体の残留量(ng)=Ws2×P/100×AT/AS×1/8,000,000×1,000,000
ここで、Ws2:イホスファミド標準品の標取量(mg)
1/8,000,000:希釈倍率
【0063】
本実施の形態では、基材100の表面から抽出した検体を、液体クロマトグラフ・タンデム型質量分析計(LC/MS/MS)を用いた分析法で実施したが、これに限定するものではない。例えば、高速液体クロマトグラフィ、液体クロマトグラフ質量分析計、ガスクロマトグラフィ、ガスクロマトグラフ−質量分析計、ガスクロマトグラフィ・タンデム型質量分析計、誘導結合プラズマ発光分析装置、誘導結合プラズマ質量分析装置、UV計、蛍光光度計等を用いた各分析法で実施することも可能である。
【0064】
[検査キットを用いたモニタリング実験]
抗がん剤調整室を設置している医療機関に協力を得て、所定の期間(1週間)における当該医療機関の抗がん剤の拡散状況をモニタリングした。その結果を図9に示す。図において「BSC」とは、抗がん剤を調製する際に使用する安全キャビネットである。図示するように、安全キャビネット前の床を含むサンプリング箇所の全てからシクロホスファミドが検出された。
【0065】
[背景技術]でも説明したように、米国薬局方総則第797章では、抗がん剤による汚染状態を定期的にモニタリングすることを推奨している。今後、日本国内でもそれに準拠する形で汚染状態のモニタリングが定期的に実施されると予測する。
【産業上の利用可能性】
【0066】
本発明の薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法は、上述した薬剤による汚染状態モニタリングのほか、例えば、カドミウム、鉛及び水銀等の有害元素による汚染状態のモニタリングにも適用可能である。
【符号の説明】
【0067】
1 検査キット
10 透明樹脂シート(シート状部材)
11 収容容器
12 手袋
13 記録用紙
14 宅配便送り状
15 鞄
100 基材
101 粘着層
102 剥離フィルム
103 サンプルID
104 切欠き
110 容器本体
111 蓋体
115 (容器本体の)底部
【技術分野】
【0001】
本発明は、薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法に関する。
【背景技術】
【0002】
薬剤の一種である抗がん剤は、悪性腫瘍(がん)の化学療法に用いられる薬剤である。抗がん剤は、がん細胞内の遺伝子に致命的な障害を及ぼす、或いは細胞分裂を阻害することによりがん細胞に対して効力を発揮する。その反面、抗がん剤は変異原性、催奇形性及び発がん性が証明されているものが多く、正常細胞にも影響を及ぼす。
【0003】
抗がん剤を取り扱う医療従事者には、調製時や投与時及び廃棄の際に抗がん剤を吸入したり、抗がん剤が皮膚に付着したりするリスクがある。また、付着した抗がん剤が手、靴底を媒介して拡散し、医療従事者のみならず病棟全体が汚染される虞がある。特に、抗がん剤の主要な投与剤形である注射剤は、アンプル、バイアルの取り扱い時にエアロゾル粒子の吸入、注射針の誤刺、バイアル、アンプルの汚染表面の接触等の被曝リスクが報告されている。
【0004】
抗がん剤を取り扱う医療従事者を被曝や環境汚染から守るため、日本病院薬剤師会は1991年に抗がん剤の取扱いに関するガイドラインを策定した(2005年、2007年及び2009年に改定。)。このガイドラインには、防護服、マスク及び手袋の着用や、薬剤の調製や投与の手順の改善、安全キャビネットの導入等、医療従事者が日常業務で抗がん剤を取扱う際に、医療従事者自身が被曝しないのはもちろんのこと、医療環境を汚染させないために、日常業務で注意すべきことが述べられている。一方、米国薬局方総則第797章では、抗がん剤による汚染状態を定期的にモニタリングすることを推奨しているが、日本国内においてはまだそのような推奨事項はなく、医療機関ごとに抗がん剤を取扱う環境が異なっているのが現状である。
【0005】
医療従事者自身の被曝や医療環境の汚染を防止するためには、医療従事者の保護対策やガイドラインを遵守する一方で、定期的に抗がん剤による汚染状態のモニタリングを行い、日常業務における抗がん剤の取扱いを継続的に見直すことが肝要である。
【0006】
そこで、従来、一定面積内に残留している抗がん剤の残留量をモニタリングする方法として、拭き取り法(以下、「スワブ法」と称する。)と呼ばれる検査方法が医療機関において実施されている(例えば、非特許文献1参照。)。
【先行技術文献】
【非特許文献】
【0007】
【非特許文献1】株式会社EXコントロールジャパン、“拭き取り検査の方法(抜粋)”、[online]、インターネット<URL: http:// www.exposurecontrol.jp/pdf/inspectingcommissions.pdf>
【発明の概要】
【発明が解決しようとする課題】
【0008】
非特許文献1に記載されているスワブ法を説明する。先ず、70cm×70cmの一定面積の被検面に例えば、水酸化ナトリウム等の薬剤を散布する。次に、綿又はガーゼ等の拭き取り部材で被検面を強く拭き取り、該被検面に付着している抗がん剤を薬剤とともに物理的に採取する。その後、当該拭き取り部材から目的成分の抗がん剤を抽出するために前処理を施し、質量分析法等の所定の分析手段によって測定する。
【0009】
非特許文献1に記載されているスワブ法の一般的な問題点として、拭き取り操作は医療に従事する現場の作業者により実施されることが一般的であり、被検面を拭き取る際、拭き取り部材で被検面を押し付ける強さが検査者によって異なる虞があるため、採取される目的成分の量に個人差が出やすいと言われている。また、拭き取り部材で被検面を拭き取る際、取り扱いに注意すべき水酸化ナトリウム等の薬剤を用いるので安全上好ましくない。
【0010】
他方、抗がん剤による汚染状態をモニタリングするには、抗がん剤の調製や投与にかかわる場所で実施する必要がある。具体的には、薬剤調整室へ搬入するトレー、薬剤調整室入口の床、安全キャビネット前の床面、安全キャビネット内、机、点滴ラインをセットする作業台、該作業台前の床面、病室内の点滴台下の床面、ナースステーション等である。これらの場所の被検面の材質は金属面、コンクリート面、タイル面等、様々である。
【0011】
しかしながら、従来のスワブ法は上述の問題点に加えて、仮に採取場所が同じであっても異なる材質の被検面から拭き取り部材で目的成分を拭き取ろうとすると、目的成分を正確に採取することが困難であり(正味の目的成分を採取できない。)、測定の信頼性に乏しいという問題がある。
【0012】
さらに、スワブ法は、モニタリング場所において過去からの抗がん剤の総蓄積量が把握できるのみであり、ある時点から例えば1週間や1ヶ月間等、検査者が意図する期間内に蓄積した抗がん剤の量がどれだけであるかを把握できない。
【0013】
モニタリング場所の被検面を何らかの方法で清浄化し、一定期間経過後に該被検面に存在している抗がん剤を拭き取ることにより対応することも考えられるが、上述したようにスワブ法は、目的成分が正確に採取することが困難であるという根本的な問題を有するため、ある時点から一定期間経過後の被験面に存在する抗がん剤の量をモニタリングすることは容易ではない。このように、従来のスワブ法は、抗がん剤による汚染状態を定量的にモニタリングするのに適切な方法ではなかった。
【0014】
そこで、本発明者等は、上述のスワブ法の問題を解決すべく鋭意検討を重ねた結果、清浄なシート状部材をモニタリング場所に設置し、表面に付着した抗がん剤を採取することで、検査者によって目的成分の採取量に個人差が生じず、また、モニタリング場所の環境や条件に左右されることなく目的成分を正確に且つ安全に採取できることを知見した。そして、採取された抗がん剤を所定の分析手段を用いて分析して該抗がん剤の情報を得ることにより、モニタリング場所での抗がん剤による汚染状態を正確に且つ定量的にモニタリングできることを見出して本発明に至ったのである。
【0015】
したがって、本発明は、このような問題点を解決することを課題としてなされたものであり、その目的とするところは、目的成分の採取量に個人差が生じず、また、モニタリング場所の材質に左右されることなく目的成分を正確に且つ安全に採取でき、モニタリング場所での薬剤による汚染状態を正確に且つ定量的にモニタリング可能な薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法を提供することにある。また、本発明の他の目的は、ある時点から一定期間経過後に蓄積した薬剤の量を容易にモニタリングできる薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法を提供することである。
【課題を解決するための手段】
【0016】
本発明の薬剤の汚染状態検査具は、シート状部材と、開口部から収容物を内部に収容した後、前記開口部を封止する封止部を備えた検体採取容器とを少なくとも含み、開口を閉じることにより内部を略密閉状態とする鞄内にこれらを収容してなる。
【0017】
本発明の薬剤の汚染状態検査具を用いた薬剤の汚染状態検査方法は、シート状部材を用意し、検査対象場所に当該シート状部材を設置するステップと、シート状部材の表面に検体を捕捉するステップと、基材の表面に検体を捕捉するステップと、捕捉した検体に水又は有機溶媒を加え、この溶液に超音波を付与又は該溶液を振とうさせることにより、検体を前記溶液中に溶解抽出させて抽出液を得るステップと、抽出液中の検体成分を所定の分析手段を用いて分析し、基材に残留する検体の情報を得るステップを含んでいる。
【発明の効果】
【0018】
本発明によれば、目的成分の採取量に個人差が生じず、また、モニタリング場所の環境や条件に左右されることなく目的成分を正確に且つ安全に採取でき、モニタリング場所での薬剤による汚染状態を正確に且つ定量的にモニタリング可能な薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法を提供することができるという効果を奏する。また、本発明は、ある時点から一定期間経過後に蓄積した薬剤の量を容易にモニタリングできるという効果を奏する。
【図面の簡単な説明】
【0019】
【図1】本実施の形態に係る検査キットの全体を示した斜視図である。
【図2】透明樹脂シートを説明する平面図である。
【図3】透明樹脂シートから剥離フィルムを剥がす状態を説明する斜視図である。
【図4】透明樹脂シートを所定の場所に設置(貼り付けた)した状態を示す斜視図である。
【図5】検体を採取した透明樹脂シート収容容器に収容する状態を説明する斜視図である。
【図6】検体を採取した透明樹脂シート収容容器に密閉収容した状態を説明する斜視図である。
【図7】記録用紙を示した平面図である。
【図8】検体(収容容器に収容)を検査部門に配送する状態を示した斜視図である。
【図9】検査キットを用いたモニタリング実験の実験結果を示した平面図である。
【発明を実施するための形態】
【0020】
以下、本発明の実施の形態に係る薬剤の汚染状態検査具(以下、単に「検査キット」と称する。)、及び該検査キットを用いた薬剤の汚染状態検査方法について、添付図面に従って説明する。なお、以下の説明では、方向や位置を表す用語(例えば、「表面」、「裏面」、「上部」、「下部」等)を便宜上用いるが、これらは発明の理解を容易にするためであり、それらの用語の意味によって本発明の技術的範囲が限定されるものではない。また、以下の説明は、本質的に例示に過ぎず、本発明、その適用物或いはその用途を制限することを意図するものではない。
【0021】
なお、本発明の「薬剤」の概念は、誤った投与、被曝や環境汚染により人体の健康状態を阻害し、死亡を含む深刻な影響をもたらし得る化学物質を含む。具体的には、国際がん研究機構(IARC:International Agency for Research on Cancer)がGroup1(ヒトに対する発がん性が認められる。)、Group2A(ヒトに対する発がん性が恐らくある。)、Group2B(ヒトに対する発がん性が疑われる。)に分類している化学物質のほか、麻薬、覚せい剤、向精神薬等の法規制薬物、例えばジクロロジフェニルトリクロロエタン(DDT)等の殺虫剤や、殺菌剤、殺鼠剤、除草剤、忌避剤、誘引剤等の農薬である。
【0022】
上述の薬剤のうち、Group1に属する化学物質としては、シクロホスファミド、メルファラン、タモキシフェン、エトポシドとシスプラチンとブレオマイシンの併用剤、ホルムアルデヒド等が含まれる。Group2Aに属する化学物質としては、シスプラチン、エトポシド、ロムスチン、アドリアマイシン等が含まれる。Group2Bに属する化学物質としては、ブレオマイシン、ダウノマイシン、メチルチオウラシル、マイトマイシンC、プロピルチオウラシル、ナフタレン等が含まれる。その他、上記Group1、2A及び2Bに属さない抗がん剤のイホスファミドも含まれる。なお、以下の実施の形態では、薬剤のうち、シクロホスファミド及びイホスファミドの抗がん剤を例示して説明する。
【0023】
[検査キット]
図1に示すように、本実施の形態の検査キット1は、透明樹脂シート(シート状部材)10と、収容容器(検体採取容器)11と、手袋12と、記録用紙13と、宅配便送り状14のほか、図示しない検体採取方法説明書を含む。透明樹脂シート10、収容容器11及び手袋12は例えば、各10セットずつ用意されている。そして、これらが運搬用の鞄15に収納されている。
【0024】
透明樹脂シート10は、抗がん剤の調製や投与にかかわる場所において抗がん剤の汚染状態をモニタリングするため、当該透明樹脂シート10を所定の場所に設置し、調製や投与を通じてエアロゾルや液滴、或いは粉末となって空気中に拡散した抗がん剤(以下、単に「検体」と称する。)や、飛散した検体が手、靴底等を媒介して拡散したものを清浄な透明樹脂シート10の表面に捕捉するものである。
【0025】
透明樹脂シート10は例えば、10cm×10cmの正方形で、厚みが0.3mmのポリエチレンテレフタレート(Polyethylene terephthalate)の樹脂フィルムで形成されている。図2に示すように、透明樹脂シート10は基材100に粘着層101が積層された二層構造のシート状部材である。粘着層101における基材100側とは反対側の面には、剥離フィルム102が被覆されている。
【0026】
図2(a)に示すように、基材100の表面(非粘着)であって、該基材100の上部右隅位置には、検体を示すサンプルID103が印刷されている。図2(b)示すように、剥離フィルム102には、上部左角の一部がカットされた切欠き104が形成されている。これは、手袋12を着用した検査者が基材100から剥離フィルム102を剥離する作業を円滑にするためである。
【0027】
また、図示するように、サンプルID103と対応する位置であって、剥離フィルム102の上部左隅位置には丸型のシール105が貼り付けられている。これは、基材100と剥離フィルム102を明確に区別することにより、透明樹脂シート10を使用する際に基材100が誤って廃棄されることを防止するためである。
【0028】
本実施の形態の透明樹脂シート10は、基材100の一方の片面に粘着層101を有するものであるが、本発明のシート状部材において、粘着層を有しない基材100のみのシート状部材であってもよいし、また、例えば、第1の基材の両面(表面と裏面)に粘着層を有し、一方の粘着層に剥離フィルムが被覆され、他方の粘着層に第2の基材が被服されている多層構造のシート状部材であってもよい。この多層構造のシート状部材を用いて検体を採取する手順は後述する。また、透明樹脂シート10の形状は正方形に限らず、短辺と長辺を有する矩形状のものや、三角形、四辺形等を含む多角形状のもの、或いは円形状のものであっても構わない。その大きさも設置する場所に応じて適宜変更可能である。
【0029】
また、本実施の形態では、シート状部材としてポリエチレンテレフタレートで形成した透明樹脂シート10を例示しているが、これに限定するものではない。ポリエチレンテレフタレートに代わる材質としては、ポリテトラフルオロエチレン(polytetrafluoroethylene:PTFE)や表面が滑らかに加工されたステンレス製の薄板等が検体を好適に捕捉できることが発明者らの実験で確認されている。しかし、ステンレス製の薄板は曲面の床に設置するには不向きであり、しかも重い。また、ポリテトラフルオロエチレンは腰が強く、曲面の床に設置するのは不向きである。これらのことを考慮すると、本発明のシート状部材としては、重量が軽くて適度な柔軟性を有するポリエチレンテレフタレート製の透明樹脂シートが好適である。なお、本発明のシート状部材は、必ずしも透明である必要はなく、所定の場所に設置したときに視認できるよう着色が施されていてもよい。
【0030】
図1に戻り、収容容器11は、検体を捕捉した透明樹脂シート10を密閉収容するための略箱状の収容容器である。図示するように、収容容器11は、収容物(この場合、透明樹脂シート10)を出し入れするための開口が形成された容器本体110と、該開口を塞ぐように着脱可能に嵌合する蓋体111からなる。容器本体110は例えば、ポリプロピレンで形成され、蓋体111は例えば、スチロール樹脂で形成されている。
【0031】
図5及び図6を参照すると、収容容器11は容器本体110の底部115が平坦に形成されている。この平坦に形成された底部115に透明樹脂シート10を戴置する。また、蓋体111の周縁部には係止片117が形成され、容器本体110の周縁部に該係止片117を係止するための図示しない溝(封止部)が形成されている。これにより、容器本体110に蓋体111を嵌合させた際に係止片117が溝に係合し、容器本体110から蓋体111が外れないようにロックできる。なお、容器本体110から蓋体111を外す場合は、ロック解除機構118を手で摘まんで外方へ引き出すことにより上記溝が破壊され、蓋体111を外すことができる。
【0032】
収容容器11の形態は、底部115に透明樹脂シート10を水平に戴置でき、蓋締めの際に容器本体110から蓋体111が簡単に外れない構造であればどのような形態の収容容器でも十分に目的を達成できる。材質についても、樹脂製に限らず例えば、アルミニウムやステンレス製の収容容器であってもよい。また、例えば、ポリプロピレンからなる透明のシ−ト材を外表面に用いて水が入らないように水封構造の袋状に形成し、開口部から透明樹脂シート10を内部に挿入した後、該開口部を気密的に閉塞するZiploc(登録商標:ジップロック)等のプラスチックファスナ−(封止部)が設けられた収容容器(検体採取容器)であってもよい。
【0033】
手袋12は、検査者の手指に検体が付着するのを防止するとともに検査者の手指の付着物や汗、油等が透明樹脂シート10に付着するのを防止するものである。このため、手袋12は医療従事者用として市販されているものが好ましい。
【0034】
図1及び図7に示すように、記録用紙13は検体の採取に関して必要事項を記録する記録媒体である。具体的には、サンプルIDの番号、透明樹脂シート10を設置した場所(サンプリング場所)、汚染源として対象とする薬剤名、透明樹脂シート10を設置した日付、及び透明樹脂シート10を回収した日付の各項目を表形式にした所謂チェックシートである。
【0035】
図1に戻り、鞄15は例えば、発泡ポリエチレンのシートと、一方の面にアルミ蒸着層を有するプラスチックフィルムとをラミネートした材料を、接着又は縫製により袋状に形成するとともに、該袋の開口の側縁部に一対のマチ部151,152が設けられた公知の保冷バッグである。図示するように、マチ部151には複数の突起153が形成されている。突起153の対向する位置であって、マチ部152には複数の孔154が形成されている。マチ部151,152を突合せるとともに、突起153を孔154に差し込むことで、鞄15が略密閉状態となる。
【0036】
鞄15の形態は、外側から収容物が視認されず、且つ開口を閉じることにより内部が略密閉できるものであればどのような形態の鞄であってもよい。なお、宅配便送り状14については説明を省略する。
【0037】
次に、本実施の形態の検査キットを用いた薬剤の汚染状態検査方法について説明する。
【0038】
[検体の採取]
先ず、検査者は、鞄15から手袋12を取り出し、該手袋12を両手に着用する。次に、図3に示すようにサンプルID103が印刷されている透明樹脂シート10(基材100)の上部右隅位置を指で掴み、もう一方の指で剥離フィルム102の切欠き104を掴んで該剥離フィルム102を基材100から剥ぎ取り、剥ぎ取った剥離フィルム102を廃棄する。
【0039】
続いて、透明樹脂シート10を抗がん剤の調製や投与にかかわる所定の場所80に設置する。具体的には図4に示すように、基材100のサンプルID103が印刷されている側を上向きにして(粘着層101側を下向きにして)所定の場所80に該基材100を直接貼り付ける。なお、上述した多層構造のシート状部材を所定の場所80に設置するときは、剥離フィルムを第1の基材から剥ぎ取り、第2の基材を上向きにして設置面に直接貼り付け、該第2の基材の表面に検体を捕捉する。
【0040】
この所定の場所80は、[発明の概要]でも説明したように、薬剤調整室へ搬入するトレー、薬剤調整室入口の床、安全キャビネット前の床面、安全キャビネット内、机、点滴ラインをセットする作業台、該作業台前の床面、病室内の点滴台下の床面、ナースステーション等である。基材100を貼り付ける面は、金属面、コンクリート面、タイル面等それぞれ材質が異なり、それらの面形状も曲面や凹凸面等、様々であるが、本実施の形態の透明樹脂シート10は、貼り付け場所の材質に制約を受けることなくどのような場所にも容易に貼り付けることができる。
【0041】
所定の場所80への基材100の貼り付けが完了すると、一定期間そのままの状態で放置する。この期間は検査者が意図的に設定する例えば、1週間や1ヶ月間等の一定期間である。つまり、基材100を貼り付けた日から該基材100を回収するまでの期間において基材100の表面に捕捉した検体の量を測定するのである。なお、基材100の貼り付け時に着用した手袋12は廃棄される。
【0042】
検査者は、基材100の上部右隅位置に印刷されているサンプルID103の番号、基材100を貼り付けた場所(サンプリング場所)、汚染源として対象とする薬剤名「シクロホスファミド」、「イホスファミド」の選択、及び基材100を所定の場所80に貼り付けた日付を記録用紙13に記録する(図7参照。)。
【0043】
上記一定期間経過後、検査者は手袋12を両手に着用した後、所定の場所80に貼り付けられている基材100を剥がし、基材100のサンプルID103が印刷されている側を上向きにして(粘着層101側を下向きにして)容器本体110の底部115に該基材100を直接貼り付ける(図5参照。)。続いて、容器本体110に蓋体111を嵌合させて基材100を収容容器11内に密閉収容する(図6参照。)。そして、基材100を所定の場所80から剥がして回収した日付を記録用紙13に記録する(図7参照。)。なお、基材100の回収時に着用した手袋12は廃棄される。
【0044】
なお、上述した多層構造のシート状部材を回収するときは、所定の場所80から第1の基材を剥ぎ取るとともに、該第1の基材から第2の基材を剥がし、該第2の基材を上述したZiploc(登録商標:ジップロック)式のプラスチックファスナ−(封止部)が設けられた収容容器に密閉収容してもよい。
【0045】
上述の作業が終わると、図8に示すように、基材100を密閉収容した収容容器11と記録用紙13を鞄15内に収容した後、該鞄15のマチ部151,152を突合せて鞄15を略密閉状態にし、鞄15の側面に宅配便送り状14を貼り付けてこれを検査部門に配送する。本実施の形態では、検査者が宅配便送り状14を鞄15に貼り付けて該鞄15(検体)を宅配便にて検査部門に配送する例を説明したが、これに限定するものではなく、検査者が鞄15(検体)を検査部門に直接持ち込んでもよい。
【0046】
このように、本実施の形態の検査キット1は、従来技術のように検体を拭き取って採取するのではなく、清浄な基材100の表面に検体を捕捉させるだけであるので、検体を安全に採取できるとともに、検体による汚染状態を正確に把握できる。また、検査者によって採取される目的成分の量にばらつきが生じない。採取される目的成分の量が正確であるため、検査者が意図的に設定した一定期間に拡散した検体の汚染状態も正確に把握できる。
【0047】
[検体の抽出方法と抽出された検体の残留量の分析方法]
ここからは、基材100の表面に付着している検体の抽出方法と、抽出した検体量がどれだけであったかの分析方法について説明する。以下の分析例では、検体としてシクロホスファミドを例示して説明する。
【0048】
なお、以下に説明する検体の抽出方法、及び抽出された検体量の分析方法については、発明者らの事前の実験において、特異性、直線性、検出限界、回収率(真度)が評価され、全ての評価項目において評価基準に適合していることが確認されている。
【0049】
ここで、特異性とは、他の影響を受けないで特異的に、それのみを測定する方法である。直線性とは、一定の濃度範囲において分析対象物(検体)の濃度(含有量)と測定結果が比例関係にあることを示す能力である。検出限界とは、文字どおり分析対象物(検体)の検出可能な最低の量である。回収率(真度)とは、十分多数の試験結果から得られた平均値と承認された標準値との一致の程度のことである。このように、これから説明する検体の抽出方法、及び抽出された検体量の分析方法は、バリデート(妥当性が確認)された方法で実施されている。
【0050】
1.試料溶液の調製
基材100を密閉収容した収容容器11について、ロック解除機構118を手で摘まんで外方へ引き出し、容器本体110から蓋体111を外す(つまり、図5に示した状態にする。)。続いて、この容器本体110に10mLの純水を加えた後、超音波発信器を作動させて該水溶液に超音波振動を5分間付与する。これにより、基材100に付着した検体(シクロホスファミド)が純水に溶解し、均一な試料溶液が得られる。なお、超音波発信器に代えて、例えば卓上振とう器により容器本体110を振とうさせることにより均一な水溶液を得ることもできる。水溶液中にゴミ等の不溶性の物質が含まれている場合は、検体を吸着しない例えば、ポリテトラフルオロエチレン(polytetrafluoroethylene:PTFE)製のフィルタで該水溶液をろ過してもよい。本調製方法は、例えば、粘着層を有しない基材100のみのシート状部材の表面に捕捉した検体、又は多層構造のシート状部材の第2の基材の表面に捕捉した検体を抽出するのに特に好ましい。
【0051】
上述のように本実施の形態に係る検体の抽出は、検体が付着している基材100に純水を加えて水溶液を作り、該水溶液に超音波を付与、又は該水溶液を振とうさせることにより検体が均一に溶解した水溶液を機械的に得るようにしている。このため、検体が均一に溶解した水溶液の抽出に熟練を要することはなく、誰でも簡単に該水溶液の抽出が可能である。
【0052】
上述の検体の抽出方法に代えて、以下のような方法も可能である。先ず、70%エタノール(消毒用エタノール)1mLを湿潤させた3cm×3cmの日局脱脂綿(第1の脱脂綿)と、溶液を湿潤させない3cm×3cmの日局脱脂綿(第2の脱脂綿)を用意し、前者の脱脂綿で検体が付着している基材100の表面を拭き取った後、後者の脱脂綿で再度基材100の表面を拭き取る。次に、拭き取り後の2つの脱脂綿を遠心沈殿管(容器)に入れ、当該遠心沈殿管に9mLの純水を加え、これをミキサーに装着して10分間激しく振り混ぜることにより試料溶液を得る。
【0053】
2.ブランク溶液の調製
未使用の容器本体110の底部115に未使用の基材100を貼り付け、この容器本体110に10mLの純水を加えた後、超音波発信器を作動させて該水溶液に超音波振動を5分間付与することにより、ブランク溶液を得る。なお、超音波発信器に代えて、例えば卓上振とう器により容器本体110を振とうさせることによりブランク溶液を得ることもできる。
【0054】
ブランク溶液の調製についても上述した試料溶液の調製と同様に、70%エタノール(消毒用エタノール)1mLを湿潤させた3cm×3cmの日局脱脂綿と、溶液を湿潤させない3cm×3cmの日局脱脂綿を用意し、前者の脱脂綿で未使用の基材100の表面を拭き取った後、後者の脱脂綿で再度基材100の表面を拭き取る。次に、拭き取り後の2つの脱脂綿を遠心沈殿管に入れ、当該遠心沈殿管に9mLの純水を加え、これをミキサーに装着して10分間激しく振り混ぜることによりブランク溶液を得てもよい。
【0055】
3.標準溶液の調製
シクロホスファミド標準品約22mgを精密に量り、これをメタノールで溶かして正確に200mLとし、シクロホスファミド標準原液とする。シクロホスファミド標準原液2mLを正確に量り、水を加えて正確に200mLとする。この液2.5mLを正確に量り、水を加えて正確に100mLとする。この液2mLを正確に量り、水を加えて正確に100mLとし、標準溶液とする(シクロホスファミド:0.5ng/mL)。
【0056】
4.検体の残留量の分析方法
上述の試料溶液及び標準溶液を5μLにつき、これらを下記の装置条件で高速液体クロマトグラフ質量分析法により試験を行い、それぞれの溶液のシクロホスファミドのピーク面積AT及びASを測定する。高速液体クロマトグラフ質量分析法は、試料の分離分析に優れる高速液体クロマトグラフ(HPLC)と、試料について高感度な分析及び構造解析に優れる質量分析計(MS)を接続した装置を用い、液体クロマトグラフで分離した成分をイオン化して質量分析計に導き、そこで質量レベルで分けて目的成分を検出する分析方法である。本実施の形態では、LC部にUPLC(Ultra Performance LC)を、MS部にタンデム4極型質量分析計を搭載した液体クロマトグラフ・タンデム型質量分析計(LC/MS/MS)を用いている。得られたピーク面積AT及びASを[数1]に代入して検体(シクロホスファミド)の残留量を算出する。
【0057】
[UPLC条件]
装置:ACQUITY UPLC(Waters社製)
カラム:ACQUITY UPLC HSS T3, 1.8μm,内径2.1mm,長さ50mm
カラム温度:40℃
注入量:5μL
サンプルクーラー:10℃
表1にグラジエント条件を示した。
【0058】
[表1]

【0059】
[MS/MS条件]
検出器:ZEVO TQ MS(Waters社製)
イオン化モード:ESI+
測定条件:MRMモード
シクロホスファミドにおける216.13(m/Z)のプレカーサーイオンの分解によって生じる105.86(m/Z)のプロダクトイオンをターゲットとした。
【0060】
[数1]
検体の残留量(ng)=Ws1×P/100×261.09/279.1×AT/AS×1/4,000,000×1,000,000
ここで、Ws1:シクロホスファミド標準品の標取量(mg)
P:含量
261.09/279.1:シクロホスファミド無水物表示量/シクロホスファミド一水和物表示量
1/4,000,000:希釈倍率,1,000,000:単位換算係数(mg→ng)
【0061】
なお、本分析例では、検体としてシクロホスファミドを例示して説明しているが、検体が例えばイホスファミドの場合は、以下のように実施する。先ず、イホスファミドが0.25ng/mの標準溶液を調製する。検体の分析の際は、液体クロマトグラフで分離したイホスファミドの成分をイオン化して質量分析計に導き、イホスファミドにおける216.13(m/Z)のプレカーサーイオンの分解によって生じる91.87(m/Z)のプロダクトイオンをターゲットとしてイホスファミドのピーク面積AT及びASを測定する。そして、得られたピーク面積AT及びASを[数2]に代入して検体(イホスファミド)の残留量を算出する。
【0062】
[数2]
検体の残留量(ng)=Ws2×P/100×AT/AS×1/8,000,000×1,000,000
ここで、Ws2:イホスファミド標準品の標取量(mg)
1/8,000,000:希釈倍率
【0063】
本実施の形態では、基材100の表面から抽出した検体を、液体クロマトグラフ・タンデム型質量分析計(LC/MS/MS)を用いた分析法で実施したが、これに限定するものではない。例えば、高速液体クロマトグラフィ、液体クロマトグラフ質量分析計、ガスクロマトグラフィ、ガスクロマトグラフ−質量分析計、ガスクロマトグラフィ・タンデム型質量分析計、誘導結合プラズマ発光分析装置、誘導結合プラズマ質量分析装置、UV計、蛍光光度計等を用いた各分析法で実施することも可能である。
【0064】
[検査キットを用いたモニタリング実験]
抗がん剤調整室を設置している医療機関に協力を得て、所定の期間(1週間)における当該医療機関の抗がん剤の拡散状況をモニタリングした。その結果を図9に示す。図において「BSC」とは、抗がん剤を調製する際に使用する安全キャビネットである。図示するように、安全キャビネット前の床を含むサンプリング箇所の全てからシクロホスファミドが検出された。
【0065】
[背景技術]でも説明したように、米国薬局方総則第797章では、抗がん剤による汚染状態を定期的にモニタリングすることを推奨している。今後、日本国内でもそれに準拠する形で汚染状態のモニタリングが定期的に実施されると予測する。
【産業上の利用可能性】
【0066】
本発明の薬剤の汚染状態検査具、及び該検査具を用いた薬剤の汚染状態検査方法は、上述した薬剤による汚染状態モニタリングのほか、例えば、カドミウム、鉛及び水銀等の有害元素による汚染状態のモニタリングにも適用可能である。
【符号の説明】
【0067】
1 検査キット
10 透明樹脂シート(シート状部材)
11 収容容器
12 手袋
13 記録用紙
14 宅配便送り状
15 鞄
100 基材
101 粘着層
102 剥離フィルム
103 サンプルID
104 切欠き
110 容器本体
111 蓋体
115 (容器本体の)底部
【特許請求の範囲】
【請求項1】
シート状部材と、
開口部から収容物を内部に収容した後、前記開口部を封止する封止部を備えた検体採取容器とを少なくとも含み、
開口を閉じることにより内部を略密閉状態とする鞄内にこれらを収容してなる薬剤の汚染状態検査具。
【請求項2】
前記シート状部材は、基材の少なくとも一方の片面に粘着層が形成されている請求項1に記載の薬剤の汚染状態検査具。
【請求項3】
前記基材は、樹脂フィルムで形成されている請求項2に記載の薬剤の汚染状態検査具。
【請求項4】
前記検体採取容器は、収容物を出し入れするための開口が形成された容器本体と該開口を塞ぐように着脱可能に嵌合する蓋体からなる請求項1から請求項3のいずれか1項に記載の薬剤の汚染状態検査具。
【請求項5】
シート状部材を用意し、検査対象場所に当該シート状部材を設置するステップと、
前記シート状部材の表面に検体を捕捉するステップと、
前記検体に水又は有機溶媒を加え、この溶液に超音波を付与又は該溶液を振とうさせることにより、前記検体を前記溶液中に溶解抽出させて抽出液を得るステップと、
前記抽出液中の検体成分を所定の分析手段を用いて分析し、前記基材に残留する検体の情報を得るステップを含む、薬剤の汚染状態検査方法。
【請求項6】
前記検体に水又は有機溶媒を加え、この溶液に超音波を付与又は該溶液を振とうさせることにより、前記検体を前記溶液中に溶解抽出させて抽出液を得るステップに代えて、
消毒液を湿潤させた第1の脱脂綿と、消毒液を湿潤させない第2の脱脂綿を用意し、前記第1の脱脂綿で前記シート状部材の表面を拭き取った後、前記第2の脱脂綿で前記シート状部材の表面を再度拭き取り、拭き取り後の前記2つの脱脂綿を容器に入れ、当該容器に水を加え、これを所定時間振り混ぜることにより前記抽出液を得るステップを含む、請求項5に記載の薬剤の汚染状態検査方法。
【請求項7】
前記検査対象場所に前記シート状部材を設置した時点から、予め定められた一定期間経過後に前記シート状部材を回収し、当該期間内において前記シート状部材の表面に捕捉した検体の情報を得る、請求項5又は請求項6に記載の薬剤の汚染状態検査方法。
【請求項8】
薬剤は、誤った投与、被曝や環境汚染により人体の健康状態を阻害し、死亡を含む深刻な影響をもたらし得る化学物質である、請求項5から請求項7のいずれか1項に記載の薬剤の汚染状態検査方法。
【請求項9】
前記化学物質は、国際がん研究機構がGroup1、Group2A、及びGroup2Bに分類している化学物質である、請求項8に記載の薬剤の汚染状態検査方法。
【請求項10】
前記所定の分析手段は、液体クロマトグラフ・タンデム型質量分析計、高速液体クロマトグラフィ、液体クロマトグラフ質量分析計、ガスクロマトグラフィ、ガスクロマトグラフ−質量分析計、ガスクロマトグラフィ・タンデム型質量分析計、誘導結合プラズマ発光分析装置、誘導結合プラズマ質量分析装置、UV計、蛍光光度計である、請求項5から請求項9のいずれか1項に記載の薬剤の汚染状態検査方法。
【請求項1】
シート状部材と、
開口部から収容物を内部に収容した後、前記開口部を封止する封止部を備えた検体採取容器とを少なくとも含み、
開口を閉じることにより内部を略密閉状態とする鞄内にこれらを収容してなる薬剤の汚染状態検査具。
【請求項2】
前記シート状部材は、基材の少なくとも一方の片面に粘着層が形成されている請求項1に記載の薬剤の汚染状態検査具。
【請求項3】
前記基材は、樹脂フィルムで形成されている請求項2に記載の薬剤の汚染状態検査具。
【請求項4】
前記検体採取容器は、収容物を出し入れするための開口が形成された容器本体と該開口を塞ぐように着脱可能に嵌合する蓋体からなる請求項1から請求項3のいずれか1項に記載の薬剤の汚染状態検査具。
【請求項5】
シート状部材を用意し、検査対象場所に当該シート状部材を設置するステップと、
前記シート状部材の表面に検体を捕捉するステップと、
前記検体に水又は有機溶媒を加え、この溶液に超音波を付与又は該溶液を振とうさせることにより、前記検体を前記溶液中に溶解抽出させて抽出液を得るステップと、
前記抽出液中の検体成分を所定の分析手段を用いて分析し、前記基材に残留する検体の情報を得るステップを含む、薬剤の汚染状態検査方法。
【請求項6】
前記検体に水又は有機溶媒を加え、この溶液に超音波を付与又は該溶液を振とうさせることにより、前記検体を前記溶液中に溶解抽出させて抽出液を得るステップに代えて、
消毒液を湿潤させた第1の脱脂綿と、消毒液を湿潤させない第2の脱脂綿を用意し、前記第1の脱脂綿で前記シート状部材の表面を拭き取った後、前記第2の脱脂綿で前記シート状部材の表面を再度拭き取り、拭き取り後の前記2つの脱脂綿を容器に入れ、当該容器に水を加え、これを所定時間振り混ぜることにより前記抽出液を得るステップを含む、請求項5に記載の薬剤の汚染状態検査方法。
【請求項7】
前記検査対象場所に前記シート状部材を設置した時点から、予め定められた一定期間経過後に前記シート状部材を回収し、当該期間内において前記シート状部材の表面に捕捉した検体の情報を得る、請求項5又は請求項6に記載の薬剤の汚染状態検査方法。
【請求項8】
薬剤は、誤った投与、被曝や環境汚染により人体の健康状態を阻害し、死亡を含む深刻な影響をもたらし得る化学物質である、請求項5から請求項7のいずれか1項に記載の薬剤の汚染状態検査方法。
【請求項9】
前記化学物質は、国際がん研究機構がGroup1、Group2A、及びGroup2Bに分類している化学物質である、請求項8に記載の薬剤の汚染状態検査方法。
【請求項10】
前記所定の分析手段は、液体クロマトグラフ・タンデム型質量分析計、高速液体クロマトグラフィ、液体クロマトグラフ質量分析計、ガスクロマトグラフィ、ガスクロマトグラフ−質量分析計、ガスクロマトグラフィ・タンデム型質量分析計、誘導結合プラズマ発光分析装置、誘導結合プラズマ質量分析装置、UV計、蛍光光度計である、請求項5から請求項9のいずれか1項に記載の薬剤の汚染状態検査方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2013−11476(P2013−11476A)
【公開日】平成25年1月17日(2013.1.17)
【国際特許分類】
【出願番号】特願2011−143241(P2011−143241)
【出願日】平成23年6月28日(2011.6.28)
【出願人】(511157516)シオノギ分析センター株式会社 (1)
【Fターム(参考)】
【公開日】平成25年1月17日(2013.1.17)
【国際特許分類】
【出願日】平成23年6月28日(2011.6.28)
【出願人】(511157516)シオノギ分析センター株式会社 (1)
【Fターム(参考)】
[ Back to top ]

