薬剤の薬物動力学を制御するデバイス
【課題】二相すなわち2モデル動力学プロファイルに基づいて、全身的吸収と改善された薬物動力学のために、皮膚の少なくとも2つの区画中への物質の投与のためのデバイスの提供。
【解決手段】該治療物質を収容する貯蔵器と、該貯蔵器と流体連絡し、皮膚の内部または下の皮内区画および皮下区画のみに該治療物質を送達するためのサイズを有する少なくとも2つの針とを含み、前記皮内区画および皮下区画は、治療物質に異なる薬物動力学を与え、前記異なる薬物動力学は、単一区画への送達に比較して、得られる複合薬物動力学に関する前記物質の効果を増大させることを含むことを特徴とする、治療物質を対象に送達する装置。
【解決手段】該治療物質を収容する貯蔵器と、該貯蔵器と流体連絡し、皮膚の内部または下の皮内区画および皮下区画のみに該治療物質を送達するためのサイズを有する少なくとも2つの針とを含み、前記皮内区画および皮下区画は、治療物質に異なる薬物動力学を与え、前記異なる薬物動力学は、単一区画への送達に比較して、得られる複合薬物動力学に関する前記物質の効果を増大させることを含むことを特徴とする、治療物質を対象に送達する装置。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、全身的吸収および改善された薬物動力学のために、皮膚の少なくとも2つの区画中への物質の投与のための方法およびデバイスに関する。
【背景技術】
【0002】
本出願は、2002年5月6日に出願した米国特許仮出願第60/377,649号、および2002年6月20日に出願した米国特許仮出願第60/389,881号に対して優先権を主張し、両仮出願は、それら全体を本明細書に組み入れられている。
【0003】
診断用の薬剤や薬物等の医薬物質を効率的かつ安全に投与することの重要性は、長い間認識されてきた。全ての医薬物質に関する重要な考慮事項であるが、近年、生物工学産業から生まれた蛋白質等の大きな分子の十分な生物学的利用能を得ることが、効率的かつ再現性のある吸収を得るというこの必要性を強調してきている(非特許文献1参照)。慣用の針の使用は、皮膚を通した投与によって、人間および動物に医薬物質を送達するための1つのアプローチを長い間提供してきた。注射の容易さを改善し、および慣用の針に付随する患者の不安および/または痛みを減少すると同時に、皮膚を通した再現性がありかつ有効な送達を達成するために、相当な努力がなされてきた。さらに、ある種の送達システムは、針を完全に排除し、および化学的メディエータ、またはイオン導入電流、もしくは熱穿孔、もしくは超音波導入などの外部の駆動力に依存して、皮膚の最外層である角質層を突破し、および皮膚の表面を通して物質を送達する。しかしながら、それらの送達システムは、再現性よく皮膚障壁を突破せず、または皮膚の表面下の所与の深さに医薬物質を送達せず、したがって、臨床的な結果が変わりやすい恐れがある。このように、針を用いることのような角質層の機械的な突破は、皮膚の表面を通した物質の投与の最も再現性のある方法を提供し、および投与された物質の配置において制御および信頼性を提供すると信じられている。
【0004】
皮膚表面の下に物質を送達するアプローチは、それらの皮下、筋肉内または静脈内の投与経路を含み、筋肉内(IM)注射および皮下(SC)注射が最も一般的に用いられてきた。
【0005】
解剖学的に、体の外部表面は、主として2層の組織層、すなわち外側の表皮および下にある真皮からなり、これらは一緒になって皮膚を構成する(概説としては、非特許文献2を参照されたい)。表皮は、75から150μmの間の総厚を有する5つの層または薄層に細分される。表皮の下には、2つの層、すなわち乳頭真皮と呼ばれる最外部分と網状真皮と呼ばれるより深い層とを含む真皮が存在する。乳頭真皮は、広い微小循環の血管叢とリンパ叢とを含む。これに対して、網状真皮は比較的に非細胞性および無血管性であり、また、高密度のコラーゲン質であり、かつ弾力のある結合組織からなる。表皮および真皮の下は、下皮とも呼ばれる皮下組織であり、それは結合組織と脂肪組織から構成される。筋肉組織は、皮下組織の下に存在する。
【0006】
上記のように、皮下組織および筋肉組織の両方は、医薬物質の投与の部位として一般的に使用されてきた。しかし、真皮は、物質投与の部位としてほとんど標的にされなかった。これは、少なくとも部分的には、皮内スペースへの正確な針の配置の困難さのためである。さらに、真皮、特に乳頭真皮は、高度の血管分布を有することが知られていたが、今まで、皮下投与に比べて改善された物質投与吸収プロファイルを得るために、この高度の血管分布が利用できるであろうことは認識されていなかった。これは、真皮よりもはるかに容易かつ予測通りに標的にされる皮下組織の中へ投与の後、小さな薬剤分子は典型的には迅速に吸収されるためである。他方、蛋白質および大きなポリペプチドのような大きな分子は、典型的には血管分布の程度にかかわらず毛細管上皮を通して十分吸収されないので、大きな分子に関してさえも、達成することがより困難な皮内投与によって、皮下投与に優る著しい吸収の利点を達成することは誰も予期しなかったのであろう。
【0007】
皮膚の透過性を高め、および皮膚を通過して体に利用される様々な薬物の拡散を増大させるために、多数の方法とデバイスが提案されてきている。
【0008】
[皮膚ベース送達のためのデバイス]
マイクロエレクトリカルメカニカルシステム(MEMS)に基づく製造技術における最近の進歩は、この組織障壁を克服し、および真皮および上部の表皮組織に対する直接的な機械的アクセスを提供する小さな針状のデバイスの開発を可能とした。最低限に侵襲的で安全な送達は、外側の進入の深度を10μmから2mmに制限し、そのようにして皮膚のより深いところに見出される神経末端および血管を避けることによって達成される。微小カニューレおよび微小針に基づく方法およびデバイスは、特許文献1に記載されている(特許文献1参照)。また、標準の鋼製カニューレも、特許文献2に記載されたデバイスと方法を使用する皮内送達に用いることができる(特許文献2参照)。これらの方法およびデバイスは、カニューレの全長、または深度制限ハブ構造を超えて露出されるカニューレの全長で画定される、制限された侵入深さ(一般に10μmから2mmの範囲)を有する小ゲージ(30Gまたはより小さい)の「微小カニューレ」を通す物質の送達を含む。
【0009】
角質層を破るためのデバイスは、角質層に侵入および実質的に貫通する長さを有する、微小研磨器および微小寸法の針または刃を含む。他のデバイスは、角質層を実質的に貫通しないで角質層に侵入する長さを有する、微小研磨器および微小寸法の針または刃を含む。微小針は、約30ゲージ以下の直径の構造を含み、それらの構造が実質上円筒形である場合、典型的には約30から50ゲージである。微小針という用語に包含する非円筒形構造は、したがって、匹敵する直径を有し、およびピラミッド状、矩形状、八角形状、楔形状、および他の適切な幾何形状を含むであろう。これらのデバイスの例は、特許文献3〜5に開示されている(特許文献3、特許文献4、特許文献5参照)。
【0010】
[薬物動力学]
比較研究は、皮膚の特定の区画およびそれらの区画内の深さに送達される薬物の薬物動力学(PK)プロファイルが劇的に変化することを示した。たとえば、ある種の薬物の薬物動力学は、皮内送達によって改善することができる(特許文献1、特許文献6参照)。現在までのところ、皮内送達を通して変化するPKの主眼は、標準のSC投与に比較した、効果の開始が向上されること、および高められた生物学的利用能に向けられてきた。
【先行技術文献】
【特許文献】
【0011】
【特許文献1】米国特許出願第606,909号明細書
【特許文献2】米国特許出願第417,671号明細書
【特許文献3】米国特許第5,879,326号明細書
【特許文献4】米国特許第5,250,023号明細書
【特許文献5】国際公開第97/48440号パンフレット
【特許文献6】米国特許出願第893,746号明細書(2002年7月18日に公告番号第20020095134号として公告)
【特許文献7】米国特許第6,200,296B1号明細書
【特許文献8】米国特許出願第606,909号明細書
【非特許文献】
【0012】
【非特許文献1】Cleland et al., Curr. Opin. Biotechnol.12:212-219,2001)
【非特許文献2】Physiology, Biochemistry, and Molecular Biology of the Skin, Second Edition, L.A.Goldsmith, Ed., Oxford University Press, New York, 1991
【非特許文献3】Hwang et al., Ann Plastic Surg 46:327-331,2001
【非特許文献4】Southwood, Plast.Reconstr,Surg 15:423-429,1955
【非特許文献5】Rushmer et al., Science 154:343-348,1966
【非特許文献6】Parker, R.S., et. al., 2000. Robust H-Infinity Glucose Control in Diabetes Using a Physiological Model. AIChE J. 46(12), 2537-2549
【非特許文献7】Sorensen, J.T., 1985. A Physiologic Model of Glucose Metabolism in Man and its Use to Design and Assess Improved Insulin Therapies for Diabetes. PhD Thesis, M.I.T.
【発明の概要】
【発明が解決しようとする課題】
【0013】
本発明は、皮膚内の2つ以上の区画または深さに対する送達の利点を組み合わせることによって、投与された薬剤物質の薬物動力学を制御するための方法およびデバイスに関する。具体的には、本発明は、浅いSCおよびID区画へ物質を送達する方法であって、ID送達で達成されるpKに類似した部分と、SC送達で達成されるpKプロファイルに類似した他の部分を有する、混成pKプロファイルを達成する方法を提供する。これは、化合物の迅速かつ高いピーク開始レベル、ならびに化合物のより低い長期循環レベルを提供する。
【課題を解決するための手段】
【0014】
この目的は、たとえば、
(a)深いIDスペースの流体の過負荷;
(b)ID/SC接合点における沈着;および
(c)皮膚の異なる位置、すなわち、浅いIDスペースおよび浅いSCスペースを標的とする単一または複数の微小針
によって達成される。
【0015】
このように、本発明は、皮膚の内部または下、少なくとも皮内スペース(2つ以上の区画または深さにアクセスする)中に物質を送達する工程を含む治療物質を組織に送達する方法を提供し、その区画または深さは物質に異なる薬物動力学を与え、それらは、得られる複合の薬物動力学に関する物質の効果を高める。2つ以上の区画へのアクセスは、2つ以上の深さまたは区画への独立的な送達によって、または2つの区画の境界の組織を標的とする送達方法、もしくは送達された物質が、たとえば拡散によって第2の区画に入るような方法で1つの区画に過負荷させる送達方法を用いることによって、達成されてよい。
【0016】
ID区画は、表皮の直下に始まり、および網状真皮の基部まで延在する皮膚層からなる組織スペースを意味する。平均して、この組織の深さは、最も外側の皮膚表面の下、約0.05−0.15mmから約1.7−2.5mmまでである。当業者は、年齢、人種、体の部位、何らかの疾患状態、および他の要因に伴う個々の生物学的変動性に基づいて、皮膚区画の絶対厚さと深さのいくらかの変動性があることを認識するであろう。
【0017】
SC区画は、網状真皮の直下で、および下にある筋肉まで延在する組織スペースを意味する。平均して、この組織スペースは、最外皮膚表面の下部の約1.7−2.5mmの深さに始まり、またボディマス指数、痩身または肥満の程度、体の部位、年齢、人種、何らかの疾患状態、および他の要因を含む生理的要因に関して高度に変動性である、より深い部分を有する。
【0018】
さらに、本発明は、物質、2つ以上の区画を含む部位または複数の部位に送達される方法を提供する。
【0019】
また、本発明は、物質がそれぞれ1つまたは複数の区画を含む複数の部位に送達される方法を提供する。
【0020】
さらに、本発明は、生理学的モデル、ルールベースモデルまたは移動平均法、治療薬剤動力学モデル、監視信号処理アルゴリズム、予測制御モデル、またはそれらの組合せを含む論理要素を有するアルゴリズムを用いる物質の制御された送達を提供する。
【0021】
本発明は、浅いSCとID送達を組み合わせることに関する方法を提供し、改善されたPK結果を達成する。これらの結果は、単独で一方の送達区画または他方を用いるだけでは達成することはできない。適切なデバイス構成および/または投与方法による個々のまたは複数部位の沈着が、独特および有益な結果を獲得できる。針を用いる物質の制御された浅いSC送達およびID送達の効果を組み合わせることの有益性は、以前には報告されていない。
【0022】
これらの方法に用いられるデバイスは、SC(またはIM)およびID送達の両方を達成するために構成されることができる。
【0023】
基礎となる技術的な原理は、微小針送達のPK結果が、投与される流体の沈着深さおよびパターン形成に特有であること、およびそのような沈着は、デバイスの設計および技術によって、またはIDスペースの流体の過負荷などの技術によって機械的に制御できることである。
【0024】
さらに、本発明は、長さ5mm未満の長さのSC注射用針(微小針ほか)を含む。約3mmの深さへの浅いSC送達は、慣行の技術を用いる深いSCとほぼ同一のPKをもたらす。より制御された特性をもたらす浅いSC送達単独の有用性は利用されていなかった。実際、以前は、5mm未満の深さは、SCスペース内ではないと考えられてきた。
【0025】
デバイス設計または技術のいずれかによる混成送達は、二相すなわち混成の動力学プロファイルをもたらす。デバイスの長さの僅かな違い(1mm対2mm対3mm)は、PK結果に劇的な違いをもたらす。SC状のプロファイルは、多くの場合に針の末端をIDスペース内に配置することが想定される針の長さによって得られることができる。浅いSC送達は、標準SC送達よりも、PK結果においてより一貫性があり、かつ均一である。
【0026】
注射によって投与される物質に関しては、標的にされる組織の深さの限界は、とりわけ、針またはカニューレの放出口が挿入される深さ、放出口の露出された高さ(垂直立ち上がり)、投与容量、投与の速度によって制御される。適切なパラメータは、過剰な実験なしに、当業者によって決定されることができる。
【0027】
本発明に従って送達することができる物質の例は、診断薬品、薬剤、およびたとえば栄養薬などの治療上または健康上の利益を提供する他の物質を含む、医薬的にまたは生物学的に活性な物質を含む。本発明に関して役に立つ可能性のある診断物質は、たとえば、イヌリン、ACTH(たとえば、コルチコトロピン注射)、黄体形成ホルモン放出ホルモン(ゴナドレリン)、成長ホルモン放出ホルモン(たとえば、酢酸セルモレリン)、コレシストキニン(シンカリド(Sincalide))、甲状腺ホルモンおよびその断片(たとえば、酢酸テリパラチド)、甲状腺放出ホルモンおよびその類似物(たとえばプロチレリン)、セクレチン等などの高分子物質を含む。
【0028】
本発明で使用することのできる治療物質は、α−1抗トリプシン、抗血管形成剤、アンチセンス、ブトルファノール、カルシトニンおよび類似物、セレデース、COX−II阻害剤、皮膚科薬剤、ジヒドロエルゴタミン、ドーパミン作用薬および拮抗薬、エンケファリンおよび他のオピオイドペプチド、表皮成長因子、エリトロポイエチンおよび類似物、卵胞刺激ホルモン、G−CSF、グルカゴン、GM−CSF、グラニセトロン、成長ホルモンおよび類似物(成長ホルモン放出ホルモンを含む)、成長ホルモン拮抗薬、ヒルジンおよびヒルログのようなヒルジン類似物、IgE抑制剤、インスリン、インシュリノトロピン(insulinotropin)および類似物、インスリン様成長因子、インターフェロン、インターロイキン、黄体形成ホルモン、黄体ホルモン放出ホルモンおよび類似物、へパリン、低分子量へパリンおよび他の天然、被修飾もしくは合成のグリコアミノグリカン、M−CSF、メトクロプラミド、ミダゾラム、モノクローナル抗体、PEG化抗体、PEG化蛋白質または親水性もしくは疎水性ポリマーもしくは他の官能基で修飾された任意の蛋白質、融合蛋白質、単鎖抗体の断片または付着した蛋白質、高分子、またはその付加官能基の任意の組合せを有する単鎖抗体の断片、麻酔性鎮痛薬、ニコチン、非ステロイド性抗炎症剤、オリゴ糖、オンダンセトロン、上皮小体ホルモンおよび類似物、上皮小体ホルモン拮抗薬、プロスタグランジン拮抗薬、プロスタグランジン、組み換え可溶性受容体、スコポラミン、セロトニン作用薬および拮抗薬、シルデナフィル、テルブタリン、血栓溶解薬、組織プラスミノゲン活性薬、TNF−およびTNF−拮抗薬、中毒、嗜癖、関節炎、コレラ、コカイン中毒、ジフテリア、破傷風、HIB、ライム病、髄膜炎菌、はしか、耳下腺炎、風疹、水痘、黄熱病、呼吸器系合胞体ウィルス、ダニ媒介日本脳炎、肺炎球菌、連鎖球菌、チフス、インフルエンザ、A型肺炎、B型肺炎、C型肺炎、およびE型肺炎を含む肝炎、中耳炎、狂犬病、ポリオ、HIV、パラインフルエンザ、ロタウイルス、エプスタイン−バーウィルス、CMV、クラミジア、分類不能型ヘモフィルス、モラクセラカタラリス(moraxella catarrhalis)、ヒト乳頭腫ウイルス、BCGを含む結核、淋菌、喘息、アテローム性動脈硬化マラリア、大腸菌(E.Coli)、アルツハイマー病、ヘリコバクター・ピロリ(H.Pylori)、サルモネラ属、糖尿病、癌、単純疱疹、ヒト乳頭腫等に係わる予防および治療抗原(サブユニット蛋白質、ペプチドおよび多糖、多糖共役体、トキソイド、遺伝子ベースのワクチン、生の弱毒化した細胞、再集合体細胞、不活性化全細胞、全細胞、ウイルス性および細菌性ベクターを含むが、それらに制限されない)を担体/補助剤と共にまたは伴わずに含むワクチン、および、通常の風邪用薬品、抗中毒薬、抗アレルギー薬、制吐剤、肥満防止薬、抗骨多孔症薬(antiosteoporeteic)、抗感染剤、鎮痛薬、麻酔薬、食欲抑制剤、抗関節炎薬、抗喘息剤、抗痙攣薬、抗欝薬、抗糖尿病剤、抗ヒスタミン薬、抗炎症剤、抗偏頭痛調合薬、抗乗り物酔い調合薬、制吐剤、抗新生物形成薬、抗パーキンソン病薬品、止痒剤、抗精神病薬、解熱剤、抗コリン作用薬、ベンゾジアゼピン拮抗薬、全身の血管、冠動脈、末梢および脳血管を含む血管拡張剤、骨刺激剤、中枢神経刺激薬、ホルモン、催眠薬、免疫抑制薬、筋弛緩薬、副交感神経遮断薬、副交感神経作用薬、プロスタグランジン、蛋白質、ペプチド、多糖類および他の高分子、精神刺激薬、鎮静剤、性機能不全および精神安定薬などの主要な治療薬の全てを含む同様の他の物質を含む。
【0029】
物質は、ボーラス、定量ボーラスまたは点滴によって送達することができ、ボーラスおよび定量ボーラス送達が好ましい。
【図面の簡単な説明】
【0030】
【図1A】2つの異なるID深さと1つのSC深さにおける皮膚へのインスリンの送達後の経時の平均グルコース濃度を示すグラフである。SC注射に関しては、29ゲージ、12.7mmの標準インスリンシリンジと針とを、ピンチアップ技術を用いて使用した。
【図1B】2つの異なるID深さと1つのSC深さにおける皮膚へのインスリンの送達後の経時の平均グルコース濃度を示すグラフである。SC注射に関しては、29ゲージ、12.7mmの標準インスリンシリンジと針とを、ピンチアップ技術を用いて使用した。
【図2】インスリンのIDおよびSC投与した状態のグルコースクランプ条件下での平均グルコース点滴速度を示すグラフである。
【図3】糖尿病の豚に1.5mmデバイスを用いて様々なインスリン濃度の投与の後の、平均血中インスリンレベルを対数プロットしたグラフである。
【図4】糖尿病の豚に2.0mmデバイスを用いて様々なインスリン濃度の投与の後の、平均血中インスリンレベルを対数プロットしたグラフである。
【図5】糖尿病の豚に3.0mmデバイスを用いて様々なインスリン濃度の投与の後の、平均血中インスリンレベルを対数プロットしたグラフである。
【図6】深さ1mmおよび3mmにおけるSC送達およびID送達を行った後の経時の血中のα−インターフェロン濃度、および2つの深さに関するその平均値を示すグラフである。
【図7A】注射デバイスの例示的構成を示す概略図である。投与される流体の通路は矢印によって示されている。図7Aは、側部放出口がIDスペースを標的とする注射を可能とし、および端部放出口がSCスペースを標的とする注射を可能とするように構成された、側部と端部放出口を備える単針を示している。
【図7B】注射デバイスの例示的構成を示す概略図である。投与流体の通路は矢印によって示されている。図7Bは、1つの針がIDスペースに位置され、および1つの針がSCスペースに位置されるような二重針構成を示している。
【図7C】注射デバイスの例示的構成を示す概略図である。投与流体の通路は矢印によって示されている。図7Cは、注射される物質が両方のスペースを標的にするように、IDとSCスペースの境界に位置される単針を示している。
【図7D】注射デバイスの例示的構成を示す概略図である。投与流体の通路は矢印によって示されている。図7Dは、過負荷にされる流体がIDとSCスペースの両方を標的とするように、IDスペースに位置される単針を示している。
【発明を実施するための形態】
【0031】
微小デバイスを用いる皮内送達に関する従来の研究は、多くの薬物、特に蛋白質、大きなポリペプチドまたは他の大きな分子量の薬物の皮内送達が、投与部位からの摂取のより速い開始、より迅速な全身的分布、ある場合においては増加された生物学的利用能をもたらすが、固有の生物学的クリアランスの機構または速度の変化をもたらさないことを示す。いくつかの研究においては、微小針の深さ、およびその結果として組織沈着スペースを変えることは、それらの薬物の実体のPKを変化させることが示された。この観察は、ヒト組換インスリンを用いた豚とヒトとにおける前臨床動物実験の両方における組換蛋白質ホルモンのような多数の物質に対して繰り返し行われてきた。
【0032】
浅いID組織スペースにおける沈着は、全身的な摂取および利用能に関するより早い薬物開始動力学、および、ある種の薬物に関する増加された利用能をもたらす。ID送達は、ID組織スペースが非常に小さく、高度に構造化したコラーゲン/エラスチンマトリクスからなり、(SCに比べて)最小限の膨張性であるという事実によって制限され、また、投与することができる総体積の量、そのような流体を投与することができる速度、およびそのような体積を投与するために要求される圧力において制約がある。
【0033】
主として、SCスペース(層)は、一方の側の表皮スペースと他方の側の筋肉またはその他の筋膜面との間に位置される。都合の悪いことに、このスペースは、決して、真皮ほどには毛細管(脈管またはリンパ管の両方)によって十分に灌流されず、それゆえ、吸収はより遅く、また、いくつかの場合においては生物学的利用能が低い。また、SC層は、物理的な位置(たとえば、腕、腹部、臀部)に基づく個体内に、および生理的な形態(痩身、標準、肥満)に基づく個人間に、極端な変動性を有する。注射、ジェット注入、および点滴等の現在のSC層への送達の実施では、単一の投与部位における単一の個体においてさえ、蛋白質、ペプチド、およびその他の分子のような治療化合物の大いに変動する沈着をもたらす。これは、これらの化合物の大いに変動する吸収を招き、そして、結果として薬物の効率を不都合に変化させる恐れがある。浅いSCスペースへの薬剤の直接的な沈着、すなわち、5mm未満の深さ、またはより好ましくは3mm未満の深さ、またはさらにより好ましくは2から3mmの深さへの直接的な沈着は、SC投与の容易性を与え、また標準のより長い針の使用および標準的実施に対して、薬物動力学のより良好な一貫性を達成する。
【0034】
また、標準的なSC投与は、多くの場合、その内部ではID沈着が起こると考えられる上部境界によって制限されると考えられてきた。この上部境界は、インスリンのような化合物に関する公表された特許およびその他の刊行物によって、深さ5mmであるとして定義されてきた。また、これは、現在の製品に反映されている(たとえば、インスリンシリンジおよび5mmの最小長さを有するペン針(特許文献7も参照されたい))。新しいデータは、動物モデルにおいて、わずか3mmのより浅い沈着が、標準の技術と同等のSCプロファイルだけでなく、薬剤動力学のより良好な再現性をももたらすことを示唆する。
【0035】
真皮と表皮の厚さは、個人間で、および個体内においては身体の異なる部位において変化する。たとえば、詳細な研究報告によれば、表皮は、約40から約90μmまでの厚さが変化し、および真皮は、表皮の真下から、体のいくつかの領域における1mm未満から、体のその他の領域における2mm直下から4mmの範囲までの深さまで、厚さが変化することが報告されている(非特許文献3、非特許文献4、非特許文献5参照)。この変化は、特定の部位における送達の深さを決定するときに考慮されなければならない。現在、薬物投与のためのいくつかの好まれる部位は、大腿部、腹部、臀部、胸部領域、および二頭筋、三頭筋、三角筋、前腕を含む腕部の様々な面を含むが、それらに限定されるものではない。
【0036】
従来技術において慣習的に使用されてきた上述の位置において、約1.7mmから2.5mmの深さへのIDの注射は、皮膚のID層とSC層との両方の内部に薬物を沈着させる。薬物は、より低いID領域および最も浅いSC領域の両方において沈着される。あるいはまた、IDスペースの内部に物質を沈着させるための長さ(公称1.7mm未満)を有する針は、注入された流体によって目標とされた組織スペースに過負荷をかけさせることができる。これが起こると、沈着された材料または薬物溶液は、より低いIDとSCスペースとの両方の内部に分配される。この結果はより長いID針で最も容易に起こる。なぜなら、下層のID組織床が、上部の真皮よりも膨張性が高い組織からなり、かつ注入された流体は最も小さい抵抗を有する経路をたどるからである。
【0037】
この混成の沈着は、SC沈着またはID沈着単独に比べて独特の薬剤動力学パラメーターをもたらす。IDスペースからの吸収は、依然としてより急速に起こり、全身的利用能(Tmax)のより迅速な開始を導く。しかし、非常に浅い真皮送達において以前見られた劇的な濃度ピークはない(特許文献8参照)。吸収を起こすことができる静脈性毛細血管およびリンパ管に対する密接な接近、および灌流の悪いSC組織床を通って灌流する必要性の減少のために、薬物吸収はより深いSC投与よりもより迅速でありかつより再現性が高い。この薬剤動力学の結果を組み合わせることは、望ましい薬剤動力学プロファイルをさらに目的に適合させるために利用することができる。これらの「二相性」プロファイルは、たとえばインスリンおよび組換蛋白質ホルモンで使用することができる。
【0038】
志願者の大腿部における通常のU−100ヒトインスリンのID送達を用いる最近のヒト臨床追跡において、標準ゲージ針および技術を用いた腹部における標準的なSC注射に優る薬物動力学上の利益が得られた。インスリンは、30g1.5mm針、34g1.0mmまたは標準SC(29Ga、12.7mm)針を用いて送達され、および血中グルコースおよびインスリンのレベルは、標準的な技術を用いて測定され、および血中グルコースは、グルコースクランプ(glucose clamp)技術を用いて一定のレベルに維持された。糖定常性を維持するために必要とされるグルコース注入の速度によって反映されるような血中グルコースの減少の薬剤動力学的応答は、SC注射を用いるよりもID注射に対してより急速に起こった。これは、以前、豚において得られた前臨床の結果とよく一致する。ヒトのおける血中インスリンレベルは、SCよりも著しく高い劇的なピーク濃度(Cmax)としては現れなかった、しかしながら、検出可能な血中インスリンレベル(Tmax)の開始は向上した。同様に、IDシステムを用いると、平均プロファイルは、早期相および後期相の吸収の両方を有する二相応答を示す傾向がある。これは、異なる組織層(IDと浅いSC)の間の薬剤の分配およびそれぞれのPK吸収パラメーターの結合を表す。また、これは、ピーク時および長期にわたる炭水化物代謝の両方に対処するために、短時間の高レベルの分泌およびより長期にわたる低レベルの分泌の両方を示す、生得のインスリン分泌をよりよく反映するものである。
【0039】
二相動力学は、広範囲の薬剤に対して適用可能であることが期待される。これらの薬物は、望まれるプロファイルが、作用の迅速な開始、および引き続く薬物の低いがより長期にわたる循環するレベルの両方を要求するようなものを含む。さらに、この点において、細胞によって生成される任意の物質送達プロファイルを複製することが可能であろう。好ましい薬物は、以下のものを含むが、それらに制限されるものではない:
【0040】
インスリン。急峻で高いピークの開始のレベルは、単純な糖または他の複雑でない炭水化物の消化および吸収から得られる高いグルコースレベルに対処し、そして、血中グルコースを迅速に「通常の」レベルに戻す。第二の低いインスリンのレベルは、複雑な炭水化物の代謝に対処するが、しかし、インスリンのより低い循環レベルに起因する低血糖の危険性を低減する。この結合されたPKの結果は、現在のところ、高価で複雑なインスリンポンプだけを用いて機械的に、または70/30の混合物のような異なるインスリンの型の調合物を混合することにより達成される。
【0041】
ホルモン、たとえば成長ホルモンは、身体によって生来的にパルス状に分泌される。IV投与によって模倣されるときに、このパルス状のプロファイルは、最小限から非陽性の結果をもたらす恐れがある。治療への応用のためには、低い循環レベルを伴ったSC送達が、生理的応答に最適であろう。ホルモンに関する二モデル動力学すなわち二相動力学の結果は、現在の調合物、投与計画および送達技術の薬物動力学的制限に起因して今まで得ることができなかった最適の結果を達成することができよう。
【0042】
COX阻害剤、モルヒネ、オピオイド、他の麻酔性鎮痛薬、トリプタンのような鎮痛剤(たとえば、偏頭痛、癌、または術後痛のためのもの)。典型的に、鎮痛剤は、浅いID送達によって達成される効果の迅速な開始を必要とするが、痛みの再発を防止するために薬物のより低く長期の循環レベルを必要とする。現在のところ、高いピークレベルを得るには、典型的には、ピークレベルに到達するためのより大量の薬剤を必要とし、そして、その後、長期の高い循環レベルをもたらす。高い循環薬物レベルの長期化は、多くの場合、COX薬物のGI効果、または麻酔性鎮痛剤に対する精神的能力または機能的能力の損失のような有害な副作用の原因である。動力学プロファイルを混合することによって、高いピークレベルを得て苦痛の軽減を生じさせ、同時に最小限の循環レベルを維持して苦痛の再発を防ぐことができるが、副作用を最小にすることができる。化学療法剤のような高い毒性レベルを有する薬物に対しても、類似の効果が期待され得る。
【0043】
勃起機能不全薬品。迅速な開始が望ましいが、効果の長期の持続もまた望まれる。これは、二相すなわち2モードの動力学プロファイルによって得ることができる。
【0044】
高分子量または疎水性薬物化合物(たとえば、モノクローナル抗体またはフェンタニールなどの麻酔剤):従来のSC投与においては、高分子量の薬物剤は、緩慢にしか吸収されない。なぜなら、吸収は、典型的には分子量の逆関数であるからである。疎水性薬剤に関しては、組織中への分配および組織との結合が吸収を遅らせる。組み合わされた動力学プロファイルは、薬物を早期に容易に利用し得るようによって効果の開始を促進し、そして連続的な効果のための蓄積物を提供する。
【0045】
抗凝血因子(たとえば、ヘパリン)。すでに生じてしまった凝血または血栓を溶解するために、高い早期のピークレベルが望ましい。しかし、高いレベルは、副作用のために長期間にわたっては望ましくない。これは、二相すなわち2モードの動力学プロファイルによって得ることができる。
【0046】
[操作の変形および代替]
薬物実体。多数の実体および多数の分類の薬品を本発明において使用することができる。特に好まれるものは、前段において述べられた薬品である。他の適切な薬品は、通常の実験を使用することによって当業者によって決定され得る。
【0047】
多数の異なる方法を用いて、2モードすなわち二相動力学を保証することができる。全ての方法は、異なる吸収特性を有する2つの別個の組織領域(IDおよび浅いSC)の間の薬物の分配に依存している。必要とされる正確な送達深さは、投薬部位または患者の個体群の間で変化するであろうが、パンチ生検のような技術、またはX線透視診断のような非侵襲性手段を使用して、容易に実験的に決定することができる。
【0048】
「より長い」IDデバイスを使用するより深いIDスペースの流体の過負荷は、実施するための最も簡単な技術である。しかしながら、それは、それに付随するより高度の変化を有するであろう。また、沈着パターン形成は、このアプローチによって変化することができ、また用いられる実際の手段によって変化し得る。本明細書で使用される際に、用語「沈着パターン形成」は、1つまたは複数の部位に物質を沈着することであり、それぞれの部位は1つまたは複数の組織区画内にある。これは、厳格な管理に対する必要性が少ないか、または広い治療的有効血中濃度投与量(たとえば、鎮痛剤、ホルモン)を有する薬剤に対して利用価値があるであろう。このアプローチは、明らかに流体の体積および/または送達速度に依存し、したがって、最適化は、大部分経験的に決定される。流体の体積および速度を特定の範囲に維持することによって、変動は最小限にされる。皮膚/SC接合部に特有の長さの単一の微小針を用いる直接沈着。この方法は、開始時に、上記の方法よりもより制御し易く、また機械的により信頼性が高いと思われる。しかしながら、ある注入はID動力学の寄与を大きく受け、他の注入はSC動力学の寄与が大きいというような、いくらかの生物学的変動が起こり得る。なぜなら、沈着は、2つの異なる吸収の領域の接合点で起きるからである。既存のデータに基づいて、このアプローチは、高い早期のCmax値を要求しない化合物に対しては最良であると思われる。また、標準のSC注射と類似点が存在するので、規制上の利益もあり、そして規制上の認可のために「生物学的等価性」を主張するのに十分なほど類似していてもよい。例は、ある種のホルモンおよびヘパリンを含む。
【0049】
他の方法は、異なる組織区画を別個に標的とする複数の微小針を伴う。このアプローチの例は、1mmの微小針と3mmの微小針とからなる、組合された2個の針の配列の使用である。このシステムは、最も高い沈着精度をもたらすであろう。なぜなら、各微小針は異なる組織区画を別個に標的とするからである。この方法は、最も制御可能な薬物動力学プロファイルを提供すると思われる。なぜなら、IDおよびSC区画における物質の沈着がより成功しそうであるからである。
【0050】
他のアプローチは、複数の管腔または放出口を有する単一の微小針を伴う:このアプローチにおいて有用な適切なデバイスの例は、1mmと3mmにおいて放出口を有するスプリンクラー針、または類似の設計概念を有する二重管腔系を含むであろう。それぞれの微小針は、それ自体の独特の流体機構、生体力学、または沈着特性を有するであろう。そのような特性は、当業者により、過度の実験なしに容易に決定されるであろう。
【0051】
[デバイス構成]
適切な送達システムは、沈着パターン形成を提供し、およびPK制御機構または手段をさらに提供することができ、治療物質の動力学を最適化することができるものであろう。そのような制御機構もしくは手段は、最適にはフィードバック制御を伴うであろう。最適化は、実験的に決定されると思われる。可能な送達システムは、制御手段と統合される、カテーテル、ペン、パッチポンプ、衝撃注入デバイス、イオン導入デバイスもしくは電気化学デバイス等を含む。それは、沈着パターン形成を提供するために、お互いに独立して使用される複数のデバイスの使用に関しては、本発明の範囲内である。したがって、例として、1つのデバイスを用いて、逐次または同時のいずれかにおいて一方の区画に対して物質を送達し、同一または異なる構成を有する別のデバイスを用いて別の区画に送達することができる。また、本発明の方法により、1個または複数のデバイスによって、逐次または同時に、相補的なまたは協同的な治療物質を送達することは、そのように所望されるならば可能である。
【0052】
もし、貯蔵器または流路が組み合せられる場合、流体力学に起因して沈着は複雑である可能性がある。考慮すべき1つの重要な要素は、より長い針は、流体の投与に対するより低い背圧を有するより容易に膨張性の組織に到達するので、より長い針は投与される薬物に対する最小の抵抗の経路となることである。したがって、流体が望ましい割合でそれぞれの位置に送達されるようにするために、複数の針または複数の放出口を有する針を有するデバイスを構成しなければならない。
【0053】
適切なデバイスの例は、異なる深さを標的とする独立の貯蔵器および流路を備える独立のデバイス;二重貯蔵器を含み、それぞれは異なる深さの独立した流路を提供する単一デバイス;異種の針長さを備える単一貯蔵器;圧力および/または流体の流れを平衡化するためのバルブまたは背圧デバイスを組み込んだ1個の多岐管および2個の針を備えたデバイス;送達を平衡化するために、1個の多岐管および異なる長さおよび直径を有する2個の針を備えるデバイス;2個以上のオリフィスを備える1個のテーパー付き針またはカニューレを有し、オリフィスの直径およびテーパーは、送達を平衡化させるように調節されるデバイス;下層のレベルのポートよりもより大きな放出口の面積を有する、浅いレベルに多数のポートを有するカニューレを備えるデバイス;浅いレベルのポートおよび下層のレベルの穴への蛇行性経路を有するカニューレを備えるデバイス;2つの異なる深さに順次的に流体を沈着することが可能な単一の伸張可能/格納可能な針を備えるデバイス;2つのスペース(たとえば、IDおよびSC)の界面に流体を送達するデバイスを含む。
【0054】
[容量沈着の変動性]
それぞれの部位に送達される薬物の量を、そのようなデバイスの適切な流体配管を通して制御することができる。得られる動力学プロファイルは、それぞれの部位特異的の区画からの加法的プロファイルに類似するであろう。
【0055】
[送達期間の影響]
パターン形成される沈着は、その部位への送達速度に依存し、およびボーラス/定量ボーラス送達に最も問題とされる(本明細書に用いる際に、「定量ボーラス送達」は、特定の速度で15分以下の時間内に起きる送達を指す)。これらの環境下で、該部位からの摂取は、実際の送達期間中に起こる時間に制限されてきた。比較すると、長期にわたる注入の間は、その部位への投与が依然として行われている間に、送達部位からの薬物の吸収が始まる。
【実施例1】
【0056】
ヒトの臨床試験からの皮内インスリン送達のための薬剤動力学の適合および生理学的モデル
皮膚の異なる深さにおいて皮内投与されるヒトインスリンの薬物動力学的効果および薬力学的効果を調べるために、ヒトの志願者についての実験を2つの微小針送達システムを用いて行った。15人の健康な男性志願者(年齢28±5.4才、BMI24.2±2.6kg/m2(平均±SD))は、10Uのヒトインスリンを、1.0mmと1.5mmの長さを有する2つの異なる微小針を通して受容し、また、10Uのヒトインスリンを、標準SC投与を通して受容した。ID微小針注入は、およそ10秒の継続時間にわたる上部大腿部に迅速なボーラスとして、30Ga、1.5mmの微小針を用いて行われた;ID微小針点滴は、2分間の総継続時間にわたって100マイクロリットル/分の速度で上部大腿部への点滴として、34Ga、1mmの微小針を用いて行われた;SC投与は、標準の29Ga、12.7mmインスリンシリンジを用いて腹部に行われた。グルコースタシス(Glucostasis)は、自動化された器具一式を用いて、オイグリセミックグルコースクランプ条件下において、連続的なプリセットレベルに維持された(標的血中グルコースレベル5.0mmol/L、内因性の基礎インスリン分泌を抑制するための0.15mU/kg/分の連続i.v.インスリン点滴、クランプ継続時間は投与後360分)。BG値を確認するため、およびインスリンとC−ペプチド定量化のために、血液サンプルを標準化された点で採取した。
【0057】
ヒト臨床試験の結果は、動物実験において予備臨床的に見られた効果とよい相関を示す。全身的に利用可能なインスリンの開始は向上し、および血中グルコース効果の開始もより速い。図1は、微小針構成およびSCへの通常のインスリンのいずれかによって、IDインスリンを受容する患者に対する平均血中インスリン値(n=55)を示す。値は、基線バックグラウンドに関して調整された。IDインスリンに対するTmaxは、比較のSC対照条件よりも著しく短い。
【0058】
グルコースクランンプ条件下では、インスリンの代謝が起きるので、追加のIVグルコースを点滴しなければならない。図2は、ID投与に関しては、SCに関するよりも著しく早期に、増加されたグルコースの点滴速度が必要とされることを示している。図2は、全ての送達条件に対する平均グルコース点滴速度、および全ての点滴速度に対する最も適合する多項式曲線(実線)を表している。必要なグルコース投与速度(Teffmax)の最大効果は、IDおよびSCに関して類似しているが、この最大効果に、ID経路による時間の約1/2で達する(表1参照)。実際、顕著なグルコース低下(Teff50%)は、投与の30分以内に起きる。繰り返しになるが、これらの応答はPK摂取データとよく一致する。
【0059】
表1に示すように、微小針で送達したインスリンは、tINS−maxおよびAUCINS−0−60に関するより低い値によって示されるように、SCに比べて作用のより速い開始を示した。
【0060】
【表1】

【0061】
イオン導入送達、吸入、および経口投与のような他のインスリン送達方法とは対照的に、微小針投与されるインスリンの相対的生物学的利用能(F)は、SCと非常に類似した。また、微小針薬物動力学測定は、作用のより迅速な開始(t50%eff−max)および(teff−max)を示した、しかし、SC注射と比較した際に、匹敵する最大代謝効果(GIRmax)を示した。いずれの注射部位についても逆の効果はなかった。内皮微小インスリン注射は、迅速かつ完全にインスリンを送達するための安全かつ効果的な方法であった。微小針送達によってもたらされる代謝効果の迅速な開始は、食事摂取中のインスリン投与に大きな可能性を提供する。
【0062】
人間の患者におけるインスリン動力学のコンピュータ化した生理学的区分モデルは、ヒトの臨床試験から得られるデータのサブセット(n=5対象)に応用して、二相の動力学の可能性および治療の有用性を最大限にするための可能性のある方法を説明する。皮下データは、単一の生理的入力区分を用いてよくモデル化された。しかし、皮内データへのモデル化されたフィッティングは、少なくとも2つの生理的組織区画からの入力を用いてのみ達成される。これは微小デバイスを用いた皮内送達の二相(または潜在的には多相の)態様を反映しており、それは、薬物動力学的に有益な結果を生みだすとともに、また、他の薬剤送達システムで従来見られなかった制御および予測関数を与える。
【0063】
インスリンのID送達の従来の動物データとは対照的に、皮内送達(ID)経路は、ヒトにおいて独特の「二相」挙動を示した。皮下(SC)入力に比べて、ID送達はより速い開始をもたらすだけでなく、同様に予期しない長期化された生理的なクリアランスすなわち減衰を示し、複数のインスリン摂取経路が関与すること示唆した。糖尿病患者におけるインシュリンの摂取および分布の生理学に基づくモデル(たとえば、非特許文献6、非特許文献7参照)を利用して平均実験データ(n=5 試験対象)をフィッティングして、どのパラメーターが測定されたインスリン吸収を最もよく表すかを決定した。
【0064】
当該モデルは、任意の生理的区画へのインスリン投与をも可能にし、および抹消組織を選択して、皮膚と皮下組織に近似させた。ボーラスインスリン送達のための1分間の投与の継続時間を選択して、計算を簡単にした。また、この入力はヒトの臨床実験(約10秒間にわたる急速なボーラスまたは2分間にわたる等価の用量の投与のいずれかであった)に用いられるID送達方法を有効に表した。抹消組織への投与に対するモデルの基本的な応答は、身体がボーラス投与に対して速やかに応答し、5分以内の完全な摂取および分布、ならびに70分以内の完全なインスリンクリアランスを示すことを示している。また、この結果は、糖尿病の動物モデルにおいて以前に得られたID送達データとよく一致する。
【0065】
SC投与をモデル化するために、体内への遅延された入力を含む送達経路が要求される。なぜなら、薬物の検出可能な開始は、抹消モデル単独で許されるよりもはるかに遅いからである。このモデル化した入力は、通常のヒトインスリンに関して許容された摂取経路の有効な表現である。添加された成分は、生物学的利用可能なインスリンの単量体形態および二量体形態に解離する吸収不能なインスリンの六量体形態の変換を表している。モデル応答は、実験データとよく一致する。変換速度は、一次である。解離は、SC組織区画からの生物学的利用能に関する律速ステップであると慣例的に考えられている。
【0066】
同じ皮下送達モデルは、IDデータ(1.5mm送達データ)に適用されるとき、そのデータの挙動と調和しない。皮下モデルシステムは、ID送達で見られた短い開始時間と急速な生物学的利用能とを取り込むことができない。同様に、抹消入力モデル単独では、ID送達に見られる長期化された減衰を取り込むことができない。
【0067】
観察されたIDデータをフィッティングするためには、2つの送達入力が要求される。第1の送達入力は、抹消皮膚区画からの急速な摂取を表し、およびより速い速度定数を提示する。動物モデルにおける以前のID送達データ(たとえば、特許文献6参照)は、急速な開始、およびこの区画からの六量体インスリン摂取の平衡化ステップがないことの両方を示した。第2の送達入力は、投与技術またはデバイス設計の結果として、SC組織区画へ侵入した投与されたインスリンに由来する「より遅い」摂取を表す。混成の区画モデルすなわち「二相」モデルの結果は、得られたIDプロファイルを良好にフィッティングする。二相動力学が、それぞれの区画が異なる摂取動力学を示す2つの区画への投与に起因することに注目することは重要である。
【0068】
また、フィッティングされたモデルにおける改良が可能である。速い吸収速度定数および遅い吸収速度定数のより良好な近似は、他の薬剤動力学フィッティング方法を用いることにより達成することができる。同様に、区画間のパーセント分布は、吸収モデルの最も良好なフィッティングによって実験的に決定されることができ、またはデバイス設計と投与技術に基づく投与に先立って、非経験的(ab initio)に設計されることができる。また、わずかに異なる摂取を有する真皮の異なる層を表す追加の区画は、実験データに対するモデル系のフィッティングをさらに改良する可能性がある。しかし、現在のデータに関しては、これらの追加区分システムは、上記のモデルよりも統計学的に良好であることは示されなかった。
【0069】
現在のフィッティングされたモデルは、単に、ヒトのIDインスリン送達の予期しない動力学の結果を、薬物動力学および生理的に容認可能なモデルに基づいて説明することができることを示すことを意図している。総合的に、単一経路はSCデータをモデル化するのに十分であるとしても、送達の単一経路は、IDデータの急速な初期開始および長期化された減衰を説明するには不十分である。ヒトのID送達の二相薬物動力学についてのこの予期しない観測は、以前に動物系で観測されていたが、通常は、より深い投与深さ(約2mm)においてであった。二相(または2モデル)動力学を有効にフィッティングし、かつ薬物動力学的にモデル化することができるという事実は、投与を、他の投与手段を用いても得られない独特の薬物動力学的な最終点に調整することができることを示唆している。これらのPK最終点を有効に予測および設計して、有効な薬物動力学結果をもたらすことができ、およびこれらの最終点を、独特のデバイス構成および投与技術を用いて、人間の投与治療において有効に達成することができる。そのような処理は、治療薬の信頼性の高い制御された送達を与え、それらの有効性を増強し、および様々な条件下のおけるそれらの投薬量を最適化する。
【実施例2】
【0070】
前臨床の糖尿病の豚の研究:様々な深さ(1.5、2.0、3.0mm)、容量および濃度でのインスリンの投与
異なる濃度(U40からU400)のインスリン10単位を、糖尿病の豚にボーラス単一微小針投与によって投与し、そして順次の時点で、インスリンレベルの定量および血中グルコースのための血液サンプルを引き抜いた。微小針は、深さを制限した31Ga、単一針シリンジベースのシステムであり、投与は数秒間(約5から15)にわたる手動で制御されたボーラスによるものであった。微小針送達深さは、1.5mm、2.0mm、3mmを含んだ。データは、n=5または6の平均である。異なるインスリン濃度の10IU投与の容量は、U40=250μL、U50=200μL、U100=100μL、U200=50μL、U400=25μLである。容量の送達精度を、較正されたガラスマイクロシリンジの使用、および送達されなかった全インスリンの重量測定による定量により保証した。
【0071】
結果
浅い深さ(1.5mm)での濃度/容量の影響
全ての濃度の1.5mm投与に関するデータを、図3に対数プロットにて示した。対数グラフは、浅いIDスペースへ短い微小針によって投与した際の、全ての濃度におけるインスリンの迅速な摂取を明確に示している。AUC(曲線下側の面積)の大部分は、45分未満の時点で見いだされる。全ての条件における平均Tmax値は、15から30分の範囲内である。平均最大濃度(Cmax)の相違が観察され、低濃度(U40およびU50)ではCmaxが低下し、最高濃度U400ではCmaxが劇的に低下した。これはより大きな容量が局所のIDスペースを「過剰充填」し、浅いSCへの漏出が現れるという仮説と一致する。非常に高い濃度においては、迅速な開始効果は、調合効果によって隠される。U400のような高度に濃縮されたインスリン溶液は、自己錯体化を起こして、それが摂取および分布を制限する。この効果は、以前に、U500インスリン(データは示さない)についても同様に見られた。本発明者らは、浅いIDスペース(<1.7mm)への単一針投与に関しては、約100μL以下の容量が、主としてIDの動力学を可能にすると結論する。100μLより大きい容量は、二相の特徴が高まる可能性を示し始める。
【0072】
中間すなわち界面深さ(2.0mm)での濃度/容量の影響
試験された全ての濃度の2.0mm投与に対するデータを、図4に対数プロットとして示す。上記のデータとは対照的に、平均のグラフは、より低いインスリン濃度であるU50に対するインスリンの迅速な摂取を示している。しかしながら、この平均グラフは、5つの個体のうち2つによってバイアスがかけられており、それら2つは15から20分間の期間において高いピーク値を示した。平均Tmaxは、より浅い送達に対して概して増加し、および40から120分の間であった。繰り返しになるが、U100送達に対する平均Tmaxは、高い後期相の吸収を有する2つの個体によってバイアスがかけられている。総合的に、2mmの送達は、減少したピーク値、わずかにより長い開始時間、および早い期間における低いAUCを示す傾向があった。この投与深さでは、低濃度/大容量が、浅いID投与に類似した高いピークを示す唯一の条件であった。この効果は、界面における沈着物が上方のより浅いIDスペースに進入する浸透効果によるものと信じられる。
【0073】
本発明者らは、この送達深さにおいて、針長さと送達容量の両方がPK結果に関する重要な制御要因であると結論する。このデータ集合に基づいて、より大きな容量がID組織区画とSC組織区画との間の界面スペースをあふれさせることにより、より迅速な開始の可能性を最大限にし、および、それゆえに二相のPK結果の増加された可能性を示す。微小針当たり100から250μLという中程度またはより大きな容量が、おそらく最も再現性のあるPK結果をもたらすであろう。
【0074】
より深い微小針深さ(3.0mm)での濃度/容量の影響
試験された全ての濃度の3.0mm投与に対するデータを、図5に対数プロットとして示す。この深さにおいて、PKプロファイルは容量と濃度によって最小限度に影響を受ける。平均プロファイルは、試験された全3種の濃度において同等である。平均開始は依然として迅速であり、20から55分の間のTmax値を伴う。この深さは完全に下皮すなわち皮下スペースの範囲内にあることが期待されるので、単一注射から二相動力学を得るための可能性は制限される。摂取のピークは、標準のSCを用いて通常見出されるよりも迅速であることは注目される。
【0075】
本発明者らは、この送達深さにおいて、針長さが容量と濃度の影響を凌駕すると結論する。減少された投与の技術依存性、および薬剤送達の増強された正確さおよび再現性に起因して、送達の一貫性はSCよりも依然として高くあるべきである。開始におけるわずかな利点は、単に皮膚に対する貯蔵物の密接な接近よって生じる可能性がある。この注射方法は、二相特性を得るために、(異なる針深さ)2つの針のアプローチを用いることによって結合できる。
【実施例3】
【0076】
2つの異なるIDで同時に投与されるα−インターフェロン送達の比較
この研究は、送達デバイスの特殊な機械設計に基づく二相動力学の達成を説明するために計画された。空間的に関連付けられる複数の生理的区画の同時充填に依存する上記の実施例に対する比較にて、この研究は、2つの生理的区画の独立した充填から得られるPKを調査することであった。インターフェロンα(0.2mL中に3百万IU、濃度1500万IU/mL)を、50μL/分に制御された速度で、1mmまたは3mmのいずれかの長さの単一の34Ga微小針によって豚に投与した。また、この投与量を、30Ga、1/2インチ針、手動のボーラス(2から15秒間)による標準のSC注射によって投与した。加えて、50μL/分で、1および3微小針の両方の34Ga微小針を通して、同時に0.1mL(全投与量の半分)を投与した。この場合、全投与量を一定(0.2mL)に維持したが、物理的に非常に近接した(約1インチ離れた)2個の微小針の投与部位の間で均等に分割した。経時の平均血清プロファイル(n=3から6)を図6に示す。
【0077】
1mmのデータは、非常に迅速な開始、高いCmax、小さなTmax、短い体内寿命を含む、ID投与に関して予測されるPK結果を示している。SCおよび3mmプロファイルは、1mm送達と比較して、全身的利用能のより遅い開始、低下したCmax、およびより長期化された循環寿命を同様に示す。この例では、3mmデータに関する平均濃度および曲線下の面積(AUC)は予想されるものより低くなった。対照的に、2つの部位における、かつ投与量を両方の微小針システム間で均等に分割する同時送達は、ID送達の劇的なピーク開始と速い吸収相の特性、ならびにSC送達の後期相の吸収およびより長い循環寿命特性の両方を示す。予期しなかったことには、2つの部位における組み合わされた投与から得られる全AUCは、単一部位単独における投与より大きく現れる。これに対する1つの可能性のある説明は、投与量を分割することは、異なる生理学的部位における別個の摂取および分配機構の利用を可能にする可能性があるということであろう。対照的に、単一部位の投与に関する摂取機構は、投与された薬物の投与量によって過負荷される可能性がある。この結果は、制御された二相動力学プロファイルのさらなる有益な結果を意味するであろう。
【0078】
これらの結果は、α−インターフェロンのような蛋白質のPKを、本発明の方法にしたがって実施される投与手段を用いて有利に制御して、特定の二相プロファイルおよび増強された生物学的利用能などの利点をもたらすことができることを示す。
【0079】
[参照による組み込み]
本発明の開示を理解しまたは完全なものとするために必要となる範囲で、本明細書中で言及される全ての刊行物、特許、および特許出願は、それぞれが個々に組み込まれているのと同程度に、参照によって明確に組み込まれている。
【技術分野】
【0001】
本発明は、全身的吸収および改善された薬物動力学のために、皮膚の少なくとも2つの区画中への物質の投与のための方法およびデバイスに関する。
【背景技術】
【0002】
本出願は、2002年5月6日に出願した米国特許仮出願第60/377,649号、および2002年6月20日に出願した米国特許仮出願第60/389,881号に対して優先権を主張し、両仮出願は、それら全体を本明細書に組み入れられている。
【0003】
診断用の薬剤や薬物等の医薬物質を効率的かつ安全に投与することの重要性は、長い間認識されてきた。全ての医薬物質に関する重要な考慮事項であるが、近年、生物工学産業から生まれた蛋白質等の大きな分子の十分な生物学的利用能を得ることが、効率的かつ再現性のある吸収を得るというこの必要性を強調してきている(非特許文献1参照)。慣用の針の使用は、皮膚を通した投与によって、人間および動物に医薬物質を送達するための1つのアプローチを長い間提供してきた。注射の容易さを改善し、および慣用の針に付随する患者の不安および/または痛みを減少すると同時に、皮膚を通した再現性がありかつ有効な送達を達成するために、相当な努力がなされてきた。さらに、ある種の送達システムは、針を完全に排除し、および化学的メディエータ、またはイオン導入電流、もしくは熱穿孔、もしくは超音波導入などの外部の駆動力に依存して、皮膚の最外層である角質層を突破し、および皮膚の表面を通して物質を送達する。しかしながら、それらの送達システムは、再現性よく皮膚障壁を突破せず、または皮膚の表面下の所与の深さに医薬物質を送達せず、したがって、臨床的な結果が変わりやすい恐れがある。このように、針を用いることのような角質層の機械的な突破は、皮膚の表面を通した物質の投与の最も再現性のある方法を提供し、および投与された物質の配置において制御および信頼性を提供すると信じられている。
【0004】
皮膚表面の下に物質を送達するアプローチは、それらの皮下、筋肉内または静脈内の投与経路を含み、筋肉内(IM)注射および皮下(SC)注射が最も一般的に用いられてきた。
【0005】
解剖学的に、体の外部表面は、主として2層の組織層、すなわち外側の表皮および下にある真皮からなり、これらは一緒になって皮膚を構成する(概説としては、非特許文献2を参照されたい)。表皮は、75から150μmの間の総厚を有する5つの層または薄層に細分される。表皮の下には、2つの層、すなわち乳頭真皮と呼ばれる最外部分と網状真皮と呼ばれるより深い層とを含む真皮が存在する。乳頭真皮は、広い微小循環の血管叢とリンパ叢とを含む。これに対して、網状真皮は比較的に非細胞性および無血管性であり、また、高密度のコラーゲン質であり、かつ弾力のある結合組織からなる。表皮および真皮の下は、下皮とも呼ばれる皮下組織であり、それは結合組織と脂肪組織から構成される。筋肉組織は、皮下組織の下に存在する。
【0006】
上記のように、皮下組織および筋肉組織の両方は、医薬物質の投与の部位として一般的に使用されてきた。しかし、真皮は、物質投与の部位としてほとんど標的にされなかった。これは、少なくとも部分的には、皮内スペースへの正確な針の配置の困難さのためである。さらに、真皮、特に乳頭真皮は、高度の血管分布を有することが知られていたが、今まで、皮下投与に比べて改善された物質投与吸収プロファイルを得るために、この高度の血管分布が利用できるであろうことは認識されていなかった。これは、真皮よりもはるかに容易かつ予測通りに標的にされる皮下組織の中へ投与の後、小さな薬剤分子は典型的には迅速に吸収されるためである。他方、蛋白質および大きなポリペプチドのような大きな分子は、典型的には血管分布の程度にかかわらず毛細管上皮を通して十分吸収されないので、大きな分子に関してさえも、達成することがより困難な皮内投与によって、皮下投与に優る著しい吸収の利点を達成することは誰も予期しなかったのであろう。
【0007】
皮膚の透過性を高め、および皮膚を通過して体に利用される様々な薬物の拡散を増大させるために、多数の方法とデバイスが提案されてきている。
【0008】
[皮膚ベース送達のためのデバイス]
マイクロエレクトリカルメカニカルシステム(MEMS)に基づく製造技術における最近の進歩は、この組織障壁を克服し、および真皮および上部の表皮組織に対する直接的な機械的アクセスを提供する小さな針状のデバイスの開発を可能とした。最低限に侵襲的で安全な送達は、外側の進入の深度を10μmから2mmに制限し、そのようにして皮膚のより深いところに見出される神経末端および血管を避けることによって達成される。微小カニューレおよび微小針に基づく方法およびデバイスは、特許文献1に記載されている(特許文献1参照)。また、標準の鋼製カニューレも、特許文献2に記載されたデバイスと方法を使用する皮内送達に用いることができる(特許文献2参照)。これらの方法およびデバイスは、カニューレの全長、または深度制限ハブ構造を超えて露出されるカニューレの全長で画定される、制限された侵入深さ(一般に10μmから2mmの範囲)を有する小ゲージ(30Gまたはより小さい)の「微小カニューレ」を通す物質の送達を含む。
【0009】
角質層を破るためのデバイスは、角質層に侵入および実質的に貫通する長さを有する、微小研磨器および微小寸法の針または刃を含む。他のデバイスは、角質層を実質的に貫通しないで角質層に侵入する長さを有する、微小研磨器および微小寸法の針または刃を含む。微小針は、約30ゲージ以下の直径の構造を含み、それらの構造が実質上円筒形である場合、典型的には約30から50ゲージである。微小針という用語に包含する非円筒形構造は、したがって、匹敵する直径を有し、およびピラミッド状、矩形状、八角形状、楔形状、および他の適切な幾何形状を含むであろう。これらのデバイスの例は、特許文献3〜5に開示されている(特許文献3、特許文献4、特許文献5参照)。
【0010】
[薬物動力学]
比較研究は、皮膚の特定の区画およびそれらの区画内の深さに送達される薬物の薬物動力学(PK)プロファイルが劇的に変化することを示した。たとえば、ある種の薬物の薬物動力学は、皮内送達によって改善することができる(特許文献1、特許文献6参照)。現在までのところ、皮内送達を通して変化するPKの主眼は、標準のSC投与に比較した、効果の開始が向上されること、および高められた生物学的利用能に向けられてきた。
【先行技術文献】
【特許文献】
【0011】
【特許文献1】米国特許出願第606,909号明細書
【特許文献2】米国特許出願第417,671号明細書
【特許文献3】米国特許第5,879,326号明細書
【特許文献4】米国特許第5,250,023号明細書
【特許文献5】国際公開第97/48440号パンフレット
【特許文献6】米国特許出願第893,746号明細書(2002年7月18日に公告番号第20020095134号として公告)
【特許文献7】米国特許第6,200,296B1号明細書
【特許文献8】米国特許出願第606,909号明細書
【非特許文献】
【0012】
【非特許文献1】Cleland et al., Curr. Opin. Biotechnol.12:212-219,2001)
【非特許文献2】Physiology, Biochemistry, and Molecular Biology of the Skin, Second Edition, L.A.Goldsmith, Ed., Oxford University Press, New York, 1991
【非特許文献3】Hwang et al., Ann Plastic Surg 46:327-331,2001
【非特許文献4】Southwood, Plast.Reconstr,Surg 15:423-429,1955
【非特許文献5】Rushmer et al., Science 154:343-348,1966
【非特許文献6】Parker, R.S., et. al., 2000. Robust H-Infinity Glucose Control in Diabetes Using a Physiological Model. AIChE J. 46(12), 2537-2549
【非特許文献7】Sorensen, J.T., 1985. A Physiologic Model of Glucose Metabolism in Man and its Use to Design and Assess Improved Insulin Therapies for Diabetes. PhD Thesis, M.I.T.
【発明の概要】
【発明が解決しようとする課題】
【0013】
本発明は、皮膚内の2つ以上の区画または深さに対する送達の利点を組み合わせることによって、投与された薬剤物質の薬物動力学を制御するための方法およびデバイスに関する。具体的には、本発明は、浅いSCおよびID区画へ物質を送達する方法であって、ID送達で達成されるpKに類似した部分と、SC送達で達成されるpKプロファイルに類似した他の部分を有する、混成pKプロファイルを達成する方法を提供する。これは、化合物の迅速かつ高いピーク開始レベル、ならびに化合物のより低い長期循環レベルを提供する。
【課題を解決するための手段】
【0014】
この目的は、たとえば、
(a)深いIDスペースの流体の過負荷;
(b)ID/SC接合点における沈着;および
(c)皮膚の異なる位置、すなわち、浅いIDスペースおよび浅いSCスペースを標的とする単一または複数の微小針
によって達成される。
【0015】
このように、本発明は、皮膚の内部または下、少なくとも皮内スペース(2つ以上の区画または深さにアクセスする)中に物質を送達する工程を含む治療物質を組織に送達する方法を提供し、その区画または深さは物質に異なる薬物動力学を与え、それらは、得られる複合の薬物動力学に関する物質の効果を高める。2つ以上の区画へのアクセスは、2つ以上の深さまたは区画への独立的な送達によって、または2つの区画の境界の組織を標的とする送達方法、もしくは送達された物質が、たとえば拡散によって第2の区画に入るような方法で1つの区画に過負荷させる送達方法を用いることによって、達成されてよい。
【0016】
ID区画は、表皮の直下に始まり、および網状真皮の基部まで延在する皮膚層からなる組織スペースを意味する。平均して、この組織の深さは、最も外側の皮膚表面の下、約0.05−0.15mmから約1.7−2.5mmまでである。当業者は、年齢、人種、体の部位、何らかの疾患状態、および他の要因に伴う個々の生物学的変動性に基づいて、皮膚区画の絶対厚さと深さのいくらかの変動性があることを認識するであろう。
【0017】
SC区画は、網状真皮の直下で、および下にある筋肉まで延在する組織スペースを意味する。平均して、この組織スペースは、最外皮膚表面の下部の約1.7−2.5mmの深さに始まり、またボディマス指数、痩身または肥満の程度、体の部位、年齢、人種、何らかの疾患状態、および他の要因を含む生理的要因に関して高度に変動性である、より深い部分を有する。
【0018】
さらに、本発明は、物質、2つ以上の区画を含む部位または複数の部位に送達される方法を提供する。
【0019】
また、本発明は、物質がそれぞれ1つまたは複数の区画を含む複数の部位に送達される方法を提供する。
【0020】
さらに、本発明は、生理学的モデル、ルールベースモデルまたは移動平均法、治療薬剤動力学モデル、監視信号処理アルゴリズム、予測制御モデル、またはそれらの組合せを含む論理要素を有するアルゴリズムを用いる物質の制御された送達を提供する。
【0021】
本発明は、浅いSCとID送達を組み合わせることに関する方法を提供し、改善されたPK結果を達成する。これらの結果は、単独で一方の送達区画または他方を用いるだけでは達成することはできない。適切なデバイス構成および/または投与方法による個々のまたは複数部位の沈着が、独特および有益な結果を獲得できる。針を用いる物質の制御された浅いSC送達およびID送達の効果を組み合わせることの有益性は、以前には報告されていない。
【0022】
これらの方法に用いられるデバイスは、SC(またはIM)およびID送達の両方を達成するために構成されることができる。
【0023】
基礎となる技術的な原理は、微小針送達のPK結果が、投与される流体の沈着深さおよびパターン形成に特有であること、およびそのような沈着は、デバイスの設計および技術によって、またはIDスペースの流体の過負荷などの技術によって機械的に制御できることである。
【0024】
さらに、本発明は、長さ5mm未満の長さのSC注射用針(微小針ほか)を含む。約3mmの深さへの浅いSC送達は、慣行の技術を用いる深いSCとほぼ同一のPKをもたらす。より制御された特性をもたらす浅いSC送達単独の有用性は利用されていなかった。実際、以前は、5mm未満の深さは、SCスペース内ではないと考えられてきた。
【0025】
デバイス設計または技術のいずれかによる混成送達は、二相すなわち混成の動力学プロファイルをもたらす。デバイスの長さの僅かな違い(1mm対2mm対3mm)は、PK結果に劇的な違いをもたらす。SC状のプロファイルは、多くの場合に針の末端をIDスペース内に配置することが想定される針の長さによって得られることができる。浅いSC送達は、標準SC送達よりも、PK結果においてより一貫性があり、かつ均一である。
【0026】
注射によって投与される物質に関しては、標的にされる組織の深さの限界は、とりわけ、針またはカニューレの放出口が挿入される深さ、放出口の露出された高さ(垂直立ち上がり)、投与容量、投与の速度によって制御される。適切なパラメータは、過剰な実験なしに、当業者によって決定されることができる。
【0027】
本発明に従って送達することができる物質の例は、診断薬品、薬剤、およびたとえば栄養薬などの治療上または健康上の利益を提供する他の物質を含む、医薬的にまたは生物学的に活性な物質を含む。本発明に関して役に立つ可能性のある診断物質は、たとえば、イヌリン、ACTH(たとえば、コルチコトロピン注射)、黄体形成ホルモン放出ホルモン(ゴナドレリン)、成長ホルモン放出ホルモン(たとえば、酢酸セルモレリン)、コレシストキニン(シンカリド(Sincalide))、甲状腺ホルモンおよびその断片(たとえば、酢酸テリパラチド)、甲状腺放出ホルモンおよびその類似物(たとえばプロチレリン)、セクレチン等などの高分子物質を含む。
【0028】
本発明で使用することのできる治療物質は、α−1抗トリプシン、抗血管形成剤、アンチセンス、ブトルファノール、カルシトニンおよび類似物、セレデース、COX−II阻害剤、皮膚科薬剤、ジヒドロエルゴタミン、ドーパミン作用薬および拮抗薬、エンケファリンおよび他のオピオイドペプチド、表皮成長因子、エリトロポイエチンおよび類似物、卵胞刺激ホルモン、G−CSF、グルカゴン、GM−CSF、グラニセトロン、成長ホルモンおよび類似物(成長ホルモン放出ホルモンを含む)、成長ホルモン拮抗薬、ヒルジンおよびヒルログのようなヒルジン類似物、IgE抑制剤、インスリン、インシュリノトロピン(insulinotropin)および類似物、インスリン様成長因子、インターフェロン、インターロイキン、黄体形成ホルモン、黄体ホルモン放出ホルモンおよび類似物、へパリン、低分子量へパリンおよび他の天然、被修飾もしくは合成のグリコアミノグリカン、M−CSF、メトクロプラミド、ミダゾラム、モノクローナル抗体、PEG化抗体、PEG化蛋白質または親水性もしくは疎水性ポリマーもしくは他の官能基で修飾された任意の蛋白質、融合蛋白質、単鎖抗体の断片または付着した蛋白質、高分子、またはその付加官能基の任意の組合せを有する単鎖抗体の断片、麻酔性鎮痛薬、ニコチン、非ステロイド性抗炎症剤、オリゴ糖、オンダンセトロン、上皮小体ホルモンおよび類似物、上皮小体ホルモン拮抗薬、プロスタグランジン拮抗薬、プロスタグランジン、組み換え可溶性受容体、スコポラミン、セロトニン作用薬および拮抗薬、シルデナフィル、テルブタリン、血栓溶解薬、組織プラスミノゲン活性薬、TNF−およびTNF−拮抗薬、中毒、嗜癖、関節炎、コレラ、コカイン中毒、ジフテリア、破傷風、HIB、ライム病、髄膜炎菌、はしか、耳下腺炎、風疹、水痘、黄熱病、呼吸器系合胞体ウィルス、ダニ媒介日本脳炎、肺炎球菌、連鎖球菌、チフス、インフルエンザ、A型肺炎、B型肺炎、C型肺炎、およびE型肺炎を含む肝炎、中耳炎、狂犬病、ポリオ、HIV、パラインフルエンザ、ロタウイルス、エプスタイン−バーウィルス、CMV、クラミジア、分類不能型ヘモフィルス、モラクセラカタラリス(moraxella catarrhalis)、ヒト乳頭腫ウイルス、BCGを含む結核、淋菌、喘息、アテローム性動脈硬化マラリア、大腸菌(E.Coli)、アルツハイマー病、ヘリコバクター・ピロリ(H.Pylori)、サルモネラ属、糖尿病、癌、単純疱疹、ヒト乳頭腫等に係わる予防および治療抗原(サブユニット蛋白質、ペプチドおよび多糖、多糖共役体、トキソイド、遺伝子ベースのワクチン、生の弱毒化した細胞、再集合体細胞、不活性化全細胞、全細胞、ウイルス性および細菌性ベクターを含むが、それらに制限されない)を担体/補助剤と共にまたは伴わずに含むワクチン、および、通常の風邪用薬品、抗中毒薬、抗アレルギー薬、制吐剤、肥満防止薬、抗骨多孔症薬(antiosteoporeteic)、抗感染剤、鎮痛薬、麻酔薬、食欲抑制剤、抗関節炎薬、抗喘息剤、抗痙攣薬、抗欝薬、抗糖尿病剤、抗ヒスタミン薬、抗炎症剤、抗偏頭痛調合薬、抗乗り物酔い調合薬、制吐剤、抗新生物形成薬、抗パーキンソン病薬品、止痒剤、抗精神病薬、解熱剤、抗コリン作用薬、ベンゾジアゼピン拮抗薬、全身の血管、冠動脈、末梢および脳血管を含む血管拡張剤、骨刺激剤、中枢神経刺激薬、ホルモン、催眠薬、免疫抑制薬、筋弛緩薬、副交感神経遮断薬、副交感神経作用薬、プロスタグランジン、蛋白質、ペプチド、多糖類および他の高分子、精神刺激薬、鎮静剤、性機能不全および精神安定薬などの主要な治療薬の全てを含む同様の他の物質を含む。
【0029】
物質は、ボーラス、定量ボーラスまたは点滴によって送達することができ、ボーラスおよび定量ボーラス送達が好ましい。
【図面の簡単な説明】
【0030】
【図1A】2つの異なるID深さと1つのSC深さにおける皮膚へのインスリンの送達後の経時の平均グルコース濃度を示すグラフである。SC注射に関しては、29ゲージ、12.7mmの標準インスリンシリンジと針とを、ピンチアップ技術を用いて使用した。
【図1B】2つの異なるID深さと1つのSC深さにおける皮膚へのインスリンの送達後の経時の平均グルコース濃度を示すグラフである。SC注射に関しては、29ゲージ、12.7mmの標準インスリンシリンジと針とを、ピンチアップ技術を用いて使用した。
【図2】インスリンのIDおよびSC投与した状態のグルコースクランプ条件下での平均グルコース点滴速度を示すグラフである。
【図3】糖尿病の豚に1.5mmデバイスを用いて様々なインスリン濃度の投与の後の、平均血中インスリンレベルを対数プロットしたグラフである。
【図4】糖尿病の豚に2.0mmデバイスを用いて様々なインスリン濃度の投与の後の、平均血中インスリンレベルを対数プロットしたグラフである。
【図5】糖尿病の豚に3.0mmデバイスを用いて様々なインスリン濃度の投与の後の、平均血中インスリンレベルを対数プロットしたグラフである。
【図6】深さ1mmおよび3mmにおけるSC送達およびID送達を行った後の経時の血中のα−インターフェロン濃度、および2つの深さに関するその平均値を示すグラフである。
【図7A】注射デバイスの例示的構成を示す概略図である。投与される流体の通路は矢印によって示されている。図7Aは、側部放出口がIDスペースを標的とする注射を可能とし、および端部放出口がSCスペースを標的とする注射を可能とするように構成された、側部と端部放出口を備える単針を示している。
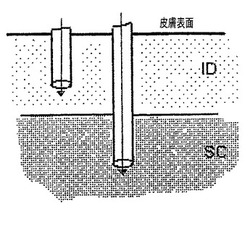
【図7B】注射デバイスの例示的構成を示す概略図である。投与流体の通路は矢印によって示されている。図7Bは、1つの針がIDスペースに位置され、および1つの針がSCスペースに位置されるような二重針構成を示している。
【図7C】注射デバイスの例示的構成を示す概略図である。投与流体の通路は矢印によって示されている。図7Cは、注射される物質が両方のスペースを標的にするように、IDとSCスペースの境界に位置される単針を示している。
【図7D】注射デバイスの例示的構成を示す概略図である。投与流体の通路は矢印によって示されている。図7Dは、過負荷にされる流体がIDとSCスペースの両方を標的とするように、IDスペースに位置される単針を示している。
【発明を実施するための形態】
【0031】
微小デバイスを用いる皮内送達に関する従来の研究は、多くの薬物、特に蛋白質、大きなポリペプチドまたは他の大きな分子量の薬物の皮内送達が、投与部位からの摂取のより速い開始、より迅速な全身的分布、ある場合においては増加された生物学的利用能をもたらすが、固有の生物学的クリアランスの機構または速度の変化をもたらさないことを示す。いくつかの研究においては、微小針の深さ、およびその結果として組織沈着スペースを変えることは、それらの薬物の実体のPKを変化させることが示された。この観察は、ヒト組換インスリンを用いた豚とヒトとにおける前臨床動物実験の両方における組換蛋白質ホルモンのような多数の物質に対して繰り返し行われてきた。
【0032】
浅いID組織スペースにおける沈着は、全身的な摂取および利用能に関するより早い薬物開始動力学、および、ある種の薬物に関する増加された利用能をもたらす。ID送達は、ID組織スペースが非常に小さく、高度に構造化したコラーゲン/エラスチンマトリクスからなり、(SCに比べて)最小限の膨張性であるという事実によって制限され、また、投与することができる総体積の量、そのような流体を投与することができる速度、およびそのような体積を投与するために要求される圧力において制約がある。
【0033】
主として、SCスペース(層)は、一方の側の表皮スペースと他方の側の筋肉またはその他の筋膜面との間に位置される。都合の悪いことに、このスペースは、決して、真皮ほどには毛細管(脈管またはリンパ管の両方)によって十分に灌流されず、それゆえ、吸収はより遅く、また、いくつかの場合においては生物学的利用能が低い。また、SC層は、物理的な位置(たとえば、腕、腹部、臀部)に基づく個体内に、および生理的な形態(痩身、標準、肥満)に基づく個人間に、極端な変動性を有する。注射、ジェット注入、および点滴等の現在のSC層への送達の実施では、単一の投与部位における単一の個体においてさえ、蛋白質、ペプチド、およびその他の分子のような治療化合物の大いに変動する沈着をもたらす。これは、これらの化合物の大いに変動する吸収を招き、そして、結果として薬物の効率を不都合に変化させる恐れがある。浅いSCスペースへの薬剤の直接的な沈着、すなわち、5mm未満の深さ、またはより好ましくは3mm未満の深さ、またはさらにより好ましくは2から3mmの深さへの直接的な沈着は、SC投与の容易性を与え、また標準のより長い針の使用および標準的実施に対して、薬物動力学のより良好な一貫性を達成する。
【0034】
また、標準的なSC投与は、多くの場合、その内部ではID沈着が起こると考えられる上部境界によって制限されると考えられてきた。この上部境界は、インスリンのような化合物に関する公表された特許およびその他の刊行物によって、深さ5mmであるとして定義されてきた。また、これは、現在の製品に反映されている(たとえば、インスリンシリンジおよび5mmの最小長さを有するペン針(特許文献7も参照されたい))。新しいデータは、動物モデルにおいて、わずか3mmのより浅い沈着が、標準の技術と同等のSCプロファイルだけでなく、薬剤動力学のより良好な再現性をももたらすことを示唆する。
【0035】
真皮と表皮の厚さは、個人間で、および個体内においては身体の異なる部位において変化する。たとえば、詳細な研究報告によれば、表皮は、約40から約90μmまでの厚さが変化し、および真皮は、表皮の真下から、体のいくつかの領域における1mm未満から、体のその他の領域における2mm直下から4mmの範囲までの深さまで、厚さが変化することが報告されている(非特許文献3、非特許文献4、非特許文献5参照)。この変化は、特定の部位における送達の深さを決定するときに考慮されなければならない。現在、薬物投与のためのいくつかの好まれる部位は、大腿部、腹部、臀部、胸部領域、および二頭筋、三頭筋、三角筋、前腕を含む腕部の様々な面を含むが、それらに限定されるものではない。
【0036】
従来技術において慣習的に使用されてきた上述の位置において、約1.7mmから2.5mmの深さへのIDの注射は、皮膚のID層とSC層との両方の内部に薬物を沈着させる。薬物は、より低いID領域および最も浅いSC領域の両方において沈着される。あるいはまた、IDスペースの内部に物質を沈着させるための長さ(公称1.7mm未満)を有する針は、注入された流体によって目標とされた組織スペースに過負荷をかけさせることができる。これが起こると、沈着された材料または薬物溶液は、より低いIDとSCスペースとの両方の内部に分配される。この結果はより長いID針で最も容易に起こる。なぜなら、下層のID組織床が、上部の真皮よりも膨張性が高い組織からなり、かつ注入された流体は最も小さい抵抗を有する経路をたどるからである。
【0037】
この混成の沈着は、SC沈着またはID沈着単独に比べて独特の薬剤動力学パラメーターをもたらす。IDスペースからの吸収は、依然としてより急速に起こり、全身的利用能(Tmax)のより迅速な開始を導く。しかし、非常に浅い真皮送達において以前見られた劇的な濃度ピークはない(特許文献8参照)。吸収を起こすことができる静脈性毛細血管およびリンパ管に対する密接な接近、および灌流の悪いSC組織床を通って灌流する必要性の減少のために、薬物吸収はより深いSC投与よりもより迅速でありかつより再現性が高い。この薬剤動力学の結果を組み合わせることは、望ましい薬剤動力学プロファイルをさらに目的に適合させるために利用することができる。これらの「二相性」プロファイルは、たとえばインスリンおよび組換蛋白質ホルモンで使用することができる。
【0038】
志願者の大腿部における通常のU−100ヒトインスリンのID送達を用いる最近のヒト臨床追跡において、標準ゲージ針および技術を用いた腹部における標準的なSC注射に優る薬物動力学上の利益が得られた。インスリンは、30g1.5mm針、34g1.0mmまたは標準SC(29Ga、12.7mm)針を用いて送達され、および血中グルコースおよびインスリンのレベルは、標準的な技術を用いて測定され、および血中グルコースは、グルコースクランプ(glucose clamp)技術を用いて一定のレベルに維持された。糖定常性を維持するために必要とされるグルコース注入の速度によって反映されるような血中グルコースの減少の薬剤動力学的応答は、SC注射を用いるよりもID注射に対してより急速に起こった。これは、以前、豚において得られた前臨床の結果とよく一致する。ヒトのおける血中インスリンレベルは、SCよりも著しく高い劇的なピーク濃度(Cmax)としては現れなかった、しかしながら、検出可能な血中インスリンレベル(Tmax)の開始は向上した。同様に、IDシステムを用いると、平均プロファイルは、早期相および後期相の吸収の両方を有する二相応答を示す傾向がある。これは、異なる組織層(IDと浅いSC)の間の薬剤の分配およびそれぞれのPK吸収パラメーターの結合を表す。また、これは、ピーク時および長期にわたる炭水化物代謝の両方に対処するために、短時間の高レベルの分泌およびより長期にわたる低レベルの分泌の両方を示す、生得のインスリン分泌をよりよく反映するものである。
【0039】
二相動力学は、広範囲の薬剤に対して適用可能であることが期待される。これらの薬物は、望まれるプロファイルが、作用の迅速な開始、および引き続く薬物の低いがより長期にわたる循環するレベルの両方を要求するようなものを含む。さらに、この点において、細胞によって生成される任意の物質送達プロファイルを複製することが可能であろう。好ましい薬物は、以下のものを含むが、それらに制限されるものではない:
【0040】
インスリン。急峻で高いピークの開始のレベルは、単純な糖または他の複雑でない炭水化物の消化および吸収から得られる高いグルコースレベルに対処し、そして、血中グルコースを迅速に「通常の」レベルに戻す。第二の低いインスリンのレベルは、複雑な炭水化物の代謝に対処するが、しかし、インスリンのより低い循環レベルに起因する低血糖の危険性を低減する。この結合されたPKの結果は、現在のところ、高価で複雑なインスリンポンプだけを用いて機械的に、または70/30の混合物のような異なるインスリンの型の調合物を混合することにより達成される。
【0041】
ホルモン、たとえば成長ホルモンは、身体によって生来的にパルス状に分泌される。IV投与によって模倣されるときに、このパルス状のプロファイルは、最小限から非陽性の結果をもたらす恐れがある。治療への応用のためには、低い循環レベルを伴ったSC送達が、生理的応答に最適であろう。ホルモンに関する二モデル動力学すなわち二相動力学の結果は、現在の調合物、投与計画および送達技術の薬物動力学的制限に起因して今まで得ることができなかった最適の結果を達成することができよう。
【0042】
COX阻害剤、モルヒネ、オピオイド、他の麻酔性鎮痛薬、トリプタンのような鎮痛剤(たとえば、偏頭痛、癌、または術後痛のためのもの)。典型的に、鎮痛剤は、浅いID送達によって達成される効果の迅速な開始を必要とするが、痛みの再発を防止するために薬物のより低く長期の循環レベルを必要とする。現在のところ、高いピークレベルを得るには、典型的には、ピークレベルに到達するためのより大量の薬剤を必要とし、そして、その後、長期の高い循環レベルをもたらす。高い循環薬物レベルの長期化は、多くの場合、COX薬物のGI効果、または麻酔性鎮痛剤に対する精神的能力または機能的能力の損失のような有害な副作用の原因である。動力学プロファイルを混合することによって、高いピークレベルを得て苦痛の軽減を生じさせ、同時に最小限の循環レベルを維持して苦痛の再発を防ぐことができるが、副作用を最小にすることができる。化学療法剤のような高い毒性レベルを有する薬物に対しても、類似の効果が期待され得る。
【0043】
勃起機能不全薬品。迅速な開始が望ましいが、効果の長期の持続もまた望まれる。これは、二相すなわち2モードの動力学プロファイルによって得ることができる。
【0044】
高分子量または疎水性薬物化合物(たとえば、モノクローナル抗体またはフェンタニールなどの麻酔剤):従来のSC投与においては、高分子量の薬物剤は、緩慢にしか吸収されない。なぜなら、吸収は、典型的には分子量の逆関数であるからである。疎水性薬剤に関しては、組織中への分配および組織との結合が吸収を遅らせる。組み合わされた動力学プロファイルは、薬物を早期に容易に利用し得るようによって効果の開始を促進し、そして連続的な効果のための蓄積物を提供する。
【0045】
抗凝血因子(たとえば、ヘパリン)。すでに生じてしまった凝血または血栓を溶解するために、高い早期のピークレベルが望ましい。しかし、高いレベルは、副作用のために長期間にわたっては望ましくない。これは、二相すなわち2モードの動力学プロファイルによって得ることができる。
【0046】
[操作の変形および代替]
薬物実体。多数の実体および多数の分類の薬品を本発明において使用することができる。特に好まれるものは、前段において述べられた薬品である。他の適切な薬品は、通常の実験を使用することによって当業者によって決定され得る。
【0047】
多数の異なる方法を用いて、2モードすなわち二相動力学を保証することができる。全ての方法は、異なる吸収特性を有する2つの別個の組織領域(IDおよび浅いSC)の間の薬物の分配に依存している。必要とされる正確な送達深さは、投薬部位または患者の個体群の間で変化するであろうが、パンチ生検のような技術、またはX線透視診断のような非侵襲性手段を使用して、容易に実験的に決定することができる。
【0048】
「より長い」IDデバイスを使用するより深いIDスペースの流体の過負荷は、実施するための最も簡単な技術である。しかしながら、それは、それに付随するより高度の変化を有するであろう。また、沈着パターン形成は、このアプローチによって変化することができ、また用いられる実際の手段によって変化し得る。本明細書で使用される際に、用語「沈着パターン形成」は、1つまたは複数の部位に物質を沈着することであり、それぞれの部位は1つまたは複数の組織区画内にある。これは、厳格な管理に対する必要性が少ないか、または広い治療的有効血中濃度投与量(たとえば、鎮痛剤、ホルモン)を有する薬剤に対して利用価値があるであろう。このアプローチは、明らかに流体の体積および/または送達速度に依存し、したがって、最適化は、大部分経験的に決定される。流体の体積および速度を特定の範囲に維持することによって、変動は最小限にされる。皮膚/SC接合部に特有の長さの単一の微小針を用いる直接沈着。この方法は、開始時に、上記の方法よりもより制御し易く、また機械的により信頼性が高いと思われる。しかしながら、ある注入はID動力学の寄与を大きく受け、他の注入はSC動力学の寄与が大きいというような、いくらかの生物学的変動が起こり得る。なぜなら、沈着は、2つの異なる吸収の領域の接合点で起きるからである。既存のデータに基づいて、このアプローチは、高い早期のCmax値を要求しない化合物に対しては最良であると思われる。また、標準のSC注射と類似点が存在するので、規制上の利益もあり、そして規制上の認可のために「生物学的等価性」を主張するのに十分なほど類似していてもよい。例は、ある種のホルモンおよびヘパリンを含む。
【0049】
他の方法は、異なる組織区画を別個に標的とする複数の微小針を伴う。このアプローチの例は、1mmの微小針と3mmの微小針とからなる、組合された2個の針の配列の使用である。このシステムは、最も高い沈着精度をもたらすであろう。なぜなら、各微小針は異なる組織区画を別個に標的とするからである。この方法は、最も制御可能な薬物動力学プロファイルを提供すると思われる。なぜなら、IDおよびSC区画における物質の沈着がより成功しそうであるからである。
【0050】
他のアプローチは、複数の管腔または放出口を有する単一の微小針を伴う:このアプローチにおいて有用な適切なデバイスの例は、1mmと3mmにおいて放出口を有するスプリンクラー針、または類似の設計概念を有する二重管腔系を含むであろう。それぞれの微小針は、それ自体の独特の流体機構、生体力学、または沈着特性を有するであろう。そのような特性は、当業者により、過度の実験なしに容易に決定されるであろう。
【0051】
[デバイス構成]
適切な送達システムは、沈着パターン形成を提供し、およびPK制御機構または手段をさらに提供することができ、治療物質の動力学を最適化することができるものであろう。そのような制御機構もしくは手段は、最適にはフィードバック制御を伴うであろう。最適化は、実験的に決定されると思われる。可能な送達システムは、制御手段と統合される、カテーテル、ペン、パッチポンプ、衝撃注入デバイス、イオン導入デバイスもしくは電気化学デバイス等を含む。それは、沈着パターン形成を提供するために、お互いに独立して使用される複数のデバイスの使用に関しては、本発明の範囲内である。したがって、例として、1つのデバイスを用いて、逐次または同時のいずれかにおいて一方の区画に対して物質を送達し、同一または異なる構成を有する別のデバイスを用いて別の区画に送達することができる。また、本発明の方法により、1個または複数のデバイスによって、逐次または同時に、相補的なまたは協同的な治療物質を送達することは、そのように所望されるならば可能である。
【0052】
もし、貯蔵器または流路が組み合せられる場合、流体力学に起因して沈着は複雑である可能性がある。考慮すべき1つの重要な要素は、より長い針は、流体の投与に対するより低い背圧を有するより容易に膨張性の組織に到達するので、より長い針は投与される薬物に対する最小の抵抗の経路となることである。したがって、流体が望ましい割合でそれぞれの位置に送達されるようにするために、複数の針または複数の放出口を有する針を有するデバイスを構成しなければならない。
【0053】
適切なデバイスの例は、異なる深さを標的とする独立の貯蔵器および流路を備える独立のデバイス;二重貯蔵器を含み、それぞれは異なる深さの独立した流路を提供する単一デバイス;異種の針長さを備える単一貯蔵器;圧力および/または流体の流れを平衡化するためのバルブまたは背圧デバイスを組み込んだ1個の多岐管および2個の針を備えたデバイス;送達を平衡化するために、1個の多岐管および異なる長さおよび直径を有する2個の針を備えるデバイス;2個以上のオリフィスを備える1個のテーパー付き針またはカニューレを有し、オリフィスの直径およびテーパーは、送達を平衡化させるように調節されるデバイス;下層のレベルのポートよりもより大きな放出口の面積を有する、浅いレベルに多数のポートを有するカニューレを備えるデバイス;浅いレベルのポートおよび下層のレベルの穴への蛇行性経路を有するカニューレを備えるデバイス;2つの異なる深さに順次的に流体を沈着することが可能な単一の伸張可能/格納可能な針を備えるデバイス;2つのスペース(たとえば、IDおよびSC)の界面に流体を送達するデバイスを含む。
【0054】
[容量沈着の変動性]
それぞれの部位に送達される薬物の量を、そのようなデバイスの適切な流体配管を通して制御することができる。得られる動力学プロファイルは、それぞれの部位特異的の区画からの加法的プロファイルに類似するであろう。
【0055】
[送達期間の影響]
パターン形成される沈着は、その部位への送達速度に依存し、およびボーラス/定量ボーラス送達に最も問題とされる(本明細書に用いる際に、「定量ボーラス送達」は、特定の速度で15分以下の時間内に起きる送達を指す)。これらの環境下で、該部位からの摂取は、実際の送達期間中に起こる時間に制限されてきた。比較すると、長期にわたる注入の間は、その部位への投与が依然として行われている間に、送達部位からの薬物の吸収が始まる。
【実施例1】
【0056】
ヒトの臨床試験からの皮内インスリン送達のための薬剤動力学の適合および生理学的モデル
皮膚の異なる深さにおいて皮内投与されるヒトインスリンの薬物動力学的効果および薬力学的効果を調べるために、ヒトの志願者についての実験を2つの微小針送達システムを用いて行った。15人の健康な男性志願者(年齢28±5.4才、BMI24.2±2.6kg/m2(平均±SD))は、10Uのヒトインスリンを、1.0mmと1.5mmの長さを有する2つの異なる微小針を通して受容し、また、10Uのヒトインスリンを、標準SC投与を通して受容した。ID微小針注入は、およそ10秒の継続時間にわたる上部大腿部に迅速なボーラスとして、30Ga、1.5mmの微小針を用いて行われた;ID微小針点滴は、2分間の総継続時間にわたって100マイクロリットル/分の速度で上部大腿部への点滴として、34Ga、1mmの微小針を用いて行われた;SC投与は、標準の29Ga、12.7mmインスリンシリンジを用いて腹部に行われた。グルコースタシス(Glucostasis)は、自動化された器具一式を用いて、オイグリセミックグルコースクランプ条件下において、連続的なプリセットレベルに維持された(標的血中グルコースレベル5.0mmol/L、内因性の基礎インスリン分泌を抑制するための0.15mU/kg/分の連続i.v.インスリン点滴、クランプ継続時間は投与後360分)。BG値を確認するため、およびインスリンとC−ペプチド定量化のために、血液サンプルを標準化された点で採取した。
【0057】
ヒト臨床試験の結果は、動物実験において予備臨床的に見られた効果とよい相関を示す。全身的に利用可能なインスリンの開始は向上し、および血中グルコース効果の開始もより速い。図1は、微小針構成およびSCへの通常のインスリンのいずれかによって、IDインスリンを受容する患者に対する平均血中インスリン値(n=55)を示す。値は、基線バックグラウンドに関して調整された。IDインスリンに対するTmaxは、比較のSC対照条件よりも著しく短い。
【0058】
グルコースクランンプ条件下では、インスリンの代謝が起きるので、追加のIVグルコースを点滴しなければならない。図2は、ID投与に関しては、SCに関するよりも著しく早期に、増加されたグルコースの点滴速度が必要とされることを示している。図2は、全ての送達条件に対する平均グルコース点滴速度、および全ての点滴速度に対する最も適合する多項式曲線(実線)を表している。必要なグルコース投与速度(Teffmax)の最大効果は、IDおよびSCに関して類似しているが、この最大効果に、ID経路による時間の約1/2で達する(表1参照)。実際、顕著なグルコース低下(Teff50%)は、投与の30分以内に起きる。繰り返しになるが、これらの応答はPK摂取データとよく一致する。
【0059】
表1に示すように、微小針で送達したインスリンは、tINS−maxおよびAUCINS−0−60に関するより低い値によって示されるように、SCに比べて作用のより速い開始を示した。
【0060】
【表1】

【0061】
イオン導入送達、吸入、および経口投与のような他のインスリン送達方法とは対照的に、微小針投与されるインスリンの相対的生物学的利用能(F)は、SCと非常に類似した。また、微小針薬物動力学測定は、作用のより迅速な開始(t50%eff−max)および(teff−max)を示した、しかし、SC注射と比較した際に、匹敵する最大代謝効果(GIRmax)を示した。いずれの注射部位についても逆の効果はなかった。内皮微小インスリン注射は、迅速かつ完全にインスリンを送達するための安全かつ効果的な方法であった。微小針送達によってもたらされる代謝効果の迅速な開始は、食事摂取中のインスリン投与に大きな可能性を提供する。
【0062】
人間の患者におけるインスリン動力学のコンピュータ化した生理学的区分モデルは、ヒトの臨床試験から得られるデータのサブセット(n=5対象)に応用して、二相の動力学の可能性および治療の有用性を最大限にするための可能性のある方法を説明する。皮下データは、単一の生理的入力区分を用いてよくモデル化された。しかし、皮内データへのモデル化されたフィッティングは、少なくとも2つの生理的組織区画からの入力を用いてのみ達成される。これは微小デバイスを用いた皮内送達の二相(または潜在的には多相の)態様を反映しており、それは、薬物動力学的に有益な結果を生みだすとともに、また、他の薬剤送達システムで従来見られなかった制御および予測関数を与える。
【0063】
インスリンのID送達の従来の動物データとは対照的に、皮内送達(ID)経路は、ヒトにおいて独特の「二相」挙動を示した。皮下(SC)入力に比べて、ID送達はより速い開始をもたらすだけでなく、同様に予期しない長期化された生理的なクリアランスすなわち減衰を示し、複数のインスリン摂取経路が関与すること示唆した。糖尿病患者におけるインシュリンの摂取および分布の生理学に基づくモデル(たとえば、非特許文献6、非特許文献7参照)を利用して平均実験データ(n=5 試験対象)をフィッティングして、どのパラメーターが測定されたインスリン吸収を最もよく表すかを決定した。
【0064】
当該モデルは、任意の生理的区画へのインスリン投与をも可能にし、および抹消組織を選択して、皮膚と皮下組織に近似させた。ボーラスインスリン送達のための1分間の投与の継続時間を選択して、計算を簡単にした。また、この入力はヒトの臨床実験(約10秒間にわたる急速なボーラスまたは2分間にわたる等価の用量の投与のいずれかであった)に用いられるID送達方法を有効に表した。抹消組織への投与に対するモデルの基本的な応答は、身体がボーラス投与に対して速やかに応答し、5分以内の完全な摂取および分布、ならびに70分以内の完全なインスリンクリアランスを示すことを示している。また、この結果は、糖尿病の動物モデルにおいて以前に得られたID送達データとよく一致する。
【0065】
SC投与をモデル化するために、体内への遅延された入力を含む送達経路が要求される。なぜなら、薬物の検出可能な開始は、抹消モデル単独で許されるよりもはるかに遅いからである。このモデル化した入力は、通常のヒトインスリンに関して許容された摂取経路の有効な表現である。添加された成分は、生物学的利用可能なインスリンの単量体形態および二量体形態に解離する吸収不能なインスリンの六量体形態の変換を表している。モデル応答は、実験データとよく一致する。変換速度は、一次である。解離は、SC組織区画からの生物学的利用能に関する律速ステップであると慣例的に考えられている。
【0066】
同じ皮下送達モデルは、IDデータ(1.5mm送達データ)に適用されるとき、そのデータの挙動と調和しない。皮下モデルシステムは、ID送達で見られた短い開始時間と急速な生物学的利用能とを取り込むことができない。同様に、抹消入力モデル単独では、ID送達に見られる長期化された減衰を取り込むことができない。
【0067】
観察されたIDデータをフィッティングするためには、2つの送達入力が要求される。第1の送達入力は、抹消皮膚区画からの急速な摂取を表し、およびより速い速度定数を提示する。動物モデルにおける以前のID送達データ(たとえば、特許文献6参照)は、急速な開始、およびこの区画からの六量体インスリン摂取の平衡化ステップがないことの両方を示した。第2の送達入力は、投与技術またはデバイス設計の結果として、SC組織区画へ侵入した投与されたインスリンに由来する「より遅い」摂取を表す。混成の区画モデルすなわち「二相」モデルの結果は、得られたIDプロファイルを良好にフィッティングする。二相動力学が、それぞれの区画が異なる摂取動力学を示す2つの区画への投与に起因することに注目することは重要である。
【0068】
また、フィッティングされたモデルにおける改良が可能である。速い吸収速度定数および遅い吸収速度定数のより良好な近似は、他の薬剤動力学フィッティング方法を用いることにより達成することができる。同様に、区画間のパーセント分布は、吸収モデルの最も良好なフィッティングによって実験的に決定されることができ、またはデバイス設計と投与技術に基づく投与に先立って、非経験的(ab initio)に設計されることができる。また、わずかに異なる摂取を有する真皮の異なる層を表す追加の区画は、実験データに対するモデル系のフィッティングをさらに改良する可能性がある。しかし、現在のデータに関しては、これらの追加区分システムは、上記のモデルよりも統計学的に良好であることは示されなかった。
【0069】
現在のフィッティングされたモデルは、単に、ヒトのIDインスリン送達の予期しない動力学の結果を、薬物動力学および生理的に容認可能なモデルに基づいて説明することができることを示すことを意図している。総合的に、単一経路はSCデータをモデル化するのに十分であるとしても、送達の単一経路は、IDデータの急速な初期開始および長期化された減衰を説明するには不十分である。ヒトのID送達の二相薬物動力学についてのこの予期しない観測は、以前に動物系で観測されていたが、通常は、より深い投与深さ(約2mm)においてであった。二相(または2モデル)動力学を有効にフィッティングし、かつ薬物動力学的にモデル化することができるという事実は、投与を、他の投与手段を用いても得られない独特の薬物動力学的な最終点に調整することができることを示唆している。これらのPK最終点を有効に予測および設計して、有効な薬物動力学結果をもたらすことができ、およびこれらの最終点を、独特のデバイス構成および投与技術を用いて、人間の投与治療において有効に達成することができる。そのような処理は、治療薬の信頼性の高い制御された送達を与え、それらの有効性を増強し、および様々な条件下のおけるそれらの投薬量を最適化する。
【実施例2】
【0070】
前臨床の糖尿病の豚の研究:様々な深さ(1.5、2.0、3.0mm)、容量および濃度でのインスリンの投与
異なる濃度(U40からU400)のインスリン10単位を、糖尿病の豚にボーラス単一微小針投与によって投与し、そして順次の時点で、インスリンレベルの定量および血中グルコースのための血液サンプルを引き抜いた。微小針は、深さを制限した31Ga、単一針シリンジベースのシステムであり、投与は数秒間(約5から15)にわたる手動で制御されたボーラスによるものであった。微小針送達深さは、1.5mm、2.0mm、3mmを含んだ。データは、n=5または6の平均である。異なるインスリン濃度の10IU投与の容量は、U40=250μL、U50=200μL、U100=100μL、U200=50μL、U400=25μLである。容量の送達精度を、較正されたガラスマイクロシリンジの使用、および送達されなかった全インスリンの重量測定による定量により保証した。
【0071】
結果
浅い深さ(1.5mm)での濃度/容量の影響
全ての濃度の1.5mm投与に関するデータを、図3に対数プロットにて示した。対数グラフは、浅いIDスペースへ短い微小針によって投与した際の、全ての濃度におけるインスリンの迅速な摂取を明確に示している。AUC(曲線下側の面積)の大部分は、45分未満の時点で見いだされる。全ての条件における平均Tmax値は、15から30分の範囲内である。平均最大濃度(Cmax)の相違が観察され、低濃度(U40およびU50)ではCmaxが低下し、最高濃度U400ではCmaxが劇的に低下した。これはより大きな容量が局所のIDスペースを「過剰充填」し、浅いSCへの漏出が現れるという仮説と一致する。非常に高い濃度においては、迅速な開始効果は、調合効果によって隠される。U400のような高度に濃縮されたインスリン溶液は、自己錯体化を起こして、それが摂取および分布を制限する。この効果は、以前に、U500インスリン(データは示さない)についても同様に見られた。本発明者らは、浅いIDスペース(<1.7mm)への単一針投与に関しては、約100μL以下の容量が、主としてIDの動力学を可能にすると結論する。100μLより大きい容量は、二相の特徴が高まる可能性を示し始める。
【0072】
中間すなわち界面深さ(2.0mm)での濃度/容量の影響
試験された全ての濃度の2.0mm投与に対するデータを、図4に対数プロットとして示す。上記のデータとは対照的に、平均のグラフは、より低いインスリン濃度であるU50に対するインスリンの迅速な摂取を示している。しかしながら、この平均グラフは、5つの個体のうち2つによってバイアスがかけられており、それら2つは15から20分間の期間において高いピーク値を示した。平均Tmaxは、より浅い送達に対して概して増加し、および40から120分の間であった。繰り返しになるが、U100送達に対する平均Tmaxは、高い後期相の吸収を有する2つの個体によってバイアスがかけられている。総合的に、2mmの送達は、減少したピーク値、わずかにより長い開始時間、および早い期間における低いAUCを示す傾向があった。この投与深さでは、低濃度/大容量が、浅いID投与に類似した高いピークを示す唯一の条件であった。この効果は、界面における沈着物が上方のより浅いIDスペースに進入する浸透効果によるものと信じられる。
【0073】
本発明者らは、この送達深さにおいて、針長さと送達容量の両方がPK結果に関する重要な制御要因であると結論する。このデータ集合に基づいて、より大きな容量がID組織区画とSC組織区画との間の界面スペースをあふれさせることにより、より迅速な開始の可能性を最大限にし、および、それゆえに二相のPK結果の増加された可能性を示す。微小針当たり100から250μLという中程度またはより大きな容量が、おそらく最も再現性のあるPK結果をもたらすであろう。
【0074】
より深い微小針深さ(3.0mm)での濃度/容量の影響
試験された全ての濃度の3.0mm投与に対するデータを、図5に対数プロットとして示す。この深さにおいて、PKプロファイルは容量と濃度によって最小限度に影響を受ける。平均プロファイルは、試験された全3種の濃度において同等である。平均開始は依然として迅速であり、20から55分の間のTmax値を伴う。この深さは完全に下皮すなわち皮下スペースの範囲内にあることが期待されるので、単一注射から二相動力学を得るための可能性は制限される。摂取のピークは、標準のSCを用いて通常見出されるよりも迅速であることは注目される。
【0075】
本発明者らは、この送達深さにおいて、針長さが容量と濃度の影響を凌駕すると結論する。減少された投与の技術依存性、および薬剤送達の増強された正確さおよび再現性に起因して、送達の一貫性はSCよりも依然として高くあるべきである。開始におけるわずかな利点は、単に皮膚に対する貯蔵物の密接な接近よって生じる可能性がある。この注射方法は、二相特性を得るために、(異なる針深さ)2つの針のアプローチを用いることによって結合できる。
【実施例3】
【0076】
2つの異なるIDで同時に投与されるα−インターフェロン送達の比較
この研究は、送達デバイスの特殊な機械設計に基づく二相動力学の達成を説明するために計画された。空間的に関連付けられる複数の生理的区画の同時充填に依存する上記の実施例に対する比較にて、この研究は、2つの生理的区画の独立した充填から得られるPKを調査することであった。インターフェロンα(0.2mL中に3百万IU、濃度1500万IU/mL)を、50μL/分に制御された速度で、1mmまたは3mmのいずれかの長さの単一の34Ga微小針によって豚に投与した。また、この投与量を、30Ga、1/2インチ針、手動のボーラス(2から15秒間)による標準のSC注射によって投与した。加えて、50μL/分で、1および3微小針の両方の34Ga微小針を通して、同時に0.1mL(全投与量の半分)を投与した。この場合、全投与量を一定(0.2mL)に維持したが、物理的に非常に近接した(約1インチ離れた)2個の微小針の投与部位の間で均等に分割した。経時の平均血清プロファイル(n=3から6)を図6に示す。
【0077】
1mmのデータは、非常に迅速な開始、高いCmax、小さなTmax、短い体内寿命を含む、ID投与に関して予測されるPK結果を示している。SCおよび3mmプロファイルは、1mm送達と比較して、全身的利用能のより遅い開始、低下したCmax、およびより長期化された循環寿命を同様に示す。この例では、3mmデータに関する平均濃度および曲線下の面積(AUC)は予想されるものより低くなった。対照的に、2つの部位における、かつ投与量を両方の微小針システム間で均等に分割する同時送達は、ID送達の劇的なピーク開始と速い吸収相の特性、ならびにSC送達の後期相の吸収およびより長い循環寿命特性の両方を示す。予期しなかったことには、2つの部位における組み合わされた投与から得られる全AUCは、単一部位単独における投与より大きく現れる。これに対する1つの可能性のある説明は、投与量を分割することは、異なる生理学的部位における別個の摂取および分配機構の利用を可能にする可能性があるということであろう。対照的に、単一部位の投与に関する摂取機構は、投与された薬物の投与量によって過負荷される可能性がある。この結果は、制御された二相動力学プロファイルのさらなる有益な結果を意味するであろう。
【0078】
これらの結果は、α−インターフェロンのような蛋白質のPKを、本発明の方法にしたがって実施される投与手段を用いて有利に制御して、特定の二相プロファイルおよび増強された生物学的利用能などの利点をもたらすことができることを示す。
【0079】
[参照による組み込み]
本発明の開示を理解しまたは完全なものとするために必要となる範囲で、本明細書中で言及される全ての刊行物、特許、および特許出願は、それぞれが個々に組み込まれているのと同程度に、参照によって明確に組み込まれている。
【特許請求の範囲】
【請求項1】
治療物質を対象に送達する装置であって、
該治療物質を収容する貯蔵器と、
該貯蔵器と流体連絡し、皮膚の内部または下の皮内区画および皮下区画のみに該治療物質を送達するためのサイズを有する少なくとも2つの針と
を含み、
前記皮内区画および皮下区画は、治療物質に異なる薬物動力学を与え、前記異なる薬物動力学は、単一区画への送達に比較して、得られる複合薬物動力学に関する前記物質の効果を増大させることを含むことを特徴とする装置。
【請求項2】
該複数の針は、異なる長さを有することを特徴とする請求項1に記載の装置。
【請求項3】
該複数の針の少なくとも1つは、約300μmから約5mmの長さであることを特徴とする請求項2に記載の装置。
【請求項4】
該複数の針の少なくとも1つは、約500μmから約1mmの長さであることを特徴とする請求項3に記載の装置。
【請求項5】
該複数の針の少なくとも1つが皮内区画に挿入される際に、該複数の針の少なくとも1つは約250μmから約2mmの深さに配置される放出口を有することを特徴とする請求項2に記載の装置。
【請求項6】
前記放出口は、前記針またはカニューレが挿入される際に、約750μmから約1.5mmの深さであることを特徴とする請求項5に記載の装置。
【請求項7】
前記放出口は、約0から約1mmの露出高を有することを特徴とする請求項6に記載の装置。
【請求項1】
治療物質を対象に送達する装置であって、
該治療物質を収容する貯蔵器と、
該貯蔵器と流体連絡し、皮膚の内部または下の皮内区画および皮下区画のみに該治療物質を送達するためのサイズを有する少なくとも2つの針と
を含み、
前記皮内区画および皮下区画は、治療物質に異なる薬物動力学を与え、前記異なる薬物動力学は、単一区画への送達に比較して、得られる複合薬物動力学に関する前記物質の効果を増大させることを含むことを特徴とする装置。
【請求項2】
該複数の針は、異なる長さを有することを特徴とする請求項1に記載の装置。
【請求項3】
該複数の針の少なくとも1つは、約300μmから約5mmの長さであることを特徴とする請求項2に記載の装置。
【請求項4】
該複数の針の少なくとも1つは、約500μmから約1mmの長さであることを特徴とする請求項3に記載の装置。
【請求項5】
該複数の針の少なくとも1つが皮内区画に挿入される際に、該複数の針の少なくとも1つは約250μmから約2mmの深さに配置される放出口を有することを特徴とする請求項2に記載の装置。
【請求項6】
前記放出口は、前記針またはカニューレが挿入される際に、約750μmから約1.5mmの深さであることを特徴とする請求項5に記載の装置。
【請求項7】
前記放出口は、約0から約1mmの露出高を有することを特徴とする請求項6に記載の装置。
【図1A】


【図1B】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7A】


【図7B】


【図7C】


【図7D】




【図1B】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7A】


【図7B】


【図7C】


【図7D】


【公開番号】特開2011−67682(P2011−67682A)
【公開日】平成23年4月7日(2011.4.7)
【国際特許分類】
【出願番号】特願2011−3317(P2011−3317)
【出願日】平成23年1月11日(2011.1.11)
【分割の表示】特願2004−503075(P2004−503075)の分割
【原出願日】平成15年5月6日(2003.5.6)
【出願人】(595117091)ベクトン・ディキンソン・アンド・カンパニー (539)
【氏名又は名称原語表記】BECTON, DICKINSON AND COMPANY
【住所又は居所原語表記】1 BECTON DRIVE, FRANKLIN LAKES, NEW JERSEY 07417−1880, UNITED STATES OF AMERICA
【Fターム(参考)】
【公開日】平成23年4月7日(2011.4.7)
【国際特許分類】
【出願日】平成23年1月11日(2011.1.11)
【分割の表示】特願2004−503075(P2004−503075)の分割
【原出願日】平成15年5月6日(2003.5.6)
【出願人】(595117091)ベクトン・ディキンソン・アンド・カンパニー (539)
【氏名又は名称原語表記】BECTON, DICKINSON AND COMPANY
【住所又は居所原語表記】1 BECTON DRIVE, FRANKLIN LAKES, NEW JERSEY 07417−1880, UNITED STATES OF AMERICA
【Fターム(参考)】
[ Back to top ]

