薬物伝達用ポリ(アミドアミン)オリゴマーヒドロゲルおよびそれを用いた薬物伝達体
【課題】本発明は、温度およびpH敏感性オリゴマーヒドロゲルおよびそれを用いた薬物伝達体に関する。
【解決手段】製造方法が簡単であり、且つ容易に体内から排出されるポリ(アミドアミン)PAAオリゴマー単独で構成された温度およびpH敏感性PAAオリゴマーヒドロゲル並びにその製造方法とそれを用いたヒドロゲル薬物伝達体を提供する。
【解決手段】製造方法が簡単であり、且つ容易に体内から排出されるポリ(アミドアミン)PAAオリゴマー単独で構成された温度およびpH敏感性PAAオリゴマーヒドロゲル並びにその製造方法とそれを用いたヒドロゲル薬物伝達体を提供する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、温度およびpH敏感性オリゴマーヒドロゲルおよびそれを用いた薬物伝達体(Drug delivery)に関し、特に、ポリ(アミドアミン)[poly(amidoamine、PAA)]オリゴマー単独で構成されるヒドロゲルおよびそれを用いた薬物伝達体に関する。
【背景技術】
【0002】
ポリマーヒドロゲルを用いた薬物伝達体の開発の例として、特許文献1には、生分解性ポリエステル高分子のA-B-A形態の3重ブロック共重合体について記載されているが、疏水性ブロック(A)は、ポリラクチド(PLA)、ポリグリコリド(PGA)およびこれらの共重合体で限定しており、親水性ブロック(B)もポリエチレングリコール(PEG)およびその誘導体で限定している。
【0003】
前記3重ブロック共重合体は、疏水性高分子と親水性高分子とのブロック共重合体(block copolymer)からなり、温度によってゾル-ゲル移転現象を起こす温度敏感性ブロック共重合体であって、前記ブロック共重合体をゾル(sol)状態の水溶液形態で体内に注入する場合、体温によってゲル(gel)状態に転移されることから、体内で安定に薬物を坦持して徐々に薬物を放出して伝達する徐放性薬物伝達体の支持体として活用している。しかしながら、温度にだけ敏感なゾル-ゲル移転特性を有するブロック共重合体を用いる場合、薬物と相互作用が弱いため、人体内への注射時に薬物の初期過多放出(initial burst release)現象が起き、体内に注射する過程では体内の温度により注射針の温度が体内の温度と熱的平衡に到達し、体内に完全に注入される前にゲル化が起きるため、注射針の詰まり現象(clogging)等の問題点があった。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】米国特許第5,476,909号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
本発明の目的は、比較的製造し易く、且つ体内から完全に排出され、温度およびpH変化によってゾル-ゲル移転を起こすPAAオリゴマーヒドロゲル、並びにその製造方法とそれを用いた薬物伝達体を提供することにある。
【0006】
なお、本発明の目的は、ヒドロゲル薬物伝達体として使用できるように薬物の初期過多放出(initial burst release)現象を抑制し、一定期間薬物の放出(sustained release)が起きるように分子設計された新概念の温度およびpH敏感性オリゴマーヒドロゲル、並びにその製造方法とそれを用いた生理活性物質を含むオリゴマーヒドロゲル薬物伝達体を提供することにある。
【0007】
なお、本発明の目的は、前記オリゴマーの構成成分、これらのモル比、及び分子量を適宜変更して癌細胞のような標的に指向性を有するだけでなく、遺伝子変移又は他の応用分野において標的指向性を有するようにデザインした温度およびpH敏感性オリゴマーヒドロゲル並びにその製造方法とそれを用いた薬物伝達体を提供することにある。
【課題を解決するための手段】
【0008】
上記の目的を達成するための本発明は、温度およびpH敏感性オリゴマーヒドロゲルにおいて、PAAオリゴマー単独で構成される温度およびpH敏感性オリゴマーヒドロゲルを提供する。
【0009】
また、本発明は、前記PAAオリゴマーが下記一般式(1)の低分子量の重合体のヒドロゲルを提供する。
【化1】

式中、Rは炭素原子数1〜10の範囲のアルキル基である。
【0010】
また、本発明は、前記PAAオリゴマーは、前駆体として1種以上のアルキレンビスアクリルアミド化合物の置換基と2次アミン基を有する1種以上のジアミン化合物の置換基との間のカップリング(coupling)により製造されるヒドロゲルを提供する。
【0011】
また、本発明は、前記PAAオリゴマーの分子量が500〜1,000g/molのヒドロゲルを提供する。
【0012】
また、本発明は、前記PAAオリゴマーがpH7.0〜7.4の範囲でヒドロゲルを形成し、pH3.0〜7.0未満でゾル状態を形成するオリゴマーヒドロゲルを提供する。
【0013】
また、本発明は、前記アルキレンビスアクリルアミド化合物が次のような一般式(2)からなるオリゴマーヒドロゲル を提供する。
【化2】

式中、Rは炭素原子数1〜10のアルキル基である。
【0014】
また、本発明の前記アルキレンビスアクリルアミド化合物は、N,N'-メチレンビスアクリルアミド(MDA)、N,N'-エチレンビスアクリルアミド、N,N'-ジイソプロピルアクリルアミド、1,4-ブチレンジアクリルアミド、1,6-ヘキシレンジアクリルアミド、1,8-オクチレンジアクリルアミド、1,10-デカンジアクリルアミドの単独又はこれらの混合物からなる群より1以上選ばれるオリゴマーヒドロゲルを提供する。
【0015】
また、本発明は、前記ジアミン化合物が次のような一般式(3)からなる2次アミン含有ジアミン化合物又はこれらの混合物のオリゴマーヒドロゲルを提供する。
【化3】

式中、R1およびR2は炭素原子数1〜10のアルキル基である。
【0016】
また、本発明の前記2次アミン基を有するジアミン化合物は、4,4'-トリメチレンジピペリジン(4,4'-trimethylenepiperidine)、N,N'-ジメチルエチレンジアミン(N,N'-dimethylethylenediamine)、ピペラジン(piperazine)、2-メチルピペラジン(2-methylpiperazine)、3-メチル-4-(3-メチルフェニル)ピペラジン{3-methyl-4-(3-methylphenyl)piperazine}、3-メチルピペラジン(3-methylpiperazine)、4-(phenylmethyl)piperazine{4-(フェニルメチル)ピペラジン}、4-(1-フェニルエチル)ピペラジン{4-(1-phenylethyl)piperazine}、4-(1,1'-ジメトキシカルボニル)ピペラジン{4-(1,1'-dimethoxycarbonyl)piperazine}、4-(2-(ビス-(2-プロペニル)アミノ)エチル)ピペラジン{4-(2-(bis-(2-propenyl)amino)ethyl)piperazine}、1-(2-アミノエチル)ピペラジン{1-(2-aminoethyl)piperazine}、4-(アミノメチル)ピペラジン{4-(aminomethyl)piperazine}、N,N'-ジメチル-1,2-エタンジアミン(N,N'-dimethyl-1,2-ethanediamine)、N,N'-ジエチル-1,2-エタンジアミン(N,N'-diethyl-1,2-ethanediamine)、N,N'-ジイソプロピル-1,2-エタンジアミン(N,N'-diisopropyl-1,2-ethanediamine)、N,N'-ジメチル-1,2-プロピルアミン(N,N'-dimethyl-1,2-propyldiamine)、N,N'-ジエチル-1,2-プロピルジアミン(N,N'-diethyl-1,2-propyldiamine)、N,N'-ジイソプロピル-1,2-プロピルアミン(N,N'-diisopropyl-1,2-propyldiamine)、N,N'-ジメチル-1,2-ヘキサンジアミン(N,N'-dimethyl-1,2-hexanediamine)、N,N'-ジメチル-N-(3-(メチルアミノ)プロピル]-1,3-プロパンジアミン{N,N-dimethyl-N-[3-(methylamino)propyl]-1,3-propanediamine}、N-[2-メチルアミノ)エトキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)ethoxyethyl]-N,N'-dimethylamine}、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)dioxyethyl]-N,N'-dimethylamine}、1,4-ジアゼパン(1,4-diazepane)単独又はこれらの混合物からなる群より1以上選ばれるオリゴマーヒドロゲルを提供する。
【0017】
また、本発明のPAAオリゴマーは、上述したアルキレンビスアクリルアミド化合物と2次アミン基を有するジアミン化合物との反応モル比が1:10〜50のオリゴマーヒドロゲルを提供する。
【0018】
また、本発明は、前記PAAオリゴマーヒドロゲルからなる薬物伝達体を提供する。
【0019】
また、本発明は、前記PAAオリゴマーヒドロゲル内に封入できる生理活性物質としてインスリン(insulin)、白血球増殖因子(G-CSF)、ヒト成長ホルモン(hGH)、エリスポエチン(Erythropoietin、EPO)、シムリン(Symlin)、エキセンディン(Exendin)、Somatokineのような蛋白質;パクリタキセル(Paclitaxel)、ドセタキセル(Docetaxel)、クロラムブシル(Chlorambucil)、インターフェロン(Interferon)、モノクローナル抗体(Monoclonal antibodies)、ワクチンなどのような抗癌剤;抗菌剤;ステロイド類;消炎鎮痛剤;性ホルモン;免疫抑制剤;抗ウイルス剤;麻酔剤;制吐剤;又は抗ヒスタミン剤を含むことができ、賦形剤、安定化剤、pH調整剤、抗酸化剤、保存剤、結合剤、崩壊剤などのような添加剤及び/又は溶媒などをさらに含むことができる薬物伝達体を提供する。
【0020】
また、本発明は、前記伝達体が経口剤又は非経口剤であり、望ましくは静脈、筋肉又は皮下注射剤形態の薬物伝達体を提供する。
【発明の効果】
【0021】
上述のように本発明に係るPAAオリゴマーヒドロゲルは、1ステップ工程によって製造され、人体内への注射時にPAAオリゴマー自体が分子量1000以下の低分子量であるため、人体内に蓄積されず、直に体外に排出されるという特徴があり、カップリング反応によりPAAオリゴマーを製造する前駆体の2次アミン基はpH変化に応じたイオン化度によって親水性又は疏水性を有するため、温度敏感性以外にpH敏感性も同時に付与され、上述した従来の温度敏感性ポリマーヒドロゲルの問題点を解決することができる。
【0022】
また、本発明に係るオリゴマーヒドロゲルは、特定のpH、例えば、体内正常細胞のpH範囲であるpH7.0〜7.4では安定し、癌細胞のような非正常細胞のpH範囲であるpH3.0〜7.0未満ではゾル(sol)状態に転移されることにより、癌細胞に標的指向性を有する薬物放出用伝達体として用いることができる。すなわち、低いpH(pH7.0未満)でポリ(アミドアミン)(PAA)オリゴマーに存在する2次アミンのイオン化度の増加によりPAA全体が水溶性に変わりゾル状態を維持することになり、pH7.0以上ではPAAのイオン化度が低下して疏水性特性を示すため、ゲル状態を形成する。上記のような特性により、本発明のPAAオリゴマーヒドロゲルは、温度だけでなくpHに敏感なゾル-ゲル移転特性を示す。
【0023】
また、本発明に係るPAAオリゴマーヒドロゲルは、体内で安全なので、医療用、遺伝子伝達、薬物伝達分野、特に薬物担持がおよび放出などの徐放性薬物伝達体に適用できるだけでなく、病の診断のための物質を非正常細胞に伝達することにより、画像診断(diagnostic imaging)等の診断用途に応用することができる。
【0024】
また、本発明に係るPAAオリゴマーヒドロゲルは、正常体内条件と同一のpH7.0〜7.4の範囲ではヒドロゲルを形成し、癌細胞のような非正常条件のpH7.0未満ではゾル状態を維持して癌細胞に標的指向性を有するデザインを適用し、さらに、前記オリゴマーヒドロゲルの構成成分、これらのモル比、分子量および/又はブロック内の官能基を適宜変更することにより、癌細胞だけでなく遺伝子変移又は他の応用分野において標的指向性を有するようにデザインした。
【図面の簡単な説明】
【0025】
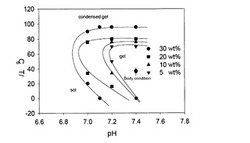
【図1】実施例7で製造したPAAオリゴマーの様々な濃度での温度およびpH変化によるゾル-ゲルの移転挙動を示すグラフである。
【図2】温度およびpHによる実施例3、7、8及び9で製造したPAAオリゴマーのゾル-ゲルの移転挙動を示すグラフである。
【図3】様々なpHでの温度増加に応じた実施例7で製造したPAAオリゴマーの粘度の変化を示すグラフである。
【図4】実施例7のPAAオリゴマーをPBSに20%濃度の注射液を製造した後に動物モデルとしてマウスを用い生体内に注射した後、5分後に形成されたゲルを示す写真である。
【発明を実施するための形態】
【0026】
以下、本発明の添付の図面を参照して、本発明の望ましい一実施例を詳しく説明するが、本発明はこれらの実施例により限定されるものではない。
【0027】
なお、図面中、同一の構成要素または部品に対してはできるだけ同一の符号を付す。また、本発明の説明において、関連公知の機能あるいは構成についての具体的な説明は、本発明の要旨を明確にするために省略する。
【0028】
本明細書において使われる程度の用語"約"、"相対的に"等は、言及された意味に固有の製造および物質許容誤差が提示された時はその数値またはその数値に近接した意味として使用され、本発明の理解のために正確にまたは絶対的な数値が言及されている開示内容を非良心的な侵害者が不当に利用することを防止するために使用する。
【0029】
ポリエチレングリコール系化合物とポリラクチド、ポリグリコリドとポリカプロラクトンなどの生分解性高分子単独およびそれらの共重合体化合物からなる従来技術の温度敏感性ブロック共重合体ポリマーヒドロゲルを単独で用いる場合、人体への注射時に生分解される過程で分解された副産物が、人体内に蓄積又は体外に排出される過程で様々な副作用を起こす恐れがある。
【0030】
このような従来技術の問題点を解決するために本発明者らは、脂肪族ポリエステル系疏水性高分子乃至親水性であり温度に敏感なポリエチレングリコール系化合物を全く用いず、pH変化によるイオン化度によって親水性又は疏水性を有するPAAオリゴマー単独で構成されたヒドロゲルを製造した。
【0031】
なお、前記ヒドロゲルは、比較的容易に製造され、人体内に注射したとき、低分子量により完全に体外に排出されるという特徴を有し、温度およびpHに敏感であるということを見出した。また、前記PAAオリゴマーヒドロゲルは、特定のpHでゾル-ゲル移転特性を示すことにより、体内と類似したpH7.0〜7.4付近でゲル化され、前記範囲以下ではゾル化されることにより、体内への注入時、従来の温度敏感性ヒドロゲルで見られた薬物の初期過多放出現象および注射針の詰まり現象が起こることなく、体内で安全にゲルを形成し、これにより、前記特定の温度および特定のpHで標的指向性を有し、徐放性放出が可能な薬物伝達体として応用できるということを見出した。
【0032】
本発明は、ポリ(アミドアミン)オリゴマー単独で構成された温度およびpH敏感性PAAオリゴマーヒドロゲルを提供する。
【0033】
本発明に係る温度およびpH敏感性PAAオリゴマーの数平均分子量(Mn)は500〜1,000であることが望ましい。前記範囲から外れる場合、すなわち、500未満の場合と1,000を超える場合、ゾル-ゲル移転が円滑に行われないだけでなく、ゲルが形成されてもゲルの強度などの弱化およびポリマーヒドロゲルの特性を示し、本発明において追求しようとする目的とは異なり実際に薬物伝達体として適用し難いこともある。
【0034】
本発明に係る温度およびpH敏感性PAAオリゴマーヒドロゲルは、例えば、下記反応式のように比較的簡単な1ステップ工程によって製造する。
[反応式]

式中、Rは1〜10の範囲のアルキル基である。
【0035】
前記反応式のように製造されたPAAオリゴマーヒドロゲルは、PAAの前駆物質のジアミン化合物の2次アミン基(-NH)とアルキレンビスアクリルアミド化合物のビニル基(CH2=CH-)とのカップリング(coupling)により製造される。
【0036】
前記反応の反応条件における反応温度および時間は特に制限がない。
【0037】
PAAオリゴマーヒドロゲルの製造に用いられるアルキレンビスアクリルアミド化合物は、N,N'-メチレンビスアクリルアミド(MDA)、N,N'-エチレンビスアクリルアミド、N,N'-ジイソプロピルアクリルアミド、1,4-ブチレンジアクリルアミド、1,6-ヘキシレンジアクリルアミド、1,8-オクチレンジアクリルアミド、1,10-デカンジアクリルアミドの単独又はこれらの混合物からなる群より選ばれる1以上である。
【0038】
また、本発明の前記2次アミン基を有するジアミン化合物は、4,4'-トリメチレンジピペリジン(4,4'-trimethylenepiperidine)、N,N'-ジメチルエチレンジアミン(N,N'-dimethylethylenediamine)、ピペラジン(piperazine)、2-メチルピペラジン(2-methylpiperazine)、3-メチル-4-(3-メチルフェニル)ピペラジン{3-methyl-4-(3-methylphenyl)piperazine}、3-メチルピペラジン(3-methylpiperazine)、4-(phenylmethyl)piperazine{4-(フェニルメチル)ピペラジン}、4-(1-フェニルエチル)ピペラジン{4-(1-phenylethyl)piperazine}、4-(1,1'-ジメトキシカルボニル)ピペラジン{4-(1,1'-dimethoxycarbonyl)piperazine}、4-(2-(ビス-(2-プロペニル)アミノ)エチル)ピペラジン{4-(2-(bis-(2-prophenyl)amino)ethyl)piperazine}、1-(2-アミノエチル)ピペラジン{1-(2-aminoethyl)piperazine}、4-(アミノメチル)ピペラジン{4-(aminomethyl)piperazine}、N,N'-ジメチル-1,2-エタンジアミン(N,N'-dimethyl-1,2-ethanediamine)、N,N'-ジエチル-1,2-エタンジアミン(N,N'-diethyl-1,2-ethanediamine)、N,N'-ジイソプロピル-1,2-エタンジアミン(N,N'-diisopropyl-1,2-ethanediamine)、N,N'-ジメチル-1,2-プロピルアミン(N,N'-dimethyl-1,2-propyldiamine)、N,N'-ジエチル-1,2-プロピルジアミン(N,N'-diethyl-1,2-propyldiamine)、N,N'-ジイソプロピル-1,2-プロピルアミン(N,N'-diisopropyl-1,2-propyldiamine)、N,N'-ジメチル-1,2-ヘキサンジアミン(N,N'-dimethyl-1,2-hexanediamine)、N,N'-ジメチル-N-(3-(メチルアミノ)プロピル]-1,3-プロパンジアミン{N,N-dimethyl-N-[3-(methylamino)propyl]-1,3-propanediamine}、N-[2-メチルアミノ)エトキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)ethoxyethyl]-N,N'-dimethylamine}、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)dioxyethyl]-N,N-dimethylamine}、1,4-ジアゼパン(1,4-diazepane)単独又はこれらの混合物からなる群より選ばれる1以上である。
【0039】
上記のような方法によって製造されたPAAオリゴマーは、FT-IRおよび1H-NMRを用いてそれぞれの官能基の導入および末端基の反応を確認でき、GPC(Gel Permeation Chromatography)を用いて重合体の分子量増加によりPAAオリゴマーの前駆物質がカップリングされた構造であることを確認することができた。また、pH敏感性を確認するために、温度に応じてpHを変化させながらゾル-ゲル移転の特性変化を測定し、これにより、本発明のPAAオリゴマーがpH敏感性特性を保有するといったことを確認することができた(図1参照)。
【0040】
また、本発明は、(a)温度およびpH敏感性PAAオリゴマーと、(b)前記PAAオリゴマー内に封入できる生理活性物質とを含む薬物伝達体を提供する。
【0041】
前記PAAオリゴマーヒドロゲルに封入できる生理活性物質は、特に制限せずいずれも使用でき、このような非制限的な例としては、インスリン、白血球増殖因子(G-CSF)、ヒト成長ホルモン(hGH)、エリスポエチン(Erythropoietin、EPO)、シムリン(Symlin)、エキセンディン(Exendin)、Somatokine等のような蛋白質;パクリタキセル(Paclitaxel)、ドセタキセル(Docetaxel)、クルロラムブシル(Chlorambucil)、インターフェロン(Interferon)、モノクローナル抗体(Monclonal antibodies)、ワクチンなどのような抗癌剤;抗菌剤;ステロイド類;消炎鎮痛剤;性ホルモン;免疫抑制剤;抗ウイルス剤;麻酔剤;制吐剤;抗ヒスタミン剤を含む。本発明の薬物伝達体は、賦形剤、安定化剤、pH調整剤、抗酸化剤、保存剤、結合剤、崩壊剤などのような当業界に知られている通常の添加剤及び/又は溶媒などをさらに含むことができる。
【0042】
また、前記PAAオリゴマーヒドロゲル薬物伝達体は、経口剤又は非経口剤の形態に製剤化して使用でき、静脈、筋肉又は皮下注射剤として製造することができる。
【0043】
さらに、本発明は、前記温度およびpH敏感性PAAオリゴマーヒドロゲルを薬物伝達用伝達体(carrier)として使用する方法を提供する。この際、PAAオリゴマーヒドロゲル内に含まれる物質は病気の治療、防止又は診断のための物質であれば特に制限がない。
【0044】
(実施例)
以下、実施例により本発明を詳しく説明する。
(実施例1〜9:ポリ(アミドアミン、PAA)オリゴマーの合成)
【0045】
[実施例1.PAAオリゴマーの製造]
4,4'-トリメチレンジピペリジン(4,4'-trimethylenedipiperidine、TMDP)30gをメタノール100mlに溶解させた後に1,10-デシレンアクリルアミド(1,10-decylenediacrylamide、DDA)を常温で添加して溶解させた後、50℃で24時間反応させ、反応終了後、未反応物を除去するために過量のアセトンに混合した後に非溶媒のクロロホルムに混合して3回沈殿させて得る。得られた沈殿物は真空乾燥器を用いて40℃で48時間真空乾燥させ、数平均分子量が500g/molのPAAオリゴマーを得、収率は70%以上であった。
【0046】
[実施例2]
PAAオリゴマーの数平均分子量が650であることを除いては、前記実施例1と同一の方法を行い、収得率は70%以上であった。
【0047】
[実施例3]
PAAオリゴマーの数平均分子量が850であることを除いては、前記実施例1と同一の方法を行い、収得率は70%以上であった。
【0048】
[実施例4]
PAAオリゴマーの数平均分子量が1,000であることを除いては、前記実施例1と同一の方法を行い、収得率は70%以上であった。
【0049】
[実施例5]
ジアミン化合物としてピペラジン(piperazine)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が500のPAAオリゴマーを得、収得率は70%以上であった。
【0050】
[実施例6]
ジアミン化合物としてピペラジン(piperazine)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が700のPAAオリゴマーを得、収得率は70%以上であった。
【0051】
[実施例7]
アルキレンビスアクリルアミド化合物として1,8-オクチレンジアクリルアミド(1,8-octylenediacrylamide、ODA)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が900のPAAオリゴマーを得、収得率は70%以上であった。
【0052】
[実施例8]
アルキレンビスアクリルアミド化合物として1,6-ヘキシレンジアクリルアミド(1,6-hexylenediacrylamide、HDA)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が900のPAAオリゴマーを得、収得率は70%以上であった。
【0053】
[実施例9]
アルキレンビスアクリルアミド化合物としてメチレンジアクリルアミド(methylenediacrylamide、HDA)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が900のPAAオリゴマーを得、収得率は70%以上であった。
【0054】
[比較例1]
PAAオリゴマーの数平均分子量が400であるものを使用したことを除いては、前記実施例1と同一の方法を行い、収得率は45%であった。
【0055】
[比較例2]
PAAオリゴマーの数平均分子量が1,200であるものを使用したことを除いては、前記実施例1と同一の方法を行い、収得率は50%であった。
【0056】
[実験例1.pH変化に応じたゾル-ゲル移転挙動の評価]
【0057】
本発明に従いPAAオリゴマーの温度およびpH変化に応じたゾル-ゲル移転挙動の評価を行った。
【0058】
実施例1から8で製造されたPAAオリゴマーを緩衝溶液に10重量%添加して溶かした後、50℃でNaOH溶液で滴定してそれぞれpH5.5、6.0、6.5、7.0、7.5に調節した。それぞれのpHを有するPAAオリゴマー溶液の温度を2℃ずつ上げながら、10分間一定の温度下で平衡状態になるようにした後、各溶液を傾けてゾル-ゲル移転挙動を測定した。温度およびpH変化に応じたブロック共重合体のゾル-ゲルの移転挙動を実施例7に基づいて図1に示した。
【0059】
図1および2に示したように、本発明のブロックPAAオリゴマーのpH変化に応じたイオン化度の変化および疏水性の変化によって、温度だけでなくpH変化によってゾル-ゲル移転挙動が可逆的に変化することを確認することができた。
【0060】
[実験例2.実施例のゲルの強度評価]
本発明により製造されたPAAオリゴマーの温度およびpH変化においてゾル-ゲル移転が起きた後のゲルの強度を調べるために温度に応じた粘度の測定を行った。
【0061】
実施例1〜9で製造されたPAAオリゴマーを緩衝溶液に30重量%添加して溶かした後、50℃でNaOH溶液で滴定してそれぞれpH7.4に調節して完全にゲル移転が起きて平衡状態になるようにした後、ヒドロゲルの粘度をGel rheometerで測定した。具体的に次のような条件下で、2つの平行板(parallel plate)で振動モード(Oscillation mode)にして測定した:制御された応力(controlled stress)=0.4 Pa、周波数(frequency)=1 rad/s、間隔(gap)=0.25mm、加熱速度(heating rate)=1℃/min。
【0062】
図3は、様々なpH値での温度に応じた実施例7で製造したヒドロゲルの粘度変化を示すグラフである。
【技術分野】
【0001】
本発明は、温度およびpH敏感性オリゴマーヒドロゲルおよびそれを用いた薬物伝達体(Drug delivery)に関し、特に、ポリ(アミドアミン)[poly(amidoamine、PAA)]オリゴマー単独で構成されるヒドロゲルおよびそれを用いた薬物伝達体に関する。
【背景技術】
【0002】
ポリマーヒドロゲルを用いた薬物伝達体の開発の例として、特許文献1には、生分解性ポリエステル高分子のA-B-A形態の3重ブロック共重合体について記載されているが、疏水性ブロック(A)は、ポリラクチド(PLA)、ポリグリコリド(PGA)およびこれらの共重合体で限定しており、親水性ブロック(B)もポリエチレングリコール(PEG)およびその誘導体で限定している。
【0003】
前記3重ブロック共重合体は、疏水性高分子と親水性高分子とのブロック共重合体(block copolymer)からなり、温度によってゾル-ゲル移転現象を起こす温度敏感性ブロック共重合体であって、前記ブロック共重合体をゾル(sol)状態の水溶液形態で体内に注入する場合、体温によってゲル(gel)状態に転移されることから、体内で安定に薬物を坦持して徐々に薬物を放出して伝達する徐放性薬物伝達体の支持体として活用している。しかしながら、温度にだけ敏感なゾル-ゲル移転特性を有するブロック共重合体を用いる場合、薬物と相互作用が弱いため、人体内への注射時に薬物の初期過多放出(initial burst release)現象が起き、体内に注射する過程では体内の温度により注射針の温度が体内の温度と熱的平衡に到達し、体内に完全に注入される前にゲル化が起きるため、注射針の詰まり現象(clogging)等の問題点があった。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】米国特許第5,476,909号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
本発明の目的は、比較的製造し易く、且つ体内から完全に排出され、温度およびpH変化によってゾル-ゲル移転を起こすPAAオリゴマーヒドロゲル、並びにその製造方法とそれを用いた薬物伝達体を提供することにある。
【0006】
なお、本発明の目的は、ヒドロゲル薬物伝達体として使用できるように薬物の初期過多放出(initial burst release)現象を抑制し、一定期間薬物の放出(sustained release)が起きるように分子設計された新概念の温度およびpH敏感性オリゴマーヒドロゲル、並びにその製造方法とそれを用いた生理活性物質を含むオリゴマーヒドロゲル薬物伝達体を提供することにある。
【0007】
なお、本発明の目的は、前記オリゴマーの構成成分、これらのモル比、及び分子量を適宜変更して癌細胞のような標的に指向性を有するだけでなく、遺伝子変移又は他の応用分野において標的指向性を有するようにデザインした温度およびpH敏感性オリゴマーヒドロゲル並びにその製造方法とそれを用いた薬物伝達体を提供することにある。
【課題を解決するための手段】
【0008】
上記の目的を達成するための本発明は、温度およびpH敏感性オリゴマーヒドロゲルにおいて、PAAオリゴマー単独で構成される温度およびpH敏感性オリゴマーヒドロゲルを提供する。
【0009】
また、本発明は、前記PAAオリゴマーが下記一般式(1)の低分子量の重合体のヒドロゲルを提供する。
【化1】

式中、Rは炭素原子数1〜10の範囲のアルキル基である。
【0010】
また、本発明は、前記PAAオリゴマーは、前駆体として1種以上のアルキレンビスアクリルアミド化合物の置換基と2次アミン基を有する1種以上のジアミン化合物の置換基との間のカップリング(coupling)により製造されるヒドロゲルを提供する。
【0011】
また、本発明は、前記PAAオリゴマーの分子量が500〜1,000g/molのヒドロゲルを提供する。
【0012】
また、本発明は、前記PAAオリゴマーがpH7.0〜7.4の範囲でヒドロゲルを形成し、pH3.0〜7.0未満でゾル状態を形成するオリゴマーヒドロゲルを提供する。
【0013】
また、本発明は、前記アルキレンビスアクリルアミド化合物が次のような一般式(2)からなるオリゴマーヒドロゲル を提供する。
【化2】

式中、Rは炭素原子数1〜10のアルキル基である。
【0014】
また、本発明の前記アルキレンビスアクリルアミド化合物は、N,N'-メチレンビスアクリルアミド(MDA)、N,N'-エチレンビスアクリルアミド、N,N'-ジイソプロピルアクリルアミド、1,4-ブチレンジアクリルアミド、1,6-ヘキシレンジアクリルアミド、1,8-オクチレンジアクリルアミド、1,10-デカンジアクリルアミドの単独又はこれらの混合物からなる群より1以上選ばれるオリゴマーヒドロゲルを提供する。
【0015】
また、本発明は、前記ジアミン化合物が次のような一般式(3)からなる2次アミン含有ジアミン化合物又はこれらの混合物のオリゴマーヒドロゲルを提供する。
【化3】

式中、R1およびR2は炭素原子数1〜10のアルキル基である。
【0016】
また、本発明の前記2次アミン基を有するジアミン化合物は、4,4'-トリメチレンジピペリジン(4,4'-trimethylenepiperidine)、N,N'-ジメチルエチレンジアミン(N,N'-dimethylethylenediamine)、ピペラジン(piperazine)、2-メチルピペラジン(2-methylpiperazine)、3-メチル-4-(3-メチルフェニル)ピペラジン{3-methyl-4-(3-methylphenyl)piperazine}、3-メチルピペラジン(3-methylpiperazine)、4-(phenylmethyl)piperazine{4-(フェニルメチル)ピペラジン}、4-(1-フェニルエチル)ピペラジン{4-(1-phenylethyl)piperazine}、4-(1,1'-ジメトキシカルボニル)ピペラジン{4-(1,1'-dimethoxycarbonyl)piperazine}、4-(2-(ビス-(2-プロペニル)アミノ)エチル)ピペラジン{4-(2-(bis-(2-propenyl)amino)ethyl)piperazine}、1-(2-アミノエチル)ピペラジン{1-(2-aminoethyl)piperazine}、4-(アミノメチル)ピペラジン{4-(aminomethyl)piperazine}、N,N'-ジメチル-1,2-エタンジアミン(N,N'-dimethyl-1,2-ethanediamine)、N,N'-ジエチル-1,2-エタンジアミン(N,N'-diethyl-1,2-ethanediamine)、N,N'-ジイソプロピル-1,2-エタンジアミン(N,N'-diisopropyl-1,2-ethanediamine)、N,N'-ジメチル-1,2-プロピルアミン(N,N'-dimethyl-1,2-propyldiamine)、N,N'-ジエチル-1,2-プロピルジアミン(N,N'-diethyl-1,2-propyldiamine)、N,N'-ジイソプロピル-1,2-プロピルアミン(N,N'-diisopropyl-1,2-propyldiamine)、N,N'-ジメチル-1,2-ヘキサンジアミン(N,N'-dimethyl-1,2-hexanediamine)、N,N'-ジメチル-N-(3-(メチルアミノ)プロピル]-1,3-プロパンジアミン{N,N-dimethyl-N-[3-(methylamino)propyl]-1,3-propanediamine}、N-[2-メチルアミノ)エトキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)ethoxyethyl]-N,N'-dimethylamine}、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)dioxyethyl]-N,N'-dimethylamine}、1,4-ジアゼパン(1,4-diazepane)単独又はこれらの混合物からなる群より1以上選ばれるオリゴマーヒドロゲルを提供する。
【0017】
また、本発明のPAAオリゴマーは、上述したアルキレンビスアクリルアミド化合物と2次アミン基を有するジアミン化合物との反応モル比が1:10〜50のオリゴマーヒドロゲルを提供する。
【0018】
また、本発明は、前記PAAオリゴマーヒドロゲルからなる薬物伝達体を提供する。
【0019】
また、本発明は、前記PAAオリゴマーヒドロゲル内に封入できる生理活性物質としてインスリン(insulin)、白血球増殖因子(G-CSF)、ヒト成長ホルモン(hGH)、エリスポエチン(Erythropoietin、EPO)、シムリン(Symlin)、エキセンディン(Exendin)、Somatokineのような蛋白質;パクリタキセル(Paclitaxel)、ドセタキセル(Docetaxel)、クロラムブシル(Chlorambucil)、インターフェロン(Interferon)、モノクローナル抗体(Monoclonal antibodies)、ワクチンなどのような抗癌剤;抗菌剤;ステロイド類;消炎鎮痛剤;性ホルモン;免疫抑制剤;抗ウイルス剤;麻酔剤;制吐剤;又は抗ヒスタミン剤を含むことができ、賦形剤、安定化剤、pH調整剤、抗酸化剤、保存剤、結合剤、崩壊剤などのような添加剤及び/又は溶媒などをさらに含むことができる薬物伝達体を提供する。
【0020】
また、本発明は、前記伝達体が経口剤又は非経口剤であり、望ましくは静脈、筋肉又は皮下注射剤形態の薬物伝達体を提供する。
【発明の効果】
【0021】
上述のように本発明に係るPAAオリゴマーヒドロゲルは、1ステップ工程によって製造され、人体内への注射時にPAAオリゴマー自体が分子量1000以下の低分子量であるため、人体内に蓄積されず、直に体外に排出されるという特徴があり、カップリング反応によりPAAオリゴマーを製造する前駆体の2次アミン基はpH変化に応じたイオン化度によって親水性又は疏水性を有するため、温度敏感性以外にpH敏感性も同時に付与され、上述した従来の温度敏感性ポリマーヒドロゲルの問題点を解決することができる。
【0022】
また、本発明に係るオリゴマーヒドロゲルは、特定のpH、例えば、体内正常細胞のpH範囲であるpH7.0〜7.4では安定し、癌細胞のような非正常細胞のpH範囲であるpH3.0〜7.0未満ではゾル(sol)状態に転移されることにより、癌細胞に標的指向性を有する薬物放出用伝達体として用いることができる。すなわち、低いpH(pH7.0未満)でポリ(アミドアミン)(PAA)オリゴマーに存在する2次アミンのイオン化度の増加によりPAA全体が水溶性に変わりゾル状態を維持することになり、pH7.0以上ではPAAのイオン化度が低下して疏水性特性を示すため、ゲル状態を形成する。上記のような特性により、本発明のPAAオリゴマーヒドロゲルは、温度だけでなくpHに敏感なゾル-ゲル移転特性を示す。
【0023】
また、本発明に係るPAAオリゴマーヒドロゲルは、体内で安全なので、医療用、遺伝子伝達、薬物伝達分野、特に薬物担持がおよび放出などの徐放性薬物伝達体に適用できるだけでなく、病の診断のための物質を非正常細胞に伝達することにより、画像診断(diagnostic imaging)等の診断用途に応用することができる。
【0024】
また、本発明に係るPAAオリゴマーヒドロゲルは、正常体内条件と同一のpH7.0〜7.4の範囲ではヒドロゲルを形成し、癌細胞のような非正常条件のpH7.0未満ではゾル状態を維持して癌細胞に標的指向性を有するデザインを適用し、さらに、前記オリゴマーヒドロゲルの構成成分、これらのモル比、分子量および/又はブロック内の官能基を適宜変更することにより、癌細胞だけでなく遺伝子変移又は他の応用分野において標的指向性を有するようにデザインした。
【図面の簡単な説明】
【0025】
【図1】実施例7で製造したPAAオリゴマーの様々な濃度での温度およびpH変化によるゾル-ゲルの移転挙動を示すグラフである。
【図2】温度およびpHによる実施例3、7、8及び9で製造したPAAオリゴマーのゾル-ゲルの移転挙動を示すグラフである。
【図3】様々なpHでの温度増加に応じた実施例7で製造したPAAオリゴマーの粘度の変化を示すグラフである。
【図4】実施例7のPAAオリゴマーをPBSに20%濃度の注射液を製造した後に動物モデルとしてマウスを用い生体内に注射した後、5分後に形成されたゲルを示す写真である。
【発明を実施するための形態】
【0026】
以下、本発明の添付の図面を参照して、本発明の望ましい一実施例を詳しく説明するが、本発明はこれらの実施例により限定されるものではない。
【0027】
なお、図面中、同一の構成要素または部品に対してはできるだけ同一の符号を付す。また、本発明の説明において、関連公知の機能あるいは構成についての具体的な説明は、本発明の要旨を明確にするために省略する。
【0028】
本明細書において使われる程度の用語"約"、"相対的に"等は、言及された意味に固有の製造および物質許容誤差が提示された時はその数値またはその数値に近接した意味として使用され、本発明の理解のために正確にまたは絶対的な数値が言及されている開示内容を非良心的な侵害者が不当に利用することを防止するために使用する。
【0029】
ポリエチレングリコール系化合物とポリラクチド、ポリグリコリドとポリカプロラクトンなどの生分解性高分子単独およびそれらの共重合体化合物からなる従来技術の温度敏感性ブロック共重合体ポリマーヒドロゲルを単独で用いる場合、人体への注射時に生分解される過程で分解された副産物が、人体内に蓄積又は体外に排出される過程で様々な副作用を起こす恐れがある。
【0030】
このような従来技術の問題点を解決するために本発明者らは、脂肪族ポリエステル系疏水性高分子乃至親水性であり温度に敏感なポリエチレングリコール系化合物を全く用いず、pH変化によるイオン化度によって親水性又は疏水性を有するPAAオリゴマー単独で構成されたヒドロゲルを製造した。
【0031】
なお、前記ヒドロゲルは、比較的容易に製造され、人体内に注射したとき、低分子量により完全に体外に排出されるという特徴を有し、温度およびpHに敏感であるということを見出した。また、前記PAAオリゴマーヒドロゲルは、特定のpHでゾル-ゲル移転特性を示すことにより、体内と類似したpH7.0〜7.4付近でゲル化され、前記範囲以下ではゾル化されることにより、体内への注入時、従来の温度敏感性ヒドロゲルで見られた薬物の初期過多放出現象および注射針の詰まり現象が起こることなく、体内で安全にゲルを形成し、これにより、前記特定の温度および特定のpHで標的指向性を有し、徐放性放出が可能な薬物伝達体として応用できるということを見出した。
【0032】
本発明は、ポリ(アミドアミン)オリゴマー単独で構成された温度およびpH敏感性PAAオリゴマーヒドロゲルを提供する。
【0033】
本発明に係る温度およびpH敏感性PAAオリゴマーの数平均分子量(Mn)は500〜1,000であることが望ましい。前記範囲から外れる場合、すなわち、500未満の場合と1,000を超える場合、ゾル-ゲル移転が円滑に行われないだけでなく、ゲルが形成されてもゲルの強度などの弱化およびポリマーヒドロゲルの特性を示し、本発明において追求しようとする目的とは異なり実際に薬物伝達体として適用し難いこともある。
【0034】
本発明に係る温度およびpH敏感性PAAオリゴマーヒドロゲルは、例えば、下記反応式のように比較的簡単な1ステップ工程によって製造する。
[反応式]

式中、Rは1〜10の範囲のアルキル基である。
【0035】
前記反応式のように製造されたPAAオリゴマーヒドロゲルは、PAAの前駆物質のジアミン化合物の2次アミン基(-NH)とアルキレンビスアクリルアミド化合物のビニル基(CH2=CH-)とのカップリング(coupling)により製造される。
【0036】
前記反応の反応条件における反応温度および時間は特に制限がない。
【0037】
PAAオリゴマーヒドロゲルの製造に用いられるアルキレンビスアクリルアミド化合物は、N,N'-メチレンビスアクリルアミド(MDA)、N,N'-エチレンビスアクリルアミド、N,N'-ジイソプロピルアクリルアミド、1,4-ブチレンジアクリルアミド、1,6-ヘキシレンジアクリルアミド、1,8-オクチレンジアクリルアミド、1,10-デカンジアクリルアミドの単独又はこれらの混合物からなる群より選ばれる1以上である。
【0038】
また、本発明の前記2次アミン基を有するジアミン化合物は、4,4'-トリメチレンジピペリジン(4,4'-trimethylenepiperidine)、N,N'-ジメチルエチレンジアミン(N,N'-dimethylethylenediamine)、ピペラジン(piperazine)、2-メチルピペラジン(2-methylpiperazine)、3-メチル-4-(3-メチルフェニル)ピペラジン{3-methyl-4-(3-methylphenyl)piperazine}、3-メチルピペラジン(3-methylpiperazine)、4-(phenylmethyl)piperazine{4-(フェニルメチル)ピペラジン}、4-(1-フェニルエチル)ピペラジン{4-(1-phenylethyl)piperazine}、4-(1,1'-ジメトキシカルボニル)ピペラジン{4-(1,1'-dimethoxycarbonyl)piperazine}、4-(2-(ビス-(2-プロペニル)アミノ)エチル)ピペラジン{4-(2-(bis-(2-prophenyl)amino)ethyl)piperazine}、1-(2-アミノエチル)ピペラジン{1-(2-aminoethyl)piperazine}、4-(アミノメチル)ピペラジン{4-(aminomethyl)piperazine}、N,N'-ジメチル-1,2-エタンジアミン(N,N'-dimethyl-1,2-ethanediamine)、N,N'-ジエチル-1,2-エタンジアミン(N,N'-diethyl-1,2-ethanediamine)、N,N'-ジイソプロピル-1,2-エタンジアミン(N,N'-diisopropyl-1,2-ethanediamine)、N,N'-ジメチル-1,2-プロピルアミン(N,N'-dimethyl-1,2-propyldiamine)、N,N'-ジエチル-1,2-プロピルジアミン(N,N'-diethyl-1,2-propyldiamine)、N,N'-ジイソプロピル-1,2-プロピルアミン(N,N'-diisopropyl-1,2-propyldiamine)、N,N'-ジメチル-1,2-ヘキサンジアミン(N,N'-dimethyl-1,2-hexanediamine)、N,N'-ジメチル-N-(3-(メチルアミノ)プロピル]-1,3-プロパンジアミン{N,N-dimethyl-N-[3-(methylamino)propyl]-1,3-propanediamine}、N-[2-メチルアミノ)エトキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)ethoxyethyl]-N,N'-dimethylamine}、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)dioxyethyl]-N,N-dimethylamine}、1,4-ジアゼパン(1,4-diazepane)単独又はこれらの混合物からなる群より選ばれる1以上である。
【0039】
上記のような方法によって製造されたPAAオリゴマーは、FT-IRおよび1H-NMRを用いてそれぞれの官能基の導入および末端基の反応を確認でき、GPC(Gel Permeation Chromatography)を用いて重合体の分子量増加によりPAAオリゴマーの前駆物質がカップリングされた構造であることを確認することができた。また、pH敏感性を確認するために、温度に応じてpHを変化させながらゾル-ゲル移転の特性変化を測定し、これにより、本発明のPAAオリゴマーがpH敏感性特性を保有するといったことを確認することができた(図1参照)。
【0040】
また、本発明は、(a)温度およびpH敏感性PAAオリゴマーと、(b)前記PAAオリゴマー内に封入できる生理活性物質とを含む薬物伝達体を提供する。
【0041】
前記PAAオリゴマーヒドロゲルに封入できる生理活性物質は、特に制限せずいずれも使用でき、このような非制限的な例としては、インスリン、白血球増殖因子(G-CSF)、ヒト成長ホルモン(hGH)、エリスポエチン(Erythropoietin、EPO)、シムリン(Symlin)、エキセンディン(Exendin)、Somatokine等のような蛋白質;パクリタキセル(Paclitaxel)、ドセタキセル(Docetaxel)、クルロラムブシル(Chlorambucil)、インターフェロン(Interferon)、モノクローナル抗体(Monclonal antibodies)、ワクチンなどのような抗癌剤;抗菌剤;ステロイド類;消炎鎮痛剤;性ホルモン;免疫抑制剤;抗ウイルス剤;麻酔剤;制吐剤;抗ヒスタミン剤を含む。本発明の薬物伝達体は、賦形剤、安定化剤、pH調整剤、抗酸化剤、保存剤、結合剤、崩壊剤などのような当業界に知られている通常の添加剤及び/又は溶媒などをさらに含むことができる。
【0042】
また、前記PAAオリゴマーヒドロゲル薬物伝達体は、経口剤又は非経口剤の形態に製剤化して使用でき、静脈、筋肉又は皮下注射剤として製造することができる。
【0043】
さらに、本発明は、前記温度およびpH敏感性PAAオリゴマーヒドロゲルを薬物伝達用伝達体(carrier)として使用する方法を提供する。この際、PAAオリゴマーヒドロゲル内に含まれる物質は病気の治療、防止又は診断のための物質であれば特に制限がない。
【0044】
(実施例)
以下、実施例により本発明を詳しく説明する。
(実施例1〜9:ポリ(アミドアミン、PAA)オリゴマーの合成)
【0045】
[実施例1.PAAオリゴマーの製造]
4,4'-トリメチレンジピペリジン(4,4'-trimethylenedipiperidine、TMDP)30gをメタノール100mlに溶解させた後に1,10-デシレンアクリルアミド(1,10-decylenediacrylamide、DDA)を常温で添加して溶解させた後、50℃で24時間反応させ、反応終了後、未反応物を除去するために過量のアセトンに混合した後に非溶媒のクロロホルムに混合して3回沈殿させて得る。得られた沈殿物は真空乾燥器を用いて40℃で48時間真空乾燥させ、数平均分子量が500g/molのPAAオリゴマーを得、収率は70%以上であった。
【0046】
[実施例2]
PAAオリゴマーの数平均分子量が650であることを除いては、前記実施例1と同一の方法を行い、収得率は70%以上であった。
【0047】
[実施例3]
PAAオリゴマーの数平均分子量が850であることを除いては、前記実施例1と同一の方法を行い、収得率は70%以上であった。
【0048】
[実施例4]
PAAオリゴマーの数平均分子量が1,000であることを除いては、前記実施例1と同一の方法を行い、収得率は70%以上であった。
【0049】
[実施例5]
ジアミン化合物としてピペラジン(piperazine)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が500のPAAオリゴマーを得、収得率は70%以上であった。
【0050】
[実施例6]
ジアミン化合物としてピペラジン(piperazine)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が700のPAAオリゴマーを得、収得率は70%以上であった。
【0051】
[実施例7]
アルキレンビスアクリルアミド化合物として1,8-オクチレンジアクリルアミド(1,8-octylenediacrylamide、ODA)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が900のPAAオリゴマーを得、収得率は70%以上であった。
【0052】
[実施例8]
アルキレンビスアクリルアミド化合物として1,6-ヘキシレンジアクリルアミド(1,6-hexylenediacrylamide、HDA)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が900のPAAオリゴマーを得、収得率は70%以上であった。
【0053】
[実施例9]
アルキレンビスアクリルアミド化合物としてメチレンジアクリルアミド(methylenediacrylamide、HDA)を使用したことを除いては、前記実施例1と同一の方法を行って分子量が900のPAAオリゴマーを得、収得率は70%以上であった。
【0054】
[比較例1]
PAAオリゴマーの数平均分子量が400であるものを使用したことを除いては、前記実施例1と同一の方法を行い、収得率は45%であった。
【0055】
[比較例2]
PAAオリゴマーの数平均分子量が1,200であるものを使用したことを除いては、前記実施例1と同一の方法を行い、収得率は50%であった。
【0056】
[実験例1.pH変化に応じたゾル-ゲル移転挙動の評価]
【0057】
本発明に従いPAAオリゴマーの温度およびpH変化に応じたゾル-ゲル移転挙動の評価を行った。
【0058】
実施例1から8で製造されたPAAオリゴマーを緩衝溶液に10重量%添加して溶かした後、50℃でNaOH溶液で滴定してそれぞれpH5.5、6.0、6.5、7.0、7.5に調節した。それぞれのpHを有するPAAオリゴマー溶液の温度を2℃ずつ上げながら、10分間一定の温度下で平衡状態になるようにした後、各溶液を傾けてゾル-ゲル移転挙動を測定した。温度およびpH変化に応じたブロック共重合体のゾル-ゲルの移転挙動を実施例7に基づいて図1に示した。
【0059】
図1および2に示したように、本発明のブロックPAAオリゴマーのpH変化に応じたイオン化度の変化および疏水性の変化によって、温度だけでなくpH変化によってゾル-ゲル移転挙動が可逆的に変化することを確認することができた。
【0060】
[実験例2.実施例のゲルの強度評価]
本発明により製造されたPAAオリゴマーの温度およびpH変化においてゾル-ゲル移転が起きた後のゲルの強度を調べるために温度に応じた粘度の測定を行った。
【0061】
実施例1〜9で製造されたPAAオリゴマーを緩衝溶液に30重量%添加して溶かした後、50℃でNaOH溶液で滴定してそれぞれpH7.4に調節して完全にゲル移転が起きて平衡状態になるようにした後、ヒドロゲルの粘度をGel rheometerで測定した。具体的に次のような条件下で、2つの平行板(parallel plate)で振動モード(Oscillation mode)にして測定した:制御された応力(controlled stress)=0.4 Pa、周波数(frequency)=1 rad/s、間隔(gap)=0.25mm、加熱速度(heating rate)=1℃/min。
【0062】
図3は、様々なpH値での温度に応じた実施例7で製造したヒドロゲルの粘度変化を示すグラフである。
【特許請求の範囲】
【請求項1】
ポリ(アミドアミン)(PAA)オリゴマー単独で構成された温度およびpH敏感性薬物伝達用PAAオリゴマーヒドロゲル。
【請求項2】
前記PAAオリゴマーは下記一般式(1)である請求項1に記載のヒドロゲル。
【化1】

式中、Rは炭素原子数1〜10範囲のアルキル基である。
【請求項3】
前記PAAオリゴマーの数平均分子量(Mn)は500〜1,000である請求項1に記載のヒドロゲル。
【請求項4】
前記PAAオリゴマーの前駆体としては、1種以上のアルキレンビスアクリルアミドの置換基と、1種以上の2次アミン基を有するジアミン化合物の置換基との間のカップリング(coupling)により製造される請求項1に記載のヒドロゲル。
【請求項5】
前記アルキレンビスアクリルアミド化合物は、N,N'-メチレンビスアクリルアミド(MDA)、N,N'-エチレンビスアクリルアミド、N,N'-ジイソプロピルアクリルアミド、1,4-ブチレンジアクリルアミド、1,6-ヘキシレンジアクリルアミド、1,8-オクチレンジアクリルアミド、1,10-デカンジアクリルアミドの単独又はこれらの混合物からなる群より1以上選ばれる請求項4に記載のヒドロゲル。
【請求項6】
前記2次アミン基を有するジアミン化合物は、4,4'-トリメチレンジピペリジン(4,4'-trimethylenepiperidine)、N,N'-ジメチルエチレンジアミン(N,N'-dimethylethylenediamine)、ピペラジン(piperazine)、2-メチルピペラジン(2-methylpiperazine)、3-メチル-4-(3-メチルフェニル)ピペラジン{3-methyl-4-(3-methylphenyl)piperazine}、3-メチルピペラジン(3-methylpiperazine)、4-(phenylmethyl)piperazine{4-(フェニルメチル)ピペラジン}、4-(1-フェニルエチル)ピペラジン{4-(1-phenylethyl) piperazine}、4-(1,1'-ジメトキシカルボニル)ピペラジン{4-(1,1'-dimethoxycarbonyl)piperazine}、4-(2-(ビス-(2-プロペニル)アミノ)エチル)ピペラジン{4-(2-(bis-(2-prophenyl)amino)ethyl)piperazine}、1-(2-アミノエチル)ピペラジン{1-(2-aminoethyl)piperazine}、4-(アミノメチル)ピペラジン{4-(aminomethyl)piperazine}、N,N'-ジメチル-1,2-エタンジアミン(N,N'-dimethyl-1,2-ethanediamine)、N,N'-ジエチル-1,2-エタンジアミン(N,N'-diethyl-1,2-ethanediamine)、N,N'-ジイソプロピル-1,2-エタンジアミン(N,N'-diisopropyl-1,2-ethanediamine)、N,N'-ジメチル-1,2-プロピルアミン(N,N'-dimethyl-1,2-propyldiamine)、N,N'-ジエチル-1,2-プロピルジアミン(N,N'-diethyl-1,2-propyldiamine)、N,N'-ジイソプロピル-1,2-プロピルアミン(N,N'-diisopropyl-1,2- propyldiamine)、N,N'-ジメチル-1,2-ヘキサンジアミン(N,N'-dimethyl-1,2-hexanediamine)、N,N'-ジメチル-N-(3-(メチルアミノ)プロピル]-1,3-プロパンジアミン{N,N-dimethyl-N-[3-(methylamino)propyl]-1,3-propanediamine}、N-[2-メチルアミノ)エトキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)ethoxyethyl]-N,N'-dimethylamine}、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)dioxyethyl]-N,N'-dimethylamine}、1,4-ジアゼパン(1,4-diazepane)単独又はこれらの混合物である請求項4に記載のヒドロゲル。
【請求項7】
アルキレンビスアクリルアミド化合物と2次アミン基を有するジアミン化合物との反応モル比は1:10〜50である請求項4に記載のヒドロゲル。
【請求項8】
前記PAAオリゴマーは、pH7.0〜7.4でヒドロゲルを形成し、pH3.0〜7.0未満でゾル状態を形成する請求項4に記載のヒドロゲル。
【請求項9】
請求項1〜8のうちいずれか1項に記載のPAAオリゴマーヒドロゲルからなる薬物伝達体。
【請求項10】
請求項1〜8のうちいずれか1項に記載のPAAオリゴマーヒドロゲルと、
前記オリゴマーヒドロゲル内に封入できる生理活性物質とを含む薬物伝達体。
【請求項11】
前記ブロック共重合体内に封入できる生理活性物質は、インスリン(insulin)、白血球増殖因子(G-CSF)、ヒト成長ホルモン(hGH)、エリスポエチン(Erythropoietin、EPO)、シムリン(Symlin)、エキセンディン(Exendin)、Somatokine等のような蛋白質;パクリタキセル(Paclitaxel)、クロラムブシル(Chlorambucil)、インターフェロン(Interferon)、モノクローナル抗体(Monoclonal antibodies)、ワクチンなどのような抗癌剤;抗菌剤;ステロイド類;消炎鎮痛剤;性ホルモン;免疫抑制剤;抗ウイルス剤;麻酔剤;制吐剤及び抗ヒスタミン剤から選ばれ、前記薬物伝達体は、賦形剤、安定化剤、pH調整剤、抗酸化剤、保存剤、結合剤と崩壊剤を含む添加剤及び溶媒から選ばれる1種以上をさらに含む請求項10に記載の薬物伝達体。
【請求項12】
前記伝達体は、経口剤又は非経口剤であり、望ましくは静脈、筋肉又は皮下注射剤の形態である請求項10に記載の薬物伝達体。
【請求項1】
ポリ(アミドアミン)(PAA)オリゴマー単独で構成された温度およびpH敏感性薬物伝達用PAAオリゴマーヒドロゲル。
【請求項2】
前記PAAオリゴマーは下記一般式(1)である請求項1に記載のヒドロゲル。
【化1】

式中、Rは炭素原子数1〜10範囲のアルキル基である。
【請求項3】
前記PAAオリゴマーの数平均分子量(Mn)は500〜1,000である請求項1に記載のヒドロゲル。
【請求項4】
前記PAAオリゴマーの前駆体としては、1種以上のアルキレンビスアクリルアミドの置換基と、1種以上の2次アミン基を有するジアミン化合物の置換基との間のカップリング(coupling)により製造される請求項1に記載のヒドロゲル。
【請求項5】
前記アルキレンビスアクリルアミド化合物は、N,N'-メチレンビスアクリルアミド(MDA)、N,N'-エチレンビスアクリルアミド、N,N'-ジイソプロピルアクリルアミド、1,4-ブチレンジアクリルアミド、1,6-ヘキシレンジアクリルアミド、1,8-オクチレンジアクリルアミド、1,10-デカンジアクリルアミドの単独又はこれらの混合物からなる群より1以上選ばれる請求項4に記載のヒドロゲル。
【請求項6】
前記2次アミン基を有するジアミン化合物は、4,4'-トリメチレンジピペリジン(4,4'-trimethylenepiperidine)、N,N'-ジメチルエチレンジアミン(N,N'-dimethylethylenediamine)、ピペラジン(piperazine)、2-メチルピペラジン(2-methylpiperazine)、3-メチル-4-(3-メチルフェニル)ピペラジン{3-methyl-4-(3-methylphenyl)piperazine}、3-メチルピペラジン(3-methylpiperazine)、4-(phenylmethyl)piperazine{4-(フェニルメチル)ピペラジン}、4-(1-フェニルエチル)ピペラジン{4-(1-phenylethyl) piperazine}、4-(1,1'-ジメトキシカルボニル)ピペラジン{4-(1,1'-dimethoxycarbonyl)piperazine}、4-(2-(ビス-(2-プロペニル)アミノ)エチル)ピペラジン{4-(2-(bis-(2-prophenyl)amino)ethyl)piperazine}、1-(2-アミノエチル)ピペラジン{1-(2-aminoethyl)piperazine}、4-(アミノメチル)ピペラジン{4-(aminomethyl)piperazine}、N,N'-ジメチル-1,2-エタンジアミン(N,N'-dimethyl-1,2-ethanediamine)、N,N'-ジエチル-1,2-エタンジアミン(N,N'-diethyl-1,2-ethanediamine)、N,N'-ジイソプロピル-1,2-エタンジアミン(N,N'-diisopropyl-1,2-ethanediamine)、N,N'-ジメチル-1,2-プロピルアミン(N,N'-dimethyl-1,2-propyldiamine)、N,N'-ジエチル-1,2-プロピルジアミン(N,N'-diethyl-1,2-propyldiamine)、N,N'-ジイソプロピル-1,2-プロピルアミン(N,N'-diisopropyl-1,2- propyldiamine)、N,N'-ジメチル-1,2-ヘキサンジアミン(N,N'-dimethyl-1,2-hexanediamine)、N,N'-ジメチル-N-(3-(メチルアミノ)プロピル]-1,3-プロパンジアミン{N,N-dimethyl-N-[3-(methylamino)propyl]-1,3-propanediamine}、N-[2-メチルアミノ)エトキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)ethoxyethyl]-N,N'-dimethylamine}、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン、N-[2-メチルアミノ)ジオキシエチル]-N,N'-ジメチルアミン{N-[2-methylamino)dioxyethyl]-N,N'-dimethylamine}、1,4-ジアゼパン(1,4-diazepane)単独又はこれらの混合物である請求項4に記載のヒドロゲル。
【請求項7】
アルキレンビスアクリルアミド化合物と2次アミン基を有するジアミン化合物との反応モル比は1:10〜50である請求項4に記載のヒドロゲル。
【請求項8】
前記PAAオリゴマーは、pH7.0〜7.4でヒドロゲルを形成し、pH3.0〜7.0未満でゾル状態を形成する請求項4に記載のヒドロゲル。
【請求項9】
請求項1〜8のうちいずれか1項に記載のPAAオリゴマーヒドロゲルからなる薬物伝達体。
【請求項10】
請求項1〜8のうちいずれか1項に記載のPAAオリゴマーヒドロゲルと、
前記オリゴマーヒドロゲル内に封入できる生理活性物質とを含む薬物伝達体。
【請求項11】
前記ブロック共重合体内に封入できる生理活性物質は、インスリン(insulin)、白血球増殖因子(G-CSF)、ヒト成長ホルモン(hGH)、エリスポエチン(Erythropoietin、EPO)、シムリン(Symlin)、エキセンディン(Exendin)、Somatokine等のような蛋白質;パクリタキセル(Paclitaxel)、クロラムブシル(Chlorambucil)、インターフェロン(Interferon)、モノクローナル抗体(Monoclonal antibodies)、ワクチンなどのような抗癌剤;抗菌剤;ステロイド類;消炎鎮痛剤;性ホルモン;免疫抑制剤;抗ウイルス剤;麻酔剤;制吐剤及び抗ヒスタミン剤から選ばれ、前記薬物伝達体は、賦形剤、安定化剤、pH調整剤、抗酸化剤、保存剤、結合剤と崩壊剤を含む添加剤及び溶媒から選ばれる1種以上をさらに含む請求項10に記載の薬物伝達体。
【請求項12】
前記伝達体は、経口剤又は非経口剤であり、望ましくは静脈、筋肉又は皮下注射剤の形態である請求項10に記載の薬物伝達体。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2011−178775(P2011−178775A)
【公開日】平成23年9月15日(2011.9.15)
【国際特許分類】
【出願番号】特願2010−246854(P2010−246854)
【出願日】平成22年11月2日(2010.11.2)
【出願人】(509017594)成均館大学校 産学協力団 (10)
【氏名又は名称原語表記】SUNGKYUNKWAN UNIVERSITY Foundation for Corporate Collaboration
【住所又は居所原語表記】300 Cheoncheon−dong, Jangan−gu, Suwon−si, Gyeonggi−do 440−746, Republic of Korea
【Fターム(参考)】
【公開日】平成23年9月15日(2011.9.15)
【国際特許分類】
【出願日】平成22年11月2日(2010.11.2)
【出願人】(509017594)成均館大学校 産学協力団 (10)
【氏名又は名称原語表記】SUNGKYUNKWAN UNIVERSITY Foundation for Corporate Collaboration
【住所又は居所原語表記】300 Cheoncheon−dong, Jangan−gu, Suwon−si, Gyeonggi−do 440−746, Republic of Korea
【Fターム(参考)】
[ Back to top ]

