薬物検知方法および装置
【課題】専門家でなくとも安全に使用して短時間で結果の得られる生体試料中の不正薬物の検知方法および装置を提供することにある。
【解決手段】生体から採取した液状サンプルを吸湿性のある布1に滴下した後に加熱・気化し、生成したガスを空気とともにコロナ放電中に導いてイオン化した後に生成したイオンをイオントラップ型質量分析計により検知する。検知した信号値があらかじめ定められた一定値以上であることを条件に当該薬物の存在を判定し、表示する。
【解決手段】生体から採取した液状サンプルを吸湿性のある布1に滴下した後に加熱・気化し、生成したガスを空気とともにコロナ放電中に導いてイオン化した後に生成したイオンをイオントラップ型質量分析計により検知する。検知した信号値があらかじめ定められた一定値以上であることを条件に当該薬物の存在を判定し、表示する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は薬物検知方法および装置に係り、特に不正薬物使用者に由来する生体試料からの薬物検知方法および装置に関するものである。
【背景技術】
【0002】
不正薬物の検知には、指示試薬を用いたキットが用いられている。しかし、キットでは各々の薬物に対応した指示薬が必要となり、候補薬物が絞れないときには多くの指示薬を準備する必要がある。また、新しい薬物に対しては指示薬自体の開発が出来るまでは対応できない問題がある。さらに、反応や操作に時間がかかるものもあり、結果が得られるまでに10分オーダーの時間が必要となることもある。
【0003】
これに対して、特許文献1には、イオンモビリティー分光法(IMS:Ion Mobility Spectrometry)を用いた装置が記載されている。IMSはあらかじめ薬物のスペクトルを採取することにより新しい薬物にも対応でき、また検知時間も10秒オーダーと短い。しかし、共存物の多い試料では共存物とのスペクトル上での分離が薬物によっては問題となる。また、有害な放射性物質やドーパントなどの化学物質の使用が必要である。さらに、IMSは水の影響を受けやすく、尿等の水を主成分とする生体試料にはそのままでは適用できない。
【0004】
一方、正確な生体試料中の薬物の分析にはGC-MS(Gas Chromatography - Mass Spectrometry)やHPLC(High Performance Liquid Chromatography)のような分析機器が使用される。しかし、これらの分析機器の分析操作は煩雑で専門家でないと実施できず、結果が出るまでに数時間を要する。
上述した本格的な分析が必要な場合でも、事前に選別して時間を要する分析の件数を減らすスクリーニング装置が多くの場合必要である。
【0005】
【特許文献1】特開平09−033486号公報
【発明の開示】
【発明が解決しようとする課題】
【0006】
専門家でなくとも、短時間で結果の得られる薬物検知方法および装置を提供する。
【課題を解決するための手段】
【0007】
上記課題は、生体に起因する液体試料を滴下された布を加熱するステップと、加熱により気化されたガスを空気とともにイオン源に導いてイオン化するステップと、生成したイオンをイオントラップ型質量分析計に導いて薬物を検知するステップとを含む薬物検知方法により、解決できる。
【0008】
また、生体に起因する液体試料を滴下された布を加熱する加熱部と、加熱部で気化されたガスをイオン化するイオン化部と、イオン化部で生成したイオンを分析するイオントラップ型質量分析計とからなる薬物検知装置により、解決できる。
【発明の効果】
【0009】
本発明により、専門家でなくとも、短時間で結果の得られる薬物検知方法および装置を提供できる。
【発明を実施するための最良の形態】
【0010】
以下、本発明の実施の形態について、実施例を用い図面を参照しながら説明する。
【実施例1】
【0011】
図1ないし図4を用いて実施例1を説明する。ここで、図1は薬物検知装置のブロック図である。図2は尿中のMDMAとMDAのマススペクトルおよびMS/MSスペクトルである。図3は尿中のMDMAとMDA濃度と信号値の関係を説明する図である。図4は薬物検知手順を説明するフローチャートである。
【0012】
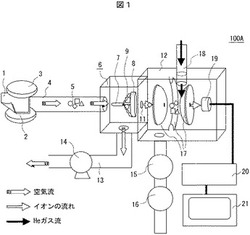
図1に示す薬物検知装置100Aにおいて、吸湿性(吸液性)のある布1に液体生体試料の液滴を滴下する。滴下された液滴は吸湿性のある布1に吸収(吸液)され、保持される。吸湿性のある布1としては、コットンなどのセルロース性の布が吸湿性および耐熱性の観点から適している。コットンの耐熱性は約260℃であり、後の加熱工程での劣化は少ない。より耐熱性が高いメタ型アラミド繊維であるコーネックスも吸水性があるので適用できる。吸湿性がないと滴下した液滴が操作中に傾けると流れてしまい保持されず、また分散されないので蒸発に時間がかかる問題が生じる。液滴量としては滴下し易くまた比較的狭い面積に保持し易い数十マイクロリットルから数百マイクロリットルが適している。検出の閾値を一定に保つためにマイクロピペット、シリンジ等により一定量を分取して滴下すると良い。検出感度の変化を気にしない場合にはスポイト等で1〜数滴滴下しても良い。
【0013】
生体試料を滴下した吸湿性のある布1は、薬物検知装置100Aのサンプル入り口に置かれ、加熱器に送り込まれる。加熱器には下部ヒータ2と上部ヒータ3が設置されており、生体試料を滴下した吸湿性のある布1が入ってくるとこれをセンサーが感知して上部ヒータ3の真下で生体試料を滴下した吸湿性のある布1はとどまり、下部ヒータ2が上昇し、両方のヒータ2、3に挟まれて加熱される。各ヒータ2、3の温度は、図示しない温度制御装置により制御され、温度を200〜250℃にすることにより、幅広い薬物に対応する。
【0014】
ここで、生体試料中の水分を蒸発させる必要があるので、100℃以上にする必要がある。また、コットンを生体試料を滴下する吸湿性のある布1として使う場合には、耐熱温度である260℃以下にすることが必要である。温度を200〜260℃にすると使用後加熱によりコットンの色が少し褐色になるため、未使用品と使用済み品を区別するのに便利である。加熱により生体試料中の比較的沸点の低い成分が蒸発するが、金属などの高沸点成分は布上に残留してこれ以上先には行かない。吸湿性のある布1は、測定終了後、薬物検知装置100Aの加熱器より手動または自動で取り出される。
【0015】
なお、生体試料は水分を多く含むためにヒータで挟まれても水分が蒸発するまでは十分に加熱されない。従って、水分が蒸発するまでの時間を事前に調べておきそれ以上の時間加熱が継続する必要がある。水分のない場合は10秒以内に不正薬物成分の分子が蒸発するが、生体試料が尿または唾液の場合、15から20秒程度必要であった。
【0016】
加熱器からは配管4が出ており、蒸発した不正薬物5は一緒に吸い込まれた空気とともに配管4を通ってイオン化装置6に送り込まれる。イオン化装置6には針電極7と対向電極8が設置されており、高電圧を印加することでこの間にコロナ放電が生じている。コロナ放電中で不正薬物分子はイオン化され不正薬物イオン9となる。イオン化のし易さは化合物により異なるが、試験の結果、覚せい剤等の不正薬物のほとんどは正イオンになり易いことがわかった。このため電気的に細孔11を通して不正薬物イオン9を真空容器12に導くことが可能である。一方、イオン化されなかった成分は空気とともに排気配管13を通って循環ポンプ14により外部に排出される。
【0017】
真空容器12にはターボ分子ポンプ15とバックアップポンプ16が設置されており、細孔11から入ってきたガスを定常的に引いて高真空を保っている。イオンは電気的に3つの電極から構成される四重極イオントラップ質量分析計17中に導かれる。細孔11の径の大きさは真空容器12の真空度を保つために限界があるが、小さくしすぎるとイオンの透過率が下がってしまい感度が出なくなる。0.1−0.3mmが好適であった。四重極イオントラップ質量分析計17に入ったイオンは、電極に高周波電界を印加することにより、四重極イオントラップ質量分析計17内に保持(トラップ)される。四重極イオントラップ質量分析計17はヘリウム導入配管18により微量のヘリウムが供給されており、イオンとの衝突によりイオンが四重極イオントラップ質量分析計17内に保持されるのを助けている。
【0018】
四重極イオントラップ質量分析計17内に保持されたイオンは、電極に印加した高周波電界を変化させることにより、m/z(質量/電荷比)の順で排出させることができる。排出されたイオンは、イオン検出器19により測定し、演算処理装置20で信号を処理することでマススペクトルを得ることができる。
【0019】
通常、コロナ放電によるイオン化では不正薬物イオンそのまままたは水素イオン付加体の正イオンの形でイオン化される。このためマススペクトル上に当該薬物に対応するm/zにピークが存在するかどうかで不正薬物イオンが存在するかどうかを判定することができる。しかし、生体試料中には様々な化合物が共存しており、偶然同じm/zにピークを化合物が存在することを排除できない。四重極イオントラップ質量分析計17は、保持したイオンについて電界を調整してヘリウムと衝突させて分解させた後に分解生成物のマススペクトル(MS/MSスペクトル)を得ることができる。生成する分解生成物は、化合物ごとに異なるので、分解前の最初のマススペクトルの情報とMS/MSスペクトルを組み合わせることにより、より正確な不正薬物の同定が可能となる。この判定は演算処理装置20で行われ、結果はディスプレイ21に表示する。
なお、四重極イオントラップ質量分析計17はリニアイオントラップ質量分析装置に置き換えることも可能である。
【0020】
図2において、薬物使用者の尿を模擬するために正常な成人の尿を採取し、そこに薬物としてMDMA(3,4-Methylenedioxymethamphetamine)、その人体内での代謝物としてMDA(3,4-Methylenedioxyamphetamine)を一定量添加したものを試料とした。この試料を、ピペットで50μlを採取してコットンを原料として製造したキュプラ長繊維不織布に滴下した。尿試料は速やかにキュプラ長繊維不織布に吸収された。図2(a)は通常のマススペクトルであり、MDMAの予想m/z位置194とMDAの予想m/z位置180にピークが認められる。他に両成分ともにm/z=163にピークが出る可能性があり、実際にその位置にピークが認められた。
【0021】
図3(a)は、縦軸に20秒間の測定中のm/z=194、180、163の各ピークの積分値を、横軸に試料中に添加した薬物濃度をプロットしたグラフである。m/z=180のY切片は大きく、薬物添加量がゼロでも大きな信号値を示している。これは尿中にm/z=180の成分が含まれているためと推定され、マススペクトルだけではMDAの検知は困難なことがわかる。このm/z=180のピークは尿中のブドウ糖に起因するものと推定される。
【0022】
一方、図2(b)のピーク180のMS/MSスペクトルではMDAは分解されてm/z=163付近にピークを生じるが、ブドウ糖は162付近にピークを生じるので区別が可能である。
【0023】
図2(c)のm/z=194のMS/MSスペクトルでは、MDMAは分解されm/z=163付近にピークが認められる。
【0024】
図3(b)は、縦軸にMS/MSスペクトルのm/z=163ピークの積分値を、横軸に薬物濃度に対してプロットしたグラフである。マススペクトルのピーク180に対するMS/MSスペクトルと、マススペクトルのピーク194に対応するMS/MSスペクトルは、共にY切片がほぼ原点付近であり、MS/MSスペクトルでは共存物の影響はほとんど認められない。
【0025】
以上からMS/MSスペクトルを使うと生体試料のように共存物の多い試料でも信頼性の高い薬物の検知が可能であることがわかる。MDMAとその代謝物であるMDAが同時に検知されるとMDMAが試料中に存在するだけではなくそれが体内に入って代謝されたと考えることができる。従って検知において代謝物の検知対象に組み入れることにより、不正薬物を服用した可能性の判定も可能となる。
【0026】
スペクトルの積分値またはスペクトル上の最大のピーク値を使い、これらの一方または両方が予め定めた閾値を超えたかどうかを演算処理装置20に判定させる。閾値を超えている場合には不正薬物またはその代謝物を検知したことをディスプレイ21に表示する。不正薬物とその代謝物の両方が検知された場合にはディスプレイ21に不正薬物使用の警報を表示する。同様な事はメタンフェタミンとその代謝物としてアンフェタミン、コカインの複数の代謝物等他の不正薬物に対しても実施可能で、これらの薬物の使用について判定に用いるマススペクトルおよびMS/MSスペクトルのピーク位置をあらかじめ演算処理装置20に登録しておいて判定させることで同じ試料から同時に検知することが可能である。
【0027】
上述した薬物の検出方法を、図4を参照して説明する。図4において、不正薬物の検出方法は、液体試料を滴下された吸湿性のある布を加熱し(S41)、液体試料中の一部成分を気化する(S42)。さらに、発生した気体成分をイオン化し(S43)、イオントラップ質量分析計でマススペクトル分析を実施し(S44)、不正薬物の可能性のあるm/zについてイオントラップ質量分析計でMS/MSスペクトル分析を実施する(S45)。さらに、ステップ44とステップ45の検知結果に基づいて、薬物の存在を判定する(S46)。
【0028】
なお、MDAをMDMAの代謝物と説明したが、単体でも合成麻薬である。薬物としては、2C−B(4-bromo-2,5-dimethoxyphenethylamine)、PMA(paramethoxyamphetamine)、覚せい剤、覚せい剤原料、ケタミン((RS)-2-(2-chlorophenyl)-2-(methylamino)cyclohexanone)等を含みこれらに限られない。また、生体試料として、尿、唾液を挙げたが、生体に起因するものならば皮膚や髪の毛等を溶液に溶解したものも生体試料であり、これらに限られない。
【0029】
本実施例によれば煩雑な化学操作が必要なく、簡便かつ迅速に生体試料中の不正薬物を検知可能である。また、代謝物の検知を組み合わせることで不正薬物が使用されたかどうかも判定することが可能となる。
【実施例2】
【0030】
図5を用いて実施例2を説明する。ここで、図5は薬物検知装置のブロック図である。
【0031】
図5において、薬液検知装置100Bの分注器31は、尿試料から50μl自動的にサンプリングし、サンプリングした尿試料32をセルロース製のキュプラ長繊維の不織布ベルト33に滴下する。滴下された尿試料は不織布ベルト33が巻き取り器34に巻き取られて前進し、加熱器上部ヒータ35の下に到達する前に不織布に吸収される。尿試料32が加熱器上部ヒータ35の位置に到着すると巻き取り器34は停止し、加熱器下部ヒータ36が上昇してきて尿試料32を吸収した不織布を挟み込んで加熱する。加熱温度はヒータ面で250℃に制御する。
【0032】
加熱された尿試料は蒸発し、水分とともに尿中の比較的沸点の低い成分が気化されて加熱配管37を通してイオン化装置38に送られる。加熱配管37は180℃に保たれており、気化された水分子等の成分が凝縮するのを防いでいる。15秒間の加熱が終了すると加熱器下部ヒータ36が下がる。次の試料が分注器31により滴下されると巻き取り器34により巻き取りが始まり、加熱を終了した試料が送られて次の試料が加熱器上部ヒータ35に到達する。
【0033】
イオン化装置38は、紫外線の照射により不正薬物分子をイオン化する。エアーポンプ40により、イオン化装置中の気体は空気とともに排気管41を通じて装置外に排出される。0.1mm径のキャピラリー細孔42を通じて真空容器43内にイオン光学系44により静電的に引き込まれる。イオン光学系44で収束させたイオンはイオントラップ型質量分析器45に送られる。イオントラップ型質量分析器45にはヘリウムボンベ46からヘリウム配管47を通じて少量のヘリウムガスが供給されている。また、真空容器43にはターボ分子ポンプ48およびダイアフラムポンプ49が繋がっており、真空排気管50を通じて排気することで真空容器43内を高真空に保っている。
【0034】
イオントラップ型質量分析器45ではm/z=60−400のマススペクトルの測定と各対象不正薬物成分に対するMS/MSスペクトルの測定がシリアルに実施される。イオントラップ型質量分析器45に保持されていたイオンは印加する高周波を操作して排出させ、コンバージョンダイノード51に送られ、そこで電子に変換される。生成した電子はシンチレータ52で光に変換され光電子増倍管53で電気信号に変換された後、演算処理装置54で処理される。処理された信号はパソコン55に送られて不正薬物が予め決められた論理に従って閾値以上に存在するかどうかを判定され、スクリーン56に判定結果が表示される。
実施例2によれば、自動操作で尿中薬物の高速検知が可能となるという効果を奏する。
【図面の簡単な説明】
【0035】
【図1】薬物検知装置のブロック図である。
【図2】尿中のMDMAとMDAのマススペクトルおよびMS/MSスペクトルである。
【図3】尿中のMDMAとMDA濃度と信号値の関係を説明する図である。
【図4】薬物検知手順を説明するフローチャートである。
【図5】他の薬物検知装置のブロック図である。
【符号の説明】
【0036】
1…吸湿性(吸液性)のある布、2…下部ヒータ、3…上部ヒータ、4…配管、5…蒸発した不正薬物、6…イオン化装置、7…針電極、8…対向電極、9…不正薬物イオン、11…細孔、12…真空容器、13…排気配管、14…循環ポンプ、15…ターボ分子ポンプ、16…バックアップポンプ、17…四重極イオントラップ質量分析計、18…ヘリウム導入配管、19…イオン検出器、20…演算処理装置、21…ディスプレイ、31…分注器、32…尿試料、33…不織布ベルト、34…巻き取り器、35…加熱器上部ヒータ、36…加熱器下部ヒータ、37…加熱配管、38…イオン化装置、40…エアーポンプ、41…排気管、42…キャピラリー細孔、43…真空容器、44…イオン光学系、45…イオントラップ型質量分析器、46…ヘリウムボンベ、47…ヘリウム配管、48…ターボ分子ポンプ、49…ダイアフラムポンプ、50…真空排気管、51…コンバージョンダイノード、52…シンチレータ、53…光電子増倍管、54…演算処理装置、55…パソコン、56…スクリーン、100…薬物検知装置。
【技術分野】
【0001】
本発明は薬物検知方法および装置に係り、特に不正薬物使用者に由来する生体試料からの薬物検知方法および装置に関するものである。
【背景技術】
【0002】
不正薬物の検知には、指示試薬を用いたキットが用いられている。しかし、キットでは各々の薬物に対応した指示薬が必要となり、候補薬物が絞れないときには多くの指示薬を準備する必要がある。また、新しい薬物に対しては指示薬自体の開発が出来るまでは対応できない問題がある。さらに、反応や操作に時間がかかるものもあり、結果が得られるまでに10分オーダーの時間が必要となることもある。
【0003】
これに対して、特許文献1には、イオンモビリティー分光法(IMS:Ion Mobility Spectrometry)を用いた装置が記載されている。IMSはあらかじめ薬物のスペクトルを採取することにより新しい薬物にも対応でき、また検知時間も10秒オーダーと短い。しかし、共存物の多い試料では共存物とのスペクトル上での分離が薬物によっては問題となる。また、有害な放射性物質やドーパントなどの化学物質の使用が必要である。さらに、IMSは水の影響を受けやすく、尿等の水を主成分とする生体試料にはそのままでは適用できない。
【0004】
一方、正確な生体試料中の薬物の分析にはGC-MS(Gas Chromatography - Mass Spectrometry)やHPLC(High Performance Liquid Chromatography)のような分析機器が使用される。しかし、これらの分析機器の分析操作は煩雑で専門家でないと実施できず、結果が出るまでに数時間を要する。
上述した本格的な分析が必要な場合でも、事前に選別して時間を要する分析の件数を減らすスクリーニング装置が多くの場合必要である。
【0005】
【特許文献1】特開平09−033486号公報
【発明の開示】
【発明が解決しようとする課題】
【0006】
専門家でなくとも、短時間で結果の得られる薬物検知方法および装置を提供する。
【課題を解決するための手段】
【0007】
上記課題は、生体に起因する液体試料を滴下された布を加熱するステップと、加熱により気化されたガスを空気とともにイオン源に導いてイオン化するステップと、生成したイオンをイオントラップ型質量分析計に導いて薬物を検知するステップとを含む薬物検知方法により、解決できる。
【0008】
また、生体に起因する液体試料を滴下された布を加熱する加熱部と、加熱部で気化されたガスをイオン化するイオン化部と、イオン化部で生成したイオンを分析するイオントラップ型質量分析計とからなる薬物検知装置により、解決できる。
【発明の効果】
【0009】
本発明により、専門家でなくとも、短時間で結果の得られる薬物検知方法および装置を提供できる。
【発明を実施するための最良の形態】
【0010】
以下、本発明の実施の形態について、実施例を用い図面を参照しながら説明する。
【実施例1】
【0011】
図1ないし図4を用いて実施例1を説明する。ここで、図1は薬物検知装置のブロック図である。図2は尿中のMDMAとMDAのマススペクトルおよびMS/MSスペクトルである。図3は尿中のMDMAとMDA濃度と信号値の関係を説明する図である。図4は薬物検知手順を説明するフローチャートである。
【0012】
図1に示す薬物検知装置100Aにおいて、吸湿性(吸液性)のある布1に液体生体試料の液滴を滴下する。滴下された液滴は吸湿性のある布1に吸収(吸液)され、保持される。吸湿性のある布1としては、コットンなどのセルロース性の布が吸湿性および耐熱性の観点から適している。コットンの耐熱性は約260℃であり、後の加熱工程での劣化は少ない。より耐熱性が高いメタ型アラミド繊維であるコーネックスも吸水性があるので適用できる。吸湿性がないと滴下した液滴が操作中に傾けると流れてしまい保持されず、また分散されないので蒸発に時間がかかる問題が生じる。液滴量としては滴下し易くまた比較的狭い面積に保持し易い数十マイクロリットルから数百マイクロリットルが適している。検出の閾値を一定に保つためにマイクロピペット、シリンジ等により一定量を分取して滴下すると良い。検出感度の変化を気にしない場合にはスポイト等で1〜数滴滴下しても良い。
【0013】
生体試料を滴下した吸湿性のある布1は、薬物検知装置100Aのサンプル入り口に置かれ、加熱器に送り込まれる。加熱器には下部ヒータ2と上部ヒータ3が設置されており、生体試料を滴下した吸湿性のある布1が入ってくるとこれをセンサーが感知して上部ヒータ3の真下で生体試料を滴下した吸湿性のある布1はとどまり、下部ヒータ2が上昇し、両方のヒータ2、3に挟まれて加熱される。各ヒータ2、3の温度は、図示しない温度制御装置により制御され、温度を200〜250℃にすることにより、幅広い薬物に対応する。
【0014】
ここで、生体試料中の水分を蒸発させる必要があるので、100℃以上にする必要がある。また、コットンを生体試料を滴下する吸湿性のある布1として使う場合には、耐熱温度である260℃以下にすることが必要である。温度を200〜260℃にすると使用後加熱によりコットンの色が少し褐色になるため、未使用品と使用済み品を区別するのに便利である。加熱により生体試料中の比較的沸点の低い成分が蒸発するが、金属などの高沸点成分は布上に残留してこれ以上先には行かない。吸湿性のある布1は、測定終了後、薬物検知装置100Aの加熱器より手動または自動で取り出される。
【0015】
なお、生体試料は水分を多く含むためにヒータで挟まれても水分が蒸発するまでは十分に加熱されない。従って、水分が蒸発するまでの時間を事前に調べておきそれ以上の時間加熱が継続する必要がある。水分のない場合は10秒以内に不正薬物成分の分子が蒸発するが、生体試料が尿または唾液の場合、15から20秒程度必要であった。
【0016】
加熱器からは配管4が出ており、蒸発した不正薬物5は一緒に吸い込まれた空気とともに配管4を通ってイオン化装置6に送り込まれる。イオン化装置6には針電極7と対向電極8が設置されており、高電圧を印加することでこの間にコロナ放電が生じている。コロナ放電中で不正薬物分子はイオン化され不正薬物イオン9となる。イオン化のし易さは化合物により異なるが、試験の結果、覚せい剤等の不正薬物のほとんどは正イオンになり易いことがわかった。このため電気的に細孔11を通して不正薬物イオン9を真空容器12に導くことが可能である。一方、イオン化されなかった成分は空気とともに排気配管13を通って循環ポンプ14により外部に排出される。
【0017】
真空容器12にはターボ分子ポンプ15とバックアップポンプ16が設置されており、細孔11から入ってきたガスを定常的に引いて高真空を保っている。イオンは電気的に3つの電極から構成される四重極イオントラップ質量分析計17中に導かれる。細孔11の径の大きさは真空容器12の真空度を保つために限界があるが、小さくしすぎるとイオンの透過率が下がってしまい感度が出なくなる。0.1−0.3mmが好適であった。四重極イオントラップ質量分析計17に入ったイオンは、電極に高周波電界を印加することにより、四重極イオントラップ質量分析計17内に保持(トラップ)される。四重極イオントラップ質量分析計17はヘリウム導入配管18により微量のヘリウムが供給されており、イオンとの衝突によりイオンが四重極イオントラップ質量分析計17内に保持されるのを助けている。
【0018】
四重極イオントラップ質量分析計17内に保持されたイオンは、電極に印加した高周波電界を変化させることにより、m/z(質量/電荷比)の順で排出させることができる。排出されたイオンは、イオン検出器19により測定し、演算処理装置20で信号を処理することでマススペクトルを得ることができる。
【0019】
通常、コロナ放電によるイオン化では不正薬物イオンそのまままたは水素イオン付加体の正イオンの形でイオン化される。このためマススペクトル上に当該薬物に対応するm/zにピークが存在するかどうかで不正薬物イオンが存在するかどうかを判定することができる。しかし、生体試料中には様々な化合物が共存しており、偶然同じm/zにピークを化合物が存在することを排除できない。四重極イオントラップ質量分析計17は、保持したイオンについて電界を調整してヘリウムと衝突させて分解させた後に分解生成物のマススペクトル(MS/MSスペクトル)を得ることができる。生成する分解生成物は、化合物ごとに異なるので、分解前の最初のマススペクトルの情報とMS/MSスペクトルを組み合わせることにより、より正確な不正薬物の同定が可能となる。この判定は演算処理装置20で行われ、結果はディスプレイ21に表示する。
なお、四重極イオントラップ質量分析計17はリニアイオントラップ質量分析装置に置き換えることも可能である。
【0020】
図2において、薬物使用者の尿を模擬するために正常な成人の尿を採取し、そこに薬物としてMDMA(3,4-Methylenedioxymethamphetamine)、その人体内での代謝物としてMDA(3,4-Methylenedioxyamphetamine)を一定量添加したものを試料とした。この試料を、ピペットで50μlを採取してコットンを原料として製造したキュプラ長繊維不織布に滴下した。尿試料は速やかにキュプラ長繊維不織布に吸収された。図2(a)は通常のマススペクトルであり、MDMAの予想m/z位置194とMDAの予想m/z位置180にピークが認められる。他に両成分ともにm/z=163にピークが出る可能性があり、実際にその位置にピークが認められた。
【0021】
図3(a)は、縦軸に20秒間の測定中のm/z=194、180、163の各ピークの積分値を、横軸に試料中に添加した薬物濃度をプロットしたグラフである。m/z=180のY切片は大きく、薬物添加量がゼロでも大きな信号値を示している。これは尿中にm/z=180の成分が含まれているためと推定され、マススペクトルだけではMDAの検知は困難なことがわかる。このm/z=180のピークは尿中のブドウ糖に起因するものと推定される。
【0022】
一方、図2(b)のピーク180のMS/MSスペクトルではMDAは分解されてm/z=163付近にピークを生じるが、ブドウ糖は162付近にピークを生じるので区別が可能である。
【0023】
図2(c)のm/z=194のMS/MSスペクトルでは、MDMAは分解されm/z=163付近にピークが認められる。
【0024】
図3(b)は、縦軸にMS/MSスペクトルのm/z=163ピークの積分値を、横軸に薬物濃度に対してプロットしたグラフである。マススペクトルのピーク180に対するMS/MSスペクトルと、マススペクトルのピーク194に対応するMS/MSスペクトルは、共にY切片がほぼ原点付近であり、MS/MSスペクトルでは共存物の影響はほとんど認められない。
【0025】
以上からMS/MSスペクトルを使うと生体試料のように共存物の多い試料でも信頼性の高い薬物の検知が可能であることがわかる。MDMAとその代謝物であるMDAが同時に検知されるとMDMAが試料中に存在するだけではなくそれが体内に入って代謝されたと考えることができる。従って検知において代謝物の検知対象に組み入れることにより、不正薬物を服用した可能性の判定も可能となる。
【0026】
スペクトルの積分値またはスペクトル上の最大のピーク値を使い、これらの一方または両方が予め定めた閾値を超えたかどうかを演算処理装置20に判定させる。閾値を超えている場合には不正薬物またはその代謝物を検知したことをディスプレイ21に表示する。不正薬物とその代謝物の両方が検知された場合にはディスプレイ21に不正薬物使用の警報を表示する。同様な事はメタンフェタミンとその代謝物としてアンフェタミン、コカインの複数の代謝物等他の不正薬物に対しても実施可能で、これらの薬物の使用について判定に用いるマススペクトルおよびMS/MSスペクトルのピーク位置をあらかじめ演算処理装置20に登録しておいて判定させることで同じ試料から同時に検知することが可能である。
【0027】
上述した薬物の検出方法を、図4を参照して説明する。図4において、不正薬物の検出方法は、液体試料を滴下された吸湿性のある布を加熱し(S41)、液体試料中の一部成分を気化する(S42)。さらに、発生した気体成分をイオン化し(S43)、イオントラップ質量分析計でマススペクトル分析を実施し(S44)、不正薬物の可能性のあるm/zについてイオントラップ質量分析計でMS/MSスペクトル分析を実施する(S45)。さらに、ステップ44とステップ45の検知結果に基づいて、薬物の存在を判定する(S46)。
【0028】
なお、MDAをMDMAの代謝物と説明したが、単体でも合成麻薬である。薬物としては、2C−B(4-bromo-2,5-dimethoxyphenethylamine)、PMA(paramethoxyamphetamine)、覚せい剤、覚せい剤原料、ケタミン((RS)-2-(2-chlorophenyl)-2-(methylamino)cyclohexanone)等を含みこれらに限られない。また、生体試料として、尿、唾液を挙げたが、生体に起因するものならば皮膚や髪の毛等を溶液に溶解したものも生体試料であり、これらに限られない。
【0029】
本実施例によれば煩雑な化学操作が必要なく、簡便かつ迅速に生体試料中の不正薬物を検知可能である。また、代謝物の検知を組み合わせることで不正薬物が使用されたかどうかも判定することが可能となる。
【実施例2】
【0030】
図5を用いて実施例2を説明する。ここで、図5は薬物検知装置のブロック図である。
【0031】
図5において、薬液検知装置100Bの分注器31は、尿試料から50μl自動的にサンプリングし、サンプリングした尿試料32をセルロース製のキュプラ長繊維の不織布ベルト33に滴下する。滴下された尿試料は不織布ベルト33が巻き取り器34に巻き取られて前進し、加熱器上部ヒータ35の下に到達する前に不織布に吸収される。尿試料32が加熱器上部ヒータ35の位置に到着すると巻き取り器34は停止し、加熱器下部ヒータ36が上昇してきて尿試料32を吸収した不織布を挟み込んで加熱する。加熱温度はヒータ面で250℃に制御する。
【0032】
加熱された尿試料は蒸発し、水分とともに尿中の比較的沸点の低い成分が気化されて加熱配管37を通してイオン化装置38に送られる。加熱配管37は180℃に保たれており、気化された水分子等の成分が凝縮するのを防いでいる。15秒間の加熱が終了すると加熱器下部ヒータ36が下がる。次の試料が分注器31により滴下されると巻き取り器34により巻き取りが始まり、加熱を終了した試料が送られて次の試料が加熱器上部ヒータ35に到達する。
【0033】
イオン化装置38は、紫外線の照射により不正薬物分子をイオン化する。エアーポンプ40により、イオン化装置中の気体は空気とともに排気管41を通じて装置外に排出される。0.1mm径のキャピラリー細孔42を通じて真空容器43内にイオン光学系44により静電的に引き込まれる。イオン光学系44で収束させたイオンはイオントラップ型質量分析器45に送られる。イオントラップ型質量分析器45にはヘリウムボンベ46からヘリウム配管47を通じて少量のヘリウムガスが供給されている。また、真空容器43にはターボ分子ポンプ48およびダイアフラムポンプ49が繋がっており、真空排気管50を通じて排気することで真空容器43内を高真空に保っている。
【0034】
イオントラップ型質量分析器45ではm/z=60−400のマススペクトルの測定と各対象不正薬物成分に対するMS/MSスペクトルの測定がシリアルに実施される。イオントラップ型質量分析器45に保持されていたイオンは印加する高周波を操作して排出させ、コンバージョンダイノード51に送られ、そこで電子に変換される。生成した電子はシンチレータ52で光に変換され光電子増倍管53で電気信号に変換された後、演算処理装置54で処理される。処理された信号はパソコン55に送られて不正薬物が予め決められた論理に従って閾値以上に存在するかどうかを判定され、スクリーン56に判定結果が表示される。
実施例2によれば、自動操作で尿中薬物の高速検知が可能となるという効果を奏する。
【図面の簡単な説明】
【0035】
【図1】薬物検知装置のブロック図である。
【図2】尿中のMDMAとMDAのマススペクトルおよびMS/MSスペクトルである。
【図3】尿中のMDMAとMDA濃度と信号値の関係を説明する図である。
【図4】薬物検知手順を説明するフローチャートである。
【図5】他の薬物検知装置のブロック図である。
【符号の説明】
【0036】
1…吸湿性(吸液性)のある布、2…下部ヒータ、3…上部ヒータ、4…配管、5…蒸発した不正薬物、6…イオン化装置、7…針電極、8…対向電極、9…不正薬物イオン、11…細孔、12…真空容器、13…排気配管、14…循環ポンプ、15…ターボ分子ポンプ、16…バックアップポンプ、17…四重極イオントラップ質量分析計、18…ヘリウム導入配管、19…イオン検出器、20…演算処理装置、21…ディスプレイ、31…分注器、32…尿試料、33…不織布ベルト、34…巻き取り器、35…加熱器上部ヒータ、36…加熱器下部ヒータ、37…加熱配管、38…イオン化装置、40…エアーポンプ、41…排気管、42…キャピラリー細孔、43…真空容器、44…イオン光学系、45…イオントラップ型質量分析器、46…ヘリウムボンベ、47…ヘリウム配管、48…ターボ分子ポンプ、49…ダイアフラムポンプ、50…真空排気管、51…コンバージョンダイノード、52…シンチレータ、53…光電子増倍管、54…演算処理装置、55…パソコン、56…スクリーン、100…薬物検知装置。
【特許請求の範囲】
【請求項1】
生体に起因する液体試料を滴下された布を加熱するステップと、加熱により気化されたガスを空気とともにイオン源に導いてイオン化するステップと、生成したイオンをイオントラップ型質量分析計に導いて前記液体試料に含む薬物を検知するステップとを含むことを特徴とする薬物検知方法。
【請求項2】
請求項1に記載の薬物検知方法であって、
前記イオンは、コロナ放電または光電離を利用していることを特徴とする薬物検知方法。
【請求項3】
請求項1または請求項2に記載の薬物検知方法であって、
前記イオントラップ型質量分析計は、予め定めた第1のm/z値のイオンを抽出し、当該m/z値の抽出イオンをヘリウムと衝突させて分解し、その分解生成物のm/z値が第2のm/z値であることを判定条件とすることを特徴とする薬物検知方法。
【請求項4】
請求項1ないし請求項3のいずれか一つに記載された薬物検知方法であって、
前記布はセルロース製で、前記布の加熱温度が100℃以上260℃以下であることを特徴とする薬物検知方法。
【請求項5】
生体に起因する液体試料を滴下された布を加熱する加熱部と、この加熱部で気化されたガスをイオン化するイオン化部と、このイオン化部で生成したイオンを分析するイオントラップ型質量分析計とからなる薬物検知装置。
【請求項6】
請求項5に記載の薬物検知装置であって、
前記イオンは、コロナ放電または光電離を利用していることを特徴とする薬物検知装置。
【請求項7】
請求項5または請求項6に記載の薬物検知装置であって、
前記イオントラップ型質量分析計は、予め定めた第1のm/z値のイオンを抽出し、当該m/z値の抽出イオンをヘリウムと衝突させて分解し、その分解生成物のm/z値が第2のm/z値であることを判定条件とすることを特徴とする薬物検知装置。
【請求項8】
請求項5ないし請求項7のいずれか一つに記載された薬物検知装置であって、
前記布はセルロース製で、前記布の加熱温度が100℃以上260℃以下であることを特徴とする薬物検知装置。
【請求項1】
生体に起因する液体試料を滴下された布を加熱するステップと、加熱により気化されたガスを空気とともにイオン源に導いてイオン化するステップと、生成したイオンをイオントラップ型質量分析計に導いて前記液体試料に含む薬物を検知するステップとを含むことを特徴とする薬物検知方法。
【請求項2】
請求項1に記載の薬物検知方法であって、
前記イオンは、コロナ放電または光電離を利用していることを特徴とする薬物検知方法。
【請求項3】
請求項1または請求項2に記載の薬物検知方法であって、
前記イオントラップ型質量分析計は、予め定めた第1のm/z値のイオンを抽出し、当該m/z値の抽出イオンをヘリウムと衝突させて分解し、その分解生成物のm/z値が第2のm/z値であることを判定条件とすることを特徴とする薬物検知方法。
【請求項4】
請求項1ないし請求項3のいずれか一つに記載された薬物検知方法であって、
前記布はセルロース製で、前記布の加熱温度が100℃以上260℃以下であることを特徴とする薬物検知方法。
【請求項5】
生体に起因する液体試料を滴下された布を加熱する加熱部と、この加熱部で気化されたガスをイオン化するイオン化部と、このイオン化部で生成したイオンを分析するイオントラップ型質量分析計とからなる薬物検知装置。
【請求項6】
請求項5に記載の薬物検知装置であって、
前記イオンは、コロナ放電または光電離を利用していることを特徴とする薬物検知装置。
【請求項7】
請求項5または請求項6に記載の薬物検知装置であって、
前記イオントラップ型質量分析計は、予め定めた第1のm/z値のイオンを抽出し、当該m/z値の抽出イオンをヘリウムと衝突させて分解し、その分解生成物のm/z値が第2のm/z値であることを判定条件とすることを特徴とする薬物検知装置。
【請求項8】
請求項5ないし請求項7のいずれか一つに記載された薬物検知装置であって、
前記布はセルロース製で、前記布の加熱温度が100℃以上260℃以下であることを特徴とする薬物検知装置。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2008−51520(P2008−51520A)
【公開日】平成20年3月6日(2008.3.6)
【国際特許分類】
【出願番号】特願2006−225138(P2006−225138)
【出願日】平成18年8月22日(2006.8.22)
【出願人】(000005108)株式会社日立製作所 (27,607)
【出願人】(592083915)警察庁科学警察研究所長 (23)
【Fターム(参考)】
【公開日】平成20年3月6日(2008.3.6)
【国際特許分類】
【出願日】平成18年8月22日(2006.8.22)
【出願人】(000005108)株式会社日立製作所 (27,607)
【出願人】(592083915)警察庁科学警察研究所長 (23)
【Fターム(参考)】
[ Back to top ]

