薬物検知装置
【課題】尿中の多様な薬物を迅速に、かつ、高感度に分析を行うための薬物検知装置を提供する。
【解決手段】質量分析部8と、液体試料1を入れるための試料容器2と、試料容器2を加熱するための試料加熱部3とを含む質量分析装置を用い、試料容器2は、液体試料1の上方にガスを通過させるための空間部101を有し、試料容器2には、試料容器2に同伴ガスを導入するための同伴ガス導入配管104と空間部101の試料ガスを質量分析部8に送るための試料ガス導入配管5とを接続する。
【解決手段】質量分析部8と、液体試料1を入れるための試料容器2と、試料容器2を加熱するための試料加熱部3とを含む質量分析装置を用い、試料容器2は、液体試料1の上方にガスを通過させるための空間部101を有し、試料容器2には、試料容器2に同伴ガスを導入するための同伴ガス導入配管104と空間部101の試料ガスを質量分析部8に送るための試料ガス導入配管5とを接続する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、薬物検知装置に関する。
【背景技術】
【0002】
以下では、ガスクロマトグラフをGC(Gas Chromatograph)、ガスクロマトグラフと質量分析計とを結合した装置をGC/MS(Gas Chromatograph / Mass Spectrometer)、大気圧化学イオン化をAPCI(Atmospheric Pressure Chemical Ionization)、化学イオン化をCI(Chemical Ionization)、電子イオン化をEI(Electron Ionization)とそれぞれ略記する。
【0003】
覚せい剤、麻薬などの違法薬物の現場捜査における検知としては、免疫法などを利用した試薬キットが用いられている。試薬キットによる検査法の場合、構造が似ている物質で偽陽性が出ることがあり、より検知精度が高くて簡便な検知方法が求められている。
【0004】
特許文献1には、尿を封入した密閉容器中のヘッドスペースガスをGCに導入し、尿中覚せい剤を分析する技術が開示されている。
【0005】
特許文献2には、試料ガスをGCカラムで分離し、GCカラム出口をAPCIイオン源のイオン分子反応領域に設け、高感度化を図る構成について記載がある。
【0006】
特許文献3には、薬物を含む液体サンプルを布に滴下し、布を上下の加熱ヒーターで挟み込み液体試料を気化させ、イオントラップ型質量分析計で分析する手法について記載がある。
【0007】
非特許文献3には、覚せい剤成分は、炭酸カリウムの溶解熱及び液性(アルカリ性)により、尿中から揮発して気相(ヘッドスペース)へ移行することが記載されている。また、非特許文献3には、呈色反応以外にも、各種の違法薬物に対するモノクローナル抗体を用い、抗原抗体反応を利用した予試験用の試薬キットが記載されている。
【0008】
特許文献4には、呈色反応による判定を用いて、取扱いが簡易で迅速な検知を可能とする覚せい剤の予試験キットが開示されている。
【0009】
非特許文献4には、大麻の呈色試験、コカインの定性試験における呈色反応の利用及びあへんの予試験における呈色試験に関する記載がある。
【0010】
特許文献5には、呈色反応を利用するあへんの検出方法および検出キットが開示されている。
【先行技術文献】
【特許文献】
【0011】
【特許文献1】特開平4−184253号公報
【特許文献2】特開2006−86002号公報
【特許文献3】特開2008−51520号公報
【特許文献4】実用新案登録第3156553号公報
【特許文献5】特公平8−27275号公報
【非特許文献】
【0012】
【非特許文献1】J. Chem. Phys.、52、212 (1970)
【非特許文献2】J. Mass Spectrom.、44、1300 (2009)
【非特許文献3】捜査のための法科学 第二部 <法工学・法化学> 令文社、pp.272〜278
【非特許文献4】薬毒物試験法と注解2006 −分析・毒性・対処法− 東京化学同人、pp.131〜145、pp.175〜185
【発明の概要】
【発明が解決しようとする課題】
【0013】
特許文献1に開示されている方法を用いて、ヘッドスペースのガスをシリンジで吸入し、質量分析装置のイオン源導入配管にシリンジ内ガスを吐出させると、シリンジ内で測定対象物が吸着し、マスクロマトグラムのピークがブロードになったり、実質的な感度が下がったりする点で改善の余地がある。
【0014】
また、特許文献3には、尿中の夾雑成分が加熱により測定対象物と同時に分析部に導入され、イオン化が阻害されて感度低下が起こる場合の対応について開示されていない。
【0015】
特許文献4に記載されている予試験キットは、覚せい剤の判定は色調見本を元にするものであり、捜査現場における車内等の空間では色の見間違いを起こす可能性がある。
【0016】
非特許文献3に記載されている各種の検査用キットは、判定を捜査員の目視によるものとしていることが多く、誤判定する問題がある。また、抗原抗体反応によると試料中の風邪薬の成分と交差反応を起こすことがあり、正確な判定が難しい場合もある。
【0017】
また、大麻試料、コカイン、あへんなどの呈色反応は、目視での確認となるため、判定が困難であり、判定を誤ることがある。また、呈色分析のための試料の抽出・精製操作は煩雑である。
【0018】
非特許文献4に記載されている大麻試料の分析においては、試料から薬物の成分をメタノールなどの有機溶媒を用いて抽出する。さらに、液−液抽出などの操作を繰り返して、大麻中の幻覚成分(取締り対象の成分)を分離精製する必要がある。
【0019】
非特許文献4に記載されているあへんのGC/MS分析を行う場合には、アヘンアルカロイド類の抽出操作を行った後、誘導体化して分析を行い、メコン酸、コデイン及びモルヒネの誘導体を検出できるが、誘導体化のための操作が煩雑である。
【0020】
特許文献5に記載されているあへんの検出は、試料の水溶性及び呈色反応で判定する必要がある。
【0021】
非特許文献4及び特許文献5に記載されている大麻、コカイン及びあへんの試料の調製方法は、それぞれ異なる。
【0022】
本発明の目的は、尿中の多様な薬物を迅速に、かつ、高感度に分析を行うための薬物検知装置を提供することにある。
【課題を解決するための手段】
【0023】
本発明の質量分析装置は、イオン化部と、質量分析部と、試料を入れるための試料容器と、前記試料容器を加熱するための試料加熱部とを含み、前記試料容器には、気相である空間部を設けるとともに、前記試料容器に同伴ガスを導入するための同伴ガス導入配管と前記空間部の試料ガスを前記イオン化部に送るための試料ガス導入配管とが接続してあり、前記イオン化部は、前記試料ガスのイオンを生成し、前記質量分析部は、前記イオンの質量分析を行うことを特徴とする。
【発明の効果】
【0024】
本発明によれば、尿中の多様な薬物を迅速かつ高感度に分析を行うことが可能となる。
【図面の簡単な説明】
【0025】
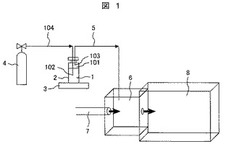
【図1】実施例の質量分析装置を示す概略構成図である。
【図2】図1のイオン化部を示す詳細構成図である。
【図3】薬物の質量スペクトル(公知例)を示すグラフである。
【図4】図1の質量分析装置の変形例を示す構成図である。
【図5A】実施例の質量分析装置による薬物(Methamphetamine:MA)の測定結果を示すグラフである。
【図5B】実施例の質量分析装置による薬物(Amphetamine:AP)の測定結果を示すグラフである。
【図5C】実施例の質量分析装置による薬物(3、4−Methylenedioxyamphetamine:MDA)の測定結果を示すグラフである。
【図5D】実施例の質量分析装置による薬物(3、4−Methylenedioxymethamphetamine:MDMA)の測定結果を示すグラフである。
【図6】他の実施例に係る質量分析装置を示す概略構成図である。
【図7】図6の質量分析装置により夾雑物と測定対象物とを分離して検出するための方式を説明するグラフである。
【図8A】実施例の質量分析装置による尿試料中の薬物(1ppm)のマススペクトルである。
【図8B】実施例の質量分析装置による尿試料中の薬物(0.1ppm)のマススペクトルである。
【図9A】実施例の質量分析装置による薬物(MA)の測定結果を示すグラフである。
【図9B】実施例の質量分析装置による薬物(AP)の測定結果を示すグラフである。
【図9C】実施例の質量分析装置による薬物(MDA)の測定結果を示すグラフである。
【図9D】実施例の質量分析装置による薬物(MDMA)の測定結果を示すグラフである。
【図9E】実施例の質量分析装置による薬物(AP)の測定結果を示すグラフである。
【図10】実施例の質量分析装置による大麻のマススペクトルである。
【図11】実施例の質量分析装置によるコカインのマススペクトルである。
【図12】実施例の質量分析装置によるあへんのマススペクトルである。
【図13】図4の質量分析装置の変形例を示す構成図である。
【発明を実施するための形態】
【0026】
本発明は、ガス中揮発成分を分析する質量分析装置に関する。特に、尿中の違法薬物を分析する質量分析装置に関する。
【0027】
本発明においては、ヘッドスペースガスを大気圧化学イオン化部(APCI部)に連続的に導入する。
【0028】
シリンジを使った注入法の場合、数〜10μLを数秒間で注入するのに対し(信号がピーク形状となる)、連続して測定対象ガスを導入するため、数分程度安定した信号強度が得られる。
【0029】
サンプルとして使用する尿の量は、高々数mL〜数十mL(ミリリットル)であるため、容器内のヘッドスペース容量も数mL〜数十mLである。一方、APCIの放電部に必要なガス流量は数百mL/分であるため、ヘッドスペースガスを数百mL/分の流量でイオン化部に流入させると、測定対象成分が希釈されてしまい、測定感度が低下してしまう。
【0030】
そこで、ヘッドスペースガスを数mL/分程度の流量でイオン化部に導入し、放電に必要なガスは別系統で導入する。
【0031】
また、別の導入方式として、細管に尿試料を注入・吸着しておき、その細管内を上記と同様、数mL/分程度の流量でHeを流してイオン化部へ導入する。このとき、試料吸着部を加熱し、かつ、時間をかけて昇温するようにすると、揮発性の違いにより尿中の夾雑物と測定対象物が時間的に分離されて揮発し、夾雑物によるイオン化の阻害を受けることなく、感度良く分析することができる。
【0032】
以下、本発明の一実施形態に係る質量分析装置及び質量分析方法について説明する。
【0033】
前記質量分析装置は、イオン化部と、質量分析部と、液体試料を入れるための試料容器と、試料容器を加熱するための試料加熱部とを含み、試料容器は、液体試料の上方にガスを通過させるための空間部を有し、試料容器には、試料容器にガスを導入するためのガス導入配管と空間部のガスをイオン化部に送るための試料ガス導入配管とが接続されている。そして、イオン化部で生成された空間部のガスのイオンの質量分析を行うようになっている。
【0034】
前記質量分析装置において、ガス導入配管の下流端部は、試料を含む液体の中に入るように配置されている。
【0035】
前記質量分析装置において、同伴ガス導入配管の下流端部は、空間部に配置されている。
【0036】
前記質量分析装置において、試料ガス導入配管の上流端部は、空間部に配置されている。
【0037】
前記質量分析装置は、試料の温度を経時的に変化させるために試料加熱部の発熱量を制御する温度制御部を有する。
【0038】
前記質量分析装置において、温度制御部は、試料の温度を段階的に上昇させる。
【0039】
前記質量分析装置において、温度制御部は、単位時間当たりの温度上昇率を設定して液体吸着部の温度を上昇させる。
【0040】
前記質量分析装置は、試料容器は、液体試料を吸着させるための液体吸着部である。
【0041】
前記質量分析装置において、液体試料は、尿を含む。
【0042】
前記質量分析装置において、試料は固体であり、試料を溶解するためのアルカリ性水溶液又は蒸留水を注入するための液注入管を備えている。
【0043】
前記質量分析方法は、試料容器に試料を入れ、試料容器の内部に同伴ガスを導入し、試料に含まれる複数種類の成分を気化し、これらの成分と同伴ガスとを混合して試料ガスとし、試料ガスの質量分析を行うものである。
【0044】
前記質量分析方法においては、試料ガスのイオンを生成し、質量分析を行う。
【0045】
前記質量分析方法においては、試料の温度を一定にして試料に含まれる複数種類の成分を気化する。
【0046】
前記質量分析方法において、試料容器は、液体試料を吸着させるための液体吸着部である。
【0047】
前記質量分析方法においては、試料容器を加熱し、試料の温度を経時的に変化させて液体試料に含まれる複数種類の成分を気化する。
【0048】
前記質量分析方法においては、試料の温度を段階的に上昇させて試料に含まれる複数種類の成分を気化する。
【0049】
前記質量分析方法においては、試料の温度の単位時間当たりの温度上昇率を設定し、試料の温度を上昇させて試料に含まれる複数種類の成分を気化する。
【0050】
前記質量分析方法は、液体吸着部に液体試料を吸着させ、液体吸着部を加熱し、液体吸着部の温度を経時的に変化させ、液体試料に含まれる複数種類の成分を分離して気化して質量分析部に送るものである。
【0051】
前記質量分析方法においては、液体吸着部の温度を段階的に上昇させて液体試料に含まれる複数種類の成分を気化する。
【0052】
前記質量分析方法においては、液体吸着部の温度の単位時間当たりの温度上昇率を設定し、液体吸着部の温度を上昇させて液体試料に含まれる複数種類の成分を気化する。
【0053】
前記質量分析方法において、液体試料は、尿を含み、液体試料に含まれる薬物及び薬物の代謝物を測定対象とする。
【0054】
前記質量分析方法においては、液体試料にアルカリ性試薬を添加する。
【0055】
前記質量分析方法においては、液体試料にアルカリ性水溶液を添加する。
【0056】
前記質量分析方法においては、液体試料に蒸留水を添加して希釈する。
【0057】
前記質量分析方法において、液体試料は、固体試料にアルカリ性水溶液又は蒸留水を添加して調製する。
【0058】
前記質量分析方法においては、試料を含む液体を60〜160℃に加熱し、その液体から発生した気体を質量分析部に送る。
【0059】
以下、実施例を用いて詳しく説明する。
【実施例1】
【0060】
図1は、実施例の質量分析装置を示す概略構成図である。
【0061】
本図において、質量分析装置は、尿試料1(液体試料)を入れるためのバイアル瓶2(試料容器)、試料ガス導入配管5、イオン化部6及び質量分析部8を接続した構成を有する。イオン化部6には、放電用ガス導入配管7が接続されている。
【0062】
バイアル瓶2には、ガスボンベ4からガス導入配管104を介してガスを導入するようになっている。このガスは、空気、窒素、ヘリウム、アルゴン等が好ましい。クリーンなガスが好ましいが、大気でも構わない。ガスは、連続的に導入することができる。
【0063】
バイアル瓶2に尿試料1を入れる際は、バイアル瓶2の上部にヘッドスペース101(空間部)を設けるようにし、ガス導入配管104の下流端部102が尿試料1の中に入れるようにするとともに、試料ガス導入配管5の上流端部103がヘッドスペース101に位置するようにする。
【0064】
バイアル瓶2に入れられた尿試料1は、加熱ヒーター3(試料加熱部)によって40〜80℃に加熱される。ガスボンベ4から数mL〜数十mL/分程度のガスをバイアル瓶2の中に導入し、ヘッドスペース101のガスを押し出してイオン化部6に導入する。
【0065】
バイアル瓶2の中のヘッドスペースガス101をイオン化部6に導入する試料ガス導入配管5は、尿試料1の吸着を防ぐため、200〜250℃程度に加熱するのが好ましい。また、ある程度の流速を確保するため、内径φ0.2〜1mm程度のキャピラリ配管を使うのがよい。
【0066】
イオン化部6には、APCIのような分子イオン又はそのプロトン付加体を生成できるものを用いるのが好ましい。ガス分析に通常用いられるEIイオン化の場合、一部の違法薬物のフラグメントパターンが一致してしまい、分別が困難である。また、迅速に分析するためにGCカラムによる分離を行わないため、多様な成分が同時にイオン化部6に導入される。このため、EIの場合は、スペクトルが複雑になってしまう。
【0067】
分子イオンM+又はそのプロトン付加体(M+H)+が生成するAPCIは、フラグメントが単純で多様な成分中から目的の測定対象成分を検出する場合に向いている。APCIの他に、CIやDARTTM(Direct Analysis in Real Time)などのイオン化方法も用いることもできる。
【0068】
ここでは、APCIを用いた例について記載する。
【0069】
また、本実施例においては、尿の場合について記載するが、唾液及び血液にも適用可能である。
【0070】
図2は、図1のイオン化部を示す詳細構成図である。
【0071】
本図において、イオン化部6と質量分析部8とは、イオン取込細孔13を介して接続されている。イオン化部6には、試料ガス導入配管5、放電用ガス導入配管7及び排気管201が接続されている。放電用ガス202(Air)は、放電用ガス導入配管7からイオン化部6に導入され、排気管201から排気されるようになっている。
【0072】
APCIは、針電極9に数kVの電圧を印加し、針先に生じるコロナ放電でガス中分子をイオン化する方法である。安定なイオン化を保つためには、数百mL〜数L/分の放電用ガスが必要であり、ヘッドスペースガスを導入するための試料ガス導入配管5とは別系統の放電用ガス導入配管7から放電用ガス202(Air)を導入する。
【0073】
違法薬物がイオン化されるプロセスは次の通りである。
【0074】
違法薬物は、アミン系の物質が多く、正イオンで感度良くイオン化できる。
【0075】
まず、コロナ放電領域11においてAir中の窒素が下記反応式(1)又は(2)に示す反応により、1次イオン(N2+あるいはN4+)に変化する(非特許文献1を参照)。
【0076】
【化1】

【0077】
【化2】

引出電極10には、約2mmφの1次イオン導入細孔203が設けてあり、生成した1次イオンが電界によりイオン−分子反応領域12に導入される。
【0078】
イオン−分子反応領域12においては、コロナ放電領域11で生成した1次イオンと、ヘッドスペースガスに含まれる測定対象物とが反応(イオン−分子反応)し、試料ガスのイオン(2次イオン:試料イオン)が生成される。薬物の場合は、主に(M+H)+としてプロトンが付加された2次イオンとなる。
【0079】
ここで、ヘッドスペースガス(試料ガス)は、試料ガス導入配管5から直接イオン−分子反応領域12に直接導入されるため、放電用ガス202で希釈されずに効率よくイオン化される。また、ヘッドスペースガス及び放電用ガス202は、連続的に供給することができる。
【0080】
生成された2次イオンは、イオン取込細孔13を介して質量分析部8に導入され、検出器で検出される。
【0081】
用いる質量分析法については、四重極型質量分析計、イオントラップ型質量分析計、飛行時間型質量分析計、フーリエ変換型質量分析計など各質量分析装置の他、イオンモビリティ型分析計なども用いることができる。
【0082】
以下では、質量分析装置を用いる場合を例に説明する。
【0083】
尿中成分には、多様な夾雑物が存在するため、タンデム質量分析を用いた測定が好ましい。
【0084】
図1においては、バイアル瓶2のヘッドスペースガス101を導入するために、ガス導入配管104の下流端部102を尿試料1の中に入れ、バブリングして導入している。しかし、尿試料1の中にガスを導入してバブリングを行うと、泡が液面に発生したり、液が飛沫となってガスに混合される飛沫同伴が発生したりするため、ヘッドスペース101における尿中薬物の濃度が安定しなくなる場合がある。これを防止するため、下流端部102を尿試料1の中に入れずにガスを導入するようにしてもよい。
【0085】
図4は、ガス導入配管104の下流端部102を尿試料1の中に入れない例を示したものである。
【0086】
本図に示す構成によれば、ガスボンベ4からのガスがヘッドスペース101に直接導入されるため、飛沫や泡の発生がなく、尿試料1から揮発する薬物がヘッドスペース101のガスに混合される。このため、ヘッドスペース101の薬物濃度が安定するようになる。
【0087】
図1及び4に示す質量分析装置において、バイアル瓶2に封入された尿試料1の温度は、加熱ヒーター3(試料加熱部)により、段階的に上昇させてもよいし、所定の加熱時間(加熱期間)において単位時間当たりの温度変化率(温度上昇率)を設定して上昇させてもよい。ここで、加熱時間の開始時は、測定開始時から一定時間後としてもよいし、所定の温度に達するまで他の条件(別の昇温速度)で加熱した後としてもよい。これらの温度を自動的に制御するための温度制御部を本実施例の質量分析装置に設置してもよい。
【0088】
図3は、大気圧化学イオン化で測定した質量スペクトルの例(非特許文献2より抜粋)を示したものである。
【0089】
左側のスペクトルは、MS/MS前のスペクトルであり、各薬物について(M+H)+が主要なピークとして検出されている。右側のスペクトルは(M+H)+をプレカーサーイオンとして取得したMS/MSスペクトルである。
【0090】
このように、プレカーサーイオンを選択し、MS/MSスペクトルを得ることにより、測定対象薬物を区別して検出することができる。
【0091】
図5A〜5Dは、尿中薬物を図1及び2に示す質量分析装置で測定した結果を示したものである。
【0092】
水及び人体尿(A及びB)にMA(Methamphetamine)、AP(Amphetamine)、MDA(3、4−Methylenedioxyamphetamine)及びMDMA(3、4−Methylenedioxymethamphetamine)を1ppm添加したものを試料溶液とし、この試料溶液2mLを用いて測定した。図中の矢印は、Heガスを導入開始したタイミングを示したものである。溶液は、バイアル瓶2の中に封入して60℃に加熱し、導入用のガスにはHeを用い、流量は4mL/分として測定を行った。
【0093】
図5A〜5Dから、4種類すべての薬剤の場合に、Heの導入開始と同時に信号強度が増大し、検出されていることがわかる。一方、違法薬物を添加していないブランクサンプルの場合は、信号強度が増加せず検出されていないことがわかる。
【0094】
図5A〜5Dに示したように、図1及び2に示す質量分析装置を用いれば、数十分程度の間、測定対象成分(尿中薬物)を含むヘッドスペースガスがイオン源内に導入される。すなわち、測定対象成分(尿中薬物)を含むヘッドスペースガスと1次イオンとが混合される。
【0095】
このため、瞬間的に信号が検出されるシリンジを用いたGCによるヘッドスペース分析に比べて、次のような利点がある。
【0096】
(1)複数の測定点で信号を確認でき、誤報(測定ミス)の低下に繋がる。
【0097】
(2)タンデム質量分析あるいは複数の薬物を測定対象とする場合に、十分な質量分析時間が確保できる。
【0098】
さらに、シリンジを用いた場合、シリンジ内に測定対象成分が吸着されてしまう懸念があるが、本実施例によれば、導入配管は、200〜250℃程度に加熱されるため、吸着による感度低下が殆ど無い。
【0099】
一方、特許文献3にあるような、尿試料を布に滴下した後、上下からヒーターで挟み込んで試料を加熱・気化する方式の場合、多様な夾雑物も同時にイオン化されてしまい、測定対象薬物のイオン化反応が抑制されて感度が低下してしまう。
【0100】
これに対して、本実施例によれば、40〜80℃に加熱した液体試料から揮発したヘッドスペースガスのみをイオン源に導入しているため、イオン源に導入される尿中の夾雑物は、40〜80℃の温度でヘッドスペース中に揮発した成分に限られ、濃度・種類ともに少なくなる。
【0101】
以上の作用により、本実施例によれば、尿中の多様な薬物を迅速かつ高感度に分析を行うことが可能となる。
【実施例2】
【0102】
特許文献3に記載されている方式において、加熱する温度を40〜80℃にすると、揮発する夾雑物も減るが、滴下する試料量が数十〜数百マイクロリットルと少ないため、目的とする測定対象薬物の揮発量も大きく減る。このため、イオン源に導入するガスに含まれる測定対象薬物の濃度が減って検出が難しくなる。
【0103】
図6に示す実施例は、この課題を解決するためのものである。すなわち、図6は、液体試料を直接加熱する方式の構成例を示すものである。
【0104】
本図においては、図1のバイアル瓶2(試料容器)に対応するものとして液体試料を吸着させる液体吸着部15を用いる。液体吸着部15の入口にはガス導入配管601が接続してあり、液体吸着部15の出口には試料ガス導入配管5が接続してある。出口側は、図1と同様に試料ガス導入配管5をキャピラリ配管としてイオン化部6(イオン源)に繋ぐ。液体吸着部15には、尿試料を1〜数十μL供給して含浸させる。
【0105】
液体吸着部15には、TENAX(登録商標) TA(Buchem BV社製)など固体表面に試料分子を吸着・保持する物質を詰めておく。液体吸着部15の温度は、ヒーター602(試料加熱部)により、ステップ状に昇温あるいは時間と共に所定の昇温速度で上昇させる。すなわち、液体吸着部15の温度は、ヒーター602(試料加熱部)により、段階的に上昇させてもよいし、所定の加熱時間(加熱期間)において単位時間当たりの温度変化率(温度上昇率)を設定して上昇させてもよい。ここで、加熱時間の開始時は、測定開始時から一定時間後としてもよいし、所定の温度に達するまで他の条件(別の昇温速度)で加熱した後としてもよい。
【0106】
なお、図示していないが、ヒーター602の発熱量を制御するために温度制御部を設置することが望ましい。
【0107】
本実施例においては、液体吸着部15に多孔体の一種を用いたが、これに限定されるものではなく、布、グラスファイバー、カーボンファイバーなどの繊維状の部材を用いてもよい。
【0108】
図7は、夾雑物と測定対象物とを分離して測定することを示すグラフである。
【0109】
本図に示すように、測定対象薬物の沸点(又は液体吸着部から脱離がピークとなる温度)と夾雑物の沸点(又は液体吸着部から脱離がピークとなる温度)との差異により、薬物と夾雑物とが分離され、夾雑物によるイオン化の阻害を受けることなく、薬物を感度良く測定することができる。すなわち、本図においては、夾雑物Aの沸点と夾雑物Bの沸点との間の温度を沸点とする測定対象薬物があった場合、その測定対象薬物が独立した濃度ピークを示すため、夾雑物と分けて検出することができる。
【0110】
図1に示すヘッドスペースガスを分析する方法においても、例えばバイアルの温度を40℃から80℃に経時的に昇温させ、夾雑物と分離しながら分析することも可能である。
【0111】
以上より、本実施例の場合も、尿中の多様な薬物を迅速かつ高感度に分析を行うことが可能となる。
【実施例3】
【0112】
実施例1および実施例2に記載の方式において、尿中の夾雑成分の阻害を低減できるが、尿の個体差によっては、阻害の影響を除去しきれないことも考えられる。
【0113】
図8A及び図8Bは、図4の構成を有する質量分析装置を用いて、尿試料およびその尿試料を蒸留水で希釈したものを試料として分析した結果を示したものである。横軸に質量mと電荷zとの比であるm/zをとり、縦軸に信号強度をとっている。
【0114】
図8Aは、試料容器に0.3gの炭酸カリウムを量り取っておき、上記の尿試料0.5mLを注加した後、密栓し、80℃にて5分間加熱し、前記質量分析装置で分析した結果を示したマススペクトルである。
【0115】
この場合、尿試料は、60%炭酸カリウムのアルカリ性溶液となっている。
【0116】
分析しようとしている薬物は、覚せい剤や合成麻薬であり、分子中に窒素原子を含むアミン系の物質であることは既に述べた。
【0117】
覚せい剤及びフェネチルアミン系の合成麻薬は、炭酸カリウムを含むアルカリ性水溶液中で遊離体となる。この遊離体は揮発性物質である。
【0118】
図8Aは、尿中に4種類の薬物(MA、AP、MDMA及びMDA)を各1ppm含む試料の分析結果(マススペクトル)を示したものである。
【0119】
図8Bは、図8Aと同様の尿試料を蒸留水で10倍希釈した後、図8Aと同様に0.5mL採取した試料を分析した結果(マススペクトル)である。
【0120】
同じ分析時間のマススペクトルにおいて、図8Aにおいては、AP及びMDAのプロトン付加分子の信号強度が低いが、図8Bにおいては、4種全てのプロトン付加分子が明瞭に検出された。
【0121】
図9A〜9Dは、MS/MS分析後のフラグメントイオンからマスクロマトグラムを取得した結果を示したものである。横軸に分析時間をとり、縦軸に信号強度をとっている。
【0122】
それぞれの薬物について、ブランク測定(60%炭酸カリウム水溶液)、1ppm(尿中)、0.1ppm(尿中)及び0.1ppm(尿中に1ppmで薬物を含む試料を蒸留水で10倍希釈)のマスクロマトグラムを示した。
【0123】
全ての薬物について分析開始直後からクロマトグラムが立ち上がり、それぞれが検出されていることが確認できた。
【0124】
ここで、図8Aの結果(1ppm)においては、4種類の薬物を十分に検出し、各種薬物のMS/MS分析後、スペクトルパターンから物質の判定を行うことが可能であった。
【0125】
ただし、図9A〜9Dの結果から、AP及びMDAの検出ピークが得られる時刻は、MA及びMDMAの検出ピークが得られる時刻と比較して、後になり、かつ、検出感度は、MA及びMDMAと比較して低くなった。
【0126】
また、図1および図2の質量分析装置において、夾雑成分の影響を低減して分析する場合、4種類を同時に分析する場合は、検出される時間に差異が生じる。
【0127】
この現象は尿中の夾雑成分による検出阻害であると考えられる。また、物質ごとの物性(沸点・蒸気圧)によるものであり、互いの気化が拮抗していることも考えられる。
【0128】
図9A〜9Dにおいては、希釈なしの1ppmを分析した場合のマスクロマトグラムと、希釈して0.1ppmを分析した場合のマスクロマトグラムとを比較すると、AP及びMDAについては、後者(0.1ppm)の方が、信号強度が最大となる時刻が早くなったことを示している。
【0129】
この結果から、蒸留水で尿試料を希釈することで、尿中の夾雑成分の影響が緩和され、4種類の薬物を迅速に検知しやすくなったといえる。
【0130】
図9Eは、希釈なしの1ppmを分析した場合、希釈して0.1ppmを分析した場合、及び、希釈して0.01ppmを分析した場合のマスクロマトグラムをAPについて示した結果である。横軸に分析時間をとり、縦軸に信号強度をとっている。
【0131】
APは、蒸留水で100倍希釈した場合(0.01ppm)においても検出された。
【0132】
一般的に、分析においては試料を希釈すると、検出感度が低下することは当然起こりうるが、本方式においては、AP及びMDAの検出感度が改善され、尿中の4種類の違法薬物を同時に迅速に分析可能となった。
【0133】
ここで、蒸留水で10倍希釈した場合、MA及びMDMAの信号強度は1ppmと比較して低下するが、検知するには十分な感度が得られている。
【0134】
したがって、薬物を含む尿を蒸留水で10倍程度まで希釈しても、4種類の違法薬物の検出を迅速かつ簡易に行うことが可能であることが示された。
【0135】
薬物検知の目的においては、4種類の薬物全てを1分以内に検知し、判定が可能であった。
【0136】
本実施例の別方法として、尿試料を先に80%炭酸カリウム水溶液等のアルカリ性水溶液で希釈してもよい。
【0137】
この場合、0.250mLの尿試料と、0.250mLの80%炭酸カリウム水溶液とを混合すると、炭酸カリウム濃度は40%となるが、炭酸カリウムの分析試料溶液中の濃度は30〜60%が望ましい。
【0138】
また、加熱温度は、80℃にて2〜5分間とすることで良好な結果が得られた。
【0139】
さらにいえば、炭酸カリウム水溶液を試料に添加する方法は、覚せい剤や麻薬の粉末・錠剤試料にも適用することも可能である。
【0140】
覚せい剤の粉末(結晶など)適量を試料溶液へ移し取り、さらに炭酸カリウム水溶液を添加し、密栓後、静かに振とうするなどして溶解し、加熱後、分析すればよい。
【実施例4】
【0141】
図10は、大麻試料を分析した結果を示したものである。横軸にm/zをとり、縦軸に信号強度をとっている。
【0142】
大麻樹脂の粉末試料1mgに対し、80%炭酸カリウム水溶液を1mL添加し、150℃に5分間加熱して、分析を行った結果のマススペクトルである。
【0143】
ここで、m/z 311のピークは、カンナビノール(Cannabinol:CBN)を示すものであり、m/z 315のピークは、Δ9−テトラヒドロカンナビノール(Δ9−Tetrahydrocannabinol:Δ9−THC)またはカンナビジオール(Cannabidiol:CBD)のプロトン付加分子のイオンを示すものである。
【0144】
上記の3種類の物質は、大麻特有に含まれる幻覚成分であり、Δ9−THCは、麻薬に指定されている取締り対象物質である。
【0145】
これらを検出することにより、分析した試料が大麻であることを判定することができる。
【0146】
従来、大麻の分析においては、メタノールなどの有機溶媒で試料から薬物の成分を抽出する(非特許文献4)。
【0147】
さらに、液−液抽出などの操作を繰り返すことにより、大麻中の幻覚成分を分離精製する必要がある。
【0148】
本実施例においては、上述した操作なしに、簡易な分析が可能であった。
【0149】
また、大麻試料においては、アルカリ性水溶液ではなく、蒸留水の添加によっても検出が可能であったため、炭酸カリウム水溶液ではなく蒸留水を添加し、加熱後に分析してもよい。蒸留水を用いた場合も大麻試料1mgに対し、蒸留水1mLを添加することで良好な結果が得られた。
【実施例5】
【0150】
図11は、コカイン試料を分析した結果である。横軸にm/zをとり、縦軸に信号強度をとっている。
【0151】
本実施例においては、試料瓶内に炭酸カリウム水溶液を0.1g量り取っておき、コカイン水溶液(50μg/mL)200μLを注加し、密栓後、80℃に5分間加熱して、分析を行った。
【0152】
従来の方法においては、呈色反応が採用されており(非特許文献4)、簡易な分析方法はこれまで実施されていなかった。
【0153】
本図は、コカイン水溶液に炭酸カリウムを少量加えてアルカリ性とし、加熱することにより、簡易にヘッドスペース分析が可能であることを示した結果である。
【0154】
また、コカイン水溶液ではなく、コカインの粉末を炭酸カリウム水溶液中に溶解し、分析することも可能であった。
【0155】
この場合、炭酸カリウム水溶液の最終濃度は30〜80%が望ましい。
【0156】
また、加熱する場合は、80℃で十分な検出が可能であったが、60〜160℃の範囲、もしくは指定の温度に徐々に昇温させるなどの手法を用いてもよい。
【実施例6】
【0157】
図12は、あへん試料を分析した結果である。横軸にm/zをとり、縦軸に信号強度をとっている。
【0158】
本図は、あへん試料10mgを試料容器に量り取り、80%炭酸カリウム水溶液200μLを添加し、密栓後、150℃にて5分間加熱後、ヘッドスペース分析を行った結果である。
【0159】
本図から、あへんに特有のメコニン、コデイン及びテバインを検出し、あへんの検知が可能であることが示された。
【0160】
上記のうち、メコニンは、あへん特有の成分である。
【0161】
また、コデイン及びテバインは、アヘンアルカロイドの一種であり、単一の物質でも取締り対象の規制物質(麻薬)に指定されている。
【0162】
従来、あへんの検知においては、アヘンアルカロイドと呼ばれる麻薬成分を対象に分析が行われてきた。
【0163】
ここで、アヘンアルカロイドとは、モルヒネやコデインなどの違法薬物成分を示す(非特許文献4)。
【0164】
これに対し、本実施例において説明する薬物検知装置の目的は、迅速な薬物の検知であり、あへんを証明する物質が得られればよい。
【0165】
本実施例においては、あへんに特有のメコニン、コデイン及びテバインを検出し、CID分析後のスペクトルパターンから、分析した物質を特定し、あへんの検知が可能であることが示された。
【0166】
したがって、呈色反応のための抽出・精製操作や、GC/MS分析のための誘導体化反応などの煩雑な操作が不要であり、簡易で迅速な分析が可能となった。
【0167】
実施例3〜6に示す通り、尿中の覚せい剤および麻薬、並びに固体試料(粉末、結晶及び錠剤)について簡易で迅速な分析が可能となった。
【0168】
さらにいえば、炭酸カリウム水溶液などのアルカリ性水溶液を用いれば、全ての分析試料について、試料容器内で混合し、加熱する共通の手法により、分析、検知及び判定を行うことが可能となった。
【0169】
実施例3〜6においては、アルカリ性水溶液の溶質として炭酸カリウムを用いたが、これ以外の溶質としては、水酸化カリウム、水酸化ナトリウムなどを用いることができる。アルカリ性水溶液のpHは11以上が望ましい。アルカリ性水溶液の溶質の濃度は、30〜80%が望ましく、30〜60%が更に望ましい。
【0170】
図13は、固体試料を溶解あるいは気化を促進するための構成を有する試料容器を示したものである。
【0171】
本図においては、バイアル瓶2には、固体試料1301を溶解するためのアルカリ性水溶液又は蒸留水を注入するための液注入管1302が設けてある。また、バイアル瓶2の内部には、磁力によって回転するスターラ1303(マグネチックスターラ)を設けてある。
【0172】
固体試料1301を溶解する場合、バイアル瓶2に固体試料1301を封入し、液注入管1302からアルカリ性水溶液又は蒸留水を注入し、スターラ1303を回転させることによりバイアル瓶2の内部の液を撹拌し、固体試料1301を溶解する。液の撹拌は、加熱ヒーター3によって液を加熱しながら行うこともできる。
【0173】
以下、本発明の効果について更に説明する。
【0174】
本発明によれば、物質の質量数と、MS/MS分析によるスペクトルパターンとから、測定した成分そのものを判定可能であるため、判定を確実にすることができる。
【0175】
また、尿試料の場合は、予め試料容器に少量の炭酸カリウムを量りとっておき、尿試料を加えるだけで尿中覚せい剤の分析が可能であり、加熱することで更なる検出感度の向上が望める。
【0176】
また、覚せい剤や麻薬の固体試料(粉末、結晶、錠剤など)の場合も、煩雑な抽出・精製の操作がなく、炭酸カリウム水溶液などのアルカリ性水溶液を添加し、試料容器内で混合する方法で検出が可能である。すなわち、尿中に溶け込んだ違法薬物、及び紛末、錠剤などの固体状の違法薬物を簡易に、かつ、迅速に分析することができる。
【0177】
また、大麻については、呈色反応のための3種類の試薬を必要としない。コカインについても、呈色反応のための3種類の試薬を必要としない。あへんについても、呈色反応のための試薬を必要とせず、アヘンアルカロイド類の抽出・精製の操作がなく、誘導体化などのステップなしに検出が可能となる。
【0178】
さらに、大麻、コカイン及びあへんの3種類の試料について調製方法が同じである。
【符号の説明】
【0179】
1:尿試料、2:バイアル瓶、3:加熱ヒーター、4:ガスボンベ、5:試料ガス導入配管、6:イオン化部、7:放電用ガス導入配管、8:質量分析部、9:針電極、10:引出電極、11:コロナ放電領域、12:イオン−分子反応領域、13:イオン取込細孔、15:液体吸着部、101:ヘッドスペース、102:下流端部、103:上流端部、104:ガス導入配管。
【技術分野】
【0001】
本発明は、薬物検知装置に関する。
【背景技術】
【0002】
以下では、ガスクロマトグラフをGC(Gas Chromatograph)、ガスクロマトグラフと質量分析計とを結合した装置をGC/MS(Gas Chromatograph / Mass Spectrometer)、大気圧化学イオン化をAPCI(Atmospheric Pressure Chemical Ionization)、化学イオン化をCI(Chemical Ionization)、電子イオン化をEI(Electron Ionization)とそれぞれ略記する。
【0003】
覚せい剤、麻薬などの違法薬物の現場捜査における検知としては、免疫法などを利用した試薬キットが用いられている。試薬キットによる検査法の場合、構造が似ている物質で偽陽性が出ることがあり、より検知精度が高くて簡便な検知方法が求められている。
【0004】
特許文献1には、尿を封入した密閉容器中のヘッドスペースガスをGCに導入し、尿中覚せい剤を分析する技術が開示されている。
【0005】
特許文献2には、試料ガスをGCカラムで分離し、GCカラム出口をAPCIイオン源のイオン分子反応領域に設け、高感度化を図る構成について記載がある。
【0006】
特許文献3には、薬物を含む液体サンプルを布に滴下し、布を上下の加熱ヒーターで挟み込み液体試料を気化させ、イオントラップ型質量分析計で分析する手法について記載がある。
【0007】
非特許文献3には、覚せい剤成分は、炭酸カリウムの溶解熱及び液性(アルカリ性)により、尿中から揮発して気相(ヘッドスペース)へ移行することが記載されている。また、非特許文献3には、呈色反応以外にも、各種の違法薬物に対するモノクローナル抗体を用い、抗原抗体反応を利用した予試験用の試薬キットが記載されている。
【0008】
特許文献4には、呈色反応による判定を用いて、取扱いが簡易で迅速な検知を可能とする覚せい剤の予試験キットが開示されている。
【0009】
非特許文献4には、大麻の呈色試験、コカインの定性試験における呈色反応の利用及びあへんの予試験における呈色試験に関する記載がある。
【0010】
特許文献5には、呈色反応を利用するあへんの検出方法および検出キットが開示されている。
【先行技術文献】
【特許文献】
【0011】
【特許文献1】特開平4−184253号公報
【特許文献2】特開2006−86002号公報
【特許文献3】特開2008−51520号公報
【特許文献4】実用新案登録第3156553号公報
【特許文献5】特公平8−27275号公報
【非特許文献】
【0012】
【非特許文献1】J. Chem. Phys.、52、212 (1970)
【非特許文献2】J. Mass Spectrom.、44、1300 (2009)
【非特許文献3】捜査のための法科学 第二部 <法工学・法化学> 令文社、pp.272〜278
【非特許文献4】薬毒物試験法と注解2006 −分析・毒性・対処法− 東京化学同人、pp.131〜145、pp.175〜185
【発明の概要】
【発明が解決しようとする課題】
【0013】
特許文献1に開示されている方法を用いて、ヘッドスペースのガスをシリンジで吸入し、質量分析装置のイオン源導入配管にシリンジ内ガスを吐出させると、シリンジ内で測定対象物が吸着し、マスクロマトグラムのピークがブロードになったり、実質的な感度が下がったりする点で改善の余地がある。
【0014】
また、特許文献3には、尿中の夾雑成分が加熱により測定対象物と同時に分析部に導入され、イオン化が阻害されて感度低下が起こる場合の対応について開示されていない。
【0015】
特許文献4に記載されている予試験キットは、覚せい剤の判定は色調見本を元にするものであり、捜査現場における車内等の空間では色の見間違いを起こす可能性がある。
【0016】
非特許文献3に記載されている各種の検査用キットは、判定を捜査員の目視によるものとしていることが多く、誤判定する問題がある。また、抗原抗体反応によると試料中の風邪薬の成分と交差反応を起こすことがあり、正確な判定が難しい場合もある。
【0017】
また、大麻試料、コカイン、あへんなどの呈色反応は、目視での確認となるため、判定が困難であり、判定を誤ることがある。また、呈色分析のための試料の抽出・精製操作は煩雑である。
【0018】
非特許文献4に記載されている大麻試料の分析においては、試料から薬物の成分をメタノールなどの有機溶媒を用いて抽出する。さらに、液−液抽出などの操作を繰り返して、大麻中の幻覚成分(取締り対象の成分)を分離精製する必要がある。
【0019】
非特許文献4に記載されているあへんのGC/MS分析を行う場合には、アヘンアルカロイド類の抽出操作を行った後、誘導体化して分析を行い、メコン酸、コデイン及びモルヒネの誘導体を検出できるが、誘導体化のための操作が煩雑である。
【0020】
特許文献5に記載されているあへんの検出は、試料の水溶性及び呈色反応で判定する必要がある。
【0021】
非特許文献4及び特許文献5に記載されている大麻、コカイン及びあへんの試料の調製方法は、それぞれ異なる。
【0022】
本発明の目的は、尿中の多様な薬物を迅速に、かつ、高感度に分析を行うための薬物検知装置を提供することにある。
【課題を解決するための手段】
【0023】
本発明の質量分析装置は、イオン化部と、質量分析部と、試料を入れるための試料容器と、前記試料容器を加熱するための試料加熱部とを含み、前記試料容器には、気相である空間部を設けるとともに、前記試料容器に同伴ガスを導入するための同伴ガス導入配管と前記空間部の試料ガスを前記イオン化部に送るための試料ガス導入配管とが接続してあり、前記イオン化部は、前記試料ガスのイオンを生成し、前記質量分析部は、前記イオンの質量分析を行うことを特徴とする。
【発明の効果】
【0024】
本発明によれば、尿中の多様な薬物を迅速かつ高感度に分析を行うことが可能となる。
【図面の簡単な説明】
【0025】
【図1】実施例の質量分析装置を示す概略構成図である。
【図2】図1のイオン化部を示す詳細構成図である。
【図3】薬物の質量スペクトル(公知例)を示すグラフである。
【図4】図1の質量分析装置の変形例を示す構成図である。
【図5A】実施例の質量分析装置による薬物(Methamphetamine:MA)の測定結果を示すグラフである。
【図5B】実施例の質量分析装置による薬物(Amphetamine:AP)の測定結果を示すグラフである。
【図5C】実施例の質量分析装置による薬物(3、4−Methylenedioxyamphetamine:MDA)の測定結果を示すグラフである。
【図5D】実施例の質量分析装置による薬物(3、4−Methylenedioxymethamphetamine:MDMA)の測定結果を示すグラフである。
【図6】他の実施例に係る質量分析装置を示す概略構成図である。
【図7】図6の質量分析装置により夾雑物と測定対象物とを分離して検出するための方式を説明するグラフである。
【図8A】実施例の質量分析装置による尿試料中の薬物(1ppm)のマススペクトルである。
【図8B】実施例の質量分析装置による尿試料中の薬物(0.1ppm)のマススペクトルである。
【図9A】実施例の質量分析装置による薬物(MA)の測定結果を示すグラフである。
【図9B】実施例の質量分析装置による薬物(AP)の測定結果を示すグラフである。
【図9C】実施例の質量分析装置による薬物(MDA)の測定結果を示すグラフである。
【図9D】実施例の質量分析装置による薬物(MDMA)の測定結果を示すグラフである。
【図9E】実施例の質量分析装置による薬物(AP)の測定結果を示すグラフである。
【図10】実施例の質量分析装置による大麻のマススペクトルである。
【図11】実施例の質量分析装置によるコカインのマススペクトルである。
【図12】実施例の質量分析装置によるあへんのマススペクトルである。
【図13】図4の質量分析装置の変形例を示す構成図である。
【発明を実施するための形態】
【0026】
本発明は、ガス中揮発成分を分析する質量分析装置に関する。特に、尿中の違法薬物を分析する質量分析装置に関する。
【0027】
本発明においては、ヘッドスペースガスを大気圧化学イオン化部(APCI部)に連続的に導入する。
【0028】
シリンジを使った注入法の場合、数〜10μLを数秒間で注入するのに対し(信号がピーク形状となる)、連続して測定対象ガスを導入するため、数分程度安定した信号強度が得られる。
【0029】
サンプルとして使用する尿の量は、高々数mL〜数十mL(ミリリットル)であるため、容器内のヘッドスペース容量も数mL〜数十mLである。一方、APCIの放電部に必要なガス流量は数百mL/分であるため、ヘッドスペースガスを数百mL/分の流量でイオン化部に流入させると、測定対象成分が希釈されてしまい、測定感度が低下してしまう。
【0030】
そこで、ヘッドスペースガスを数mL/分程度の流量でイオン化部に導入し、放電に必要なガスは別系統で導入する。
【0031】
また、別の導入方式として、細管に尿試料を注入・吸着しておき、その細管内を上記と同様、数mL/分程度の流量でHeを流してイオン化部へ導入する。このとき、試料吸着部を加熱し、かつ、時間をかけて昇温するようにすると、揮発性の違いにより尿中の夾雑物と測定対象物が時間的に分離されて揮発し、夾雑物によるイオン化の阻害を受けることなく、感度良く分析することができる。
【0032】
以下、本発明の一実施形態に係る質量分析装置及び質量分析方法について説明する。
【0033】
前記質量分析装置は、イオン化部と、質量分析部と、液体試料を入れるための試料容器と、試料容器を加熱するための試料加熱部とを含み、試料容器は、液体試料の上方にガスを通過させるための空間部を有し、試料容器には、試料容器にガスを導入するためのガス導入配管と空間部のガスをイオン化部に送るための試料ガス導入配管とが接続されている。そして、イオン化部で生成された空間部のガスのイオンの質量分析を行うようになっている。
【0034】
前記質量分析装置において、ガス導入配管の下流端部は、試料を含む液体の中に入るように配置されている。
【0035】
前記質量分析装置において、同伴ガス導入配管の下流端部は、空間部に配置されている。
【0036】
前記質量分析装置において、試料ガス導入配管の上流端部は、空間部に配置されている。
【0037】
前記質量分析装置は、試料の温度を経時的に変化させるために試料加熱部の発熱量を制御する温度制御部を有する。
【0038】
前記質量分析装置において、温度制御部は、試料の温度を段階的に上昇させる。
【0039】
前記質量分析装置において、温度制御部は、単位時間当たりの温度上昇率を設定して液体吸着部の温度を上昇させる。
【0040】
前記質量分析装置は、試料容器は、液体試料を吸着させるための液体吸着部である。
【0041】
前記質量分析装置において、液体試料は、尿を含む。
【0042】
前記質量分析装置において、試料は固体であり、試料を溶解するためのアルカリ性水溶液又は蒸留水を注入するための液注入管を備えている。
【0043】
前記質量分析方法は、試料容器に試料を入れ、試料容器の内部に同伴ガスを導入し、試料に含まれる複数種類の成分を気化し、これらの成分と同伴ガスとを混合して試料ガスとし、試料ガスの質量分析を行うものである。
【0044】
前記質量分析方法においては、試料ガスのイオンを生成し、質量分析を行う。
【0045】
前記質量分析方法においては、試料の温度を一定にして試料に含まれる複数種類の成分を気化する。
【0046】
前記質量分析方法において、試料容器は、液体試料を吸着させるための液体吸着部である。
【0047】
前記質量分析方法においては、試料容器を加熱し、試料の温度を経時的に変化させて液体試料に含まれる複数種類の成分を気化する。
【0048】
前記質量分析方法においては、試料の温度を段階的に上昇させて試料に含まれる複数種類の成分を気化する。
【0049】
前記質量分析方法においては、試料の温度の単位時間当たりの温度上昇率を設定し、試料の温度を上昇させて試料に含まれる複数種類の成分を気化する。
【0050】
前記質量分析方法は、液体吸着部に液体試料を吸着させ、液体吸着部を加熱し、液体吸着部の温度を経時的に変化させ、液体試料に含まれる複数種類の成分を分離して気化して質量分析部に送るものである。
【0051】
前記質量分析方法においては、液体吸着部の温度を段階的に上昇させて液体試料に含まれる複数種類の成分を気化する。
【0052】
前記質量分析方法においては、液体吸着部の温度の単位時間当たりの温度上昇率を設定し、液体吸着部の温度を上昇させて液体試料に含まれる複数種類の成分を気化する。
【0053】
前記質量分析方法において、液体試料は、尿を含み、液体試料に含まれる薬物及び薬物の代謝物を測定対象とする。
【0054】
前記質量分析方法においては、液体試料にアルカリ性試薬を添加する。
【0055】
前記質量分析方法においては、液体試料にアルカリ性水溶液を添加する。
【0056】
前記質量分析方法においては、液体試料に蒸留水を添加して希釈する。
【0057】
前記質量分析方法において、液体試料は、固体試料にアルカリ性水溶液又は蒸留水を添加して調製する。
【0058】
前記質量分析方法においては、試料を含む液体を60〜160℃に加熱し、その液体から発生した気体を質量分析部に送る。
【0059】
以下、実施例を用いて詳しく説明する。
【実施例1】
【0060】
図1は、実施例の質量分析装置を示す概略構成図である。
【0061】
本図において、質量分析装置は、尿試料1(液体試料)を入れるためのバイアル瓶2(試料容器)、試料ガス導入配管5、イオン化部6及び質量分析部8を接続した構成を有する。イオン化部6には、放電用ガス導入配管7が接続されている。
【0062】
バイアル瓶2には、ガスボンベ4からガス導入配管104を介してガスを導入するようになっている。このガスは、空気、窒素、ヘリウム、アルゴン等が好ましい。クリーンなガスが好ましいが、大気でも構わない。ガスは、連続的に導入することができる。
【0063】
バイアル瓶2に尿試料1を入れる際は、バイアル瓶2の上部にヘッドスペース101(空間部)を設けるようにし、ガス導入配管104の下流端部102が尿試料1の中に入れるようにするとともに、試料ガス導入配管5の上流端部103がヘッドスペース101に位置するようにする。
【0064】
バイアル瓶2に入れられた尿試料1は、加熱ヒーター3(試料加熱部)によって40〜80℃に加熱される。ガスボンベ4から数mL〜数十mL/分程度のガスをバイアル瓶2の中に導入し、ヘッドスペース101のガスを押し出してイオン化部6に導入する。
【0065】
バイアル瓶2の中のヘッドスペースガス101をイオン化部6に導入する試料ガス導入配管5は、尿試料1の吸着を防ぐため、200〜250℃程度に加熱するのが好ましい。また、ある程度の流速を確保するため、内径φ0.2〜1mm程度のキャピラリ配管を使うのがよい。
【0066】
イオン化部6には、APCIのような分子イオン又はそのプロトン付加体を生成できるものを用いるのが好ましい。ガス分析に通常用いられるEIイオン化の場合、一部の違法薬物のフラグメントパターンが一致してしまい、分別が困難である。また、迅速に分析するためにGCカラムによる分離を行わないため、多様な成分が同時にイオン化部6に導入される。このため、EIの場合は、スペクトルが複雑になってしまう。
【0067】
分子イオンM+又はそのプロトン付加体(M+H)+が生成するAPCIは、フラグメントが単純で多様な成分中から目的の測定対象成分を検出する場合に向いている。APCIの他に、CIやDARTTM(Direct Analysis in Real Time)などのイオン化方法も用いることもできる。
【0068】
ここでは、APCIを用いた例について記載する。
【0069】
また、本実施例においては、尿の場合について記載するが、唾液及び血液にも適用可能である。
【0070】
図2は、図1のイオン化部を示す詳細構成図である。
【0071】
本図において、イオン化部6と質量分析部8とは、イオン取込細孔13を介して接続されている。イオン化部6には、試料ガス導入配管5、放電用ガス導入配管7及び排気管201が接続されている。放電用ガス202(Air)は、放電用ガス導入配管7からイオン化部6に導入され、排気管201から排気されるようになっている。
【0072】
APCIは、針電極9に数kVの電圧を印加し、針先に生じるコロナ放電でガス中分子をイオン化する方法である。安定なイオン化を保つためには、数百mL〜数L/分の放電用ガスが必要であり、ヘッドスペースガスを導入するための試料ガス導入配管5とは別系統の放電用ガス導入配管7から放電用ガス202(Air)を導入する。
【0073】
違法薬物がイオン化されるプロセスは次の通りである。
【0074】
違法薬物は、アミン系の物質が多く、正イオンで感度良くイオン化できる。
【0075】
まず、コロナ放電領域11においてAir中の窒素が下記反応式(1)又は(2)に示す反応により、1次イオン(N2+あるいはN4+)に変化する(非特許文献1を参照)。
【0076】
【化1】

【0077】
【化2】

引出電極10には、約2mmφの1次イオン導入細孔203が設けてあり、生成した1次イオンが電界によりイオン−分子反応領域12に導入される。
【0078】
イオン−分子反応領域12においては、コロナ放電領域11で生成した1次イオンと、ヘッドスペースガスに含まれる測定対象物とが反応(イオン−分子反応)し、試料ガスのイオン(2次イオン:試料イオン)が生成される。薬物の場合は、主に(M+H)+としてプロトンが付加された2次イオンとなる。
【0079】
ここで、ヘッドスペースガス(試料ガス)は、試料ガス導入配管5から直接イオン−分子反応領域12に直接導入されるため、放電用ガス202で希釈されずに効率よくイオン化される。また、ヘッドスペースガス及び放電用ガス202は、連続的に供給することができる。
【0080】
生成された2次イオンは、イオン取込細孔13を介して質量分析部8に導入され、検出器で検出される。
【0081】
用いる質量分析法については、四重極型質量分析計、イオントラップ型質量分析計、飛行時間型質量分析計、フーリエ変換型質量分析計など各質量分析装置の他、イオンモビリティ型分析計なども用いることができる。
【0082】
以下では、質量分析装置を用いる場合を例に説明する。
【0083】
尿中成分には、多様な夾雑物が存在するため、タンデム質量分析を用いた測定が好ましい。
【0084】
図1においては、バイアル瓶2のヘッドスペースガス101を導入するために、ガス導入配管104の下流端部102を尿試料1の中に入れ、バブリングして導入している。しかし、尿試料1の中にガスを導入してバブリングを行うと、泡が液面に発生したり、液が飛沫となってガスに混合される飛沫同伴が発生したりするため、ヘッドスペース101における尿中薬物の濃度が安定しなくなる場合がある。これを防止するため、下流端部102を尿試料1の中に入れずにガスを導入するようにしてもよい。
【0085】
図4は、ガス導入配管104の下流端部102を尿試料1の中に入れない例を示したものである。
【0086】
本図に示す構成によれば、ガスボンベ4からのガスがヘッドスペース101に直接導入されるため、飛沫や泡の発生がなく、尿試料1から揮発する薬物がヘッドスペース101のガスに混合される。このため、ヘッドスペース101の薬物濃度が安定するようになる。
【0087】
図1及び4に示す質量分析装置において、バイアル瓶2に封入された尿試料1の温度は、加熱ヒーター3(試料加熱部)により、段階的に上昇させてもよいし、所定の加熱時間(加熱期間)において単位時間当たりの温度変化率(温度上昇率)を設定して上昇させてもよい。ここで、加熱時間の開始時は、測定開始時から一定時間後としてもよいし、所定の温度に達するまで他の条件(別の昇温速度)で加熱した後としてもよい。これらの温度を自動的に制御するための温度制御部を本実施例の質量分析装置に設置してもよい。
【0088】
図3は、大気圧化学イオン化で測定した質量スペクトルの例(非特許文献2より抜粋)を示したものである。
【0089】
左側のスペクトルは、MS/MS前のスペクトルであり、各薬物について(M+H)+が主要なピークとして検出されている。右側のスペクトルは(M+H)+をプレカーサーイオンとして取得したMS/MSスペクトルである。
【0090】
このように、プレカーサーイオンを選択し、MS/MSスペクトルを得ることにより、測定対象薬物を区別して検出することができる。
【0091】
図5A〜5Dは、尿中薬物を図1及び2に示す質量分析装置で測定した結果を示したものである。
【0092】
水及び人体尿(A及びB)にMA(Methamphetamine)、AP(Amphetamine)、MDA(3、4−Methylenedioxyamphetamine)及びMDMA(3、4−Methylenedioxymethamphetamine)を1ppm添加したものを試料溶液とし、この試料溶液2mLを用いて測定した。図中の矢印は、Heガスを導入開始したタイミングを示したものである。溶液は、バイアル瓶2の中に封入して60℃に加熱し、導入用のガスにはHeを用い、流量は4mL/分として測定を行った。
【0093】
図5A〜5Dから、4種類すべての薬剤の場合に、Heの導入開始と同時に信号強度が増大し、検出されていることがわかる。一方、違法薬物を添加していないブランクサンプルの場合は、信号強度が増加せず検出されていないことがわかる。
【0094】
図5A〜5Dに示したように、図1及び2に示す質量分析装置を用いれば、数十分程度の間、測定対象成分(尿中薬物)を含むヘッドスペースガスがイオン源内に導入される。すなわち、測定対象成分(尿中薬物)を含むヘッドスペースガスと1次イオンとが混合される。
【0095】
このため、瞬間的に信号が検出されるシリンジを用いたGCによるヘッドスペース分析に比べて、次のような利点がある。
【0096】
(1)複数の測定点で信号を確認でき、誤報(測定ミス)の低下に繋がる。
【0097】
(2)タンデム質量分析あるいは複数の薬物を測定対象とする場合に、十分な質量分析時間が確保できる。
【0098】
さらに、シリンジを用いた場合、シリンジ内に測定対象成分が吸着されてしまう懸念があるが、本実施例によれば、導入配管は、200〜250℃程度に加熱されるため、吸着による感度低下が殆ど無い。
【0099】
一方、特許文献3にあるような、尿試料を布に滴下した後、上下からヒーターで挟み込んで試料を加熱・気化する方式の場合、多様な夾雑物も同時にイオン化されてしまい、測定対象薬物のイオン化反応が抑制されて感度が低下してしまう。
【0100】
これに対して、本実施例によれば、40〜80℃に加熱した液体試料から揮発したヘッドスペースガスのみをイオン源に導入しているため、イオン源に導入される尿中の夾雑物は、40〜80℃の温度でヘッドスペース中に揮発した成分に限られ、濃度・種類ともに少なくなる。
【0101】
以上の作用により、本実施例によれば、尿中の多様な薬物を迅速かつ高感度に分析を行うことが可能となる。
【実施例2】
【0102】
特許文献3に記載されている方式において、加熱する温度を40〜80℃にすると、揮発する夾雑物も減るが、滴下する試料量が数十〜数百マイクロリットルと少ないため、目的とする測定対象薬物の揮発量も大きく減る。このため、イオン源に導入するガスに含まれる測定対象薬物の濃度が減って検出が難しくなる。
【0103】
図6に示す実施例は、この課題を解決するためのものである。すなわち、図6は、液体試料を直接加熱する方式の構成例を示すものである。
【0104】
本図においては、図1のバイアル瓶2(試料容器)に対応するものとして液体試料を吸着させる液体吸着部15を用いる。液体吸着部15の入口にはガス導入配管601が接続してあり、液体吸着部15の出口には試料ガス導入配管5が接続してある。出口側は、図1と同様に試料ガス導入配管5をキャピラリ配管としてイオン化部6(イオン源)に繋ぐ。液体吸着部15には、尿試料を1〜数十μL供給して含浸させる。
【0105】
液体吸着部15には、TENAX(登録商標) TA(Buchem BV社製)など固体表面に試料分子を吸着・保持する物質を詰めておく。液体吸着部15の温度は、ヒーター602(試料加熱部)により、ステップ状に昇温あるいは時間と共に所定の昇温速度で上昇させる。すなわち、液体吸着部15の温度は、ヒーター602(試料加熱部)により、段階的に上昇させてもよいし、所定の加熱時間(加熱期間)において単位時間当たりの温度変化率(温度上昇率)を設定して上昇させてもよい。ここで、加熱時間の開始時は、測定開始時から一定時間後としてもよいし、所定の温度に達するまで他の条件(別の昇温速度)で加熱した後としてもよい。
【0106】
なお、図示していないが、ヒーター602の発熱量を制御するために温度制御部を設置することが望ましい。
【0107】
本実施例においては、液体吸着部15に多孔体の一種を用いたが、これに限定されるものではなく、布、グラスファイバー、カーボンファイバーなどの繊維状の部材を用いてもよい。
【0108】
図7は、夾雑物と測定対象物とを分離して測定することを示すグラフである。
【0109】
本図に示すように、測定対象薬物の沸点(又は液体吸着部から脱離がピークとなる温度)と夾雑物の沸点(又は液体吸着部から脱離がピークとなる温度)との差異により、薬物と夾雑物とが分離され、夾雑物によるイオン化の阻害を受けることなく、薬物を感度良く測定することができる。すなわち、本図においては、夾雑物Aの沸点と夾雑物Bの沸点との間の温度を沸点とする測定対象薬物があった場合、その測定対象薬物が独立した濃度ピークを示すため、夾雑物と分けて検出することができる。
【0110】
図1に示すヘッドスペースガスを分析する方法においても、例えばバイアルの温度を40℃から80℃に経時的に昇温させ、夾雑物と分離しながら分析することも可能である。
【0111】
以上より、本実施例の場合も、尿中の多様な薬物を迅速かつ高感度に分析を行うことが可能となる。
【実施例3】
【0112】
実施例1および実施例2に記載の方式において、尿中の夾雑成分の阻害を低減できるが、尿の個体差によっては、阻害の影響を除去しきれないことも考えられる。
【0113】
図8A及び図8Bは、図4の構成を有する質量分析装置を用いて、尿試料およびその尿試料を蒸留水で希釈したものを試料として分析した結果を示したものである。横軸に質量mと電荷zとの比であるm/zをとり、縦軸に信号強度をとっている。
【0114】
図8Aは、試料容器に0.3gの炭酸カリウムを量り取っておき、上記の尿試料0.5mLを注加した後、密栓し、80℃にて5分間加熱し、前記質量分析装置で分析した結果を示したマススペクトルである。
【0115】
この場合、尿試料は、60%炭酸カリウムのアルカリ性溶液となっている。
【0116】
分析しようとしている薬物は、覚せい剤や合成麻薬であり、分子中に窒素原子を含むアミン系の物質であることは既に述べた。
【0117】
覚せい剤及びフェネチルアミン系の合成麻薬は、炭酸カリウムを含むアルカリ性水溶液中で遊離体となる。この遊離体は揮発性物質である。
【0118】
図8Aは、尿中に4種類の薬物(MA、AP、MDMA及びMDA)を各1ppm含む試料の分析結果(マススペクトル)を示したものである。
【0119】
図8Bは、図8Aと同様の尿試料を蒸留水で10倍希釈した後、図8Aと同様に0.5mL採取した試料を分析した結果(マススペクトル)である。
【0120】
同じ分析時間のマススペクトルにおいて、図8Aにおいては、AP及びMDAのプロトン付加分子の信号強度が低いが、図8Bにおいては、4種全てのプロトン付加分子が明瞭に検出された。
【0121】
図9A〜9Dは、MS/MS分析後のフラグメントイオンからマスクロマトグラムを取得した結果を示したものである。横軸に分析時間をとり、縦軸に信号強度をとっている。
【0122】
それぞれの薬物について、ブランク測定(60%炭酸カリウム水溶液)、1ppm(尿中)、0.1ppm(尿中)及び0.1ppm(尿中に1ppmで薬物を含む試料を蒸留水で10倍希釈)のマスクロマトグラムを示した。
【0123】
全ての薬物について分析開始直後からクロマトグラムが立ち上がり、それぞれが検出されていることが確認できた。
【0124】
ここで、図8Aの結果(1ppm)においては、4種類の薬物を十分に検出し、各種薬物のMS/MS分析後、スペクトルパターンから物質の判定を行うことが可能であった。
【0125】
ただし、図9A〜9Dの結果から、AP及びMDAの検出ピークが得られる時刻は、MA及びMDMAの検出ピークが得られる時刻と比較して、後になり、かつ、検出感度は、MA及びMDMAと比較して低くなった。
【0126】
また、図1および図2の質量分析装置において、夾雑成分の影響を低減して分析する場合、4種類を同時に分析する場合は、検出される時間に差異が生じる。
【0127】
この現象は尿中の夾雑成分による検出阻害であると考えられる。また、物質ごとの物性(沸点・蒸気圧)によるものであり、互いの気化が拮抗していることも考えられる。
【0128】
図9A〜9Dにおいては、希釈なしの1ppmを分析した場合のマスクロマトグラムと、希釈して0.1ppmを分析した場合のマスクロマトグラムとを比較すると、AP及びMDAについては、後者(0.1ppm)の方が、信号強度が最大となる時刻が早くなったことを示している。
【0129】
この結果から、蒸留水で尿試料を希釈することで、尿中の夾雑成分の影響が緩和され、4種類の薬物を迅速に検知しやすくなったといえる。
【0130】
図9Eは、希釈なしの1ppmを分析した場合、希釈して0.1ppmを分析した場合、及び、希釈して0.01ppmを分析した場合のマスクロマトグラムをAPについて示した結果である。横軸に分析時間をとり、縦軸に信号強度をとっている。
【0131】
APは、蒸留水で100倍希釈した場合(0.01ppm)においても検出された。
【0132】
一般的に、分析においては試料を希釈すると、検出感度が低下することは当然起こりうるが、本方式においては、AP及びMDAの検出感度が改善され、尿中の4種類の違法薬物を同時に迅速に分析可能となった。
【0133】
ここで、蒸留水で10倍希釈した場合、MA及びMDMAの信号強度は1ppmと比較して低下するが、検知するには十分な感度が得られている。
【0134】
したがって、薬物を含む尿を蒸留水で10倍程度まで希釈しても、4種類の違法薬物の検出を迅速かつ簡易に行うことが可能であることが示された。
【0135】
薬物検知の目的においては、4種類の薬物全てを1分以内に検知し、判定が可能であった。
【0136】
本実施例の別方法として、尿試料を先に80%炭酸カリウム水溶液等のアルカリ性水溶液で希釈してもよい。
【0137】
この場合、0.250mLの尿試料と、0.250mLの80%炭酸カリウム水溶液とを混合すると、炭酸カリウム濃度は40%となるが、炭酸カリウムの分析試料溶液中の濃度は30〜60%が望ましい。
【0138】
また、加熱温度は、80℃にて2〜5分間とすることで良好な結果が得られた。
【0139】
さらにいえば、炭酸カリウム水溶液を試料に添加する方法は、覚せい剤や麻薬の粉末・錠剤試料にも適用することも可能である。
【0140】
覚せい剤の粉末(結晶など)適量を試料溶液へ移し取り、さらに炭酸カリウム水溶液を添加し、密栓後、静かに振とうするなどして溶解し、加熱後、分析すればよい。
【実施例4】
【0141】
図10は、大麻試料を分析した結果を示したものである。横軸にm/zをとり、縦軸に信号強度をとっている。
【0142】
大麻樹脂の粉末試料1mgに対し、80%炭酸カリウム水溶液を1mL添加し、150℃に5分間加熱して、分析を行った結果のマススペクトルである。
【0143】
ここで、m/z 311のピークは、カンナビノール(Cannabinol:CBN)を示すものであり、m/z 315のピークは、Δ9−テトラヒドロカンナビノール(Δ9−Tetrahydrocannabinol:Δ9−THC)またはカンナビジオール(Cannabidiol:CBD)のプロトン付加分子のイオンを示すものである。
【0144】
上記の3種類の物質は、大麻特有に含まれる幻覚成分であり、Δ9−THCは、麻薬に指定されている取締り対象物質である。
【0145】
これらを検出することにより、分析した試料が大麻であることを判定することができる。
【0146】
従来、大麻の分析においては、メタノールなどの有機溶媒で試料から薬物の成分を抽出する(非特許文献4)。
【0147】
さらに、液−液抽出などの操作を繰り返すことにより、大麻中の幻覚成分を分離精製する必要がある。
【0148】
本実施例においては、上述した操作なしに、簡易な分析が可能であった。
【0149】
また、大麻試料においては、アルカリ性水溶液ではなく、蒸留水の添加によっても検出が可能であったため、炭酸カリウム水溶液ではなく蒸留水を添加し、加熱後に分析してもよい。蒸留水を用いた場合も大麻試料1mgに対し、蒸留水1mLを添加することで良好な結果が得られた。
【実施例5】
【0150】
図11は、コカイン試料を分析した結果である。横軸にm/zをとり、縦軸に信号強度をとっている。
【0151】
本実施例においては、試料瓶内に炭酸カリウム水溶液を0.1g量り取っておき、コカイン水溶液(50μg/mL)200μLを注加し、密栓後、80℃に5分間加熱して、分析を行った。
【0152】
従来の方法においては、呈色反応が採用されており(非特許文献4)、簡易な分析方法はこれまで実施されていなかった。
【0153】
本図は、コカイン水溶液に炭酸カリウムを少量加えてアルカリ性とし、加熱することにより、簡易にヘッドスペース分析が可能であることを示した結果である。
【0154】
また、コカイン水溶液ではなく、コカインの粉末を炭酸カリウム水溶液中に溶解し、分析することも可能であった。
【0155】
この場合、炭酸カリウム水溶液の最終濃度は30〜80%が望ましい。
【0156】
また、加熱する場合は、80℃で十分な検出が可能であったが、60〜160℃の範囲、もしくは指定の温度に徐々に昇温させるなどの手法を用いてもよい。
【実施例6】
【0157】
図12は、あへん試料を分析した結果である。横軸にm/zをとり、縦軸に信号強度をとっている。
【0158】
本図は、あへん試料10mgを試料容器に量り取り、80%炭酸カリウム水溶液200μLを添加し、密栓後、150℃にて5分間加熱後、ヘッドスペース分析を行った結果である。
【0159】
本図から、あへんに特有のメコニン、コデイン及びテバインを検出し、あへんの検知が可能であることが示された。
【0160】
上記のうち、メコニンは、あへん特有の成分である。
【0161】
また、コデイン及びテバインは、アヘンアルカロイドの一種であり、単一の物質でも取締り対象の規制物質(麻薬)に指定されている。
【0162】
従来、あへんの検知においては、アヘンアルカロイドと呼ばれる麻薬成分を対象に分析が行われてきた。
【0163】
ここで、アヘンアルカロイドとは、モルヒネやコデインなどの違法薬物成分を示す(非特許文献4)。
【0164】
これに対し、本実施例において説明する薬物検知装置の目的は、迅速な薬物の検知であり、あへんを証明する物質が得られればよい。
【0165】
本実施例においては、あへんに特有のメコニン、コデイン及びテバインを検出し、CID分析後のスペクトルパターンから、分析した物質を特定し、あへんの検知が可能であることが示された。
【0166】
したがって、呈色反応のための抽出・精製操作や、GC/MS分析のための誘導体化反応などの煩雑な操作が不要であり、簡易で迅速な分析が可能となった。
【0167】
実施例3〜6に示す通り、尿中の覚せい剤および麻薬、並びに固体試料(粉末、結晶及び錠剤)について簡易で迅速な分析が可能となった。
【0168】
さらにいえば、炭酸カリウム水溶液などのアルカリ性水溶液を用いれば、全ての分析試料について、試料容器内で混合し、加熱する共通の手法により、分析、検知及び判定を行うことが可能となった。
【0169】
実施例3〜6においては、アルカリ性水溶液の溶質として炭酸カリウムを用いたが、これ以外の溶質としては、水酸化カリウム、水酸化ナトリウムなどを用いることができる。アルカリ性水溶液のpHは11以上が望ましい。アルカリ性水溶液の溶質の濃度は、30〜80%が望ましく、30〜60%が更に望ましい。
【0170】
図13は、固体試料を溶解あるいは気化を促進するための構成を有する試料容器を示したものである。
【0171】
本図においては、バイアル瓶2には、固体試料1301を溶解するためのアルカリ性水溶液又は蒸留水を注入するための液注入管1302が設けてある。また、バイアル瓶2の内部には、磁力によって回転するスターラ1303(マグネチックスターラ)を設けてある。
【0172】
固体試料1301を溶解する場合、バイアル瓶2に固体試料1301を封入し、液注入管1302からアルカリ性水溶液又は蒸留水を注入し、スターラ1303を回転させることによりバイアル瓶2の内部の液を撹拌し、固体試料1301を溶解する。液の撹拌は、加熱ヒーター3によって液を加熱しながら行うこともできる。
【0173】
以下、本発明の効果について更に説明する。
【0174】
本発明によれば、物質の質量数と、MS/MS分析によるスペクトルパターンとから、測定した成分そのものを判定可能であるため、判定を確実にすることができる。
【0175】
また、尿試料の場合は、予め試料容器に少量の炭酸カリウムを量りとっておき、尿試料を加えるだけで尿中覚せい剤の分析が可能であり、加熱することで更なる検出感度の向上が望める。
【0176】
また、覚せい剤や麻薬の固体試料(粉末、結晶、錠剤など)の場合も、煩雑な抽出・精製の操作がなく、炭酸カリウム水溶液などのアルカリ性水溶液を添加し、試料容器内で混合する方法で検出が可能である。すなわち、尿中に溶け込んだ違法薬物、及び紛末、錠剤などの固体状の違法薬物を簡易に、かつ、迅速に分析することができる。
【0177】
また、大麻については、呈色反応のための3種類の試薬を必要としない。コカインについても、呈色反応のための3種類の試薬を必要としない。あへんについても、呈色反応のための試薬を必要とせず、アヘンアルカロイド類の抽出・精製の操作がなく、誘導体化などのステップなしに検出が可能となる。
【0178】
さらに、大麻、コカイン及びあへんの3種類の試料について調製方法が同じである。
【符号の説明】
【0179】
1:尿試料、2:バイアル瓶、3:加熱ヒーター、4:ガスボンベ、5:試料ガス導入配管、6:イオン化部、7:放電用ガス導入配管、8:質量分析部、9:針電極、10:引出電極、11:コロナ放電領域、12:イオン−分子反応領域、13:イオン取込細孔、15:液体吸着部、101:ヘッドスペース、102:下流端部、103:上流端部、104:ガス導入配管。
【特許請求の範囲】
【請求項1】
イオン化部と、質量分析部と、試料を入れるための試料容器と、前記試料容器を加熱するための試料加熱部とを含み、前記試料容器には、気相である空間部を設けるとともに、前記試料容器に同伴ガスを導入するための同伴ガス導入配管と前記空間部の試料ガスを前記イオン化部に送るための試料ガス導入配管とが接続してあり、前記イオン化部は、前記試料ガスのイオンを生成し、前記質量分析部は、前記イオンの質量分析を行うことを特徴とする質量分析装置。
【請求項2】
前記同伴ガス導入配管の下流端部は、前記試料を含む液体の中に入るように配置されていることを特徴とする請求項1記載の質量分析装置。
【請求項3】
前記同伴ガス導入配管の下流端部は、前記空間部に配置されていることを特徴とする請求項1記載の質量分析装置。
【請求項4】
前記試料ガス導入配管の上流端部は、前記空間部に配置されていることを特徴とする請求項2又は3に記載の質量分析装置。
【請求項5】
前記試料の温度を経時的に変化させるために前記試料加熱部の発熱量を制御する温度制御部を有することを特徴とする請求項1〜4のいずれか一項に記載の質量分析装置。
【請求項6】
前記温度制御部は、前記試料の温度を段階的に上昇させることを特徴とする請求項5記載の質量分析装置。
【請求項7】
前記試料容器は、液体試料を吸着させるための液体吸着部であることを特徴とする請求項1記載の質量分析装置。
【請求項8】
前記液体試料は、尿を含むことを特徴とする請求項1〜7のいずれか一項に記載の質量分析装置。
【請求項9】
前記試料は固体であり、前記試料を溶解あるいは気化を促進するためのアルカリ性水溶液又は蒸留水を注入するための液注入管を備えたことを特徴とする請求項1〜6のいずれか一項に記載の質量分析装置。
【請求項10】
試料容器に試料を入れ、前記試料容器の内部に同伴ガスを導入し、前記試料に含まれる複数種類の成分を気化し、前記成分と前記同伴ガスとを混合して試料ガスとし、前記試料ガスの質量分析を行うことを特徴とする質量分析方法。
【請求項11】
前記試料ガスのイオンを生成し、質量分析を行うことを特徴とする請求項10記載の質量分析方法。
【請求項12】
前記試料の温度を一定にして前記成分を気化することを特徴とする請求項10又は11に記載の質量分析方法。
【請求項13】
前記試料容器は、液体試料を吸着させるための液体吸着部であることを特徴とする請求項10〜12のいずれか一項に記載の質量分析方法。
【請求項14】
前記試料容器を加熱し、前記試料の温度を経時的に変化させて前記成分を気化することを特徴とする請求項10〜13のいずれか一項に記載の質量分析方法。
【請求項15】
前記試料の温度を段階的に上昇させて前記成分を気化することを特徴とする請求項14記載の質量分析方法。
【請求項16】
前記液体試料は、尿を含み、前記液体試料に含まれる薬物及び前記薬物の代謝物を測定対象とすることを特徴とする請求項13〜15のいずれか一項に記載の質量分析方法。
【請求項17】
前記液体試料にアルカリ性試薬を添加することを特徴とする請求項13〜16のいずれか一項に記載の質量分析方法。
【請求項18】
前記液体試料に蒸留水を添加して希釈することを特徴とする請求項13〜16のいずれか一項に記載の質量分析方法。
【請求項19】
前記液体試料は、固体試料にアルカリ性水溶液又は蒸留水を添加して調製することを特徴とする請求項13〜15のいずれか一項に記載の質量分析方法。
【請求項20】
前記試料を含む液体を60〜160℃に加熱し、前記液体から発生した気体を前記質量分析部に送ることを特徴とする請求項17〜19のいずれか一項に記載の質量分析方法。
【請求項1】
イオン化部と、質量分析部と、試料を入れるための試料容器と、前記試料容器を加熱するための試料加熱部とを含み、前記試料容器には、気相である空間部を設けるとともに、前記試料容器に同伴ガスを導入するための同伴ガス導入配管と前記空間部の試料ガスを前記イオン化部に送るための試料ガス導入配管とが接続してあり、前記イオン化部は、前記試料ガスのイオンを生成し、前記質量分析部は、前記イオンの質量分析を行うことを特徴とする質量分析装置。
【請求項2】
前記同伴ガス導入配管の下流端部は、前記試料を含む液体の中に入るように配置されていることを特徴とする請求項1記載の質量分析装置。
【請求項3】
前記同伴ガス導入配管の下流端部は、前記空間部に配置されていることを特徴とする請求項1記載の質量分析装置。
【請求項4】
前記試料ガス導入配管の上流端部は、前記空間部に配置されていることを特徴とする請求項2又は3に記載の質量分析装置。
【請求項5】
前記試料の温度を経時的に変化させるために前記試料加熱部の発熱量を制御する温度制御部を有することを特徴とする請求項1〜4のいずれか一項に記載の質量分析装置。
【請求項6】
前記温度制御部は、前記試料の温度を段階的に上昇させることを特徴とする請求項5記載の質量分析装置。
【請求項7】
前記試料容器は、液体試料を吸着させるための液体吸着部であることを特徴とする請求項1記載の質量分析装置。
【請求項8】
前記液体試料は、尿を含むことを特徴とする請求項1〜7のいずれか一項に記載の質量分析装置。
【請求項9】
前記試料は固体であり、前記試料を溶解あるいは気化を促進するためのアルカリ性水溶液又は蒸留水を注入するための液注入管を備えたことを特徴とする請求項1〜6のいずれか一項に記載の質量分析装置。
【請求項10】
試料容器に試料を入れ、前記試料容器の内部に同伴ガスを導入し、前記試料に含まれる複数種類の成分を気化し、前記成分と前記同伴ガスとを混合して試料ガスとし、前記試料ガスの質量分析を行うことを特徴とする質量分析方法。
【請求項11】
前記試料ガスのイオンを生成し、質量分析を行うことを特徴とする請求項10記載の質量分析方法。
【請求項12】
前記試料の温度を一定にして前記成分を気化することを特徴とする請求項10又は11に記載の質量分析方法。
【請求項13】
前記試料容器は、液体試料を吸着させるための液体吸着部であることを特徴とする請求項10〜12のいずれか一項に記載の質量分析方法。
【請求項14】
前記試料容器を加熱し、前記試料の温度を経時的に変化させて前記成分を気化することを特徴とする請求項10〜13のいずれか一項に記載の質量分析方法。
【請求項15】
前記試料の温度を段階的に上昇させて前記成分を気化することを特徴とする請求項14記載の質量分析方法。
【請求項16】
前記液体試料は、尿を含み、前記液体試料に含まれる薬物及び前記薬物の代謝物を測定対象とすることを特徴とする請求項13〜15のいずれか一項に記載の質量分析方法。
【請求項17】
前記液体試料にアルカリ性試薬を添加することを特徴とする請求項13〜16のいずれか一項に記載の質量分析方法。
【請求項18】
前記液体試料に蒸留水を添加して希釈することを特徴とする請求項13〜16のいずれか一項に記載の質量分析方法。
【請求項19】
前記液体試料は、固体試料にアルカリ性水溶液又は蒸留水を添加して調製することを特徴とする請求項13〜15のいずれか一項に記載の質量分析方法。
【請求項20】
前記試料を含む液体を60〜160℃に加熱し、前記液体から発生した気体を前記質量分析部に送ることを特徴とする請求項17〜19のいずれか一項に記載の質量分析方法。
【図1】


【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図5D】


【図6】


【図7】


【図8A】


【図8B】


【図9A】


【図9B】


【図9C】


【図9D】


【図9E】


【図10】


【図11】


【図12】


【図13】




【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図5D】


【図6】


【図7】


【図8A】


【図8B】


【図9A】


【図9B】


【図9C】


【図9D】


【図9E】


【図10】


【図11】


【図12】


【図13】


【公開番号】特開2012−69516(P2012−69516A)
【公開日】平成24年4月5日(2012.4.5)
【国際特許分類】
【出願番号】特願2011−182074(P2011−182074)
【出願日】平成23年8月24日(2011.8.24)
【出願人】(501387839)株式会社日立ハイテクノロジーズ (4,325)
【出願人】(592083915)警察庁科学警察研究所長 (23)
【Fターム(参考)】
【公開日】平成24年4月5日(2012.4.5)
【国際特許分類】
【出願日】平成23年8月24日(2011.8.24)
【出願人】(501387839)株式会社日立ハイテクノロジーズ (4,325)
【出願人】(592083915)警察庁科学警察研究所長 (23)
【Fターム(参考)】
[ Back to top ]

