薬物送達のための急速に溶解する微小穿孔器および他の適用
【課題】薬物送達のための急速に溶解する微小穿孔器を提供すること。
【解決手段】以下:溶媒の供給源、および該溶媒との接触の際に急速に溶解する複数の微小穿孔器(113)を有するアレイ、を備える、システム。この微小穿孔器は、有利には薬物を含み得るが、このシステムは、治療用化合物、予防用化合物および/または美容用化合物を送達するため、栄養送達のため、および診断適用のために、使用され得る。この溶媒は、有利には、パッチ(110)または他のレザバ内に含まれ得、これらはまた、薬物を含み得る。
【解決手段】以下:溶媒の供給源、および該溶媒との接触の際に急速に溶解する複数の微小穿孔器(113)を有するアレイ、を備える、システム。この微小穿孔器は、有利には薬物を含み得るが、このシステムは、治療用化合物、予防用化合物および/または美容用化合物を送達するため、栄養送達のため、および診断適用のために、使用され得る。この溶媒は、有利には、パッチ(110)または他のレザバ内に含まれ得、これらはまた、薬物を含み得る。
【発明の詳細な説明】
【技術分野】
【0001】
(発明の分野)
本発明は、薬物の経皮送達に関する。
【背景技術】
【0002】
(発明の背景)
有効な任意の薬物は、体内に、治療有効な速度および量で、1つ以上の生物学的バリアを横切って輸送されなければならない。多くの例において、薬物は、十分効果的に経口投与され得るが、多くの他の例において、その経口経路は、胃腸管内の重大な分解、腸膜内の乏しい吸収、および/または肝臓による最初の通過の分解のために、効果的ではない。これらの障害は、タンパク質成分、ペプチド成分およびDNA成分を含む多くのさらに新しい薬物に対して、特に問題である。例えば、組換えヒトインスリン、成長ホルモン、エリトロポイエチン、インターフェロンおよび他のタンパク質は全て、現在において、経口以外の幾つかの様式で投与されなければならない。
【0003】
代替の方法として、経皮的に、すなわち皮膚を通過または横切って、薬物を経皮的に送達させることが挙げられる。代表的には、これは、標準的なシリンジまたはカテーテルを用いる非経口注射(perental injection)を使用して達成される。不運にも、針注射は、多くの患者において、針の恐怖感、実質的な痛み、および皮膚に対する局所的損傷を引き起こし得る。針注射はまた、薬物の連続送達または連続診断の場合に問題である。
【0004】
これらの問題の1つの解決策は、経皮的に薬物を投与することであり、これは、通常薬物の皮膚を横切る拡散を含む。一旦、薬物が真皮の深さ(表皮層の下)に到達すると、薬物は、血液循環を介して、深い組織層およびその系の他の部分まで急速に拡散する。しかし、皮膚、角質層の最外層は、経皮薬物貫入に対して主なバリアを示し、その結果、多くの薬物の乏しい皮膚浸透性は、経皮送達の広い適用可能性を妨げる。
【0005】
化学エンハンサ、イオントフォレーゼ、エレクトロポレーション、超音波、および加熱素子の全てが、経皮送達を改善するために使用されてきた。しかしながら、これらの技術は、幾つかの型の薬物に対して適切ではなく、しばしば、治療レベルの送達を提供しない。さらに、これらの技術は、時折、所望されない皮膚応答を生じ、および/または1時間もしくは1日にわたる連続的な制御された薬物送達にとって非実用的である。
【0006】
幾つかの試みが、粒子または液体の注射を使用する経皮送達を改善するために行われてきた。これらの技術の主な利点は、針の排除、および汚染の発生の低減である。しかしながら、液体注射は、しばしば、痛みおよび/または真皮下出血を生じる。1つの技術、弾体粒子注射は、正確にかつ連続的に投与することが困難であり、微小出血を引き起こし得る。
【0007】
他の発明者らは、経費的な薬物送達を実施するためにミクロ針(直径約1mm)を使用してきた。ミクロ針は、針内に管腔を通して薬物を送達するために、薬物を針シャフトの外側に沿って送達するために、または後のパッチ薬物適用のための皮膚穿孔体として、使用されてきた。例えば、シリコンミクロ針が、半導体産業の作製手順を使用して開発されてきた。その例は、Allenらの特許文献1(2001年1月)、Yuzhakovらの許文献2(2001年7月)、Shermanらの特許文献3(2001年11月)、およびGartsteinらの特許文献4(2002年4月)に記載される。不運にも、シリコン針は、皮膚において可溶ではなく、使用中に破損した際にはかなりの炎症、そして感染をも引き起こし得る。
【0008】
可溶性の移植片は、徐々に溶解する処方物においてのみ、公知である。その例は、Buch−Rasmussenらの特許文献5(2002年11月)、Yamahisaらの特許文献6(1991年6月)、およびSociete de Conseils de Recherche et d’Applications Scientifiques,S.A.のWIPO 特許文献7(1996年3月公開)である。結果として、可溶性の移植片の使用のほとんどが、拡張された時間にわたって低い用量を投与することが所望されるホルモンおよび他の物質に制限されている。
【0009】
結果として、ミクロ針のアレイまたは他のミクロ移植片を製造する動機がない。生成物が徐々に溶解される間、投与は、低用量を送達するための単一ミクロ針、またはより多くの用量の送達するための単一のより大きな針もしくはペレットを使用して、うまく制御される(例えば、Sandhageら(1978年3月)の米国特許第4077406号を参照のこと)。
【先行技術文献】
【特許文献】
【0010】
【特許文献1】米国特許第6334856号明細書
【特許文献2】米国特許第6256533号明細書
【特許文献3】米国特許第6312612号明細書
【特許文献4】米国特許第6379324号明細書
【特許文献5】米国特許第6485453号明細書
【特許文献6】米国特許第5021241号明細書
【特許文献7】国際公開第9608289号パンフレット
【発明の開示】
【発明が解決しようとする課題】
【0011】
急速に溶解するミクロ移植片は、最小の痛みおよび不快感のみで中間用量の投与を可能にするために、所望される。しかし、その概念は、これまでに、ミクロ移植片の制御された溶解を妨げる角質層および表皮内の血管分布の非存在のために達成するのが困難であった。従って、特にミクロ針のアレイまたは皮膚の他の微小穿孔器を含む、急速に溶解する経皮薬物送達ビヒクルを開発する必要がある。
【課題を解決するための手段】
【0012】
急速に溶解する微小穿孔器(「RDMP」)を使用して薬物を経皮的に送達する装置および方法が記載される。本明細書において使用される場合、用語「微小穿孔器」は、一般的に、断面の形状に関わらず、針、刃、カッティング器、穿孔器、または1mm未満の平均直径を測定する任意の他のデバイスをいう。
【0013】
微小穿孔器は、好ましくは、必要に応じて1つ以上の選択された薬物を保持する固体マトリックスの可溶性(溶融性および生分解性)の材料を含む。マトリックス材料内の薬物は、間質的にまたは任意の他の適切な様式で分布され得る。微小穿孔器は、同じかまたは異なる薬物のレザバに流体結合され得、この薬物は、ミクロ針自体によって皮膚内に運搬され得るか、またはミクロ針による皮膚の穿孔によって作製されたチャネルによって、運搬され得る。好ましい実施形態において、このレザバは、皮膚に対する微小穿孔器の適用後の微小穿孔器の溶解の速度を増す溶媒を含む。このレザバは、有利にも、パッチ内に含まれ得、このレザバは、皮膚の穿孔された領域を覆う患者の皮膚と結合し、その皮膚に対してレザバを保持する接着剤のリングを備え得る。
【0014】
マトリックス内の膨潤材料の封入は、長時間切開部を開いたままにすることによって薬物輸送チャネルの形成を容易にする。このようなチャネル、特に皮膚の最外層におけるチャネルは、制御された薬物送達、または体液もしくは他の分析物をモニターするためのアクセスを提供するために、皮膚のバリア特性を有利にも減少し得る。
【0015】
微小穿孔器は、本明細書中において、薬物の適用ならびに物理/化学的特性に依存して、単一の薬物または薬物の混合物のいずれかを含むことが企図される。好ましい実施形態において、微小穿孔器は、急速に溶解し、これは、本明細書中において、微小穿孔器の少なくとも50%が1時間の投与内に皮膚内または皮膚上で溶解することを意味すると定義される。
【0016】
本発明は、例えば以下を提供する。
(項目1)
システムであって、以下:
溶媒の供給源、および
該溶媒との接触の際に急速に溶解する複数の微小穿孔器を有するアレイ、
を備える、システム。
(項目2)
項目1に記載のシステムであって、前記薬物がポリマーマトリックス材料内に含まれる、システム。
(項目3)
項目1に記載のシステムであって、前記薬物が実質的に100%の微小穿孔器を含む、システム。
(項目4)
項目1に記載のシステムであって、前記薬物がペプチドまたは核酸を含む、システム。
(項目5)
項目1に記載のシステムであって、前記薬物が多糖を含む、システム。
(項目6)
項目1に記載のシステムであって、前記薬物がワクチンを含む、システム。
(項目7)
項目1に記載のシステムであって、前記微小穿孔器が皮膚から真皮層まで貫入するのに十分に長い、システム。
(項目8)
項目1に記載のシステムであって、前記微小穿孔器が実質的に多角形の断面を有する、システム。
(項目9)
項目1に記載のシステムであって、前記微小穿孔器が実質的に尖った形状の断面を有する、システム。
(項目10)
項目1に記載のシステムであって、前記微小穿孔器が実質的に刃の形状である、システム。
(項目11)
項目1に記載のシステムであって、前記微小穿孔器が20μm以下の最小先端直径を有する、システム。
(項目12)
項目1に記載のシステムであって、少なくとも5個の前記微小穿孔器が1cm2以下の面積を有する領域内に配置される、システム。
(項目13)
項目1に記載のシステムであって、前記溶媒の供給源が、第2の薬物を含む流体レザバを備える、システム。
(項目14)
項目13に記載のシステムであって、前記レザバがパッチを備える、システム。
(項目15)
項目14に記載のシステムであって、前記微小穿孔器内に含まれる薬物が、前記パッチ内に含まれる薬物と同じである、システム。
(項目16)
項目14に記載のシステムであって、前記微小穿孔器内に含まれる薬物と、前記パッチ内に含まれる薬物とが、互いに異なる、システム。
(項目17)
項目14に記載のシステムであって、前記パッチが周辺領域の接着剤を有する、システム。
(項目18)
項目1に記載のシステムであって、前記溶媒の供給源が、アルコール、アミド、アミノ酸、リン脂質、スルホン、ピロリドンおよび界面活性剤からなる群から選択された化学エンハンサーを含む、システム。
(項目19)
項目1に記載のシステムであって、第2の薬物を含む第2のアレイの微小穿孔器をさらに備える、システム。
(項目20)
項目1に記載のシステムであって、前記微小穿孔器を皮膚に駆動する、手動操作型圧力機構をさらに備える、システム。
(項目21)
項目1に記載のシステムであって、前記微小穿孔器を皮膚内に10〜1000μm駆動する圧力機構をさらに備える、システム。
【0017】
本発明の種々の目的、特徴、局面および利点は、本発明の好ましい実施形態の以下の詳細な説明および添付の図面(同じ数字は同じ構成要素を表す)からより明らかとなる。
【図面の簡単な説明】
【0018】
【図1】図1は、患者の皮膚の模式的断面である。
【図2A】図2Aは、適切な微小穿孔器の例の斜視図である。
【図2B】図2Bは、適切な微小穿孔器の例の斜視図である。
【図2C】図2Cは、適切な微小穿孔器の例の斜視図である。
【図2D】図2Dは、適切な微小穿孔器の例の斜視図である。
【図2E】図2Eは、適切な微小穿孔器の例の斜視図である。
【図2F】図2Fは、適切な微小穿孔器の例の斜視図である。
【図2G】図2Gは、適切な微小穿孔器の例の斜視図である。
【図3】図3は、RDMPシステムの一部である、微小穿孔器のアレイおよび接着剤の周囲環状リングの平面図である。
【図4】図4は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図5】図5は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図6】図6は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図7】図7は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図8】図8は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図9】図9は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
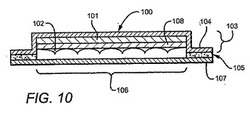
【図10】図10は、薬物レザバシステムを示す。
【図11A】図11Aは、幾つかの企図されたパッチシステムの操作を示す。
【図11B】図11Bは、幾つかの企図されたパッチシステムの操作を示す。
【図11C】図11Cは、幾つかの企図されたパッチシステムの操作を示す。
【図12A】図12Aは、幾つかの企図されたパッチシステムの操作を示す。
【図12B】図12Bは、幾つかの企図されたパッチシステムの操作を示す。
【図12C】図12Cは、幾つかの企図されたパッチシステムの操作を示す。
【図12D】図12Dは、幾つかの企図されたパッチシステムの操作を示す。
【図12E】図12Eは、幾つかの企図されたパッチシステムの操作を示す。
【図12F】図12Fは、幾つかの企図されたパッチシステムの操作を示す。
【発明を実施するための形態】
【0019】
(発明の最良の形態の説明)
図1は、角質層13、表皮層または表皮15および真皮層または真皮17を含む、皮膚11の上層の断面図である。皮膚の最外層、角質層13は、通常10ミクロン(μm)厚と20ミクロン(μm)厚との間の、死んだ細胞層である。この角質13は、脂質の疎水性細胞外マトリクス、主にセラミドによって囲まれた親水性ケラチノサイトを含む。構造的特徴および組成的特徴のために、角質13は、体内への薬物または他の分子の経皮流れならびに体外への体液および他の分析物の経皮流れ、に対する最大のバリアを提供する。角質13は、2〜3週の平均回転時間で、角質細胞の脱離によって連続的に再生される。
【0020】
角質13の下に、50μm厚と100μm厚との間の生きた真皮または真皮層15が存在する。真皮は、血管を含まず、表皮15の直下に位置する真皮17までおよび真皮17からの拡散によって自由に代謝を交換する。表皮は、1mm厚と3mm厚との間にあり、血管、リンパ管および神経を含む。一旦薬物が真皮層に達すると、薬物は、系循環を通して、潅流する。
【0021】
好ましい薬物送達システムは、急速に溶解する微小穿孔器(好ましくは、約1cm2の領域中、5、10、25、50、100または200の微小穿孔器)のアレイを含み、その少なくとも1つは、1つ以上の針または刃の固体マトリックスとして形成され、各々が、第1の末端において、皮膚の穿孔のために、尖っている(poinnted or sharpened)。各微小穿孔器は、角質を貫通するのに十分強靭でインタクトであり、この微小穿孔器(および薬物)が薬物レザバ内の体液および/または溶媒と共に患者の体内に貫入されたとき、生分解性であるか、または可溶性である。この生分解プロセスまたは溶解プロセスは、有利にも、数十秒と数時間との間の所望された時間間隔で起こり得る。
【0022】
本発明者らは、所望の溶解速度が溶媒の外部供給源を提供することによって効果的に達成され得、このような溶媒が支持パッチによって簡便に提供され得ることを発見した。多くの企図された微小穿孔器において、パッチが主な溶媒として水を薬物と共に分散することが証明された。この微小穿孔器は、同じかまたは異なる薬物の固体溶液を含むマトリックスであり得、そしてマトリックスの組成、微小穿孔器の大きさおよび形状に依存して、この微小穿孔器の少なくとも50%は、10秒〜分、および〜1時間以上の任意の所望の時間内の適用内で溶解するように作製され得る。
【0023】
図2A〜2Gは、アレイにおいて使用される微小穿孔器の企図される形状のいくつかの斜視図である。図2Aの微小穿孔器は、余分の貫入力を提供し得るいばら様先端を備える円錐である。図2Cの微小穿孔器は、従来の直線貫入先端を備える従来の円錐形である。図2Bおよび2Eの微小穿孔器は、それぞれ、円形円柱および矩形(またはより一般的に、多角形)円柱のための円柱−プラス−円錐形である。図2Dの微小穿孔器は、多角形円錐形である。図2Fおよび2Gの微小穿孔器は、皮膚に接触し、そして貫入する1つ以上の鋭いまたは切り取り刃(真っ直ぐまたは鋸歯)の配列を提供する。とがった端部または刃の端部を備える他の形状がまたここで使用され得る。
【0024】
微小穿孔器は、任意の適切な形状(図2A〜2Gに示されるように、例として、真っ直ぐまたは先細のシャフト、角錐、くさび、または刃が挙げられる)を有し得る。好ましい実施形態において、微小穿孔器の外径は、基部または第2端部において最も大きく(約1〜1000μm)、そして第1端部近くの微小穿孔器の外径は、好ましくは、5〜500μm、より好ましくは、第1端部において5〜25μmである。微小穿孔器は、有利には、20μm以下の最小先端直径を有し得る。微小穿孔器の長さは、代表的に、1〜2000μmの範囲、より好ましくは、100〜1000μmの範囲である。皮膚は、平坦およびでこぼこな表面ではなく、顕微鏡的に異なる深さを有する。さらに、角質層の厚みおよび皮膚の弾性は、人から人で、そして任意の人の身体の場所から場所で変化する。望ましい貫入深さは、有効な薬物送達および比較的痛みのない無血の貫入のための、単一値よりもむしろある範囲を有する。微小穿孔器の貫入深さは、疼痛および送達効率に影響し得る。経皮適用において、微小穿孔器の「貫入深さ」は、好ましくは、100μm未満であり、その結果、角質層を通って皮膚内に挿入される微小穿孔器が、表皮を通って貫入しない。これは、神経および血管に接触することを避けるための最適なアプローチである。このような適用において、微小穿孔器の実際の長さは、RDMPシステムが皮膚の過剰な弾性および/または粗さに起因して皮膚内に完全に挿入されないことに関連して、基底層を考慮するためにより長くあり得る。
【0025】
医療的必要性に依存して、真皮への微小穿孔器の貫入は、いくつかの適用に必要とされ得る。これらの場合において、微小穿孔器の貫入部分は、いくつかの変数(基底層または支持層の長さ、寸法、機械的特性、ならびに微小穿孔器の挿入のストロークおよび速度)を調節すること、ならびに標的皮膚弾性、皮膚硬さおよび表面粗さを考慮することによって最適化され得る。
【0026】
基底層(図3および10に示される)は、汚染から穿孔された皮膚領域を分離するための保護を提供し、そしてこの基底層は、抗菌剤を含み得、そして閉塞を作り出して、穿孔された皮膚を水和し、流体の流動を高め得る。微小穿孔器が溶解するかまたは膨潤した後に、ポータルチャネルが、微小穿孔器材料の特性に依存して、収縮または拡大する。
【0027】
微小穿孔器の第1の機能は、角質層を貫通すること、薬物送達の迅速な開始および中断を提供すること、ならびに必要に応じて引き続く薬物送達または体液モニタリングのためにチャネルを開き続けることを助けることである。微小穿孔器がかなり迅速に溶解し(これは、状況に依存する)、そして角質層を貫通するように十分強い限り、任意の生体適合性材料が、微小穿孔器として役立ち得る。
【0028】
微小穿孔器を作製する際に、鋳型は、正確な機械加工、微小機械加工(例えば、MEMS)、またはレーザベースもしくは放電機械加工を使用して、調製され得る。一旦、鋳型が調製されると、液体溶液(マトリクス材料および選択された薬剤を含む)は、鋳型で鋳造され、そして乾燥される。液体溶液の粘度ならびに他の物理的および化学的特性に依存して、さらなる力(例えば、遠心分離力または圧縮力)が、鋳型を満たすために必要とされ得る。固体溶液を形成するために、この溶媒は、空気乾燥されるか、真空乾燥されるか、または凍結乾燥される必要がある。一旦、固体溶液が形成されると、微小穿孔器は、鋳型から分離され、そして適切な形状およびサイズに切断される。
【0029】
粉末形態がマトリクス材料のために使用される場合、この粉末は、有利には、鋳型にわたって分離され得る。粉末の化学的および物理的特性に依存して、次いで、粉末の適切な加熱が適用されて、鋳型内に粘稠性の材料を融解または挿入し得る。あるいは、粉末は、結合剤を伴うかまたは伴わないで、圧力および/または熱の適用によって鋳型内に挿入され得る。微小穿孔器がアレイ内に形成された場合、アレイは、冷却され、鋳型から分離され、そしてRDMPシステム内に組み込まれる。
【0030】
アレイの作製のための別の適切なアプローチは、光架橋である。光架橋剤を含むポリマー溶液を、鋳型で鋳造し、そして照射によって凝固させる。一旦溶液が凝固すると、固体溶液がはぎ取られ、切断され、そして適切なサイズに成形される。微小穿孔器のアレイを作製するための別の実施可能なアプローチは、プランジャーに巻かれ、配列され、そして組み合わされた複数の微小繊維の製造である。
【0031】
かなり多くのポリマーが、微小穿孔器のための適切なマトリクス材料(ポリビニルピロリドン(PVP)、ポリエチレングルコール(PEG)、ポリビニルアルコール(PVA)、セルロース、ヒドロキシプロピルセルロース(HPC)、ヒドロキシエチルセルロース(HEC)、ヒドロキシプロピルメチルセルロース(HPMC)、デキストリン、モノサッカリドおよびポリサッカリド、カルボキシメチルセルロースナトリウム、ポリアルコール、ゼラチン、アラビアゴム、アルギネート、キトサンシクロデキストリンおよび他のバイオポリマーが挙げられるがこれらに限定されない)である。
【0032】
炭水化物誘導体(例えば、糖誘導体(トレハロース、グルコース、マルトース、ラクトース、ラクツロース、フルクトース、ツラノース、メリトース、メレチトース、デキストラン、ソルビトール、キシリトール、パラチニット(palatinit)およびマンニトール))が使用され得る。水可溶性ガラス(例えば、ホスフェート、ニトレートおよびカルボキシレートガラス、ならびに塩化マグネシウム、塩化カリウムおよび塩化カルシウム)はまた、マトリクス材料に、単独でまたはマトリクスポリマーと混合されて使用され得る。
【0033】
適切なマトリクス材料の他の例としては、非イオン性親水性またはイオン性界面活性剤または親油性添加剤(アルキルグルコシド、アルキルマルトシド、アルキルチオグルコシド、ラウリルマクロゴールグリセリド、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンアルキルフェノール、ポリエチレングリコール脂肪酸エステル、ポリエチレングリコールグリセロール脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、ポリオキシエチレン−ポリオキシプロピレンブロックコポリマー、ポリグリセロール脂肪酸エステル、ポリオキシエチレングリセリド、ポリオキシエチレンステロール、これらの誘導体、およびアナログ、ポリオキシエチレン植物油、ポリオキシエチレン水素化植物油、ポリオールならびに脂肪酸、グリセリド、植物油、水素化植物油およびステロールからなる群の少なくとも1つのメンバーの反応混合物、トコフェロールポリエチレングリールスクシネート、糖エステル、糖エーテル;スクログリセリド(sucroglyceride)、およびそれらの混合物から選択される)が挙げられる。
【0034】
適切なイオン性界面活性剤としては、アルキルアンモニウム塩;胆汁酸ならびにその塩、アナログおよび誘導体;アミノ酸、カルニチン、オリゴペプチドおよびポリペプチドの脂肪酸誘導体;アミノ酸、オリゴペプチドおよびポリペプチドのグリセリド誘導体;アシルラクチレート;モノ−ジグリセリドのモノ−ジアセチル化酒石酸エステル;スクシニル化モノグリセリド;モノ−ジグリセリドのクエン酸エステル;アルギン酸塩;プロピレングリコールアルギネート;レシチンおよび水素化レシチン;リゾレシチンおよび水素化リゾレシチン;リゾリン脂質およびその誘導体;リン脂質およびその誘導体;アルキル硫酸塩;脂肪酸塩;ドキュセート(docusate)ナトリウム;ならびのこれらの混合物が挙げられる。
【0035】
適切な親油性添加剤としては、アルコール、ポリオキシエチレンアルキルエーテル、脂肪酸、胆汁酸、グリセロール脂肪酸エステル、アセチル化グリセロール脂肪酸エステル、低級アルコール脂肪酸エステル、ポリエチレングリコール脂肪酸エステル;ポリエチレングリコールグリセロール脂肪酸エステル、ポリプロピレングリコール脂肪酸エステル、ポリオキシエチレングリセリド、モノ/ジグリセリドの乳酸誘導体、プロピレングリコールジグリセリド、ソルビタン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、ポリオキシエチレン−ポリオキシプロピレンブロックコポリマー、エステル交換された植物油、ステロール、ステロール誘導体、糖エステル、糖エーテル、スクログリセリド、ポリオキシエチレン植物油、ポリオキシエチレン水素化植物油、ポリオールと脂肪酸、グリセリド、植物油、水素化植物油およびステロールからなる群の少なくとも1つのメンバーとの反応混合物、ならびにこれらの混合物が挙げられる。
【0036】
本明細書中で使用されるように、微小穿孔器の「アレイ」とは、それらが規則的に間隔を空けて配置されるか否かに関わらず、少なくとも9個の微小穿孔器の任意の配置を意味する。代表的に、アレイは、より多くの微小穿孔器、好ましくは、100以上を含む。製造の簡便さのために、アレイの微小穿孔器は、一般的に(必ず出はないが)、全て、ほぼ同じサイズおよび形状であり、全て、実質的に同じ組成を有する。
【0037】
図3は、患者の皮膚の他の領域から穿孔領域を分離するために、接着剤および抗菌剤(任意)を含む環状領域33を含む基底層によって必要に応じて取り囲まれた微小穿孔器のアレイ31の上に形成されたパッチシステムの平面図である。接着剤の環状領域33は、皮膚にアレイを保持し、そして外来物体の侵入および/または外部感染を妨げるまたは可能性を減少させることが意図される。必要に応じて、薬物レザバ(図3において図示しない)は、微小穿孔器アレイ31の上に配置され得、そして/または接着剤の環状領域33によって囲われ得る。
【0038】
図4は、穿孔活性化−不活性化機構40を示す立面断面図であり、この穿孔活性化−不活性化機構40によって、1つ以上の微小穿孔器41が、患者の皮膚42を貫入するかまたは皮膚42にから引き抜かれて、微小穿孔器に含まれる薬物の送達を開始および/または中断する。薬物送達の開始または中断は、微小穿孔器の挿入または除去によって、約5分の短さで行われ得る。微小穿孔器貫入の深さは、ノブまたはネジのような穿孔調節機構41(43Aおよび43B(任意))によって調節される。微小穿孔器41は、穿孔機構トリガー45によって制御されるバネまたは類似の機構44によって患者の皮膚42内に駆動される。
【0039】
図5は、穿孔活性化−不活性化機構50を示す断面立面図であり、ここで、1つ以上の微小穿孔器51が、ネジノブまたはモーターまたは類似のデバイス55によって制御されるネジ54によって患者の皮膚52内に駆動されるかまたは患者の皮膚52から駆動される。
【0040】
図6は、穿孔活性化−不活性化機構60を示す断面立面図であり、ここで、1つ以上の微小穿孔器61が、減圧デバイス65によって患者の皮膚62へと押しやられ、次いで、バネ64によって注入され、このバネ64によって、微小穿孔器62が、活性化ハウジング66から引き出されるかまたは活性化ハウジング内に引き込む。皮膚穿孔領域における穏やかな減圧の適用は、皮膚の可変性を減少させるのに役立ち得る。
【0041】
図7は、穿孔活性化−不活性化機構70を示す断面立面図であり、ここで、1つ以上の微小穿孔器71が、ガス圧力チャンバ75およびガスレザバ76を備えるガス拡大チャンバ74によって患者の皮膚72内に駆動されるかまたは患者の皮膚72から引き出される。
【0042】
図8は、図4、5、6および/または7に示される微小穿孔器機構が、患者の皮膚81内へまたは患者の皮膚72からの対応する微小穿孔器82の運動(貫入深さを含むがこれらに限定されない)を制御するために使用され得る。この設計は、内部薬物送達のために腹腔鏡または内視鏡とともに使用され得る。
【0043】
図9は、穿孔活性化機構90を示す断面立面図であり、ここで、1つ以上の微小穿孔器91が、微小穿孔器の1つの側面への圧力(指または他の圧力機構93によって手動で適用される)によって患者の皮膚92内に駆動される。
【0044】
必要に応じて、薬物パッチシステム100(図10に示される)は、第1薬物と同じであるかまたは異なり得る第2薬物であり得る第2薬物を含む薬物レザバ101を含み、これは、微小穿孔器アレイ102の上に隣接して配置され、そして独立して制御されるレザバ薬物送達システム103を有する。薬物パッチシステム100は、好ましくは、薬物レザバ101を取り囲むバッキングフィルム104を備え、そして皮膚穿孔領域106を取り囲みシールする環状接着領域105(基底層、図3において最も良く示される)を備える。プラスチックリリースライナー107は、皮膚穿孔の前にはぎ取られ、そしてこのライナーがはぎ取られるまでアレイを保護する。
【0045】
好ましい実施形態において、パッチシステムのレザバは、薬物を含み、そして必要に応じて、液体レザバ中の化学エンハンサー、皮膚抗刺激剤、抗感染化学物質および/または液体形態の他の化学物質を含む。化学エンハンサーは、アルキルアルコール、αビスアボドール(bisabodol)、デシルアルコール、デクスパンテノール、ドデカノール、エチレングリコール、脂肪アルコール、グリセロール、ヘキサデカノール、イソプロパノール、オクタデカノール、テトラヒドロフルフリルアルコール、トリフルオロエタノール、アルキルアセトアミド、クロタミトン、ラウリルジエタノールアミド、トルアミド、ジメチルアセトアミド、ジメチルホルミド、ホルムアミド、ニコチンアミド、アシル−アミノ酸、アラニン、アルギニン、プロリン、セリン、アスパラギン酸、システイン、グルタミン酸、グリシン、バリン、ロイシン、イソロイシン、タンパク質アプロチニン、アゾン、必須油、例えば、カルボン(carvone)、シネオール、オイカリプトール、オイゲノール、メトール(methol)、メトン(methone)、テルペン脂肪酸、例えば、カルボン酸、カプリン酸、ジイソプロピルアジペート、イソプロピルミリステート(IPM)、イソステアリン酸、グリセリルモノラウレート(GML)、グリセロールモノオレエート(GMO)、乳酸、リノール酸、ラウリン酸、ラウリン酸メチル、ミリスチン酸メチル、オレイン酸、ポリエチレングリコールモノラウレート、ソルビタンモノラウレート(SMO)、スクロースココエート(cocoate)、スクロースモノラウレート、スクロースモノオレエート、トリグリセリド、大環状エンハンサー、例えば、シクロデキストリン、シクロペンタデカノンおよびシクロペンタデカノリド、リン脂質、リン脂質/ホスフェートエンハンサー、例えば、ジアルキルホスフェート、レシチン、ジオキサン、ジオキソラン、アルキルスルホン、アルキルスルホン、セチルエーテル、環状ジメチルシロキサン、デカメチルテトラシロキサン、ジアルキルスルホキシド、ジメチルスルホキシド、デシルメチルスルホキシド、ヘキサメチルジシロキサン、メチルオクチルスルホキシド、アルキルアンモニウムブロミド、ベンジルニコチネート、ブチルアゾシクロペンタネン、カプサイシン、カルシウムトリグリコレート、環状アミン、ジエチルセバケート、ジメチルアミノアセテート、エチレングリコールモノエチルエーテル、イミダゾール、メチルオルトホルメート、オキサゾリン、プロリン、尿素、ウレタン、大環状化合物、アミン、アルキルピロリドン、N−メチルピロリドン、エチルピロリドン、ピロリドン、ヒドロキシメチルピロリドン、ヘキシルピロリドン、ラウリルピロリドン、ピロリドン−カルボン酸、ラウリルピロリドンカルボン酸、ピログルタミン酸、ナトリウムデデシルスルフェート、ナトリウムデオキシコレート、ナトリウムラウリルスルフェート、ソルビタンモノパルミテート、ソルビタントリオレエート、ダイズカゼイン、テルペン、ピペラジン誘導体、ナトリウムトラウロコレート(traurocholete)、リポソーム、ビスボロール(bisbilol)、ジチオスレイトールおよびビタミンE(α−トコフェロール)から選択され得る。
【0046】
図11A/11B/11Cは、経皮適用におけるパッチ挿入プロセスの好ましい実施形態を示す断面立面図である。図11Aにおいて、パッチ110の基底層111の接着剤は、皮膚に対してパッチを保持するために皮膚112に適用される。この点において、微小穿孔器113は、皮膚112から外される。図11Bにおいて、プランジャーまたは他の機構114は、活性化されて、微小穿孔器113を皮膚112に接触させるように移動させ、角質層を貫入し、そして表皮または真皮に入る。図11Cにおいて、微小穿孔器113および基底層115は、皮膚112と接触したままで、必要に応じて、パッチシステムの残りが、皮膚から外される。好ましい実施形態において、パッチシステムの上側レザバ内のレザバの薬物分子は、完全にまたは部分的に溶解された微小穿孔器によって作製されたチャネルを通して表皮内に流れる。次いで、薬物分子は、局所処置のためまたは身体を通る輸送のために真皮内に拡散する。
【0047】
アレイの微小穿孔器が、皮膚と接触して(皮膚内または皮膚上で)溶解することが重要である。溶解は、化学的または物理的(例えば、皮膚温度で溶解することによって)、またはその両方で生じ得る。微小穿孔器の適切な溶解は、微小穿孔器の少なくとも50%(重量)が、投与の4時間以内で溶解することを意味するように本明細書中で規定される。より速い速度の溶解が好ましい多くの場合において、微小穿孔器の少なくとも50%(重量)が、投与の2時間以内、1時間以内、30分以内、または10分以内でさえ溶解する。迅速な溶解は、微小穿孔器の少なくとも50%(重量)が、投与の1時間以内に溶解することを意味するように本明細書中で規定される。
【0048】
微小穿孔器は、これらが穿孔器内に含まれる薬物を投与するのに必要な程度まで皮膚に貫通するように十分に固体である限り、「実質的に固体」であると思われる。
【0049】
好ましいパッチシステムは、第2薬物の液体形態またはゲル形態を含むレザバ、およびレザバ表面の少なくとも一部から延びる1つ以上の穿孔器を備える。パッチシステムと関連する微小穿孔器は、皮膚の角質層を貫入して、経皮的薬物投与を向上し、そして迅速な薬物送達および/または迅速な薬物中断を提供する。パッチシステムにおいて、微小穿孔器およびレザバは、単一ユニットまたは別々のユニットとして構築され得る。
【0050】
このパッチレザバは、液体の薬物または半流動体(第2の)薬物の、生物学的障壁への、または生物学的障壁を通る、持続性の制御可能な送達を提供し、その結果、微小穿孔器(moicro−perforator)(マトリックス+薬物)の挿入および溶解後に、拡散チャネルが作製され、かつ開かれたままであるように意図される。微小穿孔器の大きさ、形状、組成および局所的密度が、皮膚チャネルを介する薬物放出速度に影響する。あるいは、イオントフォレシス、ソノフォレシス(sonophoresis)、加熱成分、および機械的振動力のような他の制御機構が、角質層を介する薬物輸送を加速し得、減速し得、または制御し得る。
【0051】
パッチシステムは、好ましくは、皮膚に適用され、その結果、1つ以上の微小穿孔器が、角質層を通って、用途に依存して表皮中に、または真皮中に貫通する。好ましい実施形態において、パッチシステム中のレザバの薬物分子は、完全にまたは部分的に溶解した微小穿孔器により作製されるチャネルを通って、表皮または真皮中に流れる。薬物分子は、局所処置または体を通る輸送のために真皮中に拡散する。
【0052】
パッチおよび他のRDMPシステムは、皮膚および他の組織を介して、薬物およびワクチンならびに他の生物活性分子を含む、広範な治療剤および/または予防剤を輸送し得る。このようなシステムは、組織への最小の損傷、痛みおよび/または刺激で皮膚または他の組織障壁を通る体液への薬物送達および接近方法(access)を可能にする。薬物送達適用において、微小穿孔器は、活性薬物および所望される薬物プロフィールに依存する溶解固体マトリクスまたは膨張固体マトリクスを有利に主に含み得る。これは、即時の薬物源および続く皮膚を介する薬物送達のためのチャネルクリエーターの両方として働く。診断適用において、微小穿孔器は、一般に薬物を含まず、すぐに溶解する、生物学的に不活性な固体、またはチャネルを作製および保持するための溶解可能なマトリクスまたは膨張可能なマトリクスから実質的に完全に構成される。適用に依存して、浸透活性または抗刺激化合物は、有利な効果を有し得る。いくつかの診断的適用について、微小穿孔器が、特定の被検体の存在に反応するセンサー物質を含み得るか、またはこれから成り得ることが、企図される。
【0053】
レザバシステム中の基部層の主な機能は、薬物レザバを分離することであり、そしてレザバとシステムの残りとの間の輸送ブリッジとして働くことである。基部層材料は、適用に依存して、固体マトリクス材料と同じであり得るか、または異なる材料であり得る。レザバのないRDMPシステムにおいて、基部層は、制御された放出のために1つ以上のさらなる層または材料で積層され得る。最も外側の基部層は、不透過なバッキングフィルムとして作用し、他の場合では皮膚貫通領域に侵入し得る任意のウイルスまたは細菌に対して保護し得る。RDMPシステムの他の部分からの逆拡散を避けるために、この層は、より低い薬物溶解度を有するべきである。追加のかつ持続性の薬物送達が必要とされる場合、基部層は、より多くの薬物を含むか、または第2のレザバへの導管を提供するよう構築され得る。基部層において、抗ウイルス保護および/または抗細菌保護を有することは、感染を抑制するのに有用である。薬物送達速度を変動または制御するために、イオントフォレシス、ソノフォレシス、圧電応答または類似の応答を使用する外部物理的増大システムが、基部層および/または上張り(overlay)層の一部として提供され得る。
【0054】
図12Aは、パッチ120Aの単純なデザインを例示し、これは、バッキングを備える基部層121および皮膚123に隣接して配置される1つ以上の微小穿孔器122のアレイを備える。活性成分(薬物または薬物固体溶液)は、微小穿孔器中に含まれる。基部層は、異なる厚みを有し得るが、ほとんどの場合不透過性バッキング層である。このデザインは、有力な薬物送達のために、少ない用量を投与するために、または即座の薬物送達のために、理想的である。
【0055】
図12Bは、パッチ120Bの別のデザインを例示し、これは、微小穿孔器122および基部層124のアレイを備える。活性成分は、微小穿孔器および基部層中に含まれる。この基部層124は、微小穿孔器の最も外側の層由来の異なる組成を有し得るが、ほとんどの場合不透過性のバッキング層である。このデザインはまた、少ない用量を体系的に投与するために、または局所的適用のために有力な薬物送達のために理想的である。
【0056】
図12Cは、パッチ120Cのより複雑な設計を示す。活性成分は、微小穿孔器およびレザバ中に含まれる。基部層126の頂部部分は、薬物送達パッチ125を含む。微小穿孔器122−1の第1のアレイは、皮膚123の角質層を貫通するように向けられ、微小穿孔器122−2の第2のアレイは、レザバパッチ125中の流体を囲み、または含む膜を貫通するよう反対に向けられている。このレザバパッチ125は、アレイの適用後に適用され得るか、またはアレイと組み合され得る。このレザバは、標的化薬物送達プロフィールに依存して種々の組成物または処方物を有し得る。
【0057】
図12Dおよび12Eは、図12Bおよび12Cからそれぞれ改変されたRDMPパッチシステムの他のデザイン120Dおよび120Eを例示する。本明細書で、微小穿孔器は、薬物を全く含まないが、溶解マトリクスを備える。この活性成分は、基部層および/またはレザバのみに含まれる。薬物溶解度および濃度に依存して、基部層からの薬物放出は、制御され得る。図12Dおよび12Eに示されるシステムは、それぞれ診断目的のためにおよび持続性薬物放出適用のために、主に使用される。
【0058】
図12Fは、必要に応じて微小穿孔器固体マトリクス中に薬物を含まない、パッチシステム120Fの一部としての膨張可能な材料の使用を例示する。このデザインは、より長い(またはより短い)時間間隔の間、皮膚チャネル開口を伸ばし、そして薬物送達の持続時間を伸ばすか、または診断用途のために使用される。
【0059】
任意の薬物または他の生物活性剤が、RDMPシステムを使用して送達され得る。送達された薬物は、タンパク質、ペプチド、DNA、遺伝子、多糖類ならびに合成有機化合物および無機化合物であり得る。代表的な薬剤としては、抗感染剤、ホルモン、成長調整剤、心臓発作(cardiac action)または血流を調節するための薬物、および痛み制御のための薬物が挙げられるが、これらに限定されない。薬物は、局所的(local)処置または局部的(regional)治療もしくは全身性(systemic)治療のためであり得る。以下は、処置するのに使用される注入毎の代表的なタンパク質薬物実施例の用量である:
α−インターフェロン 11〜100μgm
多発性硬化症のためのβ−インターフェロン 22〜44μgm
貧血症に対するエリスロポイエチン 10〜30μgm
卵胞刺激ホルモン(FSH) 5〜30μgm
G−CSF 9〜15μgm
GM−CSF 250μgm
ヒト絨毛性性腺刺激ホルモン 30〜300μgm
黄体形成(leutinizing)ホルモン 2〜30μgm
サケカルシトニン 25〜50μgm
グルカゴン 1mgm
GNRHアンタゴニスト 2mgm
インスリン 0.75〜1.5mgm
ヒト成長ホルモン(GHD) 0.25〜1.5mgm
ヒト成長ホルモン(AIDS) 6mgm
テストステロン 5〜10mgm
リドカイン 2〜5%
ジクロフェナクナトリウム 100 200mgm
オキシブチニン 5〜15mgm
ケトプロフェン 75〜200mgm
アレンドロネート(Alemdronate) 10mgm
マレイン酸エナラプリル(enalpril) 10〜40mgm
フェニルプロパノールアミンHCl 75mgm
クロモリンナトリウム 3.2〜10mgm
イソトレチノイン 0.5〜2mgm/kgm
オキシトシン 1〜2単位/分/iv
パロキセチンHCl 20mgm
フルルビプロフェン 100mgm
セルタリン(sertaline) 50mgm
ベンラファキシン(venlafaxine) 75mgm
ロイプロリド 0.125〜0.25mgm
リスペリドン(risperidone) 4〜6mgm
ガランタミン臭化水素酸塩 16〜24mgm
エノキサプリン、抗凝血剤
エタナーセプト(etanercept)、慢性関節リウマチ
フェンタニール、手術後および慢性の痛み
フィルグラスチン、化学療法由来の低白血球
ヘパリン、抗凝血剤
副甲状腺ホルモン(PTH)
ソマトロピン、成長ホルモン
スマトリプタン、片頭痛
モルヒネ
オピエート抗関節炎。
【0060】
薬物は、以下を含む多くのデザイン因子を変動させることにより制御される、種々の治療速度で送達され得る:アレイの寸法、マトリクスの溶解速度、アレイ中の微小穿孔器の数および配置、パッチの大きさ、レザバの大きさおよび組成、ならびにアレイを使用する頻度。例えば、薬物を高速で送達するために設計されるデバイスは、微小穿孔器中のより活性な薬物、および/またはより早い溶解マトリクスを有し得る。持続性薬物放出のために、より少ない微小穿孔器および/または(より)遅い溶解固体マトリクスの使用が、有用である。このパッチは、皮膚または他の組織に適用されて、2〜3秒から数時間、または数日にわたる時間間隔で、連続的にまたは断続的に、または変動する速度で、薬物を送達し得る。RDMP薬物経皮送達のほとんどの適用は、表皮を標的化するが、血流への直接の送達は、パッチの貫通長を伸ばすことにより利用可能である。
【0061】
本明細書中で開示されるRDMPシステムはまた、皮膚以外の組織を経る輸送を制御するために有用である。例えば、パッチは、患者の目に挿入されて結膜、強膜、および/または角膜の問題を制御または修正し得、ゆっくり移動するアクチュエーターでの薬物の目への送達を容易にし得る。同様に、目中に挿入されるRDMPアレイは、流体の目の外への輸送を輸送を容易にし得、これは、緑内障の処置のために利点があり得る。RDMPパッチはまた、頬(口)内に、鼻内もしくは膣領域内、または腹腔鏡の補助により組織内にまたは他の接近可能な粘膜層中に挿入されて、これらの組織へのまたはこれらの組織を経る輸送を容易にし得る。例えば、薬物は、口内の局所的処置のために頬粘膜を経て送達され得る。別の例として、RDMPアレイは、例えば、胃腸管のライニング上で体内に内部的に使用され、経口摂取される薬物の摂取を容易にし得、または血管のライニングで使用されて薬物の血管壁への貫通を容易にし得る。内部組織適用の場合、生体接着RDMP材料の使用は、さらなる利点であり得る。
【0062】
別の重要な適用は、予防接種である。皮膚は、有効なワクチン送達の理想的な部位である。なぜなら、皮膚は、免疫細胞(例えば、ランゲルハンス細胞)のネットワークを含むからである。表皮への抗原性化合物を送達する際のRDMP技術のいくつかの利点が存在し、この表皮は、高密度の免疫細胞を有し、そして結果として免疫細胞系をより効果的に誘発する。RDMPシステムは、多価ワクチンを容易に発達させるための実用的なデザインであり、薬物の輸送および保存のための液体の使用よりもより大きな安定性を提供すると予期される。以下のワクチンが、とりわけ、送達され得る:
B型肝炎
HIVワクチン
インフルエンザ
ジフテリア
破傷風
百日咳
ライム病
狂犬病
肺炎双球菌
黄熱病
コレラ
種痘疹
結核
風疹
麻疹
おたふくかぜ
ロタウイルス
ボツリヌス
ヘルペスウイルス
他のDNAワクチン
B型肝炎
HIVワクチン
インフルエンザ
ジフテリア
破傷風
百日咳
ライム病
狂犬病
肺炎双球菌
黄熱病
コレラ
種痘疹
結核。
【0063】
適用の別の領域は、薬用化粧品である。パッチを含むRDMPシステムは、ボトックス毒素またはヒドロキシ酸をより効率的かつ安全に送達し、しわ形成および皮膚加齢を除去または低減させ得る。このシステムはまた、障害または異常な皮膚特徴(例えば、にきび、魚の目、いぼ、皮膚肥厚、滑液嚢腫、化学腺角化症、および過度の(hard)角質増殖症皮膚)の処置のために有用であり、これは、しばしば、顔、腕、脚または足に見出される。RDMPシステムはまた、食物パッチとして必須アミノ酸、脂肪およびビタミンを送達するのに有用である。食物パッチは、しばしば救急時に使用される。
【0064】
従って、微小穿孔器を迅速に溶解する特定の実施形態および適用が、開示された。しかし、すでに記載されたものに加えて多くのさらなる改変が、本明細書中の本発明の概念がら離れることなく可能であることが、当業者に明らかである。従って、本発明は、添付の特許請求の範囲の精神を除いて制限されるべきではない。さらに、本明細書および特許請求の範囲を解釈する際に、全ての用語は、文脈と一致する最も広範な可能性のある事柄において解釈されるべきである。特に、用語「含む(comprise)」および「含んでいる(comprising)」は、参照された要素、成分、または工程が、存在し得、または利用され得、または明示的に参照されていない他の要素、成分、または工程と組み合され得ることを示す、排他的ではない様式で要素、成分または工程をいうと解釈されるべきである。
【技術分野】
【0001】
(発明の分野)
本発明は、薬物の経皮送達に関する。
【背景技術】
【0002】
(発明の背景)
有効な任意の薬物は、体内に、治療有効な速度および量で、1つ以上の生物学的バリアを横切って輸送されなければならない。多くの例において、薬物は、十分効果的に経口投与され得るが、多くの他の例において、その経口経路は、胃腸管内の重大な分解、腸膜内の乏しい吸収、および/または肝臓による最初の通過の分解のために、効果的ではない。これらの障害は、タンパク質成分、ペプチド成分およびDNA成分を含む多くのさらに新しい薬物に対して、特に問題である。例えば、組換えヒトインスリン、成長ホルモン、エリトロポイエチン、インターフェロンおよび他のタンパク質は全て、現在において、経口以外の幾つかの様式で投与されなければならない。
【0003】
代替の方法として、経皮的に、すなわち皮膚を通過または横切って、薬物を経皮的に送達させることが挙げられる。代表的には、これは、標準的なシリンジまたはカテーテルを用いる非経口注射(perental injection)を使用して達成される。不運にも、針注射は、多くの患者において、針の恐怖感、実質的な痛み、および皮膚に対する局所的損傷を引き起こし得る。針注射はまた、薬物の連続送達または連続診断の場合に問題である。
【0004】
これらの問題の1つの解決策は、経皮的に薬物を投与することであり、これは、通常薬物の皮膚を横切る拡散を含む。一旦、薬物が真皮の深さ(表皮層の下)に到達すると、薬物は、血液循環を介して、深い組織層およびその系の他の部分まで急速に拡散する。しかし、皮膚、角質層の最外層は、経皮薬物貫入に対して主なバリアを示し、その結果、多くの薬物の乏しい皮膚浸透性は、経皮送達の広い適用可能性を妨げる。
【0005】
化学エンハンサ、イオントフォレーゼ、エレクトロポレーション、超音波、および加熱素子の全てが、経皮送達を改善するために使用されてきた。しかしながら、これらの技術は、幾つかの型の薬物に対して適切ではなく、しばしば、治療レベルの送達を提供しない。さらに、これらの技術は、時折、所望されない皮膚応答を生じ、および/または1時間もしくは1日にわたる連続的な制御された薬物送達にとって非実用的である。
【0006】
幾つかの試みが、粒子または液体の注射を使用する経皮送達を改善するために行われてきた。これらの技術の主な利点は、針の排除、および汚染の発生の低減である。しかしながら、液体注射は、しばしば、痛みおよび/または真皮下出血を生じる。1つの技術、弾体粒子注射は、正確にかつ連続的に投与することが困難であり、微小出血を引き起こし得る。
【0007】
他の発明者らは、経費的な薬物送達を実施するためにミクロ針(直径約1mm)を使用してきた。ミクロ針は、針内に管腔を通して薬物を送達するために、薬物を針シャフトの外側に沿って送達するために、または後のパッチ薬物適用のための皮膚穿孔体として、使用されてきた。例えば、シリコンミクロ針が、半導体産業の作製手順を使用して開発されてきた。その例は、Allenらの特許文献1(2001年1月)、Yuzhakovらの許文献2(2001年7月)、Shermanらの特許文献3(2001年11月)、およびGartsteinらの特許文献4(2002年4月)に記載される。不運にも、シリコン針は、皮膚において可溶ではなく、使用中に破損した際にはかなりの炎症、そして感染をも引き起こし得る。
【0008】
可溶性の移植片は、徐々に溶解する処方物においてのみ、公知である。その例は、Buch−Rasmussenらの特許文献5(2002年11月)、Yamahisaらの特許文献6(1991年6月)、およびSociete de Conseils de Recherche et d’Applications Scientifiques,S.A.のWIPO 特許文献7(1996年3月公開)である。結果として、可溶性の移植片の使用のほとんどが、拡張された時間にわたって低い用量を投与することが所望されるホルモンおよび他の物質に制限されている。
【0009】
結果として、ミクロ針のアレイまたは他のミクロ移植片を製造する動機がない。生成物が徐々に溶解される間、投与は、低用量を送達するための単一ミクロ針、またはより多くの用量の送達するための単一のより大きな針もしくはペレットを使用して、うまく制御される(例えば、Sandhageら(1978年3月)の米国特許第4077406号を参照のこと)。
【先行技術文献】
【特許文献】
【0010】
【特許文献1】米国特許第6334856号明細書
【特許文献2】米国特許第6256533号明細書
【特許文献3】米国特許第6312612号明細書
【特許文献4】米国特許第6379324号明細書
【特許文献5】米国特許第6485453号明細書
【特許文献6】米国特許第5021241号明細書
【特許文献7】国際公開第9608289号パンフレット
【発明の開示】
【発明が解決しようとする課題】
【0011】
急速に溶解するミクロ移植片は、最小の痛みおよび不快感のみで中間用量の投与を可能にするために、所望される。しかし、その概念は、これまでに、ミクロ移植片の制御された溶解を妨げる角質層および表皮内の血管分布の非存在のために達成するのが困難であった。従って、特にミクロ針のアレイまたは皮膚の他の微小穿孔器を含む、急速に溶解する経皮薬物送達ビヒクルを開発する必要がある。
【課題を解決するための手段】
【0012】
急速に溶解する微小穿孔器(「RDMP」)を使用して薬物を経皮的に送達する装置および方法が記載される。本明細書において使用される場合、用語「微小穿孔器」は、一般的に、断面の形状に関わらず、針、刃、カッティング器、穿孔器、または1mm未満の平均直径を測定する任意の他のデバイスをいう。
【0013】
微小穿孔器は、好ましくは、必要に応じて1つ以上の選択された薬物を保持する固体マトリックスの可溶性(溶融性および生分解性)の材料を含む。マトリックス材料内の薬物は、間質的にまたは任意の他の適切な様式で分布され得る。微小穿孔器は、同じかまたは異なる薬物のレザバに流体結合され得、この薬物は、ミクロ針自体によって皮膚内に運搬され得るか、またはミクロ針による皮膚の穿孔によって作製されたチャネルによって、運搬され得る。好ましい実施形態において、このレザバは、皮膚に対する微小穿孔器の適用後の微小穿孔器の溶解の速度を増す溶媒を含む。このレザバは、有利にも、パッチ内に含まれ得、このレザバは、皮膚の穿孔された領域を覆う患者の皮膚と結合し、その皮膚に対してレザバを保持する接着剤のリングを備え得る。
【0014】
マトリックス内の膨潤材料の封入は、長時間切開部を開いたままにすることによって薬物輸送チャネルの形成を容易にする。このようなチャネル、特に皮膚の最外層におけるチャネルは、制御された薬物送達、または体液もしくは他の分析物をモニターするためのアクセスを提供するために、皮膚のバリア特性を有利にも減少し得る。
【0015】
微小穿孔器は、本明細書中において、薬物の適用ならびに物理/化学的特性に依存して、単一の薬物または薬物の混合物のいずれかを含むことが企図される。好ましい実施形態において、微小穿孔器は、急速に溶解し、これは、本明細書中において、微小穿孔器の少なくとも50%が1時間の投与内に皮膚内または皮膚上で溶解することを意味すると定義される。
【0016】
本発明は、例えば以下を提供する。
(項目1)
システムであって、以下:
溶媒の供給源、および
該溶媒との接触の際に急速に溶解する複数の微小穿孔器を有するアレイ、
を備える、システム。
(項目2)
項目1に記載のシステムであって、前記薬物がポリマーマトリックス材料内に含まれる、システム。
(項目3)
項目1に記載のシステムであって、前記薬物が実質的に100%の微小穿孔器を含む、システム。
(項目4)
項目1に記載のシステムであって、前記薬物がペプチドまたは核酸を含む、システム。
(項目5)
項目1に記載のシステムであって、前記薬物が多糖を含む、システム。
(項目6)
項目1に記載のシステムであって、前記薬物がワクチンを含む、システム。
(項目7)
項目1に記載のシステムであって、前記微小穿孔器が皮膚から真皮層まで貫入するのに十分に長い、システム。
(項目8)
項目1に記載のシステムであって、前記微小穿孔器が実質的に多角形の断面を有する、システム。
(項目9)
項目1に記載のシステムであって、前記微小穿孔器が実質的に尖った形状の断面を有する、システム。
(項目10)
項目1に記載のシステムであって、前記微小穿孔器が実質的に刃の形状である、システム。
(項目11)
項目1に記載のシステムであって、前記微小穿孔器が20μm以下の最小先端直径を有する、システム。
(項目12)
項目1に記載のシステムであって、少なくとも5個の前記微小穿孔器が1cm2以下の面積を有する領域内に配置される、システム。
(項目13)
項目1に記載のシステムであって、前記溶媒の供給源が、第2の薬物を含む流体レザバを備える、システム。
(項目14)
項目13に記載のシステムであって、前記レザバがパッチを備える、システム。
(項目15)
項目14に記載のシステムであって、前記微小穿孔器内に含まれる薬物が、前記パッチ内に含まれる薬物と同じである、システム。
(項目16)
項目14に記載のシステムであって、前記微小穿孔器内に含まれる薬物と、前記パッチ内に含まれる薬物とが、互いに異なる、システム。
(項目17)
項目14に記載のシステムであって、前記パッチが周辺領域の接着剤を有する、システム。
(項目18)
項目1に記載のシステムであって、前記溶媒の供給源が、アルコール、アミド、アミノ酸、リン脂質、スルホン、ピロリドンおよび界面活性剤からなる群から選択された化学エンハンサーを含む、システム。
(項目19)
項目1に記載のシステムであって、第2の薬物を含む第2のアレイの微小穿孔器をさらに備える、システム。
(項目20)
項目1に記載のシステムであって、前記微小穿孔器を皮膚に駆動する、手動操作型圧力機構をさらに備える、システム。
(項目21)
項目1に記載のシステムであって、前記微小穿孔器を皮膚内に10〜1000μm駆動する圧力機構をさらに備える、システム。
【0017】
本発明の種々の目的、特徴、局面および利点は、本発明の好ましい実施形態の以下の詳細な説明および添付の図面(同じ数字は同じ構成要素を表す)からより明らかとなる。
【図面の簡単な説明】
【0018】
【図1】図1は、患者の皮膚の模式的断面である。
【図2A】図2Aは、適切な微小穿孔器の例の斜視図である。
【図2B】図2Bは、適切な微小穿孔器の例の斜視図である。
【図2C】図2Cは、適切な微小穿孔器の例の斜視図である。
【図2D】図2Dは、適切な微小穿孔器の例の斜視図である。
【図2E】図2Eは、適切な微小穿孔器の例の斜視図である。
【図2F】図2Fは、適切な微小穿孔器の例の斜視図である。
【図2G】図2Gは、適切な微小穿孔器の例の斜視図である。
【図3】図3は、RDMPシステムの一部である、微小穿孔器のアレイおよび接着剤の周囲環状リングの平面図である。
【図4】図4は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図5】図5は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図6】図6は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図7】図7は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図8】図8は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図9】図9は、RDMP皮膚貫入のために使用され得る活性化機構を示す。
【図10】図10は、薬物レザバシステムを示す。
【図11A】図11Aは、幾つかの企図されたパッチシステムの操作を示す。
【図11B】図11Bは、幾つかの企図されたパッチシステムの操作を示す。
【図11C】図11Cは、幾つかの企図されたパッチシステムの操作を示す。
【図12A】図12Aは、幾つかの企図されたパッチシステムの操作を示す。
【図12B】図12Bは、幾つかの企図されたパッチシステムの操作を示す。
【図12C】図12Cは、幾つかの企図されたパッチシステムの操作を示す。
【図12D】図12Dは、幾つかの企図されたパッチシステムの操作を示す。
【図12E】図12Eは、幾つかの企図されたパッチシステムの操作を示す。
【図12F】図12Fは、幾つかの企図されたパッチシステムの操作を示す。
【発明を実施するための形態】
【0019】
(発明の最良の形態の説明)
図1は、角質層13、表皮層または表皮15および真皮層または真皮17を含む、皮膚11の上層の断面図である。皮膚の最外層、角質層13は、通常10ミクロン(μm)厚と20ミクロン(μm)厚との間の、死んだ細胞層である。この角質13は、脂質の疎水性細胞外マトリクス、主にセラミドによって囲まれた親水性ケラチノサイトを含む。構造的特徴および組成的特徴のために、角質13は、体内への薬物または他の分子の経皮流れならびに体外への体液および他の分析物の経皮流れ、に対する最大のバリアを提供する。角質13は、2〜3週の平均回転時間で、角質細胞の脱離によって連続的に再生される。
【0020】
角質13の下に、50μm厚と100μm厚との間の生きた真皮または真皮層15が存在する。真皮は、血管を含まず、表皮15の直下に位置する真皮17までおよび真皮17からの拡散によって自由に代謝を交換する。表皮は、1mm厚と3mm厚との間にあり、血管、リンパ管および神経を含む。一旦薬物が真皮層に達すると、薬物は、系循環を通して、潅流する。
【0021】
好ましい薬物送達システムは、急速に溶解する微小穿孔器(好ましくは、約1cm2の領域中、5、10、25、50、100または200の微小穿孔器)のアレイを含み、その少なくとも1つは、1つ以上の針または刃の固体マトリックスとして形成され、各々が、第1の末端において、皮膚の穿孔のために、尖っている(poinnted or sharpened)。各微小穿孔器は、角質を貫通するのに十分強靭でインタクトであり、この微小穿孔器(および薬物)が薬物レザバ内の体液および/または溶媒と共に患者の体内に貫入されたとき、生分解性であるか、または可溶性である。この生分解プロセスまたは溶解プロセスは、有利にも、数十秒と数時間との間の所望された時間間隔で起こり得る。
【0022】
本発明者らは、所望の溶解速度が溶媒の外部供給源を提供することによって効果的に達成され得、このような溶媒が支持パッチによって簡便に提供され得ることを発見した。多くの企図された微小穿孔器において、パッチが主な溶媒として水を薬物と共に分散することが証明された。この微小穿孔器は、同じかまたは異なる薬物の固体溶液を含むマトリックスであり得、そしてマトリックスの組成、微小穿孔器の大きさおよび形状に依存して、この微小穿孔器の少なくとも50%は、10秒〜分、および〜1時間以上の任意の所望の時間内の適用内で溶解するように作製され得る。
【0023】
図2A〜2Gは、アレイにおいて使用される微小穿孔器の企図される形状のいくつかの斜視図である。図2Aの微小穿孔器は、余分の貫入力を提供し得るいばら様先端を備える円錐である。図2Cの微小穿孔器は、従来の直線貫入先端を備える従来の円錐形である。図2Bおよび2Eの微小穿孔器は、それぞれ、円形円柱および矩形(またはより一般的に、多角形)円柱のための円柱−プラス−円錐形である。図2Dの微小穿孔器は、多角形円錐形である。図2Fおよび2Gの微小穿孔器は、皮膚に接触し、そして貫入する1つ以上の鋭いまたは切り取り刃(真っ直ぐまたは鋸歯)の配列を提供する。とがった端部または刃の端部を備える他の形状がまたここで使用され得る。
【0024】
微小穿孔器は、任意の適切な形状(図2A〜2Gに示されるように、例として、真っ直ぐまたは先細のシャフト、角錐、くさび、または刃が挙げられる)を有し得る。好ましい実施形態において、微小穿孔器の外径は、基部または第2端部において最も大きく(約1〜1000μm)、そして第1端部近くの微小穿孔器の外径は、好ましくは、5〜500μm、より好ましくは、第1端部において5〜25μmである。微小穿孔器は、有利には、20μm以下の最小先端直径を有し得る。微小穿孔器の長さは、代表的に、1〜2000μmの範囲、より好ましくは、100〜1000μmの範囲である。皮膚は、平坦およびでこぼこな表面ではなく、顕微鏡的に異なる深さを有する。さらに、角質層の厚みおよび皮膚の弾性は、人から人で、そして任意の人の身体の場所から場所で変化する。望ましい貫入深さは、有効な薬物送達および比較的痛みのない無血の貫入のための、単一値よりもむしろある範囲を有する。微小穿孔器の貫入深さは、疼痛および送達効率に影響し得る。経皮適用において、微小穿孔器の「貫入深さ」は、好ましくは、100μm未満であり、その結果、角質層を通って皮膚内に挿入される微小穿孔器が、表皮を通って貫入しない。これは、神経および血管に接触することを避けるための最適なアプローチである。このような適用において、微小穿孔器の実際の長さは、RDMPシステムが皮膚の過剰な弾性および/または粗さに起因して皮膚内に完全に挿入されないことに関連して、基底層を考慮するためにより長くあり得る。
【0025】
医療的必要性に依存して、真皮への微小穿孔器の貫入は、いくつかの適用に必要とされ得る。これらの場合において、微小穿孔器の貫入部分は、いくつかの変数(基底層または支持層の長さ、寸法、機械的特性、ならびに微小穿孔器の挿入のストロークおよび速度)を調節すること、ならびに標的皮膚弾性、皮膚硬さおよび表面粗さを考慮することによって最適化され得る。
【0026】
基底層(図3および10に示される)は、汚染から穿孔された皮膚領域を分離するための保護を提供し、そしてこの基底層は、抗菌剤を含み得、そして閉塞を作り出して、穿孔された皮膚を水和し、流体の流動を高め得る。微小穿孔器が溶解するかまたは膨潤した後に、ポータルチャネルが、微小穿孔器材料の特性に依存して、収縮または拡大する。
【0027】
微小穿孔器の第1の機能は、角質層を貫通すること、薬物送達の迅速な開始および中断を提供すること、ならびに必要に応じて引き続く薬物送達または体液モニタリングのためにチャネルを開き続けることを助けることである。微小穿孔器がかなり迅速に溶解し(これは、状況に依存する)、そして角質層を貫通するように十分強い限り、任意の生体適合性材料が、微小穿孔器として役立ち得る。
【0028】
微小穿孔器を作製する際に、鋳型は、正確な機械加工、微小機械加工(例えば、MEMS)、またはレーザベースもしくは放電機械加工を使用して、調製され得る。一旦、鋳型が調製されると、液体溶液(マトリクス材料および選択された薬剤を含む)は、鋳型で鋳造され、そして乾燥される。液体溶液の粘度ならびに他の物理的および化学的特性に依存して、さらなる力(例えば、遠心分離力または圧縮力)が、鋳型を満たすために必要とされ得る。固体溶液を形成するために、この溶媒は、空気乾燥されるか、真空乾燥されるか、または凍結乾燥される必要がある。一旦、固体溶液が形成されると、微小穿孔器は、鋳型から分離され、そして適切な形状およびサイズに切断される。
【0029】
粉末形態がマトリクス材料のために使用される場合、この粉末は、有利には、鋳型にわたって分離され得る。粉末の化学的および物理的特性に依存して、次いで、粉末の適切な加熱が適用されて、鋳型内に粘稠性の材料を融解または挿入し得る。あるいは、粉末は、結合剤を伴うかまたは伴わないで、圧力および/または熱の適用によって鋳型内に挿入され得る。微小穿孔器がアレイ内に形成された場合、アレイは、冷却され、鋳型から分離され、そしてRDMPシステム内に組み込まれる。
【0030】
アレイの作製のための別の適切なアプローチは、光架橋である。光架橋剤を含むポリマー溶液を、鋳型で鋳造し、そして照射によって凝固させる。一旦溶液が凝固すると、固体溶液がはぎ取られ、切断され、そして適切なサイズに成形される。微小穿孔器のアレイを作製するための別の実施可能なアプローチは、プランジャーに巻かれ、配列され、そして組み合わされた複数の微小繊維の製造である。
【0031】
かなり多くのポリマーが、微小穿孔器のための適切なマトリクス材料(ポリビニルピロリドン(PVP)、ポリエチレングルコール(PEG)、ポリビニルアルコール(PVA)、セルロース、ヒドロキシプロピルセルロース(HPC)、ヒドロキシエチルセルロース(HEC)、ヒドロキシプロピルメチルセルロース(HPMC)、デキストリン、モノサッカリドおよびポリサッカリド、カルボキシメチルセルロースナトリウム、ポリアルコール、ゼラチン、アラビアゴム、アルギネート、キトサンシクロデキストリンおよび他のバイオポリマーが挙げられるがこれらに限定されない)である。
【0032】
炭水化物誘導体(例えば、糖誘導体(トレハロース、グルコース、マルトース、ラクトース、ラクツロース、フルクトース、ツラノース、メリトース、メレチトース、デキストラン、ソルビトール、キシリトール、パラチニット(palatinit)およびマンニトール))が使用され得る。水可溶性ガラス(例えば、ホスフェート、ニトレートおよびカルボキシレートガラス、ならびに塩化マグネシウム、塩化カリウムおよび塩化カルシウム)はまた、マトリクス材料に、単独でまたはマトリクスポリマーと混合されて使用され得る。
【0033】
適切なマトリクス材料の他の例としては、非イオン性親水性またはイオン性界面活性剤または親油性添加剤(アルキルグルコシド、アルキルマルトシド、アルキルチオグルコシド、ラウリルマクロゴールグリセリド、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンアルキルフェノール、ポリエチレングリコール脂肪酸エステル、ポリエチレングリコールグリセロール脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、ポリオキシエチレン−ポリオキシプロピレンブロックコポリマー、ポリグリセロール脂肪酸エステル、ポリオキシエチレングリセリド、ポリオキシエチレンステロール、これらの誘導体、およびアナログ、ポリオキシエチレン植物油、ポリオキシエチレン水素化植物油、ポリオールならびに脂肪酸、グリセリド、植物油、水素化植物油およびステロールからなる群の少なくとも1つのメンバーの反応混合物、トコフェロールポリエチレングリールスクシネート、糖エステル、糖エーテル;スクログリセリド(sucroglyceride)、およびそれらの混合物から選択される)が挙げられる。
【0034】
適切なイオン性界面活性剤としては、アルキルアンモニウム塩;胆汁酸ならびにその塩、アナログおよび誘導体;アミノ酸、カルニチン、オリゴペプチドおよびポリペプチドの脂肪酸誘導体;アミノ酸、オリゴペプチドおよびポリペプチドのグリセリド誘導体;アシルラクチレート;モノ−ジグリセリドのモノ−ジアセチル化酒石酸エステル;スクシニル化モノグリセリド;モノ−ジグリセリドのクエン酸エステル;アルギン酸塩;プロピレングリコールアルギネート;レシチンおよび水素化レシチン;リゾレシチンおよび水素化リゾレシチン;リゾリン脂質およびその誘導体;リン脂質およびその誘導体;アルキル硫酸塩;脂肪酸塩;ドキュセート(docusate)ナトリウム;ならびのこれらの混合物が挙げられる。
【0035】
適切な親油性添加剤としては、アルコール、ポリオキシエチレンアルキルエーテル、脂肪酸、胆汁酸、グリセロール脂肪酸エステル、アセチル化グリセロール脂肪酸エステル、低級アルコール脂肪酸エステル、ポリエチレングリコール脂肪酸エステル;ポリエチレングリコールグリセロール脂肪酸エステル、ポリプロピレングリコール脂肪酸エステル、ポリオキシエチレングリセリド、モノ/ジグリセリドの乳酸誘導体、プロピレングリコールジグリセリド、ソルビタン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、ポリオキシエチレン−ポリオキシプロピレンブロックコポリマー、エステル交換された植物油、ステロール、ステロール誘導体、糖エステル、糖エーテル、スクログリセリド、ポリオキシエチレン植物油、ポリオキシエチレン水素化植物油、ポリオールと脂肪酸、グリセリド、植物油、水素化植物油およびステロールからなる群の少なくとも1つのメンバーとの反応混合物、ならびにこれらの混合物が挙げられる。
【0036】
本明細書中で使用されるように、微小穿孔器の「アレイ」とは、それらが規則的に間隔を空けて配置されるか否かに関わらず、少なくとも9個の微小穿孔器の任意の配置を意味する。代表的に、アレイは、より多くの微小穿孔器、好ましくは、100以上を含む。製造の簡便さのために、アレイの微小穿孔器は、一般的に(必ず出はないが)、全て、ほぼ同じサイズおよび形状であり、全て、実質的に同じ組成を有する。
【0037】
図3は、患者の皮膚の他の領域から穿孔領域を分離するために、接着剤および抗菌剤(任意)を含む環状領域33を含む基底層によって必要に応じて取り囲まれた微小穿孔器のアレイ31の上に形成されたパッチシステムの平面図である。接着剤の環状領域33は、皮膚にアレイを保持し、そして外来物体の侵入および/または外部感染を妨げるまたは可能性を減少させることが意図される。必要に応じて、薬物レザバ(図3において図示しない)は、微小穿孔器アレイ31の上に配置され得、そして/または接着剤の環状領域33によって囲われ得る。
【0038】
図4は、穿孔活性化−不活性化機構40を示す立面断面図であり、この穿孔活性化−不活性化機構40によって、1つ以上の微小穿孔器41が、患者の皮膚42を貫入するかまたは皮膚42にから引き抜かれて、微小穿孔器に含まれる薬物の送達を開始および/または中断する。薬物送達の開始または中断は、微小穿孔器の挿入または除去によって、約5分の短さで行われ得る。微小穿孔器貫入の深さは、ノブまたはネジのような穿孔調節機構41(43Aおよび43B(任意))によって調節される。微小穿孔器41は、穿孔機構トリガー45によって制御されるバネまたは類似の機構44によって患者の皮膚42内に駆動される。
【0039】
図5は、穿孔活性化−不活性化機構50を示す断面立面図であり、ここで、1つ以上の微小穿孔器51が、ネジノブまたはモーターまたは類似のデバイス55によって制御されるネジ54によって患者の皮膚52内に駆動されるかまたは患者の皮膚52から駆動される。
【0040】
図6は、穿孔活性化−不活性化機構60を示す断面立面図であり、ここで、1つ以上の微小穿孔器61が、減圧デバイス65によって患者の皮膚62へと押しやられ、次いで、バネ64によって注入され、このバネ64によって、微小穿孔器62が、活性化ハウジング66から引き出されるかまたは活性化ハウジング内に引き込む。皮膚穿孔領域における穏やかな減圧の適用は、皮膚の可変性を減少させるのに役立ち得る。
【0041】
図7は、穿孔活性化−不活性化機構70を示す断面立面図であり、ここで、1つ以上の微小穿孔器71が、ガス圧力チャンバ75およびガスレザバ76を備えるガス拡大チャンバ74によって患者の皮膚72内に駆動されるかまたは患者の皮膚72から引き出される。
【0042】
図8は、図4、5、6および/または7に示される微小穿孔器機構が、患者の皮膚81内へまたは患者の皮膚72からの対応する微小穿孔器82の運動(貫入深さを含むがこれらに限定されない)を制御するために使用され得る。この設計は、内部薬物送達のために腹腔鏡または内視鏡とともに使用され得る。
【0043】
図9は、穿孔活性化機構90を示す断面立面図であり、ここで、1つ以上の微小穿孔器91が、微小穿孔器の1つの側面への圧力(指または他の圧力機構93によって手動で適用される)によって患者の皮膚92内に駆動される。
【0044】
必要に応じて、薬物パッチシステム100(図10に示される)は、第1薬物と同じであるかまたは異なり得る第2薬物であり得る第2薬物を含む薬物レザバ101を含み、これは、微小穿孔器アレイ102の上に隣接して配置され、そして独立して制御されるレザバ薬物送達システム103を有する。薬物パッチシステム100は、好ましくは、薬物レザバ101を取り囲むバッキングフィルム104を備え、そして皮膚穿孔領域106を取り囲みシールする環状接着領域105(基底層、図3において最も良く示される)を備える。プラスチックリリースライナー107は、皮膚穿孔の前にはぎ取られ、そしてこのライナーがはぎ取られるまでアレイを保護する。
【0045】
好ましい実施形態において、パッチシステムのレザバは、薬物を含み、そして必要に応じて、液体レザバ中の化学エンハンサー、皮膚抗刺激剤、抗感染化学物質および/または液体形態の他の化学物質を含む。化学エンハンサーは、アルキルアルコール、αビスアボドール(bisabodol)、デシルアルコール、デクスパンテノール、ドデカノール、エチレングリコール、脂肪アルコール、グリセロール、ヘキサデカノール、イソプロパノール、オクタデカノール、テトラヒドロフルフリルアルコール、トリフルオロエタノール、アルキルアセトアミド、クロタミトン、ラウリルジエタノールアミド、トルアミド、ジメチルアセトアミド、ジメチルホルミド、ホルムアミド、ニコチンアミド、アシル−アミノ酸、アラニン、アルギニン、プロリン、セリン、アスパラギン酸、システイン、グルタミン酸、グリシン、バリン、ロイシン、イソロイシン、タンパク質アプロチニン、アゾン、必須油、例えば、カルボン(carvone)、シネオール、オイカリプトール、オイゲノール、メトール(methol)、メトン(methone)、テルペン脂肪酸、例えば、カルボン酸、カプリン酸、ジイソプロピルアジペート、イソプロピルミリステート(IPM)、イソステアリン酸、グリセリルモノラウレート(GML)、グリセロールモノオレエート(GMO)、乳酸、リノール酸、ラウリン酸、ラウリン酸メチル、ミリスチン酸メチル、オレイン酸、ポリエチレングリコールモノラウレート、ソルビタンモノラウレート(SMO)、スクロースココエート(cocoate)、スクロースモノラウレート、スクロースモノオレエート、トリグリセリド、大環状エンハンサー、例えば、シクロデキストリン、シクロペンタデカノンおよびシクロペンタデカノリド、リン脂質、リン脂質/ホスフェートエンハンサー、例えば、ジアルキルホスフェート、レシチン、ジオキサン、ジオキソラン、アルキルスルホン、アルキルスルホン、セチルエーテル、環状ジメチルシロキサン、デカメチルテトラシロキサン、ジアルキルスルホキシド、ジメチルスルホキシド、デシルメチルスルホキシド、ヘキサメチルジシロキサン、メチルオクチルスルホキシド、アルキルアンモニウムブロミド、ベンジルニコチネート、ブチルアゾシクロペンタネン、カプサイシン、カルシウムトリグリコレート、環状アミン、ジエチルセバケート、ジメチルアミノアセテート、エチレングリコールモノエチルエーテル、イミダゾール、メチルオルトホルメート、オキサゾリン、プロリン、尿素、ウレタン、大環状化合物、アミン、アルキルピロリドン、N−メチルピロリドン、エチルピロリドン、ピロリドン、ヒドロキシメチルピロリドン、ヘキシルピロリドン、ラウリルピロリドン、ピロリドン−カルボン酸、ラウリルピロリドンカルボン酸、ピログルタミン酸、ナトリウムデデシルスルフェート、ナトリウムデオキシコレート、ナトリウムラウリルスルフェート、ソルビタンモノパルミテート、ソルビタントリオレエート、ダイズカゼイン、テルペン、ピペラジン誘導体、ナトリウムトラウロコレート(traurocholete)、リポソーム、ビスボロール(bisbilol)、ジチオスレイトールおよびビタミンE(α−トコフェロール)から選択され得る。
【0046】
図11A/11B/11Cは、経皮適用におけるパッチ挿入プロセスの好ましい実施形態を示す断面立面図である。図11Aにおいて、パッチ110の基底層111の接着剤は、皮膚に対してパッチを保持するために皮膚112に適用される。この点において、微小穿孔器113は、皮膚112から外される。図11Bにおいて、プランジャーまたは他の機構114は、活性化されて、微小穿孔器113を皮膚112に接触させるように移動させ、角質層を貫入し、そして表皮または真皮に入る。図11Cにおいて、微小穿孔器113および基底層115は、皮膚112と接触したままで、必要に応じて、パッチシステムの残りが、皮膚から外される。好ましい実施形態において、パッチシステムの上側レザバ内のレザバの薬物分子は、完全にまたは部分的に溶解された微小穿孔器によって作製されたチャネルを通して表皮内に流れる。次いで、薬物分子は、局所処置のためまたは身体を通る輸送のために真皮内に拡散する。
【0047】
アレイの微小穿孔器が、皮膚と接触して(皮膚内または皮膚上で)溶解することが重要である。溶解は、化学的または物理的(例えば、皮膚温度で溶解することによって)、またはその両方で生じ得る。微小穿孔器の適切な溶解は、微小穿孔器の少なくとも50%(重量)が、投与の4時間以内で溶解することを意味するように本明細書中で規定される。より速い速度の溶解が好ましい多くの場合において、微小穿孔器の少なくとも50%(重量)が、投与の2時間以内、1時間以内、30分以内、または10分以内でさえ溶解する。迅速な溶解は、微小穿孔器の少なくとも50%(重量)が、投与の1時間以内に溶解することを意味するように本明細書中で規定される。
【0048】
微小穿孔器は、これらが穿孔器内に含まれる薬物を投与するのに必要な程度まで皮膚に貫通するように十分に固体である限り、「実質的に固体」であると思われる。
【0049】
好ましいパッチシステムは、第2薬物の液体形態またはゲル形態を含むレザバ、およびレザバ表面の少なくとも一部から延びる1つ以上の穿孔器を備える。パッチシステムと関連する微小穿孔器は、皮膚の角質層を貫入して、経皮的薬物投与を向上し、そして迅速な薬物送達および/または迅速な薬物中断を提供する。パッチシステムにおいて、微小穿孔器およびレザバは、単一ユニットまたは別々のユニットとして構築され得る。
【0050】
このパッチレザバは、液体の薬物または半流動体(第2の)薬物の、生物学的障壁への、または生物学的障壁を通る、持続性の制御可能な送達を提供し、その結果、微小穿孔器(moicro−perforator)(マトリックス+薬物)の挿入および溶解後に、拡散チャネルが作製され、かつ開かれたままであるように意図される。微小穿孔器の大きさ、形状、組成および局所的密度が、皮膚チャネルを介する薬物放出速度に影響する。あるいは、イオントフォレシス、ソノフォレシス(sonophoresis)、加熱成分、および機械的振動力のような他の制御機構が、角質層を介する薬物輸送を加速し得、減速し得、または制御し得る。
【0051】
パッチシステムは、好ましくは、皮膚に適用され、その結果、1つ以上の微小穿孔器が、角質層を通って、用途に依存して表皮中に、または真皮中に貫通する。好ましい実施形態において、パッチシステム中のレザバの薬物分子は、完全にまたは部分的に溶解した微小穿孔器により作製されるチャネルを通って、表皮または真皮中に流れる。薬物分子は、局所処置または体を通る輸送のために真皮中に拡散する。
【0052】
パッチおよび他のRDMPシステムは、皮膚および他の組織を介して、薬物およびワクチンならびに他の生物活性分子を含む、広範な治療剤および/または予防剤を輸送し得る。このようなシステムは、組織への最小の損傷、痛みおよび/または刺激で皮膚または他の組織障壁を通る体液への薬物送達および接近方法(access)を可能にする。薬物送達適用において、微小穿孔器は、活性薬物および所望される薬物プロフィールに依存する溶解固体マトリクスまたは膨張固体マトリクスを有利に主に含み得る。これは、即時の薬物源および続く皮膚を介する薬物送達のためのチャネルクリエーターの両方として働く。診断適用において、微小穿孔器は、一般に薬物を含まず、すぐに溶解する、生物学的に不活性な固体、またはチャネルを作製および保持するための溶解可能なマトリクスまたは膨張可能なマトリクスから実質的に完全に構成される。適用に依存して、浸透活性または抗刺激化合物は、有利な効果を有し得る。いくつかの診断的適用について、微小穿孔器が、特定の被検体の存在に反応するセンサー物質を含み得るか、またはこれから成り得ることが、企図される。
【0053】
レザバシステム中の基部層の主な機能は、薬物レザバを分離することであり、そしてレザバとシステムの残りとの間の輸送ブリッジとして働くことである。基部層材料は、適用に依存して、固体マトリクス材料と同じであり得るか、または異なる材料であり得る。レザバのないRDMPシステムにおいて、基部層は、制御された放出のために1つ以上のさらなる層または材料で積層され得る。最も外側の基部層は、不透過なバッキングフィルムとして作用し、他の場合では皮膚貫通領域に侵入し得る任意のウイルスまたは細菌に対して保護し得る。RDMPシステムの他の部分からの逆拡散を避けるために、この層は、より低い薬物溶解度を有するべきである。追加のかつ持続性の薬物送達が必要とされる場合、基部層は、より多くの薬物を含むか、または第2のレザバへの導管を提供するよう構築され得る。基部層において、抗ウイルス保護および/または抗細菌保護を有することは、感染を抑制するのに有用である。薬物送達速度を変動または制御するために、イオントフォレシス、ソノフォレシス、圧電応答または類似の応答を使用する外部物理的増大システムが、基部層および/または上張り(overlay)層の一部として提供され得る。
【0054】
図12Aは、パッチ120Aの単純なデザインを例示し、これは、バッキングを備える基部層121および皮膚123に隣接して配置される1つ以上の微小穿孔器122のアレイを備える。活性成分(薬物または薬物固体溶液)は、微小穿孔器中に含まれる。基部層は、異なる厚みを有し得るが、ほとんどの場合不透過性バッキング層である。このデザインは、有力な薬物送達のために、少ない用量を投与するために、または即座の薬物送達のために、理想的である。
【0055】
図12Bは、パッチ120Bの別のデザインを例示し、これは、微小穿孔器122および基部層124のアレイを備える。活性成分は、微小穿孔器および基部層中に含まれる。この基部層124は、微小穿孔器の最も外側の層由来の異なる組成を有し得るが、ほとんどの場合不透過性のバッキング層である。このデザインはまた、少ない用量を体系的に投与するために、または局所的適用のために有力な薬物送達のために理想的である。
【0056】
図12Cは、パッチ120Cのより複雑な設計を示す。活性成分は、微小穿孔器およびレザバ中に含まれる。基部層126の頂部部分は、薬物送達パッチ125を含む。微小穿孔器122−1の第1のアレイは、皮膚123の角質層を貫通するように向けられ、微小穿孔器122−2の第2のアレイは、レザバパッチ125中の流体を囲み、または含む膜を貫通するよう反対に向けられている。このレザバパッチ125は、アレイの適用後に適用され得るか、またはアレイと組み合され得る。このレザバは、標的化薬物送達プロフィールに依存して種々の組成物または処方物を有し得る。
【0057】
図12Dおよび12Eは、図12Bおよび12Cからそれぞれ改変されたRDMPパッチシステムの他のデザイン120Dおよび120Eを例示する。本明細書で、微小穿孔器は、薬物を全く含まないが、溶解マトリクスを備える。この活性成分は、基部層および/またはレザバのみに含まれる。薬物溶解度および濃度に依存して、基部層からの薬物放出は、制御され得る。図12Dおよび12Eに示されるシステムは、それぞれ診断目的のためにおよび持続性薬物放出適用のために、主に使用される。
【0058】
図12Fは、必要に応じて微小穿孔器固体マトリクス中に薬物を含まない、パッチシステム120Fの一部としての膨張可能な材料の使用を例示する。このデザインは、より長い(またはより短い)時間間隔の間、皮膚チャネル開口を伸ばし、そして薬物送達の持続時間を伸ばすか、または診断用途のために使用される。
【0059】
任意の薬物または他の生物活性剤が、RDMPシステムを使用して送達され得る。送達された薬物は、タンパク質、ペプチド、DNA、遺伝子、多糖類ならびに合成有機化合物および無機化合物であり得る。代表的な薬剤としては、抗感染剤、ホルモン、成長調整剤、心臓発作(cardiac action)または血流を調節するための薬物、および痛み制御のための薬物が挙げられるが、これらに限定されない。薬物は、局所的(local)処置または局部的(regional)治療もしくは全身性(systemic)治療のためであり得る。以下は、処置するのに使用される注入毎の代表的なタンパク質薬物実施例の用量である:
α−インターフェロン 11〜100μgm
多発性硬化症のためのβ−インターフェロン 22〜44μgm
貧血症に対するエリスロポイエチン 10〜30μgm
卵胞刺激ホルモン(FSH) 5〜30μgm
G−CSF 9〜15μgm
GM−CSF 250μgm
ヒト絨毛性性腺刺激ホルモン 30〜300μgm
黄体形成(leutinizing)ホルモン 2〜30μgm
サケカルシトニン 25〜50μgm
グルカゴン 1mgm
GNRHアンタゴニスト 2mgm
インスリン 0.75〜1.5mgm
ヒト成長ホルモン(GHD) 0.25〜1.5mgm
ヒト成長ホルモン(AIDS) 6mgm
テストステロン 5〜10mgm
リドカイン 2〜5%
ジクロフェナクナトリウム 100 200mgm
オキシブチニン 5〜15mgm
ケトプロフェン 75〜200mgm
アレンドロネート(Alemdronate) 10mgm
マレイン酸エナラプリル(enalpril) 10〜40mgm
フェニルプロパノールアミンHCl 75mgm
クロモリンナトリウム 3.2〜10mgm
イソトレチノイン 0.5〜2mgm/kgm
オキシトシン 1〜2単位/分/iv
パロキセチンHCl 20mgm
フルルビプロフェン 100mgm
セルタリン(sertaline) 50mgm
ベンラファキシン(venlafaxine) 75mgm
ロイプロリド 0.125〜0.25mgm
リスペリドン(risperidone) 4〜6mgm
ガランタミン臭化水素酸塩 16〜24mgm
エノキサプリン、抗凝血剤
エタナーセプト(etanercept)、慢性関節リウマチ
フェンタニール、手術後および慢性の痛み
フィルグラスチン、化学療法由来の低白血球
ヘパリン、抗凝血剤
副甲状腺ホルモン(PTH)
ソマトロピン、成長ホルモン
スマトリプタン、片頭痛
モルヒネ
オピエート抗関節炎。
【0060】
薬物は、以下を含む多くのデザイン因子を変動させることにより制御される、種々の治療速度で送達され得る:アレイの寸法、マトリクスの溶解速度、アレイ中の微小穿孔器の数および配置、パッチの大きさ、レザバの大きさおよび組成、ならびにアレイを使用する頻度。例えば、薬物を高速で送達するために設計されるデバイスは、微小穿孔器中のより活性な薬物、および/またはより早い溶解マトリクスを有し得る。持続性薬物放出のために、より少ない微小穿孔器および/または(より)遅い溶解固体マトリクスの使用が、有用である。このパッチは、皮膚または他の組織に適用されて、2〜3秒から数時間、または数日にわたる時間間隔で、連続的にまたは断続的に、または変動する速度で、薬物を送達し得る。RDMP薬物経皮送達のほとんどの適用は、表皮を標的化するが、血流への直接の送達は、パッチの貫通長を伸ばすことにより利用可能である。
【0061】
本明細書中で開示されるRDMPシステムはまた、皮膚以外の組織を経る輸送を制御するために有用である。例えば、パッチは、患者の目に挿入されて結膜、強膜、および/または角膜の問題を制御または修正し得、ゆっくり移動するアクチュエーターでの薬物の目への送達を容易にし得る。同様に、目中に挿入されるRDMPアレイは、流体の目の外への輸送を輸送を容易にし得、これは、緑内障の処置のために利点があり得る。RDMPパッチはまた、頬(口)内に、鼻内もしくは膣領域内、または腹腔鏡の補助により組織内にまたは他の接近可能な粘膜層中に挿入されて、これらの組織へのまたはこれらの組織を経る輸送を容易にし得る。例えば、薬物は、口内の局所的処置のために頬粘膜を経て送達され得る。別の例として、RDMPアレイは、例えば、胃腸管のライニング上で体内に内部的に使用され、経口摂取される薬物の摂取を容易にし得、または血管のライニングで使用されて薬物の血管壁への貫通を容易にし得る。内部組織適用の場合、生体接着RDMP材料の使用は、さらなる利点であり得る。
【0062】
別の重要な適用は、予防接種である。皮膚は、有効なワクチン送達の理想的な部位である。なぜなら、皮膚は、免疫細胞(例えば、ランゲルハンス細胞)のネットワークを含むからである。表皮への抗原性化合物を送達する際のRDMP技術のいくつかの利点が存在し、この表皮は、高密度の免疫細胞を有し、そして結果として免疫細胞系をより効果的に誘発する。RDMPシステムは、多価ワクチンを容易に発達させるための実用的なデザインであり、薬物の輸送および保存のための液体の使用よりもより大きな安定性を提供すると予期される。以下のワクチンが、とりわけ、送達され得る:
B型肝炎
HIVワクチン
インフルエンザ
ジフテリア
破傷風
百日咳
ライム病
狂犬病
肺炎双球菌
黄熱病
コレラ
種痘疹
結核
風疹
麻疹
おたふくかぜ
ロタウイルス
ボツリヌス
ヘルペスウイルス
他のDNAワクチン
B型肝炎
HIVワクチン
インフルエンザ
ジフテリア
破傷風
百日咳
ライム病
狂犬病
肺炎双球菌
黄熱病
コレラ
種痘疹
結核。
【0063】
適用の別の領域は、薬用化粧品である。パッチを含むRDMPシステムは、ボトックス毒素またはヒドロキシ酸をより効率的かつ安全に送達し、しわ形成および皮膚加齢を除去または低減させ得る。このシステムはまた、障害または異常な皮膚特徴(例えば、にきび、魚の目、いぼ、皮膚肥厚、滑液嚢腫、化学腺角化症、および過度の(hard)角質増殖症皮膚)の処置のために有用であり、これは、しばしば、顔、腕、脚または足に見出される。RDMPシステムはまた、食物パッチとして必須アミノ酸、脂肪およびビタミンを送達するのに有用である。食物パッチは、しばしば救急時に使用される。
【0064】
従って、微小穿孔器を迅速に溶解する特定の実施形態および適用が、開示された。しかし、すでに記載されたものに加えて多くのさらなる改変が、本明細書中の本発明の概念がら離れることなく可能であることが、当業者に明らかである。従って、本発明は、添付の特許請求の範囲の精神を除いて制限されるべきではない。さらに、本明細書および特許請求の範囲を解釈する際に、全ての用語は、文脈と一致する最も広範な可能性のある事柄において解釈されるべきである。特に、用語「含む(comprise)」および「含んでいる(comprising)」は、参照された要素、成分、または工程が、存在し得、または利用され得、または明示的に参照されていない他の要素、成分、または工程と組み合され得ることを示す、排他的ではない様式で要素、成分または工程をいうと解釈されるべきである。
【特許請求の範囲】
【請求項1】
明細書に記載の発明。
【請求項1】
明細書に記載の発明。
【図1】


【図2A】


【図2B】


【図2C】


【図2D】


【図2E】


【図2F】


【図2G】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11A】


【図11B】


【図11C】


【図12A】


【図12B】


【図12C】


【図12D】


【図12E】


【図12F】




【図2A】


【図2B】


【図2C】


【図2D】


【図2E】


【図2F】


【図2G】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11A】


【図11B】


【図11C】


【図12A】


【図12B】


【図12C】


【図12D】


【図12E】


【図12F】


【公開番号】特開2010−46548(P2010−46548A)
【公開日】平成22年3月4日(2010.3.4)
【国際特許分類】
【出願番号】特願2009−275003(P2009−275003)
【出願日】平成21年12月2日(2009.12.2)
【分割の表示】特願2004−516176(P2004−516176)の分割
【原出願日】平成15年6月19日(2003.6.19)
【出願人】(504470901)
【Fターム(参考)】
【公開日】平成22年3月4日(2010.3.4)
【国際特許分類】
【出願日】平成21年12月2日(2009.12.2)
【分割の表示】特願2004−516176(P2004−516176)の分割
【原出願日】平成15年6月19日(2003.6.19)
【出願人】(504470901)

【Fターム(参考)】
[ Back to top ]

