蛍光体
【課題】特性の優れた新たな蛍光体を提供する。
【解決手段】ある態様の蛍光体は、M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2及びEu2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、可視光を発する。M1O2は、SiO2を主成分とし、該SiO2の結晶構造がクリストバライトであってもよい。
【解決手段】ある態様の蛍光体は、M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2及びEu2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、可視光を発する。M1O2は、SiO2を主成分とし、該SiO2の結晶構造がクリストバライトであってもよい。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、蛍光体に関する。
【背景技術】
【0002】
発光素子と、当該発光素子が発生する光により励起され当該発光素子とは異なる波長域の光を発生する蛍光体とを組み合わせることにより、所望の色の光を得るように構成された種々の発光装置が知られている。
【0003】
特に近年、長寿命かつ消費電力が少ない白色発光装置として、紫外線又は短波長可視光を発光する発光ダイオード(LED)やレーザダイオード(LD)等の半導体発光素子と、これらを励起光源とする蛍光体とを組み合わせることで白色光を得るように構成された発光装置が注目されている。
【0004】
また、このような発光装置に適した蛍光体の開発も多く行われている。例えば、特許文献1には、金属ケイ酸塩−シリカ系多形蛍光体が開示されている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2006−274263号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明はこうした状況に鑑みてなされたものであり、その目的とするところは、特性の優れた新たな蛍光体を提供することにある。
【課題を解決するための手段】
【0007】
上記課題を解決するために、本発明のある態様の蛍光体は、M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2及びEu2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、可視光を発する。
【0008】
M1O2は、SiO2を主成分とし、該SiO2の結晶構造がクリストバライトであってもよい。
【0009】
2価の金属イオンM2としてMn2+を含んでもよい。
【0010】
なお、以上の構成要素の任意の組合せ、本発明の表現を方法、装置、システム、などの間で変換したものもまた、本発明の態様として有効である。
【発明の効果】
【0011】
本発明によれば、特性の優れた新たな蛍光体を提供できる。
【図面の簡単な説明】
【0012】
【図1】本実施の形態に係る発光モジュールの概略断面図である。
【図2】第1の実施の形態における第2の蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【図3】各実施例に係る蛍光体の発光特性の傾向を示す図である。
【図4】各実施例に係る蛍光体の励起特性を示す図である。
【図5】実施例1〜7及び比較例7に係る蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【図6】本実施の形態に係る第2の蛍光体を用いた発光モジュール及び第2の蛍光体を用いていない発光モジュールのそれぞれの発光スペクトルを示す図である。
【図7】第2の実施の形態における第3の蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【図8】実施例9,10に係る蛍光体の発光特性の傾向を示す図である。
【図9】実施例9,10に係る蛍光体の励起特性を示す図である。
【図10】実施例9及び実施例10に係る蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【図11】本実施の形態に係る第3の蛍光体を用いた発光モジュール及び第3の蛍光体を用いていない発光モジュールのそれぞれの発光スペクトルを示す図である。
【発明を実施するための形態】
【0013】
以下、図面を参照しながら、本発明を実施するための形態について詳細に説明する。なお、図面の説明において同一の要素には同一の符号を付し、重複する説明を適宜省略する。
【0014】
[第1の実施の形態]
図1は、本実施の形態に係る発光モジュールの概略断面図である。図1に示す発光モジュール10は、基板12上に一対の電極14(陽極)及び電極16(陰極)が形成されている。電極14上には半導体発光素子18がマウント部材20により固定されている。半導体発光素子18と電極14はマウント部材20により導通されており、半導体発光素子18と電極16はワイヤー22により導通されている。半導体発光素子の出射面の上には蛍光体フィルタ24が設置されている。
【0015】
基板12は、導電性を有しないが熱伝導性は高い材料によって形成されることが好ましく、例えば、セラミック基板(窒化アルミニウム基板、アルミナ基板、ムライト基板、ガラスセラミック基板)やガラスエポキシ基板等を用いることができる。
【0016】
電極14及び電極16は、金や銅等の金属材料によって形成された導電層である。
【0017】
半導体発光素子18は、本発明の発光モジュールに用いられる発光素子の一例であり、例えば、紫外線又は短波長可視光を発光するLEDやLD等を用いることができる。具体例として、InGaN系の化合物半導体を挙げることができる。InGaN系の化合物半導体は、Inの含有量によって発光波長域が変化する。Inの含有量が多いと発光波長が長波長となり、少ない場合は短波長となる傾向を示すが、ピーク波長が400nm付近となる程度にInが含有されたInGaN系の化合物半導体が発光における量子効率が最も高いことが確認されている。
【0018】
マウント部材20は、例えば銀ペースト等の導電性接着剤又は金錫共晶はんだ等であり、半導体発光素子18の下面を電極14に固定し、半導体発光素子18の下面側電極と基板12上の電極14を電気的に接続する。
【0019】
ワイヤー22は、金ワイヤー等の導電部材であり、例えば超音波熱圧着等により半導体発光素子18の上面側電極及び電極16に接合され、両者を電気的に接続する。
【0020】
蛍光体フィルタ24は、後述する各蛍光体がバインダー部材に分散されている。蛍光体フィルタ24は、例えば、液状又はゲル状のバインダー部材に蛍光体を混入した蛍光体ペーストを作製した後、その蛍光体ペーストを光学ガラス上面に所定の膜厚に塗布し、その後に蛍光体ペーストのバインダー部材を硬化することにより形成される。バインダー部材としては、例えば、シリコーン樹脂やフッ素樹脂等を用いることができる。また、本実施の形態に係る発光モジュールは、励起光源として紫外線又は短波長可視光を用いることから、耐紫外線性能に優れたバインダー部材が好ましい。
【0021】
また、蛍光体フィルタ24は、蛍光体以外の種々の物性を有する物質が混入されていてもよい。バインダー部材よりも屈折率の高い物質、例えば、金属酸化物、フッ素化合物、硫化物等が蛍光体フィルタ24に混入されることにより、蛍光体フィルタ24の屈折率を高めることができる。これにより、半導体発光素子18から発生する光が蛍光体フィルタ24へ入射する際に生ずる全反射が低減され、蛍光体フィルタ24への励起光の取り込み効率を向上させるという効果が得られる。更に、混入する物質の粒子径をナノサイズにすることで、蛍光体フィルタ24の透明度を低下させることなく屈折率を高めることができる。また、アルミナ、ジルコニア、酸化チタン等の平均粒径0.3〜3μm程度の白色粉末を光散乱剤として蛍光体フィルタ24に混入することができる。これにより、発光面内の輝度,色度むらを防止することができる。
【0022】
次に、第1の形態に係る発光モジュールに用いられる各蛍光体について詳述する。
【0023】
(第1の蛍光体)
本実施の形態に係る第1の蛍光体は、黄色発光蛍光体である。黄色発光蛍光体(以下、「黄色蛍光体」と称する。)の好適な一例として、一般式がM1O2・aM2O・bM3X2:M4c(ただし、M1はSi、Ge、Ti、Zr及びSnからなる群より選ばれる少なくとも1種の元素、M2はMg、Ca、Sr、Ba及びZnからなる群より選ばれる少なくとも1種の元素、M3はMg、Ca、Sr、Ba及びZnからなる群より選ばれる少なくとも1種の元素、Xは少なくとも1種のハロゲン元素、M4は希土類元素及びMnからなる群より選ばれるEu2+を必須とする少なくとも1種の元素を示す。aは0.1≦a≦1.3、bは0.1≦b≦0.25の範囲である。)で表される黄色蛍光体が挙げられる。また、この黄色蛍光体は、紫外線又は短波長可視光により励起され、青色蛍光体が発する可視光と混色することで白色を実現する可視光を発する。より具体的には、黄色蛍光体は、560〜600nmの波長域にピーク波長を有する可視光を発する。
【0024】
(第2の蛍光体)
本実施の形態に係る第2の蛍光体は、青色発光蛍光体である。青色発光蛍光体(以下、「青色蛍光体」)の好適な一例として、M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2及びEu2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、青色の可視光を発する蛍光体が挙げられる。
【0025】
なお、2価の金属イオンのうち5%以内を3価および/または1価の金属イオンに置き換えてもよい。3価の金属イオンの例としては、Sc、Y、ランタニド(ランタノイド)、B、Al、Ga、Inなどが挙げられる。また、1価の金属イオンの例としては、Li、Na、K、Rb、Csなどが挙げられる。
【0026】
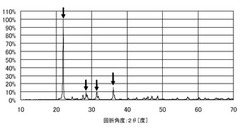
このような青色蛍光体として、M1O2は、SiO2を主成分とし、SiO2の結晶構造がクリストバライトである。図2は、第1の実施の形態における第2の蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【0027】
本実施の形態に係る第2の蛍光体は、図2に示すように、回折角2θが21度〜23度の間に最も高い回折強度が存在する。また、その回折強度を100%としたとき、第2の蛍光体は、回折角35度〜37度に13%〜22%、30度〜32度に7%〜17%、27.5度〜29.5度に6%〜20%の回折強度が生じる結晶構造である。このような結果より、本実施の形態に係る第2の蛍光体は、シリカ(SiO2)を主成分とし、クリストバライト又はそれに類似した結晶構造を有する新規な物質であることがわかる。
【0028】
以下に、第1の実施の形態を各実施例によって更に具体的に説明する。
【0029】
(実施例1)
はじめに、SiO2、CaI2、NH4I、CaF2及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において、5%のH2を含むN2雰囲気中、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体1を得た。
【0030】
(実施例2)
はじめに、SiO2、CaI2、NH4I、MgF2及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において、5%のH2を含むN2雰囲気中、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体2を得た。
【0031】
(実施例3)
はじめに、SiO2、CaCl2、NH4I、SrF2及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体3を得た。
【0032】
(実施例4)
はじめに、SiO2、CaCl2、NH4I、BaF2及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体4を得た。
【0033】
(実施例5)
はじめに、SiO2、CaH2、NH4I、NH4Br、及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体5を得た。
【0034】
(実施例6)
はじめに、SiO2、CaH2、NH4I、NH4Cl及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体6を得た。
【0035】
(実施例7)
はじめに、SiO2、CaI2、NH4I、及びEuCl3を出発原料とし後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体7を得た。
【0036】
(実施例8)
はじめに、SiO2、CaH2、NH4I、CaF2、Al2O3、Li2CO3及びEu2O3を出発原料とし後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体8を得た。蛍光体8は、3価の金属イオンと1価の金属イオンの合計が、2価の金属イオンの合計に対して5%入っている。
【0037】
【表1】

【0038】
なお、表1に示す各元素の値は、Ca=1.0として規格化した仕込みmol比を示す。
【0039】
図3は、各実施例に係る蛍光体の発光特性の傾向を示す図である。図4は、各実施例に係る蛍光体の励起特性を示す図である。実施例に係る蛍光体は、図3に示す発光特性より、470nm前後にピーク波長がある蛍光体である。また、図4に示す励起特性より、400nm前後の近紫外光を良く吸収し、発光する蛍光体である。
【0040】
次に各比較例について説明する。
【0041】
(比較例1)
はじめに、SrCO3、NH4Cl、SrHPO4、及びEu2O3を出発原料とし、これらの元素(モル)比がSrCO3:NH4Cl:SrHPO4:Eu2O3=1.98:1.40:3.00:0.01となるように秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1200℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z1を得た。
【0042】
(比較例2)
はじめに、SiO2、CaI2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z2を得た。
【0043】
(比較例3)
はじめに、SiO2、CaCl2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z3を得た。
【0044】
(比較例4)
はじめに、SiO2、CaCl2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z4を得た。
【0045】
(比較例5)
はじめに、SiO2、CaCl2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z5を得た。
【0046】
(比較例6)
はじめに、SiO2、CaH2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z6を得た。
【0047】
(比較例7)
はじめに、SiO2、Ca(OH)2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z7を得た。
【0048】
(比較例8)
はじめに、SiO2、CaH2、NH4I、CaF2、Al2O3、Li2CO3及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z8を得た。蛍光体Z8は、3価の金属イオンと1価の金属イオンの合計が、2価の金属イオンの合計に対して10%入っている。
【0049】
図5は、実施例1〜7及び比較例7に係る蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【0050】
図5に示すように、実施例1〜7に係る蛍光体は、22度付近にシリカの回折ピークが見られる蛍光体である。しかし、比較例7に係る蛍光体は、22度付近にシリカの回折ピークが見られず、30度付近(図5に示す矢印)にCaSiO3を示す回折ピークが見られる。これは、比較例7に係る蛍光体が、Ca(OH)2を原料としたために、原料混合物中のO(酸素)量が増加し、CaSiO3が生成したためである。
【0051】
次に、蛍光体を製造する際の原料混合物における各元素の好ましい仕込みモル比について説明する。表1のA値は、4価の金属元素(例えば、シリコン元素)に対するハロゲン元素の割合(モル比:X/M1)、B値は、2価の金属イオン(例えば、カルシウム元素やマグネシウム元素)に対する4価の金属元素の割合(モル比:M1/M2)、C値は、2価の金属イオンに占めるEuイオンの割合(モル比:Eu/M2)である。
【0052】
実施例1、比較例2より、B値が0.97から0.49に減少すると、発光強度は111%から49%に低下する。よって、B値は0.97以上が好ましい。また、実施例2より、B値が17.47の場合でも、発光強度は高い。つまり、0.97≦B≦17.47の範囲で発光強度が高い。よって、B値は、0.97≦B≦17.47を満たす範囲が望ましい。
【0053】
実施例2、比較例3は、ハロゲン量が少ない例である。実施例2、比較例3より、A値が0.029から0.017に減少すると、発光強度は110%から73%に低下する。一方、実施例4、比較例4はハロゲン量が多い例である。実施例4、比較例4より、A値が2.218から2.567に増加すると発光強度は、114%から70%に低下する。つまり、0.029≦A≦2.218の範囲で発光強度が高い。よって、A値は、0.029≦A≦2.218の範囲が望ましい。
【0054】
実施例5、比較例5はEuの量が少ない例である。実施例5、比較例5より、C値が0.005から0.002に減少すると、発光強度は113%から55%に低下する。一方実施例6、比較例6はEuの量が多い例である。実施例6、比較例6より、C値が、0.177から0.265に増加すると発光強度は、116%から67%に低下する。つまり、0.005≦C≦0.177の範囲で発光強度が高い。よって、C値は、0.005≦C≦0.177の範囲が望ましい。
【0055】
以上のように、各実施例に係る蛍光体は、その合成時に、ハロゲン元素の出発原料として、M3X(M3は、NH4あるいは1価の金属)、又はM2X2(M2は2価の金属イオン)の組成式で表される化合物を用いて作製される。
【0056】
実施例8と比較例8は、3価の金属イオンと1価の金属イオンを入れた例である。実施例8、比較例8より、D値(後述)が0.05から0.10に増加すると、発光強度が112%から63%に低下する。原料に3価と1価の金属イオンを含んでいない実施例3,4に係る蛍光体においては、D値=0であり、発光強度は114%と高い。つまり、0≦D≦0.05の範囲で発光強度が高い。よって、D値は、0≦D≦0.05の範囲が好ましい。
【0057】
なお、D値は、1価の金属イオン(M3)と3価の金属イオン(M4)の合計のモル数を2価の金属イオン(M2)の合計のモル数で割った値であり、
D値=(M3+M4)/M2
で表される。
【0058】
また、各実施例に係る蛍光体は、原料として、化合物M1O2(M1は、Si、Ge、Ti、Zr及びSnからなる群より選ばれるSiを必須とする少なくとも1種の元素)と、M2X2又はM2H2(M2は、Mg、Ca、Sr、Ba、Mn及びEu2+からなる群より選ばれるCa、Eu2+を必須とする2価の金属イオン)と、M3X(M3は、NH4、Li、Na、K、Rb及びCsからなる群より選ばれるNH4イオンを必須とする少なくとも1価のイオン、Xは、I、F、Cl及びBrからなる群より選ばれるIを必須とする少なくとも一種のハロゲン元素)と、を使用している。
【0059】
次に、実施例に係る蛍光体を組み合わせた発光モジュールの特性について説明する。図6は、本実施の形態に係る第2の蛍光体を用いた発光モジュール及び第2の蛍光体を用いていない発光モジュールのそれぞれの発光スペクトルを示す図である。
【0060】
本実施の形態に係る第2の蛍光体を用いた発光モジュール1は、比較例1に記載の蛍光体Z1(Srアパタイト)と、各実施例に代表される第2の蛍光体と、黄色蛍光体(第1の蛍光体)とを1:1:4の比(重量比)で混合した蛍光体層を有している。一方、第2の蛍光体を用いていない発光モジュール2は、比較例1に記載の蛍光体Z1(Srアパタイト)と、黄色蛍光体(第1の蛍光体)とを1:2の比(重量比)で混合した蛍光体層を有している。なお、発光モジュール1及び発光モジュール2は、発光のピーク波長が400nm前後の励起光源としてUV−LEDを備えている。
【0061】
表2は、各発光モジュールの発光強度、色温度、色度(Cx,Cy)、演色性(平均演色評価数Ra)の結果を示している。なお、発光強度は、発光モジュール2の場合を100%として規格化した値である。この結果から、本実施の形態に係る第2の蛍光体を有していない発光モジュール2の演色性がRa=75であるのに対し、第2の蛍光体を有している発光モジュール1の演色性がRa=80である。つまり、各実施例に代表される本実施の形態に係る第2の蛍光体は、演色性を高める効果がある。換言すれば、本実施の形態に係る第2の蛍光体は、特性の優れた蛍光体ということができる。
【0062】
【表2】

【0063】
[第2の実施の形態]
本実施の形態に係る第3の蛍光体は、前述の第2の蛍光体と類似した構造を有しているが、Mnを含むことで赤色に発光する蛍光体である。なお、第1の実施の形態と同様の構成については、説明を適宜省略する。
【0064】
第2の実施の形態に係る発光モジュールは、蛍光体の種類が一部異なる以外は、第1の実施の形態に係る発光モジュールと同様の構成である。
【0065】
(第1の蛍光体)
第1の実施の形態に係る黄色蛍光体と同じである。
【0066】
(第3の蛍光体)
本実施の形態に係る第3の蛍光体は、赤色発光蛍光体である。赤色発光蛍光体(以下、「赤色蛍光体」)の好適な一例として、M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2、Eu2+及びMn2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、赤色の可視光を発する蛍光体が挙げられる。
【0067】
このような赤色蛍光体として、M1O2は、SiO2を主成分とし、SiO2の結晶構造がクリストバライトである。図7は、第2の実施の形態における第3の蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【0068】
本実施の形態に係る第3の蛍光体は、図7に示すように、回折角が2θが21度〜23度の間に最も高い回折強度が存在する。また、その回折強度を100%としたとき、第3の蛍光体は、35度〜37度に10%〜30%、30度〜32度に5%〜20%、27.5度〜29.5度に6%〜30%の回折強度が生じる結晶構造である。このような、結果より、本実施の形態に係る第3の蛍光体は、シリカ(SiO2)を主成分とし、クリストバライト又はそれに類似した結晶構造を有する新規な物質であることがわかる。
【0069】
以下、第2の実施の形態を各実施例によって更に具体的に説明する。
【0070】
(実施例9)
はじめに、SiO2、CaH2、MnCl2、NH4I、CaF2及びEu2O3を出発原料とし、後述する表3に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において、5%のH2を含むN2雰囲気中、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体9を得た。
【0071】
(実施例10)
はじめに、SiO2、CaH2、MnCO3、NH4I、NH4F及びEu2O3を出発原料とし、後述する表3に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において、5%のH2を含むN2雰囲気中、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体10を得た。
【0072】
【表3】

【0073】
なお、表3に示す各元素の値は、Ca=1.0として規格化した仕込みmol比を示す。
【0074】
図8は、実施例9,10に係る蛍光体の発光特性の傾向を示す図である。図9は、実施例9,10に係る蛍光体の励起特性を示す図である。実施例9,10に係る蛍光体は、図8に示す発光特性より、635nm前後にピーク波長がある蛍光体である。また、図9に示す励起特性より、400nm前後の近紫外光を良く吸収し、発光する蛍光体である。
【0075】
次に比較例について説明する。
【0076】
(比較例9)
はじめに、SrCO3、NH4Cl、SrHPO4、及びEu2O3を出発原料とし、これらの元素(モル)比がSrCO3:NH4Cl:SrHPO4:Eu2O3=1.98:1.40:3.00:0.01となるように秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1200℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z9を得た。
【0077】
図10は、実施例9及び実施例10に係る蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【0078】
図10に示すように、実施例9,10に係る蛍光体は、22度付近にシリカの回折ピークが見られる蛍光体である。
【0079】
以上のように、実施例9,10に係る蛍光体は、その合成時に、ハロゲン元素の出発原料として、M3X(M3は、NH4あるいは1価の金属)、又はM2X2(M2は2価の金属イオン)の組成式で表される化合物を用いて作製される。
【0080】
また、実施例9,10に係る蛍光体は、原料として、化合物M1O2(M1は、Si、Ge、Ti、Zr及びSnからなる群より選ばれるSiを必須とする少なくとも1種の元素)と、M2X2又はM2H2(M2は、Mg、Ca、Sr、Ba、Mn及びEu2+からなる群より選ばれるCa、Eu2+、Mnを必須とする2価の金属イオン)と、M3X(M3は、NH4、Li、Na、K、Rb及びCsからなる群より選ばれるNH4イオンを必須とする少なくとも1価のイオン、Xは、I、F、Cl及びBrからなる群より選ばれるIを必須とする少なくとも一種のハロゲン元素)と、を使用している。なお、M2の原料において、例えばCaO、CaCO3などの酸素を含む原料の割合を60%以下とするとよい。
【0081】
次に、実施例に係る蛍光体を組み合わせた発光モジュールの特性について説明する。図11は、本実施の形態に係る第3の蛍光体を用いた発光モジュール及び第3の蛍光体を用いていない発光モジュールのそれぞれの発光スペクトルを示す図である。
【0082】
本実施の形態に係る第3の蛍光体を用いた発光モジュール3は、比較例9に記載の蛍光体Z9(Srアパタイト)と、各実施例に代表される第3の蛍光体と、黄色蛍光体(第1の蛍光体)とを1.3:2.7:1.0の比(重量比)で混合した蛍光体層を有している。一方、第3の蛍光体を用いていない発光モジュール4は、比較例9に記載の蛍光体Z9(Srアパタイト)と、黄色蛍光体(第1の蛍光体)とを1.3:2.7の比(重量比)で混合した蛍光体層を有している。なお、発光モジュール3及び発光モジュール4は、発光のピーク波長が400nm前後の励起光源としてUV−LEDを備えている。
【0083】
表4は、各発光モジュールの色度(Cx,Cy)、演色性(平均演色評価数Ra)の結果を示している。この結果から、本実施の形態に係る第3の蛍光体を有していない発光モジュール4の演色性がRa=75であるのに対し、第3の蛍光体を有している発光モジュール3の演色性がRa=85である。つまり、各実施例に代表される本実施の形態に係る第3の蛍光体は、演色性を高める効果がある。換言すれば、本実施の形態に係る第3の蛍光体は、特性の優れた蛍光体ということができる。
【0084】
【表4】

【0085】
以上、本発明を実施の形態や実施例をもとに説明した。この実施の形態は例示であり、それらの各構成要素や各処理プロセスの組合せにいろいろな変形例が可能なこと、またそうした変形例も本発明の範囲にあることは当業者に理解されるところである。
【産業上の利用可能性】
【0086】
本発明の蛍光体は、種々の灯具、例えば照明用灯具、ディスプレイ用バックライト、車両用灯具等に適用される発光モジュールに利用することができる。
【符号の説明】
【0087】
10 発光モジュール、 12 基板、 14,16 電極、 18 半導体発光素子、 20 マウント部材、 22 ワイヤー、 24 蛍光体フィルタ。
【技術分野】
【0001】
本発明は、蛍光体に関する。
【背景技術】
【0002】
発光素子と、当該発光素子が発生する光により励起され当該発光素子とは異なる波長域の光を発生する蛍光体とを組み合わせることにより、所望の色の光を得るように構成された種々の発光装置が知られている。
【0003】
特に近年、長寿命かつ消費電力が少ない白色発光装置として、紫外線又は短波長可視光を発光する発光ダイオード(LED)やレーザダイオード(LD)等の半導体発光素子と、これらを励起光源とする蛍光体とを組み合わせることで白色光を得るように構成された発光装置が注目されている。
【0004】
また、このような発光装置に適した蛍光体の開発も多く行われている。例えば、特許文献1には、金属ケイ酸塩−シリカ系多形蛍光体が開示されている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2006−274263号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明はこうした状況に鑑みてなされたものであり、その目的とするところは、特性の優れた新たな蛍光体を提供することにある。
【課題を解決するための手段】
【0007】
上記課題を解決するために、本発明のある態様の蛍光体は、M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2及びEu2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、可視光を発する。
【0008】
M1O2は、SiO2を主成分とし、該SiO2の結晶構造がクリストバライトであってもよい。
【0009】
2価の金属イオンM2としてMn2+を含んでもよい。
【0010】
なお、以上の構成要素の任意の組合せ、本発明の表現を方法、装置、システム、などの間で変換したものもまた、本発明の態様として有効である。
【発明の効果】
【0011】
本発明によれば、特性の優れた新たな蛍光体を提供できる。
【図面の簡単な説明】
【0012】
【図1】本実施の形態に係る発光モジュールの概略断面図である。
【図2】第1の実施の形態における第2の蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【図3】各実施例に係る蛍光体の発光特性の傾向を示す図である。
【図4】各実施例に係る蛍光体の励起特性を示す図である。
【図5】実施例1〜7及び比較例7に係る蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【図6】本実施の形態に係る第2の蛍光体を用いた発光モジュール及び第2の蛍光体を用いていない発光モジュールのそれぞれの発光スペクトルを示す図である。
【図7】第2の実施の形態における第3の蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【図8】実施例9,10に係る蛍光体の発光特性の傾向を示す図である。
【図9】実施例9,10に係る蛍光体の励起特性を示す図である。
【図10】実施例9及び実施例10に係る蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【図11】本実施の形態に係る第3の蛍光体を用いた発光モジュール及び第3の蛍光体を用いていない発光モジュールのそれぞれの発光スペクトルを示す図である。
【発明を実施するための形態】
【0013】
以下、図面を参照しながら、本発明を実施するための形態について詳細に説明する。なお、図面の説明において同一の要素には同一の符号を付し、重複する説明を適宜省略する。
【0014】
[第1の実施の形態]
図1は、本実施の形態に係る発光モジュールの概略断面図である。図1に示す発光モジュール10は、基板12上に一対の電極14(陽極)及び電極16(陰極)が形成されている。電極14上には半導体発光素子18がマウント部材20により固定されている。半導体発光素子18と電極14はマウント部材20により導通されており、半導体発光素子18と電極16はワイヤー22により導通されている。半導体発光素子の出射面の上には蛍光体フィルタ24が設置されている。
【0015】
基板12は、導電性を有しないが熱伝導性は高い材料によって形成されることが好ましく、例えば、セラミック基板(窒化アルミニウム基板、アルミナ基板、ムライト基板、ガラスセラミック基板)やガラスエポキシ基板等を用いることができる。
【0016】
電極14及び電極16は、金や銅等の金属材料によって形成された導電層である。
【0017】
半導体発光素子18は、本発明の発光モジュールに用いられる発光素子の一例であり、例えば、紫外線又は短波長可視光を発光するLEDやLD等を用いることができる。具体例として、InGaN系の化合物半導体を挙げることができる。InGaN系の化合物半導体は、Inの含有量によって発光波長域が変化する。Inの含有量が多いと発光波長が長波長となり、少ない場合は短波長となる傾向を示すが、ピーク波長が400nm付近となる程度にInが含有されたInGaN系の化合物半導体が発光における量子効率が最も高いことが確認されている。
【0018】
マウント部材20は、例えば銀ペースト等の導電性接着剤又は金錫共晶はんだ等であり、半導体発光素子18の下面を電極14に固定し、半導体発光素子18の下面側電極と基板12上の電極14を電気的に接続する。
【0019】
ワイヤー22は、金ワイヤー等の導電部材であり、例えば超音波熱圧着等により半導体発光素子18の上面側電極及び電極16に接合され、両者を電気的に接続する。
【0020】
蛍光体フィルタ24は、後述する各蛍光体がバインダー部材に分散されている。蛍光体フィルタ24は、例えば、液状又はゲル状のバインダー部材に蛍光体を混入した蛍光体ペーストを作製した後、その蛍光体ペーストを光学ガラス上面に所定の膜厚に塗布し、その後に蛍光体ペーストのバインダー部材を硬化することにより形成される。バインダー部材としては、例えば、シリコーン樹脂やフッ素樹脂等を用いることができる。また、本実施の形態に係る発光モジュールは、励起光源として紫外線又は短波長可視光を用いることから、耐紫外線性能に優れたバインダー部材が好ましい。
【0021】
また、蛍光体フィルタ24は、蛍光体以外の種々の物性を有する物質が混入されていてもよい。バインダー部材よりも屈折率の高い物質、例えば、金属酸化物、フッ素化合物、硫化物等が蛍光体フィルタ24に混入されることにより、蛍光体フィルタ24の屈折率を高めることができる。これにより、半導体発光素子18から発生する光が蛍光体フィルタ24へ入射する際に生ずる全反射が低減され、蛍光体フィルタ24への励起光の取り込み効率を向上させるという効果が得られる。更に、混入する物質の粒子径をナノサイズにすることで、蛍光体フィルタ24の透明度を低下させることなく屈折率を高めることができる。また、アルミナ、ジルコニア、酸化チタン等の平均粒径0.3〜3μm程度の白色粉末を光散乱剤として蛍光体フィルタ24に混入することができる。これにより、発光面内の輝度,色度むらを防止することができる。
【0022】
次に、第1の形態に係る発光モジュールに用いられる各蛍光体について詳述する。
【0023】
(第1の蛍光体)
本実施の形態に係る第1の蛍光体は、黄色発光蛍光体である。黄色発光蛍光体(以下、「黄色蛍光体」と称する。)の好適な一例として、一般式がM1O2・aM2O・bM3X2:M4c(ただし、M1はSi、Ge、Ti、Zr及びSnからなる群より選ばれる少なくとも1種の元素、M2はMg、Ca、Sr、Ba及びZnからなる群より選ばれる少なくとも1種の元素、M3はMg、Ca、Sr、Ba及びZnからなる群より選ばれる少なくとも1種の元素、Xは少なくとも1種のハロゲン元素、M4は希土類元素及びMnからなる群より選ばれるEu2+を必須とする少なくとも1種の元素を示す。aは0.1≦a≦1.3、bは0.1≦b≦0.25の範囲である。)で表される黄色蛍光体が挙げられる。また、この黄色蛍光体は、紫外線又は短波長可視光により励起され、青色蛍光体が発する可視光と混色することで白色を実現する可視光を発する。より具体的には、黄色蛍光体は、560〜600nmの波長域にピーク波長を有する可視光を発する。
【0024】
(第2の蛍光体)
本実施の形態に係る第2の蛍光体は、青色発光蛍光体である。青色発光蛍光体(以下、「青色蛍光体」)の好適な一例として、M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2及びEu2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、青色の可視光を発する蛍光体が挙げられる。
【0025】
なお、2価の金属イオンのうち5%以内を3価および/または1価の金属イオンに置き換えてもよい。3価の金属イオンの例としては、Sc、Y、ランタニド(ランタノイド)、B、Al、Ga、Inなどが挙げられる。また、1価の金属イオンの例としては、Li、Na、K、Rb、Csなどが挙げられる。
【0026】
このような青色蛍光体として、M1O2は、SiO2を主成分とし、SiO2の結晶構造がクリストバライトである。図2は、第1の実施の形態における第2の蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【0027】
本実施の形態に係る第2の蛍光体は、図2に示すように、回折角2θが21度〜23度の間に最も高い回折強度が存在する。また、その回折強度を100%としたとき、第2の蛍光体は、回折角35度〜37度に13%〜22%、30度〜32度に7%〜17%、27.5度〜29.5度に6%〜20%の回折強度が生じる結晶構造である。このような結果より、本実施の形態に係る第2の蛍光体は、シリカ(SiO2)を主成分とし、クリストバライト又はそれに類似した結晶構造を有する新規な物質であることがわかる。
【0028】
以下に、第1の実施の形態を各実施例によって更に具体的に説明する。
【0029】
(実施例1)
はじめに、SiO2、CaI2、NH4I、CaF2及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において、5%のH2を含むN2雰囲気中、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体1を得た。
【0030】
(実施例2)
はじめに、SiO2、CaI2、NH4I、MgF2及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において、5%のH2を含むN2雰囲気中、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体2を得た。
【0031】
(実施例3)
はじめに、SiO2、CaCl2、NH4I、SrF2及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体3を得た。
【0032】
(実施例4)
はじめに、SiO2、CaCl2、NH4I、BaF2及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体4を得た。
【0033】
(実施例5)
はじめに、SiO2、CaH2、NH4I、NH4Br、及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体5を得た。
【0034】
(実施例6)
はじめに、SiO2、CaH2、NH4I、NH4Cl及びEu2O3を出発原料とし、後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体6を得た。
【0035】
(実施例7)
はじめに、SiO2、CaI2、NH4I、及びEuCl3を出発原料とし後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体7を得た。
【0036】
(実施例8)
はじめに、SiO2、CaH2、NH4I、CaF2、Al2O3、Li2CO3及びEu2O3を出発原料とし後述する表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体8を得た。蛍光体8は、3価の金属イオンと1価の金属イオンの合計が、2価の金属イオンの合計に対して5%入っている。
【0037】
【表1】

【0038】
なお、表1に示す各元素の値は、Ca=1.0として規格化した仕込みmol比を示す。
【0039】
図3は、各実施例に係る蛍光体の発光特性の傾向を示す図である。図4は、各実施例に係る蛍光体の励起特性を示す図である。実施例に係る蛍光体は、図3に示す発光特性より、470nm前後にピーク波長がある蛍光体である。また、図4に示す励起特性より、400nm前後の近紫外光を良く吸収し、発光する蛍光体である。
【0040】
次に各比較例について説明する。
【0041】
(比較例1)
はじめに、SrCO3、NH4Cl、SrHPO4、及びEu2O3を出発原料とし、これらの元素(モル)比がSrCO3:NH4Cl:SrHPO4:Eu2O3=1.98:1.40:3.00:0.01となるように秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1200℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z1を得た。
【0042】
(比較例2)
はじめに、SiO2、CaI2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z2を得た。
【0043】
(比較例3)
はじめに、SiO2、CaCl2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z3を得た。
【0044】
(比較例4)
はじめに、SiO2、CaCl2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z4を得た。
【0045】
(比較例5)
はじめに、SiO2、CaCl2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z5を得た。
【0046】
(比較例6)
はじめに、SiO2、CaH2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z6を得た。
【0047】
(比較例7)
はじめに、SiO2、Ca(OH)2、NH4I、及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z7を得た。
【0048】
(比較例8)
はじめに、SiO2、CaH2、NH4I、CaF2、Al2O3、Li2CO3及びEu2O3を出発原料とし、表1に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z8を得た。蛍光体Z8は、3価の金属イオンと1価の金属イオンの合計が、2価の金属イオンの合計に対して10%入っている。
【0049】
図5は、実施例1〜7及び比較例7に係る蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【0050】
図5に示すように、実施例1〜7に係る蛍光体は、22度付近にシリカの回折ピークが見られる蛍光体である。しかし、比較例7に係る蛍光体は、22度付近にシリカの回折ピークが見られず、30度付近(図5に示す矢印)にCaSiO3を示す回折ピークが見られる。これは、比較例7に係る蛍光体が、Ca(OH)2を原料としたために、原料混合物中のO(酸素)量が増加し、CaSiO3が生成したためである。
【0051】
次に、蛍光体を製造する際の原料混合物における各元素の好ましい仕込みモル比について説明する。表1のA値は、4価の金属元素(例えば、シリコン元素)に対するハロゲン元素の割合(モル比:X/M1)、B値は、2価の金属イオン(例えば、カルシウム元素やマグネシウム元素)に対する4価の金属元素の割合(モル比:M1/M2)、C値は、2価の金属イオンに占めるEuイオンの割合(モル比:Eu/M2)である。
【0052】
実施例1、比較例2より、B値が0.97から0.49に減少すると、発光強度は111%から49%に低下する。よって、B値は0.97以上が好ましい。また、実施例2より、B値が17.47の場合でも、発光強度は高い。つまり、0.97≦B≦17.47の範囲で発光強度が高い。よって、B値は、0.97≦B≦17.47を満たす範囲が望ましい。
【0053】
実施例2、比較例3は、ハロゲン量が少ない例である。実施例2、比較例3より、A値が0.029から0.017に減少すると、発光強度は110%から73%に低下する。一方、実施例4、比較例4はハロゲン量が多い例である。実施例4、比較例4より、A値が2.218から2.567に増加すると発光強度は、114%から70%に低下する。つまり、0.029≦A≦2.218の範囲で発光強度が高い。よって、A値は、0.029≦A≦2.218の範囲が望ましい。
【0054】
実施例5、比較例5はEuの量が少ない例である。実施例5、比較例5より、C値が0.005から0.002に減少すると、発光強度は113%から55%に低下する。一方実施例6、比較例6はEuの量が多い例である。実施例6、比較例6より、C値が、0.177から0.265に増加すると発光強度は、116%から67%に低下する。つまり、0.005≦C≦0.177の範囲で発光強度が高い。よって、C値は、0.005≦C≦0.177の範囲が望ましい。
【0055】
以上のように、各実施例に係る蛍光体は、その合成時に、ハロゲン元素の出発原料として、M3X(M3は、NH4あるいは1価の金属)、又はM2X2(M2は2価の金属イオン)の組成式で表される化合物を用いて作製される。
【0056】
実施例8と比較例8は、3価の金属イオンと1価の金属イオンを入れた例である。実施例8、比較例8より、D値(後述)が0.05から0.10に増加すると、発光強度が112%から63%に低下する。原料に3価と1価の金属イオンを含んでいない実施例3,4に係る蛍光体においては、D値=0であり、発光強度は114%と高い。つまり、0≦D≦0.05の範囲で発光強度が高い。よって、D値は、0≦D≦0.05の範囲が好ましい。
【0057】
なお、D値は、1価の金属イオン(M3)と3価の金属イオン(M4)の合計のモル数を2価の金属イオン(M2)の合計のモル数で割った値であり、
D値=(M3+M4)/M2
で表される。
【0058】
また、各実施例に係る蛍光体は、原料として、化合物M1O2(M1は、Si、Ge、Ti、Zr及びSnからなる群より選ばれるSiを必須とする少なくとも1種の元素)と、M2X2又はM2H2(M2は、Mg、Ca、Sr、Ba、Mn及びEu2+からなる群より選ばれるCa、Eu2+を必須とする2価の金属イオン)と、M3X(M3は、NH4、Li、Na、K、Rb及びCsからなる群より選ばれるNH4イオンを必須とする少なくとも1価のイオン、Xは、I、F、Cl及びBrからなる群より選ばれるIを必須とする少なくとも一種のハロゲン元素)と、を使用している。
【0059】
次に、実施例に係る蛍光体を組み合わせた発光モジュールの特性について説明する。図6は、本実施の形態に係る第2の蛍光体を用いた発光モジュール及び第2の蛍光体を用いていない発光モジュールのそれぞれの発光スペクトルを示す図である。
【0060】
本実施の形態に係る第2の蛍光体を用いた発光モジュール1は、比較例1に記載の蛍光体Z1(Srアパタイト)と、各実施例に代表される第2の蛍光体と、黄色蛍光体(第1の蛍光体)とを1:1:4の比(重量比)で混合した蛍光体層を有している。一方、第2の蛍光体を用いていない発光モジュール2は、比較例1に記載の蛍光体Z1(Srアパタイト)と、黄色蛍光体(第1の蛍光体)とを1:2の比(重量比)で混合した蛍光体層を有している。なお、発光モジュール1及び発光モジュール2は、発光のピーク波長が400nm前後の励起光源としてUV−LEDを備えている。
【0061】
表2は、各発光モジュールの発光強度、色温度、色度(Cx,Cy)、演色性(平均演色評価数Ra)の結果を示している。なお、発光強度は、発光モジュール2の場合を100%として規格化した値である。この結果から、本実施の形態に係る第2の蛍光体を有していない発光モジュール2の演色性がRa=75であるのに対し、第2の蛍光体を有している発光モジュール1の演色性がRa=80である。つまり、各実施例に代表される本実施の形態に係る第2の蛍光体は、演色性を高める効果がある。換言すれば、本実施の形態に係る第2の蛍光体は、特性の優れた蛍光体ということができる。
【0062】
【表2】

【0063】
[第2の実施の形態]
本実施の形態に係る第3の蛍光体は、前述の第2の蛍光体と類似した構造を有しているが、Mnを含むことで赤色に発光する蛍光体である。なお、第1の実施の形態と同様の構成については、説明を適宜省略する。
【0064】
第2の実施の形態に係る発光モジュールは、蛍光体の種類が一部異なる以外は、第1の実施の形態に係る発光モジュールと同様の構成である。
【0065】
(第1の蛍光体)
第1の実施の形態に係る黄色蛍光体と同じである。
【0066】
(第3の蛍光体)
本実施の形態に係る第3の蛍光体は、赤色発光蛍光体である。赤色発光蛍光体(以下、「赤色蛍光体」)の好適な一例として、M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2、Eu2+及びMn2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、赤色の可視光を発する蛍光体が挙げられる。
【0067】
このような赤色蛍光体として、M1O2は、SiO2を主成分とし、SiO2の結晶構造がクリストバライトである。図7は、第2の実施の形態における第3の蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【0068】
本実施の形態に係る第3の蛍光体は、図7に示すように、回折角が2θが21度〜23度の間に最も高い回折強度が存在する。また、その回折強度を100%としたとき、第3の蛍光体は、35度〜37度に10%〜30%、30度〜32度に5%〜20%、27.5度〜29.5度に6%〜30%の回折強度が生じる結晶構造である。このような、結果より、本実施の形態に係る第3の蛍光体は、シリカ(SiO2)を主成分とし、クリストバライト又はそれに類似した結晶構造を有する新規な物質であることがわかる。
【0069】
以下、第2の実施の形態を各実施例によって更に具体的に説明する。
【0070】
(実施例9)
はじめに、SiO2、CaH2、MnCl2、NH4I、CaF2及びEu2O3を出発原料とし、後述する表3に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において、5%のH2を含むN2雰囲気中、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体9を得た。
【0071】
(実施例10)
はじめに、SiO2、CaH2、MnCO3、NH4I、NH4F及びEu2O3を出発原料とし、後述する表3に示すような元素比になるように、秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において、5%のH2を含むN2雰囲気中、1000℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体10を得た。
【0072】
【表3】

【0073】
なお、表3に示す各元素の値は、Ca=1.0として規格化した仕込みmol比を示す。
【0074】
図8は、実施例9,10に係る蛍光体の発光特性の傾向を示す図である。図9は、実施例9,10に係る蛍光体の励起特性を示す図である。実施例9,10に係る蛍光体は、図8に示す発光特性より、635nm前後にピーク波長がある蛍光体である。また、図9に示す励起特性より、400nm前後の近紫外光を良く吸収し、発光する蛍光体である。
【0075】
次に比較例について説明する。
【0076】
(比較例9)
はじめに、SrCO3、NH4Cl、SrHPO4、及びEu2O3を出発原料とし、これらの元素(モル)比がSrCO3:NH4Cl:SrHPO4:Eu2O3=1.98:1.40:3.00:0.01となるように秤量した各原料を、大気中でアルミナ乳鉢に入れ約30分粉砕混合し、原料混合物を得た。この原料混合物をアルミナ坩堝に入れ、還元雰囲気の電気炉において5%のH2を含むN2雰囲気中で、1200℃で3〜5時間焼成し、焼成物を得た。得られた焼成物を温純水で丹念に洗浄し、蛍光体Z9を得た。
【0077】
図10は、実施例9及び実施例10に係る蛍光体について、CuのKα特性X線を用いたX線回折の測定結果を示す図である。
【0078】
図10に示すように、実施例9,10に係る蛍光体は、22度付近にシリカの回折ピークが見られる蛍光体である。
【0079】
以上のように、実施例9,10に係る蛍光体は、その合成時に、ハロゲン元素の出発原料として、M3X(M3は、NH4あるいは1価の金属)、又はM2X2(M2は2価の金属イオン)の組成式で表される化合物を用いて作製される。
【0080】
また、実施例9,10に係る蛍光体は、原料として、化合物M1O2(M1は、Si、Ge、Ti、Zr及びSnからなる群より選ばれるSiを必須とする少なくとも1種の元素)と、M2X2又はM2H2(M2は、Mg、Ca、Sr、Ba、Mn及びEu2+からなる群より選ばれるCa、Eu2+、Mnを必須とする2価の金属イオン)と、M3X(M3は、NH4、Li、Na、K、Rb及びCsからなる群より選ばれるNH4イオンを必須とする少なくとも1価のイオン、Xは、I、F、Cl及びBrからなる群より選ばれるIを必須とする少なくとも一種のハロゲン元素)と、を使用している。なお、M2の原料において、例えばCaO、CaCO3などの酸素を含む原料の割合を60%以下とするとよい。
【0081】
次に、実施例に係る蛍光体を組み合わせた発光モジュールの特性について説明する。図11は、本実施の形態に係る第3の蛍光体を用いた発光モジュール及び第3の蛍光体を用いていない発光モジュールのそれぞれの発光スペクトルを示す図である。
【0082】
本実施の形態に係る第3の蛍光体を用いた発光モジュール3は、比較例9に記載の蛍光体Z9(Srアパタイト)と、各実施例に代表される第3の蛍光体と、黄色蛍光体(第1の蛍光体)とを1.3:2.7:1.0の比(重量比)で混合した蛍光体層を有している。一方、第3の蛍光体を用いていない発光モジュール4は、比較例9に記載の蛍光体Z9(Srアパタイト)と、黄色蛍光体(第1の蛍光体)とを1.3:2.7の比(重量比)で混合した蛍光体層を有している。なお、発光モジュール3及び発光モジュール4は、発光のピーク波長が400nm前後の励起光源としてUV−LEDを備えている。
【0083】
表4は、各発光モジュールの色度(Cx,Cy)、演色性(平均演色評価数Ra)の結果を示している。この結果から、本実施の形態に係る第3の蛍光体を有していない発光モジュール4の演色性がRa=75であるのに対し、第3の蛍光体を有している発光モジュール3の演色性がRa=85である。つまり、各実施例に代表される本実施の形態に係る第3の蛍光体は、演色性を高める効果がある。換言すれば、本実施の形態に係る第3の蛍光体は、特性の優れた蛍光体ということができる。
【0084】
【表4】

【0085】
以上、本発明を実施の形態や実施例をもとに説明した。この実施の形態は例示であり、それらの各構成要素や各処理プロセスの組合せにいろいろな変形例が可能なこと、またそうした変形例も本発明の範囲にあることは当業者に理解されるところである。
【産業上の利用可能性】
【0086】
本発明の蛍光体は、種々の灯具、例えば照明用灯具、ディスプレイ用バックライト、車両用灯具等に適用される発光モジュールに利用することができる。
【符号の説明】
【0087】
10 発光モジュール、 12 基板、 14,16 電極、 18 半導体発光素子、 20 マウント部材、 22 ワイヤー、 24 蛍光体フィルタ。
【特許請求の範囲】
【請求項1】
M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2及びEu2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、可視光を発する蛍光体。
【請求項2】
前記M1O2は、SiO2を主成分とし、該SiO2の結晶構造がクリストバライトであることを特徴とする請求項1に記載の蛍光体。
【請求項3】
2価の金属イオンM2としてMn2+を含むことを特徴とする請求項1または2に記載の蛍光体。
【請求項1】
M1O2(M1は4価の金属元素)を主骨格とし、ハロゲン元素X(Xは、F、Cl、Br及びIからなる群より選ばれる少なくとも一種以上の元素)と2価の金属イオンM2及びEu2+を必須とした酸化物結晶を含み、紫外線又は短波長可視光により励起され、可視光を発する蛍光体。
【請求項2】
前記M1O2は、SiO2を主成分とし、該SiO2の結晶構造がクリストバライトであることを特徴とする請求項1に記載の蛍光体。
【請求項3】
2価の金属イオンM2としてMn2+を含むことを特徴とする請求項1または2に記載の蛍光体。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【公開番号】特開2013−95879(P2013−95879A)
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願番号】特願2011−241612(P2011−241612)
【出願日】平成23年11月2日(2011.11.2)
【出願人】(000001133)株式会社小糸製作所 (1,575)
【Fターム(参考)】
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願日】平成23年11月2日(2011.11.2)
【出願人】(000001133)株式会社小糸製作所 (1,575)
【Fターム(参考)】
[ Back to top ]

