蛍光測定装置、蛍光測定用ウェル、蛍光測定方法
【課題】 DNAの増幅等において、極めて高い感度で蛍光をリアルタイムで測定可能な蛍光測定装置等を提供する。
【解決手段】 ウェル3は、内部に反応溶液15を保持可能である。ウェル3は、反応溶液と接する側から、内部樹脂層19および外部樹脂層23の二層構造で構成される。ここで、内部樹脂層19の屈折率は、外部樹脂層23よりも高い。また、導波路9は、中央部にコア部25が設けられ、コア部25を覆うように外周部にクラッド部27が設けられる。コア部25を構成する樹脂の屈折率は、クラッド部27を構成する樹脂の屈折率よりも高い。ウェル3と導波路9との接合部では、内部樹脂層19とコア部25とが接合される。また、外部樹脂層23とクラッド部27とが接合される。したがって、内部樹脂層19内に封じ込められた光は、コア部25に導出され、コア部25内を伝播する。
【解決手段】 ウェル3は、内部に反応溶液15を保持可能である。ウェル3は、反応溶液と接する側から、内部樹脂層19および外部樹脂層23の二層構造で構成される。ここで、内部樹脂層19の屈折率は、外部樹脂層23よりも高い。また、導波路9は、中央部にコア部25が設けられ、コア部25を覆うように外周部にクラッド部27が設けられる。コア部25を構成する樹脂の屈折率は、クラッド部27を構成する樹脂の屈折率よりも高い。ウェル3と導波路9との接合部では、内部樹脂層19とコア部25とが接合される。また、外部樹脂層23とクラッド部27とが接合される。したがって、内部樹脂層19内に封じ込められた光は、コア部25に導出され、コア部25内を伝播する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、生体材料の反応あるいは生成あるいは、PCR(Polymerase Chain Reaction)などの蛍光測定装置およびこれらの装置を用いた蛍光測定方法に関するものである。
【背景技術】
【0002】
PCR法は、ごく微量のDNAから目的とするDNA領域を短時間で増殖する方法として知られている。その原理は、2本鎖DNA上の2つの既知配列を利用して、相互いの合成方向が向かい合うような2つのプライマDNAを設計する。これらのプライマに挟まれた領域のDNAが合成されると、それが次のサイクルでは鋳型になる。このような反応を繰り返すことで、DNA鎖を幾何級数的に増幅することができる。
【0003】
DNAを増幅するPCR装置は、例えば、反応溶液の温度を50℃台、70℃台、90℃台に3段階に変え、変性、アニーリング、ポリメラーゼ伸長の各工程を繰り返すことでDNAを増幅する。なお、3段階の温度制御を一通り行うと理論上DNA量は2倍となる。
【0004】
このような、PCR装置において、DNAの増幅の進行を把握する手段としては、DNAの増幅に応じて発生する、または消滅する蛍光を測定する方法がある。例えば、ヘアピンプライマPCR法では、ヘアピン領域に低分子が特異的に結合するシトシンバルジ領域が導入され、DNA鎖の合成が進行し、PCRによりヘアピンプライマのヘアピン構造が開かれると、シトシンバルジ構造が消失する。このため蛍光色素が遊離して、蛍光強度が低下する。
【0005】
また、例えばTaq Man PCR法では、蛍光基と消光基で標識されたオリゴマーを用い、DNAの増幅に伴って消光基が消滅することで、DNA鎖の合成が進行によって蛍光強度が増加するものである。すなわち、いずれの場合においても、反応系の蛍光を検出することで、PCRの進行を把握することができる。
【0006】
このような、リアルタイムPCRに関しては、例えば、伸長性の優れたDNAポリメラーゼをPCRに用いることにより、より短時間で遺伝子を検出することが可能な遺伝子の増幅方法が開示されている(特許文献1)。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2010−239880号公報
【発明の概要】
【発明が解決しようとする課題】
【0008】
図9は、このようなリアルタイムPCRによって、蛍光を測定するためのウェル近傍を示す概略図である。まず、図9(a)に示すように、ウェル109内に各種の構成を含む反応溶液113が入れられる。この状態で、上方より照射・受光部111より光を照射する(図中矢印I方向)。照射・受光部111は、例えば光ファイバであり、図示を省略した光源および蛍光測定器に接続されている。
【0009】
光が照射された反応溶液からは、PCRの進行に応じた蛍光が発生(消失)する。図9(b)は、仮に蛍光発生中心115を蛍光の発生する中心であるとした場合に、蛍光の発生する状態を示す模式図である。蛍光発生中心115から発生する蛍光は、蛍光発生中心115を中心に全方向に(蛍光発生中心115を中心とする球体を仮定した場合の球面方向に対して)略均一に発生する(図中矢印J方向)。
【0010】
この際、例えば照射・受光部111の受光面と蛍光発生中心115との距離をLとすると、仮想受光面117(半径Lの球体の表面積)は、4πL2で表わされる。すなわち、ウェル109での反射等を無視すれば、反応溶液から発生した蛍光は、4πL2の表面積を有する仮想受光面117の表面全体に均一に到達する。
【0011】
ここで、照射・受光部111の受光面の面積をaとすれば、実際に発生した蛍光の内、受光できる蛍光の量は、全体の4πL2の面積の内、面積aの受光可能領域119(図中におけるハッチング部)のみとなる。すなわち、それ以外の方向に進んだ蛍光は、受光されることなく散逸する。
【0012】
ここで、照射・受光部111の径を5mmΦとし、距離Lを10mmとする。すると、仮想受光面117の全表面積(4×π×102)は、1257mm2程度となる。また、受光面の面積は(π×2.52)は、約20mm2程度となる。したがって、発生した蛍光に対して、20/1257=約1.6%程度となる。
【0013】
このように、従来の蛍光測定装置においては、実際に生じた蛍光のほとんどが外部に漏れ出しており、発生した蛍光の内、わずかしか受光することができない。すなわち、蛍光を受光する効率が極めて悪い。したがって、例えば、医療分野において、被検査サンプル中の抗原(例えばウィルス)量が十分でないと検出精度を確保することが困難である。
【0014】
特に、通常は多数のウェル内の蛍光を同時または順次に測定するため、複数のウェルプレート又は測定器が移動して測定を行う。この際、図9に示すように、測定距離が大きくなるほどに蛍光量は減衰するので、その感度は低下する。また隣のウェルの蛍光量の影響を受け易くなる。したがって、個々のウェル内の蛍光を高感度に測定することは困難である。また、特殊な試薬を用いて感度を得る方法もあるが、このような方法では反応溶液自体が高価であるため、より安価かつ高感度に測定可能な方法が望まれている。
【0015】
本発明は、このような問題に鑑みてなされたもので、DNAの増幅等において、極めて高い感度で蛍光をリアルタイムで測定可能な蛍光測定装置等を提供することを目的とする。
【課題を解決するための手段】
【0016】
前述した目的を達するために第1の発明は、蛍光測定装置であって、反応溶液を保持するウェルと前記ウェルの外周部に配置され、反応溶液の温度を調整可能な温度調整部と前記ウェルの下方に設けられる導波路と前記ウェル内で発生する蛍光を測定する蛍光測定器とを具備し、前記ウェルは、少なくとも外部樹脂層と内部樹脂層の二層構造であり、前記内部樹脂層の屈折率は前記外部樹脂層の屈折率よりも大きく、前記導波路は内部に前記内部樹脂層と同一の材質からなるコア部と外部に前記外部樹脂層と同一の材質からなるクラッド部を有して、前記ウェルと一体で構成されるとともに、複数の前記ウェルが連結されてウェルプレートを形成し、前記温度調整部によって前記反応溶液の温度を調整することで反応溶液中で生体材料の反応あるいは生成を行うことができ、前記ウェル内で発生した蛍光を前記内部樹脂層に封じ込めて前記コア部に導出して前記蛍光測定器によって測定可能であることを特徴とする蛍光測定装置である。
【0017】
前記温度調整部は、前記均熱板と前記均熱板の下部に設けられる熱電素子と前記熱電素子の下部に配置される冷却部とを具備し、前記ウェルおよび前記導波路が前記温度調整部を貫通して設けられることが望ましい。
【0018】
前記ウェルの上端面には、反射膜が形成されてもよい。前記導波路の端部には光源が設けられ、前記光源は、前記導波路を介して前記ウェル内の前記反応溶液に光を照射し、前記蛍光測定器は、前記導波路からの蛍光を光フィルタを介して測定可能であってもよい。
【0019】
前記ウェルを構成する樹脂は、内部樹脂層としては、たとえば、耐熱性を有するポリカーボネート樹脂、変性ポリカーボネート樹脂、ポリアミド、高Tg成分モノマーとのアクリル系重合体、ノルボルネン系樹脂、シリコーン樹脂、架橋アクリル樹脂などを用いることができ、また、外部樹脂層には、一般的には耐熱性が高く、内部樹脂層よりも低屈折率のポリカーボネート樹脂、シリコーン樹脂、フッ素系樹脂やポリアミドを用いることができる。
【0020】
第1の発明によれば、ウェルの周囲に温調可能な温度調整部が設けられるため、DNAの分離、抽出、増幅などの生体材料の反応あるいは生成および蛍光の測定を連続して行うことができる。
【0021】
また、ウェルが二層構造で構成され、内部樹脂層の屈折率を外部樹脂層の屈折率よりも大きくすることで、ウェル内に入れられた反応溶液中からの蛍光をウェルの内部樹脂層に封じ込めることができる。また、内部樹脂層がウェルの下部で導波路に接続されるため、蛍光を導波路に導入することができる。したがって、導波路に接続された蛍光測定器で蛍光を効率良く測定することができる。
【0022】
また、ウェル内で生じる蛍光を直接導波路に導出することで、従来の方法と比較して、外部に散逸する蛍光成分を抑えることができる。このため、極めて高い感度で蛍光を測定することができる。
【0023】
また、ウェルの上端面に反射膜を形成することで、内部樹脂層内の蛍光がウェルの上端面から漏れてしまうことがない。
【0024】
また、温度調整部が、均熱板、熱電素子および冷却部から構成され、ウェルおよび導波路が温度調整部を貫通して設けられれば、ウェル内の反応溶液の温度を迅速に調整することができる。また、温度調整部に設けられたウェルは、温度調整部に形成された貫通孔に配置されるため、測定後は容易に温度調整部から使用済みのウェルを取り外し、交換が可能である。このため、取り扱い性に優れる。
【0025】
なお、熱電素子としては、例えばペルチェ素子を用いることが望ましい。ペルチェ素子への電圧負荷方向を制御することで、昇温および降温の制御を行うことができる。したがって、ウェル内の反応溶液を迅速に規定の温度に調整することができる。
【0026】
また、ウェルを構成する樹脂として、内部樹脂層の樹脂としては、ポリカーボネート(耐熱温度125−135℃)、変性ポリカーボネート(耐熱温度145℃)、高Tg成分モノマーとのアクリル系重合体、ノルボルネン系樹脂(耐熱温度150℃)、シリコーン樹脂(150−170℃)、架橋アクリル樹脂(耐熱温度175℃)から選択することで、PCRにおける熱でウェルが損傷することがない。また、内部樹脂層の樹脂にPMMAを用いても、外部樹脂層にα―フルオロアクリレート系樹脂を用いたプラスチック光ファイバを用いれば、耐熱性を向上させることができる。
【0027】
尚、本装置を加熱の必要がない試験に用いる場合には、内部樹脂層の樹脂として、最も一般的に使用されているPMMA、ポリスチレンなどを用いた汎用プラスチックファイバを用いることもできる。
【0028】
上述の内部樹脂層の樹脂としては、外部樹脂層の樹脂より、屈折率が高く、導波路のコア材との相溶性あるいは親和性に優れ、さらに耐熱性に優れる樹脂ならば、いかなる樹脂をも用いることができる。
【0029】
第2の発明は、蛍光測定用の反応溶液を保持する蛍光測定用ウェルであって、前記反応溶液の保持部は、少なくとも外部樹脂層と内部樹脂層の二層構造であり、前記内部樹脂層の屈折率は、前記外部樹脂層の屈折率よりも大きく、前記保持部の下方に前記保持部と一体で形成される導波路は、内部に前記内部樹脂層と同一の材質からなるコア部と、外部に前記外部樹脂層と同一の材質からなるクラッド部を有し、複数の前記保持部が連結されて構成されることを特徴とする蛍光測定用ウェルである。
【0030】
第2の発明によれば、高感度な測定が可能なウェルを容易に得ることができる。
【0031】
第3の発明は、蛍光測定方法であって、第1の発明にかかる蛍光測定装置の温度調整部を制御して、前記ウェル内に保持された反応溶液の温度を調整することで、反応溶液中の蛍光色素で標識した生体材料の反応あるいは生成の進行を、前記反応溶液からの蛍光を連続して前記光測定器で測定することを特徴とする蛍光測定方法である。
【0032】
また、第1の発明にかかる蛍光測定装置の温度調整部を制御して、前記ウェル内に保持された反応溶液を昇温して、鋳型DNAを一本鎖に分離する変性工程と、前記変性工程から降温し、プライマをDNAにハイブリダイズするアニーリング工程と、前記アニーリング工程から昇温し、DNAポリメラーゼの酵素反応により、プライマに挟まれたDNA領域を増幅するポリメラーゼ伸長工程と、前記ポリメラーゼ伸長工程から降温し、DNA領域の増幅の進行を前記光測定器で測定する蛍光測定工程と、を具備することを特徴とする蛍光測定方法である。
【0033】
また、前記反応溶液中の蛍光を前記光測定器により測定後、測定を終了した反応溶液を保持するウェルプレートを前記温度調整部より取り外し、新たな測定対象である反応溶液を保持するウェルプレートに交換した後、蛍光測定を繰り返すこともできる。
【0034】
第3の発明によれば、ウエル内に保持された反応溶液の温度を調整することで、反応溶液中の蛍光色素で標識した生体材料の反応あるいは生成を、前記反応溶液からの蛍光を連続して前記光測定器で測定することができ、さらには、DNAの分離、抽出、増幅を同一ウェル内で行うことが可能であるとともに、DNA増幅工程に対して連続してDNA増幅の進行を把握するための蛍光測定を行うことができる。
【発明の効果】
【0035】
本発明によれば、DNAの増幅等において、極めて高い感度で蛍光をリアルタイムで測定可能な蛍光測定装置等を提供することができる。
【図面の簡単な説明】
【0036】
【図1】蛍光測定装置1を示す概略図。
【図2】ウェル3の拡大図。
【図3】ウェル3および導波路9の屈折率の分布図であり、(a)は図2のC−C線断面における分布図、(b)は図2のD−D線断面における分布図。
【図4】ウェルの断面拡大図であり、(a)は図2のA部拡大図、(b)は図2のB部拡大図。
【図5】ウェルで受光可能な領域を示す概念図。
【図6】ウェル3の全体斜視図。
【図7】PCR測定の温度サイクルを示す概念図。
【図8】他の実施形態を示す図で、蛍光測定装置1aを示す概略図。
【図9】従来の受光領域を示す概念図。
【発明を実施するための形態】
【0037】
以下、図面を参照しながら、本発明の実施形態について説明する。図1は、蛍光測定装置1を示す概略図である。蛍光測定装置1は主に、複数のウェル3a、3b、・・・、3nと、複数の光源5a、5b、・・・、5nと、導波路9a、9b、・・・、9nと、光学フィルタ11a、11b、・・・、11nと、蛍光測定器13a、13b、・・・、13nおよび各ウェルの温度調整を行う温度調整部12等から構成される。なお、簡単のため、図ではウェルは3つのみ示すが、例えば、一つのプレート上には例えば4列×6段=24個のウェルが配置される。
【0038】
ウェル3a、3b、・・・、3n(以下、総称してウェル3とする)は、内部に反応溶液15を保持可能である。ウェル3は、反応溶液を保持する部位の高さが約10mmであり、外径が約8〜10φ(内径約6〜8φ)程度である。また、ウェル3の下部にはそれぞれ導波路9a、9b、・・・、9n(以下、総称して導波路9とする)が一体で形成される。
【0039】
各ウェル3は、上部において連結部4で連結される。すなわち、各ウェル3は所定の間隔で一体に形成される。なお、本発明では、個々のウェルを分離して構成してもよく、図示したように、複数のウェルを一体で形成してもよい。以下の説明においては、複数のウェルが連結されたものウェルプレートと称する。
【0040】
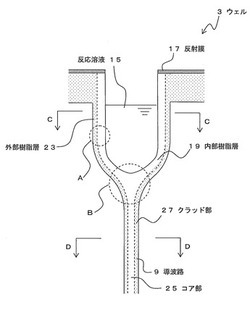
図2(a)は、ウェル3の拡大図である。また、図3はウェルを含む屈折率の分布図であり、図3(a)は図2のC−C線断面における分布図、図3(b)は図2のD−D線断面における分布図である。また、図4(a)は、図2のA部拡大図、図4(b)は図2のB部拡大図である。ウェル3は、反応溶液と接する側から、内部樹脂層19および外部樹脂層23の二層構造で構成される。ここで、図3(a)、図3(b)に示すように、内部樹脂層19の屈折率は、外部樹脂層23よりも高い。
【0041】
図3(a)のLは反応溶液15の領域の屈折率である。また、図3(a)、図3(b)のMは内部樹脂層19の屈折率であり、Nは外部樹脂層23の屈折率である。なお、Nの両側は空気層であり、屈折率は1.0である。反応溶液15の屈折率は、使用する溶液による。内部樹脂層19の屈折率は、例えば1.50〜1.70程度であり、外部樹脂層23の屈折率は、例えば、1.48以下程度である。すなわち、内部樹脂層19の内部に光を封じ込めることが可能である。
【0042】
なお、ウェル3は、例えば、内部樹脂層は、耐熱性を有するポリカーボネート樹脂、変性ポリカーボネート樹脂、ポリアミド、高Tg成分モノマーとのアクリル系重合体、ノルボルネン系樹脂、シリコーン樹脂、架橋アクリル樹脂等の例えば110℃以上(さらに望ましくは120℃以上)の耐熱性を有する樹脂中から、反応溶液等に対する耐薬品性を考慮して選定した材質で構成する。外部樹脂層には、一般的にはフッ素系樹脂やポリアミドを用いる。また、屈折率の調整は、各層を構成する樹脂材質を変更することにより行ってもよく、または、同材質の母材に適宜添加剤を添加してもよい。
【0043】
また、ウェル3を構成する材料としては、樹脂材料よりも耐熱性に優れるガラスを用いてもよい。このようなガラスとしては、例えば、300から400℃で成形可能な、SiO2あるいはNa2Oを含有する多成分ガラスを用いることができる。
【0044】
また、図4(b)に示すように、導波路9は、中央部にコア部25が設けられ、コア部25を覆うように外周部にクラッド部27が設けられる。コア部25を構成する樹脂の屈折率は、クラッド部27を構成する樹脂の屈折率よりも高い。例えば、コア部25は内部樹脂層19と同一の材質で構成されることが望ましいが、内部樹脂層の樹脂と、コア部を構成する樹脂は、互いに相溶性を有し、互いの屈折率が同一または近似するものを用いてもよい。同様に、クラッド部27は外部樹脂層23と同一の材質で構成されることが望ましいが、外部樹脂層の樹脂と、クラッド部を構成する樹脂は、互いに相溶性を有し、互いの屈折率が同一または近似するものを用いてもよい。ここで、コア部と内部樹脂層の屈折率は、同一または近時する必要があるが、両者を比べた場合に、コア部の屈折率が内部樹脂層の屈折率より大きければ良い。ここで、互いの屈折率が近似するとは、例えば、屈折率の違いが0.1程度以下であり、さらに好ましくは0.05以下であることが望ましい。なお、導波路9としてはプラスチックファイバを用いてもよい。
【0045】
ウェル3と導波路9との接合部では、内部樹脂層19とコア部25とが一体で形成される。また、外部樹脂層23とクラッド部27とが一体で形成される。したがって、内部樹脂層19内に封じ込められた光は、コア部25に導出され、コア部25内を伝播する。
【0046】
また、図1に示すように、ウェル3の上方には光源5a、5b、・・・、5n(以下、総称して光源5とする)がそれぞれ配置される。光源5は、それぞれのウェル3内の反応溶液に所定の波長の光を照射する。光源5としては、レーザやLED等を用いることができる。
【0047】
ウェル3の上端面には、反射膜17が設けられる。反射膜17は、ウェル3(内部樹脂層19)内の光が、ウェル3の上端から漏れだすことを防止するものである。反射膜17としては、酸化ケイ素、酸化チタン、酸化ニオブなどの物質を蒸着などによって形成すればよく、また、反射膜成分を塗布してもよい。反射膜17の形成方法は問わない。
【0048】
ウェル3の上面には、蓋2が設けられる。蓋2は、例えば透明なガラス板または樹脂板である。したがって、前述の光源5からの光を透過する。蓋2は、反応溶液の昇温時に、反応溶液の蒸発を防止し、隣接する各ウェルの反応溶液が蒸気によって混入しあうことを防止するものである。
【0049】
ウェル3の外周部には、温度調整部12が設けられる。温度調整部12は、均熱板7、熱電素子8、冷却部10から構成される。均熱板7、熱電素子、冷却部10は例えば一体で構成される。温度調整部12は、図示を省略した制御部に接続されており、ウェル3内部の反応溶液15の温度調整が可能である。
【0050】
均熱板7は例えばアルミニウム板や銅板等の金属板である。均熱板7は下部に設けられる熱電素子8の熱を均一に分散させるものである。均熱板7としては、6mm程度の厚みであり、例えば、ウェルの高さ程度に設定すればよい。
【0051】
熱電素子8は、均熱板7の下部に接合される。熱電素子8は、例えばペルチェ素子である。熱電素子8に対して電圧を付与することで、熱電素子8を昇温または降温することができる。熱電素子8(層)の厚みは、例えば1.5〜2mm程度とすればよい。
【0052】
熱電素子8の下部には冷却部10が設けられる。冷却部10は、熱電素子8自体を冷却するものである。冷却部10としては、例えばアルミニウム製のフィン材等を用い、また、図示を省略したファンによって空冷することができる。冷却部10としては、例えば10〜20mm程度とすればよい。
【0053】
温度調整部12は、熱電素子8、および冷却部10の動作を制御することで、ウェル3内部の反応溶液15の温度を迅速に制御することができる。なお、温度サイクルについては後述する。
【0054】
均熱板7、熱電素子8、冷却部10からなる温度調整部12には、貫通孔が形成される。貫通孔には、ウェル3および導波路9が挿入される。なお、導波路9の挿入性を高めるために、貫通孔にあらかじめパイプを配置してもよい。貫通孔にウェル3および導波路9を挿入することで、温度調整部12とウェル3を接触させることができる。
【0055】
なお、本発明では、ウェル3および導波路9を温度調整部12から取り外すことで、ウェルの交換を容易に行うことができる。すなわち、ウェル3自体を使い捨てとし、温度調整部12を繰り返し使用することで、常に新たなウェルを使用することができ、交換作業性にも優れる。
【0056】
また、貫通孔の加工性および反応溶液の温度を均一にするため、均熱板7の位置にウェル3の外径変化部を配置することが望ましい。均熱板7は金属板であり、比較的加工が容易であるため、ウェルの外径に応じた複雑な形状にも容易に対応が可能であるが、熱電素子8はその加工性や設計の自由度が低いため、熱電素子8における貫通孔は、導波路9のように径が変化しない部位とすることが望ましい。
【0057】
導波路9には、それぞれ光学フィルタ11a、11b、・・・、11n(以下、総称して光学フィルタ11とする)が接続され、さらに光学フィルタ11を介して蛍光測定器13a、13b、・・・、13n(以下、総称して蛍光測定器13とする)と接続される。光学フィルタ11は、反応溶液15内で発生する蛍光成分以外の光(例えば照射光成分)を除去するものである。光学フィルタ11を通過した蛍光は、各蛍光測定器13で測定される。
【0058】
すなわち、ウェル3内部の反応溶液15では、温度調整部12による温度調整によって、DNAの増幅が行われる。この際観察される蛍光成分はウェル3内部の内部樹脂層19内に封じ込められる。内部樹脂層19内の蛍光は、導波路9に導出されて光学フィルタ11を介して光測定器13で測定される。以上により、蛍光の増減をリアルタイムで監視することができる。
【0059】
なお、蛍光測定器は、各ウェル毎に配置してもよいが、ウェル3または蛍光測定器13を相対的に移動させることで、一つの蛍光測定器によって複数のウェル内の蛍光を測定してもよい。
【0060】
例えば、ウェルが複数列×複数段に配置されている場合に、ウェルの列の数だけ蛍光測定器13を設けて、各列の蛍光を測定する。次に、当該列に垂直な方向に順次ウェル(または蛍光測定器)を相対的に移動させ、次の段における各列の蛍光を測定する。以上を繰り返すことで、各列のウェルを各段ごとに順次測定することができる。なお、光スイッチ等を用いて、ウェルと蛍光測定器とを光接続し、光スイッチを切り替えてもよい。
【0061】
図5は、図9と同様に、ウェル3を用いた場合における反応溶液中から発生した蛍光の拡散状態を示す図である。ここで、光源5から蛍光発生中心29までの距離をLとする。光源5から光を反応溶液に照射すると、反応溶液から発生する蛍光は、蛍光発生中心29から全方向に略均一に拡散する(図中矢印E)。
【0062】
蛍光発生中心29から発生した蛍光は、半径Lの球体表面である仮想受光面31の表面全体に略均一に到達する。しかしながら、光源5が受光部を兼ねる場合(図9のように従来の測定の場合)には、受光可能な蛍光は、前述したように受光部の面積に対応する部位のみとなる。
【0063】
一方、本発明では、ウェル3の内面から上方に向かって拡散する蛍光以外は、全てウェル3(内部樹脂層19)に蛍光が封じ込められる。また、前述のように、ウェル3の上面方向には反射膜17が形成されるため、ウェル3内部に封じ込められた光は全てウェル3の下部の導波路9へ出光される。
【0064】
すなわち、本発明のウェル3を用いることで、仮想受光面31において、ウェル3の開口から漏れだす光以外の光を全てウェル3内に封じ込めることができる。このため、仮想受光面31において、受光可能領域33は、ウェル3の開口部以外の全ての方向(図中ハッチングで示した領域)となる。したがって、従来と比較して、極めて効率良く発生した蛍光を測定することができる。
【0065】
次に、ウェル3の製造方法の一例を説明する。図6は、ウェルプレート35の全体(一部断面)を示す斜視図である。前述の通り、ウェルプレート35(複数のウェルが連結されたもの)は、必要に応じて連結部4で連結されて一体で形成される。ウェルプレート35としては、例えば射出成形で成形される。
【0066】
この際、ウェル部および導波路9は一体で形成されることが望ましい。なお、本発明におけるウェルは、2層構造となっているが、これは同時に射出成型してもよく、別々に成形してもよい。例えば、内部樹脂層19とコア部25とを構成する樹脂によって全体を成形後、さらに外部樹脂層23およびクラッド部27を構成する樹脂で被覆してもよい。
【0067】
また、ウェル部と導波路部を別々に成形してから接合して一体化してもよい。または、ウェル(ウェルプレート)と導波路とを別々で構成し、ウェルと導波路との間にマッチングオイルを塗り、マッチングオイルと介してウェルと導波路とを密着させてもよい。さらには、ウェルおよび導波路を縦割りして、複数に分割した状態で射出し、その後それらを接合して一体化してもよい。また、ウェル部と連結部とを別体で成形し、接着剤等で接着してウェルプレートを形成してもよい。なお、ウェルの配置数等は図示した例には限られない。
【0068】
次に、温度調整部12による反応溶液の温度調整のサイクルについて説明する。図7はPCR測定の温度サイクルを示す概念図である。前述したように、増幅サイクル39は、変性工程41、アニーリング工程43、ポリメラーゼ伸長工程45からなる。
【0069】
変性工程41は、約95℃の温度で鋳型DNAを一本鎖に分離する工程である。アニーリング工程43は、約50℃に降温し、プライマをDNAにハイブリダイズする工程である。ポリメラーゼ伸長工程45は、約70℃に昇温し、DNAポリメラーゼの酵素反応により、プライマに挟まれたDNA領域を増幅する工程である。前述したウェル3等を用いたリアルタイム蛍光測定によって、ポリメラーゼ伸長工程の進行を把握することができる。蛍光測定によってプライマに挟まれたDNA領域が2倍に増幅されたと判断されると、増幅サイクル39をさらに繰り返し、DNAの増幅を行うことができる。
【0070】
以上説明したように、本実施の形態によれば、ウェル3の周囲に温度調整部12が配置されるため、反応溶液15の温度を各工程に適した温度に調整することができる。このため、ウェル3の内部のみで増幅サイクルを連続して繰り返すことができる。また、熱電素子8を用いるため、昇温のみならず降温の制御も行うことができる。また、均熱板7を用いることで、ウェル3内の反応溶液15を均一に温度制御することができる。
【0071】
また、ウェル3が、屈折率の異なる二層構造で形成され、さらにウェル3の下部に導波路9が一体化されるため、ウェル3内部から浸入した光をウェル3に封じ込め、導波路9に導出することができる。このため、微量の蛍光であっても従来と比較して極めて感度良く検出することができる。
【0072】
また、ウェル上端面に反射膜17が設けられるため、光がウェル外に漏れ出すことを防止することができる。反射膜17は、ウェルの形状によっては、ウェル底部の曲率の大きな部分において、ウェル外周部に蛍光が外部樹脂層の外周面から漏光した場合でも、外部樹脂層の外周面に反射膜を形成することにより、光がウェル外に漏れ出すことを防止できることから、ウェル底部の曲率の設計の自由度を広げることができる。
【0073】
次に、第2の実施の形態について説明する。図8は、第2の実施の形態にかかる蛍光測定装置1aを示す概略図である。なお、以下の説明において、蛍光測定装置1と同様の機能を奏する構成については、図1〜図3等と同様の符号を付し、重複する説明を省略する。
【0074】
蛍光測定装置1aは、蛍光測定装置1と略同様の構成であるが、光源5の配置が異なる。蛍光測定装置1aでは、光源5a、5bは、導波路9の下部に配置される。
【0075】
光を発光する光源5a、5bは、アイソレータ47およびハーフミラー49を介してウェル3a、3bの下部に、光ファイバ51等によって光接続される。アイソレータ47は、光源5a、5b側からの光のみを透過し、ウェル3a、3b側から光源方向への光の通過を遮蔽するものである。
【0076】
ハーフミラー49は、光源5a、5bからの光の一部を透過して、ウェル3a、3b方向に光を伝送する。ハーフミラー49の先端部は、導波路9のコア部に光接続される。コア内部に導入された光は、導波路9a、9bおよびウェル3a、3b内に閉じ込められ、その一部が反応溶液15に照射される。すなわち、光源5a、5bからの照射光が反応溶液15に照射される。尚、戻り光によるノイズが無視できるようであれば、アイソレータ47を省略することも可能である。
【0077】
反応溶液15からの蛍光は、再びウェル3a、3bの内部樹脂層および導波路9a、9bのコア部内部に閉じ込められる。したがって、蛍光は、ハーフミラー49によって一部が反射されてフィルタ11a、11b方向へ分光される。フィルタ11a、11bでは、出射光成分が除去されて、光測定器13a、13bに蛍光のみが伝送され、光測定器13a、13bによって光が検出される。
【0078】
なお、蛍光測定装置1aでは、蓋2は透明であってもよく、または内面の全面に反射膜を形成してもよい。蓋2が透明であれば、内部の様子を外部から視認することが可能である。また、蓋2に反射膜を形成すれば、ウェルの開口部からの蛍光の散逸を防止することができる。
【0079】
また、ハーフミラーに代えて光カプラを用いてもよい。また、ハーフミラーに代えて、ある特定の波長の光のみを反射して、その他の波長を透過する波長選択型のミラー型フィルタを配置してもよい。この場合、当該ミラー型フィルタは、照射光は透過させるが、検体から発生した蛍光のみを光測定器13a、13b側に反射させることができる。なお、この場合には、光測定器13a、13bの前に別途光学フィルタを用いる必要はない。
【0080】
また、光源および光測定器は、ウェル等の下部に配置した例を図示したが、光ファイバ51等によって照射光および蛍光を導光すれば、ウェルから離れた位置で照射および蛍光測定を行うこともできる。
【0081】
以上説明したように、第2の実施の形態によれば、蛍光測定装置1と同様の効果を得ることができる。また、蓋2の内面が蒸気に水滴が付着することで、光源からの光が遮断され、光量が不安定となることがない。
【0082】
以上、添付図を参照しながら、本発明の実施の形態を説明したが、本発明の技術的範囲は、前述した実施の形態に左右されない。当業者であれば、特許請求の範囲に記載された技術的思想の範疇内において各種の変更例または修正例に想到し得ることは明らかであり、それらについても当然に本発明の技術的範囲に属するものと了解される。
【0083】
例えば、上述の実施形態では、熱サイクルによって反応溶液中でDNAの分離、抽出および増幅と、ウェル内で発生した蛍光の測定を行う方法について説明したが、本発明はこれに限られない。例えば、熱原を用いずに、細胞等の蛍光測定やそれを用いた細胞のスクリーニングにも利用することもできる。
【符号の説明】
【0084】
1、1a………蛍光測定装置
2………蓋
3、3a、3b、3n………ウェル
4………連結部
5、5a、5b、5n………光源
7………均熱板
8………熱電素子
9a、9b、9n………導波路
10………冷却部
11a、11b、11n………光学フィルタ
12………温度調整部
13、13a、13b、13n………蛍光測定器
15………反応溶液
17………反射膜
19………内部樹脂層
23………外部樹脂層
25………コア部
27………クラッド部
29………蛍光発生中心
31………仮想受光面
33………受光可能領域
35………ウェルプレート
39………増幅サイクル
41………変性工程
43………アニーリング工程
45………ポリメラーゼ伸長工程
47………アイソレータ
49………ハーフミラー
51………光ファイバ
109………ウェル
111………照射・受光部
113………反応溶液
115………蛍光発生中心
117………仮想受光面
119………受光可能領域
【技術分野】
【0001】
本発明は、生体材料の反応あるいは生成あるいは、PCR(Polymerase Chain Reaction)などの蛍光測定装置およびこれらの装置を用いた蛍光測定方法に関するものである。
【背景技術】
【0002】
PCR法は、ごく微量のDNAから目的とするDNA領域を短時間で増殖する方法として知られている。その原理は、2本鎖DNA上の2つの既知配列を利用して、相互いの合成方向が向かい合うような2つのプライマDNAを設計する。これらのプライマに挟まれた領域のDNAが合成されると、それが次のサイクルでは鋳型になる。このような反応を繰り返すことで、DNA鎖を幾何級数的に増幅することができる。
【0003】
DNAを増幅するPCR装置は、例えば、反応溶液の温度を50℃台、70℃台、90℃台に3段階に変え、変性、アニーリング、ポリメラーゼ伸長の各工程を繰り返すことでDNAを増幅する。なお、3段階の温度制御を一通り行うと理論上DNA量は2倍となる。
【0004】
このような、PCR装置において、DNAの増幅の進行を把握する手段としては、DNAの増幅に応じて発生する、または消滅する蛍光を測定する方法がある。例えば、ヘアピンプライマPCR法では、ヘアピン領域に低分子が特異的に結合するシトシンバルジ領域が導入され、DNA鎖の合成が進行し、PCRによりヘアピンプライマのヘアピン構造が開かれると、シトシンバルジ構造が消失する。このため蛍光色素が遊離して、蛍光強度が低下する。
【0005】
また、例えばTaq Man PCR法では、蛍光基と消光基で標識されたオリゴマーを用い、DNAの増幅に伴って消光基が消滅することで、DNA鎖の合成が進行によって蛍光強度が増加するものである。すなわち、いずれの場合においても、反応系の蛍光を検出することで、PCRの進行を把握することができる。
【0006】
このような、リアルタイムPCRに関しては、例えば、伸長性の優れたDNAポリメラーゼをPCRに用いることにより、より短時間で遺伝子を検出することが可能な遺伝子の増幅方法が開示されている(特許文献1)。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2010−239880号公報
【発明の概要】
【発明が解決しようとする課題】
【0008】
図9は、このようなリアルタイムPCRによって、蛍光を測定するためのウェル近傍を示す概略図である。まず、図9(a)に示すように、ウェル109内に各種の構成を含む反応溶液113が入れられる。この状態で、上方より照射・受光部111より光を照射する(図中矢印I方向)。照射・受光部111は、例えば光ファイバであり、図示を省略した光源および蛍光測定器に接続されている。
【0009】
光が照射された反応溶液からは、PCRの進行に応じた蛍光が発生(消失)する。図9(b)は、仮に蛍光発生中心115を蛍光の発生する中心であるとした場合に、蛍光の発生する状態を示す模式図である。蛍光発生中心115から発生する蛍光は、蛍光発生中心115を中心に全方向に(蛍光発生中心115を中心とする球体を仮定した場合の球面方向に対して)略均一に発生する(図中矢印J方向)。
【0010】
この際、例えば照射・受光部111の受光面と蛍光発生中心115との距離をLとすると、仮想受光面117(半径Lの球体の表面積)は、4πL2で表わされる。すなわち、ウェル109での反射等を無視すれば、反応溶液から発生した蛍光は、4πL2の表面積を有する仮想受光面117の表面全体に均一に到達する。
【0011】
ここで、照射・受光部111の受光面の面積をaとすれば、実際に発生した蛍光の内、受光できる蛍光の量は、全体の4πL2の面積の内、面積aの受光可能領域119(図中におけるハッチング部)のみとなる。すなわち、それ以外の方向に進んだ蛍光は、受光されることなく散逸する。
【0012】
ここで、照射・受光部111の径を5mmΦとし、距離Lを10mmとする。すると、仮想受光面117の全表面積(4×π×102)は、1257mm2程度となる。また、受光面の面積は(π×2.52)は、約20mm2程度となる。したがって、発生した蛍光に対して、20/1257=約1.6%程度となる。
【0013】
このように、従来の蛍光測定装置においては、実際に生じた蛍光のほとんどが外部に漏れ出しており、発生した蛍光の内、わずかしか受光することができない。すなわち、蛍光を受光する効率が極めて悪い。したがって、例えば、医療分野において、被検査サンプル中の抗原(例えばウィルス)量が十分でないと検出精度を確保することが困難である。
【0014】
特に、通常は多数のウェル内の蛍光を同時または順次に測定するため、複数のウェルプレート又は測定器が移動して測定を行う。この際、図9に示すように、測定距離が大きくなるほどに蛍光量は減衰するので、その感度は低下する。また隣のウェルの蛍光量の影響を受け易くなる。したがって、個々のウェル内の蛍光を高感度に測定することは困難である。また、特殊な試薬を用いて感度を得る方法もあるが、このような方法では反応溶液自体が高価であるため、より安価かつ高感度に測定可能な方法が望まれている。
【0015】
本発明は、このような問題に鑑みてなされたもので、DNAの増幅等において、極めて高い感度で蛍光をリアルタイムで測定可能な蛍光測定装置等を提供することを目的とする。
【課題を解決するための手段】
【0016】
前述した目的を達するために第1の発明は、蛍光測定装置であって、反応溶液を保持するウェルと前記ウェルの外周部に配置され、反応溶液の温度を調整可能な温度調整部と前記ウェルの下方に設けられる導波路と前記ウェル内で発生する蛍光を測定する蛍光測定器とを具備し、前記ウェルは、少なくとも外部樹脂層と内部樹脂層の二層構造であり、前記内部樹脂層の屈折率は前記外部樹脂層の屈折率よりも大きく、前記導波路は内部に前記内部樹脂層と同一の材質からなるコア部と外部に前記外部樹脂層と同一の材質からなるクラッド部を有して、前記ウェルと一体で構成されるとともに、複数の前記ウェルが連結されてウェルプレートを形成し、前記温度調整部によって前記反応溶液の温度を調整することで反応溶液中で生体材料の反応あるいは生成を行うことができ、前記ウェル内で発生した蛍光を前記内部樹脂層に封じ込めて前記コア部に導出して前記蛍光測定器によって測定可能であることを特徴とする蛍光測定装置である。
【0017】
前記温度調整部は、前記均熱板と前記均熱板の下部に設けられる熱電素子と前記熱電素子の下部に配置される冷却部とを具備し、前記ウェルおよび前記導波路が前記温度調整部を貫通して設けられることが望ましい。
【0018】
前記ウェルの上端面には、反射膜が形成されてもよい。前記導波路の端部には光源が設けられ、前記光源は、前記導波路を介して前記ウェル内の前記反応溶液に光を照射し、前記蛍光測定器は、前記導波路からの蛍光を光フィルタを介して測定可能であってもよい。
【0019】
前記ウェルを構成する樹脂は、内部樹脂層としては、たとえば、耐熱性を有するポリカーボネート樹脂、変性ポリカーボネート樹脂、ポリアミド、高Tg成分モノマーとのアクリル系重合体、ノルボルネン系樹脂、シリコーン樹脂、架橋アクリル樹脂などを用いることができ、また、外部樹脂層には、一般的には耐熱性が高く、内部樹脂層よりも低屈折率のポリカーボネート樹脂、シリコーン樹脂、フッ素系樹脂やポリアミドを用いることができる。
【0020】
第1の発明によれば、ウェルの周囲に温調可能な温度調整部が設けられるため、DNAの分離、抽出、増幅などの生体材料の反応あるいは生成および蛍光の測定を連続して行うことができる。
【0021】
また、ウェルが二層構造で構成され、内部樹脂層の屈折率を外部樹脂層の屈折率よりも大きくすることで、ウェル内に入れられた反応溶液中からの蛍光をウェルの内部樹脂層に封じ込めることができる。また、内部樹脂層がウェルの下部で導波路に接続されるため、蛍光を導波路に導入することができる。したがって、導波路に接続された蛍光測定器で蛍光を効率良く測定することができる。
【0022】
また、ウェル内で生じる蛍光を直接導波路に導出することで、従来の方法と比較して、外部に散逸する蛍光成分を抑えることができる。このため、極めて高い感度で蛍光を測定することができる。
【0023】
また、ウェルの上端面に反射膜を形成することで、内部樹脂層内の蛍光がウェルの上端面から漏れてしまうことがない。
【0024】
また、温度調整部が、均熱板、熱電素子および冷却部から構成され、ウェルおよび導波路が温度調整部を貫通して設けられれば、ウェル内の反応溶液の温度を迅速に調整することができる。また、温度調整部に設けられたウェルは、温度調整部に形成された貫通孔に配置されるため、測定後は容易に温度調整部から使用済みのウェルを取り外し、交換が可能である。このため、取り扱い性に優れる。
【0025】
なお、熱電素子としては、例えばペルチェ素子を用いることが望ましい。ペルチェ素子への電圧負荷方向を制御することで、昇温および降温の制御を行うことができる。したがって、ウェル内の反応溶液を迅速に規定の温度に調整することができる。
【0026】
また、ウェルを構成する樹脂として、内部樹脂層の樹脂としては、ポリカーボネート(耐熱温度125−135℃)、変性ポリカーボネート(耐熱温度145℃)、高Tg成分モノマーとのアクリル系重合体、ノルボルネン系樹脂(耐熱温度150℃)、シリコーン樹脂(150−170℃)、架橋アクリル樹脂(耐熱温度175℃)から選択することで、PCRにおける熱でウェルが損傷することがない。また、内部樹脂層の樹脂にPMMAを用いても、外部樹脂層にα―フルオロアクリレート系樹脂を用いたプラスチック光ファイバを用いれば、耐熱性を向上させることができる。
【0027】
尚、本装置を加熱の必要がない試験に用いる場合には、内部樹脂層の樹脂として、最も一般的に使用されているPMMA、ポリスチレンなどを用いた汎用プラスチックファイバを用いることもできる。
【0028】
上述の内部樹脂層の樹脂としては、外部樹脂層の樹脂より、屈折率が高く、導波路のコア材との相溶性あるいは親和性に優れ、さらに耐熱性に優れる樹脂ならば、いかなる樹脂をも用いることができる。
【0029】
第2の発明は、蛍光測定用の反応溶液を保持する蛍光測定用ウェルであって、前記反応溶液の保持部は、少なくとも外部樹脂層と内部樹脂層の二層構造であり、前記内部樹脂層の屈折率は、前記外部樹脂層の屈折率よりも大きく、前記保持部の下方に前記保持部と一体で形成される導波路は、内部に前記内部樹脂層と同一の材質からなるコア部と、外部に前記外部樹脂層と同一の材質からなるクラッド部を有し、複数の前記保持部が連結されて構成されることを特徴とする蛍光測定用ウェルである。
【0030】
第2の発明によれば、高感度な測定が可能なウェルを容易に得ることができる。
【0031】
第3の発明は、蛍光測定方法であって、第1の発明にかかる蛍光測定装置の温度調整部を制御して、前記ウェル内に保持された反応溶液の温度を調整することで、反応溶液中の蛍光色素で標識した生体材料の反応あるいは生成の進行を、前記反応溶液からの蛍光を連続して前記光測定器で測定することを特徴とする蛍光測定方法である。
【0032】
また、第1の発明にかかる蛍光測定装置の温度調整部を制御して、前記ウェル内に保持された反応溶液を昇温して、鋳型DNAを一本鎖に分離する変性工程と、前記変性工程から降温し、プライマをDNAにハイブリダイズするアニーリング工程と、前記アニーリング工程から昇温し、DNAポリメラーゼの酵素反応により、プライマに挟まれたDNA領域を増幅するポリメラーゼ伸長工程と、前記ポリメラーゼ伸長工程から降温し、DNA領域の増幅の進行を前記光測定器で測定する蛍光測定工程と、を具備することを特徴とする蛍光測定方法である。
【0033】
また、前記反応溶液中の蛍光を前記光測定器により測定後、測定を終了した反応溶液を保持するウェルプレートを前記温度調整部より取り外し、新たな測定対象である反応溶液を保持するウェルプレートに交換した後、蛍光測定を繰り返すこともできる。
【0034】
第3の発明によれば、ウエル内に保持された反応溶液の温度を調整することで、反応溶液中の蛍光色素で標識した生体材料の反応あるいは生成を、前記反応溶液からの蛍光を連続して前記光測定器で測定することができ、さらには、DNAの分離、抽出、増幅を同一ウェル内で行うことが可能であるとともに、DNA増幅工程に対して連続してDNA増幅の進行を把握するための蛍光測定を行うことができる。
【発明の効果】
【0035】
本発明によれば、DNAの増幅等において、極めて高い感度で蛍光をリアルタイムで測定可能な蛍光測定装置等を提供することができる。
【図面の簡単な説明】
【0036】
【図1】蛍光測定装置1を示す概略図。
【図2】ウェル3の拡大図。
【図3】ウェル3および導波路9の屈折率の分布図であり、(a)は図2のC−C線断面における分布図、(b)は図2のD−D線断面における分布図。
【図4】ウェルの断面拡大図であり、(a)は図2のA部拡大図、(b)は図2のB部拡大図。
【図5】ウェルで受光可能な領域を示す概念図。
【図6】ウェル3の全体斜視図。
【図7】PCR測定の温度サイクルを示す概念図。
【図8】他の実施形態を示す図で、蛍光測定装置1aを示す概略図。
【図9】従来の受光領域を示す概念図。
【発明を実施するための形態】
【0037】
以下、図面を参照しながら、本発明の実施形態について説明する。図1は、蛍光測定装置1を示す概略図である。蛍光測定装置1は主に、複数のウェル3a、3b、・・・、3nと、複数の光源5a、5b、・・・、5nと、導波路9a、9b、・・・、9nと、光学フィルタ11a、11b、・・・、11nと、蛍光測定器13a、13b、・・・、13nおよび各ウェルの温度調整を行う温度調整部12等から構成される。なお、簡単のため、図ではウェルは3つのみ示すが、例えば、一つのプレート上には例えば4列×6段=24個のウェルが配置される。
【0038】
ウェル3a、3b、・・・、3n(以下、総称してウェル3とする)は、内部に反応溶液15を保持可能である。ウェル3は、反応溶液を保持する部位の高さが約10mmであり、外径が約8〜10φ(内径約6〜8φ)程度である。また、ウェル3の下部にはそれぞれ導波路9a、9b、・・・、9n(以下、総称して導波路9とする)が一体で形成される。
【0039】
各ウェル3は、上部において連結部4で連結される。すなわち、各ウェル3は所定の間隔で一体に形成される。なお、本発明では、個々のウェルを分離して構成してもよく、図示したように、複数のウェルを一体で形成してもよい。以下の説明においては、複数のウェルが連結されたものウェルプレートと称する。
【0040】
図2(a)は、ウェル3の拡大図である。また、図3はウェルを含む屈折率の分布図であり、図3(a)は図2のC−C線断面における分布図、図3(b)は図2のD−D線断面における分布図である。また、図4(a)は、図2のA部拡大図、図4(b)は図2のB部拡大図である。ウェル3は、反応溶液と接する側から、内部樹脂層19および外部樹脂層23の二層構造で構成される。ここで、図3(a)、図3(b)に示すように、内部樹脂層19の屈折率は、外部樹脂層23よりも高い。
【0041】
図3(a)のLは反応溶液15の領域の屈折率である。また、図3(a)、図3(b)のMは内部樹脂層19の屈折率であり、Nは外部樹脂層23の屈折率である。なお、Nの両側は空気層であり、屈折率は1.0である。反応溶液15の屈折率は、使用する溶液による。内部樹脂層19の屈折率は、例えば1.50〜1.70程度であり、外部樹脂層23の屈折率は、例えば、1.48以下程度である。すなわち、内部樹脂層19の内部に光を封じ込めることが可能である。
【0042】
なお、ウェル3は、例えば、内部樹脂層は、耐熱性を有するポリカーボネート樹脂、変性ポリカーボネート樹脂、ポリアミド、高Tg成分モノマーとのアクリル系重合体、ノルボルネン系樹脂、シリコーン樹脂、架橋アクリル樹脂等の例えば110℃以上(さらに望ましくは120℃以上)の耐熱性を有する樹脂中から、反応溶液等に対する耐薬品性を考慮して選定した材質で構成する。外部樹脂層には、一般的にはフッ素系樹脂やポリアミドを用いる。また、屈折率の調整は、各層を構成する樹脂材質を変更することにより行ってもよく、または、同材質の母材に適宜添加剤を添加してもよい。
【0043】
また、ウェル3を構成する材料としては、樹脂材料よりも耐熱性に優れるガラスを用いてもよい。このようなガラスとしては、例えば、300から400℃で成形可能な、SiO2あるいはNa2Oを含有する多成分ガラスを用いることができる。
【0044】
また、図4(b)に示すように、導波路9は、中央部にコア部25が設けられ、コア部25を覆うように外周部にクラッド部27が設けられる。コア部25を構成する樹脂の屈折率は、クラッド部27を構成する樹脂の屈折率よりも高い。例えば、コア部25は内部樹脂層19と同一の材質で構成されることが望ましいが、内部樹脂層の樹脂と、コア部を構成する樹脂は、互いに相溶性を有し、互いの屈折率が同一または近似するものを用いてもよい。同様に、クラッド部27は外部樹脂層23と同一の材質で構成されることが望ましいが、外部樹脂層の樹脂と、クラッド部を構成する樹脂は、互いに相溶性を有し、互いの屈折率が同一または近似するものを用いてもよい。ここで、コア部と内部樹脂層の屈折率は、同一または近時する必要があるが、両者を比べた場合に、コア部の屈折率が内部樹脂層の屈折率より大きければ良い。ここで、互いの屈折率が近似するとは、例えば、屈折率の違いが0.1程度以下であり、さらに好ましくは0.05以下であることが望ましい。なお、導波路9としてはプラスチックファイバを用いてもよい。
【0045】
ウェル3と導波路9との接合部では、内部樹脂層19とコア部25とが一体で形成される。また、外部樹脂層23とクラッド部27とが一体で形成される。したがって、内部樹脂層19内に封じ込められた光は、コア部25に導出され、コア部25内を伝播する。
【0046】
また、図1に示すように、ウェル3の上方には光源5a、5b、・・・、5n(以下、総称して光源5とする)がそれぞれ配置される。光源5は、それぞれのウェル3内の反応溶液に所定の波長の光を照射する。光源5としては、レーザやLED等を用いることができる。
【0047】
ウェル3の上端面には、反射膜17が設けられる。反射膜17は、ウェル3(内部樹脂層19)内の光が、ウェル3の上端から漏れだすことを防止するものである。反射膜17としては、酸化ケイ素、酸化チタン、酸化ニオブなどの物質を蒸着などによって形成すればよく、また、反射膜成分を塗布してもよい。反射膜17の形成方法は問わない。
【0048】
ウェル3の上面には、蓋2が設けられる。蓋2は、例えば透明なガラス板または樹脂板である。したがって、前述の光源5からの光を透過する。蓋2は、反応溶液の昇温時に、反応溶液の蒸発を防止し、隣接する各ウェルの反応溶液が蒸気によって混入しあうことを防止するものである。
【0049】
ウェル3の外周部には、温度調整部12が設けられる。温度調整部12は、均熱板7、熱電素子8、冷却部10から構成される。均熱板7、熱電素子、冷却部10は例えば一体で構成される。温度調整部12は、図示を省略した制御部に接続されており、ウェル3内部の反応溶液15の温度調整が可能である。
【0050】
均熱板7は例えばアルミニウム板や銅板等の金属板である。均熱板7は下部に設けられる熱電素子8の熱を均一に分散させるものである。均熱板7としては、6mm程度の厚みであり、例えば、ウェルの高さ程度に設定すればよい。
【0051】
熱電素子8は、均熱板7の下部に接合される。熱電素子8は、例えばペルチェ素子である。熱電素子8に対して電圧を付与することで、熱電素子8を昇温または降温することができる。熱電素子8(層)の厚みは、例えば1.5〜2mm程度とすればよい。
【0052】
熱電素子8の下部には冷却部10が設けられる。冷却部10は、熱電素子8自体を冷却するものである。冷却部10としては、例えばアルミニウム製のフィン材等を用い、また、図示を省略したファンによって空冷することができる。冷却部10としては、例えば10〜20mm程度とすればよい。
【0053】
温度調整部12は、熱電素子8、および冷却部10の動作を制御することで、ウェル3内部の反応溶液15の温度を迅速に制御することができる。なお、温度サイクルについては後述する。
【0054】
均熱板7、熱電素子8、冷却部10からなる温度調整部12には、貫通孔が形成される。貫通孔には、ウェル3および導波路9が挿入される。なお、導波路9の挿入性を高めるために、貫通孔にあらかじめパイプを配置してもよい。貫通孔にウェル3および導波路9を挿入することで、温度調整部12とウェル3を接触させることができる。
【0055】
なお、本発明では、ウェル3および導波路9を温度調整部12から取り外すことで、ウェルの交換を容易に行うことができる。すなわち、ウェル3自体を使い捨てとし、温度調整部12を繰り返し使用することで、常に新たなウェルを使用することができ、交換作業性にも優れる。
【0056】
また、貫通孔の加工性および反応溶液の温度を均一にするため、均熱板7の位置にウェル3の外径変化部を配置することが望ましい。均熱板7は金属板であり、比較的加工が容易であるため、ウェルの外径に応じた複雑な形状にも容易に対応が可能であるが、熱電素子8はその加工性や設計の自由度が低いため、熱電素子8における貫通孔は、導波路9のように径が変化しない部位とすることが望ましい。
【0057】
導波路9には、それぞれ光学フィルタ11a、11b、・・・、11n(以下、総称して光学フィルタ11とする)が接続され、さらに光学フィルタ11を介して蛍光測定器13a、13b、・・・、13n(以下、総称して蛍光測定器13とする)と接続される。光学フィルタ11は、反応溶液15内で発生する蛍光成分以外の光(例えば照射光成分)を除去するものである。光学フィルタ11を通過した蛍光は、各蛍光測定器13で測定される。
【0058】
すなわち、ウェル3内部の反応溶液15では、温度調整部12による温度調整によって、DNAの増幅が行われる。この際観察される蛍光成分はウェル3内部の内部樹脂層19内に封じ込められる。内部樹脂層19内の蛍光は、導波路9に導出されて光学フィルタ11を介して光測定器13で測定される。以上により、蛍光の増減をリアルタイムで監視することができる。
【0059】
なお、蛍光測定器は、各ウェル毎に配置してもよいが、ウェル3または蛍光測定器13を相対的に移動させることで、一つの蛍光測定器によって複数のウェル内の蛍光を測定してもよい。
【0060】
例えば、ウェルが複数列×複数段に配置されている場合に、ウェルの列の数だけ蛍光測定器13を設けて、各列の蛍光を測定する。次に、当該列に垂直な方向に順次ウェル(または蛍光測定器)を相対的に移動させ、次の段における各列の蛍光を測定する。以上を繰り返すことで、各列のウェルを各段ごとに順次測定することができる。なお、光スイッチ等を用いて、ウェルと蛍光測定器とを光接続し、光スイッチを切り替えてもよい。
【0061】
図5は、図9と同様に、ウェル3を用いた場合における反応溶液中から発生した蛍光の拡散状態を示す図である。ここで、光源5から蛍光発生中心29までの距離をLとする。光源5から光を反応溶液に照射すると、反応溶液から発生する蛍光は、蛍光発生中心29から全方向に略均一に拡散する(図中矢印E)。
【0062】
蛍光発生中心29から発生した蛍光は、半径Lの球体表面である仮想受光面31の表面全体に略均一に到達する。しかしながら、光源5が受光部を兼ねる場合(図9のように従来の測定の場合)には、受光可能な蛍光は、前述したように受光部の面積に対応する部位のみとなる。
【0063】
一方、本発明では、ウェル3の内面から上方に向かって拡散する蛍光以外は、全てウェル3(内部樹脂層19)に蛍光が封じ込められる。また、前述のように、ウェル3の上面方向には反射膜17が形成されるため、ウェル3内部に封じ込められた光は全てウェル3の下部の導波路9へ出光される。
【0064】
すなわち、本発明のウェル3を用いることで、仮想受光面31において、ウェル3の開口から漏れだす光以外の光を全てウェル3内に封じ込めることができる。このため、仮想受光面31において、受光可能領域33は、ウェル3の開口部以外の全ての方向(図中ハッチングで示した領域)となる。したがって、従来と比較して、極めて効率良く発生した蛍光を測定することができる。
【0065】
次に、ウェル3の製造方法の一例を説明する。図6は、ウェルプレート35の全体(一部断面)を示す斜視図である。前述の通り、ウェルプレート35(複数のウェルが連結されたもの)は、必要に応じて連結部4で連結されて一体で形成される。ウェルプレート35としては、例えば射出成形で成形される。
【0066】
この際、ウェル部および導波路9は一体で形成されることが望ましい。なお、本発明におけるウェルは、2層構造となっているが、これは同時に射出成型してもよく、別々に成形してもよい。例えば、内部樹脂層19とコア部25とを構成する樹脂によって全体を成形後、さらに外部樹脂層23およびクラッド部27を構成する樹脂で被覆してもよい。
【0067】
また、ウェル部と導波路部を別々に成形してから接合して一体化してもよい。または、ウェル(ウェルプレート)と導波路とを別々で構成し、ウェルと導波路との間にマッチングオイルを塗り、マッチングオイルと介してウェルと導波路とを密着させてもよい。さらには、ウェルおよび導波路を縦割りして、複数に分割した状態で射出し、その後それらを接合して一体化してもよい。また、ウェル部と連結部とを別体で成形し、接着剤等で接着してウェルプレートを形成してもよい。なお、ウェルの配置数等は図示した例には限られない。
【0068】
次に、温度調整部12による反応溶液の温度調整のサイクルについて説明する。図7はPCR測定の温度サイクルを示す概念図である。前述したように、増幅サイクル39は、変性工程41、アニーリング工程43、ポリメラーゼ伸長工程45からなる。
【0069】
変性工程41は、約95℃の温度で鋳型DNAを一本鎖に分離する工程である。アニーリング工程43は、約50℃に降温し、プライマをDNAにハイブリダイズする工程である。ポリメラーゼ伸長工程45は、約70℃に昇温し、DNAポリメラーゼの酵素反応により、プライマに挟まれたDNA領域を増幅する工程である。前述したウェル3等を用いたリアルタイム蛍光測定によって、ポリメラーゼ伸長工程の進行を把握することができる。蛍光測定によってプライマに挟まれたDNA領域が2倍に増幅されたと判断されると、増幅サイクル39をさらに繰り返し、DNAの増幅を行うことができる。
【0070】
以上説明したように、本実施の形態によれば、ウェル3の周囲に温度調整部12が配置されるため、反応溶液15の温度を各工程に適した温度に調整することができる。このため、ウェル3の内部のみで増幅サイクルを連続して繰り返すことができる。また、熱電素子8を用いるため、昇温のみならず降温の制御も行うことができる。また、均熱板7を用いることで、ウェル3内の反応溶液15を均一に温度制御することができる。
【0071】
また、ウェル3が、屈折率の異なる二層構造で形成され、さらにウェル3の下部に導波路9が一体化されるため、ウェル3内部から浸入した光をウェル3に封じ込め、導波路9に導出することができる。このため、微量の蛍光であっても従来と比較して極めて感度良く検出することができる。
【0072】
また、ウェル上端面に反射膜17が設けられるため、光がウェル外に漏れ出すことを防止することができる。反射膜17は、ウェルの形状によっては、ウェル底部の曲率の大きな部分において、ウェル外周部に蛍光が外部樹脂層の外周面から漏光した場合でも、外部樹脂層の外周面に反射膜を形成することにより、光がウェル外に漏れ出すことを防止できることから、ウェル底部の曲率の設計の自由度を広げることができる。
【0073】
次に、第2の実施の形態について説明する。図8は、第2の実施の形態にかかる蛍光測定装置1aを示す概略図である。なお、以下の説明において、蛍光測定装置1と同様の機能を奏する構成については、図1〜図3等と同様の符号を付し、重複する説明を省略する。
【0074】
蛍光測定装置1aは、蛍光測定装置1と略同様の構成であるが、光源5の配置が異なる。蛍光測定装置1aでは、光源5a、5bは、導波路9の下部に配置される。
【0075】
光を発光する光源5a、5bは、アイソレータ47およびハーフミラー49を介してウェル3a、3bの下部に、光ファイバ51等によって光接続される。アイソレータ47は、光源5a、5b側からの光のみを透過し、ウェル3a、3b側から光源方向への光の通過を遮蔽するものである。
【0076】
ハーフミラー49は、光源5a、5bからの光の一部を透過して、ウェル3a、3b方向に光を伝送する。ハーフミラー49の先端部は、導波路9のコア部に光接続される。コア内部に導入された光は、導波路9a、9bおよびウェル3a、3b内に閉じ込められ、その一部が反応溶液15に照射される。すなわち、光源5a、5bからの照射光が反応溶液15に照射される。尚、戻り光によるノイズが無視できるようであれば、アイソレータ47を省略することも可能である。
【0077】
反応溶液15からの蛍光は、再びウェル3a、3bの内部樹脂層および導波路9a、9bのコア部内部に閉じ込められる。したがって、蛍光は、ハーフミラー49によって一部が反射されてフィルタ11a、11b方向へ分光される。フィルタ11a、11bでは、出射光成分が除去されて、光測定器13a、13bに蛍光のみが伝送され、光測定器13a、13bによって光が検出される。
【0078】
なお、蛍光測定装置1aでは、蓋2は透明であってもよく、または内面の全面に反射膜を形成してもよい。蓋2が透明であれば、内部の様子を外部から視認することが可能である。また、蓋2に反射膜を形成すれば、ウェルの開口部からの蛍光の散逸を防止することができる。
【0079】
また、ハーフミラーに代えて光カプラを用いてもよい。また、ハーフミラーに代えて、ある特定の波長の光のみを反射して、その他の波長を透過する波長選択型のミラー型フィルタを配置してもよい。この場合、当該ミラー型フィルタは、照射光は透過させるが、検体から発生した蛍光のみを光測定器13a、13b側に反射させることができる。なお、この場合には、光測定器13a、13bの前に別途光学フィルタを用いる必要はない。
【0080】
また、光源および光測定器は、ウェル等の下部に配置した例を図示したが、光ファイバ51等によって照射光および蛍光を導光すれば、ウェルから離れた位置で照射および蛍光測定を行うこともできる。
【0081】
以上説明したように、第2の実施の形態によれば、蛍光測定装置1と同様の効果を得ることができる。また、蓋2の内面が蒸気に水滴が付着することで、光源からの光が遮断され、光量が不安定となることがない。
【0082】
以上、添付図を参照しながら、本発明の実施の形態を説明したが、本発明の技術的範囲は、前述した実施の形態に左右されない。当業者であれば、特許請求の範囲に記載された技術的思想の範疇内において各種の変更例または修正例に想到し得ることは明らかであり、それらについても当然に本発明の技術的範囲に属するものと了解される。
【0083】
例えば、上述の実施形態では、熱サイクルによって反応溶液中でDNAの分離、抽出および増幅と、ウェル内で発生した蛍光の測定を行う方法について説明したが、本発明はこれに限られない。例えば、熱原を用いずに、細胞等の蛍光測定やそれを用いた細胞のスクリーニングにも利用することもできる。
【符号の説明】
【0084】
1、1a………蛍光測定装置
2………蓋
3、3a、3b、3n………ウェル
4………連結部
5、5a、5b、5n………光源
7………均熱板
8………熱電素子
9a、9b、9n………導波路
10………冷却部
11a、11b、11n………光学フィルタ
12………温度調整部
13、13a、13b、13n………蛍光測定器
15………反応溶液
17………反射膜
19………内部樹脂層
23………外部樹脂層
25………コア部
27………クラッド部
29………蛍光発生中心
31………仮想受光面
33………受光可能領域
35………ウェルプレート
39………増幅サイクル
41………変性工程
43………アニーリング工程
45………ポリメラーゼ伸長工程
47………アイソレータ
49………ハーフミラー
51………光ファイバ
109………ウェル
111………照射・受光部
113………反応溶液
115………蛍光発生中心
117………仮想受光面
119………受光可能領域
【特許請求の範囲】
【請求項1】
蛍光測定装置であって、
反応溶液を保持するウェルと、
前記ウェルの外周部に配置され、反応溶液の温度を調整可能な温度調整部と、
前記ウェルの下方に設けられる導波路と、
前記ウェル内で発生する蛍光を測定する蛍光測定器と、を具備し、
前記ウェルは、少なくとも外部樹脂層と、内部樹脂層の二層構造であり、
前記内部樹脂層の屈折率は、前記外部樹脂層の屈折率よりも大きく、
前記導波路は、内部に前記内部樹脂層と同一の材質からなるコア部と、外部に前記外部樹脂層と同一の材質からなるクラッド部を有して、前記ウェルと一体で構成されるとともに、複数の前記ウェルが連結されてウェルプレートを形成し、
前記温度調整部によって前記反応溶液の温度を調整することで、反応溶液中で生体材料の反応あるいは生成を行うことができ、前記ウェル内で発生した蛍光を、前記内部樹脂層に封じ込めて前記コア部に導出して前記蛍光測定器によって測定可能であることを特徴とする蛍光測定装置。
【請求項2】
前記温度調整部は、
均熱板と、
前記均熱板の下部に設けられる熱電素子と、
前記熱電素子の下部に配置される冷却部と、を具備し、
前記ウェルおよび前記導波路が前記温度調整部を貫通して設けられることを特徴とする請求項1記載の蛍光測定装置。
【請求項3】
前記ウェルの上端面又は外部樹脂層の外周面の少なくともいずれかには、反射膜が形成されることを特徴とする請求項1または請求項2に記載の蛍光測定装置。
【請求項4】
前記導波路の端部には光源が設けられ、
前記光源は、前記導波路を介して前記ウェル内の前記反応溶液に光を照射し、
前記蛍光測定器は、前記導波路からの蛍光を光フィルタを介して測定可能であることを特徴とする請求項1から請求項3のいずれかに記載の蛍光測定装置。
【請求項5】
前記ウェルのコアを構成する樹脂は、ポリカーボネート、変性ポリカーボネート、高Tg成分モノマーとのアクリル系重合体、ノルボルネン系樹脂、シリコーン樹脂のいずれかであることを特徴とする請求項1から請求項4のいずれかに記載の蛍光測定装置。
【請求項6】
蛍光測定用の反応溶液を保持する蛍光測定用ウェルであって、
前記反応溶液の保持部は、少なくとも外部樹脂層と内部樹脂層の二層構造であり、
前記内部樹脂層の屈折率は、前記外部樹脂層の屈折率よりも大きく、
前記保持部の下方に前記保持部と一体で形成される導波路は、内部に前記内部樹脂層と同一の材質からなるコア部と、外部に前記外部樹脂層と同一の材質からなるクラッド部を有し、
複数の前記保持部が連結されて構成されることを特徴とする蛍光測定用ウェル。
【請求項7】
請求項1に記載の蛍光測定装置の温度調整部を制御して、前記ウェル内に保持された反応溶液の温度を調整することで、反応溶液中の蛍光色素で標識した生体材料の反応あるいは生成の進行を、前記反応溶液からの蛍光を連続して前記光測定器で測定することを特徴とする蛍光測定方法。
【請求項8】
請求項1に記載の蛍光測定装置の温度調整部を制御して、前記ウェル内に保持された反応溶液を昇温して、鋳型DNAを一本鎖に分離する変性工程と、前記変性工程から降温し、プライマをDNAにハイブリダイズするアニーリング工程と、前記アニーリング工程から昇温し、DNAポリメラーゼの酵素反応により、プライマに挟まれたDNA領域を増幅するポリメラーゼ伸長工程と、前記ポリメラーゼ伸長工程から降温し、DNA領域の増幅の進行を前記光測定器で測定する蛍光測定工程と、を具備することを特徴とする蛍光測定方法。
【請求項9】
前記反応溶液中の蛍光を前記光測定器により測定後、測定を終了した反応溶液を保持するウェルプレートを前記温度調整部より取り外し、新たな測定対象である反応溶液を保持するウェルプレートに交換した後、蛍光測定を繰り返すことを特徴とする請求項7または請求項8記載の蛍光測定方法。
【請求項1】
蛍光測定装置であって、
反応溶液を保持するウェルと、
前記ウェルの外周部に配置され、反応溶液の温度を調整可能な温度調整部と、
前記ウェルの下方に設けられる導波路と、
前記ウェル内で発生する蛍光を測定する蛍光測定器と、を具備し、
前記ウェルは、少なくとも外部樹脂層と、内部樹脂層の二層構造であり、
前記内部樹脂層の屈折率は、前記外部樹脂層の屈折率よりも大きく、
前記導波路は、内部に前記内部樹脂層と同一の材質からなるコア部と、外部に前記外部樹脂層と同一の材質からなるクラッド部を有して、前記ウェルと一体で構成されるとともに、複数の前記ウェルが連結されてウェルプレートを形成し、
前記温度調整部によって前記反応溶液の温度を調整することで、反応溶液中で生体材料の反応あるいは生成を行うことができ、前記ウェル内で発生した蛍光を、前記内部樹脂層に封じ込めて前記コア部に導出して前記蛍光測定器によって測定可能であることを特徴とする蛍光測定装置。
【請求項2】
前記温度調整部は、
均熱板と、
前記均熱板の下部に設けられる熱電素子と、
前記熱電素子の下部に配置される冷却部と、を具備し、
前記ウェルおよび前記導波路が前記温度調整部を貫通して設けられることを特徴とする請求項1記載の蛍光測定装置。
【請求項3】
前記ウェルの上端面又は外部樹脂層の外周面の少なくともいずれかには、反射膜が形成されることを特徴とする請求項1または請求項2に記載の蛍光測定装置。
【請求項4】
前記導波路の端部には光源が設けられ、
前記光源は、前記導波路を介して前記ウェル内の前記反応溶液に光を照射し、
前記蛍光測定器は、前記導波路からの蛍光を光フィルタを介して測定可能であることを特徴とする請求項1から請求項3のいずれかに記載の蛍光測定装置。
【請求項5】
前記ウェルのコアを構成する樹脂は、ポリカーボネート、変性ポリカーボネート、高Tg成分モノマーとのアクリル系重合体、ノルボルネン系樹脂、シリコーン樹脂のいずれかであることを特徴とする請求項1から請求項4のいずれかに記載の蛍光測定装置。
【請求項6】
蛍光測定用の反応溶液を保持する蛍光測定用ウェルであって、
前記反応溶液の保持部は、少なくとも外部樹脂層と内部樹脂層の二層構造であり、
前記内部樹脂層の屈折率は、前記外部樹脂層の屈折率よりも大きく、
前記保持部の下方に前記保持部と一体で形成される導波路は、内部に前記内部樹脂層と同一の材質からなるコア部と、外部に前記外部樹脂層と同一の材質からなるクラッド部を有し、
複数の前記保持部が連結されて構成されることを特徴とする蛍光測定用ウェル。
【請求項7】
請求項1に記載の蛍光測定装置の温度調整部を制御して、前記ウェル内に保持された反応溶液の温度を調整することで、反応溶液中の蛍光色素で標識した生体材料の反応あるいは生成の進行を、前記反応溶液からの蛍光を連続して前記光測定器で測定することを特徴とする蛍光測定方法。
【請求項8】
請求項1に記載の蛍光測定装置の温度調整部を制御して、前記ウェル内に保持された反応溶液を昇温して、鋳型DNAを一本鎖に分離する変性工程と、前記変性工程から降温し、プライマをDNAにハイブリダイズするアニーリング工程と、前記アニーリング工程から昇温し、DNAポリメラーゼの酵素反応により、プライマに挟まれたDNA領域を増幅するポリメラーゼ伸長工程と、前記ポリメラーゼ伸長工程から降温し、DNA領域の増幅の進行を前記光測定器で測定する蛍光測定工程と、を具備することを特徴とする蛍光測定方法。
【請求項9】
前記反応溶液中の蛍光を前記光測定器により測定後、測定を終了した反応溶液を保持するウェルプレートを前記温度調整部より取り外し、新たな測定対象である反応溶液を保持するウェルプレートに交換した後、蛍光測定を繰り返すことを特徴とする請求項7または請求項8記載の蛍光測定方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2013−53911(P2013−53911A)
【公開日】平成25年3月21日(2013.3.21)
【国際特許分類】
【出願番号】特願2011−191892(P2011−191892)
【出願日】平成23年9月2日(2011.9.2)
【出願人】(509133768)株式会社古河電工アドバンストエンジニアリング (7)
【出願人】(000005290)古河電気工業株式会社 (4,457)
【Fターム(参考)】
【公開日】平成25年3月21日(2013.3.21)
【国際特許分類】
【出願日】平成23年9月2日(2011.9.2)
【出願人】(509133768)株式会社古河電工アドバンストエンジニアリング (7)
【出願人】(000005290)古河電気工業株式会社 (4,457)
【Fターム(参考)】
[ Back to top ]

