蛍光特性のあるカルサイト結晶およびその製造方法
【課題】結晶は広い範囲の波長によって励起され、広い範囲の蛍光波長を放出ことができる、容易に製造することが可能な炭酸カルシウム質蛍光体の提供。
【解決手段】新規細菌Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)を酢酸ナトリウム、塩化カルシウム、および硫酸マグネシウムを含む結晶形成溶液中でインキュベートすることにより、細胞外に、260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる、カルサイト型構造を有する炭酸カルシウム質蛍光体が形成される。
【解決手段】新規細菌Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)を酢酸ナトリウム、塩化カルシウム、および硫酸マグネシウムを含む結晶形成溶液中でインキュベートすることにより、細胞外に、260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる、カルサイト型構造を有する炭酸カルシウム質蛍光体が形成される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、カルサイト型構造を有する炭酸カルシウム質蛍光体および細菌を用いて当該蛍光体を製造する方法に関する。
【背景技術】
【0002】
生物が生体、細胞の内外に無機鉱物結晶を作る作用をバイオミネラリゼーション(biomineralization)という。この言葉は1947年日本の真珠研究者によってはじめて使われ、一つの研究分野が誕生した。バイオミネラリゼーションは細菌などの原核生物からほ乳動物などの真核生物まで普遍的に見られる。たとえば円石藻のウロコ(ココリス)、軟体動物の貝殻、甲殻類の外骨格、魚類の耳石やウロコ、脊椎動物の骨や歯の形成、植物のプラントオパールなどがあげられる。バイオミネラリゼーションによって作られる結晶は通常大部分が無機鉱物から成るが、微量の有機物(有機基質)を含む。この有機基質がバイオミネラリゼーションを制御していると考えられてきたが、未だに不明な点が多い。バイオミネラリゼーションの研究はこれまで多方面から行われてきた。
【0003】
細菌によるバイオミネラリゼーションでは、細胞外または細胞内に無機結晶が形成されることが知られている。細胞外に結晶が形成される例として、細菌によるカルサイト(炭酸カルシウム)形成があげられる。ある種の海洋性細菌はカルサイトを形成する能力があり、この能力と海底の炭酸カルシウム堆積物との関連性が調べられている(非特許文献1)。Boquetらは多くの種類の土壌細菌が酢酸カルシウム、酵母エキス、グルコースを含む固形培地上でカルサイトを形成することを初めて報告した(非特許文献2)。Sanchez-Romanらは19種類の中等度好塩性細菌について、カルシウムとマグネシウムの割合を変化させた培地にて炭酸塩鉱物とリン酸塩鉱物形成を調査し、形成された鉱物がカルサイトやストルバイトであることを報告した(非特許文献3)。Baskarらは鍾乳石から単離された細菌が鍾乳石形成にどのような地質学的影響を及ぼすのか研究を進め、微生物活性は鍾乳石やカルサイト形成の重要な因子であることを報告した (非特許文献4)。
【0004】
細胞内に無機結晶が形成される例としては、磁性細菌の微小磁石が挙げられる。磁性細菌は細胞内にナノサイズのマグネタイト(Fe3O4)結晶あるいはグレガイト(Fe3S4)結晶を室温、中性の環境下で生成し、地磁気センサーとして利用している。その結晶型は種に特異的であり、その大きさも極めて均一であることから、生物工学分野の研究者の興味を集めている。
【0005】
しかしながら、バイオミネラリゼーションの観点から材料科学にアプローチした研究は多くはない。
【0006】
従来から知られている蛍光体のほとんどは、その製造時に高純度かつ高価な希土類酸化物を付活剤として使用している。炭酸カルシウム結晶においても、結晶形成時にユーロピウムやセリウム、テルビウムなどを付活剤として添加すると、蛍光特性をもった炭酸カルシウム結晶が得られることが知られている。たとえばユーロピウム付活バテライト型炭酸カルシウム結晶は最大励起波長330nm、最大蛍光波長620nmで赤色蛍光を発する(特許文献1)。付活剤としてセリウムとテルビウムを使用した場合、励起波長300-450nm、最大放出波長545nmの緑色蛍光を発する炭酸カルシウム結晶が得られる(特許文献2)。特許文献3ではマンガンおよびセリウムにより付活された、ブラックライト(300〜450nm)照射により赤色蛍光発光する炭酸カルシウム質蛍光体が開示されている。しかしながらこれらの蛍光体は常温にて発光強度が激しく減少するという欠点がある。またこれらの蛍光体の放出波長幅は50nmほどである。特許文献4では製造コストを低減させることを目的として、カルサイト型構造を有する炭酸カルシウム結晶にスズを固溶させて蛍光体とする技術が開示されている。しかしながらこの蛍光体もまた放出波長幅が狭いものであった。
【0007】
【特許文献1】特開2001−279241号公報
【特許文献2】特許第3985584号公報
【特許文献3】特許第3965823号公報
【特許文献4】特開平10−226786号公報
【非特許文献1】Brennan, S.T., Lowenstein, T.K., Horita, J (2004) Seawater chemistry and the advent of biocalcification. Geology 32, 473-476
【非特許文献2】Boquet E, Boronat A, Ramos-Cormenzana A (1973) Production of calcite (calcium carbonate) crystals by soil bacteria is a general phenomenon. Nature, 264, 527-529.
【非特許文献3】Sanchez-Roman M, Rivadeneyra MA, Vasconcelos C, McKenzie JA. Biomineralization of carbonate and phosphate by moderately halophilic bacteria.FEMS Microbiol Ecol. 2007 Aug;61(2):273-84.
【非特許文献4】Baskar, S., Baskar, R., Mauclaire, L. and McKenzie, J.A. (2006). Microbially induced calcite precipitation in culture experiments: Possible origin for stalactites in Sahastradhara caves, Dehradun, India, Current Science, v. 90, 58-64.
【非特許文献5】極限環境微生物とその利用 堀越弘毅、関口武司、中村聡、井上明 講談社サイエンティフィク
【非特許文献6】Fujita Y, Taylor JL, Gresham TL, Delwiche ME, Colwell FS, Mcling TL, Petzke LM, Smith RW. Stimulation of microbial urea hydrolysis in groundwater to enhance calcite precipitation. Environ Sci Technol. 2008 Apr 15;42(8):3025-32.
【非特許文献7】Bachmeier KL, Williams AE, Warmington JR, Bang SS. Urease activity in microbiologically-induced calcite precipitation. J Biotechnol. 2002 Feb 14;93(2):171-81.
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明は、結晶は広い範囲の波長によって励起され、広い範囲の蛍光波長を放出ことができる、安価かつ容易に製造することが可能な炭酸カルシウム質蛍光体を提供することを目的とする。
【課題を解決するための手段】
【0009】
本発明者らは驚くべきことに、新規細菌であるGeobacillus thermoglucosidasius NY05が、水中に炭素数1または2のカルボン酸塩、カルシウム塩、およびマグネシウム塩を含む結晶形成溶液中または該結晶形成溶液のゲル化物上においてインキュベートされたときに、広い範囲の波長によって励起され、広い範囲の蛍光波長を発する、従来にない蛍光特性を有するカルサイト型構造を有する炭酸カルシウム結晶を細胞外に形成することを見出し、本発明を完成させるに至った。
【0010】
本発明は以下の発明を包含する。
(1)
260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる、カルサイト型構造を有する炭酸カルシウム質蛍光体。
(2)
カルサイト型構造を有する炭酸カルシウム結晶にマグネシウム、ナトリウム、ケイ素、硫黄、リンおよび塩素が固溶している、(1)の蛍光体。
【0011】
(3)
Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)を、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに形成される炭酸カルシウム質蛍光体。
【0012】
(4)
前記結晶形成溶液または前記ゲル化物が、他の無機塩をさらに含む、(3)の炭酸カルシウム質蛍光体。
【0013】
(5)
Geobacillus thermoglucosidasius に属する細菌であって、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに(1)の蛍光体を形成する能力を有する細菌。
【0014】
(6)
Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)またはその変異株である、(5)の細菌。
【0015】
(7)
カルサイト型構造を有する炭酸カルシウム質蛍光体の製造方法であって、(5)または(6)の細菌を、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む結晶形成溶液中または該結晶形成溶液のゲル化物上にて、好気条件でインキュベートする工程を含む方法。
【発明の効果】
【0016】
本発明の新規Geobacillus thermoglucosidasiusにより、広い範囲の波長によって励起され、広い範囲の蛍光波長を発することが可能な、新規炭酸カルシウム蛍光体を容易に製造することができる。本発明では高価な希土類元素を使用する必要がない。
【0017】
本発明の蛍光体は発光強度の減少がほとんどなく、安定性にすぐれている。
【発明を実施するための最良の形態】
【0018】
1.細菌
本発明において結晶の形成に使用する細菌は、Geobacillus thermoglucosidasius に属する細菌であって、蒸留水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる、カルサイト型構造を有する炭酸カルシウム質蛍光体を形成する能力を有するものであれば特に限定されない。より好ましくは、Geobacillus thermoglucosidasius に属する細菌であって、蒸留水中に酢酸ナトリウム、および塩化カルシウムを含む(さらに他の無機塩を含んでもよい)、pHが5.5〜5.8に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、55〜70℃の温度にて好気条件でインキュベートしたときに、上記特徴を有する炭酸カルシウム質蛍光体を形成する能力を有する細菌である。特に好ましい細菌は、本発明者により単離された新規好熱性細菌であるGeobacillus thermoglucosidasius NY05(受託番号FERM P-21717)である。本発明では更に、G. thermoglucosidasius NY05の変異株であって、同様の結晶形成能を有するものも使用できる。ここで変異株とはG. thermoglucosidasius NY05が変異誘発処理された変異株である。変異誘発処理は任意の適当な変異原を用いて行われ得る。ここで、「変異原」なる語は、その広義において、例えば変異原効果を有する薬剤のみならずUV照射のごとき変異原効果を有する処理をも含むものと理解すべきである。適当な変異原の例としてエチルメタンスルホネート、UV照射、N−メチル−N′−ニトロ−N−ニトロソグアニジン、ブロモウラシルのようなヌクレオチド塩基類似体及びアクリジン類が挙げられるが、他の任意の効果的な変異原もまた使用され得る。このような変異株としては、例えば、16SrRNAの遺伝子の部分配列が配列番号1で表される、G. thermoglucosidasius NY05の変異株等が挙げられる。
【0019】
本発明の新規細菌は、一般的な細菌用の培地を用いて培養し増殖させることができる。培地としては、例えばトリプトソーヤ(SCD)の寒天培地または液体培地が挙げられる。実施例に示すように、G. thermoglucosidasius NY05の培養には温度としては約60℃が好適であり、pHは約7.0が好適である。
【0020】
また、本発明の新規細菌を固体及び液体で培養するときの培養容器は、一般的な微生物の培養に用いられる装置を用いることができ、特に方法を限定するものではない。例えば、小規模の培養では試験管、フラスコ、シャーレなどを用いることができ、大規模の培養にはジャーファメンター、通気攪拌できるタンクなどを使用することができる。
【0021】
2.細菌を用いた結晶(蛍光体)の形成
上記の細菌を、結晶形成溶液中または該結晶形成溶液のゲル化物上にて、好気条件でインキュベートすることにより、細菌の細胞外に、カルサイト型構造の炭酸カルシウム質蛍光体が形成される。
【0022】
結晶形成溶液は、水中に炭素数1または2のカルボン酸塩とカルシウム塩とを少なくとも含む溶液が好ましい。他の無機塩が更に含まれていることがより好ましい。
【0023】
カルボン酸塩の炭素数が3以上の場合には炭酸カルシウム結晶が形成されない。カルボン酸塩としてはギ酸ナトリウムおよび酢酸ナトリウムが好ましい。結晶形成溶液中のカルボン酸塩の濃度は12.5〜50.0 mM が好ましい。
【0024】
カルシウム塩もまた結晶形成に不可欠である。カルシウム塩としては塩化カルシウムが特に好ましい。結晶形成溶液中のカルシウム塩の濃度は5〜10 mMが好ましい。
【0025】
結晶形成溶液中には、他の無機塩がさらに添加されていることが好ましい。無機塩としては例えば銅塩、ニッケル塩、カドミウム塩、亜鉛塩、アルミニウム塩が挙げられ、マグネシウム塩が特に好ましい。結晶形成溶液中にマグネシウム塩を添加することにより結晶形成が促進される。また、マグネシウムは炭酸カルシウム結晶中に固溶する。マグネシウム塩としては硫酸マグネシウムが特に好ましい。結晶形成溶液中のマグネシウム塩の濃度は1〜5 mMが好ましい。また、その他の無機塩中の金属もまた結晶中にドープされ、結晶の蛍光特性を改変することが可能となる。特に、ニッケル塩を添加することが好ましい。ニッケル塩が0.1 mM未満の濃度で添加されたとき、結晶の形成が促進される。
【0026】
結晶形成溶液は弱酸性であることが好ましい。具体的には、pHが5.5〜5.8に調節されていることが好ましい。pHの調節は例えば酢酸により行うことができる。
【0027】
結晶形成溶液は液体として使用することもできるが、寒天等のゲル化剤を用いてゲル化して使用することがより好ましい。結晶形成溶液のゲル化物(結晶形成ゲル)上では、結晶形成速度が大幅に向上するからである。
【0028】
細菌のインキュベートは好気条件のもと行う。酸素が存在しない嫌気条件下では結晶が形成されない。
【0029】
インキュベート温度は45〜70℃の範囲が好ましく、55〜70℃の範囲がより好ましい。この範囲外の温度条件では結晶が全く形成されないか、形成速度が遅い。
【0030】
インキュベート時間は、細菌を結晶形成溶液中に懸濁させる場合には数日間以上、例えば8〜10日間であることが好ましく、細菌を結晶形成ゲル上に載せる場合には数時間以上、例えば24〜48時間であることが好ましい。
【0031】
3.結晶(蛍光体)
本発明で得られる蛍光体は、カルサイト型構造を有する炭酸カルシウムの母体結晶にマグネシウム、ナトリウム、ケイ素、硫黄、リンおよび塩素からなる群から選択される元素の少なくとも1種、好ましくは全てが固溶してなる構造を有する。結晶中の元素の量は特に限定されないが、炭酸カルシウムの母体結晶を構成する炭素、酸素、カルシウムを主成分とし、カルシウムの原子数を100(原子%)としたとき、原子数換算でマグネシウムが0〜25 (結晶形成溶液中にマグネシウム塩が含まれる場合には 15〜25)、ナトリウムが10〜15、ケイ素が4〜6、硫黄が2〜3、リンが1〜2、塩素が1〜2であることが好ましい。結晶を構成する元素は、結晶形成溶液、結晶形成ゲル、または気相中の元素に由来するか、或いは、細菌の細胞に含まれる元素(培養段階で培地等の環境から細胞中に導入された元素も含む)に由来する。
【0032】
本発明で得られる結晶は、260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる。さらに、365±5 nmの波長の光により励起されたときに青色蛍光を放出し、480±20 nmの波長の光により励起されたときに緑色蛍光を放出し、545±15 nmの波長の光により励起されたときに赤色蛍光を発することができる結晶であることが好ましい。また350 nmの光により励起されると、375〜550 nmの非常に幅広い範囲の蛍光を発することができる結晶であることが好ましい。このように幅広い波長範囲の光により励起され、幅広い波長範囲の蛍光を放出する、カルサイト型構造を有する炭酸カルシウム質蛍光体は従来存在しない。
【0033】
4.結晶の用途
本発明により得られる結晶は発光強度の減少がほとんどなく、安定性にすぐれている。したがって、インクジェット用紙用塗工材などの機能材料として応用できる可能性がある。また生化学研究における蛍光マーカー、バイオデバイス、発光ダイオード、半導体において応用できる可能性がある。本発明の細菌を用いると、金属イオンをドーピングしても結晶形成が認められる。したがってさまざまな蛍光特性を持った無機材料が得られると期待される。
【実施例】
【0034】
本発明者は好熱性細菌が細胞外無機結晶を形成することを初めて見出した。以下に、単離した好熱性細菌の生理学的性質、結晶の形成条件、結晶の組成、光学的性質、応用の可能性について述べる。
【0035】
方法および材料
好熱性細菌の単離
高温にて有機性廃棄物を効率的に有機酸に変換する微生物コンソーシアムの選抜を行った。5%の有機性廃棄物、1mg/ml塩化アンモニウム、pH8.0、60℃の条件にて、もっとも多く有機酸を産生する微生物コンソーシアムを選抜した。さらにこの微生物コンソーシアムの中から、トリプトソーヤ(SCD)寒天培地(日水製薬)を用いて好熱性細菌を純粋単離した。
【0036】
単離細菌の最適生育温度、pH
単離細菌を5ml SCD液体培地(pH7.0)に植え60℃,24時間震盪させ、前培養とした。前培養された単離細菌をSCD液体培地(pH7.0)に1/100量加え、37-80℃で24時間震盪した。その後濁度を測定することにより生育最適温度を求めた。
【0037】
pH5.0-9.0のSCD液体培地を調製した。pHは酢酸および水酸化ナトリウム水溶液にて調整した。それぞれのpHのSCD液体培地に前培養された単離細菌を1/100量加え、60℃にて24時間震盪した。その後濁度を測定することにより、生育最適pHを求めた。
【0038】
単離細菌の同定
グラム染色は常法に従った。単離細菌の形態や蛍光特性は蛍光顕微鏡Axioskop2 plus(Zeiss)にて観察された。分離菌の酸素に対する態度は、嫌気ジャー内で嫌気パックをもちいて嫌気環境をつくり、嫌気ジャー内における生育を調べることにより判断した。
【0039】
単離細菌の全DNAはDNA抽出キットISOPLANT(宝酒造)を用いて抽出し、精製した。精製された単離細菌の全DNAを鋳型にして、原核生物用プライマー5'-AGTTTGATC(A/ C)TGGCTCA-3'と5'-AAGGAGGTGATCCAGC-3'を用いて16rRNA遺伝子を増幅した。増幅されたDNAはアガロースゲル電気泳動の後、抽出され、pCRIIベクター(Invitrogen)に連結された。このプラスミドを大腸菌に導入して増幅させ、精製の後常法にしたがってrRNA遺伝子の塩基配列を決定した。
【0040】
結晶の基本的な製造法
単離細菌を5ml SCD液体培地に植え、60℃,24時間震盪させ、前培養とした。前培養液1mlをSCD液体培地100mlに加え、60℃で48時間震盪し、本培養とした。遠心により細胞を集め、酢酸にてpHを5.5-5.8に調整した25mM酢酸ナトリウム、7.0mM塩化カルシウム、2.0mM硫酸マグネシウムを含む蒸留水(結晶形成溶液)にて洗浄した。最終的には細胞をガラス製三角フラスコあるいはポリプロピレン製容器中にて500mLの結晶形成溶液に懸濁させ、60℃、100rpmにて10日間震盪させた(水溶液法aqueous solution method)。
【0041】
結晶形成溶液を1.5%(W/V)寒天(Nakalai tesque)を用いてゲル化させた(結晶形成ゲル)。SDC寒天培地に単離細菌を植え60℃、18時間インキュベートし、コロニーを形成させた。白金耳を用いてコロニーを掻き取り、結晶形成ゲル表面に乗せ、60℃で24-72時間インキュベートした(ゲル法)。
【0042】
結晶の精製
水溶液法においては、結晶は底に沈殿するか、容器の底や壁面に固着して成長する。インキュベートの後、結晶形成溶液のみを捨てさり、壁面や底に固着した結晶をスパチェラなどでかきとった。かきとられた結晶は滅菌蒸留水で数回洗浄し、エタノールで洗浄した後、60℃の下で乾燥させた。
【0043】
ゲル法においては、結晶が形成されたゲル部分を切り取り、テストチューブに移し、寒天溶解溶液(Buffer QX1, Qiagen cat. No. 20912)にてゲルを溶かした。結晶はテストチューブの底に速やかに沈殿するので、容易に溶液部分や細菌の凝集物を捨て去ることができる。チューブの底に沈殿した結晶は滅菌蒸留水で数回洗浄し、エタノールで洗浄した後、60℃の下で乾燥させた。
【0044】
蛍光顕微鏡、偏光顕微鏡
単離細菌の働きにより形成された結晶の形態は、実体顕微鏡SZX-ILLK100 (Olympus)、 光学顕微鏡BZ-9000(Keyence)、蛍光顕微鏡Axioskop2plus(Zeiss)および偏光顕微鏡Eclipse-ME600 (Nicon)にて調べられた。
【0045】
蛍光顕微鏡観察においては、励起波長として365±5、480±20、545±15nm、放出波長としてそれぞれ400以上, 535, 610±37.5nmを通すフィルターをそれぞれ使用した。
【0046】
結晶の蛍光特性
単離細菌の触媒により形成され、精製された結晶の蛍光特性は蛍光顕微鏡、蛍光分光測定装置SPEX Fluorolog-3(Horiba)にて調べられた。励起波長を変化させながら、蛍光スペクトルを測定するマトリックススキャンニングを実施した。スキャン開始励起波長は250nm、最終励起波長は400nmとした。5nm間隔の励起波長において、それぞれ310から700nmの放出波長強度を測定した。
【0047】
結晶の組成
単離細菌の触媒により形成され、精製された結晶の元素組成はエネルギー分散型X線分析装置EDX (Energy dispersive X-ray analysis) EMAX-5770(Horiba)にて調べられた。加圧電圧(管電圧)、プロープ電流はそれぞれ20.0kV 0.26nAとした。
【0048】
X線回折装置としては、リガクX線回折装置RINT-2000に銅回転対陰極とグラファイトモノクロメーター、シンチレーションカウンター、回転試料台を取り付けて使用した。測定条件は出力40kV、100-200mA、発散スリット(Divergence slit)1/2°、受光スリット(Receiving slit)0.15mm、操作範囲2θ=20°〜90°、連続計数法で計数間隔0.01°、スキャンスピード4.0°/min とし、Bragg-Brentano法で操作した。
【0049】
結果
単離した細菌の生理学的性質
単離細菌は長軸2-5μm、短軸0.5μmの長桿菌で(図1A)、運動性はなく、胞子形成が認められた(図1B, C, D)。グラム染色性は陽性であった。好気条件、嫌気条件のいずれでも生育可能であった。本単離細菌は図1E,Fに示すように強い自家蛍光を有していた。SCD液体培地(pH7.0)における生育では、生育最適温度は60℃であった。70℃以上、 45℃以下では生育することはできなかった(図2A)。したがって単離細菌は中等度好熱性細菌といえる(非特許文献5)。また37℃以下では生育できないので、偏性好熱性細菌といえる(非特許文献5)。SCD液体培地を用いた60℃における培養では、単離細菌はpH7.0で最も良好な生育を示したが、pH5.0ではほとんど生育が認められなかった(図2B)。単離細菌は酸性領域では生育しないという性質を持っていた。16srRNA遺伝子の塩基配列は約1500pbのうち595bpが決定された(配列番号1)。ブラスト(BLAST)解析の結果、Geobacillus thermoglucosidasiusの16srRNA遺伝子と最も近縁であることがわかった(表1)。したがって単離細菌の名称をG. thermoglucosidasius NY05とした。G. thermoglucosidasius NY05は平成20年11月7日付けで独立行政法人産業技術総合研究所特許生物寄託センターに受託番号FERM P-21717として寄託された。
【0050】
【表1】

【0051】
結晶の大きさとかたち
結晶の形成を水溶液法にて行った場合、8日から10日で白色の結晶が容器壁面、底部に強固に付着して出現した。図3Aに水溶液法にて形成された結晶の光学顕微鏡写真を示す。長さ100-150μmの紡錘形結晶が確認された。ゲル法においては、3-4時間でコロニー中あるいはその周辺のゲル内部に20μm程度の結晶が見いだされるようになる。24-48時間で図5Aに示すように100-200μの六方晶形のような形態の結晶が出現した。いずれの結晶も肉眼ではうすい黄白色に見える。ゲル法は水溶液法に比べて、結晶形成速度は顕著に速いといえる。オートクレーブにて死滅させた単離細菌のコロニーを用いて、ゲル法にて結晶形成を調べた結果、結晶形成は確認されなかったので、結晶形成は単離細菌による生物反応であることが示された。
【0052】
結晶の形成条件
表2はゲル法により、結晶形成に必須な元素を調べた結果である。単離細菌の触媒作用による結晶形成は25mM酢酸ナトリウム、7.0mM塩化カルシウム、2.0mM硫酸マグネシウム中で起こる(Reagent A)。結晶形成ゲルから、酢酸ナトリウムまたは塩化カルシウムをのぞくと結晶形成は見られなかった(Reagent B, C)。一方硫酸マグネシウムを除いた結晶形成ゲルにおいては結晶形成が認められた(Reagent D)。したがって酢酸由来の炭素とカルシウムは結晶形成には必須であると考えられる。
【0053】
【表2】

【0054】
結晶形成温度の範囲を、ゲル法にて調べた。表3に示すように結晶は60℃から70℃の範囲で形成された。50℃-40℃では結晶形成能力は弱くなった。80℃、30℃では結晶は全く形成されなかった。したがって結晶形成に最も適している温度は60℃であるとした。
【0055】
嫌気パックと嫌気ジャーを用いて嫌気条件を作り、ゲル法において結晶が形成されるか調べた。温度は60℃とした。表3に示すように好気条件では、良好な結晶形成が見られたが、嫌気条件では結晶形成が認められなかった。したがって好気条件は結晶形成には必須であると考えられる。
【0056】
【表3】

【0057】
結晶形成溶液中の酢酸ナトリウムの濃度の結晶形成に及ぼす影響を調べた。結晶形成溶液中の塩化カルシウム、硫酸マグネシウムは従来の濃度とした。表4に示すように酢酸ナトリウムの濃度が12.5から50mMの範囲内において、良好な結晶形成が認められたが、75mMでは結晶形成効率が悪化し、100mMでは結晶形成は認められなくなった。
【0058】
結晶形成に係る酢酸ナトリウム以外の炭素が調べられた。濃度は結晶形成溶液中の酢酸ナトリウムの濃度と同様に25mMとした。表4に示すように、蟻酸は結晶形成を促したが、プロピオン酸ナトリウム、クエン酸ナトリウム、メチルアルコール、エチルアルコールには結晶形成を促さなかった。結晶形成には、C1およびC2化合物のカルボキシル炭素が利用されると考えられる。
【0059】
【表4】

【0060】
結晶形成溶液に重金属イオン(銅、ニッケル、カドミウム、亜鉛、アルミニウム)をドープし、ゲル法にて結晶形成を調べた(表5)。いずれの重金属イオンも濃度0.01-0.1mMにおいて結晶形成が認められた。しかし銅のドープに見られるように、高濃度の重金属イオンは結晶形成を阻害する。特にカドミウムは0.1mMで結晶形成を阻害した。銅イオンをドープした場合、図6に示すように突起が多く見られる結晶を形成した。0.01mMニッケルドーピングは結晶形成を促進する傾向が見られた。
【0061】
【表5】

【0062】
結晶の光学特性
水溶液法で形成させた結晶を偏光顕微鏡で観察した。図3Bに示すように、偏光特性が観察されたので、鉱物等の結晶形態であることを証明している。
【0063】
単離細菌の触媒作用により形成される結晶を蛍光顕微鏡で観察したところ、顕著な蛍光特性があることがわかった。図4,5に示すように、水溶液法、ゲル法で形成されたいずれの結晶においても、励起波長を365±5、480±20、545±15 nmとすると、それぞれ青、緑、赤の蛍光が観察された。励起波長を変化させながら、蛍光スペクトルを測定するマトリックススキャンニングを実施したところ(図7)、結晶は260-400nmの広範囲の波長で励起されることができ、350-600nmの波長を発することがわかった。最大励起波長、最大放出波長はそれぞれ369.6、446.9nmであった。図8は励起波長350nmで測定した蛍光スペクトル例である。単離細菌の触媒作用により形成された結晶は350nmで励起されると、非常に広い範囲の波長(375-550nm)を放出し、最大放出波長は439nmであった。
【0064】
結晶の組成
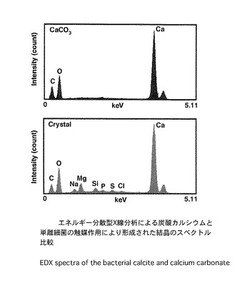
結晶の組成を調べるため、エネルギー分散型X線分析装置EDX (Energy dispersive X-rayによる解析を行った。図9に示すように単離細菌の触媒作用により形成された結晶は、炭素、酸素、カルシウムを多く含み、わずかな量のマグネシウム、ナトリウム、ケイ素、硫黄、リン、クロルで構成されることがわかった。カルシウムの原子数を100(原子%)とすると、マグネシウム19.1、ナトリウム12.2、ケイ素5.1、硫黄2.35、クロル1.22、リン1.83、であった。結晶には炭酸カルシウムの特徴である、塩酸と激しく反応し、ガスを放出して溶解するメインゲン反応 (Meingen reaction)が確認された。また図9に示すように炭酸カルシウム標品のスペクトルと類似していたため結晶は炭酸カルシウムの一種ではないかと思われる。結晶は嫌気環境では形成されないので、結晶中の酸素は空気中の酸素由来である可能性がある。
【0065】
結晶のx線回折波形を図10に示す。粉末炭酸カルシウム標品と結晶のx線回折波形のピーク位置は回折角60度までは一致していたが、ピーク強度は異なっていた。また60度を超える回折角については回折パターンが異なっていた。結晶の回折パターンをThe Powder Diffraction File (PDF-2) (International Centre for Diffraction Data)のデータベースと照合したところ、Calcite, magnesian [(Ca, Mg)CO3] (PDF#00-043-0697)が同定された。したがって単離細菌の触媒作用により形成された結晶はカルサイト型炭酸カルシウム結晶で、一部のカルシウム原子がマグネシウム、ナトリウム、硫黄、クロル、リンで置換された構造を持つと予想される。
【0066】
考察
Bacillus pasteuriiは細胞外にカルサイトを形成することがBachmeierらによって報告された(非特許文献6、7)。ウレアーゼ阻害剤存在下ではカルサイト形成が阻害されるし、ウレアーゼの活性部位に存在するニッケルを添加するとカルサイト形成が上昇すると報告している。しかしながら本発明の単離細菌のカルサイト結晶形成において、ウレアーゼ阻害剤である5mMアセトヒドロキサム酸存在下で結晶形成を試みたところ、結晶形成は阻害されなかったので、単離菌によるカルサイト結晶形成機構にはウレアーゼは関与していないと考えられた(表5)。またpHの上昇も認められなかった。
【0067】
本発明の単離細菌のカルサイト結晶形成機構は、ウレアーゼの酵素化学的反応のみによって起こるケースや、細胞内でナノサイズの結晶核が形成され、それを細胞外に放出し、他の酵素作用によって、結晶が成長するというケースが考えられる。ゲル法における結晶形成において、コロニーの周辺部にも結晶が形成された。このことは単離菌は、結晶形成に係る因子を細胞外に放出しているという説を支持している。
【0068】
G. thermoglucosidasiusの触媒作用により形成された結晶は広い範囲の波長によって励起され、広い範囲の蛍光波長を発することより、これまでに知られた炭酸カルシウム蛍光体にない蛍光特性を備えている。希土類元素を含んでおらず、マグネシウム、ナトリウム、硫黄、リンなどが固溶した状態にあることより、新規炭酸カルシウム蛍光体であるといえる。
【図面の簡単な説明】
【0069】
【図1】図1は単離した細菌の顕微鏡写真を示す。
【図2】図2は単離細菌のSCD液体培地における生育最適温度およびpHを示す。
【図3】図3は水溶液法にて形成された結晶の(A)光学顕微鏡観察および(B)偏光顕微鏡観察結果を示す。
【図4】図4は水溶液法によって製造された結晶の光学および蛍光顕微鏡観察結果を示す。
【図5】図5はゲル法によって製造された結晶の光学および蛍光顕微鏡観察結果を示す。
【図6】図6は銅イオン0.01mMをドープしゲル法により形成された結晶を示す。
【図7】図7は結晶の蛍光特性を表すスペクトルを示す。
【図8】図8は励起波長350nmで測定した結晶の蛍光スペクトルを示す。
【図9】図9は炭酸カルシウムおよび本発明の単離細菌の触媒作用により形成された結晶のエネルギー分散型X線分析によるスペクトルを示す。
【図10】図10は炭酸カルシウムおよび本発明の単離細菌の触媒作用により形成された結晶のX線回折図形を示す。
【技術分野】
【0001】
本発明は、カルサイト型構造を有する炭酸カルシウム質蛍光体および細菌を用いて当該蛍光体を製造する方法に関する。
【背景技術】
【0002】
生物が生体、細胞の内外に無機鉱物結晶を作る作用をバイオミネラリゼーション(biomineralization)という。この言葉は1947年日本の真珠研究者によってはじめて使われ、一つの研究分野が誕生した。バイオミネラリゼーションは細菌などの原核生物からほ乳動物などの真核生物まで普遍的に見られる。たとえば円石藻のウロコ(ココリス)、軟体動物の貝殻、甲殻類の外骨格、魚類の耳石やウロコ、脊椎動物の骨や歯の形成、植物のプラントオパールなどがあげられる。バイオミネラリゼーションによって作られる結晶は通常大部分が無機鉱物から成るが、微量の有機物(有機基質)を含む。この有機基質がバイオミネラリゼーションを制御していると考えられてきたが、未だに不明な点が多い。バイオミネラリゼーションの研究はこれまで多方面から行われてきた。
【0003】
細菌によるバイオミネラリゼーションでは、細胞外または細胞内に無機結晶が形成されることが知られている。細胞外に結晶が形成される例として、細菌によるカルサイト(炭酸カルシウム)形成があげられる。ある種の海洋性細菌はカルサイトを形成する能力があり、この能力と海底の炭酸カルシウム堆積物との関連性が調べられている(非特許文献1)。Boquetらは多くの種類の土壌細菌が酢酸カルシウム、酵母エキス、グルコースを含む固形培地上でカルサイトを形成することを初めて報告した(非特許文献2)。Sanchez-Romanらは19種類の中等度好塩性細菌について、カルシウムとマグネシウムの割合を変化させた培地にて炭酸塩鉱物とリン酸塩鉱物形成を調査し、形成された鉱物がカルサイトやストルバイトであることを報告した(非特許文献3)。Baskarらは鍾乳石から単離された細菌が鍾乳石形成にどのような地質学的影響を及ぼすのか研究を進め、微生物活性は鍾乳石やカルサイト形成の重要な因子であることを報告した (非特許文献4)。
【0004】
細胞内に無機結晶が形成される例としては、磁性細菌の微小磁石が挙げられる。磁性細菌は細胞内にナノサイズのマグネタイト(Fe3O4)結晶あるいはグレガイト(Fe3S4)結晶を室温、中性の環境下で生成し、地磁気センサーとして利用している。その結晶型は種に特異的であり、その大きさも極めて均一であることから、生物工学分野の研究者の興味を集めている。
【0005】
しかしながら、バイオミネラリゼーションの観点から材料科学にアプローチした研究は多くはない。
【0006】
従来から知られている蛍光体のほとんどは、その製造時に高純度かつ高価な希土類酸化物を付活剤として使用している。炭酸カルシウム結晶においても、結晶形成時にユーロピウムやセリウム、テルビウムなどを付活剤として添加すると、蛍光特性をもった炭酸カルシウム結晶が得られることが知られている。たとえばユーロピウム付活バテライト型炭酸カルシウム結晶は最大励起波長330nm、最大蛍光波長620nmで赤色蛍光を発する(特許文献1)。付活剤としてセリウムとテルビウムを使用した場合、励起波長300-450nm、最大放出波長545nmの緑色蛍光を発する炭酸カルシウム結晶が得られる(特許文献2)。特許文献3ではマンガンおよびセリウムにより付活された、ブラックライト(300〜450nm)照射により赤色蛍光発光する炭酸カルシウム質蛍光体が開示されている。しかしながらこれらの蛍光体は常温にて発光強度が激しく減少するという欠点がある。またこれらの蛍光体の放出波長幅は50nmほどである。特許文献4では製造コストを低減させることを目的として、カルサイト型構造を有する炭酸カルシウム結晶にスズを固溶させて蛍光体とする技術が開示されている。しかしながらこの蛍光体もまた放出波長幅が狭いものであった。
【0007】
【特許文献1】特開2001−279241号公報
【特許文献2】特許第3985584号公報
【特許文献3】特許第3965823号公報
【特許文献4】特開平10−226786号公報
【非特許文献1】Brennan, S.T., Lowenstein, T.K., Horita, J (2004) Seawater chemistry and the advent of biocalcification. Geology 32, 473-476
【非特許文献2】Boquet E, Boronat A, Ramos-Cormenzana A (1973) Production of calcite (calcium carbonate) crystals by soil bacteria is a general phenomenon. Nature, 264, 527-529.
【非特許文献3】Sanchez-Roman M, Rivadeneyra MA, Vasconcelos C, McKenzie JA. Biomineralization of carbonate and phosphate by moderately halophilic bacteria.FEMS Microbiol Ecol. 2007 Aug;61(2):273-84.
【非特許文献4】Baskar, S., Baskar, R., Mauclaire, L. and McKenzie, J.A. (2006). Microbially induced calcite precipitation in culture experiments: Possible origin for stalactites in Sahastradhara caves, Dehradun, India, Current Science, v. 90, 58-64.
【非特許文献5】極限環境微生物とその利用 堀越弘毅、関口武司、中村聡、井上明 講談社サイエンティフィク
【非特許文献6】Fujita Y, Taylor JL, Gresham TL, Delwiche ME, Colwell FS, Mcling TL, Petzke LM, Smith RW. Stimulation of microbial urea hydrolysis in groundwater to enhance calcite precipitation. Environ Sci Technol. 2008 Apr 15;42(8):3025-32.
【非特許文献7】Bachmeier KL, Williams AE, Warmington JR, Bang SS. Urease activity in microbiologically-induced calcite precipitation. J Biotechnol. 2002 Feb 14;93(2):171-81.
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明は、結晶は広い範囲の波長によって励起され、広い範囲の蛍光波長を放出ことができる、安価かつ容易に製造することが可能な炭酸カルシウム質蛍光体を提供することを目的とする。
【課題を解決するための手段】
【0009】
本発明者らは驚くべきことに、新規細菌であるGeobacillus thermoglucosidasius NY05が、水中に炭素数1または2のカルボン酸塩、カルシウム塩、およびマグネシウム塩を含む結晶形成溶液中または該結晶形成溶液のゲル化物上においてインキュベートされたときに、広い範囲の波長によって励起され、広い範囲の蛍光波長を発する、従来にない蛍光特性を有するカルサイト型構造を有する炭酸カルシウム結晶を細胞外に形成することを見出し、本発明を完成させるに至った。
【0010】
本発明は以下の発明を包含する。
(1)
260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる、カルサイト型構造を有する炭酸カルシウム質蛍光体。
(2)
カルサイト型構造を有する炭酸カルシウム結晶にマグネシウム、ナトリウム、ケイ素、硫黄、リンおよび塩素が固溶している、(1)の蛍光体。
【0011】
(3)
Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)を、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに形成される炭酸カルシウム質蛍光体。
【0012】
(4)
前記結晶形成溶液または前記ゲル化物が、他の無機塩をさらに含む、(3)の炭酸カルシウム質蛍光体。
【0013】
(5)
Geobacillus thermoglucosidasius に属する細菌であって、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに(1)の蛍光体を形成する能力を有する細菌。
【0014】
(6)
Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)またはその変異株である、(5)の細菌。
【0015】
(7)
カルサイト型構造を有する炭酸カルシウム質蛍光体の製造方法であって、(5)または(6)の細菌を、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む結晶形成溶液中または該結晶形成溶液のゲル化物上にて、好気条件でインキュベートする工程を含む方法。
【発明の効果】
【0016】
本発明の新規Geobacillus thermoglucosidasiusにより、広い範囲の波長によって励起され、広い範囲の蛍光波長を発することが可能な、新規炭酸カルシウム蛍光体を容易に製造することができる。本発明では高価な希土類元素を使用する必要がない。
【0017】
本発明の蛍光体は発光強度の減少がほとんどなく、安定性にすぐれている。
【発明を実施するための最良の形態】
【0018】
1.細菌
本発明において結晶の形成に使用する細菌は、Geobacillus thermoglucosidasius に属する細菌であって、蒸留水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる、カルサイト型構造を有する炭酸カルシウム質蛍光体を形成する能力を有するものであれば特に限定されない。より好ましくは、Geobacillus thermoglucosidasius に属する細菌であって、蒸留水中に酢酸ナトリウム、および塩化カルシウムを含む(さらに他の無機塩を含んでもよい)、pHが5.5〜5.8に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、55〜70℃の温度にて好気条件でインキュベートしたときに、上記特徴を有する炭酸カルシウム質蛍光体を形成する能力を有する細菌である。特に好ましい細菌は、本発明者により単離された新規好熱性細菌であるGeobacillus thermoglucosidasius NY05(受託番号FERM P-21717)である。本発明では更に、G. thermoglucosidasius NY05の変異株であって、同様の結晶形成能を有するものも使用できる。ここで変異株とはG. thermoglucosidasius NY05が変異誘発処理された変異株である。変異誘発処理は任意の適当な変異原を用いて行われ得る。ここで、「変異原」なる語は、その広義において、例えば変異原効果を有する薬剤のみならずUV照射のごとき変異原効果を有する処理をも含むものと理解すべきである。適当な変異原の例としてエチルメタンスルホネート、UV照射、N−メチル−N′−ニトロ−N−ニトロソグアニジン、ブロモウラシルのようなヌクレオチド塩基類似体及びアクリジン類が挙げられるが、他の任意の効果的な変異原もまた使用され得る。このような変異株としては、例えば、16SrRNAの遺伝子の部分配列が配列番号1で表される、G. thermoglucosidasius NY05の変異株等が挙げられる。
【0019】
本発明の新規細菌は、一般的な細菌用の培地を用いて培養し増殖させることができる。培地としては、例えばトリプトソーヤ(SCD)の寒天培地または液体培地が挙げられる。実施例に示すように、G. thermoglucosidasius NY05の培養には温度としては約60℃が好適であり、pHは約7.0が好適である。
【0020】
また、本発明の新規細菌を固体及び液体で培養するときの培養容器は、一般的な微生物の培養に用いられる装置を用いることができ、特に方法を限定するものではない。例えば、小規模の培養では試験管、フラスコ、シャーレなどを用いることができ、大規模の培養にはジャーファメンター、通気攪拌できるタンクなどを使用することができる。
【0021】
2.細菌を用いた結晶(蛍光体)の形成
上記の細菌を、結晶形成溶液中または該結晶形成溶液のゲル化物上にて、好気条件でインキュベートすることにより、細菌の細胞外に、カルサイト型構造の炭酸カルシウム質蛍光体が形成される。
【0022】
結晶形成溶液は、水中に炭素数1または2のカルボン酸塩とカルシウム塩とを少なくとも含む溶液が好ましい。他の無機塩が更に含まれていることがより好ましい。
【0023】
カルボン酸塩の炭素数が3以上の場合には炭酸カルシウム結晶が形成されない。カルボン酸塩としてはギ酸ナトリウムおよび酢酸ナトリウムが好ましい。結晶形成溶液中のカルボン酸塩の濃度は12.5〜50.0 mM が好ましい。
【0024】
カルシウム塩もまた結晶形成に不可欠である。カルシウム塩としては塩化カルシウムが特に好ましい。結晶形成溶液中のカルシウム塩の濃度は5〜10 mMが好ましい。
【0025】
結晶形成溶液中には、他の無機塩がさらに添加されていることが好ましい。無機塩としては例えば銅塩、ニッケル塩、カドミウム塩、亜鉛塩、アルミニウム塩が挙げられ、マグネシウム塩が特に好ましい。結晶形成溶液中にマグネシウム塩を添加することにより結晶形成が促進される。また、マグネシウムは炭酸カルシウム結晶中に固溶する。マグネシウム塩としては硫酸マグネシウムが特に好ましい。結晶形成溶液中のマグネシウム塩の濃度は1〜5 mMが好ましい。また、その他の無機塩中の金属もまた結晶中にドープされ、結晶の蛍光特性を改変することが可能となる。特に、ニッケル塩を添加することが好ましい。ニッケル塩が0.1 mM未満の濃度で添加されたとき、結晶の形成が促進される。
【0026】
結晶形成溶液は弱酸性であることが好ましい。具体的には、pHが5.5〜5.8に調節されていることが好ましい。pHの調節は例えば酢酸により行うことができる。
【0027】
結晶形成溶液は液体として使用することもできるが、寒天等のゲル化剤を用いてゲル化して使用することがより好ましい。結晶形成溶液のゲル化物(結晶形成ゲル)上では、結晶形成速度が大幅に向上するからである。
【0028】
細菌のインキュベートは好気条件のもと行う。酸素が存在しない嫌気条件下では結晶が形成されない。
【0029】
インキュベート温度は45〜70℃の範囲が好ましく、55〜70℃の範囲がより好ましい。この範囲外の温度条件では結晶が全く形成されないか、形成速度が遅い。
【0030】
インキュベート時間は、細菌を結晶形成溶液中に懸濁させる場合には数日間以上、例えば8〜10日間であることが好ましく、細菌を結晶形成ゲル上に載せる場合には数時間以上、例えば24〜48時間であることが好ましい。
【0031】
3.結晶(蛍光体)
本発明で得られる蛍光体は、カルサイト型構造を有する炭酸カルシウムの母体結晶にマグネシウム、ナトリウム、ケイ素、硫黄、リンおよび塩素からなる群から選択される元素の少なくとも1種、好ましくは全てが固溶してなる構造を有する。結晶中の元素の量は特に限定されないが、炭酸カルシウムの母体結晶を構成する炭素、酸素、カルシウムを主成分とし、カルシウムの原子数を100(原子%)としたとき、原子数換算でマグネシウムが0〜25 (結晶形成溶液中にマグネシウム塩が含まれる場合には 15〜25)、ナトリウムが10〜15、ケイ素が4〜6、硫黄が2〜3、リンが1〜2、塩素が1〜2であることが好ましい。結晶を構成する元素は、結晶形成溶液、結晶形成ゲル、または気相中の元素に由来するか、或いは、細菌の細胞に含まれる元素(培養段階で培地等の環境から細胞中に導入された元素も含む)に由来する。
【0032】
本発明で得られる結晶は、260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる。さらに、365±5 nmの波長の光により励起されたときに青色蛍光を放出し、480±20 nmの波長の光により励起されたときに緑色蛍光を放出し、545±15 nmの波長の光により励起されたときに赤色蛍光を発することができる結晶であることが好ましい。また350 nmの光により励起されると、375〜550 nmの非常に幅広い範囲の蛍光を発することができる結晶であることが好ましい。このように幅広い波長範囲の光により励起され、幅広い波長範囲の蛍光を放出する、カルサイト型構造を有する炭酸カルシウム質蛍光体は従来存在しない。
【0033】
4.結晶の用途
本発明により得られる結晶は発光強度の減少がほとんどなく、安定性にすぐれている。したがって、インクジェット用紙用塗工材などの機能材料として応用できる可能性がある。また生化学研究における蛍光マーカー、バイオデバイス、発光ダイオード、半導体において応用できる可能性がある。本発明の細菌を用いると、金属イオンをドーピングしても結晶形成が認められる。したがってさまざまな蛍光特性を持った無機材料が得られると期待される。
【実施例】
【0034】
本発明者は好熱性細菌が細胞外無機結晶を形成することを初めて見出した。以下に、単離した好熱性細菌の生理学的性質、結晶の形成条件、結晶の組成、光学的性質、応用の可能性について述べる。
【0035】
方法および材料
好熱性細菌の単離
高温にて有機性廃棄物を効率的に有機酸に変換する微生物コンソーシアムの選抜を行った。5%の有機性廃棄物、1mg/ml塩化アンモニウム、pH8.0、60℃の条件にて、もっとも多く有機酸を産生する微生物コンソーシアムを選抜した。さらにこの微生物コンソーシアムの中から、トリプトソーヤ(SCD)寒天培地(日水製薬)を用いて好熱性細菌を純粋単離した。
【0036】
単離細菌の最適生育温度、pH
単離細菌を5ml SCD液体培地(pH7.0)に植え60℃,24時間震盪させ、前培養とした。前培養された単離細菌をSCD液体培地(pH7.0)に1/100量加え、37-80℃で24時間震盪した。その後濁度を測定することにより生育最適温度を求めた。
【0037】
pH5.0-9.0のSCD液体培地を調製した。pHは酢酸および水酸化ナトリウム水溶液にて調整した。それぞれのpHのSCD液体培地に前培養された単離細菌を1/100量加え、60℃にて24時間震盪した。その後濁度を測定することにより、生育最適pHを求めた。
【0038】
単離細菌の同定
グラム染色は常法に従った。単離細菌の形態や蛍光特性は蛍光顕微鏡Axioskop2 plus(Zeiss)にて観察された。分離菌の酸素に対する態度は、嫌気ジャー内で嫌気パックをもちいて嫌気環境をつくり、嫌気ジャー内における生育を調べることにより判断した。
【0039】
単離細菌の全DNAはDNA抽出キットISOPLANT(宝酒造)を用いて抽出し、精製した。精製された単離細菌の全DNAを鋳型にして、原核生物用プライマー5'-AGTTTGATC(A/ C)TGGCTCA-3'と5'-AAGGAGGTGATCCAGC-3'を用いて16rRNA遺伝子を増幅した。増幅されたDNAはアガロースゲル電気泳動の後、抽出され、pCRIIベクター(Invitrogen)に連結された。このプラスミドを大腸菌に導入して増幅させ、精製の後常法にしたがってrRNA遺伝子の塩基配列を決定した。
【0040】
結晶の基本的な製造法
単離細菌を5ml SCD液体培地に植え、60℃,24時間震盪させ、前培養とした。前培養液1mlをSCD液体培地100mlに加え、60℃で48時間震盪し、本培養とした。遠心により細胞を集め、酢酸にてpHを5.5-5.8に調整した25mM酢酸ナトリウム、7.0mM塩化カルシウム、2.0mM硫酸マグネシウムを含む蒸留水(結晶形成溶液)にて洗浄した。最終的には細胞をガラス製三角フラスコあるいはポリプロピレン製容器中にて500mLの結晶形成溶液に懸濁させ、60℃、100rpmにて10日間震盪させた(水溶液法aqueous solution method)。
【0041】
結晶形成溶液を1.5%(W/V)寒天(Nakalai tesque)を用いてゲル化させた(結晶形成ゲル)。SDC寒天培地に単離細菌を植え60℃、18時間インキュベートし、コロニーを形成させた。白金耳を用いてコロニーを掻き取り、結晶形成ゲル表面に乗せ、60℃で24-72時間インキュベートした(ゲル法)。
【0042】
結晶の精製
水溶液法においては、結晶は底に沈殿するか、容器の底や壁面に固着して成長する。インキュベートの後、結晶形成溶液のみを捨てさり、壁面や底に固着した結晶をスパチェラなどでかきとった。かきとられた結晶は滅菌蒸留水で数回洗浄し、エタノールで洗浄した後、60℃の下で乾燥させた。
【0043】
ゲル法においては、結晶が形成されたゲル部分を切り取り、テストチューブに移し、寒天溶解溶液(Buffer QX1, Qiagen cat. No. 20912)にてゲルを溶かした。結晶はテストチューブの底に速やかに沈殿するので、容易に溶液部分や細菌の凝集物を捨て去ることができる。チューブの底に沈殿した結晶は滅菌蒸留水で数回洗浄し、エタノールで洗浄した後、60℃の下で乾燥させた。
【0044】
蛍光顕微鏡、偏光顕微鏡
単離細菌の働きにより形成された結晶の形態は、実体顕微鏡SZX-ILLK100 (Olympus)、 光学顕微鏡BZ-9000(Keyence)、蛍光顕微鏡Axioskop2plus(Zeiss)および偏光顕微鏡Eclipse-ME600 (Nicon)にて調べられた。
【0045】
蛍光顕微鏡観察においては、励起波長として365±5、480±20、545±15nm、放出波長としてそれぞれ400以上, 535, 610±37.5nmを通すフィルターをそれぞれ使用した。
【0046】
結晶の蛍光特性
単離細菌の触媒により形成され、精製された結晶の蛍光特性は蛍光顕微鏡、蛍光分光測定装置SPEX Fluorolog-3(Horiba)にて調べられた。励起波長を変化させながら、蛍光スペクトルを測定するマトリックススキャンニングを実施した。スキャン開始励起波長は250nm、最終励起波長は400nmとした。5nm間隔の励起波長において、それぞれ310から700nmの放出波長強度を測定した。
【0047】
結晶の組成
単離細菌の触媒により形成され、精製された結晶の元素組成はエネルギー分散型X線分析装置EDX (Energy dispersive X-ray analysis) EMAX-5770(Horiba)にて調べられた。加圧電圧(管電圧)、プロープ電流はそれぞれ20.0kV 0.26nAとした。
【0048】
X線回折装置としては、リガクX線回折装置RINT-2000に銅回転対陰極とグラファイトモノクロメーター、シンチレーションカウンター、回転試料台を取り付けて使用した。測定条件は出力40kV、100-200mA、発散スリット(Divergence slit)1/2°、受光スリット(Receiving slit)0.15mm、操作範囲2θ=20°〜90°、連続計数法で計数間隔0.01°、スキャンスピード4.0°/min とし、Bragg-Brentano法で操作した。
【0049】
結果
単離した細菌の生理学的性質
単離細菌は長軸2-5μm、短軸0.5μmの長桿菌で(図1A)、運動性はなく、胞子形成が認められた(図1B, C, D)。グラム染色性は陽性であった。好気条件、嫌気条件のいずれでも生育可能であった。本単離細菌は図1E,Fに示すように強い自家蛍光を有していた。SCD液体培地(pH7.0)における生育では、生育最適温度は60℃であった。70℃以上、 45℃以下では生育することはできなかった(図2A)。したがって単離細菌は中等度好熱性細菌といえる(非特許文献5)。また37℃以下では生育できないので、偏性好熱性細菌といえる(非特許文献5)。SCD液体培地を用いた60℃における培養では、単離細菌はpH7.0で最も良好な生育を示したが、pH5.0ではほとんど生育が認められなかった(図2B)。単離細菌は酸性領域では生育しないという性質を持っていた。16srRNA遺伝子の塩基配列は約1500pbのうち595bpが決定された(配列番号1)。ブラスト(BLAST)解析の結果、Geobacillus thermoglucosidasiusの16srRNA遺伝子と最も近縁であることがわかった(表1)。したがって単離細菌の名称をG. thermoglucosidasius NY05とした。G. thermoglucosidasius NY05は平成20年11月7日付けで独立行政法人産業技術総合研究所特許生物寄託センターに受託番号FERM P-21717として寄託された。
【0050】
【表1】

【0051】
結晶の大きさとかたち
結晶の形成を水溶液法にて行った場合、8日から10日で白色の結晶が容器壁面、底部に強固に付着して出現した。図3Aに水溶液法にて形成された結晶の光学顕微鏡写真を示す。長さ100-150μmの紡錘形結晶が確認された。ゲル法においては、3-4時間でコロニー中あるいはその周辺のゲル内部に20μm程度の結晶が見いだされるようになる。24-48時間で図5Aに示すように100-200μの六方晶形のような形態の結晶が出現した。いずれの結晶も肉眼ではうすい黄白色に見える。ゲル法は水溶液法に比べて、結晶形成速度は顕著に速いといえる。オートクレーブにて死滅させた単離細菌のコロニーを用いて、ゲル法にて結晶形成を調べた結果、結晶形成は確認されなかったので、結晶形成は単離細菌による生物反応であることが示された。
【0052】
結晶の形成条件
表2はゲル法により、結晶形成に必須な元素を調べた結果である。単離細菌の触媒作用による結晶形成は25mM酢酸ナトリウム、7.0mM塩化カルシウム、2.0mM硫酸マグネシウム中で起こる(Reagent A)。結晶形成ゲルから、酢酸ナトリウムまたは塩化カルシウムをのぞくと結晶形成は見られなかった(Reagent B, C)。一方硫酸マグネシウムを除いた結晶形成ゲルにおいては結晶形成が認められた(Reagent D)。したがって酢酸由来の炭素とカルシウムは結晶形成には必須であると考えられる。
【0053】
【表2】

【0054】
結晶形成温度の範囲を、ゲル法にて調べた。表3に示すように結晶は60℃から70℃の範囲で形成された。50℃-40℃では結晶形成能力は弱くなった。80℃、30℃では結晶は全く形成されなかった。したがって結晶形成に最も適している温度は60℃であるとした。
【0055】
嫌気パックと嫌気ジャーを用いて嫌気条件を作り、ゲル法において結晶が形成されるか調べた。温度は60℃とした。表3に示すように好気条件では、良好な結晶形成が見られたが、嫌気条件では結晶形成が認められなかった。したがって好気条件は結晶形成には必須であると考えられる。
【0056】
【表3】

【0057】
結晶形成溶液中の酢酸ナトリウムの濃度の結晶形成に及ぼす影響を調べた。結晶形成溶液中の塩化カルシウム、硫酸マグネシウムは従来の濃度とした。表4に示すように酢酸ナトリウムの濃度が12.5から50mMの範囲内において、良好な結晶形成が認められたが、75mMでは結晶形成効率が悪化し、100mMでは結晶形成は認められなくなった。
【0058】
結晶形成に係る酢酸ナトリウム以外の炭素が調べられた。濃度は結晶形成溶液中の酢酸ナトリウムの濃度と同様に25mMとした。表4に示すように、蟻酸は結晶形成を促したが、プロピオン酸ナトリウム、クエン酸ナトリウム、メチルアルコール、エチルアルコールには結晶形成を促さなかった。結晶形成には、C1およびC2化合物のカルボキシル炭素が利用されると考えられる。
【0059】
【表4】

【0060】
結晶形成溶液に重金属イオン(銅、ニッケル、カドミウム、亜鉛、アルミニウム)をドープし、ゲル法にて結晶形成を調べた(表5)。いずれの重金属イオンも濃度0.01-0.1mMにおいて結晶形成が認められた。しかし銅のドープに見られるように、高濃度の重金属イオンは結晶形成を阻害する。特にカドミウムは0.1mMで結晶形成を阻害した。銅イオンをドープした場合、図6に示すように突起が多く見られる結晶を形成した。0.01mMニッケルドーピングは結晶形成を促進する傾向が見られた。
【0061】
【表5】

【0062】
結晶の光学特性
水溶液法で形成させた結晶を偏光顕微鏡で観察した。図3Bに示すように、偏光特性が観察されたので、鉱物等の結晶形態であることを証明している。
【0063】
単離細菌の触媒作用により形成される結晶を蛍光顕微鏡で観察したところ、顕著な蛍光特性があることがわかった。図4,5に示すように、水溶液法、ゲル法で形成されたいずれの結晶においても、励起波長を365±5、480±20、545±15 nmとすると、それぞれ青、緑、赤の蛍光が観察された。励起波長を変化させながら、蛍光スペクトルを測定するマトリックススキャンニングを実施したところ(図7)、結晶は260-400nmの広範囲の波長で励起されることができ、350-600nmの波長を発することがわかった。最大励起波長、最大放出波長はそれぞれ369.6、446.9nmであった。図8は励起波長350nmで測定した蛍光スペクトル例である。単離細菌の触媒作用により形成された結晶は350nmで励起されると、非常に広い範囲の波長(375-550nm)を放出し、最大放出波長は439nmであった。
【0064】
結晶の組成
結晶の組成を調べるため、エネルギー分散型X線分析装置EDX (Energy dispersive X-rayによる解析を行った。図9に示すように単離細菌の触媒作用により形成された結晶は、炭素、酸素、カルシウムを多く含み、わずかな量のマグネシウム、ナトリウム、ケイ素、硫黄、リン、クロルで構成されることがわかった。カルシウムの原子数を100(原子%)とすると、マグネシウム19.1、ナトリウム12.2、ケイ素5.1、硫黄2.35、クロル1.22、リン1.83、であった。結晶には炭酸カルシウムの特徴である、塩酸と激しく反応し、ガスを放出して溶解するメインゲン反応 (Meingen reaction)が確認された。また図9に示すように炭酸カルシウム標品のスペクトルと類似していたため結晶は炭酸カルシウムの一種ではないかと思われる。結晶は嫌気環境では形成されないので、結晶中の酸素は空気中の酸素由来である可能性がある。
【0065】
結晶のx線回折波形を図10に示す。粉末炭酸カルシウム標品と結晶のx線回折波形のピーク位置は回折角60度までは一致していたが、ピーク強度は異なっていた。また60度を超える回折角については回折パターンが異なっていた。結晶の回折パターンをThe Powder Diffraction File (PDF-2) (International Centre for Diffraction Data)のデータベースと照合したところ、Calcite, magnesian [(Ca, Mg)CO3] (PDF#00-043-0697)が同定された。したがって単離細菌の触媒作用により形成された結晶はカルサイト型炭酸カルシウム結晶で、一部のカルシウム原子がマグネシウム、ナトリウム、硫黄、クロル、リンで置換された構造を持つと予想される。
【0066】
考察
Bacillus pasteuriiは細胞外にカルサイトを形成することがBachmeierらによって報告された(非特許文献6、7)。ウレアーゼ阻害剤存在下ではカルサイト形成が阻害されるし、ウレアーゼの活性部位に存在するニッケルを添加するとカルサイト形成が上昇すると報告している。しかしながら本発明の単離細菌のカルサイト結晶形成において、ウレアーゼ阻害剤である5mMアセトヒドロキサム酸存在下で結晶形成を試みたところ、結晶形成は阻害されなかったので、単離菌によるカルサイト結晶形成機構にはウレアーゼは関与していないと考えられた(表5)。またpHの上昇も認められなかった。
【0067】
本発明の単離細菌のカルサイト結晶形成機構は、ウレアーゼの酵素化学的反応のみによって起こるケースや、細胞内でナノサイズの結晶核が形成され、それを細胞外に放出し、他の酵素作用によって、結晶が成長するというケースが考えられる。ゲル法における結晶形成において、コロニーの周辺部にも結晶が形成された。このことは単離菌は、結晶形成に係る因子を細胞外に放出しているという説を支持している。
【0068】
G. thermoglucosidasiusの触媒作用により形成された結晶は広い範囲の波長によって励起され、広い範囲の蛍光波長を発することより、これまでに知られた炭酸カルシウム蛍光体にない蛍光特性を備えている。希土類元素を含んでおらず、マグネシウム、ナトリウム、硫黄、リンなどが固溶した状態にあることより、新規炭酸カルシウム蛍光体であるといえる。
【図面の簡単な説明】
【0069】
【図1】図1は単離した細菌の顕微鏡写真を示す。
【図2】図2は単離細菌のSCD液体培地における生育最適温度およびpHを示す。
【図3】図3は水溶液法にて形成された結晶の(A)光学顕微鏡観察および(B)偏光顕微鏡観察結果を示す。
【図4】図4は水溶液法によって製造された結晶の光学および蛍光顕微鏡観察結果を示す。
【図5】図5はゲル法によって製造された結晶の光学および蛍光顕微鏡観察結果を示す。
【図6】図6は銅イオン0.01mMをドープしゲル法により形成された結晶を示す。
【図7】図7は結晶の蛍光特性を表すスペクトルを示す。
【図8】図8は励起波長350nmで測定した結晶の蛍光スペクトルを示す。
【図9】図9は炭酸カルシウムおよび本発明の単離細菌の触媒作用により形成された結晶のエネルギー分散型X線分析によるスペクトルを示す。
【図10】図10は炭酸カルシウムおよび本発明の単離細菌の触媒作用により形成された結晶のX線回折図形を示す。
【特許請求の範囲】
【請求項1】
260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる、カルサイト型構造を有する炭酸カルシウム質蛍光体。
【請求項2】
カルサイト型構造を有する炭酸カルシウム結晶にマグネシウム、ナトリウム、ケイ素、硫黄、リンおよび塩素が固溶している、請求項1の蛍光体。
【請求項3】
Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)を、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに形成される炭酸カルシウム質蛍光体。
【請求項4】
前記結晶形成溶液または前記ゲル化物が、他の無機塩をさらに含む、請求項3の炭酸カルシウム質蛍光体。
【請求項5】
Geobacillus thermoglucosidasius に属する細菌であって、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに請求項1の蛍光体を形成する能力を有する細菌。
【請求項6】
Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)またはその変異株である、請求項5の細菌。
【請求項7】
カルサイト型構造を有する炭酸カルシウム質蛍光体の製造方法であって、請求項5または6の細菌を、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む結晶形成溶液中または該結晶形成溶液のゲル化物上にて、好気条件でインキュベートする工程を含む方法。
【請求項1】
260〜400 nmの範囲の波長の光により励起されたときに350〜600 nmの範囲の波長の蛍光を発することができる、カルサイト型構造を有する炭酸カルシウム質蛍光体。
【請求項2】
カルサイト型構造を有する炭酸カルシウム結晶にマグネシウム、ナトリウム、ケイ素、硫黄、リンおよび塩素が固溶している、請求項1の蛍光体。
【請求項3】
Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)を、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに形成される炭酸カルシウム質蛍光体。
【請求項4】
前記結晶形成溶液または前記ゲル化物が、他の無機塩をさらに含む、請求項3の炭酸カルシウム質蛍光体。
【請求項5】
Geobacillus thermoglucosidasius に属する細菌であって、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む弱酸性に調整された結晶形成溶液中または該結晶形成溶液のゲル化物上にて、45〜70℃の温度にて好気条件でインキュベートしたときに請求項1の蛍光体を形成する能力を有する細菌。
【請求項6】
Geobacillus thermoglucosidasius NY05(受託番号FERM P-21717)またはその変異株である、請求項5の細菌。
【請求項7】
カルサイト型構造を有する炭酸カルシウム質蛍光体の製造方法であって、請求項5または6の細菌を、水中に炭素数1または2のカルボン酸塩、およびカルシウム塩を含む結晶形成溶液中または該結晶形成溶液のゲル化物上にて、好気条件でインキュベートする工程を含む方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【公開番号】特開2010−150387(P2010−150387A)
【公開日】平成22年7月8日(2010.7.8)
【国際特許分類】
【出願番号】特願2008−329933(P2008−329933)
【出願日】平成20年12月25日(2008.12.25)
【出願人】(504224153)国立大学法人 宮崎大学 (239)
【Fターム(参考)】
【公開日】平成22年7月8日(2010.7.8)
【国際特許分類】
【出願日】平成20年12月25日(2008.12.25)
【出願人】(504224153)国立大学法人 宮崎大学 (239)
【Fターム(参考)】
[ Back to top ]

