血液凝固分析装置
【課題】装置が複雑化および大型化するのを抑制しながら、複数の分析項目を測定することが可能な血液凝固分析装置を提供する。
【解決手段】キュベット250中の血液試料と試薬とが混和された測定試料を測定する測定部70を備え、キュベット250を保持するための挿入孔71aの側面から当該挿入孔71aに保持されたキュベット250へ向けて、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を照射するランプユニット40と、複数の波長の光が照射されたキュベット250中の測定試料からの光を受光する光電変換素子72bとを含み、制御装置4は、ランプユニット40から照射された複数の波長の光のうちのいずれかの波長の光に対応する光電変換素子72bの受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するようにしている。
【解決手段】キュベット250中の血液試料と試薬とが混和された測定試料を測定する測定部70を備え、キュベット250を保持するための挿入孔71aの側面から当該挿入孔71aに保持されたキュベット250へ向けて、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を照射するランプユニット40と、複数の波長の光が照射されたキュベット250中の測定試料からの光を受光する光電変換素子72bとを含み、制御装置4は、ランプユニット40から照射された複数の波長の光のうちのいずれかの波長の光に対応する光電変換素子72bの受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するようにしている。
【発明の詳細な説明】
【技術分野】
【0001】
この発明は、血液凝固分析装置に関し、特に、血液試料と試薬とが混和された測定試料を測定する測定部を備えた血液凝固分析装置に関する。
【背景技術】
【0002】
従来、血漿に所定の測定試薬を添加した測定試料を透光製容器に収容して、その透光製容器に光を照射したときの散乱光や透過光などを取得するように構成された血液凝固分析装置が知られている(たとえば、特許文献1参照)。
【0003】
上記特許文献1に記載の血液凝固分析装置では、透光性容器を収容する収容部に、互いに異なる波長の光を照射する第1光源および第2光源と、第1光源または第2光源からの光を検出する光検出器とが設けられている。また、透光性容器は収容部において第1の容器位置と第2の容器位置とに移動可能に構成されている。この特許文献1に記載の血液凝固分析装置では、第1の容器位置において第1光源からの光を検出し、第2の容器位置において第2光源からの光を検出することにより、1つの検出器で複数の分析項目の測定を行うことが可能に構成されている。
【0004】
【特許文献1】特開2002−196007号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかしながら、上記特許文献1に記載の血液凝固分析装置では、収容部において透光性容器の位置を変更するための機構を設ける必要があるので、その分、装置の複雑化および大型化を招くという問題点がある。
【0006】
この発明は、上記のような課題を解決するためになされたものであり、この発明の1つの目的は、装置が複雑化および大型化するのを抑制しながら、複数の分析項目を測定することが可能な血液凝固分析装置を提供することである。
【課題を解決するための手段および発明の効果】
【0007】
この発明の第1の局面による血液凝固分析装置は、反応容器中の血液試料と試薬とが混和された測定試料を測定する測定部と、測定部による測定結果を分析する分析部とを備え、測定部は、反応容器を保持するための保持部と、保持部の側面から当該保持部に保持された反応容器へ向けて、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を照射する光照射部と、複数の波長の光が照射された反応容器中の測定試料からの光を受光する受光部とを含み、分析部は、光照射部から照射された複数の波長の光のうちのいずれかの波長の光に対応する受光部の受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するように構成されている。
【0008】
この第1の局面による血液凝固分析装置では、上記のように、複数の波長の光が照射された反応容器中の測定試料からの光を受光部によって受光することによって、波長毎に複数の受光部を設ける必要がないため、装置が複雑化および大型化するのを抑制することができる。また、測定部に、反応容器を保持するための保持部と、保持部の側面から当該保持部に保持された反応容器へ向けて、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を照射する光照射部と、複数の波長の光が照射された反応容器中の測定試料からの光を受光する受光部とを設けることによって、血液凝固時間測定と、合成基質測定および免疫比濁測定の少なくともいずれか一方との複数の分析項目を測定することができる。
【0009】
上記第1の局面による血液凝固分析装置において、好ましくは、光照射部は、複数の波長の光のうちの少なくとも1つの波長の光を所定の反応期間に渡って照射するように構成されている。このように構成すれば、所定の反応期間に渡って照射した光の波長に対応する分析項目を測定することができる。
【0010】
この場合、好ましくは、光照射部は、少なくとも1つの波長の光を、断続的に複数回照射するように構成されている。このように構成すれば、複数回照射した光による複数の測定結果により、所定の反応期間に渡って照射した光の波長に対応する分析項目を分析することができる。
【0011】
上記光照射部が少なくとも1つの波長の光を断続的に複数回照射する構成において、好ましくは、光照射部は、少なくとも1つの波長の光と、少なくとも1つの波長の光以外の波長の光とを時分割で照射するように構成されている。このように構成すれば、1つの波長に対応する分析項目と、その波長以外の波長に対応する分析項目との両方を容易に測定することができる。
【0012】
この場合、好ましくは、光源部と、光源部から発せられた光を透過して所定の異なる波長の光を抽出する複数の光学フィルタを含む光学抽出部と、光学フィルタを透過した光を光照射部に導く導光部と、複数の光学フィルタが順次光源部の光路に配置されるように光学抽出部を移動させる移動部とをさらに備える。このように構成すれば、光源部から発せられた光から、順次光源部の光路に配置される複数の光学フィルタによって所定の異なる複数の波長の光を順次抽出し、抽出した異なる波長の複数の光を導光部によって光照射部に導くことができる。これにより、容易に複数の波長の光を断続的に光照射部から照射することができる。
【0013】
上記光源部、光学抽出部、導光部および移動部を備える構成において、好ましくは、光源部は、1つの光源からなる。このように構成すれば、1つの光源による光から異なる波長の複数の光を抽出して、光照射部から照射することができる。
【0014】
上記光照射部が複数の波長の光のうちの少なくとも1つの波長の光を所定の反応期間に渡って照射する構成において、好ましくは、光照射部は、少なくとも1つの光を、所定の反応期間に渡って連続的に照射するように構成されている。このように構成すれば、連続的に照射した光による連続した測定結果により、所定の反応期間に渡って照射した光の波長に対応する分析項目を分析することができる。
【0015】
上記第1の局面による血液凝固分析装置において、好ましくは、測定部は、複数の保持部を有し、複数の保持部にそれぞれ保持された各反応容器中の測定試料を個別に測定することが可能であるように複数の光照射部および複数の受光部を含む。このように構成すれば、複数の測定試料を測定することができるので、装置の処理能力を向上させることができる。
【0016】
上記第1の局面による血液凝固分析装置において、好ましくは、光照射部は、さらに、血小板凝集測定用の第4波長の光を照射することが可能なように構成されている。このように構成すれば、光照射部により測定試料に第4波長の光を照射することにより血小板凝集測定を行うことができる。
【0017】
この場合、好ましくは、血液凝固時間測定、合成基質測定、免疫比濁測定および血小板凝集測定の際、受光部は、測定試料を透過した透過光を受光するように構成されている。このように構成すれば、測定試料を透過した透過光により血液凝固時間測定、合成基質測定、免疫比濁測定および血小板凝集測定を行うことができる。
【0018】
上記第1の局面による血液凝固分析装置において、好ましくは、血液凝固時間測定の際、受光部は、測定試料により散乱された散乱光を受光するように構成されている。このように構成すれば、測定試料により散乱された散乱光により血液凝固時間測定を行うことができる。
【0019】
この場合、好ましくは、光照射部は、血液凝固時間測定用の第1波長の光を照射する第1照射部と、合成基質測定用の第2波長の光と免疫比濁測定用の第3波長の光との少なくとも一方を照射する第2照射部とを含む。このように構成すれば、第1照射部から第1波長の光を照射して試料からの散乱光により血液凝固時間測定を行い、第2照射部により第2波長および第3波長を照射して試料からの透過光により合成基質測定および免疫比濁測定を行うことができる。
【0020】
この発明の第2の局面による血液凝固分析装置は、反応容器中の血液試料と試薬とが混和された測定試料を測定する測定部と、測定部による測定結果を分析する分析部とを備え、測定部は、反応容器を保持するための保持部と、保持部の側面から当該保持部に保持された反応容器へ向けて光を照射する光照射部と、反応容器中の測定試料からの光から互いに異なる波長の複数の光をそれぞれ抽出する光学抽出部と、光学抽出部により抽出された光を受光する受光部とを含み、分析部は、複数の波長のうちのいずれかの波長に対応する受光部の受光結果に基づいて、その波長に対応する分析項目の分析結果を取得するように構成されている。
【0021】
この第2の局面による血液凝固分析装置では、上記のように、光学抽出部により抽出された互いに異なる波長の複数の光を受光部によって受光することによって、波長毎に複数の受光部を設ける必要がないため、装置が複雑化および大型化するのを抑制することができる。また、測定試料からの光から互いに異なる波長の複数の光をそれぞれ抽出する光学抽出部と、光学抽出部により抽出された光を受光する受光部とを設けることによって、測定試料の情報を有する測定試料からの光から光学抽出部により互いに異なる波長の複数の光を抽出することができる。これらの互いに異なる波長の複数の光を受光部が受光することによって、それぞれの波長に対応する複数の分析項目を測定することができる。
【0022】
この発明の第3の局面による血液凝固分析装置は、血液試料と試薬とが混和された測定試料をそれぞれ収容した複数の反応容器を保持し、各反応容器中の測定試料を測定する測定部と、測定部による測定結果を分析する分析部とを備え、測定部は、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を、少なくとも1つの反応容器に対して照射する光照射部と、複数の波長の光が照射された反応容器中の測定試料からの光を受光する受光部とを含み、分析部は、光照射部から照射された複数の波長の光のうちのいずれかの波長の光に対応する受光部の受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するように構成されている。
【0023】
この第3の局面による血液凝固分析装置では、上記のように、複数の波長の光が照射された反応容器中の測定試料からの光を受光部によって受光することによって、波長毎に複数の受光部を設ける必要がないため、装置が複雑化および大型化するのを抑制することができる。また、測定部に、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を、少なくとも1つの反応容器に対して照射する光照射部と、複数の波長の光が照射された反応容器中の測定試料からの光を受光する受光部とを設けることによって、血液凝固時間測定と、合成基質測定および免疫比濁測定の少なくともいずれか一方との複数の分析項目を測定することができる。
【発明を実施するための最良の形態】
【0024】
以下、本発明を具体化した実施形態を図面に基づいて説明する。
【0025】
(第1実施形態)
図1および図2は、それぞれ、本発明の第1実施形態による血液凝固分析装置の全体構成を示す斜視図および平面図である。また、図3〜図15は、図1に示した第1実施形態による血液凝固分析装置の構成を説明するための図である。まず、図1〜図15を参照して、本発明の第1実施形態による血液凝固分析装置1の全体構成について説明する。
【0026】
本発明の第1実施形態による血液凝固分析装置1は、血液の凝固・線溶機能に関連する特定の物質の量や活性の度合いを光学的に測定して分析するための装置であり、血液検体としては血漿が用いられる。第1実施形態による血液凝固分析装置1では、凝固時間法、合成基質法、免疫比濁法および血小板凝集法を用いて血液検体の光学的な測定を行うことによって、血液検体の凝固時間を測定している。
【0027】
凝固時間法では、試料に660nmの波長の光が照射され、試料からの透過光または散乱光を光検出器で検出することによって、フィブリノーゲンがフィブリンに転化する時間が分析される。凝固時間法の測定項目としては、PT(プロトロンビン時間)、APTT(活性化部分トロンボプラスチン時間)やFbg(フィブリノーゲン量)などがある。また、合成基質法では、試料に405nmの波長の光が照射され、試料からの透過光が光検出器で検出される。合成基質法の測定項目としては、ATIII、α2−PI(α2−プラスミンインヒビター)、PLG(プラスミノーゲン)などがある。また、免疫比濁法では、800nmの波長の光が試料に照射され、試料からの散乱光または透過光が光検出器で検出される。免疫比濁法の測定項目としては、Dダイマー、FDPなどがある。また、血小板凝集法では、試料に575nmの波長の光が照射され、試料からの透過光または散乱光が光検出器で検出される。
【0028】
この血液凝固分析装置1は、図1および図2に示すように、検出機構部2と、検出機構部2の前面側に配置された搬送機構部3と、検出機構部2に電気的に接続された制御装置4とにより構成されている。また、検出機構部2および搬送機構部3は、検出機構部2内に設けられた制御基板5(図2参照)により制御される。
【0029】
搬送機構部3は、検出機構部2に血液検体を供給するために、血液検体を収容した複数(第1実施形態では、10本)の試験管200が載置されたラック201を検出機構部2の吸引位置2a(図2参照)に搬送する機能を有している。また、搬送機構部3は、未処理の血液検体を収容した試験管200が収納されたラック201をセットするためのラックセット領域3aと、処理済みの血液検体を収容した試験管200が収納されたラック201を収容するためのラック収容領域3bとを有している。
【0030】
検出機構部2は、搬送機構部3から供給された血液検体に対して光学的な測定を行うことにより、供給された血液検体に関する光学的な情報を取得することが可能なように構成されている。第1実施形態では、搬送機構部3のラック201に載置された試験管200から検出機構部2のキュベット250(図9参照)内に分注された血液検体に対して光学的な測定が行われる。また、検出機構部2は、図1および図2に示すように、キュベット供給機構部10と、回転搬送部20と、検体分注アーム30と、ランプユニット40と、試薬分注アーム50と、キュベット移送部60と、測定部70と、緊急検体セット部80と、流体部90とを備えている。
【0031】
また、キュベット供給機構部10は、ユーザによって無造作に投入された複数のキュベット250を回転搬送部20に順次供給することが可能なように構成されている。このキュベット供給機構部10は、図1および図2に示すように、第1ホッパ11aと、第1ホッパ11aからキュベット250が供給されるとともに、第1ホッパ11aよりも小さい第2ホッパ11bと、第2ホッパ11bからキュベット250が供給される2つの誘導板12と、2つの誘導板12の下端に配置された支持台13と、支持台13から所定の間隔を隔てて設けられた供給用キャッチャ部14とを含んでいる。第1ホッパ11a内に供給されたキュベット250は、第1ホッパ11aよりも小さい第2ホッパ11bを介して、誘導板12上を、支持台13に向かって滑り落ちながら移動するように構成されている。また、支持台13は、誘導板12を滑り落ちて移動したキュベット250を、供給用キャッチャ部14が把持可能な位置まで回転移送する機能を有している。そして、供給用キャッチャ部14は、支持台13により回転移送されたキュベット250を回転搬送部20に供給するために設けられている。
【0032】
また、図2に示すように、検出機構部2には、上述した供給用キャッチャ部14から所定の間隔を隔てて、キュベット250を廃棄するための廃棄用孔15と、廃棄用孔15の下方に設置された廃棄ボックス16とが設けられている。上述した供給用キャッチャ部14は、回転搬送部20のキュベット搬送テーブル23上のキュベット250を、廃棄用孔15を介して廃棄ボックス16に廃棄することが可能である。すなわち、供給用キャッチャ部14は、キュベット250の供給と廃棄との両方を行うことが可能である。
【0033】
回転搬送部20は、キュベット供給機構部10から供給されたキュベット250と、血液検体を凝固させる試薬を収容した試薬容器(図示せず)とを回転方向に搬送するために設けられている。この回転搬送部20は、図2に示すように、円形状の試薬テーブル21と、円形状の試薬テーブル21の外側に配置された円環形状の試薬テーブル22と、円環形状の試薬テーブル22の外側に配置された円環形状のキュベット搬送テーブル23とにより構成されている。これらのキュベット搬送テーブル23、試薬テーブル21および試薬テーブル22は、それぞれ、時計回り方向および反時計回り方向の両方に回転可能で、かつ、各々のテーブルが互いに独立して回転可能なように構成されている。
【0034】
試薬テーブル21および22は、図2に示すように、それぞれ、円周方向に沿って所定の間隔を隔てて設けられた複数の孔部21aおよび22aを含んでいる。試薬テーブル21および22の孔部21aおよび22aは、血液を凝固させる試薬を収容した複数の試薬容器(図示せず)を載置するために設けられている。また、キュベット搬送テーブル23は、それぞれ、円周方向に沿って所定の間隔を隔てて設けられた円筒形状の複数の保持部23aを含んでいる。保持部23aは、キュベット供給機構部10から供給されたキュベット250を保持するために設けられている。また、キュベット搬送テーブル23の保持部23aに保持されたキュベット250には、検体分注アーム30によって搬送機構部3に載置されるラック201に収納された試験管200に収容されている血液検体が分注される。
【0035】
検体分注アーム30は、搬送機構部3により吸引位置2aに搬送された試験管200に収容される血液検体を吸引するとともに、吸引した血液検体を回転搬送部20に移送されたキュベット250内に分注する機能を有している。
【0036】
ランプユニット40は、図2に示すように、測定部70で行われる光学的な測定に用いられる光を供給するために設けられている。このランプユニット40は、図4および図5に示すように、光源としてのハロゲンランプ41と、集光レンズ42a〜42cと、円盤形状のフィルタ部43と、モータ44と、光透過型のセンサ45と、光ファイバカプラ46と、21本の分岐光ファイバ47(図5参照)とから構成されている。
【0037】
ハロゲンランプ41は、図4に示すように、ハロゲンランプ41が発熱することによって熱せられた空気を冷却するための複数のフィンを有するランプケース41aに収容されている。集光レンズ42a〜42cは、ハロゲンランプ41から照射された光を集光する機能を有している。そして、集光レンズ42a〜42cは、ハロゲンランプ41から照射された光を光ファイバカプラ46に導く光路上に配置されている。また、ハロゲンランプ41から照射されて集光レンズ42a〜42cにより集光された光は、後述するフィルタ部43の光学フィルタ43b〜43fのいずれか1つを透過して光ファイバカプラ46に導かれる。
【0038】
また、ランプユニット40のフィルタ部43は、図4に示すように、モータ44のモータ軸(図示せず)を中心に回転可能に取り付けられている。これにより、モータ44の駆動によって、フィルタ部43が軸を中心として回転するように構成されている。このフィルタ部43は、図6および図7に示すように、5つの光透過特性(透過波長)のそれぞれ異なる光学フィルタ43b〜43fが設けられるフィルタ板43aを備えている。フィルタ板43aには、光学フィルタ43b〜43fを取り付けるための5つの孔43gと、光が透過しないように閉塞される孔43hとが設けられている。そして、5つの孔43gには、それぞれ、光透過特性(透過波長)の異なる5つの光学フィルタ43b、43c、43d、43eおよび43fが設置されている。この孔43gおよび43hは、フィルタ部43の回転方向に沿って所定の角度間隔(第1実施形態では、60°の等間隔)で設けられている。なお、孔43hは、予備の孔であり、フィルタの追加が必要となった場合には、フィルタが装着される。
【0039】
光学フィルタ43b、43c、43d、43eおよび43fは、それぞれ、340nm、405nm、575nm、660nmおよび800nmの波長の光を透過し、その他の波長の光は透過しない。したがって、光学フィルタ43b、43c、43d、43eおよび43fを透過した光は、それぞれ、340nm、405nm、575nm、660nmおよび800nmの波長特性を有する。
【0040】
また、図7に示すように、フィルタ板43aは、円周方向に沿って所定の角度間隔(第1実施形態では、60°の等間隔)で6つのスリットが設けられている。それら6つのスリットのうち1つは、他の5つの通常スリット43iよりもフィルタ板43aの回転方向のスリット幅が大きい原点スリット43jである。原点スリット43jおよび通常スリット43iは、隣接する孔43gおよび43hの間の中間角度位置に所定の角度間隔(第1実施形態では、60°の等間隔)で形成されている。
【0041】
また、ランプユニット40から後述するキュベット載置部71のキュベット250に光が照射される際には、フィルタ部43が実質的に等速回転するようにモータ44の駆動が制御基板5により制御されるように構成されている。したがって、フィルタ板43aの回転に伴って、集光レンズ42a〜42c(図4参照)により集光された光の光路上に光透過特性の異なる5つの光学フィルタ43b〜43fと、1つの遮光された孔43h(図5参照)とが断続的に順次配置される。このため、波長特性の異なる5種類の光が断続的に順次照射される。なお、第1実施形態では、フィルタ部43は、0.1秒間に1回転するように構成されている。したがって、後述するキュベット載置部71のキュベット250には、0.1秒間に5種類の波長特性の異なる光が時分割で順次照射される。そして、測定部70では、光電変換素子72b(参照光用光電変換素子72e)により、0.1秒間毎に5種類の波長に対応する5個の電気信号が取得されるように構成されている。
【0042】
また、光透過型のセンサ45は、図6に示すように、フィルタ部43の回転に伴う原点スリット43jおよび通常スリット43iの通過を検出するために設けられている。このセンサ45は、原点スリット43jおよび通常スリット43iが通過すると、スリットを介して光源からの光を受光部が検出し、検出信号を出力する。なお、原点スリット43jは、通常スリット43iよりもスリット幅が大きいので、原点スリット43jが通過した場合には、センサ45から出力される検出信号は、通常スリット43iが通過した場合の検出信号よりも、出力期間が長い。したがって、センサ45からの検出信号に基づいて、フィルタ部43が正常に回転しているか否かを監視することが可能となる。
【0043】
また、光ファイバカプラ46は、21本の分岐光ファイバ47に光学フィルタ43b〜43fを通過した光を入射させる機能を有している。つまり、光ファイバカプラ46は、21本の分岐光ファイバ47に対して、同時に同質の光を導いている。また、21本の分岐光ファイバ47の先端は、図2に示すように、測定部70に接続されており、ランプユニット40からの光を測定部70にセットされるキュベット250内の測定用試料に導いている。具体的には、図8および図9に示すように、21本の分岐光ファイバ47は、それぞれ、測定部70の後述する20個の挿入孔71aおよび1つの参照光用測定孔71bの側面から、保持されているキュベット250に対して光を供給するように配置されている。したがって、光学フィルタ43b〜43fを断続的に通過する波長特性の異なる5種類の光は、分岐光ファイバ47を介して、測定部70の各々に供給されている。
【0044】
試薬分注アーム50は、図1および図2に示すように、回転搬送部20に載置された試薬容器(図示せず)内の試薬を回転搬送部20に保持されたキュベット250に分注することにより、キュベット250内の血液検体に試薬を混合するために設けられている。血液検体に試薬が添加されることにより、測定用試料が調製される。また、キュベット移送部60は、キュベット250を回転搬送部20と測定部70との間で移送するために設けられている。
【0045】
測定部70は、血液検体に試薬を混和して調製された測定用試料の加温を行うとともに、ランプユニット40によって複数の波長の光が照射された測定用試料から光を経時的に受け、各々の波長について、経時的な光学的な情報を取得するために設けられている。具体的には、測定部70は、ランプユニット40から照射される5種類の光(340nm、405nm、575nm、660nmおよび800nm)を用いて、経過時間毎に透過光量を取得している。なお、分岐光ファイバ47から照射される660nmの波長を有する光は、Fbg(フィブリノーゲン量)、PT(プロトロンビン時間)およびAPTT(活性化部分トロンボプラスチン時間)などの凝固時間法による測定項目を測定する際に用いられるメイン波長である。また、800nmの波長を有する光は、Fbg、PTおよびAPTTなどの凝固時間法による測定項目を測定する際に用いられるサブ波長である。合成基質法の測定項目であるATIIIの測定波長は405nmであり、免疫比濁法の測定項目であるDダイマーおよびFDPの測定波長は800nmである。また、血小板凝集の測定波長は、575nmである。このように、第1実施形態に係る血液凝固分析装置1は、1つの光源としてのハロゲンランプ41から照射された光をフィルタ部43の光学フィルタ43b〜43fに通して複数の波長の光を得、これらの光を用いて様々な測定項目の測定を行うように構成されている。
【0046】
この測定部70は、図2に示すように、キュベット載置部71と、キュベット載置部71の下方に配置された検出部72とにより構成されている。キュベット載置部71には、図9に示すように、キュベット250を挿入するための20個の挿入孔71aと、キュベット250を挿入せずに参照光を測定するための1つの参照光用測定孔71bとが設けられている。また、キュベット載置部71には、挿入孔71aに挿入されたキュベット250を所定の温度に加温するための加温部71cが設けられている。
【0047】
また、参照光用測定孔71bは、分岐光ファイバ47から照射された光の特性を監視するために設けられている。具体的には、分岐光ファイバ47から照射された光を直接検出部72の参照光用光電変換素子72eに受光させることにより、ランプユニット40のハロゲンランプ41(図4参照)に由来する揺らぎなどの特性を電気信号として検出している。そして、検出した光の特性(電気信号)を挿入孔71aに挿入されたキュベット250内の測定用試料の透過光に対応する信号から減算処理することにより、測定用試料の透過光に対応する信号を補正する。これにより、光学的な情報の測定毎に光の特性による微差が生じるのを抑制することが可能である。
【0048】
また、測定部70の検出部72は、挿入孔71aに挿入されたキュベット250内の測定用試料に対して複数の条件下で光学的な測定を行うことが可能なように構成されている。この検出部72には、図8および図9に示すように、キュベット250が挿入される各挿入孔71aに対応して、コリメータレンズ72a、光電変換素子72bおよびプリアンプ72cが設けられる。また、図8に示すように、参照光用測定孔71bに対応して、参照光用コリメータレンズ72d、参照光用光電変換素子72eおよび参照光用プリアンプ72fが設けられている。また、図10に示すように、20個の挿入孔71aのうち所定の挿入孔の下部には、回転可能なマグネット72gが配置されている。血小板凝集法により測定を行う場合には、測定試料が収容されたキュベット250に、磁性を有する棒状のスターラーバー260が投入される。このスターラーバー260がマグネット72gの回転に伴い回転することにより、測定中に測定試料を攪拌することが可能である。このような構成により、第1実施形態による血液凝固分析装置1は、血小板凝集法による測定を行うことが可能に構成されている。
【0049】
コリメータレンズ72aは、図8に示すように、ランプユニット40(図1参照)からの光を誘導する分岐光ファイバ47の端部と、対応する挿入孔71aとの間に設置されている。このコリメータレンズ72aは、分岐光ファイバ47から出射された光を平行光にするために設けられている。また、光電変換素子72bは、挿入孔71aを挟んで分岐光ファイバ47の端部に対向するように設置された基板73の挿入孔71a側の面に取り付けられている。プリアンプ72cは、基板73の挿入孔71aと反対側の面に取り付けられている。また、光電変換素子72bは、挿入孔71aに挿入されたキュベット250内の測定用試料に光を照射したときに測定用試料を透過する光(以下、透過光という)を検出するとともに、検出した透過光に対応する電気信号(アナログ信号)を出力する機能を有している。検出部72のプリアンプ72cは、光電変換素子72bからの電気信号(アナログ信号)を増幅するために設けられている。
【0050】
また、参照光用測定孔71bに対応して検出部72に設けられた参照光用コリメータレンズ72d、参照光用光電変換素子72eおよび参照光用プリアンプ72fは、それぞれ、挿入孔71aに対応して検出部72に設けられたコリメータレンズ72a、光電変換素子72bおよびプリアンプ72cと同様に構成されている。なお、参照光用光電変換素子72eには、参照光として、分岐光ファイバ47から出射された光が参照光用コリメータレンズ72dを透過した後、直接入射されるように構成されている。すなわち、参照光用光電変換素子72eは、測定用試料を収容するキュベット250を介さずに照射される参照光を検出するとともに、検出した参照光に対応する電気信号(アナログ信号)を出力するように構成されている。
【0051】
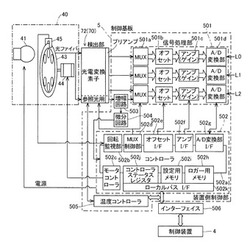
制御基板5は、測定部70の下方に配置されている。この制御基板5は、検出機構部2および搬送機構部3などの動作の制御や、測定部70から出力された光学的情報(電気信号)の処理および記憶などを行う機能を有している。また、制御基板5には、図11および図12に示すように、信号処理部501、装置側制御部502、増幅回路503、微分回路504および温度コントローラ505(図12参照)が設けられている。信号処理部501は、ランプユニット40から測定用試料に光が照射されたときに、光電変換素子72bが透過光を検出して出力する信号の処理を行うために設けられている。この信号処理部501は、図12に示すように、3つのマルチプレクサ(MUX)501aと、3つのオフセット回路501bと、3つのアンプ501cと、3つのA/D変換部501dとを有している。そして、それぞれ1つのマルチプレクサ501a、オフセット回路501b、アンプ501cおよびA/D変換部501dによって、1つの信号処理ラインL0が構成されている。信号処理部501には、この信号処理ラインL0に加えて、信号処理ラインL0と同様の構成を有する信号処理ラインL1およびL2が設けられている。すなわち、信号処理部501には、検出部72から出力された複数のアナログ信号の処理を行うための3つの信号処理ラインL0〜L2が設けられている。
【0052】
図13に示すように、マルチプレクサ501aは、複数のプリアンプ72c(参照光用プリアンプ72f)に接続されている。このマルチプレクサ501aは、複数の光電変換素子72b(参照光用光電変換素子72e)からプリアンプ72c(参照光用プリアンプ72f)を介して入力される複数のアナログ信号から1つずつ選択して順次オフセット回路501bへ出力するように構成されている。オフセット回路501bは、マルチプレクサ501aから出力された信号の補正を行う機能を有している。具体的には、オフセット回路501bは、測定に用いられた挿入孔71aまたは参照光用測定孔71bに対応したオフセット値が装置側制御部502(図12参照)から供給される。そして、オフセット回路501bは、マルチプレクサ501aから出力される透過光に対応する信号から上記のオフセット値を減算処理することにより、マルチプレクサ501aから出力される透過光に対応する信号を補正するように構成されている。
【0053】
アンプ501cは、オフセット回路501bから出力されたアナログ信号を増幅する機能を有している。このアンプ501cのゲイン(増幅率)は、Lゲイン、および、Lゲインよりも高い値のHゲインの2種類に切り替えられるように装置側制御部502により制御される。そして、アンプ501cにより増幅されたLゲイン(増幅率)の信号とHゲイン(増幅率)の信号とは、それぞれ、互いに異なるタイミングでA/D変換部501dに入力されるように構成されている。A/D変換部501dは、それぞれ、アンプ501cに接続されており、そのアンプ501cによりLゲインおよびHゲインの信号(アナログ信号)に増幅された処理済アナログ信号をデジタル信号(データ)に変換するために設けられている。
【0054】
なお、第1実施形態では、A/D変換部501dからは、図13に示すように、チャンネルCH0〜CH47に対応する48個(1つのA/D変換部につき16個)のデータが出力されるように構成されている。なお、このチャンネルCH0〜CH47の内、チャンネルCH0〜CH41の42個のチャンネルのデータは、それぞれ、各光電変換素子72bまたは参照光用光電変換素子72eから得られた電気信号に基づいたデータに対応している。すなわち、20個の光電変換素子72bから得られた20個のデータは、それぞれ、信号処理部501のアンプ501cによりLゲイン(増幅率)およびHゲイン(増幅率)で増幅されることによって40個のデータになる。また、1つの参照光用光電変換素子72eから得られた1つのデータは、信号処理部501(図12参照)のアンプ501cにおいてLゲイン(増幅率)およびHゲイン(増幅率)で増幅されることにより2つのデータになる。この40個のデータと、参照光に対応する2つのデータとを合計した42個のデータがチャンネルCH0〜CH41のデータに対応している。なお、チャンネルCH0〜CH47の内、残りの6つのチャンネルCH42〜CH47は、第1実施形態では使用されない予備のチャンネルであり、このチャンネルCH42〜CH47のデータは、光電変換素子72bまたは参照光用光電変換素子72eからの電気信号には対応していない。
【0055】
また、装置側制御部502は、検出機構部2および搬送機構部3の動作を制御する機能と、A/D変換部501dから出力されるデジタル信号(データ)を取得して記憶する機能とを有している。この装置側制御部502は、図12に示すように、コントローラ502a、フィルタ部回転監視部502b、モータコントローラ502c、マルチプレクサ制御部502d、オフセットインターフェイス502e、アンプインターフェイス502f、A/D変換部インターフェイス502g、ロガー用メモリ502h、設定用メモリ502i、コントローラステータスレジスタ502jおよびローカルバスインターフェイス502kを含んでいる。
【0056】
コントローラ502aは、装置側制御部502による各種の制御を統括する機能を有している。また、フィルタ部回転監視部502bは、ランプユニット40のフィルタ部43が正常に回転しているか否かを監視するために設けられている。このフィルタ部回転監視部502bには、フィルタ部43の回転に伴う原点スリット43j(図7参照)または通常スリット43iの通過を検出するセンサ45からの検出信号が入力されるように構成されている。そして、フィルタ部回転監視部502bにより、センサ45から原点スリット43j(図7参照)の検出信号が出力される時間間隔と、センサ45から通常スリット43i(図7参照)の検出信号が出力される時間間隔と、センサ45から原点スリット43jの検出信号が出力されてから次に再度原点スリット43jの検出信号が出力されるまでの間に通常スリット43iの検出信号が出力される回数とが監視されることによって、フィルタ部43が正常に回転しているか否かが監視される。また、モータコントローラ502cは、フィルタ部43を回転させるモータ44の回転数を制御する機能を有している。また、マルチプレクサ制御部502dは、マルチプレクサ501aの動作を制御する機能を有している。具体的には、マルチプレクサ制御部502dは、複数のマルチプレクサ501aがアナログ信号を選択する時刻をそれぞれ異ならせるようにマルチプレクサ501aの動作を制御している。
【0057】
また、コントローラ502aは、図12に示すように、オフセットインターフェイス502e、アンプインターフェイス502fおよびA/D変換部インターフェイス502gを介してそれぞれ信号処理部501のオフセット回路501b、アンプ501cおよびA/D変換部501dの動作の制御を行うように構成されている。具体的には、コントローラ502aは、オフセットインターフェイス502eを介してオフセット回路501bに所定のオフセット値を供給するとともに、オフセット回路501bがマルチプレクサ501aからの信号からそのオフセット値を減算することにより補正処理を行うのを制御する。また、コントローラ502aは、アンプインターフェイス502fを介してアンプ501cがLゲインおよびHゲインになるように制御するとともに、アンプ501cによるオフセット回路501bからの信号の増幅処理を制御する。また、コントローラ502aは、A/D変換部インターフェイス502gを介してA/D変換部501dによるアンプ501cからの信号(アナログ信号)のデジタル信号への変換処理を制御する。また、A/D変換部501dにより取得されたデジタル信号(データ)は、A/D変換部インターフェイス502gおよびコントローラ502aを介してロガー用メモリ502hに入力されるとともに記憶されるように構成されている。この際、コントローラ502aは、複数のA/D変換部501dが複数のデジタル信号を出力する期間が互いに重複しないように、A/D変換部インターフェイス502gを介してA/D変換部501dの動作を制御している。
【0058】
また、コントローラ502aは、所定の信号処理ライン(L0からL2のいずれか)のマルチプレクサ501a、オフセット回路501bおよびアンプ501cによるアナログ信号処理が行われる期間に、その所定の信号処理ラインとは別の信号処理ラインのA/D変換部501dによる変換処理および装置側制御部502のロガー用メモリ502hへのデータ記憶処理が行われるように、各信号ラインL0〜L2におけるマルチプレクサ501a、オフセット回路501b、アンプ501c、A/D変換部501dおよびロガー用メモリ502hのうち処理を実行するものを切り替える機能を有する。なお、この点については、後の分析動作の説明において詳細に説明する。
【0059】
ロガー用メモリ502hは、所定の光電変換素子72bから出力されたアナログ信号に対応するデジタル信号(データ)を、ロガー用メモリ502hのアドレスによって識別可能に記憶するために設けられている。このロガー用メモリ502hは、図14に示すように、128バイト単位の32個のエリア0〜31によって構成されている。このエリア0〜31には、それぞれ、5つの光学フィルタ43b〜43f(図7参照)の透過光に対応するデータおよび閉塞された孔43hに対応するデータが記憶される。すなわち、フィルタ部43が1回転する毎に、5つの異なる光透過特性を有する光学フィルタ43b〜43fの透過光に対応するデータが発生する。そして、これらの5つのデータがそれぞれロガー用メモリ502h(図14参照)のエリア0から順番にエリア毎に記憶される。また6番目のエリアには、孔43hに対応するデータとして“0”が記憶される。これにより、フィルタ部43の1回転(約100msec)毎にロガー用メモリ502hの6つのエリアが使用されるとともに、エリア31まで使用された後は、エリア0に戻ってデータが上書きされるように構成されている。
【0060】
また、ロガー用メモリ502hの各エリア0〜31は、それぞれ、128個のアドレスを有している。たとえば、エリア0は、000h〜00Fh、010h〜01Fh、020h〜02Fh、030h〜03Fh、040h〜04Fh、050h〜05Fh、060h〜06Fhおよび070h〜07Fhの128個のアドレスを有している。そして、000h〜05Fhの96個のアドレスに上記したチャンネルCH0〜CH47(図13参照)のデータが記憶されるように構成されている。チャンネルCH0〜CH47の各データは、それぞれ、2つのアドレスに記憶されるように構成されている。なお、前述のように第1実施形態では、チャンネルCH42〜47からはデータが出力されないので、これらのチャンネルに対応するアドレスには、データは記憶されない。
【0061】
また、図14に示したロガー用メモリ502hのエリア0におけるアドレス060h〜06Fhおよび070h〜07Ehは、第1実施形態ではデータの記憶されない予備のアドレスである。また、エリア0の最後のアドレス07Fhには、フィルタ番号(0〜4)が記憶される。このフィルタ番号(0〜4)は、5つの光学フィルタ43b〜43f(図7参照)を識別するための番号である。光学フィルタは、原点スリット43jが通過するタイミングを検出することによって識別できる。この5つの光学フィルタ43b〜43fに対応するフィルタ番号(0〜4)がアドレス07Fhに記憶されることにより、エリア0に記憶されたデータがどの光学フィルタ(43b〜43f)の透過光に対応するデータかが識別されるように構成されている。
【0062】
また、図12に示した設定用メモリ502iは、オフセット回路501bに供給するオフセット値と、アンプ501cに供給するゲイン(増幅率)などの設定値を記憶させるために設けられている。また、コントローラステータスレジスタ502jは、フィルタ部43が正常に回転しているか否か、A/D変換部501dによるアナログ信号からデジタル信号への変換エラーの有無、制御部4aによるロガー用メモリ502hからのデータの取得状況、および、制御部4aからの測定開始の指示の有無といった情報を一時的に記憶するために設けられている。また、装置側制御部502は、ローカルバスインターフェイス502kおよびインターフェイス506を介して、ロガー用メモリ502hに記憶された測定用試料のデータ(光学的情報)を制御部4aに送信する機能を有するように構成されている。
【0063】
また、図12に示した制御基板5の増幅回路503は、参照光用光電変換素子72e(図13参照)から参照光用プリアンプ72fを介して出力された信号が入力されるとともに、その入力された信号を増幅する機能を有している。この増幅回路503は、図15に示すように、2つの抵抗503aおよび503bと、1つのオペアンプ503cとによって構成されている。抵抗503aの一方端には、参照光用プリアンプ72fからの参照光に対応する信号が入力されるとともに、他方端は、オペアンプ503cの反転入力端子に接続されている。また、抵抗503bは、オペアンプ503cの出力端子と反転入力端子との間に接続されている。また、オペアンプ503cの非反転入力端子は、接地されている。また、オペアンプ503cの出力は、信号処理部501(図12参照)のマルチプレクサ501aと、微分回路504とにそれぞれ入力されるように構成されている。
【0064】
制御基板5の微分回路504は、増幅回路503からの参照光に対応する信号(以下、参照信号という)の微分信号を生成する機能を有している。この微分回路504は、図15に示すように、2つの抵抗504aおよび504bと、2つのコンデンサ504cおよび504dと、1つのオペアンプ504eとによって構成されている。抵抗504aの一方端には、増幅回路503からの参照信号が入力されるとともに、他方端は、コンデンサ504cの一方電極に接続されている。また、コンデンサ504cの他方電極はオペアンプ504eの反転入力端子に接続されている。また、抵抗504bおよびコンデンサ504dは、共に、オペアンプ504eの出力端子と反転入力端子との間に接続されている。また、オペアンプ504eの非反転入力端子は、接地されている。また、オペアンプ504eの出力は、図示しないコンパレータを介して装置側制御部502(図12参照)のコントローラ502aへ入力されるように構成されている。
【0065】
また、図12に示した制御基板5の温度コントローラ505は、測定部70の加温部71c(図2参照)の温度を制御する機能を有している。この温度コントローラ505は、図12に示すように、インターフェイス506を介して制御部4aから入力される設定温度(約37°)に応じて、測定部70の加温部71cの温度を制御するように構成されている。
【0066】
緊急検体セット部80は、図1および図2に示すように、緊急を要する血液検体に対しての検体分析処理を行うために設けられている。この緊急検体セット部80は、搬送機構部3から供給された血液検体に対しての検体分析処理が行われている際に、緊急検体を割り込ませることが可能なように構成されている。また、流体部90は、血液凝固分析装置1のシャットダウン処理の際に、各分注アームに設けられるノズルに洗浄液などの液体を供給するために設けられている。
【0067】
制御装置4(図1参照)は、パーソナルコンピュータ(PC)などからなり、CPU、ROM、RAMなどからなる制御部4aと、表示部4bと、キーボード4cとを含んでいる。また、表示部4bは、血液検体中に存在する干渉物質(ヘモグロビン、乳び(脂質)およびビリルビン)に関する情報や、測定部70から送信されたデジタル信号のデータを分析して得られた分析結果(凝固時間)などを表示するために設けられている。
【0068】
次に、制御装置4の構成について説明する。制御装置4は、図3に示すように、制御部4aと、表示部4bと、キーボード4cとから主として構成されたコンピュータ401によって構成されている。制御部4aは、CPU401aと、ROM401bと、RAM401cと、ハードディスク401dと、読出装置401eと、入出力インタフェース401fと、通信インタフェース401gと、画像出力インタフェース401hとから主として構成されている。CPU401a、ROM401b、RAM401c、ハードディスク401d、読出装置401e、入出力インタフェース401f、通信インタフェース401g、および画像出力インタフェース401hは、バス401iによって接続されている。
【0069】
CPU401aは、ROM401bに記憶されているコンピュータプログラムおよびRAM401cにロードされたコンピュータプログラムを実行することが可能である。そして、後述するようなアプリケーションプログラム404aをCPU401aが実行することにより、コンピュータ401が制御装置4として機能する。
【0070】
ROM401bは、マスクROM、PROM、EPROM、EEPROMなどによって構成されており、CPU401aに実行されるコンピュータプログラムおよびこれに用いるデータなどが記録されている。
【0071】
RAM401cは、SRAMまたはDRAMなどによって構成されている。RAM401cは、ROM401bおよびハードディスク401dに記録されているコンピュータプログラムの読み出しに用いられる。また、これらのコンピュータプログラムを実行するときに、CPU401aの作業領域として利用される。
【0072】
ハードディスク401dは、オペレーティングシステムおよびアプリケーションプログラムなど、CPU401aに実行させるための種々のコンピュータプログラムおよびそのコンピュータプログラムの実行に用いるデータがインストールされている。第1実施形態に係る血液凝固時間測定用のアプリケーションプログラム404aも、このハードディスク401dにインストールされている。
【0073】
読出装置401eは、フレキシブルディスクドライブ、CD−ROMドライブ、またはDVD−ROMドライブなどによって構成されており、可搬型記録媒体404に記録されたコンピュータプログラムまたはデータを読み出すことができる。また、可搬型記録媒体404には、血液凝固時間測定用のアプリケーションプログラム404aが格納されており、コンピュータ401がその可搬型記録媒体404からアプリケーションプログラム404aを読み出し、そのアプリケーションプログラム404aをハードディスク401dにインストールすることが可能である。
【0074】
なお、上記アプリケーションプログラム404aは、可搬型記録媒体404によって提供されるのみならず、電気通信回線(有線、無線を問わない)によってコンピュータ401と通信可能に接続された外部の機器から上記電気通信回線を通じて提供することも可能である。たとえば、上記アプリケーションプログラム404aがインターネット上のサーバコンピュータのハードディスク内に格納されており、このサーバコンピュータにコンピュータ401がアクセスして、そのアプリケーションプログラム404aをダウンロードし、これをハードディスク401dにインストールすることも可能である。
【0075】
また、ハードディスク401dには、たとえば、米マイクロソフト社が製造販売するWindows(登録商標)などのグラフィカルユーザインタフェース環境を提供するオペレーティングシステムがインストールされている。以下の説明においては、第1実施形態に係るアプリケーションプログラム404aは上記オペレーティングシステム上で動作するものとしている。
【0076】
出力インタフェース401fは、たとえば、USB、IEEE1394、RS−232Cなどのシリアルインタフェース、SCSI、IDE、IEEE1284などのパラレルインタフェース、およびD/A変換器、A/D変換器などからなるアナログインタフェースなどから構成されている。入出力インタフェース401fには、キーボード4cが接続されており、ユーザがそのキーボード4cを使用することにより、コンピュータ401にデータを入力することが可能である。
【0077】
通信インタフェース401gは、たとえば、Ethernet(登録商標)インタフェースである。コンピュータ401は、その通信インタフェース401gにより、所定の通信プロトコルを使用して検出機構部2との間でデータの送受信が可能である。
【0078】
画像出力インタフェース401hは、LCDまたはCRTなどで構成された表示部4bに接続されており、CPU401aから与えられた画像データに応じた映像信号を表示部4bに出力するようになっている。表示部4bは、入力された映像信号にしたがって、画像(画面)を表示する。
【0079】
また、制御部4aのハードディスク401dにインストールされた血液凝固時間測定用のアプリケーションプログラム404aは、検出機構部2の測定部70から送信された測定用試料の透過光量(デジタル信号のデータ)を用いて、測定用試料の凝固時間を測定している。この凝固時間は、キュベット250内の血液検体を凝固させる試薬が添加された時点から、測定用試料(試薬が添加された血液検体)が流動性を失うまでの時間(凝固時間)である。この測定用試料が流動性を失う凝固反応は、血液検体中のフィブリノーゲンが、添加された試薬によりフィブリンに変化する反応である。そして、第1実施形態の血液凝固分析装置1では、血液検体中のフィブリノーゲン量に依存して反応するこの凝固反応を、測定用試料の透過光量の変化量(反応前の透過光量と反応後の透過光量との差)によって確認している。
【0080】
次に、図1、図4および図16を参照して、制御装置4の制御部4aによる血液凝固分析装置1の装置本体(検出機構部2および搬送機構部3)の制御の概略について説明する。
【0081】
血液凝固分析装置1は、制御装置4および装置本体の電源を投入することによって起動する。
【0082】
これらの電源が投入されると、まず、図16に示したステップS1において、PC本体4bにより、初期設定が行われる。この初期設定では、制御部4aに記憶されているソフトウェアの初期化や、後述するpクロックを制御基板5の装置側制御部502から取得する処理などが行われる。なお、装置本体(検出機構部2および搬送機構部3)の電源投入により、ステップS1の初期設定時には、ランプユニット40(図4参照)のハロゲンランプ41から光が照射されるとともに、フィルタ部43が10回転/秒の回転速度での等速回転を開始する。このハロゲンランプ41からの光の照射、および、フィルタ部43の回転は、装置本体(検出機構部2および搬送機構部3)の電源がオフ状態にされるまで継続される。そして、ステップS2において、使用者による検体分析情報の入力を受け付ける処理が行われる。すなわち、使用者は、制御装置4(図1参照)のキーボード4cを用いて、表示部4bに出力される検体分析一覧表中の検体番号および測定項目の欄などに情報の入力を行う。これらの検体分析情報は、制御部4aに保存される。
【0083】
そして、ステップS3において、制御部4aにより分析処理の指示が行われる。これにより、装置本体(検出機構部2および搬送機構部3)による分析処理が行われる。その後、ステップS4において、制御部4aにより、血液凝固分析装置1のシャットダウンの指示が入力されたか否かが判断される。そして、ステップS4において、制御部4aにより、血液凝固分析装置1のシャットダウンの指示が入力されていないと判断された場合には、ステップS2に戻り、使用者による他の検体分析情報の入力を受け付ける処理が行われる。一方、ステップS4において、制御部4aにより、血液凝固分析装置1のシャットダウンの指示が入力されたと判断された場合には、ステップS5において、シャットダウン処理が行われる。このシャットダウン処理により、血液凝固分析装置1の電源が自動的にオフ状態になり、血液凝固分析装置1の動作が終了される。
【0084】
次に、図4、図8、図11、図12、図17および図18を参照して、制御基板5の装置側制御部502によるpクロックの算出処理の方法について詳細に説明する。
【0085】
まず、図17のステップS11において、フィルタ部43が回転している状態で、装置側制御部502により、センサ45からの信号に基づいてセンサ45がスリットを検出した時点のクロック数N21が検出される。次に、図18に示すように、フィルタ部43(図4参照)の等速回転中に、ランプユニット40から参照光用光電変換素子72e(図8参照)に入射される参照光の光量は、「参照光の光量」として示した波形のように変化する。なお、図18中の期間Aは、ランプユニット40(図4参照)において、回転しているフィルタ部43のいずれかの光学フィルタ43b〜43fがハロゲンランプ41からの光の通路に配置される期間である。この期間Aにおいて、ハロゲンランプ41からの光の通路に光学フィルタ43b〜43fが差し掛かると、参照光の光量は徐々に増加し始める。その後、ハロゲンランプ41からの光の通路が完全に光学フィルタ43b〜43f内に収まることにより、参照光の光量は一定となる。その後、ハロゲンランプ41からの光の通路から光学フィルタ43b〜43fが外れ始めると、参照光の光量は徐々に減少し始めるとともに、ハロゲンランプ41からの光の通路から光学フィルタ43b〜43fが完全に外れると参照光の光量は0になる。
【0086】
そして、参照光は、図11に示すように、参照光用光電変換素子72eにより電気信号に変換されるとともに、その変換された電気信号は、参照光用プリアンプ72fおよび増幅回路503により増幅される。そして、増幅回路503から参照光に対応する信号(以下、参照信号という)が出力されるとともに、この参照信号は、微分回路504に入力される。そして、微分回路504により、図18に「参照信号の微分信号」として示した波形を有する参照信号の微分信号が生成される。この参照信号の微分信号は、コンパレータ(図示せず)を介して微分回路504(図12参照)から装置側制御部502に入力される。
【0087】
そして、図17のステップS12において、装置側制御部502により、この参照信号の微分信号が所定の負のしきい値(+)に到達した時点のクロック数N1が検出される。具体的には、図18に示すように、参照光の光量の増加に伴って参照信号の微分信号が立ち上がる。そして、微分信号が所定の正のしきい値(+)に到達するのに応答して、微分回路504(図12参照)から微分信号が入力される図示しないコンパレータにおいてHレベルに立ち上がるパルス信号が出力される。このパルス信号は、装置側制御部502のコントローラ502aに入力されるとともに、コントローラ502aでは、パルス信号がHレベルに立ち上った時点のクロック数N1が検出される。このようにして、装置側制御部502のコントローラ502aにより、参照信号の微分信号が所定の正のしきい値(+)に到達した時点のクロック数N1が検出される。
【0088】
この後、図18に示すように、参照光の光量はさらに増加するとともに、所定の値で一定となる。そして、その後、参照光の光量は徐々に減少する。これに伴って、参照信号の微分信号は、徐々に立ち下がる。そして、図17のステップS13において、装置側制御部502により、参照信号の微分信号が所定の負のしきい値(−)に到達した時点のクロック数(N2)が検出される。具体的には、参照信号の微分信号が徐々に立ち下がるとともに、所定の負のしきい値(−)に到達するのに応答して、微分回路504(図12参照)から微分信号が入力される図示しないコンパレータにおいてHレベルに立ち上がるパルス信号が出力される。このパルス信号は、装置側制御部502のコントローラ502aに入力されるとともに、コントローラ502aでは、パルス信号がHレベルに立ち上った時点のクロック数N2が検出される。このようにして、装置側制御部502のコントローラ502aにより、参照信号の微分信号が所定の負のしきい値(−)に到達した時点のクロック数N2が検出される。
【0089】
そして、図17のステップS14において、装置側制御部502により、クロック数N1からクロック数N2までの間にカウントされるクロック数(Nクロック)がN=N2−N1の式により算出される。そして、ステップS15において、装置側制御部502により、測定用試料の透過光に対応する信号の取得を開始するタイミングを決定するためのクロック数(nクロック)がn=(N−m)/2の式を用いて算出される。なお、この式において、mクロックは、装置側制御部502が測定用試料の透過光に対応する信号を取得する際に要する適切な期間として予め設定されたクロック数である。
【0090】
そして、ステップS16において、制御基板5の装置側制御部502により、スリットの検出から参照信号の立ち上がりまでのクロック数(Pクロック)がP=N1−N21の式を用いて算出される。そして、ステップS17において、装置側制御部502により、測定用試料の透過光に対応する信号の取得を開始するタイミングを決定するためのクロック数(pクロック)がp=P+nの式を用いて算出される。このように、第1実施形態では、フィルタ部43に設けられたスリットを用いて、装置側制御部502が透過光に対応する信号の取得を開始するタイミングを算出している。
【0091】
そして、図18からわかるように、N21クロックから上記のように算出したpクロック後に、マルチプレクサ501aによりmクロックの期間だけ測定用試料の透過光に対応する検出部72からの信号の取得を行えば、ランプユニット40からの照射光の光量が安定している期間の信号を取得することができる。
【0092】
次に、図8、図12、図13および図19〜図21を参照して、上記した図16のステップS3の処理について詳細に説明する。
【0093】
まず、図19のステップS21において、制御部4aにより検体の吸引が指示される。これにより、回転搬送部20に保持されたキュベット250から検体分注アーム30により検体が吸引される。
【0094】
そして、ステップS22において、制御部4aにより測定用試料の調製が指示される。これにより、検出機構部2において、検体分注アーム30により吸引された検体が複数のキュベット250に分注されるとともに、試薬分注アーム50により、試薬容器(図示せず)内の血液の凝固を開始させるための試薬がそれらの複数のキュベット250内の検体に添加される。このようにして、測定用試料の調製が行われる。そして、キュベット移送部60により、測定用試料が収容されたキュベット250が測定部70のキュベット載置部71の挿入孔71aに移動される。
【0095】
そして、ステップS23において、制御部4aにより測定の指示が行われる。これにより、測定部70において、測定用試料の測定が開始される。以下、この測定について詳細に説明する。
【0096】
挿入孔71aに移動されたキュベット250(図8参照)には、上記のようにランプユニット40から5種類の異なる波長特性(340nm、405nm、575nm、660nmおよび800nm)の光が断続的に順次照射される。そして、キュベット250を透過した光は、光電変換素子72b、プリアンプ72c、マルチプレクサ501a、オフセット回路501b、アンプ501c、A/D変換部11dを介して、デジタルデータに変換され、ロガー用メモリ502hに記憶される。
【0097】
ここで、図13を参照して、信号処理部501の動作について説明する。
【0098】
マルチプレクサ501a、オフセット回路501b、アンプ501cおよびA/D変換部501dによる電気信号の処理は、マルチプレクサ501a、オフセット回路501b、アンプ501cおよびA/D変換部501dからなる3つの信号処理ラインL0〜L2において、部分的に並行して行われる。すなわち、図13に示すように、信号処理ラインL0におけるマルチプレクサ501a、オフセット回路501bおよびアンプ501cによる電気信号の処理と、信号処理ラインL1におけるA/D変換部501dによる変換処理および装置側制御部502のロガー用メモリ502h(図12参照)へのデータ記憶処理とが並行して行われる。また、同様に、信号処理ラインL1におけるマルチプレクサ501a、オフセット回路501bおよびアンプ501cによる電気信号の処理と、信号処理ラインL2におけるA/D変換部501dによる変換処理および装置側制御部502のロガー用メモリ502h(図12参照)へのデータ記憶処理とが並行して行われる。また、信号処理ラインL2におけるマルチプレクサ501a、オフセット回路501bおよびアンプ501cによる電気信号の処理と、信号処理ラインL0におけるA/D変換部501dによる変換処理および装置側制御部502のロガー用メモリ502h(図12参照)へのデータ記憶処理とが並行して行われる。
【0099】
そして、これらの電気信号の部分的な並行処理は、図20に示すように、3つの信号処理ラインL0〜L2を順次使用して48μsec単位で行われる。具体的には、まず、図20に示したステップ0では、信号処理ラインL0においてマルチプレクサ501aによるチャンネルCH0への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理が行われる。このステップ0では、信号処理ラインL1およびL2は、電気信号の安定待ちの状態(信号待ち処理)であり、電気信号の処理は行われない。そして、図20のステップ1では、信号処理ラインL1において、マルチプレクサ501aによるチャンネルCH16への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理が行われる。このステップ1では、信号処理ラインL0およびL2は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0100】
そして、図20のステップ2において、信号処理ラインL0のA/D変換部501dによるチャンネルCH0の電気信号のA/D変換処理およびロガー用メモリ502hへのデータ記憶処理と、信号処理ラインL2におけるマルチプレクサ501aによるチャンネルCH32への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理とが並行して行われる。このステップ2では、信号処理ラインL1は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0101】
そして、図20のステップ3において、信号処理ラインL0におけるマルチプレクサ501aによるチャンネルCH1への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理と、信号処理ラインL1のA/D変換部501dによるチャンネルCH16の電気信号のA/D変換処理およびロガー用メモリ502hへのデータ記憶処理とが並行して行われる。このステップ3では、信号処理ラインL2は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0102】
そして、図20のステップ4において、信号処理ラインL1におけるマルチプレクサ501aによるチャンネルCH17への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理と、信号処理ラインL2のA/D変換部501dによるチャンネルCH32の電気信号のA/D変換処理およびロガー用メモリ502hへのデータ記憶処理とが並行して行われる。このステップ4では、信号処理ラインL0は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0103】
そして、上記のステップ2〜4による処理と同様の並行処理が、信号処理ラインL0〜L2において、ステップ49まで信号処理を行うチャンネルを切り替えながら繰り返し行われる。そして、ステップ50では、信号処理ラインL2においてマルチプレクサ501aによるチャンネルCH32への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理が行われる。このステップ50では、信号処理ラインL0およびL1は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0104】
なお、マルチプレクサ501a、オフセット回路501b、およびアンプ501cは、いずれも、信号処理の直後は、出力信号が安定しない。第1実施形態では、このような不安定な信号が分析物の解析に使用されることを防止するため、上記の電気信号の安定待ちの期間が設けられている。
【0105】
上記のようにして、ステップ0〜50の51個のステップにより全てのチャンネルCH0〜CH47の電気信号の処理が行われる。なお、この51個のステップによる電気信号の処理は、2.45msec(=48μsec×51ステップ)の期間に行われる。また、この51個のステップによる電気信号の処理は、後述するmクロックのデータ取得処理の期間内に1回行われる。
【0106】
ロガー用メモリ502hへのデータ記憶処理においては、前述のように、ハロゲンランプ41からの光が透過した光学フィルタおよびチャンネルが特定できるように、所定のアドレスにデータが記憶される。このようにしてロガー用メモリ502hに記憶されたデータは、所定のタイミングに制御部4aに送信される。
【0107】
そして、図19のステップS24において、制御部4aは、測定部70からの波長特性および増幅率の異なる10種類の光学的情報(データ)、すなわち、5種類の光学フィルタ43b〜43fにそれぞれ対応するLゲインおよびHゲインのデータのうち、分析に適している光学的情報(データ)を選択し、その光学的情報を解析する。そして、ステップS25において、測定用試料の解析結果(第1実施形態では、図21に示すような凝固曲線および凝固時間など)を表示部4bに出力する。
【0108】
次に、図12、図18および図22を参照して、第1実施形態の制御基板5の装置側制御部502によるデータ取得処理について説明する。このデータ取得処理は、制御部4aが分析処理の指示(図16のステップS3)をすることによって開始される。
【0109】
まず、図22に示したステップS31において、装置側制御部502(図12参照)により、センサ45からの信号に基づいてセンサ45がスリットを検出したか否かが判断される。スリットが検出されると、ステップS32において、装置側制御部502により、スリット検出の時点から初期設定において算出したpクロック(図18参照)が経過するのを待つ処理が実行される。
【0110】
そして、スリットが検出されてからpクロックが経過すると、ステップS33において、装置側制御部502により、3つのA/D変換部11dからそれぞれ出力されるデジタルデータの取得を開始する処理が実行される。そして、ステップS34において、装置側制御部502により、デジタルデータの取得の開始からmクロックが経過するのを待つ処理が実行される。そして、mクロックが経過すると、ステップS35において、装置側制御部502は、デジタルデータの取得を終了する。そして、ステップS36において、装置側制御部502により、制御部4aから分析指示を受信してから所定時間が経過したか否かを判断する処理が実行される。所定時間が経過していれば、データ取得処理を終了し、経過していなければ、ステップS31の処理に戻る。
【0111】
次に、図2、図14、図19、図21および図23を参照して、第1実施形態の制御装置4の制御部4aによるデータ取得処理について説明する。この処理は、制御装置4の電源が投入されるとともに開始される。
【0112】
まず、図23のステップS40において、制御部4aは、ロガー502hに新たにデータが記憶されたか否かを監視し、データが100msec分(フィルタ部43の1回転分)記憶されるまで待つ。具体的には、ロガー502hに、100msec分のデータが蓄積されると、装置側制御部502から、それを知らせる通知が送信されるので、制御部4aは、その通知が送信されるのを待つ。そして、ステップS41において、制御部4aにより、ロガー用メモリ502hからその100msec分のデータ(部分時系列データ)がインターフェイス506およびローカルバスインターフェイス502kを介して取得される。すなわち、図14に示すように、ロガー用メモリ502hのエリア0〜5にフィルタ部43の1回転分に対応する100msec分のデータが蓄積されると、このエリア0〜5に蓄積されたデータが制御部4aにより取得される。
【0113】
そして、ステップS42において、制御部4aにより、制御装置4がシャットダウン指示を受け付けたか否かの判断が行われる。そして、シャットダウン指示を受け付けていない場合には、ステップS40の処理に戻る。シャットダウン指示を受け付けた場合には、データ取得処理を終了する。なお、ステップS41において、2回目にデータが取得される場合には、1回目にデータが取得されたロガー用メモリ502hのエリア0〜5の次の6つのエリア6〜11のデータが取得される。このように、制御部4aによりロガー用メモリ502hからデータ取得される際には、6つのエリア毎のデータが順次取得される。
【0114】
なお、制御部4aでは、ステップS41でロガー用メモリ502hから取得した複数の部分時系列データの内、測定用試料が収容されたキュベット250(図2参照)が測定部70の挿入孔71aに挿入された時点以降の部分時系列データが時系列順に組み合わされて、所定の時系列データが作成される。そして、制御部4aでは、その作成された時系列データに基づいて図21に示すような凝固曲線が作成される。そして、制御部4aでは、その作成された凝固曲線から測定用試料の凝固時間を求める。具体的には、図21に示した凝固曲線のグラフにおいて、透過光の強度が100%と0%との中間の50%になる時点tを求めるとともに、その時点tのスタート時点からの経過時間を凝固時間として算出する。この凝固時間は、前述のように、図19のステップS25において、表示部3cに表示される。
【0115】
第1実施形態では、上記のように、複数の波長の光が照射されたキュベット250中の測定試料からの光を光電変換素子72bによって受光することによって、波長毎に複数の光電変換素子72bを設ける必要がないため、装置が複雑化および大型化するのを抑制することができる。また、血液凝固時間測定用の660nmの波長の光、合成基質測定用の405nmの波長の光、免疫比濁測定用の800nmの波長の光および血小板凝集測定用の575nmの光を、測定部70の挿入孔71aに保持されたキュベット250の測定試料へ照射して、測定試料からの光を光電変換素子72bによって受光することによって、血液凝固時間測定、合成基質測定、免疫比濁測定および血小板凝集測定の4種類の分析項目を測定することができる。
【0116】
また、第1実施形態では、上記のように、4種類の波長の光を、断続的に複数回照射することによって、複数回照射した光による複数の測定結果により、所定の反応期間に渡って照射した光の波長に対応する分析項目を分析することができる。
【0117】
また、第1実施形態では、上記のように、4種類の波長の光を時分割で照射することによって、4種類の波長に対応する4種類の測定項目を容易に同時に測定することができる。
【0118】
また、第1実施形態では、上記のように、5つの光学フィルタ43b〜43fが設けられたフィルタ部43をモータ44によって回転させることにより、ハロゲンランプ41から発された光の光路に5種類の光学フィルタ43b〜43fを順次配置させることによって、所定の異なる5種類の波長の光を抽出することができる。また、抽出した異なる波長の複数の光を分岐光ファイバ47によって測定部70に導くことができる。これにより、容易に4種類の分析項目(血液凝固測定、合成基質測定、免疫比濁測定および血小板凝集測定)の測定を行うことができる。
【0119】
また、第1実施形態では、上記のように、1つのハロゲンランプ41による光から異なる波長の5種類の光を測定部70に導くことができる。
【0120】
また、第1実施形態では、上記のように、測定部70に20個の挿入孔71aを設け、20個の挿入孔71aにそれぞれ対応して20個の光電変換素子72bを設けることによって、20個の測定試料を同時に測定することができるので、装置の処理能力を向上させることができる。
【0121】
また、第1実施形態では、上記のように、血液凝固時間測定、合成基質測定、免疫比濁測定および血小板凝集測定を、測定試料を透過した透過光により行うことができる。
【0122】
(第2実施形態)
図24〜図26は、本発明の第2実施形態による血液凝固分析装置のランプユニットの詳細を説明するための図である。図27〜図29は、本発明の第2実施形態による血液凝固分析装置の測定部の詳細を説明するための図である。図24〜図29を参照して、この第2実施形態では、上記第1実施形態と異なり、2つの光源を設けるとともに、凝固時間法では試料からの散乱光により測定を行い、凝固時間法以外の測定法では試料からの透過光により測定を行うように構成した例を説明する。なお、第2実施形態におけるランプユニット140および測定部170以外の構成は上記第1実施形態と同じである。
【0123】
第2実施形態によるランプユニット140は、図24に示すように、光源としてのハロゲンランプ141および660nmの波長の光を発振するレーザ発光素子142と、集光レンズ143a〜143cと、円盤形状のフィルタ部144と、モータ145と、光透過型のセンサ146と、2つの光ファイバカプラ147および148と、21本の分岐光ファイバ149(図27参照)と、20本の分岐光ファイバ150(図27参照)とから構成されている。なお、ハロゲンランプ141、集光レンズ143a〜143c、モータ145および光透過型のセンサ146は、それぞれ、上記第1実施形態におけるハロゲンランプ41、集光レンズ42a〜42c、モータ44およびセンサ45と同様の構成を有している。
【0124】
また、ランプユニット40のフィルタ部144は、図24に示すように、モータ145のモータ軸(図示せず)を中心に回転するように構成されている。このフィルタ部144は、4つの光透過特性(透過波長)のそれぞれ異なる4つの光学フィルタ144b〜144eが設けられるフィルタ板144aを備えている。フィルタ板144aには、4つの光学フィルタ144b〜144eを取り付けるための4つの孔144fと、光が透過しないように閉塞される孔144gおよび144hとが設けられている。そして、4つの孔144fには、それぞれ、光透過特性(透過波長)の異なる4つの光学フィルタ144b〜144eが設置されている。なお、閉塞される孔144gは、予備の孔であり、フィルタの追加が必要になった場合には、フィルタが装着される。この光学フィルタ144b〜144eを介してハロゲンランプ141からの光のうち所定の波長を有する光が光ファイバカプラ147に入射するように構成されている。また、フィルタ板144aには、後述するスリット板144jの原点スリット144lと同じ大きさのスリット144iが設けられている。このスリット板144jの原点スリット144lおよびフィルタ板144aのスリット144iを介してレーザ発光素子142からのレーザが光ファイバカプラ148に入射するように構成されている。
【0125】
4つの光学フィルタ144b〜144eは、それぞれ、340nm、405nm、575nmおよび800nmの波長の光を透過し、その他の波長の光は透過しない。したがって、4つの光学フィルタ144b〜144eを透過した光は、それぞれ、340nm、405nm、575nmおよび800nmの波長特性を有する。
【0126】
また、第2実施形態では、フィルタ板144aのハロゲンランプ141と反対側にフィルタ板144aと等しい大きさを有するスリット板144jが設けられている。このスリット板144jには、円周方向に沿って所定の角度間隔(第2実施形態では、60°の等間隔)で6つのスリットが設けられている。それら6つのスリットのうち1つは、他の5つの通常スリット144kよりもフィルタ部144の回転方向のスリット幅が大きい原点スリット144lである。原点スリット144lおよび通常スリット144kは、フィルタ板144aの4つの孔144f、閉塞される孔144gおよび144hの間の中間角度位置に所定の角度間隔(第2実施形態では、60°の等間隔)で形成されている。この原点スリット144lおよび通常スリット144kとセンサ146とによりフィルタ部144の回転が監視される。
【0127】
また、第2実施形態では、フィルタ板144aの回転に伴って、集光レンズ143a〜143cにより集光された光の光路上に光透過特性の異なる4つの光学フィルタ144b〜144eと、予備の孔144gとが断続的に順次配置されるように構成されている。この時、図26に示すように、レーザ発光素子142からのレーザは、フィルタ板144aによって遮断されるように構成されている。また、図25に示すように、集光レンズ143a〜143cにより集光された光の光路上に、遮光された孔144hが配置されたときに、レーザ発光素子142からのレーザの光路上に、フィルタ板144aのスリット144iおよびスリット板144jの原点スリット144lが配置されるように構成されている。これにより、レーザ発光素子142からの660nmの光と、ハロゲンランプ141からの光のうち所定の波長(340nm、405nm、575nmおよび800nm)を有する光とが時分割で光ファイバカプラ147または148に入射するように構成されている。
【0128】
また、光ファイバカプラ147および148は、それぞれ、入射した光を21本の分岐光ファイバ149および20本の光ファイバ150に入射させる機能を有している。また、21本の分岐光ファイバ149および20本の分岐光ファイバ150の先端は、図27に示すように、測定部170に接続されている。そして、図27および図29に示すように、21本の分岐光ファイバ149は、それぞれ、測定部170の後述する20個の挿入孔171aおよび1つの参照光用測定孔171bに光を供給するように配置されている。また、20本の分岐光ファイバ150も、それぞれ、測定部170の20個の挿入孔171aに光を供給するように配置されている。
【0129】
測定部170は、キュベット載置部171と検出部172とを含んでいる。キュベット載置部171は、測定試料が収容されたキュベット250が挿入される20個の挿入孔171aと、1つの参照光用測定孔171bとを含む。また、検出部172には、20個の挿入孔171aおよび1つの参照光用測定孔171bにそれぞれ対応して20個の光電変換素子172aおよび1つの参照光用光電変換素子172bが設けられている。
【0130】
また、図28および図29に示すように、分岐光ファイバ149の測定部170側の先端は、それぞれ20個の光電変換素子172aおよび1つの参照光用光電変換素子172bに向けて配置されている。合成基質法、免疫比濁法および血小板凝集法による測定を行う際には、この分岐光ファイバ149の測定部170側の先端からの光(複数のフィルタにより特定の波長特性を有する光)が、挿入孔171aの側面からキュベット250へ照射され、当該光がキュベット250内の測定試料を透過して光電変換素子172aに入射することにより、複数のフィルタにより特定の波長特性を有する光(340nm、405nm、575nmおよび800nmの波長の光)の透過光が測定されるように構成されている。
【0131】
また、第2実施形態では、20個の分岐光ファイバ150の先端は、それぞれ、20個の挿入孔171aの下方から垂直上方に向けて配置されている。また、挿入孔171aの近傍には、光を反射させるためのミラー173が分岐光ファイバ150の先端と対応する位置に配置されている。凝固時間法で測定する場合には、このミラー173により、分岐光ファイバ150の先端からの光(660nmの波長特性を有するレーザ光)が挿入孔171aの側面からキュベット250へ照射され、当該光がキュベット250内の測定試料に入射し、測定試料による散乱光が光電変換素子172aにより検出されるように構成されている。
【0132】
このように第2実施形態では、凝固時間法(血液凝固時間測定)を散乱光で測定し、合成基質法、免疫比濁法および血小板凝集法を透過光により測定するように構成されている。
【0133】
第2実施形態では、上記のように、ハロゲンランプ141からの光およびレーザ発光素子142からの光をそれぞれ分岐光ファイバ149および分岐光ファイバ150により挿入孔171aに導くことによって、血液凝固時間測定を散乱光により行い、合成基質測定、免疫比濁測定および血小板凝集測定を透過光により行うことができる。
【0134】
なお、今回開示された実施形態は、すべての点で例示であって制限的なものではないと考えられるべきである。本発明の範囲は、上記した実施形態の説明ではなく特許請求の範囲によって示され、さらに特許請求の範囲と均等の意味および範囲内でのすべての変更が含まれる。
【0135】
たとえば、上記第1実施形態では、5つの光学フィルタ43b〜43fが設けられたフィルタ部43を回転させることにより、5つの光学フィルタ43b〜43fを順次ハロゲンランプ41からの光の光路に配置させて複数の波長の光を抽出する例を示したが、本発明はこれに限らず、図30に示す第1変形例のように複数の光源300a〜300dの発光のタイミングを電気的に切換制御するように構成してもよい。この第1変形例では、4つの光源300a〜300dが設けられており、4つの光源300a〜300dは、それぞれ、特定の波長特性を有する光(たとえば、凝固時間測定用の660nmの波長の光、合成基質測定用の405nmの波長の光、免疫比濁測定用の800nmの波長の光および血小板凝集測定用の575nmの波長の光など)を発するレーザ発光素子またはLEDなどからなる。4つの光源300a〜300dは切換制御回路301により電気的に順次発光するように制御される。4つの光源300a〜300dから発された光は、ミラー302aおよびダイクロイックミラー302bにより光ファイバカプラ303に入射し、光ファイバカプラ303から分岐光ファイバ304を介して測定部305に導入されるように構成されている。このように構成しても、4種類の波長の光が順次測定部305に導入されるので、4種類の測定項目(凝固時間測定など)の測定を行うことができる。
【0136】
また、上記第1変形例において示した構成において、1つの光源を連続的に発光させるように切換制御回路301を制御してもよい。たとえば、660nmの波長の光を発する光源300aを連続的に発光させて凝固時間測定を行うことにより、より正確な測定結果を得ることができる。
【0137】
また、上記第1実施形態および第2実施形態では、フィルタ部により抽出した特定の波長の光を測定試料に照射するように構成した例を示したが、本発明はこれに限らず、図31に示す第2変形例のように、フィルタ部311を測定試料312と受光部313との間に設けてもよい。この第2変形例では、光源314から発された光が測定試料312に照射され、測定試料312からの透過光または散乱光が複数の光学フィルタ311aが設けられた回転可能なフィルタ部311を介して受光部313により受光されるように構成される。また、他の測定試料315と受光部316との間には、特定の波長の光を抽出する固定フィルタ317が設けられる。このように構成しても、複数の測定項目を測定することができる。
【0138】
また、上記第1および第2実施形態では、制御装置4を血液凝固分析装置1の装置本体(検出機構部2および搬送機構部3)とは別に設けた例を示したが、本発明はこれに限らず、制御装置4と血液凝固分析装置1の装置本体(検出機構部2および搬送機構部3)とを一体化してもよい。
【0139】
また、上記第1および第2実施形態では、挿入孔71aおよび171aをそれぞれ20個設けた例を示したが、本発明はこれに限らず、挿入孔を20個より多く設けてもよいし、少なく設けてもよい。
【0140】
また、上記第2実施形態では、フィルタ部144の予備の孔144gを閉塞した例を示したが、本発明はこれに限らず、予備の孔144gに、レーザ発光素子142が発する光と同じ660nmの波長の光を透過する光学フィルタを取り付けてもよい。このように構成すれば、660nmの波長の凝固時間測定用の光を分岐光ファイバ150のみならず分岐光ファイバ149からも測定試料に照射することができる。これにより、凝固時間測定を透過光と散乱光との両方で測定することができる。
【図面の簡単な説明】
【0141】
【図1】本発明の第1実施形態による血液凝固分析装置の全体構成を示した斜視図である。
【図2】図1に示した血液凝固分析装置の平面図である。
【図3】第1実施形態による血液凝固分析装置の制御装置のブロック図である。
【図4】第1実施形態による血液凝固分析装置のランプユニットを示した斜視図である。
【図5】第1実施形態による血液凝固分析装置のランプユニットの構成を説明するための模式図である。
【図6】図4に示したランプユニットのフィルタ部を示した拡大斜視図である。
【図7】図4に示したランプユニットのフィルタ部を示した正面図である。
【図8】図1に示した第1実施形態による血液凝固分析装置の測定部の検出部の内部構造を説明するための概略図である。
【図9】図1に示した第1実施形態による血液凝固分析装置の測定部の検出部の構成を説明するための断面図である。
【図10】血小板凝集測定を行う場合の図9に対応する断面図である。
【図11】図1に示した第1実施形態による血液凝固分析装置の測定部の構成を説明するためのブロック図である。
【図12】本発明の第1実施形態による血液凝固分析装置の測定部および制御基板の構成要素を説明するためのブロック図である。
【図13】本発明の第1実施形態による血液凝固分析装置の検出部および信号処理部の構成を説明するためのブロック図である。
【図14】本発明の第1実施形態による血液凝固分析装置の制御基板のロガー用メモリの構成を説明するための図である。
【図15】本発明の第1実施形態による血液凝固分析装置の制御基板の増幅回路および微分回路の回路構成を示した回路図である。
【図16】本発明の第1実施形態による血液凝固分析装置の制御装置の制御部による制御方法の概略を示したフローチャートである。
【図17】図16のステップS1に示した初期設定において、装置側制御部によるpクロックの算出処理を示すフローチャートである。
【図18】図17に示したpクロックの算出処理方法において用いるスリット検出信号並びに参照光の光量および参照信号の微分信号の変化を示した波形図である。
【図19】図16のステップS3における制御装置の制御部による分析処理の詳細(サブルーチン)を示したフローチャートである。
【図20】本発明の第1実施形態による血液凝固分析装置の信号処理部における信号処理の方法を示した図である。
【図21】本発明の第1実施形態による血液凝固分析装置によって作成される凝固曲線を示したグラフである。
【図22】本発明の第1実施形態の装置側制御部によるデータ取得処理の方法を説明するためのフローチャートである。
【図23】本発明の第1実施形態の制御装置の制御部によるデータ取得処理の方法を説明するためのフローチャートである。
【図24】本発明の第2実施形態による血液凝固分析装置のランプユニットを示した斜視図である。
【図25】本発明の第2実施形態による血液凝固分析装置のランプユニットを正面から見た場合の斜視図である。
【図26】本発明の第2実施形態による血液凝固分析装置のランプユニットを正面から見た場合の斜視図である。
【図27】本発明の第2実施形態による血液凝固分析装置の測定部の検出部の内部構造を説明するための概略図である。
【図28】本発明の第2実施形態による血液凝固分析装置の測定部の検出部の内部構造を説明するための斜視図である。
【図29】本発明の第2実施形態による血液凝固分析装置の測定部の検出部の内部構造を説明するための模式図である。
【図30】本発明の第1実施形態の第1変形例の模式図である。
【図31】本発明の第1実施形態の第2変形例の模式図である。
【符号の説明】
【0142】
1 血液凝固分析装置
4 制御装置(分析部)
41、141 ハロゲンランプ(光源部、光源)
43、144 フィルタ部(光学抽出部)
43b〜43f、144b〜144e 光学フィルタ
44、145 モータ(移動部)
46、149 分岐光ファイバ(導光部)
70、170 測定部
71a、171a 挿入孔(保持部)
72b、172a 光電変換素子(受光部)
250 キュベット(反応容器)
【技術分野】
【0001】
この発明は、血液凝固分析装置に関し、特に、血液試料と試薬とが混和された測定試料を測定する測定部を備えた血液凝固分析装置に関する。
【背景技術】
【0002】
従来、血漿に所定の測定試薬を添加した測定試料を透光製容器に収容して、その透光製容器に光を照射したときの散乱光や透過光などを取得するように構成された血液凝固分析装置が知られている(たとえば、特許文献1参照)。
【0003】
上記特許文献1に記載の血液凝固分析装置では、透光性容器を収容する収容部に、互いに異なる波長の光を照射する第1光源および第2光源と、第1光源または第2光源からの光を検出する光検出器とが設けられている。また、透光性容器は収容部において第1の容器位置と第2の容器位置とに移動可能に構成されている。この特許文献1に記載の血液凝固分析装置では、第1の容器位置において第1光源からの光を検出し、第2の容器位置において第2光源からの光を検出することにより、1つの検出器で複数の分析項目の測定を行うことが可能に構成されている。
【0004】
【特許文献1】特開2002−196007号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかしながら、上記特許文献1に記載の血液凝固分析装置では、収容部において透光性容器の位置を変更するための機構を設ける必要があるので、その分、装置の複雑化および大型化を招くという問題点がある。
【0006】
この発明は、上記のような課題を解決するためになされたものであり、この発明の1つの目的は、装置が複雑化および大型化するのを抑制しながら、複数の分析項目を測定することが可能な血液凝固分析装置を提供することである。
【課題を解決するための手段および発明の効果】
【0007】
この発明の第1の局面による血液凝固分析装置は、反応容器中の血液試料と試薬とが混和された測定試料を測定する測定部と、測定部による測定結果を分析する分析部とを備え、測定部は、反応容器を保持するための保持部と、保持部の側面から当該保持部に保持された反応容器へ向けて、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を照射する光照射部と、複数の波長の光が照射された反応容器中の測定試料からの光を受光する受光部とを含み、分析部は、光照射部から照射された複数の波長の光のうちのいずれかの波長の光に対応する受光部の受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するように構成されている。
【0008】
この第1の局面による血液凝固分析装置では、上記のように、複数の波長の光が照射された反応容器中の測定試料からの光を受光部によって受光することによって、波長毎に複数の受光部を設ける必要がないため、装置が複雑化および大型化するのを抑制することができる。また、測定部に、反応容器を保持するための保持部と、保持部の側面から当該保持部に保持された反応容器へ向けて、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を照射する光照射部と、複数の波長の光が照射された反応容器中の測定試料からの光を受光する受光部とを設けることによって、血液凝固時間測定と、合成基質測定および免疫比濁測定の少なくともいずれか一方との複数の分析項目を測定することができる。
【0009】
上記第1の局面による血液凝固分析装置において、好ましくは、光照射部は、複数の波長の光のうちの少なくとも1つの波長の光を所定の反応期間に渡って照射するように構成されている。このように構成すれば、所定の反応期間に渡って照射した光の波長に対応する分析項目を測定することができる。
【0010】
この場合、好ましくは、光照射部は、少なくとも1つの波長の光を、断続的に複数回照射するように構成されている。このように構成すれば、複数回照射した光による複数の測定結果により、所定の反応期間に渡って照射した光の波長に対応する分析項目を分析することができる。
【0011】
上記光照射部が少なくとも1つの波長の光を断続的に複数回照射する構成において、好ましくは、光照射部は、少なくとも1つの波長の光と、少なくとも1つの波長の光以外の波長の光とを時分割で照射するように構成されている。このように構成すれば、1つの波長に対応する分析項目と、その波長以外の波長に対応する分析項目との両方を容易に測定することができる。
【0012】
この場合、好ましくは、光源部と、光源部から発せられた光を透過して所定の異なる波長の光を抽出する複数の光学フィルタを含む光学抽出部と、光学フィルタを透過した光を光照射部に導く導光部と、複数の光学フィルタが順次光源部の光路に配置されるように光学抽出部を移動させる移動部とをさらに備える。このように構成すれば、光源部から発せられた光から、順次光源部の光路に配置される複数の光学フィルタによって所定の異なる複数の波長の光を順次抽出し、抽出した異なる波長の複数の光を導光部によって光照射部に導くことができる。これにより、容易に複数の波長の光を断続的に光照射部から照射することができる。
【0013】
上記光源部、光学抽出部、導光部および移動部を備える構成において、好ましくは、光源部は、1つの光源からなる。このように構成すれば、1つの光源による光から異なる波長の複数の光を抽出して、光照射部から照射することができる。
【0014】
上記光照射部が複数の波長の光のうちの少なくとも1つの波長の光を所定の反応期間に渡って照射する構成において、好ましくは、光照射部は、少なくとも1つの光を、所定の反応期間に渡って連続的に照射するように構成されている。このように構成すれば、連続的に照射した光による連続した測定結果により、所定の反応期間に渡って照射した光の波長に対応する分析項目を分析することができる。
【0015】
上記第1の局面による血液凝固分析装置において、好ましくは、測定部は、複数の保持部を有し、複数の保持部にそれぞれ保持された各反応容器中の測定試料を個別に測定することが可能であるように複数の光照射部および複数の受光部を含む。このように構成すれば、複数の測定試料を測定することができるので、装置の処理能力を向上させることができる。
【0016】
上記第1の局面による血液凝固分析装置において、好ましくは、光照射部は、さらに、血小板凝集測定用の第4波長の光を照射することが可能なように構成されている。このように構成すれば、光照射部により測定試料に第4波長の光を照射することにより血小板凝集測定を行うことができる。
【0017】
この場合、好ましくは、血液凝固時間測定、合成基質測定、免疫比濁測定および血小板凝集測定の際、受光部は、測定試料を透過した透過光を受光するように構成されている。このように構成すれば、測定試料を透過した透過光により血液凝固時間測定、合成基質測定、免疫比濁測定および血小板凝集測定を行うことができる。
【0018】
上記第1の局面による血液凝固分析装置において、好ましくは、血液凝固時間測定の際、受光部は、測定試料により散乱された散乱光を受光するように構成されている。このように構成すれば、測定試料により散乱された散乱光により血液凝固時間測定を行うことができる。
【0019】
この場合、好ましくは、光照射部は、血液凝固時間測定用の第1波長の光を照射する第1照射部と、合成基質測定用の第2波長の光と免疫比濁測定用の第3波長の光との少なくとも一方を照射する第2照射部とを含む。このように構成すれば、第1照射部から第1波長の光を照射して試料からの散乱光により血液凝固時間測定を行い、第2照射部により第2波長および第3波長を照射して試料からの透過光により合成基質測定および免疫比濁測定を行うことができる。
【0020】
この発明の第2の局面による血液凝固分析装置は、反応容器中の血液試料と試薬とが混和された測定試料を測定する測定部と、測定部による測定結果を分析する分析部とを備え、測定部は、反応容器を保持するための保持部と、保持部の側面から当該保持部に保持された反応容器へ向けて光を照射する光照射部と、反応容器中の測定試料からの光から互いに異なる波長の複数の光をそれぞれ抽出する光学抽出部と、光学抽出部により抽出された光を受光する受光部とを含み、分析部は、複数の波長のうちのいずれかの波長に対応する受光部の受光結果に基づいて、その波長に対応する分析項目の分析結果を取得するように構成されている。
【0021】
この第2の局面による血液凝固分析装置では、上記のように、光学抽出部により抽出された互いに異なる波長の複数の光を受光部によって受光することによって、波長毎に複数の受光部を設ける必要がないため、装置が複雑化および大型化するのを抑制することができる。また、測定試料からの光から互いに異なる波長の複数の光をそれぞれ抽出する光学抽出部と、光学抽出部により抽出された光を受光する受光部とを設けることによって、測定試料の情報を有する測定試料からの光から光学抽出部により互いに異なる波長の複数の光を抽出することができる。これらの互いに異なる波長の複数の光を受光部が受光することによって、それぞれの波長に対応する複数の分析項目を測定することができる。
【0022】
この発明の第3の局面による血液凝固分析装置は、血液試料と試薬とが混和された測定試料をそれぞれ収容した複数の反応容器を保持し、各反応容器中の測定試料を測定する測定部と、測定部による測定結果を分析する分析部とを備え、測定部は、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を、少なくとも1つの反応容器に対して照射する光照射部と、複数の波長の光が照射された反応容器中の測定試料からの光を受光する受光部とを含み、分析部は、光照射部から照射された複数の波長の光のうちのいずれかの波長の光に対応する受光部の受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するように構成されている。
【0023】
この第3の局面による血液凝固分析装置では、上記のように、複数の波長の光が照射された反応容器中の測定試料からの光を受光部によって受光することによって、波長毎に複数の受光部を設ける必要がないため、装置が複雑化および大型化するのを抑制することができる。また、測定部に、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を、少なくとも1つの反応容器に対して照射する光照射部と、複数の波長の光が照射された反応容器中の測定試料からの光を受光する受光部とを設けることによって、血液凝固時間測定と、合成基質測定および免疫比濁測定の少なくともいずれか一方との複数の分析項目を測定することができる。
【発明を実施するための最良の形態】
【0024】
以下、本発明を具体化した実施形態を図面に基づいて説明する。
【0025】
(第1実施形態)
図1および図2は、それぞれ、本発明の第1実施形態による血液凝固分析装置の全体構成を示す斜視図および平面図である。また、図3〜図15は、図1に示した第1実施形態による血液凝固分析装置の構成を説明するための図である。まず、図1〜図15を参照して、本発明の第1実施形態による血液凝固分析装置1の全体構成について説明する。
【0026】
本発明の第1実施形態による血液凝固分析装置1は、血液の凝固・線溶機能に関連する特定の物質の量や活性の度合いを光学的に測定して分析するための装置であり、血液検体としては血漿が用いられる。第1実施形態による血液凝固分析装置1では、凝固時間法、合成基質法、免疫比濁法および血小板凝集法を用いて血液検体の光学的な測定を行うことによって、血液検体の凝固時間を測定している。
【0027】
凝固時間法では、試料に660nmの波長の光が照射され、試料からの透過光または散乱光を光検出器で検出することによって、フィブリノーゲンがフィブリンに転化する時間が分析される。凝固時間法の測定項目としては、PT(プロトロンビン時間)、APTT(活性化部分トロンボプラスチン時間)やFbg(フィブリノーゲン量)などがある。また、合成基質法では、試料に405nmの波長の光が照射され、試料からの透過光が光検出器で検出される。合成基質法の測定項目としては、ATIII、α2−PI(α2−プラスミンインヒビター)、PLG(プラスミノーゲン)などがある。また、免疫比濁法では、800nmの波長の光が試料に照射され、試料からの散乱光または透過光が光検出器で検出される。免疫比濁法の測定項目としては、Dダイマー、FDPなどがある。また、血小板凝集法では、試料に575nmの波長の光が照射され、試料からの透過光または散乱光が光検出器で検出される。
【0028】
この血液凝固分析装置1は、図1および図2に示すように、検出機構部2と、検出機構部2の前面側に配置された搬送機構部3と、検出機構部2に電気的に接続された制御装置4とにより構成されている。また、検出機構部2および搬送機構部3は、検出機構部2内に設けられた制御基板5(図2参照)により制御される。
【0029】
搬送機構部3は、検出機構部2に血液検体を供給するために、血液検体を収容した複数(第1実施形態では、10本)の試験管200が載置されたラック201を検出機構部2の吸引位置2a(図2参照)に搬送する機能を有している。また、搬送機構部3は、未処理の血液検体を収容した試験管200が収納されたラック201をセットするためのラックセット領域3aと、処理済みの血液検体を収容した試験管200が収納されたラック201を収容するためのラック収容領域3bとを有している。
【0030】
検出機構部2は、搬送機構部3から供給された血液検体に対して光学的な測定を行うことにより、供給された血液検体に関する光学的な情報を取得することが可能なように構成されている。第1実施形態では、搬送機構部3のラック201に載置された試験管200から検出機構部2のキュベット250(図9参照)内に分注された血液検体に対して光学的な測定が行われる。また、検出機構部2は、図1および図2に示すように、キュベット供給機構部10と、回転搬送部20と、検体分注アーム30と、ランプユニット40と、試薬分注アーム50と、キュベット移送部60と、測定部70と、緊急検体セット部80と、流体部90とを備えている。
【0031】
また、キュベット供給機構部10は、ユーザによって無造作に投入された複数のキュベット250を回転搬送部20に順次供給することが可能なように構成されている。このキュベット供給機構部10は、図1および図2に示すように、第1ホッパ11aと、第1ホッパ11aからキュベット250が供給されるとともに、第1ホッパ11aよりも小さい第2ホッパ11bと、第2ホッパ11bからキュベット250が供給される2つの誘導板12と、2つの誘導板12の下端に配置された支持台13と、支持台13から所定の間隔を隔てて設けられた供給用キャッチャ部14とを含んでいる。第1ホッパ11a内に供給されたキュベット250は、第1ホッパ11aよりも小さい第2ホッパ11bを介して、誘導板12上を、支持台13に向かって滑り落ちながら移動するように構成されている。また、支持台13は、誘導板12を滑り落ちて移動したキュベット250を、供給用キャッチャ部14が把持可能な位置まで回転移送する機能を有している。そして、供給用キャッチャ部14は、支持台13により回転移送されたキュベット250を回転搬送部20に供給するために設けられている。
【0032】
また、図2に示すように、検出機構部2には、上述した供給用キャッチャ部14から所定の間隔を隔てて、キュベット250を廃棄するための廃棄用孔15と、廃棄用孔15の下方に設置された廃棄ボックス16とが設けられている。上述した供給用キャッチャ部14は、回転搬送部20のキュベット搬送テーブル23上のキュベット250を、廃棄用孔15を介して廃棄ボックス16に廃棄することが可能である。すなわち、供給用キャッチャ部14は、キュベット250の供給と廃棄との両方を行うことが可能である。
【0033】
回転搬送部20は、キュベット供給機構部10から供給されたキュベット250と、血液検体を凝固させる試薬を収容した試薬容器(図示せず)とを回転方向に搬送するために設けられている。この回転搬送部20は、図2に示すように、円形状の試薬テーブル21と、円形状の試薬テーブル21の外側に配置された円環形状の試薬テーブル22と、円環形状の試薬テーブル22の外側に配置された円環形状のキュベット搬送テーブル23とにより構成されている。これらのキュベット搬送テーブル23、試薬テーブル21および試薬テーブル22は、それぞれ、時計回り方向および反時計回り方向の両方に回転可能で、かつ、各々のテーブルが互いに独立して回転可能なように構成されている。
【0034】
試薬テーブル21および22は、図2に示すように、それぞれ、円周方向に沿って所定の間隔を隔てて設けられた複数の孔部21aおよび22aを含んでいる。試薬テーブル21および22の孔部21aおよび22aは、血液を凝固させる試薬を収容した複数の試薬容器(図示せず)を載置するために設けられている。また、キュベット搬送テーブル23は、それぞれ、円周方向に沿って所定の間隔を隔てて設けられた円筒形状の複数の保持部23aを含んでいる。保持部23aは、キュベット供給機構部10から供給されたキュベット250を保持するために設けられている。また、キュベット搬送テーブル23の保持部23aに保持されたキュベット250には、検体分注アーム30によって搬送機構部3に載置されるラック201に収納された試験管200に収容されている血液検体が分注される。
【0035】
検体分注アーム30は、搬送機構部3により吸引位置2aに搬送された試験管200に収容される血液検体を吸引するとともに、吸引した血液検体を回転搬送部20に移送されたキュベット250内に分注する機能を有している。
【0036】
ランプユニット40は、図2に示すように、測定部70で行われる光学的な測定に用いられる光を供給するために設けられている。このランプユニット40は、図4および図5に示すように、光源としてのハロゲンランプ41と、集光レンズ42a〜42cと、円盤形状のフィルタ部43と、モータ44と、光透過型のセンサ45と、光ファイバカプラ46と、21本の分岐光ファイバ47(図5参照)とから構成されている。
【0037】
ハロゲンランプ41は、図4に示すように、ハロゲンランプ41が発熱することによって熱せられた空気を冷却するための複数のフィンを有するランプケース41aに収容されている。集光レンズ42a〜42cは、ハロゲンランプ41から照射された光を集光する機能を有している。そして、集光レンズ42a〜42cは、ハロゲンランプ41から照射された光を光ファイバカプラ46に導く光路上に配置されている。また、ハロゲンランプ41から照射されて集光レンズ42a〜42cにより集光された光は、後述するフィルタ部43の光学フィルタ43b〜43fのいずれか1つを透過して光ファイバカプラ46に導かれる。
【0038】
また、ランプユニット40のフィルタ部43は、図4に示すように、モータ44のモータ軸(図示せず)を中心に回転可能に取り付けられている。これにより、モータ44の駆動によって、フィルタ部43が軸を中心として回転するように構成されている。このフィルタ部43は、図6および図7に示すように、5つの光透過特性(透過波長)のそれぞれ異なる光学フィルタ43b〜43fが設けられるフィルタ板43aを備えている。フィルタ板43aには、光学フィルタ43b〜43fを取り付けるための5つの孔43gと、光が透過しないように閉塞される孔43hとが設けられている。そして、5つの孔43gには、それぞれ、光透過特性(透過波長)の異なる5つの光学フィルタ43b、43c、43d、43eおよび43fが設置されている。この孔43gおよび43hは、フィルタ部43の回転方向に沿って所定の角度間隔(第1実施形態では、60°の等間隔)で設けられている。なお、孔43hは、予備の孔であり、フィルタの追加が必要となった場合には、フィルタが装着される。
【0039】
光学フィルタ43b、43c、43d、43eおよび43fは、それぞれ、340nm、405nm、575nm、660nmおよび800nmの波長の光を透過し、その他の波長の光は透過しない。したがって、光学フィルタ43b、43c、43d、43eおよび43fを透過した光は、それぞれ、340nm、405nm、575nm、660nmおよび800nmの波長特性を有する。
【0040】
また、図7に示すように、フィルタ板43aは、円周方向に沿って所定の角度間隔(第1実施形態では、60°の等間隔)で6つのスリットが設けられている。それら6つのスリットのうち1つは、他の5つの通常スリット43iよりもフィルタ板43aの回転方向のスリット幅が大きい原点スリット43jである。原点スリット43jおよび通常スリット43iは、隣接する孔43gおよび43hの間の中間角度位置に所定の角度間隔(第1実施形態では、60°の等間隔)で形成されている。
【0041】
また、ランプユニット40から後述するキュベット載置部71のキュベット250に光が照射される際には、フィルタ部43が実質的に等速回転するようにモータ44の駆動が制御基板5により制御されるように構成されている。したがって、フィルタ板43aの回転に伴って、集光レンズ42a〜42c(図4参照)により集光された光の光路上に光透過特性の異なる5つの光学フィルタ43b〜43fと、1つの遮光された孔43h(図5参照)とが断続的に順次配置される。このため、波長特性の異なる5種類の光が断続的に順次照射される。なお、第1実施形態では、フィルタ部43は、0.1秒間に1回転するように構成されている。したがって、後述するキュベット載置部71のキュベット250には、0.1秒間に5種類の波長特性の異なる光が時分割で順次照射される。そして、測定部70では、光電変換素子72b(参照光用光電変換素子72e)により、0.1秒間毎に5種類の波長に対応する5個の電気信号が取得されるように構成されている。
【0042】
また、光透過型のセンサ45は、図6に示すように、フィルタ部43の回転に伴う原点スリット43jおよび通常スリット43iの通過を検出するために設けられている。このセンサ45は、原点スリット43jおよび通常スリット43iが通過すると、スリットを介して光源からの光を受光部が検出し、検出信号を出力する。なお、原点スリット43jは、通常スリット43iよりもスリット幅が大きいので、原点スリット43jが通過した場合には、センサ45から出力される検出信号は、通常スリット43iが通過した場合の検出信号よりも、出力期間が長い。したがって、センサ45からの検出信号に基づいて、フィルタ部43が正常に回転しているか否かを監視することが可能となる。
【0043】
また、光ファイバカプラ46は、21本の分岐光ファイバ47に光学フィルタ43b〜43fを通過した光を入射させる機能を有している。つまり、光ファイバカプラ46は、21本の分岐光ファイバ47に対して、同時に同質の光を導いている。また、21本の分岐光ファイバ47の先端は、図2に示すように、測定部70に接続されており、ランプユニット40からの光を測定部70にセットされるキュベット250内の測定用試料に導いている。具体的には、図8および図9に示すように、21本の分岐光ファイバ47は、それぞれ、測定部70の後述する20個の挿入孔71aおよび1つの参照光用測定孔71bの側面から、保持されているキュベット250に対して光を供給するように配置されている。したがって、光学フィルタ43b〜43fを断続的に通過する波長特性の異なる5種類の光は、分岐光ファイバ47を介して、測定部70の各々に供給されている。
【0044】
試薬分注アーム50は、図1および図2に示すように、回転搬送部20に載置された試薬容器(図示せず)内の試薬を回転搬送部20に保持されたキュベット250に分注することにより、キュベット250内の血液検体に試薬を混合するために設けられている。血液検体に試薬が添加されることにより、測定用試料が調製される。また、キュベット移送部60は、キュベット250を回転搬送部20と測定部70との間で移送するために設けられている。
【0045】
測定部70は、血液検体に試薬を混和して調製された測定用試料の加温を行うとともに、ランプユニット40によって複数の波長の光が照射された測定用試料から光を経時的に受け、各々の波長について、経時的な光学的な情報を取得するために設けられている。具体的には、測定部70は、ランプユニット40から照射される5種類の光(340nm、405nm、575nm、660nmおよび800nm)を用いて、経過時間毎に透過光量を取得している。なお、分岐光ファイバ47から照射される660nmの波長を有する光は、Fbg(フィブリノーゲン量)、PT(プロトロンビン時間)およびAPTT(活性化部分トロンボプラスチン時間)などの凝固時間法による測定項目を測定する際に用いられるメイン波長である。また、800nmの波長を有する光は、Fbg、PTおよびAPTTなどの凝固時間法による測定項目を測定する際に用いられるサブ波長である。合成基質法の測定項目であるATIIIの測定波長は405nmであり、免疫比濁法の測定項目であるDダイマーおよびFDPの測定波長は800nmである。また、血小板凝集の測定波長は、575nmである。このように、第1実施形態に係る血液凝固分析装置1は、1つの光源としてのハロゲンランプ41から照射された光をフィルタ部43の光学フィルタ43b〜43fに通して複数の波長の光を得、これらの光を用いて様々な測定項目の測定を行うように構成されている。
【0046】
この測定部70は、図2に示すように、キュベット載置部71と、キュベット載置部71の下方に配置された検出部72とにより構成されている。キュベット載置部71には、図9に示すように、キュベット250を挿入するための20個の挿入孔71aと、キュベット250を挿入せずに参照光を測定するための1つの参照光用測定孔71bとが設けられている。また、キュベット載置部71には、挿入孔71aに挿入されたキュベット250を所定の温度に加温するための加温部71cが設けられている。
【0047】
また、参照光用測定孔71bは、分岐光ファイバ47から照射された光の特性を監視するために設けられている。具体的には、分岐光ファイバ47から照射された光を直接検出部72の参照光用光電変換素子72eに受光させることにより、ランプユニット40のハロゲンランプ41(図4参照)に由来する揺らぎなどの特性を電気信号として検出している。そして、検出した光の特性(電気信号)を挿入孔71aに挿入されたキュベット250内の測定用試料の透過光に対応する信号から減算処理することにより、測定用試料の透過光に対応する信号を補正する。これにより、光学的な情報の測定毎に光の特性による微差が生じるのを抑制することが可能である。
【0048】
また、測定部70の検出部72は、挿入孔71aに挿入されたキュベット250内の測定用試料に対して複数の条件下で光学的な測定を行うことが可能なように構成されている。この検出部72には、図8および図9に示すように、キュベット250が挿入される各挿入孔71aに対応して、コリメータレンズ72a、光電変換素子72bおよびプリアンプ72cが設けられる。また、図8に示すように、参照光用測定孔71bに対応して、参照光用コリメータレンズ72d、参照光用光電変換素子72eおよび参照光用プリアンプ72fが設けられている。また、図10に示すように、20個の挿入孔71aのうち所定の挿入孔の下部には、回転可能なマグネット72gが配置されている。血小板凝集法により測定を行う場合には、測定試料が収容されたキュベット250に、磁性を有する棒状のスターラーバー260が投入される。このスターラーバー260がマグネット72gの回転に伴い回転することにより、測定中に測定試料を攪拌することが可能である。このような構成により、第1実施形態による血液凝固分析装置1は、血小板凝集法による測定を行うことが可能に構成されている。
【0049】
コリメータレンズ72aは、図8に示すように、ランプユニット40(図1参照)からの光を誘導する分岐光ファイバ47の端部と、対応する挿入孔71aとの間に設置されている。このコリメータレンズ72aは、分岐光ファイバ47から出射された光を平行光にするために設けられている。また、光電変換素子72bは、挿入孔71aを挟んで分岐光ファイバ47の端部に対向するように設置された基板73の挿入孔71a側の面に取り付けられている。プリアンプ72cは、基板73の挿入孔71aと反対側の面に取り付けられている。また、光電変換素子72bは、挿入孔71aに挿入されたキュベット250内の測定用試料に光を照射したときに測定用試料を透過する光(以下、透過光という)を検出するとともに、検出した透過光に対応する電気信号(アナログ信号)を出力する機能を有している。検出部72のプリアンプ72cは、光電変換素子72bからの電気信号(アナログ信号)を増幅するために設けられている。
【0050】
また、参照光用測定孔71bに対応して検出部72に設けられた参照光用コリメータレンズ72d、参照光用光電変換素子72eおよび参照光用プリアンプ72fは、それぞれ、挿入孔71aに対応して検出部72に設けられたコリメータレンズ72a、光電変換素子72bおよびプリアンプ72cと同様に構成されている。なお、参照光用光電変換素子72eには、参照光として、分岐光ファイバ47から出射された光が参照光用コリメータレンズ72dを透過した後、直接入射されるように構成されている。すなわち、参照光用光電変換素子72eは、測定用試料を収容するキュベット250を介さずに照射される参照光を検出するとともに、検出した参照光に対応する電気信号(アナログ信号)を出力するように構成されている。
【0051】
制御基板5は、測定部70の下方に配置されている。この制御基板5は、検出機構部2および搬送機構部3などの動作の制御や、測定部70から出力された光学的情報(電気信号)の処理および記憶などを行う機能を有している。また、制御基板5には、図11および図12に示すように、信号処理部501、装置側制御部502、増幅回路503、微分回路504および温度コントローラ505(図12参照)が設けられている。信号処理部501は、ランプユニット40から測定用試料に光が照射されたときに、光電変換素子72bが透過光を検出して出力する信号の処理を行うために設けられている。この信号処理部501は、図12に示すように、3つのマルチプレクサ(MUX)501aと、3つのオフセット回路501bと、3つのアンプ501cと、3つのA/D変換部501dとを有している。そして、それぞれ1つのマルチプレクサ501a、オフセット回路501b、アンプ501cおよびA/D変換部501dによって、1つの信号処理ラインL0が構成されている。信号処理部501には、この信号処理ラインL0に加えて、信号処理ラインL0と同様の構成を有する信号処理ラインL1およびL2が設けられている。すなわち、信号処理部501には、検出部72から出力された複数のアナログ信号の処理を行うための3つの信号処理ラインL0〜L2が設けられている。
【0052】
図13に示すように、マルチプレクサ501aは、複数のプリアンプ72c(参照光用プリアンプ72f)に接続されている。このマルチプレクサ501aは、複数の光電変換素子72b(参照光用光電変換素子72e)からプリアンプ72c(参照光用プリアンプ72f)を介して入力される複数のアナログ信号から1つずつ選択して順次オフセット回路501bへ出力するように構成されている。オフセット回路501bは、マルチプレクサ501aから出力された信号の補正を行う機能を有している。具体的には、オフセット回路501bは、測定に用いられた挿入孔71aまたは参照光用測定孔71bに対応したオフセット値が装置側制御部502(図12参照)から供給される。そして、オフセット回路501bは、マルチプレクサ501aから出力される透過光に対応する信号から上記のオフセット値を減算処理することにより、マルチプレクサ501aから出力される透過光に対応する信号を補正するように構成されている。
【0053】
アンプ501cは、オフセット回路501bから出力されたアナログ信号を増幅する機能を有している。このアンプ501cのゲイン(増幅率)は、Lゲイン、および、Lゲインよりも高い値のHゲインの2種類に切り替えられるように装置側制御部502により制御される。そして、アンプ501cにより増幅されたLゲイン(増幅率)の信号とHゲイン(増幅率)の信号とは、それぞれ、互いに異なるタイミングでA/D変換部501dに入力されるように構成されている。A/D変換部501dは、それぞれ、アンプ501cに接続されており、そのアンプ501cによりLゲインおよびHゲインの信号(アナログ信号)に増幅された処理済アナログ信号をデジタル信号(データ)に変換するために設けられている。
【0054】
なお、第1実施形態では、A/D変換部501dからは、図13に示すように、チャンネルCH0〜CH47に対応する48個(1つのA/D変換部につき16個)のデータが出力されるように構成されている。なお、このチャンネルCH0〜CH47の内、チャンネルCH0〜CH41の42個のチャンネルのデータは、それぞれ、各光電変換素子72bまたは参照光用光電変換素子72eから得られた電気信号に基づいたデータに対応している。すなわち、20個の光電変換素子72bから得られた20個のデータは、それぞれ、信号処理部501のアンプ501cによりLゲイン(増幅率)およびHゲイン(増幅率)で増幅されることによって40個のデータになる。また、1つの参照光用光電変換素子72eから得られた1つのデータは、信号処理部501(図12参照)のアンプ501cにおいてLゲイン(増幅率)およびHゲイン(増幅率)で増幅されることにより2つのデータになる。この40個のデータと、参照光に対応する2つのデータとを合計した42個のデータがチャンネルCH0〜CH41のデータに対応している。なお、チャンネルCH0〜CH47の内、残りの6つのチャンネルCH42〜CH47は、第1実施形態では使用されない予備のチャンネルであり、このチャンネルCH42〜CH47のデータは、光電変換素子72bまたは参照光用光電変換素子72eからの電気信号には対応していない。
【0055】
また、装置側制御部502は、検出機構部2および搬送機構部3の動作を制御する機能と、A/D変換部501dから出力されるデジタル信号(データ)を取得して記憶する機能とを有している。この装置側制御部502は、図12に示すように、コントローラ502a、フィルタ部回転監視部502b、モータコントローラ502c、マルチプレクサ制御部502d、オフセットインターフェイス502e、アンプインターフェイス502f、A/D変換部インターフェイス502g、ロガー用メモリ502h、設定用メモリ502i、コントローラステータスレジスタ502jおよびローカルバスインターフェイス502kを含んでいる。
【0056】
コントローラ502aは、装置側制御部502による各種の制御を統括する機能を有している。また、フィルタ部回転監視部502bは、ランプユニット40のフィルタ部43が正常に回転しているか否かを監視するために設けられている。このフィルタ部回転監視部502bには、フィルタ部43の回転に伴う原点スリット43j(図7参照)または通常スリット43iの通過を検出するセンサ45からの検出信号が入力されるように構成されている。そして、フィルタ部回転監視部502bにより、センサ45から原点スリット43j(図7参照)の検出信号が出力される時間間隔と、センサ45から通常スリット43i(図7参照)の検出信号が出力される時間間隔と、センサ45から原点スリット43jの検出信号が出力されてから次に再度原点スリット43jの検出信号が出力されるまでの間に通常スリット43iの検出信号が出力される回数とが監視されることによって、フィルタ部43が正常に回転しているか否かが監視される。また、モータコントローラ502cは、フィルタ部43を回転させるモータ44の回転数を制御する機能を有している。また、マルチプレクサ制御部502dは、マルチプレクサ501aの動作を制御する機能を有している。具体的には、マルチプレクサ制御部502dは、複数のマルチプレクサ501aがアナログ信号を選択する時刻をそれぞれ異ならせるようにマルチプレクサ501aの動作を制御している。
【0057】
また、コントローラ502aは、図12に示すように、オフセットインターフェイス502e、アンプインターフェイス502fおよびA/D変換部インターフェイス502gを介してそれぞれ信号処理部501のオフセット回路501b、アンプ501cおよびA/D変換部501dの動作の制御を行うように構成されている。具体的には、コントローラ502aは、オフセットインターフェイス502eを介してオフセット回路501bに所定のオフセット値を供給するとともに、オフセット回路501bがマルチプレクサ501aからの信号からそのオフセット値を減算することにより補正処理を行うのを制御する。また、コントローラ502aは、アンプインターフェイス502fを介してアンプ501cがLゲインおよびHゲインになるように制御するとともに、アンプ501cによるオフセット回路501bからの信号の増幅処理を制御する。また、コントローラ502aは、A/D変換部インターフェイス502gを介してA/D変換部501dによるアンプ501cからの信号(アナログ信号)のデジタル信号への変換処理を制御する。また、A/D変換部501dにより取得されたデジタル信号(データ)は、A/D変換部インターフェイス502gおよびコントローラ502aを介してロガー用メモリ502hに入力されるとともに記憶されるように構成されている。この際、コントローラ502aは、複数のA/D変換部501dが複数のデジタル信号を出力する期間が互いに重複しないように、A/D変換部インターフェイス502gを介してA/D変換部501dの動作を制御している。
【0058】
また、コントローラ502aは、所定の信号処理ライン(L0からL2のいずれか)のマルチプレクサ501a、オフセット回路501bおよびアンプ501cによるアナログ信号処理が行われる期間に、その所定の信号処理ラインとは別の信号処理ラインのA/D変換部501dによる変換処理および装置側制御部502のロガー用メモリ502hへのデータ記憶処理が行われるように、各信号ラインL0〜L2におけるマルチプレクサ501a、オフセット回路501b、アンプ501c、A/D変換部501dおよびロガー用メモリ502hのうち処理を実行するものを切り替える機能を有する。なお、この点については、後の分析動作の説明において詳細に説明する。
【0059】
ロガー用メモリ502hは、所定の光電変換素子72bから出力されたアナログ信号に対応するデジタル信号(データ)を、ロガー用メモリ502hのアドレスによって識別可能に記憶するために設けられている。このロガー用メモリ502hは、図14に示すように、128バイト単位の32個のエリア0〜31によって構成されている。このエリア0〜31には、それぞれ、5つの光学フィルタ43b〜43f(図7参照)の透過光に対応するデータおよび閉塞された孔43hに対応するデータが記憶される。すなわち、フィルタ部43が1回転する毎に、5つの異なる光透過特性を有する光学フィルタ43b〜43fの透過光に対応するデータが発生する。そして、これらの5つのデータがそれぞれロガー用メモリ502h(図14参照)のエリア0から順番にエリア毎に記憶される。また6番目のエリアには、孔43hに対応するデータとして“0”が記憶される。これにより、フィルタ部43の1回転(約100msec)毎にロガー用メモリ502hの6つのエリアが使用されるとともに、エリア31まで使用された後は、エリア0に戻ってデータが上書きされるように構成されている。
【0060】
また、ロガー用メモリ502hの各エリア0〜31は、それぞれ、128個のアドレスを有している。たとえば、エリア0は、000h〜00Fh、010h〜01Fh、020h〜02Fh、030h〜03Fh、040h〜04Fh、050h〜05Fh、060h〜06Fhおよび070h〜07Fhの128個のアドレスを有している。そして、000h〜05Fhの96個のアドレスに上記したチャンネルCH0〜CH47(図13参照)のデータが記憶されるように構成されている。チャンネルCH0〜CH47の各データは、それぞれ、2つのアドレスに記憶されるように構成されている。なお、前述のように第1実施形態では、チャンネルCH42〜47からはデータが出力されないので、これらのチャンネルに対応するアドレスには、データは記憶されない。
【0061】
また、図14に示したロガー用メモリ502hのエリア0におけるアドレス060h〜06Fhおよび070h〜07Ehは、第1実施形態ではデータの記憶されない予備のアドレスである。また、エリア0の最後のアドレス07Fhには、フィルタ番号(0〜4)が記憶される。このフィルタ番号(0〜4)は、5つの光学フィルタ43b〜43f(図7参照)を識別するための番号である。光学フィルタは、原点スリット43jが通過するタイミングを検出することによって識別できる。この5つの光学フィルタ43b〜43fに対応するフィルタ番号(0〜4)がアドレス07Fhに記憶されることにより、エリア0に記憶されたデータがどの光学フィルタ(43b〜43f)の透過光に対応するデータかが識別されるように構成されている。
【0062】
また、図12に示した設定用メモリ502iは、オフセット回路501bに供給するオフセット値と、アンプ501cに供給するゲイン(増幅率)などの設定値を記憶させるために設けられている。また、コントローラステータスレジスタ502jは、フィルタ部43が正常に回転しているか否か、A/D変換部501dによるアナログ信号からデジタル信号への変換エラーの有無、制御部4aによるロガー用メモリ502hからのデータの取得状況、および、制御部4aからの測定開始の指示の有無といった情報を一時的に記憶するために設けられている。また、装置側制御部502は、ローカルバスインターフェイス502kおよびインターフェイス506を介して、ロガー用メモリ502hに記憶された測定用試料のデータ(光学的情報)を制御部4aに送信する機能を有するように構成されている。
【0063】
また、図12に示した制御基板5の増幅回路503は、参照光用光電変換素子72e(図13参照)から参照光用プリアンプ72fを介して出力された信号が入力されるとともに、その入力された信号を増幅する機能を有している。この増幅回路503は、図15に示すように、2つの抵抗503aおよび503bと、1つのオペアンプ503cとによって構成されている。抵抗503aの一方端には、参照光用プリアンプ72fからの参照光に対応する信号が入力されるとともに、他方端は、オペアンプ503cの反転入力端子に接続されている。また、抵抗503bは、オペアンプ503cの出力端子と反転入力端子との間に接続されている。また、オペアンプ503cの非反転入力端子は、接地されている。また、オペアンプ503cの出力は、信号処理部501(図12参照)のマルチプレクサ501aと、微分回路504とにそれぞれ入力されるように構成されている。
【0064】
制御基板5の微分回路504は、増幅回路503からの参照光に対応する信号(以下、参照信号という)の微分信号を生成する機能を有している。この微分回路504は、図15に示すように、2つの抵抗504aおよび504bと、2つのコンデンサ504cおよび504dと、1つのオペアンプ504eとによって構成されている。抵抗504aの一方端には、増幅回路503からの参照信号が入力されるとともに、他方端は、コンデンサ504cの一方電極に接続されている。また、コンデンサ504cの他方電極はオペアンプ504eの反転入力端子に接続されている。また、抵抗504bおよびコンデンサ504dは、共に、オペアンプ504eの出力端子と反転入力端子との間に接続されている。また、オペアンプ504eの非反転入力端子は、接地されている。また、オペアンプ504eの出力は、図示しないコンパレータを介して装置側制御部502(図12参照)のコントローラ502aへ入力されるように構成されている。
【0065】
また、図12に示した制御基板5の温度コントローラ505は、測定部70の加温部71c(図2参照)の温度を制御する機能を有している。この温度コントローラ505は、図12に示すように、インターフェイス506を介して制御部4aから入力される設定温度(約37°)に応じて、測定部70の加温部71cの温度を制御するように構成されている。
【0066】
緊急検体セット部80は、図1および図2に示すように、緊急を要する血液検体に対しての検体分析処理を行うために設けられている。この緊急検体セット部80は、搬送機構部3から供給された血液検体に対しての検体分析処理が行われている際に、緊急検体を割り込ませることが可能なように構成されている。また、流体部90は、血液凝固分析装置1のシャットダウン処理の際に、各分注アームに設けられるノズルに洗浄液などの液体を供給するために設けられている。
【0067】
制御装置4(図1参照)は、パーソナルコンピュータ(PC)などからなり、CPU、ROM、RAMなどからなる制御部4aと、表示部4bと、キーボード4cとを含んでいる。また、表示部4bは、血液検体中に存在する干渉物質(ヘモグロビン、乳び(脂質)およびビリルビン)に関する情報や、測定部70から送信されたデジタル信号のデータを分析して得られた分析結果(凝固時間)などを表示するために設けられている。
【0068】
次に、制御装置4の構成について説明する。制御装置4は、図3に示すように、制御部4aと、表示部4bと、キーボード4cとから主として構成されたコンピュータ401によって構成されている。制御部4aは、CPU401aと、ROM401bと、RAM401cと、ハードディスク401dと、読出装置401eと、入出力インタフェース401fと、通信インタフェース401gと、画像出力インタフェース401hとから主として構成されている。CPU401a、ROM401b、RAM401c、ハードディスク401d、読出装置401e、入出力インタフェース401f、通信インタフェース401g、および画像出力インタフェース401hは、バス401iによって接続されている。
【0069】
CPU401aは、ROM401bに記憶されているコンピュータプログラムおよびRAM401cにロードされたコンピュータプログラムを実行することが可能である。そして、後述するようなアプリケーションプログラム404aをCPU401aが実行することにより、コンピュータ401が制御装置4として機能する。
【0070】
ROM401bは、マスクROM、PROM、EPROM、EEPROMなどによって構成されており、CPU401aに実行されるコンピュータプログラムおよびこれに用いるデータなどが記録されている。
【0071】
RAM401cは、SRAMまたはDRAMなどによって構成されている。RAM401cは、ROM401bおよびハードディスク401dに記録されているコンピュータプログラムの読み出しに用いられる。また、これらのコンピュータプログラムを実行するときに、CPU401aの作業領域として利用される。
【0072】
ハードディスク401dは、オペレーティングシステムおよびアプリケーションプログラムなど、CPU401aに実行させるための種々のコンピュータプログラムおよびそのコンピュータプログラムの実行に用いるデータがインストールされている。第1実施形態に係る血液凝固時間測定用のアプリケーションプログラム404aも、このハードディスク401dにインストールされている。
【0073】
読出装置401eは、フレキシブルディスクドライブ、CD−ROMドライブ、またはDVD−ROMドライブなどによって構成されており、可搬型記録媒体404に記録されたコンピュータプログラムまたはデータを読み出すことができる。また、可搬型記録媒体404には、血液凝固時間測定用のアプリケーションプログラム404aが格納されており、コンピュータ401がその可搬型記録媒体404からアプリケーションプログラム404aを読み出し、そのアプリケーションプログラム404aをハードディスク401dにインストールすることが可能である。
【0074】
なお、上記アプリケーションプログラム404aは、可搬型記録媒体404によって提供されるのみならず、電気通信回線(有線、無線を問わない)によってコンピュータ401と通信可能に接続された外部の機器から上記電気通信回線を通じて提供することも可能である。たとえば、上記アプリケーションプログラム404aがインターネット上のサーバコンピュータのハードディスク内に格納されており、このサーバコンピュータにコンピュータ401がアクセスして、そのアプリケーションプログラム404aをダウンロードし、これをハードディスク401dにインストールすることも可能である。
【0075】
また、ハードディスク401dには、たとえば、米マイクロソフト社が製造販売するWindows(登録商標)などのグラフィカルユーザインタフェース環境を提供するオペレーティングシステムがインストールされている。以下の説明においては、第1実施形態に係るアプリケーションプログラム404aは上記オペレーティングシステム上で動作するものとしている。
【0076】
出力インタフェース401fは、たとえば、USB、IEEE1394、RS−232Cなどのシリアルインタフェース、SCSI、IDE、IEEE1284などのパラレルインタフェース、およびD/A変換器、A/D変換器などからなるアナログインタフェースなどから構成されている。入出力インタフェース401fには、キーボード4cが接続されており、ユーザがそのキーボード4cを使用することにより、コンピュータ401にデータを入力することが可能である。
【0077】
通信インタフェース401gは、たとえば、Ethernet(登録商標)インタフェースである。コンピュータ401は、その通信インタフェース401gにより、所定の通信プロトコルを使用して検出機構部2との間でデータの送受信が可能である。
【0078】
画像出力インタフェース401hは、LCDまたはCRTなどで構成された表示部4bに接続されており、CPU401aから与えられた画像データに応じた映像信号を表示部4bに出力するようになっている。表示部4bは、入力された映像信号にしたがって、画像(画面)を表示する。
【0079】
また、制御部4aのハードディスク401dにインストールされた血液凝固時間測定用のアプリケーションプログラム404aは、検出機構部2の測定部70から送信された測定用試料の透過光量(デジタル信号のデータ)を用いて、測定用試料の凝固時間を測定している。この凝固時間は、キュベット250内の血液検体を凝固させる試薬が添加された時点から、測定用試料(試薬が添加された血液検体)が流動性を失うまでの時間(凝固時間)である。この測定用試料が流動性を失う凝固反応は、血液検体中のフィブリノーゲンが、添加された試薬によりフィブリンに変化する反応である。そして、第1実施形態の血液凝固分析装置1では、血液検体中のフィブリノーゲン量に依存して反応するこの凝固反応を、測定用試料の透過光量の変化量(反応前の透過光量と反応後の透過光量との差)によって確認している。
【0080】
次に、図1、図4および図16を参照して、制御装置4の制御部4aによる血液凝固分析装置1の装置本体(検出機構部2および搬送機構部3)の制御の概略について説明する。
【0081】
血液凝固分析装置1は、制御装置4および装置本体の電源を投入することによって起動する。
【0082】
これらの電源が投入されると、まず、図16に示したステップS1において、PC本体4bにより、初期設定が行われる。この初期設定では、制御部4aに記憶されているソフトウェアの初期化や、後述するpクロックを制御基板5の装置側制御部502から取得する処理などが行われる。なお、装置本体(検出機構部2および搬送機構部3)の電源投入により、ステップS1の初期設定時には、ランプユニット40(図4参照)のハロゲンランプ41から光が照射されるとともに、フィルタ部43が10回転/秒の回転速度での等速回転を開始する。このハロゲンランプ41からの光の照射、および、フィルタ部43の回転は、装置本体(検出機構部2および搬送機構部3)の電源がオフ状態にされるまで継続される。そして、ステップS2において、使用者による検体分析情報の入力を受け付ける処理が行われる。すなわち、使用者は、制御装置4(図1参照)のキーボード4cを用いて、表示部4bに出力される検体分析一覧表中の検体番号および測定項目の欄などに情報の入力を行う。これらの検体分析情報は、制御部4aに保存される。
【0083】
そして、ステップS3において、制御部4aにより分析処理の指示が行われる。これにより、装置本体(検出機構部2および搬送機構部3)による分析処理が行われる。その後、ステップS4において、制御部4aにより、血液凝固分析装置1のシャットダウンの指示が入力されたか否かが判断される。そして、ステップS4において、制御部4aにより、血液凝固分析装置1のシャットダウンの指示が入力されていないと判断された場合には、ステップS2に戻り、使用者による他の検体分析情報の入力を受け付ける処理が行われる。一方、ステップS4において、制御部4aにより、血液凝固分析装置1のシャットダウンの指示が入力されたと判断された場合には、ステップS5において、シャットダウン処理が行われる。このシャットダウン処理により、血液凝固分析装置1の電源が自動的にオフ状態になり、血液凝固分析装置1の動作が終了される。
【0084】
次に、図4、図8、図11、図12、図17および図18を参照して、制御基板5の装置側制御部502によるpクロックの算出処理の方法について詳細に説明する。
【0085】
まず、図17のステップS11において、フィルタ部43が回転している状態で、装置側制御部502により、センサ45からの信号に基づいてセンサ45がスリットを検出した時点のクロック数N21が検出される。次に、図18に示すように、フィルタ部43(図4参照)の等速回転中に、ランプユニット40から参照光用光電変換素子72e(図8参照)に入射される参照光の光量は、「参照光の光量」として示した波形のように変化する。なお、図18中の期間Aは、ランプユニット40(図4参照)において、回転しているフィルタ部43のいずれかの光学フィルタ43b〜43fがハロゲンランプ41からの光の通路に配置される期間である。この期間Aにおいて、ハロゲンランプ41からの光の通路に光学フィルタ43b〜43fが差し掛かると、参照光の光量は徐々に増加し始める。その後、ハロゲンランプ41からの光の通路が完全に光学フィルタ43b〜43f内に収まることにより、参照光の光量は一定となる。その後、ハロゲンランプ41からの光の通路から光学フィルタ43b〜43fが外れ始めると、参照光の光量は徐々に減少し始めるとともに、ハロゲンランプ41からの光の通路から光学フィルタ43b〜43fが完全に外れると参照光の光量は0になる。
【0086】
そして、参照光は、図11に示すように、参照光用光電変換素子72eにより電気信号に変換されるとともに、その変換された電気信号は、参照光用プリアンプ72fおよび増幅回路503により増幅される。そして、増幅回路503から参照光に対応する信号(以下、参照信号という)が出力されるとともに、この参照信号は、微分回路504に入力される。そして、微分回路504により、図18に「参照信号の微分信号」として示した波形を有する参照信号の微分信号が生成される。この参照信号の微分信号は、コンパレータ(図示せず)を介して微分回路504(図12参照)から装置側制御部502に入力される。
【0087】
そして、図17のステップS12において、装置側制御部502により、この参照信号の微分信号が所定の負のしきい値(+)に到達した時点のクロック数N1が検出される。具体的には、図18に示すように、参照光の光量の増加に伴って参照信号の微分信号が立ち上がる。そして、微分信号が所定の正のしきい値(+)に到達するのに応答して、微分回路504(図12参照)から微分信号が入力される図示しないコンパレータにおいてHレベルに立ち上がるパルス信号が出力される。このパルス信号は、装置側制御部502のコントローラ502aに入力されるとともに、コントローラ502aでは、パルス信号がHレベルに立ち上った時点のクロック数N1が検出される。このようにして、装置側制御部502のコントローラ502aにより、参照信号の微分信号が所定の正のしきい値(+)に到達した時点のクロック数N1が検出される。
【0088】
この後、図18に示すように、参照光の光量はさらに増加するとともに、所定の値で一定となる。そして、その後、参照光の光量は徐々に減少する。これに伴って、参照信号の微分信号は、徐々に立ち下がる。そして、図17のステップS13において、装置側制御部502により、参照信号の微分信号が所定の負のしきい値(−)に到達した時点のクロック数(N2)が検出される。具体的には、参照信号の微分信号が徐々に立ち下がるとともに、所定の負のしきい値(−)に到達するのに応答して、微分回路504(図12参照)から微分信号が入力される図示しないコンパレータにおいてHレベルに立ち上がるパルス信号が出力される。このパルス信号は、装置側制御部502のコントローラ502aに入力されるとともに、コントローラ502aでは、パルス信号がHレベルに立ち上った時点のクロック数N2が検出される。このようにして、装置側制御部502のコントローラ502aにより、参照信号の微分信号が所定の負のしきい値(−)に到達した時点のクロック数N2が検出される。
【0089】
そして、図17のステップS14において、装置側制御部502により、クロック数N1からクロック数N2までの間にカウントされるクロック数(Nクロック)がN=N2−N1の式により算出される。そして、ステップS15において、装置側制御部502により、測定用試料の透過光に対応する信号の取得を開始するタイミングを決定するためのクロック数(nクロック)がn=(N−m)/2の式を用いて算出される。なお、この式において、mクロックは、装置側制御部502が測定用試料の透過光に対応する信号を取得する際に要する適切な期間として予め設定されたクロック数である。
【0090】
そして、ステップS16において、制御基板5の装置側制御部502により、スリットの検出から参照信号の立ち上がりまでのクロック数(Pクロック)がP=N1−N21の式を用いて算出される。そして、ステップS17において、装置側制御部502により、測定用試料の透過光に対応する信号の取得を開始するタイミングを決定するためのクロック数(pクロック)がp=P+nの式を用いて算出される。このように、第1実施形態では、フィルタ部43に設けられたスリットを用いて、装置側制御部502が透過光に対応する信号の取得を開始するタイミングを算出している。
【0091】
そして、図18からわかるように、N21クロックから上記のように算出したpクロック後に、マルチプレクサ501aによりmクロックの期間だけ測定用試料の透過光に対応する検出部72からの信号の取得を行えば、ランプユニット40からの照射光の光量が安定している期間の信号を取得することができる。
【0092】
次に、図8、図12、図13および図19〜図21を参照して、上記した図16のステップS3の処理について詳細に説明する。
【0093】
まず、図19のステップS21において、制御部4aにより検体の吸引が指示される。これにより、回転搬送部20に保持されたキュベット250から検体分注アーム30により検体が吸引される。
【0094】
そして、ステップS22において、制御部4aにより測定用試料の調製が指示される。これにより、検出機構部2において、検体分注アーム30により吸引された検体が複数のキュベット250に分注されるとともに、試薬分注アーム50により、試薬容器(図示せず)内の血液の凝固を開始させるための試薬がそれらの複数のキュベット250内の検体に添加される。このようにして、測定用試料の調製が行われる。そして、キュベット移送部60により、測定用試料が収容されたキュベット250が測定部70のキュベット載置部71の挿入孔71aに移動される。
【0095】
そして、ステップS23において、制御部4aにより測定の指示が行われる。これにより、測定部70において、測定用試料の測定が開始される。以下、この測定について詳細に説明する。
【0096】
挿入孔71aに移動されたキュベット250(図8参照)には、上記のようにランプユニット40から5種類の異なる波長特性(340nm、405nm、575nm、660nmおよび800nm)の光が断続的に順次照射される。そして、キュベット250を透過した光は、光電変換素子72b、プリアンプ72c、マルチプレクサ501a、オフセット回路501b、アンプ501c、A/D変換部11dを介して、デジタルデータに変換され、ロガー用メモリ502hに記憶される。
【0097】
ここで、図13を参照して、信号処理部501の動作について説明する。
【0098】
マルチプレクサ501a、オフセット回路501b、アンプ501cおよびA/D変換部501dによる電気信号の処理は、マルチプレクサ501a、オフセット回路501b、アンプ501cおよびA/D変換部501dからなる3つの信号処理ラインL0〜L2において、部分的に並行して行われる。すなわち、図13に示すように、信号処理ラインL0におけるマルチプレクサ501a、オフセット回路501bおよびアンプ501cによる電気信号の処理と、信号処理ラインL1におけるA/D変換部501dによる変換処理および装置側制御部502のロガー用メモリ502h(図12参照)へのデータ記憶処理とが並行して行われる。また、同様に、信号処理ラインL1におけるマルチプレクサ501a、オフセット回路501bおよびアンプ501cによる電気信号の処理と、信号処理ラインL2におけるA/D変換部501dによる変換処理および装置側制御部502のロガー用メモリ502h(図12参照)へのデータ記憶処理とが並行して行われる。また、信号処理ラインL2におけるマルチプレクサ501a、オフセット回路501bおよびアンプ501cによる電気信号の処理と、信号処理ラインL0におけるA/D変換部501dによる変換処理および装置側制御部502のロガー用メモリ502h(図12参照)へのデータ記憶処理とが並行して行われる。
【0099】
そして、これらの電気信号の部分的な並行処理は、図20に示すように、3つの信号処理ラインL0〜L2を順次使用して48μsec単位で行われる。具体的には、まず、図20に示したステップ0では、信号処理ラインL0においてマルチプレクサ501aによるチャンネルCH0への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理が行われる。このステップ0では、信号処理ラインL1およびL2は、電気信号の安定待ちの状態(信号待ち処理)であり、電気信号の処理は行われない。そして、図20のステップ1では、信号処理ラインL1において、マルチプレクサ501aによるチャンネルCH16への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理が行われる。このステップ1では、信号処理ラインL0およびL2は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0100】
そして、図20のステップ2において、信号処理ラインL0のA/D変換部501dによるチャンネルCH0の電気信号のA/D変換処理およびロガー用メモリ502hへのデータ記憶処理と、信号処理ラインL2におけるマルチプレクサ501aによるチャンネルCH32への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理とが並行して行われる。このステップ2では、信号処理ラインL1は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0101】
そして、図20のステップ3において、信号処理ラインL0におけるマルチプレクサ501aによるチャンネルCH1への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理と、信号処理ラインL1のA/D変換部501dによるチャンネルCH16の電気信号のA/D変換処理およびロガー用メモリ502hへのデータ記憶処理とが並行して行われる。このステップ3では、信号処理ラインL2は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0102】
そして、図20のステップ4において、信号処理ラインL1におけるマルチプレクサ501aによるチャンネルCH17への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理と、信号処理ラインL2のA/D変換部501dによるチャンネルCH32の電気信号のA/D変換処理およびロガー用メモリ502hへのデータ記憶処理とが並行して行われる。このステップ4では、信号処理ラインL0は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0103】
そして、上記のステップ2〜4による処理と同様の並行処理が、信号処理ラインL0〜L2において、ステップ49まで信号処理を行うチャンネルを切り替えながら繰り返し行われる。そして、ステップ50では、信号処理ラインL2においてマルチプレクサ501aによるチャンネルCH32への切替処理、オフセット回路501bによる補正処理およびアンプ501cによる増幅処理が行われる。このステップ50では、信号処理ラインL0およびL1は、電気信号の安定待ちの状態であり、電気信号の処理は行われない。
【0104】
なお、マルチプレクサ501a、オフセット回路501b、およびアンプ501cは、いずれも、信号処理の直後は、出力信号が安定しない。第1実施形態では、このような不安定な信号が分析物の解析に使用されることを防止するため、上記の電気信号の安定待ちの期間が設けられている。
【0105】
上記のようにして、ステップ0〜50の51個のステップにより全てのチャンネルCH0〜CH47の電気信号の処理が行われる。なお、この51個のステップによる電気信号の処理は、2.45msec(=48μsec×51ステップ)の期間に行われる。また、この51個のステップによる電気信号の処理は、後述するmクロックのデータ取得処理の期間内に1回行われる。
【0106】
ロガー用メモリ502hへのデータ記憶処理においては、前述のように、ハロゲンランプ41からの光が透過した光学フィルタおよびチャンネルが特定できるように、所定のアドレスにデータが記憶される。このようにしてロガー用メモリ502hに記憶されたデータは、所定のタイミングに制御部4aに送信される。
【0107】
そして、図19のステップS24において、制御部4aは、測定部70からの波長特性および増幅率の異なる10種類の光学的情報(データ)、すなわち、5種類の光学フィルタ43b〜43fにそれぞれ対応するLゲインおよびHゲインのデータのうち、分析に適している光学的情報(データ)を選択し、その光学的情報を解析する。そして、ステップS25において、測定用試料の解析結果(第1実施形態では、図21に示すような凝固曲線および凝固時間など)を表示部4bに出力する。
【0108】
次に、図12、図18および図22を参照して、第1実施形態の制御基板5の装置側制御部502によるデータ取得処理について説明する。このデータ取得処理は、制御部4aが分析処理の指示(図16のステップS3)をすることによって開始される。
【0109】
まず、図22に示したステップS31において、装置側制御部502(図12参照)により、センサ45からの信号に基づいてセンサ45がスリットを検出したか否かが判断される。スリットが検出されると、ステップS32において、装置側制御部502により、スリット検出の時点から初期設定において算出したpクロック(図18参照)が経過するのを待つ処理が実行される。
【0110】
そして、スリットが検出されてからpクロックが経過すると、ステップS33において、装置側制御部502により、3つのA/D変換部11dからそれぞれ出力されるデジタルデータの取得を開始する処理が実行される。そして、ステップS34において、装置側制御部502により、デジタルデータの取得の開始からmクロックが経過するのを待つ処理が実行される。そして、mクロックが経過すると、ステップS35において、装置側制御部502は、デジタルデータの取得を終了する。そして、ステップS36において、装置側制御部502により、制御部4aから分析指示を受信してから所定時間が経過したか否かを判断する処理が実行される。所定時間が経過していれば、データ取得処理を終了し、経過していなければ、ステップS31の処理に戻る。
【0111】
次に、図2、図14、図19、図21および図23を参照して、第1実施形態の制御装置4の制御部4aによるデータ取得処理について説明する。この処理は、制御装置4の電源が投入されるとともに開始される。
【0112】
まず、図23のステップS40において、制御部4aは、ロガー502hに新たにデータが記憶されたか否かを監視し、データが100msec分(フィルタ部43の1回転分)記憶されるまで待つ。具体的には、ロガー502hに、100msec分のデータが蓄積されると、装置側制御部502から、それを知らせる通知が送信されるので、制御部4aは、その通知が送信されるのを待つ。そして、ステップS41において、制御部4aにより、ロガー用メモリ502hからその100msec分のデータ(部分時系列データ)がインターフェイス506およびローカルバスインターフェイス502kを介して取得される。すなわち、図14に示すように、ロガー用メモリ502hのエリア0〜5にフィルタ部43の1回転分に対応する100msec分のデータが蓄積されると、このエリア0〜5に蓄積されたデータが制御部4aにより取得される。
【0113】
そして、ステップS42において、制御部4aにより、制御装置4がシャットダウン指示を受け付けたか否かの判断が行われる。そして、シャットダウン指示を受け付けていない場合には、ステップS40の処理に戻る。シャットダウン指示を受け付けた場合には、データ取得処理を終了する。なお、ステップS41において、2回目にデータが取得される場合には、1回目にデータが取得されたロガー用メモリ502hのエリア0〜5の次の6つのエリア6〜11のデータが取得される。このように、制御部4aによりロガー用メモリ502hからデータ取得される際には、6つのエリア毎のデータが順次取得される。
【0114】
なお、制御部4aでは、ステップS41でロガー用メモリ502hから取得した複数の部分時系列データの内、測定用試料が収容されたキュベット250(図2参照)が測定部70の挿入孔71aに挿入された時点以降の部分時系列データが時系列順に組み合わされて、所定の時系列データが作成される。そして、制御部4aでは、その作成された時系列データに基づいて図21に示すような凝固曲線が作成される。そして、制御部4aでは、その作成された凝固曲線から測定用試料の凝固時間を求める。具体的には、図21に示した凝固曲線のグラフにおいて、透過光の強度が100%と0%との中間の50%になる時点tを求めるとともに、その時点tのスタート時点からの経過時間を凝固時間として算出する。この凝固時間は、前述のように、図19のステップS25において、表示部3cに表示される。
【0115】
第1実施形態では、上記のように、複数の波長の光が照射されたキュベット250中の測定試料からの光を光電変換素子72bによって受光することによって、波長毎に複数の光電変換素子72bを設ける必要がないため、装置が複雑化および大型化するのを抑制することができる。また、血液凝固時間測定用の660nmの波長の光、合成基質測定用の405nmの波長の光、免疫比濁測定用の800nmの波長の光および血小板凝集測定用の575nmの光を、測定部70の挿入孔71aに保持されたキュベット250の測定試料へ照射して、測定試料からの光を光電変換素子72bによって受光することによって、血液凝固時間測定、合成基質測定、免疫比濁測定および血小板凝集測定の4種類の分析項目を測定することができる。
【0116】
また、第1実施形態では、上記のように、4種類の波長の光を、断続的に複数回照射することによって、複数回照射した光による複数の測定結果により、所定の反応期間に渡って照射した光の波長に対応する分析項目を分析することができる。
【0117】
また、第1実施形態では、上記のように、4種類の波長の光を時分割で照射することによって、4種類の波長に対応する4種類の測定項目を容易に同時に測定することができる。
【0118】
また、第1実施形態では、上記のように、5つの光学フィルタ43b〜43fが設けられたフィルタ部43をモータ44によって回転させることにより、ハロゲンランプ41から発された光の光路に5種類の光学フィルタ43b〜43fを順次配置させることによって、所定の異なる5種類の波長の光を抽出することができる。また、抽出した異なる波長の複数の光を分岐光ファイバ47によって測定部70に導くことができる。これにより、容易に4種類の分析項目(血液凝固測定、合成基質測定、免疫比濁測定および血小板凝集測定)の測定を行うことができる。
【0119】
また、第1実施形態では、上記のように、1つのハロゲンランプ41による光から異なる波長の5種類の光を測定部70に導くことができる。
【0120】
また、第1実施形態では、上記のように、測定部70に20個の挿入孔71aを設け、20個の挿入孔71aにそれぞれ対応して20個の光電変換素子72bを設けることによって、20個の測定試料を同時に測定することができるので、装置の処理能力を向上させることができる。
【0121】
また、第1実施形態では、上記のように、血液凝固時間測定、合成基質測定、免疫比濁測定および血小板凝集測定を、測定試料を透過した透過光により行うことができる。
【0122】
(第2実施形態)
図24〜図26は、本発明の第2実施形態による血液凝固分析装置のランプユニットの詳細を説明するための図である。図27〜図29は、本発明の第2実施形態による血液凝固分析装置の測定部の詳細を説明するための図である。図24〜図29を参照して、この第2実施形態では、上記第1実施形態と異なり、2つの光源を設けるとともに、凝固時間法では試料からの散乱光により測定を行い、凝固時間法以外の測定法では試料からの透過光により測定を行うように構成した例を説明する。なお、第2実施形態におけるランプユニット140および測定部170以外の構成は上記第1実施形態と同じである。
【0123】
第2実施形態によるランプユニット140は、図24に示すように、光源としてのハロゲンランプ141および660nmの波長の光を発振するレーザ発光素子142と、集光レンズ143a〜143cと、円盤形状のフィルタ部144と、モータ145と、光透過型のセンサ146と、2つの光ファイバカプラ147および148と、21本の分岐光ファイバ149(図27参照)と、20本の分岐光ファイバ150(図27参照)とから構成されている。なお、ハロゲンランプ141、集光レンズ143a〜143c、モータ145および光透過型のセンサ146は、それぞれ、上記第1実施形態におけるハロゲンランプ41、集光レンズ42a〜42c、モータ44およびセンサ45と同様の構成を有している。
【0124】
また、ランプユニット40のフィルタ部144は、図24に示すように、モータ145のモータ軸(図示せず)を中心に回転するように構成されている。このフィルタ部144は、4つの光透過特性(透過波長)のそれぞれ異なる4つの光学フィルタ144b〜144eが設けられるフィルタ板144aを備えている。フィルタ板144aには、4つの光学フィルタ144b〜144eを取り付けるための4つの孔144fと、光が透過しないように閉塞される孔144gおよび144hとが設けられている。そして、4つの孔144fには、それぞれ、光透過特性(透過波長)の異なる4つの光学フィルタ144b〜144eが設置されている。なお、閉塞される孔144gは、予備の孔であり、フィルタの追加が必要になった場合には、フィルタが装着される。この光学フィルタ144b〜144eを介してハロゲンランプ141からの光のうち所定の波長を有する光が光ファイバカプラ147に入射するように構成されている。また、フィルタ板144aには、後述するスリット板144jの原点スリット144lと同じ大きさのスリット144iが設けられている。このスリット板144jの原点スリット144lおよびフィルタ板144aのスリット144iを介してレーザ発光素子142からのレーザが光ファイバカプラ148に入射するように構成されている。
【0125】
4つの光学フィルタ144b〜144eは、それぞれ、340nm、405nm、575nmおよび800nmの波長の光を透過し、その他の波長の光は透過しない。したがって、4つの光学フィルタ144b〜144eを透過した光は、それぞれ、340nm、405nm、575nmおよび800nmの波長特性を有する。
【0126】
また、第2実施形態では、フィルタ板144aのハロゲンランプ141と反対側にフィルタ板144aと等しい大きさを有するスリット板144jが設けられている。このスリット板144jには、円周方向に沿って所定の角度間隔(第2実施形態では、60°の等間隔)で6つのスリットが設けられている。それら6つのスリットのうち1つは、他の5つの通常スリット144kよりもフィルタ部144の回転方向のスリット幅が大きい原点スリット144lである。原点スリット144lおよび通常スリット144kは、フィルタ板144aの4つの孔144f、閉塞される孔144gおよび144hの間の中間角度位置に所定の角度間隔(第2実施形態では、60°の等間隔)で形成されている。この原点スリット144lおよび通常スリット144kとセンサ146とによりフィルタ部144の回転が監視される。
【0127】
また、第2実施形態では、フィルタ板144aの回転に伴って、集光レンズ143a〜143cにより集光された光の光路上に光透過特性の異なる4つの光学フィルタ144b〜144eと、予備の孔144gとが断続的に順次配置されるように構成されている。この時、図26に示すように、レーザ発光素子142からのレーザは、フィルタ板144aによって遮断されるように構成されている。また、図25に示すように、集光レンズ143a〜143cにより集光された光の光路上に、遮光された孔144hが配置されたときに、レーザ発光素子142からのレーザの光路上に、フィルタ板144aのスリット144iおよびスリット板144jの原点スリット144lが配置されるように構成されている。これにより、レーザ発光素子142からの660nmの光と、ハロゲンランプ141からの光のうち所定の波長(340nm、405nm、575nmおよび800nm)を有する光とが時分割で光ファイバカプラ147または148に入射するように構成されている。
【0128】
また、光ファイバカプラ147および148は、それぞれ、入射した光を21本の分岐光ファイバ149および20本の光ファイバ150に入射させる機能を有している。また、21本の分岐光ファイバ149および20本の分岐光ファイバ150の先端は、図27に示すように、測定部170に接続されている。そして、図27および図29に示すように、21本の分岐光ファイバ149は、それぞれ、測定部170の後述する20個の挿入孔171aおよび1つの参照光用測定孔171bに光を供給するように配置されている。また、20本の分岐光ファイバ150も、それぞれ、測定部170の20個の挿入孔171aに光を供給するように配置されている。
【0129】
測定部170は、キュベット載置部171と検出部172とを含んでいる。キュベット載置部171は、測定試料が収容されたキュベット250が挿入される20個の挿入孔171aと、1つの参照光用測定孔171bとを含む。また、検出部172には、20個の挿入孔171aおよび1つの参照光用測定孔171bにそれぞれ対応して20個の光電変換素子172aおよび1つの参照光用光電変換素子172bが設けられている。
【0130】
また、図28および図29に示すように、分岐光ファイバ149の測定部170側の先端は、それぞれ20個の光電変換素子172aおよび1つの参照光用光電変換素子172bに向けて配置されている。合成基質法、免疫比濁法および血小板凝集法による測定を行う際には、この分岐光ファイバ149の測定部170側の先端からの光(複数のフィルタにより特定の波長特性を有する光)が、挿入孔171aの側面からキュベット250へ照射され、当該光がキュベット250内の測定試料を透過して光電変換素子172aに入射することにより、複数のフィルタにより特定の波長特性を有する光(340nm、405nm、575nmおよび800nmの波長の光)の透過光が測定されるように構成されている。
【0131】
また、第2実施形態では、20個の分岐光ファイバ150の先端は、それぞれ、20個の挿入孔171aの下方から垂直上方に向けて配置されている。また、挿入孔171aの近傍には、光を反射させるためのミラー173が分岐光ファイバ150の先端と対応する位置に配置されている。凝固時間法で測定する場合には、このミラー173により、分岐光ファイバ150の先端からの光(660nmの波長特性を有するレーザ光)が挿入孔171aの側面からキュベット250へ照射され、当該光がキュベット250内の測定試料に入射し、測定試料による散乱光が光電変換素子172aにより検出されるように構成されている。
【0132】
このように第2実施形態では、凝固時間法(血液凝固時間測定)を散乱光で測定し、合成基質法、免疫比濁法および血小板凝集法を透過光により測定するように構成されている。
【0133】
第2実施形態では、上記のように、ハロゲンランプ141からの光およびレーザ発光素子142からの光をそれぞれ分岐光ファイバ149および分岐光ファイバ150により挿入孔171aに導くことによって、血液凝固時間測定を散乱光により行い、合成基質測定、免疫比濁測定および血小板凝集測定を透過光により行うことができる。
【0134】
なお、今回開示された実施形態は、すべての点で例示であって制限的なものではないと考えられるべきである。本発明の範囲は、上記した実施形態の説明ではなく特許請求の範囲によって示され、さらに特許請求の範囲と均等の意味および範囲内でのすべての変更が含まれる。
【0135】
たとえば、上記第1実施形態では、5つの光学フィルタ43b〜43fが設けられたフィルタ部43を回転させることにより、5つの光学フィルタ43b〜43fを順次ハロゲンランプ41からの光の光路に配置させて複数の波長の光を抽出する例を示したが、本発明はこれに限らず、図30に示す第1変形例のように複数の光源300a〜300dの発光のタイミングを電気的に切換制御するように構成してもよい。この第1変形例では、4つの光源300a〜300dが設けられており、4つの光源300a〜300dは、それぞれ、特定の波長特性を有する光(たとえば、凝固時間測定用の660nmの波長の光、合成基質測定用の405nmの波長の光、免疫比濁測定用の800nmの波長の光および血小板凝集測定用の575nmの波長の光など)を発するレーザ発光素子またはLEDなどからなる。4つの光源300a〜300dは切換制御回路301により電気的に順次発光するように制御される。4つの光源300a〜300dから発された光は、ミラー302aおよびダイクロイックミラー302bにより光ファイバカプラ303に入射し、光ファイバカプラ303から分岐光ファイバ304を介して測定部305に導入されるように構成されている。このように構成しても、4種類の波長の光が順次測定部305に導入されるので、4種類の測定項目(凝固時間測定など)の測定を行うことができる。
【0136】
また、上記第1変形例において示した構成において、1つの光源を連続的に発光させるように切換制御回路301を制御してもよい。たとえば、660nmの波長の光を発する光源300aを連続的に発光させて凝固時間測定を行うことにより、より正確な測定結果を得ることができる。
【0137】
また、上記第1実施形態および第2実施形態では、フィルタ部により抽出した特定の波長の光を測定試料に照射するように構成した例を示したが、本発明はこれに限らず、図31に示す第2変形例のように、フィルタ部311を測定試料312と受光部313との間に設けてもよい。この第2変形例では、光源314から発された光が測定試料312に照射され、測定試料312からの透過光または散乱光が複数の光学フィルタ311aが設けられた回転可能なフィルタ部311を介して受光部313により受光されるように構成される。また、他の測定試料315と受光部316との間には、特定の波長の光を抽出する固定フィルタ317が設けられる。このように構成しても、複数の測定項目を測定することができる。
【0138】
また、上記第1および第2実施形態では、制御装置4を血液凝固分析装置1の装置本体(検出機構部2および搬送機構部3)とは別に設けた例を示したが、本発明はこれに限らず、制御装置4と血液凝固分析装置1の装置本体(検出機構部2および搬送機構部3)とを一体化してもよい。
【0139】
また、上記第1および第2実施形態では、挿入孔71aおよび171aをそれぞれ20個設けた例を示したが、本発明はこれに限らず、挿入孔を20個より多く設けてもよいし、少なく設けてもよい。
【0140】
また、上記第2実施形態では、フィルタ部144の予備の孔144gを閉塞した例を示したが、本発明はこれに限らず、予備の孔144gに、レーザ発光素子142が発する光と同じ660nmの波長の光を透過する光学フィルタを取り付けてもよい。このように構成すれば、660nmの波長の凝固時間測定用の光を分岐光ファイバ150のみならず分岐光ファイバ149からも測定試料に照射することができる。これにより、凝固時間測定を透過光と散乱光との両方で測定することができる。
【図面の簡単な説明】
【0141】
【図1】本発明の第1実施形態による血液凝固分析装置の全体構成を示した斜視図である。
【図2】図1に示した血液凝固分析装置の平面図である。
【図3】第1実施形態による血液凝固分析装置の制御装置のブロック図である。
【図4】第1実施形態による血液凝固分析装置のランプユニットを示した斜視図である。
【図5】第1実施形態による血液凝固分析装置のランプユニットの構成を説明するための模式図である。
【図6】図4に示したランプユニットのフィルタ部を示した拡大斜視図である。
【図7】図4に示したランプユニットのフィルタ部を示した正面図である。
【図8】図1に示した第1実施形態による血液凝固分析装置の測定部の検出部の内部構造を説明するための概略図である。
【図9】図1に示した第1実施形態による血液凝固分析装置の測定部の検出部の構成を説明するための断面図である。
【図10】血小板凝集測定を行う場合の図9に対応する断面図である。
【図11】図1に示した第1実施形態による血液凝固分析装置の測定部の構成を説明するためのブロック図である。
【図12】本発明の第1実施形態による血液凝固分析装置の測定部および制御基板の構成要素を説明するためのブロック図である。
【図13】本発明の第1実施形態による血液凝固分析装置の検出部および信号処理部の構成を説明するためのブロック図である。
【図14】本発明の第1実施形態による血液凝固分析装置の制御基板のロガー用メモリの構成を説明するための図である。
【図15】本発明の第1実施形態による血液凝固分析装置の制御基板の増幅回路および微分回路の回路構成を示した回路図である。
【図16】本発明の第1実施形態による血液凝固分析装置の制御装置の制御部による制御方法の概略を示したフローチャートである。
【図17】図16のステップS1に示した初期設定において、装置側制御部によるpクロックの算出処理を示すフローチャートである。
【図18】図17に示したpクロックの算出処理方法において用いるスリット検出信号並びに参照光の光量および参照信号の微分信号の変化を示した波形図である。
【図19】図16のステップS3における制御装置の制御部による分析処理の詳細(サブルーチン)を示したフローチャートである。
【図20】本発明の第1実施形態による血液凝固分析装置の信号処理部における信号処理の方法を示した図である。
【図21】本発明の第1実施形態による血液凝固分析装置によって作成される凝固曲線を示したグラフである。
【図22】本発明の第1実施形態の装置側制御部によるデータ取得処理の方法を説明するためのフローチャートである。
【図23】本発明の第1実施形態の制御装置の制御部によるデータ取得処理の方法を説明するためのフローチャートである。
【図24】本発明の第2実施形態による血液凝固分析装置のランプユニットを示した斜視図である。
【図25】本発明の第2実施形態による血液凝固分析装置のランプユニットを正面から見た場合の斜視図である。
【図26】本発明の第2実施形態による血液凝固分析装置のランプユニットを正面から見た場合の斜視図である。
【図27】本発明の第2実施形態による血液凝固分析装置の測定部の検出部の内部構造を説明するための概略図である。
【図28】本発明の第2実施形態による血液凝固分析装置の測定部の検出部の内部構造を説明するための斜視図である。
【図29】本発明の第2実施形態による血液凝固分析装置の測定部の検出部の内部構造を説明するための模式図である。
【図30】本発明の第1実施形態の第1変形例の模式図である。
【図31】本発明の第1実施形態の第2変形例の模式図である。
【符号の説明】
【0142】
1 血液凝固分析装置
4 制御装置(分析部)
41、141 ハロゲンランプ(光源部、光源)
43、144 フィルタ部(光学抽出部)
43b〜43f、144b〜144e 光学フィルタ
44、145 モータ(移動部)
46、149 分岐光ファイバ(導光部)
70、170 測定部
71a、171a 挿入孔(保持部)
72b、172a 光電変換素子(受光部)
250 キュベット(反応容器)
【特許請求の範囲】
【請求項1】
反応容器中の血液試料と試薬とが混和された測定試料を測定する測定部と、
前記測定部による測定結果を分析する分析部とを備え、
前記測定部は、
前記反応容器を保持するための保持部と、
前記保持部の側面から当該保持部に保持された反応容器へ向けて、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を照射する光照射部と、
前記複数の波長の光が照射された反応容器中の前記測定試料からの光を受光する受光部 とを含み、
前記分析部は、前記光照射部から照射された複数の波長の光のうちのいずれかの波長の光に対応する前記受光部の受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するように構成されている、血液凝固分析装置。
【請求項2】
前記光照射部は、前記複数の波長の光のうちの少なくとも1つの波長の光を所定の反応期間に渡って照射するように構成されている、請求項1に記載の血液凝固分析装置。
【請求項3】
前記光照射部は、前記少なくとも1つの波長の光を、断続的に複数回照射するように構成されている、請求項2に記載の血液凝固分析装置。
【請求項4】
前記光照射部は、前記少なくとも1つの波長の光と、前記少なくとも1つの波長の光以外の波長の光とを時分割で照射するように構成されている、請求項3に記載の血液凝固分析装置。
【請求項5】
光源部と、
前記光源部から発せられた光を透過して所定の異なる波長の光を抽出する複数の光学フィルタを含む光学抽出部と、
前記光学フィルタを透過した光を前記光照射部に導く導光部と、
前記複数の光学フィルタが順次前記光源部の光路に配置されるように前記光学抽出部を移動させる移動部とをさらに備える、請求項4に記載の血液凝固分析装置。
【請求項6】
前記光源部は、1つの光源からなる、請求項5に記載の血液凝固分析装置。
【請求項7】
前記光照射部は、前記少なくとも1つの光を、前記所定の反応期間に渡って連続的に照射するように構成されている、請求項2に記載の血液凝固分析装置。
【請求項8】
前記測定部は、複数の前記保持部を有し、前記複数の保持部にそれぞれ保持された各反応容器中の測定試料を個別に測定することが可能であるように複数の光照射部および複数の受光部を含む、請求項1〜7のいずれか1項に記載の血液凝固分析装置。
【請求項9】
前記光照射部は、さらに、血小板凝集測定用の第4波長の光を照射することが可能なように構成されている、請求項1〜8のいずれか1項に記載の血液凝固分析装置。
【請求項10】
前記血液凝固時間測定、前記合成基質測定、前記免疫比濁測定および前記血小板凝集測定の際、前記受光部は、前記測定試料を透過した透過光を受光するように構成されている、請求項9に記載の血液凝固分析装置。
【請求項11】
前記血液凝固時間測定の際、前記受光部は、前記測定試料により散乱された散乱光を受光するように構成されている、請求項1〜9のいずれか1項に記載の血液凝固分析装置。
【請求項12】
前記光照射部は、
前記血液凝固時間測定用の第1波長の光を照射する第1照射部と、
前記合成基質測定用の第2波長の光と免疫比濁測定用の第3波長の光との少なくとも一方を照射する第2照射部とを含む、請求項11に記載の血液凝固分析装置。
【請求項13】
反応容器中の血液試料と試薬とが混和された測定試料を測定する測定部と、
前記測定部による測定結果を分析する分析部とを備え、
前記測定部は、
前記反応容器を保持するための保持部と、
前記保持部の側面から当該保持部に保持された反応容器へ向けて光を照射する光照射部と、
前記反応容器中の測定試料からの光から互いに異なる波長の複数の光をそれぞれ抽出する光学抽出部と、
前記光学抽出部により抽出された光を受光する受光部とを含み、
前記分析部は、前記複数の波長のうちのいずれかの波長に対応する前記受光部の受光結果に基づいて、その波長に対応する分析項目の分析結果を取得するように構成されている、血液凝固分析装置。
【請求項14】
血液試料と試薬とが混和された測定試料をそれぞれ収容した複数の反応容器を保持し、各反応容器中の測定試料を測定する測定部と、
前記測定部による測定結果を分析する分析部とを備え、
前記測定部は、
血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を、少なくとも1つの反応容器に対して照射する光照射部と、
前記複数の波長の光が照射された反応容器中の前記測定試料からの光を受光する受光部とを含み、
前記分析部は、前記光照射部から照射された複数の波長の光のうちのいずれかの波長の光に対応する前記受光部の受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するように構成されている、血液凝固分析装置。
【請求項1】
反応容器中の血液試料と試薬とが混和された測定試料を測定する測定部と、
前記測定部による測定結果を分析する分析部とを備え、
前記測定部は、
前記反応容器を保持するための保持部と、
前記保持部の側面から当該保持部に保持された反応容器へ向けて、血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を照射する光照射部と、
前記複数の波長の光が照射された反応容器中の前記測定試料からの光を受光する受光部 とを含み、
前記分析部は、前記光照射部から照射された複数の波長の光のうちのいずれかの波長の光に対応する前記受光部の受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するように構成されている、血液凝固分析装置。
【請求項2】
前記光照射部は、前記複数の波長の光のうちの少なくとも1つの波長の光を所定の反応期間に渡って照射するように構成されている、請求項1に記載の血液凝固分析装置。
【請求項3】
前記光照射部は、前記少なくとも1つの波長の光を、断続的に複数回照射するように構成されている、請求項2に記載の血液凝固分析装置。
【請求項4】
前記光照射部は、前記少なくとも1つの波長の光と、前記少なくとも1つの波長の光以外の波長の光とを時分割で照射するように構成されている、請求項3に記載の血液凝固分析装置。
【請求項5】
光源部と、
前記光源部から発せられた光を透過して所定の異なる波長の光を抽出する複数の光学フィルタを含む光学抽出部と、
前記光学フィルタを透過した光を前記光照射部に導く導光部と、
前記複数の光学フィルタが順次前記光源部の光路に配置されるように前記光学抽出部を移動させる移動部とをさらに備える、請求項4に記載の血液凝固分析装置。
【請求項6】
前記光源部は、1つの光源からなる、請求項5に記載の血液凝固分析装置。
【請求項7】
前記光照射部は、前記少なくとも1つの光を、前記所定の反応期間に渡って連続的に照射するように構成されている、請求項2に記載の血液凝固分析装置。
【請求項8】
前記測定部は、複数の前記保持部を有し、前記複数の保持部にそれぞれ保持された各反応容器中の測定試料を個別に測定することが可能であるように複数の光照射部および複数の受光部を含む、請求項1〜7のいずれか1項に記載の血液凝固分析装置。
【請求項9】
前記光照射部は、さらに、血小板凝集測定用の第4波長の光を照射することが可能なように構成されている、請求項1〜8のいずれか1項に記載の血液凝固分析装置。
【請求項10】
前記血液凝固時間測定、前記合成基質測定、前記免疫比濁測定および前記血小板凝集測定の際、前記受光部は、前記測定試料を透過した透過光を受光するように構成されている、請求項9に記載の血液凝固分析装置。
【請求項11】
前記血液凝固時間測定の際、前記受光部は、前記測定試料により散乱された散乱光を受光するように構成されている、請求項1〜9のいずれか1項に記載の血液凝固分析装置。
【請求項12】
前記光照射部は、
前記血液凝固時間測定用の第1波長の光を照射する第1照射部と、
前記合成基質測定用の第2波長の光と免疫比濁測定用の第3波長の光との少なくとも一方を照射する第2照射部とを含む、請求項11に記載の血液凝固分析装置。
【請求項13】
反応容器中の血液試料と試薬とが混和された測定試料を測定する測定部と、
前記測定部による測定結果を分析する分析部とを備え、
前記測定部は、
前記反応容器を保持するための保持部と、
前記保持部の側面から当該保持部に保持された反応容器へ向けて光を照射する光照射部と、
前記反応容器中の測定試料からの光から互いに異なる波長の複数の光をそれぞれ抽出する光学抽出部と、
前記光学抽出部により抽出された光を受光する受光部とを含み、
前記分析部は、前記複数の波長のうちのいずれかの波長に対応する前記受光部の受光結果に基づいて、その波長に対応する分析項目の分析結果を取得するように構成されている、血液凝固分析装置。
【請求項14】
血液試料と試薬とが混和された測定試料をそれぞれ収容した複数の反応容器を保持し、各反応容器中の測定試料を測定する測定部と、
前記測定部による測定結果を分析する分析部とを備え、
前記測定部は、
血液凝固時間測定用の第1波長の光と、合成基質測定用の第2波長の光および免疫比濁測定用の第3波長の光の少なくともいずれか一方とを含む複数の波長の光を、少なくとも1つの反応容器に対して照射する光照射部と、
前記複数の波長の光が照射された反応容器中の前記測定試料からの光を受光する受光部とを含み、
前記分析部は、前記光照射部から照射された複数の波長の光のうちのいずれかの波長の光に対応する前記受光部の受光結果に基づいて、その波長の光に対応する分析項目の分析結果を取得するように構成されている、血液凝固分析装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【公開番号】特開2008−46031(P2008−46031A)
【公開日】平成20年2月28日(2008.2.28)
【国際特許分類】
【出願番号】特願2006−222969(P2006−222969)
【出願日】平成18年8月18日(2006.8.18)
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
【公開日】平成20年2月28日(2008.2.28)
【国際特許分類】
【出願日】平成18年8月18日(2006.8.18)
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
[ Back to top ]

