血液凝固時間測定装置
【課題】血液凝固因子に作用する試薬を用い、光学的信号の時系列的変化を分析することにより血液凝固時間測定する方法において、検体の血液凝固時間PTに影響されず高精度な異常判定をすることができる血液凝固時間測定方法を提供する。
【解決手段】測定部で測定された血液凝固時間PTおよび血液凝固時間における受光データF(PT)に基づいてチェック領域および正常範囲閾値を設定し、正常範囲内にある否かを判断することにより、検体の血液凝固時間PTに影響されず良好な異常判定を行うことが可能となる。
【解決手段】測定部で測定された血液凝固時間PTおよび血液凝固時間における受光データF(PT)に基づいてチェック領域および正常範囲閾値を設定し、正常範囲内にある否かを判断することにより、検体の血液凝固時間PTに影響されず良好な異常判定を行うことが可能となる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、被分析試料中の物質と反応して吸光、発光、蛍光、散乱光などの光学的な変化を伴う光学的信号を分析することにより血液凝固時間を測定する血液凝固時間測定装置に関するものである。
【背景技術】
【0002】
以下、従来の血液凝固時間測定装置について図11、図12を用いて説明する。従来の血液凝固時間測定装置は図11に示すような構成となっていた(例えば、特許文献1参照。)。
【0003】
図11において、透明な試験管51には、測定される血漿が予め収容され、試薬供給器52からピペット53を介して例えばPT試薬等の試薬が試験管51へ供給され、LED54からの光が試験管1に照射される。試験管51の内部で散乱した散乱光はフォトダイオード55に受光され、散乱光量が検出される。
【0004】
計測部56は、散乱光量の飽和を検出する検出部56aと、散乱光量が増加するか否かを判定する判定部56bと、散乱光量の飽和を検出した時にその後の所定時間内に散乱光量がさらに増加するか否かを判定し増加するときには次の飽和を検出するという処理がくり返し行なわれるように検出部56aと判定部56bとを制御する制御部56cと、散乱光量の飽和が最終的に検出されたとき、その飽和値に基づいて凝固時間を算出する算出部56dを備え、フォトダイオード55の出力信号を処理して、処理結果をCRT57に表示するようになっている。なお計測部56は、CPU,ROM,RAMからなるマイクロコンピュータから構成されている。
【0005】
図12は、図11の従来の血液凝固時間測定装置を用いて測定されたデータの一例を示している。横軸は、測定される血漿と試薬を混合した後の経過時間を示す。縦軸は、検出される受光光量を示している。この場合、血液凝固時間は、受光光量の変化量が飽和した時の50%になる時刻で測定される。さらに、測定データに異常がないかどうかを判断するために、以下のような異常判定を行なっている。
【0006】
まず、反応速度の異常を判断するために、例えば、受光光量が飽和光量の50%の領域H2を中心としてプラスマイナス4%になる領域をチェック領域に設定し、このチェック領域内での受光光量の変化率を求め、正常範囲内であるかどうかを判断している。
【0007】
次に、初期反応の有無の判定として、例えば反応開始後20秒あたりの反応初期にチェック領域を設定し、この部分での受光光量の変化率を求め、正常範囲内であるかどうかにより判断している。
【0008】
さらに、反応曲線のドリフトの有無を判定するために、2つのチェック領域を設定し、それぞれのチェック領域での受光光量の変化率の求め、2つの変化率の比率をさらに求め、正常範囲内であるかどうかにより判断している。例えば、チェック領域は、受光光量が飽和光量の46%〜54%の領域(H2−h〜H2+h)と、6%〜14%の領域(H1−h〜H1+h)に設定している。
【0009】
また、反応開始時刻が早すぎないかどうかの判定として、受光光量が所定値を超える時刻を求め、正常範囲かどうかを判断している。
【特許文献1】特開2003−169700号公報
【発明の開示】
【発明が解決しようとする課題】
【0010】
しかしながら、このような従来の血液凝固時間測定装置では、測定される受光光量は、測定される血液の血液凝固能の差により、光量変化量だけでなく、変化開始時刻、変化率に大きな差が存在し、精度の高い異常判定を行なうことができないという課題がある。血液凝固時間の測定値は、抗凝固剤の投薬量を決定するために用いられるため、その測定誤差は生命に関わる危険性が高い。従って、非常に高い信頼性が必要である。もし、装置や化学反応に何らかの異常を検知した場合、安全にその異常をユーザーに認知させる必要があり、決して信頼性の無い測定結果を表示してはならない。
【0011】
この点について今少し説明する。図13に実際に測定した受光光量の測定データを示す。図13は、それぞれ血液凝固時間が異なる場合、言い換えれば国際標準比(以降INR値と記す)が異なる場合のプロファイルの違いを示したものである。図からわかるように、INR値が大きいほど変化開始の時刻が遅く、変化量の大きさ、すなわち変化率が小さくなる傾向がある。また、変化開始している時刻が同じ、すなわち、同じINR値であるプロファイルでも、変化量の大きさやプロファイルの傾き、すなわち変化率が異なっている。
【0012】
したがって、従来の血液凝固時間測定装置では、INR値の違いによって生じる変化開始時刻の違いや傾きの違いのため、最適なチェック領域を設定することが難しく、また、最適な異常判定の閾値を設定することが難しいという課題がある。
【0013】
さらに、従来の血液凝固時間測定装置では、異常判定をするチェック領域を受光光量の飽和値を基に設定しているので、微分値の最大時刻を検知した時点で測定完了することができる高速測定方法では異常判定を行なうことができないという課題がある。
【0014】
本発明は、これらの課題を解決するためになされたものであり、精度の高い異常判定を行ない、血液凝固時間を測定することのできる血液凝固時間測定装置を提供することを目的とする。
【課題を解決するための手段】
【0015】
上記の課題を解決するために、本発明(請求項1)の血液凝固時間測定装置は、血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、前記光学的信号を電気的な受光信号に変換する受光器と、前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、前記データ測定部で測定された受光データを一時的に保持するデータ保持部と、前記データ保持部に保持された受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、前記異常判定部が、前記血液凝固時間演算部により求められた血液凝固時間および該血液凝固時間における前記測定した受光データの値に基づいて、異常判定を行うチェック領域および該チェック領域における正常範囲を設定し、前記測定した受光データが前記正常範囲内にあるか否かを判定する、ことを特徴とするものである。
【0016】
これにより、チェック領域およびチェック領域における正常範囲を、検体の血液凝固時間および受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことを可能とできる。
【0017】
また、本発明(請求項2)の血液凝固時間測定装置は、血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、前記光学的信号を電気的な受光信号に変換する受光器と、前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、前記異常判定部が、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間における値に基づいて、少なくとも1つの判定基準値を設定し、かつ、前記血液凝固時間演算部により求められた血液凝固時間に基づいて、前記測定された受光データの値が前記判定基準値と等しくなる時刻の正常上限時刻および正常下限時刻を設定し、前記測定された受光データの値が前記判定基準値と等しくなる時刻を求め、該求めた時刻が前記正常上限時刻および前記正常下限時刻で設定される正常時刻範囲内にあるか否かを判定する、ことを特徴とするものである。
【0018】
これにより、判定基準値、および受光データの値が前記判定基準値に等しくなる時刻の正常範囲を、検体の血液凝固時間および受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことを可能とできる。
【0019】
また、本発明(請求項3)の血液凝固時間測定装置は、血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、前記光学的信号を電気的な受光信号に変換する受光器と、前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、前記異常判定部が、前記血液凝固時間演算部により求められた血液凝固時間に基づいて、少なくとも1つの判定基準時刻を設定し、かつ、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間における値に基づいて、前記測定した受光データの前記判定基準時刻における値の正常上限値および正常下限値を設定し、前記測定した受光データの前記判定基準時刻における値を求め、前記求めた値が前記正常上限値および前記正常下限値で設定される正常値範囲内にあるか否かを判定する、ことを特徴とするものである。
【0020】
これにより、判定基準時刻、および判定基準時刻における受光データの値の正常範囲を、検体の血液凝固時間および受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことを可能とできる。
【発明の効果】
【0021】
本発明の血液凝固時間測定装置によれば、測定データから求めた血液凝固時間および該血液凝固時間における受光光量データの値に基づいて、チェック領域および該チェック領域における正常上限値および正常下限値を設定するようにしたから、異常判定を行なうチェック領域が、検体の血液凝固能に依存せず、受光データの変化量、変化率の違いや反応開始時間の違いなどに影響されないので、検体の血液凝固時間に影響されずに高精度な異常判定を行うことができる効果がある。
【0022】
また、本発明の血液凝固時間測定装置によれば、チェック領域を設定するために受光光量の飽和値を知る必要がないため、微分値の最大時刻を検知した時点で測定完了することができる高速測定方法においても良好な異常判定を行なうことができる効果がある。
【発明を実施するための最良の形態】
【0023】
(実施の形態1)
以下に、本発明の実施の形態について、図面に基づいて説明する。
図1は、本発明の実施の形態1における血液凝固時間測定装置100の斜視図である。
【0024】
図1において、本実施の形態1の血液凝固時間測定装置100には、試験片3を設置するための光学台6が設けられている。試験片3上の反応部4には、血液5の凝固反応に応じて蛍光強度を変化させるような化学反応を起こさせる試薬が含まれている。光学台6の上には、ホルダー20が装着されており、試験片3が適切な測定位置に配置できるように挿入路を形成している。さらにホルダー20は、弾性構造になっており、試験片3を温度制御手段21に押し当てて、熱伝導性を高める役割を果たしている。
【0025】
試験片3を血液凝固時間測定装置100の光学台6上に設置した際に、反応部4は、光学台6上に設けられた窓部7に合致するように位置決めされる。試験片3はホルダー20によって温度制御手段21に押し当てられるような構造となっている。光学台6上には電極22が備えられており、試験片3を使った試料の測定時には、試料の点着を検出したり、測定中の試料の抵抗値など測定したりする目的で試験片3上に備えられている電極と接続されるようになっている。また血液凝固時間測定装置100には、測定中の外光や埃等の侵入を防止する目的で、閉状態で光学台6を遮光できるような開閉可能な蓋8が設けられている。
【0026】
図2は、光学台6の断面を示す図である。光学台6の内部には、温度制御手段21、光源9、光源フィルタ12、レンズ10、受光フィルタ13、受光手段11が備えられている。
【0027】
温度制御手段21は、血液5と反応部4内に含まれている反応物質との反応が最も活性化する温度、もしくは、反応が最も安定するような温度になるように反応部4の温度を制御するための温度制御手段である。例えば、アルミナ系セラミック基板上に厚膜抵抗体などの加温手段と、温度検出用のサーミスタなどの温度検出手段をそなえた面状ヒーターなどにより構成する事ができる。また、制御温度が動作環境温度よりも低いような冷却を必要とする場合においては、加温手段の代替としてペルチェ素子のような加温冷却手段を用いる事により構成することができる。なお、加温または加温冷却手段は、一例をあげたに過ぎず、加温または冷却する事ができるものであれば他のものも用いる事ができる。なお、温度制御が不要な場合では、温度制御手段21を必ずしも備える必要はない。
【0028】
光源9は、反応部4に対して光学的エネルギーを印加するためのものであり、例えば白熱電球、LED、半導体レーザー、有機EL等を用いることができる。光源9は、駆動手段に接続され、測定中は光学的出力が安定して得られるように制御されている。
【0029】
光源フィルタ12は、光源9から射出される光路上に配置されており、これにより光源9から発せられた光のうち、光源フィルタ12の特性により選択された波長帯域の光を反応部4へ照射することができる。光学フィルタ12の特性は、血液5と反応部4内の反応物質との反応に伴う光学的な波長により透過波長帯域および遮断波長帯域が決まり、バンドパスフィルタ、ショートパスフィルタ、ロングパスフィルタ、マルチパスフィルタなどを用いる事ができる。なお、光源9が半導体レーザーダイオードのような単一波長である場合や、LEDなどの特定の波長帯域幅だけであり、かつ、受光すべき波長に影響しない場合においては、光源フィルタ12を必ずしも備える必要はない。
【0030】
レンズ10は、試験片3上の反応部4に面する側が平面であり、受光手段11に面する側がレンズ曲面となっている。本実施の形態では、平面側は、反応部4にほとんど接するような位置に配置されている。実際には、接触による傷や汚染の防止のために300〜500μm程度の隙間ができるようにしている。本実施の形態では、光学的効率を向上させる目的でレンズ10を入れているが、受光量をそれほどあげる必要がない場合は、レンズ10を備えなくても構わない。
【0031】
光源フィルタ12により選択された波長の光は、レンズ10のレンズ曲面側から入射し、平面側より出射して反応部4へ照射される。
【0032】
反応部4内の反応物質と点着された血液5の反応により、蛍光物質が生成されて蛍光特性が表れ、励起光を照射する事によって、蛍光を発するようになる。
【0033】
反応部4より発せられた蛍光は、レンズ10の平面側から入射し、曲面側より出射され、受光フィルタ13を透過して、受光手段11によって受光される。
【0034】
受光フィルタ13は、反応部4から発せられた蛍光のみを透過させ、それ以外の不要な光を阻止する目的の光学フィルタである。この受光フィルタ13の特性は、血液5と反応部4内の反応物質との反応に伴う光学的な波長に関連した要求仕様に基づいて決まり、少なくとも、励起光源波長帯域を遮断し、反応部4からの光学信号の波長帯域を透過させるようなフィルタ特性が必要となる。望ましくは、反応部4から得られる光学的信号の波長のみを透過させ、それ以外の不要な光の波長を遮断するようなバンドパスフィルタが望ましいが、要求仕様によっては、ショートパスフィルタ、ロングパスフィルタ、マルチパスフィルタなどを用いる事ができる場合もある。
【0035】
受光手段11に受光された光学的信号は、光電変換された後、信号処理回路により、所定の信号分析が行なわれる。信号処理回路は一般的にアナログ増幅回路、アナログ−デジタル変換回路、マイクロプロセッサ等から構成される。
【0036】
図3は、血液凝固時間測定装置100の構成を示すブロック図である。図において、図1、図2と同一符号は同一又は相当部分である。また、30は光源9を駆動するLEDドライバである。32はCPUであり、制御部33、血液凝固時間演算部34、異常検知部35、データ測定部36、およびデータ保持部37を備える。また38は受光手段11が出力する光電流を電圧に変換する電流電圧変換回路(I/V)、39はI/V38のアナログ出力をデジタル信号に変換するアナログ−デジタル変換回路(A/D)である。40は測定結果等を表示するLCD表示器、41はデータを血液凝固時間測定装置100の外部に出力する出力ポート、42は外部メモリ、43はCPU32の動作クロックを発生するタイマーである。31は操作スイッチであり、CPU32の制御部33は操作スイッチ31からの操作入力に応じて測定動作が行われるように各部を制御する。
【0037】
以上のように構成された血液凝固時間測定装置100の測定動作について説明する。
図7は、測定動作のフローチャートである。
【0038】
ユーザーが操作スイッチ31を操作することにより、血液凝固時間測定装置100は、測定モードに移行する。まず、最初に、ユーザーに対して試験片3を挿入するよう、LCD表示器40に試験片挿入指示メッセージを表示する(ステップS1)。
【0039】
ホルダー20が取付けられている光学台6の所定の位置に試験片3を挿入されると、電極ピン22の電極間抵抗値が変化することにより試験片3が装着された事を検知する(ステップS2)。その後、温度制御手段21により試験片3上の反応部4が所定の温度、例えば血液凝固反応が安定する37℃になるように温度制御を行なう(ステップS3)。
【0040】
温度が所定温度に達した後、分析対象である血液5を反応部4へ点着するようにLCD表示器40に点着指示メッセージを表示する(ステップS4)。
【0041】
ユーザーにより点着されると、電極間の抵抗値の変化が生じ、これを検知してデータ測定を開始する(ステップS5)。
【0042】
測定開始と同時に、LCD表示器40に蓋閉め指示メッセージを表示する(ステップS6)。
【0043】
その後、予め決められた時間毎、例えば、5秒毎にLEDドライバ30により光源9を点灯させることにより反応部4へ励起光を照射し、受光手段11より得られる受光信号をI/V38およびA/D39を通してデータ測定部36で測定し、光源9を消灯する。光源9を消灯するのは、低消費電力、光源寿命、蛍光退色などのデメリットを軽減するためのものであり、特に問題とならない場合には、消灯しなくても構わない。このようにして、反応部4から得られる光学的信号強度を受光手段11により電気信号に変換し、適切に構成された増幅回路により増幅し、A/D39によりデジタルデータに変換した後、データ測定部36で測定し、その時系列的な測定データを記憶手段であるデータ保持部37により一時記憶してゆく。そして、各々の測定毎に、一次微分を演算しながら最大値になる時刻を監視する。一次微分が最大値となる時刻を検知し、測定を終了する。(ステップS7、S8、S9)
【0044】
受光データには電気的または光学的なノイズが含まれる場合が多く、各々の測定毎のA/D変換は1回だけではなく複数回のサンプリングを行い、一般的に用いられる安定化手法、例えば、平均値、中心値、分布偏差が大きい部分を除外したデータの平均化などの方法により行なうことが好ましい。また、前後の複数のデータから平滑化処理、例えば、前後データの平均値、重み付け加算値、中心値など方法により処理した後に演算をおこなうのが望ましい。
【0045】
受光データ測定終了後、データ保持部37に記憶された時系列データをもとに血液凝固時間演算部34によって、血液凝固時間PT値およびINR値を演算する(ステップS10)。
【0046】
以下に、血液凝固時間およびINR値を求める方法の一例として、一次微分を利用した演算方法を示す。本発明の進歩性の一つとして高速測定方法にも有効であるため、一次微分を利用した演算部の例を示すが、他の演算方法による場合でも本発明は同様に有効であり、この演算方法に限定するものではない。
【0047】
図4は、測定データの一例を示した図である。図において、23は受光信号データを示すグラフであり、24はその一次微分を示すグラフである。
【0048】
受光データ23において、測定開始から約30秒までの間に、受光信号に変化がない部分が存在する。この部分では、血液凝固による蛍光変化は起こっていないため、この部分の受光データは蛍光以外の定常的なオフセット成分によるものである。
【0049】
測定される受光信号には、反応部4から得られる純粋に血液凝固反応に応じた蛍光信号と、それ以外の不要な光による受光信号が含まれる。後者の要因としては、光源9から発せられた光が、レンズ10の表面や反応部4で反射した反射光のうち受光フィルタ13で阻止しきれずに透過してきた不要な光による成分が支配的である。また、電気的なオフセット信号も含まれている。以降の測定において定常的なオフセット信号となる。
【0050】
以下、本実施の形態1における血液凝固時間(PTsec)および国際標準値(INR)を算出する方法を示す。
【0051】
(1)受光データ23を時間微分し、一次微分24を求め、一次微分24が最大となる時刻T1を求める。図4では、一次微分24は、説明を解りやすくするために正規化したものを示しているが、特に正規化する必要はない。
【0052】
(2)受光データ23上の時刻T1の点を求める。
【0053】
(3)時刻T1を基準として、所定の時間関係にある点T2、T3、T4、T5における受光データ23上の点を求める。例えば、データの測定間隔が5秒間隔として、T1の時刻を基準にT2が5秒前、T3が5秒後、T4が10秒前、T5が10秒後とする。なお、この例では、時間間隔を5秒、サンプル点数を5個としたが、測定装置の全体性能に影響がない限り、測定間隔を短くし、サンプリング数を多くする事が望ましい。少なくともサンプル点は、2点以上とする。
【0054】
(4)受光データ23上の時刻T1,T2,T3,T4,T5の5点のデータより近似直線25を求める。ここで、精度的に問題ない限り、正確な近似直線でない近似計算、または、実質的に近似直線と同等な直線式でも本発明の効果は同様に得られる。本例では5点を用いて近似直線を求めているが、サンプリング間隔を短くし、さらに多くの点から近似直線25を求めるのが望ましい。また、最も簡単な処理で実現しようとする場合、サンプル点はT2およびT3とし、2点を結ぶ傾きをもったT1からT3までのいずれかの点を含む直線を近似直線25としてもよい。
【0055】
(5)受光データ23のうち、蛍光反応以外の要因による定常的なオフセットデータを表すベースライン26を求める。例えば、受光データ23の最小値とする方法が最も簡単である。また、別の方法としては、受光データ23が所定の閾値以上になる時刻を求め、測定開始から閾値を超える時刻までの間の少なくとも2点以上のデータの平均値とする方法でもよい。この場合、採用するデータとしては、最小値側から所定データ数、または、分布的に最小値側に分布する所定%に含まれるデータを採用するのが好ましい。また、これ以外の方法でも実質的に同等であれば本発明の効果は同様に得られる。
【0056】
(6)近似直線25とベースライン26が交差する点の時刻Tmを求める。
【0057】
(7)補正式により、血液凝固時間PTsecおよび国際標準値INRを演算する。上記で求められたTmは、使用する反応試薬や測定器の光学検出性能に依存するところが大きく、測定方法によって補正式は全く異なる。また、測定する試料の種類、例えば、穿刺血、クエン酸血、血漿などの違いによっても補正式は異なる。従って、詳細な式については、本実発明の効果には影響無いので省略する。
【0058】
図5(a)は、実際に行ったクリニックスタディのデータを分析して得られたグラフであり、上記の算出方法で測定された血液凝固時間PTを横軸とし、受光データが、血液凝固時間PTにおける受光データの3.0倍になる時刻を縦軸とし、160個のデータをプロットして、これらの相関を示したものである。同様に、図5(b)は、実際に行ったクリニックスタディのデータを分析して得られたグラフであり、上記の算出方法で測定された血液凝固時間PTを横軸とし、受光データが、血液凝固時間PTにおける受光データの2.0倍になる時刻を縦軸とし、160個のデータをプロットして、これらの相関を示したものである。同様に、図5(c)は、実際に行ったクリニックスタディのデータを分析して得られたグラフであり、上記の算出方法で測定された血液凝固時間PTを横軸とし、受光データが、血液凝固時間PTにおける受光データの0.7倍になる時刻を縦軸とし、160個のデータをプロットして、これらの相関を示したものである。
【0059】
ここで、それぞれのグラフにおいて、160個の測定データを対象に最小二乗法により近似直線を引いてみる。図5(a)の近似直線の傾きa1は、1.3293、切片b1は、0.2867である。また、図5(b)の近似直線の傾きa2は、1.202、切片b2は、−0.7534である。また、図5(c)の近似直線の傾きa3は、0.8751、切片b3は、2.0128である。
【0060】
図5(a)〜図5(c)に示すグラフより、ほとんどの測定データが近似直線近傍に集中していることがわかる。すなわち、それぞれの測定データは、血液凝固時間PT値およびINR値が異なる値であるにも関わらず、相関に直線性があるといえる。さらに、前記近似直線から比較的大きく離れたデータ、すなわち丸印で囲んだ測定データを個々に分析してみると、受光データ23のプロファイルが歪んでおり、測定される血液凝固時間PT値およびINR値の測定誤差が非常に大きいことが分かった。また、近似直線近傍にあるデータの受光データ23は、プロファイルの歪が非常に少なく、測定される血液凝固時間PT値およびINR値の測定誤差も少ないことが分かった。
【0061】
以上の分析により、血液凝固時間PT値およびINR値と近似直線からの乖離との関係があり、乖離が大きいものほどプロファイル歪が大きく、血液凝固時間PT値およびNR値の測定誤差が大きくなる確率が高くなるといえる。従って、近似直線を基準として、基準からの乖離が所定の誤差率、例えば、±15%以内を正常範囲として上限閾値、下限閾値を設定し、上限閾値から下限閾値の間の範囲内にあるかどうかを判断する事により、測定誤差が大きい可能性があるデータを除外する事が可能となる。
【0062】
そこで、近似直線が標準値であると仮定し、標準値からの誤差が所定の誤差率となる上限閾値直線および下限閾値直線を設定する。例えば、誤差率を±15%に設定すると図5(a)、(b)、(c)のグラフ中の点線のようになる。丸印で囲んだデータは、上限閾値直線および下限閾値値直線の間の正常範囲から外れており、異常データと判定することが可能となる。
【0063】
我々が開発した血液凝固時間測定装置で得られたデータでは、血液凝固時間と血液凝固時間の受光データの3倍、2倍、0.7倍になる時刻に注目して異常判定を行ったが、他の装置に適用した場合、最適な時刻の条件は異なるので、クリニックスタディを実施して最適値を求めて、設定する必要がある。また、近似直線を用いて相関関係を表現することができたが、他の装置を用いた場合、近似直線ではなく、近似曲線で表す必要がある場合もある。その場合は、近似直線、上限閾値直線、下限閾値直線を近似曲線とすれば、本発明の効果を得ることができる。
【0064】
また、CPUの性能やメモリ領域の制約があるため、本実施の形態1では、チェック領域を3点に設定している。チェック領域は、1点でも異常判定を行うことは可能であるが、多ければ多いほどより厳しい異常判定が可能となり、複数設定することが望ましい。
【0065】
以下、本実施の形態1による血液凝固時間測定装置における異常判定の動作について説明する。
図9は、異常判定の動作のフローチャートを示す図である。
【0066】
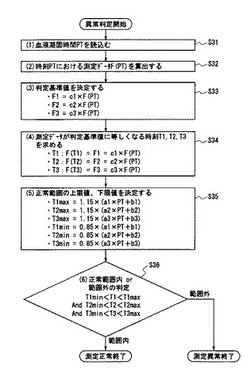
まず、血液凝固時間演算部34で算出された血液凝固時間PTを受取る(ステップS31)。
【0067】
次に、データ保持部37に保持されている受光データの時系列データから血液凝固時間PTにおける受光データF(PT)を算出する。受光データの時系列データは、所定の時間間隔で測定された離散的な値なので、時間間隔を非常に短い時間にしない限り、血液凝固時間PTに丁度一致した測定データは存在しない確率が非常に高い。したがって、離散的なデータ間を直線補間または多項式補間を用いてデータ補間することが望ましい(ステップS32)。
【0068】
次に、異常判定するチェック領域を決定するために、判定基準値F1,F2,F3を〔式1〕〜〔式3〕で示される式を用いて決定する。本実施の形態1では、判定基準値として血液凝固時間PTにおける受光データF(PT)の3倍、2倍、0.7倍となる3つの点を選択した。この倍率は、一例であり、これに限るものではない(ステップS33)。
【0069】
〔式1〕 F1=c1×F(PT) (但しc1=3.0)
【0070】
〔式2〕 F2=c2×F(PT) (但しc2=2.0)
【0071】
〔式3〕 F3=c3×F(PT) (但しc3=0.7)
【0072】
次に、測定データF(t)が判定基準値F1に等しくなる時刻T1、測定データF(t)が判定基準値F2に等しくなる時刻T2、測定データF(t)が判定基準値F3に等しくなる時刻T3を求める。受光データF(t)は、離散的な時系列データであるので、直線補間または多項式補間を用いてデータ補間することが望ましい。時刻T1における測定データをF(T1)、時刻T2における測定データをF(T2)、時刻T3における測定データをF(T3)とすると、〔式4〕〜〔式6〕のような関係式が成り立つ(ステップS34)。
【0073】
〔式4〕 T1:F(T1)=F1=c1×F(PT) (但しc1=3.0)
【0074】
〔式5〕 T2:F(T2)=F2=c2×F(PT) (但しc2=2.0)
【0075】
〔式6〕 T3:F(T3)=F3=c3×F(PT) (但しc3=0.7)
【0076】
次に、時刻T1、T2、T3の正常範囲の上限閾値および下限閾値を決定する。時刻T1の正常上限閾値をT1max、時刻T1の正常下限閾値をT1min、時刻T2の正常上限閾値をT2max、時刻T2の正常下限閾値をT2min、時刻T3の正常上限閾値をT3max、時刻T3の正常下限閾値をT3minとする。例えば、正常範囲を±15%とした場合、算出式は〔式7〕〜〔式12〕のようになる。
【0077】
a1、b1は、図5(a)に示された近似直線の傾きと切片であり、a2、b2は、図5(b)に示された近似直線の傾きと切片であり、a3、b3は、図5(c)に示された近似直線の傾きと切片である(ステップS35)。
【0078】
〔式7〕 T1max=1.15×(a1×PT+b1)
【0079】
〔式8〕 T2max=1.15×(a2×PT+b2)
【0080】
〔式9〕 T3max=1.15×(a3×PT+b3)
【0081】
〔式10〕 T1min=0.85×(a1×PT+b1)
【0082】
〔式11〕 T2min=0.85×(a2×PT+b2)
【0083】
〔式12〕 T3min=0.85×(a3×PT+b3)
【0084】
なお、規格値を±15%という値は、あくまで一例に過ぎず、血液凝固時間測定装置の特性や異常判定の要求精度により、クリニックスタディなどの実測データに基づいて最適に設定する必要がある。
【0085】
次に、ステップS34で求めたT1、T2、T3が、ステップS35で決定した正常範囲内から外れていないかどうかを判定する。すなわち〔式13〕〜〔式15〕で示した不等式を満足するかどうか判断する。全ての不等式が成立すれば、異常なしと判断し、いずれか一つでも成立しない場合、測定データのプロファイルに異常があると判断する(ステップS36)。
【0086】
〔式13〕 T1min<T1<T1max
【0087】
〔式14〕 T2min<T2<T2max
【0088】
〔式15〕 T3min<T3<T3max
【0089】
最後に、異常判定結果に応じた処理を行う。異常が検知されなかった場合は、血液凝固時間演算部で求めた血液凝固時間PTおよびINR値をLCD表示器40に表示する(図7のステップS12)。
【0090】
一方、異常検知した場合は、LCD表示器40にエラー表示を行いユーザーに認知させる(図7のステップS13)。ここで、出力ポート41にプリンタを接続していれば、必要に応じて測定結果を印刷することができる。また、出力ポート41にPCを接続していれば、PCにデータ送信することができる。さらに、測定結果を血液凝固時間測定装置内にある外部メモリ42に保存して、後で測定結果を読み出すことも可能である。
【0091】
このように本実施の形態1の血液凝固時間測定装置によれば、測定した受光データの、血液凝固時間演算部34により求められた血液凝固時間PTにおける値F(PT)に基づいて、判定基準値F1,F2,F3を設定し、かつ、血液凝固時間演算部34により求められた血液凝固時間PTに基づいて、測定された受光データの値が前記判定基準値F1,F2,F3と等しくなる時刻T1,T2,T3の正常上限時刻T1max,T2max,T3maxおよび正常下限時刻T1min,T2min,T3minを設定し、測定された受光データの値が判定基準値F1,F2,F3と等しくなる時刻T1,T2,T3を求め、該求めた時刻が前記正常上限時刻および前記正常下限時刻で設定される正常時刻範囲内にあるかを判定することにより異常判定を行なうようにしたので、判定基準値、および測定データの値が判定基準値に等しくなる時刻の正常範囲を、検体の血液凝固時間および該血液凝固時間における受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、本実施の形態1では、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことができる。
【0092】
(実施の形態2)
以下に本発明の実施の形態2における血液凝固時間測定装置について説明する。
【0093】
本実施の形態2による血液凝固時間測定装置は、図1〜3に示す実施の形態1による血液凝固時間測定装置100と同様の構成を有し、異常判定部35による異常判定の動作のみにおいて異なるものである。
【0094】
以下、本実施の形態2による血液凝固時間測定装置における異常判定の動作について説明する。
【0095】
図6(a)は、実際に行ったクリニックスタディのデータを分析して得られたグラフであり、実施の形態1の算出方法で測定された血液凝固時間PTの時刻における受光データを横軸とし、血液凝固時間PTの1.1倍となる時刻における受光データを縦軸とし、160個のデータをプロットして、これらの相関を示したものである。同様に、図6(b)は、血液凝固時間PTの時刻における受光データを横軸とし、血液凝固時間PTの1.2倍となる時刻における受光データを縦軸とし、160個のデータをプロットして、これらの相関を示したものである。同様に、図6(c)は、血液凝固時間PTの時刻における受光データを横軸とし、血液凝固時間PTの1.3倍となる時刻における受光データを縦軸とし、160個のデータをプロットして、これらの相関を示したものである。
【0096】
ここで、それぞれのグラフにおいて、160個の測定データを対象に最小二乗法により近似二次曲線を引いてみる。図6(a)の近似二次曲線の二次係数j1は−0.0009、一次係数k1は1.6135、定数項l1は−0.9942である。また、図6(b)の近似二次曲線の二次係数j2は−0.0024、一次係数k2は2.3638、定数項はl2は−1.9774である。また、図6(c)の近似二次曲線の二次係数j3は−0.0039、一次係数k3は3.1594、定数項l3は−2.1428である。
【0097】
図6(a)〜図6(c)に示すグラフより、ほとんどの測定データが近似二次曲線近傍に集中していることがわかる。さらに、前記近似二次曲線から比較的大きく離れたデータ、すなわち丸印で囲んだ測定データを個々に分析してみると、受光データ23のプロファイルが歪んでおり、測定される血液凝固時間PT値およびINR値の測定誤差が非常に大きいことが分かった。また、近似二次曲線近傍にあるデータの受光データ23は、プロファイルの歪が非常に少なく、測定される血液凝固時間PT値およびINR値の測定誤差も少ないことが分かった。
【0098】
以上の分析により、血液凝固時間PT値およびINR値と近似二次曲線からの乖離との関係があり、乖離が大きいものほどプロファイル歪が大きく、血液凝固時間PT値およびNR値の測定誤差が大きくなる確率が高くなるといえる。従って、近似二次曲線を基準として、基準からの乖離が所定の誤差率、例えば、±15%以内を正常範囲として上限閾値、下限閾値を設定し、上限閾値から下限閾値の間の範囲内にあるかどうかを判断する事により、測定誤差が大きい可能性があるデータを除外する事が可能となる。
【0099】
そこで、近似二次曲線が標準値であると仮定し、標準値からの誤差が所定の誤差率となる上限閾値直線および下限閾値直線を設定する。例えば、誤差率を±15%に設定すると図6(a)、(b)、(c)のグラフ中の点線のようになる。丸印で囲まれたデータは、上限閾値直線および下限閾値値直線の間の正常範囲から外れており、異常データと判定することが可能となる。
【0100】
我々が開発した血液凝固時間測定装置で得られたデータでは、血液凝固時間における受光データと血液凝固時間の1.1倍、1.2倍、1.3倍の時刻における受光データに注目して異常判定を行ったが、他の装置に適用した場合、最適な時刻の条件は異なるので、クリニックスタディを実施して最適値を求めて、設定する必要がある。
【0101】
また、CPUの性能やメモリ領域の制約があるため、本実施の形態2では、チェック領域を3点に設定している。チェック領域は、1点でも異常判定を行うことは可能であるが、多ければ多いほどより厳しい異常判定が可能となり、複数設定することが望ましい。
【0102】
図10は、本発明の実施の形態2における異常判定のフローチャートを示している。
まず、血液凝固時間演算部34で算出された血液凝固時間PTを受取る(ステップS41)。
【0103】
次に、データ保持部37に保持されている受光データの時系列データから血液凝固時間PTにおける受光データF(PT)を算出する。実施の形態1と同様に、離散的なデータ間を直線補間または多項式補間を用いてデータ補間することが望ましい(ステップS42)。
【0104】
次に、異常判定するチェック領域を決定するために、判定基準時刻t1、t2、t3を〔式16〕〜〔式18〕で示される式を用いて決定する。本実施の形態2では、判定基準時刻として血液凝固時間PTの1.1倍、1.2倍、1.3倍となる3つの点を選択した。この倍率は、一例であり、これに限るものではない(ステップS43)。
【0105】
〔式16〕 t1=d1×PT (但しd1=1.1)
【0106】
〔式17〕 t2=d2×PT (但しd2=1.2)
【0107】
〔式18〕 t3=d3×PT (但しd3=1.3)
【0108】
次に、データ保持部37に保持されている受光データの時系列データから判定基準時刻t1、t2、t3における受光データf1(=F(t1))、f2(=F(t2))、f3(=F(t3))を〔式19〕〜〔式21〕に基づいて算出する。受光データの時系列データは、所定の時間間隔で測定された離散的な値なので、時間間隔を非常に短い時間にしない限り、判定基準時刻t1、t2、t3に丁度一致した測定データは存在しない確率が非常に高い。したがって、離散的なデータ間を直線補間または多項式補間を用いてデータ補間することが望ましい(ステップS44)。
【0109】
〔式19〕 f1=F(t1)=F(d1×PT) (但しd1=1.1)
【0110】
〔式20〕 f2=F(t2)=F(d2×PT) (但しd2=1.2)
【0111】
〔式21〕 f3=F(t3)=F(d3×PT) (但しd3=1.3)
【0112】
次に、時刻t1、t2、t3における受光データf1、f2、f3の正常範囲の上限閾値および下限閾値を決定する。例えば、正常範囲を±15%とした場合、算出式は〔式22〕〜〔式27〕のようになる。ここで、f1maxは時刻t1における受光データf1の正常上限値、f2maxは時刻t2における受光データf2の正常上限値、f3maxは時刻t3における受光データf3の正常上限値、f1minは時刻t1における受光データf1の正常下限値、f2minは時刻t2における受光データf2の正常下限値、f3minは時刻t3における受光データf3の正常下限値である。
【0113】
j1、k1、およびl1は、図6(a)に示される近似二次曲線の二次係数、一次係数、および定数項であり、j2、k2、およびl3は、図6(b)に示される近似二次曲線の二次係数、一次係数、および定数項であり、j3、k3、およびl3は、図6(c)に示される近似二次曲線の二次係数、一次係数、および定数項である(ステップS45)。
【0114】
〔式22〕 f1max=1.15×(j1×F(PT)×F(PT)+k1×F(PT)+l1)
【0115】
〔式23〕 f2max=1.15×(j2×F(PT)×F(PT)+k2×F(PT)+l2)
【0116】
〔式24〕 f3max=1.15×(j3×F(PT)×F(PT)+k3×F(PT)+l3)
【0117】
〔式25〕 f1min=0.85×(j1×F(PT)×F(PT)+k1×F(PT)+l1)
【0118】
〔式26〕 f2min=0.85×(j2×F(PT)×F(PT)+k2×F(PT)+l2)
【0119】
〔式27〕 f3min=0.85×(j3×F(PT)×F(PT)+k3×F(PT)+l3)
【0120】
ただし、
【0121】
j1=-0.0009、k1=1.6135、l1=-0.9942
【0122】
j2=-0.0024、k2=2.3638、l2=-1.9774
【0123】
j3=-0.0039、k3=3.1594、l3=-2.1428である。
【0124】
なお、規格値を±15%という値は、あくまで一例に過ぎず、血液凝固時間測定装置の特性や異常判定の要求精度によってクリニックスタディなどの実測データに基づいて最適に設定する必要がある。
【0125】
次に、ステップS44で求めたf1、f2、f3が、ステップS45で決定した正常範囲内から外れていないかどうかを判定する。すなわち〔式28〕〜〔式30〕で示した不等式を満足するかどうか判断する。全ての不等式が成立すれば、異常なしと判断し、いずれか一つでも成立しない場合、測定データのプロファイルに異常があると判断する(ステップS46)。
【0126】
〔式28〕 f1min<f1<f1max
【0127】
〔式29〕 f2min<f2<f2max
【0128】
〔式30〕 f3min<f3<f3max
【0129】
最後に、異常判定結果に応じた処理を行う。すなわち、上記実施の形態1と同様、異常が検知されなかった場合は、血液凝固時間演算部で求めた血液凝固時間PTおよびINR値をLCD表示器40に表示し、異常検知した場合は、LCD表示器40にエラー表示を行いユーザーに認知させる。ここで、出力ポート41にプリンタを接続していれば、必要に応じて測定結果を印刷することができる。また、出力ポート41にPCを接続していれば、PCにデータ送信することができる。さらに、測定結果を血液凝固時間測定器内にある外部メモリ42に保存して、後で測定結果を読み出すことも可能である。
【0130】
このように本実施の形態2の血液凝固時間測定装置によれば、前記血液凝固時間演算部により求められた血液凝固時間PTに基づいて、判定基準時刻t1,t2,t3を設定し、かつ、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間PTにおける値F(PT)に基づいて、測定した受光データの判定基準時刻t1,t2,t3における値f1,f2,f3の正常上限値f1max,f2max,f3maxおよび正常下限値f1min,f2min,f3minを設定し、測定した受光データの判定基準時刻t1,t2,t3における値f1,f2,f3を求め、該求めた値が前記正常上限値および前記正常下限値で設定される正常値範囲内にあるかを判定することにより異常判定を行なうようにしたので、判定基準時刻、および該判定基準時刻における受光データの正常範囲を、検体の血液凝固時間および該血液凝固時間における受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、本実施の形態2においても上記実施の形態1と同様、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことができる。
【産業上の利用可能性】
【0131】
本発明にかかる血液凝固時間測定装置は、検体の受光光量差や反応開始時刻の影響を排除することができ、光量検体の血液凝固能や固体差に依存することなく良好な異常検知が可能となる。また、血液凝固反応が飽和するまで測定する必要が無く短時間で測定するような高速演算方法においても良好な効果を得ることが可能となる。
【図面の簡単な説明】
【0132】
【図1】本発明の実施の形態1による血液凝固時間測定装置の斜視図
【図2】本発明の実施の形態1による血液凝固時間測定装置の光学台の断面図
【図3】本発明の実施の形態1による血液凝固時間測定装置のブロック図
【図4】本発明の実施の形態1による血液凝固時間測定装置における血液凝固時間の測定フローを示す図
【図5】本発明の実施の形態1において用いるクリニックスタディの測定データを示す図
【図6】本発明の実施の形態2において用いるクリニックスタディの測定データを示す図
【図7】本発明の実施の形態1による血液凝固時間測定装置における測定動作のフローチャート図
【図8】本発明の実施の形態1による血液凝固時間測定装置における血液凝固時間の演算のフローチャート図
【図9】本発明の実施の形態1による血液凝固時間測定装置における血液凝固時間の異常判定動作のフローチャート図
【図10】本発明の実施の形態2による血液凝固時間測定装置における血液凝固時間の異常判定動作のフローチャート図
【図11】従来の光学的方法を用いた血液凝固時間装置の構成図
【図12】従来の光学的方法を用いた血液凝固時間の測定方法を説明するための図
【図13】従来の問題点を説明するための図
【符号の説明】
【0133】
1 血液凝固時間測定装置
3 試験片
4 反応部
5 試料
6 光学台
7 窓部
8 蓋
9 光源
10 レンズ
11 受光手段
12 光源フィルタ
13 受光フィルタ
20 ホルダー
21 温度制御手段
22 電極
23 受光データ
24 一次微分
25 近似直線
30 LEDドライバ
31 操作スイッチ
32 CPU
33 制御部
34 血液凝固時間演算部
35 異常判定部
36 データ測定部
37 データ保持部
38 電流電圧変換回路
39 アナログ−デジタル変換回路
40 LCD表示器
41 出力ポート
42 外部メモリ
43 タイマー
51 試験管
52 試薬供給装置
53 ピペット
54 LED
55 フォトダイオード
56 計測部
57 CRT
【技術分野】
【0001】
本発明は、被分析試料中の物質と反応して吸光、発光、蛍光、散乱光などの光学的な変化を伴う光学的信号を分析することにより血液凝固時間を測定する血液凝固時間測定装置に関するものである。
【背景技術】
【0002】
以下、従来の血液凝固時間測定装置について図11、図12を用いて説明する。従来の血液凝固時間測定装置は図11に示すような構成となっていた(例えば、特許文献1参照。)。
【0003】
図11において、透明な試験管51には、測定される血漿が予め収容され、試薬供給器52からピペット53を介して例えばPT試薬等の試薬が試験管51へ供給され、LED54からの光が試験管1に照射される。試験管51の内部で散乱した散乱光はフォトダイオード55に受光され、散乱光量が検出される。
【0004】
計測部56は、散乱光量の飽和を検出する検出部56aと、散乱光量が増加するか否かを判定する判定部56bと、散乱光量の飽和を検出した時にその後の所定時間内に散乱光量がさらに増加するか否かを判定し増加するときには次の飽和を検出するという処理がくり返し行なわれるように検出部56aと判定部56bとを制御する制御部56cと、散乱光量の飽和が最終的に検出されたとき、その飽和値に基づいて凝固時間を算出する算出部56dを備え、フォトダイオード55の出力信号を処理して、処理結果をCRT57に表示するようになっている。なお計測部56は、CPU,ROM,RAMからなるマイクロコンピュータから構成されている。
【0005】
図12は、図11の従来の血液凝固時間測定装置を用いて測定されたデータの一例を示している。横軸は、測定される血漿と試薬を混合した後の経過時間を示す。縦軸は、検出される受光光量を示している。この場合、血液凝固時間は、受光光量の変化量が飽和した時の50%になる時刻で測定される。さらに、測定データに異常がないかどうかを判断するために、以下のような異常判定を行なっている。
【0006】
まず、反応速度の異常を判断するために、例えば、受光光量が飽和光量の50%の領域H2を中心としてプラスマイナス4%になる領域をチェック領域に設定し、このチェック領域内での受光光量の変化率を求め、正常範囲内であるかどうかを判断している。
【0007】
次に、初期反応の有無の判定として、例えば反応開始後20秒あたりの反応初期にチェック領域を設定し、この部分での受光光量の変化率を求め、正常範囲内であるかどうかにより判断している。
【0008】
さらに、反応曲線のドリフトの有無を判定するために、2つのチェック領域を設定し、それぞれのチェック領域での受光光量の変化率の求め、2つの変化率の比率をさらに求め、正常範囲内であるかどうかにより判断している。例えば、チェック領域は、受光光量が飽和光量の46%〜54%の領域(H2−h〜H2+h)と、6%〜14%の領域(H1−h〜H1+h)に設定している。
【0009】
また、反応開始時刻が早すぎないかどうかの判定として、受光光量が所定値を超える時刻を求め、正常範囲かどうかを判断している。
【特許文献1】特開2003−169700号公報
【発明の開示】
【発明が解決しようとする課題】
【0010】
しかしながら、このような従来の血液凝固時間測定装置では、測定される受光光量は、測定される血液の血液凝固能の差により、光量変化量だけでなく、変化開始時刻、変化率に大きな差が存在し、精度の高い異常判定を行なうことができないという課題がある。血液凝固時間の測定値は、抗凝固剤の投薬量を決定するために用いられるため、その測定誤差は生命に関わる危険性が高い。従って、非常に高い信頼性が必要である。もし、装置や化学反応に何らかの異常を検知した場合、安全にその異常をユーザーに認知させる必要があり、決して信頼性の無い測定結果を表示してはならない。
【0011】
この点について今少し説明する。図13に実際に測定した受光光量の測定データを示す。図13は、それぞれ血液凝固時間が異なる場合、言い換えれば国際標準比(以降INR値と記す)が異なる場合のプロファイルの違いを示したものである。図からわかるように、INR値が大きいほど変化開始の時刻が遅く、変化量の大きさ、すなわち変化率が小さくなる傾向がある。また、変化開始している時刻が同じ、すなわち、同じINR値であるプロファイルでも、変化量の大きさやプロファイルの傾き、すなわち変化率が異なっている。
【0012】
したがって、従来の血液凝固時間測定装置では、INR値の違いによって生じる変化開始時刻の違いや傾きの違いのため、最適なチェック領域を設定することが難しく、また、最適な異常判定の閾値を設定することが難しいという課題がある。
【0013】
さらに、従来の血液凝固時間測定装置では、異常判定をするチェック領域を受光光量の飽和値を基に設定しているので、微分値の最大時刻を検知した時点で測定完了することができる高速測定方法では異常判定を行なうことができないという課題がある。
【0014】
本発明は、これらの課題を解決するためになされたものであり、精度の高い異常判定を行ない、血液凝固時間を測定することのできる血液凝固時間測定装置を提供することを目的とする。
【課題を解決するための手段】
【0015】
上記の課題を解決するために、本発明(請求項1)の血液凝固時間測定装置は、血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、前記光学的信号を電気的な受光信号に変換する受光器と、前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、前記データ測定部で測定された受光データを一時的に保持するデータ保持部と、前記データ保持部に保持された受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、前記異常判定部が、前記血液凝固時間演算部により求められた血液凝固時間および該血液凝固時間における前記測定した受光データの値に基づいて、異常判定を行うチェック領域および該チェック領域における正常範囲を設定し、前記測定した受光データが前記正常範囲内にあるか否かを判定する、ことを特徴とするものである。
【0016】
これにより、チェック領域およびチェック領域における正常範囲を、検体の血液凝固時間および受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことを可能とできる。
【0017】
また、本発明(請求項2)の血液凝固時間測定装置は、血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、前記光学的信号を電気的な受光信号に変換する受光器と、前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、前記異常判定部が、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間における値に基づいて、少なくとも1つの判定基準値を設定し、かつ、前記血液凝固時間演算部により求められた血液凝固時間に基づいて、前記測定された受光データの値が前記判定基準値と等しくなる時刻の正常上限時刻および正常下限時刻を設定し、前記測定された受光データの値が前記判定基準値と等しくなる時刻を求め、該求めた時刻が前記正常上限時刻および前記正常下限時刻で設定される正常時刻範囲内にあるか否かを判定する、ことを特徴とするものである。
【0018】
これにより、判定基準値、および受光データの値が前記判定基準値に等しくなる時刻の正常範囲を、検体の血液凝固時間および受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことを可能とできる。
【0019】
また、本発明(請求項3)の血液凝固時間測定装置は、血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、前記光学的信号を電気的な受光信号に変換する受光器と、前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、前記異常判定部が、前記血液凝固時間演算部により求められた血液凝固時間に基づいて、少なくとも1つの判定基準時刻を設定し、かつ、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間における値に基づいて、前記測定した受光データの前記判定基準時刻における値の正常上限値および正常下限値を設定し、前記測定した受光データの前記判定基準時刻における値を求め、前記求めた値が前記正常上限値および前記正常下限値で設定される正常値範囲内にあるか否かを判定する、ことを特徴とするものである。
【0020】
これにより、判定基準時刻、および判定基準時刻における受光データの値の正常範囲を、検体の血液凝固時間および受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことを可能とできる。
【発明の効果】
【0021】
本発明の血液凝固時間測定装置によれば、測定データから求めた血液凝固時間および該血液凝固時間における受光光量データの値に基づいて、チェック領域および該チェック領域における正常上限値および正常下限値を設定するようにしたから、異常判定を行なうチェック領域が、検体の血液凝固能に依存せず、受光データの変化量、変化率の違いや反応開始時間の違いなどに影響されないので、検体の血液凝固時間に影響されずに高精度な異常判定を行うことができる効果がある。
【0022】
また、本発明の血液凝固時間測定装置によれば、チェック領域を設定するために受光光量の飽和値を知る必要がないため、微分値の最大時刻を検知した時点で測定完了することができる高速測定方法においても良好な異常判定を行なうことができる効果がある。
【発明を実施するための最良の形態】
【0023】
(実施の形態1)
以下に、本発明の実施の形態について、図面に基づいて説明する。
図1は、本発明の実施の形態1における血液凝固時間測定装置100の斜視図である。
【0024】
図1において、本実施の形態1の血液凝固時間測定装置100には、試験片3を設置するための光学台6が設けられている。試験片3上の反応部4には、血液5の凝固反応に応じて蛍光強度を変化させるような化学反応を起こさせる試薬が含まれている。光学台6の上には、ホルダー20が装着されており、試験片3が適切な測定位置に配置できるように挿入路を形成している。さらにホルダー20は、弾性構造になっており、試験片3を温度制御手段21に押し当てて、熱伝導性を高める役割を果たしている。
【0025】
試験片3を血液凝固時間測定装置100の光学台6上に設置した際に、反応部4は、光学台6上に設けられた窓部7に合致するように位置決めされる。試験片3はホルダー20によって温度制御手段21に押し当てられるような構造となっている。光学台6上には電極22が備えられており、試験片3を使った試料の測定時には、試料の点着を検出したり、測定中の試料の抵抗値など測定したりする目的で試験片3上に備えられている電極と接続されるようになっている。また血液凝固時間測定装置100には、測定中の外光や埃等の侵入を防止する目的で、閉状態で光学台6を遮光できるような開閉可能な蓋8が設けられている。
【0026】
図2は、光学台6の断面を示す図である。光学台6の内部には、温度制御手段21、光源9、光源フィルタ12、レンズ10、受光フィルタ13、受光手段11が備えられている。
【0027】
温度制御手段21は、血液5と反応部4内に含まれている反応物質との反応が最も活性化する温度、もしくは、反応が最も安定するような温度になるように反応部4の温度を制御するための温度制御手段である。例えば、アルミナ系セラミック基板上に厚膜抵抗体などの加温手段と、温度検出用のサーミスタなどの温度検出手段をそなえた面状ヒーターなどにより構成する事ができる。また、制御温度が動作環境温度よりも低いような冷却を必要とする場合においては、加温手段の代替としてペルチェ素子のような加温冷却手段を用いる事により構成することができる。なお、加温または加温冷却手段は、一例をあげたに過ぎず、加温または冷却する事ができるものであれば他のものも用いる事ができる。なお、温度制御が不要な場合では、温度制御手段21を必ずしも備える必要はない。
【0028】
光源9は、反応部4に対して光学的エネルギーを印加するためのものであり、例えば白熱電球、LED、半導体レーザー、有機EL等を用いることができる。光源9は、駆動手段に接続され、測定中は光学的出力が安定して得られるように制御されている。
【0029】
光源フィルタ12は、光源9から射出される光路上に配置されており、これにより光源9から発せられた光のうち、光源フィルタ12の特性により選択された波長帯域の光を反応部4へ照射することができる。光学フィルタ12の特性は、血液5と反応部4内の反応物質との反応に伴う光学的な波長により透過波長帯域および遮断波長帯域が決まり、バンドパスフィルタ、ショートパスフィルタ、ロングパスフィルタ、マルチパスフィルタなどを用いる事ができる。なお、光源9が半導体レーザーダイオードのような単一波長である場合や、LEDなどの特定の波長帯域幅だけであり、かつ、受光すべき波長に影響しない場合においては、光源フィルタ12を必ずしも備える必要はない。
【0030】
レンズ10は、試験片3上の反応部4に面する側が平面であり、受光手段11に面する側がレンズ曲面となっている。本実施の形態では、平面側は、反応部4にほとんど接するような位置に配置されている。実際には、接触による傷や汚染の防止のために300〜500μm程度の隙間ができるようにしている。本実施の形態では、光学的効率を向上させる目的でレンズ10を入れているが、受光量をそれほどあげる必要がない場合は、レンズ10を備えなくても構わない。
【0031】
光源フィルタ12により選択された波長の光は、レンズ10のレンズ曲面側から入射し、平面側より出射して反応部4へ照射される。
【0032】
反応部4内の反応物質と点着された血液5の反応により、蛍光物質が生成されて蛍光特性が表れ、励起光を照射する事によって、蛍光を発するようになる。
【0033】
反応部4より発せられた蛍光は、レンズ10の平面側から入射し、曲面側より出射され、受光フィルタ13を透過して、受光手段11によって受光される。
【0034】
受光フィルタ13は、反応部4から発せられた蛍光のみを透過させ、それ以外の不要な光を阻止する目的の光学フィルタである。この受光フィルタ13の特性は、血液5と反応部4内の反応物質との反応に伴う光学的な波長に関連した要求仕様に基づいて決まり、少なくとも、励起光源波長帯域を遮断し、反応部4からの光学信号の波長帯域を透過させるようなフィルタ特性が必要となる。望ましくは、反応部4から得られる光学的信号の波長のみを透過させ、それ以外の不要な光の波長を遮断するようなバンドパスフィルタが望ましいが、要求仕様によっては、ショートパスフィルタ、ロングパスフィルタ、マルチパスフィルタなどを用いる事ができる場合もある。
【0035】
受光手段11に受光された光学的信号は、光電変換された後、信号処理回路により、所定の信号分析が行なわれる。信号処理回路は一般的にアナログ増幅回路、アナログ−デジタル変換回路、マイクロプロセッサ等から構成される。
【0036】
図3は、血液凝固時間測定装置100の構成を示すブロック図である。図において、図1、図2と同一符号は同一又は相当部分である。また、30は光源9を駆動するLEDドライバである。32はCPUであり、制御部33、血液凝固時間演算部34、異常検知部35、データ測定部36、およびデータ保持部37を備える。また38は受光手段11が出力する光電流を電圧に変換する電流電圧変換回路(I/V)、39はI/V38のアナログ出力をデジタル信号に変換するアナログ−デジタル変換回路(A/D)である。40は測定結果等を表示するLCD表示器、41はデータを血液凝固時間測定装置100の外部に出力する出力ポート、42は外部メモリ、43はCPU32の動作クロックを発生するタイマーである。31は操作スイッチであり、CPU32の制御部33は操作スイッチ31からの操作入力に応じて測定動作が行われるように各部を制御する。
【0037】
以上のように構成された血液凝固時間測定装置100の測定動作について説明する。
図7は、測定動作のフローチャートである。
【0038】
ユーザーが操作スイッチ31を操作することにより、血液凝固時間測定装置100は、測定モードに移行する。まず、最初に、ユーザーに対して試験片3を挿入するよう、LCD表示器40に試験片挿入指示メッセージを表示する(ステップS1)。
【0039】
ホルダー20が取付けられている光学台6の所定の位置に試験片3を挿入されると、電極ピン22の電極間抵抗値が変化することにより試験片3が装着された事を検知する(ステップS2)。その後、温度制御手段21により試験片3上の反応部4が所定の温度、例えば血液凝固反応が安定する37℃になるように温度制御を行なう(ステップS3)。
【0040】
温度が所定温度に達した後、分析対象である血液5を反応部4へ点着するようにLCD表示器40に点着指示メッセージを表示する(ステップS4)。
【0041】
ユーザーにより点着されると、電極間の抵抗値の変化が生じ、これを検知してデータ測定を開始する(ステップS5)。
【0042】
測定開始と同時に、LCD表示器40に蓋閉め指示メッセージを表示する(ステップS6)。
【0043】
その後、予め決められた時間毎、例えば、5秒毎にLEDドライバ30により光源9を点灯させることにより反応部4へ励起光を照射し、受光手段11より得られる受光信号をI/V38およびA/D39を通してデータ測定部36で測定し、光源9を消灯する。光源9を消灯するのは、低消費電力、光源寿命、蛍光退色などのデメリットを軽減するためのものであり、特に問題とならない場合には、消灯しなくても構わない。このようにして、反応部4から得られる光学的信号強度を受光手段11により電気信号に変換し、適切に構成された増幅回路により増幅し、A/D39によりデジタルデータに変換した後、データ測定部36で測定し、その時系列的な測定データを記憶手段であるデータ保持部37により一時記憶してゆく。そして、各々の測定毎に、一次微分を演算しながら最大値になる時刻を監視する。一次微分が最大値となる時刻を検知し、測定を終了する。(ステップS7、S8、S9)
【0044】
受光データには電気的または光学的なノイズが含まれる場合が多く、各々の測定毎のA/D変換は1回だけではなく複数回のサンプリングを行い、一般的に用いられる安定化手法、例えば、平均値、中心値、分布偏差が大きい部分を除外したデータの平均化などの方法により行なうことが好ましい。また、前後の複数のデータから平滑化処理、例えば、前後データの平均値、重み付け加算値、中心値など方法により処理した後に演算をおこなうのが望ましい。
【0045】
受光データ測定終了後、データ保持部37に記憶された時系列データをもとに血液凝固時間演算部34によって、血液凝固時間PT値およびINR値を演算する(ステップS10)。
【0046】
以下に、血液凝固時間およびINR値を求める方法の一例として、一次微分を利用した演算方法を示す。本発明の進歩性の一つとして高速測定方法にも有効であるため、一次微分を利用した演算部の例を示すが、他の演算方法による場合でも本発明は同様に有効であり、この演算方法に限定するものではない。
【0047】
図4は、測定データの一例を示した図である。図において、23は受光信号データを示すグラフであり、24はその一次微分を示すグラフである。
【0048】
受光データ23において、測定開始から約30秒までの間に、受光信号に変化がない部分が存在する。この部分では、血液凝固による蛍光変化は起こっていないため、この部分の受光データは蛍光以外の定常的なオフセット成分によるものである。
【0049】
測定される受光信号には、反応部4から得られる純粋に血液凝固反応に応じた蛍光信号と、それ以外の不要な光による受光信号が含まれる。後者の要因としては、光源9から発せられた光が、レンズ10の表面や反応部4で反射した反射光のうち受光フィルタ13で阻止しきれずに透過してきた不要な光による成分が支配的である。また、電気的なオフセット信号も含まれている。以降の測定において定常的なオフセット信号となる。
【0050】
以下、本実施の形態1における血液凝固時間(PTsec)および国際標準値(INR)を算出する方法を示す。
【0051】
(1)受光データ23を時間微分し、一次微分24を求め、一次微分24が最大となる時刻T1を求める。図4では、一次微分24は、説明を解りやすくするために正規化したものを示しているが、特に正規化する必要はない。
【0052】
(2)受光データ23上の時刻T1の点を求める。
【0053】
(3)時刻T1を基準として、所定の時間関係にある点T2、T3、T4、T5における受光データ23上の点を求める。例えば、データの測定間隔が5秒間隔として、T1の時刻を基準にT2が5秒前、T3が5秒後、T4が10秒前、T5が10秒後とする。なお、この例では、時間間隔を5秒、サンプル点数を5個としたが、測定装置の全体性能に影響がない限り、測定間隔を短くし、サンプリング数を多くする事が望ましい。少なくともサンプル点は、2点以上とする。
【0054】
(4)受光データ23上の時刻T1,T2,T3,T4,T5の5点のデータより近似直線25を求める。ここで、精度的に問題ない限り、正確な近似直線でない近似計算、または、実質的に近似直線と同等な直線式でも本発明の効果は同様に得られる。本例では5点を用いて近似直線を求めているが、サンプリング間隔を短くし、さらに多くの点から近似直線25を求めるのが望ましい。また、最も簡単な処理で実現しようとする場合、サンプル点はT2およびT3とし、2点を結ぶ傾きをもったT1からT3までのいずれかの点を含む直線を近似直線25としてもよい。
【0055】
(5)受光データ23のうち、蛍光反応以外の要因による定常的なオフセットデータを表すベースライン26を求める。例えば、受光データ23の最小値とする方法が最も簡単である。また、別の方法としては、受光データ23が所定の閾値以上になる時刻を求め、測定開始から閾値を超える時刻までの間の少なくとも2点以上のデータの平均値とする方法でもよい。この場合、採用するデータとしては、最小値側から所定データ数、または、分布的に最小値側に分布する所定%に含まれるデータを採用するのが好ましい。また、これ以外の方法でも実質的に同等であれば本発明の効果は同様に得られる。
【0056】
(6)近似直線25とベースライン26が交差する点の時刻Tmを求める。
【0057】
(7)補正式により、血液凝固時間PTsecおよび国際標準値INRを演算する。上記で求められたTmは、使用する反応試薬や測定器の光学検出性能に依存するところが大きく、測定方法によって補正式は全く異なる。また、測定する試料の種類、例えば、穿刺血、クエン酸血、血漿などの違いによっても補正式は異なる。従って、詳細な式については、本実発明の効果には影響無いので省略する。
【0058】
図5(a)は、実際に行ったクリニックスタディのデータを分析して得られたグラフであり、上記の算出方法で測定された血液凝固時間PTを横軸とし、受光データが、血液凝固時間PTにおける受光データの3.0倍になる時刻を縦軸とし、160個のデータをプロットして、これらの相関を示したものである。同様に、図5(b)は、実際に行ったクリニックスタディのデータを分析して得られたグラフであり、上記の算出方法で測定された血液凝固時間PTを横軸とし、受光データが、血液凝固時間PTにおける受光データの2.0倍になる時刻を縦軸とし、160個のデータをプロットして、これらの相関を示したものである。同様に、図5(c)は、実際に行ったクリニックスタディのデータを分析して得られたグラフであり、上記の算出方法で測定された血液凝固時間PTを横軸とし、受光データが、血液凝固時間PTにおける受光データの0.7倍になる時刻を縦軸とし、160個のデータをプロットして、これらの相関を示したものである。
【0059】
ここで、それぞれのグラフにおいて、160個の測定データを対象に最小二乗法により近似直線を引いてみる。図5(a)の近似直線の傾きa1は、1.3293、切片b1は、0.2867である。また、図5(b)の近似直線の傾きa2は、1.202、切片b2は、−0.7534である。また、図5(c)の近似直線の傾きa3は、0.8751、切片b3は、2.0128である。
【0060】
図5(a)〜図5(c)に示すグラフより、ほとんどの測定データが近似直線近傍に集中していることがわかる。すなわち、それぞれの測定データは、血液凝固時間PT値およびINR値が異なる値であるにも関わらず、相関に直線性があるといえる。さらに、前記近似直線から比較的大きく離れたデータ、すなわち丸印で囲んだ測定データを個々に分析してみると、受光データ23のプロファイルが歪んでおり、測定される血液凝固時間PT値およびINR値の測定誤差が非常に大きいことが分かった。また、近似直線近傍にあるデータの受光データ23は、プロファイルの歪が非常に少なく、測定される血液凝固時間PT値およびINR値の測定誤差も少ないことが分かった。
【0061】
以上の分析により、血液凝固時間PT値およびINR値と近似直線からの乖離との関係があり、乖離が大きいものほどプロファイル歪が大きく、血液凝固時間PT値およびNR値の測定誤差が大きくなる確率が高くなるといえる。従って、近似直線を基準として、基準からの乖離が所定の誤差率、例えば、±15%以内を正常範囲として上限閾値、下限閾値を設定し、上限閾値から下限閾値の間の範囲内にあるかどうかを判断する事により、測定誤差が大きい可能性があるデータを除外する事が可能となる。
【0062】
そこで、近似直線が標準値であると仮定し、標準値からの誤差が所定の誤差率となる上限閾値直線および下限閾値直線を設定する。例えば、誤差率を±15%に設定すると図5(a)、(b)、(c)のグラフ中の点線のようになる。丸印で囲んだデータは、上限閾値直線および下限閾値値直線の間の正常範囲から外れており、異常データと判定することが可能となる。
【0063】
我々が開発した血液凝固時間測定装置で得られたデータでは、血液凝固時間と血液凝固時間の受光データの3倍、2倍、0.7倍になる時刻に注目して異常判定を行ったが、他の装置に適用した場合、最適な時刻の条件は異なるので、クリニックスタディを実施して最適値を求めて、設定する必要がある。また、近似直線を用いて相関関係を表現することができたが、他の装置を用いた場合、近似直線ではなく、近似曲線で表す必要がある場合もある。その場合は、近似直線、上限閾値直線、下限閾値直線を近似曲線とすれば、本発明の効果を得ることができる。
【0064】
また、CPUの性能やメモリ領域の制約があるため、本実施の形態1では、チェック領域を3点に設定している。チェック領域は、1点でも異常判定を行うことは可能であるが、多ければ多いほどより厳しい異常判定が可能となり、複数設定することが望ましい。
【0065】
以下、本実施の形態1による血液凝固時間測定装置における異常判定の動作について説明する。
図9は、異常判定の動作のフローチャートを示す図である。
【0066】
まず、血液凝固時間演算部34で算出された血液凝固時間PTを受取る(ステップS31)。
【0067】
次に、データ保持部37に保持されている受光データの時系列データから血液凝固時間PTにおける受光データF(PT)を算出する。受光データの時系列データは、所定の時間間隔で測定された離散的な値なので、時間間隔を非常に短い時間にしない限り、血液凝固時間PTに丁度一致した測定データは存在しない確率が非常に高い。したがって、離散的なデータ間を直線補間または多項式補間を用いてデータ補間することが望ましい(ステップS32)。
【0068】
次に、異常判定するチェック領域を決定するために、判定基準値F1,F2,F3を〔式1〕〜〔式3〕で示される式を用いて決定する。本実施の形態1では、判定基準値として血液凝固時間PTにおける受光データF(PT)の3倍、2倍、0.7倍となる3つの点を選択した。この倍率は、一例であり、これに限るものではない(ステップS33)。
【0069】
〔式1〕 F1=c1×F(PT) (但しc1=3.0)
【0070】
〔式2〕 F2=c2×F(PT) (但しc2=2.0)
【0071】
〔式3〕 F3=c3×F(PT) (但しc3=0.7)
【0072】
次に、測定データF(t)が判定基準値F1に等しくなる時刻T1、測定データF(t)が判定基準値F2に等しくなる時刻T2、測定データF(t)が判定基準値F3に等しくなる時刻T3を求める。受光データF(t)は、離散的な時系列データであるので、直線補間または多項式補間を用いてデータ補間することが望ましい。時刻T1における測定データをF(T1)、時刻T2における測定データをF(T2)、時刻T3における測定データをF(T3)とすると、〔式4〕〜〔式6〕のような関係式が成り立つ(ステップS34)。
【0073】
〔式4〕 T1:F(T1)=F1=c1×F(PT) (但しc1=3.0)
【0074】
〔式5〕 T2:F(T2)=F2=c2×F(PT) (但しc2=2.0)
【0075】
〔式6〕 T3:F(T3)=F3=c3×F(PT) (但しc3=0.7)
【0076】
次に、時刻T1、T2、T3の正常範囲の上限閾値および下限閾値を決定する。時刻T1の正常上限閾値をT1max、時刻T1の正常下限閾値をT1min、時刻T2の正常上限閾値をT2max、時刻T2の正常下限閾値をT2min、時刻T3の正常上限閾値をT3max、時刻T3の正常下限閾値をT3minとする。例えば、正常範囲を±15%とした場合、算出式は〔式7〕〜〔式12〕のようになる。
【0077】
a1、b1は、図5(a)に示された近似直線の傾きと切片であり、a2、b2は、図5(b)に示された近似直線の傾きと切片であり、a3、b3は、図5(c)に示された近似直線の傾きと切片である(ステップS35)。
【0078】
〔式7〕 T1max=1.15×(a1×PT+b1)
【0079】
〔式8〕 T2max=1.15×(a2×PT+b2)
【0080】
〔式9〕 T3max=1.15×(a3×PT+b3)
【0081】
〔式10〕 T1min=0.85×(a1×PT+b1)
【0082】
〔式11〕 T2min=0.85×(a2×PT+b2)
【0083】
〔式12〕 T3min=0.85×(a3×PT+b3)
【0084】
なお、規格値を±15%という値は、あくまで一例に過ぎず、血液凝固時間測定装置の特性や異常判定の要求精度により、クリニックスタディなどの実測データに基づいて最適に設定する必要がある。
【0085】
次に、ステップS34で求めたT1、T2、T3が、ステップS35で決定した正常範囲内から外れていないかどうかを判定する。すなわち〔式13〕〜〔式15〕で示した不等式を満足するかどうか判断する。全ての不等式が成立すれば、異常なしと判断し、いずれか一つでも成立しない場合、測定データのプロファイルに異常があると判断する(ステップS36)。
【0086】
〔式13〕 T1min<T1<T1max
【0087】
〔式14〕 T2min<T2<T2max
【0088】
〔式15〕 T3min<T3<T3max
【0089】
最後に、異常判定結果に応じた処理を行う。異常が検知されなかった場合は、血液凝固時間演算部で求めた血液凝固時間PTおよびINR値をLCD表示器40に表示する(図7のステップS12)。
【0090】
一方、異常検知した場合は、LCD表示器40にエラー表示を行いユーザーに認知させる(図7のステップS13)。ここで、出力ポート41にプリンタを接続していれば、必要に応じて測定結果を印刷することができる。また、出力ポート41にPCを接続していれば、PCにデータ送信することができる。さらに、測定結果を血液凝固時間測定装置内にある外部メモリ42に保存して、後で測定結果を読み出すことも可能である。
【0091】
このように本実施の形態1の血液凝固時間測定装置によれば、測定した受光データの、血液凝固時間演算部34により求められた血液凝固時間PTにおける値F(PT)に基づいて、判定基準値F1,F2,F3を設定し、かつ、血液凝固時間演算部34により求められた血液凝固時間PTに基づいて、測定された受光データの値が前記判定基準値F1,F2,F3と等しくなる時刻T1,T2,T3の正常上限時刻T1max,T2max,T3maxおよび正常下限時刻T1min,T2min,T3minを設定し、測定された受光データの値が判定基準値F1,F2,F3と等しくなる時刻T1,T2,T3を求め、該求めた時刻が前記正常上限時刻および前記正常下限時刻で設定される正常時刻範囲内にあるかを判定することにより異常判定を行なうようにしたので、判定基準値、および測定データの値が判定基準値に等しくなる時刻の正常範囲を、検体の血液凝固時間および該血液凝固時間における受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、本実施の形態1では、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことができる。
【0092】
(実施の形態2)
以下に本発明の実施の形態2における血液凝固時間測定装置について説明する。
【0093】
本実施の形態2による血液凝固時間測定装置は、図1〜3に示す実施の形態1による血液凝固時間測定装置100と同様の構成を有し、異常判定部35による異常判定の動作のみにおいて異なるものである。
【0094】
以下、本実施の形態2による血液凝固時間測定装置における異常判定の動作について説明する。
【0095】
図6(a)は、実際に行ったクリニックスタディのデータを分析して得られたグラフであり、実施の形態1の算出方法で測定された血液凝固時間PTの時刻における受光データを横軸とし、血液凝固時間PTの1.1倍となる時刻における受光データを縦軸とし、160個のデータをプロットして、これらの相関を示したものである。同様に、図6(b)は、血液凝固時間PTの時刻における受光データを横軸とし、血液凝固時間PTの1.2倍となる時刻における受光データを縦軸とし、160個のデータをプロットして、これらの相関を示したものである。同様に、図6(c)は、血液凝固時間PTの時刻における受光データを横軸とし、血液凝固時間PTの1.3倍となる時刻における受光データを縦軸とし、160個のデータをプロットして、これらの相関を示したものである。
【0096】
ここで、それぞれのグラフにおいて、160個の測定データを対象に最小二乗法により近似二次曲線を引いてみる。図6(a)の近似二次曲線の二次係数j1は−0.0009、一次係数k1は1.6135、定数項l1は−0.9942である。また、図6(b)の近似二次曲線の二次係数j2は−0.0024、一次係数k2は2.3638、定数項はl2は−1.9774である。また、図6(c)の近似二次曲線の二次係数j3は−0.0039、一次係数k3は3.1594、定数項l3は−2.1428である。
【0097】
図6(a)〜図6(c)に示すグラフより、ほとんどの測定データが近似二次曲線近傍に集中していることがわかる。さらに、前記近似二次曲線から比較的大きく離れたデータ、すなわち丸印で囲んだ測定データを個々に分析してみると、受光データ23のプロファイルが歪んでおり、測定される血液凝固時間PT値およびINR値の測定誤差が非常に大きいことが分かった。また、近似二次曲線近傍にあるデータの受光データ23は、プロファイルの歪が非常に少なく、測定される血液凝固時間PT値およびINR値の測定誤差も少ないことが分かった。
【0098】
以上の分析により、血液凝固時間PT値およびINR値と近似二次曲線からの乖離との関係があり、乖離が大きいものほどプロファイル歪が大きく、血液凝固時間PT値およびNR値の測定誤差が大きくなる確率が高くなるといえる。従って、近似二次曲線を基準として、基準からの乖離が所定の誤差率、例えば、±15%以内を正常範囲として上限閾値、下限閾値を設定し、上限閾値から下限閾値の間の範囲内にあるかどうかを判断する事により、測定誤差が大きい可能性があるデータを除外する事が可能となる。
【0099】
そこで、近似二次曲線が標準値であると仮定し、標準値からの誤差が所定の誤差率となる上限閾値直線および下限閾値直線を設定する。例えば、誤差率を±15%に設定すると図6(a)、(b)、(c)のグラフ中の点線のようになる。丸印で囲まれたデータは、上限閾値直線および下限閾値値直線の間の正常範囲から外れており、異常データと判定することが可能となる。
【0100】
我々が開発した血液凝固時間測定装置で得られたデータでは、血液凝固時間における受光データと血液凝固時間の1.1倍、1.2倍、1.3倍の時刻における受光データに注目して異常判定を行ったが、他の装置に適用した場合、最適な時刻の条件は異なるので、クリニックスタディを実施して最適値を求めて、設定する必要がある。
【0101】
また、CPUの性能やメモリ領域の制約があるため、本実施の形態2では、チェック領域を3点に設定している。チェック領域は、1点でも異常判定を行うことは可能であるが、多ければ多いほどより厳しい異常判定が可能となり、複数設定することが望ましい。
【0102】
図10は、本発明の実施の形態2における異常判定のフローチャートを示している。
まず、血液凝固時間演算部34で算出された血液凝固時間PTを受取る(ステップS41)。
【0103】
次に、データ保持部37に保持されている受光データの時系列データから血液凝固時間PTにおける受光データF(PT)を算出する。実施の形態1と同様に、離散的なデータ間を直線補間または多項式補間を用いてデータ補間することが望ましい(ステップS42)。
【0104】
次に、異常判定するチェック領域を決定するために、判定基準時刻t1、t2、t3を〔式16〕〜〔式18〕で示される式を用いて決定する。本実施の形態2では、判定基準時刻として血液凝固時間PTの1.1倍、1.2倍、1.3倍となる3つの点を選択した。この倍率は、一例であり、これに限るものではない(ステップS43)。
【0105】
〔式16〕 t1=d1×PT (但しd1=1.1)
【0106】
〔式17〕 t2=d2×PT (但しd2=1.2)
【0107】
〔式18〕 t3=d3×PT (但しd3=1.3)
【0108】
次に、データ保持部37に保持されている受光データの時系列データから判定基準時刻t1、t2、t3における受光データf1(=F(t1))、f2(=F(t2))、f3(=F(t3))を〔式19〕〜〔式21〕に基づいて算出する。受光データの時系列データは、所定の時間間隔で測定された離散的な値なので、時間間隔を非常に短い時間にしない限り、判定基準時刻t1、t2、t3に丁度一致した測定データは存在しない確率が非常に高い。したがって、離散的なデータ間を直線補間または多項式補間を用いてデータ補間することが望ましい(ステップS44)。
【0109】
〔式19〕 f1=F(t1)=F(d1×PT) (但しd1=1.1)
【0110】
〔式20〕 f2=F(t2)=F(d2×PT) (但しd2=1.2)
【0111】
〔式21〕 f3=F(t3)=F(d3×PT) (但しd3=1.3)
【0112】
次に、時刻t1、t2、t3における受光データf1、f2、f3の正常範囲の上限閾値および下限閾値を決定する。例えば、正常範囲を±15%とした場合、算出式は〔式22〕〜〔式27〕のようになる。ここで、f1maxは時刻t1における受光データf1の正常上限値、f2maxは時刻t2における受光データf2の正常上限値、f3maxは時刻t3における受光データf3の正常上限値、f1minは時刻t1における受光データf1の正常下限値、f2minは時刻t2における受光データf2の正常下限値、f3minは時刻t3における受光データf3の正常下限値である。
【0113】
j1、k1、およびl1は、図6(a)に示される近似二次曲線の二次係数、一次係数、および定数項であり、j2、k2、およびl3は、図6(b)に示される近似二次曲線の二次係数、一次係数、および定数項であり、j3、k3、およびl3は、図6(c)に示される近似二次曲線の二次係数、一次係数、および定数項である(ステップS45)。
【0114】
〔式22〕 f1max=1.15×(j1×F(PT)×F(PT)+k1×F(PT)+l1)
【0115】
〔式23〕 f2max=1.15×(j2×F(PT)×F(PT)+k2×F(PT)+l2)
【0116】
〔式24〕 f3max=1.15×(j3×F(PT)×F(PT)+k3×F(PT)+l3)
【0117】
〔式25〕 f1min=0.85×(j1×F(PT)×F(PT)+k1×F(PT)+l1)
【0118】
〔式26〕 f2min=0.85×(j2×F(PT)×F(PT)+k2×F(PT)+l2)
【0119】
〔式27〕 f3min=0.85×(j3×F(PT)×F(PT)+k3×F(PT)+l3)
【0120】
ただし、
【0121】
j1=-0.0009、k1=1.6135、l1=-0.9942
【0122】
j2=-0.0024、k2=2.3638、l2=-1.9774
【0123】
j3=-0.0039、k3=3.1594、l3=-2.1428である。
【0124】
なお、規格値を±15%という値は、あくまで一例に過ぎず、血液凝固時間測定装置の特性や異常判定の要求精度によってクリニックスタディなどの実測データに基づいて最適に設定する必要がある。
【0125】
次に、ステップS44で求めたf1、f2、f3が、ステップS45で決定した正常範囲内から外れていないかどうかを判定する。すなわち〔式28〕〜〔式30〕で示した不等式を満足するかどうか判断する。全ての不等式が成立すれば、異常なしと判断し、いずれか一つでも成立しない場合、測定データのプロファイルに異常があると判断する(ステップS46)。
【0126】
〔式28〕 f1min<f1<f1max
【0127】
〔式29〕 f2min<f2<f2max
【0128】
〔式30〕 f3min<f3<f3max
【0129】
最後に、異常判定結果に応じた処理を行う。すなわち、上記実施の形態1と同様、異常が検知されなかった場合は、血液凝固時間演算部で求めた血液凝固時間PTおよびINR値をLCD表示器40に表示し、異常検知した場合は、LCD表示器40にエラー表示を行いユーザーに認知させる。ここで、出力ポート41にプリンタを接続していれば、必要に応じて測定結果を印刷することができる。また、出力ポート41にPCを接続していれば、PCにデータ送信することができる。さらに、測定結果を血液凝固時間測定器内にある外部メモリ42に保存して、後で測定結果を読み出すことも可能である。
【0130】
このように本実施の形態2の血液凝固時間測定装置によれば、前記血液凝固時間演算部により求められた血液凝固時間PTに基づいて、判定基準時刻t1,t2,t3を設定し、かつ、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間PTにおける値F(PT)に基づいて、測定した受光データの判定基準時刻t1,t2,t3における値f1,f2,f3の正常上限値f1max,f2max,f3maxおよび正常下限値f1min,f2min,f3minを設定し、測定した受光データの判定基準時刻t1,t2,t3における値f1,f2,f3を求め、該求めた値が前記正常上限値および前記正常下限値で設定される正常値範囲内にあるかを判定することにより異常判定を行なうようにしたので、判定基準時刻、および該判定基準時刻における受光データの正常範囲を、検体の血液凝固時間および該血液凝固時間における受光データの値に応じて設定でき、検体の血液凝固時間に影響されることなく、測定データの高精度な異常判定を行うことができる。また、本実施の形態2においても上記実施の形態1と同様、チェック領域を設定するために受光光量の飽和値を知る必要がないため、受光データの微分値の最大時刻を検知した時点で測定を完了する高速測定方法においても良好な異常判定を行なうことができる。
【産業上の利用可能性】
【0131】
本発明にかかる血液凝固時間測定装置は、検体の受光光量差や反応開始時刻の影響を排除することができ、光量検体の血液凝固能や固体差に依存することなく良好な異常検知が可能となる。また、血液凝固反応が飽和するまで測定する必要が無く短時間で測定するような高速演算方法においても良好な効果を得ることが可能となる。
【図面の簡単な説明】
【0132】
【図1】本発明の実施の形態1による血液凝固時間測定装置の斜視図
【図2】本発明の実施の形態1による血液凝固時間測定装置の光学台の断面図
【図3】本発明の実施の形態1による血液凝固時間測定装置のブロック図
【図4】本発明の実施の形態1による血液凝固時間測定装置における血液凝固時間の測定フローを示す図
【図5】本発明の実施の形態1において用いるクリニックスタディの測定データを示す図
【図6】本発明の実施の形態2において用いるクリニックスタディの測定データを示す図
【図7】本発明の実施の形態1による血液凝固時間測定装置における測定動作のフローチャート図
【図8】本発明の実施の形態1による血液凝固時間測定装置における血液凝固時間の演算のフローチャート図
【図9】本発明の実施の形態1による血液凝固時間測定装置における血液凝固時間の異常判定動作のフローチャート図
【図10】本発明の実施の形態2による血液凝固時間測定装置における血液凝固時間の異常判定動作のフローチャート図
【図11】従来の光学的方法を用いた血液凝固時間装置の構成図
【図12】従来の光学的方法を用いた血液凝固時間の測定方法を説明するための図
【図13】従来の問題点を説明するための図
【符号の説明】
【0133】
1 血液凝固時間測定装置
3 試験片
4 反応部
5 試料
6 光学台
7 窓部
8 蓋
9 光源
10 レンズ
11 受光手段
12 光源フィルタ
13 受光フィルタ
20 ホルダー
21 温度制御手段
22 電極
23 受光データ
24 一次微分
25 近似直線
30 LEDドライバ
31 操作スイッチ
32 CPU
33 制御部
34 血液凝固時間演算部
35 異常判定部
36 データ測定部
37 データ保持部
38 電流電圧変換回路
39 アナログ−デジタル変換回路
40 LCD表示器
41 出力ポート
42 外部メモリ
43 タイマー
51 試験管
52 試薬供給装置
53 ピペット
54 LED
55 フォトダイオード
56 計測部
57 CRT
【特許請求の範囲】
【請求項1】
血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、
前記光学的信号を電気的な受光信号に変換する受光器と、
前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、
前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、
前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、
前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、
前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、
前記異常判定部は、前記血液凝固時間演算部により求められた血液凝固時間および該血液凝固時間における前記測定した受光データの値に基づいて、異常判定を行うチェック領域および該チェック領域における正常範囲を設定し、前記測定した受光データが前記正常範囲内にあるか否かを判定する、
ことを特徴とする血液凝固時間測定装置。
【請求項2】
血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、
前記光学的信号を電気的な受光信号に変換する受光器と、
前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、
前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、
前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、
前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、
前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、
前記異常判定部は、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間における値に基づいて、少なくとも1つの判定基準値を設定し、かつ、前記血液凝固時間演算部により求められた血液凝固時間に基づいて、前記測定された受光データの値が前記判定基準値と等しくなる時刻の正常上限時刻および正常下限時刻を設定し、前記測定された受光データの値が前記判定基準値と等しくなる時刻を求め、該求めた時刻が前記正常上限時刻および前記正常下限時刻で設定される正常時刻範囲内にあるか否かを判定する、
ことを特徴とする血液凝固時間測定装置。
【請求項3】
血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、
前記光学的信号を電気的な受光信号に変換する受光器と、
前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、
前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、
前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、
前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、
前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、
前記異常判定部は、前記血液凝固時間演算部により求められた血液凝固時間に基づいて、少なくとも1つの判定基準時刻を設定し、かつ、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間における値に基づいて、前記測定した受光データの前記判定基準時刻における値の正常上限値および正常下限値を設定し、前記測定した受光データの前記判定基準時刻における値を求め、前記求めた値が前記正常上限値および前記正常下限値で設定される正常値範囲内にあるか否かを判定する、
ことを特徴とする血液凝固時間測定装置。
【請求項1】
血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、
前記光学的信号を電気的な受光信号に変換する受光器と、
前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、
前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、
前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、
前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、
前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、
前記異常判定部は、前記血液凝固時間演算部により求められた血液凝固時間および該血液凝固時間における前記測定した受光データの値に基づいて、異常判定を行うチェック領域および該チェック領域における正常範囲を設定し、前記測定した受光データが前記正常範囲内にあるか否かを判定する、
ことを特徴とする血液凝固時間測定装置。
【請求項2】
血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、
前記光学的信号を電気的な受光信号に変換する受光器と、
前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、
前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、
前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、
前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、
前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、
前記異常判定部は、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間における値に基づいて、少なくとも1つの判定基準値を設定し、かつ、前記血液凝固時間演算部により求められた血液凝固時間に基づいて、前記測定された受光データの値が前記判定基準値と等しくなる時刻の正常上限時刻および正常下限時刻を設定し、前記測定された受光データの値が前記判定基準値と等しくなる時刻を求め、該求めた時刻が前記正常上限時刻および前記正常下限時刻で設定される正常時刻範囲内にあるか否かを判定する、
ことを特徴とする血液凝固時間測定装置。
【請求項3】
血液に含まれる凝固作用に関与する成分と反応して観測可能な光学的変化を示す反応試薬を使い、光学的信号変化を分析することにより血液凝固時間を測定する血液凝固時間測定装置であって、
前記光学的信号を電気的な受光信号に変換する受光器と、
前記受光器からの受光信号をデジタルの受光データに変換するA/D変換器と、
前記A/D変換器から得られる受光データを予め設定された時間間隔毎に測定するデータ測定部と、
前記データ測定部で測定された各受光データを一時的に保持するデータ保持部と、
前記データ保持部に保持された複数の受光データに基づいて血液凝固時間を求める血液凝固時間演算部と、
前記測定した受光データに異常があるか否かを判定する異常判定部とを備え、
前記異常判定部は、前記血液凝固時間演算部により求められた血液凝固時間に基づいて、少なくとも1つの判定基準時刻を設定し、かつ、前記測定した受光データの、前記血液凝固時間演算部により求められた血液凝固時間における値に基づいて、前記測定した受光データの前記判定基準時刻における値の正常上限値および正常下限値を設定し、前記測定した受光データの前記判定基準時刻における値を求め、前記求めた値が前記正常上限値および前記正常下限値で設定される正常値範囲内にあるか否かを判定する、
ことを特徴とする血液凝固時間測定装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【公開番号】特開2008−209350(P2008−209350A)
【公開日】平成20年9月11日(2008.9.11)
【国際特許分類】
【出願番号】特願2007−48554(P2007−48554)
【出願日】平成19年2月28日(2007.2.28)
【出願人】(000005821)松下電器産業株式会社 (73,050)
【Fターム(参考)】
【公開日】平成20年9月11日(2008.9.11)
【国際特許分類】
【出願日】平成19年2月28日(2007.2.28)
【出願人】(000005821)松下電器産業株式会社 (73,050)
【Fターム(参考)】
[ Back to top ]

