血管内皮細胞を用いた血栓観測方法および血栓観測装置
【課題】 血流と同等環境下における血液凝固および血栓形成を総合的に評価する装置および方法を提供する。
【解決手段】 その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室に抗凝固処理された血液を、抗凝固処理を解除しつつ流して前記細胞培養室における血栓の生成を観測することを特徴とする血栓形成観測方法、および、血管を模した流路に抗凝固処理された血液を、抗凝固処理を解除しつつ流して血栓の生成を観測する血栓観測装置であって、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室と、該細胞培養室に接続されて前記細胞培養室に血液を流入させる流入管と、該流入管に接続されて前記流入管に抗凝固処理を解除する薬剤を投入する薬剤管と、を有することを特徴とする血栓観測装置。
【解決手段】 その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室に抗凝固処理された血液を、抗凝固処理を解除しつつ流して前記細胞培養室における血栓の生成を観測することを特徴とする血栓形成観測方法、および、血管を模した流路に抗凝固処理された血液を、抗凝固処理を解除しつつ流して血栓の生成を観測する血栓観測装置であって、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室と、該細胞培養室に接続されて前記細胞培養室に血液を流入させる流入管と、該流入管に接続されて前記流入管に抗凝固処理を解除する薬剤を投入する薬剤管と、を有することを特徴とする血栓観測装置。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、患者等に投与した抗血栓薬の効能評価などに使用できる、血栓観測方法および血栓観測装置に関し、具体的には、生体外で、血流と同等環境下における血液凝固および血栓形成を総合的に評価する方法および装置に関する。
【背景技術】
【0002】
心筋梗塞、脳梗塞、エコノミークラス症候群等、多種多様な血栓性疾患が存在する。心筋梗塞に代表されるアテローム血栓症は動脈硬化領域でのアテロームプラークが壊れることで露出した組織因子やコラーゲンによって引き起こされる。
一方、エコノミークラス症候群や深部静脈血栓症等の静脈血栓症は、血管内皮細胞に覆われた血管内において、主に静脈内血の鬱滞によって発症する。血流の鬱滞に加え、凝固制御系や線溶系因子の先天異常や糖尿病、外傷、癌等の基礎疾患等、種々の凝固亢進要因が複合し静脈血栓症の発症リスクを高める。
このようにアテローム血栓症は明らかに血管病変に起因して血栓形成が起きるのに対して、静脈血栓症は血管内皮細胞に覆われた血管内において起こる血栓症で有り、鬱血に加え、凝固系活性化、血小板及び白血球の活性化、及び血管内皮細胞の活性化等が総合的に関与する。白血球の活性化は内皮細胞との接着能を高め、その結果、内皮細胞を活性化する。活性化した白血球や内皮細胞は表面に組織因子を発現し、凝固系を活性化し、活性化した凝固系はさらに血小板、白血球、内皮細胞を活性化する。
このような静脈血栓症におけるリスクの評価、抗血栓療法における抗血栓効果のモニタリングには試験管内における静的な試験では不十分であり、血流の存在下、凝固、血小板、白血球、内皮細胞の総合的な評価が重要である。
【0003】
従来、血液凝固能の評価は、血漿を用いた部分活性化トロンボプラスチン時間(APTT)、トロンボプラスチン時間(PT)、によって検査されている。APTTは主に内因系凝固、PTは外因系凝固を反映する。血小板の検査としては多血小板血漿を用い、ADP、コラーゲン等の血小板活性化物質を加え透過度の変化等によって血小板の凝集能を評価する事もできる。また、全血凝固時間、カルシウム再添加全血凝固時間等によって全血の凝固時間の測定もなされる。さらに、全血を用いた検査系としてはトロンボエラストグラムが用いられ、血液凝固、血小板活性化に伴う血液成分の粘度変化がモニタリングされる。
しかしながら、生体内では血流下で血栓が成長するのに対し、上記の検査方法等は閉鎖された試験管内での測定であるため、血栓が生体内で成長する状態を反映することはできない。
【0004】
この問題点を解決する提案として、特許文献1には、評価すべき抗血栓薬が投入された血液をコラーゲンセル上を通過させ、血小板を蛍光標識する事で血小板の粘着、凝集を共焦点顕微鏡装置によりモニタリングする方法が開示されている。
しかし、この文献に記載の発明は、抗凝固薬の存在下で観測を行うために、凝固系によって起こる血小板の粘着、凝集による血栓が形成されず、また、血栓の生成能の低下を、血小板の形態変化を観測することで評価するものであり、凝固系と連動した血小板活性化が反映されない。したがって、抗血小板薬の薬効を評価するには使用できるが、血栓そのものや血栓形成過程全体をモニターする事はできない。血小板は凝固系によって活性化され、凝固系は活性化血小板によって促進される。すなわち抗凝固処理された血液は、血小板の活性化も抑制されてしまい抗血栓薬の効能を観測することはできない。さりとて、抗凝固処理を行わなければ血液は直ちに凝固してしまうので、試験に供することはできない。
また、特許文献2には、血管内皮細胞が培養されたチャンバ内に白血球を含む溶液を流し込んで、白血球と血管内皮細胞とのインタラクションを発生させて、白血球接着現象を画像解析する方法が開示されている。
しかしながら、この方法でも凝固系の活性化等は反映されず、観察できる血栓形成は生体内で生じる血栓形成を十分反映しているとはいえないものであった。
【特許文献1】特開2004−251630号公報
【特許文献2】特開2001−264318号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
本発明は、上記事情に鑑み、生体外で、血管内皮細胞と血液成分との接触環境下における凝固系、血小板、白血球を総合的に評価する方法および装置を提供することを課題とする。
【課題を解決するための手段】
【0006】
前記課題を解決するため、本発明は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室に、抗凝固処理された血液を、抗凝固処理を解除しつつ流して前記細胞培養室における血栓の形成を観測することを特徴とする、血栓観測方法を提供する。
本発明の血栓観測方法においては、白血球および/または血小板の血管内皮細胞への接着を指標にして血栓形成を観測することが好ましい。
また、白血球および/または血小板を標識物質で標識し、該標識を検出することにより白血球および/または血小板の血管内皮細胞への接着を観測することが好ましい。
また、抗凝固処理はトロンビン阻害効果を有する1本鎖DNA又はRNAによる処理が好ましく、抗凝固処理を解除するためには、前記トロンビン阻害効果を有する1本鎖DNA又はRNAに対するアンチセンスDNA又はアンチセンスRNAを用いることが好ましい。
【0007】
また、本発明は、血管を模した流路に抗凝固処理された血液を、抗凝固処理を解除しつつ流して血栓の生成を観測する血栓観測装置であって、
該血栓観測装置は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室と、該細胞培養室に接続されて前記細胞培養室に血液を流入させる流入管と、該流入管に接続されて前記流入管に抗凝固処理を解除する薬剤を投入する薬剤管と、を有することを特徴とする血栓観測装置を提供する。
【発明の効果】
【0008】
本発明の血栓観測方法および血栓観測装置によれば、抗凝固処理された血液を、抗凝固処理を解除しつつ流して血管内皮細胞上での血栓の形成を観測することができるので、抗血栓薬の効能を人体内に近い環境で観測することができる。また、採血時に抗凝固剤を用いることができるため、採血後の検体を一定期間保存することができ、検査時期を任意に選択できる利点を有する。
【0009】
本発明の血栓観測装置をマイクロチップ上に形成すると、少量の血液でも観測が可能となる。また、流入管および/または薬剤管を加圧するポンプを有することで、所定圧力で、所定時間、血液や抗凝固処理を解除する薬剤を安定して流すことができる。
また、細胞培養室における血液の流入時および/または流出時の圧力を測定することで、極めて簡易な装置で容易に、血栓形成の有無を確認することができる。
【発明を実施するための最良の形態】
【0010】
本発明の血栓形成観測方法において使用する血液は、白血球および/または血小板を含
むものであればよいが、例えば、全血や多血小板血漿などを用いることができる。
血液は、抗凝固処理をしたものを使用する。抗凝固処理に使用できる抗凝固剤としては、クエン酸ナトリウム、クエン酸カリウム、シュウ酸ナトリウム、シュウ酸カリウム、ACD(Acid Citrate Dextrose)、エチレンジアミンテトラ酢酸(EDTA)塩などを挙げることができる。このような抗凝固剤は、粉末、凍結乾燥品、水溶液などの溶液として使用することができるが、既存の3.2%クエン酸ナトリウムを用いるのが容易に入手できることから好ましい。この場合、血液9容に対してこの抗凝固剤1容とするのが好ましい。
【0011】
その他の抗凝固剤として、トロンビン阻害効果を有する1本鎖DNA又はRNAが使用できる。トロンビン阻害効果を有する1本鎖DNA又はRNAとしては、1本鎖オリゴDNAであるトロンビンアプタマー(Blood. 1993 Jun 15;81(12):3271−6.)などが挙げられる。トロンビン阻害効果を有する1本鎖DNA又はRNAの長さはトロンビン阻害効果を有する限り特に制限されないが、3〜30塩基が好ましい。
なお、抗凝固剤は2種類以上用いてもよい。
【0012】
次に、抗凝固処理をした血液を、抗凝固処理を解除しつつ、血管内皮細胞が付着した細胞培養室へ流入させる。抗凝固処理をした血液を、抗凝固処理を解除しつつ細胞培養室に流入させるには、例えば、血液注入口と、細胞培養室と、これらをつなぐ流路を用意し、抗凝固処理をした血液を血液注入口に注入し、該血液注入口と細胞培養室との間に設けられた抗凝固解除剤注入口から抗凝固解除剤含有液を注入して、抗凝固処理された血液と抗凝固解除剤を流路内で混合させ、このようにして抗凝固処理が解除された血液が細胞培養室へ流入するようにすればよい。血液の流速や、流路の長さなどは、血液が、抗凝固解除剤と十分に混合されたのちに、細胞培養室に流入して血栓を形成できるように適宜調整すればよい。また、流速は細胞培養室に付着した血管内皮細胞がはがれにくいような流速にすることが好ましい。
【0013】
抗凝固処理を解除する薬剤(抗凝固解除剤ともよぶ)としては、塩化カルシウム、臭化カルシウム、ヨウ化カルシウム等のハロゲン化カルシウム、リン酸カルシウム、硫酸カルシウム、硝酸カルシウム、重炭酸カルシウム等の無機酸カルシウム塩、蟻酸、酢酸、プロピオン酸、酪酸、アルギン酸、乳酸、グルコン酸、グリセリン酸、グリセロリン酸等の有機酸のカルシウム塩、などの遊離カルシウム供与体であるカルシウム化合物を挙げることができる。これらは、クエン酸やEDTA等のキレート作用に基づいた抗凝固処理剤に作用して処理効果を無効化して血液凝固を促進するものである。
【0014】
また、1本鎖オリゴDNAであるトロンビンアプタマー(Blood. 1993 Jun 15;81(12):3271−6.)を抗凝固剤として用いた場合には、トロンビンアプタマーに対するアンチセンスDNAまたはアンチセンスRNA等のトロンビンアプタマーの機能を阻害する物質が抗凝固解除剤として使用可能である。この際用いられるアンチセンスDNAは実質的にトロンビンアプタマーの抗トロンビン作用を無効化するものであれば、トロンビンアプタマーの一部に対するものであってもよい。
なお、抗凝固剤としてトロンビンアプタマーを用いた場合には、患者の血液中のカルシウム、マグネシウム、亜鉛等の種々の2価金属イオン濃度を的確に反映した試験が可能で有り、キレート剤添加による細胞のダメージも起こらない。
例えば、終濃度5μMのトロンビンアプタマーを用いて抗凝固処理を行い、15μMのトロンビンアプタマーアンチセンスDNAを用いて可逆的に抗凝固処理を解除することができる。より血液サンプル保存が長時間に及ぶ場合には、30μg/mlのコーン由来トリプシンインヒビター等で接触因子の活性化を阻害してもよい。
なお、観測する血液試料が希釈されない為に、抗凝固解除試薬の容量は抗凝固処理血液
に対し10分の1もしくはそれ以下であることが望ましい。
【0015】
抗凝固解除剤と混合された血液は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室に到達し、血液中の白血球および/または血小板が血管内皮細胞と作用することにより、血管内皮細胞上での相互作用や血栓形成が観測される。
ここで、細胞培養室に付着させる血管内皮細胞としては、株化細胞でも初代培養細胞でもよい。血管内皮細胞の由来は特に制限されないが、ヒトにおける血栓形成を評価するためにはヒト由来の血管内皮細胞を使用することが好ましい。血管内皮細胞としては、臍帯静脈内皮細胞、臍帯動脈内皮細胞、大動脈内皮細胞、冠状動脈内皮細胞、皮膚微小血管内皮細胞などが例示できる。
血管内皮細胞は、シートやプレート上であらかじめ培養したものを細胞培養室に設置するか、あるいは、細胞培養室内であらかじめ培養したものを使用することが可能である。血管内皮細胞を培養する場合、細胞の接着をよくするため、細胞培養室内の血管内皮細胞接着面をあらかじめコラーゲンコートしておき、その上に血管内皮細胞を培養することが好ましい。
取り扱いを考慮して、図1に示されるような、スライドグラス(またはプラスチック製プレート)と流路部材を接着させてなるマイクロチップ内に血管内皮細胞を培養して細胞培養室とすることが望ましい。また、血管内皮細胞は、血栓観測時にコンフルエントの状態になっているものを使用することが好ましい。
【0016】
血栓形成は、一定時間血液を通過させた後、生理食塩水等で細胞培養室を洗浄し、細胞培養室内から血液を除去する事によって目視によって評価する事が出来る。特に多血小板血漿を用いた血栓形成の観察においては透過度が高くなり観察が容易であり肉眼による血栓形成の観察も可能である。
【0017】
本発明の血栓形成観測方法においては、白血球および/または血小板の血管内皮細胞への接着を指標にして血栓形成を観測することもできる。この場合、白血球および/または血小板を標識物質で標識し、該標識を検出することにより白血球および/または血小板の血管内皮細胞への接着を観測することがより好ましい。
白血球および/または血小板を標識するための標識物質としては、蛍光物質、放射性物質などが挙げられる。
白血球および/または血小板を標識するための蛍光物質としては、メパクリンなどが挙げられ、蛍光光学顕微鏡や蛍光実態顕微鏡を用いて血栓形成を観察することができる。
例えば、10μM程度のメパクリンを血液に加えることにより、簡便に白血球、血小板を緑色に染色することが可能である。
白血球および/または血小板を蛍光標識して蛍光顕微鏡でモニターする方法としては、特許文献1に開示されている方法が例示される。本発明の方法によれば、共焦点レーザー顕微鏡を用いずとも、安価な蛍光実体顕微鏡を用いることでリアルタイムに血栓形成が観測でき、より簡便な観測が可能である。
なお、蛍光を利用して血栓形成を観察する際には、細胞培養室を透明な素材とし、細胞培養室の細胞が付着している側、すなわち、血液が流れる側とは反対側から観察することが好ましい。
なお、標識物質はそれ自体が白血球および/または血小板と結合しうるものであってもよいし、白血球および/または血小板を認識しうる物質が標識されていてもよい。例えば、白血球および/または血小板に特異的な抗体を標識物質で標識して検出に使用してもよい。このような抗体としては、抗GPIIbIIIa抗体などが挙げられる。
【0018】
本発明の血栓観測装置は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室と、該細胞培養室に接続されて前記細胞培養室に血液を流入させる流入管と、該流入管に接続されて前記流入管に抗凝固処理を解除する薬剤を投入する薬剤管と、を有するこ
とを特徴とする血栓観測装置である。
本発明の血栓観測装置は、さらに、細胞培養室に接続された、細胞培養室を通過した血液を排出するための排出管を備えるものであることが好ましい。
本発明の血栓観測装置は、さらに、流入管および/または薬剤管を加圧するポンプを備えるものであることが好ましい。
本発明の血栓観測装置は、さらに、圧力測定装置を備えるものであることが好ましい。
【0019】
細胞培養室は、血管内皮細胞付着部と、該血管内皮細胞付着部上に血液が通過する流路を有する形状が好ましい。血栓形成室は、透明な、ガラスや熱可塑性樹脂などで製造することができる。細胞培養室の血管内皮細胞付着部以外の面は、血液が付着しないように、シリコン樹脂などで形成されるか、または、ヘパリン、シリコン、もしくはPVLAなどで表面処理されていることが好ましい。
流入管、薬剤管及び排出管も、透明な、ガラスや熱可塑性樹脂などで製造することができ、管内部がヘパリン、シリコン、もしくはPVLAなどで表面処理されていることが好ましい。
【実施例】
【0020】
以下、本発明の血栓観測装置の好ましい態様を、図1及び図2を参照して説明する。
図1に示すように、本形態例に係る血栓観測装置1は、細胞培養室10と、該細胞培養室10に接続されて前記細胞培養室に血液を流入させる流入管11と、該流入管11に接続されて前記流入管11に抗凝固処理を解除する薬剤を投入する薬剤管12と、該細胞培養室10に接続されて前記細胞培養室から血液を排出させる排出管13を備える。
【0021】
まず、流路部材A、スライドガラス(底面)Bおよび蓋Cを組み合わせて内部に細胞培養室を有するマイクロチップを作製する。
PDMS(ポリジメチルシロキサン)製の流路部材Aは、血液の流路となりうる、上面から下面に貫通した溝を有する構造を持つ。流路部材Aの長さは1mm〜10cmとすることが好ましく、溝を、流路幅20μm〜1cm、深さ20μm〜1cmとすることが好ましい。
スライドガラスBは流路部材Aとの接着面がコラーゲンコートされており、このスライドガラスBを流路部材Aと可逆または不可逆的に接着させることにより、流路部材Aの溝とスライドガラスBに囲まれた空間が生じる。なお、流路部材Aの素材をPDMSとすることで接着剤等を用いずとも、自己接着性によってスライドガラスBを圧着させることが可能である。
次に、別途、細胞培養ディッシュ内で培養された血管内皮細胞をトリプシン処理等によってディッシュから剥離させ、血管内皮細胞を回収した後、培地に懸濁する。該血管内皮細胞懸濁液を流路部材AとスライドガラスBの接着によって出来る空間に添加し、1時間程度インキュベートしてスライドガラスBへ血管内皮細胞を接着させる。こうして得られた血管内皮細胞を接着させた流路部材A及びスライドガラスBからなるユニットを新たに用意したディッシュに入れ、培地でディッシュ全体を満たしCO2インキュベーター内で血管内皮細胞を培養する。以上の細胞の取り扱いは無菌条件下で行うことが望ましい。
目的とする細胞密度まで培養を行った後、流路部材AとスライドグラスBからなるユニットに蓋Cを圧着させる。蓋Cは内面(ユニットとの接着面)がへパリンまたはPVLA等で抗血栓処理された透明プラスチックかシリコンコートされている板状のガラス又は透明プラスチックを用いる事が望ましい。流路部材A、スライドガラスB、および蓋Cをクリップ等で固定することにより流路からの液漏れを簡単に防ぐことが可能である。
なお、流路部材A、スライドガラスB、および蓋Cは滅菌して使用される。これらは放射線又は加圧蒸気によって滅菌されることが望ましい。
また、蓋Cには、流路部材Aの溝の両端に相当する箇所に穴が2箇所設けられている。蓋Cの穴に接続された流入管11より抗凝固処理血液を流入させ、該流入管に分岐して接
続された薬剤管12より抗凝固解除液を流入させ、抗凝固処理血液を抗凝固処理を解除しながら細胞培養室に流入させる。また、蓋Cの他方の穴には排出管を接続し、細胞培養室を通過した血液が排出されるようにする。
細胞培養室を顕微鏡観測することで、血液凝固、内皮細胞、血小板、白血球の各因子の相互作用や血栓形成を観測することが可能である。流入する血液を例えばメパクリン処理し、メパクリンの蛍光を観察することで、白血球、血小板の血管内皮細胞との相互作用をリアルタイムに観測することができる。なお、蛍光を観察するときはスライドガラスB側から細胞培養室を観察することが好ましい。
また、一定時間血液を流入させた後、内部を生理食塩水等で洗浄することで、付着する血栓を直接的に目視確認することも可能である。
【0022】
図2は、流路部材Aの溝をY字型にし、流路部材AとスライドガラスBからなるユニット内で抗凝固処理された血液と抗凝固解除剤が混合されるようにした、血栓観測装置の態様を示す。すなわち、流路部材AのY字型の溝は細胞培養室と、流入管の一部および薬剤管の一部を構成する。図1と同様、コラーゲン処理されたスライドガラスBを流路部材Aに接着させ、流路部材Aの溝とスライドガラスBによって生じる空間に血管内皮細胞を加えて細胞を接着させ、このユニットにY字の3箇所の端に相当する箇所に穴の開いた蓋Cを接着させる。なお、図2の態様においては、血管内皮細胞は、Y字の流路内において、細胞培養室だけでなく、流入管の一部および薬剤管の一部に相当する部分にも接着していてもよい。
蓋Cの各穴に流入管、薬剤管および排出管のチューブを図2のように接続することにより血栓観測装置が得られる。流入管11より抗凝固処理血液を、薬剤管12より抗凝固解除液をそれぞれ流入させることにより、Y字の流路内で抗凝固処理血液が抗凝固処理解除剤と混合され、混合された血液が細胞培養室に流入し、血栓が形成される。これを図1と同様にして観測する。
【0023】
以上、本発明を好適な実施の形態に基づいて説明してきたが、本発明は上述の実施例や形態例に限定されるものではなく、本発明の要旨を逸脱しない範囲で種々の改変が可能である。
【図面の簡単な説明】
【0024】
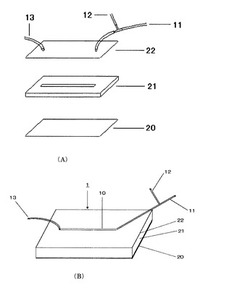
【図1】本発明の第1の形態例に係る血栓観測装置を示す概念図である。(A)は血栓観測装置を構成する流路部材、スライドガラス及び蓋を示す図であり、(B)は血栓観測装置の完成図である。
【図2】本発明の第2の形態例に係る血栓観測装置を示す概念図である。(A)は血栓観測装置を構成する流路部材、スライドガラス及び蓋を示す図であり、(B)は血栓観測装置の完成図である。
【符号の説明】
【0025】
1…血栓観測装置、10…細胞培養室、11…流入管、12…薬剤管、13…排出管。
20…スライドガラスB、21…流路部材A、22…蓋C
【技術分野】
【0001】
本発明は、患者等に投与した抗血栓薬の効能評価などに使用できる、血栓観測方法および血栓観測装置に関し、具体的には、生体外で、血流と同等環境下における血液凝固および血栓形成を総合的に評価する方法および装置に関する。
【背景技術】
【0002】
心筋梗塞、脳梗塞、エコノミークラス症候群等、多種多様な血栓性疾患が存在する。心筋梗塞に代表されるアテローム血栓症は動脈硬化領域でのアテロームプラークが壊れることで露出した組織因子やコラーゲンによって引き起こされる。
一方、エコノミークラス症候群や深部静脈血栓症等の静脈血栓症は、血管内皮細胞に覆われた血管内において、主に静脈内血の鬱滞によって発症する。血流の鬱滞に加え、凝固制御系や線溶系因子の先天異常や糖尿病、外傷、癌等の基礎疾患等、種々の凝固亢進要因が複合し静脈血栓症の発症リスクを高める。
このようにアテローム血栓症は明らかに血管病変に起因して血栓形成が起きるのに対して、静脈血栓症は血管内皮細胞に覆われた血管内において起こる血栓症で有り、鬱血に加え、凝固系活性化、血小板及び白血球の活性化、及び血管内皮細胞の活性化等が総合的に関与する。白血球の活性化は内皮細胞との接着能を高め、その結果、内皮細胞を活性化する。活性化した白血球や内皮細胞は表面に組織因子を発現し、凝固系を活性化し、活性化した凝固系はさらに血小板、白血球、内皮細胞を活性化する。
このような静脈血栓症におけるリスクの評価、抗血栓療法における抗血栓効果のモニタリングには試験管内における静的な試験では不十分であり、血流の存在下、凝固、血小板、白血球、内皮細胞の総合的な評価が重要である。
【0003】
従来、血液凝固能の評価は、血漿を用いた部分活性化トロンボプラスチン時間(APTT)、トロンボプラスチン時間(PT)、によって検査されている。APTTは主に内因系凝固、PTは外因系凝固を反映する。血小板の検査としては多血小板血漿を用い、ADP、コラーゲン等の血小板活性化物質を加え透過度の変化等によって血小板の凝集能を評価する事もできる。また、全血凝固時間、カルシウム再添加全血凝固時間等によって全血の凝固時間の測定もなされる。さらに、全血を用いた検査系としてはトロンボエラストグラムが用いられ、血液凝固、血小板活性化に伴う血液成分の粘度変化がモニタリングされる。
しかしながら、生体内では血流下で血栓が成長するのに対し、上記の検査方法等は閉鎖された試験管内での測定であるため、血栓が生体内で成長する状態を反映することはできない。
【0004】
この問題点を解決する提案として、特許文献1には、評価すべき抗血栓薬が投入された血液をコラーゲンセル上を通過させ、血小板を蛍光標識する事で血小板の粘着、凝集を共焦点顕微鏡装置によりモニタリングする方法が開示されている。
しかし、この文献に記載の発明は、抗凝固薬の存在下で観測を行うために、凝固系によって起こる血小板の粘着、凝集による血栓が形成されず、また、血栓の生成能の低下を、血小板の形態変化を観測することで評価するものであり、凝固系と連動した血小板活性化が反映されない。したがって、抗血小板薬の薬効を評価するには使用できるが、血栓そのものや血栓形成過程全体をモニターする事はできない。血小板は凝固系によって活性化され、凝固系は活性化血小板によって促進される。すなわち抗凝固処理された血液は、血小板の活性化も抑制されてしまい抗血栓薬の効能を観測することはできない。さりとて、抗凝固処理を行わなければ血液は直ちに凝固してしまうので、試験に供することはできない。
また、特許文献2には、血管内皮細胞が培養されたチャンバ内に白血球を含む溶液を流し込んで、白血球と血管内皮細胞とのインタラクションを発生させて、白血球接着現象を画像解析する方法が開示されている。
しかしながら、この方法でも凝固系の活性化等は反映されず、観察できる血栓形成は生体内で生じる血栓形成を十分反映しているとはいえないものであった。
【特許文献1】特開2004−251630号公報
【特許文献2】特開2001−264318号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
本発明は、上記事情に鑑み、生体外で、血管内皮細胞と血液成分との接触環境下における凝固系、血小板、白血球を総合的に評価する方法および装置を提供することを課題とする。
【課題を解決するための手段】
【0006】
前記課題を解決するため、本発明は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室に、抗凝固処理された血液を、抗凝固処理を解除しつつ流して前記細胞培養室における血栓の形成を観測することを特徴とする、血栓観測方法を提供する。
本発明の血栓観測方法においては、白血球および/または血小板の血管内皮細胞への接着を指標にして血栓形成を観測することが好ましい。
また、白血球および/または血小板を標識物質で標識し、該標識を検出することにより白血球および/または血小板の血管内皮細胞への接着を観測することが好ましい。
また、抗凝固処理はトロンビン阻害効果を有する1本鎖DNA又はRNAによる処理が好ましく、抗凝固処理を解除するためには、前記トロンビン阻害効果を有する1本鎖DNA又はRNAに対するアンチセンスDNA又はアンチセンスRNAを用いることが好ましい。
【0007】
また、本発明は、血管を模した流路に抗凝固処理された血液を、抗凝固処理を解除しつつ流して血栓の生成を観測する血栓観測装置であって、
該血栓観測装置は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室と、該細胞培養室に接続されて前記細胞培養室に血液を流入させる流入管と、該流入管に接続されて前記流入管に抗凝固処理を解除する薬剤を投入する薬剤管と、を有することを特徴とする血栓観測装置を提供する。
【発明の効果】
【0008】
本発明の血栓観測方法および血栓観測装置によれば、抗凝固処理された血液を、抗凝固処理を解除しつつ流して血管内皮細胞上での血栓の形成を観測することができるので、抗血栓薬の効能を人体内に近い環境で観測することができる。また、採血時に抗凝固剤を用いることができるため、採血後の検体を一定期間保存することができ、検査時期を任意に選択できる利点を有する。
【0009】
本発明の血栓観測装置をマイクロチップ上に形成すると、少量の血液でも観測が可能となる。また、流入管および/または薬剤管を加圧するポンプを有することで、所定圧力で、所定時間、血液や抗凝固処理を解除する薬剤を安定して流すことができる。
また、細胞培養室における血液の流入時および/または流出時の圧力を測定することで、極めて簡易な装置で容易に、血栓形成の有無を確認することができる。
【発明を実施するための最良の形態】
【0010】
本発明の血栓形成観測方法において使用する血液は、白血球および/または血小板を含
むものであればよいが、例えば、全血や多血小板血漿などを用いることができる。
血液は、抗凝固処理をしたものを使用する。抗凝固処理に使用できる抗凝固剤としては、クエン酸ナトリウム、クエン酸カリウム、シュウ酸ナトリウム、シュウ酸カリウム、ACD(Acid Citrate Dextrose)、エチレンジアミンテトラ酢酸(EDTA)塩などを挙げることができる。このような抗凝固剤は、粉末、凍結乾燥品、水溶液などの溶液として使用することができるが、既存の3.2%クエン酸ナトリウムを用いるのが容易に入手できることから好ましい。この場合、血液9容に対してこの抗凝固剤1容とするのが好ましい。
【0011】
その他の抗凝固剤として、トロンビン阻害効果を有する1本鎖DNA又はRNAが使用できる。トロンビン阻害効果を有する1本鎖DNA又はRNAとしては、1本鎖オリゴDNAであるトロンビンアプタマー(Blood. 1993 Jun 15;81(12):3271−6.)などが挙げられる。トロンビン阻害効果を有する1本鎖DNA又はRNAの長さはトロンビン阻害効果を有する限り特に制限されないが、3〜30塩基が好ましい。
なお、抗凝固剤は2種類以上用いてもよい。
【0012】
次に、抗凝固処理をした血液を、抗凝固処理を解除しつつ、血管内皮細胞が付着した細胞培養室へ流入させる。抗凝固処理をした血液を、抗凝固処理を解除しつつ細胞培養室に流入させるには、例えば、血液注入口と、細胞培養室と、これらをつなぐ流路を用意し、抗凝固処理をした血液を血液注入口に注入し、該血液注入口と細胞培養室との間に設けられた抗凝固解除剤注入口から抗凝固解除剤含有液を注入して、抗凝固処理された血液と抗凝固解除剤を流路内で混合させ、このようにして抗凝固処理が解除された血液が細胞培養室へ流入するようにすればよい。血液の流速や、流路の長さなどは、血液が、抗凝固解除剤と十分に混合されたのちに、細胞培養室に流入して血栓を形成できるように適宜調整すればよい。また、流速は細胞培養室に付着した血管内皮細胞がはがれにくいような流速にすることが好ましい。
【0013】
抗凝固処理を解除する薬剤(抗凝固解除剤ともよぶ)としては、塩化カルシウム、臭化カルシウム、ヨウ化カルシウム等のハロゲン化カルシウム、リン酸カルシウム、硫酸カルシウム、硝酸カルシウム、重炭酸カルシウム等の無機酸カルシウム塩、蟻酸、酢酸、プロピオン酸、酪酸、アルギン酸、乳酸、グルコン酸、グリセリン酸、グリセロリン酸等の有機酸のカルシウム塩、などの遊離カルシウム供与体であるカルシウム化合物を挙げることができる。これらは、クエン酸やEDTA等のキレート作用に基づいた抗凝固処理剤に作用して処理効果を無効化して血液凝固を促進するものである。
【0014】
また、1本鎖オリゴDNAであるトロンビンアプタマー(Blood. 1993 Jun 15;81(12):3271−6.)を抗凝固剤として用いた場合には、トロンビンアプタマーに対するアンチセンスDNAまたはアンチセンスRNA等のトロンビンアプタマーの機能を阻害する物質が抗凝固解除剤として使用可能である。この際用いられるアンチセンスDNAは実質的にトロンビンアプタマーの抗トロンビン作用を無効化するものであれば、トロンビンアプタマーの一部に対するものであってもよい。
なお、抗凝固剤としてトロンビンアプタマーを用いた場合には、患者の血液中のカルシウム、マグネシウム、亜鉛等の種々の2価金属イオン濃度を的確に反映した試験が可能で有り、キレート剤添加による細胞のダメージも起こらない。
例えば、終濃度5μMのトロンビンアプタマーを用いて抗凝固処理を行い、15μMのトロンビンアプタマーアンチセンスDNAを用いて可逆的に抗凝固処理を解除することができる。より血液サンプル保存が長時間に及ぶ場合には、30μg/mlのコーン由来トリプシンインヒビター等で接触因子の活性化を阻害してもよい。
なお、観測する血液試料が希釈されない為に、抗凝固解除試薬の容量は抗凝固処理血液
に対し10分の1もしくはそれ以下であることが望ましい。
【0015】
抗凝固解除剤と混合された血液は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室に到達し、血液中の白血球および/または血小板が血管内皮細胞と作用することにより、血管内皮細胞上での相互作用や血栓形成が観測される。
ここで、細胞培養室に付着させる血管内皮細胞としては、株化細胞でも初代培養細胞でもよい。血管内皮細胞の由来は特に制限されないが、ヒトにおける血栓形成を評価するためにはヒト由来の血管内皮細胞を使用することが好ましい。血管内皮細胞としては、臍帯静脈内皮細胞、臍帯動脈内皮細胞、大動脈内皮細胞、冠状動脈内皮細胞、皮膚微小血管内皮細胞などが例示できる。
血管内皮細胞は、シートやプレート上であらかじめ培養したものを細胞培養室に設置するか、あるいは、細胞培養室内であらかじめ培養したものを使用することが可能である。血管内皮細胞を培養する場合、細胞の接着をよくするため、細胞培養室内の血管内皮細胞接着面をあらかじめコラーゲンコートしておき、その上に血管内皮細胞を培養することが好ましい。
取り扱いを考慮して、図1に示されるような、スライドグラス(またはプラスチック製プレート)と流路部材を接着させてなるマイクロチップ内に血管内皮細胞を培養して細胞培養室とすることが望ましい。また、血管内皮細胞は、血栓観測時にコンフルエントの状態になっているものを使用することが好ましい。
【0016】
血栓形成は、一定時間血液を通過させた後、生理食塩水等で細胞培養室を洗浄し、細胞培養室内から血液を除去する事によって目視によって評価する事が出来る。特に多血小板血漿を用いた血栓形成の観察においては透過度が高くなり観察が容易であり肉眼による血栓形成の観察も可能である。
【0017】
本発明の血栓形成観測方法においては、白血球および/または血小板の血管内皮細胞への接着を指標にして血栓形成を観測することもできる。この場合、白血球および/または血小板を標識物質で標識し、該標識を検出することにより白血球および/または血小板の血管内皮細胞への接着を観測することがより好ましい。
白血球および/または血小板を標識するための標識物質としては、蛍光物質、放射性物質などが挙げられる。
白血球および/または血小板を標識するための蛍光物質としては、メパクリンなどが挙げられ、蛍光光学顕微鏡や蛍光実態顕微鏡を用いて血栓形成を観察することができる。
例えば、10μM程度のメパクリンを血液に加えることにより、簡便に白血球、血小板を緑色に染色することが可能である。
白血球および/または血小板を蛍光標識して蛍光顕微鏡でモニターする方法としては、特許文献1に開示されている方法が例示される。本発明の方法によれば、共焦点レーザー顕微鏡を用いずとも、安価な蛍光実体顕微鏡を用いることでリアルタイムに血栓形成が観測でき、より簡便な観測が可能である。
なお、蛍光を利用して血栓形成を観察する際には、細胞培養室を透明な素材とし、細胞培養室の細胞が付着している側、すなわち、血液が流れる側とは反対側から観察することが好ましい。
なお、標識物質はそれ自体が白血球および/または血小板と結合しうるものであってもよいし、白血球および/または血小板を認識しうる物質が標識されていてもよい。例えば、白血球および/または血小板に特異的な抗体を標識物質で標識して検出に使用してもよい。このような抗体としては、抗GPIIbIIIa抗体などが挙げられる。
【0018】
本発明の血栓観測装置は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室と、該細胞培養室に接続されて前記細胞培養室に血液を流入させる流入管と、該流入管に接続されて前記流入管に抗凝固処理を解除する薬剤を投入する薬剤管と、を有するこ
とを特徴とする血栓観測装置である。
本発明の血栓観測装置は、さらに、細胞培養室に接続された、細胞培養室を通過した血液を排出するための排出管を備えるものであることが好ましい。
本発明の血栓観測装置は、さらに、流入管および/または薬剤管を加圧するポンプを備えるものであることが好ましい。
本発明の血栓観測装置は、さらに、圧力測定装置を備えるものであることが好ましい。
【0019】
細胞培養室は、血管内皮細胞付着部と、該血管内皮細胞付着部上に血液が通過する流路を有する形状が好ましい。血栓形成室は、透明な、ガラスや熱可塑性樹脂などで製造することができる。細胞培養室の血管内皮細胞付着部以外の面は、血液が付着しないように、シリコン樹脂などで形成されるか、または、ヘパリン、シリコン、もしくはPVLAなどで表面処理されていることが好ましい。
流入管、薬剤管及び排出管も、透明な、ガラスや熱可塑性樹脂などで製造することができ、管内部がヘパリン、シリコン、もしくはPVLAなどで表面処理されていることが好ましい。
【実施例】
【0020】
以下、本発明の血栓観測装置の好ましい態様を、図1及び図2を参照して説明する。
図1に示すように、本形態例に係る血栓観測装置1は、細胞培養室10と、該細胞培養室10に接続されて前記細胞培養室に血液を流入させる流入管11と、該流入管11に接続されて前記流入管11に抗凝固処理を解除する薬剤を投入する薬剤管12と、該細胞培養室10に接続されて前記細胞培養室から血液を排出させる排出管13を備える。
【0021】
まず、流路部材A、スライドガラス(底面)Bおよび蓋Cを組み合わせて内部に細胞培養室を有するマイクロチップを作製する。
PDMS(ポリジメチルシロキサン)製の流路部材Aは、血液の流路となりうる、上面から下面に貫通した溝を有する構造を持つ。流路部材Aの長さは1mm〜10cmとすることが好ましく、溝を、流路幅20μm〜1cm、深さ20μm〜1cmとすることが好ましい。
スライドガラスBは流路部材Aとの接着面がコラーゲンコートされており、このスライドガラスBを流路部材Aと可逆または不可逆的に接着させることにより、流路部材Aの溝とスライドガラスBに囲まれた空間が生じる。なお、流路部材Aの素材をPDMSとすることで接着剤等を用いずとも、自己接着性によってスライドガラスBを圧着させることが可能である。
次に、別途、細胞培養ディッシュ内で培養された血管内皮細胞をトリプシン処理等によってディッシュから剥離させ、血管内皮細胞を回収した後、培地に懸濁する。該血管内皮細胞懸濁液を流路部材AとスライドガラスBの接着によって出来る空間に添加し、1時間程度インキュベートしてスライドガラスBへ血管内皮細胞を接着させる。こうして得られた血管内皮細胞を接着させた流路部材A及びスライドガラスBからなるユニットを新たに用意したディッシュに入れ、培地でディッシュ全体を満たしCO2インキュベーター内で血管内皮細胞を培養する。以上の細胞の取り扱いは無菌条件下で行うことが望ましい。
目的とする細胞密度まで培養を行った後、流路部材AとスライドグラスBからなるユニットに蓋Cを圧着させる。蓋Cは内面(ユニットとの接着面)がへパリンまたはPVLA等で抗血栓処理された透明プラスチックかシリコンコートされている板状のガラス又は透明プラスチックを用いる事が望ましい。流路部材A、スライドガラスB、および蓋Cをクリップ等で固定することにより流路からの液漏れを簡単に防ぐことが可能である。
なお、流路部材A、スライドガラスB、および蓋Cは滅菌して使用される。これらは放射線又は加圧蒸気によって滅菌されることが望ましい。
また、蓋Cには、流路部材Aの溝の両端に相当する箇所に穴が2箇所設けられている。蓋Cの穴に接続された流入管11より抗凝固処理血液を流入させ、該流入管に分岐して接
続された薬剤管12より抗凝固解除液を流入させ、抗凝固処理血液を抗凝固処理を解除しながら細胞培養室に流入させる。また、蓋Cの他方の穴には排出管を接続し、細胞培養室を通過した血液が排出されるようにする。
細胞培養室を顕微鏡観測することで、血液凝固、内皮細胞、血小板、白血球の各因子の相互作用や血栓形成を観測することが可能である。流入する血液を例えばメパクリン処理し、メパクリンの蛍光を観察することで、白血球、血小板の血管内皮細胞との相互作用をリアルタイムに観測することができる。なお、蛍光を観察するときはスライドガラスB側から細胞培養室を観察することが好ましい。
また、一定時間血液を流入させた後、内部を生理食塩水等で洗浄することで、付着する血栓を直接的に目視確認することも可能である。
【0022】
図2は、流路部材Aの溝をY字型にし、流路部材AとスライドガラスBからなるユニット内で抗凝固処理された血液と抗凝固解除剤が混合されるようにした、血栓観測装置の態様を示す。すなわち、流路部材AのY字型の溝は細胞培養室と、流入管の一部および薬剤管の一部を構成する。図1と同様、コラーゲン処理されたスライドガラスBを流路部材Aに接着させ、流路部材Aの溝とスライドガラスBによって生じる空間に血管内皮細胞を加えて細胞を接着させ、このユニットにY字の3箇所の端に相当する箇所に穴の開いた蓋Cを接着させる。なお、図2の態様においては、血管内皮細胞は、Y字の流路内において、細胞培養室だけでなく、流入管の一部および薬剤管の一部に相当する部分にも接着していてもよい。
蓋Cの各穴に流入管、薬剤管および排出管のチューブを図2のように接続することにより血栓観測装置が得られる。流入管11より抗凝固処理血液を、薬剤管12より抗凝固解除液をそれぞれ流入させることにより、Y字の流路内で抗凝固処理血液が抗凝固処理解除剤と混合され、混合された血液が細胞培養室に流入し、血栓が形成される。これを図1と同様にして観測する。
【0023】
以上、本発明を好適な実施の形態に基づいて説明してきたが、本発明は上述の実施例や形態例に限定されるものではなく、本発明の要旨を逸脱しない範囲で種々の改変が可能である。
【図面の簡単な説明】
【0024】
【図1】本発明の第1の形態例に係る血栓観測装置を示す概念図である。(A)は血栓観測装置を構成する流路部材、スライドガラス及び蓋を示す図であり、(B)は血栓観測装置の完成図である。
【図2】本発明の第2の形態例に係る血栓観測装置を示す概念図である。(A)は血栓観測装置を構成する流路部材、スライドガラス及び蓋を示す図であり、(B)は血栓観測装置の完成図である。
【符号の説明】
【0025】
1…血栓観測装置、10…細胞培養室、11…流入管、12…薬剤管、13…排出管。
20…スライドガラスB、21…流路部材A、22…蓋C
【特許請求の範囲】
【請求項1】
その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室に、抗凝固処理された血液を、抗凝固処理を解除しつつ流して前記細胞培養室における血栓の生成を観測することを特徴とする、血栓観測方法。
【請求項2】
白血球および/または血小板の血管内皮細胞への接着を指標にして血栓の形成を観測する、請求項1に記載の方法。
【請求項3】
白血球および/または血小板を標識物質で標識し、該標識を検出することにより白血球および/または血小板の血管内皮細胞への接着を観測する、請求項2に記載の方法。
【請求項4】
前記抗凝固処理がトロンビン阻害効果を有する1本鎖DNA又はRNAによる処理であり、該トロンビン阻害効果を有する1本鎖DNA又はRNAに対するアンチセンスDNA又はアンチセンスRNAを用いて抗凝固処理を解除することを特徴とする、請求項1〜3のいずれか一項に記載の血栓観測方法。
【請求項5】
血管を模した流路に抗凝固処理された血液を、抗凝固処理を解除しつつ流して血栓の形成を観測する血栓観測装置であって、
該血栓観測装置は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室と、該細胞培養室に接続されて前記細胞培養室に血液を流入させる流入管と、該流入管に接続されて前記流入管に抗凝固処理を解除する薬剤を投入する薬剤管と、を有することを特徴とする血栓観測装置。
【請求項1】
その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室に、抗凝固処理された血液を、抗凝固処理を解除しつつ流して前記細胞培養室における血栓の生成を観測することを特徴とする、血栓観測方法。
【請求項2】
白血球および/または血小板の血管内皮細胞への接着を指標にして血栓の形成を観測する、請求項1に記載の方法。
【請求項3】
白血球および/または血小板を標識物質で標識し、該標識を検出することにより白血球および/または血小板の血管内皮細胞への接着を観測する、請求項2に記載の方法。
【請求項4】
前記抗凝固処理がトロンビン阻害効果を有する1本鎖DNA又はRNAによる処理であり、該トロンビン阻害効果を有する1本鎖DNA又はRNAに対するアンチセンスDNA又はアンチセンスRNAを用いて抗凝固処理を解除することを特徴とする、請求項1〜3のいずれか一項に記載の血栓観測方法。
【請求項5】
血管を模した流路に抗凝固処理された血液を、抗凝固処理を解除しつつ流して血栓の形成を観測する血栓観測装置であって、
該血栓観測装置は、その内部の少なくとも一部に血管内皮細胞が付着した細胞培養室と、該細胞培養室に接続されて前記細胞培養室に血液を流入させる流入管と、該流入管に接続されて前記流入管に抗凝固処理を解除する薬剤を投入する薬剤管と、を有することを特徴とする血栓観測装置。
【図1】


【図2】




【図2】


【公開番号】特開2007−298486(P2007−298486A)
【公開日】平成19年11月15日(2007.11.15)
【国際特許分類】
【出願番号】特願2006−129077(P2006−129077)
【出願日】平成18年5月8日(2006.5.8)
【出願人】(000224101)藤森工業株式会社 (292)
【出願人】(599074176)
【Fターム(参考)】
【公開日】平成19年11月15日(2007.11.15)
【国際特許分類】
【出願日】平成18年5月8日(2006.5.8)
【出願人】(000224101)藤森工業株式会社 (292)
【出願人】(599074176)

【Fターム(参考)】
[ Back to top ]

