血管形成促進剤
【課題】 本発明は、本発明は、血管形成を促進させる手段を提供することを目的とする。
【解決手段】 本発明は、アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩を有効成分として含有する血管形成促進剤、及び、虚血性疾患の予防又は治療剤に関する。本発明はまたアペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩を用いた、人工血管の製造方法、疾患の診断方法、有用物質のスクリーニング方法に関する。
【解決手段】 本発明は、アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩を有効成分として含有する血管形成促進剤、及び、虚血性疾患の予防又は治療剤に関する。本発明はまたアペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩を用いた、人工血管の製造方法、疾患の診断方法、有用物質のスクリーニング方法に関する。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩を有効成分として含有する血管形成促進剤。
【請求項2】
アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩を有効成分として含有する虚血性疾患の予防又は治療剤。
【請求項3】
アペリンをコードする遺伝子を含む血管形成促進剤。
【請求項4】
アペリンをコードする遺伝子を含む虚血性疾患の予防又は治療剤。
【請求項5】
血管新生を促進する作用を有する、請求項1又は3に記載の血管形成促進剤。
【請求項6】
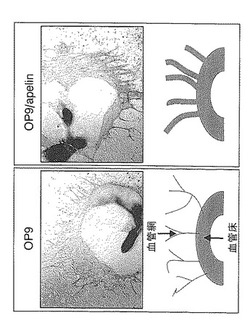
血管腔の拡張を促進する作用を有する、請求項1又は3に記載の血管形成促進剤。
【請求項7】
アペリンが配列番号1で表されるアミノ酸配列と同一又は実質的に同一のアミノ酸配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項8】
アペリンが配列番号5、7、9又は11で表されるアミノ酸配列の部分配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項9】
アペリンが(a)配列番号5、7、9又は11で表されるアミノ酸配列の第6番目から第77番目のアミノ酸配列を有するペプチド、(b)配列番号5、7、9又は11で表されるアミノ酸配列の第40番目から第77番目のアミノ酸配列を有するペプチド、(c)配列番号5、7、9又は11で表されるアミノ酸配列の第42番目から第77番目のアミノ酸配列を有するペプチド、(d)配列番号5、7、9又は11で表されるアミノ酸配列の第47番目から第77番目のアミノ酸配列を有するペプチド、(e)配列番号5、7、9又は11で表されるアミノ酸配列の第61番目から第77番目のアミノ酸配列を有するペプチド、(f)配列番号5、7、9又は11で表されるアミノ酸配列の第65番目から第77番目のアミノ酸配列を有するペプチド又はそのN末端のアミノ酸(Gln)がピログルタミン酸化したアミノ酸配列を有するペプチド、(g)配列番号5、7、9又は11で表されるアミノ酸配列の第1番目から第25番目のアミノ酸配列を有するペプチド、(h)配列番号5、7、9又は11で表されるアミノ酸配列の第6番目から第25番目のアミノ酸配列を有するペプチド、(i)配列番号5、7、9又は11で表されるアミノ酸配列の第42番目から第64番目のアミノ酸配列を有するペプチド、(j)配列番号5、7、9又は11で表されるアミノ酸配列の第61番目から第64番目のアミノ酸配列を有するペプチド、(k)配列番号5、7、9又は11で表されるアミノ酸配列の第43番目から第77番目のアミノ酸配列を有するペプチド、(l)配列番号5、7、9又は11で表されるアミノ酸配列の第41番目から第77番目のアミノ酸配列を有するペプチド、(m)配列番号5、7、9又は11で表されるアミノ酸配列の第66番目から第77番目のアミノ酸配列を有するペプチド、(n)配列番号5、7、9又は11で表されるアミノ酸配列の第67番目から第77番目のアミノ酸配列を有するペプチド、(o)配列番号5、7、9又は11で表されるアミノ酸配列の第64番目から第77番目のアミノ酸配列を有するペプチド、(p)配列番号5、7、9又は11で表されるアミノ酸配列の第63番目から第77番目のアミノ酸配列を有するペプチド、(q)配列番号5、7、9又は11で表されるアミノ酸配列の第65番目から第76番目のアミノ酸配列を有するペプチド又は(r)配列番号5、7、9又は11で表されるアミノ酸配列の第65番目から第75番目のアミノ酸配列を有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項10】
アペリンが配列番号5、7、9又は11で表されるアミノ酸配列の第65番目から第77番目のアミノ酸配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項11】
アペリンがpGlu−Arg−Pro−Arg−Leu−Ser−His−Lys−Gly−Pro−Met−Pro−Pheで表されるアミノ酸配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項12】
アペリンが配列番号5、7、9又は11で表されるアミノ酸配列の第42番目から第77番目のアミノ酸配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項13】
アペリンの修飾体が式:
X1−Arg−Pro−Arg−X2−Ser−His−X3−Gly−Pro−X4−X5 (I)
[式中、X1は水素原子又はそれぞれ同一又は異なって側鎖が置換されていてもよい1〜25個のアミノ酸からなるアミノ酸残基又はペプチド鎖を示し、X2は側鎖が置換されていてもよい中性アミノ酸残基を示し、X3は側鎖が置換されていてもよい中性アミノ酸残基、側鎖が置換されていてもよい芳香性アミノ酸残基又は側鎖が置換されていてもよい塩基性アミノ酸残基を示し、X4は結合手又は側鎖が置換されていてもよい中性又は芳香性アミノ酸残基を示し、X5は(イ)側鎖が置換されていてもよいアミノ酸残基又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたアミノ酸誘導体、(ロ)水酸基又は(ハ)側鎖が置換されていてもよいアミノ酸残基と側鎖が置換されていてもよいアミノ酸残基が結合してなるジペプチド鎖又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたペプチド誘導体を示し、式中の−Arg−Pro−Arg−、−Ser−His−又は−Gly−Pro−中の各アミノ酸残基の側鎖は置換されていてもよい。但し、X2がLeuを、X3がLysを、X4がMetを示し、かつX5が(イ)Pro又は(ロ)Pro−Pheを示し、式中の−Arg−Pro−Arg−が無置換の−Arg−Pro−Arg−を、−Ser−His−が無置換の−Ser−His−を、且つ−Gly−Pro−が無置換の−Gly−Pro−を示す場合を除く。]
で表される化合物である請求項1、2、5及び6の何れか1項に記載の剤。
【請求項14】
アペリンの修飾体が式:
P1−Arg−Pro−Arg−Leu−Phe−P2−P3−Gly−Pro−P4−P5 (II)
[式中、P1は水素原子又はそれぞれ同一又は異なって側鎖が置換されていてもよい1〜25個のアミノ酸からなるアミノ酸残基又はペプチド鎖を示し、P2は側鎖が置換されていてもよい中性アミノ酸残基又は側鎖が置換されていてもよい塩基性アミノ酸残基を示し、P3は側鎖が置換されていてもよい中性アミノ酸残基、側鎖が置換されていてもよい芳香性アミノ酸残基又は側鎖が置換されていてもよい塩基性アミノ酸残基を示し、P4は結合手又は側鎖が置換されていてもよい中性又は芳香性アミノ酸残基を示し、P5は(イ)側鎖が置換されていてもよいアミノ酸残基又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたアミノ酸誘導体、(ロ)水酸基又は(ハ)側鎖が置換されていてもよいアミノ酸残基と側鎖が置換されていてもよいアミノ酸残基が結合してなるジペプチド鎖又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたペプチド誘導体を示し、式中の−Arg−Pro−Arg−Leu−Phe−又は−Gly−Pro−中の各アミノ酸残基の側鎖は置換されていてもよい。]
で表される化合物である請求項1、2、5及び6の何れか1項に記載の剤。
【請求項15】
アペリンの修飾体が式:
Q1−Arg−Pro−Arg−Leu−Ser−Ala−Q2−Gly−Q5−Q3−Q4 (III)
[式中、Q1は水素原子又はそれぞれ同一又は異なって側鎖が置換されていてもよい1〜25個のアミノ酸からなるアミノ酸残基又はペプチド鎖を示し、Q2は側鎖が置換されていてもよい中性アミノ酸残基、側鎖が置換されていてもよい芳香性アミノ酸残基又は側鎖が置換されていてもよい塩基性アミノ酸残基を示し、Q3は結合手又は側鎖が置換されていてもよい中性又は芳香性アミノ酸残基を示し、Q4は(イ)側鎖が置換されていてもよいアミノ酸残基又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたアミノ酸誘導体、(ロ)水酸基又は(ハ)側鎖が置換されていてもよいアミノ酸残基と側鎖が置換されていてもよいアミノ酸残基が結合してなるジペプチド鎖又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたペプチド誘導体を示し、Q5は側鎖が置換されていてもよい中性アミノ酸残基を示し、式中の−Arg−Pro−Arg−Leu−Ser−Ala−中の各アミノ酸残基の側鎖は置換されていてもよい。]
で表される化合物である請求項1、2、5及び6の何れか1項に記載の剤。
【請求項16】
アペリンの修飾体が式:
R1−Arg−Pro−Arg−Leu−Ser−His−Lys−Gly−Pro−R2−Pro−R3 (IV)
[式中、R1は水素原子又はそれぞれ同一又は異なって側鎖が置換されていてもよい1〜25個のアミノ酸からなるアミノ酸残基又はペプチド鎖を示し、R2は置換されていてもよいCha、置換されていてもよいMet又は置換されていてもよいNleを示し、R3は置換されていてもよいPhe(Cl)、置換されていてもよいPhe、置換されていてもよいNal(2)、置換されていてもよいCha又は置換されていてもよいTyrを示し、式中の−Arg−Pro−Arg−Leu−Ser−His−Lys−Gly−Pro又は−Pro−中の各アミノ酸残基の側鎖は置換されていてもよい。]
で表される化合物である請求項1、2、5及び6の何れか1項に記載の剤。
【請求項17】
請求項1、3及び5〜16の何れか1項に記載の血管形成促進剤を用いて、血管系に分化可能な細胞からin vitroにおいて人工血管を製造する方法。
【請求項18】
被験体から採取された検体中のアペリン濃度を測定し、測定値を健常者及び虚血性疾患患者の測定値と対比することにより虚血性疾患を診断する方法。
【請求項19】
被験体から採取された検体中のアペリン濃度を測定し、測定値を健常者及び血管が過剰増殖する疾患の患者の測定値と対比することにより血管が過剰増殖する疾患を診断する方法。
【請求項20】
被験体から採取された検体中のアペリン濃度を測定し、測定値を健常者及び血管怒張又は毛細血管拡張を呈する疾患の患者の測定値と対比することにより血管怒張又は毛細血管拡張を呈する疾患を診断する方法。
【請求項21】
(a)アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩、及び/又は、(b)配列番号3で表されるアミノ酸配列と同一若しくは実質的に同一のアミノ酸配列を含有するアペリン受容体、その部分ペプチド若しくはその塩を用いることを特徴とする、血管形成促進剤又は虚血性疾患の治療若しくは予防剤のスクリーニング方法。
【請求項22】
(a)アペリンをコードするDNAを含有するDNA、及び/又は、(b)配列番号3で表されるアミノ酸配列と同一若しくは実質的に同一のアミノ酸配列を含有するアペリン受容体若しくはその部分ペプチドをコードするDNAを含有するDNAを用いることを特徴とする、血管形成促進剤又は虚血性疾患の治療若しくは予防剤のスクリーニング方法。
【請求項23】
(a)アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩、及び/又は、(b)配列番号3で表されるアミノ酸配列と同一若しくは実質的に同一のアミノ酸配列を含有するアペリン受容体、その部分ペプチド若しくはその塩を用いることを特徴とする、血管形成抑制剤又は血管怒張若しくは毛細血管拡張を呈する疾患の予防若しくは治療剤のスクリーニング方法。
【請求項24】
(a)アペリンをコードするDNAを含有するDNA、及び/又は、(b)配列番号3で表されるアミノ酸配列と同一若しくは実質的に同一のアミノ酸配列を含有するアペリン受容体若しくはその部分ペプチドをコードするDNAを含有するDNAを用いることを特徴とする、血管形成抑制剤又は血管怒張若しくは毛細血管拡張を呈する疾患の予防若しくは治療剤のスクリーニング方法。
【請求項1】
アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩を有効成分として含有する血管形成促進剤。
【請求項2】
アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩を有効成分として含有する虚血性疾患の予防又は治療剤。
【請求項3】
アペリンをコードする遺伝子を含む血管形成促進剤。
【請求項4】
アペリンをコードする遺伝子を含む虚血性疾患の予防又は治療剤。
【請求項5】
血管新生を促進する作用を有する、請求項1又は3に記載の血管形成促進剤。
【請求項6】
血管腔の拡張を促進する作用を有する、請求項1又は3に記載の血管形成促進剤。
【請求項7】
アペリンが配列番号1で表されるアミノ酸配列と同一又は実質的に同一のアミノ酸配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項8】
アペリンが配列番号5、7、9又は11で表されるアミノ酸配列の部分配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項9】
アペリンが(a)配列番号5、7、9又は11で表されるアミノ酸配列の第6番目から第77番目のアミノ酸配列を有するペプチド、(b)配列番号5、7、9又は11で表されるアミノ酸配列の第40番目から第77番目のアミノ酸配列を有するペプチド、(c)配列番号5、7、9又は11で表されるアミノ酸配列の第42番目から第77番目のアミノ酸配列を有するペプチド、(d)配列番号5、7、9又は11で表されるアミノ酸配列の第47番目から第77番目のアミノ酸配列を有するペプチド、(e)配列番号5、7、9又は11で表されるアミノ酸配列の第61番目から第77番目のアミノ酸配列を有するペプチド、(f)配列番号5、7、9又は11で表されるアミノ酸配列の第65番目から第77番目のアミノ酸配列を有するペプチド又はそのN末端のアミノ酸(Gln)がピログルタミン酸化したアミノ酸配列を有するペプチド、(g)配列番号5、7、9又は11で表されるアミノ酸配列の第1番目から第25番目のアミノ酸配列を有するペプチド、(h)配列番号5、7、9又は11で表されるアミノ酸配列の第6番目から第25番目のアミノ酸配列を有するペプチド、(i)配列番号5、7、9又は11で表されるアミノ酸配列の第42番目から第64番目のアミノ酸配列を有するペプチド、(j)配列番号5、7、9又は11で表されるアミノ酸配列の第61番目から第64番目のアミノ酸配列を有するペプチド、(k)配列番号5、7、9又は11で表されるアミノ酸配列の第43番目から第77番目のアミノ酸配列を有するペプチド、(l)配列番号5、7、9又は11で表されるアミノ酸配列の第41番目から第77番目のアミノ酸配列を有するペプチド、(m)配列番号5、7、9又は11で表されるアミノ酸配列の第66番目から第77番目のアミノ酸配列を有するペプチド、(n)配列番号5、7、9又は11で表されるアミノ酸配列の第67番目から第77番目のアミノ酸配列を有するペプチド、(o)配列番号5、7、9又は11で表されるアミノ酸配列の第64番目から第77番目のアミノ酸配列を有するペプチド、(p)配列番号5、7、9又は11で表されるアミノ酸配列の第63番目から第77番目のアミノ酸配列を有するペプチド、(q)配列番号5、7、9又は11で表されるアミノ酸配列の第65番目から第76番目のアミノ酸配列を有するペプチド又は(r)配列番号5、7、9又は11で表されるアミノ酸配列の第65番目から第75番目のアミノ酸配列を有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項10】
アペリンが配列番号5、7、9又は11で表されるアミノ酸配列の第65番目から第77番目のアミノ酸配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項11】
アペリンがpGlu−Arg−Pro−Arg−Leu−Ser−His−Lys−Gly−Pro−Met−Pro−Pheで表されるアミノ酸配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項12】
アペリンが配列番号5、7、9又は11で表されるアミノ酸配列の第42番目から第77番目のアミノ酸配列を含有するペプチドである請求項1〜6の何れか1項に記載の剤。
【請求項13】
アペリンの修飾体が式:
X1−Arg−Pro−Arg−X2−Ser−His−X3−Gly−Pro−X4−X5 (I)
[式中、X1は水素原子又はそれぞれ同一又は異なって側鎖が置換されていてもよい1〜25個のアミノ酸からなるアミノ酸残基又はペプチド鎖を示し、X2は側鎖が置換されていてもよい中性アミノ酸残基を示し、X3は側鎖が置換されていてもよい中性アミノ酸残基、側鎖が置換されていてもよい芳香性アミノ酸残基又は側鎖が置換されていてもよい塩基性アミノ酸残基を示し、X4は結合手又は側鎖が置換されていてもよい中性又は芳香性アミノ酸残基を示し、X5は(イ)側鎖が置換されていてもよいアミノ酸残基又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたアミノ酸誘導体、(ロ)水酸基又は(ハ)側鎖が置換されていてもよいアミノ酸残基と側鎖が置換されていてもよいアミノ酸残基が結合してなるジペプチド鎖又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたペプチド誘導体を示し、式中の−Arg−Pro−Arg−、−Ser−His−又は−Gly−Pro−中の各アミノ酸残基の側鎖は置換されていてもよい。但し、X2がLeuを、X3がLysを、X4がMetを示し、かつX5が(イ)Pro又は(ロ)Pro−Pheを示し、式中の−Arg−Pro−Arg−が無置換の−Arg−Pro−Arg−を、−Ser−His−が無置換の−Ser−His−を、且つ−Gly−Pro−が無置換の−Gly−Pro−を示す場合を除く。]
で表される化合物である請求項1、2、5及び6の何れか1項に記載の剤。
【請求項14】
アペリンの修飾体が式:
P1−Arg−Pro−Arg−Leu−Phe−P2−P3−Gly−Pro−P4−P5 (II)
[式中、P1は水素原子又はそれぞれ同一又は異なって側鎖が置換されていてもよい1〜25個のアミノ酸からなるアミノ酸残基又はペプチド鎖を示し、P2は側鎖が置換されていてもよい中性アミノ酸残基又は側鎖が置換されていてもよい塩基性アミノ酸残基を示し、P3は側鎖が置換されていてもよい中性アミノ酸残基、側鎖が置換されていてもよい芳香性アミノ酸残基又は側鎖が置換されていてもよい塩基性アミノ酸残基を示し、P4は結合手又は側鎖が置換されていてもよい中性又は芳香性アミノ酸残基を示し、P5は(イ)側鎖が置換されていてもよいアミノ酸残基又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたアミノ酸誘導体、(ロ)水酸基又は(ハ)側鎖が置換されていてもよいアミノ酸残基と側鎖が置換されていてもよいアミノ酸残基が結合してなるジペプチド鎖又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたペプチド誘導体を示し、式中の−Arg−Pro−Arg−Leu−Phe−又は−Gly−Pro−中の各アミノ酸残基の側鎖は置換されていてもよい。]
で表される化合物である請求項1、2、5及び6の何れか1項に記載の剤。
【請求項15】
アペリンの修飾体が式:
Q1−Arg−Pro−Arg−Leu−Ser−Ala−Q2−Gly−Q5−Q3−Q4 (III)
[式中、Q1は水素原子又はそれぞれ同一又は異なって側鎖が置換されていてもよい1〜25個のアミノ酸からなるアミノ酸残基又はペプチド鎖を示し、Q2は側鎖が置換されていてもよい中性アミノ酸残基、側鎖が置換されていてもよい芳香性アミノ酸残基又は側鎖が置換されていてもよい塩基性アミノ酸残基を示し、Q3は結合手又は側鎖が置換されていてもよい中性又は芳香性アミノ酸残基を示し、Q4は(イ)側鎖が置換されていてもよいアミノ酸残基又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたアミノ酸誘導体、(ロ)水酸基又は(ハ)側鎖が置換されていてもよいアミノ酸残基と側鎖が置換されていてもよいアミノ酸残基が結合してなるジペプチド鎖又はそのC末端カルボキシル基がヒドロキシメチル基又はホルミル基に還元されたペプチド誘導体を示し、Q5は側鎖が置換されていてもよい中性アミノ酸残基を示し、式中の−Arg−Pro−Arg−Leu−Ser−Ala−中の各アミノ酸残基の側鎖は置換されていてもよい。]
で表される化合物である請求項1、2、5及び6の何れか1項に記載の剤。
【請求項16】
アペリンの修飾体が式:
R1−Arg−Pro−Arg−Leu−Ser−His−Lys−Gly−Pro−R2−Pro−R3 (IV)
[式中、R1は水素原子又はそれぞれ同一又は異なって側鎖が置換されていてもよい1〜25個のアミノ酸からなるアミノ酸残基又はペプチド鎖を示し、R2は置換されていてもよいCha、置換されていてもよいMet又は置換されていてもよいNleを示し、R3は置換されていてもよいPhe(Cl)、置換されていてもよいPhe、置換されていてもよいNal(2)、置換されていてもよいCha又は置換されていてもよいTyrを示し、式中の−Arg−Pro−Arg−Leu−Ser−His−Lys−Gly−Pro又は−Pro−中の各アミノ酸残基の側鎖は置換されていてもよい。]
で表される化合物である請求項1、2、5及び6の何れか1項に記載の剤。
【請求項17】
請求項1、3及び5〜16の何れか1項に記載の血管形成促進剤を用いて、血管系に分化可能な細胞からin vitroにおいて人工血管を製造する方法。
【請求項18】
被験体から採取された検体中のアペリン濃度を測定し、測定値を健常者及び虚血性疾患患者の測定値と対比することにより虚血性疾患を診断する方法。
【請求項19】
被験体から採取された検体中のアペリン濃度を測定し、測定値を健常者及び血管が過剰増殖する疾患の患者の測定値と対比することにより血管が過剰増殖する疾患を診断する方法。
【請求項20】
被験体から採取された検体中のアペリン濃度を測定し、測定値を健常者及び血管怒張又は毛細血管拡張を呈する疾患の患者の測定値と対比することにより血管怒張又は毛細血管拡張を呈する疾患を診断する方法。
【請求項21】
(a)アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩、及び/又は、(b)配列番号3で表されるアミノ酸配列と同一若しくは実質的に同一のアミノ酸配列を含有するアペリン受容体、その部分ペプチド若しくはその塩を用いることを特徴とする、血管形成促進剤又は虚血性疾患の治療若しくは予防剤のスクリーニング方法。
【請求項22】
(a)アペリンをコードするDNAを含有するDNA、及び/又は、(b)配列番号3で表されるアミノ酸配列と同一若しくは実質的に同一のアミノ酸配列を含有するアペリン受容体若しくはその部分ペプチドをコードするDNAを含有するDNAを用いることを特徴とする、血管形成促進剤又は虚血性疾患の治療若しくは予防剤のスクリーニング方法。
【請求項23】
(a)アペリン、その修飾体、それらのアミド、それらのエステル又はそれらの塩、及び/又は、(b)配列番号3で表されるアミノ酸配列と同一若しくは実質的に同一のアミノ酸配列を含有するアペリン受容体、その部分ペプチド若しくはその塩を用いることを特徴とする、血管形成抑制剤又は血管怒張若しくは毛細血管拡張を呈する疾患の予防若しくは治療剤のスクリーニング方法。
【請求項24】
(a)アペリンをコードするDNAを含有するDNA、及び/又は、(b)配列番号3で表されるアミノ酸配列と同一若しくは実質的に同一のアミノ酸配列を含有するアペリン受容体若しくはその部分ペプチドをコードするDNAを含有するDNAを用いることを特徴とする、血管形成抑制剤又は血管怒張若しくは毛細血管拡張を呈する疾患の予防若しくは治療剤のスクリーニング方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2008−13436(P2008−13436A)
【公開日】平成20年1月24日(2008.1.24)
【国際特許分類】
【出願番号】特願2004−300653(P2004−300653)
【出願日】平成16年10月14日(2004.10.14)
【出願人】(504160781)国立大学法人金沢大学 (282)
【Fターム(参考)】
【公開日】平成20年1月24日(2008.1.24)
【国際特許分類】
【出願日】平成16年10月14日(2004.10.14)
【出願人】(504160781)国立大学法人金沢大学 (282)
【Fターム(参考)】
[ Back to top ]

