血糖値センサ
【課題】低侵襲かつ連続に、血糖値を検出する。
【解決手段】光学センサ1は、血糖値に関する情報を経皮的に検出する。ゲル部10は、グルコース応答性を有し、皮膚4に貼り付けられるグルコース応答性ゲルを有する。ゲル部10には、グルコース応答性ゲルに水分を補給するグルコース非応答性ゲルも含まれている。検出部11は、皮膚4を通して浸透するグルコースによるグルコース応答性ゲルの膨潤度を光学的に検出する。検出された膨潤度に基づいて、血糖値の推定値が算出される。
【解決手段】光学センサ1は、血糖値に関する情報を経皮的に検出する。ゲル部10は、グルコース応答性を有し、皮膚4に貼り付けられるグルコース応答性ゲルを有する。ゲル部10には、グルコース応答性ゲルに水分を補給するグルコース非応答性ゲルも含まれている。検出部11は、皮膚4を通して浸透するグルコースによるグルコース応答性ゲルの膨潤度を光学的に検出する。検出された膨潤度に基づいて、血糖値の推定値が算出される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、血糖値を検出する血糖値センサに関する。
【背景技術】
【0002】
予防医学や医療費抑制が叫ばれる中で、血管障害リスクを多面的に抑制することは大変有意義である。分子レベルではグルコースや中性脂肪、コレステロール、ストレスマーカーなどが血管障害の重要な原因物質とされる。また、疫学的には過食、飲酒、喫煙、運動不足などが血管障害の誘発因子とされており、メタボリックシンドローム(通称メタボ)や糖尿病などが血管障害のリスクファクタとして挙げられている。このような背景から、初期のメタボ患者や糖尿病患者及びその予備軍に対して血管障害リスクの原因物質、誘発因子及びリスクファクタを抑制するように積極介入することの意義は大きいと考えられる。
【0003】
現状行われているいわゆるメタボ検診や、今後活用が進むHbA1C計測などの検診によって、これまで見過ごされていた隠れ糖尿病罹患者が顕在化する時代が到来すると思われる。特に、糖尿病患者の大部分は食事や運動などの生活習慣を改善することによって合併症の発生リスクを大幅に抑制することができることから、自己管理の重要性が叫ばれている。
【0004】
血糖値を自己管理をする際に、血糖値センサは主要な役割を担っている(例えば、特許文献1参照)。しかし、現状では、血糖値センサは、日内変動の激しい血糖値の瞬間的な値を計測するものであるため、計測結果のばらつきが大きい。現状の血糖値センサの計測操作は簡便ではあるものの、準備から片付けまでには数分以上を要するため、仕事中や旅行中などで昼食後1時間後又は2時間後の血糖値を正確に計測するのには困難がつきまとう。
【0005】
また、糖尿病患者にとって大きなリスクである低血糖症状に対して、1日数回程度の血糖値の計測では足りない。しかも、指裂血を計測対象とする穿刺採血方式を採用しているため、利用者からの不満は大きいうえ、データ再現性も必ずしも高いものではない。
【0006】
一方で、連続的に血糖値を計測できる次世代のセンサとして期待されている酵素電極埋め込み方式のセンサは、現状の血糖値センサ以上に侵襲性が高い(例えば、特許文献2参照)。逆に、研究段階にあるほぼすべての非侵襲の血糖値センサは、現状の血糖値センサよりもデータ再現性に乏しく、原理的にその向上は期待しがたい。
【0007】
血糖値推定値を非侵襲に得るセンサとしては経皮イオントフォレシス方式を採用した腕時計型のセンサが最もよく知られている(例えば、特許文献3参照)。しかしながら、この方式では、イオントフォレシスの電気刺激が結果的に侵襲的であったため、多くのケースで皮膚に損傷を与えているのが実情である。
【0008】
血糖値は、低血糖などの最低レベルであっても一般的な生化学分析としては十分に高濃度である。血糖由来の糖は、中性の低分子であるため、積極的な電気刺激など無しに皮膚上に自然拡散だけでも移動してくることが知られている。この位置の糖は皮膚細胞によって随時消費されるため、大血管から採血される血液中の血糖値と比較すればその濃度は確実に低く、血糖値とは一致しない。このため、血糖値センサの測定の対象としては不適当であると考えられている。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開平8−338798号公報
【特許文献2】特開2003−265444号公報
【特許文献3】特許第4295970号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
このように、血糖値センサを開発する業界では、10年以上の間、世界的に非侵襲・連続計測を最大の課題として抱えているが、未だにその課題は解決されていない。
【0011】
本発明は、上記実情に鑑みてなされたもので、低侵襲かつ連続に、血糖値を検出することができる血糖値センサを提供することを目的とする。
【課題を解決するための手段】
【0012】
上記目的を達成するために、本発明の第1の観点に係る血糖値センサは、
血糖値に関する情報を経皮的に検出する血糖値センサであって、
皮膚に貼り付けられ、グルコースに応答して膨潤するグルコース応答性ゲルと、
前記グルコース応答性ゲルに水分を補給する水分補給部と、
皮膚を通して浸透するグルコースによる前記グルコース応答性ゲルの膨潤度を光学的に検出する検出部と、
前記検出部により検出された前記グルコース応答性ゲルの膨潤度に基づいて、血糖値の推定値を算出する推定部と、
前記推定部によって算出された血糖値の推定値を記憶する記憶部と、
を備える。
【0013】
前記グルコース応答性ゲルが、ボロン酸基を官能基として有する、
こととしてもよい。
【0014】
前記水分補給部は、
グルコース応答性を有しないグルコース非応答性ゲルである、
こととしてもよい。
【0015】
前記検出部は、
前記グルコース応答性ゲルの第1の膨潤度と、
前記グルコース非応答性ゲルの第2の膨潤度と、
を同時に検出し、
前記推定部は、
前記第1の膨潤度と前記第2の膨潤度との違いに基づいて、前記血糖値の推定値を算出する、
こととしてもよい。
【0016】
前記検出部は、
表面プラズモン共鳴又は前記グルコース応答性ゲルが当接する光導波路内における光の全反射により発生する該光の位相の遅延に基づいて、前記グルコース応答性ゲルの膨潤度を検出する、
こととしてもよい。
【発明の効果】
【0017】
本発明に係る血糖値センサによれば、グルコースにより膨潤するグルコース応答性ゲルを皮膚に貼り付けて、その膨潤度を光学的に検出することにより、血糖値を間接的に計測する。このゲルは、グルコースによる親和性に基づく可逆な構造変化を起こして膨潤するものであるので、連続的な血糖値の計測が可能である。また、酸化酵素などによって刺激性の副産物を生成することなく低侵襲に血糖値の計測が可能である。
【図面の簡単な説明】
【0018】
【図1】本発明の第1の実施形態に係る血糖値センサの構成を示す斜視図である。
【図2】図1の血糖値センサの構成を示す模式図である。
【図3】図2の検出部の光学系の構成を示す図である。
【図4】界面でレーザ光が反射する様子を示す図である。
【図5】グルコース応答性ゲルが、グルコースに応答して膨潤したときの反射光強度の入射角依存性を示すグラフである。
【図6】フォトダイオードで検出される反射光強度の時間変化の一例である。
【図7】本発明の第2の実施形態に係る血糖値センサにおける検出部の一部の構成を示す図である。
【図8】本発明の第3の実施形態に係る検出部の構成を示す図である。
【図9】導波路のレーザ光の光路を説明するための図である。
【図10】本発明の第4の実施形態に係る血糖値センサの光学センサの構造を示す模式図である。
【図11】図10の光学センサの構造を示す上面図である。
【図12】血糖値センサの他の構成例を示す模式図である。
【発明を実施するための形態】
【0019】
本発明の実施の形態について、図面を参照して詳細に説明する。
【0020】
(第1の実施形態)
まず、本発明の第1の実施形態について説明する。
【0021】
図1には、本実施形態に係る血糖値センサ100の斜視図が示されている。図1に示すように、血糖値センサ100は、光学センサ1と携帯端末2とを備える。
【0022】
光学センサ1は、貼り付け用フィルム3によって例えば上腕部に貼り付けられている。光学センサ1は、血糖値に関する情報を経皮的に検出する。光学センサ1は、検出した血糖値に関する情報を、ボディエリアネットワーク(BAN)により、携帯端末2に送信する無線通信機能を有している。ここで、ボディエリアネットワークとは、極めて近距離で行われる通信ネットワークである。このボディエリアネットワークを用いれば、例えば人が携帯する装置間での通信が可能となる。
【0023】
携帯端末2は、ボディエリアネットワークにより、光学センサ1と無線通信可能な無線通信機能を有している。携帯端末2は、この無線通信機能を用いて、光学センサ1によって検出された血糖値に関する情報(後述するゲル部10のゲル20Aのグルコースによる膨潤度)を受信する。携帯端末2は、受信した血糖値に関する情報に基づいて血糖値の推定値を算出し、算出された血糖値の推定値を記憶する。このようにして、ある期間における血糖値の推移が取得される。
【0024】
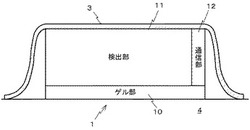
図2には、光学センサ1の構成が模式的に示されている。図2に示すように、光学センサ1は、ゲル部10と、光学検出部11と、通信部12とを備えている。
【0025】
図3に示すように、ゲル部10には、2種類のゲル20A、20Bが設置されている。
【0026】
一方のゲル20Aは、グルコース応答性を有するグルコース応答性ゲルである。ゲル20Aには、ボロン酸基を官能基として有するもの、より好ましくは、フェニルボロン酸基が付与されたものが用いられる。
【0027】
フェニルボロン酸基を有するゲル20Aは、水分等に含まれる水酸基との結合と分離を繰り返している。ゲル20Aは、水酸基と結合し、さらにグルコースが結びつくと、電荷を帯び、その電荷による反発力でゲル20Aが膨潤する。ゲル20Aは、膨潤すると、その誘電率が変化する。検出部11は、この誘電率の変化を光学的に計測する。
【0028】
なお、グルコースとの結び付きが失われると、ゲル20Aは再び収縮する。このように、ゲル20Aは、周辺のグルコースの濃度に応じて膨潤と収縮とを繰り返すので、グルコースの濃度の連続計測が可能となる。
【0029】
ゲル20Aとして好適なものには、例えば、4−(ジヒドロキシボロノ)スチレン、3−(メタ)アクリルアミドフェニルボロン酸、N−(4’−ビニルベンジル)−4−フェニルボロン酸カルボキサミド、3−((メタ)アクリルアミジルグリシルアミド)フェニルボロン酸、3−(メタ)アクリルアミド−2−トリフルオロメチルフェニルボロン酸、3−(メタ)アクリルアミド−4−ペンタフルオロエチルフェニルボロン酸、5−(メタ)アクリルアミド−2−ヘプタフルオロプロピルフェニルボロン酸、5−((メタ)アクリルアミジルグリシルアミド)−2−ヘプタフルオロプロピルフェニルボロン酸、5−(メタ)アクリルアミド−2,4,6−ビス(ヘプタフルオロプロピル)フェニルボロン酸、3−(メタ)アクリルアミド−2−(1,1,2,2,3,3−ヘキサフルオロプロピル)フェニルボロン酸、3−(メタ)アクリルアミド−4−(1−クロロ−1,1,2,2,3,3−ヘキサフルオロプロピル)フェニルボロン酸、5−(メタ)アクリルアミド−2−(ペルフルオロ−1,4−ジメチル2,5−ジオキサオクチル)フェニルボロン酸などがある。
【0030】
他方のゲル20Bは、グルコース応答性を有しないグルコース非応答性ゲルである。ゲル20Bには、例えばゲル20Aと同じゲル骨格を有し、フェニルボロン酸基が付与されていないものを用いることができる。ゲル20Bは、ゲル20Aに対して水分を補給する水分補給部として機能する。
【0031】
ゲル20Bは、グルコースによって膨潤することはないが、汗や体表温度等の他の環境要因に応じてその誘電率が変化する。これはゲル20Aについても同じである。検出部11は、このような他の環境要因によるゲル20Aの誘電率の変化を相殺するために、ゲル20Bについても検出部11により、誘電率の変化を光学的に測定する。
【0032】
これらのゲル20A、20Bは、皮膚4に直接貼り付けられる。
【0033】
検出部11は、皮膚4に浸透したグルコースによるゲル20Aの膨潤度を光学的に検出する。検出部11は、図3に示すように、光源30と、ビームサンプラ31と、ビーム強度計32と、ビームスプリッタ33と、偏光板34と、プリズム35と、金属薄膜36と、対物レンズ37と、フォトダイオード38A、38Bとを備える。
【0034】
光源30は、例えば半導体レーザである。この半導体レーザは、例えば波長が635nmのレーザ光を発振出力する。レーザ光のビーム径は、0.1〜1mm程度でよい。なお、光源30として、赤色、白色LED(Light Emitting Diode)等を用いてもよい。
【0035】
光源30から出力されたレーザ光は、ビームサンプラ31に入射する。ビームサンプラ31は、一部のレーザ光の成分を反射して、ビーム強度計32に入射させる。ビーム強度計32は、入力されたレーザ光の強度を計測する。この計測値は、検出されるレーザ光の反射光強度の補正に用いられる。
【0036】
ビームスプリッタ33は、ビームサンプラ31を通過したレーザ光を2つに分岐させる。
【0037】
偏光板34は、入射した2つのレーザ光を直線偏光に変換して出射する。この直線偏光は、後述するプリズム35と金属薄膜36との間の界面Fに対してP偏光となる。
【0038】
プリズム35としては、屈折率の高いガラスが採用される。プリズム35は、偏光板34によりP偏光となった2つのレーザ光を入射する。
【0039】
プリズム35上には金属薄膜36が蒸着されている。金属薄膜36は、例えば金膜(Au)である。この他、Ag、Cu、Zn、Al、Kなどの薄膜も、金属薄膜36として用いることができる。金属薄膜36の厚みは、例えば50nmである。金属薄膜36は、プリズム35上に例えば蒸着により成膜されている。
【0040】
図4に示すように、プリズム35に入射した2つのレーザ光は、プリズム35と金属薄膜36の間の界面Fに、全反射条件を満たしエバネッセント光による表面プラズモン共鳴現象を発生させる入射角θで入射する。
【0041】
界面Fで反射した2つのレーザ光は、プリズム35から出射して、対物レンズ37に入射する。対物レンズ37は、各レーザ光を屈折させて出射する。対物レンズ37から出射された2つのレーザ光は、フォトダイオード38A、38Bに到達する。
【0042】
フォトダイオード38A、38Bは、界面Fで反射されたレーザ光を受光する。フォトダイオード38A、38Bは、その反射光の強度を検出する。
【0043】
図5のグラフには、フォトダイオード38A、38Bで受光される反射光の強度の入射角依存性の一例が示されている。このグラフでは、横軸が界面Fへの平行光束の入射角度θを示しており、縦軸がその入射角θにおける反射光の強度を示している。図5には、2本の特性曲線(a)、(b)が示されている。
【0044】
特性曲線(a)は、ゲル20Aがまだ膨潤していない状態での反射光の強度の入射角依存性を示す曲線である。この曲線によれば、表面プラズモン共鳴現象により、入射角θ1において反射光の強度が最も減衰している。この入射角θ1を、共鳴角という。本実施形態では、当初の反射光の強度が最も暗くなるように、界面Fへのレーザ光の入射角度をθ1に設定している。
【0045】
特性曲線(b)は、ゲル20Aがグルコースに応答して膨潤したときの反射光強度の入射角依存性を示す曲線である。ゲル20Aは、誘電体であり、皮膚4を浸透して出てきたグルコースにより膨潤すると、その誘電率(屈折率)が低下し、反射光強度の入射角依存性が特性曲線(a)から特性曲線(b)へシフトし、共鳴角もθ1からθ2へシフトする。
【0046】
ゲル20Aがグルコースに応答して膨潤すると、入射角θ1での反射光強度もI1からI2へ変化する。フォトダイオード38Aでは、この反射光強度の変化を観測することができる。図6には、フォトダイオード38Aの反射光強度の時間変化の一例が示されている。図6に示すように、ゲル20Aがグルコースに応答し膨潤すると、ゲル20Aの誘電率(屈折率)が低下して、結果的に、反射光強度が変化する。
【0047】
一方、ゲル20Bについてはグルコースに対して膨潤しないため、その反射光強度はグルコースに応じて変化せず、その変化は汗や体表温などの他の変動要因によるものとなる。
【0048】
図2に戻り、通信部12は、ゲル20Aの膨潤に対応するフォトダイオード38Aの出力値と、ゲル20Bに対応するフォトダイオード38Bの出力値とを、ボディエリアネットワークにより、携帯端末2に送信する。
【0049】
携帯端末2(図1参照)は、これらの出力値を受信し、受信した出力値に基づいて、血糖値の推定値を算出する。より具体的には、携帯端末2は、フォトダイオード38Aの出力値から、フォトダイオード38Bの出力値を差し引いて、他の変動要因による誘電率の変化分を除去した上で、血糖値の推定値を算出する。
【0050】
ゲル20A、20Bの膨潤度とフォトダイオード38A、38Bの出力値との相関関係、ゲル20Aの膨潤度と皮膚4内のグルコース濃度との相関関係、皮膚4内のグルコース濃度と血糖値との相関関係は予め求められ、携帯端末2に保持されている。携帯端末2は、これらの相関関係に基づいて、血糖値の推定値を算出する。
【0051】
携帯端末2は、算出した推定値を記憶する。このような処理が所定の時間間隔で繰り返し行われることにより、所定の期間(例えば、1時間)の血糖値の推移が取得される。なお、携帯端末2は、算出した推定値が予め設定した閾値を下回るか、あるいは算出した推定値の時間変化が有意な血糖値の低下を示しているか否かを判定することにより、低血糖の危険性を検出するようにしてもよい。低血糖の危険性が検出されると、携帯端末2は、発信音を鳴らしたり、バイブレーションで筐体を鳴動させたり、表示画面に警告を表示させるなどして、その危険性を外部に報知するようにしてもよい。
【0052】
以上詳細に説明したように、本実施形態に係る血糖値センサ100によれば、グルコースにより膨潤するグルコース応答性のゲル20Aを皮膚4に貼り付けて、その膨潤度を光学的に検出することにより、血糖値を間接的に計測する。このゲル20Aは、親和性に基づく可逆な構造変化を起こして膨潤するものであるので、連続的な血糖値の計測が可能である。また、この血糖値センサ100によれば、酸化酵素などによって刺激性の副産物を生成することなく、低侵襲に血糖値の計測が可能である。
【0053】
(第2の実施形態)
次に、本発明の第2の実施形態について説明する。
【0054】
本実施形態に係る血糖値センサ100は、検出部11の構成が上記第1の実施形態に係る血糖値センサ100と異なる。
【0055】
図7には、本実施形態に係る検出部11の構成が示されている。図7に示すように、本実施形態に係る検出部11は、プリズム35の代わりに、導波路40が設けられている。この導波路40は、例えばポリマー製とすることができる。
【0056】
導波路40は、光源30から発せられ、偏光板34を通過し、入射したレーザ光を、入射角度θで金属薄膜36上で複数回反射させた後、出射する。導波路40から出射された反射光は、上記第1の実施形態と同様に、フォトダイオード38Aに入射されてその強度が検出される。
【0057】
本実施形態によれば、レーザ光を金属薄膜36に複数回反射させることができるので、表面プラズモン共鳴によるレーザ光の減衰率を向上することができる。これにより、反射光強度の変化に対するセンサの感度を向上させることができる。
【0058】
(第3の実施形態)
次に、本発明の第3の実施形態について説明する。
【0059】
本実施形態に係る血糖値センサ100では、検出部11の構成が、上記第1、第2の実施形態に係る血糖値センサ100と異なる。
【0060】
図8には、本実施形態に係る検出部11の一部の構成が示されている。図8に示すように、この検出部11は、光源50と、ハーフミラー51と、ミラー52と、導波路53、54と、ミラー55、ハーフミラー56と、干渉計57と、を備える。
【0061】
光源50は、上記第1の実施形態に係る光源30(図3参照)と同様に、レーザ光を出射する。
【0062】
ハーフミラー51は、光源50から発せられたレーザ光を分岐させる。ミラー52は、ハーフミラー51で反射されたレーザ光を全反射する。
【0063】
導波路53は、グルコース応答性ゲルであるゲル20Aに接するように設けられている。図9には、導波路53におけるレーザ光の進路が示されている。図9に示すように、本実施形態では、ゲル20Aと導波路40との間に金属薄膜36が設けられていない。ゲル20Bと導波路40との間も同様である。
【0064】
導波路53は、レーザ光を入射角度θで複数回反射させた後、出射する。ゲル20Aと接する面で全反射する際に発生するエバネッセント光により、反射するレーザ光の位相は、遅延する。ゲル20Aは、皮膚4を介して浸透したグルコースにより膨潤して、誘電率が変化する。ゲル20Aの誘電率が変化すると、反射するレーザ光の位相の遅延量も変化する。
【0065】
導波路54は、グルコース非応答性ゲルであるゲル20Bに接するように設けられている。この導波路54における反射するレーザ光の位相の遅延量の変化は、グルコースの濃度とは無関係で、他の環境要因によるものである。
【0066】
導波路54から出射されたレーザ光は、ミラー55で反射され、ハーフミラー56で反射され、干渉計57に至る。一方、導波路53から出射されたレーザ光は、ハーフミラー56を経て、干渉計57に至る。
【0067】
干渉計57は、入射した2つのレーザ光の干渉縞を検出し、その干渉縞に基づいて、2つのレーザ光の位相差を検出する。この位相差は、通信部12により、携帯端末2に送信される。
【0068】
レーザ光の位相差と皮膚4内のグルコース濃度との相関関係、皮膚4内のグルコース濃度と血糖値との相関関係は予め求められており、携帯端末2に保持されている。携帯端末2は、これらの相関関係に基づいて、血糖値の推定値を算出する。携帯端末2は、算出された血糖値の推定値を記憶する。
【0069】
(第4の実施形態)
次に、本発明の第4の実施形態について説明する。
【0070】
図10には、本実施形態に係る血糖値センサ100の光学センサ1の構造が示されており、図11には、光学センサ1の上面図が示されている。
【0071】
図10、図11に示すように、導波路53、54の両端には、結合回折格子70、71が設けられている。レーザダイオード60から出射されたレーザ光は、結合回折格子70を介して導波路53、54へ入射する。
【0072】
結合回折格子70によるレーザ光の1次回折光は、上記第3の実施形態での導波路53内のレーザ光と同様に、導波路53、54内で全反射を繰り返しつつ、結合回折格子71に到達する。結合回折格子71によりレーザ光の1次回折光は、LSI63上に形成されたフォトダイオード61に入射する。
【0073】
フォトダイオード61の検出値は、上記各実施形態と同様に、通信部12により携帯端末2に送信され、携帯端末2で血糖値の推定値が求められ、記憶される。
【0074】
このように、本実施形態によれば、結合回折格子70、71を備えているので、レーザダイオード60と導波路53、54との光結合や、導波路53、54とフォトダイオード61との光結合とが容易になる。
【0075】
また、本実施形態によれば、結合回折格子70、71を備えているので、レーザダイオード60やフォトダイオード61を、その結合回折格子70、71の下部に設けることができる。これにより、光学センサ1のダイサイズを0.1〜3mm角程度に小さくすることができる。
【0076】
以上詳細に説明したように、上記各実施形態に係る血糖値センサ100によれば、経皮血糖値センサ100で一般的に利用されるイオントフォレシスのように、人体に電圧を印加する必要がなくなるので、皮膚4が炎症するリスクを回避することができる。
【0077】
また、本実施形態によれば、血糖値センサ100で利用されている内部の酵素反応、電気化学反応を伴わないため、副次的な健康リスクを低減することができるうえ、一般的な血糖値センサよりも長時間安定的に利用することができると予想される。
【0078】
上記各実施形態で用いられた導波路は、平板の導波路に限られない。例えば導波路として光ファイバーを用いることができる。
【0079】
また、上記各実施形態では、フェニルボロン酸基を有するゲルを用いたが、その他のボロン酸基を含有するゲルであっても、グルコース応答性(グルコースにより膨潤して屈折率が変化する性質)を有していれば用いることが可能である。
【0080】
また、上記各実施形態では、グルコース応答性を有しないゲル20Bをゲル20Aへの水分補給部としたが、水分補給部をゲル部10とは独立して設けるようにしてもよい。図12には、このような構成の血糖値センサ100が模式的に示されている。図12に示すように、血糖値センサ100では、水分補給部13がさらに設けられている。水分補給部13はゲル部10と接しており、水分をゲル部10に直接補給できるようになっている。
【0081】
水分補給部13は、ゲル部10以外には、水分の過度な蒸散や漏出が抑えられるように液密に構成されている。水分補給部13の内部を空洞とし、その空洞に液体が充填されるようにすることができる。また、水分補給部13の内部にガーゼや、綿、布、又はゲル状の部材などを充填し、それらの部材によって液体が保持されるようにしてもよい。
【0082】
なお、上記各実施形態に係る血糖値センサ100による計測を行う場合、計測精度を向上させるため、その計測の前に、血糖値センサ100のゲル部10を当接させる体表部分の角質層をできるだけ除去しておくのが望ましい。
【0083】
なお、本発明は、上記実施の形態及び図面によって限定されるものではない。本発明の要旨を変更しない範囲で実施の形態及び図面に変更を加えることができるのはもちろんである。
【産業上の利用可能性】
【0084】
本発明は、血糖値の検出に好適であり、特に、医療分野などに有用である。
【符号の説明】
【0085】
1 光学センサ
2 携帯端末
3 貼り付け用フィルム
4 皮膚
10 ゲル部
11 検出部
12 通信部
13 水分補給部
20A、20B ゲル
30 光源
31 ビームサンプラ
32 ビーム強度計
33 ビームスプリッタ
34 偏光板
35 プリズム
36 金属薄膜
37 対物レンズ
38A、38B フォトダイオード
40 導波路
50 光源
51 ハーフミラー
52 ミラー
53、54 導波路
55 ミラー
56 ハーフミラー
57 干渉計
70、71 結合回折格子
100 血糖値センサ
【技術分野】
【0001】
本発明は、血糖値を検出する血糖値センサに関する。
【背景技術】
【0002】
予防医学や医療費抑制が叫ばれる中で、血管障害リスクを多面的に抑制することは大変有意義である。分子レベルではグルコースや中性脂肪、コレステロール、ストレスマーカーなどが血管障害の重要な原因物質とされる。また、疫学的には過食、飲酒、喫煙、運動不足などが血管障害の誘発因子とされており、メタボリックシンドローム(通称メタボ)や糖尿病などが血管障害のリスクファクタとして挙げられている。このような背景から、初期のメタボ患者や糖尿病患者及びその予備軍に対して血管障害リスクの原因物質、誘発因子及びリスクファクタを抑制するように積極介入することの意義は大きいと考えられる。
【0003】
現状行われているいわゆるメタボ検診や、今後活用が進むHbA1C計測などの検診によって、これまで見過ごされていた隠れ糖尿病罹患者が顕在化する時代が到来すると思われる。特に、糖尿病患者の大部分は食事や運動などの生活習慣を改善することによって合併症の発生リスクを大幅に抑制することができることから、自己管理の重要性が叫ばれている。
【0004】
血糖値を自己管理をする際に、血糖値センサは主要な役割を担っている(例えば、特許文献1参照)。しかし、現状では、血糖値センサは、日内変動の激しい血糖値の瞬間的な値を計測するものであるため、計測結果のばらつきが大きい。現状の血糖値センサの計測操作は簡便ではあるものの、準備から片付けまでには数分以上を要するため、仕事中や旅行中などで昼食後1時間後又は2時間後の血糖値を正確に計測するのには困難がつきまとう。
【0005】
また、糖尿病患者にとって大きなリスクである低血糖症状に対して、1日数回程度の血糖値の計測では足りない。しかも、指裂血を計測対象とする穿刺採血方式を採用しているため、利用者からの不満は大きいうえ、データ再現性も必ずしも高いものではない。
【0006】
一方で、連続的に血糖値を計測できる次世代のセンサとして期待されている酵素電極埋め込み方式のセンサは、現状の血糖値センサ以上に侵襲性が高い(例えば、特許文献2参照)。逆に、研究段階にあるほぼすべての非侵襲の血糖値センサは、現状の血糖値センサよりもデータ再現性に乏しく、原理的にその向上は期待しがたい。
【0007】
血糖値推定値を非侵襲に得るセンサとしては経皮イオントフォレシス方式を採用した腕時計型のセンサが最もよく知られている(例えば、特許文献3参照)。しかしながら、この方式では、イオントフォレシスの電気刺激が結果的に侵襲的であったため、多くのケースで皮膚に損傷を与えているのが実情である。
【0008】
血糖値は、低血糖などの最低レベルであっても一般的な生化学分析としては十分に高濃度である。血糖由来の糖は、中性の低分子であるため、積極的な電気刺激など無しに皮膚上に自然拡散だけでも移動してくることが知られている。この位置の糖は皮膚細胞によって随時消費されるため、大血管から採血される血液中の血糖値と比較すればその濃度は確実に低く、血糖値とは一致しない。このため、血糖値センサの測定の対象としては不適当であると考えられている。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開平8−338798号公報
【特許文献2】特開2003−265444号公報
【特許文献3】特許第4295970号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
このように、血糖値センサを開発する業界では、10年以上の間、世界的に非侵襲・連続計測を最大の課題として抱えているが、未だにその課題は解決されていない。
【0011】
本発明は、上記実情に鑑みてなされたもので、低侵襲かつ連続に、血糖値を検出することができる血糖値センサを提供することを目的とする。
【課題を解決するための手段】
【0012】
上記目的を達成するために、本発明の第1の観点に係る血糖値センサは、
血糖値に関する情報を経皮的に検出する血糖値センサであって、
皮膚に貼り付けられ、グルコースに応答して膨潤するグルコース応答性ゲルと、
前記グルコース応答性ゲルに水分を補給する水分補給部と、
皮膚を通して浸透するグルコースによる前記グルコース応答性ゲルの膨潤度を光学的に検出する検出部と、
前記検出部により検出された前記グルコース応答性ゲルの膨潤度に基づいて、血糖値の推定値を算出する推定部と、
前記推定部によって算出された血糖値の推定値を記憶する記憶部と、
を備える。
【0013】
前記グルコース応答性ゲルが、ボロン酸基を官能基として有する、
こととしてもよい。
【0014】
前記水分補給部は、
グルコース応答性を有しないグルコース非応答性ゲルである、
こととしてもよい。
【0015】
前記検出部は、
前記グルコース応答性ゲルの第1の膨潤度と、
前記グルコース非応答性ゲルの第2の膨潤度と、
を同時に検出し、
前記推定部は、
前記第1の膨潤度と前記第2の膨潤度との違いに基づいて、前記血糖値の推定値を算出する、
こととしてもよい。
【0016】
前記検出部は、
表面プラズモン共鳴又は前記グルコース応答性ゲルが当接する光導波路内における光の全反射により発生する該光の位相の遅延に基づいて、前記グルコース応答性ゲルの膨潤度を検出する、
こととしてもよい。
【発明の効果】
【0017】
本発明に係る血糖値センサによれば、グルコースにより膨潤するグルコース応答性ゲルを皮膚に貼り付けて、その膨潤度を光学的に検出することにより、血糖値を間接的に計測する。このゲルは、グルコースによる親和性に基づく可逆な構造変化を起こして膨潤するものであるので、連続的な血糖値の計測が可能である。また、酸化酵素などによって刺激性の副産物を生成することなく低侵襲に血糖値の計測が可能である。
【図面の簡単な説明】
【0018】
【図1】本発明の第1の実施形態に係る血糖値センサの構成を示す斜視図である。
【図2】図1の血糖値センサの構成を示す模式図である。
【図3】図2の検出部の光学系の構成を示す図である。
【図4】界面でレーザ光が反射する様子を示す図である。
【図5】グルコース応答性ゲルが、グルコースに応答して膨潤したときの反射光強度の入射角依存性を示すグラフである。
【図6】フォトダイオードで検出される反射光強度の時間変化の一例である。
【図7】本発明の第2の実施形態に係る血糖値センサにおける検出部の一部の構成を示す図である。
【図8】本発明の第3の実施形態に係る検出部の構成を示す図である。
【図9】導波路のレーザ光の光路を説明するための図である。
【図10】本発明の第4の実施形態に係る血糖値センサの光学センサの構造を示す模式図である。
【図11】図10の光学センサの構造を示す上面図である。
【図12】血糖値センサの他の構成例を示す模式図である。
【発明を実施するための形態】
【0019】
本発明の実施の形態について、図面を参照して詳細に説明する。
【0020】
(第1の実施形態)
まず、本発明の第1の実施形態について説明する。
【0021】
図1には、本実施形態に係る血糖値センサ100の斜視図が示されている。図1に示すように、血糖値センサ100は、光学センサ1と携帯端末2とを備える。
【0022】
光学センサ1は、貼り付け用フィルム3によって例えば上腕部に貼り付けられている。光学センサ1は、血糖値に関する情報を経皮的に検出する。光学センサ1は、検出した血糖値に関する情報を、ボディエリアネットワーク(BAN)により、携帯端末2に送信する無線通信機能を有している。ここで、ボディエリアネットワークとは、極めて近距離で行われる通信ネットワークである。このボディエリアネットワークを用いれば、例えば人が携帯する装置間での通信が可能となる。
【0023】
携帯端末2は、ボディエリアネットワークにより、光学センサ1と無線通信可能な無線通信機能を有している。携帯端末2は、この無線通信機能を用いて、光学センサ1によって検出された血糖値に関する情報(後述するゲル部10のゲル20Aのグルコースによる膨潤度)を受信する。携帯端末2は、受信した血糖値に関する情報に基づいて血糖値の推定値を算出し、算出された血糖値の推定値を記憶する。このようにして、ある期間における血糖値の推移が取得される。
【0024】
図2には、光学センサ1の構成が模式的に示されている。図2に示すように、光学センサ1は、ゲル部10と、光学検出部11と、通信部12とを備えている。
【0025】
図3に示すように、ゲル部10には、2種類のゲル20A、20Bが設置されている。
【0026】
一方のゲル20Aは、グルコース応答性を有するグルコース応答性ゲルである。ゲル20Aには、ボロン酸基を官能基として有するもの、より好ましくは、フェニルボロン酸基が付与されたものが用いられる。
【0027】
フェニルボロン酸基を有するゲル20Aは、水分等に含まれる水酸基との結合と分離を繰り返している。ゲル20Aは、水酸基と結合し、さらにグルコースが結びつくと、電荷を帯び、その電荷による反発力でゲル20Aが膨潤する。ゲル20Aは、膨潤すると、その誘電率が変化する。検出部11は、この誘電率の変化を光学的に計測する。
【0028】
なお、グルコースとの結び付きが失われると、ゲル20Aは再び収縮する。このように、ゲル20Aは、周辺のグルコースの濃度に応じて膨潤と収縮とを繰り返すので、グルコースの濃度の連続計測が可能となる。
【0029】
ゲル20Aとして好適なものには、例えば、4−(ジヒドロキシボロノ)スチレン、3−(メタ)アクリルアミドフェニルボロン酸、N−(4’−ビニルベンジル)−4−フェニルボロン酸カルボキサミド、3−((メタ)アクリルアミジルグリシルアミド)フェニルボロン酸、3−(メタ)アクリルアミド−2−トリフルオロメチルフェニルボロン酸、3−(メタ)アクリルアミド−4−ペンタフルオロエチルフェニルボロン酸、5−(メタ)アクリルアミド−2−ヘプタフルオロプロピルフェニルボロン酸、5−((メタ)アクリルアミジルグリシルアミド)−2−ヘプタフルオロプロピルフェニルボロン酸、5−(メタ)アクリルアミド−2,4,6−ビス(ヘプタフルオロプロピル)フェニルボロン酸、3−(メタ)アクリルアミド−2−(1,1,2,2,3,3−ヘキサフルオロプロピル)フェニルボロン酸、3−(メタ)アクリルアミド−4−(1−クロロ−1,1,2,2,3,3−ヘキサフルオロプロピル)フェニルボロン酸、5−(メタ)アクリルアミド−2−(ペルフルオロ−1,4−ジメチル2,5−ジオキサオクチル)フェニルボロン酸などがある。
【0030】
他方のゲル20Bは、グルコース応答性を有しないグルコース非応答性ゲルである。ゲル20Bには、例えばゲル20Aと同じゲル骨格を有し、フェニルボロン酸基が付与されていないものを用いることができる。ゲル20Bは、ゲル20Aに対して水分を補給する水分補給部として機能する。
【0031】
ゲル20Bは、グルコースによって膨潤することはないが、汗や体表温度等の他の環境要因に応じてその誘電率が変化する。これはゲル20Aについても同じである。検出部11は、このような他の環境要因によるゲル20Aの誘電率の変化を相殺するために、ゲル20Bについても検出部11により、誘電率の変化を光学的に測定する。
【0032】
これらのゲル20A、20Bは、皮膚4に直接貼り付けられる。
【0033】
検出部11は、皮膚4に浸透したグルコースによるゲル20Aの膨潤度を光学的に検出する。検出部11は、図3に示すように、光源30と、ビームサンプラ31と、ビーム強度計32と、ビームスプリッタ33と、偏光板34と、プリズム35と、金属薄膜36と、対物レンズ37と、フォトダイオード38A、38Bとを備える。
【0034】
光源30は、例えば半導体レーザである。この半導体レーザは、例えば波長が635nmのレーザ光を発振出力する。レーザ光のビーム径は、0.1〜1mm程度でよい。なお、光源30として、赤色、白色LED(Light Emitting Diode)等を用いてもよい。
【0035】
光源30から出力されたレーザ光は、ビームサンプラ31に入射する。ビームサンプラ31は、一部のレーザ光の成分を反射して、ビーム強度計32に入射させる。ビーム強度計32は、入力されたレーザ光の強度を計測する。この計測値は、検出されるレーザ光の反射光強度の補正に用いられる。
【0036】
ビームスプリッタ33は、ビームサンプラ31を通過したレーザ光を2つに分岐させる。
【0037】
偏光板34は、入射した2つのレーザ光を直線偏光に変換して出射する。この直線偏光は、後述するプリズム35と金属薄膜36との間の界面Fに対してP偏光となる。
【0038】
プリズム35としては、屈折率の高いガラスが採用される。プリズム35は、偏光板34によりP偏光となった2つのレーザ光を入射する。
【0039】
プリズム35上には金属薄膜36が蒸着されている。金属薄膜36は、例えば金膜(Au)である。この他、Ag、Cu、Zn、Al、Kなどの薄膜も、金属薄膜36として用いることができる。金属薄膜36の厚みは、例えば50nmである。金属薄膜36は、プリズム35上に例えば蒸着により成膜されている。
【0040】
図4に示すように、プリズム35に入射した2つのレーザ光は、プリズム35と金属薄膜36の間の界面Fに、全反射条件を満たしエバネッセント光による表面プラズモン共鳴現象を発生させる入射角θで入射する。
【0041】
界面Fで反射した2つのレーザ光は、プリズム35から出射して、対物レンズ37に入射する。対物レンズ37は、各レーザ光を屈折させて出射する。対物レンズ37から出射された2つのレーザ光は、フォトダイオード38A、38Bに到達する。
【0042】
フォトダイオード38A、38Bは、界面Fで反射されたレーザ光を受光する。フォトダイオード38A、38Bは、その反射光の強度を検出する。
【0043】
図5のグラフには、フォトダイオード38A、38Bで受光される反射光の強度の入射角依存性の一例が示されている。このグラフでは、横軸が界面Fへの平行光束の入射角度θを示しており、縦軸がその入射角θにおける反射光の強度を示している。図5には、2本の特性曲線(a)、(b)が示されている。
【0044】
特性曲線(a)は、ゲル20Aがまだ膨潤していない状態での反射光の強度の入射角依存性を示す曲線である。この曲線によれば、表面プラズモン共鳴現象により、入射角θ1において反射光の強度が最も減衰している。この入射角θ1を、共鳴角という。本実施形態では、当初の反射光の強度が最も暗くなるように、界面Fへのレーザ光の入射角度をθ1に設定している。
【0045】
特性曲線(b)は、ゲル20Aがグルコースに応答して膨潤したときの反射光強度の入射角依存性を示す曲線である。ゲル20Aは、誘電体であり、皮膚4を浸透して出てきたグルコースにより膨潤すると、その誘電率(屈折率)が低下し、反射光強度の入射角依存性が特性曲線(a)から特性曲線(b)へシフトし、共鳴角もθ1からθ2へシフトする。
【0046】
ゲル20Aがグルコースに応答して膨潤すると、入射角θ1での反射光強度もI1からI2へ変化する。フォトダイオード38Aでは、この反射光強度の変化を観測することができる。図6には、フォトダイオード38Aの反射光強度の時間変化の一例が示されている。図6に示すように、ゲル20Aがグルコースに応答し膨潤すると、ゲル20Aの誘電率(屈折率)が低下して、結果的に、反射光強度が変化する。
【0047】
一方、ゲル20Bについてはグルコースに対して膨潤しないため、その反射光強度はグルコースに応じて変化せず、その変化は汗や体表温などの他の変動要因によるものとなる。
【0048】
図2に戻り、通信部12は、ゲル20Aの膨潤に対応するフォトダイオード38Aの出力値と、ゲル20Bに対応するフォトダイオード38Bの出力値とを、ボディエリアネットワークにより、携帯端末2に送信する。
【0049】
携帯端末2(図1参照)は、これらの出力値を受信し、受信した出力値に基づいて、血糖値の推定値を算出する。より具体的には、携帯端末2は、フォトダイオード38Aの出力値から、フォトダイオード38Bの出力値を差し引いて、他の変動要因による誘電率の変化分を除去した上で、血糖値の推定値を算出する。
【0050】
ゲル20A、20Bの膨潤度とフォトダイオード38A、38Bの出力値との相関関係、ゲル20Aの膨潤度と皮膚4内のグルコース濃度との相関関係、皮膚4内のグルコース濃度と血糖値との相関関係は予め求められ、携帯端末2に保持されている。携帯端末2は、これらの相関関係に基づいて、血糖値の推定値を算出する。
【0051】
携帯端末2は、算出した推定値を記憶する。このような処理が所定の時間間隔で繰り返し行われることにより、所定の期間(例えば、1時間)の血糖値の推移が取得される。なお、携帯端末2は、算出した推定値が予め設定した閾値を下回るか、あるいは算出した推定値の時間変化が有意な血糖値の低下を示しているか否かを判定することにより、低血糖の危険性を検出するようにしてもよい。低血糖の危険性が検出されると、携帯端末2は、発信音を鳴らしたり、バイブレーションで筐体を鳴動させたり、表示画面に警告を表示させるなどして、その危険性を外部に報知するようにしてもよい。
【0052】
以上詳細に説明したように、本実施形態に係る血糖値センサ100によれば、グルコースにより膨潤するグルコース応答性のゲル20Aを皮膚4に貼り付けて、その膨潤度を光学的に検出することにより、血糖値を間接的に計測する。このゲル20Aは、親和性に基づく可逆な構造変化を起こして膨潤するものであるので、連続的な血糖値の計測が可能である。また、この血糖値センサ100によれば、酸化酵素などによって刺激性の副産物を生成することなく、低侵襲に血糖値の計測が可能である。
【0053】
(第2の実施形態)
次に、本発明の第2の実施形態について説明する。
【0054】
本実施形態に係る血糖値センサ100は、検出部11の構成が上記第1の実施形態に係る血糖値センサ100と異なる。
【0055】
図7には、本実施形態に係る検出部11の構成が示されている。図7に示すように、本実施形態に係る検出部11は、プリズム35の代わりに、導波路40が設けられている。この導波路40は、例えばポリマー製とすることができる。
【0056】
導波路40は、光源30から発せられ、偏光板34を通過し、入射したレーザ光を、入射角度θで金属薄膜36上で複数回反射させた後、出射する。導波路40から出射された反射光は、上記第1の実施形態と同様に、フォトダイオード38Aに入射されてその強度が検出される。
【0057】
本実施形態によれば、レーザ光を金属薄膜36に複数回反射させることができるので、表面プラズモン共鳴によるレーザ光の減衰率を向上することができる。これにより、反射光強度の変化に対するセンサの感度を向上させることができる。
【0058】
(第3の実施形態)
次に、本発明の第3の実施形態について説明する。
【0059】
本実施形態に係る血糖値センサ100では、検出部11の構成が、上記第1、第2の実施形態に係る血糖値センサ100と異なる。
【0060】
図8には、本実施形態に係る検出部11の一部の構成が示されている。図8に示すように、この検出部11は、光源50と、ハーフミラー51と、ミラー52と、導波路53、54と、ミラー55、ハーフミラー56と、干渉計57と、を備える。
【0061】
光源50は、上記第1の実施形態に係る光源30(図3参照)と同様に、レーザ光を出射する。
【0062】
ハーフミラー51は、光源50から発せられたレーザ光を分岐させる。ミラー52は、ハーフミラー51で反射されたレーザ光を全反射する。
【0063】
導波路53は、グルコース応答性ゲルであるゲル20Aに接するように設けられている。図9には、導波路53におけるレーザ光の進路が示されている。図9に示すように、本実施形態では、ゲル20Aと導波路40との間に金属薄膜36が設けられていない。ゲル20Bと導波路40との間も同様である。
【0064】
導波路53は、レーザ光を入射角度θで複数回反射させた後、出射する。ゲル20Aと接する面で全反射する際に発生するエバネッセント光により、反射するレーザ光の位相は、遅延する。ゲル20Aは、皮膚4を介して浸透したグルコースにより膨潤して、誘電率が変化する。ゲル20Aの誘電率が変化すると、反射するレーザ光の位相の遅延量も変化する。
【0065】
導波路54は、グルコース非応答性ゲルであるゲル20Bに接するように設けられている。この導波路54における反射するレーザ光の位相の遅延量の変化は、グルコースの濃度とは無関係で、他の環境要因によるものである。
【0066】
導波路54から出射されたレーザ光は、ミラー55で反射され、ハーフミラー56で反射され、干渉計57に至る。一方、導波路53から出射されたレーザ光は、ハーフミラー56を経て、干渉計57に至る。
【0067】
干渉計57は、入射した2つのレーザ光の干渉縞を検出し、その干渉縞に基づいて、2つのレーザ光の位相差を検出する。この位相差は、通信部12により、携帯端末2に送信される。
【0068】
レーザ光の位相差と皮膚4内のグルコース濃度との相関関係、皮膚4内のグルコース濃度と血糖値との相関関係は予め求められており、携帯端末2に保持されている。携帯端末2は、これらの相関関係に基づいて、血糖値の推定値を算出する。携帯端末2は、算出された血糖値の推定値を記憶する。
【0069】
(第4の実施形態)
次に、本発明の第4の実施形態について説明する。
【0070】
図10には、本実施形態に係る血糖値センサ100の光学センサ1の構造が示されており、図11には、光学センサ1の上面図が示されている。
【0071】
図10、図11に示すように、導波路53、54の両端には、結合回折格子70、71が設けられている。レーザダイオード60から出射されたレーザ光は、結合回折格子70を介して導波路53、54へ入射する。
【0072】
結合回折格子70によるレーザ光の1次回折光は、上記第3の実施形態での導波路53内のレーザ光と同様に、導波路53、54内で全反射を繰り返しつつ、結合回折格子71に到達する。結合回折格子71によりレーザ光の1次回折光は、LSI63上に形成されたフォトダイオード61に入射する。
【0073】
フォトダイオード61の検出値は、上記各実施形態と同様に、通信部12により携帯端末2に送信され、携帯端末2で血糖値の推定値が求められ、記憶される。
【0074】
このように、本実施形態によれば、結合回折格子70、71を備えているので、レーザダイオード60と導波路53、54との光結合や、導波路53、54とフォトダイオード61との光結合とが容易になる。
【0075】
また、本実施形態によれば、結合回折格子70、71を備えているので、レーザダイオード60やフォトダイオード61を、その結合回折格子70、71の下部に設けることができる。これにより、光学センサ1のダイサイズを0.1〜3mm角程度に小さくすることができる。
【0076】
以上詳細に説明したように、上記各実施形態に係る血糖値センサ100によれば、経皮血糖値センサ100で一般的に利用されるイオントフォレシスのように、人体に電圧を印加する必要がなくなるので、皮膚4が炎症するリスクを回避することができる。
【0077】
また、本実施形態によれば、血糖値センサ100で利用されている内部の酵素反応、電気化学反応を伴わないため、副次的な健康リスクを低減することができるうえ、一般的な血糖値センサよりも長時間安定的に利用することができると予想される。
【0078】
上記各実施形態で用いられた導波路は、平板の導波路に限られない。例えば導波路として光ファイバーを用いることができる。
【0079】
また、上記各実施形態では、フェニルボロン酸基を有するゲルを用いたが、その他のボロン酸基を含有するゲルであっても、グルコース応答性(グルコースにより膨潤して屈折率が変化する性質)を有していれば用いることが可能である。
【0080】
また、上記各実施形態では、グルコース応答性を有しないゲル20Bをゲル20Aへの水分補給部としたが、水分補給部をゲル部10とは独立して設けるようにしてもよい。図12には、このような構成の血糖値センサ100が模式的に示されている。図12に示すように、血糖値センサ100では、水分補給部13がさらに設けられている。水分補給部13はゲル部10と接しており、水分をゲル部10に直接補給できるようになっている。
【0081】
水分補給部13は、ゲル部10以外には、水分の過度な蒸散や漏出が抑えられるように液密に構成されている。水分補給部13の内部を空洞とし、その空洞に液体が充填されるようにすることができる。また、水分補給部13の内部にガーゼや、綿、布、又はゲル状の部材などを充填し、それらの部材によって液体が保持されるようにしてもよい。
【0082】
なお、上記各実施形態に係る血糖値センサ100による計測を行う場合、計測精度を向上させるため、その計測の前に、血糖値センサ100のゲル部10を当接させる体表部分の角質層をできるだけ除去しておくのが望ましい。
【0083】
なお、本発明は、上記実施の形態及び図面によって限定されるものではない。本発明の要旨を変更しない範囲で実施の形態及び図面に変更を加えることができるのはもちろんである。
【産業上の利用可能性】
【0084】
本発明は、血糖値の検出に好適であり、特に、医療分野などに有用である。
【符号の説明】
【0085】
1 光学センサ
2 携帯端末
3 貼り付け用フィルム
4 皮膚
10 ゲル部
11 検出部
12 通信部
13 水分補給部
20A、20B ゲル
30 光源
31 ビームサンプラ
32 ビーム強度計
33 ビームスプリッタ
34 偏光板
35 プリズム
36 金属薄膜
37 対物レンズ
38A、38B フォトダイオード
40 導波路
50 光源
51 ハーフミラー
52 ミラー
53、54 導波路
55 ミラー
56 ハーフミラー
57 干渉計
70、71 結合回折格子
100 血糖値センサ
【特許請求の範囲】
【請求項1】
血糖値に関する情報を経皮的に検出する血糖値センサであって、
皮膚に貼り付けられ、グルコースに応答して膨潤するグルコース応答性ゲルと、
前記グルコース応答性ゲルに水分を補給する水分補給部と、
皮膚を通して浸透するグルコースによる前記グルコース応答性ゲルの膨潤度を光学的に検出する検出部と、
前記検出部により検出された前記グルコース応答性ゲルの膨潤度に基づいて、血糖値の推定値を算出する推定部と、
前記推定部によって算出された血糖値の推定値を記憶する記憶部と、
を備える血糖値センサ。
【請求項2】
前記グルコース応答性ゲルが、ボロン酸基を官能基として有する、
ことを特徴とする請求項1に記載の血糖値センサ。
【請求項3】
前記水分補給部は、
グルコース応答性を有しないグルコース非応答性ゲルである、
ことを特徴とする請求項2に記載の血糖値センサ。
【請求項4】
前記検出部は、
前記グルコース応答性ゲルの第1の膨潤度と、
前記グルコース非応答性ゲルの第2の膨潤度と、
を同時に検出し、
前記推定部は、
前記第1の膨潤度と前記第2の膨潤度との違いに基づいて、前記血糖値の推定値を算出する、
ことを特徴とする請求項1乃至3のいずれか一項に記載の血糖値センサ。
【請求項5】
前記検出部は、
表面プラズモン共鳴又は前記グルコース応答性ゲルが当接する光導波路内における光の全反射により発生する該光の位相の遅延に基づいて、前記グルコース応答性ゲルの膨潤度を検出する、
ことを特徴とする請求項1乃至4のいずれか一項に記載の血糖値センサ。
【請求項1】
血糖値に関する情報を経皮的に検出する血糖値センサであって、
皮膚に貼り付けられ、グルコースに応答して膨潤するグルコース応答性ゲルと、
前記グルコース応答性ゲルに水分を補給する水分補給部と、
皮膚を通して浸透するグルコースによる前記グルコース応答性ゲルの膨潤度を光学的に検出する検出部と、
前記検出部により検出された前記グルコース応答性ゲルの膨潤度に基づいて、血糖値の推定値を算出する推定部と、
前記推定部によって算出された血糖値の推定値を記憶する記憶部と、
を備える血糖値センサ。
【請求項2】
前記グルコース応答性ゲルが、ボロン酸基を官能基として有する、
ことを特徴とする請求項1に記載の血糖値センサ。
【請求項3】
前記水分補給部は、
グルコース応答性を有しないグルコース非応答性ゲルである、
ことを特徴とする請求項2に記載の血糖値センサ。
【請求項4】
前記検出部は、
前記グルコース応答性ゲルの第1の膨潤度と、
前記グルコース非応答性ゲルの第2の膨潤度と、
を同時に検出し、
前記推定部は、
前記第1の膨潤度と前記第2の膨潤度との違いに基づいて、前記血糖値の推定値を算出する、
ことを特徴とする請求項1乃至3のいずれか一項に記載の血糖値センサ。
【請求項5】
前記検出部は、
表面プラズモン共鳴又は前記グルコース応答性ゲルが当接する光導波路内における光の全反射により発生する該光の位相の遅延に基づいて、前記グルコース応答性ゲルの膨潤度を検出する、
ことを特徴とする請求項1乃至4のいずれか一項に記載の血糖値センサ。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【公開番号】特開2012−70907(P2012−70907A)
【公開日】平成24年4月12日(2012.4.12)
【国際特許分類】
【出願番号】特願2010−217558(P2010−217558)
【出願日】平成22年9月28日(2010.9.28)
【出願人】(504136568)国立大学法人広島大学 (924)
【Fターム(参考)】
【公開日】平成24年4月12日(2012.4.12)
【国際特許分類】
【出願日】平成22年9月28日(2010.9.28)
【出願人】(504136568)国立大学法人広島大学 (924)
【Fターム(参考)】
[ Back to top ]

